RU84381U1 - Устройство для автоматизированного выделения нуклеиновых кислот - Google Patents
Устройство для автоматизированного выделения нуклеиновых кислот Download PDFInfo
- Publication number
- RU84381U1 RU84381U1 RU2009105294/22U RU2009105294U RU84381U1 RU 84381 U1 RU84381 U1 RU 84381U1 RU 2009105294/22 U RU2009105294/22 U RU 2009105294/22U RU 2009105294 U RU2009105294 U RU 2009105294U RU 84381 U1 RU84381 U1 RU 84381U1
- Authority
- RU
- Russia
- Prior art keywords
- cartridge
- reservoirs
- nucleic acids
- lysis
- reagents
- Prior art date
Links
- 150000007523 nucleic acids Chemical class 0.000 title claims abstract description 45
- 108020004707 nucleic acids Proteins 0.000 title claims abstract description 44
- 102000039446 nucleic acids Human genes 0.000 title claims abstract description 44
- 238000002955 isolation Methods 0.000 title description 23
- 238000000746 purification Methods 0.000 claims abstract description 34
- 239000003153 chemical reaction reagent Substances 0.000 claims abstract description 33
- 239000011541 reaction mixture Substances 0.000 claims abstract description 33
- 239000012472 biological sample Substances 0.000 claims abstract description 30
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims abstract description 28
- 239000012139 lysis buffer Substances 0.000 claims abstract description 24
- 239000002594 sorbent Substances 0.000 claims abstract description 21
- 239000011534 wash buffer Substances 0.000 claims abstract description 21
- 239000007790 solid phase Substances 0.000 claims abstract description 19
- 239000000243 solution Substances 0.000 claims abstract description 19
- 230000009089 cytolysis Effects 0.000 claims abstract description 17
- 230000003612 virological effect Effects 0.000 claims abstract description 17
- 244000005700 microbiome Species 0.000 claims abstract description 16
- 238000010438 heat treatment Methods 0.000 claims abstract description 15
- 238000010828 elution Methods 0.000 claims abstract description 14
- 239000002245 particle Substances 0.000 claims abstract description 14
- 230000027455 binding Effects 0.000 claims abstract description 12
- 238000000605 extraction Methods 0.000 claims abstract description 12
- 239000000203 mixture Substances 0.000 claims abstract description 12
- 238000002156 mixing Methods 0.000 claims abstract description 11
- 239000002699 waste material Substances 0.000 claims abstract description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 8
- IDGUHHHQCWSQLU-UHFFFAOYSA-N ethanol;hydrate Chemical compound O.CCO IDGUHHHQCWSQLU-UHFFFAOYSA-N 0.000 claims abstract description 7
- 238000005406 washing Methods 0.000 claims abstract description 7
- JEGUKCSWCFPDGT-UHFFFAOYSA-N h2o hydrate Chemical compound O.O JEGUKCSWCFPDGT-UHFFFAOYSA-N 0.000 claims abstract description 3
- 238000011534 incubation Methods 0.000 claims abstract description 3
- 210000004027 cell Anatomy 0.000 claims description 24
- 239000003795 chemical substances by application Substances 0.000 claims description 17
- 230000003196 chaotropic effect Effects 0.000 claims description 15
- 102000016943 Muramidase Human genes 0.000 claims description 12
- 108010014251 Muramidase Proteins 0.000 claims description 12
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 claims description 12
- 229960000274 lysozyme Drugs 0.000 claims description 12
- 239000004325 lysozyme Substances 0.000 claims description 12
- 235000010335 lysozyme Nutrition 0.000 claims description 12
- 238000012545 processing Methods 0.000 claims description 12
- 108010067770 Endopeptidase K Proteins 0.000 claims description 10
- 239000003599 detergent Substances 0.000 claims description 10
- 239000007788 liquid Substances 0.000 claims description 9
- 102000004169 proteins and genes Human genes 0.000 claims description 9
- -1 polypropylene Polymers 0.000 claims description 8
- 108090000623 proteins and genes Proteins 0.000 claims description 8
- 229920005372 Plexiglas® Polymers 0.000 claims description 6
- 239000004698 Polyethylene Substances 0.000 claims description 6
- 238000004090 dissolution Methods 0.000 claims description 6
- 239000012530 fluid Substances 0.000 claims description 6
- 239000000463 material Substances 0.000 claims description 6
- 229920000573 polyethylene Polymers 0.000 claims description 6
- 229920001296 polysiloxane Polymers 0.000 claims description 6
- 239000002904 solvent Substances 0.000 claims description 6
- 238000003756 stirring Methods 0.000 claims description 6
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 claims description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 5
- 230000006378 damage Effects 0.000 claims description 5
- 241000700605 Viruses Species 0.000 claims description 4
- 229910052736 halogen Inorganic materials 0.000 claims description 4
- 150000002367 halogens Chemical class 0.000 claims description 4
- 239000006166 lysate Substances 0.000 claims description 4
- 239000004743 Polypropylene Substances 0.000 claims description 3
- 210000000234 capsid Anatomy 0.000 claims description 3
- 210000002421 cell wall Anatomy 0.000 claims description 3
- 239000013078 crystal Substances 0.000 claims description 3
- 239000003365 glass fiber Substances 0.000 claims description 3
- 229960000789 guanidine hydrochloride Drugs 0.000 claims description 3
- PJJJBBJSCAKJQF-UHFFFAOYSA-N guanidinium chloride Chemical compound [Cl-].NC(N)=[NH2+] PJJJBBJSCAKJQF-UHFFFAOYSA-N 0.000 claims description 3
- 150000003839 salts Chemical class 0.000 claims description 3
- 239000013013 elastic material Substances 0.000 claims description 2
- 239000000499 gel Substances 0.000 claims description 2
- 239000011521 glass Substances 0.000 claims description 2
- ZJYYHGLJYGJLLN-UHFFFAOYSA-N guanidinium thiocyanate Chemical compound SC#N.NC(N)=N ZJYYHGLJYGJLLN-UHFFFAOYSA-N 0.000 claims description 2
- 229920000515 polycarbonate Polymers 0.000 claims description 2
- 239000004417 polycarbonate Substances 0.000 claims description 2
- 229920000642 polymer Polymers 0.000 claims description 2
- 229920001155 polypropylene Polymers 0.000 claims description 2
- 239000000377 silicon dioxide Substances 0.000 claims description 2
- 238000000034 method Methods 0.000 description 25
- 239000000523 sample Substances 0.000 description 22
- 238000004458 analytical method Methods 0.000 description 11
- 239000000872 buffer Substances 0.000 description 8
- 238000001514 detection method Methods 0.000 description 8
- 210000004369 blood Anatomy 0.000 description 7
- 239000008280 blood Substances 0.000 description 7
- 208000015181 infectious disease Diseases 0.000 description 6
- 239000012528 membrane Substances 0.000 description 6
- 210000003296 saliva Anatomy 0.000 description 6
- 230000003321 amplification Effects 0.000 description 5
- 238000001914 filtration Methods 0.000 description 5
- 238000003199 nucleic acid amplification method Methods 0.000 description 5
- 241000193388 Bacillus thuringiensis Species 0.000 description 4
- 238000012408 PCR amplification Methods 0.000 description 4
- 229940097012 bacillus thuringiensis Drugs 0.000 description 4
- 230000001580 bacterial effect Effects 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 241000894006 Bacteria Species 0.000 description 3
- 241000709744 Enterobacterio phage MS2 Species 0.000 description 3
- 241000588724 Escherichia coli Species 0.000 description 3
- 239000013060 biological fluid Substances 0.000 description 3
- 230000006037 cell lysis Effects 0.000 description 3
- 238000005119 centrifugation Methods 0.000 description 3
- 230000001276 controlling effect Effects 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 239000006249 magnetic particle Substances 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 244000000010 microbial pathogen Species 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 238000003753 real-time PCR Methods 0.000 description 3
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 2
- 241001504639 Alcedo atthis Species 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 230000004568 DNA-binding Effects 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- 239000011543 agarose gel Substances 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 238000001962 electrophoresis Methods 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000011010 flushing procedure Methods 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 238000009434 installation Methods 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 210000002381 plasma Anatomy 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- BMYCCWYAFNPAQC-UHFFFAOYSA-N 2-[dodecyl(methyl)azaniumyl]acetate Chemical group CCCCCCCCCCCCN(C)CC(O)=O BMYCCWYAFNPAQC-UHFFFAOYSA-N 0.000 description 1
- 101710132601 Capsid protein Proteins 0.000 description 1
- 101710094648 Coat protein Proteins 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102100021181 Golgi phosphoprotein 3 Human genes 0.000 description 1
- 241000764238 Isis Species 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- 101710125418 Major capsid protein Proteins 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 241000204031 Mycoplasma Species 0.000 description 1
- 108091005461 Nucleic proteins Proteins 0.000 description 1
- 101710141454 Nucleoprotein Proteins 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- 101710083689 Probable capsid protein Proteins 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 239000012620 biological material Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 239000012531 culture fluid Substances 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 238000012252 genetic analysis Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000012678 infectious agent Substances 0.000 description 1
- 238000001746 injection moulding Methods 0.000 description 1
- 238000002032 lab-on-a-chip Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 238000011005 laboratory method Methods 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 230000002934 lysing effect Effects 0.000 description 1
- 239000000696 magnetic material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000002159 nanocrystal Substances 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 238000001821 nucleic acid purification Methods 0.000 description 1
- 229920002113 octoxynol Polymers 0.000 description 1
- 238000011017 operating method Methods 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 239000002985 plastic film Substances 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000003757 reverse transcription PCR Methods 0.000 description 1
- 229920000260 silastic Polymers 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 238000009210 therapy by ultrasound Methods 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 238000004804 winding Methods 0.000 description 1
Landscapes
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
1. Устройство для автоматизированного выделения нуклеиновых кислот из биологических образцов, состоящее из (а) картриджа, содержащего резервуары с реагентами для лизиса клеток, микроорганизмов и вирусных частиц, очистки и элюции нуклеиновых кислот, каналы, микроколонки и клапаны, и (б) управляющей установки-контроллера, осуществляющей подачу давления, нагрев, перемешивание реагентов в индивидуальных резервуарах картриджа и перемещение реакционных смесей и растворов в резервуарах картриджа, характеризующееся тем, что картридж содержит приемную камеру для ввода биологического образца, резервуары с сухими реакционными смесями буферов для лизиса и буфера для промывки, микроколонку с твердофазным сорбентом для связывания нуклеиновых кислот, резервуары для этанола, смеси вода-этанол и воды для растворения сухих компонентов промывочного буфера, промывки микроколонки и элюции нуклеиновых кислот, связавшихся с твердофазным сорбентом в микроколонке, выходной порт, совместимый со стандартной микропробиркой, резервуар для сбора отходов реакций, а управляющая установка-контроллер содержит блок соленоидов для управления клапанами картриджа, блок нагревателей, блок электромагнитных мешалок, компрессор и блок электронного управления. ! 2. Устройство по п.1, характеризующееся тем, что картридж помещают в управляющую установку-контроллер, обеспечивающую заданные скорости перемещения реакционных смесей и реагентов в резервуарах картриджа, температурно-временные режимы инкубации и перемешивания реакционных смесей в отдельных резервуарах картриджа. ! 3. Устройство по п.1, характеризующееся тем, что картридж содержи
Description
Полезная модель относится к области молекулярной биологии, биотехнологии, микробиологии и медицине и касается устройства для автоматизированного выделения нуклеиновых кислот (НК), в котором осуществляются все стадии выделения и очистки НК из биологических образцов. Процедура выделения и очистки НК выполняется внутри картриджа, изолированного от внешней среды, что сводит к минимуму риск заражения персонала. Полученную очищенную ДНК можно непосредственно использовать для проведения ПЦР.
Выделение и очистка нуклеиновых кислот (НК) из биологического материала (животные и растительные клетки, ткани, физиологические жидкости (кровь, слюна и др.)), а также из образцов почв, пищевых продуктов, воды и др. является необходимой стадией при проведении широкого круга исследований в разных областях науки, включая молекулярно-генетические исследования, а также в клинической диагностике, фармакологии, медицине, биотехнологии, охране окружающей среды и др. Современные требования к лабораторным методам выделения НК включают быстроту и эффективность проведения всех этапов выделения и безопасность выполнения процедуры для персонала, универсальность протокола для получения очищенной ДНК и РНК из различных биологических образцов. Возрастают требования к чистоте получаемых препаратов и воспроизводимости процедуры выделения.
Выделение и очистка НК в биохимических лабораториях и медицинских центрах в настоящее время производится, в основном, в ручном режиме. Первым этапом выделения является разрушение клеточных стенок или вирусного капсида (лизис), после которого необходимо проводить отделение белков и нерастворимых частиц. Большинство методик выделения НК включает несколько стадий центрифугирования, что является одной из наиболее трудоемких процедур, которые приводят также к уменьшению выхода НК за счет больших потерь при отборе супернатанта после центрифугирования. В некоторых методах выделения и очистки НК используются токсичные органические растворители, такие, как фенол, хлороформ и др., что требует дополнительных мер защиты персонала лабораторий. Кроме того, при работе с патогенными микроорганизмами и вирусами существует риск заражения персонала.
Таким образом, недостатками ручных процедур являются трудоемкость, недостаточно высокий выход НК, частое использование токсичных органических растворителей, риск заражения персонала при работе с патогенными микроорганизмами. Поэтому, в данной области существует острая потребность в разработке устройства для автоматизированного выделения НК, которое позволяло бы быстро получать высокоочищенные НК с высоким выходом и исключило или свело к минимуму контакт персонала с патогенным или инфекционным материалом.
В настоящее время существует ряд автоматизированных устройств для обработки биологических образцов и выделения НК. Роботизированные системы COBAS AmpliPrep компании Roche Diagnostics (США/Швейцария), Thermo′s KingFisher компании Thermo Electron (США), QIAsymphony SP и BioRobot MDx компании Qiagen (Германия), предназначенные для выделения и очистки ДНК и РНК из биологических жидкостей, таких как сыворотка и плазма крови, слюна, моча, основаны на применении технологии, использующей магнитные частицы. Все эти системы позволяют одновременно обрабатывать несколько биологических образцов, например, 24 образца физиологических жидкостей в устройстве Thermo′s KingFisher, 96 образцов для выделения вирусных НК или геномной ДНК из образцов крови в приборе QIAsymphony SP. Система QIAsymphony SP включает картриджи, заполненные необходимыми реагентами, дозированно подаваемые для обработки образца. Картриджи в процессе выделения открываются автоматически, что сводит к минимуму риск заражения или контаминации.
Известны также рабочие станции для автоматической экстракции и очистки НК, которые с использованием роботов воспроизводят ручные способы выделения НК, включающие последовательное перемещение пробирок, фильтрацию, дозирование реагентов. Например, компанией Bioneer Corp.заявлено устройство для автоматической очистки ДНК (Automatic DNA purification apparatus, патент WO/2001/025482), состоящее из многочисленных контейнеров для растворов, каналов для прохождения жидкостей, регулируемых клапанами, вакуумного блока, штативов, шприцов для точного количественного введения и отсасывания жидкостей.
Компанией Corbett Technologies (Австралия) разработана настольная рабочая станция "X-tractor GeneTM System" для экстракции НК из образцов объемом до 200 мкл, полностью воспроизводящая ручное выделение НК.
Компанией Isis Pharmaceuticals, США запатентована полностью автоматизированная система-робот для идентификации биологически-опасных агентов (Automatic identification of bioagents, патент WO/2005/009202). Система состоит из двух блоков, разделенных воздушным шлюзом, в первом из которых проводится выделение и очистка ДНК, а во втором - ПЦР для идентификации агента.
Все эти устройства являются сложными конструкциями, основанными на применении робототехники, недостатками которых является их громоздкость, высокая стоимость (более 70 тыс. долл. США), дороговизна проведения анализов и эксплуатации, что делает невозможным их использования в небольших лабораториях и центрах. Кроме того, они являются закрытыми системами, не допускающими вмешательство оператора в ход процесса. При эксплуатации таких систем необходимы постоянные закупки реагентов данной фирмы, которые предназначены для данного конкретного прибора
Другой класс установок для автоматизированного выделения НК включает более простые и дешевые устройства, которые позволяют хотя бы частично автоматизировать процесс.
Фирмой Millipore Corporation (США) запатентовано устройство для выделения НК из клеток, вирусных частиц и микоплазмы, состоящее из системы фильтрующих элементов (пористых мембран), через которые последовательно пропускают образец (Filter device for the isolation of a nucleic acid, EP 183242 A2). На первой мембране осуществляется лизис клеток; полученный лизат поступает на стекловолоконный фильтр для последующей очистки и элюции НК. Фильтрующие мембраны соединены системой клапанов. Устройство может быть как одноразового, так и многоразового использования. Для одновременной обработки нескольких образцов несколько фильтрующих устройств могут быть собраны в кассету. Недостатками данного устройства являются необходимость ручного введения реагентов и наличие стадий центрифугирования.
Запатентовано устройство для выделения НК (Nucleic acid isolation, WO/2005/012521, Invitrogen Corp., США), представляющее собой картридж, состоящий из пробирки, соединенной с фильтрующим элементом и далее с колонкой для очистки НК. Фильтрующий элемент содержит несколько слоев фильтров, колонка включает носитель, способный связывать НК, например носитель с переменным зарядом. Манипуляции с образцом осуществляются с помощью шприца или насоса. Недостатком данного устройства является необходимость предварительной ручной обработки образца перед введением его в картридж: проведение лизиса клеток, разбавление сыворотки крови и т.п.
Описан ряд микрофлюидных устройств для получения очищенных нуклеиновых кислот, содержащих сеть микроканалов диаметром 100 мкм и менее, через которые пропускаются биологические образцы и растворы реагентов. В состав микрофлюидных систем входят также перемешивающие устройства, микродозаторы, микронасосы, фильтры и др.
Запатентованы микрофлюидное устройство для очистки ДНК при взаимодействии образца с диатомитом (Purification and amplification of nucleic acids in a microfluidic device, WO/2008/002725, Bio-Rad, США), микрофлюидное устройство для выделение геномной ДНК из лейкоцитов человека, в котором ДНК из образца связывается с поверхностью канала, модифицированного ДНК-связывающим реагентом (DNA purification and analysis on nanoengineered surfaces, WO/2006/081324); микрочип, в котором очистка ДНК происходит путем последовательного прохождения через серию хроматографических микроколонок, селективно сорбирующих примесные вещества, такие как белки, пептиды, липиды, лектины и др., а последняя колонка селективно связывает ДНК (DNA purification in a multi-stage, multi-phase microchip, WO/2008/058204). Недостатком таких устройств является низкий выход НК, а также необходимость ручного введения реагентов на разных стадиях выделения и очистки.
Описано микрофлюидное устройство и метод концентрирования и очистки НК из биологических образцов (Methods for nucleic acid isolation and kits using a microfluidic device and concentration step, WO/2005/068627, 3M Innovative Properties company, США), включающее резервуар для загрузки образца и камеры для обработки и перемешивания, соединенные каналами и клапанами. Образец после загрузки подвергается действию лизирующего раствора, переходит далее в камеру для обработки, где проходит несколько стадий концентрирования и разбавления, а также дополнительный лизис и удаление раствора, содержащего ингибиторы, которые мешают проведению ПНР с полученной ДНК. Недостатком данной системы является возможность лишь частичной очистки НК, в основном, от ингибиторов ПЦР.
Предложено монолитное микрофлюидное устройство для экстракции ДНК и РНК, в основном, из образцов крови (Nucleic acid purification chip, WO/2005/066343, Сингапур), состоящее из субстрата на основе кремния, входных и выходных отверстий для введения и выведения образца крови, а также буферов для обработки образца в объеме нескольких микролитров, микромешалки, камеры для лизиса, камеры, содержащей ДНК-связывающий материал и систему клапанов. Устройство позволяет выделять НК только из образца определенного типа (кровь).
Примером более сложной микрофлюидной системы является система, представляющая собой совокупность модулей, в первом из которых происходит связывание и очистка целевого продукта (НК), а второй модуль является собственно микрофлюидным устройством, осуществляющим детекцию и анализ полученного продукта (Microfluidic devices, WO/2008/030631, Microchip biotechnologies, США). Лизис клеток осуществляется обработкой ультразвуком в проточном режиме. Очистка ДНК осуществляется путем взаимодействия с магнитными частицами, содержащими аффинный носитель. Магнитное поле создается вращающимся магнитным блоком.
Фирмой Siemens (Германия) предложен плоский картридж (карта) для автоматического анализа ДНК или белков, содержащий систему микроканалов и микрополостей, формирующих емкости для содержащихся в них сухих реагентов, а также способ его изготовления методом литья под давлением (Arrangement for integrated and automated DNA or protein analysis in a single-use cartridge, method for producing such a cartridge and operating method for DNA or protein analysis using such a cartridge, WO/2006/042838). Сухие реагенты вносятся в открытые каналы, которые после этого заклеиваются пленкой. Картридж является одноразовым устройством. Образец вносится в готовый к анализу картридж, и результаты получают в полностью автоматическом режиме при помещении картриджа в считывающее устройство.
Описан также ряд микрофлюидных аппаратов, в которых одновременно производится выделение ДНК и ее ПЦР-амплификация, а в ряде устройств и последующая детекция. Примером такой системы может служить устройство для выделения и амплификации ДНК из биологических жидкостей фирмы Micronics (США) (Method and system for microfluidic manipulation, amplification and analysis of fluids, for example, bacteria assays and antiglobulin testing, WO/2004/065010, патент США 7,416,892). Устройство представляет собой одноразовую микрофлюидную карту и предназначено для анализа бактерий в биологических жидкостях и диагностики некоторых заболеваний. Карта имеет встроенную фильтрующую мембрану, на которой задерживаются клетки, которые далее подвергаются лизису. Через мембрану последовательно пропускают серию растворов: растворы для отмывки, растворы, содержащие ферменты, растворы для амплификации и детекции. Проводится ПЦР-амплификация полученной ДНК в соответствующем температурном режиме, а далее ПЦР-продукт смывается с мембраны и передается на детектирующий элемент.
Описана микрофлюидная система («лаборатория-на-чипе») для детекции некоторых возбудителей инфекционных заболеваний (Университет Пенсильвании, США), состоящая из коллектора образца (слюны), одноразовой пластиковой кассеты (микрофлюидный чип) для обработки образца, включающей систему для проведения лизиса, экстракции НК, ПЦР, мечения ПЦР-продукта, и управляющей платформы-контроллера для управления подачей реагентов, температурой, клапанами, а также лазерного сканера для считывания результатов (Z. Chen, M.G. Mauk, J. Wang, W.R. Abrams, P.L. Corstjens, R.S. Niedbala, D. Malamud, H.H. Bau, A microfluidic system for saliva-based detection of infectious diseases. Ann. NY Acad. Sci., 2007, v. 1098, p.429-436).
Фирмой Canon U.S. Life Sciences, США предложено устройство для анализа геномной ДНК, состоящее из картриджа, в котором проводится выделение ДНК, инжектора, с помощью которого ДНК передается на микрофлюидный чип, включающий зону для ПЦР-амплификации, зону для детекции и зону для анализа ДНК (Method and molecular diagnostic device for detection, analysis and identification of genomic DNA, WO 2007028084). Выделение ДНК происходит в реакционной камере с использованием магнитных частиц или материалов, меняющих свойства под действием электрического заряда.
Предложен полностью автоматизированный портативный микрофлюидный чип для обнаружения патогенных микроорганизмов методом ПЦР с детекцией в реальном времени (Real-time PCR detection of microorganisms using an integrated microfluidic platform, WO/2006/085948, Cornell Research Foundation, США). Микрочип включает модуль для лизиса очистки ДНК, который с помощью микроканалов соединен с модулем для ПЦР-детекции. Детекция осуществляется методом ПЦР в реальном времени с использованием флуоресцентного красителя. Устройство можно использовать как в лабораториях, так и в полевых условиях.
Таким образом, в настоящее время разработан ряд устройств для автоматического выделения и очистки НК, включающий сложные роботизированные системы, в том числе устройства для одновременно выделения ДНК и ее ПЦР-амплификации, и более простые и дешевые аппараты. Автоматические роботизированные системы дороги, громоздки и сложны в использовании, а более простые системы либо требуют дополнительной ручной обработки образца, либо осуществляют неполную очистку НК, либо выход НК недостаточен, либо они предназначены для выделения ДНК из образца определенного типа, например, только из крови, слюны и др., либо проводят анализ образца на наличие одного конкретного заболевания. Не существует универсального устройства, которое позволяет быстро, воспроизводимо и с высоким выходом выделять НК из биологических образцов в полностью автоматическом режиме.
В данной области существует острая потребность в разработке устройства для автоматизированного выделения НК, который бы выгодно отличался от известных из уровня техники решений простотой проведения анализа, высоким выходом НК и невысокой стоимостью. Чрезвычайно важно проведение всех операций выделения и очистке в автоматическом режиме, чтобы полностью исключить контакт персонала с патогенными и инфицированными образцами.
Предлагаемая полезная модель позволяет проводить в автоматическом режиме все стадии выделения и очистки НК, включая лизис клеток, микроорганизмов и вирусных частиц, очистку и элюцию НК. Полностью исключен контакт персонала с биологическим образцом. Процедура выделения и очистки НК происходит быстро (около 40 мин) и с высоким выходом (более 90%). Полученную ДНК можно использовать для проведения ПЦР.
На Фиг.1 представлена фотография полезной модели-устройства для автоматизированного выделения НК из биологических образцов. Картридж (1) помещают в управляющую установку-контроллер (2). Процедура выделения и очистки НК с использованием устройства управляется компьютером (3).
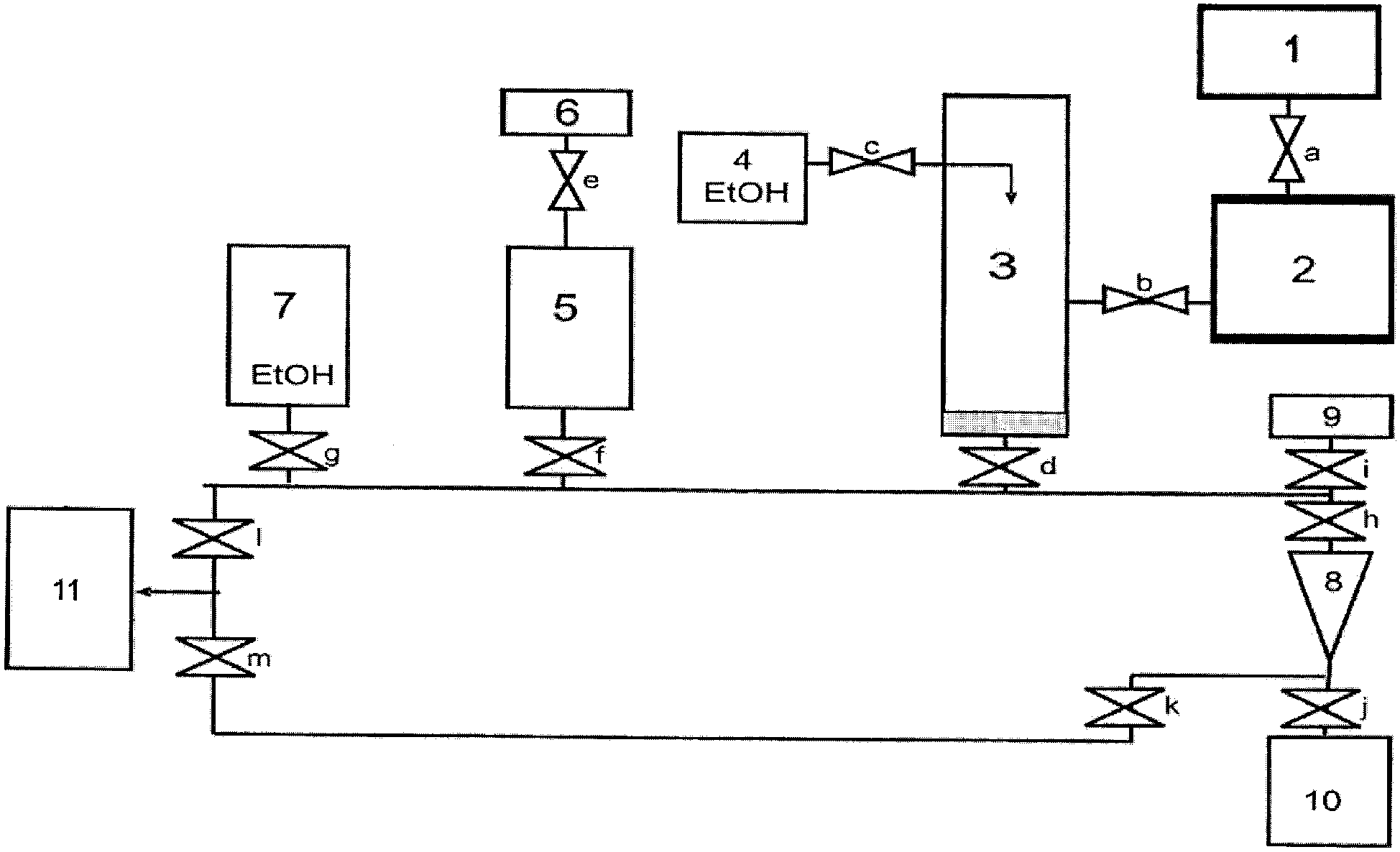
На Фиг.2 представлена принципиальная схема картриджа для автоматизированного выделения НК с обозначением резервуаров с необходимыми реагентами.
1 - приемная камера для образца;
2 - резервуар для лизирующего буфера, содержащего лизоцим. Раствор в резервуаре нагревается при использовании нагревательного элемента и перемешивается электромагнитной мешалкой;
3 - резервуар для лизирующего буфера, содержащего хаотропный агент, протеиназу К, детергент. Раствор в резервуаре нагревается при использовании нагревательного элемента и перемешивается электромагнитной мешалкой;
4 - резервуар, содержащий этанол;
5 - резервуар для промывочного буфера, содержащего хаотропный агент. Раствор в резервуаре нагревается при использовании нагревательного элемента и перемешивается электромагнитной мешалкой;
6 - резервуар, содержащий растворитель для промывочного буфера (смесь этанол-вода);
7 - резервуар, содержащий этанол;
8 - микроколонка с твердофазным сорбентом для связывания нуклеиновых кислот;
9 - резервуар для раствора для элюции НК с микроколонки (вода);
10 - резервуар для сбора очищенной НК;
11 - резервуар для сбора отходов;
а-m - клапаны, регулирующие перемещение реакционных смесей и реагентов в каналах и резервуарах картриджа. Управляются установкой-контроллером.
Фиг.3 представляет конструктивные элементы картриджа.
А - верхняя панель (крышка), оргстекло, 2 мм. На верхней панели расположены:
1 - отверстия для поршней (16 шт.);
2 - отверстие для приемной камеры образца;
3 - отверстия для фиксирующих винтов (4 шт.);
П1 - прокладка, силикон, 2 мм;
П2 - прокладка, полиэтилен, пленка, 50 мкм;
Б - основная рабочая платформа, оргстекло, 8 мм;
П3 - прокладка, полиэтилен, пленка, 50 мкм;
П4 - прокладка, силикон, 2 мм;
В - нижняя панель (крышка), оргстекло, 2 мм.
Фиг.4 представляет фотографию управляющей установки-контроллера (без картриджа).
1 - блок соленоидов для управления клапанами картриджа;
2 - блок поршней;
3 - блок галогенных ламп нагревателя;
4 - направляющие салазки для помещения картриджа в управляющую установку-контроллер;
5 - блок электромагнитных мешалок;
6 - компрессор;
7 - блок электронного управления.
На Фиг.5 представлена схематическая диаграмма устройства клапана.
1 - соленоид постоянного тока;
2 - поршень;
3 - запорная головка клапана;
А - верхняя панель картриджа (см. Фиг.3);
П1 - прокладка между верхней панелью и основной рабочей платформой картриджа, силикон (см. Фиг.3);
П2 - прокладка между верхней панелью и основной рабочей платформой картриджа, полиэтилен (см. Фиг.3);
Б - основная рабочая платформа картриджа (см. Фиг.3);
IN - входной канал;
OUT - выходной канал.
Фиг.6 представляет результаты выделения НК из бактериальных клеток.
А. Грам-положительные бактериальные клетки Bacillus thuringiensis (10s клеток/мл).
Электрофорез в 1% агарозном геле. Дорожки:
1 - ДНК Bacillus thuringiensis;
2 - ДНК, выделенная из клеток Bacillus thuringiensis, ручным методом;
3 - ДНК, выделенная из клеток Bacillus thuringiensis, с использованием устройства для автоматизированного выделения нуклеиновых кислот;
4 - маркер λ/Hind III.
Б. Грам-отрицательные бактериальные клетки Escherichia coli. Выделение НК из ночной культуры клеток. Электрофорез в 1% агарозном геле. Дорожки:
1 - маркер λ/Hind III;
2 - НК, выделенные из клеток E.coli, ручным методом;
3, 4 - НК, выделенные из клеток E.coli, с использованием устройства для автоматизированного выделения нуклеиновых кислот.
Фиг.7 представляет результаты проведения ОТ-ПЦР с РНК бактериофага MS2 с использованием РНК, выделенной различными методами. ПЦР проводили с праймерами, комплементарными участку последовательности Coat протеина.
1 - РНК бактериофага MS2, выделенная ручным методом;
2, 3 - РНК бактериофага MS2, выделенная с использованием устройства для автоматизированного выделения нуклеиновых кислот;
4 - положительный контроль реакции;
5 - отрицательный контроль реакции;
6 - маркер λ/Hind III.
Устройство для автоматизированного выделения нуклеиновых кислот из биологических образцов состоит из картриджа, содержащего резервуары с реагентами для лизиса клеток, микроорганизмов и вирусных частиц, очистки и элюции нуклеиновых кислот, каналы, микроколонки и клапаны, и управляющей установки-контроллера, осуществляющей подачу давления, нагрев, перемешивание реагентов в индивидуальных резервуарах картриджа, а также перемещение реакционных смесей и растворов (Фиг.1).
Картридж содержит приемную камеру для ввода биологического образца, резервуары с сухими реакционными смесями буферов для лизиса и буфера для промывки, микроколонку с твердофазным сорбентом для связывания нуклеиновых кислот, резервуары для этанола, смеси вода-этанол и воды для растворения сухих компонентов промывочного буфера, промывки микроколонки и элюции нуклеиновых кислот, связавшихся с твердофазным сорбентом в микроколонке, выходной порт, совместимый со стандартной микропробиркой, резервуар для сбора отходов реакций (Фиг.2). В процессе изготовления в резервуар 2 объемом 1,5 мл помещают сухую смесь реагентов для лизирующего буфера, содержащую лизоцим, в резервуар 3 объемом 1,5 мл - сухую смесь реагентов для лизирующего буфера, содержащую хаотропный агент, протеиназу К и детергент, в резервуар 5 объемом 1,0 мл - сухую смесь реагентов для промывочного буфера, содержащую хаотропный агент; микроколонку 8 заполняют твердофазным сорбентом для связывания нуклеиновых кислот, резервуар 4 объемом 0,5 мл и резервуар 7 объемом 1,0 мл - этанолом, резервуар 6 объемом 0,5 мл - смесью этанол-вода, резервуар 9 объемом 0,2 мл - водой. Объем резервуара для сбора отходов реакций составляет 5,0 мл.
Картридж содержит только резервуары с реагентами и клапаны для коммутации газожидкостных потоков, в то время как все необходимые электромагнитные компоненты, осуществляющие подачу давления, перемещение реакционных смесей и реагентов в резервуарах картриджа, нагрев и перемешивание в индивидуальных резервуарах картриджа, размещены в управляющей установке-контроллере. Управляющая установка-контроллер обеспечивает заданные скорости перемещения реакционных смесей и реагентов в резервуарах картриджа, температурно-временные режимы инкубации и перемешивания реакционных смесей в отдельных резервуарах картриджа.
Готовый к работе картридж помещают в управляющую установку-контроллер. Ввод картриджа происходит вдоль верхних и нижних направляющих салазок (см. Фиг.4), которые обеспечивают его точное позиционирование.
Биологический образец помещают в приемную камеру картриджа, и далее все стадии лизиса клеток, микроорганизмов и вирусных частиц, очистки и элюции нуклеиновых кислот осуществляются последовательно в резервуарах картриджа, изолированных от внешней среды. Процедура выделения и очистки НК с использованием данного устройства управляется компьютером.
После введения биологического образца в приемную камеру картриджа осуществляются последовательные стадии его обработки. Процедура выделения и очистки НК состоит из следующих стадий (Фиг.2):
а) лизис клеток, микроорганизмов и вирусных частиц с использованием лизирующего буфера, содержащего лизоцим.
Биологический образец (100-500 мл) помещают в приемную камеру 1 с помощью пипетки или любого дозирующего устройства. Открывается клапан а, и образец поступает в резервуар 2. Клапан b и остальные клапаны закрыты. В резервуаре 2 происходит растворение сухой реакционной смеси для лизирующего буфера, содержащего лизоцим, причем растворителем является жидкий биологический образец. Растворение сухой реакционной смеси буфера для лизиса, содержащего лизоцим, и разрушение компонентов клеточной стенки микроорганизмов и вирусного капсида после поступления биологического образца из приемной камеры в резервуар 2 происходят одновременно при интенсивном перемешивании и нагревании до температуры 37°С в течение 10 мин.
Перемешивание осуществляется блоком электромагнитных мешалок, а нагревание - блоком галогенных ламп нагревателя, входящих в состав управляющей установки-контроллера.
В качестве лизирующего буфера, содержащего лизоцим, используют, например, 10 мМ трис-НС1 буфер, содержащий 1 мМ этилендиаминтетрауксусной кислоты и 50 мг/мл лизоцима, рН 8,0.
б) лизис клеток, микроорганизмов и вирусных частиц с использованием лизирующего буфера, содержащего хаотропный агент, протеиназу К, детергент.
Через открытый клапан b (остальные клапаны закрыты) реакционная смесь поступает в резервуар 3. В резервуаре 3 происходит растворение сухой реакционной смеси для лизирующего буфера, содержащего хаотропный агент, протеиназу К, детергент, причем растворителем является жидкий биологический образец, поступивший из резервуара 2 и обработанный буфером для лизиса, содержащего лизоцим. Растворение сухой реакционной смеси буфера для лизиса, содержащего хаотропный агент, протеиназу К, детергент, и окончательное разрушение клеток, микроорганизмов и вирусов с высвобождением нуклеиновых кислот происходят одновременно при интенсивном перемешивании и нагревании до температуры 55°С в течение 10 мин.
Во время осуществления процедуры лизиса в резервуаре 3 растворитель для промывочного буфера (смесь этанол-вода) из резервуара 6 поступает в резервуар 5, содержащий сухую реакционную смесь промывочного буфера, в состав которой входит хаотропный агент (клапан е открыт, клапан f закрыт). Растворение сухой реакционной смеси буфера для промывки происходит в резервуаре 5 при перемешивании и нагревании до температуры 55°С.
Перемешивание осуществляется блоком электромагнитных мешалок, а нагревание - блоком галогенных ламп нагревателя, входящих в состав управляющей установки-контроллера.
В качестве хаотропного агента, входящего в состав одного из буферов для лизиса и буфера для промывки, используют гуанидинтиоцианат или гуанидингидрохлорид, в качестве детергента - Тритон Х-100 или N-лаурилсаркозил.
В качестве лизирующего буфера, содержащего хаотропный агент, протеиназу К, детергент, используют, например, 10 мМ трис-НС1 буфер, содержащий 1 мМ этилендиаминтетрауксусной кислоты, 4,5 М гуанидингидрохлорида, 1 мг/мл протеиназы К, 0,5% Тритон Х-100, рН 8,0.
в) добавление этанола к полученному лизату биологического образца.
С целью создания оптимальных условий связывания нуклеиновых кислот с твердофазным сорбентом к лизату биологического образца, полученному после обработки вторым лизирующим буфером, в резервуар 3 добавляют этанол из резервуара 4 (клапан с открыт, остальные клапаны закрыты).
г) связывание нуклеиновых кислот на микроколонке, содержащей твердофазный сорбент.
Реакционная смесь из резервуара 3 после лизиса и добавления этанола, содержащая нуклеиновые кислоты и белки, поступает на микроколонку 8 с твердофазным сорбентом. Нуклеиновые кислоты сорбируются на сорбенте, а вещества, не связавшиеся с носителем проходят в резервуар для сбора отходов 11 (клапаны d, h, k и m открыты, клапаны l, g, f, i и j закрыты).
Твердофазный сорбент выбирают из группы сорбентов, включающей силикагели, стекловолоконные фильтры, химически модифицированное стекло.
д) отмывка нуклеиновых кислот от белков и кристаллов соли на микроколонке, содержащей твердофазный сорбент, с использованием промывочного буфера и этанола;
Для отмывки твердофазного сорбента от белков на микроколонку подается промывочный буфер из резервуара 5; промывочный раствор проходит в резервуар для сбора отходов 11 (клапаны f, h, k и m открыты, клапаны l, g, d, i и j закрыты).
Для отмывки твердофазного сорбента от кристаллов соли на микроколонку подается этанол из резервуара 7; промывочный раствор проходит в резервуар для сбора отходов 11 (клапаны g, h, k и m открыты, клапаны l, f, d, i и j закрыты).
е) элюция нуклеиновых кислот с микроколонки.
После промывки носителя нуклеиновые кислоты элюируют пропусканием через микроколонку раствора для элюции НК (вода) из резервуара 9 (клапаны i, h, j открыты, клапаны l, g, f, d, k и m закрыты). НК поступают в резервуар для сбора очищенной НК 10.
Выходной порт картриджа совместим со стандартной микропробиркой объемом 0,2 мл, которую можно использовать для проведения ПЦР.
Растворение сухих реакционных смесей обоих буферов для лизиса и буфера для промывки происходит при нагревании и перемешивании с помощью устройств, входящих в состав управляющей установки-контроллера. Все клапаны, регулирующие перемещение реакционных смесей и реагентов в каналах и резервуарах картриджа (клапаны а-m на Фиг.2) управляются установкой-контроллером.
Картридж состоит из нескольких конструктивных элементов: основная рабочая платформа, содержащая резервуары с реагентами, каналы, микроколонку и резервуар для сбора отходов реакций, верхняя и нижняя панели (крышки), эластичные прокладки (Фиг.3). Материал основной рабочей платформы и верхней и нижней панелей картриджа выбирают из группы полимеров, не сорбирующих нуклеиновые кислоты, включающей оргстекло, полипропилен, поликарбонат. Материал прокладок картриджа выбирают из группы эластичных материалов, не сорбирующих НК, включающей силикон, полиэтилен.
Например, в одном из воплощений основная рабочая платформа и верхняя и нижняя панели картриджа сделаны из оргстекла (Акрима 72), толщина 8 мм и 2 мм соответственно, эластичные прокладки - из силикона Силастик Т4, толщина 2 мм, и полиэтиленовой пленки универсальной, сорт Н, толщина 50 мкм.
Элементы картриджа скреплены между собой 4 фиксирующими винтами, расположенными по краям панелей. На верхней панели расположены 16 отверстий для поршней клапанов, отверстие для приемной камеры образца, 4 отверстия для фиксирующих винтов (см. Фиг 3). Линейные размеры картриджа (длина×ширина×высота) составляют 94×64×40 мм.
Управляющая установка-контроллер содержит блок соленоидов для управления клапанами картриджа, блок поршней, блок нагревателей, блок электромагнитных мешалок, компрессор и блок электронного управления (Фиг.4). Коммутация воздушных и жидкостных потоков в картридже осуществляется 16 клапанами с электрическим управлением. После помещения картриджа в блок управления и срабатывания запорного механизма картридж занимает положение, при котором штоки всех 16 соленоидов оказываются точно над соответствующими запорными головками клапанов картриджа.
Перемещение реакционных смесей и реагентов в резервуарах картриджа осуществляется подачей давления в соответствующие резервуары с помощью компрессора по системе каналов, причем перераспределение давления по резервуарам и потоки жидкостей по каналам организованы системой клапанов, выполненных с использованием эластичной прокладки картриджа. Компрессор представляет собой мембранный либо плунжерный насос, способный создавать избыточное давление воздуха до 2 атм.
Диаграмма устройства клапана приведена на Фиг.5. Клапан состоит из соленоида, поршня и запорной головки. Поршень обеспечивает необходимое давление на запорную головку клапана, удерживая клапан в закрытом положении. При подаче напряжения на обмотку соленоида поршень поднимается, освобождая запорную головку клапана, и клапан открывается. Клапан вмонтирован в основную рабочую платформу картриджа (Б), в которой проделаны два отверстия 0,8 мм в диаметре для входа и выхода (IN и OUT). Между основной рабочей платформой (Б) и верхней панелью (А) находятся эластичные прокладки П1 и П2, которые обеспечивают открытие и закрытие клапана и, соответственно, возможность перетекания жидкости из резервуаров картриджа.
Для формирования рабочих поверхностей клапанов используют, например, полиэтилен и тефлон.
Представленная полезная модель позволяет проводить выделение и очистку НК из биологического образца (кровь, плазма, слюна, культуральные жидкости), содержащего 104 или более клеток, бактерий и/или вирусных частиц. Результаты выделения НК из бактериальных клеток и вирусных частиц представлены на Фиг.6 и 7. Полезная модель позволяет проводить выделение НК клеток микроорганизмов и/или вирусов в автоматическом режиме с низкими потерями, низкой себестоимостью, малым временем, необходимым для получения результата. Способ не требует дорогостоящего оборудования и высококвалифицированного персонала. Полученный препарат НК может быть использован без дополнительной очистки непосредственно в амплификации (Фиг.7) или гибридизации НК с целью непосредственной идентификации инфекционного агента в исследуемом образце или для проведения дальнейшего молекулярно-генетического анализа.
Claims (18)
1. Устройство для автоматизированного выделения нуклеиновых кислот из биологических образцов, состоящее из (а) картриджа, содержащего резервуары с реагентами для лизиса клеток, микроорганизмов и вирусных частиц, очистки и элюции нуклеиновых кислот, каналы, микроколонки и клапаны, и (б) управляющей установки-контроллера, осуществляющей подачу давления, нагрев, перемешивание реагентов в индивидуальных резервуарах картриджа и перемещение реакционных смесей и растворов в резервуарах картриджа, характеризующееся тем, что картридж содержит приемную камеру для ввода биологического образца, резервуары с сухими реакционными смесями буферов для лизиса и буфера для промывки, микроколонку с твердофазным сорбентом для связывания нуклеиновых кислот, резервуары для этанола, смеси вода-этанол и воды для растворения сухих компонентов промывочного буфера, промывки микроколонки и элюции нуклеиновых кислот, связавшихся с твердофазным сорбентом в микроколонке, выходной порт, совместимый со стандартной микропробиркой, резервуар для сбора отходов реакций, а управляющая установка-контроллер содержит блок соленоидов для управления клапанами картриджа, блок нагревателей, блок электромагнитных мешалок, компрессор и блок электронного управления.
2. Устройство по п.1, характеризующееся тем, что картридж помещают в управляющую установку-контроллер, обеспечивающую заданные скорости перемещения реакционных смесей и реагентов в резервуарах картриджа, температурно-временные режимы инкубации и перемешивания реакционных смесей в отдельных резервуарах картриджа.
3. Устройство по п.1, характеризующееся тем, что картридж содержит только резервуары с реагентами и клапаны для коммутации газожидкостных потоков, в то время как все необходимые электромагнитные компоненты, осуществляющие подачу давления, перемещение реакционных смесей и реагентов в резервуарах картриджа, нагрев и перемешивание в индивидуальных резервуарах картриджа, размещены в управляющей установке-контроллере.
4. Устройство по п.1, характеризующееся тем, что биологический образец помещают в приемную камеру картриджа, и далее все стадии лизиса клеток, микроорганизмов и вирусных частиц, очистки и элюции нуклеиновых кислот осуществляются последовательно в резервуарах картриджа, изолированных от внешней среды.
5. Устройство по п.1, характеризующееся тем, что после введения биологического образца в приемную камеру картриджа осуществляются последовательные стадии его обработки, включающие:
а) лизис клеток, микроорганизмов и вирусных частиц с использованием лизирующего буфера, содержащего лизоцим;
б) лизис клеток, микроорганизмов и вирусных частиц с использованием лизирующего буфера, содержащего хаотропный агент, протеиназу K, детергент;
в) добавление этанола к полученному лизату биологического образца с целью создания оптимальных условий связывания нуклеиновых кислот с твердофазным сорбентом;
г) связывание нуклеиновых кислот на микроколонке, содержащей твердофазный сорбент;
д) отмывку нуклеиновых кислот от белков и кристаллов соли на микроколонке, содержащей твердофазный сорбент, с использованием промывочного буфера и этанола;
е) элюцию нуклеиновых кислот с микроколонки.
6. Устройство по п.1, характеризующееся тем, что картридж состоит из следующих конструктивных элементов: основная рабочая платформа, содержащая резервуары с реагентами, каналы, микроколонку и резервуар для сбора отходов реакций, верхняя и нижняя панели (крышки), эластичные прокладки.
7. Устройство по п.6, характеризующееся тем, что материал основной рабочей платформы и верхней и нижней панелей картриджа выбирают из группы полимеров, не сорбирующих нуклеиновые кислоты, включающей оргстекло, полипропилен, поликарбонат.
8. Устройство по п.6, характеризующееся тем, что материал прокладок картриджа выбирают из группы эластичных материалов, не сорбирующих нуклеиновые кислоты, включающей силикон, полиэтилен.
9. Устройство по п.1, характеризующееся тем, что перемещение реакционных смесей и реагентов в резервуарах картриджа осуществляется подачей давления в соответствующие резервуары по системе каналов, причем перераспределение давления по резервуарам и потоки жидкостей по каналам организованы системой клапанов, выполненных с использованием эластичной прокладки картриджа.
10. Устройство по п.1, характеризующееся тем, что картридж содержит резервуары с сухими реакционными смесями буфера для лизиса, содержащего лизоцим, буфера для лизиса, содержащего хаотропный агент, протеиназу K, детергент, и буфера для промывки, содержащего хаотропный агент, и резервуары, в которых жидкими компонентами являются только вода и этанол.
11. Устройство по п.1, характеризующееся тем, что растворителем для сухих реакционных смесей обоих буферов для лизиса является жидкий биологический образец, а растворителем для сухой реакционной смеси промывочного буфера является смесь вода-этанол, подающаяся из соответствующий резервуара.
12. Устройство по п.1, характеризующееся тем, что растворение сухих реакционных смесей обоих буферов для лизиса и буфера для промывки происходит при нагревании и перемешивании с помощью устройств, входящих в состав управляющей установки-контроллера.
13. Устройство по п.1, характеризующееся тем, что растворение сухой реакционной смеси буфера для лизиса, содержащего лизоцим, и разрушение компонентов клеточной стенки микроорганизмов и вирусного капсида после поступления биологического образца из приемной камеры в соответствующий резервуар происходят одновременно при перемешивании и нагревании.
14. Устройство по п.1, характеризующееся тем, что после поступления в соответствующий резервуар биологического образца, обработанного буфером для лизиса, содержащего лизоцим, растворение сухой реакционной смеси буфера для лизиса, содержащего хаотропный агент, протеиназу K и детергент, окончательное разрушение клеток, микроорганизмов и вирусов с высвобождением нуклеиновых кислот происходят одновременно при перемешивании и нагревании.
15. Устройство по пп.12-14, характеризующееся тем, что перемешивание осуществляется блоком электромагнитных мешалок, а нагревание осуществляется блоком галогенных ламп нагревателя, входящих в состав управляющей установки-контроллера.
16. Устройство по п.10, характеризующееся тем, что в качестве хаотропного агента, входящего в состав одного из буферов для лизиса и буфера для промывки, используют гуанидинтиоцианат или гуанидингидрохлорид.
17. Устройство по п.1, характеризующееся тем, что твердофазный сорбент для связывания нуклеиновых кислот выбирают из группы сорбентов, включающей силикагели, стекловолоконные фильтры, химически модифицированное стекло.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2009105294/22U RU84381U1 (ru) | 2009-02-17 | 2009-02-17 | Устройство для автоматизированного выделения нуклеиновых кислот |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2009105294/22U RU84381U1 (ru) | 2009-02-17 | 2009-02-17 | Устройство для автоматизированного выделения нуклеиновых кислот |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU84381U1 true RU84381U1 (ru) | 2009-07-10 |
Family
ID=41046204
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2009105294/22U RU84381U1 (ru) | 2009-02-17 | 2009-02-17 | Устройство для автоматизированного выделения нуклеиновых кислот |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU84381U1 (ru) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2484139C1 (ru) * | 2012-05-17 | 2013-06-10 | Общество с ограниченной ответственностью "Научно-Производственное Объединение ДНК-Технология" | Устройство для выделения нуклеиновых кислот |
| RU2545404C2 (ru) * | 2010-04-30 | 2015-03-27 | Байонир Корпорейшн | Устройство для автоматической очистки биологических образцов, оснащенное элементом для приложения магнитного поля, способ извлечения целевого вещества из биологического образца и способ экспрессии и очистки белка |
| RU2595374C2 (ru) * | 2014-04-09 | 2016-08-27 | Федеральное Государственное Бюджетное Учреждение Науки Институт Молекулярной Биологии Им. В.А. Энгельгардта Российской Академии Наук (Имб Ран) | Способ автоматизированного выделения с одновременной очисткой нуклеиновых кислот из нескольких биологических образцов |
| RU2630642C1 (ru) * | 2016-11-15 | 2017-09-11 | Общество с ограниченной ответственностью "Научно Производственное Объединение ДНК-Технология" | Устройство для выделения нуклеиновых кислот |
| RU2645088C2 (ru) * | 2012-06-25 | 2018-02-15 | Инпеко Холдинг Лтд. | Устройство с множеством штативов для размещения емкостей с биологическим продуктом, выгружаемых из хранилища для хранения упомянутых емкостей, связанного с лабораторной автоматизированной системой |
| RU2681914C2 (ru) * | 2013-10-15 | 2019-03-13 | Байо Молекьюлар Системс Пти Лтд | Усовершенствованный амплификатор |
| RU2768005C1 (ru) * | 2021-09-02 | 2022-03-22 | Общество С Ограниченной Ответственностью "Тробио" | Одноразовый картридж для выделения нуклеиновых кислот и их последующей амплификации (варианты) |
| RU2784821C2 (ru) * | 2020-10-26 | 2022-11-29 | Российская Федерация, от имени которой выступает Министерство обороны Российской Федерации | Автоматизированный прибор для выделения, очистки и анализа нуклеиновых кислот методом пцр-рв |
-
2009
- 2009-02-17 RU RU2009105294/22U patent/RU84381U1/ru active IP Right Revival
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2545404C2 (ru) * | 2010-04-30 | 2015-03-27 | Байонир Корпорейшн | Устройство для автоматической очистки биологических образцов, оснащенное элементом для приложения магнитного поля, способ извлечения целевого вещества из биологического образца и способ экспрессии и очистки белка |
| RU2484139C1 (ru) * | 2012-05-17 | 2013-06-10 | Общество с ограниченной ответственностью "Научно-Производственное Объединение ДНК-Технология" | Устройство для выделения нуклеиновых кислот |
| RU2645088C2 (ru) * | 2012-06-25 | 2018-02-15 | Инпеко Холдинг Лтд. | Устройство с множеством штативов для размещения емкостей с биологическим продуктом, выгружаемых из хранилища для хранения упомянутых емкостей, связанного с лабораторной автоматизированной системой |
| RU2681914C2 (ru) * | 2013-10-15 | 2019-03-13 | Байо Молекьюлар Системс Пти Лтд | Усовершенствованный амплификатор |
| RU2595374C2 (ru) * | 2014-04-09 | 2016-08-27 | Федеральное Государственное Бюджетное Учреждение Науки Институт Молекулярной Биологии Им. В.А. Энгельгардта Российской Академии Наук (Имб Ран) | Способ автоматизированного выделения с одновременной очисткой нуклеиновых кислот из нескольких биологических образцов |
| RU2630642C1 (ru) * | 2016-11-15 | 2017-09-11 | Общество с ограниченной ответственностью "Научно Производственное Объединение ДНК-Технология" | Устройство для выделения нуклеиновых кислот |
| RU2784821C2 (ru) * | 2020-10-26 | 2022-11-29 | Российская Федерация, от имени которой выступает Министерство обороны Российской Федерации | Автоматизированный прибор для выделения, очистки и анализа нуклеиновых кислот методом пцр-рв |
| RU2768005C1 (ru) * | 2021-09-02 | 2022-03-22 | Общество С Ограниченной Ответственностью "Тробио" | Одноразовый картридж для выделения нуклеиновых кислот и их последующей амплификации (варианты) |
| RU2790849C1 (ru) * | 2022-08-27 | 2023-02-28 | Общество С Ограниченной Ответственностью "Тробио" | Одноразовый картридж для выделения нуклеиновых кислот и их последующей амплификации |
| RU221186U1 (ru) * | 2023-04-20 | 2023-10-24 | Общество с ограниченной ответственностью "Биодайв" | Картридж для детекции молекул |
| RU2828813C1 (ru) * | 2023-06-26 | 2024-10-21 | Автономная некоммерческая образовательная организация высшего образования "Научно-технологический университет "Сириус" | Способ очистки и выделения высокомолекулярных нуклеиновых кислот, гель и устройство для его осуществления |
| RU2828813C9 (ru) * | 2023-06-26 | 2024-12-10 | Автономная некоммерческая образовательная организация высшего образования "Научно-технологический университет "Сириус" | Способ очистки и выделения высокомолекулярных нуклеиновых кислот, гель и устройство для его осуществления |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2380418C1 (ru) | Сменный микрофлюидный модуль для автоматизированного выделения и очистки нуклеиновых кислот из биологических образцов и способ выделения и очистки нуклеиновых кислот с его использованием | |
| US10464065B2 (en) | Nucleic acid purification | |
| US9028777B2 (en) | Automated cellular material preparation | |
| US9506847B2 (en) | Method and system for selective isolation of target biological molecules in a general purpose system | |
| US20240353439A1 (en) | Fluidic bridge device and sample processing methods | |
| RU84381U1 (ru) | Устройство для автоматизированного выделения нуклеиновых кислот | |
| CN113817600A (zh) | 样品处理及检测装置及其应用 | |
| US20080153078A1 (en) | System for isolating biomolecules from a sample | |
| CN1717280A (zh) | 用于处理流体样本的设备 | |
| RU110746U1 (ru) | Устройство для одновременного автоматизированного выделения и очистки нуклеиновых кислот из нескольких биологических образцов | |
| CN205570357U (zh) | 一种提取及检测生物样本的装置 | |
| AU2017235971B2 (en) | Nucleic Acid Purification | |
| WO2007122819A1 (ja) | 液体を媒体とする反応のための装置 | |
| WO2020113192A1 (en) | Systems and methods for on-chip analysis of nucleic acids and for multiplexed analysis of cells | |
| RU2595374C2 (ru) | Способ автоматизированного выделения с одновременной очисткой нуклеиновых кислот из нескольких биологических образцов | |
| RU134929U1 (ru) | Устройство для экстракции и очистки нуклеиновых кислот (микронк) | |
| WO2004048564A1 (ja) | 検体前処理デバイス | |
| Gärtner et al. | A microfluidic toolbox approach to CBRNE sensing | |
| AU2013205155A1 (en) | Nucleic acid purification |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM1K | Utility model has become invalid (non-payment of fees) |
Effective date: 20120218 |
|
| NF1K | Reinstatement of utility model |
Effective date: 20140110 |