RU2752902C1 - Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 - Google Patents
Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 Download PDFInfo
- Publication number
- RU2752902C1 RU2752902C1 RU2021101361A RU2021101361A RU2752902C1 RU 2752902 C1 RU2752902 C1 RU 2752902C1 RU 2021101361 A RU2021101361 A RU 2021101361A RU 2021101361 A RU2021101361 A RU 2021101361A RU 2752902 C1 RU2752902 C1 RU 2752902C1
- Authority
- RU
- Russia
- Prior art keywords
- cov
- sars
- rna
- coronavirus
- abl1
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 30
- 238000001514 detection method Methods 0.000 title claims abstract description 15
- 108091034117 Oligonucleotide Proteins 0.000 title description 10
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 title description 9
- 238000007403 mPCR Methods 0.000 title description 4
- 241001678559 COVID-19 virus Species 0.000 claims abstract description 49
- 239000002773 nucleotide Substances 0.000 claims abstract description 24
- 125000003729 nucleotide group Chemical group 0.000 claims abstract description 24
- 238000012360 testing method Methods 0.000 claims abstract description 16
- 230000000295 complement effect Effects 0.000 claims abstract description 14
- 239000007850 fluorescent dye Substances 0.000 claims abstract description 13
- 239000003155 DNA primer Substances 0.000 claims abstract description 12
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 12
- 101100268646 Homo sapiens ABL1 gene Proteins 0.000 claims abstract description 3
- 108091032973 (ribonucleotides)n+m Proteins 0.000 claims description 40
- 238000006243 chemical reaction Methods 0.000 claims description 18
- 239000002299 complementary DNA Substances 0.000 claims description 13
- 108020004999 messenger RNA Proteins 0.000 claims description 12
- 239000000523 sample Substances 0.000 claims description 10
- 239000000203 mixture Substances 0.000 claims description 6
- 108010006785 Taq Polymerase Proteins 0.000 claims description 3
- 239000001226 triphosphate Substances 0.000 claims description 3
- 235000011178 triphosphate Nutrition 0.000 claims description 3
- 125000002264 triphosphate group Chemical class [H]OP(=O)(O[H])OP(=O)(O[H])OP(=O)(O[H])O* 0.000 claims description 2
- 208000025721 COVID-19 Diseases 0.000 abstract description 19
- 101000823316 Homo sapiens Tyrosine-protein kinase ABL1 Proteins 0.000 abstract description 18
- 239000000463 material Substances 0.000 abstract description 12
- 230000003321 amplification Effects 0.000 abstract description 9
- 238000003199 nucleic acid amplification method Methods 0.000 abstract description 9
- 230000002068 genetic effect Effects 0.000 abstract description 5
- 238000003745 diagnosis Methods 0.000 abstract description 4
- 238000003759 clinical diagnosis Methods 0.000 abstract description 3
- 239000003814 drug Substances 0.000 abstract description 3
- 238000002123 RNA extraction Methods 0.000 abstract description 2
- 238000012544 monitoring process Methods 0.000 abstract description 2
- 238000005070 sampling Methods 0.000 abstract description 2
- 230000000694 effects Effects 0.000 abstract 1
- 238000003757 reverse transcription PCR Methods 0.000 abstract 1
- 239000000126 substance Substances 0.000 abstract 1
- 238000003753 real-time PCR Methods 0.000 description 14
- 241000711573 Coronaviridae Species 0.000 description 12
- 108091028043 Nucleic acid sequence Proteins 0.000 description 8
- 239000013615 primer Substances 0.000 description 8
- 102100022596 Tyrosine-protein kinase ABL1 Human genes 0.000 description 7
- 239000003153 chemical reaction reagent Substances 0.000 description 7
- 241000008904 Betacoronavirus Species 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 238000010839 reverse transcription Methods 0.000 description 6
- 201000010099 disease Diseases 0.000 description 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 5
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 5
- 238000002955 isolation Methods 0.000 description 5
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 4
- 201000003176 Severe Acute Respiratory Syndrome Diseases 0.000 description 4
- 210000001989 nasopharynx Anatomy 0.000 description 4
- 238000011161 development Methods 0.000 description 3
- 231100000676 disease causative agent Toxicity 0.000 description 3
- 230000014509 gene expression Effects 0.000 description 3
- 210000003928 nasal cavity Anatomy 0.000 description 3
- 210000003300 oropharynx Anatomy 0.000 description 3
- 238000003752 polymerase chain reaction Methods 0.000 description 3
- 239000013641 positive control Substances 0.000 description 3
- 230000035945 sensitivity Effects 0.000 description 3
- 108020004414 DNA Proteins 0.000 description 2
- 101100110026 Danio rerio ascl1b gene Proteins 0.000 description 2
- 239000012620 biological material Substances 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 238000011109 contamination Methods 0.000 description 2
- 230000007123 defense Effects 0.000 description 2
- 102000048392 human ABL1 Human genes 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 239000002987 primer (paints) Substances 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 238000007480 sanger sequencing Methods 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- JEPVUMTVFPQKQE-AAKCMJRZSA-N 2-[(1s,2s,3r,4s)-1,2,3,4,5-pentahydroxypentyl]-1,3-thiazolidine-4-carboxylic acid Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)C1NC(C(O)=O)CS1 JEPVUMTVFPQKQE-AAKCMJRZSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical group C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- 108700039887 Essential Genes Proteins 0.000 description 1
- 101150001779 ORF1a gene Proteins 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 241000008910 Severe acute respiratory syndrome-related coronavirus Species 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- -1 deoxyribonucleotide triphosphates Chemical class 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000012678 infectious agent Substances 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 230000007918 pathogenicity Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 238000003908 quality control method Methods 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 238000011896 sensitive detection Methods 0.000 description 1
- 230000010473 stable expression Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6806—Preparing nucleic acids for analysis, e.g. for polymerase chain reaction [PCR] assay
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- General Health & Medical Sciences (AREA)
- Analytical Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Plant Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Изобретение относится к области медицины и молекулярной биологии, а именно к молекулярно-генетической диагностике COVID-19 на основе выявления РНК коронавируса SARS-CoV-2. Синтезированные олигонуклеотидые праймеры и флуоресцентные зонды являются комплементарными исключительно нуклеотидной последовательности (ORF1ab и N участка) генома коронавируса SARS-CoV-2 и человеческого гена ABL1. А также разработан способ детекции РНК коронавируса SARS-CoV-2 с помощью мультиплексной ПЦР-РВ, основанной на амплификации ORF1ab и N участков гена коронавируса SARS-CoV-2 и человеческой РНК гена ABL1 в качестве внутреннего контроля. Изобретение позволяет достоверно подтвердить клинический диагноз COVID-19 с минимальным количеством исследуемого материала, 10 мкл, путем контроля качества отбора пробы и выделения РНК по амплификации РНК человеческого гена ABL1 и определения присутствия/отсутствия РНК коронавируса SARS-CoV-2 по амплификации относительно контрольных образцов. 2 н.п. ф-лы, 5 ил., 6 табл., 5 пр.
Description
Изобретение относится к области медицины и молекулярной биологии, а именно к молекулярно-генетической диагностике COVID-19 на основе выявления РНК коронавируса SARS-CoV-2 в биологическом материале пациентов с подозрением на COVID-19.
В конце декабря 2019 г. в городе Ухань (КНР) были отмечены первые случаи пневмонии, возбудителем которой оказался новый коронавирус 2019-nCoV. В начале февраля 2020 г. международный комитет по таксономии вирусов дал официальное название новому коронавирусу, как SARS-CoV-2 {Severe acute respiratory syndrome-related coronavirus 2), а заболевание получило название COVID-19 (Coronavirus disease 2019).
Выявление РНК вируса SARS-CoV-2 основано на постановке полимеразной цепной реакции в режиме реального времени (ПЦР-РВ) с обратной транскрипцией и рекомендовано Всемирной организацией здравоохранения (ВОЗ) в качестве молекулярно-генетического метода диагностики COVID-19 [1].
Известен «Набор синтетических олигонуклеотидов для выявления РНК коронавируса» [2], состоящий из 6 пар синтетических олигонуклеотидов. Однако, предлагаемый набор имеет ряд недостатков, заключающихся в том, что все 6 пар предлагаемых синтетических олигонуклеотидов являются специфичными только одному ORF1b участку генома коронавируса SARS-CoV-2 и предназначены для анализа ПЦР реакции по температуре плавления ПЦР продукта с присутствием интеркалирующего красителя SYBR Green или методом горизонтального гель-электрофореза. Таким образом, они не соответствуют критериям, рекомендованным ВОЗ для выявления РНК SARS-CoV-2 методом ПЦР-РВ. Также представленный способ обладает относительно низкой чувствительностью.
Известен «Способ выявления кДНК коронавируса SARS-CoV-2 с помощью синтетических олигонуклеотидных праймеров в полимеразной цепной реакции» [3]. Вышеуказанный способ имеет ряд недостатков, а именно: способ имеет низкую чувствительность, обусловленную электрофоретической детекцией ПЦР продуктов в 1,5%-ном агарозном геле, также отсутствует возможность контроля эффективности прохождения ПЦР реакции, что отражено на рисунке 1 в описании к изобретению, где количество ПЦР продукта значительно меньше в реакции с праймерами на участок ORF1ab по сравнению с праймерами на участок N1. Кроме того, имеется высокий риск контаминации при работе с ПЦР продуктом на этапах электрофоретической детекции и необходимость наличия достаточного количества исходного материала, так как реакция для исследования одного образца должна проходить в 4-х отдельных пробирках.
Известен метод обнаружения коронавируса [4]. Основным недостатком предложенного способа обнаружения коронавируса является низкая чувствительность, обусловленная использованием для визуализации продукта амплификации тест полосок (из фильтровальной бумаги или хитозана, пропитанных стрептавидином) по сравнению с рекомендованной ВОЗ.
Известны «Тест-система и способ для выявления РНК коронавируса SARS-COV-2, вируса-возбудителя коронавирусного заболевания 2019 COVID-19 методом полимеразной цепной реакции в режиме реального времени (варианты)» [5]. Основным недостатком описанного способа является использование в качестве положительного контроля праймеров специфичных для мРНК человеческих генов GAPDH (SBT0014 и SBT0015) и АСТВ (SBT0011 и SBT0012), амплифицирующих в реакции ПЦР также геномные последовательности ДНК GAPDH (NG_007073.2) и АСТВ (NG 007992.1). Учитывая, что в исходном материале мРНК всегда присутствуют примеси человеческой ДНК, использование этих праймеров в качестве внутреннего контроля прохождения реакции обратной транскрипции (получения кДНК) не корректно. Более того, сравнение уровней экспрессии GAPDH в 72 различных тканях человека показало относительно низкую экспрессию его в органах дыхательной системы [6].
Также, Ishige Т. и соавторами была опубликована статья о высокочувствительной мультиплексной RT-PCR для молекулярной диагностики COVID-19 в клинических лабораториях с использованием ранее известных праймеров, в том числе для человеческой мРНК гена ABL1 [7]. Однако, нуклеотидные последовательности праймеров и зонда для мРНК ABL1, заимствованные из работ Beillard, Е и соавторов, могут также амплифицировать геномную нуклеотидную последовательность ABL1 человека [8] и не эффективны для контроля прохождения реакции обратной транскрипции.
Основной задачей, решаемой настоящим изобретением является синтез специфичных синтетических олигонуклеотидов и флуоресцентных зондов, амплифицирующих в реакции ПЦР-РВ только нуклеотидные последовательности генома коронавируса SARS-CoV-2 и человеческой мРНК со стабильной экспрессией в различных клетках человека. А также разработка способа мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2, гарантирующего надежный результат анализов по двум областям генома коронавируса, и не имеющего перечисленных выше недостатков.
Поставленная задача решается данной группой изобретений. В рамках данной разработки сконструированы синтетические олигонуклеотидные праймеры и флуоресцентные зонды с оригинальной нуклеотидной последовательностью специфичной двум (ORFlab и N) генам SARS-CoV-2 и разработан надежный способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2. Разработанный способ из-за мультиплексности (все реакция по трем каналам проходят в одной пробирке с 10 мкл кДНК) процесса амплификации требует малое количество исследуемого материала и содержит в качестве внутреннего контроля синтезированные олигонуклеотидные праймеры и флуоресцентный зонд человеческого гена ABL1, позволяющие контролировать качество и количество исследуемого образца, при этом не имеет риска контаминации при использовании.
Технический результат изобретения заключается в расширении арсенала средств молекулярно-генетической диагностики коронавирусной болезни COVID-19, а также в повышении достоверности и надежности диагностики новой инфекции, за счет гарантированного определения наличия в образце достаточного количества генетического материала человека.
Дополнительным техническим результатом является возможность проведения анализа с относительно низким количеством исследуемого материала за счет совмещенности ПЦР-РВ в одной пробирке, и использования внутреннего контроля определения высококопийной мРНК человека, позволяющий оценить наличие человеческого биологического материала в мазке и, таким образом, исключить ложно-отрицательные результаты, связанные с некачественным взятием мазка или попыткой фальсификации пробы.
Сущность изобретения пояснена на графических материалах: Фиг. 1 - где число циклов (Ct) и кривые накопления продуктов мультиплексной ПЦР-РВ представлены по трем разным каналам детекции: человеческой кДНК ABL1 в желтом (RG) и генов ORF1ab и гена N коронавируса SARS-CoV-2 в оранжевом (ROX) и красном каналах (Су5); Фиг. 2 - Схематическое представление графических кривых и пороговых циклов мультиплексной ПЦР-РВ по трем каналам амплификации и варианты интерпретации результатов анализа;
Фиг. 3 - Графики кривых мультиплексной ПЦР-РВ и значение пороговых циклов человеческого гена ABL1 и ORFlab коронавируса SARS-CoV-2 в материале от пациентов с COVID-19 и здоровых доноров;
Фиг. 4 - Графики кривых ПЦР-РВ и значение пороговых циклов человеческого гена ABL1 и ORF1ab коронавируса SARS-CoV-2
Примечание:
№536 и 537 образцы мазков, взятых из носовой полости и ротоглотки пациентов с подозрением на COVID-19,
ПКО - положительный контрольный образец, содержащий кДНК SARS-CoV-2, выделенную из мазка носовой полости пациента с COVID-19,
ОКО - отрицательный контрольный образец, содержащий кДНК ABL1, выделенную из мазка носовой полости здорового человека;
Фиг. 5 - Хроматограмма прямого секвенирования по Сэнгеру ORFla участка генома SARS-CoV-2.
Сущность изобретения пояснена следующими перечнями последовательностей нуклеотидов, комплементарных участкам генома коронавируса SARS-CoV-2 (NC_045512.2) и ABL1 (NM_005157.6):
SEQ ID NO: 1 последовательность нуклеотидов комплементарная 3211-3234 нуклеотидам генома коронавируса SARS-CoV-2;
SEQ ID NO: 2 последовательность нуклеотидов комплементарная 3307-3328 нуклеотидам генома коронавируса SARS-CoV-2;
SEQ ID NO: 3 последовательность нуклеотидов комплементарная 3240-3262 нуклеотидам генома коронавируса SARS-CoV-2;
SEQ ID NO: 4 последовательность нуклеотидов комплементарная 28715-28734 нуклеотидам генома коронавируса SARS-CoV-2;
SEQ ID NO: 5 последовательность нуклеотидов комплементарная 28774-28793 нуклеотидам генома коронавируса SARS-CoV-2;
SEQ ID NO:6 последовательность нуклеотидов комплементарная 28735-28759 нуклеотидам генома коронавируса SARS-CoV-2;
SEQ ID NO:7 последовательность нуклеотидов комплементарная 684-703 нуклеотидам мРНК ABL1;
SEQ ID NO: 8 последовательность нуклеотидов комплементарная 748-768 нуклеотидам мРНК ABL1;
SEQ ID NO: 9 последовательность нуклеотидов комплементарная 777-796 нуклеотидам мРНК ABL1;
Конкретная реализация заявляемого изобретения представлена созданием синтетических олигонуклеотидных праймеров и флуоресцентных зондов для детекции РНК коронавируса SARS-CoV-2, комплементарных уникальным нуклеотидным последовательностям генов коронавируса SARS-CoV-2, нуклеотидные последовательности которых представлены в таблице 1, и мРНК человеческого гена ABL1, нуклеотидные последовательности которого представлены в таблице 2, а также разработкой способа мультиплексной ПЦР-РВ.
Способ выявления РНК коронавируса SARS-CoV-2 с помощью мультиплексной ПЦР-РВ осуществляется с использованием разработанных олигонуклеотидных праймеров и флуоресцентных зондов (таблица 1), 10х ПЦР буфера, смеси четырех дезоксирибонуклеотидтрифосфатов, MqCl2, Taq полимеразы, положительного (ПКО) и отрицательного (ОКО) контрольных образцов, внутреннего контроля, в виде олигонуклеотидных праймеров и флуоресцентного зонда человеческого гена ABL1 (таблица 2). Перечень, концентрация и объем компонентов представлены в таблице 3.
Сущность группы изобретений пояснена примерами конкретной реализации, которые не ограничивают объем изобретения. Пример 1. Постановка мультиплексной ПЦР-РВ.
Выявление РНК коронавируса SARS-CoV-2 осуществляют с помощью мультиплексной ПЦР-РВ в одной пробирке, способ включает следующие этапы.
Отбор исследуемого материала. Исследуемый материал отбирается из носоглотки или ротоглотки с использованием специальных тампонов и полным соблюдением требований безопасности при работе с инфекционными агентами 2-3 группы патогенности.
Выделение РНК исследуемого материала. Выделение РНК из содержимого осуществляется общепринятым стандартным методом с использованием реагентов, предназначенных для этой цели.
Получение кДНК исследуемого материала. Получение кДНК осуществляется путем реакции обратной транскрипции (ОТ) общепринятым стандартным методом с наборами реагентов, предназначенных для этой цели. Для проведения реакции необходима РНК исследуемого образца в объеме по крайней мере 10 мкл.
Проведение реакции. Компоненты реакционной смеси и их количество для одной реакции мультиплексной ПЦР-РВ представлены в таблице 3. Для одной реакции мультиплексной ПЦР-РВ с объемом 25 мкл готовят смесь раствора 1 (смесь праймеров и флуоресцентных зондов для ORF1ab и N генов коронавируса SARS-CoV-2 и человеческого гена ABL1) и раствора 2 (10х ПЦР буфер, эквивалентная смесь четырех дезоксинуклеотидтрифосфатов, Taq-полимераза, MqCl2 25 мМ) по 7,5 мкл каждого, соответственно. Смесь реагентов готовят с учетом еще двух (ПКО и ОКО) контрольных образцов. В микропробирки с реагентами для исследуемых образцов вносят по 10 мкл кДНК, а в микропробирки для ПКО и ОКО вносят по 10 мкл положительный и отрицательный контрольные образцы. Мультиплексную ПЦР-РВ проводят в амплификаторе "Rotor-Gene Q" («Qiagen», USA) или CFX96 Touch ("Bio-Rad" США) в температурном профиле: 95°С - 600 с, 45 циклов 95°С - 20 с, 60°С -45 с.
Интерпретация результатов мультиплексной ПЦР-РВ. Принцип оценки анализа заключается в определение значений порогового числа (Ct) циклов амплификации по каждому из трех каналов (Фиг. 1). Критерии оценки представлены в таблице 4 и пояснены на Фиг. 2.
Пример 2. Поступили образцы мазков №536 и №537 из носоглотки от двух пациентов с подозрением на COVID-19. Выделение РНК в объеме 30 мкл и получение кДНК осуществлено с использованием набора реагентов для выделения РНК «Амплисорб» и «Reverta L» компании Интерлабсервис (Россия), согласно инструкции производителя.
Далее собрана реакционная смесь в объеме 25 мкл для мультиплексной ПЦР-РВ в соответствии с таблицей 3.
Мультиплексная ПЦР-РВ осуществлена в амплификаторе «Rotor-Gene Q («Qiagen», USA) в температурном профиле: 95°С - 600 с, 45 циклов 95°С -20 с, 60°С-45 с.
Обработанные результаты представлены на Фиг 4.
Интерпретация результатов. Образцы мазков №536 и №537 содержат достаточное количество исходного материала, на что указывает значение Ct амплификации РНК человеческого гена ABL1 в контрольных (ПКО и ОКО) и анализируемом образце, по желтому (yellow) каналу. В оранжевом (orange) и красном (red) канале отражается Ct ORFlab и N генов коронавируса SARS-CoV-2 в исследуемом и ПКО образцах. Результат мультиплексной ПЦР-РВ показал присутствие РНК коронавируса SARS-CoOV-2 в исследуемых образцах.
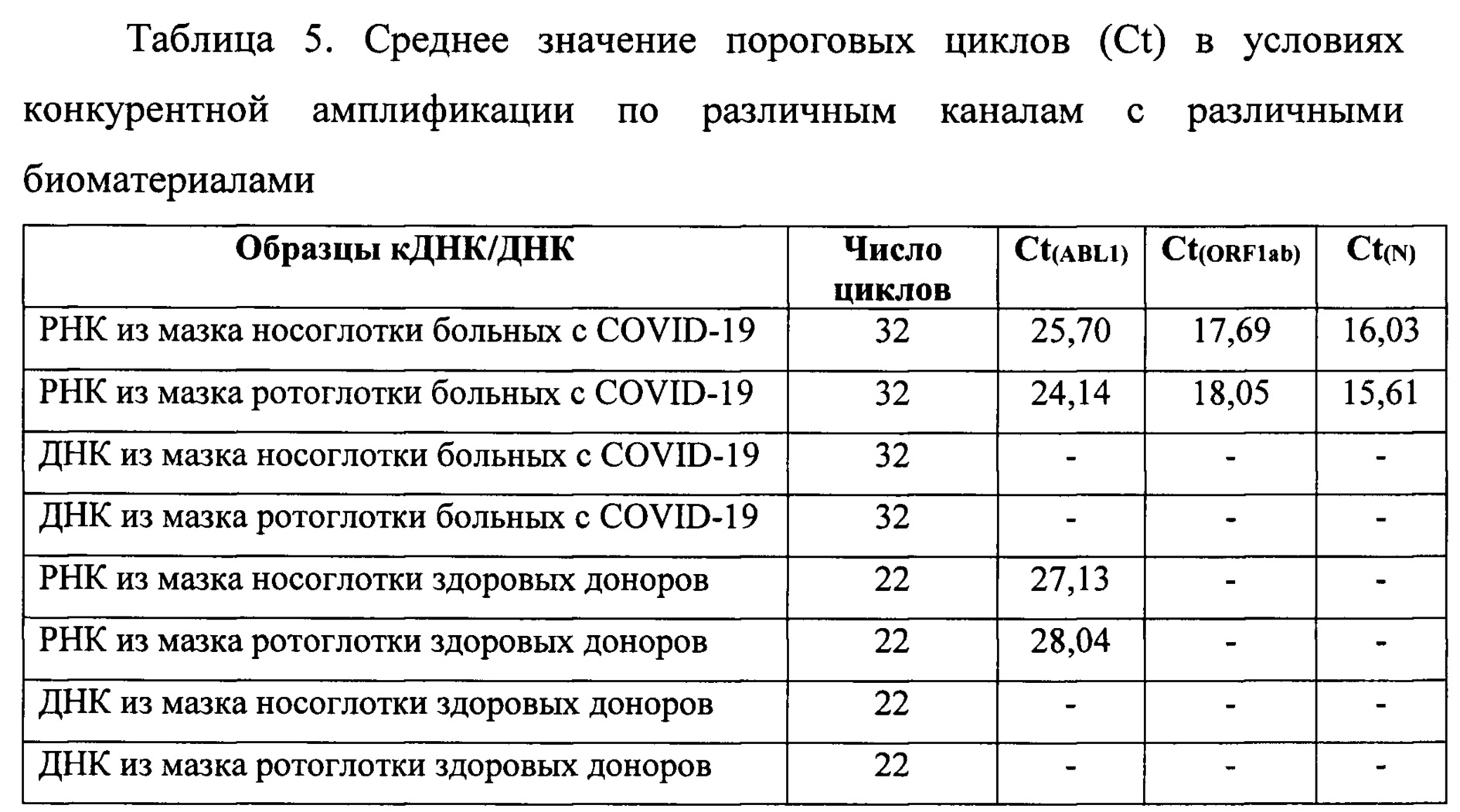
Пример 3. Для проверки аналитической возможности предлагаемого способа из мазков носоглотки и ротоглотки 32 пациентов с COVID-19 и 22 здоровых доноров крови были выделены РНК и ДНК. Все образцы предварительно анализированы с использованием набора реагентов "ПЦР-РВ -2019-nCov" (ФГБУ "48 ЦНИИ" МО РФ) на наличия РНК SARS-COV-2. Выделение РНК и получения кДНК осуществлено с использованием набора реагентов "РИБО-преп" и "Реверта-L" ("Интерлабсервис" Россия), согласно инструкции производителя. Мультиплексная ПЦР-РВ проведена на амлификаторе "Rotor-Gene Q" («Qiagen», USA) в режиме: 95°С - 600 с, 45 циклов 95°С - 20 с, 60°С - 45 с. Среднее значение пороговых циклов (Ct) в условиях конкурентной амплификации по различным каналам приведены в таблице 5.
Как видно, из таблицы 5, разработанный набор синтетических олигонуклеотидов и флюоресцентных зондов для контрольного гена является исключительно РНК специфичным, что делает возможными его применение в качестве внутреннего контроля прохождения реакции обратной транскрипции.
Пример 4. Специфичность набора предлагаемых синтетических олигонуклеотидов и флюоресцентых зондов исключительно в отношении РНК вируса SARS-CoV-2 была проверена методом прямого секвенирования по Сэнгеру полученных продуктов мультиплексной ПЦР-РВ с использованием праймеров представленных в таблице 6.
Таблица 6. Нуклеотидные последовательности синтетических олигонуклеотидных праймеров для секвенирования участка генов ORFlab и N коронавируса SARS-CoV-2
Хроматограмма прямого секвенирования по Сэнгеру ORF1a участка генома SARS-CoV-2 представлена на Фиг. 5. Согласно сравнению с базой данных ttps://www.ncbi.nlm.nih.gov/datasets/coronaviras/genomes/прочитанные нуклеотидные последовательности 100% соответствуют только различным изолятам SARS-CoV-2.Таким образом, изобретение позволяет достоверно подтвердить клинический диагноз COVID-19 путем контроля качества отбора пробы и выделения РНК по амплификации РНК человеческого гена ABL1 и присутствия/отсутствия РНК коронавируса SARS-CoV-2 относительно контрольных образцов и может быть использовано в молекулярно-генетической диагностике.
Пример 5. Специфичность предлагаемого способа ПЦР-РВ исследовали на образцах мазков из носоглотки 133 пациентов с клиническим диагнозом COVID-19, подтвержденным зарегистрированными в РФ наборами для выявления коронавируса SARS-CoV-2 компании «BIONEER» (Южная Корея) и ФГБУ «48 ЦНИИ» Минобороны России (Россия). Контрольной группой послужили 69 образцов мазков из носоглотки и ротоглотки здоровых доноров крови, SARS-CoV-2 негативность которых также подтверждена вышеуказанными наборами. Специфичность способа оказалась равной 98,5% (SARS-CoV-2 положительными были 131 из 133 образцов). Результаты части исследований представлены на Фиг 3.
Источники информации, принятые во внимание при составлении описания изобретения к заявке на выдачу патента РФ на изобретение «Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2»:
1. https://www.whojnt/emergencies/diseases/novel-coronavirus-2019/technical-guidance/laboratory-guidance.
2. Патент RU 2720713 «Набор синтетических олигонуклеотидов для выявления РНК коронавируса», C12Q 1/6806, опубликован 12.05.2020 г.
3. Патент RU 2727054 «Способ выявления кДНК коронавируса SARS-CoV-2 с помощью синтетических олигонуклеотидных праймеров в полимеразной цепной реакции», C12Q 1/6806, опубликован 17.07.2020 г.
4. Патент US 10689716 «Materials and methods for detecting coronavirus», C12Q 1/68, C12Q1/70, опубликован 23.06.2020 г.
5. Патент RU 2731390 «Тест-система и способ для выявления РНК коронавируса SARS-COV-2, вируса-возбудителя коронавирусного заболевания 2019 COVID-19, методом полимеразной цепной реакции в режиме реального времени (Варианты)», C12Q 1/6806, опубликован 02.09.2020 г.
6. Barber RD, Harmer DW, Coleman RA, Clark BJ. GAPDH as a housekeeping gene: analysis of GAPDH mRNA expression in a panel of 72 human tissues. Physiol Genomics. 2005;21(3):3 89-395. doi:10.1152/physiolgenomics.00025.2005.
7. Ishige T, Murata S, Taniguchi T, Miyabe A, Kitamura K, Kawasaki K, Nishimura M, Igari H, Matsushita K. Highly sensitive detection of SARS-CoV-2 RNA by multiplex rRT-PCR for molecular diagnosis of COVID-19 by clinical laboratories. Clin Chim Acta. 2020 Aug;507:139-142. doi: 10.1016/j.cca.2020.04.023. Epub 2020 Apr 23. PMID: 32335089; PMCID: PMC7179514.
8. Beillard, E., Pallisgaard, N., van der Velden, V. et al. Evaluation of candidate control genes for diagnosis and residual disease detection in leukemic patients using 'real-time' quantitative reverse-transcriptase polymerase chain reaction (RQ-PCR) - a Europe against cancer program. Leukemia 17, 2474-2486 (2003). https://doi.org/10.1038/sj.leu.2403136.
--->
Перечень последовательностей
<110> Федеральное государственное бюджетное учреждение «Национальный
медицинский исследовательский центр гематологии» Министерства
здравоохранения Российской Федерации (ФГБУ "НМИЦ гематологии" Минздрава
России)
Federal Governmental Budgetary Institution «National Research Center for
Hematology»
<120> Набор олигонуклеотидов и способ мультиплексной полимеразной цепной
реакции в режиме реального времени для выявления РНК SARS-CoV-2
<160> 9
<210> 1
<211> 24
<212> RNA
<213> Betacoronavirus
<400> 1
TGATAGTCAA CAAACTGTTG GTCA
<210> 2
<211> 22
<212> RNA
<213> Betacoronavirus
<400> 2
CTGAACAACT GGTGTAAGTT CC
<210> 3
<211> 23
<212> RNA
<213> Betacoronavirus
<400> 3
ACGGCAGTGA GGACAATCAG ACA
<210> 4
<211> 20
<212> RNA
<213> Betacoronavirus
<400> 4
ACCCGCAATC CTGCTAACAA
<210> 5
<211> 20
<212> RNA
<213> Betacoronavirus
<400> 5
CTGCGTAGAA GCCTTTTGGC
<210> 6
<211> 25
<212> RNA
<213> Betacoronavirus
<400> 6
TGCTGCAATC GTGCTACAAC TTCCT
<210> 7
<211> 20
<212> RNA
<213> Homo
<400> 7
CGCTGAGATA CGAAGGGAGG
<210> 8
<211> 20
<212> RNA
<213> Homo
<400> 8
ATGATGAACC AACTCGGCCA
<210> 9
<211> 20
<212> RNA
<213> Homo
<400> 9
CGTCTCCTCC GAGAGCCGCT
<---
Claims (12)
1. Набор синтетических олигонуклеотидных праймеров и флуоресцентных зондов, комплементарных нуклеотидной последовательности генов ORF1ab и N коронавируса SARS-CoV-2, для использования в способе мультиплексной ПЦР-РВ для выявления РНК коронавируса SARS-CoV-2:
ORF1ab_Fv: 5'-TGATAGTCAACAAACTGTTGGTCA-3';
ORF1ab_Rv: 5'-CTGAACAACTGGTGTAAGTTCC-3';
ORF1ab_Pr: FAM 5'-ACGGCAGTGAGGACAATCAGACA-3' BQH1;
N_Fv: 5'-ACCCGCAATCCTGCTAACAA-3';
N_Rv: 5'-CTGCGTAGAAGCCTTTTGGC-3';
N_Pr: ROX 5'-TGCTGCAATCGTGCTACAACTTCCT-3' BQH2.
2. Способ мультиплексной ПЦР-РВ для выявления РНК коронавируса SARS-CoV-2 с использованием набора синтетических олигонуклеотидных праймеров и флуоресцентных зондов по п.1, 10х ПЦР буфера, смеси четырех дезоксинуклеотидтрифосфатов, Taq-полимеразы, MqCl2, внутреннего контроля качества и количества исследуемого образца в виде, при этом реакция проходит в одной пробирке с кДНК в объеме 10 мкл анализируемого синтетических олигонуклеотидных праймеров и флуоресцентного зонда, комплементарных нуклеотидной последовательности человнческой мРНК гена ABL1:
ABL1_Fv: 5'-CGCTGAGATACGAAGGGAGG-3';
ABL1_Rv: 5'-ATGATGAACCAACTCGGCCA-3';
ABL1_Pr: R6G 5'-CGTCTCCTCCGAGAGCCGCT-3' BQH1;
характеризующийся также тем, что реакция проходит в одной пробирке.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2021101361A RU2752902C1 (ru) | 2021-01-22 | 2021-01-22 | Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2021101361A RU2752902C1 (ru) | 2021-01-22 | 2021-01-22 | Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2752902C1 true RU2752902C1 (ru) | 2021-08-11 |
Family
ID=77349261
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2021101361A RU2752902C1 (ru) | 2021-01-22 | 2021-01-22 | Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2752902C1 (ru) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2720713C1 (ru) * | 2020-03-27 | 2020-05-12 | Евгений Олегович Рубальский | Набор синтетических олигонуклеотидов для выявления рнк коронавируса |
| US10689716B1 (en) * | 2020-03-19 | 2020-06-23 | University Of Miami | Materials and methods for detecting coronavirus |
| RU2732608C1 (ru) * | 2020-04-09 | 2020-09-21 | Федеральное государственное бюджетное учреждение "48 Центральный научно-исследовательский институт" Министерства обороны Российской Федерации | Набор реагентов для выявления РНК вируса SARS-CoV-2, возбудителя нового коронавирусного заболевания COVID-2019, методом обратной транскрипции-полимеразной цепной реакции в реальном времени |
-
2021
- 2021-01-22 RU RU2021101361A patent/RU2752902C1/ru active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10689716B1 (en) * | 2020-03-19 | 2020-06-23 | University Of Miami | Materials and methods for detecting coronavirus |
| RU2720713C1 (ru) * | 2020-03-27 | 2020-05-12 | Евгений Олегович Рубальский | Набор синтетических олигонуклеотидов для выявления рнк коронавируса |
| RU2732608C1 (ru) * | 2020-04-09 | 2020-09-21 | Федеральное государственное бюджетное учреждение "48 Центральный научно-исследовательский институт" Министерства обороны Российской Федерации | Набор реагентов для выявления РНК вируса SARS-CoV-2, возбудителя нового коронавирусного заболевания COVID-2019, методом обратной транскрипции-полимеразной цепной реакции в реальном времени |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3269823B1 (en) | Method for assisting detection of alzheimer's disease or mild cognitive impairment | |
| CN110093413A (zh) | 检测β地中海贫血的引物组和试剂盒 | |
| CN111321227A (zh) | 白血病mef2d基因及znf384基因的多重荧光rt-pcr检测方法 | |
| CN111286559B (zh) | 检测非洲猪瘟病毒的引物、探针及试剂盒 | |
| CN108642156B (zh) | 一种t790m基因突变的数字pcr检测试剂盒及其检测方法 | |
| CN117233400A (zh) | 一种用于多发性骨髓瘤诊断与预后评估的kcnn3基因检测试剂盒及其应用 | |
| EP2857521A1 (en) | Method for assessing endometriosis | |
| KR102492149B1 (ko) | 난소암 진단 또는 감별진단을 위한 마이크로rna-1246 및 이의 용도 | |
| RU2752902C1 (ru) | Набор олигонуклеотидов и способ мультиплексной полимеразной цепной реакции в режиме реального времени для выявления РНК SARS-CoV-2 | |
| US9528161B2 (en) | Materials and methods for quality-controlled two-color RT-QPCR diagnostic testing of formalin fixed embedded and/or fresh-frozen samples | |
| Marin-Maldonado et al. | Comparative analysis of onychomycosis in Puerto Rico using molecular and conventional approaches | |
| CN110656171B (zh) | 小核仁核糖核酸snord33作为生物标记物用于制备检测试剂盒中的用途 | |
| KR102601998B1 (ko) | 자궁경부암의 급성 종양 반응 진단용 키트 | |
| US11965879B2 (en) | Method for diagnosing and assessing endometriosis | |
| CN110577994B (zh) | 无创诊断男性骨质疏松症的产品 | |
| KR20220052462A (ko) | 난소암 진단 또는 감별진단을 위한 마이크로rna-1290 및 이의 용도 | |
| JP2023020631A (ja) | 全身性エリテマトーデスを検査する方法 | |
| CN119710009B (zh) | 一种用于检测linc01480基因表达的试剂盒及其制备方法和应用 | |
| RU2795017C1 (ru) | Олигонуклеотиды для определения мутации S:Ins214EPE SARS-CoV-2 | |
| JP7748744B2 (ja) | 関節リウマチを検査する方法 | |
| CN113817817B (zh) | 一种诊断过敏性气道炎症的方法 | |
| CN111172282A (zh) | 外泌体miRNA在制备肺癌早期诊断试剂盒中的应用及肺癌早期诊断检测试剂盒 | |
| CN113684261B (zh) | 利用荧光定量pcr检测znf384基因重排的引物和探针及试剂盒 | |
| KR102870611B1 (ko) | 위암 조기진단을 위한 바이오마커 조성물 및 이를 이용한 진단방법 | |
| US20240254573A1 (en) | Methods and systems for hpv detection and quantification |