RU2564758C1 - Способ моделирования токсического гепатита формалином и этиловым спиртом в токсикологическом эксперименте - Google Patents
Способ моделирования токсического гепатита формалином и этиловым спиртом в токсикологическом эксперименте Download PDFInfo
- Publication number
- RU2564758C1 RU2564758C1 RU2014109234/14A RU2014109234A RU2564758C1 RU 2564758 C1 RU2564758 C1 RU 2564758C1 RU 2014109234/14 A RU2014109234/14 A RU 2014109234/14A RU 2014109234 A RU2014109234 A RU 2014109234A RU 2564758 C1 RU2564758 C1 RU 2564758C1
- Authority
- RU
- Russia
- Prior art keywords
- toxic
- liver
- ethanol
- simulating
- days
- Prior art date
Links
Landscapes
- Medicinal Preparation (AREA)
- Medicines Containing Plant Substances (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Изобретение относится к медицине, а именно к экспериментальной биологии, токсикологии, и может быть использовано для изучения формирования и прогрессирования изменений печени, возникающих под действием токсико-химических повреждающих факторов. Для этого предложен способ моделирования подострого токсического поражения печени. Способ включает введение крысам-самцам перорально в течение 21 дня формалина. Введение осуществляют через день, из расчета 0,2 мл на 100 г массы животного. Одновременно воздействуют 10% раствором этанола, который используют вместо питьевой воды свободным поением животных. Способ обеспечивает развитие выраженных дегенеративных повреждений практически всех участков печени, что подтверждается повышением трансаминаз в сыворотке крови, креатининемией, снижением синтетической функции печени и развитием холестаза. 1 табл., 3 пр.
Description
Изобретение относится к медицине, а именно к экспериментальной биологии, токсикологии, и может быть использовано для изучения способов формирования и изучения прогрессирования изменений в печени, возникающих в эксперименте, под действием токсико-химических повреждающих факторов.
Основными инициаторами неинфекционных заболеваний печени у людей являются неправильное питание и злоупотребление алкоголем. Кроме того, разнообразные химические вещества, широко применяемые в промышленности, зачастую вызывают токсические поражения, сопровождающиеся различными нарушениями ферментативного равновесия в ней и изменением активности ферментов печеночного поражения. В связи с этим для изучения механизмов формирования неинфекционных заболеваний печени и возможности их профилактики и лечения природными факторами требуются экспериментальные модели, наиболее приближенные к реальным клиническим условиям.
Известны способы моделирования токсического гепатита у крыс путем помещения животного в клетку с открытым резервуаром, наполненным 70%-ным раствором формалина. В этих условиях лабораторные животные содержатся в течение 5-7 месяцев (пат. RU 94026117. Способ создания модели гепатита печени млекопитающих. Бояринов Г.А., Смирнов В.П., Кауров Я.В. и др., опубл. 27.08.1996), а также трехкратного подкожного введения масляного раствора четыреххлористого углерода (CCl4) с интервалом инъекций в 4 суток, из расчета 0,45 мл раствора на 100 г массы тела животного в течение 44 дней (Глушакова Е.С.Функциональное состояние печени в норме при экспериментальном токсическом гепатите и его физиотерапевтической коррекции в разные фазы окологодового цикла: автореферат дис. канд. биол. наук: 14.00.51, 14.00.16 / Глушакова Елена Сергеевна. - Томск, 2005. - 20 с).
Недостатками перечисленных выше способов моделирования токсической гепатопатии являются трудоемкий и длительный период моделирования от одного до семи месяцев, воздействие формалина на дыхательную и сердечно-сосудистую системы. Кроме того, при создании концентраций аэрозолей и удержании на заданном уровне в затравочных камерах отмечаются значительные трудности. Кроме того, количество вещества, попавшее в организм, зависит не только от его концентрации в воздухе, но и от степени его дисперсности в воздухе, а также от индивидуально выраженных защитных способностей верхних дыхательных путей лабораторных животных, что приводит к очень низкой степени воспроизводимости результатов исследования. Введение 50% масляного раствора четыреххлористого углерода в виде инъекций отличается от формирования большинства профессиональных заболеваний токсическими веществами путем поступления в организм ингаляционно или per os.
Наиболее близким по технической сущности к предлагаемому изобретению является способ инициации токсического гепатита посредством поения животных 10% раствором этанола в сочетании с инъекциями 50% масляного раствора четыреххлористого углерода с интервалом инъекций в 4 суток из расчета 0,45 мл раствора на 100 г массы животного в течение 30 дней (Скакун Н.П. Эффективность антиоксидантов при комбинированном поражении печени четыреххлористым углеродом и этанолом / Н.П. Скакун, С.Ф.Ковальчук // Фармакология и токсикология. - 1987. - №3. - С. 104-107).
Недостатком данного способа является способ введения четыреххлористого углерода, а также длительность создания экспериментальной патологической модели. При этом следует отметить, что основным временным показателем для создания экспериментальных моделей подострого токсического гепатита токсическими веществами является 21 день, что четко соблюдается при нашем варианте моделирования.
Техническим результатом предлагаемого способа является решение задачи, заключающейся в создании модели токсического гепатита 10% этанолом в сочетании с формалином в более короткие сроки, и с соответствующей картиной поражения, более физиологичным способом, с высокой воспроизводимостью, что позволяет более полно изучить патофизиологические механизмы развития патологии. Преимущества предлагаемой модели в том, что она легко воспроизводима, результат достигается за более короткий промежуток времени по сравнению с прототипом. Повышение воспроизводимости формирования подострого патологического процесса в печени и сокращение сроков опыта достигаются за счет потенцирования гепатотоксического эффекта, вызванного воздействием 10% раствором этанола и формалина.
Указанный технический результат достигается воздействием токсического средства, которое вводят крысам-самцам перорально шприцем в течение 21 дня, в качестве токсического средства используют формалин (CH2O), который вводят через день, из расчета 0,2 мл на 100 г массы животного с одновременным ежедневным использованием вместо питьевой воды 10% раствора этанола (С2Н5ОН) свободным поением.
Способ осуществлялся следующим образом. Для достижения адекватности предлагаемой модели изучено 50 крыс-самцов линии Вистар массой тела 180-200 г, разделенных на группы. Первую группу представляют 10 интактных животных. 20 крысам-самцам, представляющим вторую группу, вводят токсическое средство через день перорально, шприцем, в течение 21 дня, в качестве токсического средства используют формалин (СН2О) из расчета 0,2 мл на 100 г массы животного, с одновременным ежедневным использованием вместо питьевой воды 10% раствора этанола (С2Н5ОН) свободным поением.
20 крысам-самцам третьей группы инициируют токсическое поражение печени путем поения животных 10% раствором этанола ежедневно вместо питьевой воды в сочетании с инъекциями 50% масляного раствора четыреххлористого углерода (CCL4) с интервалом инъекций в 4 суток из расчета 0,45 мл на 100 г массы тела животного в течение 30 дней по способу прототипа.
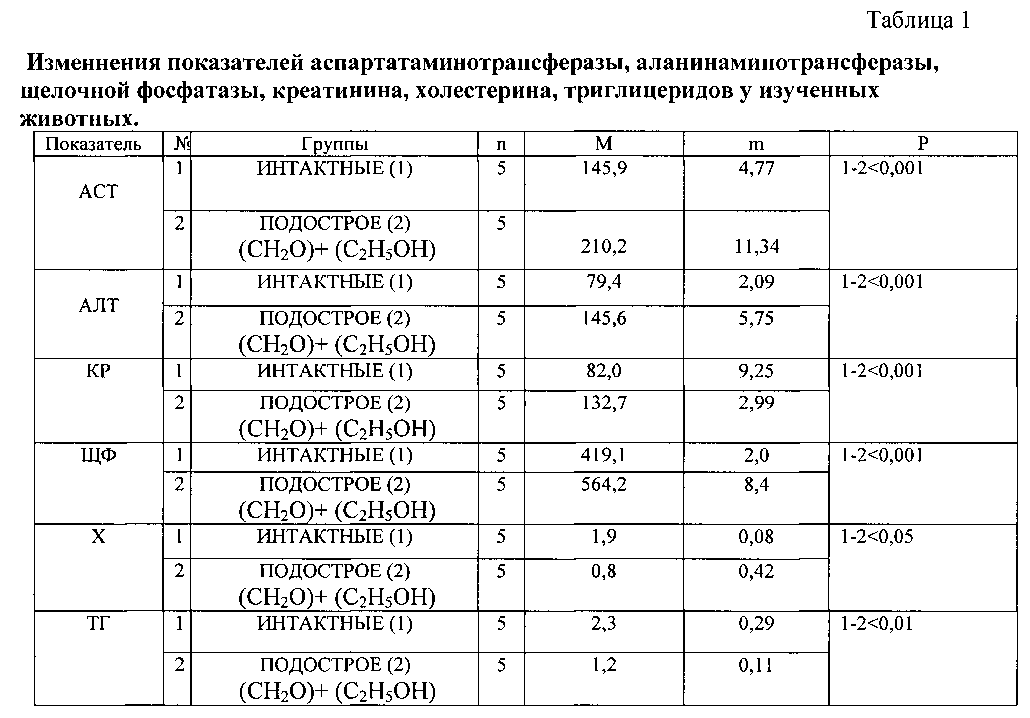
На 21 день животных декапитируют с последующим проведением лабораторных тестов. Изучают содержание в сыворотке крови аспартатаминотрансферазы (ACT) и аланинаминотрансферазы (АЛТ) в (Ед/л), креатинина (КР) в (мкмоль/л), щелочной фосфатазы (ЩФ) в (МЕ/л), холестерина (X) в (ммоль/л), триглицеридов (ТГ) в (ммоль/л).
Приготовление формалина (CH2O) производили путем растворения формальдегида в воде до концентрации 40%, и разведения 96° спирта до 10%-ной концентрации.
Способ апробирован в условиях отдела изучения механизмов действия физических факторов (ОИМДФФ) ФГБУ ПГНИИК ФМБА России.
Способ может быть проиллюстрирован следующими примерами.
Пример №1. Интактная крыса-самец линии Вистар №5, масса тела 190 г. Дополнительных воздействий не получает. Исследование животного осуществляется одновременно с животными опытной группы. Содержание в крови КР - 78,2 мкмоль/л, ЩФ - 395,4 МЕ/л, ACT - 141,3 Ед/л, АЛТ - 83,4 Ед/л, X - 1,9 ммоль/л, ТГ - 2,3 ммоль/л.
Пример №2. Крыса-самец линии Вистар №13, масса тела - 200 г. Осуществляют поение животного 10% раствором этанола ежедневно вместо питьевой воды в сочетании с инъекциями 50% масляного раствора четыреххлористого углерода (CCl4) с интервалом инъекций в 4 суток в течение 30 дней из расчета 0,45 мл на 100 г массы тела животного. КР - 112,7 мкмоль/л, ЩФ - 477,2 МЕ/л, ACT - 200,0 Ед/л, АЛТ - 105,8 Ед/л, X - 1,8 ммоль/л, ТГ - 1,6 ммоль/л. Результат расценен как подострое отравление.
Пример №3. Крыса-самец №35 линии Вистар, масса тела 195 г. Вводят токсическое средство через день перорально шприцем в течение 21 дня, в качестве токсического средства используют формалин (CH2O) из расчета 0,2 мл на 100 г массы животного с одновременным ежедневным использованием вместо питьевой воды 10% раствора этанола (С2Н5ОН) свободным поением.
Содержание в крови КР - 86,7 мкмоль/л, ЩФ - 591,2 МЕ/л, ACT - 215,1 Ед/л, АЛТ - 138,4 Ед/л, X - 0,9 ммоль/л, ТГ - 1,2 ммоль/л. Результат расценен как подострое отравление.
Из представленной таблицы следует, что увеличение содержания ACT; АЛТ (Р<0,001), а также повышение КР (Р<0,001) в сыворотке крови указывают на усиление степени поражения печени и свидетельствуют о повреждении гепатоцитов, значительное снижение показателей X и ТГ (Р<0,05, Р<0,01) указывает на снижение синтетической функции печени, а повышение уровня ШФ (Р<0,001) - на развитие холестаза.
Таким образом, повышение воспроизводимости формирования подострого патологического процесса в печени и сокращение сроков опыта достигается за счет потенцирования гепатотоксического эффекта, вызванного воздействием 10% раствором этанола и формалина. Преимущества предлагаемой модели в том, что она легко воспроизводима, результат достигается за более короткий промежуток времени по сравнению с прототипом.
Claims (1)
- Способ моделирования подострого токсического поражения печени, включающий воздействие токсическим средством, которое вводят крысам-самцам перорально шприцем в течение 21 дня, отличающийся тем, что в качестве токсического средства используют формалин (CH2O), который вводят через день из расчета 0,2 мл на 100 г массы животного с одновременным ежедневным использованием вместо питьевой воды 10% раствора этанола (С2Н5ОН) свободным поением.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014109234/14A RU2564758C1 (ru) | 2014-03-11 | 2014-03-11 | Способ моделирования токсического гепатита формалином и этиловым спиртом в токсикологическом эксперименте |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2014109234/14A RU2564758C1 (ru) | 2014-03-11 | 2014-03-11 | Способ моделирования токсического гепатита формалином и этиловым спиртом в токсикологическом эксперименте |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2014109234A RU2014109234A (ru) | 2015-09-20 |
| RU2564758C1 true RU2564758C1 (ru) | 2015-10-10 |
Family
ID=54147465
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2014109234/14A RU2564758C1 (ru) | 2014-03-11 | 2014-03-11 | Способ моделирования токсического гепатита формалином и этиловым спиртом в токсикологическом эксперименте |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2564758C1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2822194C1 (ru) * | 2024-02-21 | 2024-07-03 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Санкт-Петербургский государственный университет ветеринарной медицины" | Способ моделирования токсического гепатита с использованием фталевого ангидрида |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU94026117A (ru) * | 1994-07-14 | 1996-08-27 | Нижегородский государственный медицинский институт | Способ создания модели гепатита и цирроза печени млекопитающих |
| RU2197018C2 (ru) * | 2000-02-16 | 2003-01-20 | Уфимский научно-исследовательский институт медицины труда и экологии человека | Способ моделирования цирроза печени |
| US20100179798A1 (en) * | 2008-12-10 | 2010-07-15 | Strand Life Sciences Pvt Ltd. | Method for Predicting Organ Toxicity and a System Thereof |
| CN101788480A (zh) * | 2010-01-29 | 2010-07-28 | 浙江大学 | 基于荧光标记的肝毒性物质筛选和评价方法 |
| RU2487421C1 (ru) * | 2011-11-10 | 2013-07-10 | Федеральное государственное бюджетное учреждение "Пятигорский государственный научно-исследовательский институт курортологии Федерального медико-биологического агентства" (ФГБУ ПГНИИК ФМБА России) | Способ моделирования токсического поражения четыреххлористым углеродом в токсикологическом эксперименте |
-
2014
- 2014-03-11 RU RU2014109234/14A patent/RU2564758C1/ru not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU94026117A (ru) * | 1994-07-14 | 1996-08-27 | Нижегородский государственный медицинский институт | Способ создания модели гепатита и цирроза печени млекопитающих |
| RU2197018C2 (ru) * | 2000-02-16 | 2003-01-20 | Уфимский научно-исследовательский институт медицины труда и экологии человека | Способ моделирования цирроза печени |
| US20100179798A1 (en) * | 2008-12-10 | 2010-07-15 | Strand Life Sciences Pvt Ltd. | Method for Predicting Organ Toxicity and a System Thereof |
| CN101788480A (zh) * | 2010-01-29 | 2010-07-28 | 浙江大学 | 基于荧光标记的肝毒性物质筛选和评价方法 |
| RU2487421C1 (ru) * | 2011-11-10 | 2013-07-10 | Федеральное государственное бюджетное учреждение "Пятигорский государственный научно-исследовательский институт курортологии Федерального медико-биологического агентства" (ФГБУ ПГНИИК ФМБА России) | Способ моделирования токсического поражения четыреххлористым углеродом в токсикологическом эксперименте |
Non-Patent Citations (1)
| Title |
|---|
| МИНИГАЛИЕВА И. А. Экспериментальное испытание комплекса биопротекторов от токсических эффектов формальдегида, Токсикологический вестник, 2006, N 5, С. 13-17. RUBAJ M et al. Effects of D-penicillamine and encorton on the fibrotic processes in experimental liver cirrhosis in ratsPatol Pol. 1990;41(1-2):76-89, abstr * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2822194C1 (ru) * | 2024-02-21 | 2024-07-03 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Санкт-Петербургский государственный университет ветеринарной медицины" | Способ моделирования токсического гепатита с использованием фталевого ангидрида |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2014109234A (ru) | 2015-09-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ehninger et al. | Longevity, aging and rapamycin | |
| Kohda et al. | Glucocorticoid receptor activation is involved in producing abnormal phenotypes of single-prolonged stress rats: a putative post-traumatic stress disorder model | |
| Garza et al. | Leptin restores adult hippocampal neurogenesis in a chronic unpredictable stress model of depression and reverses glucocorticoid-induced inhibition of GSK-3β/β-catenin signaling | |
| Morera et al. | Chronic heat stress up-regulates leptin and adiponectin secretion and expression and improves leptin, adiponectin and insulin sensitivity in mice | |
| Feinberg et al. | Recognition memory for social and non-social odors: differential effects of neurotoxic lesions to the hippocampus and perirhinal cortex | |
| Shioda et al. | A novel cognitive enhancer, ZSET1446/ST101, promotes hippocampal neurogenesis and ameliorates depressive behavior in olfactory bulbectomized mice | |
| Olescowicz et al. | Antidepressant and pro-neurogenic effects of agmatine in a mouse model of stress induced by chronic exposure to corticosterone | |
| Meneghini et al. | The noradrenergic component in tapentadol action counteracts μ-opioid receptor–mediated adverse effects on adult neurogenesis | |
| Kaur et al. | Curcumin supplementation improves mitochondrial and behavioral deficits in experimental model of chronic epilepsy | |
| Maraslioglu et al. | Chronic Ethanol Feeding Modulates Inflammatory Mediators, Activation of Nuclear Factor‐κB, and Responsiveness to Endotoxin in Murine Kupffer Cells and Circulating Leukocytes | |
| Wang et al. | Protective roles of hepatic GABA signaling in acute liver injury of rats | |
| Wang et al. | Activation of sphingosine 1-phosphate receptor 2 attenuates chemotherapy-induced neuropathy | |
| Lima et al. | Time-dependent sensitization of stress responses in zebrafish: a putative model for post-traumatic stress disorder | |
| Niehaus et al. | Plasticity of addiction: a mesolimbic dopamine short-circuit? | |
| Kwon et al. | Vitamin D3 up-regulated protein 1 deficiency accelerates liver regeneration after partial hepatectomy in mice | |
| Wang et al. | Potential involvement of adiponectin signaling in regulating physical exercise-elicited hippocampal neurogenesis and dendritic morphology in stressed mice | |
| Cording et al. | Altered motor learning and coordination in mouse models of autism spectrum disorder | |
| Buhr et al. | The influence of moderate physical activity on brain monoaminergic responses to binge-patterned alcohol ingestion in female mice | |
| Danilova et al. | Accelerated liver recovery after acute CCl4 poisoning in rats treated with sodium phthalhydrazide | |
| RU2564758C1 (ru) | Способ моделирования токсического гепатита формалином и этиловым спиртом в токсикологическом эксперименте | |
| Gerding et al. | Intravital staining of the internal limiting membrane with a novel heavy solution of brilliant blue G | |
| Taheri et al. | Mild permanent chronic thyroid hormones insufficiency induces cognitive dysfunction in the adult male and female rats | |
| RU2487421C1 (ru) | Способ моделирования токсического поражения четыреххлористым углеродом в токсикологическом эксперименте | |
| RU2627444C1 (ru) | Способ моделирования подострого токсического поражения печени формалином | |
| RU2461892C1 (ru) | Способ моделирования хронической токсической артериальной гипертонии и кардиопатии у экспериментальных животных |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20170312 |
|
| NF4A | Reinstatement of patent |
Effective date: 20190815 |
|
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20200430 |
|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20210312 |