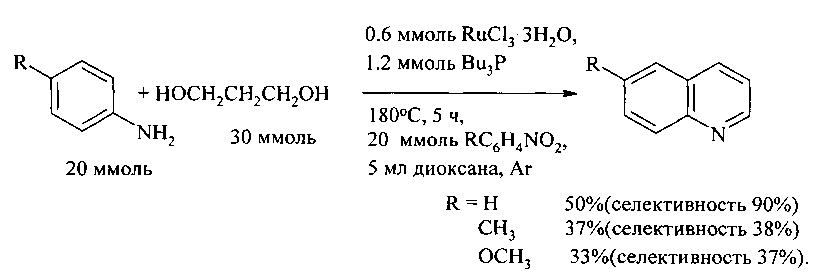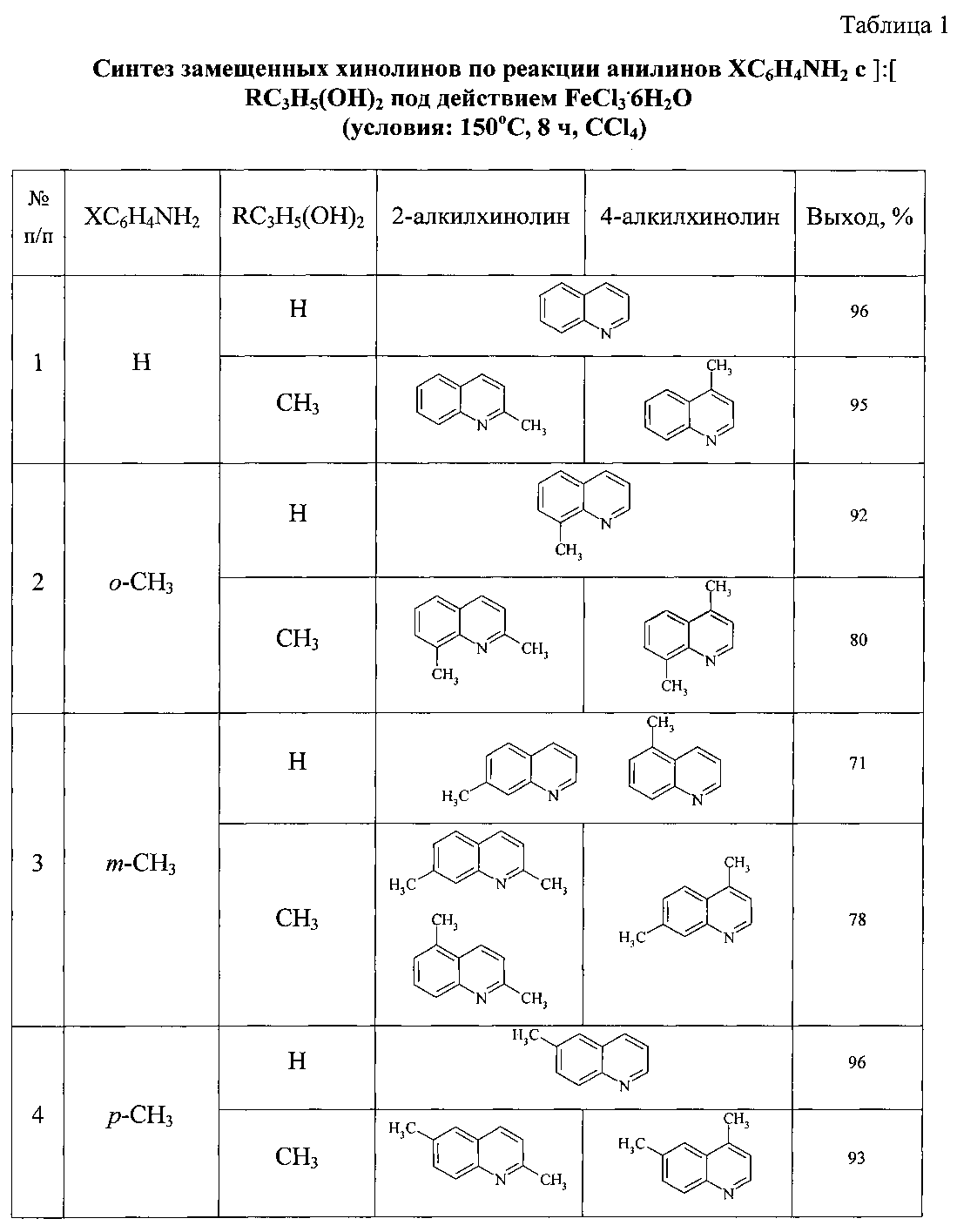RU2561503C2 - СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ - Google Patents
СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ Download PDFInfo
- Publication number
- RU2561503C2 RU2561503C2 RU2013151207/04A RU2013151207A RU2561503C2 RU 2561503 C2 RU2561503 C2 RU 2561503C2 RU 2013151207/04 A RU2013151207/04 A RU 2013151207/04A RU 2013151207 A RU2013151207 A RU 2013151207A RU 2561503 C2 RU2561503 C2 RU 2561503C2
- Authority
- RU
- Russia
- Prior art keywords
- ppm
- nmr spectrum
- fecl
- diols
- cdcl
- Prior art date
Links
- 229940111121 antirheumatic drug quinolines Drugs 0.000 title claims abstract description 19
- 239000003054 catalyst Substances 0.000 title claims abstract description 19
- 150000003248 quinolines Chemical class 0.000 title claims abstract description 19
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 title claims abstract description 18
- 150000000185 1,3-diols Chemical class 0.000 title claims abstract description 10
- 238000000034 method Methods 0.000 title claims abstract description 10
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 title abstract 6
- 238000006243 chemical reaction Methods 0.000 claims abstract description 10
- 150000001448 anilines Chemical class 0.000 claims abstract description 9
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 claims abstract description 8
- DNIAPMSPPWPWGF-VKHMYHEASA-N (+)-propylene glycol Chemical compound C[C@H](O)CO DNIAPMSPPWPWGF-VKHMYHEASA-N 0.000 claims abstract description 5
- YPFDHNVEDLHUCE-UHFFFAOYSA-N 1,3-propanediol Substances OCCCO YPFDHNVEDLHUCE-UHFFFAOYSA-N 0.000 claims abstract description 5
- 229920000166 polytrimethylene carbonate Polymers 0.000 claims abstract description 5
- 150000002009 diols Chemical class 0.000 claims abstract description 4
- 230000003993 interaction Effects 0.000 claims abstract description 4
- LZKLAOYSENRNKR-LNTINUHCSA-N iron;(z)-4-oxoniumylidenepent-2-en-2-olate Chemical compound [Fe].C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O LZKLAOYSENRNKR-LNTINUHCSA-N 0.000 claims abstract description 3
- 239000012044 organic layer Substances 0.000 claims abstract description 3
- 239000002904 solvent Substances 0.000 claims abstract description 3
- 229910052742 iron Inorganic materials 0.000 claims description 4
- 235000019437 butane-1,3-diol Nutrition 0.000 claims 1
- 229910052739 hydrogen Inorganic materials 0.000 abstract description 27
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 abstract description 9
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 abstract description 5
- 239000003153 chemical reaction reagent Substances 0.000 abstract description 5
- 238000004519 manufacturing process Methods 0.000 abstract description 3
- 239000012467 final product Substances 0.000 abstract description 2
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 abstract description 2
- 229910021578 Iron(III) chloride Inorganic materials 0.000 abstract 2
- RBTARNINKXHZNM-UHFFFAOYSA-K iron trichloride Chemical compound Cl[Fe](Cl)Cl RBTARNINKXHZNM-UHFFFAOYSA-K 0.000 abstract 2
- 229910021577 Iron(II) chloride Inorganic materials 0.000 abstract 1
- NMCUIPGRVMDVDB-UHFFFAOYSA-L iron dichloride Chemical compound Cl[Fe]Cl NMCUIPGRVMDVDB-UHFFFAOYSA-L 0.000 abstract 1
- 239000000126 substance Substances 0.000 abstract 1
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 33
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 30
- 238000001819 mass spectrum Methods 0.000 description 26
- 239000007788 liquid Substances 0.000 description 12
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 7
- 229910052707 ruthenium Inorganic materials 0.000 description 6
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 5
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- LQNUZADURLCDLV-UHFFFAOYSA-N nitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC=C1 LQNUZADURLCDLV-UHFFFAOYSA-N 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 239000006227 byproduct Substances 0.000 description 3
- 125000001309 chloro group Chemical group Cl* 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- JJPSZKIOGBRMHK-UHFFFAOYSA-N 2,6-dimethylquinoline Chemical compound N1=C(C)C=CC2=CC(C)=CC=C21 JJPSZKIOGBRMHK-UHFFFAOYSA-N 0.000 description 2
- QXKPLNCZSFACPU-UHFFFAOYSA-N 2,7-dimethylquinoline Chemical compound C1=CC(C)=NC2=CC(C)=CC=C21 QXKPLNCZSFACPU-UHFFFAOYSA-N 0.000 description 2
- BELFSAVWJLQIBB-UHFFFAOYSA-N 2,8-dimethylquinoline Chemical compound C1=CC=C(C)C2=NC(C)=CC=C21 BELFSAVWJLQIBB-UHFFFAOYSA-N 0.000 description 2
- JTLZWQVUPZYROB-UHFFFAOYSA-N 4,6-dimethylquinoline Chemical compound N1=CC=C(C)C2=CC(C)=CC=C21 JTLZWQVUPZYROB-UHFFFAOYSA-N 0.000 description 2
- LOMBYWOEYMBBGZ-UHFFFAOYSA-N 4,7-dimethylquinoline Chemical compound CC1=CC=NC2=CC(C)=CC=C21 LOMBYWOEYMBBGZ-UHFFFAOYSA-N 0.000 description 2
- MUDSDYNRBDKLGK-UHFFFAOYSA-N 4-methylquinoline Chemical compound C1=CC=C2C(C)=CC=NC2=C1 MUDSDYNRBDKLGK-UHFFFAOYSA-N 0.000 description 2
- LMYVCXSKCQSIEQ-UHFFFAOYSA-N 5-methylquinoline Chemical compound C1=CC=C2C(C)=CC=CC2=N1 LMYVCXSKCQSIEQ-UHFFFAOYSA-N 0.000 description 2
- MBVGYFIYXWVPQY-UHFFFAOYSA-N 6-methoxy-4-methylquinoline Chemical compound N1=CC=C(C)C2=CC(OC)=CC=C21 MBVGYFIYXWVPQY-UHFFFAOYSA-N 0.000 description 2
- LUYISICIYVKBTA-UHFFFAOYSA-N 6-methylquinoline Chemical compound N1=CC=CC2=CC(C)=CC=C21 LUYISICIYVKBTA-UHFFFAOYSA-N 0.000 description 2
- KDYVCOSVYOSHOL-UHFFFAOYSA-N 7-methylquinoline Chemical compound C1=CC=NC2=CC(C)=CC=C21 KDYVCOSVYOSHOL-UHFFFAOYSA-N 0.000 description 2
- JRLTTZUODKEYDH-UHFFFAOYSA-N 8-methylquinoline Chemical compound C1=CN=C2C(C)=CC=CC2=C1 JRLTTZUODKEYDH-UHFFFAOYSA-N 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 2
- -1 aliphatic aldehydes Chemical class 0.000 description 2
- 239000003708 ampul Substances 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 238000009833 condensation Methods 0.000 description 2
- 230000005494 condensation Effects 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- SMUQFGGVLNAIOZ-UHFFFAOYSA-N quinaldine Chemical compound C1=CC=CC2=NC(C)=CC=C21 SMUQFGGVLNAIOZ-UHFFFAOYSA-N 0.000 description 2
- 229910052703 rhodium Inorganic materials 0.000 description 2
- 239000010948 rhodium Substances 0.000 description 2
- NBYLBWHHTUWMER-UHFFFAOYSA-N 2-Methylquinolin-8-ol Chemical compound C1=CC=C(O)C2=NC(C)=CC=C21 NBYLBWHHTUWMER-UHFFFAOYSA-N 0.000 description 1
- DULGUAMZWACUFO-UHFFFAOYSA-N 4,8-dimethylquinoline Chemical compound C1=CC=C2C(C)=CC=NC2=C1C DULGUAMZWACUFO-UHFFFAOYSA-N 0.000 description 1
- OYUKRQOCPFZNHR-UHFFFAOYSA-N 4-methylquinolin-8-ol Chemical compound C1=CC=C2C(C)=CC=NC2=C1O OYUKRQOCPFZNHR-UHFFFAOYSA-N 0.000 description 1
- VNFYMAPAENTMMO-UHFFFAOYSA-N 5-chloro-2-methylquinoline Chemical compound ClC1=CC=CC2=NC(C)=CC=C21 VNFYMAPAENTMMO-UHFFFAOYSA-N 0.000 description 1
- HJSRGOVAIOPERP-UHFFFAOYSA-N 5-chloroquinoline Chemical compound C1=CC=C2C(Cl)=CC=CC2=N1 HJSRGOVAIOPERP-UHFFFAOYSA-N 0.000 description 1
- OCCIBGIEIBQGAJ-UHFFFAOYSA-N 6-chloro-2-methylquinoline Chemical compound C1=C(Cl)C=CC2=NC(C)=CC=C21 OCCIBGIEIBQGAJ-UHFFFAOYSA-N 0.000 description 1
- NPPPLXJXZOCDHJ-UHFFFAOYSA-N 6-chloro-4-methylquinoline Chemical compound C1=C(Cl)C=C2C(C)=CC=NC2=C1 NPPPLXJXZOCDHJ-UHFFFAOYSA-N 0.000 description 1
- GKJSZXGYFJBYRQ-UHFFFAOYSA-N 6-chloroquinoline Chemical compound N1=CC=CC2=CC(Cl)=CC=C21 GKJSZXGYFJBYRQ-UHFFFAOYSA-N 0.000 description 1
- NAGJQQFMJKMXJQ-UHFFFAOYSA-N 6-methoxy-2-methylquinoline Chemical compound N1=C(C)C=CC2=CC(OC)=CC=C21 NAGJQQFMJKMXJQ-UHFFFAOYSA-N 0.000 description 1
- HFDLDPJYCIEXJP-UHFFFAOYSA-N 6-methoxyquinoline Chemical compound N1=CC=CC2=CC(OC)=CC=C21 HFDLDPJYCIEXJP-UHFFFAOYSA-N 0.000 description 1
- WQZQFYRSYLXBGP-UHFFFAOYSA-N 7-chloro-2-methylquinoline Chemical compound C1=CC(Cl)=CC2=NC(C)=CC=C21 WQZQFYRSYLXBGP-UHFFFAOYSA-N 0.000 description 1
- OUFGWFRCXZIEPM-UHFFFAOYSA-N 7-chloro-4-methylquinoline Chemical compound ClC1=CC=C2C(C)=CC=NC2=C1 OUFGWFRCXZIEPM-UHFFFAOYSA-N 0.000 description 1
- QNGUPQRODVPRDC-UHFFFAOYSA-N 7-chloroquinoline Chemical compound C1=CC=NC2=CC(Cl)=CC=C21 QNGUPQRODVPRDC-UHFFFAOYSA-N 0.000 description 1
- 239000005725 8-Hydroxyquinoline Substances 0.000 description 1
- VVLYDFPOGMTMFJ-UHFFFAOYSA-N 8-chloro-2-methylquinoline Chemical compound C1=CC=C(Cl)C2=NC(C)=CC=C21 VVLYDFPOGMTMFJ-UHFFFAOYSA-N 0.000 description 1
- GSPZRQVQAVVSTQ-UHFFFAOYSA-N 8-chloro-4-methylquinoline Chemical compound C1=CC=C2C(C)=CC=NC2=C1Cl GSPZRQVQAVVSTQ-UHFFFAOYSA-N 0.000 description 1
- RUSMDMDNFUYZTM-UHFFFAOYSA-N 8-chloroquinoline Chemical compound C1=CN=C2C(Cl)=CC=CC2=C1 RUSMDMDNFUYZTM-UHFFFAOYSA-N 0.000 description 1
- ZPVSAUSAHRIAQM-UHFFFAOYSA-N 8-ethyl-2-methylquinoline Chemical compound C1=C(C)N=C2C(CC)=CC=CC2=C1 ZPVSAUSAHRIAQM-UHFFFAOYSA-N 0.000 description 1
- VQWUHSRBAWSSEM-UHFFFAOYSA-N 8-ethyl-4-methylquinoline Chemical compound C1=CN=C2C(CC)=CC=CC2=C1C VQWUHSRBAWSSEM-UHFFFAOYSA-N 0.000 description 1
- WSNATRDCOFYLCB-UHFFFAOYSA-N 8-ethylquinoline Chemical compound C1=CN=C2C(CC)=CC=CC2=C1 WSNATRDCOFYLCB-UHFFFAOYSA-N 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000001773 anti-convulsant effect Effects 0.000 description 1
- 230000000078 anti-malarial effect Effects 0.000 description 1
- 239000001961 anticonvulsive agent Substances 0.000 description 1
- 229960003965 antiepileptics Drugs 0.000 description 1
- 239000003430 antimalarial agent Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 238000005899 aromatization reaction Methods 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- 238000005260 corrosion Methods 0.000 description 1
- 230000007797 corrosion Effects 0.000 description 1
- 238000006356 dehydrogenation reaction Methods 0.000 description 1
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000007074 heterocyclization reaction Methods 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 229960003540 oxyquinoline Drugs 0.000 description 1
- UCUUFSAXZMGPGH-UHFFFAOYSA-N penta-1,4-dien-3-one Chemical class C=CC(=O)C=C UCUUFSAXZMGPGH-UHFFFAOYSA-N 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- MCJGNVYPOGVAJF-UHFFFAOYSA-N quinolin-8-ol Chemical compound C1=CN=C2C(O)=CC=CC2=C1 MCJGNVYPOGVAJF-UHFFFAOYSA-N 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 150000003303 ruthenium Chemical class 0.000 description 1
- 150000003304 ruthenium compounds Chemical class 0.000 description 1
- YBCAZPLXEGKKFM-UHFFFAOYSA-K ruthenium(iii) chloride Chemical compound [Cl-].[Cl-].[Cl-].[Ru+3] YBCAZPLXEGKKFM-UHFFFAOYSA-K 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
Landscapes
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
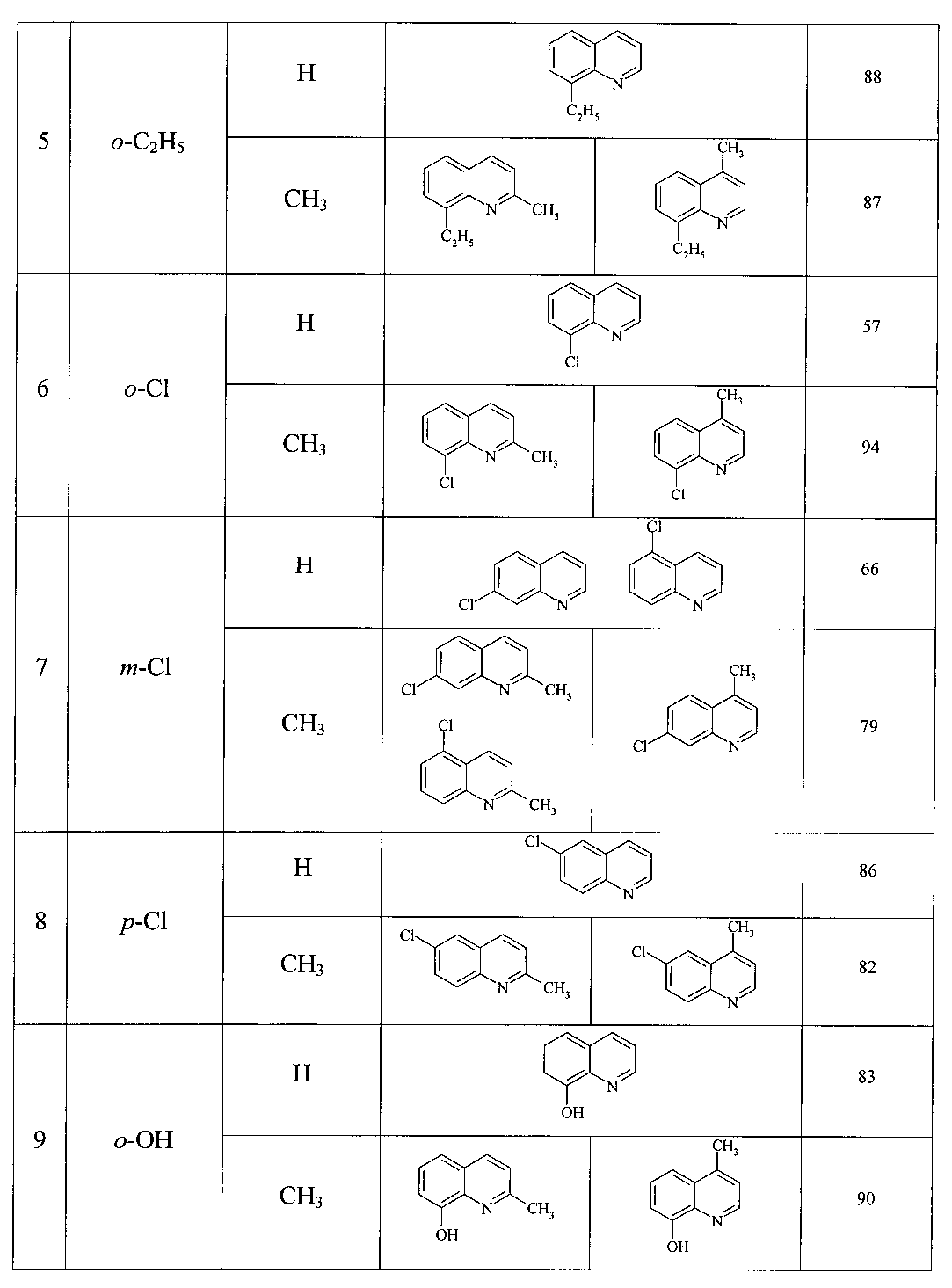
Изобретение относится к области органической химии, а именно к способу получения замещенных хинолинов формулы где R1 и R2 = Н; R1 = СН3, R2 = Н; R1 = Н, R2 = СН3; Х = Н, о-СН3, м-СН3, п-СН3, о-С2Н5, о-Cl, м-Cl, п-Cl, п-ОМе, о-ОН, взаимодействием анилинов с 1,3-диолами под действием катализаторов, отличающемуся тем, что замещенные анилины формулы XC6H4NH2, где X - указанное выше, подвергают взаимодействию с 1,3-диолами (1,3-пропандиолом или 1,3-бутандиолом) и CCl4 в присутствии катализатора, выбранного из ряда FeCl3·6H2O, FeCl3, FeCl2·4H2O, Fe(C5H5)2, Fe(acac)3, Fe(OAc)2 и Fe2(CO)9, при мольном соотношении [катализатор]:[анилин]:[CCl4]:[диол]=1:100:200:400, при 150°C в течение 8 ч, полученную реакционную массу нейтрализуют, органический слой экстрагируют CH2Cl2, отфильтровывают и отгоняют растворитель. Технический результат: разработан новый способ получения замещенных хинолинов, отличающийся удешевлением себестоимости конечного продукта за счет использования доступных исходных реагентов. 1 табл., 1 пр.
Description
Предлагаемое изобретение относится к области органической химии, в частности, к способу получения замещенных хинолинов.
Хинолин и его производные находят широкое применение в качестве синтонов при получении ингибиторов кислотной коррозии металлов, красителей и фармацевтических препаратов, проявляющих антималярийную, противосудорожную и антибактериальную активность [1. Larsen R.D., Corley E.G., King A.O., Carrol J.D., Davis P., Verhoeven T.R., Reider P.J., Labelle M., Gaunthier J.Y., Xiang Y.B., Zamboni R.J. // J. Org. Chem. 1996, 61, 3398-3405; 2. Chen Y.-L., Fang K.-C., Sheu J.-Y., Hsu S.-L., Tzeng C.-C. // J. Med. Chem. 2001, 44, 2374-2377; 3. Roma G., Braccio M.D., Grossi G., Mattioli F., Ghia M. // Eur. J. Med. Chem. 2000, 35, 1021-1035; 4. Dube D., Blouin M., Brideau C., Chan C.-C., Desmarais S., Ethier D., Falgueyret J.P., Friesen R.W., Girard M., Girard Y., Guay J., Riendeau D., Tgari P., Young R.N. // Bioorg. Med. Chem. Lett. 1988, 8, 1255-1260; 5. Maguire M.P., Sheets K.R., McVety K., Spada A.P., Zilberstein, A. // J. Med. Chem. 1994, 37, 2129-2137].
Известные методы синтеза замещенных хинолинов основаны на реакциях доступного анилина и его производных с различными органическими субстратами под действием металлокомплексных катализаторов.
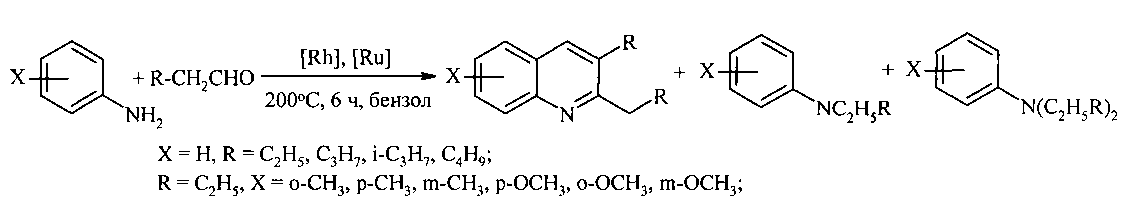
Так, конденсация анилина с алифатическими альдегидами при 200°C под действием комплексов Ru и Rh приводит к замещенным хинолинам с выходами 60-80% [6. Джемилев У.М., Селимов Ф.А., Хуснутдинов Р.А., Фатыхов А.А., Халилов Л.М., Толстиков Г.А. // Известия Академии наук СССР 1991, 6, 1407-1413].
Недостатки метода:
1. Необходимость использования дорогостоящих рутениевых и родиевых катализаторов.
2. Реакция протекает неселективно, наряду с хинолинами образуются побочные продукты алкил- и диалкиланилины (20-40%).
3. Высокая температура - 200°C.
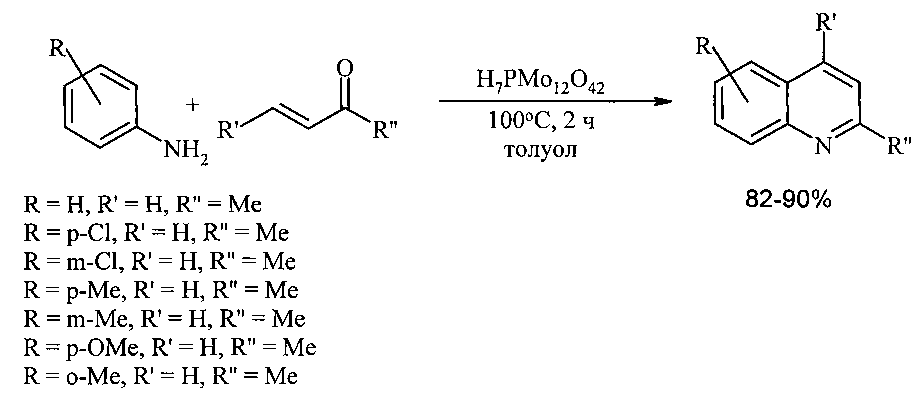
Эффективным катализатором синтеза хинолинов конденсацией анилинов с винилкетонами является фосфорномолибденовая кислота. Реакция в присутствии H7PMo12O42 проходит в среде толуола при 80°C в течение 50 мин. Выходы хинолинов составляют 87-97% [7. Chaskar A., Padalkar V., Phatangare К., Langi В., Shah С. // Synt. Commun., 40(15), 2336-2340; 2010].
Недостатки метода:
1. Необходимость применения труднодоступных и дорогостоящих реагентов фосфорномолибденовой кислоты и алкилвинилкетонов.
Как известно из литературных данных, комплексы рутения обладают способностью к дегидрированию спиртов, превращая их в альдегиды. Это свойство рутениевых катализаторов успешно использовано в ряде работ для синтеза хинолинов с участием 1,3-диолов. В частности, система RuCl3·xH2O-PBu3-MgBr2·Et2O активно катализирует гетероциклизацию 1,3-диолов с анилинами [8. Monrad N.R., Madsen R. // Org. Biomol. Chem., 2011, 9(2), 610-615].
Недостатки метода:
1. Необходимость применения дорогостоящих рутениевых катализаторов.
2. Низкий выход целевого продукта (20-61%).
В работе [9. Tsuji Y., Nishimura Н., Huh К.Т., Watanabe Y. // J. Organometal. Chem. - 1985. - V. 286. - P. 44-46] циклоконденсацию анилина и его производных (4-RC6H4NH2, R=Н, Me, МеО) с 1,3-пропандиолом в присутствии соединений рутения, с образованием хинолинов проводили при 180°C в течение 5 ч в присутствии нитробензола, играющего роль акцептора водорода. В работе в качестве активирующих лигандов хлорида рутения в реакции анилинов с 1,3-диолами был испытан большой ассортимент фосфорорганических лигандов (PBu3, PEt3, РСу3, PEt2Ph, PEtPh2, PPh3, P(OPh)3, P(OBu)3, PPh2CH2PPh2, PPh2(CH2)2PPh2, PPh2(CH2)3PPh2, PPh2(CH2)4PPh2) и лучшие результаты получены при использовании каталитических систем RuCl3·nH2O - PBu3 и RuCl3·nH2O - PEt3 и проведении реакции при повышенной температуре кипячением в диглиме в течение 5 ч. Важно отметить, что при повышенной темпертуре использование акцептора водорода не требуется, ароматизация осуществляется путем дегидрирования под действием рутениевого катализатора
Прототип имеет следующие недостатки:
1. Необходимость применения дорогостоящих рутениевых катализаторов.
2. Низкий выход целевого продукта менее 50%.
3. Необходимость использования дополнительного реагента нитробензола в качестве акцептора водорода в стехиометрическом количестве.
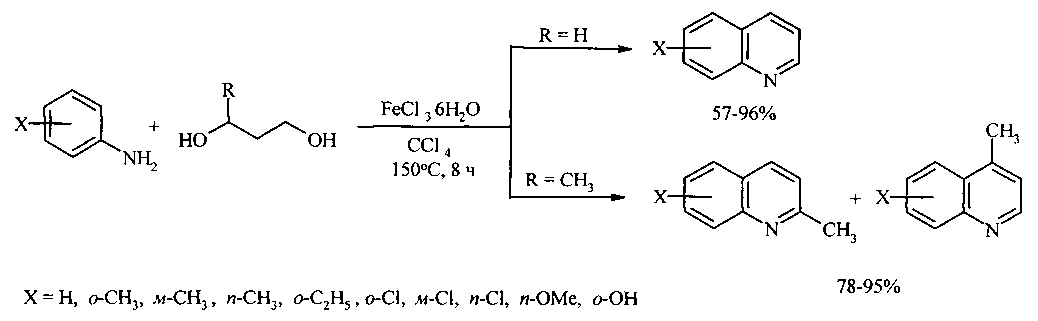
Авторами предлагается новый способ получения замещенных хинолинов взаимодействием анилина с 1,3-диолами и CCl4 под действием железосодержащих катализаторов.
Задачей предлагаемого изобретения является удешевление себестоимости конечного продукта за счет использования доступного и дешевого катализатора - FeCl3·6H2O.
Сущность способа заключается во взаимодействии анилина и его производных общей формулы XC6H4NH2, где X=Н, о-СН3, м-СН3, п-СН3, о-С2Н5, о-Cl, м-Cl, п-Cl, п-ОМе, о-ОН с 1,3-диолами, а именно с 1,3-пропандиолом и 1,3-бутандиолом под действием следующих железосодержащих катализаторов: FeCl3·6H2O, FeCl3, FeCl2·4H2O, Fe(C5H5)2, Fe(acac)3, Fe(OAc)2 и Fe2(CO)9, лучшим из которых является FeCl3·6H2O в среде CCl4. Продуктами реакции являются замещенные хинолины, выходы которых составили 57-96%. Синтез проходит при 150°C в среде CCl4 в течение 8 ч при следующих мольных соотношениях катализатора и реагентов: [FeCl3·6H2O]:[XC6H4NH2]:[CCl4]:[диол]=1:100:200:400.
Преимущества предполагаемого метода.
1. Доступность и дешевизна исходных реагентов - замещенного анилина, CCl4, диолов и катализатора FeCl3·H2O - и удешевление себестоимости и упрощение технологии.
2. Высокая селективность реакции по хинолинам и отсутствие в реакционной массе побочных продуктов - N-алкиланилинов.
3. Отсутствие побочных продуктов облегчает выделение и очистку целевых замещенных хинолинов.
4. Высокий выход замещенных хинолинов (57-96%).
Предлагаемый способ поясняется примерами.
ПРИМЕР 1. Получение замещенных хинолинов
В ампулу в токе аргона загружали 6 мг (1 ммоль) FeCl3·H2O, 0.2 мл (100 ммоль) замещенного анилина, 0.42 мл (200 ммоль) CCl4 и 400 ммоль RC3H5(OH)2 (0,63 мл 1,3-пропандиола, 0,77 мл 1,3-бутандиола). Запаянную ампулу помещали в автоклав, автоклав герметично закрывали и нагревали при 150°C в течение 8 ч, затем автоклав охлаждали до ~20°C, ампулу вскрывали, реакционную массу нейтрализовали 10% водным раствором Na2CO3 (перемешивание на магнитной мешалке в течение 0.5-1 часа), органический слой экстрагировали хлористым метиленом и отфильтровывали. Растворители отгоняли, остаток перегоняли под вакуумом.
Строение полученных замещенных хинолинов доказано методами ЯМР, масс-спектрометрии, а также сравнением с известными образцами и литературными данными.
Хинолин [10. Boyd, Derek R. Can. J. Chem. 2002, 80, 589]. Выход 96%. T кип. 42-43°C/0.2 мм рт. ст. Спектр ЯМР13С(δ, м.д.):120.98(С3), 126.67(С6), 127.79(С5), 128.93(С4а), 129.02(С8), 129.39(С7), 140.01(С4), 148.20(С8а), 149.99 (С2). Спектр ЯМР1Н(CDCl3, δ, м.д.): 7.42 т (1H, С3Н, J 8 Гц), 7.54 т (1Н, С6Н, J 8 Гц), 7.71 т (1H, С7Н, J 8 Гц), 7.82 д (1Н, С5Н, J 8.4 Гц), 8.09 д (1Н, С4Н, J 7.6 Гц), 8.17 д (1Н, С8Н, J 8.4 Гц) 8.93 д (1H, С2Н, J 8 Гц). Масс-спектр, m/z (Iотн. (%)): 129.00 [М]+ (100), 130 (11), 118 (28), 102 (22), 76 (7), 51 (10).
8-Метилхинолин [11. Claret, P.A. Org. Magn. Reson. 1976, 8, 147; Derdau, V. Chem. Eur. J. 2009, 15, 10397]. Выход 92%. T кип. 47-48°C/0.3 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 18.11 (СН3), 120.77 (С3), 125.79 (С6), 126.22 (С5), 128.32 (С4а), 129.57 (С7), 137.02 (С8), 136.23 (С4), 147.41 (С8а), 149.22 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.83 с (3Н, СН3), 7.39 т (1Н, С3Н, J 8 Гц), 7.44 т (1Н, С6Н, J 8.4 Гц), 7.52 д (1Н, С7Н, J 8 Гц), 7.66 д (1Н, С5Н, J 8 Гц), 8.12 д (1Н, С4Н, J 8.8 Гц), 8.95 д (1Н, С2Н, J 8 Гц). Масс-спектр, m/z (Iотн. (%)): 143.00[М]+(100), 144 (11), 142 (43), 115 (14), 89 (6), 51 (4).
7-Метилхинолин [12. Su, J.A.; Org. Magn. Resonance 1977, 10, 122; Chakrabarty, M.R. J. Mol. Spect. 1969, 30, 348; (c) Osborne, A.G. Tetrahedron 1983, 39, 2831]. Выход 71% (7-метил-:5-метил-=2:1). T кип. 50-51°C/0.2 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 21.77 (СН3), 120.18 (С3), 126.31 (С4а), 127.42 (С5), 128.38 (С8), 128.71 (С6), 135.63 (С4), 139.53 (С7), 148.67 (С8а), 150.10 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.56 с (3Н, СН3), 7.32 т (1Н, С3Н, J 8 Гц), 7.41 д (1Н, С6Н, J 6.8 Гц), 7.68 д (1Н, С5Н, J 8 Гц), 7.89 с (1Н, С8Н), 8.06 д (1Н, С4Н, J 8 Гц), 8.88 д (1Н, С2Н, J 8 Гц). Масс-спектр, m/z (Iотн. (%)): 143.00 [М]+ (100), 144 (11), 142 (45), 115 (16), 89 (7), 51 (5). 5-Метилхинолин. Спектр ЯМР 13С (δ, м.д.): 22.34 (СН3), 120.10 (С3), 126.01 (С6), 127.38 (С8), 128.10 (С4а), 129.55 (С7), 132.76 (С4), 134.78 (С5), 147.64 (С8а), 149.78 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.68 с (3Н, СН3), 7.21 т (1Н, С3Н, J 8 Гц), 7.36 д (1Н, С6Н, J 7.6 Гц), 7.71 т (1Н, С7Н, J 8 Гц), 7.92 д (1Н, С8Н), 7.99 д (1Н, С4Н, J 8 Гц), 8.83 д (1H, С2Н, J 8 Гц).
6-Метилхинолин [13. Bhayana, В. Org. Lett. 2009, 11, 3954]. Выход 96%. Т кип. 73-74°C/0.5 мм рт. ст. Маслянистая желтая жидкость. Спектр ЯМР 13С (δ, м.д.): 21.42 (СН3), 121.01 (С3), 126.54 (С5), 128.33 (С4а), 128.98 (С8), 131.48 (С7), 135.20 (С4), 136.19 (С6), 147.07 (С8а), 149.40 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.52 с (3Н, СН3), 7.34 т (1Н, C3H, J 7.6 Гц), 7.55 д (1H, С7Н, J 8 Гц), 7.58 с (1Н, С5Н), 7.97 д (1Н, С8Н, J 8 Гц), 8.05 д (1Н, С4Н, J 8 Гц), 8.85 д (1H, С2Н, J 8 Гц). Масс-спектр, m/z (Iотн. (%)): 143.00 [М]+ (100), 144 (11), 142 (48), 115 (14), 89 (6), 71 (4), 51 (3).
8-Этилхинолин [14. Lu, В. J. Am. Chem. Soc. 2010, 132, 14070]. Выход 88%. Желтая жидкость. Т кип. 269°C. Спектр ЯМР 13С (δ, м.д.): 15.39 (СН3), 24.95 (СН2), 121.15 (С3), 126.16 (С6), 126.77 (С4а), 128.25 (С5), 128.71 (С7), 136.72 (С8), 143.24 (С4), 147.09 (С8а), 149.59 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.40 т (2Н, СН3, J 8 Гц), 3.32 к (2Н, СН2, J 7.6 Гц), 7.39 т (1Н, С3Н, J 6.8 Гц), 7.48 т (1Н, С6Н, J 8 Гц), 7.57 д (1Н, С5Н, J 8 Гц), 7.66 д (1Н, С7Н, J 8 Гц), 8.14 д (1Н, С4Н, J 7.6 Гц), 8.95 д (1Н, С2Н, J 8.8 Гц).
8-Хлорхинолин [15. Arjunan, V. J. Mol. Struct. 2011, 988, 91]. Выход 57%. T кип. 93-94°C/0.5 мм рт. ст. Желтая жидкость. Спектр ЯМР 13С (δ, м.д.): 121.78 (С3), 126.35 (С6), 127.09 (С5), 128.79 (С4а), 133.23 (С8), 129.43 (С7), 136.41 (С4), 144.20 (С8а), 150.79 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 7.44 т (1Н, С6Н, J 8 Гц), 7.45 т (1Н, С3Н, J 8 Гц), 7.73 д (1Н, С5Н, J 8 Гц), 7.81 д (1Н, С7Н, J 8.4 Гц), 8.13 д (1H, С4Н, J 8 Гц), 9.02 д (1Н, С2Н, J 7.6 Гц). Масс-спектр, m/z (Iотн. (%)): 163.00 [М]+ (100), 165 (33), 164 (12), 128 (26), 127(12), 101 (10), 75 (9).
7-Хлорхинолин [16. Joseph-Nathan, P. Magnetic Resonance in Chemistry 1990, 28, 299; Hirner, J.J. Tetrahedron Lett. 2009, 50, 4989]. Выход 66% (7-хлор-:5-хлор-=2:1). T кип. 70-71°C/0.2 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 121.65 (С3), 126.64 (С4а), 127.34 (С6), 128.13 (С8), 129.09 (С5), 135.49 (С7), 136.13 (С4), 148.56 (С8а), 151.08 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 7.23-7.30 м (1Н, С3Н), 7.35-7.55 м (1H, С6Н), 7.69 д (1Н, С5Н, J 8 Гц), 8.00 с (1H, С8Н), 8.13 д (1Н, С4Н, J 8 Гц), 8.99 д (1H, С2Н, J 8 Гц).
5-Хлорхинолин. Спектр ЯМР 13С (δ, м.д.): 122.05 (С3), 127.88 (С4а), 126.63 (С8), 127.29 (С6), 129.01 (С7), 135.49 (С5), 136.13 (С4), 149.07 (С8а), 151.14 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 7.23-7.30 м (1Н, С3Н), 7.35-7.55 м (1Н, С6Н), 7.76 д (1H, С7Н, J 8 Гц), 8.03 д (1H, С8Н, J 7.6 Гц), 8.10 д (1H, С4Н, J 8 Гц), 9.01 д (1Н, С2Н, J 8 Гц).
6-Хлорхинолин [17. Gaywood, А.Р. New J. Chem. 2010, 34, 236]. Выход 86%). Светло-желтая жидкость. Т кип. 126-127°C/10 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 121.79 (С3), 126.29 (С5), 128.77 (С4а), 130.21 (С7), 131.06 (С8), 132.15 (С6), 135.03 (С4), 146.42 (С8а), 150.53 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 7.40 т (1Н, С3Н, J 7.6 Гц), 7.63 д (1H, С7Н, J 8 Гц), 7.78 с (1H, С5Н), 8.03 д (1Н, С4Н, J 8 Гц), 8.05 д (1Н, С8Н, J 8.4 Гц), 8.90 д (1Н, С2Н, J 8 Гц). Масс-спектр, m/z (Iотн.. (%)): 163.00 [М]+ (100), 165 (31), 164 (13), 136 (8), 101 (9), 75 (8), 68 (5).
6-Метоксихинолин [18. Monrad, R.N.; Madsen, R. Org. Biomol. Chem. 2011, 9, 610]. Выход 69%. Светло-желтая жидкость. T кип. 91-92°C/0.4 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 55.40 (ОСН3), 105.09 (С5), 121.26 (С3), 122.23 (С7), 129.25 (С4а), 130.73 (С8), 134.73 (С4), 144.43 (С8а), 147.83 (С2), 157.63 (С6). Спектр ЯМР 1H (CDCl3, δ, м.д.): 3.87 с (3Н, ОСН3), 6.99 с (1Н, С5Н), 7.29 д (1Н, С7Н, J 7.6 Гц), 7.33 т (1H, С3Н, J 7.6 Гц), 7.95 д (1Н, С4Н, J 8 Гц), 7.98 д (1H, С8Н, J 8.4 Гц), 8.75 д (1Н, С2Н, J 7.6 Гц). Масс-спектр, m/z (Iотн. (%)): 159.00 [М]+ (100), 160 (12), 144 (11), 129 (14), 116 (67), 89 (17), 63 (9).
8-Гидроксихинолин [19. Fomichev, A.A. Khimiya Geterotsiklicheskikh Soedinenii 1977, 9, 1235]. Выход 79%. Белый кристаллический порошок. Т пл. 72-76°C. Спектр ЯМР 13С (δ, м.д.): 110.60 (С7), 118.03 (С5), 121.59 (С3), 127.65 (С6), 128.63 (С4а), 136.18 (С4), 138.29 (С8а), 148.09 (С2), 152.51 (С8). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 7.19 д (1Н, С7Н, J 8 Гц), 7.33 д (1H, С5Н, J 8.8 Гц), 7.43 т (1Н, С3Н, J 8 Гц), 7.46 т (1H, С6Н, J 7.2 Гц), 8.15 д (1Н, С4Н, J 8 Гц), 8.30 уш. с (1Н, ОН), 8.79 д (1H, С2Н, J 7.6 Гц). Масс-спектр, m/z (Iотн. (%)): 145.00 [М]+ (100), 146 (10), 117 (51), 90 (18), 89 (17), 63 (11), 59 (9).
2-Метилхинолин [20. Khusnutdinov, R.I.; Bayguzina, A.R.; Aminov, R.I.; Dzhemilev, U.M. Russ. J. Org. Chem. 2012, 48, 679]. Выход 95% (2-метил-:4-метил-=1:2). Маслянистая желтая жидкость. Т кип. 80-81°C/2 мм рт. ст. (Т кип. 248°C, 105-107°C/10 мм рт. ст. [268]. Спектр ЯМР 13С (δ, м.д.): 25.12 (СН3), 121.74 (С3), 125.45 (С6), 126.32 (С4а), 127.37 (С5), 128.80 (С8), 129.19 (С7), 135.84 (С4), 147.76 (С8а), 158.67 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.78 с (3Н, СН3), 7.22 д (1Н, С3Н, J 8 Гц), 7.68 т (1Н, С7Н, J А Гц), 7.46 т (1Н, С6Н, J6.4 Гц), 7.73 д (1Н, С5Н, J9.2 Гц), 7.91 д (1Н, С4Н, J9.2 Гц), 7.91 д (1H, С8Н, J 9.2 Гц). Масс-спектр, m/z (Iотн. (%)): 143.18 [М]+ (100), 128 (20), 115 (22), 101 (5), 89 (4), 75 (5), 51 (4).
4-Метилхинолин [21. De, Kavita J. Org. Chem. 2009, 74, 6260]. Спектр ЯМР 13C (δ, м.д.): 18.40 (CH3), 121.87 (С3), 123.85 (С5), 126.33 (С6), 127.99 (С4а), 128.95 (С7), 129.76 (С8), 144.50 (С4), 147.76 (С8а), 150.01 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.68 с (3Н, СН3), 7.18 д (1Н, С3Н, J8 Гц), 7.53 т (1Н, С6Н, J 7.6 Гц), 7.68 т (1H, С7Н, J 7.6 Гц), 7.95 д (1Н, С5Н, /9.2 Гц), 8.09 д (1Н, С8Н, J 8.4 Гц), 8.73 д (1Н, С2Н, J 8.4 Гц). Масс-спектр, m/z (Iотн. (%)): 143.18 [М]+ (100), 128 (34), 115 (19), 101 (8), 89 (5), 75 (4), 51(4).
2,8-Диметилхинолин [22. Sridharan, V. Tetrahedron 2006, 63, 673]. Выход 80% (2,8-диметил-:4,8-диметил-=1:2). Маслянистая желтая жидкость. Т кип. 65-66°C/0.3 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 21.56 (СН3), 25.67 (СН3), 121.63 (С3), 125.29 (С5), 126.98 (С6), 127.33 (С4а), 128.26 (С7), 136.50 (С8), 137.49 (С4), 144.67 (С8а), 157.85 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.) 2.65 с (3Н, СН3), 2.87 с (3Н, СН3), 6.98 д (1H, С5Н, J 8 Гц), 7.24 д (1Н, С3Н, J 8.4 Гц), 7.38 т (1Н, С6Н, J 8 Гц), 7.65 д (1H, С7Н, J 8 Гц), 7.89 д (1Н, С4Н, J 7.6 Гц). Масс-спектр, m/z (Iотн. (%)): 157.00 [М]+ (100), 156 (31), 143 (10), 115 (8), 71 (4), 65 (2), 52 (2).
4,8-Диметилхинолин. Спектр ЯМР 13С (δ, м.д.): 18.91 (СН3), 18.94 (СН3), 121.79 (С3), 125.55 (С6), 126.07 (С5), 129.42 (С7), 136.26 (С8), 139.45 (С4а), 148.84 (С4), 147.00 (С8а), 148.94 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.) 2.79 с (3Н, СН3), 2.89 с (3Н, СН3), 7.15-7.30 м (1Н, С3Н), 7.47 т (1Н, С6Н, J 7.2 Гц), 7.50-7.65 м (1Н, С7) 7.86 д (1H, С5Н, J 8.4 Гц), 8.84 д (1H, С2Н, J 7.6 Гц). Масс-спектр, m/z (Iотн. (%)): 157.00 [М]+ (100), 156 (31), 143 (10), 115 (8), 71 (4), 65 (2), 52 (2).
2,7-Диметилхинолин [23. Matsubara, Y. Angew. Chem., Int. Ed. 2011, 50, 7670]. Выход 78% (2,7-диметил-:2,5-диметил-:4,7-диметил-=2:1:3). Маслянистая желтая жидкость, Т кип. 53-54°C/0.25 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 21.78 (СН3), 25.29 (СН3), 121.00 (С3), 124.48 (С5), 127.03 (С4а), 127.78 (С8), 127.81 (С7), 135.65 (С6), 139.40 (С4), 148.26 (С8а), 158.71 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.) 2.40 с (3Н, СН3), 2.64 с (3Н, СН3), 7.00 д (1Н, С5Н, J 8 Гц), 7.03 д (1Н, С6Н, J 8 Гц), 7.47 д (1Н, С4Н, J 7.6 Гц), 7.78 д (1Н, С3Н, J 8.4 Гц), 7.79 с (1Н, С8Н). Масс-спектр, m/z (Iотн. (%)): 157.00 [М]+ (100), 156 (28), 142 (11), 115 (11), 89 (4), 65 (4), 51 (4).
4,7-Диметилхинолин [21. De, Kavita J. Org. Chem. 2009, 74, 6260]. Спектр ЯМР 13C (δ, м.д.): 18.61 (CH3), 21.72 (СН3), 121.13 (С3), 123.56 (С6), 126.34 (С5), 128.56 (С4а), 128.82 (С8), 139.3 (С7), 144.15 (С4), 148.10 (С8а), 150.04 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.) 2.54 с (3Н, СН3), 2.64 с (3Н, СН3), 7.14 д (1Н, С3Н, J 7.2 Гц), 7.38 д (1Н, С8Н, J 6.8 Гц), 7.85-7.95 м (1H, С5,6Н), 8.71 д (1Н, С2Н, J 8 Гц).
2,6-Диметилхинолин [24. Sridharan, V. Tetrahedron 2006, 63, 673]. Выход 93% (2,6-диметил-:4,6-диметил=1:1). Т кип. 75-76°C/0.4 мм рт.ст. Спектр ЯМР 13С (δ, м.д.): 21.36 (СН3), 25.13 (СН3), 121.78 (С3), 126.37 (С5), 126.42 (С4а), 128.35 (С8), 131.50 (С7), 135.19 (С6), 135.41 (С4), 146.76 (С8а), 157.84 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.54 с (3Н, СН3), 2.72 с (СН3), 7.21 д (1Н, С3Н, J 8 Гц), 7.59 д (1Н, С7Н, J 8.4 Гц), 7.73 с (1Н, С5Н), 7.95 д (1Н, С4Н, J 7.2 Гц), 7.93 д (1Н, С8Н, J 8.4 Гц). Масс-спектр, m/z (Iотн. (%)): 157.00 [М]+ (100), 156 (32), 142 (8), 115 (8), 89 (3), 77 (3), 65 (3).
4,6-Диметилхинолин [21. De, Kavita J. Org. Chem. 2009, 74, 6260]. Спектр ЯМР 13C (δ, м.д.): 18.61 (CH3), 21.80 (СН3), 121.81 (С3), 122.75 (С5), 128.20 (С4а), 129.60 (С8), 131.34 (С7), 136.02 (С4), 143.53 (С6), 146.46 (С8а), 149.21 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.59 с (3Н, СН3), 2.69 с (3Н, СН3), 7.16 д (1Н, С3Н, J 8 Гц), 7.52 д (1Н, С7Н, J 8.4 Гц), 7.72 с (1Н, С5Н), 7.99 д (1Н, С8Н, J 8.4 Гц), 8.69 д (1Н, С2Н, J 7.6 Гц). Масс-спектр, m/z (Iотн. (%)): 158.00 [М]+ (100).
2-Метил-8-этилхинолин. Выход 87% (2-метил-8-этил-:4-метил-8-этил-=1:2). Маслянистая желтая жидкость Т кип. 73-74°C/0.2 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 15.15 (СН2СН3), 24.34 (СН2СН3), 25.68 (СН3), 121.82 (С3), 125.43 (С5), 126.07 (С6), 126.24 (С4а), 128.34 (С7), 136.15 (С8), 142.38 (С4), 146.47 (С8а), 157.65 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.30-1.60 м (3Н, СН3), 2.78 с (3Н, СН3), 3.30-3.50 м (2Н, СН2), 7.43 т (1Н, С6Н, J 7.2 Гц), 7.56 д (1H, С7Н, J 6.8 Гц), 7.55-7.68 м (1Н, С5Н), 7.99 с (1Н, С4Н). Масс-спектр, m/z (Iотн. (%)): 170.10 [М]+ (100), 171 (83), 143 (63), 128 (16), 115 (36), 63 (40), 51 (50).
4-Метил-8-этилхинолин. Спектр ЯМР 13С (δ, м.д.): 15.22 (СН2СН3), 25.00 (СН2СН3), 18.97 (СН3), 121.79 (С3), 125.39 (С5), 126.03 (С6), 126.43 (С4а), 127.67 (С7), 136.22 (С8), 143.40 (С4), 144.36 (С8а), 148.91 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1.30-1.60 м (3Н, СН3), 2.68 с (3Н, СН3), 3.30-3.50 м (2Н, СН2), 7.51 т (1Н, С6Н, J 7.6 Гц), 7.60 д (1Н, С7Н, J 7.6 Гц), 7.86 д (1Н, С5Н, J 8.4 Гц), 7.99 с (1Н, С4Н). Масс-спектр, m/z (Iотн. (%)): 170.10 [М]+ (100), 171 (83), 143 (63), 128 (16), 115 (36), 63 (40), 51 (50).
2-Метил-8-хлорхинолин. Выход 94% (2-метил-8-хлор-:4-метил-8-хлор-:=1:3). Т кип. 87-89°C/0.2 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 25.19 (СН3), 122.84 (С3), 125.45(С6), 126.32 (С4а), 127.37 (С5), 128.80 (С7), 130.13 (С8), 137.89 (С4), 148.56 (С8а), 161.87 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.84 с (3Н, СН3), 7.38-7.50 м (1Н, С3,6Н), 7.82 д (1H, С7Н, J 7.6 Гц), 8.00 д (1Н, С4Н, J 8.4 Гц), 8.03 д (1Н, С5Н, J 8 Гц). Масс-спектр, m/z (Iотн. (%)): 177. 1 [М]+.
4-Метил-8-хлорхинолин. Спектр ЯМР 13С (δ, м.д.): 18.98 (СН3), 121.68 (С3), 125.41 (С6), 126.41 (С4а), 127.71 (С7), 127.65 (С5), 142.30 (С8), 143.28 (С4), 144.53 (С8а), 148.84 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.68 с (3Н, СН3), 7.20-7.40 м (1Н, С3Н), 7.45-7.60 м (1Н, С6Н), 7.58 д (1Н, С7Н, J 7.6 Гц), 7.84 д (1Н, С5Н, J 8.4 Гц), 8.80 м (1Н, С2Н). Масс-спектр, m/z (Iотн. (%)): 177. 1 [М]+, 142 (14), 115 (15), 76 (7).
2-Метил-7-хлорхинолин. Выход 79% (2-метил-7-хлор:2-метил-5-хлор:4-метил-7-хлор=2:1:3). Маслянистая желтая жидкость, Т кип. 70-71°C/0.2 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 25.38 (СН3), 122.17 (С3), 124.89 (С6), 126.69 (С4а), 124.86 (С5), 127.85 (С8), 135.11 (С7), 135.84 (С4), 148.36 (С8а), 159.99 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.63 с (3Н, СН3), 7.12 д (1Н, С3Н, J 7.6 Гц), 7.25 д (1H, С6Н, J 7.6 Гц), 7.48 д (1Н, С5Н, J 9.2 Гц), 7.84 д (1Н, С4Н, J 8.4 Гц), 7.93 с (1H, С8Н). Масс-спектр, m/z (Iотн. (%)): 177 [М]+ (100), 179 (32), 178 (12), 142 (16), 115 (15), 76 (6).
2-Метил-5-хлорхинолин Спектр ЯМР 13С (δ, м.д.): 25.38 (СН3), 122.82 (С3), 124.96 (С6), 126.63 (С8), 126.69 (С4а), 130.08 (С7), 132.85 (С4), 134.88 (С5), 148.14 (С8а), 159.80 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.66 с (3Н, СН3), 7.11 д (1Н, С3Н, J 7.6 Гц), 7.24 д (1H, С6Н, J 7.6 Гц), 7.45 т (1H, С7Н, J 8.4 Гц), 7.84 д (1Н, С4Н, J 8 Гц), 8.20 д (1H, С8Н, J 7.6 Гц).
4-Метил-7-хлорхинолин. Спектр ЯМР 13С (δ, м.д.): 18.55 (СН3), 122.04 (С3), 125.23 (С6), 127.82 (С4а), 130.25 (С5), 127.16 (С8), 134.90 (С7), 144.40 (С4), 150.19 (С8а), 151.14 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.75 с (3Н, СН3), 7.10-7.20 м (1Н, С3Н), 7.30-7.55 м (1Н, С6Н), 7.70-8.00 м (1Н, С5Н), 8.07 с (1Н, С8Н), 8.60-8.78 м (1Н, С2Н). Масс-спектр, m/z (Iотн. (%)): 177 [М]+ (100), 179 (34), 178 (10), 143 (12), 115 (19), 76 (9).
2-Метил-6-хлорхинолин [25. Ramesh, С. Tetrahedron Lett. 2010, 51, 5234]. Выход 82% (2-Метил-6-хлор-:4-Метил-6-хлор-=1:2). Маслянистая желтая жидкость, Т кип. 70-71°C/0.2 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 25.30 (СН3), 122.89 (С3), 135.21 (С6), 128.99 (С4а), 126.41 (С5), 122.89 (С8), 130.16 (С7), 135.21 (С4), 145.55 (С8а), 159.01 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.69 с (3Н,СН3), 7.28 д (1Н, С3Н, J 7.6 Гц), 7.60 д (1Н, С7Н, J 7.6 Гц), 7.73 с (1Н, С5Н), 7.91 д (1Н, С8Н, J 8.4 Гц) 8.03 д (1H, С4Н, J 7.6 Гц). Масс-спектр, m/z (Iотн. (%)): 177 [М]+ (100), 179 (47), 142 (48), 116 (27), 99 (24), 51 (23).
4-Метил-6-хлорхинолин. Спектр ЯМР 13С (δ, м.д.): 18.57 (СН3), 122.85 (С3), 135.10 (С6), 127.05 (С4а), 126.11 (С5), 122.85 (С8), 130.26 (С7), 143.93 (С4), 145.86 (С8а), 150.07 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.69 с (3Н,СН3), 7.25 д (1Н, С3Н, J 7.6 Гц), 7.72 д (1Н, С7Н, J7.6 Гц), 7.72 с (1Н, С5Н), 8.10 д (1H, С8Н, J 8.4 Гц), 8.76 д (1H, С2Н, J 8 Гц). Масс-спектр, m/z (Iотн. (%)): 177 [М]+ (100), 179 (42), 142 (51), 116 (27), 99 (14), 51 (27).
2-Метил-6-метоксихинолин [26. Choi, H.Y. J. Org. Chem. 2005, 70, 1222]. Выход 89% (2-метил-6-метокси-:4-метил-6-метокси-=1:1). Маслянистая желтая жидкость, Т кип. 95-96°C/0.4 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 24.85 (СН3), 55.42 (ОСН3), 121.71 (С3), 122.01 (С6), 127.32 (С4а), 129.89 (С7), 134.78 (С4), 143.67 (С5), 155.49 (С8а), 157.45 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.69 с (3Н, СН3), 3.76 с (3Н, -ОСН3), 6.89 д (1Н, С3Н, J 8 Гц), 7.48 д (1Н, С7Н, J 7.6 Гц), 7.63 с (1Н, С5Н), 7.71 д (1Н, С4Н, J 8.4 Гц), 7.91 д (1Н, С8Н, J 9.2 Гц). Масс-спектр, m/z (Iотн. (%)): 173 [М]+ (100), 158 (38), 130 (80), 103 (23), 77 (23).
4-Метил-6-метоксихинолин Спектр ЯМР 13С (δ, м.д.): 18.80 (СН3), 55.53 (ОСН3), 101.9 (С5), 121.47 (С7), 122.15 (С3), 129.25 (С4а), 131.46 (С4), 142.73 (С8), 144.01 (С8а), 147.67 (С2), 157.60 (С6). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.63 с (3Н, СН3), 3.94 с (3Н, ОСН3), 7.15-7.18 м (2Н, С3,5Н), 7.35 д (1Н, С7Н, J 7.6 Гц), 8.00 д (1Н, С8Н, J 8.4 Гц), 8.61 д (1H, С2Н, J 8.8 Гц).
8-Гидрокси-2-метилхинолин [27. Chen, M.-Y. J. Chin. Chem. Soc. 2004, 51, 735]. Выход 90% (8-гидрокси-2-метил-:8-гидрокси-4-метил-=1:1).T кип. 64-65°C/0.2 мм рт. ст. Спектр ЯМР 13С (δ, м.д.): 24.82 (СН3), 110.32 (С7), 117.37 (С5), 122.57 (С3), 126.59 (С6), 127.98 (С4а), 136.04 (С4), 138.65 (С8а), 151.80 (С8), 156.77 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.72 с (3Н, СН3), 7.14 д (1Н, С7Н, J 7.6 Гц), 7.27 д (1H, С5Н, J 4.4 Гц), 7.29 д (1Н, С3Н, J 8.4 Гц), 7.38 т (1Н, С6Н, J 7.6 Гц), 8.02 д (1Н, С4Н, J 8 Гц). Масс-спектр, m/z (Iотн (%)): 159 [М]+ (100), 160 (12), 131 (53), 130 (24), 89 (4), 77 (7).
8-Гидрокси-4-метилхинолин. Спектр ЯМР 13С (δ, м.д.): 18.72 (СН3), 109.68 (С7), 114.87 (С5), 122.46 (С3), 127.2 (С4а), 128.41 (С6), 138.04 (С4), 145.00 (С8а), 147.30 (С8), 152.57 (С2). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 2.68 с (3Н, СН3), 7.12-7.28 м (2Н, С3,5Н), 7.43-7.45 м (2Н, С6,7Н), 8.61 д (1Н, С2Н, J 8.4 Гц). Масс-спектр, m/z (Iотн (%)): 159 [М]+ (100), 160 (12), 131 (77).
Claims (1)
- Способ получения замещенных хинолинов формулы
взаимодействием анилинов с 1,3-диолами под действием катализаторов, отличающийся тем, что замещенные анилины формулы XC6H4NH2, где X - указанное выше, подвергают взаимодействию с 1,3-диолами (1,3-пропандиолом или 1,3-бутандиолом) и CCl4 в присутствии катализатора, выбранного из ряда FeCl3·6H2O, FeCl3, FeCl2·4H2O, Fe(C5H5)2, Fe(acac)3, Fe(OAc)2 и Fe2(CO)9, при мольном соотношении [катализатор]:[анилин]:[CCl4]:[диол]=1:100:200:400, при 150°C в течение 8 ч, полученную реакционную массу нейтрализуют, органический слой экстрагируют CH2Cl2, отфильтровывают и отгоняют растворитель.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013151207/04A RU2561503C2 (ru) | 2013-11-18 | 2013-11-18 | СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013151207/04A RU2561503C2 (ru) | 2013-11-18 | 2013-11-18 | СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2013151207A RU2013151207A (ru) | 2015-05-27 |
| RU2561503C2 true RU2561503C2 (ru) | 2015-08-27 |
Family
ID=53284750
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2013151207/04A RU2561503C2 (ru) | 2013-11-18 | 2013-11-18 | СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2561503C2 (ru) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2614251C2 (ru) * | 2015-07-06 | 2017-03-24 | Федеральное государственное бюджетное учреждение науки Институт нефтехимии и катализа Российской академии наук | СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,2-ДИОЛОВ И ССl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4599449A (en) * | 1984-06-25 | 1986-07-08 | Ethyl Corporation | Catalytic alkylation of aromatic amines with alkanols |
-
2013
- 2013-11-18 RU RU2013151207/04A patent/RU2561503C2/ru not_active IP Right Cessation
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4599449A (en) * | 1984-06-25 | 1986-07-08 | Ethyl Corporation | Catalytic alkylation of aromatic amines with alkanols |
Non-Patent Citations (1)
| Title |
|---|
| Хуснутдинов Р.И. и др.: "Синтез замещенных хинолинов реакцией анилинов со спиртами и ССl4 под действием Fe-содержащих катализаторов", Известия Академии Наук, Серия химическая, 1, 2013, стр.134-138. * |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2013151207A (ru) | 2015-05-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Zare et al. | Ionic liquid 1, 3-disulfonic acid imidazolium hydrogen sulfate: A novel and highly efficient catalyst for the preparation of 1-carbamatoalkyl-2-naphthols and 1-amidoalkyl-2-naphthols | |
| Karmakar et al. | Phosphatase-mimicking activity of a unique penta-nuclear zinc (II) complex with a reduced Schiff base ligand: assessment of its ability to sense nitroaromatics | |
| Agrahari et al. | Synthesis and crystal structures of salen-type Cu (ii) and Ni (ii) Schiff base complexes: application in [3+ 2]-cycloaddition and A 3-coupling reactions | |
| Parekh et al. | Ether-tethered Ru (II)/TsDPEN complexes; synthesis and applications to asymmetric transfer hydrogenation | |
| ES2644115T3 (es) | Imidodifosfatos quirales y sus derivados | |
| Gopalaiah et al. | Iron-catalyzed cascade reaction of 2-aminobenzyl alcohols with benzylamines: synthesis of quinazolines by trapping of ammonia | |
| CN112779001A (zh) | 一种近红外粘度荧光探针的制备及其应用 | |
| US20140288306A1 (en) | Process for preparing amines from alcohols and ammonia | |
| JP7010822B2 (ja) | キラルなホスホルアミドイミデートおよびその誘導体 | |
| Wang et al. | Synthesis, structure and catalytic properties of CNN pincer palladium (II) and ruthenium (II) complexes with N-substituted-2-aminomethyl-6-phenylpyridines | |
| Rodríguez-Lugo et al. | Synthesis, characterization and Pd (II)-coordination chemistry of the ligand tris (quinolin-8-yl) phosphite. Application in the catalytic aerobic oxidation of amines | |
| Mamedov et al. | A novel acid-catalyzed rearrangement of 2-substituted-3-(2-nitrophenyl) oxiranes for the synthesis of di-and mono-oxalamides | |
| Samanta et al. | A mononuclear copper (II) complex immobilized in mesoporous silica: an efficient heterogeneous catalyst for the aerobic oxidation of benzylic alcohols | |
| RU2561503C2 (ru) | СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,3-ДИОЛОВ И CCl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ | |
| Kumar et al. | Metal-free C (sp 3)–H bond activation: first synthesis of diaryl-pyridinium-azaarene-butenolate zwitterionic salts on chalcones | |
| Basu et al. | Mononuclear organogermanium (iv) catalysts for a [3+ 2] cycloaddition reaction | |
| Radhakrishna et al. | 1, 2, 3-Triazole based ligands with phosphine and pyridine functionalities: synthesis, Pd II and Pt II chemistry and catalytic studies | |
| CN103524423B (zh) | 4,6-二氯代嘧啶-5-乙醛的制备方法 | |
| Xue et al. | Iron (II) complexes with functionalized amine-pyrazolyl tripodal ligands in the cross-coupling of aryl Grignard with alkyl halides | |
| Pradhan et al. | A discrete self-assembled palladium nano-cage catalyses Suzuki–Miyaura coupling heterogeneously and Heck–Mizoroki coupling homogeneously | |
| Lasri et al. | Pd II-promoted [2+ 3] cycloaddition of pyrroline N-oxide to organonitriles. Application of (Δ 4-1, 2, 4-oxadiazoline)-Pd II complexes in the Suzuki–Miyaura reaction | |
| US7888509B2 (en) | Chiral 1,8-diarylnaphthalenes, methods of making them, and their use as sensors | |
| RU2504540C2 (ru) | Способ получения 2- и 2,3-замещенных хинолинов | |
| Smrečki et al. | Preparation and characterization of palladium (II) complexes with N-arylalkyliminodiacetic acids. Catalytic activity of complexes in methoxycarbonylation of iodobenzene | |
| RU2614251C2 (ru) | СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОЛИНОВ ИЗ АНИЛИНА, 1,2-ДИОЛОВ И ССl4 ПОД ДЕЙСТВИЕМ ЖЕЛЕЗОСОДЕРЖАЩИХ КАТАЛИЗАТОРОВ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20151119 |