RU2462236C2 - Липосомальная нанокапсула - Google Patents
Липосомальная нанокапсула Download PDFInfo
- Publication number
- RU2462236C2 RU2462236C2 RU2010110834/15A RU2010110834A RU2462236C2 RU 2462236 C2 RU2462236 C2 RU 2462236C2 RU 2010110834/15 A RU2010110834/15 A RU 2010110834/15A RU 2010110834 A RU2010110834 A RU 2010110834A RU 2462236 C2 RU2462236 C2 RU 2462236C2
- Authority
- RU
- Russia
- Prior art keywords
- liposomal
- nanocapsule
- peloids
- lipid
- extract
- Prior art date
Links
- 239000002088 nanocapsule Substances 0.000 title claims abstract description 20
- 150000002632 lipids Chemical class 0.000 claims abstract description 28
- 239000000284 extract Substances 0.000 claims abstract description 20
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 claims abstract description 18
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 14
- 239000002537 cosmetic Substances 0.000 claims abstract description 10
- 230000002209 hydrophobic effect Effects 0.000 claims abstract description 10
- 229930003427 Vitamin E Natural products 0.000 claims abstract description 9
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 claims abstract description 9
- 235000019165 vitamin E Nutrition 0.000 claims abstract description 9
- 229940046009 vitamin E Drugs 0.000 claims abstract description 9
- 239000011709 vitamin E Substances 0.000 claims abstract description 9
- 239000003814 drug Substances 0.000 claims abstract description 7
- 150000003904 phospholipids Chemical class 0.000 claims abstract description 3
- 239000003381 stabilizer Substances 0.000 claims abstract description 3
- 230000001225 therapeutic effect Effects 0.000 claims description 8
- 239000012528 membrane Substances 0.000 claims description 7
- 239000006286 aqueous extract Substances 0.000 claims description 2
- 239000000126 substance Substances 0.000 abstract description 7
- 230000000694 effects Effects 0.000 abstract description 6
- 230000000144 pharmacologic effect Effects 0.000 abstract description 2
- 239000011248 coating agent Substances 0.000 abstract 2
- 238000000576 coating method Methods 0.000 abstract 2
- 239000002502 liposome Substances 0.000 description 13
- 239000012071 phase Substances 0.000 description 11
- 239000003921 oil Substances 0.000 description 10
- 235000019198 oils Nutrition 0.000 description 10
- 239000000203 mixture Substances 0.000 description 5
- 239000002105 nanoparticle Substances 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 238000000605 extraction Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 239000011148 porous material Substances 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 210000000865 mononuclear phagocyte system Anatomy 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 206010061218 Inflammation Diseases 0.000 description 2
- 108700022034 Opsonin Proteins Proteins 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 229960004679 doxorubicin Drugs 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 235000019441 ethanol Nutrition 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 238000000034 method Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000700157 Rattus norvegicus Species 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 230000036528 appetite Effects 0.000 description 1
- 235000019789 appetite Nutrition 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 210000002421 cell wall Anatomy 0.000 description 1
- 229940044683 chemotherapy drug Drugs 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Natural products C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 229940088679 drug related substance Drugs 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 150000002433 hydrophilic molecules Chemical class 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 150000002634 lipophilic molecules Chemical class 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 238000000622 liquid--liquid extraction Methods 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 229940042880 natural phospholipid Drugs 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 238000005728 strengthening Methods 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
Images
Landscapes
- Medicinal Preparation (AREA)
- Cosmetics (AREA)
Abstract
Изобретение относится к липосомальной препаративной форме для лечебно-косметического и наружного фармакологического применения. Липосомальная нанокапсула представляет собой полую сферу, образованную двухслойной липидной оболочкой, содержащей внешний и внутренний гидрофильные слои, включающие водный экстракт пелоидов, между которыми расположена гидрофобная область двухслойной липидной оболочки, включающая липидный экстракт пелоидов, полярно заряженные молекулы которой расположены на поверхностях внешнего и внутреннего гидрофильных слоев. При этом липосомальная нанокапсула содержит, %: водный экстракт пелоидов - 74%, липидный экстракт пелоидов - 20%, витамин Е - 5%, стабилизатор на фосфолипидной основе - 1%. Изобретение обеспечивает усиление лечебно-косметического эффекта липосомальной нанокапсулы. 1 ил., 1 табл., 2 пр.
Description
Изобретение относится к области прикладной биотехнологии, а именно к конструкциям липосомальных препаративных форм для лечебно-косметического и наружного фармакологического применения.
К одному из типов нанокапсул относят липосомы, которые являются контейнерами для доставки лекарственных средств. Мембрана липосом состоит из природных фосфолипидов, что определяет их многие привлекательные качества. Они нетоксичны, биодеградируемы, при определенных условиях могут поглощаться клетками, их мембрана может сливаться с клеточной мембраной, что приводит к внутриклеточной доставке их содержимого.
Очень важное свойство липосом (как, впрочем, и других наночастиц) стало основой для конструирования эффективных лекарственных препаратов. Речь идет о соотношении размеров наночастиц и диаметра пор капилляров. Так как размер наночастиц больше диаметра пор капилляров, их объем распределения ограничивается контрпараметрами введения. Например, при внутривенном введении они не выходят за пределы кровотока, т.е. должны плохо проникать в органы и ткани. Следовательно, резко понижается токсическое действие субстанции, ассоциированной с наночастицами. С другой стороны, это свойство может служить основой для направленной доставки химиотерапевтических препаратов в очаги воспаления и деформации, так как капилляры, снабжающие эти области кровью, как правило, сильно перфорированные. Следовательно, наночастицы будут накапливаться в очагах воспаления и деформации. Это явление получило название пассивное нацеливание. Таким образом, существуют две причины, вследствие которых липосомальные препараты противовоспалительных и регенерирующих субстанций очень эффективны: уменьшение токсичности и пассивное нацеливание.
В настоящее время на мировом фармацевтическом рынке появилось несколько липосомальных препаратов (Northfelt D.W., Kaplan L., Russell J. et al. (1995) in Stealth Liposomes (Lasic D.D., Martin F.J., eds). 257-266. CRC Press; Bogner J.R., Goebl F-D. (1995) in Stealth Liposomes (Lasic D.D., Martin F.J., eds). 267-278. CRC Press).
Однако недостатком вышеприведенных аналогов - липосомальных препаратов - является быстрое выведение липосом из крови, которое связано с поглощением их ретикулоэндотелиальной системой (РЭС) печени и селезенки. Это происходит вследствие взаимодействия липосом с белками плазмы - опсонинами (в основном, компонентами комплемента). Опсонины «метят» липосомы, делают их мишенями для клеток РЭС.
Известна конструкция липосомы фосфоролипидов (патент РФ №2270683, опубл. 27.02.2006 г.), которая стерически стабилизирована ковалентно связанными димирилфосфаэтаноламином и полиэтиленгликолем 2000.
Недостатком данной липосомы является то, что она не содержит лекарственный препарат и предназначена только для аэрозольного введения в организм, а не для инъекций.
Аналогом также является липосомальная нанокапсула, представляющая собой полую сферу, образованную двухслойной липидной оболочкой из фосфотидилхолина и димиристоилфосфотидилглицерина, содержащую внешний и внутренний гидрофильные липидные слои, между которыми расположена гидрофобная область двухслойной липидной оболочки. Кроме того, нанокапсула содержит лекарственное вещество доксорубицин, положительно заряженные молекулы которого расположены на поверхностях внешнего и внутреннего гидрофильных липидных слоев и прикреплены к молекулам отрицательно заряженного димиристоилфосфотидилглицерина (полезная модель RU 42953 U1, МПК A61K 9/127, опубл. 27.12.2004 г.).
Однако недостатком вышеприведенной липосомальной нанокапсулы является специфичность действия лекарственного средства доксорубицина и, следовательно, очень узкая область применения.
Наиболее близким техническим решением (прототипом) является липосомальная нанокапсула (ПМ №95519 от 10.07.2010), представляющая собой полую сферу, образованную двухслойной липидной оболочкой, содержащей внешний и внутренний гидрофильный слой, между которыми расположена гидрофобная область двухслойной липидной оболочки, полярно заряженные молекулы которой расположены на поверхностях внешнего и внутреннего гидрофильных слоев. Липидная оболочка содержит в качестве внутреннего и внешнего гидрофильных слоев водный экстракт пелоидов, а гидрофобной областью служит липидный экстракт пелоидов.
Однако такие нанокапсулы характеризуются недостаточным лечебно-косметическим эффектом.
Техническим результатом предлагаемого изобретения является усиление лечебно-косметического эффекта.
Указанный технический результат достигается тем, что в липосомальной нанокапсуле, представляющей собой полую сферу, образованную двухслойной липидной оболочкой, содержащей внешний и внутренний гидрофильные слои, между которыми расположена гидрофобная область двухслойной липидной оболочки, полярно заряженные молекулы которой расположены на поверхностях внешнего и внутреннего гидрофильных слоев, причем двухслойная липидная оболочка содержит в качестве внешнего и внутреннего гидрофильных слоев водный экстракт пелоидов, а гидрофобной областью служит липидный экстракт пелоидов, согласно заявляемому техническому решению липидная оболочка дополнительно содержит в качестве лечебно-косметического средства витамин Е при следующем содержании всех компонентов липосомальной нанокапсулы, %:
водный экстракт пелоидов - 74;
липидный экстракт пелоидов - 20;
витамин Е - 5;
стабилизатор на фосфолипидной основе - 1.
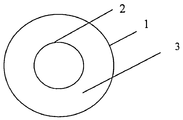
Изобретение поясняется чертежом, где представлена конструкция липосомальной нанокапсулы.
Липосомальная нанокапсула представляет собой полую сферу, образованную двухслойной оболочкой, содержащей внешний 1 и внутренний 2 гидрофильные слои на основе водного экстракта пелоидов, между которыми расположена гидрофобная область 3 двухслойной оболочки на основе липидного экстракта пелоидов, содержащего указанное процентное содержание витамина Е (5%). Водный и липидный экстракты пелоидов проявляют выраженный лечебно-косметический эффект.
Примеры получения липосомальной нанокапсулы
Пример 1. Технология получения липосомальной нанокапсулы с лечебно-косметическими биологически-активными субстанциями
Водный и масляный экстракты пелоидов смешивают друг с другом до образования однородной эмульсии и давят на экструдере последовательно через мембраны с размерами пор 1000, 800, 400, 200 и 100 нм по нескольку раз сквозь каждую мембрану. Потом продукт фильтруют через фильтр с размером пор 220 нм для стерилизации, разливают по флаконам.
Пример 2. Приготовление экстрактов и комплексов на основе пелоидов
Применение в качестве экстрагента двухфазной системы растворителей (спирто-водная смесь/масло) позволяет за один технологический цикл получить сразу водно-спиртовое и масляное извлечения, т.е. проэкстрагировать из сырья гидрофильные и гидрофобные вещества. Двухфазная экстракция основана на предварительном смачивании сырья 96% этиловым спиртом и выдержке его в течение 1,5-2 ч. Затем добавляют масло растительное и очищенную воду, доводя до необходимой концентрации спирто-водный экстрагент и соотношение фаз (сырье/масло/спирто-водная смесь). Экстрагирование ведут при нагревании (80°С) и периодическом перемешивании. Затем разделяют по плотности вытяжки (спирто-водную и масляную).
Высокая эффективность метода экстракции двухфазной системой экстрагентов по сравнению с экстракцией маслом определяется ролью спиртовой фазы (ее составом и количеством) как фактора набухания растительного сырья, промежуточного растворителя и переносчика липофильных веществ из клеток сухого растительного сырья в масляную фазу. При контакте сырья с жидкими фазами экстрагентов спирто-водная смесь благодаря меньшей вязкости легко проникает в растительный материал, десорбирует внутриклеточные БАВ и путем диффузии переносит их через пористые клеточные стенки в спирто-водную фазу. Затем протекает процесс экстракции жидкость-жидкость (спирто-водный раствор - масло) при перемешивании мешалкой. Между спирто-водной и масляной фазами происходит процесс массопередачи, приводящий к перераспределению гидро- и липофильных соединений между фазами в соответствии с коэффициентами распределения. При этом преимущественно гидрофильные вещества остаются в спирто-водной фазе, а липофильные переходят в масляную. Выход по данной технологии составляет 60-70%.
Результаты исследования липосомального препарата на проявление местного лечебного эффекта
Задачей этапа экспериментальных исследований явилось изучение местного и общебиологического эффекта при аппликации нанолипосомальной капсулы на основе экстрактов пелоидов и витамина Е на кожную поверхность.
Проведены 20 серий экспериментов (6 контрольных и 14 опытных) на 276 белых беспородных крысах-самцах массой 200-300 г. Крысы помещались в отдельные клетки и наблюдались в течение 27 дней. Обработка кожи производилась ежедневно, один раз в сутки, утром в 9-00 ч. В то же время ежедневно проводились как общее наблюдение за животными (поведение, общее состояние, аппетит, сон, естественные отправления), так и характер состояния кожи (внешний вид, характер и скорость эпителизации, наличие и характер выделений). На 2, 7, 14, 21, 27-е сутки проводился забор материала на биохимические, иммунологические, патоморфологические исследования.
Проведенные исследования (см. таблицу) подтверждают усиление лечебно-косметического эффекта по сравнению с прототипом.
| Содержание нейтральных липидов в поверхностной липидной пленке кожи, % | ||
| Показатель | После аппликации липосомальной нанокапсулы без витамина Е | После аппликации липосомальной нанокапсулы с витамином Е |
| ФЛ | 11,21±1,26 | 10,85±0,80 |
| ХС | 20,00±1,81 | 21,07±0,76 |
| ЖК | 8,92±1,28 | 9,50±1,06 |
| ТАГ | 20,50±1,94 | 21,15±1,78 |
| ЭХС | 39,14±3,09 | 45,00±1,39 |
| Примечание ФЛ - фосфолипиды; ХС - холестерин; ЖК - жирные кислоты; ТАГ - триацилглицериды; ЭХС - эфиры холестерина |
||
Таким образом, применение данного средства обеспечивает положительную динамику клинико-биохимических показателей системы крови, а также состояния кожных покровов.
Claims (1)
- Липосомальная нанокапсула, представляющая собой полую сферу, образованную двухслойной липидной оболочкой, содержащей внешний и внутренний гидрофильные слои, между которыми расположена гидрофобная область двухслойной липидной оболочки, полярно заряженные молекулы которой расположены на поверхностях внешнего и внутреннего гидрофильных слоев, причем двухслойная липидная оболочка содержит в качестве внешнего и внутреннего гидрофильных слоев водный экстракт пелоидов, а гидрофобной областью служит липидный экстракт пелоидов, отличающаяся тем, что липидная оболочка дополнительно содержит в качестве лечебно-косметического средства витамин Е при следующем содержании всех компонентов липосомальной нанокапсулы, %:
Водный экстракт пелоидов 74 Липидный экстракт пелоидов 20 Витамин Е 5 Стабилизатор на фосфолипидной основе 1
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010110834/15A RU2462236C2 (ru) | 2010-03-22 | 2010-03-22 | Липосомальная нанокапсула |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2010110834/15A RU2462236C2 (ru) | 2010-03-22 | 2010-03-22 | Липосомальная нанокапсула |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010110834A RU2010110834A (ru) | 2011-09-27 |
| RU2462236C2 true RU2462236C2 (ru) | 2012-09-27 |
Family
ID=44803590
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010110834/15A RU2462236C2 (ru) | 2010-03-22 | 2010-03-22 | Липосомальная нанокапсула |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2462236C2 (ru) |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2556118C1 (ru) * | 2014-03-31 | 2015-07-10 | Александр Александрович Кролевец | Способ получения нанокапсул сел-плекса, обладающих супрамолекулярными свойствами |
| RU2555785C1 (ru) * | 2014-03-03 | 2015-07-10 | Александр Александрович Кролевец | Способ получения нанокапсул сульфата хондроитина в ксантановой камеди в гексане |
| RU2556200C1 (ru) * | 2014-05-06 | 2015-07-10 | Александр Александрович Кролевец | Способ получения нанокапсул цитокининов в альгинате натрия |
| RU2557975C1 (ru) * | 2014-03-26 | 2015-07-27 | Александр Александрович Кролевец | Способ получения нанокапсул сульфата глюкозамина в каррагинане |
| RU2559572C1 (ru) * | 2014-07-29 | 2015-08-10 | Александр Александрович Кролевец | Способ получения нанокапсул 2-цис-4-транс-абсцизовой кислоты |
| RU2559571C1 (ru) * | 2014-07-01 | 2015-08-10 | Александр Александрович Кролевец | Способ получения нанокапсул албендазола |
| RU2559577C1 (ru) * | 2014-04-08 | 2015-08-10 | Александр Александрович Кролевец | Способ получения нанокапсул витаминов в геллановой камеди |
| RU2560520C1 (ru) * | 2014-07-01 | 2015-08-20 | Александр Александрович Кролевец | Способ получения нанокапсул аденина в альгинате натрия |
| RU2560663C1 (ru) * | 2014-07-01 | 2015-08-20 | Александр Александрович Кролевец | Способ получения нанокапсул антибиотиков в агар-агаре |
| RU2560519C1 (ru) * | 2014-05-27 | 2015-08-20 | Александр Александрович Кролевец | Способ получения нанокапсул 2,4-дихлорфеноксиуксусной кислоты |
| RU2562561C1 (ru) * | 2014-04-01 | 2015-09-10 | Александр Александрович Кролевец | Способ получения нанокапсул витаминов в каррагинане |
| RU2565392C1 (ru) * | 2014-04-07 | 2015-10-20 | Александр Александрович Кролевец | Способ получения нанокапсул витаминов в ксантановой камеди |
| RU2598342C2 (ru) * | 2014-07-01 | 2016-09-20 | Александр Александрович Кролевец | Способ получения нанокапсул кинетина в альгинате натрия |
| RU2599006C1 (ru) * | 2015-05-26 | 2016-10-10 | Федеральное государственное автономное образовательное учреждение высшего образования "Белгородский государственный национальный исследовательский университет" (НИУ "БелГУ") | Способ получения нанокапсулированного иодида калия в альгинате натрия |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4016100A (en) * | 1975-01-27 | 1977-04-05 | Tanabe Seiyaku Co., Ltd. | Method of preparing a controlled release liquid pharmaceutical composition |
| RU2154465C2 (ru) * | 1994-04-12 | 2000-08-20 | Липожель | Микросферы, способ их получения |
| RU2166332C2 (ru) * | 1994-07-12 | 2001-05-10 | Скотиа Липидтекник АБ | Двуслойные препараты |
| RU42953U1 (ru) * | 2004-07-02 | 2004-12-27 | Закрытое акционерное общество "Вектор-Медика" | Липосомальная нанокапсула с доксорубицином |
| KR100726720B1 (ko) * | 2005-12-26 | 2007-06-11 | 코스맥스 주식회사 | 수난용성 활성물질을 하이드록시알킬화 사이클로덱스트린과리포좀으로 이중 안정화 시킨 나노캡슐 리포좀 조성물 |
-
2010
- 2010-03-22 RU RU2010110834/15A patent/RU2462236C2/ru not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4016100A (en) * | 1975-01-27 | 1977-04-05 | Tanabe Seiyaku Co., Ltd. | Method of preparing a controlled release liquid pharmaceutical composition |
| RU2154465C2 (ru) * | 1994-04-12 | 2000-08-20 | Липожель | Микросферы, способ их получения |
| RU2166332C2 (ru) * | 1994-07-12 | 2001-05-10 | Скотиа Липидтекник АБ | Двуслойные препараты |
| RU42953U1 (ru) * | 2004-07-02 | 2004-12-27 | Закрытое акционерное общество "Вектор-Медика" | Липосомальная нанокапсула с доксорубицином |
| KR100726720B1 (ko) * | 2005-12-26 | 2007-06-11 | 코스맥스 주식회사 | 수난용성 활성물질을 하이드록시알킬화 사이클로덱스트린과리포좀으로 이중 안정화 시킨 나노캡슐 리포좀 조성물 |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2555785C1 (ru) * | 2014-03-03 | 2015-07-10 | Александр Александрович Кролевец | Способ получения нанокапсул сульфата хондроитина в ксантановой камеди в гексане |
| RU2557975C1 (ru) * | 2014-03-26 | 2015-07-27 | Александр Александрович Кролевец | Способ получения нанокапсул сульфата глюкозамина в каррагинане |
| RU2556118C1 (ru) * | 2014-03-31 | 2015-07-10 | Александр Александрович Кролевец | Способ получения нанокапсул сел-плекса, обладающих супрамолекулярными свойствами |
| RU2562561C1 (ru) * | 2014-04-01 | 2015-09-10 | Александр Александрович Кролевец | Способ получения нанокапсул витаминов в каррагинане |
| RU2565392C1 (ru) * | 2014-04-07 | 2015-10-20 | Александр Александрович Кролевец | Способ получения нанокапсул витаминов в ксантановой камеди |
| RU2559577C1 (ru) * | 2014-04-08 | 2015-08-10 | Александр Александрович Кролевец | Способ получения нанокапсул витаминов в геллановой камеди |
| RU2556200C1 (ru) * | 2014-05-06 | 2015-07-10 | Александр Александрович Кролевец | Способ получения нанокапсул цитокининов в альгинате натрия |
| RU2560519C1 (ru) * | 2014-05-27 | 2015-08-20 | Александр Александрович Кролевец | Способ получения нанокапсул 2,4-дихлорфеноксиуксусной кислоты |
| RU2559571C1 (ru) * | 2014-07-01 | 2015-08-10 | Александр Александрович Кролевец | Способ получения нанокапсул албендазола |
| RU2560520C1 (ru) * | 2014-07-01 | 2015-08-20 | Александр Александрович Кролевец | Способ получения нанокапсул аденина в альгинате натрия |
| RU2560663C1 (ru) * | 2014-07-01 | 2015-08-20 | Александр Александрович Кролевец | Способ получения нанокапсул антибиотиков в агар-агаре |
| RU2598342C2 (ru) * | 2014-07-01 | 2016-09-20 | Александр Александрович Кролевец | Способ получения нанокапсул кинетина в альгинате натрия |
| RU2559572C1 (ru) * | 2014-07-29 | 2015-08-10 | Александр Александрович Кролевец | Способ получения нанокапсул 2-цис-4-транс-абсцизовой кислоты |
| RU2599006C1 (ru) * | 2015-05-26 | 2016-10-10 | Федеральное государственное автономное образовательное учреждение высшего образования "Белгородский государственный национальный исследовательский университет" (НИУ "БелГУ") | Способ получения нанокапсулированного иодида калия в альгинате натрия |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2010110834A (ru) | 2011-09-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2462236C2 (ru) | Липосомальная нанокапсула | |
| Chaves et al. | Current applications of liposomes for the delivery of vitamins: a systematic review | |
| Fereig et al. | Tackling the various classes of nano-therapeutics employed in topical therapy of psoriasis | |
| Gaynanova et al. | Self-assembling drug formulations with tunable permeability and biodegradability | |
| Yang et al. | Development of triptolide-nanoemulsion gels for percutaneous administration: physicochemical, transport, pharmacokinetic and pharmacodynamic characteristics | |
| Yang et al. | Enhanced oral bioavailability of silymarin using liposomes containing a bile salt: preparation by supercritical fluid technology and evaluation in vitro and in vivo | |
| Das et al. | Ethosomes as novel vesicular carrier: An overview of the principle, preparation and its applications | |
| Jing et al. | A novel polyethylene glycol mediated lipid nanoemulsion as drug delivery carrier for paclitaxel | |
| CN105456194A (zh) | 厚朴酚脂质体及其衍生制剂和制备方法 | |
| CN105708847A (zh) | 人参皂苷多组分共载靶向纳米体系的制备方法及其应用 | |
| Shinde et al. | Recent advances in vesicular drug delivery system | |
| Firthouse et al. | Formulation and evaluation of miconazole niosomes | |
| Wu et al. | Cholesterol and phospholipid-free multilamellar niosomes regulate transdermal permeation of a hydrophobic agent potentially administrated for treating diseases in deep hair follicles | |
| CN102485212B (zh) | 苹果酸舒尼替尼脂质体及其制备方法 | |
| KR20100024050A (ko) | 다중소포성 리포좀, 그 제조방법 및 이를 포함한 의약용 또는 화장료 조성물 | |
| CN102670508B (zh) | 一种稳定的脂质体及其制备方法 | |
| Tallam et al. | A review on phytosomes as innovative delivery systems for phytochemicals | |
| Thy et al. | Applications of lecithin in emulsion stabilization and advanced delivery systems in cosmetics: A mini-review | |
| KR102569192B1 (ko) | 장쇄 세라마이드가 포함된 지질 나노입자 및 이를 포함하는 세포 성장용 조성물 | |
| Panda et al. | Nanocochleates: A novel lipid-based nanocarrier system for drug delivery | |
| CN106361702B (zh) | 一种硫酸或盐酸黄连素多囊脂质体及其制备方法 | |
| Chen et al. | Preparation of triptolide ethosomes | |
| CN101829057B (zh) | 水杨酸脂质体和其系列外用制剂的制备方法及在痤疮治疗中应用 | |
| CN114224841B (zh) | 一种wgx-50脂质体、制备方法及应用 | |
| CN101816632A (zh) | 一种复合功能脂质体及其制备方法和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20160323 |