RU2201980C2 - Method of extraction of noble metals from solutions of their salts (versions) - Google Patents
Method of extraction of noble metals from solutions of their salts (versions) Download PDFInfo
- Publication number
- RU2201980C2 RU2201980C2 RU2000126217/02A RU2000126217A RU2201980C2 RU 2201980 C2 RU2201980 C2 RU 2201980C2 RU 2000126217/02 A RU2000126217/02 A RU 2000126217/02A RU 2000126217 A RU2000126217 A RU 2000126217A RU 2201980 C2 RU2201980 C2 RU 2201980C2
- Authority
- RU
- Russia
- Prior art keywords
- solutions
- metals
- sorbent
- processed
- carbon
- Prior art date
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P10/00—Technologies related to metal processing
- Y02P10/20—Recycling
Abstract
Description
Изобретение относится к области гидрометаллургии и очистки сточных вод, а именно к способам извлечения благородных металлов из растворов их солей, и может быть использовано для извлечения тяжелых металлов из растворов. The invention relates to the field of hydrometallurgy and wastewater treatment, and in particular to methods for extracting precious metals from solutions of their salts, and can be used to extract heavy metals from solutions.
Известны способы извлечения благородных металлов из разнообразных по составу растворов с использованием анионообменных смол. Так, по патенту США ( 3473921, МКИ В 01 D 15/04) извлечение благородных металлов из растворов ведут с использованием анионита, включающего хлорметилированный сополимер стиролдидивинилбензола, прореагировавший с мочевиной. По патенту Великобритании ( 1452618, МКИ В 01 D 15/04)благородные металлы извлекают из растворов, применяя анионит, содержащий четвертичные аммониевые основания. Known methods for the extraction of precious metals from a variety of solutions using anion-exchange resins. So, according to US patent (3473921, MKI B 01 D 15/04), the extraction of precious metals from solutions is carried out using anion exchange resin, including a chloromethylated styrene-divinylbenzene copolymer, which has reacted with urea. According to UK patent (1452618, MKI B 01 D 15/04), noble metals are recovered from solutions using anion exchange resin containing quaternary ammonium bases.
Недостатком анионитов является пониженная стойкость, невысокий их срок службы при извлечении благородных металлов из растворов, содержащих активный хлор. The disadvantage of anion exchangers is reduced durability, their low life when extracting precious metals from solutions containing active chlorine.
Известны способы извлечения благородных металлов из растворов с использованием угольных сорбентов. Known methods for the extraction of precious metals from solutions using coal sorbents.
Так, известен способ извлечения золота из растворов медно-обогатительных фабрик (Лебедев К.Б., Тавкин Н.И. Извлечение золота из сливов сгустителей. //Цветные металлы. - 1973. - 8. - С. 71). Согласно этому способу в контактный чан, или флотомашину, или в слив сгустителя добавляется активированный уголь в присутствии цианидов с последующим выделением угля. Недостатком способа является повышенный расход угля, достигающий 2,0-2,5 г/л, и потери золота. So, there is a known method for extracting gold from solutions of copper processing plants (Lebedev KB, Tavkin NI. Extraction of gold from plum thickeners. // Non-ferrous metals. - 1973. - 8. - P. 71). According to this method, activated carbon in the presence of cyanides is added to the contact tank, or flotation machine, or to the thickener drain, followed by the release of coal. The disadvantage of this method is the increased consumption of coal, reaching 2.0-2.5 g / l, and the loss of gold.
По другому способу (патент США 2753528 от 03.07.56) извлечение золота из разубоженных сточных вод флотационных фабрик осуществляют в колонне, заполненной углем. Недостатком способа является достаточно большой расход угля. In another method (US Pat. No. 2,753,528 of July 3, 566), gold is extracted from diluted wastewater from flotation plants in a column filled with coal. The disadvantage of this method is a fairly large consumption of coal.
Наиболее близким к заявляемому способу (вариантам) по технической сущности является способ, получивший название гальванокоагуляции, основанный на использовании эффекта гальванического элемента железо (алюминий)-кокс или железо (алюминий)-медь, помещенного в очищаемый раствор, при переменном контакте элементов гальванопары между собой. За счет разности электрохимических потенциалов железо поляризуется анодно и переходит в раствор с последующим выпадением в осадок в виде оксигидратов, на поверхности которых адсорбируются отрицательно заряженные анионы. Кокс или медь в гальванопаре поляризуется катодно, в результате чего осуществляется электроосаждение катионов на катоде (Дзюбинский Ф.А., Феофанов В.А. и др. /Кондиционирование оборотных вод методом гальванокоагуляции. //Цветная металлургия - 1990. - 8. - с.66-68). Таким образом происходит извлечение металлов из растворов. Closest to the claimed method (options) in technical essence is a method called galvanic coagulation, based on the use of the galvanic cell element iron (aluminum) -coke or iron (aluminum) -copper, placed in the solution to be cleaned, with alternating contact between the elements of the galvanic pair . Due to the difference in electrochemical potentials, the iron is polarized anode and goes into solution, followed by precipitation in the form of oxyhydrates, on the surface of which negatively charged anions are adsorbed. Coke or copper in a galvanic couple is polarized cathodically, resulting in the electrodeposition of cations at the cathode (Dzyubinsky F.A., Feofanov V.A. et al. / Conditioning of circulating water by galvanocoagulation. // Non-ferrous metallurgy - 1990. - 8. - p. .66-68). Thus, metals are extracted from solutions.
Недостатком указанного способа является достаточно низкая степень извлечения металлов из раствора, образование значительного количества шламистого осадка, невысокое содержание извлекаемых металлов в осадке и невысокие значения перерабатываемых объемов раствора. The disadvantage of this method is the relatively low degree of extraction of metals from the solution, the formation of a significant amount of sludge sludge, a low content of recoverable metals in the sediment and low values of the processed volumes of the solution.
Изобретение направлено на достижение технического результата - повышение степени извлечения благородных металлов, достижение высоких содержаний извлекаемых элементов в осадке, образующемся при переработке растворов, упрощение схемы выделения элементов, увеличение количества удельных объемов перерабатываемых растворов. The invention is aimed at achieving a technical result - increasing the degree of extraction of precious metals, achieving high contents of recoverable elements in the precipitate formed during the processing of solutions, simplifying the scheme of separation of elements, increasing the number of specific volumes of processed solutions.
Для достижения технического результата в способе извлечения благородных металлов из растворов их солей, включающем взаимодействие перерабатываемых хлоридсодержащих растворов в сорбционной колонне с углеродным сорбентом, насыщение сорбента и его переработку, согласно изобретению для извлечения благородных металлов из растворов перерабатываемые хлорсодержащие растворы предварительно подвергают взаимодействию с загрузкой из термодинамически нестабильных металлов, их сплавов, клинкера цинкового производства и/или соединений термодинамически нестабильных металлов в низшей степени окисления до величины рН, при которых снижается концентрация активного хлора и сохраняется концентрация извлекаемых металлов в перерабатываемом растворе, после чего растворы перерабатывают с использованием углеродного сорбента упорядоченной и/или неупорядоченной структуры. Для достижения технического результата по второму варианту перерабатываемые хлоридсодержащие растворы пропускают через загрузку из углеродного сорбента упорядоченной и/или неупорядоченной структуры в присутствии термодинамически нестабильных металлов, их сплавов и/или клинкера цинкового производства, доменных пылей при постоянном контакте элементов сорбента между собой. To achieve a technical result in a method for the extraction of precious metals from solutions of their salts, including the interaction of processed chloride-containing solutions in a sorption column with a carbon sorbent, saturation of the sorbent and its processing, according to the invention, to process precious metals from solutions, processed chlorine-containing solutions are preliminarily interacted with loading from thermodynamically unstable metals, their alloys, zinc clinker and / or thermo compounds dynamically unstable metals to a low degree of oxidation to a pH at which the concentration of active chlorine decreases and the concentration of recoverable metals in the processed solution is maintained, after which the solutions are processed using a carbon sorbent of an ordered and / or disordered structure. To achieve a technical result according to the second embodiment, the processed chloride-containing solutions are passed through a charged and / or disordered structure from a carbon sorbent in the presence of thermodynamically unstable metals, their alloys and / or zinc production clinker, blast dusts with constant contact between the sorbent elements.
Переработку растворов осуществляют в сорбционных колоннах с зажатым слоем сорбента при направлении растворов снизу вверх. Processing solutions is carried out in sorption columns with a clamped layer of sorbent in the direction of the solutions from the bottom up.
Перерабатываемые растворы дополнительно содержат активные галогены и ионы ртути. Processed solutions additionally contain active halogens and mercury ions.
Загрузку колонны из термодинамически неустойчивых металлов и/или клинкера цинкового производства периодически перемешивают, а образующиеся при этом шламы направляют на извлечение благородных металлов. The column loading from thermodynamically unstable metals and / or zinc clinker is periodically mixed, and the resulting sludge is sent to the recovery of precious metals.
Сорбент в колонне также подвергают периодическому перемешиванию, а образующиеся при этом шламы направляют на извлечение благородных металлов. The sorbent in the column is also subjected to periodic mixing, and the resulting sludge is sent to the extraction of precious metals.
В качестве термодинамически неустойчивых металлов используют алюминий, цинк, железо, марганец, медь и/или сплавы этих металлов. As thermodynamically unstable metals, aluminum, zinc, iron, manganese, copper and / or alloys of these metals are used.
В качестве соединений металлов переменной валентности в низшей степени окисления используют оксиды и/или их соли. As compounds of metals of variable valency in the lowest oxidation state, oxides and / or their salts are used.
В качестве углерода неупорядоченной структуры используют активированный уголь. Activated carbon is used as the carbon of the disordered structure.
В качестве углерода упорядоченной структуры используют природный графит после химического модифицирования и термической обработки. As carbon of an ordered structure, natural graphite is used after chemical modification and heat treatment.
Способ осуществляют следующим образом. The method is as follows.
Независимо от варианта переработку растворов осуществляют в сорбционных колоннах с зажатым слоем сорбента при направлении растворов снизу вверх. Regardless of the option, the processing of solutions is carried out in sorption columns with a clamped layer of sorbent in the direction of the solutions from the bottom up.
Скорость движения растворов регулируют таким образом, чтобы величина Eh на выходе из колонны не превышала значений 700 мв. Это вызвано тем, что при более высоких значениях окислительно-восстановительного потенциала начинается "проскок" золота в маточные растворы, т.е. потеря золота. The speed of movement of the solutions is regulated so that the value of Eh at the outlet of the column does not exceed 700 mV. This is due to the fact that, at higher values of the redox potential, the “slip” of gold into the mother liquors begins, i.e. loss of gold.
Перерабатываемые растворы дополнительно содержат активные галогены и ионы ртути. Processed solutions additionally contain active halogens and mercury ions.
По первому варианту перерабатываемые растворы предварительно направляют в сорбционную колонну, заполненную термодинамически нестабильными металлами, выбираемыми из ряда: Al, Zn, Fe, Cu, Mn, их сплавами, клинкером цинкового производства, и/или дозируют в растворы соединения металлов переменной валентности в низшей степени окисления. В качестве таких соединений используют оксиды и растворы солей Fe2+, Sn2+, Cu+.According to the first embodiment, the processed solutions are preliminarily sent to a sorption column filled with thermodynamically unstable metals selected from the series: Al, Zn, Fe, Cu, Mn, their alloys, zinc clinker, and / or to a lower degree are metered into solutions of metal compounds of variable valence oxidation. Oxides and solutions of salts of Fe 2+ , Sn 2+ , Cu + are used as such compounds.
Количество металла в колонне и вводимые в раствор соединения Fe2+, Sn+ или Cu+, а также объем перерабатываемого раствора выбирают из условия сохранения таких минимальных значений рН и Eh перед контактом с углеродным сорбентом, при которых извлекаемые металлы еще удерживаются в растворенном состоянии. Минимальное значение окислительно-восстановительного потенциала и величину рН, при которых извлекаемые металлы еще удерживаются в растворенном состоянии, устанавливают опытным путем в зависимости от используемой загрузки колонны для предварительной дезактивации активного хлора и концентрации хлор-иона и золота в перерабатываемых растворах.The amount of metal in the column and the compounds Fe 2+ , Sn + or Cu + introduced into the solution, as well as the volume of the solution to be treated, are selected from the condition that the minimum pH and Eh values are maintained before contact with the carbon sorbent at which the metals to be recovered are still kept in a dissolved state. The minimum value of the redox potential and the pH value at which the metals to be recovered are still kept in a dissolved state are established empirically, depending on the used column loading for preliminary deactivation of active chlorine and the concentration of chlorine ion and gold in the processed solutions.
На этой стадии происходит дезактивация активного хлора путем контакта продуктивного раствора с термодинамически неустойчивыми металлами, их сплавами и/или соединениями металлов переменной валентности в низшей степени окисления при сохранении концентрации хлор-иона извлекаемых элементов. Благодаря предварительной дезактивации активного хлора значительно повышается емкость используемых на следующей стадии угольных сорбентов, что способствует снижению их удельных норм расхода. At this stage, active chlorine is deactivated by contacting the productive solution with thermodynamically unstable metals, their alloys and / or compounds of metals of variable valency in a low oxidation state while maintaining the concentration of chlorine ion of the recoverable elements. Due to the preliminary deactivation of active chlorine, the capacity of the coal sorbents used in the next stage is significantly increased, which helps to reduce their specific consumption rates.
Содержимое колонны, состоящее из термодинамически неустойчивых металлов, и/или их сплавов, и/или клинкера цинкового производства, периодически перемешивают для очистки от образующихся на ее поверхности продуктов окисления, которые удаляют в отдельную емкость. Собранные продукты окисления отделяют от раствора и направляют совместно с насыщенным угольным сорбентом на переработку. Частоту перемешивания загрузки устанавливают опытным путем. The contents of the column, consisting of thermodynamically unstable metals, and / or their alloys, and / or zinc clinker, are periodically mixed to remove oxidation products formed on its surface, which are removed in a separate container. The collected oxidation products are separated from the solution and sent together with the saturated carbon sorbent for processing. The mixing frequency of the load is established empirically.
Затем перерабатываемые растворы поступают во вторую колонну, где они взаимодействуют с углеродным сорбентом упорядоченной или неупорядоченной структуры, в качестве которого используют активированный уголь или природный графит после его химической и термической обработки. Then the processed solutions enter the second column, where they interact with a carbon sorbent of an ordered or disordered structure, which uses activated carbon or natural graphite after its chemical and thermal treatment.
По второму варианту способа перерабатываемые растворы пропускают через углеродный сорбент упорядоченной и/или неупорядоченной структуры в присутствии термодинамически нестабильных металлов, их сплавов, и/или клинкера цинкового производства, и/или доменных пылей при постоянном контакте элементов сорбента между собой. According to the second variant of the method, the processed solutions are passed through a carbon sorbent of an ordered and / or disordered structure in the presence of thermodynamically unstable metals, their alloys, and / or zinc clinker, and / or blast furnace dusts with constant contact between the sorbent elements.
Содержимое колонны периодически перемешивают, а образующиеся при этом шламы совместно с насыщенным углеродным сорбентом направляют на переработку. The contents of the column are periodically mixed, and the resulting sludge together with a saturated carbon sorbent is sent for processing.
Независимо от варианта способа в качестве термодинамически неустойчивых металлов используют алюминий, цинк, железо, марганец, медь, и/или сплавы этих металлов, и/или клинкер цинкового производства; в качестве соединений металлов переменной валентности в низшей степени окисления используют оксиды и/или их соли; в качестве углерода неупорядоченной структуры используют активированный уголь, а в качестве углерода упорядоченной структуры используют природный графит после химического модифицирования и термической обработки. Regardless of the method variant, aluminum, zinc, iron, manganese, copper, and / or alloys of these metals, and / or zinc clinker are used as thermodynamically unstable metals; oxides and / or their salts are used as compounds of metals of variable valence in the lowest oxidation state; activated carbon is used as the carbon of the disordered structure, and natural graphite after chemical modification and heat treatment is used as the carbon of the ordered structure.
При достижении Eh перерабатываемых растворов более 700 мв на выходе из сорбционной колонны (по первому варианту способа) прекращают подачу перерабатываемых растворов в колонну, выгружают сорбент и направляют его на извлечение благородных металлов и ртути; по второму варианту прекращают подачу перерабатываемых растворов, интенсивно перемешивают сорбент в колонне для очистки от образующихся на его поверхности продуктов окисления, которые удаляют в отдельную емкость. Собранные продукты окисления отделяют от раствора и направляют на извлечение благородных металлов и ртути. По мере уменьшения количества термодинамически неустойчивых металлов по первому варианту и сорбента - по второму варианту их объемы восполняют. When Eh of the processed solutions reaches more than 700 mV at the outlet of the sorption column (according to the first variant of the method), the feed of the processed solutions to the column is stopped, the sorbent is discharged and sent to extract noble metals and mercury; according to the second option, the flow of the processed solutions is stopped, the sorbent is intensively mixed in the column to clean the oxidation products formed on its surface, which are removed in a separate container. The collected oxidation products are separated from the solution and sent to the recovery of noble metals and mercury. As the number of thermodynamically unstable metals decreases according to the first embodiment and the sorbent - according to the second embodiment, their volumes are replenished.
Степень извлечения золота по обоим вариантам предлагаемого способа составляет 95-98%, а платины и ртути 70-75%. В случае необходимости более полного улавливания платины и ртути растворы направляют во вторую сорбционную колонну. Степень их извлечения при этом возрастает до 92-95%. The degree of gold recovery for both variants of the proposed method is 95-98%, and platinum and mercury 70-75%. If necessary, more complete capture of platinum and mercury, the solutions are sent to the second sorption column. The degree of their extraction in this case increases to 92-95%.
Механизм извлечения золота и платины заключается в том, что при взаимодействии перерабатываемых растворов со смесью сорбента и термодинамически неустойчивого металла, и/или его сплава, и/или клинкера цинкового производства образуется короткозамкнутая гальваническая пара, в которой металл является анодом, а углеродный сорбент - катодом. В результате протекания электрохимических реакций происходит анодное растворение металла, выделение водорода, восстановление ионов извлекаемых металлов на катоде, изменение Eh и рН среды. Одновременно с этим образуются оксигидраты различного состава, с которыми дополнительно соосаждаются извлекаемые металлы. The mechanism for extracting gold and platinum is that during the interaction of the processed solutions with a mixture of a sorbent and a thermodynamically unstable metal, and / or its alloy, and / or zinc clinker, a short-circuited galvanic pair is formed in which the metal is the anode and the carbon sorbent is the cathode . As a result of the occurrence of electrochemical reactions, anodic dissolution of the metal occurs, hydrogen evolution, reduction of extracted metal ions at the cathode, change in Eh and pH of the medium. At the same time, oxyhydrates of various compositions are formed, with which the extracted metals are additionally precipitated.
Примеры осуществления способа. Examples of the method.
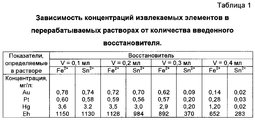
Сначала определяли возможность использования растворов солей металлов переменной валентности в низшей степени окисления для снижения содержания активного хлора в перерабатываемом растворе при сохранении концентраций благородных металлов. В раствор состава, мг/л: Аu - 0,8; Pt - 0,6; Нg - 3,6; активный хлор - 80,0; рН 2,5; Eh - 1180 мв объемом по 100 мл каждый вводили соответственно различные объемы хлоридов Fe2+, Sn2+ с концентрацией 200 г/л каждый. Растворы перемешивали и фильтровали. В фильтрате определяли содержание извлекаемых металлов и величину Eh.First, the possibility of using solutions of metal salts of variable valence in the lowest oxidation state was determined to reduce the active chlorine content in the processed solution while maintaining the concentrations of noble metals. In a solution of the composition, mg / l: Au - 0.8; Pt 0.6; Hg 3.6; active chlorine - 80.0; pH 2.5; Eh - 1180 mV in a volume of 100 ml each, respectively, different volumes of Fe 2+ , Sn 2+ chlorides were introduced with a concentration of 200 g / l each. The solutions were stirred and filtered. The content of recoverable metals and the value of Eh were determined in the filtrate.
Результаты определений представлены в таблице 1. The results of the determinations are presented in table 1.
Как видно из данных таблицы 1, введением достаточного количества солей Fe2+ или Sn2+ можно уменьшить величину Eh перерабатываемого раствора при практическом сохранении исходных концентраций извлекаемых металлов, что позволяет увеличить срок службы углеродного сорбента и его сорбционную емкость. Увеличение объема вводимых растворов Fe2+ или Sn2+ приводит к полной нейтрализации активного хлора и образованию элементных микрочастиц Аu, Pt, Нg, трудно удерживаемых угольным сорбентом на последующем этапе переработки продуктивных растворов, что способствует потере извлекаемых металлов на сорбционном переделе.As can be seen from the data in Table 1, by introducing a sufficient amount of Fe 2+ or Sn 2+ salts, the Eh value of the processed solution can be reduced while the initial concentrations of the extracted metals are practically retained, which can increase the service life of the carbon sorbent and its sorption capacity. An increase in the volume of injected Fe 2+ or Sn 2+ solutions leads to the complete neutralization of active chlorine and the formation of Au, Pt, Hg elemental microparticles, which are difficult to hold with a carbon sorbent at the subsequent stage of processing of productive solutions, which contributes to the loss of recoverable metals at the sorption stage.
Затем определяли интервал значений рН и Eh, при которых извлекаемые металлы еще удерживаются в растворенном состоянии после взаимодействия с термодинамически нестабильными металлами. Раствор состава, мг/л: Аu - 0,8; Pt - 0,6; Нg - 3,6; активный хлор 80,0; рН 2,5; Eh - 1180 мв обрабатывали твердым гидроксидом натрия до задаваемых опытом значений рН и пропускали через колонки, заполненные стружкой этих металлов, в оптимальном интервале скоростей 2-4 объема раствора на объем стружки в час. Then, the range of pH and Eh values was determined at which the extracted metals are still kept in a dissolved state after interaction with thermodynamically unstable metals. The solution of the composition, mg / l: Au - 0.8; Pt 0.6; Hg 3.6; active chlorine 80.0; pH 2.5; Eh - 1180 mV was treated with solid sodium hydroxide to pH values determined by experiment and passed through columns filled with chips of these metals in the optimal range of speeds of 2-4 solution volumes per chip volume per hour.
Растворы на выходе из трубки анализировали. Результаты определений представлены в таблице 2. Solutions at the outlet of the tube were analyzed. The determination results are presented in table 2.
Из таблицы видно, что при рН≤4,5 содержание извлекаемых элементов в растворах после взаимодействия с термодинамически нестабильными металлами меняется незначительно при существенном уменьшении величины Eh. The table shows that at pH≤4.5, the content of recoverable elements in solutions after interaction with thermodynamically unstable metals varies slightly with a significant decrease in Eh.
Дальнейшее увеличение значений рН в поступающем на переработку растворе способствует гидролизу солей алюминия и железа и образованию соответствующих осадков гидроксидов и оксигидратов переменного состава, с которыми частично соосаждается золото, платина и ртуть, что в последующем приводит к забиванию угольного сорбента, снижению производительности колонн и возможному выносу шламов из установки, что связано с потерей благородных металлов
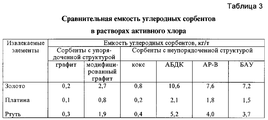
Для выбора углеродсодержащей пары, короткозамкнутого гальванического элемента углерод-металл, наиболее подходящей для извлечения благородных металлов и ртути из раствора, навески углеродсодержащих материалов упорядоченной и неупорядоченной структуры весом 1 г каждая помещали в модельный раствор состава, мг/л: хлор-ион - 600; активный хлор - 65; Au - 2,6; Pt - 0,8; Нg - 8,0 при рН 2,5, Eh - 1175 мв и перемешивали в течение 24 часов. В качестве углеродсодержащих материалов испытывали кокс, природный графит, активированные угли марок АБДК, АР-В, БАУ и модифицированный графит после химической и термической обработок. По окончании опыта растворы отфильтровывали, сорбенты промывали подкисленной водой и определяли их емкость по Au, Pt, Нg. Результаты определений приведены в таблице 3.A further increase in the pH in the solution fed to the processing contributes to the hydrolysis of aluminum and iron salts and the formation of corresponding precipitates of hydroxides and oxyhydrates of variable composition, with which gold, platinum and mercury are partially precipitated, which subsequently leads to clogging of the carbon sorbent, lower column productivity and possible removal sludge from the plant, which is associated with the loss of precious metals
To select a carbon-containing pair, a carbon-metal short-circuited galvanic cell, most suitable for extracting noble metals and mercury from a solution, weighed samples of carbon-containing materials of ordered and disordered structure weighing 1 g each were placed in a model solution, mg / l: chlorine-ion - 600; active chlorine - 65; Au - 2.6; Pt 0.8; Hg - 8.0 at pH 2.5, Eh - 1175 mV and was stirred for 24 hours. Coke, natural graphite, activated carbons of the ABDK, AR-V, BAU grades and modified graphite after chemical and thermal treatments were tested as carbon-containing materials. At the end of the experiment, the solutions were filtered, the sorbents were washed with acidified water, and their capacity was determined by Au, Pt, and Hg. The determination results are shown in table 3.
Как видно из таблицы 3, сорбенты с неупорядоченной структурой обладают повышенной емкостью по сравнению с сорбентами упорядоченной структуры и по возрастанию сорбционной емкости к извлекаемым металлам их можно расположить в ряд: кокс, БАУ, АР-В, АБДК. Графит обладает наименьшей емкостью, однако после модифицирования его емкостные характеристики возрастают и его можно использовать для извлечения указанных металлов. Таким образом, наилучшим из испытанных сорбентов с неупорядоченной структурой является активированный уголь АБДК, а из сорбентов с кристаллической структурой - модифицированный сорбент. As can be seen from table 3, sorbents with a disordered structure have an increased capacity compared with sorbents of an ordered structure and in increasing sorption capacity to recoverable metals, they can be arranged in a row: coke, BAU, AR-V, ABDC. Graphite has the smallest capacity, but after modification, its capacitive characteristics increase and it can be used to extract these metals. Thus, the best of the tested sorbents with a disordered structure is activated carbon ABDK, and of the sorbents with a crystalline structure, a modified sorbent.
Использование того или иного сорбента в производственных условиях будет определяться экономической целесообразностью, доступностью и экологическими соображениями. The use of a sorbent in a production environment will be determined by economic feasibility, accessibility and environmental considerations.
Для выбора материала анода короткозамкнутого гальванического элемента, используемого в предлагаемом способе, навески сорбентов весом 3 г каждая, взятых в соотношении их элементов металл : углерод = 2:1, контактировали с раствором состава, мг/л: хлор-ион - 600, активный хлор - 65, Au - 2,6, Pt - 0,8; Нg - 8,0 при рН 2,5; Eh - 1175 мв до полного их насыщения по золоту. To select the anode material of the short-circuited galvanic cell used in the proposed method, weighed samples of sorbents weighing 3 g each, taken in the ratio of their elements metal: carbon = 2: 1, were in contact with a solution of the composition, mg / l: chlorine-ion - 600, active chlorine - 65, Au - 2.6, Pt - 0.8; Hg - 8.0 at pH 2.5; Eh - 1175 mV until they are completely saturated with gold.
По окончании опыта сорбенты промывали водой и анализировали на содержание Au, Pt, Нg. В качестве анода использовали стружку термодинамически неустойчивых металлов, их сплавов, а также клинкер цинкового производства. В качестве сплавов использовали: ферромарганец состава, %: Мu - 70, с-b - 7, Fe - 21-22; деформируемый алюминиевый сплав, содержащий в качестве добавок Сu, Мn, Si, клинкер состава, %: Fe - 35,2; коксик - 18,8; Сu - 3,9; Zn - 0,9; г/т: Au - 6,6; Аg - 353,0; Zn - 60,2. At the end of the experiment, the sorbents were washed with water and analyzed for the content of Au, Pt, and Hg. Chips of thermodynamically unstable metals and their alloys, as well as zinc clinker, were used as an anode. As alloys used: ferromanganese composition,%: Mu - 70, c-b - 7, Fe - 21-22; wrought aluminum alloy containing, as additives, Cu, Mn, Si, clinker composition,%: Fe - 35.2; coke - 18.8; Cu - 3.9; Zn - 0.9; g / t: Au - 6.6; Ag - 353.0; Zn - 60.2.
В аналогичных условиях проводили определение емкости сорбентов по способу-прототипу. Результаты определений представлены в табл. 4. In similar conditions, the sorbent capacity was determined by the prototype method. The results of the determinations are presented in table. 4.
Как видно из данных таблицы 4, емкость сорбентов по предлагаемому способу во всех случаях выше, чем по способу-прототипу, причем в случае использования сплавов емкость образуемого сорбента несколько выше, чем емкость сорбента при использовании чистых металлов. Наибольшей емкостью по анализируемым металлам обладает сорбент на базе клинкера цинкового производства и активированного угля. Аналогичные зависимости были получены и при использовании в качестве анода меди. As can be seen from the data of table 4, the capacity of the sorbents according to the proposed method is in all cases higher than by the prototype method, and in the case of using alloys, the capacity of the formed sorbent is slightly higher than the capacity of the sorbent when using pure metals. The sorbent based on zinc clinker and activated carbon has the largest capacity for the metals being analyzed. Similar dependences were obtained when using copper as an anode.
Предлагаемый способ извлечения благородных металлов из раствора был испытан в производственных условиях. The proposed method for the extraction of precious metals from solution was tested under production conditions.
По первому варианту способ осуществляли следующим образом. Перерабатываемый раствор состава, мг/л: Сl- - 4000; активный хлор - 80; Au - 1,2; Pt - 0,3; Нg - 4,0; pН 2,5; Eh - 1180 мв последовательно пропускали через колонну, заполненную одним из термодинамически неустойчивых металлов и/или его сплавом, а затем через колонну с активированным углем или модифицированным графитом. Процесс прекращали при появлении "проскока" по золоту. Сорбент извлекали, промывали, анализировали на содержание Au, Pt, Нg. Параллельно проводили определение емкости сорбента по способу-прототипу. Результаты определений представлены в таблице 5.According to the first embodiment, the method was carried out as follows. The processed solution of composition, mg / l: Сl - - 4000; active chlorine - 80; Au - 1.2; Pt 0.3; Hg - 4.0; pH 2.5; Eh - 1180 mV was successively passed through a column filled with one of thermodynamically unstable metals and / or its alloy, and then through a column with activated carbon or modified graphite. The process was stopped when a jump in gold appeared. The sorbent was removed, washed, and analyzed for Au, Pt, and Hg content. In parallel, the sorbent capacity was determined by the prototype method. The determination results are presented in table 5.
Как видно из данных таблицы 5, предварительная дезактивация активного хлора путем взаимодействия перерабатываемого раствора с термодинамически нестабильными металлами и/или их сплавами при сохранении концентрации извлекаемых элементов и последующем пропускании его через угольный сорбент значительно повышает емкость используемых сорбентов, что способствует снижению их удельных норм расхода. As can be seen from the data in Table 5, the preliminary deactivation of active chlorine by reacting the processed solution with thermodynamically unstable metals and / or their alloys while maintaining the concentration of recoverable elements and then passing it through a carbon sorbent significantly increases the capacity of the sorbents used, which helps to reduce their specific consumption rates.
По второму варианту способ осуществляли следующим образом. According to the second embodiment, the method was carried out as follows.
Перерабатываемый раствор состава, мг/л: Сl- - 4000, активный хлор - 80; Au - 1,2; Pt - 0,3; Нg - 4,0; pН 2,5; Eh - 1180 мв пропускали через углеродный сорбент, в качестве которого использовали активированный уголь и модифицированный графит, в присутствии термодинамически нестабильных металлов, а именно клинкера цинкового производства. Элементы сорбента находились в постоянном контакте между собой. Причем соотношения металл : углеродный сорбент (М:У) были следующие:
М:У=0,25; 0,5; 2,0; 4,0; 5,0.The processed solution of the composition, mg / l: Сl - - 4000, active chlorine - 80; Au - 1.2; Pt 0.3; Hg - 4.0; pH 2.5; Eh - 1180 mV was passed through a carbon sorbent, which used activated carbon and modified graphite, in the presence of thermodynamically unstable metals, namely zinc clinker. The sorbent elements were in constant contact with each other. Moreover, the ratio of metal: carbon sorbent (M: U) were as follows:
M: Y = 0.25; 0.5; 2.0; 4.0; 5.0.
Параллельно проводили испытания по способу-прототипу с использованием в качестве сорбента пар: кокс-железо и графит-железо. Испытание прекращали при появлении "проскока" по золоту. Результаты определений представлены в таблице 6 и на чертеже. Как видно из данных табл. 6 и чертежа, увеличение отношения М: У от 0,25 до 0,5 сопровождается резким увеличением удельного объема переработанных растворов. Дальнейшее его увеличение до 2,0 характеризуется плавным и незначительным возрастанием переработанного удельного объема растворов, а после 2,0 имеет тенденцию к снижению, более резкую в интервале 4,0-5,0. In parallel, tests were carried out according to the prototype method using pairs: coke-iron and graphite-iron as sorbent. The test was terminated when a "slip" in gold. The determination results are presented in table 6 and in the drawing. As can be seen from the data table. 6 and the drawing, an increase in the ratio M: Y from 0.25 to 0.5 is accompanied by a sharp increase in the specific volume of the processed solutions. Its further increase to 2.0 is characterized by a smooth and insignificant increase in the processed specific volume of solutions, and after 2.0 it tends to decrease, more sharply in the range of 4.0-5.0.
Аналогичная зависимость наблюдается и по способу-прототипу. Таким образом, предпочтительным интервалом значений М:У является интервал 0,5 - 4,0, причем выбор того или иного значения определяется составом перерабатываемого раствора и его показателями рН и Eh. A similar dependence is observed by the prototype method. Thus, the preferred range of values of M: Y is the interval 0.5 to 4.0, and the choice of a particular value is determined by the composition of the processed solution and its pH and Eh.
Таким образом, приведенные примеры показывают возможность осуществления предложенного способа извлечения благородных металлов из содержащих активный хлор и ионы ртути растворов и его несомненные преимущества по сравнению со способом-прототипом. Thus, the above examples show the possibility of implementing the proposed method for the extraction of precious metals from solutions containing active chlorine and mercury ions and its undoubted advantages in comparison with the prototype method.
То есть предложенный способ позволяет извлекать благородные металлы из растворов их солей, в том числе из растворов, содержащих активный хлор и ионы ртути. That is, the proposed method allows you to extract precious metals from solutions of their salts, including solutions containing active chlorine and mercury ions.
Claims (16)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2000126217/02A RU2201980C2 (en) | 2000-10-18 | 2000-10-18 | Method of extraction of noble metals from solutions of their salts (versions) |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2000126217/02A RU2201980C2 (en) | 2000-10-18 | 2000-10-18 | Method of extraction of noble metals from solutions of their salts (versions) |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2000126217A RU2000126217A (en) | 2002-09-27 |
| RU2201980C2 true RU2201980C2 (en) | 2003-04-10 |
Family
ID=20241157
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2000126217/02A RU2201980C2 (en) | 2000-10-18 | 2000-10-18 | Method of extraction of noble metals from solutions of their salts (versions) |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2201980C2 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2502568C2 (en) * | 2012-02-20 | 2013-12-27 | Открытое акционерное общество "Территориальная генерирующая компания № 11" | Complex processing of coal combustion flue ash |
| RU2568539C2 (en) * | 2014-03-25 | 2015-11-20 | Сергей Николаевич Круглов | Gold extraction from chlorine-bearing solutions |
-
2000
- 2000-10-18 RU RU2000126217/02A patent/RU2201980C2/en active
Non-Patent Citations (1)
| Title |
|---|
| МЕРЕТУКОВ М.А. и др. Металлургия благородных металлов. Зарубежный опыт. - М.: Металлургия, 1991, с.270. * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2502568C2 (en) * | 2012-02-20 | 2013-12-27 | Открытое акционерное общество "Территориальная генерирующая компания № 11" | Complex processing of coal combustion flue ash |
| RU2568539C2 (en) * | 2014-03-25 | 2015-11-20 | Сергей Николаевич Круглов | Gold extraction from chlorine-bearing solutions |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US4167481A (en) | Process for the removal of metals from solution | |
| CN1006722B (en) | Gold recovery process | |
| CA1240521A (en) | Recovery of cyanide from waste waters by an ion exchange process | |
| US6551514B1 (en) | Cyanide detoxification process | |
| US20100258448A1 (en) | Use of a rare earth for the removal of antimony and bismuth | |
| US3766036A (en) | Process for the removal of ionic metallic impurities from water | |
| CN103781923A (en) | Process for purifying zinc oxide | |
| CN110564977A (en) | Method for recovering nickel resource from chemical nickel waste liquid | |
| US5534234A (en) | Recovery of manganese from leach solutions | |
| JP5403224B2 (en) | How to recover bismuth | |
| US4250030A (en) | Process for the removal of cyanides from effluent | |
| NZ205153A (en) | Hydrometallurgical process for recovery of gold or silver from ores | |
| RU2201980C2 (en) | Method of extraction of noble metals from solutions of their salts (versions) | |
| JPH07286221A (en) | Method for recovering rhenium from nonferrous metal refining process | |
| EP0134644A1 (en) | Process for the purification of zinc sulphate solutions | |
| CN1805793A (en) | A resin and process for extracting non-ferrous metals | |
| RU2718440C1 (en) | Method of cleaning recirculating zinc solutions of leaching from lignosulphonates | |
| US3699207A (en) | Process for the purification of cadmium solutions | |
| CN1297067A (en) | Method for purifying copper electrolyte by solvent extraction | |
| CN218666204U (en) | System for retrieve gold, silver, copper in follow sulphur concentrate calcine washing waste liquid | |
| RU2410455C1 (en) | Method of extracting stibium from sulphate solutions | |
| CN212403822U (en) | Non ferrous metal waste water treatment device is smelted to wet process | |
| RU2003708C1 (en) | Method for ion-exchange recovery of nonferrous metals from acid media | |
| SU1629336A1 (en) | Method for removing chlorine from zinc sulphate solution | |
| JP2008196039A (en) | Method of removing fluorine from processing liquid used in wet zinc smelting |