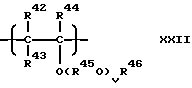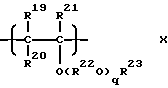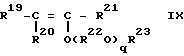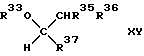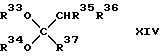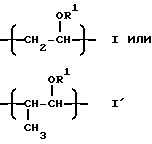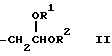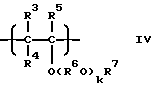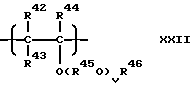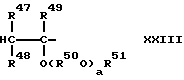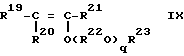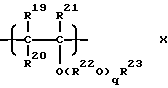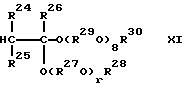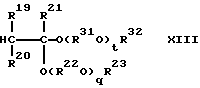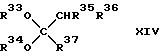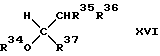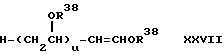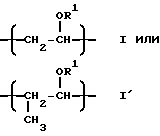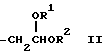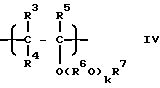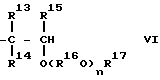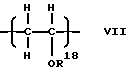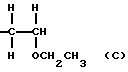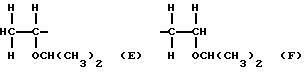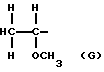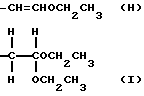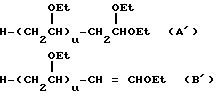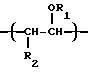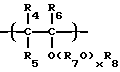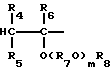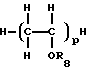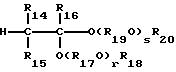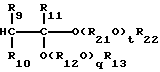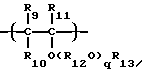RU2139889C1 - Polyvinyl ether (variants), method of preparation thereof and lubricating oil based thereon for rifrigerators - Google Patents
Polyvinyl ether (variants), method of preparation thereof and lubricating oil based thereon for rifrigerators Download PDFInfo
- Publication number
- RU2139889C1 RU2139889C1 RU94046370/04A RU94046370A RU2139889C1 RU 2139889 C1 RU2139889 C1 RU 2139889C1 RU 94046370/04 A RU94046370/04 A RU 94046370/04A RU 94046370 A RU94046370 A RU 94046370A RU 2139889 C1 RU2139889 C1 RU 2139889C1
- Authority
- RU
- Russia
- Prior art keywords
- general formula
- reaction
- same
- pressure
- hydrocarbon group
- Prior art date
Links
- SXYFYMNOFLQURS-UHFFFAOYSA-N CCC(CC)C1CCCC1 Chemical compound CCC(CC)C1CCCC1 SXYFYMNOFLQURS-UHFFFAOYSA-N 0.000 description 1
Images
Abstract
Description
Настоящее изобретение относится к новому смазочному маслу для холодильников компрессионного типа, новому способу получения простых поливиниловых эфиров и простых эфиров и новому простому поливиниловому эфиру. В частности, настоящее изобретение касается (I) смазочного масла для компрессионных холодильников, которое содержит в качестве основного компонента простой поливиниловый эфир, имеющий отличную совместимость с водородсодержащими флонами (фреонами ["флон" означает в общем хлорфторуглерод (CFC), гидрофторуглерод (HFC) и гидрофторуглерод (HCFC)], такими, как 1,1,1,2-тетрафторэтан (называемый далее как флон-134а) и т.п., которые могут быть использованы в качестве хладагента, вместо соединений, вызывающих загрязнение окружающей среды, таких, как дихлорфторэтан (называемый далее как флон-12) и т. п. и имеющий отличные смазочные свойства, (2) способа эффективного и промышленно выгодного получения простого поливинилового эфира, имеющего широкий диапазон применения в качестве растворителя, смазочного масла, клея, смолы и т. п. (3) способа эффективного и промышленно выгодного получения полезного простого эфира, имеющего широкий диапазон применения в качестве растворителя, смазочного масла и т.п., путем гидрирования ацеталя или кеталя, и (4) нового простого поливинилового эфира, пригодного для использования в качестве смазочного масла для компрессионных холодильников, электроизоляционного (трансформаторного) масла, органического растворителя, поверхностно-активного вещества и т.п. The present invention relates to a new lubricating oil for compression-type refrigerators, a new method for producing polyvinyl ethers and ethers, and a new polyvinyl ether. In particular, the present invention relates to (I) a lubricating oil for compression refrigerators, which comprises as its main component polyvinyl ether having excellent compatibility with hydrogen-containing flons (freons ["flon" means generally chlorofluorocarbon (CFC), hydrofluorocarbon (HFC) and hydrofluorocarbon (HCFC)], such as 1,1,1,2-tetrafluoroethane (hereinafter referred to as flon-134a) and the like, which can be used as a refrigerant, instead of compounds that cause environmental pollution, such like dichlorofluoride tan (hereinafter referred to as flon-12), etc., and having excellent lubricating properties, (2) a method for efficiently and industrially producing polyvinyl ether, having a wide range of applications as a solvent, lubricating oil, glue, resin, etc. p. (3) a method for efficient and industrially profitable production of a useful ether having a wide range of applications as a solvent, lubricating oil, etc., by hydrogenation of acetal or ketal, and (4) a new polyvinyl ether suitable for use as a lubricating oil for compression refrigerators, electrical insulating (transformer) oil, organic solvent, surfactant, etc.
Холодильники компрессионного типа обычно состоят из компрессора, конденсатора, регулирующего (дроссельного) вентиля и испарителя и имеют конструкцию, при которой смесь хладагента и смазочного масла циркулирует в замкнутой системе. В зависимости от типа оборудования в холодильнике компрессионного типа обычно температура высокая в компрессоре и низкая в холодильной камере, причем обычно необходимо, чтобы хладагент и смазочное масло циркулировали в системе разделения на фазы в широком диапазоне температур. Если в процессе работы холодильника происходит разделение фаз, это оказывает существенное вредное влияние на срок службы и производительность аппарата. Например, когда фазовое разделение хладагента и смазочного масла происходит на участке компрессора, то ухудшается смазка движущихся частей и образуются задиры, что значительно уменьшает срок службы аппарата. Когда фазовое разделение происходит в испарителе, то снижается эффективность теплообмена из-за присутствия смазочного масла высокой вязкости. Compression-type refrigerators typically consist of a compressor, condenser, control (throttle) valve and evaporator and are designed in which a mixture of refrigerant and lubricating oil circulates in a closed system. Depending on the type of equipment in a compression type refrigerator, the temperature is usually high in the compressor and low in the refrigerator, and it is usually necessary that the refrigerant and lubricating oil circulate in the phase separation system over a wide temperature range. If phase separation occurs during the operation of the refrigerator, this has a significant detrimental effect on the service life and performance of the device. For example, when the phase separation of the refrigerant and the lubricating oil occurs in the compressor area, the lubrication of the moving parts deteriorates and scoring forms, which significantly reduces the service life of the apparatus. When phase separation occurs in the evaporator, the heat transfer efficiency is reduced due to the presence of high viscosity lubricating oil.
Поскольку смазочное масло для холодильника используют с целью смазки движущихся частей в холодильниках, то естественно важны его смазочные свойства. В частности, поскольку температура в компрессоре высока, важное значение имеет вязкость, обеспечивающая удерживание масляной пленки, необходимой для смазки. Требуемая вязкость различна в зависимости от типа используемого компрессора и рабочих условий, и обычно является предпочтительным, чтобы вязкость (кинематическая вязкость) смазочного масла перед смешиванием с хладагентом составляла 5-1000 сс при 40oC. При вязкости более низкой, чем в указанном диапазоне, масляная пленка становится тонкой, что приводит к недостаточному смазыванию, а когда вязкость выше, чем в указанном диапазоне, то снижается эффективность теплообмена.Since lubricating oil for a refrigerator is used to lubricate moving parts in refrigerators, its lubricating properties are naturally important. In particular, since the temperature in the compressor is high, viscosity is important to maintain the oil film required for lubrication. The required viscosity varies depending on the type of compressor used and the operating conditions, and it is usually preferred that the viscosity (kinematic viscosity) of the lubricating oil before mixing with the refrigerant is 5-1000 cc at 40 ° C. With a viscosity lower than the specified range, the oil film becomes thin, which leads to insufficient lubrication, and when the viscosity is higher than in the specified range, the heat transfer efficiency decreases.
Электрические холодильники имеют электродвигатель и компрессор, заключенные в один корпус, и потому необходимо, чтобы смазочное масло для их смазки обладало высокой элекроизоляционной способностью. Обычно необходимо объемное собственное сопротивление 1012 Ом•см или более при 80oC. Если сопротивление ниже указанного значения, то повышается возможность утечки электричества.Electric refrigerators have an electric motor and compressor, enclosed in one case, and therefore it is necessary that the lubricating oil for their lubrication has a high electrical insulating ability. Typically, a volumetric intrinsic resistance of 10 12 Ω • cm or more is required at 80 ° C. If the resistance is lower than the indicated value, the possibility of electric leakage is increased.
В качестве хладагента для холодильников компрессионного типа до сих пор использовали в основном флон-12, а в качестве смазочного масла - различные сорта минеральных и синтетических масел, удовлетворяющих указанным выше требованиям. Однако хлорфторуглероды (CFC), включающие флон-12, имеют более строго ограниченное применение во всем мире, потому что они вносят в окружающую среду загрязнение, приводящее к разрушению озонового слоя. По этой причине привлекают внимание как новые виды хладагента водородсодержащие флоны, такие, как, гидрофторуглероды (HFC), и гидрохлорфторуглероды (HCFC). В качестве хладагента для холодильников компрессионного типа предпочтительными являются водородсодержащие фторуглероды, в частности гидрофторуглероды (HFC) типа флон-134a, потому что они имеют незначительную возможность разрушения озонового слоя и могут заменять флон-12 с небольшим изменением конструкции используемых до сих пор холодильников. So far, mainly flon-12 has been used as a refrigerant for compression type refrigerators, and various types of mineral and synthetic oils meeting the above requirements have been used as lubricating oil. However, chlorofluorocarbons (CFCs), including flon-12, have a more strictly limited use worldwide because they introduce pollution into the environment, leading to the destruction of the ozone layer. For this reason, hydrogen-containing flons, such as hydrofluorocarbons (HFC) and hydrochlorofluorocarbons (HCFC), are attracting attention as new types of refrigerant. Hydrogen-containing fluorocarbons, in particular hydrofluorocarbons (HFCs) of the flon-134a type, are preferred as refrigerant for compression type refrigerators, because they have little chance of destroying the ozone layer and can replace flon-12 with a slight change in the design of the refrigerators used so far.
Естественно, что при использовании в качестве хладагента для холодильников компрессионного типа описанного выше водородсодержащего флона, такого, как флон-134а, флон-32, флон-125, флон-22 и т.п., вместо флона-12 требуется смазочное масло, имеющее хорошую совместимость с водородсодержащим флоном, таким, как флон-134а, флон-32, флон-125, флон-22 и т.п., и хорошую смазочную способность, удовлетворяющую описанным выше требованиям. Однако, поскольку смазочные масла, используемые до сих пор в сочетании с флоном-12, не имеют хорошей совместимости с водородсодержащим флоном, таким, как флон-134а, флон-32, флон-125 и т.п., то необходимо новое смазочное масло, пригодное для этих соединений. Желательно, чтобы при использовании нового смазочного масла не нужны были большие изменения в конструкции аппарата. Нежелательно, чтобы пришлось производить значительные изменения конструкции ныне существующих аппаратов из-за нового смазочного масла. Naturally, when using the hydrogen-containing flon described above, such as flon-134a, flon-32a, flon-125, flon-22, etc., as a refrigerant for refrigerators of the compression type, instead of flon-12, a lubricant having good compatibility with a hydrogen-containing flon, such as flon-134a, flon-32, flon-125, flon-22, etc., and good lubricity that meets the requirements described above. However, since the lubricating oils used so far in combination with flon-12 do not have good compatibility with a hydrogen-containing flon, such as flon-134a, flon-32, flon-125, etc., a new lubricating oil is necessary suitable for these compounds. It is advisable that when using a new lubricating oil, large changes in the design of the apparatus are not needed. It is undesirable that it was necessary to make significant changes in the design of existing machines due to the new lubricating oil.
Известно использование, например, полиоксиалкиленгликолей в качестве смазочного масла, имеющего совместимость с флоном-134а. Такие смазочные масла раскрыты, например, в отчете о поиске N 17463 (октябрь 1978), описании к патенту США N 4755316, выложенных заявках на патент Японии N 1989 - 256094, N 1989-259093, N 1989-259094, N 1989-271491, N 1990-43290, N 1990-84491, NN 1990-132176-132178, N 1990-132179, N 1990-173195, NN 1990-180986-180987, NN 1990-182780 -182781, N 1990-242888, N 1990-258895, N 1990-269195, N 1990-272097, N 1990-305893, N 1991-28296, N 1991-33193, NN 1991-103496 - 103497, N 1991-50297, N 1991-52995, NN 1991-70794 - 70795, N 1991-79696, N 1991-106992, N 1991-109492, N 1991-121195, N 1991-205492, N 1991-231992, N 1991-231994, 1992-15295, N 1992-39394 и NN 1992-41591 - 41592. Однако смазочные масла из полиоксиалкиленгликолей обычно имеют низкое объемное собственное сопротивление и, кроме того, в указанных выше описаниях не раскрыт ни один пример, удовлетворяющий значению 1012 Ом•см или более при 80oC.It is known to use, for example, polyoxyalkylene glycols as a lubricating oil having compatibility with flon-134a. Such lubricating oils are disclosed, for example, in the search report N 17463 (October 1978), the description of US patent N 4755316, Japanese patent application laid N N 1989 - 256094, N 1989-259093, N 1989-259094, N 1989-271491, N 1990-43290, N 1990-84491, NN 1990-132176-132178, N 1990-132179, N 1990-173195, NN 1990-180986-180987, NN 1990-182780 -182781, N 1990-242888, N 1990-258895 N 1990-269195; N 1990-272097; N 1990-305893; N 1991-28296; N 1991-33193; NN 1991-103496 - 103497; N 1991-50297; N 1991-52995; NN 1991-70794 - 70795; N 1991-79696, N 1991-106992, N 1991-109492, N 1991-121195, N 1991-205492, N 1991-231992, N 1991-231994, 1992-15295, N 1992-39394 and NN 1992-43991 - 41592 However, polyoxyalkylene glycol lubricating oils usually have a low volumetric intrinsic resistance and, in addition to On the other hand, in the above descriptions, not a single example is satisfied that satisfies a value of 10 12 Ohm • cm or more at 80 o C.
Кроме смазочных масел из полиоксиалкиленгликолей в качестве соединений, совместимых с флоном-134а, раскрыты смазочные масла из сложных эфиров в выложенном описании к патенту Великобритании N 2216541, N 6979 (1990), выложенных заявках на патент Японии N 1990-276894, N 1991-128992, N 1991-88892, N 1991-179091, N 1991-252497, N 1991-275799, N 1991-4294, N 1992-20597 и описании к патенту США N 5021179. Однако смазочные масла из сложных эфиров не обладают достаточной совместимостью из-за фазового разделения при высокой вязкости смазочных масел при более низких температурах, даже если они показывают хорошую совместимость при более высоких температурах. In addition to lubricants from polyoxyalkylene glycols as compounds compatible with flon-134a, ester lubricants are disclosed in the laid-out description to UK patent N 2216541, N 6979 (1990), Japanese Patent Application Laid-Open N 1990-276894, N 1991-128992 , N 1991-88892, N 1991-179091, N 1991-252497, N 1991-275799, N 1991-4294, N 1992-20597 and the description of US patent N 5021179. However, lubricating oils from esters do not have sufficient compatibility because for phase separation at high viscosity lubricating oils at lower temperatures, even if they show good with compatibility at higher temperatures.
Таким образом, оказывается, что в настоящее время фактически еще не раскрыто смазочное масло для холодильников компрессионного типа, имеющее отличную совместимость с флоном -134а, превосходные стабильность и смазочные свойства и объемное собственное сопротивление при 80oC, составляющее 1012 Ом•см или более. Создание такой смазки весьма желательно.Thus, it turns out that at present the lubricant oil for compression refrigerators has not yet been disclosed, which has excellent compatibility with the -134a flon, excellent stability and lubricating properties, and a volumetric intrinsic resistance at 80 ° C. of 10 12 Ω · cm or more . The creation of such a lubricant is highly desirable.
Важными соединениями, имеющими широкий диапазон применения в качестве растворителей, смазочных масел, клеящих веществ, смол и т.п., являются простые поливиниловые эфиры, способы получения которых известны как способы полимеризации, радикальной, катионной или радиационной, мономеров, являющихся простым виниловым эфиром ("Gosei Kobunshi III", публикация Asakura Shoten под редакцией Shunsuke Murahashi, Minoru Imotu and Hisashi Jani). Однако эти традиционные способы не всегда удовлетворительны из-за того, что не легко получить соединение, имеющее требуемую степень полимеризации, что процесс сложен, что трудно управлять реакцией, что требуется большое количество растворителя и т.п. Поэтому весьма желательна разработка способа получения простого поливинилового эфира без вышеуказанных проблем. Important compounds having a wide range of applications as solvents, lubricants, adhesives, resins, etc., are polyvinyl ethers, the production methods of which are known as polymerization methods, radical, cationic or radiation, monomers, which are simple vinyl ether ( "Gosei Kobunshi III", publication by Asakura Shoten edited by Shunsuke Murahashi, Minoru Imotu and Hisashi Jani). However, these traditional methods are not always satisfactory due to the fact that it is not easy to obtain a compound having the desired degree of polymerization, that the process is complicated, that it is difficult to control the reaction, that a large amount of solvent, etc. is required. Therefore, it is highly desirable to develop a method for producing a simple polyvinyl ether without the above problems.
Известны ("Sikken Kagaku Koza, т.20, 4-ое издание, публикация Maruzen) способы получения простого эфира, имеющего широкую область применения в качестве растворителя и смазки, из ацеталей или кеталей, такие, например, как способ с использованием кислоты и гидрида щелочного металла, способ с использованием кремниевого реагента и способ с использованием диборана или т.п. Known ("Sikken Kagaku Koza, v.20, 4th edition, Maruzen publication) methods for producing a simple ether, having a wide scope as a solvent and lubricant, from acetals or ketals, such as, for example, the method using acid and hydride alkali metal method using a silicon reagent and a method using diborane or the like
Однако в этих реакциях используют стехиометрические количества очень дорогих материалов, таких как гидрид щелочного металла, диборан и кремниевый реагент, в качестве гидрирующего реагента, и потому указанные способы не являются предпочтительными для промышленного производства. However, stoichiometric amounts of very expensive materials, such as alkali metal hydride, diborane and silicon reagent, are used as hydrogenation reagent in these reactions, and therefore, these methods are not preferred for industrial production.
Известен способ сочетания кислотного катализатора и каталитического гидрирования. W.Z.Howard (I.Org.Chem., т.26, стр. 1026, 1961 г.) описал получение простого эфира путем каталитического гидрокрекинга кеталя с использованием катализатора, в котором родий нанесен на оксид алюминия, в присутствии хлористоводородной кислоты. A known method of combining an acid catalyst and catalytic hydrogenation. W.Z. Howard (I. Org. Chem., Vol. 26, p. 1026, 1961) described the preparation of an ether by catalytic hydrocracking of a ketal using a catalyst in which rhodium is supported on alumina in the presence of hydrochloric acid.
В описании к патенту США N 4088700 представлен способ получения простого эфира путем каталитического гидрокрекинга 1,3-диоксоранов, являющихся циклическими ацеталями, с использованием платинового или родиевого катализатора в присутствии кислоты Льюиса, такой, как трифторид бора, трихлорид алюминия и т. п. Однако, поскольку в этих способах получения используют хлористоводородную кислоту, трифторид бора, трихлорид алюминия или т.п., то возникает проблема коррозии оборудования при использовании обычного его типа, а необходимая в этом случае специальная обработка делает эти способы непривлекательными. U.S. Pat. No. 4,088,700 describes a process for producing an ether by catalytic hydrocracking of 1,3-dioxoranes which are cyclic acetals using a platinum or rhodium catalyst in the presence of a Lewis acid such as boron trifluoride, aluminum trichloride, etc. However, since hydrochloric acid, boron trifluoride, aluminum trichloride or the like are used in these production methods, there is a problem of corrosion of the equipment when using its usual type, and the necessary Social processing makes these methods unattractive.
В выложенных заявках на патент Японии N 1983-4739 и N 1983-177929 предложен осуществляемый без использования кислоты способ получения простого эфира путем гидрокрекинга ацеталей с использованием палладиевого катализатора, нанесенного на уголь. Вызываемой использованием кислоты проблемы коррозии нет, но степень превращения ацеталя как сырьевого материала не является удовлетворительной. Japanese Patent Application Laid-Open N 1983-4739 and N 1983-177929 disclose an acid-free process for producing an ether by hydrocracking acetals using a palladium catalyst supported on coal. There is no corrosion problem caused by the use of acid, but the degree of conversion of acetal as a raw material is not satisfactory.
Таким образом, еще нет способа получения простого эфира из имеющего достаточную реакционную способность ацеталя или кеталя, который бы(способ) обеспечивал хорошую избирательность и не вызывал коррозию оборудования, и потому разработка такого способа весьма желательна. Thus, there is still no way to obtain ether from acetal or ketal having sufficient reactivity, which (method) provides good selectivity and does not cause corrosion of equipment, and therefore the development of such a method is highly desirable.
С другой стороны, для применений в качестве смазочных масел, электроизоляционных масел и растворителей необходима текучесть и потому желателен полимер, имеющий низкую степень полимеризации. Что касается общеизвестных полиалкилвиниловых простых эфиров, то примеры синтеза различных их типов описаны в "Jikhen Kagaku", том 18, "Reaction of organic compounds 11(А)", издание Химического общества Японии (публикация Maruzen). В случае алкилвиниловых эфиров, имеющих низкую молекулярную массу и алкильную группу из 3 или менее углеродных атомов, из вышеупомянутых примеров самая низкая молекулярная масса полимера составляет, например, 2545 для полимера метилвинилового эфира, 4000 для полимера этилвинилового эфира, 4830 для полимера н-пропилвинилового эфира и 4580 для полимера изопропилвинилового эфира. Полимер метилвинилового эфира, имеющий молекулярную массу 3000, описан в Macromolecules, том 17, стр. 2228 (1984), а полимер этилвинилового эфира, имеющий молекулярную массу 2600, описан в Macromolecules, том 18, стр. 2 (1985). Однако указанные значения молекулярной массы предполагают, что эти полимеры имеют очень низкую текучесть и при комнатной температуре представляют собой полутвердые вещества. On the other hand, for applications as lubricating oils, electrical insulating oils and solvents, fluidity is necessary and therefore a polymer having a low degree of polymerization is desirable. As for the well-known polyalkyl vinyl ethers, examples of the synthesis of their various types are described in "Jikhen Kagaku", volume 18, "Reaction of organic compounds 11 (A)", publication of the Chemical Society of Japan (publication Maruzen). In the case of alkyl vinyl ethers having a low molecular weight and an alkyl group of 3 or less carbon atoms, from the above examples, the lowest molecular weight of the polymer is, for example, 2545 for the methyl vinyl ether polymer, 4000 for the ethyl vinyl ether polymer, 4830 for the n-propyl vinyl ether polymer and 4580 for an isopropyl vinyl ether polymer. A polymer of methyl vinyl ether having a molecular weight of 3000 is described in Macromolecules, Volume 17, p. 2228 (1984), and a polymer of ethyl vinyl ether having a molecular weight of 2600 is described in Macromolecules, Volume 18, p. 2 (1985). However, the indicated molecular weight values suggest that these polymers have very low fluidity and are semi-solid at room temperature.
В случае соединений, имеющих алкильную группу с 4 или более атомами углерода, обнаружен пример, в котором выделен димер, и пример, в котором получен полимер, имеющий молекулярную массу 600. На полимеры простых алкилвиниловых эфиров, имеющих алкильную группу с 4 или более атомами углерода, не удовлетворяют необходимым требованиям, потому что они не совместимы с гидрофторуглеродами, такими, как флон-134а. In the case of compounds having an alkyl group with 4 or more carbon atoms, an example is found in which a dimer is isolated and an example in which a polymer having a molecular weight of 600 is obtained. For polymers of vinyl vinyl ethers having an alkyl group with 4 or more carbon atoms , do not meet the necessary requirements, because they are not compatible with hydrofluorocarbons, such as flon-134a.
Как описано выше, полимер простого алкилвинилового эфира и алкильной группой, имеющей 3 или менее атомов углерода, который имеет молекулярную массу 1200 или ниже, еще не известен. As described above, a polymer of an alkyl vinyl ether and an alkyl group having 3 or less carbon atoms, which has a molecular weight of 1200 or lower, is not yet known.
Концевыми группами этих полимеров являются олефины в случае кислотных катализаторов и ацетали, когда присутствует спирт, а в случае присутствия воды образуются также ацетальные и альдегидные концевые группы. Олефин на конце цепи иногда вызывает окрашивание и увеличение вязкости в присутствии кислоты, а альдегидная концевая группа также иногда вызывает окрашивание. Ацетали разлагаются в присутствии кислоты на олефины и спирты. Олефины реагируют друг с другом, вызывая окрашивание и увеличение вязкости, а когда дополнительно присутствует вода, то образуются альдегиды, также иногда вызывающие окрашивание. Но простой поливиниловый эфир, не имеющий структур типа ацеталей, альдегидов и олефинов, вызывающих деструкцию, на концах молекулы и обладающий превосходной стабильностью, до сих пор еще не известен. The end groups of these polymers are olefins in the case of acid catalysts and acetals, when alcohol is present, and in the presence of water, acetal and aldehyde end groups are also formed. Olefin at the end of the chain sometimes causes staining and viscosity increase in the presence of acid, and the aldehyde end group also sometimes causes staining. Acetals decompose in the presence of acid into olefins and alcohols. Olefins react with each other, causing staining and increasing viscosity, and when water is additionally present, aldehydes are formed, which also sometimes cause staining. But polyvinyl ether, which does not have structures such as acetals, aldehydes and olefins that cause degradation at the ends of the molecule and has excellent stability, is still not known.
В описанных выше условиях было разработано настоящее изобретение с целью создания (1) смазочного масла для холодильников компрессионного типа, обладающего отличной совместимостью с водородсодержащими флонами (фреонами), такими, как флон-134а, флон-32, флон-125, и т.п. которые могут заменять хладагент флон-12 и другие флоны, которые сильно разлагаются и, в частности вызывают проблему загрязнения окружающей среды, во всем диапазоне рабочих температур, имеющего превосходные стабильность и смазочные свойства и имеющего объемное собственное электрическое сопротивление 1012 Ом•см или более при 80oC), (2) промышленно выгодного способа получения простого поливинилового эфира, имеющего высокую степень полимеризации, с использованием простого, надежного, безопасного и производительного процесса, (3) способа эффективного получения простого эфира путем гидрирования ацеталя или кеталя с использованием катализатора, имеющего достаточную реакционную активность и превосходную избирательность и не вызывающего коррозии оборудования, и (4) нового поливинилового простого эфира для предпочтительного использования, в частности, в качестве смазочного масла для описанных выше холодильников компрессионного типа.Under the conditions described above, the present invention was developed with the aim of creating (1) a lubricating oil for compression type refrigerators having excellent compatibility with hydrogen-containing flons (freons), such as flon-134a, flon-32, flon-125, etc. . which can replace the flon-12 refrigerant and other flons, which are highly decomposed and, in particular, cause environmental pollution, over the entire operating temperature range, which has excellent stability and lubricating properties and has a volume intrinsic electrical resistance of 10 12 Ohm • cm or more at 80 o C), (2) an industrially advantageous method for producing a simple polyvinyl ether having a high degree of polymerization using a simple, reliable, safe and efficient process, (3) an eff active production of ether by hydrogenation of acetal or ketal using a catalyst having sufficient reactivity and excellent selectivity and non-corrosive equipment, and (4) a new polyvinyl ether for preferred use, in particular, as a lubricating oil for the compression refrigerators described above type.
В результате проведенных данными изобретателями интенсивных исследований с целью достижения описанных выше целей было открыто, (1) что первая из указанных целей может быть достигнута с помощью смазочного масла, содержащего в качестве основного его компонента простой поливиниловый эфир, имеющий специфическую структуру), (2) что вторая цель может быть достигнута путем добавления по каплям представляющего собой простой виниловый эфир мономера к особому инициатору в присутствии катализатора и полимеризации мономера, (3) что третья цель может быть достигнута путем использования твердого катализатора, имеющего кислотные свойства и гидрирующую способность, в качестве упомянутого катализатора и (4) что четвертая цель может быть достигнута с помощью (а) простого поливинилового эфира, который является гомополимером или сополимером простого алкилвинилового эфира, имеющего алкильную группу с 1-3 атомами углерода, имеет среднемассовую молекулярную массу и диапазоне 300-1200 и имеет концевые группы специфической структуры и (о) полимера алкилвинилового простого эфира специфической структуры, который не содержит ни ненасыщенной связи, ни ацетальной и альдегидной структур и имеет среднемассовую молекулярную массу в определенном диапазоне. Настоящее изобретение было сделано на основе вышеупомянутого открытия. As a result of intensive research conducted by these inventors in order to achieve the goals described above, it was discovered (1) that the first of these goals can be achieved with a lubricating oil containing polyvinyl ether having a specific structure as its main component), (2) that the second goal can be achieved by adding dropwise a simple vinyl ether monomer to a particular initiator in the presence of a catalyst and polymerizing the monomer, (3) that the third goal can can be achieved by using a solid catalyst having acidic properties and hydrogenating ability as said catalyst and (4) that the fourth goal can be achieved using (a) a simple polyvinyl ether, which is a homopolymer or copolymer of an alkyl vinyl ether having an alkyl group with 1-3 carbon atoms, has a mass-average molecular weight and a range of 300-1200 and has end groups of a specific structure and (o) a specific vinyl vinyl ether polymer specific uctury, which does not contain either an unsaturated bond or acetal and aldehyde structures and has a mass-average molecular weight in a certain range. The present invention has been made based on the aforementioned discovery.
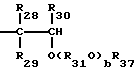
Таким образом, смазочное масло для холодильников компрессионного типа, которое создано в соответствии с первой целью настоящего изобретения, содержит в качестве основного его компонента простой поливиниловый эфир, имеющий составляющие звенья, выраженные общей формулой (XXII):
где R42, R43 и R44 - каждый атом водорода или углеводородная группа, имеющая 1-8 атомов углерода, и могут быть одинаковыми или отличающимися друг от друга, R45 - двухвалентная углеводородная группа, имеющая 2-10 атомов углерода, R46 - углеводородная группа, имеющая 1-10 атомов углерода, V - число, среднее значение которого находится в диапазоне 0-10, и R45 O могут быть одинаковыми или отличающимися друг от друга, когда имеется несколько групп R45O.Thus, the lubricating oil for refrigerators of the compression type, which is created in accordance with the first objective of the present invention, contains as its main component a simple polyvinyl ether having constituent units expressed by the general formula (XXII):
where R 42 , R 43 and R 44 are each hydrogen atom or a hydrocarbon group having 1-8 carbon atoms, and may be the same or different from each other, R 45 is a divalent hydrocarbon group having 2-10 carbon atoms, R 46 a hydrocarbon group having 1-10 carbon atoms, V is a number whose average value is in the range of 0-10, and R 45 O may be the same or different from each other when there are several R 45 O groups.
Способ получения простого поливинилового эфира, содержащего составляющие звенья, выраженные общей формулой (X):
где R19, R20 и R21 - каждый атом водорода или углеводородная группа, имеющая 1-8 атомов углерода, и могут быть одинаковыми или отличающимися друг от друга, R22 - двухвалентная углеводородная группа, имеющая 2-10 атомов углерода, R23 - углеводородная группа, имеющая 1-10 атомов углерода, q - число, среднее значение которого находится в диапазоне 0-10, и R22O могут быть одинаковыми или отличающимися друг от друга, когда имеется несколько групп R22O, который (способ) создан в соответствии со второй целью настоящего изобретения, включает в себя полимеризацию представляющего собой простой виниловый эфир мономера, имеющего общую формулу (IX):
где R19-R23 и q - такие, как указанные ранее, путем использования сочетания кислоты Брэнстеда (апротонной кислоты), кислоты Льюиса или металлоорганического соединения с водой, спиртом, фенолом, ацеталием или аддуктом простого винилового эфира и карбоновой кислоты в качестве инициатора.A method of producing a simple polyvinyl ether containing constituent units expressed by the general formula (X):
where R 19 , R 20 and R 21 are each hydrogen atom or a hydrocarbon group having 1-8 carbon atoms, and may be the same or different from each other, R 22 is a divalent hydrocarbon group having 2-10 carbon atoms, R 23 - a hydrocarbon group having 1-10 carbon atoms, q is a number whose average value is in the range 0-10, and R 22 O can be the same or different from each other when there are several groups of R 22 O, which (method) created in accordance with the second objective of the present invention, includes the polymerization of pre resents a vinyl ether monomer having the general formula (IX):
where R 19 -R 23 and q are as previously described by using a combination of Branstead acid (aprotic acid), Lewis acid or an organometallic compound with water, alcohol, phenol, acetal or an adduct of vinyl ether and carboxylic acid as an initiator.
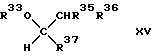
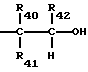
Способ получения простого эфира, выраженного общей формулой (XV):
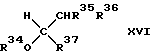
или общей формулой (XVI):
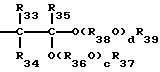
где R33 и R34 - каждый углеводородная группа или углеводородная группа, содержащая атомы кислорода простого эфира в основной цепи, в боковой цепи или и той и другой цепях, и могут быть одинаковыми или отличающимися друг от друга, а R35, R36 и R37 - каждый атом водорода, углеводородная группа или углеводородная группа, содержащая атомы эфирного кислорода в основной цепи, в боковой цепи или в той и другой цепях, и могут быть одинаковыми или разными, который (способ) создан в соответствии с третьей целью настоящего изобретения, включает в себя введение ацеталя или кеталя, выраженного общей формулой (XIV):
где R33, R34, R35, R36 и R37 - такие же, как указанные выше, в химическое взаимодействие с водородом в присутствии твердого катализатора, имеющего кислотные свойства и гидрирующую способность.A method for producing an ether expressed by the general formula (XV):
or general formula (XVI):
where R 33 and R 34 are each hydrocarbon group or hydrocarbon group containing ether oxygen atoms in the main chain, in the side chain, or both, and may be the same or different from each other, and R 35 , R 36 and R 37 is each hydrogen atom, hydrocarbon group or hydrocarbon group containing ether oxygen atoms in the main chain, in the side chain or in both chains, and may be the same or different, which (method) is created in accordance with the third objective of the present invention includes introduction acetal or ketal expressed by the general formula (XIV):
where R 33 , R 34 , R 35 , R 36 and R 37 are the same as above, in the chemical interaction with hydrogen in the presence of a solid catalyst having acidic properties and hydrogenation ability.
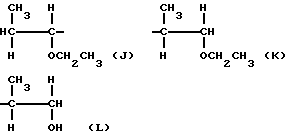
Простой поливиниловый эфир, созданный в соответствии с четвертой целью настоящего изобретения, содержит гомополимер или сополимер простого алкилвинилового эфира, содержащий составляющие звенья, выраженные общей формулой (I) или (I'):
где R1 - алкильная группа, имеющая 1-3 атома углерода, и имеющий среднемассовую молекулярную массу 300-1200 и одну концевую группировку, имеющую структуру, выраженную общей формулой: (II):
или общей формулой (III):
-CH=CHORa (III),
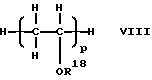
где R1 - такой же, как указанный выше, R2 - углеводородная группа, имеющая 1 - 8 атомов углерода, и Ra - один из радикалов R1 и R2, а простой поливиниловый эфир, также созданный в соответствии с четвертой целью настоящего изобретения, содержит составляющие звенья, выраженные общей формулой (IV):
где R3, R4 и R5 - каждый атом водорода или алкильная группа, имеющая 1 - 4 атома углерода, и могут быть одинаковыми или отличающимися друг от друга, R6 - алкиленовая группа, имеющая 2 - 4 углеродных атома, R7 - алкильная группа, имеющая 1 - 10 углеродных атомов, k - число, среднее значение которого находится в диапазоне 1 - 10, R3 и R7 могут быть одинаковыми или разными в разных составляющих звеньях и R6 могут быть одинаковыми или отличающимися друг от друга, когда составляющее звено содержит несколько радикалов R6, причем упомянутый поливиниловый эфир не содержит ни ненасыщенной связи, ни ацетальной и альдегидной структур в молекуле и имеет среднемассовую молекулярную массу 300 - 3000.The polyvinyl ether created in accordance with the fourth objective of the present invention contains a homopolymer or copolymer of alkyl vinyl ether containing constituent units expressed by the general formula (I) or (I '):
where R 1 is an alkyl group having 1-3 carbon atoms and having a weight average molecular weight of 300-1200 and one end moiety having a structure expressed by the general formula: (II):
or general formula (III):
-CH = CHOR a (III),
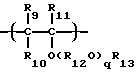
where R 1 is the same as above, R 2 is a hydrocarbon group having 1 to 8 carbon atoms, and R a is one of the radicals R 1 and R 2 , and polyvinyl ether, also created in accordance with the fourth purpose of this the invention contains constituent units expressed by the general formula (IV):
where R 3 , R 4 and R 5 are each hydrogen atom or an alkyl group having 1 to 4 carbon atoms, and may be the same or different from each other, R 6 is an alkylene group having 2 to 4 carbon atoms, R 7 is an alkyl group having 1 to 10 carbon atoms, k is a number whose average value is in the range of 1 to 10, R 3 and R 7 may be the same or different in different constituent units, and R 6 may be the same or different from each other, when the constituting unit contains a plurality of radicals R 6, wherein said polyvinyl ester is not sod rzhit no unsaturated bond or acetal and aldehyde structures in the molecule and has a weight average molecular weight of 300 - 3000.
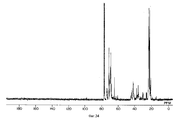
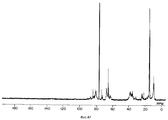
Далее дается краткое описание чертежей, на которых: фигуры 1, 4, 7, 8, 11, 12, 15, 18, 21, 24, 27, 30, 33, 36, 37, 40, 43, 46 и 49 - Спектры поглощения в инфракрасной области поливиниловых эфиров, полученных в примерах 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 и 25A соответственно,
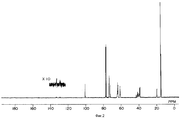
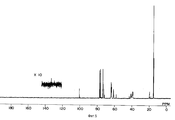
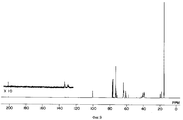
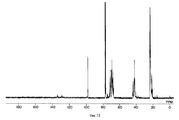
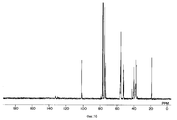
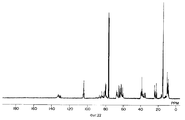
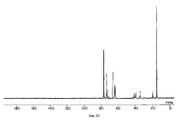
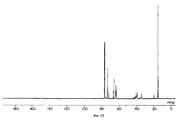
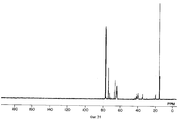
фигуры 2, 5, 9, 13, 16, 19, 22, 25, 28, 31, 34, 38, 41, 44, 47 и 50 - ЯМР 13C-Спектры простых поливиниловых эфиров, полученных в примерах 8, 9, 11, 13, 14, 15, 16, 17, 18, 19, 20, 22, 23, 24, 25 и 25A соответственно,
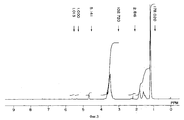
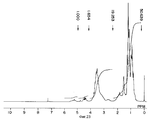
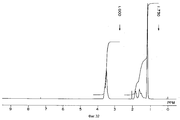
фигуры 3, 6, 10, 14, 17, 20, 23, 26, 29, 32, 35, 39, 42, 45, 48 и 51 - ЯМР 1H-спектры поливинилэфира, полученного в примерах 8, 9, 11, 13, 14, 15, 16, 17, 18, 19, 20, 22, 23, 24, 25 и 25A, соответственно, и
фигуры 52 и 53 - ЯМР 1H-спектры олигомера ацеталя, полученного в примере 37 (1), и простого эфира, полученного в примере 37 (2), соответственно.The following is a brief description of the drawings, in which: Figures 1, 4, 7, 8, 11, 12, 15, 18, 21, 24, 27, 30, 33, 36, 37, 40, 43, 46, and 49 — Absorption Spectra in the infrared region of the polyvinyl esters obtained in examples 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 and 25A, respectively,
figures 2, 5, 9, 13, 16, 19, 22, 25, 28, 31, 34, 38, 41, 44, 47 and 50 — NMR 13 C Spectra of polyvinyl ethers obtained in Examples 8, 9, 11 , 13, 14, 15, 16, 17, 18, 19, 20, 22, 23, 24, 25, and 25A, respectively,
figures 3, 6, 10, 14, 17, 20, 23, 26, 29, 32, 35, 39, 42, 45, 48 and 51 - NMR 1 H-spectra of polyvinyl ether obtained in examples 8, 9, 11, 13 , 14, 15, 16, 17, 18, 19, 20, 22, 23, 24, 25, and 25A, respectively, and
figures 52 and 53 are NMR 1 H-spectra of the acetal oligomer obtained in Example 37 (1) and the ether obtained in Example 37 (2), respectively.
Сначала ведется описание смазочного масла для холодильников компрессионного типа в соответствии с третьей целью настоящего изобретения. A description is first made of a lubricating oil for compression type refrigerators in accordance with a third objective of the present invention.
Предназначенное для компрессионных холодильников смазочное масло в соответствии с настоящим изобретением содержит в качестве основного компонента простой поливиниловый эфир, имеющий составляющие звенья, выраженные общей формулой (XXII):
где R42, R43 и R44 - каждый атом водорода или углеводородная группа, имеющая 1 - 8 атомов углерода, и могут быть одинаковыми или отличающимися друг от друга, R45 - двухвалентная углеводородная группа, имеющая 2 - 10 атомов углерода, R46 - углеводородная группа, имеющая 1 - 10 атомов углерода, V - число, среднее значение которого находится в диапазоне 0 - 10, R42 - R46 могут быть одинаковыми или отличающимися друг от друга в разных составляющих звеньях и R45O могут быть одинаковыми или разными, когда имеется несколько R45O.The lubricating oil for compression refrigerators in accordance with the present invention contains, as a main component, polyvinyl ether having constituent units expressed by the general formula (XXII):
where R 42 , R 43 and R 44 are each hydrogen atom or a hydrocarbon group having 1 to 8 carbon atoms, and may be the same or different from each other, R 45 is a divalent hydrocarbon group having 2 to 10 carbon atoms, R 46 a hydrocarbon group having 1 to 10 carbon atoms, V is a number whose average value is in the range of 0 to 10, R 42 to R 46 may be the same or different from each other in different constituent units, and R 45 O may be the same or different when there are several R 45 O.
В формуле (XXII) R42, R43 и R44 представляет собой каждый атом водорода или углеводородную группу, имеющую 1 - 8 атомов углерода, и могут быть одинаковыми или отличающимися друг от друга. Конкретными примерами описанной выше углеводородной группы являются алкильная группа, такая, как метильная, этильная, н-пропильная, изопропильная, н-бутильная, изобутильная, вторбутильная, трет-бутильная группы, различные виды пентильной группы, различные виды гексильной группы, различные виды гептильной группы и различные виды октильной группы, циклоалкильная группа, такая как циклопентильная, циклогексильная, различные виды метилциклогексильной, этилциклогексильной, диметилциклогексильной групп и т.п., арильная группа, такая как фенильная группа, различные виды метилфенильной, этилфенильной и диметилфенильной группы, или арилалкильная группа, такая, как бензильная группа, различные виды фенилэтильной группы и различные виды метилбензильной группы. R42, R43 и R44 представляют собой предпочтительно атом водорода или алифатическую углеводородную группу, имеющую 5 или менее атомов углерода (соответственно), а более предпочтительно атом водорода или углеводородную группу, имеющую 3 или менее атомов углерода, соответственно.In the formula (XXII), R 42 , R 43 and R 44 represents each hydrogen atom or a hydrocarbon group having 1 to 8 carbon atoms, and may be the same or different from each other. Specific examples of the hydrocarbon group described above are an alkyl group such as methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, sec-butyl, tert-butyl groups, various types of pentyl groups, various types of hexyl groups, various types of heptyl groups and various kinds of octyl group, cycloalkyl group such as cyclopentyl, cyclohexyl, various types of methylcyclohexyl, ethylcyclohexyl, dimethylcyclohexyl groups and the like, an aryl group such as phen an alkyl group, various types of methylphenyl, ethylphenyl and dimethylphenyl groups, or an arylalkyl group such as a benzyl group, various types of phenylethyl group and various types of methylbenzyl group. R 42 , R 43 and R 44 are preferably a hydrogen atom or an aliphatic hydrocarbon group having 5 or less carbon atoms (respectively), and more preferably a hydrogen atom or a hydrocarbon group having 3 or less carbon atoms, respectively.
R45 в формуле (XXII) представляет собой двухвалентную углеводородную группу, имеющую 2 - 10 атомов углерода, которой является, например, двухвалентная алифатическая группа, такая, как этиленовая, фенилэтиленовая, 1,2-пропиленовая, 2-фенил-1,2-пропиленовая, 1,3-пропиленовая группы и различные виды бутиленовой, пентиленовой, гексиленовой, гептиленовой, октиленовой, нониленовой и дециленовой групп, алициклическая группа, имеющая два положения связывания на алициклическом углеводороде, таком, как циклогексан, метилциклогексан, этилциклогексан, диметилциклогексан, пропилциклогексан и т.п., двухвалентный ароматический углеводород; такой, как различные виды фениленовой, метиленовой, этилфениленовой, диметилфениленовой, найтиленовой и т.п. групп, алкилароматическая группа, имеющая одно положение одновалентного связывания на каждой части алкильной группы и ароматической части алкилароматического углеводорода, такого как толуол, ксилол, этилбензол и т.п. или алкилароматическая группа, имеющая положения связывания на частях алкильных групп полиалкилароматического углеводорода, такого, как ксилол, диэтилбензол и т.п.R 45 in the formula (XXII) is a divalent hydrocarbon group having 2 to 10 carbon atoms, which is, for example, a divalent aliphatic group, such as ethylene, phenylethylene, 1,2-propylene, 2-phenyl-1,2- propylene, 1,3-propylene groups and various types of butylene, pentylene, hexylene, heptylene, octylene, nonylene and decylene groups, an alicyclic group having two bonding positions on an alicyclic hydrocarbon such as cyclohexane, methylcyclohexane, ethylcyclohexane, d cyclohexane, propylcyclohexane and the like, a divalent aromatic hydrocarbon; such as various types of phenylene, methylene, ethylphenylene, dimethylphenylene, naphthylene, etc. groups, an alkyl aromatic group having one monovalent binding position on each part of the alkyl group and the aromatic part of the alkyl aromatic hydrocarbon such as toluene, xylene, ethylbenzene and the like. or an alkyl aromatic group having binding positions on parts of the alkyl groups of a polyalkyl aromatic hydrocarbon, such as xylene, diethylbenzene and the like.
Особо предпочтительной из них является алифатическая группа, имеющая 2 - 4 атома углерода. Несколько группировок R45O могут быть одинаковыми или отличающимися друг от друга.Particularly preferred of these is an aliphatic group having 2 to 4 carbon atoms. Several R 45 O moieties may be the same or different from each other.
В формуле (XXII) k представляет собой число повторений, причем среднее значение k находится в диапазоне 0 - 10, а предпочтительно в диапазоне 0 - 5. In the formula (XXII), k represents the number of repetitions, the average value of k being in the range of 0-10, and preferably in the range of 0-5.
В формуле (XXII) R46 - углеводородная группа, имеющая 1 - 10 атомов углерода, и примером такой группы является алкильная группа, такая, как метильная, этильная, н-пропильная, изопропильная, н-бутильная, изобутильная, втор-бутильная, трет-бутильная группы, различные виды пентильной, гексильной, гептильной группы, октильной, нонильной и децильной группы, циклоалкильная группа, такая как циклопентильная, циклогексильная, группы и различные виды метилциклогексильной, пропилциклогексильной, диметилциклогексильной групп и т.п., арильная группа, такая как фенильная группа, различные виды метилфенильной, этилфенильной, диметилфенильной, пропилфенильной, триметилфенильной, бутилфенильной, нафтильной и т.п. или арилалкильная группа, такая, как бензильная группа, различные виды фенилэтильной, метилбензильной, фенилпропильной и бутилфенильной группы. Из них предпочтительными являются углеводороды, имеющие 8 или менее атомов углерода. Когда V= 0, особо предпочтительной является алкильная группа, имеющая 1 - 6 атомов, а когда V = 1 или более, то особо предпочтительной является алкильная группа, имеющая 1 - 4 атомов углерода.In formula (XXII), R 46 is a hydrocarbon group having 1 to 10 carbon atoms, and an example of such a group is an alkyl group such as methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, sec-butyl, tert -butyl groups, various types of pentyl, hexyl, heptyl groups, octyl, nonyl and decyl groups, cycloalkyl groups such as cyclopentyl, cyclohexyl groups and various types of methylcyclohexyl, propylcyclohexyl, dimethylcyclohexyl groups and the like, an aryl group such ac phenyl group, various types of methylphenyl, ethylphenyl, dimethylphenyl, propylphenyl, trimethylphenyl, butylphenyl, naphthyl, etc. or an arylalkyl group, such as a benzyl group, various kinds of phenylethyl, methylbenzyl, phenylpropyl and butylphenyl groups. Of these, hydrocarbons having 8 or less carbon atoms are preferred. When V = 0, an alkyl group having 1 to 6 atoms is particularly preferred, and when V = 1 or more, an alkyl group having 1 to 4 carbon atoms is particularly preferred.
Число повторений в поливиниловом эфире, выраженном формулой (XXII), которое соответствует степени полимеризации, может быть подходящим образом выбрано в соответствии с требуемой кинематической вязкостью, которая обычно находится в диапазоне 5 - 1000 сс при 40oC, а предпочтительно - в диапазоне 5 - 800 сс при 40oC.The number of repetitions in the polyvinyl ether expressed by the formula (XXII), which corresponds to the degree of polymerization, can be appropriately selected in accordance with the desired kinematic viscosity, which is usually in the range of 5 to 1000 cc at 40 o C, and preferably in the range of 5 to 800 cc at 40 o C.
Поливинилэфир может быть получен путем полимеризации соответствующего винилэфирного мономера, и описанный ниже способ получения поливинилэфира, являющийся второй целью настоящего изобретения, может быть осуществлен как способ полимеризации. The polyvinyl ester can be obtained by polymerization of the corresponding vinyl ester monomer, and the polyvinyl ether production method described below, which is the second objective of the present invention, can be carried out as a polymerization method.
Концевые группы полученного поливинилового эфира могут быть преобразованы до требуемой структуры с помощью способа, раскрытого в примерах осуществления настоящего изобретения, или с помощью традиционных способов. Преобразуемая группа представляет собой насыщенный углеводород, простой эфир, спирт, кетон, амид, имид, нитрил или т.п. The end groups of the resulting polyvinyl ether can be converted to the desired structure using the method disclosed in the embodiments of the present invention, or using traditional methods. The group to be converted is a saturated hydrocarbon, ether, alcohol, ketone, amide, imide, nitrile or the like.
В качестве простого поливинилового эфира, являющегося основным компонентом смазочного масла в соответствии с настоящим изобретением, предпочтительно используют соединения, имеющие показанные ниже концевые структуры;
(1) Структура, в которой одно концевое звено выражено формулой (XXIII):
где R47, R48, и R49 - каждый атом водорода или углеводородная группа, имеющая 1 - 8 атомов углерода и могут быть одинаковыми или разными, R50 - двухвалентная углеводородная группа, имеющая 2 - 20 атомов углерода, R51 - углеводородная группа, имеющая 1 - 10 атомов углерода, a - число, среднее значение которого находится в диапазоне 0 - 10, и R50O могут быть одинаковыми или разными, когда имеется несколько групп R50O, а другое концевое звено выражено формулой (XXIV):
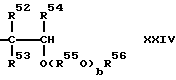
где R52, R53 и R54 - каждый атом водорода или углеводородная группа, имеющая 1 - 8 атомов углерода, и могут быть одинаковыми или отличающимися друг от друга, R55 - двухвалентная углеводородная группа, имеющая 2 - 10 атомов углерода, R56 - углеводородная группа, имеющая 1 - 10 атомов углерода, b - число, среднее значение которого находится в диапазоне 0 - 10, и R50O могут быть одинаковыми или разными, когда имеется несколько групп R50O.As the simple polyvinyl ether, which is the main component of the lubricating oil in accordance with the present invention, it is preferable to use compounds having the following end structures;
(1) A structure in which one end link is expressed by formula (XXIII):
where R 47 , R 48 , and R 49 are each hydrogen atom or a hydrocarbon group having 1 to 8 carbon atoms and may be the same or different, R 50 is a divalent hydrocarbon group having 2 to 20 carbon atoms, R 51 is a hydrocarbon group having 1 to 10 carbon atoms, a is a number whose average value is in the
where R 52 , R 53 and R 54 are each hydrogen atom or a hydrocarbon group having 1 to 8 carbon atoms, and may be the same or different from each other, R 55 is a divalent hydrocarbon group having 2 to 10 carbon atoms, R 56 - a hydrocarbon group having 1 to 10 carbon atoms, b is a number whose average value is in the range of 0 to 10, and R 50 O may be the same or different when there are several groups of R 50 O.
(2) Структура, в которой одно концевое звено выражено формулой (XXIII), а другое - формулой (XXV):
где R57, R58 и R59 - каждый атом водорода или углеводородная группа, имеющая 1 - 8 атомов углерода, и могут быть одинаковыми или разными, R60 и R62 - соответственно двухвалентная углеводородная группа, имеющая 2 - 10 атомов углерода, группа, имеющая 1 - 8 атомов углерода, и могут быть одинаковыми или разными, R61 и R63 - каждый углеводородная группа, имеющая 1 - 10 атомов углерода, и могут быть одинаковыми или разными, c и d каждый - число, среднее значение которого находится в диапазоне 0 - 10, и могут быть одинаковыми или отличающимися друг от друга, R60O могут быть одинаковыми или отличающимися друг от друга, когда имеется несколько групп R60O, и R62O могут быть одинаковыми или разными, когда имеется несколько групп R62O.(2) A structure in which one end link is expressed by formula (XXIII) and the other by formula (XXV):
where R 57 , R 58 and R 59 are each hydrogen atom or a hydrocarbon group having 1 to 8 carbon atoms, and may be the same or different, R 60 and R 62 are respectively a divalent hydrocarbon group having 2 to 10 carbon atoms, a group having 1 to 8 carbon atoms, and may be the same or different, R 61 and R 63 are each hydrocarbon group having 1 to 10 carbon atoms, and may be the same or different, c and d each is a number whose average value is in the range of 0 - 10, and may be the same or different from each other, R 60 O may be dinakovymi or different from each other when there are multiple R 60 O groups, and R 62 O may be the same or different when there are several groups of R 62 O.
(3) Структура, в которой одно концевое звено выражено формулой (XXIII), а другое - содержит ненасыщенную двойную связь, и
(4) Структура, в которой одно концевое звено выражено формулой (XXIII), а другое - формулой (XXVI):
где R64, R65 и R66 каждый - атом водорода или углеводородная группа, имеющая 1 - 8 атомов углерода, и могут быть одинаковыми или разными.(3) A structure in which one end link is expressed by formula (XXIII) and the other contains an unsaturated double bond, and
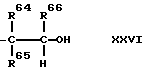
(4) A structure in which one end link is expressed by formula (XXIII) and the other by formula (XXVI):
where R 64 , R 65 and R 66 each is a hydrogen atom or a hydrocarbon group having 1 to 8 carbon atoms, and may be the same or different.
Поливинилэфир может быть смесью двух или более соединений, имеющих концевые структуры, выбранные из группы, состоящей из структур (1) - (4). Предпочтительными примерами такой смеси являются смеси соединения, имеющего структуру (1), и соединения, имеющего структуру (4) и смесь соединения, имеющего структуру (2) и соединения, имеющего структуру (3). Polyvinyl ether can be a mixture of two or more compounds having terminal structures selected from the group consisting of structures (1) to (4). Preferred examples of such a mixture are mixtures of a compound having structure (1) and a compound having structure (4) and a mixture of a compound having structure (2) and a compound having structure (3).
Смазочное масло в соответствии с настоящим изобретением содержит в качестве основного компонента описанный выше простой поливиниловый эфир. Поскольку кинематическая вязкость смазочного масла перед смешиванием с хладагентом находится предпочтительно в диапазоне 5-1000 сс при 40oC cc при 40oC, то описанные выше исходные материалы, инициатор и условия выбирают таким образом, чтобы получить поливинилэфир, имеющий кинематическую вязкость в указанном диапазоне. Средняя молекулярная масса этого полимера находится обычно в диапазоне 150-2000, а предпочтительно в диапазоне 150-4000. Когда кинематическая вязкость полимера находится за пределами указанного диапазона, ее можно отрегулировать до значения в указанном диапазоне путем смешивания с другим полимером, имеющим подходящую кинематическую вязкость.The lubricating oil in accordance with the present invention contains the polyvinyl ether described above as a main component. Since the kinematic viscosity of the lubricating oil before mixing with the refrigerant is preferably in the range of 5-1000 cc at 40 ° C cc at 40 ° C, the starting materials, initiator and conditions described above are selected so as to obtain a polyvinyl ester having a kinematic viscosity in the specified range . The average molecular weight of this polymer is usually in the range of 150-2000, and preferably in the range of 150-4000. When the kinematic viscosity of the polymer is outside the specified range, it can be adjusted to a value in the specified range by mixing with another polymer having a suitable kinematic viscosity.
В предназначенном для холодильников смазочном масле в соответствии с настоящим изобретением поливиниловый эфир, выраженный формулой (XXII), описанной выше, может быть использован один или в виде сочетания из двух или более видов. Он может быть использован также путем смешивания с другими видами смазочных масел. In the lubricating oil for refrigerators in accordance with the present invention, the polyvinyl ether expressed by the formula (XXII) described above can be used alone or in combination of two or more kinds. It can also be used by mixing with other types of lubricating oils.
В предназначенное для холодильников смазочное масло в соответствии с настоящим изобретением могут быть добавлены по желанию различные виды используемых в традиционных смазочных маслах присадок, таких, как присадки, повышающие стойкость к нагрузкам, выносители хлора, антиоксиданты, дезактиваторы металлов, противопенные присадки, моюще-диспергирующие вещества, присадки, понижающие температурную зависимость вязкости, присадки, регулирующие маслянистость, противоизносные присадки, противозадирные присадки, присадки против ржавчины, замедлители коррозии, присадки, понижающие температуру застывания масла и т.п. Various types of additives used in conventional lubricating oils can be added to the lubricant for refrigerators in accordance with the present invention, such as additives to increase resistance to stress, chlorine scavengers, antioxidants, metal deactivators, antifoam agents, detergents and dispersants , viscosity reducing agents, oil control agents, antiwear additives, extreme pressure additives, anti-rust additives, for corrosion retardants, additives that lower the pour point of oil, etc.
Примерами описанных выше присадок, повышающих стойкость к нагрузкам, являются серосодержащие органические соединения, такие, как моносульфиды, полисульфиды, сульфоксиды, сульфоны, тиосульфинаты, сульфинированные масла и эфиры, тиокарбонаты, тиофены, тиазолы, эфиры метансульфокислоты и т.п. Эфиры фосфорной кислоты, такие, как моноэфиры фосфорной кислоты, диэфиры фосфорной кислоты, триэфиры фосфорной кислоты (трикрезилфосфат) и т.п., эфиры фосфорной кислоты, такие, как моноэфиры, диэфиры и триэфиры фосфористой кислоты и т. п., эфиры тиофосфорной кислоты, такие, как триэфиры тиофосфорной кислоты, эфиры жирных кислот, такие, как эфиры высших жирных кислот, эфиры жирных гидроксиларилкислот, сложные эфиры многоатомных спиртов, содержащих карбоновые кислоты, эфиры акриловой кислоты и т.п., органические хлорсодержащие присадки, такие, как хлорированные углеводороды, хлорпроизводные карбоновых кислот и т. п. , органические фторсодержащие присадки, такие, как фторированные алифатические карбоновые кислоты, фторэтиленовые смолы, фторалкилполисилоксаны, фторированный графит и т.п., спиртовые присадки, такие как высшие спирты и т.п., присадки, содержание соединения металлов, такие, как соли нафтеновой кислоты (нафтенат свинца), соли жирных кислот (свинцовые соли жирных кислот), соли тиофосфатов (диалкилдитиофосфаты цинка), соли тиокарбаминовой кислоты, молибденорганические соединения, оловоорганические соединения, германийорганические соединения, сложные эфиры борной кислоты и т.п. Examples of the load resistance additives described above are sulfur-containing organic compounds such as monosulfides, polysulfides, sulfoxides, sulfones, thiosulfinates, sulfonated oils and esters, thiocarbonates, thiophenes, thiazoles, methanesulfonic acid esters and the like. Phosphoric acid esters, such as phosphoric acid monoesters, phosphoric acid diesters, phosphoric acid esters (tricresyl phosphate) and the like, phosphoric acid esters, such as monoesters, diesters and phosphoric acid esters and the like, thiophosphoric esters such as thiophosphoric acid esters, fatty acid esters, such as higher fatty acid esters, hydroxylaryl fatty acid esters, polyhydric alcohol esters containing carboxylic acids, acrylic acid esters and the like, organic chlorine additives, such such as chlorinated hydrocarbons, chlorine derivatives of carboxylic acids, etc., organic fluorine-containing additives, such as fluorinated aliphatic carboxylic acids, fluoroethylene resins, fluoroalkyl polysiloxanes, fluorinated graphite, etc., alcohol additives, such as higher alcohols and the like. , additives, metal compound content, such as salts of naphthenic acid (lead naphthenate), salts of fatty acids (lead salts of fatty acids), salts of thiophosphates (zinc dialkyldithiophosphates), salts of thiocarbamic acid, organomolybdenum Connections, organotin compounds, organogermanium compounds, boric acid esters and the like
Примерами выносителя хлора являются соединения, имеющие простую глицидноэфирную группу, моноэфиры эпоксижирных кислот, эпоксидированные жиры и масла, соединения, имеющие эпоксициклоалкильную группу и т.п. Примерами антиоксидантов являются фенолы (2,6-ди-трет-бутил-пара-крезол), ароматические амины ( α - нафтиламин) и т.п. Примерами дезактиваторов металлов являются производные бензотриазола и т.п. Примерами противопенных присадок являются силиконовое масло (диметилполисилоксан), полиметакрилаты и т.п. Примерами моюще- диспергирующих агентов являются сульфонаты, феноляты, сукцинимиды и т. п. Примерами присадок, понижающих температурную зависимость вязкости масла, являются полиметакрилаты, полиизобутилен, сополимеры этилена и пропилена, сополимеры гидрированного стирола и диена и т.п. Examples of a chlorine scavenger are compounds having a simple glycidic ether group, epoxy fatty acid monoesters, epoxidized fats and oils, compounds having an epoxycycloalkyl group, and the like. Examples of antioxidants are phenols (2,6-di-tert-butyl-para-cresol), aromatic amines (α-naphthylamine) and the like. Examples of metal deactivators are benzotriazole derivatives and the like. Examples of antifoam additives are silicone oil (dimethylpolysiloxane), polymethacrylates, and the like. Examples of detergent-dispersing agents are sulfonates, phenolates, succinimides, etc. Examples of additives that lower the temperature dependence of the viscosity of an oil are polymethacrylates, polyisobutylene, ethylene and propylene copolymers, hydrogenated styrene and diene copolymers, and the like.
Смазочное масло в соответствии с настоящим изобретением используют в качестве смазочного масла для холодильников компрессионного типа из-за отличной совместимости его с хладагентами и превосходных смазочных свойств. В противоположность традиционным смазочным маслам смазочное масло в соответствии с настоящим изобретением имеет отличную совместимость с водородсодержащими флонами, такими, как флон-134а, и т.п., которыми более конкретно является, кроме описанного выше флона -134а, 1,1-дихлор-2,2,2-трифторэтан(флон-123), 1-хлор-1,1-дифторэтан (флон-142 b) 1,1-дифторэтан (флон-152а), хлордифторметан (флон-22), трифторметан (флон-23), дифторметан (флон-32), пентафторэтан (флон-125) и т.п. The lubricating oil according to the present invention is used as a lubricating oil for compression type refrigerators due to its excellent compatibility with refrigerants and excellent lubricating properties. In contrast to traditional lubricating oils, the lubricating oil in accordance with the present invention has excellent compatibility with hydrogen-containing flons, such as flon-134a, and the like, which more specifically is, in addition to the above-described flon-134a, 1,1-dichloro- 2,2,2-trifluoroethane (flon-123), 1-chloro-1,1-difluoroethane (flon-142 b) 1,1-difluoroethane (flon-152a), chlorodifluoromethane (flon-22), trifluoromethane (flon- 23), difluoromethane (flon-32), pentafluoroethane (flon-125), etc.
Смазочное масло в соответствии с настоящим изобретением может быть использовано в смеси с другим смазочным маслом для холодильников компрессионного типа с целью улучшения совместимости с холодильным агентом. The lubricating oil in accordance with the present invention can be used in a mixture with other lubricating oil for compression type refrigerators in order to improve compatibility with the refrigerant.
Ниже описан способ получения простого поливинилового эфира. The following describes a method for producing a simple polyvinyl ether.
В способе получения поливинилэфира в качестве исходного винилэфирного мономера используют соединение, выраженное формулой (IX):
В представленной выше формуле R19, R20 и R21 каждый - атом водорода или углеводород, имеющий 1-8 атомов углерода, и могут быть одинаковыми или разными. Примерами углеводородной группы являются те группы, которые представлены в примерах при описывании радикалов R42-R44 (XXII). R19, R20 и R21 каждый - предпочтительно атом водорода или алифатическая углеводородная группа, имеющая 5 или менее атомов углерода, а более предпочтительно атом водорода или углеводородная группа имеющая 3 или менее атомов углерода.In the method for producing polyvinyl ester, the compound expressed by formula (IX) is used as the starting vinyl ester monomer:
In the above formula, R 19 , R 20 and R 21 each is a hydrogen atom or a hydrocarbon having 1-8 carbon atoms, and may be the same or different. Examples of the hydrocarbon group are those groups that are presented in the examples when describing the radicals R 42 -R 44 (XXII). R 19 , R 20 and R 21 are each preferably a hydrogen atom or an aliphatic hydrocarbon group having 5 or less carbon atoms, and more preferably a hydrogen atom or a hydrocarbon group having 3 or less carbon atoms.
В формуле (IX) R22 представляет собой двухвалентную углеводородную группу, имеющую 2-10 атомов углерода, причем примерами двухвалентной углеводородной группы являются те группы, которые представлены в качестве примеров при описании радикала R45 в формуле (XXII). R22 - предпочтительно алифатическая группа, имеющая 2-4 атома углерода, и R22O могут быть одинаковыми или разными.In the formula (IX), R 22 represents a divalent hydrocarbon group having 2-10 carbon atoms, and examples of the divalent hydrocarbon group are those groups that are presented as examples when describing the radical R 45 in the formula (XXII). R 22 is preferably an aliphatic group having 2-4 carbon atoms, and R 22 O may be the same or different.
В формуле (IX) q представляет собой число повторений, и среднее значение q находится в диапазоне 0-10, а предпочтительно в диапазоне 0-5. In formula (IX), q is the number of repetitions, and the average value of q is in the range of 0-10, and preferably in the range of 0-5.
R23 в формуле (IX) представляет собой углеводородную группу, имеющую 1-10 атомов углерода, и ее примерами являются те же группы, что представлены в качестве примеров при описании радикала R46 в формуле (XXII). R23 - предпочтительно углеводородная группа, имеющая 8 или менее атомов углерода. Когда q=0, особенно предпочтительной является алкильная группа, имеющая 1-6 атомов углерода, а когда q= 1 или более, то особенно предпочтительна алкильная группа, имеющая 1-4 атома углерода.R 23 in the formula (IX) is a hydrocarbon group having 1-10 carbon atoms, and its examples are the same groups that are presented as examples when describing the radical R 46 in the formula (XXII). R 23 is preferably a hydrocarbon group having 8 or less carbon atoms. When q = 0, an alkyl group having 1-6 carbon atoms is particularly preferred, and when q = 1 or more, an alkyl group having 1-4 carbon atoms is particularly preferred.
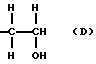
Примерами мономера, представляющего собой простой виниловый эфир, выраженный формулой (IX), являются винилметиловый, винилэтиловый, винил-н-пропиловый, винилизопропиловый, винил-н-бутиловый, винилизобутиловый, винил-втор-бутиловый, винил-трет-бутиловый, винил-н-пентиловый, винил-н-гексиловый, винил-2-метоксиэтиловый, винил-2-этоксиэтиловый, винил-2-метокси-1-метилэтиловый, винил-2-метоксипропиловый, винил-3,6-диоксагептиловый, винил-3,6,9-триоксадециловый, винил-1,4-диметил-3,6-диоксагептиловый, винил-1,4,7-триметил-3,6,9-триоксадециловый эфиры, 1-метоксипропен, 1-этоксипропен, 1-н-пропоксипропен, 1-изопропоксипропен, 1-н-бутоксипропен, 1-изобутоксипропен, 1-втор-бутоксипропен, 1-трет-бутоксипропен, 1-метоксипропен, 2-этоксипропен, 2-н-пропоксипропен, 2-изопропоксипропен, 2-н-бутоксипропен, 2-изобутоксипропен, 2-втор-бутоксипропен, 2-трет-бутоксипропен, 1-метокси-1-бутен, 1-этокси-1-бутен, 1-н-пропокси-1-бутен, 1-изопропокси-1-бутен, 1-н-бутокси-1-бутен, 1-изобутокси-1-бутен, 1-втор-бутокси-1-бутен, 1-трет-бутокси-1-бутен, 2-метокси-1-бутен, 2-этокси-1-бутен, 2-н-пропокси-1-бутен, 2-изопропокси-1-бутен, 2-н-бутокси-1-бутен, 2-изобутокси-1-бутен, 2-втор-бутокси-1-бутен, 2-трет-бутокси-1-бутен, 2-метокси-2-бутен, 2-этокси-2-бутен, 2-н-пропокси-2-бутен, 2-изопропокси-2-бутен, 2-н-бутокси-2-бутен, 2-изобутокси-2-бутен, 2-втор-бутокси-2-бутен, 2-трет-бутокси-2-бутен и т.п. Эти виниловые эфиры могут быть получены любым традиционным способом. Examples of the monomer, which is a simple vinyl ether, expressed by the formula (IX) are vinyl methyl, vinyl ethyl, vinyl n-propyl, vinyl isopropyl, vinyl n-butyl, vinyl isobutyl, vinyl-sec-butyl, vinyl-tert-butyl, vinyl n-pentyl, vinyl-n-hexyl, vinyl-2-methoxyethyl, vinyl-2-ethoxyethyl, vinyl-2-methoxy-1-methylethyl, vinyl-2-methoxypropyl, vinyl-3,6-dioxaheptyl, vinyl-3, 6,9-trioxadecyl, vinyl-1,4-dimethyl-3,6-dioxaheptyl, vinyl-1,4,7-trimethyl-3,6,9-trioxadecyl esters, 1-methox ipropen, 1-ethoxypropene, 1-n-propoxypropene, 1-isopropoxypropene, 1-n-butoxypropene, 1-isobutoxypropene, 1-sec-butoxypropene, 1-tert-butoxypropene, 1-methoxypropene, 2-ethoxypropene, 2-n- propoxypropene, 2-isopropoxypropene, 2-n-butoxypropene, 2-isobutoxypropene, 2-sec-butoxypropene, 2-tert-butoxypropene, 1-methoxy-1-butene, 1-ethoxy-1-butene, 1-n-propoxy- 1-butene, 1-isopropoxy-1-butene, 1-n-butoxy-1-butene, 1-isobutoxy-1-butene, 1-sec-butoxy-1-butene, 1-tert-butoxy-1-butene, 2-methoxy-1-butene, 2-ethoxy-1-butene, 2-n-propoxy-1-butene, 2-isopropoxy-1-butene, 2-n-butoxy-1-butene, 2- zobutoxy-1-butene, 2-sec-butoxy-1-butene, 2-tert-butoxy-1-butene, 2-methoxy-2-butene, 2-ethoxy-2-butene, 2-n-propoxy-2- butene, 2-isopropoxy-2-butene, 2-n-butoxy-2-butene, 2-isobutoxy-2-butene, 2-sec-butoxy-2-butene, 2-tert-butoxy-2-butene, etc. P. These vinyl esters can be obtained in any conventional manner.
В способе в соответствии с настоящим изобретением в качестве инициатора можно использовать сочетание кислоты Брэнстеда (апротонной кислоты), кислоты Льюиса или металлоорганического соединения и воды, спирта, фенола, ацеталя или продукта присоединения простого винилового эфира и карбоновой кислоты. In the method according to the invention, a combination of Bransted acid (aprotic acid), Lewis acid or an organometallic compound and water, alcohol, phenol, acetal or a vinyl ether and carboxylic acid addition product can be used as initiator.
Примерами апротонной кислоты являются фтористоводородная, хлористоводородная, бромистоводородная, азотная, серная, трихлоруксусная, трифторуксусная кислоты и т.п. Примерами кислоты Льюиса являются трифторид бора, трихлорид алюминия, трибромид алюминия, тетрахлорид олова, дихлорид цинка, хлорид железа (3) и т.п. Из указанных кислот Льюиса особенно предпочтительными являются трифторид бора и его комплексы. Примерами металлоорганического соединения являются диэтилалюминийхлорид, этилалюминийхлорид, диэтилцинк и т. п. Examples of aprotic acid are hydrofluoric, hydrochloric, hydrobromic, nitric, sulfuric, trichloroacetic, trifluoroacetic acids and the like. Examples of Lewis acids are boron trifluoride, aluminum trichloride, aluminum tribromide, tin tetrachloride, zinc dichloride, iron chloride (3), and the like. Of these Lewis acids, boron trifluoride and its complexes are particularly preferred. Examples of the organometallic compound are diethylaluminium chloride, ethylaluminium chloride, diethylzinc, etc.
Подходящее соединение может быть выбрано из воды, спирта, фенола, ацеталя или аддукта простого винилового эфира с карбоновой кислотой и использовано в сочетании с апротонной кислотой (кислотой Брэнстеда), кислотой Льюиса или металлоорганическим соединением. A suitable compound may be selected from water, alcohol, phenol, acetal, or a vinyl ether adduct with a carboxylic acid and used in combination with aprotic acid (Bransted acid), Lewis acid, or an organometallic compound.
Примерами упомянутого выше спирта являются насыщенные алифатические спирты, имеющие 1-10 атомов углерода, такие, как метанол, этанол, пропанол, изопропанол, бутанол, изобутанол, втор-бутанол, трет-бутанол, различные виды пантанола, гексанола и октанола и т.п. спирты, содержащие кислород, связанный как простая эфирная связь, такие, как моноалкиловые эфиры этиленгликоля, моноариловые эфиры этиленгликоля, моноалкиловые эфиры пропиленгликоля, моноариловые эфиры пропиленгликоля, моноалкиловые эфиры полиэтиленгликоля, моноариловые эфиры полиэтиленгликоля, моноалкиловые эфиры полипропиленгликоля моноариловые эфиры полипропиленгликоля, 1,3-диметокси-2-пропанол, 1-этокси-3-метокси- 2-пропанол, 1,3-диэтокси-2-пропанол и т.п. и тому подобное соединения. Из указанных соединений предпочтительными являются алифатические спирты, имеющие 3 или менее атомов углерода, и особо предпочтительны метанол и этанол. В качестве спирта, содержащего кислород, связанный как простая эфирная связь, предпочтительными являются соединения этой структуры, имеющие 14 или менее атомов углерода. Examples of the above-mentioned alcohol are saturated aliphatic alcohols having 1-10 carbon atoms, such as methanol, ethanol, propanol, isopropanol, butanol, isobutanol, sec-butanol, tert-butanol, various kinds of pantanol, hexanol and octanol, etc. . alcohols containing oxygen bound as an ether bond, such as ethylene glycol monoalkyl ethers, ethylene glycol monoaryl ethers, propylene glycol monoalkyl ethers, propylene glycol monoaryl ethers, polyethylene glycol monoalkyl ethers, polyethylene glycol monoaryl ethers, polyethylene glycol ethers -2-propanol, 1-ethoxy-3-methoxy-2-propanol, 1,3-diethoxy-2-propanol and the like. and the like compounds. Of these compounds, aliphatic alcohols having 3 or less carbon atoms are preferred, and methanol and ethanol are particularly preferred. As an alcohol containing oxygen bound as an ether bond, compounds of this structure having 14 or less carbon atoms are preferred.
Примерами фенола являются фенол, различные виды крезола и тому подобные соединения. Examples of phenol are phenol, various types of cresol and the like.
Примерами ацеталя являются диметилацеталь ацетальдегида, диэтилацеталь ацетальдегида, метилэтилацеталь ацетальдегида, ди-н-пропилацеталь ацетальдегида, метил-н-пропилацеталь ацетальдегида, этил-н-пропилацеталь, ацетальдегида, диизопропилацеталь ацетальдегида, метилизопропилацеталь ацетальдегида, этилизопропилацеталь ацетальдегида, н-пропилизопропилацеталь ацетальдегида, ди-н-бутилацеталь ацетальдегида, метил-н-бутилацеталь ацетальдегида, этил-н-бутилацеталь ацетальдегида, н-пропил-н-бутилацеталь ацетальдегида, изопропил-н-бутилацеталь ацетальдегида, диизобутилацеталь ацетальдегида, метилизобутилацеталь ацетальдегида, этилизобутилацеталь ацетальдегида, н-пропилизобутилацеталь ацетальдегида, изопропилизобутилацеталь ацетальдегида, н-бутилизобутилацеталь ацетальдегида, ди-вторбутилацеталь ацетальдегида, метил-втор-бутилацеталь ацетальдегида, этил-втор-бутилацеталь ацетальдегида, н-пропил-вторбутилацеталь ацетальдегида, изопропил-втор-бутилацеталь ацетальдегида, н-бутил-втор-бутилацеталь ацетальдегида, изобутил-втор-бутилацеталь ацетальдегида, ди-трет-бутилацеталь ацетальдегида, метил-трет-бутилацетат ацетальдегида, этил-трет-бутилацеталь ацетальдегида, н-пропил-трет-бутилацеталь ацетальдегида, изопропил-трет-бутилацеталь ацетальдегида, н-бутил-трет-бутилацеталь ацетальдегида, изобутил-трет-бутилацеталь ацетальдегида, втор-бутил-трет-бутилацеталь ацетальдегида, ди ( β -метоксиэтил)ацеталь ацетальдегида, ( β -метоксиизопропил)-ацеталь ацетальдегида, диметилацеталь пропиональдегида, диэтилацеталь пропиональдегида, метилэтилацеталь пропиональдегида, ди-н-пропилацеталь пропиональдегида, метил-н-пропилацеталь пропиональдегида, этил-н-пропилацеталь пропиональдегида, диизопропилацеталь пропиональдегида, метилизопропилацеталь пропиональдегида, этилизопропилацеталь пропинальдегида, н-пропилизопропилацеталь пропиональдегида, ди-н-бутилацеталь пропиональдегида, метил-н-бутилацеталь пропиональдегида, этил-н-бутилацеталь пропиональдегида, н-пропил-н-бутилацеталь пропиональдегида, изопропил-н-бутилацеталь пропиональдегида, диизобутилацеталь пропиональдегида, метилизобутилацеталь пропиональдегида, этилизобутилацеталь пропиональдегида, н-пропилизобутилацеталь пропиональдегида, изопропилизобутилацеталь пропиональдегида, н-бутилизобутилацеталь пропиональдегида, ди-втор-бутилацеталь пропиональдегида, метил-вторбутилацеталь пропиональдегида, этил-вторбутилацеталь пропиональдегида, н-пропил-втор-бутилацеталь пропиональдегида, изопропил-втор-бутилацеталь пропиональдегида, н-бутил-втор-бутилацеталь пропиональдегида, изобутил-втор-бутилацеталь пропиональдегида, ди-трет-бутилацеталь пропиональдегида, метил-трет-бутилацеталь пропиональдегида, этил-трет-бутилацеталь пропиональдегида, н-пропил-трет-бутилацеталь пропиональдегида, изопропил-трет-бутилацеталь пропиональдегида, н-бутил-трет-бутилацеталь пропиональдегида, изобутил-трет-бутилацеталь пропиональдегида, втор-трет-бутилацеталь пропиональдегида, ди ( β -метоксиэтил)ацеталь пропиональдегида, ди ( β -метоксиизопропил)ацеталь пропиональдегида, диметилацеталь н-бутиральдегида, диэтилацеталь н-бутиральдегида, метилэтилацеталь н-бутиральдегида, ди-н-пропилацеталь н-бутиральдегида, метил-н-пропилацеталь н-бутиральдегида, этил-н-пропилацеталь н-бутиральдегида, диизопропилацеталь н-бутиральдегида, метилизопропилацеталь н-бутиральдегида, этилизопропилацеталь н-бутиральдегида,
н-пропилизопропилацеталь н-бутиральдегида, ди-н-бутилацеталь н-бутиральдегида, метил-н-бутилацеталь н-бутиральдегида, этил-н-бутилацеталь н-бутиральдегида, н-пропил-н-бутилацеталь н-бутиральдегида, изопропил-н-бутилацеталь н-бутиральдегида, диизобутилацеталь н-бутиральдегида, метилизобутилацеталь н-бутиральдегида, этилизобутилацеталь и-бутиральдегида, н-пропилизобутилацеталь, н-бутиральдегида, изопропил-изобутилацеталь н-бутиральдегида, н-бутилизобутилацеталь н-бутиральдегида, ди-втор-бутилацеталь н-бутиральдегида, метил-втор-бутилацеталь н-бутиральдегида, этил-втор-бутилацеталь, н-бутиральдегида, н-пропил-втор-бутилацеталь н-бутиральдегида, изопропил-втор-бутилацеталь н-бутиральдегида, н-бутил-втор-бутилацеталь н-бутиральдегида, изобутил-втор-бутилацеталь н-бутиральдегида, ди-трет-бутилацеталь н-бутиральдегида, метил-трет-бутилацеталь н-бутиральдегида, этил-трет-бутилацеталь н-бутиральдегида, н-пропил-трет-бутилацеталь н-бутиральдегида, изопропил-трет-бутилацеталь н-бутиральдегида, н-бутил-трет-бутилацеталь н-бутиральдегида, изобутил-трет-бутилацеталь н-бутиральдегида, втор-бутил-трет-бутилацеталь н-бутиральдегида, ди( β -метоксиэтил)-ацеталь н-бутиральдегида, ди( β -метоксиизопропил)ацеталь н-бутиральдегида и т.п.Examples of acetal are acetaldehyde dimethyl acetal, acetaldehyde diethyl acetal, acetaldehyde methyl ethyl acetal, acetaldehyde di-n-propyl acetal, methyl n-propyl acetal, acetaldehyde, acetaldehyde diisopropyl acetal, acetone di-propyl acetaldehyde, methyl isopropyl acetal acetaldehyde, ethyl isopropyl acetal acetaldehyde, acetaldehyde n-butyl acetal, acetaldehyde methyl n-butyl acetal, acetaldehyde ethyl n-butyl acetal, acetaldehyde n-propyl n-butyl acetal, isopropyl n-butyl acetaldehyde acetaldehyde, acetaldehyde diisobutyl acetal, acetaldehyde methyl isobutyl acetal, acetaldehyde ethyl isobutyl acetal, acetaldehyde n-propyl isobutyl acetaldehyde, acetaldehyde acetaldehyde di-sec-butyl acetaldehyde acetaldehyde acetaldehyde acetaldehyde acetaldehyde , isopropyl-sec-butyl acetaldehyde, n-butyl sec-butyl acetaldehyde, isobutyl sec-butyl acetaldehyde, di-tr acetaldehyde t-butyl acetal, acetaldehyde methyl tert-butyl acetate, acetaldehyde ethyl tert-butyl acetal, acetaldehyde n-propyl tert-butyl acetaldehyde, acetaldehyde n-butyl tert-butyl acetaldehyde, isobutyl tert-butyl acetaldehyde , sec-butyl tert-butyl acetaldehyde, di (β-methoxyethyl) acetaldehyde acetal, (β-methoxyisopropyl) acetaldehyde acetal, propionaldehyde dimethyl acetal, propionaldehyde diethyl acetal, propionaldehyde methyl ethyl acetal, propional di-n-propyl acetal dehydide, propionaldehyde methyl-n-propylacetal, propionaldehyde ethyl-n-propylacetal, propionaldehyde diisopropylacetal, propionaldehyde methylisopropylacetal propinaldehyde ethylisopropylacetal propionaldehyde n-propylisopropylacetalide, di-n-butyl-acetaldehyde propionaldehyde , n-propyl-n-butylacetal propionaldehyde, isopropyl-n-butylacetal propionaldehyde, diisobutyl acetal propionaldehyde, methyl isobutyl acetal propionaldehyde, ethyl isobut ilatsetal propionaldehyde, n-propionaldehyde propilizobutilatsetal, izopropilizobutilatsetal propionaldehyde, n-butilizobutilatsetal propionaldehyde di-vtorbutilatsetal propionaldehyde, methyl vtorbutilatsetal propionaldehyde, ethyl vtorbutilatsetal propionaldehyde, n-propyl vtorbutilatsetal propionaldehyde, iso-vtorbutilatsetal propionaldehyde, n -butyl-sec-butylacetal of propionaldehyde, isobutyl-sec-butylacetal of propionaldehyde, di-tert-butylacetal of propionaldehyde, methyl tert-butylacetal propionalalde guide, propionaldehyde ethyl tert-butyl acetal, propionaldehyde n-propyl-tert-butyl acetaldehyde, propionaldehyde isopropyl tert-butyl acetaldehyde, propionaldehyde n-butyl tert-butyl acetaldehyde, propionaldehyde isobutyl tert-butyl acetal, di-tert-butyl acetaldehyde β-methoxyethyl) propionaldehyde acetal, di (β-methoxyisopropyl) propionaldehyde acetal, n-butyraldehyde dimethyl acetal, n-butyraldehyde diethyl acetal, n-butyraldehyde methyl ethyl acetal, n-butyraldehyde di-n-propyl acetal n-butyl acetal n-methyl acetal ide, ethyl-n-propilatsetal n-butyraldehyde, n-butyraldehyde diizopropilatsetal, metilizopropilatsetal n-butyraldehyde, n-butyraldehyde etilizopropilatsetal,
n-butyl aldehyde n-propylisopropylacetal, n-butyraldehyde di-n-butyl acetal, n-butyraldehyde methyl n-butyl acetal, n-butyraldehyde ethyl n-butyl acetal, n-butyl n-butyl acetal n-butyl acetal n-butyl acetal n-butyraldehyde, diisobutyl acetal n-butyraldehyde, methyl isobutyl acetal n-butyraldehyde, ethyl isobutyl acetal and-butyraldehyde, n-propyl isobutyl acetal, n-butyraldehyde, isopropyl-isobutylacetal n-butyraldehyde-butyldehyde-butyldehyde-butylidehyde methyl sec-buti n-butyraldehyde acetal, ethyl-sec-butyl acetal, n-butyraldehyde, n-propyl-sec-butyl acetal n-butyraldehyde, isopropyl sec-butyl acetal n-butyraldehyde, n-butyl sec-butyl acetal n-butyraldehyde, from n-butyraldehyde butyl acetal, n-butyraldehyde di-tert-butyl acetal, n-butyraldehyde methyl tert-butyl acetal, n-butyraldehyde ethyl t-butyl acetal, n-propyl tert-butyl acetal n-butyraldehyde, isopropyl n-butyraldehyde butyraldehyde, n-butyl tert-butyl acetal n-butyraldehyde isobutyl tert-butyl acetal n-butyl aldehyde, sec-butyl tert-butyl acetal, n-butyraldehyde di (β-methoxyethyl) -atsetal n-butyraldehyde di (β -metoksiizopropil) n-butyraldehyde acetal, etc.
Примерами карбоновой кислоты, используемой для образования аддукта с виниловым эфиром, являются уксусная, пропионовая, н-масляная, изомасляная, н-валериановая, изовалериановая, 2-метилмасляная, триметилуксусная, н-капроновая, 2,2-диметилмасляная, 2-метилвалериановая, 3-метилвалериановая, 4-метилвалериановая, энантовая, 2-метилкапроновая, каприловая, 2-этилкапроновая, 2-н-пропилвалериановая, н-нонановая, 3,5,5-триметилкапроновая, ундекановая кислоты и т.п. Examples of the carboxylic acid used to form the adduct with vinyl ether are acetic, propionic, n-butyric, isobutyric, n-valerianic, isovalerianic, 2-methylbutyric, trimethylacetic, n-caproic, 2,2-dimethylbutyric, 2-
Простой виниловый эфир может быть одинаковым с теми, что используют для полимеризации, или отличающимся от них, и его конкретными примерами являются те же самые соединения, которые указаны в качестве примеров в описании винилэфирных мономеров, выраженных формулой (IX). Аддукт винилового эфира и карбоновой кислоты может быть получен смешиванием этих соединений и проведения реакции при температуре примерно 0-100oC. Аддукт может быть использован для реакции после выделения путем перегонки или как таковой без выделения.Vinyl ether may be the same as or used for polymerization, and specific examples are the same compounds that are indicated as examples in the description of vinyl ether monomers expressed by formula (IX). The vinyl ester and carboxylic acid adduct can be obtained by mixing these compounds and carrying out the reaction at a temperature of about 0-100 ° C. The adduct can be used for the reaction after isolation by distillation or as such without isolation.
К инициированному концу цепи полимера присоединяют водород, когда используют воду, спирт или фенол, и группу, образованную путем отщепления одной из алкоксигрупп от используемого ацеталя, когда используют ацеталь. При использовании аддукта винилового эфира с карбоновой кислотой присоединяют группу, образованную путем отщепления алкилкарбоксигруппы, производной от карбоновой кислоты, от аддукта винилового эфира и карбоновой кислоты. Hydrogen is attached to the initiated end of the polymer chain when water, alcohol or phenol is used, and a group formed by cleavage of one of the alkoxy groups from the acetal used when acetal is used. When using a vinyl ester adduct with a carboxylic acid, a group formed by cleaving an alkyl carboxy group derived from a carboxylic acid from a vinyl ester adduct and a carboxylic acid is attached.
С другой стороны, на оборванном конце цепи полимера образуется ацеталь, олефин или альдегид, когда используют воду, спирт, фенол или ацеталь. А когда используют аддукт винилового эфира с карбоновой кислотой, то образуется произведенный от карбоновой кислоты сложный эфир полуацеталя. Когда этот сложный эфир полуацеталя подвергают гидролизу в присутствии кислоты, образуется альдегид. On the other hand, acetal, olefin or aldehyde is formed at the dangling end of the polymer chain when water, alcohol, phenol or acetal is used. And when a vinyl ester adduct with a carboxylic acid is used, a semi-acetal ester derived from the carboxylic acid is formed. When this hemiacetal ester is hydrolyzed in the presence of an acid, an aldehyde is formed.
Температура полимеризации винилэфирного мономера, выраженного формулой (IX) находится обычно в диапазоне - 80-150oC, а предпочтительно 0-100oC, хотя ее можно изменять в зависимости от вида исходных материалов и инициатора. Реакцию полимеризации заключают за время примерно от 10 секунд до 10 часов.The polymerization temperature of the vinyl ester monomer expressed by the formula (IX) is usually in the range of 80-150 ° C, and preferably 0-100 ° C, although it can be changed depending on the type of the starting materials and the initiator. The polymerization reaction is concluded in a time of from about 10 seconds to 10 hours.
Для регулирования молекулярной массы при реакции полимеризации ее можно уменьшать путем увеличения количества воды, спирта, фенола, ацеталя или аддукта винилового эфира с карбоновой кислотой относительно количества винилэфирного мономера, выраженного формулой (IX), а также путем увеличения количества кислоты Брэнстеда или кислоты Льюиса. To control the molecular weight during the polymerization reaction, it can be reduced by increasing the amount of water, alcohol, phenol, acetal, or the adduct of vinyl ether with a carboxylic acid relative to the amount of vinyl ester monomer expressed by formula (IX), as well as by increasing the amount of Branstead acid or Lewis acid.
Полимеризация может быть выполнена без растворителя, но может быть использован растворитель, инертный в условиях проведения реакции. Тип растворителя особенно не ограничивают. Предпочтительными примерами растворителя являются углеводородные растворителя являются углеводородные растворители, такие, как гексан, бензол, толуол и т.п. и эфирные растворители, такие, как диэтиловый эфир, 1,2-диметосиэтан, тетрагидрофуран и т.п. Реакция полимеризации может быть закончена путем добавления щелочи. The polymerization can be carried out without a solvent, but a solvent inert under the conditions of the reaction can be used. The type of solvent is not particularly limited. Preferred examples of the solvent are hydrocarbon solvents are hydrocarbon solvents such as hexane, benzene, toluene and the like. and ethereal solvents such as diethyl ether, 1,2-dimethoxyethane, tetrahydrofuran and the like. The polymerization reaction can be completed by adding alkali.
Описанными выше способами получают простой поливиниловый эфир, имеющий составляющее звено, выраженное формулой (X):
где R19-R23 и q - такие же, как указано выше.By the methods described above, polyvinyl ether is prepared having a constituent unit expressed by the formula (X):
where R 19 -R 23 and q are the same as described above.
Из способов получения поливинилового эфира предпочтительными являются два описанных ниже способа. Of the methods for producing polyvinyl ether, the two methods described below are preferred.
Первым из предпочтительных способов является способ полимеризации винилэфирного мономера в присутствии кислоты Льюиса в качестве катализатора и ацеталя, выраженного формулой (XI):
В ацетале формулы (XI), используемом в описанном выше способе, R24, R25 и R26 - каждый - атом водорода или углеводородная группа, имеющая 1-8 атомов углерода, и могут быть одинаковыми или разными. Примерами углеводородной группы являются те же самые группы, которые представлены в качестве примеров при описании радикалов R42 и R44 в формуле (XXII). R27 и R29 представляют собой каждый двухвалентную углеводородную группу, имеющую 2 - 10 атомов углерода, и могут быть одинаковыми или отличающимися друг от друга. Примерами двухвалентной углеводородной группы являются те же самые группы, что представлены в качестве примеров при описании R45 в формуле (XXII). Несколько групп R27O и R29O могут быть соответственно одинаковыми или разными. Далее, r и s каждый - число повторений, среднее значение которого находится в диапазоне 1 - 10, предпочтительно 0 - 5, и могут быть одинаковыми или разными, R28 и R30 каждый - углеводородная группа, имеющая 1 - 10 атомов углерода, и могут быть одинаковыми или разными. Примерами углеводородной группы, имеющей 1 - 10 углеродных атомов, являются те же самые группы, что представлены в качестве примеров при описании R46 в формуле (XXII). В качестве R28 особо предпочтительными являются алкильная группа, имеющая 1 - 6 атомов углерода, когда r = 0, и алкильная группа, имеющая 1 - 4 атома углерода, когда r = 1 или более. В качестве R30 особо предпочтительными являются алкильная группа, имеющая 1 - 6 атомов углерода, когда s = 0, и алкильная группа, имеющая 1 - 4 атома углерода, когда s = 1, или более.The first of the preferred methods is a method for the polymerization of a vinyl ester monomer in the presence of a Lewis acid as a catalyst and acetal expressed by the formula (XI):
In the acetal of formula (XI) used in the above method, R 24 , R 25 and R 26 are each a hydrogen atom or a hydrocarbon group having 1-8 carbon atoms, and may be the same or different. Examples of the hydrocarbon group are the same groups that are presented as examples in the description of the radicals R 42 and R 44 in the formula (XXII). R 27 and R 29 represent each divalent hydrocarbon group having 2 to 10 carbon atoms, and may be the same or different from each other. Examples of a divalent hydrocarbon group are the same groups that are presented as examples in the description of R 45 in the formula (XXII). Several groups of R 27 O and R 29 O may be the same or different, respectively. Further, r and s each is the number of repetitions, the average value of which is in the range of 1-10, preferably 0-5, and may be the same or different, R 28 and R 30 each is a hydrocarbon group having 1-10 carbon atoms, and may be the same or different. Examples of a hydrocarbon group having 1 to 10 carbon atoms are the same groups that are presented as examples in the description of R 46 in the formula (XXII). As R 28 , an alkyl group having 1 to 6 carbon atoms when r = 0 and an alkyl group having 1 to 4 carbon atoms when r = 1 or more are particularly preferred. As R 30 , an alkyl group having 1 to 6 carbon atoms when s = 0 and an alkyl group having 1 to 4 carbon atoms when s = 1 or more are particularly preferred.
Примерами ацеталя, выраженного формулой (XI), являются те же самые соединения, что представлены в качестве примеров при данном выше описании ацеталей. Examples of acetal expressed by formula (XI) are the same compounds that are presented as examples in the above description of acetals.
Вторым предпочтительным способом является способ, при котором получают ацеталь, имеющий формулу (XIII):
где R19-R23, R31, R32, q и t - такие же, как указанные выше, путем добавления винилэфирного мономера, выраженного формулой (IX), к спирту, выраженному формулой (XII):
R32 (OR31)tOH (XII)
в присутствии кислоты Льюиса в качестве катализатора, после чего к ацеталю добавляют еще винилэфирный мономер, выраженный формулой (IX), и полимеризуют.A second preferred method is a method in which an acetal having the formula (XIII) is prepared:
where R 19 -R 23 , R 31 , R 32 , q and t are the same as above by adding the vinyl ester monomer expressed by formula (IX) to the alcohol expressed by formula (XII):
R 32 (OR 31 ) t OH (XII)
in the presence of a Lewis acid as a catalyst, after which another vinyl ester monomer of the formula (IX) is added to the acetal and polymerized.
В спирте, выраженном формулой (XII), R31 - двухвалентная углеводородная группа, имеющая 2 - 10 атомов углерода, примерами которой являются те же группы, что представлены в качестве примеров при описании радикала R45 в формуле (XXII) Несколько групп R31O могут быть одинаковыми или разными. Далее, t - число повторений, среднее значение которого находится в диапазоне 0 - 10, а предпочтительно в диапазоне 0 - 5. R32 - углеводородная группа, имеющая 1 - 10 атомов углерода, примерами которой являются те же группы, что представлены в качестве примеров при описании R46 в формуле (XXII). В качестве R32 особо предпочтительными являются алкильная группа, имеющая 1 - 6 атомов углерода, когда t = 0, и алкильная группа, имеющая 1 - 4 атома углерода, когда t = 1 или более.In the alcohol expressed by the formula (XII), R 31 is a divalent hydrocarbon group having 2 to 10 carbon atoms, examples of which are the same groups that are presented as examples when describing the radical R 45 in the formula (XXII) Several R 31 O groups may be the same or different. Further, t is the number of repetitions, the average value of which is in the range 0 - 10, and preferably in the range 0 - 5. R 32 is a hydrocarbon group having 1 to 10 carbon atoms, examples of which are the same groups that are presented as examples when describing R 46 in the formula (XXII). As R 32 , an alkyl group having 1 to 6 carbon atoms when t = 0 and an alkyl group having 1 to 4 carbon atoms when t = 1 or more are particularly preferred.
Примерами спирта, выраженного формулой (XII), являются те же самые спирты, что представлены в качестве примеров при описании спиртов, указанных выше. Examples of the alcohol expressed by the formula (XII) are the same alcohols that are presented as examples in the description of the alcohols mentioned above.
Примерами кислоты Льюиса, используемой в качестве катализатора в первом и втором предпочтительных способах, являются те же самые кислоты, что представлены в качестве примеров при данном выше описании используемых в качестве катализатора кислот Льюиса. Из этих соединений особенно предпочтительными являются трифторид бора и его комплексы. Examples of the Lewis acid used as a catalyst in the first and second preferred methods are the same acids that are presented as examples in the above description of the Lewis acids used as a catalyst. Of these compounds, boron trifluoride and its complexes are particularly preferred.
Полимеризация винилэфирного мономера в первом и втором предпочтительных способах может быть проведена при температуре обычно в диапазоне - 80 - +150oC, а предпочтительно в диапазоне 0 - 100oC, но ее можно изменять в зависимости от вида исходных материалов и инициатора. При использовании ацеталя наблюдается выделение тепла от полимеризации без периода индукции, а при использовании спирта выделение тепла от полимеризации без периода индукции происходит после образования ацеталя. Таким образом, регулирование температуры во время реакции можно легко осуществлять путем добавления винилэфирного мономера со скоростью, которая уравновешивает способность аппарата выделять тепло. Полимеризацию заканчивают обычно через период времени от 10 секунд до 10 часов после начала реакции.The polymerization of the vinyl ester monomer in the first and second preferred methods can be carried out at a temperature usually in the range of - 80 - +150 o C, and preferably in the range of 0 - 100 o C, but it can be changed depending on the type of starting materials and initiator. When using acetal, heat is generated from polymerization without an induction period, and when using alcohol, heat is released from polymerization without an induction period after the formation of acetal. Thus, temperature control during the reaction can be easily done by adding a vinyl ester monomer at a rate that balances the ability of the apparatus to generate heat. The polymerization is usually completed after a period of time from 10 seconds to 10 hours after the start of the reaction.
После проведения полимеризации так, как было описано выше, требуемый поливиниловый эфир может быть получен путем отделения и очистки любым традиционным способом в соответствии с необходимостью. After the polymerization is carried out as described above, the desired polyvinyl ether can be obtained by separation and purification by any conventional method as required.
В способе получения простого эфира в качестве исходного материала используют ацеталь или кеталь формулы (XIV):
В формуле (XIV) R33 и R34 каждый - углеводородная группа, такая, как метильная, этильная, н-пропильная, изопропильная, группы и т.п. или углеводородная группа: содержащая атомы эфирного кислорода в основной цепи, в боковой цепи или и в той, и в другой цепях, такая, как группы, выраженные формулами:
где R - углеводородная группа, имеющая 1 - 10 атомов углерода, и W - целое число от 1 до 500. R33 и R34 могут быть одинаковыми или разными. R35, R36 и R37 каждый - атом водорода, углеводородная группа или углеводородная группа, содержащая атомы эфирного кислорода в основной, боковой или той и другой цепях. Примерами углеводородной группы или углеводородной группы, содержащей атомы эфирного кислорода, являются те же самые группы, что указаны в качестве примеров при описании радикалов R33 и R34, группы, выраженные формулой:
где R - углеводородная группа, имеющая 1 - 10 атомов углерода, и W - целое число от 1 до 500, и тому подобные группы,
R35, R36 и R37 могут быть одинаковыми или отличающимися друг от друга.In the method for producing ether, an acetal or a ketal of formula (XIV) is used as a starting material:
In the formula (XIV), R 33 and R 34 are each a hydrocarbon group, such as methyl, ethyl, n-propyl, isopropyl, groups and the like. or a hydrocarbon group: containing ether oxygen atoms in the main chain, in the side chain, or in both chains, such as groups expressed by the formulas:
where R is a hydrocarbon group having 1 to 10 carbon atoms, and W is an integer from 1 to 500. R 33 and R 34 may be the same or different. R 35 , R 36 and R 37 each is a hydrogen atom, a hydrocarbon group or a hydrocarbon group containing ether oxygen atoms in the main, side or one and the other chains. Examples of a hydrocarbon group or a hydrocarbon group containing ether oxygen atoms are the same groups that are indicated as examples when describing the radicals R 33 and R 34 , groups expressed by the formula:
where R is a hydrocarbon group having 1 to 10 carbon atoms, and W is an integer from 1 to 500, and the like groups,
R 35 , R 36 and R 37 may be the same or different from each other.
В соответствии с настоящим изобретением простой эфир, выраженный формулой (XV):
или
где R33, R34, R35, R36 и R37 - такие же, как указанные выше, получают путем проведения реакции между ацеталем или кеталем, выраженными формулой (XIV) и водородом в присутствии твердого катализатора, обладающего кислотными свойствами и гидрирующей способностью.In accordance with the present invention, an ether expressed by the formula (XV):
or
where R 33 , R 34 , R 35 , R 36 and R 37 are the same as those described above, obtained by reaction between acetal or ketal expressed by formula (XIV) and hydrogen in the presence of a solid catalyst having acidic properties and hydrogenation ability .
В качестве ацеталя или кеталя формулы (XIV) предпочтительным является соединение, выраженное формулой (XVII):
где R38 и R39 каждый - углеводородная группа, имеющая 1-20 атомов углерода, или углеводородная группа, содержащая атомы кислорода простого эфира и могут быть одинаковыми или разными, R38 - одинаковый с составляющими звеньями или отличающийся от них и - целое число от 1 до 500. В данном случае получают в качестве упомянутого простого эфира соединение, выраженное формулой (XVIII):
где R38, R39 и U - такие же, как указанные выше.As acetal or ketal of formula (XIV), a compound expressed by formula (XVII) is preferred:
where R 38 and R 39 each is a hydrocarbon group having 1-20 carbon atoms, or a hydrocarbon group containing ether oxygen atoms and can be the same or different, R 38 is the same with or different from the constituent units and is an integer from 1 to 500. In this case, a compound expressed by the formula (XVIII) is obtained as said ether:
where R 38 , R 39 and U are the same as above.
В соединении, выраженном формулой (XVII), иногда содержится соединение, выраженное формулой: (XXVII):
где R38 и U - такие же, как указанные выше, и в данном случае полученным соединением является соединение, выраженное описанной выше формулой (XVIII), или смесь соединения, выраженного формулой (XVIII), и соединения, выраженного формулой (XIX).In the compound expressed by formula (XVII), sometimes contains a compound expressed by formula: (XXVII):
where R 38 and U are the same as above, and in this case, the obtained compound is a compound expressed by the above formula (XVIII), or a mixture of a compound expressed by the formula (XVIII) and a compound expressed by the formula (XIX).
В качестве ацеталя и кеталя, выраженных формулой (XIV), хорошо также использовать соединение, выраженное формулой (XX):
R40CH(OR41)2 (XX)
где R40 и R41 каждый - углеводородная группа, имеющая 1 - 20 атомов углерода, и могут быть одинаковыми или разными. В этом случае в качестве простого эфира получают соединение, выраженное формулой (XXI):
R40CH2OR41 (XXI),
где R40 и R41 - такие же, как указанные выше.As the acetal and ketal expressed by the formula (XIV), it is also good to use the compound expressed by the formula (XX):
R 40 CH (OR 41 ) 2 (XX)
where R 40 and R 41 each is a hydrocarbon group having 1 to 20 carbon atoms, and may be the same or different. In this case, as a simple ether get the compound expressed by formula (XXI):
R 40 CH 2 OR 41 (XXI),
where R 40 and R 41 are the same as above.
В предлагаемом в соответствии с настоящим изобретением способе используют твердый катализатор, обладающий кислотными свойствами и гидрирующей способностью. В качестве твердого катализатора, обладающего кислотными свойствами и гидрирующей способностью, используют сочетание из двух видов катализатора, которыми являются катализатор гидрирования и твердый кислотный катализатор, или твердый кислотный катализатор, обладающий гидрирующей способностью. The process according to the invention uses a solid catalyst having acidic properties and hydrogenating ability. As a solid catalyst having acidic properties and a hydrogenating ability, a combination of two types of catalyst is used, which are a hydrogenation catalyst and a solid acid catalyst, or a solid acid catalyst having a hydrogenating ability.
Катализатор гидрирования особенно не ограничивают, и можно использовать различные типы обычно используемого катализатора гидрирования. Примерами особо эффективного катализатора являются (1) металлы, такие, как никель, палладий, родий и рутений в единственном числе или в качестве основного компонента, (2) катализатор, имеющий в качестве компонента металлический катализатор из группы (1), нанесенный на активированный уголь, оксид алюминия, диатомовую землю (кизельгур) или т.п. и (3) катализаторы Ренея: такие как никель Ренея и кобальт Ренея. The hydrogenation catalyst is not particularly limited, and various types of commonly used hydrogenation catalyst can be used. Examples of a particularly effective catalyst are (1) metals, such as nickel, palladium, rhodium and ruthenium in the singular or as a main component, (2) a catalyst having as a component a metal catalyst from group (1) supported on activated carbon , alumina, diatomaceous earth (kieselguhr) or the like. and (3) Raney catalysts: such as Raney nickel and Raney cobalt.
Твердый кислотный катализатор особенно не ограничивают, и можно использовать различные типы обычно используемого твердого кислотного катализатора. Например, особенно эффективными являются активированная глина, кислая глина, различные виды цеолита, ионообменные смолы, диоксид кремния, оксид алюминия и гетерополикислоты. The solid acid catalyst is not particularly limited, and various types of commonly used solid acid catalyst can be used. For example, activated clay, acid clay, various types of zeolite, ion exchange resins, silica, alumina and heteropoly acids are particularly effective.
Твердый кислотный катализатор, обладающий гидрирующей способностью особенно не ограничивают, и могут быть использованы различные виды обычно используемого твердого кислотного катализатора, обладающего гидрирующей способностью. Например, особенно эффективными являются катализаторы, в которых на различные виды цеолита нанесены никель, палладий, платина, рутений или тому подобное. The solid acid catalyst having a hydrogenating ability is not particularly limited, and various kinds of commonly used solid acid catalyst having a hydrogenating ability can be used. For example, catalysts are particularly effective in which nickel, palladium, platinum, ruthenium or the like are coated on various types of zeolite.
Для осуществления способа в соответствии с настоящим изобретением предпочтительно используют следующие количества катализатора. При использовании комбинированного катализатора количество гидрирующего катализатора составляет 0,1 - 50 мас.% и количество твердого катализатора - 0,1 - 50 мас. % от количества реагирующих материалов соответственно. Когда используют твердый кислотный катализатор, обладающий гидрирующей способностью, количество его составляет 0,1 - 50 мас.% от количества реагирующих материалов. Когда количество составляет менее 0,1 мас.%, недостаточна продолжительность реакции, а когда количество превышает 50 мас.%, то чрезмерно большое количество катализатора по отношению к реагирующим материалам вызывает проблему снижения производительности. The following amounts of catalyst are preferably used to carry out the process of the present invention. When using a combined catalyst, the amount of hydrogenation catalyst is 0.1 to 50 wt.% And the amount of solid catalyst is 0.1 to 50 wt. % of the amount of reacting materials, respectively. When using a solid acid catalyst having a hydrogenating ability, its amount is 0.1 to 50 wt.% Of the amount of reacting materials. When the amount is less than 0.1 wt.%, The reaction time is insufficient, and when the amount exceeds 50 wt.%, An excessively large amount of catalyst with respect to the reacting materials causes a problem in reducing productivity.
В соответствии с настоящим изобретением осуществляют реакцию ацеталя или кеталя формулы (XIV) с водородом в присутствии описанного выше катализатора. Является предпочтительным, когда газообразный водород и ацеталь или кеталь вводят в контакт друг с другом в молярном отношении 1:10 - 200:1. Когда молярное отношение меньше значения в указанном диапазоне, недостаточна продолжительность реакции, а когда оно превышает значения в указанном диапазоне, то возникает проблема снижения производительности. In accordance with the present invention, acetal or ketal of formula (XIV) is reacted with hydrogen in the presence of the catalyst described above. It is preferred that hydrogen gas and acetal or ketal are brought into contact with each other in a molar ratio of 1:10 to 200: 1. When the molar ratio is less than the value in the indicated range, the reaction time is insufficient, and when it exceeds the values in the indicated range, the problem of reducing productivity arises.
Предпочтительными условиями реакции, проводимой в соответствии со способом по настоящему изобретению, являются следующие: температура реакции - 10 - 250oC, парциальное давление водорода - 1 - 200 кг/см2, время реакции в случае периодической реакции - 0,1 - 10 часов, и в случае проточной системы часовая объемно-массовая скорость (WHSV) реагирующей жидкости - 0,01 - 100/час, и часовая объемная скорость (GHSV) газообразного водорода - 100 - 10000/час.The preferred reaction conditions carried out in accordance with the method of the present invention are the following: the reaction temperature is 10 - 250 o C, the partial pressure of hydrogen is 1 - 200 kg / cm 2 the reaction time in the case of a periodic reaction is 0.1 to 10 hours , and in the case of a flow system, the hourly space-mass velocity (WHSV) of the reacting liquid is 0.01 to 100 / hour, and the hourly space velocity (GHSV) of hydrogen gas is 100 to 10000 / hour.
Реакция может быть проведена без растворителя, но может быть использован растворитель при условии, что он устойчив при условиях проведения реакции. Примерами подходящих растворителей являются углеводородные растворители, такие, как гексан, пентан и октан. The reaction can be carried out without a solvent, but a solvent can be used provided that it is stable under the reaction conditions. Examples of suitable solvents are hydrocarbon solvents such as hexane, pentane and octane.
Путем описанной выше реакции обеспечивают отщепление от ацеталя или кеталя формулы (XIV) группы - OR33 или - OR34 и замену ее на водород с образованием при этом простого эфира, выраженного формулой (XV) или формулой (XVI). Эта реакция ясно показывает, что, даже когда любой из радикалов R33-R37 представляет собой углеводородную группу, содержащую атомы эфирного кислорода, водород реагирует не с эфирным кислородом, а только с кислородом в части ацеталя или кеталя.By the reaction described above, the formula (XIV) of the group - OR 33 or - OR 34 is cleaved from the acetal or ketal and replaced with hydrogen, thereby forming an ether expressed by the formula (XV) or the formula (XVI). This reaction clearly shows that even when any of the radicals R 33 -R 37 represents a hydrocarbon group containing ether oxygen atoms, hydrogen does not react with ether oxygen, but only with oxygen in the part of acetal or ketal.
После окончания продукт реакции может быть отделен от катализатора обычной фильтрацией или декантацией. Отделенный катализатор может быть использован опять без особой обработки. After completion, the reaction product can be separated from the catalyst by conventional filtration or decantation. The separated catalyst can be used again without much processing.
Продукт реакции может быть выделен такими методами, как перегонка, экстракция, промывка и высушивание, если это потребуется. The reaction product can be isolated by methods such as distillation, extraction, washing and drying, if necessary.
Ниже описано новое соединение - простой поливиниловый эфир как вторая цель настоящего изобретения. A new compound, polyvinyl ether, is described below as a second object of the present invention.
В соответствии с настоящим изобретением в качестве нового поливинилового эфира предлагаются два вида соединений. In accordance with the present invention, two types of compounds are provided as the new polyvinyl ether.
Первое из новых соединений содержит гомополимер или сополимер простого алкилвинилового эфира, имеющего алкильную группу с 1-3 атомами углерода. Необходимо, чтобы среднемассовая молекулярная масса полимера находилась в диапазоне 300 - 1200, а предпочтительно в диапазоне 400 - 1000. Отношение среднемассовой молекулярной массы к среднечисленной молекулярной массе находится обычно в диапазоне 1,05 - 1,50, а предпочтительно в диапазоне 1,06 - 1,40. The first of the new compounds contains a homopolymer or copolymer of a simple vinyl vinyl ether having an alkyl group with 1-3 carbon atoms. It is necessary that the weight average molecular weight of the polymer is in the range of 300 to 1200, and preferably in the range of 400 to 1000. The ratio of the weight average molecular weight to number average molecular weight is usually in the range of 1.05 - 1.50, and preferably in the range of 1.06 - 1.40.
Поливиниловый эфир в соответствии с настоящим изобретением может быть получен путем полимеризации соответствующего мономера - простого винилового эфира. Примерами винилэфирного мономера являются винилметиловый, винилэтиловый, винил-н-пропиловый, винилизопропиловый эфиры, 1-метокси1-пропен, 1-этокси-1-пропен и 1-пропокси-1-пропен. Винилэфирный мономер может быть использован в единственном числе или в виде сочетания из двух или более видов. The polyvinyl ether in accordance with the present invention can be obtained by polymerization of the corresponding monomer - simple vinyl ether. Examples of the vinyl ester monomer are vinyl methyl, vinyl ethyl, vinyl n-propyl, vinyl isopropyl ethers, 1-methoxy1-propene, 1-ethoxy-1-propene and 1-propoxy-1-propene. The vinyl ester monomer may be used singularly or as a combination of two or more kinds.
В качестве способа полимеризации винилэфирного мономера может быть осуществлен способ получения простого поливинилового эфира, являющийся целью настоящего изобретения. В соответствии с этим способом поливиниловый эфир по настоящему изобретению получают путем полимеризации винилэфирного мономера с использованием сочетания апротонной кислоты, кислоты Льюиса или металлоорганического соединения со спиртом или ацеталем в качестве инициатора. В качестве апротонной кислоты, кислоты Льюиса, металлоорганического соединения и ацеталя пригодны соединения, представленные в качестве примеров при описании способа получения поливинилового эфира в соответствии с второй целью настоящего изобретения. As a method for polymerizing a vinyl ether monomer, a method for producing a polyvinyl ether can be carried out, which is an object of the present invention. In accordance with this method, the polyvinyl ether of the present invention is prepared by polymerizing a vinyl ester monomer using a combination of aprotic acid, Lewis acid or an organometallic compound with alcohol or acetal as an initiator. Suitable aprotic acid, Lewis acid, organometallic compound and acetal are the compounds shown as examples in the description of the method for producing polyvinyl ether in accordance with the second objective of the present invention.
Примерами спирта являются метанол, этанол, пропанол, изопропанол, бутанол, изобутанол, втор-бутанол, трет-бутанол, различные виды пентанола и гексанола и т. п. Из указанных соединений предпочтительными являются спирты, имеющие 3 или менее атомов углерода. В частности, предпочтительны метанол и этанол. Examples of the alcohol are methanol, ethanol, propanol, isopropanol, butanol, isobutanol, sec-butanol, tert-butanol, various types of pentanol and hexanol, etc. Of these compounds, alcohols having 3 or less carbon atoms are preferred. In particular, methanol and ethanol are preferred.
Полученный указанным образом поливиниловый эфир в соответствии с настоящим изобретением содержит гомополимер или сополимер алкилвинилового эфира, содержащего один или несколько видов составляющих звеньев, выраженных формулой (I) или (I'):
где R1 - алкильная группа, имеющая 1-3 атома углерода, причем одна концевая группа имеет структуру, выраженную формулой (II):
или формулой (III)
-CH=CHORa
где R1 - такой же, как указанный выше, R2 - углеводородная группа, имеющая 1-8 атомов углерода, и Ra - любой из радикалов R1 и R2.Thus obtained polyvinyl ether in accordance with the present invention contains a homopolymer or copolymer of alkyl vinyl ether containing one or more kinds of constituent units, expressed by the formula (I) or (I '):
where R 1 is an alkyl group having 1-3 carbon atoms, and one end group has a structure expressed by formula (II):
or formula (III)
-CH = CHOR a
where R 1 is the same as above, R 2 is a hydrocarbon group having 1-8 carbon atoms, and R a is any of the radicals R 1 and R 2 .
В формуле (II) R2 произведен из остаточной группы, образованной путем отщепления гидроксильной группы от спирта, или из остаточной группы, образованной путем отщепления атома кислорода от алкоксигруппы в ацетале, который, как и спирт, используют для инициирования полимеризации.In formula (II), R 2 is derived from a residual group formed by cleavage of a hydroxyl group from an alcohol, or from a residual group formed by cleavage of an oxygen atom from an alkoxy group in acetal, which, like alcohol, is used to initiate polymerization.
При использовании спирта к инициированному концу цепи полимера присоединяют водород, а при использовании ацеталя - остаточную группу, образованную путем отщепления одной из алкоксигрупп от ацеталя. К оборванному концу присоединяют ацетальную группу, выраженную описанной выше формулой (II), или олефиновую группу, выраженную описанной выше формулой (III). When using alcohol, hydrogen is attached to the initiated end of the polymer chain, and when using acetal, the residual group formed by cleavage of one of the alkoxy groups from acetal. An acetal group expressed by the above formula (II) or an olefin group expressed by the above formula (III) is attached to the dangling end.
Гомополимер или сополимер простого алкилвинилового эфира может содержать оборванную концевую группу, выраженную исключительно только формулой (II), только формулой (III) или имеющую структуру, смешанную из упомянутых двух. The alkyl vinyl ether homopolymer or copolymer may contain a dangling end group expressed solely by formula (II), only formula (III), or having a structure mixed from the two.
Полимеризация может быть проведена при температуре в диапазоне - 80 - 150oC, предпочтительно 0 - 100oC, и ее можно изменять в зависимости от вида исходных материалов и инициатора. Реакцию полимеризации заканчивают обычно через период времени от 10 секунд до 10 часов после начала реакции.The polymerization can be carried out at a temperature in the range of - 80 - 150 o C, preferably 0 - 100 o C, and it can be changed depending on the type of starting materials and initiator. The polymerization reaction is usually completed after a period of time from 10 seconds to 10 hours after the start of the reaction.
Для регулирования молекулярной массы при реакции полимеризации молекулярную массу полимера уменьшают путем увеличения количества спирта или ацеталя. To control the molecular weight during the polymerization reaction, the molecular weight of the polymer is reduced by increasing the amount of alcohol or acetal.
Полимеризация может быть осуществлена без растворителя, но можно использовать растворитель, если он устойчив в условиях реакции. Растворитель особенно не ограничивают. Предпочтительными примерами растворителя являются углеводородные растворители, такие, как гексан, бензол, и толуол и эфирные растворители, такие, как диэтиловый эфир, 1,2-диметоксиэтан и тетрагидрофуран. Реакция полимеризации может быть закончена путем добавления щелочи. The polymerization can be carried out without a solvent, but a solvent can be used if it is stable under the reaction conditions. The solvent is not particularly limited. Preferred examples of the solvent are hydrocarbon solvents such as hexane, benzene, and toluene and ether solvents such as diethyl ether, 1,2-dimethoxyethane and tetrahydrofuran. The polymerization reaction can be completed by adding alkali.
Второй простой поливиниловый эфир в соответствии с настоящим изобретением содержит составляющие звенья, выраженные формулой (I):
В представленной выше формуле (IV) R3, R4 и R5 каждый представляет собой атом водорода или алкильную группу, имеющую 1-4 атома углерода. Примерами алкильной группы являются метильная, этильная, н-пропильная, изопропильная, н-бутильная, изобутильная, втор-бутильная и трет-бутильная группы, R3, R4 и R5 могут быть одинаковыми или разными. Из водорода и указанных выше групп предпочтительными являются водород и метильная и этильная группы, причем является предпочтительным, чтобы по крайней мере один из радикалов R3, R4 и R5 был атомом водорода.The second polyvinyl ether in accordance with the present invention contains constituent units expressed by formula (I):
In the above formula (IV), R 3 , R 4 and R 5 each represents a hydrogen atom or an alkyl group having 1-4 carbon atoms. Examples of the alkyl group are methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, sec-butyl and tert-butyl groups, R 3 , R 4 and R 5 may be the same or different. Of the hydrogen and the above groups, hydrogen and methyl and ethyl groups are preferred, with it being preferred that at least one of the radicals R 3 , R 4 and R 5 be a hydrogen atom.
R6 в формуле (IV) представляет собой алкиленовую группу, имеющую 2-4 атома углерода, а более конкретно этиленовую, триметиленовую, метилэтиленовую, тетраметиленовую, 1,1-диметилэтиленовую или 1,2-диметилэтиленовую группу. Из них особенно предпочтительными являются алкиленовые группы, имеющие 2 или 3 атома углерода. В формуле (IV) k - число повторений группы R6O, среднее значение которого находится в диапазоне 0 - 10, а предпочтительно 0 - 5.R 6 in the formula (IV) is an alkylene group having 2-4 carbon atoms, and more specifically, an ethylene, trimethylene, methylene, tetramethylene, 1,1-dimethylethylene or 1,2-dimethylethylene group. Of these, alkylene groups having 2 or 3 carbon atoms are particularly preferred. In formula (IV), k is the number of repetitions of the group R 6 O, the average value of which is in the range of 0-10, and preferably 0-5.
R7 в формуле (IV) является алкильной группой, имеющей 1 - 10 атомов углерода. Примерами алкильной группы являются алкильные группы, такие, как метильная, этильная, н-пропильная, изопропильная, н-бутильная, изобутильная, втор-бутильная, трет-бутильная группа, различные виды пентильной, гексильной и октильной групп, циклоалкильные группы, такие, как циклопентильная, циклогексильная группы, различные виды метилциклогексильной, этилциклогексильной, и диметилциклогексильной групп, и т.п. группы. Из них предпочтительными являются алкильные группы, имеющие 8 или менее атомов углерода. Когда k = 0, особенно предпочтительны алкильные группы, имеющие 1-6 атомов углерода, а когда k = 1 или более, то особенно предпочтительными являются алкильные группы, имеющие 1-4 атома углерода.R 7 in the formula (IV) is an alkyl group having 1 to 10 carbon atoms. Examples of the alkyl group are alkyl groups such as methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, sec-butyl, tert-butyl group, various kinds of pentyl, hexyl and octyl groups, cycloalkyl groups, such as cyclopentyl, cyclohexyl groups, various types of methylcyclohexyl, ethylcyclohexyl, and dimethylcyclohexyl groups, and the like. groups. Of these, alkyl groups having 8 or less carbon atoms are preferred. When k = 0, alkyl groups having 1-6 carbon atoms are particularly preferred, and when k = 1 or more, alkyl groups having 1-4 carbon atoms are particularly preferred.
R3-R7 могут быть одинаковыми или разными в ряду составляющих звеньев, и когда составляющее звено содержит несколько групп R6O, то они могут быть одинаковыми или отличающимися друг от друга.R 3 -R 7 may be the same or different in the series of constituent units, and when the constituent unit contains several R 6 O groups, they may be the same or different from each other.
Необходимо, чтобы поливинилэфир в соответствии с настоящим изобретением не содержал в молекуле ненасыщенной связи и ацетальной и альдегидной стуктур. Поливинилэфир обычно имеет структуру, в которой один конец цепи выражен формулой (V):
где R8, R9 и R10 каждый - атом водорода или алкильная группа, имеющая 1-4 атома углерода, и могут быть одинаковыми или разными, R11 - алкиленовая группа, имеющая 2-4 атома углерода, R12 - алкильная группа, имеющая 1-10 атомов углерода, m - число, среднее значение которого находится в диапазоне 0-10, и несколько групп R11O могут быть одинаковыми или разными, а другой конец цепи выражен формулой (VI):
где R13, R14 и R15 каждый - атом водорода или алкильная группа, имеющая 1-4 атома углерода, и могут быть одинаковыми или разными, R16 - алкильная группа, имеющая 2-4 атома углерода, R17 - алкильная группа, имеющая 1-10 атомов углерода, n - число, среднее значение которого находится в диапазоне 0-10, и несколько групп R16O могут быть одинаковыми или отличающимися друг от друга.It is necessary that the polyvinyl ether in accordance with the present invention does not contain an unsaturated bond and acetal and aldehyde structures in the molecule. Polyvinyl ether usually has a structure in which one end of the chain is expressed by formula (V):
where R 8 , R 9 and R 10 each is a hydrogen atom or an alkyl group having 1-4 carbon atoms, and may be the same or different, R 11 is an alkylene group having 2-4 carbon atoms, R 12 is an alkyl group, having 1-10 carbon atoms, m is a number whose average value is in the range of 0-10, and several R 11 O groups can be the same or different, and the other end of the chain is expressed by formula (VI):
where R 13 , R 14 and R 15 each is a hydrogen atom or an alkyl group having 1-4 carbon atoms, and may be the same or different, R 16 is an alkyl group having 2-4 carbon atoms, R 17 is an alkyl group, having 1-10 carbon atoms, n is a number whose average value is in the range 0-10, and several R 16 O groups may be the same or different from each other.
В описанной выше формуле (V) R8, R9 и R10 каждый - атом водорода или алкильная группа, имеющая 1-4 атома углерода. Примерами алкильной группы являются те же самые группы, что представлены в качестве примеров при описании радикалов R3-R5 в формуле (IV). R8, R9 и R10 могут быть одинаковыми или разными. Из них предпочтительными являются атом водорода и метильная и этильная группы, причем является предпочтительными, чтобы по крайней мере один из радикалов R8, R9 и R10 был атомом водорода.In the above formula (V), R 8 , R 9 and R 10 are each a hydrogen atom or an alkyl group having 1-4 carbon atoms. Examples of the alkyl group are the same groups that are presented as examples in the description of the radicals R 3 -R 5 in the formula (IV). R 8 , R 9 and R 10 may be the same or different. Of these, a hydrogen atom and methyl and ethyl groups are preferred, and it is preferred that at least one of the radicals R 8 , R 9 and R 10 be a hydrogen atom.
R11 в формуле (V) представляет собой алкиленовую группу, имеющую 2-4 атома углерода. Примерами алкиленовой группы являются те же самые группы, что представлены в качестве примеров при описании R6 в формуле (IV). Из них особенно предпочтительными являются алкиленовые группы, имеющие 2 или 3 атома углерода. В формуле (V) m - число повторений группы R11O, среднее значение которого находится в диапазоне 0-10, а предпочтительно 0-5. При наличии нескольких групп R11O они могут быть одинаковыми или разными.R 11 in the formula (V) is an alkylene group having 2-4 carbon atoms. Examples of alkylene groups are the same groups that are presented as examples in the description of R 6 in the formula (IV). Of these, alkylene groups having 2 or 3 carbon atoms are particularly preferred. In the formula (V), m is the number of repetitions of the group R 11 O, the average value of which is in the range of 0-10, and preferably 0-5. In the presence of several R 11 O groups, they may be the same or different.
R12 в формуле (V) представляют собой алкильную группу, имеющую 1-10 атомов углерода. Примерами алкильной группы являются те же самые группы, что представлены в качестве примеров при описании R7 в формуле (IV). Из них предпочтительными являются алкильные группы, имеющие 8 или менее атомов углерода. Когда m= 0, особенно предпочтительны алкильные группы, имеющие 1-6 атомов углерода, а когда m=1 или более, то особенно значительными являются алкильные группы, имеющие 1-4 атома углерода.R 12 in the formula (V) is an alkyl group having 1-10 carbon atoms. Examples of the alkyl group are the same groups that are presented as examples in the description of R 7 in the formula (IV). Of these, alkyl groups having 8 or less carbon atoms are preferred. When m = 0, alkyl groups having 1-6 carbon atoms are particularly preferred, and when m = 1 or more, alkyl groups having 1-4 carbon atoms are especially significant.
В описанной выше формуле (VI) R13, R14 и R15 каждый представляет собой атом водорода или алкильную группу, имеющую 1-4 атома углерода. Примерами алкильной группы являются те же самые группы, что представлены в качестве примеров при описании R3-R5 в формуле (IV), R13, R14 и R15 могут быть одинаковыми или разными. Из них предпочтительными являются атомы водорода и метильная и этильная группы, причем является предпочтительным, чтобы крайней мере один из радикалов R13, R14 и R15 был атом водорода.In the above formula (VI), R 13 , R 14 and R 15 each represents a hydrogen atom or an alkyl group having 1-4 carbon atoms. Examples of the alkyl group are the same groups that are presented as examples in the description of R 3 -R 5 in the formula (IV), R 13 , R 14 and R 15 may be the same or different. Of these, hydrogen atoms and methyl and ethyl groups are preferred, with at least one of the radicals R 13 , R 14 and R 15 being a hydrogen atom.
R16 в формуле (VI) представляет собой алкиленовую группу, имеющую 2-4 атома углерода. Примерами алкиленовой группы являются те же самые группы, что представлены в качестве примеров при описании R6 в формуле (IV). Из них особенно предпочтительными являются алкиленовые группы, имеющие 2 или 3 атома углерода. В формуле (VI) n - число повторений группы R16O, среднее значение которого находится в диапазоне 0-10, а предпочтительно 0-5. При наличии нескольких групп R16O они могут быть одинаковыми или разными.R 16 in the formula (VI) represents an alkylene group having 2-4 carbon atoms. Examples of alkylene groups are the same groups that are presented as examples in the description of R 6 in the formula (IV). Of these, alkylene groups having 2 or 3 carbon atoms are particularly preferred. In formula (VI), n is the number of repetitions of the group R 16 O, the average value of which is in the range of 0-10, and preferably 0-5. In the presence of several R 16 O groups, they may be the same or different.
R17 в формуле (VI) представляет собой алкильную группу, имеющую 1-10 атомов углерода. Примерами алкильной группы являются те же самые группы, что представлены в качестве примеров при описании R7 в формуле (IV). Из них предпочтительными являются алкильные группы, имеющие 8 или менее атомов углерода. Когда n= 0, особенно предпочтительны алкильные группы, имеющие 1-6 атомов углерода, а когда n=1 или более, то особенно предпочтительными являются алкильные группы, имеющие 1-4 атома углерода.R 17 in the formula (VI) represents an alkyl group having 1-10 carbon atoms. Examples of the alkyl group are the same groups that are presented as examples in the description of R 7 in the formula (IV). Of these, alkyl groups having 8 or less carbon atoms are preferred. When n = 0, alkyl groups having 1-6 carbon atoms are particularly preferred, and when n = 1 or more, alkyl groups having 1-4 carbon atoms are particularly preferred.
Поливиниловый эфир в соответствии с настоящим изобретением имеет среднемассовую молекулярную массу в диапазоне 300 - 3000, предпочтительно 400-2000 и более предпочтительно 400-1000 и степень полимеризации предпочтительно в диапазоне 5-10. Отношение среднемассовой молекулярной массы к среднечисловой молекулярной массе находится в диапазоне 1,05-2,00, а предпочтительны 1,06-1,90. The polyvinyl ether in accordance with the present invention has a weight average molecular weight in the range of 300-3000, preferably 400-2000, and more preferably 400-1000, and the degree of polymerization is preferably in the range of 5-10. The ratio of the weight average molecular weight to number average molecular weight is in the range of 1.05-2.00, and 1.06-1.90 is preferred.
Предпочтительными соединениями в ряде поливиниловых эфиров в соответствии с настоящим изобретением являются соединения, которые имеют составляющие звенья, выраженные формулой (VII):
где R18 - алкильная группа, имеющая 1-4 атома углерода, и может быть одинаковым с остальными составляющими звеньями или отличающимися от них, не содержит ненасыщенной связи и ацетальной и альдегидной структур и имеет среднемассовую молекулярную массу в диапазоне 300-3000. Из них предпочтительными являются соединения, имеющие составляющие звенья, выраженные формулой (VIII):
где R18 - такой, указанный выше, и p - степень полимеризации, и среднемассовую молекулярную массу в диапазоне 300-3000, предпочтительно 400-1000.Preferred compounds in the series of polyvinyl esters in accordance with the present invention are compounds that have constituent units expressed by formula (VII):
where R 18 is an alkyl group having 1-4 carbon atoms, and may be the same with the other constituent units or different from them, does not contain an unsaturated bond and acetal and aldehyde structures and has a weight average molecular weight in the range of 300-3000. Of these, preferred are compounds having constituent units expressed by formula (VIII):
where R 18 is the one indicated above and p is the degree of polymerization and the weight average molecular weight in the range of 300-3000, preferably 400-1000.
Поливиниловый эфир в соответствии с настоящим изобретением может быть получен (a) способом полимеризации соответствующего винилэфирного мономера и (b) способом обработки олефинов, ацеталей и альдегидов в полимеризационном продукте. The polyvinyl ether in accordance with the present invention can be obtained (a) by polymerizing a suitable vinyl ester monomer and (b) by treating olefins, acetals and aldehydes in a polymerization product.
(a) Способ полимеризации
В качестве способа полимеризации может быть осуществлен способ получения простого поливинилового эфира, являющийся описанной выше второй целью настоящего изобретения.(a) Polymerization Method
As the polymerization method, a method for producing a polyvinyl ether can be carried out, which is the second objective of the present invention described above.
(b) Способ обработки
В этом способе ненасыщенные связи, ацетали и альдегиды в полимеризационном продукте преобразуют в насыщенные связи и простые эфиры.(b) Processing Method
In this method, unsaturated bonds, acetals and aldehydes in the polymerization product are converted to saturated bonds and ethers.
(1) Ненасыщенные связи
Ненасыщенные связи, образованные на конце цепи полимера путем полимеризации, могут быть преобразованы в насыщенные связи в традиционных условиях, таких, как температура реакции 20-200oC, давление водорода - 1-100 кг/см2, и в присутствии катализатора гидрирования. В качестве катализатора гидрирования предпочтительны платиновые, родиевые, рутениевые, никелевые, кобальтовые катализаторы и т.п.(1) Unsaturated bonds
Unsaturated bonds formed at the end of the polymer chain by polymerization can be converted to saturated bonds under traditional conditions, such as a reaction temperature of 20-200 ° C, a hydrogen pressure of 1-100 kg / cm 2 , and in the presence of a hydrogenation catalyst. As the hydrogenation catalyst, platinum, rhodium, ruthenium, nickel, cobalt catalysts and the like are preferred.
(2) Альдегиды
Альдегиды, образованные путем гидролиза ацеталей или сложных эфиров, произведенных от карбоновых кислот и полуацеталей, могут быть превращены в спирты посредством реакции гидрирования и затем дополнительно превращены в простые эфиры посредством синтеза Вильямсона. В частности, в качестве гидрирующего катализатора особенно предпочтительны пластиновые, палладиевые, рутениевые и никелевые катализаторы, и реакция может быть проведена при температуре 20-200oC и давлении водорода 1-100 кг/см2. Реакцию превращения в простые эфиры обычно осуществляют способом, при котором гидроксильную группу вводят во взаимодействие с щелочным металлом, таким, как металлический натрий, гидридом щелочного металла, таким, как гидрид натрия, гидроксидом щелочного металла, таким, как гидроксид натрия, или полученной из низшего спирта солью щелочного металла, такой, как метоксид натрия, для получения соли щелочного металла продукта полимеризации, после чего продукт вводят во взаимодействие с галогеналкилом или сложным эфиром сульфокислоты, соответственно имеющим 1-10 атомов углерода, или способом, при котором гидроксильную группу в продукте полимеризации превращают в сложные эфиры сульфокислоты или галогениды, после чего продукт вводят во взаимодействие с алифатическим спиртом, имеющим 1-10 атомов углерода, или его солью щелочного металла.(2) Aldehydes
Aldehydes formed by the hydrolysis of acetals or esters derived from carboxylic acids and semi-acetals can be converted to alcohols via a hydrogenation reaction and then further converted to ethers via Williamson synthesis. In particular, plate, palladium, ruthenium and nickel catalysts are particularly preferred as the hydrogenation catalyst, and the reaction can be carried out at a temperature of 20-200 ° C and a hydrogen pressure of 1-100 kg / cm 2 . The ether conversion reaction is usually carried out by a process in which a hydroxyl group is reacted with an alkali metal such as sodium metal, an alkali metal hydride such as sodium hydride, an alkali metal hydroxide such as sodium hydroxide or derived from a lower alcohol with an alkali metal salt such as sodium methoxide to obtain an alkali metal salt of the polymerization product, after which the product is reacted with halogenated or sulfonic acid ester, respectively having 1-10 carbon atoms, or a method in which the hydroxyl group in the polymerization product is converted to sulfonic acid esters or halides, after which the product is reacted with an aliphatic alcohol having 1-10 carbon atoms or an alkali metal salt thereof.
(3) Ацеталь
Ацеталь, образованный на конце цепи полимеризации, образует в результате реакции с водой в присутствии кислотного катализатора, такого, как хлористоводородная кислота, серная кислота и сульфокислота, альдегиды, которые могут быть превращены в простые эфиры описанными выше способами. Примерами способа непосредственного превращения ацеталей в простые эфиры являются способ с использованием LiAlH4-BF3, LiAlH4-AlCl3, B2H6, NaB (CN)H3-HCl или (CH3O)AlH2, способ с использованием кремниевых реагентов и т.п., которые описаны в Jikken Kagaku Koza, 4-ое издание, том 20, стр. 202 (published by Maruzen), и способ с проведением реакции в среде водорода в присутствии каталитической системы в виде сочетания оксида платины и хлористоводородной кислоты, который (способ) описан в Jan T. Karrison and Shuyen Harrison, Compendium of Organic Synthetic Methods, стр. 317 (1971).(3) Acetal
The acetal formed at the end of the polymerization chain forms, by reaction with water in the presence of an acid catalyst, such as hydrochloric acid, sulfuric acid and sulfonic acid, aldehydes, which can be converted into ethers by the methods described above. Examples of the method for directly converting acetals to ethers are a method using LiAlH 4 -BF 3 , LiAlH 4 -AlCl 3 , B 2 H 6 , NaB (CN) H 3 -HCl or (CH 3 O) AlH 2 , a method using silicon reagents and the like, which are described in Jikken Kagaku Koza, 4th edition,
Кроме того, ацетали могут быть эффективно превращены в простые эфиры способом получения простого эфира, являющимся третьей целью настоящего изобретения и включающим в себя гидрирование в присутствии твердого катализатора, обладающего кислотными свойствами и гидрирующей способностью. В качестве применяемого для реакции твердого катализатора, обладающего кислотными свойствами и гидрирующей способностью, и условий реакции могут быть использованы твердые катализаторы и условия реакции, описанные в связи с получением простого эфира. In addition, acetals can be effectively converted to ethers by the ether preparation process, which is the third objective of the present invention and includes hydrogenation in the presence of a solid catalyst having acidic properties and hydrogenating ability. Solid catalysts and reaction conditions described in connection with the preparation of an ether can be used as a solid catalyst having acidic and hydrogenating properties and reaction conditions used for the reaction.
Смазочное масло для компрессионных холодильников в соответствии с настоящим изобретением имеет превосходные совместимость с хладагентом, стабильность, электроизоляционную способность и смазочные свойства. Поэтому оно является особенно подходящим в качестве смазочного масла для компрессионных холодильников, в которых в качестве холодильного агента используют флон-134a. Lubricating oil for compression refrigerators in accordance with the present invention has excellent refrigerant compatibility, stability, electrical insulating ability and lubricating properties. Therefore, it is particularly suitable as a lubricating oil for compression refrigerators in which flon-134a is used as a refrigerant.
Способом получения поливинилового эфира в соответствии с настоящим изобретением можно, используя простые процессы, надежно, безопасно, эффективно и промышленно выгодно получить поливиниловый эфир с требуемой там степенью полимеризации, имеющий широкую область применения, например, в качестве растворителя, смазочного масла, клеящего вещества или смолы. By the method for producing polyvinyl ether in accordance with the present invention, it is possible, using simple processes, to reliably, safely, efficiently and industrially obtain polyvinyl ether with the degree of polymerization required therein, having a wide range of applications, for example, as a solvent, lubricating oil, adhesive or resin .
Способом получения простого эфира можно получить простой эфир из ацеталя или кеталя с высокой степенью превращения и высокой избирательностью, причем поскольку не возникает проблема коррозии, то можно использовать оборудование, применяемое для обычных производств. В соответствии со способом по настоящему изобретению гидрируют только ацетали и кетали, и даже когда исходный ацеталь или кеталь содержит углеводородные группы, имеющие атомы эфирного кислорода, часть эфирного кислорода остается нетронутой и ацетальная связь превращается в простую эфирную связь. By the method of producing ether, ether can be obtained from acetal or ketal with a high degree of conversion and high selectivity, and since there is no corrosion problem, equipment used for conventional production can be used. According to the method of the present invention, only acetals and ketals are hydrogenated, and even when the starting acetal or ketal contains hydrocarbon groups having ether oxygen atoms, part of the ether oxygen remains intact and the acetal bond is converted to a simple ether bond.
Далее, простой поливиниловый эфир в соответствии с настоящим изобретением содержит гомополимер или сополимер простого алкилвинилового эфира, имеющего алкильную группу с 1-3 атомами углерода, и имеет относительно низкую молекулярную массу и более узкое ее распределение, причем гомополимер или сополимер винилового мономера не имеет в молекуле ни ненасыщенных связей, ни ацетальных и альдегидных структур. Поливиниловый эфир имеет превосходную совместимость, в частности, с водородсодержащими флонами, такими, как флон-134a, превосходные стабильность и смазочные свойства и объемное собственное электрическое сопротивление при 80oC, равное 1012 Ом•см или более, и весьма пригоден для использования в качестве смазочного масла для холодильников компрессионного типа.Further, the polyvinyl ether in accordance with the present invention contains a homopolymer or copolymer of a simple vinyl vinyl ether having an alkyl group with 1-3 carbon atoms, and has a relatively low molecular weight and narrower distribution thereof, and the homopolymer or copolymer of vinyl monomer does not have in the molecule neither unsaturated bonds, nor acetal and aldehyde structures. Polyvinyl ether has excellent compatibility, in particular with hydrogen-containing flons, such as flon-134a, excellent stability and lubricating properties, and a volumetric intrinsic electrical resistance at 80 ° C. of 10 12 Ω · cm or more and is very suitable for use in as lubricating oil for compressors.
Поливинилэфир пригоден также для использования в качестве электроизолирующего агента, органического растворителя, поверхностно-активного вещества и т.п. Polyvinyl ether is also suitable for use as an electrically insulating agent, an organic solvent, a surfactant, and the like.
Далее настоящее изобретение описано более подробно со ссылками на примеры. Однако изобретение не ограничивается описанными примерами. Further, the present invention is described in more detail with reference to examples. However, the invention is not limited to the described examples.
Ниже описаны методы измерения кинематической вязкости, средней молекулярной массы, совместимости с флоном и объемного собственного электрического сопротивления и метод испытания на гидролиз поливинилового эфира. Methods for measuring kinematic viscosity, average molecular weight, compatibility with flon, and intrinsic volumetric electrical resistance and a test method for hydrolysis of polyvinyl ether are described below.
(1) Кинематическая вязкость
Кинематическую вязкость измеряли в соответствии с методом японского промышленного стандарта K-2283(1983) с использованием стеклянного капиллярного вискозиметра.(1) Kinematic viscosity
Kinematic viscosity was measured in accordance with the method of Japanese industrial standard K-2283 (1983) using a glass capillary viscometer.
(2) Средняя молекулярная масса (примеры 8-25 и 25A)
Используя прибор и условия, описанные ниже, измеряли среднемассовую и среднечисловую молекулярные массы и по результатам измерений определяли дисперсность (отношение среднемассовой молекулярной массы к среднечисловой молекулярной массе)
Прибор: изделие "Ниппон Банко Когио Ко, Лтд" 880-PU (насос)
Шодекс RI SE-61 (детектор)
Колонка: TSK H8 + G 2000 H8 + G 1000 H8
Температура: комнатная
Растворитель: ТГФ (тетрагидрофуран)
Скорость элюирования: 1,4 мл/мин
Стандартное вещество: полиэтиленгликоль
(3) Испытание на совместимость
(а) флон-134a.(2) Average molecular weight (examples 8-25 and 25A)
Using the device and the conditions described below, the mass average and number average molecular weights were measured and the dispersion (the ratio of the mass average molecular weight to the number average molecular weight) was determined from the measurement results
Device: product "Nippon Banco Kogio Co., Ltd." 880-PU (pump)
Shodeks RI SE-61 (detector)
Column: TSK H8 +
Temperature: room
Solvent: THF (tetrahydrofuran)
Elution Rate: 1.4 ml / min
Standard substance: polyethylene glycol
(3) Compatibility Test
(a) flon-134a.
В стойкую к давлению стеклянную ампулу загружали образец в заданном количестве, установленном так, чтобы оно составляло 5 вес.% или 10 вес.% от флона -134a, (1,1,1,2-тетрафторэтан), и ампулу соединяли с вакуумной линией и с линией для газообразного флона -134a. Ампулу дегазировали в вакууме при комнатной температуре, охлаждали жидким азотом, а затем вводили в нее заданное количество флона-134. После этого ампулу запаивали и измеряли температуру начала разделения фаз следующим образом. Для измерения совместимости при низких температурах образец медленно охлаждали до комнатной температуры до -60oC в термостате, а для измерения совместимости при высоких температурах образец медленно нагревали от комнатной температуры до +80oC. Является предпочтительным, чтобы температура фазового разделения была более низкой в области низких температур, но более высокой в области высоких температур.The sample was loaded into a pressure-resistant glass ampoule in a predetermined amount, set to be 5 wt.% Or 10 wt.% From -134a flon (1,1,1,2-tetrafluoroethane), and the ampoule was connected to a vacuum line and with the line for gaseous flon-134a. The ampoule was degassed in vacuo at room temperature, cooled with liquid nitrogen, and then a predetermined amount of flon-134 was introduced into it. After this, the ampoule was sealed and the temperature of the onset of phase separation was measured as follows. To measure compatibility at low temperatures, the sample was slowly cooled to room temperature to -60 o C in a thermostat, and to measure compatibility at high temperatures, the sample was slowly heated from room temperature to +80 o C. It is preferred that the phase separation temperature be lower at low temperatures, but higher in high temperatures.
(b) Флон-32
В стойкую к давлению стеклянную ампулу загружали образец в заданном количестве, установленном так, чтобы оно составляло 10 вес.% или 20 вес.% от флона-32 (дифторметан), и ампулу соединяли с вакуумной линией и с линией газообразного флона-32. Ампулу дегазировали в вакууме при комнатной температуре охлаждали жидким азотом, а затем вводили в нее заданное количество флона-32. После этого ампулу запаивали и измеряли температуру начала разделения фаз следующим образом. Для измерения совместимости при низких температурах образец медленно охлаждали до комнатной температуры в термостате, а для измерения совместимости при высоких температурах образец медленно нагревали от комнатной температуры до +40oC. Является предпочтительным, чтобы температура фазового разделения была более низкой в области низких температур, но более высокой в области высоких температур.(b) Flon-32
The sample was loaded into a pressure-resistant glass ampoule in a predetermined amount, set so that it was 10 wt.% Or 20 wt.% Of flon-32 (difluoromethane), and the ampoule was connected to a vacuum line and to a line of gaseous flon-32. The ampoule was degassed in vacuo at room temperature, cooled with liquid nitrogen, and then a predetermined amount of flon-32 was introduced into it. After this, the ampoule was sealed and the temperature of the onset of phase separation was measured as follows. To measure compatibility at low temperatures, the sample was slowly cooled to room temperature in a thermostat, and to measure compatibility at high temperatures, the sample was slowly heated from room temperature to +40 o C. It is preferable that the phase separation temperature be lower at low temperatures, but higher at high temperatures.
(4) Объемное собственное электрическое сопротивление
Образец высушивали под пониженным давлением (0,3-0,8 мм рт.столба) при 100oC в течение 1 часа и затем погружали в предназначенный для измерения объемного собственного сопротивления сосуд для жидкости, который помещали в термостат при 80oC. После выдерживания образец в термостате при 80oC в течение 40 минут измеряли объемное собственное сопротивление при приложенном напряжении 250 В с использованием измерителя сверхвысокого удельного сопротивления изоляции типа Р8340 (торговая марка) производства ф. "Адвантест Ко".(4) Volume intrinsic electrical resistance
The sample was dried under reduced pressure (0.3-0.8 mm Hg) at 100 o C for 1 hour and then immersed in a vessel for measuring the volumetric intrinsic resistance of the liquid, which was placed in a thermostat at 80 o C. After holding the sample in a thermostat at 80 o C for 40 minutes, the volumetric intrinsic resistance was measured at an applied voltage of 250 V using an ultrahigh specific resistance meter of type P8340 (trademark) manufactured by f. Advantest Co.
(5) Испытание на гидролиз
В стойкую к давлению склянку емкостью 250 мл помещали 75 г образца 25 г воды и кусочек меди (13 х 50 мм) и среду в склянке заменяли азотом. Образец выдерживали во вращающемся термостате при температуре 102oC в течение 192 часов. После завершения испытания визуально обследовали внешний вид образца и состояние кусочка меди, а также измеряли общее кислотное число.(5) Hydrolysis Test
75 g of a sample of 25 g of water and a piece of copper (13 x 50 mm) were placed in a pressure-resistant flask with a capacity of 250 ml and the medium in the flask was replaced with nitrogen. The sample was kept in a rotating thermostat at a temperature of 102 o C for 192 hours. After completion of the test, the appearance of the sample and the condition of the piece of copper were visually examined, and the total acid number was measured.
Пример 1 приготовления
В колбу загружали 100 г (с водой) никеля Ренея (М300Т, производство ф. "Кавакен файн кемикал Ко, Лтд") и к нему добавляли 100 г абсолютного этанола при достаточном перемешивании. Смесь отстаивали для осаждения никеля Ренея, после чего удаляли супернатант путем декантации. Оставшийся в колбе никель Ренея обрабатывали так же, как описано выше, еще 5 раз. Полученный в этом примере приготовления никель Ренея использовали в примерах, смочив его этанолом.Preparation Example 1
100 g (with water) of Raney Nickel (M300T, manufactured by Kawaken Fine Chemical Co., Ltd.) was charged into a flask and 100 g of absolute ethanol was added to it with sufficient stirring. The mixture was sedimented to precipitate Raney nickel, after which the supernatant was removed by decantation. The remaining Raney nickel in the flask was treated as described above, another 5 times. Obtained in this preparation example, Raney nickel was used in the examples, moistened with ethanol.
Пример 2 приготовления
В грушевидную колбу емкостью 100 мл помещали 20 г цеолита (HSZ330HUA, производство ф. "Тосо Ко, Лтд) затем колбу погружали в масляную ванну при 150oC и откачивали из нее воздух посредством масляного ротационного вакуумного насоса в течение 1 часа. После охлаждения до комнатной температуры в колбе восстанавливали атмосферное давление путем введения сухого азота. Используемые в примерах цеолиты - это те, что получены в этом примере приготовления.Preparation Example 2
20 g of zeolite (HSZ330HUA, manufactured by Toso Co., Ltd.) were placed in a pear-shaped flask with a capacity of 100 ml, then the flask was immersed in an oil bath at 150 ° C and air was pumped out of it by means of an oil rotary vacuum pump for 1 hour. At room temperature, atmospheric pressure was restored in the flask by introducing dry nitrogen.The zeolites used in the examples are those obtained in this preparation example.
Пример 3 приготовления
В грушевидную колбу емкостью 100 мл помещали 20 г активированной глины (продукт ф. "Вако джан-яку Ко, Лтд). Затем колбу погружали в масляную ванну при 150oC и откачивали из нее воздух посредством масляного ротационного вакуумного насоса в течение 1 часа. После охлаждения до комнатной температуры в колбе восстанавливали атмосферное давление путем введения сухого азота. Используемые в примерах активированные глины - это те, что получены в данном примере приготовления.Preparation Example 3
20 g of activated clay (product of Wako jan-yaku Co., Ltd.) was placed in a 100 ml pear-shaped flask. The flask was then immersed in an oil bath at 150 ° C and air was pumped out of it by means of an oil rotary vacuum pump for 1 hour. After cooling to room temperature, atmospheric pressure was restored in the flask by introducing dry nitrogen.The activated clays used in the examples are those obtained in this preparation example.
Пример 1
В 5-литровую стеклянную колбу, снабженную капельной воронкой, холодильником и мешалкой, загружали 600 г простого этилвинилового эфира, 72 г метанола и 2400 г гексана и охлаждали водой при перемешивании. Когда температура достигала 5oC, добавляли раствор, приготовленный путем растворения 3,6 г диэтилэфирата трифторида бора в 20 г тетрагидрофурана, и смесь перемешивали в течение 1 часа. В течение этого периода начиналась реакция и температура реакционной жидкости повышалась, причем наблюдалось обратное стекание этилвинилового эфира в холодильнике. Реакционную смесь переносили в промывочный сосуд и промывали ее 1500 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза, а затем 1500 мл воды 3 раза. Продукт концентрировали, используя роторным испарителем, и высушивали при пониженном давлении (0,2 мм рт. ст.) при 50oC в течение 1 часа, получив в результате 468 г сырого (неочищенного) продукта.Example 1
In a 5 liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, 600 g of ethyl vinyl ether, 72 g of methanol and 2400 g of hexane were charged and cooled with water with stirring. When the temperature reached 5 ° C., a solution prepared by dissolving 3.6 g of boron trifluoride diethyl etherate in 20 g of tetrahydrofuran was added, and the mixture was stirred for 1 hour. During this period, the reaction began and the temperature of the reaction liquid increased, and the reverse flow of ethyl vinyl ether in the refrigerator was observed. The reaction mixture was transferred to a washing vessel and washed with 1500 ml of a 3% (by weight) aqueous solution of
В 5-литровую стеклянную колбу, снабженную капельной воронкой, холодильником и мешалкой, загружали 400 г неочищенного продукта, полученного так, как описано выше, 500 г ацетона, 800 г воды и 10 г концентрированной хлористоводородной кислоты (35 мас. %) и смесь перемешивали при 50-60oC в течение 3 часов. После нейтрализации хлористоводородной кислоты гидрокарбонатом натрия удаляли ацетон и т.п. под пониженным давление, используя роторный испаритель, и оставшийся продукт выливали в 400 мл гексана. После удаления водной фазы продукт промывали 400 мл воды один раз. Гексановую фазу переносили в автоклав и гидрировали, использовав 0,8 г оксида платины в качестве катализатора, при давлении водорода 20 кг/см2 и 50oC в течение 1 часа. После удаления оксида платины путем фильтрования продукт переносили в 2-литровую стеклянную колбу, добавляли 40 г метанола и 8 г борогидрида натрия и перемешивали в течение 1 часа при комнатной температуре. Продукт слабо подкисляли водным раствором уксусной кислоты, после чего производили нейтрализацию уксусной кислоты гидрокарбонатом натрия. Промывали продукт один раз 400 мл воды и удаляли растворитель и воду под пониженным давлением, использовав для этого роторный испаритель.400 g of a crude product obtained as described above, 500 g of acetone, 800 g of water and 10 g of concentrated hydrochloric acid (35 wt.%) Were charged into a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, and the mixture was stirred at 50-60 o C for 3 hours. After neutralization of hydrochloric acid with sodium bicarbonate, acetone and the like were removed. under reduced pressure using a rotary evaporator and the remaining product was poured into 400 ml of hexane. After removal of the aqueous phase, the product was washed with 400 ml of water once. The hexane phase was transferred to an autoclave and hydrogenated using 0.8 g of platinum oxide as a catalyst at a hydrogen pressure of 20 kg / cm 2 and 50 ° C. for 1 hour. After removing platinum oxide by filtration, the product was transferred to a 2 liter glass flask, 40 g of methanol and 8 g of sodium borohydride were added and stirred for 1 hour at room temperature. The product was slightly acidified with an aqueous solution of acetic acid, after which the acetic acid was neutralized with sodium bicarbonate. The product was washed once with 400 ml of water and the solvent and water were removed under reduced pressure using a rotary evaporator.
Полученный в результате остаточный продукт растворяли в 300 мл тетрагидрофурана и проводили реакцию с 12 г гидрида натрия в течение 1 часа. Во время этой реакции наблюдалось выделение газообразного водорода. Затем к реакционной смеси добавляли по каплям в течение 30 минут 120 г метилиодида. В течение этого периода наблюдалось выделение тепла. После капельного добавления метилиодида реакционную смесь перемешивали еще 1 час. Использовав роторный испаритель, удаляли под пониженным давлением растворитель и непрореагировавшие материалы. Остаток переносили в 2-литровый промывочный сосуд и после растворения в 400 мл гексана промывали 400 мл воды 5 раз. Затем, добавив 40 г ионообменной смолы, продукт перемешивали 3 часа. Из продукта удаляли ионообменную смолу путем фильтрования и гексан под пониженным давлением посредством роторного испарителя. Выход полученного описанным образом поливинилового эфира составил 200 г. The resulting residual product was dissolved in 300 ml of tetrahydrofuran and reacted with 12 g of sodium hydride for 1 hour. During this reaction, evolution of hydrogen gas was observed. Then, 120 g of methyl iodide was added dropwise to the reaction mixture over 30 minutes. During this period, heat was observed. After dropwise addition of methyl iodide, the reaction mixture was stirred for another 1 hour. Using a rotary evaporator, the solvent and unreacted materials were removed under reduced pressure. The residue was transferred to a 2 liter washing vessel and, after dissolving in 400 ml of hexane, washed with 400 ml of
Были получены спектр ядерного магнитного резонанса (далее сокращено ЯМР) и спектр инфракрасного излучения (далее сокращено ИК) продукта, которые подтвердили, что одной из концевых структур полимера была структура (A), а другой -(B):
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное электрическое сопротивление и стойкость к гидролизу полимера простого этилвинилового эфира.A nuclear magnetic resonance spectrum (hereinafter referred to as NMR) and an infrared spectrum (hereinafter referred to as IR) of the product were obtained, which confirmed that one of the terminal structures of the polymer was structure (A) and the other (B):
Kinematic viscosity, flon compatibility, intrinsic electrical resistance, and hydrolysis resistance of the ethyl vinyl ether polymer were measured.
Результаты показаны в табл. 1 (см в конце описания). The results are shown in table. 1 (see end of description).
Пример 2
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 600 г этилвинилового эфира, 60 г метанола и 2400 г гексана и охлаждали водой при перемешивании. Когда температура достигала 5oC, добавляли раствор, приготовленный путем растворения 3,6 г диэтилэфирата трифторида бора в 20 г тетрагидрофурана, и смесь перемешивали 1 час. В течение этого периода начиналась реакция и повышалась температура реакции, причем в холодильнике наблюдалось обратное стекание этилвинилового эфира. Реакционную смесь переносили в промывочный сосуд и промывали 1500 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза, а затем 1500 мл воды 3 раза. Продукт концентрировали с помощью роторного испарителя и высушивали под пониженным давлением (0,2 мм рт. ст.) при 50oC в течение 1 часа, получив в результате 452 г неочищенного продукта.Example 2
600 g of ethyl vinyl ether, 60 g of methanol and 2400 g of hexane were charged into a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, and cooled with stirring with water. When the temperature reached 5 ° C., a solution prepared by dissolving 3.6 g of boron trifluoride diethyl etherate in 20 g of tetrahydrofuran was added, and the mixture was stirred for 1 hour. During this period, the reaction began and the reaction temperature increased, and in the refrigerator, the reverse flow of ethyl vinyl ether was observed. The reaction mixture was transferred to a washing vessel and washed with 1500 ml of a 3% (by weight) aqueous solution of
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 400 г полученного так, как описано выше, неочищенного продукта, 500 г ацетона, 800 г и 10 г концентрированной хлористоводородной кислоты (35 мас.%) и перемешивали при 50-60oC в течение 3 часов. После нейтрализации хлористоводородной кислоты гидрокарбонатом натрия удаляли под пониженным давлением ацетон и т.п., использовав для этого роторный испаритель, и оставшийся продукт выливали в 400 мл гексана. После удаления водной фазы продукт промывали один раз 400 мл воды. Гексановую фазу переносили в автоклав и гидрировали с использованием 0,8 г оксида платины в качестве катализатора при давлении водорода 20 кг/см2 и 50oC в течение 1 часа. После удаления оксидно-платинового катализатора путем фильтрования продукт переносили в 2-литровую стеклянную колбу, добавляли 40 г метанола и 8 г борогидрида натрия и перемешивали 1 час при комнатной температуре. Продукт слабо подкисляли водным раствором уксусной кислоты, после чего нейтрализовали уксусную кислоту гидрокарбонатом натрия. Продукт промывали один раз 400 мл воды и с помощью роторного испарителя удаляли под пониженным давлением растворитель и воду.400 g of the crude product obtained as described above, 500 g of acetone, 800 g and 10 g of concentrated hydrochloric acid (35 wt.%) Were charged into a 5-liter glass flask equipped with a dropping funnel, refrigerator and stirrer and stirred at 50 -60 o C for 3 hours. After neutralization of hydrochloric acid with sodium bicarbonate, acetone and the like were removed under reduced pressure using a rotary evaporator, and the remaining product was poured into 400 ml of hexane. After removal of the aqueous phase, the product was washed once with 400 ml of water. The hexane phase was transferred to an autoclave and hydrogenated using 0.8 g of platinum oxide as a catalyst at a hydrogen pressure of 20 kg / cm 2 and 50 ° C. for 1 hour. After removal of the platinum oxide catalyst by filtration, the product was transferred to a 2 liter glass flask, 40 g of methanol and 8 g of sodium borohydride were added and stirred for 1 hour at room temperature. The product was slightly acidified with an aqueous solution of acetic acid, after which the acetic acid was neutralized with sodium bicarbonate. The product was washed once with 400 ml of water, and the solvent and water were removed under reduced pressure using a rotary evaporator.
Полученный описанным выше образом остаточный продукт растворяли в 300 мл тетрагидрофурана и проводили реакцию с 12 г гидрида натрия в течение 1 часа. Во время этой реакции наблюдалось выделение газообразного водорода. Затем в реакционную смесь добавляли по каплям в течение 30 минут 120 г метилиодида. В течение этого периода наблюдалось выделение тепла. После капельного добавления метилиодида реакционную смесь перемешивали еще 1 час. Использовав роторный испаритель, удаляли под пониженным давлением растворитель и непрореагировавшие материалы. Остаток переносили в 2-литровый промывочный сосуд и после растворения в 400 мл гексана промывали 400 мл воды 5 раз. Затем, добавив 40 г ионообменной смолы, продукт перемешивали 3 часа. Удалив из продукта ионообменную смолу путем фильтрования, удаляли под пониженным давлением гексан с использованием роторного испарителя. Выход полученного в результате поливинилового эфира составлял 208 г. Были получены ЯМР- и ИК- спектры продукта, которые показали, что одной из концевых структур полимера была структура (A), а другой -(B). The residual product obtained as described above was dissolved in 300 ml of tetrahydrofuran and the reaction was carried out with 12 g of sodium hydride for 1 hour. During this reaction, evolution of hydrogen gas was observed. Then, 120 g of methyl iodide was added dropwise to the reaction mixture over 30 minutes. During this period, heat was observed. After dropwise addition of methyl iodide, the reaction mixture was stirred for another 1 hour. Using a rotary evaporator, the solvent and unreacted materials were removed under reduced pressure. The residue was transferred to a 2 liter washing vessel and, after dissolving in 400 ml of hexane, washed with 400 ml of
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полимера этилвинилового эфира. Результаты показаны в таблице 1. Kinematic viscosity, flon compatibility, intrinsic resistance and hydrolysis resistance of the ethyl vinyl ether polymer were measured. The results are shown in table 1.
Пример 3
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 500 г гексана, к нему добавляли раствор, приготовленный путем растворения 12 г диэтилового трифторида бора в 24 г тетрагидрофурана, и смесь охлаждали до 5oC в ванне с ледяной водой. В капельную воронку загружали 2000 г этилвинилового эфира и 120 г метанола и позволяли смеси капать в течение 1 часа 30 минут. В течение этого периода начиналась реакция и повышалась температура реакционной смеси. Температуру поддерживали на уровне примерно 30oC путем охлаждения посредством ванны с ледяной водой. После окончания капания продолжали перемешивание еще 30 минут. Реакционную смесь переносили в промывочный сосуд и промывали 1500 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза, а затем 1500 мл воды 3 раза. Посредством роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие материалы, получив в результате 1806 г неочищенного продукта.Example 3
500 g of hexane was charged into a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, a solution prepared by dissolving 12 g of boron diethyl trifluoride in 24 g of tetrahydrofuran was added, and the mixture was cooled to 5 ° C in an ice water bath . 2000 g of ethyl vinyl ether and 120 g of methanol were charged into a dropping funnel and the mixture was allowed to drip for 1 hour 30 minutes. During this period, the reaction began and the temperature of the reaction mixture increased. The temperature was maintained at about 30.degree . C. by cooling with an ice water bath. After completion of the dripping, stirring was continued for another 30 minutes. The reaction mixture was transferred to a washing vessel and washed with 1500 ml of a 3% (by weight) aqueous solution of
В 2-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 400 г сырого продукта, полученного описанным выше образом, и 300 г тетрагидрофурана и затем добавляли 15 г алюмогидрида лития с последующим перемешиванием в течение 30 минут. В капельную воронку загружали 196 г диэтилэфирата трифторида бора и давали ему возможность капать в течение 1 часа. Во время капания наблюдалось выделение тепла, и температуру поддерживали на уровне 10-20oC путем охлаждения в ванне с ледяной водой. После окончания капания реакционную смесь перемешивали еще 30 минут, после чего нейтрализовали путем добавления гидроксида натрия. Полученный в результате осадок удаляли путем фильтрования, а жидкую фазу обрабатывали в роторном испарителе для удаления образованного спирта, растворителя и воды под пониженным давлением. Оставшийся продукт переносили в 2-литровый промывной сосуд и растворяли в 500 мл гексана. Раствор промывали 200 мл 5%-ного (по массе) водного раствора гидроксида натрия 10 раз и затем 200 мл воды 3 раза. К раствору добавили 100 г ионообменной смолы, и смесь перемешивали в течение 3 часов. После удаления ионообменной смолы путем фильтрования удаляли под пониженным давлением гексан с использованием для этого роторного испарителя. Выход полимера этилвинилового эфира составлял 235 г. ЯМР- и ИК- спектры продукта показали, что одной из концевых структур полимера была структура (A), а другой - смесь структур (B) и (C):
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу. Результаты показаны в таблице 1.In a 2 liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, 400 g of the crude product obtained as described above and 300 g of tetrahydrofuran were charged and then 15 g of lithium aluminum hydride was added, followed by stirring for 30 minutes. 196 g of boron trifluoride diethyl etherate was charged into a dropping funnel and allowed to drip for 1 hour. Heat was observed during the dripping, and the temperature was maintained at 10-20 ° C. by cooling in an ice water bath. After the completion of the dripping, the reaction mixture was stirred for another 30 minutes, after which it was neutralized by adding sodium hydroxide. The resulting precipitate was removed by filtration, and the liquid phase was treated in a rotary evaporator to remove the formed alcohol, solvent and water under reduced pressure. The remaining product was transferred to a 2 liter washing vessel and dissolved in 500 ml of hexane. The solution was washed with 200 ml of a 5% (by weight) aqueous
Kinematic viscosity, flon compatibility, intrinsic volume resistance, and hydrolysis resistance were measured. The results are shown in table 1.
Пример 4
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 500 г диэтилацеталя ацетальдегида и 5,0 г диэтилэфирата трифторида бора. В капельную воронку загружали 2500 г этилвинилового эфира и позволяли ему капать в течение 1 часов 30 минут. В течение этого периода начиналась реакция, и температура реакционной смеси повышалась. Температуру поддерживали на уровне примерно 25oC охлаждения в ванне с ледяной водой. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. С помощью роторного испарителя под пониженным давлением растворитель и непрореагировавшие сырьевые материалы, получив в результате 2833 г неочищенного продукта.Example 4
1000 g of toluene, 500 g of acetaldehyde diethyl acetal and 5.0 g of boron trifluoride diethyl etherate were charged into a 5 liter glass flask equipped with a dropping funnel, refrigerator and stirrer. 2500 g of ethyl vinyl ether was charged into a dropping funnel and allowed to drip for 1 hour 30 minutes. During this period, the reaction began, and the temperature of the reaction mixture increased. The temperature was maintained at about 25 ° C. cooling in an ice water bath. After dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 1000 ml of a 5% (by weight) aqueous solution of
В автоклав загружали 600 г неочищенного продукта, 600 г гексана, 60 г никеля Ренея и 60 г цеолита. Вводили в автоклав водород, давление которого регулировали до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, давление которого регулировали до 20 кг/см2, и после перемешивания в течение примерно 30 секунд сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. Реакцию проводили при 130oC в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 100 мл гексана дважды. Промывную и реакционную жидкость объединяли друг с другом и фильтровали через фильтровальную бумагу. Объединенную жидкость переносили затем в промывной сосуд и промывали 500 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 500 мл дистиллированной воды 5 раз. Посредством роторного испарителя удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 468 г.600 g of crude product, 600 g of hexane, 60 g of Raney nickel and 60 g of zeolite were charged into an autoclave. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, the pressure of which was regulated to 20 kg / cm 2 , and after stirring for about 30 seconds it was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. The reaction was carried out at 130 o C for 1 hour. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 100 ml of hexane twice. The wash and reaction liquid were combined with each other and filtered through filter paper. The combined liquid was then transferred to a washing vessel and washed with 500 ml of a 5% (by weight) aqueous solution of
ЯМР- ИК- спектры продукта показали, что одной из концевых структур полимера была структура (A), а другой - смесь (C) и (D), в которой (C) была основной структурой, в (D) - второстепенной. NMR-IR spectra of the product showed that one of the terminal structures of the polymer was structure (A), and the other was a mixture of (C) and (D), in which (C) was the main structure, in (D) it was secondary.
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полимера этилвинилового эфира. Результаты показаны в таблице 1.
Kinematic viscosity, flon compatibility, intrinsic resistance and hydrolysis resistance of the ethyl vinyl ether polymer were measured. The results are shown in table 1.
Пример 5
Использовав катализатор, уловленный путем декантации в примере 4, проводили реакцию с 600 г неочищенного продукта, полученного в примере 4, таким образом, как в примере 4. Выход составлял 501 г. Это показало, что катализатор может быть использован повторно.Example 5
Using the catalyst trapped by decantation in Example 4, a reaction was carried out with 600 g of the crude product obtained in Example 4, as in Example 4. The yield was 501 g. This showed that the catalyst could be reused.
ЯМР- и ИК- спектры продукта показали, сто одной из концевых структур полимера была структура (A), а другой - смесь (C) и (D), в которой (C) была основной структурой, а (D) - второстепенной. The NMR and IR spectra of the product showed that one of the terminal structures of the polymer was structure (A), and the other was a mixture of (C) and (D), in which (C) was the main structure and (D) was secondary.
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полимера этилвинилового эфира. Kinematic viscosity, flon compatibility, intrinsic resistance and hydrolysis resistance of the ethyl vinyl ether polymer were measured.
Пример 6
В стеклянную колбу емкостью 1 литр, снабженную капельной воронкой, холодильником и мешалкой, загружали 250 г толуола, 36,82 г изопропилового спирта и 4,35 г диэтилэфирата трифторида бора. В капельную воронку загружали 500 г изопропилвинилового эфира, который выдавали по каплям за 30 минут. В течение этого периода начиналась реакция, и повышалась температура реакционного раствора. Температуру выдерживали на уровне примерно 30oC путем охлаждения в ванне с ледяной водой. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 130 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 200 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие сырьевые материалы, получив в результате 475,3 г неочищенного продукта.Example 6
A 1 liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 250 g of toluene, 36.82 g of isopropyl alcohol and 4.35 g of boron trifluoride diethyl ether. 500 g of isopropyl vinyl ether was charged into a dropping funnel, which was added dropwise in 30 minutes. During this period, the reaction began, and the temperature of the reaction solution increased. The temperature was maintained at about 30 ° C. by cooling in an ice water bath. After dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 130 ml of a 3% by weight aqueous solution of
В автоклав загружали 380 г неочищенного продукта, 100 г гексана, 45 г никеля Ренея и 45 г цеолита. Вводили в автоклав водород, давление которого регулировали до 20 кг/см2. после перемешивания в течение примерно 30 секунд давление сбрасывали. Вновь вводили водород в автоклав, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление сбрасывали. Повторив эту операцию еще раз давление водорода повышали до 50 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. Проводили реакцию при 130oC в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом наблюдалось падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа, и отделяли реакционную жидкость путем декантации. Катализатор промывали 100 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Катализатор можно было использовать повторно. Объединенную жидкость переносили затем в промывной сосуд и промывали 200 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 200 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под пониженным давлением гексан, воду и т.п.380 g of crude product, 100 g of hexane, 45 g of Raney nickel and 45 g of zeolite were charged into an autoclave. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 20 kg / cm 2 . after stirring for about 30 seconds, the pressure was released. Hydrogen was reintroduced into the autoclave, providing a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the pressure was released. Repeating this operation once again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. The reaction was carried out at 130 ° C. for 1 hour. The reaction proceeded during and after an increase in temperature, and a pressure drop was observed. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour, and the reaction liquid was separated by decantation. The catalyst was washed with 100 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. The catalyst could be reused. The combined liquid was then transferred to a washing vessel and washed with 200 ml of a 5% (by weight) aqueous solution of
Выход составлял 287 г. The yield was 287 g.
ЯМР и ИК-спектры показали, что одной из концевых структур была структурой (E), а другой - смесь (F) и (D), в которой (F) была основной структурой, а (D) - второстепенной. NMR and IR spectra showed that one of the terminal structures was structure (E), and the other was a mixture of (F) and (D), in which (F) was the main structure, and (D) was the secondary structure.
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полимера изопропилвинилового эфира. Результаты показаны в таблице 1.
Kinematic viscosity, flon compatibility, intrinsic resistance and hydrolysis resistance of isopropyl vinyl ether polymer were measured. The results are shown in table 1.
Пример 7
В автоклав емкостью 1 литр загружали 200 г толуола, 5,5 г метанола и 1,2 г диэтилфирата трифторида бора и атмосферу в автоклаве заменяли азотом. Перемешивая содержимое автоклава, добавляли в него под давлением 200 г метилвинилового эфира в течение 4 часов. В течение этого периода начиналась реакция, и происходило выделение тепла. Реакцию проводили, поддерживая температуру в автоклаве на уровне примерно 5oC путем охлаждения автоклава в ванне с ледяной водой. После окончания добавления метилвинилового эфира под давлением раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 100 мл 5%- (по массе) водного раствора гидроксида натрия 3 раза и затем 100 мл воды 3 раза. Посредством роторного испарителя удаляли растворитель и непрореагировавшие исходные материалы, получив в результате 165 г неочищенного продукта.Example 7
200 g of toluene, 5.5 g of methanol and 1.2 g of boron trifluoride diethyl etherate were charged into a 1 liter autoclave and the atmosphere in the autoclave was replaced with nitrogen. While stirring the contents of the autoclave, 200 g of methyl vinyl ether was added thereto over 4 hours. During this period, the reaction began and heat was released. The reaction was carried out while maintaining the temperature in the autoclave at about 5 ° C. by cooling the autoclave in an ice water bath. After the completion of the addition of methyl vinyl ether under pressure, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 100 ml of a 5% - (by weight) aqueous solution of
В автоклав загружали 165 г неочищенного продукта, 200 г гексана 15 г никеля Ренея и 15 г цеолита. Вводили в автоклав водород, давление которого регулировали до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород с обеспечением давления водорода 20 кг/см2 и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, повышали давление водорода до 50 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. Реакцию проводили при 130oC в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом наблюдалось падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддерживание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 50 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Удаляли под пониженным давлением гексан, пользуясь роторным испарителем, и добавляли 300 г хлороформа. Затем жидкость переносили в промывной сосуд и промывали ее 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 100 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под пониженным давлением хлороформ, воду и т.п.165 g of crude product, 200 g of hexane, 15 g of Raney nickel and 15 g of zeolite were charged into an autoclave. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave with a hydrogen pressure of 20 kg / cm 2 and after stirring for about 30 seconds, the hydrogen pressure was relieved. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. The reaction was carried out at 130 o C for 1 hour. The reaction proceeded during and after an increase in temperature, and a pressure drop was observed. The pressure increase with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby maintaining the hydrogen pressure during the reaction at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 50 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. Hexane was removed under reduced pressure using a rotary evaporator, and 300 g of chloroform was added. Then the liquid was transferred into a washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
Выход составил 150 г. The yield was 150 g.
ЯМР и ИК-спектры продукта подтвердили, что одной из концевых структур полимера была структура (G), а другой - смесь (B) и (D), в которой (B) была основной структурой, а (D) - второстепенной. The NMR and IR spectra of the product confirmed that one of the terminal structures of the polymer was structure (G), and the other was a mixture of (B) and (D), in which (B) was the main structure and (D) was the secondary structure.
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полимера метилвинилового эфира. Результаты показаны в таблице 1.
Kinematic viscosity, flon compatibility, intrinsic resistance and hydrolysis resistance of the methyl vinyl ether polymer were measured. The results are shown in table 1.
Пример 7A
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 500 г диэтилацеталя ацетальдегида и 5,0 диэтилэфирата трифторида бора. В капельную воронку загружали 2500 г этилвинилового эфира и выдавали его по каплям за 2 часа 30 минут. В течение этого периода начиналась реакция, и температура реакционного раствора повышалась. Путем охлаждения в ванне с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие материалы, получив в результате 2833 г неочищенного продукта.Example 7A
In a 5 liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, 1000 g of toluene, 500 g of acetaldehyde diethyl acetal and 5.0 boron trifluoride diethyl etherate were charged. 2500 g of ethyl vinyl ether was charged into a dropping funnel and dispensed dropwise in 2 hours 30 minutes. During this period, the reaction began, and the temperature of the reaction solution increased. By cooling in an ice water bath, the temperature was maintained at about 25 ° C. After completion of the dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 1000 ml of a 5% (by weight) aqueous solution of
ЯМР и ИК-спектры показали, что одной из концевых структур полимера была структура (A), а другой - смесь (H) и (I), в которой отношение (H)/(I) составляло 1/4,5. NMR and IR spectra showed that one of the terminal structures of the polymer was structure (A), and the other was a mixture of (H) and (I), in which the ratio (H) / (I) was 1 / 4.5.
Пример 7B
В двухлитровый автоклав, изготовленный из SUS-316L, загружали 700 г полимера этилвинилового эфира, полученного в примере 7A, 35 г никеля Ренея, 35 г цеолита и 1,5 г воды. Вводили в автоклав водород, давление которого регулировали до 10 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Вновь вводили в автоклав водород, обеспечивая его давление 10 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 35 кг/см2 и повышали температуру до 140oC за 30 минут при перемешивании. При 140oC реакцию проводили в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и понижение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 35 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры, и снижали давление до атмосферного. Продукт реакции фильтровали через фильтровальную бумагу. Затем продукт реакции переносили в 2-литровый промывной сосуд, разбавляли 300 г гексана и промывали 250 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 250 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 550 г. ЯМР и ИК-спектры продукта показали, что одной из концевых структур полимера была структура (A), а другой - смесь (C) и (D).
Example 7B
In a two-liter autoclave made from SUS-316L, 700 g of the ethyl vinyl ether polymer obtained in Example 7A, 35 g of Raney nickel, 35 g of zeolite and 1.5 g of water were charged. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 10 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Hydrogen was reintroduced into the autoclave, providing a pressure of 10 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 35 kg / cm 2 and the temperature was raised to 140 o C for 30 minutes with stirring. At 140 ° C., the reaction was carried out for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the decrease in pressure as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 35 kg / cm 2 . After the reaction, the reaction mixture was cooled to room temperature, and the pressure was reduced to atmospheric. The reaction product was filtered through filter paper. Then the reaction product was transferred to a 2-liter washing vessel, diluted with 300 g of hexane and washed with 250 ml of a 5% (by weight) aqueous solution of
Пример 7C
В стеклянную колбу емкостью 500 мл, снабженную капельной воронкой, холодильником и мешалкой, загружали 50 г толуола, 17,7 г диэтилацеталя ацетальдегида и 1,5 диэтилфирата трифторида бора. В капельную воронку загружали 43 г этилвинилового эфира, который выпускали по каплям за 50 минут. От тепла реакции температура реакционного раствора повышалась, и ее поддерживали на уровне примерно 30oC путем охлаждения с помощью ванны с ледяной водой. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывалку и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натря 3 раза и затем 150 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 120 г сырого продукта. Сырой продукт имел кинематическую вязкость 48,8 сс при 40oC. ЯМР и ИК-спектры показали, что одной из концевых структур полимера была смесь (A) и (E), а другой - смесь (H), (I) и структур, в которых оксиэтильные группы в (H) и (I) замещены на оксиизопропильную группу соответственно.Example 7C
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 50 g of toluene, 17.7 g of acetaldehyde diethyl acetal and 1.5 boron trifluoride diethyl etherate. 43 g of ethyl vinyl ether was charged into a dropping funnel, which was dropped in 50 minutes. The heat of the reaction increased the temperature of the reaction solution and kept it at about 30 ° C. by cooling with an ice water bath. After dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a wash and washed with 100 ml of a 5% (by weight) aqueous solution of
Пример 7D
В автоклав емкостью 1 л, изготовленный из SUS-316L, загружали 110 г сополимера этилвинилового эфира и изопропилвинилового эфира, полученного в примере 7C, 300 г гексана, 5,5 г никеля Ренея и 5,5 г цеолита. Вводили в автоклав водород, давление которого регулировали до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление на уровне 29 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, повышали давление водорода до 50 кг/см2 и повышали температуру до 140oC за 30 минут при перемешивании. При 140oC реакцию проводили в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Продукт реакции фильтровали через фильтровальную бумагу. После этого продукт реакции переносили в промывной сосуд и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 дистиллированной воды 5 раз. Использовав роторный испаритель, удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 97 г. ЯМР и ИК-спектры показали, что одной из концевых структур полимера была смесь (A) и (E), а другой - смесь (C), (F) и (D), в которой (C) и (F) были основными структурами, а (D) - второстепенной.Example 7D
In a 1 L autoclave made of SUS-316L, 110 g of a copolymer of ethyl vinyl ether and isopropyl vinyl ether obtained in Example 7C, 300 g of hexane, 5.5 g of Raney nickel and 5.5 g of zeolite were charged. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing a pressure of 29 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 140 o C for 30 minutes with stirring. At 140 ° C., the reaction was carried out for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The reaction product was filtered through filter paper. After this, the reaction product was transferred to a washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
Пример 7E
В стеклянную колбу емкостью 500 мл, снабженную капельной воронкой, холодильником и мешалкой, загружали 80 г толуола, 40 г диэтилацеталя пропиональдегида и 0,4 г диэтилэфирата трифторида бора. В капельную воронку загружали 116 г 1-этокси-1-пропена, и выпускали его по каплям за 60 минут. Тепло от реакции повышало температуру реакционного раствора, и ее поддерживали на уровне примерно 30oC путем охлаждения с помощью ванны с ледяной водой. После окончания капания раствор перемешивали еще 40 минут. Реакционную смесь переносили в промывной сосуд и промывали 150 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 200 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 140 г неочищенного продукта. Этот продукт имел кинематическую вязкость 34,4 сс при 40oC.Example 7E
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 80 g of toluene, 40 g of propionaldehyde diethyl acetal and 0.4 g of boron trifluoride diethyl etherate. 116 g of 1-ethoxy-1-propene were charged into a dropping funnel, and it was released dropwise in 60 minutes. The heat from the reaction raised the temperature of the reaction solution and was maintained at about 30 ° C. by cooling with an ice water bath. After dripping, the solution was stirred for another 40 minutes. The reaction mixture was transferred to a washing vessel and washed with 150 ml of a 5% (by weight) aqueous solution of
В автоклав емкостью 1 литр, изготовленный из SUS-316L, загружали 120 г упомянутого неочищенного продукта, 300 г гексана, 6 г никеля Ренея и 6 цеолита. Вводили в автоклав водород, давление которого доводили до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили водород в автоклав, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2, и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 50 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Объединенную жидкость затем переносили в однолитровый промывной сосуд и промывали 150 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 200 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 95 г ЯМР и ИК-спектры продукта показали, что одной из концевых структур полимера была структура (J), а другой смесь (K) и (L), в которой (K) была основной структурой и (L)-второстепенной.A 1 liter autoclave made from SUS-316L was charged with 120 g of the above crude product, 300 g of hexane, 6 g of Raney nickel and 6 zeolite. Hydrogen was introduced into the autoclave, the pressure of which was brought to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again, hydrogen was introduced into the autoclave, providing a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 50 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. The combined liquid was then transferred to a one-liter washing vessel and washed with 150 ml of a 5% (by weight) aqueous solution of
Пример 7F
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 304 г этанола и 7,8 г диэтилэфирата трифторида бора. В капельную воронку загружали 3284 г этилвинилового эфира, который выпускали затем по каплям за 4 часа 30 минут. В течение этого периода тепло реакции повышало температуру реакционного раствора, и путем охлаждения с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывочный сосуд и промывали 1100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1100 мл воды 3 раза. Посредством роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 3397 г неочищенного продукта.
Example 7F
In a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, 1000 g of toluene, 304 g of ethanol and 7.8 g of boron trifluoride diethyl ether were charged. 3284 g of ethyl vinyl ether was charged into a dropping funnel, which was then released dropwise in 4 hours 30 minutes. During this period, the heat of reaction increased the temperature of the reaction solution, and by cooling with an ice water bath, the temperature was maintained at about 25 ° C. After the completion of the dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 1100 ml of a 5% (by weight) aqueous
В 2-литровый автоклав, изготовленный из SUS-316L, загружали 600 г полученного неочищенного продукта, 600 г гексана, 18 г никеля Ренея и 18 г цеолита. Вводили в автоклав водород, давление которого доводили до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2 и повышали температуру до 140oC за 30 минут при перемешивании. При 140oC реакцию проводили в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли путем декантации реакционную жидкость. Катализатор промывали 100 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Затем объединенную жидкость переносили в промывной сосуд и промывали 500 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 500 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 492 г. ЯМР и ИК-спектры продукта показали, что одной из концевых структур полимера была структура (A), а другой - смесь (C) и (D), в которой (C) была основной структурой, а (D) - второстепенной.A 2 liter autoclave made from SUS-316L was charged with 600 g of the obtained crude product, 600 g of hexane, 18 g of Raney nickel and 18 g of zeolite. Hydrogen was introduced into the autoclave, the pressure of which was brought to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing it with a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 140 o C for 30 minutes with stirring. At 140 ° C., the reaction was carried out for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 100 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. Then, the combined liquid was transferred to a washing vessel and washed with 500 ml of a 5% (by weight) aqueous solution of
Пример 7G
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 500 г диэтилацеталя ацетальдегида и 5,0 г диэтилэфирата трифторида бора. В капельную воронку загружали 2700 г этилвинилового эфира, который выпускали оттуда по каплям за 3 часа.Example 7G
1000 g of toluene, 500 g of acetaldehyde diethyl acetal and 5.0 g of boron trifluoride diethyl etherate were charged into a 5 liter glass flask equipped with a dropping funnel, refrigerator and stirrer. 2700 g of ethyl vinyl ether was charged into a dropping funnel, which was released dropwise from there in 3 hours.
Тепло реакции повышало температуру реакционного раствора, и путем охлаждения раствора в ванне с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 3040 г неочищенного продукта. Этот продукт имел кинематическую вязкость 42,1 сс при 40oC.The heat of reaction increased the temperature of the reaction solution, and by cooling the solution in an ice water bath, the temperature was maintained at about 25 ° C. After the completion of the dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 1000 ml of a 5% (by weight) aqueous solution of
В 2-литровый автоклав, изготовленный из SUS-316L, загружали 600 г полученного неочищенного продукта, 600 г гексана, 18 г никеля Ренея и 18 г цеолита. Вводили в автоклав водород, давление которого доводили до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2 и повышали температуру до 140oC за 30 минут при перемешивании. Реакцию проводили при 140oC в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 100 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Объединенную жидкость затем переносили в промывной сосуд и промывали 500 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 500 мл дистиллированной воды 5 раза. Посредством роторного испарителя удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 495 г. Полимер имел такие же концевые структуры, как в примере 4.A 2 liter autoclave made from SUS-316L was charged with 600 g of the obtained crude product, 600 g of hexane, 18 g of Raney nickel and 18 g of zeolite. Hydrogen was introduced into the autoclave, the pressure of which was brought to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing it with a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 140 o C for 30 minutes with stirring. The reaction was carried out at 140 ° C. for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 100 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. The combined liquid was then transferred to a washing vessel and washed with 500 ml of a 5% (by weight) aqueous solution of
Пример 7H
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 450 г диэтилацеталя ацетальдегида и 4,5 г диэтилэфирата трифторида бора. В капельную воронку загружали 3200 г этилвинилового эфира и выпускали его по каплям за 4 часа 10 минут. Тепло реакции повышало температуру реакционного раствора, и путем охлаждения раствора в ванне с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. Посредством роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 3466 г неочищенного продукта. Этот продукт имел кинематическую вязкость 76,1 сс при 40oC.Example 7H
1000 g of toluene, 450 g of acetaldehyde diethyl acetal and 4.5 g of boron trifluoride diethyl etherate were charged into a 5 liter glass flask equipped with a dropping funnel, refrigerator and stirrer. 3200 g of ethyl vinyl ether were charged into a dropping funnel and released dropwise in 4
В 2-литровый автоклав, изготовленный из SUS-316L, загружали 600 г полученного неочищенного продукта, 600 г гексана, 18 г никеля Ренея и 18 г цеолита. Вводили в автоклав водород, давление которого доводили до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, повышали давление водорода до 50 кг/см2 и повышали температуру до 140oC за 30 минут при перемешивании. Реакцию проводили при 140oC в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 100 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Затем объединенную жидкость переносили в промывной сосуд и промывали 500 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 500 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 498 г. Полимер имел концевые структуры такие же, как в примере 4.A 2 liter autoclave made from SUS-316L was charged with 600 g of the obtained crude product, 600 g of hexane, 18 g of Raney nickel and 18 g of zeolite. Hydrogen was introduced into the autoclave, the pressure of which was brought to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing it with a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 140 o C for 30 minutes with stirring. The reaction was carried out at 140 ° C. for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 100 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. Then, the combined liquid was transferred to a washing vessel and washed with 500 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, совместимость с флоном (флон-134a), объемное собственное сопротивление и стойкость к гидролизу полимеров, полученных в примерах 7A-7H. Результаты показаны в таблице IA (см. в конце описания). Была также измерена совместимость полимеров, полученных в примерах 7G и 7H с флоном - 32, и результаты показаны в таблице IB (см. в конце описания). Kinematic viscosity, flon compatibility (flon-134a), intrinsic resistance, and hydrolysis resistance of the polymers obtained in Examples 7A-7H were measured. The results are shown in table IA (see end of description). The compatibility of the polymers obtained in examples 7G and 7H with flon - 32 was also measured, and the results are shown in table IB (see the end of the description).
Сравнительный пример 1
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу рыночного парафинового минерального масла (VG 32). Результаты показаны в таблице 1A.Comparative Example 1
Kinematic viscosity, flon compatibility, intrinsic resistance and hydrolysis resistance of market paraffin mineral oil (VG 32) were measured. The results are shown in table 1A.
Сравнительный пример 2
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полипропиленгликоля Унилаб МВ11 (продукт ф. "Ниппон Юши Ко, Лтд). Результаты показаны в таблице 1A.Reference Example 2
Kinematic viscosity, flon compatibility, intrinsic resistance, and hydrolysis resistance of Unilab MV11 polypropylene glycol (product of F. Nippon Yushi Co., Ltd.) were measured. The results are shown in Table 1A.
Сравнительный пример 3
В 5-литровую стеклянную колбу, снабженную трубкой Дина и Старка, холодильником и мешалкой, загружали 1091 г пентаэритрита и 3909 г н-гексановой кислоты и смесь нагревали при перемешивании. Когда температура раствора достигала 200oC, ее поддерживали постоянной в течение 3 часов. Затем температуру повышали до 220oC и держали на этом уровне 10 часов. В течение этого периода начиналась реакция и образовывалась вода. После окончания реакции реакционный раствор охлаждали до 150oC и извлекали под пониженным давлением основную часть непрореагировавшей гексановой кислоты. Оставшийся раствор переносили в промывочный сосуд и после растворения в 2 литрах гексана промывали 1500 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и 1500 мл воды 3 раза. Затем добавляли 800 г ионообменной смолы и смесь перемешивали 3 часа. Удаляли ионообменную смолу путем фильтрования и удаляли под пониженным давлением гексан, использовав для этого роторный испаритель. Выход сложного эфира многоатомного спирта составлял 3390 г.Reference Example 3
1091 g of pentaerythritol and 3909 g of n-hexanoic acid were charged into a 5 liter glass flask equipped with a Dean and Stark tube, refrigerator and stirrer, and the mixture was heated with stirring. When the temperature of the solution reached 200 ° C., it was kept constant for 3 hours. Then the temperature was raised to 220 o C and kept at this level for 10 hours. During this period, the reaction began and water formed. After completion of the reaction, the reaction solution was cooled to 150 ° C and the majority of unreacted hexanoic acid was recovered under reduced pressure. The remaining solution was transferred to a washing vessel and, after dissolving in 2 liters of hexane, washed with 1500 ml of a 3% (by weight) aqueous solution of
Были измерены кинематическая вязкость, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полученного выше полимера. Результаты представлены в таблице 1A. Kinematic viscosity, compatibility with the flon, intrinsic volume resistance, and hydrolysis resistance of the polymer obtained above were measured. The results are presented in table 1A.
Пример 8
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 234 г этанола и 6,0 г диэтилэфирата трифторида бора. В капельную воронку загружали 2526 г этилвинилового эфира, который выпускали оттуда по каплям за 3 часа 20 минут. В течение этого периода тепло реакции повышало температуру реакционного раствора, и путем охлаждения раствора с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. До тех пор пока количество мономера не достигло величины, эквивалентной количеству этанола, мономер выпускали по каплям медленно, потому что имел место индукционный период теплообразования. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 870 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 870 мл воды 3 раза. Посредством роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 2622 г полимера этилвинилового эфира. Продукт имел светло-желтый цвет.Example 8
In a 5 liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, 1000 g of toluene, 234 g of ethanol and 6.0 g of boron trifluoride diethyl ether were charged. 2526 g of ethyl vinyl ether was charged into a dropping funnel, which was released dropwise from there in 3
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полученного, как описано выше, полимера этилвинилового эфира. Результаты представлены в таблице 2. The kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon and intrinsic resistance of the ethyl vinyl ether polymer obtained as described above were measured. The results are presented in table 2.
На фигурах 1, 2 и 3 показаны соответственно спектр инфракрасного поглощения, ЯМР 13C-спектр и ЯМР 1H-спектр.In figures 1, 2 and 3, respectively, the infrared absorption spectrum, 13 C NMR spectrum and 1 H NMR spectrum are shown.
На фиг. 2 пики при 101 м.д., 129 м.д. и 134 м.д. относятся к атому углерода, подчеркнутому в следующих формулах соответственно.:
-CH2-CH(OC2H5)2
-CH=CH-OC2H5
-CH=CH-OC2H5
На фиг. 3 пики при 4,7 м.д. 5,35 м.д. и 5,6 м.д. относятся к атому водорода, подчеркнутому в следующих ниже формулах соответственно:
-CH2-CH(OC2H5)2
-CH=CH-OC2H5
-CH=CH-OC2H5
Таким образом, концевой структурой соединения была смесь структур формулы (II) и формулы (III) и отношение массовых чисел молекулы, полученное из отношения протона (II):(III)=5,1:1.In FIG. 2 peaks at 101 ppm, 129 ppm and 134 ppm refer to the carbon atom underlined in the following formulas, respectively:
-CH 2 -CH (OC 2 H 5 ) 2
-CH = CH-OC 2 H 5
-CH = CH-OC 2 H 5
In FIG. 3 peaks at 4.7 ppm 5.35 ppm and 5.6 ppm refer to the hydrogen atom, underlined in the following formulas, respectively:
-CH 2 -CH (OC 2 H 5 ) 2
-CH = CH-OC 2 H 5
-CH = CH-OC 2 H 5
Thus, the terminal structure of the compound was a mixture of the structures of formula (II) and formula (III) and the mass ratio of the molecule obtained from the ratio of proton (II) :( III) = 5.1: 1.
Пример 9
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 195 г этанола и 5,0 г диэтилэфирата трифторида бора. В капельную воронку загружали 3005 г этилвинилового эфира и выдавали его по каплям за 3 часа 50 минут. В течение этого периода тепло реакции повышало температуру реакционного раствора, и путем охлаждения раствора с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. До тех пор пока количество мономера не достигало величины, эквивалентной количеству этанола, мономер выпускали по каплям медленно, потому что имел место индукционный период тепловыделения. После окончания капания раствор перемешивали еще 5 минут. Затем реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 3008 г полимера этилвинилового эфира. Продукт имел светло-желтый цвет.Example 9
1000 g of toluene, 195 g of ethanol and 5.0 g of boron trifluoride diethyl etherate were charged into a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer. 3005 g of ethyl vinyl ether was charged into a dropping funnel and dispensed dropwise in 3 hours 50 minutes. During this period, the heat of reaction increased the temperature of the reaction solution, and by cooling the solution with an ice water bath, the temperature was maintained at about 25 ° C. Until the amount of monomer reached an equivalent amount of ethanol, the monomer was slowly released dropwise. because there was an induction period of heat release. After dripping, the solution was stirred for another 5 minutes. Then the reaction mixture was transferred to a washing vessel and washed with 1000 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полученного так, как описано выше, полимера этилвинилового эфира. Результаты представлены в таблице 2. The kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon, and intrinsic resistance of the ethyl vinyl ether polymer obtained as described above were measured. The results are presented in table 2.
На фигурах 4, 5 и 6 показаны спектры соответственно инфракрасного поглощения, ЯМР 13C и ЯМР 1H. Концевой структурой соединения была смесь структур формулы (II) и формулы (III), и отношение массовых чисел молекулы, полученное таким же методом, как в примере 8, составляло: (II):(III): = 3,9:1.Figures 4, 5 and 6 show infrared absorption spectra, 13 C NMR, and 1 H NMR, respectively. The terminal structure of the compound was a mixture of structures of formula (II) and formula (III), and the mass ratio of the molecule obtained by the same method as in Example 8, was: (II) :( III): = 3.9: 1.
Пример 10
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 450 г диэтилацеталя ацетальдегида и 4,5 г диэтилэфирата трифторида бора. В капельную воронку загружали 3200 г этилвинилового эфира, после чего выдавали его по каплям за 4 часа 10 минут. В течение этого периода происходило повышение температуры реакционного раствора от тепла реакции, и путем охлаждения раствора с помощью ванны с ледяной водой температуры поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Затем реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 3466 г полимера этилвинилового эфира. Продукт имел светло-желтый цвет.Example 10
1000 g of toluene, 450 g of acetaldehyde diethyl acetal and 4.5 g of boron trifluoride diethyl etherate were charged into a 5 liter glass flask equipped with a dropping funnel, refrigerator and stirrer. 3200 g of ethyl vinyl ether was charged into a dropping funnel, after which it was dispensed dropwise in 4
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полученного так, как описано выше, полимера этилвинилового эфира. Результаты представлены в табл. 2 (см. в конце описания). The kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon, and intrinsic resistance of the ethyl vinyl ether polymer obtained as described above were measured. The results are presented in table. 2 (see the end of the description).
Спектр инфракрасного поглощения показан на фиг. 7. The infrared absorption spectrum is shown in FIG. 7.
Пример 11
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 195 г этанола и 4,5 г диэтилэфирата трифторида бора. В капельную воронку загружали 3875 г этилвинилового эфира, после чего выдавали его по каплям за 4 часа 40 минут. В течение этого периода происходило повышение температуры реакционного раствора от тепла реакции, и путем охлаждения раствора с помощью ванны с ледяной водой температуры поддерживали на уровне примерно 25oC. До тех пор пока количество мономера не достигало величины, эквивалентной количеству этанола, мономер выпускали по каплям медленно, потому что имел место индукционный период тепловыделения. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 3867 г полимера этилвинилового эфира. Продукт имел светло-желтый цвет.Example 11
1000 g of toluene, 195 g of ethanol and 4.5 g of boron trifluoride diethyl etherate were charged into a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer. 3875 g of ethyl vinyl ether was charged into a dropping funnel, after which it was dispensed dropwise in 4
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полученного так, как описано выше, полимера этилвинилового эфира. Результаты представлены в таблице 2. The kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon, and intrinsic resistance of the ethyl vinyl ether polymer obtained as described above were measured. The results are presented in table 2.
На фигурах 8, 9 и 10 показаны спектры соответственно инфракрасного поглощения, ЯМР 13C и ЯМР 1H.In figures 8, 9 and 10 shows the spectra, respectively, of infrared absorption, 13 C NMR and 1 H. NMR.
Отношение массовых чисел молекулы формулы (II) и формулы (III), полученное таким же образом, как в примере 8, составляло: (II):(III)=2,9:1. The mass ratio of the molecule of formula (II) and formula (III), obtained in the same manner as in example 8, was: (II) :( III) = 2.9: 1.
Пример 12
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 125 г толуола, 19,4 г изопропилового спирта и 2,3 г диэтилэфирата трифторида бора. В капельную воронку загружали 250 г изопропилвинилового эфира и затем выдавали его по каплям за 30 минут. В течение этого периода происходило повышение температуры реакционного раствора от тепла реакции, и путем охлаждения раствора с помощью ванны с ледяной водой температуры поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 80 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 80 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 238 г полимера изопропилвинилового эфира. Продукт имел светло-желтый цвет.Example 12
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 125 g of toluene, 19.4 g of isopropyl alcohol and 2.3 g of boron trifluoride diethyl etherate. 250 g of isopropyl vinyl ether was charged into a dropping funnel, and then it was dispensed dropwise in 30 minutes. During this period, the temperature of the reaction solution increased as a result of the reaction heat, and by cooling the solution with an ice water bath, the temperature was maintained at about 25 ° C. After the completion of the dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 80 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полимера изопропилвинилового эфира, полученного так, как описано выше. Результаты представлены в таблице 2. Kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon and intrinsic resistance of the isopropyl vinyl ether polymer obtained as described above were measured. The results are presented in table 2.
На фиг. 11 показан спектр инфракрасного поглощения. In FIG. 11 shows an infrared absorption spectrum.
Пример 13
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 125 г толуола, 17,4 изопропилового спирта и 2,1 диэтилэфирата трифторида бора. В капельную воронку загружали 250 г изопропилвинилового эфира и выдавали его по каплям в течение 30 минут. В течение этого периода происходило повышение температуры реакционного раствора от тепла реакции, и путем охлаждения раствора с помощью ванны с ледяной водой температуру раствора поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 80 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 80 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 236 г полимера изопропилвинилового эфира. Продукт имел светло-желтый цвет.Example 13
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 125 g of toluene, 17.4 isopropyl alcohol and 2.1 boron trifluoride diethyl etherate. 250 g of isopropyl vinyl ether was charged into a dropping funnel and dispensed dropwise over 30 minutes. During this period, the temperature of the reaction solution increased as a result of the reaction heat, and by cooling the solution with an ice water bath, the temperature of the solution was maintained at about 25 ° C. After the completion of the dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 80 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полимера изопропилвинилового эфира, полученного так, как описано выше. Результаты представлены в таблице 2. Kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon and intrinsic resistance of the isopropyl vinyl ether polymer obtained as described above were measured. The results are presented in table 2.
На фигурах 12, 13 и 14 показаны спектры соответственно инфракрасного поглощения, ЯМР 13C и ЯМР 1H.In figures 12, 13 and 14 shows the spectra, respectively, of infrared absorption, 13 C NMR and 1 H. NMR.
Отношение массовых чисел молекул формулы (II) и формулы (III), полученные таким же методом, как в примере 8, составляло: (II):(III)=3,8:1. The mass ratio of the molecules of formula (II) and formula (III), obtained by the same method as in example 8, was: (II) :( III) = 3.8: 1.
Пример 14
В автоклав из нержавеющей стали емкостью 200 мл, снабженный мешалкой, загружали 40 г толуола, 2,5 г метанола и 0,18 г диэтилэфирата трифторида бора. После закрытия автоклава атмосферу в нем заменяли азотом. Добавляли в автоклав 47 г метилвинилового эфира из баллона под давлением соединения за 5 часов. В течение этого периода происходило повышение температуры реакционного раствора от тепла реакции, и путем охлаждения раствора с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания добавления раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 50 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 100 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 42 г полимера метилвинилового эфира. Продукт имел светло-желтый цвет.Example 14
A 200 ml stainless steel autoclave equipped with a stirrer was charged with 40 g of toluene, 2.5 g of methanol and 0.18 g of boron trifluoride diethyl etherate. After the autoclave was closed, the atmosphere in it was replaced with nitrogen. 47 g of methyl vinyl ether was added to the autoclave from a balloon under compound pressure for 5 hours. During this period, the temperature of the reaction solution increased as a result of the heat of reaction, and the temperature was maintained at about 25 ° C. by cooling the solution with an ice water bath. After the addition was complete, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 50 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полученного, как описано выше, полимера метилвинилового эфира. The kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon and intrinsic resistance of the methyl vinyl ether polymer obtained as described above were measured.
Результаты представлены в таблице 2. The results are presented in table 2.
На фигурах 15, 16 и 17 показаны спектры соответственно инфракрасного поглощения, ЯМР 13C и ЯМР 1H. Отношение массовых чисел молекулы формулы (II) и формулы (III), полученное таким же методом, как в примере 8, составляло: (II):(III)=8,9:1.In figures 15, 16 and 17 shows the spectra of infrared absorption, NMR 13 C and NMR 1 H. : (III) = 8.9: 1.
Пример 15
Были измерены средние молекулярные массы и дисперсность молекулярной массы полученного в описанном выше примере 7C сополимера этилвинилового и изопропилвинилового эфиров. Результаты измерений показаны в таблице 2 вместе с результатами измерений кинематической вязкости, совместимости с флоном и объемного собственного сопротивления.Example 15
The average molecular weights and the molecular weight dispersion were measured in the copolymer of ethyl vinyl ether and isopropyl vinyl ether obtained in the above Example 7C. The measurement results are shown in table 2 together with the results of measurements of kinematic viscosity, compatibility with the flon and volume intrinsic resistance.
Спектры поглощения в инфракрасной области, ЯМР 13C и ЯМР 1H показаны на фигурах 18, 19 и 20 соответственно.Absorption spectra in the infrared region, 13 C NMR and 1 H NMR are shown in figures 18, 19 and 20, respectively.
Отношение массовых чисел молекулы формулы (II) и формулы (III), полученное таким же методом, как в примере 8, составляло: (II):(III) = 3,1:1. The mass ratio of the molecule of formula (II) and formula (III) obtained by the same method as in example 8 was: (II) :( III) = 3.1: 1.
Пример 16
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 50 г толуола, 4,6 г этилового спирта и 0,2 диэтилэфирата трифторида бора. В капельную воронку загружали 86 г 1-этокси-1-пропена и затем выдавали его по каплям за 50 минут. В течение этого периода происходило повышение температуры реакционного раствора от тепла реакции, и путем охлаждения раствора с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 30oC. После окончания капания раствор перемешивали еще 30 минут. Затем реакционную смесь переносили в промывной сосуд и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 84 г полимера 1-этокси-1-пропена.Example 16
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 50 g of toluene, 4.6 g of ethyl alcohol and 0.2 boron trifluoride diethyl etherate. 86 g of 1-ethoxy-1-propene were charged into a dropping funnel, and then it was dispensed dropwise in 50 minutes. During this period, the temperature of the reaction solution increased as a result of the heat of reaction, and the temperature was maintained at about 30 ° C by cooling the solution with an ice water bath. After completion of the dripping, the solution was stirred for another 30 minutes. Then the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном и объемное собственное сопротивление полученного, как описано выше, полимера 1-этокси-1-пропена. Результаты представлены в табл. 2. Kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon and intrinsic resistance of the 1-ethoxy-1-propene polymer obtained as described above were measured. The results are presented in table. 2.
Спектры поглощения в инфракрасной области, ЯМР 13C и ЯМР 1H показаны на фигурах 21, 22 и 23 соответственно.Absorption spectra in the infrared region, 13 C NMR and 1 H NMR are shown in figures 21, 22 and 23, respectively.
Пример 17
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 304 г этанола и 7,8 г диэтилэфирата трифторида бора. В капельную воронку загружали 3284 г этилвинилового эфира и выпускали его по каплям за 4 часа 30 минут. Тепло реакции повышало температуру раствора, и путем охлаждения с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Затем реакционную смесь переносили в промывной сосуд и промывали 1100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1100 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие материалы, получив в результате 3397 г неочищенного продукта. Были получены спектры ЯМР 1H и ЯМР 13C неочищенного продукта. ЯМР 1H-спектр имел пики при 4,7 м.д, 5,35 м.д. и 5,6 м.д., а ЯМР 13C - при 101 м.д., 129 м.д. и 134 м.д.Example 17
In a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer, 1000 g of toluene, 304 g of ethanol and 7.8 g of boron trifluoride diethyl ether were charged. 3284 g of ethyl vinyl ether was charged into a dropping funnel and released dropwise in 4 hours 30 minutes. The heat of reaction increased the temperature of the solution, and by cooling with an ice water bath, the temperature was maintained at about 25 ° C. After the completion of the dripping, the solution was stirred for another 5 minutes. Then the reaction mixture was transferred to a washing vessel and washed with 1100 ml of a 5% (by weight) aqueous solution of
Неочищенный продукт имел кинематическую вязкость 17,8 сс при 40oC.The crude product had a kinematic viscosity of 17.8 cc at 40 ° C.
Путем дополнительной обработки неочищенного продукта тем же способом, что и в примере 7F, получили 492 г полимера этилвинилового эфира. By further processing the crude product in the same manner as in Example 7F, 492 g of an ethyl vinyl ether polymer was obtained.
Были изменены средние молекулярные массы и дисперсность молекулярной массы полученного так, как описано выше, полимера этилвинилового эфира. Результаты измерений представлены в таблице 3 вместе с результатами измерений кинематической вязкости, совместимости с флоном и объемного собственного сопротивления. The average molecular weights and molecular dispersion of the molecular weight of the ethyl vinyl ether polymer obtained as described above were changed. The measurement results are presented in table 3 together with the results of measurements of kinematic viscosity, compatibility with the flon and volume intrinsic resistance.
Спектры инфракрасного поглощения, ЯМР 13C и ЯМР 1H показаны на фигурах 24, 25 и 26 соответственно.The infrared absorption spectra, 13 C NMR and 1 H NMR are shown in figures 24, 25 and 26, respectively.
В ЯМР 1H -спектре этого полимера пики 4,7 5,35 и 5,6 м.д., имевшиеся в спектре описанного выше неочищенного продукта, не были найдены. В спектре ЯМР 13C этого полимера пики при 101, 129 и 134 м.д. тоже отсутствовали. Кроме того в области 9,7 м.д. ЯМР 1H-спектра обычно находили пик, относящийся к водороду альдегида, а в области 200 м.д. в спектре ЯМР 13C обычно находился пик, относящийся к углероду альдегида. Ни один из этих пиков не был найден в спектрах полученного так, как описано выше, полимера. Следовательно, можно считать, что полученный полимер не содержит ненасыщенной связи и ацетальной и альдегидной структур.In the 1 H NMR spectrum of this polymer, the peaks of 4.7 5.35 and 5.6 ppm, which were in the spectrum of the crude product described above, were not found. The 13 C NMR spectrum of this polymer peaks at 101, 129, and 134 ppm. also absent. In addition, in the region of 9.7 ppm. 1 H NMR of the spectrum usually found a peak related to the hydrogen of the aldehyde, and in the region of 200 ppm in the 13 C NMR spectrum, there was usually a peak related to the carbon of the aldehyde. None of these peaks were found in the spectra of the polymer obtained as described above. Therefore, we can assume that the obtained polymer does not contain unsaturated bonds and acetal and aldehyde structures.
Пример 18
Были измерены средние молекулярные массы и дисперсность молекулярной массы полимера этилвинилового эфира, полученного в описанном выше примере 7G. Результаты измерений представлены в таблице 3 вместе с результатами измерений кинематической вязкости, совместимости с флоном и объемного собственного сопротивления.Example 18
The average molecular weights and molecular weight dispersion of the polymer of ethyl vinyl ether obtained in Example 7G described above were measured. The measurement results are presented in table 3 together with the results of measurements of kinematic viscosity, compatibility with the flon and volume intrinsic resistance.
Спектры инфракрасного поглощения, ЯМР 13C и ЯМР 1H показаны на фигурах 27, 28 и 29 соответственно.The infrared absorption spectra, 13 C NMR and 1 H NMR are shown in figures 27, 28 and 29, respectively.
По той же самой причине, что и в примере 17, полученный выше полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 19
Были измерены средние молекулярные массы и дисперсность молекулярной массы полимера этилвинилового эфира, полученного в описанном выше примере 7H. Результаты измерений представлены в таблице 3 вместе с результатами измерений кинематической вязкости, совместимости с флоном и объемного собственного сопротивления.Example 19
The average molecular weights and molecular weight dispersion of the polymer of ethyl vinyl ether obtained in Example 7H described above were measured. The measurement results are presented in table 3 together with the results of measurements of kinematic viscosity, compatibility with the flon and volume intrinsic resistance.
Спектры инфракрасного поглощения, ЯМР 13C и ЯМР 1H показаны на фигурах 30, 31 и 32 соответственно.The infrared absorption spectra, 13 C NMR and 1 H NMR are shown in figures 30, 31 and 32, respectively.
По той же самой причине, что и в примере 17, полученный выше полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 20
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 95 г толуола, 14,7 г изопропилового спирта и 1,8 г диэтилэфирата трифторида бора. В капельную воронку загружали 190 г изопропилвинилового эфира и выпускали его по каплям за 30 минут. Тепло реакции повышало температуру реакционного раствора, и путем охлаждения с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Затем реакционную смесь переносили в промывной сосуд и промывали 70 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 70 мл воды 3 раза. Использовав роторный испаритель, удаляли под пониженным давлением растворитель и непрореагировавшие материалы, получив в результате 179 г неочищенного продукта. Этот продукт имел кинематическую вязкость 27,0 сс при 40oC. В автоклав емкостью 1 л, изготовленный из SUS-316L, загружали 171 г полученного неочищенного продукта, 130 г гексана, 20 г никеля Ренея и 20 г цеолита. В автоклав вводили водород, давление которого доводили до 20 кг/см3. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC проводили реакцию в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры, и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 100 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Объединенную жидкость затем переносили в 2-литровый промывной сосуд и промывали 50 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 50 мл дистиллированной воды 5 раз. Использовав роторный испаритель, удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 131 г.Example 20
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 95 g of toluene, 14.7 g of isopropyl alcohol and 1.8 g of boron trifluoride diethyl etherate. 190 g of isopropyl vinyl ether was charged into a dropping funnel and released dropwise in 30 minutes. The heat of reaction increased the temperature of the reaction solution, and by cooling with an ice-water bath, the temperature was maintained at about 25 ° C. After completion of the dripping, the solution was stirred for another 5 minutes. Then the reaction mixture was transferred to a washing vessel and washed with 70 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полученного выше полимера изопропилвинилового эфира. Результаты представлены в табл. 3 (см. в конце описания). Kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon, intrinsic resistance, and hydrolysis resistance of the isopropyl vinyl ether polymer obtained above were measured. The results are presented in table. 3 (see the end of the description).
Спектры инфракрасного поглощения, ЯМР 13C и ЯМР 1H показаны на фигурах 33, 34 и 35 соответственно.The infrared absorption spectra, 13 C NMR and 1 H NMR are shown in figures 33, 34 and 35, respectively.
По той же самой причине, что и в примере 17, полученный как описано выше полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained as described above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 21
Были измерены средние молекулярные массы и дисперсность молекулярной массы полученного в описанном выше примере 6 полимера изопропилвинилового эфира. Результаты измерений представлены в таблице 3 вместе с результатами измерений кинематической вязкости, совместимости с флоном и объемного собственного сопротивления.Example 21
The average molecular weights and the molecular weight dispersion of the isopropyl vinyl ether polymer obtained in the above Example 6 were measured. The measurement results are presented in table 3 together with the results of measurements of kinematic viscosity, compatibility with the flon and volume intrinsic resistance.
Спектр инфракрасного поглощения показан на фиг. 36. The infrared absorption spectrum is shown in FIG. 36.
По той же самой причине, что и в примере 17, полученный, как описано выше, полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained as described above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 22
В автоклав из нержавеющей стали емкостью 200 мл, снабженный мешалкой, загружали 40 г толуола, 6,4 метанола и 0,45 г диэтилэфирата трифторида бора. Автоклав плотно закрывали и атмосферу в автоклаве заменяли азотом. Добавляли в автоклав 107 г метилвинилового эфира из бомбы под давлением соединения за 5 часов. Тепло реакции повышало температуру реакционного раствора, и путем охлаждения раствора с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания добавления раствора перемешивали еще 10 минут. Затем реакционную смесь переносили в промывной сосуд и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 95 г неочищенного продукта. Этот продукт имел кинематическую вязкость 56,9 сс при 40oC.Example 22
A 200 ml stainless steel autoclave equipped with a stirrer was charged with 40 g of toluene, 6.4 methanol and 0.45 g of boron trifluoride diethyl etherate. The autoclave was tightly closed and the atmosphere in the autoclave was replaced with nitrogen. 107 g of methyl vinyl ether was added to the autoclave from a bomb under compound pressure for 5 hours. The heat of reaction increased the temperature of the reaction solution, and by cooling the solution with an ice water bath, the temperature was maintained at about 25 ° C. After the addition was complete, the solution was stirred for another 10 minutes. Then the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
В однолитровый автоклав, изготовленный из SUS-316L, загружали 90 г полученного неочищенного продукта, 300 г гексана, 4,5 г никеля Ренея и 4,5 г цеолита. В автоклав вводили водород, давление которого регулировали до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 30 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. После того, как с помощью роторного испарителя удаляли под пониженным давлением гексан, к остаточному продукту добавляли 100 мл толуола, и затем продукт переносили в промывной сосуд и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под пониженным давлением толуол, воду и т.п. Выход составлял 80,5 г.A one liter autoclave made from SUS-316L was charged with 90 g of the obtained crude product, 300 g of hexane, 4.5 g of Raney nickel and 4.5 g of zeolite. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing it with a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 1 hour. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 30 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. After hexane was removed using a rotary evaporator under reduced pressure, 100 ml of toluene was added to the residual product, and then the product was transferred to a washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полученного выше полимера метилвинилового эфира. Результаты представлены в таблице 3. Kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon, intrinsic resistance, and hydrolysis resistance of the methyl vinyl ether polymer obtained above were measured. The results are presented in table 3.
Спектры поглощения в инфракрасной области, ЯМР 13C и ЯМР 1H показаны на фигурах 37, 38 и 39 соответственно.Absorption spectra in the infrared region, 13 C NMR and 1 H NMR are shown in figures 37, 38 and 39, respectively.
По той же самой причине, что и в примере 17, полученный выше полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 23
Были измерены средние молекулярные массы и дисперность молекулярной массы полученного в описанном выше примере 7D сополимера этилвинилового и изопропилового эфиров. Результаты измерений представлены в таблице 3 вместе с результатами измерений кинематической вязкости, совместимости с флоном и объемного собственного сопротивления.Example 23
The average molecular weights and the molecular dispersion of the molecular weight of the ethyl vinyl isopropyl ester copolymer obtained in the above Example 7D were measured. The measurement results are presented in table 3 together with the results of measurements of kinematic viscosity, compatibility with the flon and volume intrinsic resistance.
Спектры инфракрасного поглощения, ЯМР 13C и ЯМР 1H показаны на фигурах 40, 41 и 42 соответственно.The infrared absorption spectra, 13 C NMR and 1 H NMR are shown in figures 40, 41 and 42, respectively.
По той же самой причине, что и в примере 17, полученный выше полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 24
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 50 г толуола, 11 г изобутилового спирта и 0,5 диэтилэфирата трифторида бора.Example 24
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 50 g of toluene, 11 g of isobutyl alcohol and 0.5 boron trifluoride diethyl etherate.
В капельную воронку загружали 100 г изобутилвинилового эфира и затем выпускали его оттуда по каплям за 55 минут. Тепло реакции повышало температуру реакционного раствора, и путем охлаждения раствора с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 30oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 мл воды 3 раза. Посредством роторного испарителя удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 107 г неочищенного продукта. Этот продукт имел кинематическую вязкость 52,4 сс при 40oC.100 g of isobutyl vinyl ether was charged into a dropping funnel, and then it was dropped therefrom in 55 minutes. The heat of reaction increased the temperature of the reaction solution, and by cooling the solution with an ice water bath, the temperature was maintained at about 30 ° C. After the completion of the dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
В однолитровый автоклав, изготовленный из SUS-316L, загружали 90 г полученного неочищенного продукта, 300 г гексана, 4,8 г никеля Ренея и 4,8 г цеолита. В автоклав вводили водород, давление которого регулировали до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять в автоклав вводили водород, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2 и повышали температуру до 140oC за 30 минут при перемешивании. При 140oC реакцию проводили в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры с падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 30 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. Объединенную жидкость затем переносили в промывной сосуд емкостью 1 литр и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 мл дистиллированной воды 5 раз. С помощью роторного испарителя удаляли под повышенным давлением гексан, воду и т.п. Выход составлял 80,5 г.A one liter autoclave made from SUS-316L was charged with 90 g of the obtained crude product, 300 g of hexane, 4.8 g of Raney nickel and 4.8 g of zeolite. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 140 o C for 30 minutes with stirring. At 140 ° C., the reaction was carried out for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The pressure increase with increasing temperature with the pressure drop as a result of the reaction was suitably compensated by lowering or increasing the pressure, thereby maintaining the hydrogen pressure during the reaction at a level of 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 30 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. The combined liquid was then transferred to a 1 liter washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, средние молекулярные массы, дисперсность молекулярной массы, совместимость с флоном, объемное собственное сопротивление и стойкость к гидролизу полученного, как описано выше, полимера изобутилвинилового эфира. Результаты представлены в таблице 3. The kinematic viscosity, average molecular weights, molecular weight dispersion, compatibility with the flon, intrinsic resistance, and hydrolysis resistance of the isobutyl vinyl ether polymer obtained as described above were measured. The results are presented in table 3.
Спектры инфракрасного поглощения, ЯМР 13C и ЯМР 1H показаны на фигурах 43, 44 и 45 соответственно.The infrared absorption spectra, 13 C NMR and 1 H NMR are shown in figures 43, 44 and 45, respectively.
По той же самой причине, что и в примере 17, полученный выше полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 25
Были измерены средние молекулярные массы и дисперсность молекулярной массы полученного в описанном выше примере 7E полимера 1-этокси-1-пропена. Результаты измерений представлены в таблице 3 вместе с результатами измерений кинематической вязкости, совместимости в флоном и объемного собственного сопротивления.Example 25
The average molecular weights and the molecular weight dispersion of the 1-ethoxy-1-propene polymer obtained in the above Example 7E were measured. The measurement results are presented in table 3 together with the results of measurements of kinematic viscosity, compatibility in the flon and volume intrinsic resistance.
Спектры инфракрасного поглощения, ЯМР 15C и ЯМР 1H показаны на фигурах 46, 47 и 48 соответственно.The infrared absorption spectra, 15 C NMR and 1 H NMR are shown in figures 46, 47 and 48, respectively.
По той же самой причине, что и в примере 17, полученный выше полимер не содержал ни ненасыщенный связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained above did not contain either an unsaturated bond or an acetal and aldehyde structure.
Пример 25A
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 100 г толуола, 21,3 диметоксиэтилацеталя ацетальдегида и 0,45 г диэтилэфирата трифторида бора. В капельную воронку загружали 112 г метоксиэтилвинилового эфира и выдавали его по каплям за 50 минут. Тепло реакции повышало температуру реакционного раствора, и путем охлаждения раствора с помощью ванны с ледяной водой температуру поддерживали на уровне примерно 25oC. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и добавляли в нее 200 мл хлороформа. Продукт промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженном давлением растворитель и непрореагировавшие исходные материалы, получив в результате 129 г неочищенного продукта. Неочищенный продукт имел кинематическую вязкость 33,3 сс при 40oC.Example 25A
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 100 g of toluene, 21.3 acetaldehyde dimethoxyethyl acetal and 0.45 g of boron trifluoride diethyl etherate. 112 g of methoxyethyl vinyl ether was charged into a dropping funnel and dispensed dropwise in 50 minutes. The heat of reaction increased the temperature of the reaction solution, and by cooling the solution with an ice water bath, the temperature was maintained at about 25 ° C. After the completion of the dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and 200 ml of chloroform was added thereto. The product was washed with 100 ml of a 5% (by weight) aqueous solution of
В однолитровый автоклав, изготовленный из SUS-316L, загружали 110 г неочищенного продукта, 300 г гексана, 5,5 никеля Ренея, 5,5 г цеолита. В автоклав вводили водород, давление которого до 20 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление 20 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 50 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 2 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 50 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Осаждали катализатор путем отстаивания в течение 1 часа и отделяли реакционную жидкость путем декантации. Катализатор промывали 30 мл гексана дважды. Промывную жидкость объединяли с реакционной жидкостью и фильтровали через фильтровальную бумагу. С помощью роторного испарителя из объединенной жидкости удаляли под пониженным давлением гексан и в оставшийся продукт добавляли 200 мл хлороформа. Продукт затем переносили в промывной сосуд и промывали 100 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 150 мл дистиллированной воды 5 раз. Пользуясь роторным испарителем, удаляли под пониженным давлением растворитель, воду и т.п. Выход составлял 94 г.Into a one liter autoclave made from SUS-316L, 110 g of crude product, 300 g of hexane, 5.5 Raney nickel, 5.5 g zeolite were charged. Hydrogen was introduced into the autoclave, the pressure of which was up to 20 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing it with a pressure of 20 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 50 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 50 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The catalyst was precipitated by settling for 1 hour and the reaction liquid was separated by decantation. The catalyst was washed with 30 ml of hexane twice. The wash liquid was combined with the reaction liquid and filtered through filter paper. Using a rotary evaporator, hexane was removed from the combined liquid under reduced pressure, and 200 ml of chloroform was added to the remaining product. The product was then transferred to a washing vessel and washed with 100 ml of a 5% (by weight) aqueous solution of
Были измерены кинематическая вязкость, совместимость с флоном и стойкость к гидролизу полученного выше полимера метоксиэтилвинилового эфира. Результаты представлены в таблице 3. The kinematic viscosity, compatibility with the flon and the hydrolysis resistance of the methoxyethyl vinyl ether polymer obtained above were measured. The results are presented in table 3.
Спектры инфракрасного поглощения, ЯМР 13C и ЯМР 1H показаны на фигурах 49, 50 и 51 соответственно.The infrared absorption spectra, 13 C NMR and 1 H NMR are shown in figures 49, 50 and 51, respectively.
По той же самой причине, что и в примере 17, полученный выше полимер не содержал ни ненасыщенной связи, ни ацетальной и альдегидной структур. For the same reason as in Example 17, the polymer obtained above did not contain either an unsaturated bond or acetal and aldehyde structures.
Пример 26
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 195 г этанола и 5,0 г диэтилэфирата трифторида бора. Температура раствора была 14oC. К раствору добавляли 102 г этилвинилового эфира. Тепло реакции повышало температуру реакционного раствора, и реакционный раствор перемешивали с одновременным охлаждением посредством ванны с ледяной водой. (Спустя 3 минуты после добавления, температура раствора достигала максимума 21oC. Реакцию проводили с охлаждением посредством ванны с ледяной водой на всех последующих стадиях). После снижения температуры до 15oC опять добавляли 102 г этилвинилового эфира. Опять имело место выделение тепла, и температура повышалась. Снизив температуру до 15oC, добавляли еще 102 г этилвинилового эфира. Опять наблюдалось выделение тепла, и температура раствора опять повышалась. Во время снижения температуры раствора добавляли по каплям этилвиниловый эфир, и в ответ на это добавление сразу же происходило выделение тепла. После этого в раствор вводили по каплям 2700 г этилвинилового эфира с примерно постоянной скоростью (около 20 см3 в минуту) таким образом, чтобы температура реакционного раствора постоянно держалась на уровне примерно 25oC. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 1000 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и низкокипящие компоненты, получив в результате 3040 г продукта. Продукт имел светло-желтый цвет.Example 26
1000 g of toluene, 195 g of ethanol and 5.0 g of boron trifluoride diethyl etherate were charged into a 5-liter glass flask equipped with a dropping funnel, a refrigerator and a stirrer. The temperature of the solution was 14 ° C. 102 g of ethyl vinyl ether was added to the solution. The heat of reaction increased the temperature of the reaction solution, and the reaction solution was stirred while cooling with an ice water bath. (3 minutes after the addition, the temperature of the solution reached a maximum of 21 ° C. The reaction was carried out with cooling by means of a bath of ice water in all subsequent stages). After lowering the temperature to 15 ° C., 102 g of ethyl vinyl ether was again added. Again, heat was generated and the temperature rose. By lowering the temperature to 15 ° C., another 102 g of ethyl vinyl ether was added. Again, heat was observed, and the temperature of the solution rose again. While the solution was lowering the temperature, ethyl vinyl ether was added dropwise, and heat was immediately generated in response to this addition. After that, 2700 g of ethyl vinyl ether was added dropwise into the solution at an approximately constant speed (about 20 cm 3 per minute) so that the temperature of the reaction solution was constantly kept at about 25 ° C. After the completion of the dripping, the reaction mixture was transferred to a washing vessel and washed 1000 ml of a 3% (by weight) aqueous solution of
Продукт имел кинематическую вязкость 44,3 сс при 40oC и 5,90 сс при 100oC.The product had a kinematic viscosity of 44.3 ss at 40 o C and 5.90 ss at 100 o C.
Пример 27
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 36 г диэтилацеталя ацетальдегида, 80 г толуола и 0,36 г диэтилэфирата трифторида бора. Температура раствора была 15oC. При добавлении в раствор по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 256 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью (около 5 см3 в минуту) таким образом, чтобы температура реакционного раствора держалась постоянной на уровне 25oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 100 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 100 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и низкокипящие компоненты, получив 277 г продукта. Продукт имел светло-желтый цвет.Example 27
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 36 g of acetaldehyde diethyl acetal, 80 g of toluene and 0.36 g of boron trifluoride diethyl etherate. The temperature of the solution was 15 ° C. When ethyl vinyl ether was added dropwise to the solution, heat was generated immediately in response to this, and 256 g of ethyl vinyl ether was added dropwise at an approximately constant speed (about 5 cm 3 per minute) so that the temperature the reaction solution was kept constant at 25 o C while cooling the solution through a bath of ice water. After completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 3% (by weight) aqueous solution of
Продукт имел кинематическую вязкость 130,7 сс при 40oC и 11,8 сс при 100oC.The product had a kinematic viscosity of 130.7 cc at 40 ° C and 11.8 cc at 100 ° C.
Пример 28
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 18 г диэтилацеталя ацетальдегида, 80 г толуола, и 0,18 г диэтилэфирата трифторида бора. Температура раствора была 15oC. При добавлении в раствор по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 256 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью (около 5 см3 в минуту) таким образом, чтобы температура реакционного раствора держалась постоянной на уровне 25oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 100 мл 3-% ного водного раствора гидроксида натрия 3 раза и 100 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и низкокипящие компоненты, получив 261 г продукта. Продукт имел светло-желтый цвет. Продукт имел кинематическую вязкость 993,1 сс при 40oC и 44,7 сс при 100oC.Example 28
A 500 ml glass flask equipped with a dropping funnel, refrigerator and stirrer was charged with 18 g of acetaldehyde diethyl acetal, 80 g of toluene, and 0.18 g of boron trifluoride diethyl etherate. The temperature of the solution was 15 ° C. When ethyl vinyl ether was added dropwise to the solution, heat was generated immediately in response to this, and 256 g of ethyl vinyl ether was added dropwise at an approximately constant speed (about 5 cm 3 per minute) so that the temperature the reaction solution was kept constant at 25 o C while cooling the solution through a bath of ice water. After the completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 3% aqueous
Пример 29
В стеклянную колбу, емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 9 г диэтилацеталя ацетальдегида, 80 г толуола и 0,09 г диэтилэфирата трифторида бора. Температура раствора была 15oC. При добавлении к раствору по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 256 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью (около 5 см3 в минуту) таким образом, чтобы температура реакционного раствора держалась постоянной на уровне 25oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 100 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 100 мл воды 3 раза. Пользуясь роторным испарителем, удаляли под пониженным давлением растворитель и низкокипящие компоненты и в результате получили 255 г продукта. Продукт был светло-желтого цвета.Example 29
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 9 g of acetaldehyde diethyl acetal, 80 g of toluene and 0.09 g of boron trifluoride diethyl etherate. The temperature of the solution was 15 ° C. When ethyl vinyl ether was added dropwise to the solution, heat was generated immediately in response to this, and 256 g of ethyl vinyl ether was added dropwise at an approximately constant rate (about 5 cm 3 per minute) so that the temperature the reaction solution was kept constant at 25 o C while cooling the solution through a bath of ice water. After completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 3% (by weight) aqueous solution of
Продукт имел кинематическую вязкость 9356 сс при 40oC и 225,5 сс при 100oC.The product had a kinematic viscosity of 9356 cc at 40 o C and 225.5 cc at 100 o C.
Пример 30
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 4 г диэтилацеталя ацетальдегида, 80 г толуола и 0,04 г диэтилэфирата трифторида бора. Температура раствора была 15oC. При добавлении к раствору по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 256 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью (около 5 см3 в минуту) таким образом, чтобы температура реакционного раствора держалась постоянной на уровне 25oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 100 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 100 мл воды 3 раза. Пользуясь роторным испарителем, удалили под пониженным давлением растворитель и низкокипящие компоненты, получив в результате 252 г продукта. Продукт имел светло-желтый цвет.Example 30
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 4 g of acetaldehyde diethyl acetal, 80 g of toluene and 0.04 g of boron trifluoride diethyl etherate. The temperature of the solution was 15 ° C. When ethyl vinyl ether was added dropwise to the solution, heat was generated immediately in response to this, and 256 g of ethyl vinyl ether was added dropwise at an approximately constant speed (about 5 cm 3 per minute) so that the temperature the reaction solution was kept constant at 25 o C while cooling the solution through a bath of ice water. After completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 3% (by weight) aqueous solution of
Продукт имел среднемассовую молекулярную массу 2079 и среднечисловую молекулярную массу 6750. The product had a weight average molecular weight of 2079 and a number average molecular weight of 6750.
Средние молекулярные массы получали методом ГПХ (гельпроникающей хроматографии) при следующих условиях (эти условия были использованы только в этом примере):
Прибор: изделие ф. "Ниппон Банко Ко, Лтд" (насос)
Шодекс RI SE-61 (детектор)
Колонка: TSK HM+GMH6х2 + G2000H8
Температура: комнатная
Растворитель: ТГФ
Скорость элюирования: 1,4 мл/мин
Стандартное вещество: полистирол
Пример 31
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 16 г диэтилацеталя ацетальдегида, 80 г толуола и 0,16 г диэтилэфирата трифторида бора. Температура раствора была 15oC. При добавлении к раствору по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 256 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью (около 5 см3 в минуту) таким образом, чтобы температура раствора держалась постоянной на уровне 25oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 100 мл 3%-ного (массе) водного раствора гидроксида натрия 3 раза и затем 100 мл воды 3 раза. Пользуясь роторным испарителем, удаляли под пониженным давлением растворитель и низкокипящие компоненты, и в результате получили 262 г продукта. Продукт имел светло-желтый цвет.Average molecular weights were obtained by GPC (gel permeation chromatography) under the following conditions (these conditions were used only in this example):
Device: product f. Nippon Banco Co., Ltd. (pump)
Shodeks RI SE-61 (detector)
Column: TSK HM + GMH6x2 + G2000H8
Temperature: room
Solvent: THF
Elution Rate: 1.4 ml / min
Standard substance: polystyrene
Example 31
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 16 g of acetaldehyde diethyl acetal, 80 g of toluene and 0.16 g of boron trifluoride diethyl etherate. The temperature of the solution was 15 ° C. When ethyl vinyl ether was added dropwise to the solution, heat was generated immediately in response to this, and 256 g of ethyl vinyl ether was added dropwise at an approximately constant rate (about 5 cm 3 per minute) so that the temperature the solution was kept constant at 25 o C while cooling the solution through a bath of ice water. After completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 3% (by weight) aqueous solution of
Продукт имел кинематическую вязкость 1746 сс при 40oC и 64,6 сс при 100oC.The product had a kinematic viscosity of 1746 cc at 40 o C and 64.6 cc at 100 o C.
Пример 32
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 15 г диэтилацеталя ацетальдегида, 80 г толуола и 0,15 г диэтилэфирата трифторида бора. Температура раствора была 15oC. При добавлении к раствору по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 256 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью (около 5 см3 в минуту) таким образом, чтобы температура реакционного раствора держалась постоянной на уровне 25oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 100 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и 100 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и низкокипящие компоненты, получив в результате 260 г продукта. Продукт был светло-желтого цвета.Example 32
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 15 g of acetaldehyde diethyl acetal, 80 g of toluene and 0.15 g of boron trifluoride diethyl etherate. The temperature of the solution was 15 ° C. When ethyl vinyl ether was added dropwise to the solution, heat was generated immediately in response to this, and 256 g of ethyl vinyl ether was added dropwise at an approximately constant speed (about 5 cm 3 per minute) so that the temperature the reaction solution was kept constant at 25 o C while cooling the solution through a bath of ice water. After the completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 100 ml of a 3% (by weight) aqueous solution of
Продукт имел кинематическую вязкость 1903 сс при 40oC и 68,1 сс при 100oC.The product had a kinematic viscosity of 1903 cc at 40 ° C and 68.1 cc at 100 ° C.
Пример 33
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 4 г диэтилацетальдегида, 30 г толуола и 0,4 г FeCl3 • 6H2O. Температура раствора была 10oC. При добавлении к раствору по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 30 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью таким образом, чтобы температура реакционного раствора держалась постоянной на уровне 10oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 15 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 15 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и низкокипящие компоненты, и в результате получили 30,6 г продукта. Продукт был темно-желтого цвета.Example 33
In a 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer, 4 g of diethyl acetaldehyde, 30 g of toluene and 0.4 g of FeCl 3 · 6H 2 O were charged. The temperature of the solution was 10 ° C. Ethyl vinyl ether was added dropwise to the solution. heat was released immediately in response to this, and 30 g of ethyl vinyl ether was added dropwise at an approximately constant speed so that the temperature of the reaction solution was kept constant at 10 ° C. while cooling the solution by means of a bath of ice water. After the completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 15 ml of a 3% (by weight) aqueous solution of
Продукт имел кинематическую вязкость 21,86 сс при 40oC и 3,94 сс при 100oC.The product had a kinematic viscosity of 21.86 ss at 40 o C and 3.94 ss at 100 o C.
Пример 34
В стеклянную колбу емкостью 500 мл, оборудованную капельной воронкой, холодильником и мешалкой, загружали 3 г диэтилацеталя ацетальдегида, 30 г толуола и 0,18 г FeCl3. Температура раствора была 15oC. При добавлении к раствору по каплям этилвинилового эфира сразу же в ответ на это происходило выделение тепла, и 30 г этилвинилового эфира добавляли по каплям с примерно постоянной скоростью таким образом, чтобы температура раствора держалась постоянной на уровне 30oC при охлаждении раствора посредством ванны с ледяной водой. После окончания капания реакционную смесь переносили в промывной сосуд и промывали 15 мл 3%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 15 мл воды 3 раза. С помощью роторного испарителя удаляли под пониженным давлением растворитель и низкокипящие компоненты, и в результате получили 29,4 г продукта. Продукт был темно-желтого цвета.Example 34
A 500 ml glass flask equipped with a dropping funnel, a refrigerator and a stirrer was charged with 3 g of acetaldehyde diethyl acetal, 30 g of toluene and 0.18 g of FeCl 3 . The temperature of the solution was 15 ° C. When ethyl vinyl ether was added dropwise to the solution, heat was released immediately in response to this, and 30 g of ethyl vinyl ether was added dropwise at an approximately constant rate so that the temperature of the solution was kept constant at 30 ° C. while cooling the solution through a bath of ice water. After the completion of the dripping, the reaction mixture was transferred to a washing vessel and washed with 15 ml of a 3% (by weight) aqueous solution of
Продукт имел кинематическую вязкость 326,7 сс при 40oC и 25,69 сс при 100oC.The product had a kinematic viscosity of 326.7 ss at 40 o C and 25.69 ss at 100 o C.
Пример 35
В однолитровый автоклав, изготовленный из SUS-316L, загружали 100 г диэтилацеталя ацетальдегида, 100 г н-гептана, 3,0 г никеля Ренея и 3,0 г цеолита. Вводили в автоклав водород, давление которого доводили до 10 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление на уровне 10 кг/см2, и после помешивания в течение примерно 30 секунд давление водорода сбрасывали. Затем давление водорода повышали до 30 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 2 часов 30 минут. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 30 кг/см2. После окончания реакции реакционную смесь охлаждали до 20oC и снижали давление до атмосферного. Посредством газовой хроматографии проводили количественный и качественный анализы продукта реакции. Степень превращения диэтилацеталя ацетальдегида составляла 94,9%, а избирательность диэтилового эфира была 68,3%.Example 35
In a one liter autoclave made from SUS-316L, 100 g of acetaldehyde diethyl acetal, 100 g of n-heptane, 3.0 g of Raney nickel and 3.0 g of zeolite were charged. Hydrogen was introduced into the autoclave, the pressure of which was brought to 10 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing a pressure of 10 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Then the hydrogen pressure was increased to 30 kg / cm 2 and the temperature was increased to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 2 hours 30 minutes. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 30 kg / cm 2 . After the reaction, the reaction mixture was cooled to 20 o C and reduced the pressure to atmospheric. By gas chromatography, quantitative and qualitative analyzes of the reaction product were carried out. The degree of conversion of acetaldehyde diethyl acetal was 94.9%, and the selectivity of diethyl ether was 68.3%.
Пример 36
В однолитровый автоклав, изготовленный из SUS-316L, загружали 100 г диэтилацеталя пропиональдегида, 100 г н-октана, 6,0 г никеля Ренея и 6,0 г цеолита. Вводили в автоклав водород, давление которого доводили до 10 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление на уровне 10 кг/см и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Затем давление водорода повышали до 30 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 1 часа 30 минут. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 30 кг/см2. После окончания реакции реакционную смесь охлаждали до 20oC и снижали давление до атмосферного. Посредством газовой хроматографии проводили количественный и качественный анализы продукта реакции. Степень превращения диэтилацеталя пропиональдегида составляла 97,0%, а избирательность этил-н-пропилового эфира была 72,0%.Example 36
In a one liter autoclave made from SUS-316L, 100 g of propionaldehyde diethyl acetal, 100 g of n-octane, 6.0 g of Raney nickel and 6.0 g of zeolite were charged. Hydrogen was introduced into the autoclave, the pressure of which was brought to 10 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing a pressure of 10 kg / cm, and after stirring for about 30 seconds, the hydrogen pressure was released. Then the hydrogen pressure was increased to 30 kg / cm 2 and the temperature was increased to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 1 hour 30 minutes. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 30 kg / cm 2 . After the reaction, the reaction mixture was cooled to 20 o C and reduced the pressure to atmospheric. By gas chromatography, quantitative and qualitative analyzes of the reaction product were carried out. The degree of conversion of propionaldehyde diethyl acetal was 97.0%, and the selectivity of ethyl n-propyl ether was 72.0%.
Пример 37
(1) Получение материала
В 5-литровую стеклянную колбу, оборудованную капельной воронкой, холодильником и мешалкой, загружали 1000 г толуола, 500 г диэтилацеталя ацетальдегида и 5,0 г диэтилэфирата трифторида бора. В капельную воронку загружали 2500 г этилвинилового эфира и затем выпускали его по каплям за 2 часа 30 минут. В течение этого периода начиналась реакция и повышалась температура реакционного раствора. Температуру поддерживали на уровне примерно 25oC путем охлаждения реакционного раствора с помощью ванны с ледяной водой. После окончания капания раствор перемешивали еще 5 минут. Реакционную смесь переносили в промывной сосуд и промывали 1000 мл 5%-ного (по массе) водного раствора гидроксида натрия 3 раза и затем 1000 мл воды 3 раза. Пользуясь роторным испарителем, удаляли под пониженным давлением растворитель и непрореагировавшие исходные материалы, получив в результате 2833 г продукта. ЯМР 1Н-спектр этого продукта показан на фиг. 52. Как показал этот спектр, продукт имел структуру представленных ниже формул (A') и (B'). Продукт имел кинематическую вязкость 5,18 сс при 100oC и 38,12 cc при 40oC
.Example 37
(1) Receiving material
1000 g of toluene, 500 g of acetaldehyde diethyl acetal and 5.0 g of boron trifluoride diethyl etherate were charged into a 5 liter glass flask equipped with a dropping funnel, refrigerator and stirrer. 2500 g of ethyl vinyl ether was charged into a dropping funnel and then released dropwise in 2 hours 30 minutes. During this period, the reaction began and the temperature of the reaction solution increased. The temperature was maintained at about 25 ° C. by cooling the reaction solution with an ice water bath. After dripping, the solution was stirred for another 5 minutes. The reaction mixture was transferred to a washing vessel and washed with 1000 ml of a 5% (by weight) aqueous solution of
.
Отношение массовых чисел молекулы было: (A'):(B')= 4,5:1, и среднее значение составляло 5,6. The mass ratio of the molecule was: (A ') :( B') = 4.5: 1, and the average value was 5.6.
(2) В однолитровый автоклав, изготовленный из SUS-316L, загружали 200 г олигомера, полученного так, как описано выше в параграфе (1), 6,0 г никеля Ренея и 6,0 г цеолита. Вводили в автоклав водород, давление которого регулировали до 10 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород, обеспечивая его давление на уровне 10 кг/см2, и после перемешивания в течение примерно 30 секунд давление водорода сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 25 кг/см2 и повышали температуру до 140oC за 30 минут при перемешивании. При 140oC реакцию проводили в течение 2 часов. Реакция протекала во время и после повышения температуры, при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 25 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. К реакционной смеси добавляли 100 мл гексана. Осаждали катализатор путем отстаивания в течение 30 минут и отделяли реакционный раствор путем декантации. Гексановый раствор объединяли с реакционным раствором и фильтровали через фильтровальную бумагу. Катализатор повторно использовали в примере 39. C помощью роторного испарителя удаляли под пониженным давлением гексан, воду и т.п. Выход составлял 162 г.(2) In a one liter autoclave made from SUS-316L, 200 g of an oligomer prepared as described above in paragraph (1), 6.0 g of Raney nickel and 6.0 g of zeolite were charged. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 10 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave, providing a pressure of 10 kg / cm 2 , and after stirring for about 30 seconds, the hydrogen pressure was released. Repeating this operation again, the hydrogen pressure was increased to 25 kg / cm 2 and the temperature was raised to 140 o C for 30 minutes with stirring. At 140 ° C., the reaction was carried out for 2 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 25 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. 100 ml of hexane was added to the reaction mixture. The catalyst was precipitated by settling for 30 minutes and the reaction solution was separated by decantation. The hexane solution was combined with the reaction solution and filtered through filter paper. The catalyst was reused in Example 39. Hexane, water, and the like were removed under reduced pressure using a rotary evaporator. The yield was 162 g.
ЯМР 1H - спектр этого продукта показан на фиг. 53. Как показал этот спектр, исходный ацеталь был превращен в простой эфир, представленный формулой (C'):
где Et - этильная группа. Степень превращения составляла 100%. Кинематическая вязкость была 4,90 сс при 100oC и 29,50 сс при 40oC. Олигомер зтилвинилового эфира, имеющий представленную выше формулу (B'), тоже был превращен в простой эфир, имеющий представленную выше формулу (C'). 1 H NMR — The spectrum of this product is shown in FIG. 53. As this spectrum showed, the starting acetal was converted to ether represented by the formula (C '):
where E t is an ethyl group. The degree of conversion was 100%. The kinematic viscosity was 4.90 cc at 100 ° C and 29.50 cc at 40 ° C. The vinyl ether oligomer having the above formula (B ′) was also converted to an ether having the above formula (C ′).
Пример 38
В однолитровый автоклав, изготовленный из SUS-316L, загружали 200 г олигомера, полученного в описанном выше примере 37(1), 20 r никеля Ренея и 20 г цеолита. Вводили в автоклав водород, давление которого регулировали до 7 кг/см2. После перемешивания в течение 30 секунд давление сбрасывали. Повторив эту операцию еще раз, давление водорода доводили до 7 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 2 часов 30 минут. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления.Example 38
In a one liter autoclave made from SUS-316L, 200 g of the oligomer obtained in Example 37 (1) described above, 20 r of Raney nickel and 20 g of zeolite were charged. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 7 kg / cm 2 . After stirring for 30 seconds, the pressure was released. Repeating this operation again, the hydrogen pressure was adjusted to 7 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 2 hours 30 minutes. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred.
Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 7 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Реакционную смесь фильтровали и с помощью роторного испарителя из профильтрованного раствора удаляли под пониженным давлением воду и т.п. Выход составлял 160 г. В результате этой процедуры из исходного ацеталя был получен такой же простой эфир, как в примере 37(2), причем степень превращения составляла 100%. Кинематическая вязкость была 4,77 сс при 100oC и 30,27 сс при 40oC.The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 7 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The reaction mixture was filtered and, using a rotary evaporator, water and the like were removed from the filtered solution under reduced pressure. The yield was 160 g. As a result of this procedure, the same ether was obtained from the starting acetal as in Example 37 (2), the degree of conversion being 100%. The kinematic viscosity was 4.77 ss at 100 o C and 30.27 ss at 40 o C.
Пример 39
В автоклав, использованный в примере 37(2), в котором остался катализатор, загружали 200 г олигомера, полученного в примере 37(1), проводили реакцию так же, как в примере 37(2). Выход составлял 164 г. В результате этой процедуры из исходного ацеталя был получен такой же, как в примере 37(2), простой эфир, причем степень конверсии составляла 100%. Кинематическая вязкость была 4,93 сс при 100oC и 29,13 сс при 40oC.Example 39
In the autoclave used in example 37 (2), in which the catalyst remained, 200 g of the oligomer obtained in example 37 (1) was loaded, the reaction was carried out in the same way as in example 37 (2). The yield was 164 g. As a result of this procedure, the ether was obtained from the starting acetal as in Example 37 (2), and the degree of conversion was 100%. The kinematic viscosity was 4.93 ss at 100 o C and 29.13 ss at 40 o C.
Пример 40
(1) Получение материала
Реакцию осуществляли так же, как в примере 37(1) за исключением того, что количество ацетальдегида было 450 г, количество эфирата трифторида бора - 4,5 г и количество этилвинилового эфира - 2800 г. Выход составлял 3175 г. Продукт имел такую же структуру, как и продукт, полученный в примере 37(1). Кинематическая вязкость составляла 6,79 сс при 100oC и 59,68 сс при 40oC. Отношение массовых чисел молекулы было: (A'):(B')=8:1, а среднее значение составляло 6,8.Example 40
(1) Receiving material
The reaction was carried out as in example 37 (1) except that the amount of acetaldehyde was 450 g, the amount of boron trifluoride etherate was 4.5 g and the amount of ethyl vinyl ether was 2800 g. The yield was 3175 g. The product had the same structure , as well as the product obtained in example 37 (1). The kinematic viscosity was 6.79 ss at 100 o C and 59.68 ss at 40 o C. The ratio of the mass numbers of the molecule was: (A ') :( B') = 8: 1, and the average value was 6.8.
(2) В однолитровый автоклав, изготовленный из SUS-316L загружали 200 г олигомера, полученного в описанном выше параграфе (1), 10 г никеля Ренея и 15 г активированной глины. Вводили в автоклав водород, давление которого регулировали до 10 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Вновь вводили в автоклав водород и доводили его давление до 10 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Повторив эту операцию еще раз, давление водорода повышали до 3 кг/см2 и повышали температуру до 150oC за 40 минут при перемешивании. При 150oC реакцию проводили в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления при повышении температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 30 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снимали давление до атмосферного. Реакционную смесь фильтровали, и с помощью роторного испарителя из раствора удаляли под пониженным давлением воду и т.п. Выход составлял 158 г. В результате этой процедуры из исходного ацеталя был получен такой же, как в примере 37(2), простой эфир, причем степень превращения составляла 100%. Кинематическая вязкость была 7,06 сс при 100oC и 57,32 сс при 40oC.(2) In a one liter autoclave made from SUS-316L, 200 g of the oligomer obtained in the above paragraph (1), 10 g of Raney nickel and 15 g of activated clay were charged. Hydrogen was introduced into the autoclave, the pressure of which was regulated to 10 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Hydrogen was reintroduced into the autoclave and its pressure was adjusted to 10 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Repeating this operation again, the hydrogen pressure was increased to 3 kg / cm 2 and the temperature was raised to 150 o C for 40 minutes with stirring. At 150 ° C., the reaction was carried out for 1 hour. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby maintaining the hydrogen pressure during the reaction at 30 kg / cm 2 . After the completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was removed to atmospheric. The reaction mixture was filtered, and water and the like were removed from the solution using a rotary evaporator. The yield was 158 g. As a result of this procedure, the ether was obtained from the starting acetal as in Example 37 (2), and the degree of conversion was 100%. The kinematic viscosity was 7.06 cc at 100 o C and 57.32 cc at 40 o C.
Пример 41
В однолитровый автоклав, изготовленный из SUS-316L, загружали 200 г олигомера, полученного в описанном выше примере 37(1), 10 г цеолита и 5,0 г Pd/C (несущий 5% Pd, продукт ф. "Вако Джан-яку Ко, Лтд"). Вводили в автоклав водород, давление которого регулировали до 7 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Вновь вводили в автоклав водород и доводили его давление до 7 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Повторив эту операцию еще раз, давление водорода доводили до 7 кг/см2 и повышали температуру до 120oC за 30 минут при перемешивании. При 120oC реакцию провозили в течение 7 часов. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 7 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снимали давление до атмосферного. Реакционную смесь фильтровали и с помощью роторного испарителя из профильтрованного раствора удаляли под пониженным давлением воду и т.п. Выход составляя 167,2 г. В результате этой процедуры из исходного ацеталя был получен такой же простой эфир, как в примере 37(2), причем степень превращения составляла 100%. Кинематическая вязкость была 5,28 сс при 100oC и 32,93 сс при 40oC.Example 41
In a one liter autoclave made from SUS-316L, 200 g of the oligomer obtained in Example 37 (1) described above, 10 g of zeolite and 5.0 g of Pd / C (carrying 5% Pd, product of Wako Jan-yaku f.) Were charged. Co., Ltd. "). Hydrogen was introduced into the autoclave, the pressure of which was regulated to 7 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Hydrogen was reintroduced into the autoclave and its pressure was adjusted to 7 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Repeating this operation again, the hydrogen pressure was adjusted to 7 kg / cm 2 and the temperature was raised to 120 o C for 30 minutes with stirring. At 120 ° C., the reaction was transported for 7 hours. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 7 kg / cm 2 . After the completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was removed to atmospheric. The reaction mixture was filtered and, using a rotary evaporator, water and the like were removed from the filtered solution under reduced pressure. The yield was 167.2 g. As a result of this procedure, the same ether was obtained from the starting acetal as in Example 37 (2), the degree of conversion being 100%. The kinematic viscosity was 5.28 ss at 100 o C and 32.93 ss at 40 o C.
Пример 42
В автоклав емкостью 1 л, изготовленный из SUS-316L, загружали 200 г олигомера, полученного так, как описано выше в параграфе (1), 20 г цеолита и 20 г Ru/C (несущего 5% Ru, продукт ф."Вако Джан-яку Ко, Лтд.") Вводили в автоклав водород, давление которого регулировали до 30 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород и регулировали его давление до 30 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Повторив эту операцию еще раз, давление водорода доводили до 30 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 30 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Реакционную смесь фильтровали и с помощью роторного испарителя из профильтрованного раствора удаляли под пониженным давлением воду и т.п. Выход составлял 156 г. В результате этой процедуры из исходного ацеталя был получен такой же простой эфир, как в примере 37(2), причем степень превращения была равна 100%. Кинематическая вязкость составляла 5,18 сс при 100oC и 31,53 сс при 40oC.Example 42
In a 1 L autoclave made of SUS-316L, 200 g of an oligomer prepared as described above in paragraph (1), 20 g of zeolite and 20 g of Ru / C (bearing 5% Ru, product of F. Waco Jan -yako Co., Ltd. ") Hydrogen was introduced into the autoclave, the pressure of which was regulated to 30 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave and its pressure was adjusted to 30 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Repeating this operation again, the hydrogen pressure was adjusted to 30 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 1 hour. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 30 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The reaction mixture was filtered and, using a rotary evaporator, water and the like were removed from the filtered solution under reduced pressure. The yield was 156 g. As a result of this procedure, the same ether was obtained from the starting acetal as in Example 37 (2), and the degree of conversion was 100%. The kinematic viscosity was 5.18 ss at 100 o C and 31.53 ss at 40 o C.
Пример 43
В автоклав емкостью 2 литра, изготовленный из SUS - 316L, загружали 15 г Ni диатомовой земли и 350 г гексана. После замены атмосферы в автоклаве водородом давление водорода доводили до 30 кг/смoC. Повышали температуру до 150oC за 30 минут при перемешивании и в течение 30 минут проводили активационную обработку катализатора. После охлаждения автоклава загружали в него 300 г олигомера, полученного в описанном выше примере 37(1), и 15 г цеолита. Вводили в автоклав водород и доводили его давление до 30 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Опять вводили в автоклав водород и доводили давление водорода в автоклаве до 30 кг/см2. После перемешивания в течение примерно 30 секунд давление сбрасывали. Повторив эту операцию еще раз, доводили давление водорода до 30 кг/см2 и повышали температуру до 130oC за 30 минут при перемешивании. При 130oC реакцию проводили в течение 1 часа. Реакция протекала во время и после повышения температуры, и при этом происходило падение давления. Рост давления с повышением температуры и падение давления в результате реакции подходящим образом компенсировали путем понижения или повышения давления, обеспечивая тем самым поддержание давления водорода во время реакции на уровне 30 кг/см2. После окончания реакции реакционную смесь охлаждали до комнатной температуры и снижали давление до атмосферного. Реакционную смесь фильтровали и с помощью роторного испарителя из профильтрованного раствора удаляли под пониженным давлением воду и т.п. Выход составлял 240 г.Example 43
A 2 liter autoclave made of SUS-316L was charged with 15 g of Ni diatomaceous earth and 350 g of hexane. After replacing the atmosphere in the autoclave with hydrogen, the hydrogen pressure was brought to 30 kg / cm o C. The temperature was raised to 150 o C for 30 minutes with stirring and the catalyst was activated for 30 minutes. After cooling the autoclave, 300 g of the oligomer obtained in Example 37 (1) described above and 15 g of zeolite were charged. Hydrogen was introduced into the autoclave and its pressure was adjusted to 30 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Again hydrogen was introduced into the autoclave and the pressure of hydrogen in the autoclave was adjusted to 30 kg / cm 2 . After stirring for about 30 seconds, the pressure was released. Repeating this operation again, the hydrogen pressure was adjusted to 30 kg / cm 2 and the temperature was raised to 130 o C for 30 minutes with stirring. At 130 ° C., the reaction was carried out for 1 hour. The reaction proceeded during and after an increase in temperature, and a pressure drop occurred. The increase in pressure with increasing temperature and the pressure drop as a result of the reaction were suitably compensated by lowering or increasing the pressure, thereby ensuring that the hydrogen pressure during the reaction was maintained at 30 kg / cm 2 . After completion of the reaction, the reaction mixture was cooled to room temperature and the pressure was reduced to atmospheric. The reaction mixture was filtered and, using a rotary evaporator, water and the like were removed from the filtered solution under reduced pressure. The yield was 240 g.
Степень конверсии исходного ацеталя была равна 100%, как и в примере 37. Кинематическая вязкость составляла 5,38 сс при 100oC и 33,12 сс при 40oC.The degree of conversion of the starting acetal was 100%, as in Example 37. The kinematic viscosity was 5.38 ss at 100 o C and 33.12 ss at 40 o C.
Claims (27)
где R1 - H или CH3;
R2 - алкил C1 - C3,
имеющий среднемассовую молекулярную массу 300 - 1200, причем один конец цепи имеет структуру, выраженную общей формулой II
или формулой III
-CH=CHORa,
где R2 - такой же, как указанный выше,
R3 - углеводородная группа, имеющая 1 - 8 атомов углерода;
Ra - один из радикалов R2 и R3.1. A simple polyvinyl ether, which is a homo - or copolymer of a simple vinyl vinyl ether of the General formula I
where R 1 is H or CH 3 ;
R 2 is alkyl C 1 - C 3 ,
having a weight average molecular weight of 300 to 1200, with one end of the chain having a structure expressed by general formula II
or formula III
-CH = CHOR a ,
where R 2 is the same as above
R 3 is a hydrocarbon group having 1 to 8 carbon atoms;
R a is one of the radicals R 2 and R 3 .
где R4, R5 и R6 - каждый атом водорода или алкильная группа C1 - C4 и могут быть одинаковыми или разными;
R7 - алкиленовая группа C2 - C4;
R8 - алкильная группа C1 - C10;
х - число, среднее значение которого находится в диапазоне 1 - 10;
R7О могут быть одинаковыми или разными, когда составляющее звено содержит несколько R7О, со среднемассовой молекулярной массой 300 - 3000.5. A simple polyvinyl ether, representing a homo - or copolymer of a simple vinyl vinyl ether of the General formula IV
where R 4 , R 5 and R 6 are each hydrogen atom or an alkyl group C 1 - C 4 and may be the same or different;
R 7 is an alkylene group C 2 - C 4 ;
R 8 is an alkyl group C 1 - C 10 ;
x is a number whose average value is in the range of 1-10;
R 7 O may be the same or different when the constituent unit contains several R 7 O, with a weight average molecular weight of 300 to 3000.
где R4 - R8 определены выше;
m - число, среднее значение которого находится в диапазоне 0 - 10,
несколько группировок R7О могут быть одинаковыми или разными,
а другой конец цепи выражен общей формулой
где R4 - R8 определены выше;
n - число, среднее значение которого находится в диапазоне 0 - 10;
несколько группировок R7О могут быть одинаковыми или разными.6. The simple polyvinyl ether according to claim 5, characterized in that one end of the chain is expressed by the General formula
where R 4 - R 8 are as defined above;
m is a number whose average value is in the range 0 - 10,
several groups of R 7 O may be the same or different,
and the other end of the chain is expressed by the general formula
where R 4 - R 8 are as defined above;
n is a number whose average value is in the range 0 - 10;
several R 7 O moieties may be the same or different.
8. Простой поливиниловый эфир по п.5 общей формулы IV, в которой R4 = R5 = R6 - являются водородом, х = 0, R8 является алкильной группой C1 - C4, структурной формулы
где р - степень полимеризации.7. The polyvinyl ether according to claim 5 of general formula IV, characterized in that R 8 is an alkyl group C 1 - C 4 and in the series of constituent units may be the same or different and has the structural formula
8. The polyvinyl ether according to claim 5 of general formula IV, in which R 4 = R 5 = R 6 - are hydrogen, x = 0, R 8 is an alkyl group C 1 - C 4 , structural formula
where p is the degree of polymerization.
где R9, R10 и R11 - каждый атом водорода или углеводородная группа с C1 - C8 и могут быть одинаковыми или разными;
R12 - двухвалентная углеводородная группа с C2 - C10;
R13 - углеводородная группа с C1 - C10;
q - число, среднее значение которого находится в диапазоне 0 - 10;
R12 могут быть одинаковыми или разными, когда имеется несколько группировок R12О,
отличающийся тем, что проводят полимеризацию мономера простого винилового эфира общей формулы VI
где R9 - R13 и q обозначены выше,
в присутствии апротонной кислоты, кислоты Льюиса или металлоорганического соединения и инициатора, выбранного из группы, включающей воду, спирт, фенол, ацеталь или аддукт простого винилового эфира и карбоновой кислоты.11. A method of obtaining a simple polyvinyl ether of General formula V
where R 9 , R 10 and R 11 are each hydrogen atom or a hydrocarbon group with C 1 - C 8 and may be the same or different;
R 12 is a divalent hydrocarbon group with C 2 - C 10 ;
R 13 is a hydrocarbon group with C 1 - C 10 ;
q is a number whose average value is in the range 0 - 10;
R 12 may be the same or different when there are several groups of R 12 O,
characterized in that the polymerization of the vinyl ether monomer of the general formula VI is carried out
where R 9 - R 13 and q are indicated above,
in the presence of aprotic acid, Lewis acid, or an organometallic compound and an initiator selected from the group consisting of water, alcohol, phenol, acetal, or the adduct of vinyl ether and carboxylic acid.
где R14, R15 и R16 - каждый атом водорода или углеводородная группа с C1 - C8 и могут быть одинаковыми или разными;
R17 и R18 - каждый двухвалентная углеводородная группа с C2 - C10 и могут быть одинаковыми или разными;
R19 и R20 - каждый углеводородная группа с C1 - C10 и могут быть одинаковыми или разными;
s и r - каждый число, среднее значение которого находится в диапазоне 0 - 10;
R17О могут быть одинаковыми или разными, когда имеется несколько группировок R17О;
R19О могут быть одинаковыми или разными, когда имеется несколько группировок R19О.12. The method according to claim 11, characterized in that the polymerization of a simple vinyl ether of General formula VI is carried out in the presence of Lewis acid and acetal of General formula VII
where R 14 , R 15 and R 16 are each hydrogen atom or a hydrocarbon group with C 1 - C 8 and may be the same or different;
R 17 and R 18 are each divalent hydrocarbon group with C 2 - C 10 and may be the same or different;
R 19 and R 20 are each C 1 - C 10 hydrocarbon group and may be the same or different;
s and r - each number whose average value is in the range 0 - 10;
R 17 O may be the same or different when there are several groups of R 17 O;
R 19 O may be the same or different when there are several groups of R 19 O.
где R9 - R13 и q имеют значения в соответствии с п.10;
R21 - двухвалентная углеводородная группа с C2 - C10;
R22 - углеводородная группа с C1 - C10;
t - число, среднее значение которого находится в диапазоне 0 - 10;
R21О - могут быть одинаковыми или разными, когда имеется несколько группировок R21О,
путем добавления простого винилового эфира общей формулы VI к спирту общей формулы
R22(OR21)tOH,
где R22, R21 и t имеют значения, соответствующие общей формуле VIII,
в присутствии кислоты Льюиса в качестве катализатора, затем к полученному ацеталю добавляют новую порцию простого винилового эфира общей формулы VI и проводят полимеризацию.13. The method according to claim 11, characterized in that the acetal of general formula VIII is first obtained
where R 9 - R 13 and q have the meanings in accordance with paragraph 10;
R 21 is a divalent hydrocarbon group with C 2 - C 10 ;
R 22 is a hydrocarbon group with C 1 - C 10 ;
t is a number whose average value is in the range 0 - 10;
R 21 O - may be the same or different when there are several groups of R 21 O,
by adding a vinyl ether of general formula VI to an alcohol of general formula
R 22 (OR 21 ) t OH,
where R 22 , R 21 and t have the meanings corresponding to the general formula VIII,
in the presence of a Lewis acid as a catalyst, then a new portion of the vinyl ether of general formula VI is added to the obtained acetal and polymerization is carried out.
где R9 - R13 и q имеют значения, соответствующие общей формуле V по п. 11.16. Lubricating oil for compressor-type refrigerators, including, as a main component, polyvinyl ether of the general formula IX
where R 9 - R 13 and q have the meanings corresponding to the general formula V according to claim 11.
где R23, R24, R25 - каждый атом водорода или углеводородная группа с C1 - C8 и могут быть одинаковыми или разными;
R26 - двухвалентная углеводородная группа с C2 - C20;
R27 - углеводородная группа с C1 - C10;
а - число, среднее значение которого находится в диапазоне 0 - 10;
R26О могут быть одинаковыми или разными, когда имеется несколько группировок R26О,
а другое концевое звено выражено общей формулой XI
где R28, R29 и R30 - каждый атом водорода или углеводородная группа с C1 - C8 и могут быть одинаковыми или разными;
R31 - двухвалентная углеводородная группа с C2 - C10;
R32 - углеводородная группа с C1 - C10;
b - число, среднее значение которого находится в диапазоне 0 - 10;
R31О - могут быть одинаковыми или разными, когда имеется несколько группировок R31О.17. Lubricating oil according to clause 16, characterized in that one end chain link of a simple polyvinyl ether is expressed by the general formula X
where R 23 , R 24 , R 25 is each hydrogen atom or a hydrocarbon group with C 1 - C 8 and may be the same or different;
R 26 is a divalent hydrocarbon group with C 2 - C 20 ;
R 27 is a hydrocarbon group with C 1 - C 10 ;
and - a number whose average value is in the range 0 - 10;
R 26 O may be the same or different when there are several groups of R 26 O,
and the other end link is expressed by the general formula XI
where R 28 , R 29 and R 30 are each hydrogen atom or a hydrocarbon group with C 1 - C 8 and may be the same or different;
R 31 is a divalent hydrocarbon group with C 2 - C 10 ;
R 32 is a hydrocarbon group with C 1 - C 10 ;
b is a number whose average value is in the range 0 - 10;
R 31 O - may be the same or different when there are several groups of R 31 O.
где R33, R34, R35 - каждый атом водорода или углеводородная группа с C1 - C8 и могут быть одинаковыми или разными;
R36 и R38 - каждый двухвалентная углеводородная группа с C2 - C10 и могут быть одинаковыми или разными;
R37 и R39 - каждая углеводородная группа с C1 - C10 и могут быть одинаковыми или разными;
c и d - число, среднее значение которого находится в диапазоне 0 - 10, и могут быть одинаковыми или разными;
R36О могут быть одинаковыми или разными, когда имеется несколько группировок R36О.18. Lubricating oil according to claim 17, characterized in that one end chain link of a simple polyvinyl ether is expressed by the general formula X, and the other by the general formula XII
where R 33 , R 34 , R 35 is each hydrogen atom or a hydrocarbon group with C 1 - C 8 and may be the same or different;
R 36 and R 38 are each divalent hydrocarbon group with C 2 - C 10 and may be the same or different;
R 37 and R 39 - each hydrocarbon group with C 1 - C 10 and may be the same or different;
c and d - a number whose average value is in the range 0 - 10, and can be the same or different;
R 36 O may be the same or different when there are several groups of R 36 O.
где R40, R41 и R42 - каждый атом водорода или углеводородная группа с C1 - C8 и могут быть одинаковыми или разными.20. Lubricating oil according to clause 16, characterized in that one end link of a simple polyvinyl ether is expressed by the general formula XIII
where R 40 , R 41 and R 42 are each hydrogen atom or a hydrocarbon group with C 1 - C 8 and may be the same or different.
25.05.93 по пп.1 - 10;
04.06.92 по пп.11 - 29.Priority on points:
05/25/93 according to claims 1 to 10;
06/04/92 according to claims 11-29.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP143922/1992 | 1992-06-04 | ||
| JP143922/92 | 1992-06-04 | ||
| JP14392292 | 1992-06-04 | ||
| JP237842/1992 | 1992-09-07 | ||
| PCT/JP1993/000690 WO1993024435A1 (en) | 1992-06-04 | 1993-05-25 | Polyvinyl ether compound and lubricating oil |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU99112121/04A Division RU2182571C2 (en) | 1992-06-04 | 1993-05-25 | Method of synthesis of ether |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU94046370A RU94046370A (en) | 1996-10-10 |
| RU2139889C1 true RU2139889C1 (en) | 1999-10-20 |
Family
ID=15350222
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU94046370/04A RU2139889C1 (en) | 1992-06-04 | 1993-05-25 | Polyvinyl ether (variants), method of preparation thereof and lubricating oil based thereon for rifrigerators |
Country Status (2)
| Country | Link |
|---|---|
| CN (1) | CN100375738C (en) |
| RU (1) | RU2139889C1 (en) |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2487525A (en) * | 1949-11-08 | Dialkylidene diethers | ||
| US2165962A (en) * | 1936-10-29 | 1939-07-11 | Ig Farbenindustrie Ag | Production of alkylidene diethers or ether-esters |
| DE2434057C2 (en) * | 1974-07-16 | 1982-08-19 | Hoechst Ag, 6000 Frankfurt | Process for the production of glycol dimethyl ethers |
-
1993
- 1993-05-25 RU RU94046370/04A patent/RU2139889C1/en not_active IP Right Cessation
- 1993-06-04 CN CNB001353756A patent/CN100375738C/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| CN100375738C (en) | 2008-03-19 |
| RU94046370A (en) | 1996-10-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1059279B1 (en) | Polyvinyl ether compound and method of preperation | |
| US6656891B1 (en) | Refrigerating machine oil composition | |
| JP3173684B2 (en) | Lubricating oil for compression refrigerators | |
| JP5069120B2 (en) | Lubricating oil for compression type refrigerators | |
| US7927503B2 (en) | Lubricant for compression type refrigerating machine and refrigerating device using same | |
| RU2139919C1 (en) | Lubricating oil for compression refrigerators (versions) | |
| JP3583175B2 (en) | Lubricating oil for compression refrigerators | |
| US20100132397A1 (en) | Lubricant for compression refrigerating machine and refrigerating apparatus using the same | |
| RU2139889C1 (en) | Polyvinyl ether (variants), method of preparation thereof and lubricating oil based thereon for rifrigerators | |
| JP3163594B2 (en) | Polyvinyl ether compound | |
| JP4132209B2 (en) | Fluid composition for refrigerator | |
| KR100264423B1 (en) | Lubricating oil for compression-type refrigerators comprising an improved polyvinyl ether compound | |
| JP3163593B2 (en) | Polyvinyl ether compound | |
| JPH04275397A (en) | Lubricating oil for compression-type refrigerating machine and production thereof | |
| JPH07179872A (en) | Production of lubricating oil for compression refrigerator |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20030526 |