KR20220149352A - Composition for preventing or treating autoimmune disease comprising compound isolated from Paeonia lactiflora extract as effective component - Google Patents
Composition for preventing or treating autoimmune disease comprising compound isolated from Paeonia lactiflora extract as effective component Download PDFInfo
- Publication number
- KR20220149352A KR20220149352A KR1020210056874A KR20210056874A KR20220149352A KR 20220149352 A KR20220149352 A KR 20220149352A KR 1020210056874 A KR1020210056874 A KR 1020210056874A KR 20210056874 A KR20210056874 A KR 20210056874A KR 20220149352 A KR20220149352 A KR 20220149352A
- Authority
- KR
- South Korea
- Prior art keywords
- acid
- preventing
- autoimmune diseases
- pharmaceutical composition
- treating autoimmune
- Prior art date
Links
- 208000023275 Autoimmune disease Diseases 0.000 title claims abstract description 58
- 239000000203 mixture Substances 0.000 title claims abstract description 54
- 150000001875 compounds Chemical class 0.000 title claims abstract description 52
- 239000000284 extract Substances 0.000 title claims abstract description 50
- 244000236658 Paeonia lactiflora Species 0.000 title 1
- 235000008598 Paeonia lactiflora Nutrition 0.000 title 1
- 150000003839 salts Chemical class 0.000 claims abstract description 34
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 141
- 235000004347 Perilla Nutrition 0.000 claims description 123
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 claims description 51
- 239000000469 ethanolic extract Substances 0.000 claims description 50
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 claims description 48
- 239000008194 pharmaceutical composition Substances 0.000 claims description 39
- 238000000034 method Methods 0.000 claims description 38
- 239000002904 solvent Substances 0.000 claims description 33
- 239000004480 active ingredient Substances 0.000 claims description 31
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 30
- 239000002037 dichloromethane fraction Substances 0.000 claims description 30
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 claims description 27
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 26
- 238000005194 fractionation Methods 0.000 claims description 22
- 238000000605 extraction Methods 0.000 claims description 21
- 235000013305 food Nutrition 0.000 claims description 16
- 238000000926 separation method Methods 0.000 claims description 12
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims description 9
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 claims description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims description 9
- 238000009472 formulation Methods 0.000 claims description 9
- 238000010898 silica gel chromatography Methods 0.000 claims description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 8
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 8
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 claims description 6
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 claims description 6
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 claims description 6
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 6
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 claims description 6
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 claims description 6
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 claims description 6
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 claims description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 claims description 6
- 150000007522 mineralic acids Chemical class 0.000 claims description 6
- 150000007524 organic acids Chemical class 0.000 claims description 6
- 239000003085 diluting agent Substances 0.000 claims description 5
- 239000007788 liquid Substances 0.000 claims description 5
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims description 4
- 239000000843 powder Substances 0.000 claims description 4
- 239000000725 suspension Substances 0.000 claims description 4
- 235000020357 syrup Nutrition 0.000 claims description 4
- 239000006188 syrup Substances 0.000 claims description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 claims description 4
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 claims description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 claims description 3
- 239000005711 Benzoic acid Substances 0.000 claims description 3
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 claims description 3
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 claims description 3
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 claims description 3
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 claims description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 claims description 3
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 claims description 3
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 claims description 3
- 235000011054 acetic acid Nutrition 0.000 claims description 3
- 239000000443 aerosol Substances 0.000 claims description 3
- 235000003704 aspartic acid Nutrition 0.000 claims description 3
- 235000010233 benzoic acid Nutrition 0.000 claims description 3
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 claims description 3
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 claims description 3
- 239000002775 capsule Substances 0.000 claims description 3
- 235000015165 citric acid Nutrition 0.000 claims description 3
- 239000006071 cream Substances 0.000 claims description 3
- 235000019253 formic acid Nutrition 0.000 claims description 3
- 239000000499 gel Substances 0.000 claims description 3
- 239000000174 gluconic acid Substances 0.000 claims description 3
- 235000012208 gluconic acid Nutrition 0.000 claims description 3
- 235000013922 glutamic acid Nutrition 0.000 claims description 3
- 239000004220 glutamic acid Substances 0.000 claims description 3
- 239000008187 granular material Substances 0.000 claims description 3
- 238000002347 injection Methods 0.000 claims description 3
- 239000007924 injection Substances 0.000 claims description 3
- 150000007529 inorganic bases Chemical class 0.000 claims description 3
- 239000004310 lactic acid Substances 0.000 claims description 3
- 235000014655 lactic acid Nutrition 0.000 claims description 3
- 239000006210 lotion Substances 0.000 claims description 3
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 claims description 3
- 239000011976 maleic acid Substances 0.000 claims description 3
- 229940098779 methanesulfonic acid Drugs 0.000 claims description 3
- 239000002674 ointment Substances 0.000 claims description 3
- 235000006408 oxalic acid Nutrition 0.000 claims description 3
- 239000006187 pill Substances 0.000 claims description 3
- 235000019260 propionic acid Nutrition 0.000 claims description 3
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 claims description 3
- 239000003826 tablet Substances 0.000 claims description 3
- 239000011975 tartaric acid Substances 0.000 claims description 3
- 235000002906 tartaric acid Nutrition 0.000 claims description 3
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 claims description 3
- STGNLGBPLOVYMA-MAZDBSFSSA-N (E)-but-2-enedioic acid Chemical compound OC(=O)\C=C\C(O)=O.OC(=O)\C=C\C(O)=O STGNLGBPLOVYMA-MAZDBSFSSA-N 0.000 claims description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 claims description 2
- 238000001467 acupuncture Methods 0.000 claims description 2
- 239000012530 fluid Substances 0.000 claims description 2
- 150000007530 organic bases Chemical class 0.000 claims description 2
- 239000011574 phosphorus Substances 0.000 claims description 2
- 229910052698 phosphorus Inorganic materials 0.000 claims description 2
- 241000229722 Perilla <angiosperm> Species 0.000 claims 7
- 244000124853 Perilla frutescens Species 0.000 abstract description 117
- 239000000126 substance Substances 0.000 abstract description 2
- 235000004348 Perilla frutescens Nutrition 0.000 abstract 1
- 102000013691 Interleukin-17 Human genes 0.000 description 59
- 108050003558 Interleukin-17 Proteins 0.000 description 59
- OXVUXGFZHDKYLS-BLIWDXROSA-N Tormentic acid Chemical compound C1[C@@H](O)[C@H](O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C(O)=O)CC[C@@H](C)[C@](O)(C)[C@H]5C4=CC[C@@H]3[C@]21C OXVUXGFZHDKYLS-BLIWDXROSA-N 0.000 description 40
- BLFLLBZGZJTVJG-UHFFFAOYSA-N benzocaine Chemical compound CCOC(=O)C1=CC=C(N)C=C1 BLFLLBZGZJTVJG-UHFFFAOYSA-N 0.000 description 30
- 230000001988 toxicity Effects 0.000 description 20
- 231100000419 toxicity Toxicity 0.000 description 20
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 19
- 238000011156 evaluation Methods 0.000 description 18
- 210000004027 cell Anatomy 0.000 description 17
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- 201000010099 disease Diseases 0.000 description 15
- DOUMFZQKYFQNTF-WUTVXBCWSA-N (R)-rosmarinic acid Chemical compound C([C@H](C(=O)O)OC(=O)\C=C\C=1C=C(O)C(O)=CC=1)C1=CC=C(O)C(O)=C1 DOUMFZQKYFQNTF-WUTVXBCWSA-N 0.000 description 14
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 14
- 235000019439 ethyl acetate Nutrition 0.000 description 14
- 230000000694 effects Effects 0.000 description 13
- 230000002757 inflammatory effect Effects 0.000 description 13
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 12
- 210000000068 Th17 cell Anatomy 0.000 description 12
- 230000002401 inhibitory effect Effects 0.000 description 12
- 238000005259 measurement Methods 0.000 description 12
- 230000008569 process Effects 0.000 description 12
- 210000000936 intestine Anatomy 0.000 description 11
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- 208000004232 Enteritis Diseases 0.000 description 9
- 241000699670 Mus sp. Species 0.000 description 9
- 230000037396 body weight Effects 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 8
- 239000002253 acid Substances 0.000 description 8
- 239000003814 drug Substances 0.000 description 8
- 206010061218 Inflammation Diseases 0.000 description 7
- 108090001005 Interleukin-6 Proteins 0.000 description 7
- ZZAFFYPNLYCDEP-HNNXBMFYSA-N Rosmarinsaeure Natural products OC(=O)[C@H](Cc1cccc(O)c1O)OC(=O)C=Cc2ccc(O)c(O)c2 ZZAFFYPNLYCDEP-HNNXBMFYSA-N 0.000 description 7
- 210000001744 T-lymphocyte Anatomy 0.000 description 7
- 230000004069 differentiation Effects 0.000 description 7
- 230000004054 inflammatory process Effects 0.000 description 7
- 230000005764 inhibitory process Effects 0.000 description 7
- KBOPZPXVLCULAV-UHFFFAOYSA-N mesalamine Chemical compound NC1=CC=C(O)C(C(O)=O)=C1 KBOPZPXVLCULAV-UHFFFAOYSA-N 0.000 description 7
- 229960004963 mesalazine Drugs 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 206010039073 rheumatoid arthritis Diseases 0.000 description 7
- DOUMFZQKYFQNTF-MRXNPFEDSA-N rosemarinic acid Natural products C([C@H](C(=O)O)OC(=O)C=CC=1C=C(O)C(O)=CC=1)C1=CC=C(O)C(O)=C1 DOUMFZQKYFQNTF-MRXNPFEDSA-N 0.000 description 7
- TVHVQJFBWRLYOD-UHFFFAOYSA-N rosmarinic acid Natural products OC(=O)C(Cc1ccc(O)c(O)c1)OC(=Cc2ccc(O)c(O)c2)C=O TVHVQJFBWRLYOD-UHFFFAOYSA-N 0.000 description 7
- VULLSLYDWNGNKZ-UHFFFAOYSA-N 12319Tetrahydroxyurs-12-en-28-oic acid Natural products OC1C(O)C(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C)C(O)(C)C5C4=CCC3C21C VULLSLYDWNGNKZ-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- 208000011231 Crohn disease Diseases 0.000 description 6
- OXVUXGFZHDKYLS-UHFFFAOYSA-N Jacarandic acid Natural products C1C(O)C(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C)C(O)(C)C5C4=CCC3C21C OXVUXGFZHDKYLS-UHFFFAOYSA-N 0.000 description 6
- 244000269722 Thea sinensis Species 0.000 description 6
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 6
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 6
- 230000003833 cell viability Effects 0.000 description 6
- 210000004748 cultured cell Anatomy 0.000 description 6
- 235000013399 edible fruits Nutrition 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 6
- 239000003981 vehicle Substances 0.000 description 6
- 102000004127 Cytokines Human genes 0.000 description 5
- 108090000695 Cytokines Proteins 0.000 description 5
- 238000010171 animal model Methods 0.000 description 5
- 239000012223 aqueous fraction Substances 0.000 description 5
- 239000002034 butanolic fraction Substances 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 235000009569 green tea Nutrition 0.000 description 5
- 230000006872 improvement Effects 0.000 description 5
- 230000002265 prevention Effects 0.000 description 5
- 239000012453 solvate Substances 0.000 description 5
- 210000000952 spleen Anatomy 0.000 description 5
- WCGUUGGRBIKTOS-GPOJBZKASA-N (3beta)-3-hydroxyurs-12-en-28-oic acid Chemical compound C1C[C@H](O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C(O)=O)CC[C@@H](C)[C@H](C)[C@H]5C4=CC[C@@H]3[C@]21C WCGUUGGRBIKTOS-GPOJBZKASA-N 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 239000011324 bead Substances 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- -1 for example Substances 0.000 description 4
- 230000036732 histological change Effects 0.000 description 4
- 230000000968 intestinal effect Effects 0.000 description 4
- 238000002826 magnetic-activated cell sorting Methods 0.000 description 4
- 239000003960 organic solvent Substances 0.000 description 4
- 210000000496 pancreas Anatomy 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 239000000377 silicon dioxide Substances 0.000 description 4
- 229940096998 ursolic acid Drugs 0.000 description 4
- PLSAJKYPRJGMHO-UHFFFAOYSA-N ursolic acid Natural products CC1CCC2(CCC3(C)C(C=CC4C5(C)CCC(O)C(C)(C)C5CCC34C)C2C1C)C(=O)O PLSAJKYPRJGMHO-UHFFFAOYSA-N 0.000 description 4
- 241000723353 Chrysanthemum Species 0.000 description 3
- 235000007516 Chrysanthemum Nutrition 0.000 description 3
- 101000693735 Homo sapiens Prefoldin subunit 4 Proteins 0.000 description 3
- 235000006964 Perilla frutescens var acuta Nutrition 0.000 description 3
- 240000001979 Perilla frutescens var. acuta Species 0.000 description 3
- 102100025542 Prefoldin subunit 4 Human genes 0.000 description 3
- 102000040945 Transcription factor Human genes 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- 230000005856 abnormality Effects 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 235000008504 concentrate Nutrition 0.000 description 3
- 239000012141 concentrate Substances 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 239000002038 ethyl acetate fraction Substances 0.000 description 3
- 239000002044 hexane fraction Substances 0.000 description 3
- 210000001503 joint Anatomy 0.000 description 3
- 210000001165 lymph node Anatomy 0.000 description 3
- 210000004400 mucous membrane Anatomy 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 210000003289 regulatory T cell Anatomy 0.000 description 3
- 210000003491 skin Anatomy 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 229940124597 therapeutic agent Drugs 0.000 description 3
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 208000035186 Hemolytic Autoimmune Anemia Diseases 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 238000005481 NMR spectroscopy Methods 0.000 description 2
- 230000002159 abnormal effect Effects 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- 230000001363 autoimmune Effects 0.000 description 2
- 201000000448 autoimmune hemolytic anemia Diseases 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 238000001460 carbon-13 nuclear magnetic resonance spectrum Methods 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229940125904 compound 1 Drugs 0.000 description 2
- 235000009508 confectionery Nutrition 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- 238000002481 ethanol extraction Methods 0.000 description 2
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 2
- 235000013376 functional food Nutrition 0.000 description 2
- 241000411851 herbal medicine Species 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 238000010212 intracellular staining Methods 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- VMGAPWLDMVPYIA-HIDZBRGKSA-N n'-amino-n-iminomethanimidamide Chemical compound N\N=C\N=N VMGAPWLDMVPYIA-HIDZBRGKSA-N 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000010287 polarization Effects 0.000 description 2
- 230000003449 preventive effect Effects 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- JUJWROOIHBZHMG-RALIUCGRSA-N pyridine-d5 Chemical compound [2H]C1=NC([2H])=C([2H])C([2H])=C1[2H] JUJWROOIHBZHMG-RALIUCGRSA-N 0.000 description 2
- BOLDJAUMGUJJKM-LSDHHAIUSA-N renifolin D Natural products CC(=C)[C@@H]1Cc2c(O)c(O)ccc2[C@H]1CC(=O)c3ccc(O)cc3O BOLDJAUMGUJJKM-LSDHHAIUSA-N 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N Acetylene Chemical compound C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 208000006820 Arthralgia Diseases 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 238000011740 C57BL/6 mouse Methods 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 201000003066 Diffuse Scleroderma Diseases 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 206010017533 Fungal infection Diseases 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 1
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 1
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 1
- 208000003807 Graves Disease Diseases 0.000 description 1
- 208000015023 Graves' disease Diseases 0.000 description 1
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 1
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 1
- 101000716102 Homo sapiens T-cell surface glycoprotein CD4 Proteins 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102100026878 Interleukin-2 receptor subunit alpha Human genes 0.000 description 1
- 102100030703 Interleukin-22 Human genes 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 241000207923 Lamiaceae Species 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 208000031888 Mycoses Diseases 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 201000009594 Systemic Scleroderma Diseases 0.000 description 1
- 206010042953 Systemic sclerosis Diseases 0.000 description 1
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 description 1
- 210000000662 T-lymphocyte subset Anatomy 0.000 description 1
- 208000025865 Ulcer Diseases 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 235000013334 alcoholic beverage Nutrition 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 1
- 210000000436 anus Anatomy 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 230000005784 autoimmunity Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 208000022362 bacterial infectious disease Diseases 0.000 description 1
- 235000013361 beverage Nutrition 0.000 description 1
- 238000012472 bioassay-guided isolation Methods 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- FUFJGUQYACFECW-UHFFFAOYSA-L calcium hydrogenphosphate Chemical compound [Ca+2].OP([O-])([O-])=O FUFJGUQYACFECW-UHFFFAOYSA-L 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 235000019219 chocolate Nutrition 0.000 description 1
- 210000001612 chondrocyte Anatomy 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000037976 chronic inflammation Diseases 0.000 description 1
- 230000006020 chronic inflammation Effects 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 235000013365 dairy product Nutrition 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 235000019700 dicalcium phosphate Nutrition 0.000 description 1
- WBKFWQBXFREOFH-UHFFFAOYSA-N dichloromethane;ethyl acetate Chemical compound ClCCl.CCOC(C)=O WBKFWQBXFREOFH-UHFFFAOYSA-N 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 239000003651 drinking water Substances 0.000 description 1
- 235000020188 drinking water Nutrition 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 210000001508 eye Anatomy 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 235000012041 food component Nutrition 0.000 description 1
- 239000005417 food ingredient Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 210000001280 germinal center Anatomy 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 235000013402 health food Nutrition 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 210000002443 helper t lymphocyte Anatomy 0.000 description 1
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 1
- 125000004404 heteroalkyl group Chemical group 0.000 description 1
- 125000001072 heteroaryl group Chemical group 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 230000004957 immunoregulator effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 229910001867 inorganic solvent Inorganic materials 0.000 description 1
- 239000003049 inorganic solvent Substances 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 108010074108 interleukin-21 Proteins 0.000 description 1
- 108010074109 interleukin-22 Proteins 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- PGHMRUGBZOYCAA-ADZNBVRBSA-N ionomycin Chemical compound O1[C@H](C[C@H](O)[C@H](C)[C@H](O)[C@H](C)/C=C/C[C@@H](C)C[C@@H](C)C(/O)=C/C(=O)[C@@H](C)C[C@@H](C)C[C@@H](CCC(O)=O)C)CC[C@@]1(C)[C@@H]1O[C@](C)([C@@H](C)O)CC1 PGHMRUGBZOYCAA-ADZNBVRBSA-N 0.000 description 1
- PGHMRUGBZOYCAA-UHFFFAOYSA-N ionomycin Natural products O1C(CC(O)C(C)C(O)C(C)C=CCC(C)CC(C)C(O)=CC(=O)C(C)CC(C)CC(CCC(O)=O)C)CCC1(C)C1OC(C)(C(C)O)CC1 PGHMRUGBZOYCAA-UHFFFAOYSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 229940031703 low substituted hydroxypropyl cellulose Drugs 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 206010025135 lupus erythematosus Diseases 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 238000003808 methanol extraction Methods 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 235000013336 milk Nutrition 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- 210000004080 milk Anatomy 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- 230000004682 mucosal barrier function Effects 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 231100001083 no cytotoxicity Toxicity 0.000 description 1
- 239000012454 non-polar solvent Substances 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 210000000963 osteoblast Anatomy 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 239000000419 plant extract Substances 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000009703 regulation of cell differentiation Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 235000011888 snacks Nutrition 0.000 description 1
- 229940079832 sodium starch glycolate Drugs 0.000 description 1
- 239000008109 sodium starch glycolate Substances 0.000 description 1
- 229920003109 sodium starch glycolate Polymers 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 210000002437 synoviocyte Anatomy 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 235000013616 tea Nutrition 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 230000037317 transdermal delivery Effects 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 238000002137 ultrasound extraction Methods 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 150000003722 vitamin derivatives Chemical class 0.000 description 1
- 238000003809 water extraction Methods 0.000 description 1
- 235000013618 yogurt Nutrition 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/53—Lamiaceae or Labiatae (Mint family), e.g. thyme, rosemary or lavender
- A61K36/535—Perilla (beefsteak plant)
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/105—Plant extracts, their artificial duplicates or their derivatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/191—Carboxylic acids, e.g. valproic acid having two or more hydroxy groups, e.g. gluconic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2200/00—Function of food ingredients
- A23V2200/30—Foods, ingredients or supplements having a functional effect on health
- A23V2200/324—Foods, ingredients or supplements having a functional effect on health having an effect on the immune system
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2250/00—Food ingredients
- A23V2250/30—Other Organic compounds
Abstract
Description
자소엽 (Perilla leaves, Perilla frutescens var. acuta)에서 분리한 화합물을 유효성분으로 포함하는 자가면역질환 예방 및 치료용 조성물에 관한 것으로서, 보다 구체적으로는 자소엽 추출물로부터 분리한 화합물을 유효성분으로 포함하고 Th17 세포로의 분화 및 IL-17의 생성을 억제하여 자가면역질환의 예방, 개선 또는 치료에 사용될 수 있는 조성물에 관한 것이다. It relates to a composition for preventing and treating autoimmune diseases comprising a compound isolated from perilla leaves, Perilla frutescens var. acuta as an active ingredient, and more specifically, comprising a compound isolated from perilla leaf extract as an active ingredient And it relates to a composition that can be used for the prevention, improvement or treatment of autoimmune diseases by inhibiting the differentiation into Th17 cells and the production of IL-17.
CD4+ T세포는 특정 사이토카인과 전사인자의 발현에 따라 Th1 (T helper type1), Th2 (T helper type2), CD4+CD25+ 면역조절 T세포 (regulatory T cell)와 Th17 세포 (T helper 17 cell) 등의 아형으로 구분될 수 있다. 이 중 IL-17을 생산하는 Th17 세포는 동물모델과 인간세포 연구 결과들을 통해 염증 및 자가면역 병인에 직접적인 역할과 병원체에 대한 숙주 방어 또는 이상 면역반응 유도 등의 역할이 규명되었다. IL-17과 Th17 세포가 염증과 자가면역질환에서 주요 병인 역할이 규명되면서 이들에 대한 억제와 조절이 질환 치료를 위한 중요 전략으로 제안되었고, Th17 세포계열 사이토카인의 억제, 중화 및 특이 전사인자들의 억제 조절을 통한 잠재적 표적 치료 방법 등이 연구되고 있는 상황이다.According to the expression of specific cytokines and transcription factors, CD4 + T cells are Th1 (T helper type1), Th2 (T helper type2), CD4 + CD25 + immunoregulatory T cells (regulatory T cells) and Th17 cells (
류마티스 관절염은 신체 여러 조직 및 장기에 영향을 미치는 자가면역질환이다. 그 증상으로 손가락 마디 등의 관절에 심각한 통증을 야기하고 관절 이외에 근육, 폐, 심장, 피부, 혈관, 신경 및 눈 등의 여러 장기에도 이상을 초래한다. 비록 상기 증상이 현저하게 나타나지 않더라도 시간의 변화에 따라 점차적으로 진행되어 관절 손상 및 기능적 이상을 초래하는 질환으로 발전된다. Rheumatoid arthritis is an autoimmune disease that affects various tissues and organs in the body. As a symptom, it causes severe pain in joints such as knuckles and causes abnormalities in various organs such as muscles, lungs, heart, skin, blood vessels, nerves and eyes in addition to joints. Although the above symptoms do not appear significantly, it gradually progresses with time and develops into a disease that causes joint damage and functional abnormalities.
크론병은 입에서 항문에 이르는 소화관의 임의의 부위에 궤양 등의 병변이 비연속적으로 발생하는 질환으로서, 그 증상으로 복통, 설사등이 빈발하고 중증의 경우 발열, 하혈 등이 나타난다. Crohn's disease is a disease in which lesions such as ulcers occur discontinuously in any part of the digestive tract from the mouth to the anus.
류마티스 관절염과 크론병 등의 자가면역질환은 TH17의 분화에 따른 IL-17의 발현량의 증가가 그 원인의 하나로 보고되어 있다. 실제로 IL-17는 G-CSF와 GM-CSF의 발현 촉진을 통해 과립백혈구 형성 (granulopoiesis)을 향상시키며 종자중심 (germinal center) 형성과 자가항체 생산을 촉진하는 효과가 관찰된다. 이와 관련하여 염증성 자가 면역질환인 류마티스 관절염 환자의 경우 혈청에서 IL-17이 높게 검출되며 IL-17A는 류마티스 관절염 환자의 활막세포 내 IL-1β 와 IL-6의 발현을 유도시킨다. 또한, IL-17의 주요기능으로 연골세포와 조골세포 (osteoblasts) 내 기질 생산을 억제시켜 관절 손상을 일으키고 조직재생의 결핍에 이르게 한다고 알려져 있다. In autoimmune diseases such as rheumatoid arthritis and Crohn's disease, an increase in the expression level of IL-17 according to the differentiation of TH17 has been reported as one of the causes. In fact, IL-17 enhances granulopoiesis by promoting the expression of G-CSF and GM-CSF, and has the effect of promoting the formation of germinal centers and the production of autoantibodies. In this regard, in patients with rheumatoid arthritis, an inflammatory autoimmune disease, IL-17 is detected high in serum, and IL-17A induces the expression of IL-1β and IL-6 in the synovial cells of rheumatoid arthritis patients. In addition, as a major function of IL-17, it is known that it inhibits matrix production in chondrocytes and osteoblasts, causing joint damage and leading to a lack of tissue regeneration.
류마티스 관절염이나 크론병과 같은 자가면역질환은 현재까지도 그 치료 또는 예방제가 제공되지 않아 많은 환자가 고통을 겪고 있다. 따라서, 효과가 우수하면서도, 안전하고 부작용을 일으키지 않는 자가면역질환의 예방 및 치료제의 개발이 절실히 요구된다. Autoimmune diseases, such as rheumatoid arthritis and Crohn's disease, have not yet been treated or prevented, and many patients suffer. Therefore, there is an urgent need to develop a preventive and therapeutic agent for autoimmune diseases that is effective and does not cause side effects while being safe.
본 발명의 연구자들은 류마티스 관절염이나 염증성 장질환, 크론병과 같은 자가면역질환의 예방 및 치료제를 개발하던 중 자소엽 추출물과 이로부터 분리한 화합물인 토멘트산 (tormentic acid)이 이와 같은 질병에 유효하게 적용될 수 있다는 것을 발견하여 본 발명을 완성하였다. The researchers of the present invention were developing a preventive and therapeutic agent for autoimmune diseases such as rheumatoid arthritis, inflammatory bowel disease, and Crohn's disease. The present invention has been completed by finding that it can be applied.
일 양상은 자소엽 추출물로부터 분리한 화학식 1로 표시되는 화합물 또는 이의 약학적으로 허용 가능한 염을 유효성분으로 포함하는 자가면역질환 예방 또는 치료용 약학적 조성물에 관한 것이다.One aspect relates to a pharmaceutical composition for preventing or treating autoimmune diseases, comprising as an active ingredient the compound represented by Formula 1 or a pharmaceutically acceptable salt thereof isolated from a perilla leaf extract.
다른 일 양상은 상기 자가면역질환 예방 또는 치료용 약학적 조성물의 제조 방법에 관한 것이다. Another aspect relates to a method of preparing a pharmaceutical composition for preventing or treating the autoimmune disease.
다른 일 양상은 자소엽 추출물로부터 분리한 화학식 1로 표시되는 화합물 또는 이의 약학적으로 허용 가능한 염을 유효성분으로 포함하는 자가면역질환 예방 또는 개선용 식품학적 조성물에 관한 것이다.Another aspect relates to a food composition for preventing or improving autoimmune diseases, comprising as an active ingredient the compound represented by Formula 1 or a pharmaceutically acceptable salt thereof isolated from the perilla leaf extract.
다른 일 양상은 상기 조성물을 이용한 자가면역질환의 예방, 치료, 또는 개선 방법에 관한 것이다. Another aspect relates to a method for preventing, treating, or improving an autoimmune disease using the composition.
(1) 자소엽 추출물로부터 분리된 하기 화학식 1로 표시되는 화합물 또는 그의 염을 유효성분으로 포함하는 자가면역질환 예방 또는 치료용 약학적 조성물:(1) A pharmaceutical composition for preventing or treating autoimmune diseases, comprising as an active ingredient a compound represented by the following formula (1) or a salt thereof isolated from the perilla leaf extract:
[화학식 1][Formula 1]
. .
(2) 상기 자소엽 추출물의 추출용매는 물, C1 내지 C4의 알코올 또는 이들의 혼합물인 것인 자가면역질환 예방 또는 치료용 약학적 조성물. (2) The extraction solvent of the perilla leaf extract is water, C 1 to C 4 alcohol, or a mixture thereof. A pharmaceutical composition for preventing or treating autoimmune diseases.
(3) 상기 화합물은 자소엽 추출물에 물, C1 내지 C5의 직쇄 또는 분지형 알코올, 헥산, 디클로로메탄, 및 에틸아세테이트로 이루어진 군에서 선택된 1종 이상의 용매를 첨가하여 분리되는 것인 자가면역질환 예방 또는 치료용 약학적 조성물. (3) the compound is isolated by adding one or more solvents selected from the group consisting of water, C 1 to C 5 linear or branched alcohol, hexane, dichloromethane, and ethyl acetate to the perilla leaf extract. A pharmaceutical composition for preventing or treating a disease.
(4) 상기 화합물은 자소엽 추출물에 헥산, 디클로로메탄, 에틸아세테이트, 부탄올 및 물로 이루어진 군에서 선택된 1종 이상의 용매를 첨가하여 분리되는 것인 자가면역질환 예방 또는 치료용 약학적 조성물. (4) The compound is a pharmaceutical composition for preventing or treating autoimmune diseases, wherein the compound is isolated by adding one or more solvents selected from the group consisting of hexane, dichloromethane, ethyl acetate, butanol and water to the perilla leaf extract.
(5) 상기 화합물은 자소엽 에탄올 추출물에 헥산, 디클로로메탄, 에틸아세테이트, 부탄올 및 물을 순차적으로 첨가하여 분리되는 것인 자가면역질환 예방 또는 치료용 약학적 조성물. (5) The compound is a pharmaceutical composition for preventing or treating autoimmune diseases, wherein the compound is separated by sequentially adding hexane, dichloromethane, ethyl acetate, butanol and water to the ethanol extract of perilla leaf.
(6) 상기 분리는 디클로로메탄으로 분획하여 얻어진 디클로로메탄층을 실리카젤 컬럼크로마토그래피법을 통해 분리하는 것인 자가면역질환 예방 또는 치료용 약학적 조성물. (6) The separation is a pharmaceutical composition for preventing or treating autoimmune diseases by separating the dichloromethane layer obtained by fractionation with dichloromethane through silica gel column chromatography.
(7) 실리카젤 컬럼크로마토그래피법은 용매의 농도구배법(gradient method)을 통해 분리하는 것인 자가면역질환 예방 또는 치료용 약학적 조성물. (7) Silica gel column chromatography method is a pharmaceutical composition for preventing or treating autoimmune diseases that is separated through a gradient method of a solvent.
(8) 상기 염은 무기산, 유기산, 무기 염기 또는 유기 염기와의 생리학적으로 허용되는 염인 것인 자가면역질환 예방 또는 치료용 약학적 조성물. (8) The salt is a physiologically acceptable salt with an inorganic acid, an organic acid, an inorganic base, or an autoimmune disease prevention or treatment pharmaceutical composition.
(9) 상기 무기산은 염산, 브롬산, 황산 및 인산으로 이루어진 그룹에서 선택되는 1종 이상이며, 상기 유기산은 구연산 (citric acid), 초산, 젖산, 주석산 (tartariac acid), 말레인산, 푸마르산 (fumaric acid), 포름산, 프로피온산 (propionic acid), 옥살산, 트리플루오로아세트산, 벤조산, 글루콘산, 메탄술폰산, 글리콜산, 숙신산, 4-톨루엔술폰산, 글루탐산 및 아스파르트산으로 이루어진 그룹에서 선택된 1종 이상인 것인 자가면역질환 예방 또는 치료용 약학적 조성물.(9) the inorganic acid is at least one selected from the group consisting of hydrochloric acid, hydrobromic acid, sulfuric acid and phosphoric acid, and the organic acid is citric acid, acetic acid, lactic acid, tartaric acid, maleic acid, fumaric acid ), formic acid, propionic acid, oxalic acid, trifluoroacetic acid, benzoic acid, gluconic acid, methanesulfonic acid, glycolic acid, succinic acid, 4-toluenesulfonic acid, one or more selected from the group consisting of glutamic acid and aspartic acid A pharmaceutical composition for preventing or treating immune diseases.
(10) 상기 약학적 조성물은 희석제 또는 담체를 더 포함하는 것인 자가면역질환 예방 또는 치료용 약학적 조성물.(10) The pharmaceutical composition for preventing or treating autoimmune diseases further comprising a diluent or a carrier.
(11) 경구형 제제 또는 비경구형 제제로 제형화된 것인 자가면역질환 예방 또는 치료용 약학적 조성물.(11) A pharmaceutical composition for preventing or treating autoimmune diseases that is formulated as an oral formulation or parenteral formulation.
(12) 상기 경구형 제제는 정제, 캡슐제, 환제, 산제, 과립제, 현탁화제 또는 시럽제이고, 상기 비경구형 제제는 크림제, 로션제, 연고제, 액제, 겔제, 카타플라스마제, 패취제, 에어로솔제, 유동엑스제, 엘릭서제, 침제, 향낭, 또는 주사제인 것인 자가면역질환 예방 또는 치료용 약학적 조성물.(12) The oral preparations are tablets, capsules, pills, powders, granules, suspensions or syrups, and the parenteral preparations are creams, lotions, ointments, liquids, gels, cataplasmas, patches, and aerosols. , Liquid extract, elixir, acupuncture, sachet, or injection is a pharmaceutical composition for preventing or treating autoimmune diseases.
(13) 자소엽을 50 %(v/v) 내지 100 %(v/v) 에탄올로 추출하는 단계;(13) extracting the perilla leaves with 50% (v/v) to 100% (v/v) ethanol;
상기 단계로부터 얻어진 에탄올 추출물을 30 %(v/v) 내지 99 %(v/v) 디클로로메탄으로 분획하는 단계; 및 fractionating the ethanol extract obtained from the above step with 30% (v/v) to 99% (v/v) dichloromethane; and
상기 단계로부터 얻어진 디클로로메탄 분획물을 실리카젤 컬럼크로마토그래피법으로 분리하여 청구항 1의 화학식 1의 화합물을 얻는 단계;를 포함하는, 상기 자가면역질환 예방 또는 치료용 약학적 조성물의 제조방법.Separating the dichloromethane fraction obtained from the above step by silica gel column chromatography to obtain the compound of
(14) 자소엽 추출물로부터 분리된 하기 화학식 1로 표시되는 화합물 또는 그의 염을 유효성분으로 포함하는 자가면역질환 예방 또는 치료용 식품용 조성물:(14) A food composition for the prevention or treatment of autoimmune diseases, comprising as an active ingredient a compound represented by the following formula (1) or a salt thereof isolated from the perilla leaf extract:
[화학식 1][Formula 1]
. .
일 양상에 따른 자소엽 추출물로부터 분리한 화학식 1로 표시되는 화합물 또는 그의 염은 IL-17의 생성을 억제하고, 보다 구체적으로는 Th17 세포의 분극화 (polarization)를 억제하여 IL-17의 발현을 효과적으로 억제할 수 있다. 이에 따라 상기 화합물 또는 그의 염을 유효성분으로 포함하는 조성물은 자가면역질환 예방, 개선, 또는 치료에 이용될 수 있다. The compound represented by Formula 1 or a salt thereof isolated from the perilla leaf extract according to an aspect inhibits the production of IL-17, and more specifically, inhibits the polarization of Th17 cells to effectively inhibit the expression of IL-17. can be suppressed Accordingly, the composition comprising the compound or a salt thereof as an active ingredient can be used for preventing, improving, or treating autoimmune diseases.
도 1은 자소엽 추출물의 용매 분획 과정 (scheme)을 나타낸다.
도 2A는 자소엽, 천년초 열매, 천년초 줄기, 및 구절초의 각 에탄올 추출물의 독성 평가에 따른 세포 생존률(%)를 나타내고, 도 2B는 자소엽, 천년초 열매, 천년초 줄기, 구절초, 및 녹차의 각 에탄올 추출물의 IL-17A 발현률(%)을 나타낸다.
도 3A는 자소엽 분획물의 독성 평가에 따른 세포 생존률(%)를 나타내고, 도 3B는 자소엽 분획물의 IL-17A 발현률(%)을 나타낸다.
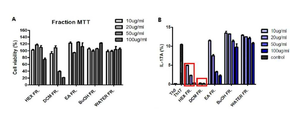
도 4A는 자소엽 디클로로메탄 (DCM) 분획물의 독성 평가에 따른 세포 생존률(%)를 나타내고, 도 4B는 상기 DCM 분획물의 IL-17A 발현률(%)을 나타낸다.
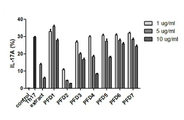
도 5는 자소엽 디클로로메탄 (DCM) 각 서브 분획물의 IL-17A 발현률(%)을 나타낸다.
도 6은 PFD4-2 서브 분획물 (subfraction)의 TLC 결과를 나타낸다.
도 7A는 PFD4-2-5-6의 1H-NMR 스펙트럼(400MHz, CD3OD) 결과를 나타낸다.
도 7B는 PFD4-2-5-6의 13C-NMR 스펙트럼(100MHz, CD3OD) 결과를 나타낸다.
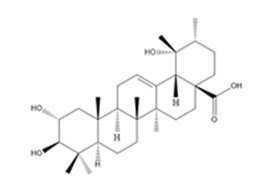
도 7C는 자소엽 디클로로메탄 분획물로부터 활성 성분으로 분리한 화합물인 토멘트산의 구조를 나타낸다.
도 8은 자소엽 에탄올 추출물의 디클로로메탄 분획물로부터 토멘트산의 분리 과정을 나타낸다.
도 9는 자소엽에서 분리한 PFD 4-2-5-6 (토멘트산)과 로즈마린산을 이용하여 측정한 IL-17A 발현률(%)을 나타낸다.
도 10은 자소엽 에탄올 추출물, 자소엽으로부터 분리한 PFD 4-2-5-6 (토멘트산), 토멘트산 표준품, 및 PFD 2-3-2-2 (우르솔산)을 이용하여 측정한 IL-17A 발현률(%)을 나타낸다.
도 11은 DSS 유발 염증성 장염 모델에 자소엽 추출물과 이로부터 분리한 토멘트산의 처치 과정을 나타낸다.
도 12A 및 12B는 DSS 유발 염증성 장염 동물 모델에서 자소엽 추출물, 토멘트산, 메살라진 처치 후 장의 길이 변화를 측정한 결과를 나타낸다.
도 13A 및 13B는 DSS 유발 염증성 장염 동물 모델에서 장의 조직학적 변화를 나타낸다.
도 14A, 14B, 14C는 각각 비장 (Spleen), 장간막림프절(mesenteric lymph nodes, MLN), 점막 고유층 백혈구 (lamina propria leukocytes, LPL)에서 CD4+ IL-17+ 세포 발현률(%)을 나타낸다. 1 shows the solvent fractionation process (scheme) of perilla leaf extract.
Figure 2A shows the cell viability (%) according to the toxicity evaluation of each ethanol extract of perilla, cheonnyeoncho fruit, cheonnyeoncho stem, and gujeolcho, and FIG. The IL-17A expression rate (%) of the extract is shown.
Fig. 3A shows the cell viability (%) according to the toxicity evaluation of the pericidal fraction, and Fig. 3B shows the IL-17A expression rate (%) of the pericidal fraction.
4A shows the cell viability (%) according to the toxicity evaluation of the perilla dichloromethane (DCM) fraction, and FIG. 4B shows the IL-17A expression rate (%) of the DCM fraction.
5 shows the IL-17A expression rate (%) of each sub-fraction of perilla dichloromethane (DCM).
6 shows the TLC results of the PFD4-2 subfraction.
7A shows the 1 H-NMR spectrum (400 MHz, CD 3 OD) result of PFD4-2-5-6.
7B shows the 13 C-NMR spectrum (100 MHz, CD 3 OD) result of PFD4-2-5-6.
Fig. 7C shows the structure of tomentic acid, a compound isolated as an active ingredient from a dichloromethane fraction of perilla leaves.
8 shows the separation process of tomentic acid from the dichloromethane fraction of perilla leaf ethanol extract.
FIG. 9 shows the IL-17A expression rate (%) measured using PFD 4-2-5-6 (tomentic acid) and rosmarinic acid isolated from perilla leaflets.
FIG. 10 shows measurements of perilla leaf ethanol extract, PFD 4-2-5-6 (tomentic acid) isolated from perilla leaf, tomentic acid standard, and PFD 2-3-2-2 (ursolic acid). IL-17A expression rate (%) is shown.
11 shows the treatment process of perilla leaf extract and tomentic acid isolated therefrom in a DSS-induced inflammatory enteritis model.
12A and 12B show the results of measuring changes in the length of the intestine after treatment with perilla leaf extract, tomentic acid, and mesalazine in an animal model of DSS-induced inflammatory enteritis.
13A and 13B show histological changes in the intestine in an animal model of DSS-induced inflammatory enteritis.
14A, 14B, and 14C show the expression rate (%) of CD4 + IL-17 + cells in the spleen (Spleen), mesenteric lymph nodes (MLN), and lamina propria leukocytes (LPL), respectively.
이하, 본 발명을 보다 상세하게 설명한다.Hereinafter, the present invention will be described in more detail.
본 발명에서 사용되는 모든 기술용어는, 달리 정의되지 않는 이상, 본 발명의 관련 분야에서 통상의 당업자가 일반적으로 이해하는 바와 같은 의미로 사용된다. 또한, 본 명세서에는 바람직한 방법이나 시료가 기재되나, 이와 유사하거나 동등한 것들도 본 발명의 범주에 포함된다. 본 명세서에 참고문헌으로 기재되는 모든 간행물의 내용은 본 발명에 전체가 참고로 통합된다.All technical terms used in the present invention, unless otherwise defined, have the same meaning as commonly understood by one of ordinary skill in the art of the present invention. In addition, although preferred methods and samples are described herein, similar or equivalent ones are also included in the scope of the present invention. The contents of all publications herein incorporated by reference are hereby incorporated by reference in their entirety.
일 양상은 자소엽 추출물로부터 분리된 하기 화학식 1로 표시되는 화합물 또는 그의 염을 유효성분으로 포함하는 자가면역질환 예방 또는 치료용 약학적 조성물을 제공한다. One aspect provides a pharmaceutical composition for preventing or treating autoimmune diseases, comprising as an active ingredient a compound represented by
[화학식 1][Formula 1]
본 명세서에서 사용된 용어 "자가면역질환"은 면역계의 이상으로 자기 세포를 공격하거나 자가 기관에 이상반응을 일으키는 질환을 말한다. 예를 들어, 류마티스 관절염, 크론병, 전신성 경피증 (Progressive systemic sclerosis, Scleroderma), 전신 홍반성 낭창 (lupus), 췌장세포 항체에 의한 인슐린 의존성 소아기 당뇨병, 다발성 경화증 (multiple sclerosis),자가면역성 용혈성 빈혈 (Autoimmune hemolytic anemia), 중증 근무력증 (Myasthenia gravis), 그레이브씨 갑상선 항진증 (Grave's disease) 또는 염증성 장질환을 들 수 있다. As used herein, the term "autoimmune disease" refers to a disease that attacks one's own cells due to an abnormality in the immune system or causes an abnormal reaction in an autologous organ. For example, rheumatoid arthritis, Crohn's disease, progressive systemic sclerosis (Scleroderma), systemic lupus erythematosus (lupus), insulin-dependent childhood diabetes mellitus caused by pancreatic cell antibody, multiple sclerosis, autoimmune hemolytic anemia ( Autoimmune hemolytic anemia), Myasthenia gravis, Grave's disease or inflammatory bowel disease.
일 구체 예에서, 상기 자가면역질환은 염증성 장 질환이다. 크론병, 궤양성 대장염 등으로 나타나는 염증성 장 질환은 점막의 과도한 염증으로 발생하는 만성 염증성 자가면역질환이다. In one embodiment, the autoimmune disease is inflammatory bowel disease. Inflammatory bowel disease, such as Crohn's disease and ulcerative colitis, is a chronic inflammatory autoimmune disease caused by excessive inflammation of the mucous membrane.
본 명세서에서 사용된 용어 "추출"은 생약의 성분을 약학적 조성물에 편입하기 위하여 분리하는 것을 의미한다. 다만, 단계별 구체적인 내용에 따라 생약에서 유효성분을 분리하는 최초 단계의 의미로 선해 될 수 있다.As used herein, the term “extraction” refers to separating the components of a herbal medicine for incorporation into a pharmaceutical composition. However, depending on the specific content of each step, it may be harmful in the sense of the first step of separating the active ingredient from the herbal medicine.
본 명세서에서 "자소엽 (Perilla leaves, Perilla frutescens var. acuta)"은 꿀풀과에 속하는 1년생 초본인 차조기 (Perilla frutescens var. acuta KUDO.)의 잎을 지칭한다. As used herein, "Perilla leaves, Perilla frutescens var. acuta " refers to the leaves of perilla frutescens var. acuta KUDO., an annual herb belonging to the family Lamiaceae.
상기 자소엽 추출물의 추출 용매는 물 또는 유기용매, 또는 이들의 혼합물일 수 있다. 상기 유기용매는 예를 들어, C1 내지 C4의 알코올, 에틸아세테이트 또는 아세톤 등의 극성용매, 또는 에테르, 클로로포름, 벤젠, 헥산 또는 디클로로메탄의 비극성용매 또는 이들의 혼합용매일 수 있다. The extraction solvent of the perilla leaf extract may be water, an organic solvent, or a mixture thereof. The organic solvent may be, for example, a C 1 to C 4 alcohol, a polar solvent such as ethyl acetate or acetone, or a non-polar solvent such as ether, chloroform, benzene, hexane or dichloromethane, or a mixed solvent thereof.
상기 알코올은 1 내지 100% (v/v)일 수 있다. 또는 상기 알코올은 알코올의 희석수 예컨대 알코올을 1 내지 99%(v/v)로 물에 희석하여 제공될 수 있다. The alcohol may be 1 to 100% (v/v). Alternatively, the alcohol may be provided by diluting the alcohol with dilution water such as 1 to 99% (v/v) of the alcohol in water.
일 구체 예에서, 상기 자소엽 추출물의 추출용매는 물, C1 내지 C4의 알코올 또는 이들의 혼합물이다. 일 구체 예에서, 상기 추출용매는 에탄올일 수 있다.In one embodiment, the extraction solvent of the perilla leaf extract is water, C 1 to C 4 alcohol, or a mixture thereof. In one embodiment, the extraction solvent may be ethanol.
일 구체 예에 따른 에탄올은 자소엽 추출물로부터 토멘트산을 높은 함량으로 추출하기에 바람직한 추출용매이다. 예를 들어, 물 추출 시에는 토멘트산이 거의 포함되지 않으므로 에탄올 추출이 보다 바람직하다. 또한, 메탄올 추출 시에는 메탄올로 인한 독성이 있으므로 약학적 조성물 또는 식품용 조성물로 사용하기 위해 에탄올 추출이 보다 바람직하다. Ethanol according to an embodiment is a preferred extraction solvent for extracting tomentic acid in a high content from the perilla leaf extract. For example, ethanol extraction is more preferable since thomentic acid is hardly included during water extraction. In addition, during methanol extraction, ethanol extraction is more preferable for use as a pharmaceutical composition or a food composition because there is toxicity due to methanol.
충분하고 효과적인 유효 성분 추출을 위하여 상기 추출 용매는 자소엽 중량을 기준으로 1 내지 30배 부피 배, 바람직하게는 2 내지 10 부피 배일 수 있다. 상기 "부피 배"란 자소엽의 중량과 대비한 용매의 부피, 즉, g 당 ml에 대응하는 배수를 의미한다.For sufficient and effective extraction of the active ingredient, the extraction solvent may be 1 to 30 times by volume, preferably 2 to 10 times by volume, based on the weight of perilla leaf. The term “fold by volume” means a multiple of the volume of solvent compared to the weight of the perilla leaf, that is, a multiple corresponding to ml per gram.
상기 추출물의 추출온도는, 4℃내지 120℃에서 수행될 수 있다. 또한, 상기 추출시간은 12시간 내지 120시간일 수 있다. 상기 추출온도가 4℃보다 낮은 경우 추출이 잘 안 될 수 있으며, 120℃를 넘는 경우 추출물이 변성될 수 있다. 상기 추출시간이 12시간보다 낮은 경우 유효성분이 일부 추출되지 않을 수 있으며, 120시간을 넘길 경우 유효성분 이외의 불순물 성분이 함께 추출될 수 있으므로 바람직하지 않다. 또는 상기 추출온도는 상온일 수 있다. The extraction temperature of the extract may be carried out at 4 ℃ to 120 ℃. In addition, the extraction time may be 12 hours to 120 hours. If the extraction temperature is lower than 4 ℃, the extraction may be difficult, and if it exceeds 120 ℃, the extract may be denatured. If the extraction time is less than 12 hours, some of the active ingredients may not be extracted, and if it exceeds 120 hours, impurities other than the active ingredients may be extracted together, which is not preferable. Alternatively, the extraction temperature may be room temperature.
필요에 따라 추출과정은 1 내지 10회, 예를 들어 2 내지 5회 반복할 수 있다. If necessary, the extraction process may be repeated 1 to 10 times, for example, 2 to 5 times.
상기 자소엽 추출물은 통상의 식물 추출물의 제조방법에 따라 제조된 것일 수 있으며, 구체적으로는 냉침추출법, 온침추출법, 열 추출법, 초음파 추출법 등일 수 있으며, 통상의 추출기기, 초음파분쇄 추출기 또는 분획기를 이용할 수 있다.The perilla leaf extract may be prepared according to a conventional method for producing a plant extract, and specifically may be a cold extraction method, a warm needle extraction method, a heat extraction method, an ultrasonic extraction method, etc. can
상기 자소엽 추출물은 추출 용매로 추출 후, 자소엽 찌꺼기를 제거하고, 필터 페이퍼로 여과한 후 여액을 진공회전농축기 또는 진공건조기를 사용하여 농축한 후, 실온에서 보관할 수 있다.The perilla leaf extract can be extracted with an extraction solvent, the perilla leaves are removed, filtered through filter paper, and the filtrate is concentrated using a vacuum rotary concentrator or vacuum dryer, and then stored at room temperature.
더 나은 유효 활성 물질을 얻기 위해서, 혹은 불순물을 제거하기 위해서 분획과정이 추가될 수 있다. 상기 분획이란 추출물에 분획 용매를 가하여 분리하는 수단을 의미한다. 추출에 이은 분획물은 자소엽 추출물에 분획 용매를 가하여 분획하여 얻어지며, 예컨대, 상기 얻어진 자소엽 추출물에 물, C1 내지 C5의 직쇄 또는 분지형 알코올, 헥산, 디클로로메탄 에틸아세테이트, 클로로포름, 아세톤, 에테르 및 벤젠으로 이루어진 군에서 선택된 1종 이상의 분획 용매를 가하여 분획하여 얻어진 것일 수 있다.Fractionation may be added to obtain a better active active substance or to remove impurities. The fraction means a means for separating by adding a fractionation solvent to the extract. The fraction following the extraction is obtained by adding a fractionation solvent to the perilla leaf extract, for example, water, C 1 to C 5 linear or branched alcohol, hexane, dichloromethane ethyl acetate, chloroform, acetone. , may be obtained by fractionation by adding one or more fractionation solvents selected from the group consisting of ether and benzene.
상기 분획 용매로서 2종 이상을 사용하는 경우, 분획물은 2종 이상의 분획 용매를 동시 또는 순서에 따라 사용하여 용매 분획을 수행하여 얻어진 각각의 용매 분획물일 수 있다. 예컨대, 분획물은 n-헥산, 디클로로메탄, 에틸아세테이트, 부탄올 및 물의 순서에 따라 용매 분획을 수행하여 얻어진 각각의 용매 분획물일 수 있다.When two or more types of fractionation solvents are used, the fractions may be individual solvent fractions obtained by performing solvent fractionation using two or more types of fractionation solvents simultaneously or sequentially. For example, the fraction may be each solvent fraction obtained by performing solvent fractionation in the order of n-hexane, dichloromethane, ethyl acetate, butanol and water.
상기 분획 용매는 예를 들어, 10 %(v/v) 내지 99 %(v/v) 수용액이거나 또는 농도 100%(v/v)의 용매일 수 있다. The fractionation solvent may be, for example, a 10% (v/v) to 99% (v/v) aqueous solution or a solvent having a concentration of 100% (v/v).
일 구체 예에서, 상기 화학식 1의 화합물은 자소엽 추출물에 헥산, 디클로로메탄, 에틸아세테이트, 부탄올 및 클로로포름으로 이루어진 군으로부터 선택된 1종 이상의 유기용매 또는 물을 이용하여, 동시 또는 순차적으로 분획 과정을 더 실시하여 분획물로 얻어질 수 있다. In one embodiment, the compound of
일 구체 예에서, 상기 화합물은 자소엽 추출물에 물, C1 내지 C5의 직쇄 또는 분지형 알코올, 헥산, 디클로로메탄, 및 에틸아세테이트로 이루어진 군에서 선택된 1종 이상의 용매를 첨가하여 분리된다 .In one embodiment, the compound is isolated by adding one or more solvents selected from the group consisting of water, C 1 to C 5 linear or branched alcohol, hexane, dichloromethane, and ethyl acetate to the perilla leaf extract.
일 구체 예에서, 상기 화합물은 자소엽 추출물에 헥산, 디클로로메탄, 에틸아세테이트, 부탄올 및 물로 이루어진 군에서 선택된 1종 이상의 용매를 첨가하여 분리된다. In one embodiment, the compound is isolated by adding one or more solvents selected from the group consisting of hexane, dichloromethane, ethyl acetate, butanol and water to the perilla leaf extract.
일 구체 예에서, 상기 화합물은 자소엽 에탄올 추출물에 헥산, 디클로로메탄, 및 에틸아세테이트을 순차적으로 첨가하여 분리될 수 있다. 예를 들어, 상기 화합물은 자소엽 에탄올 추출물의 디클로로메탄 (dichloromethane, DCM) 분획물로부터 분리될 수 있다. In one embodiment, the compound may be isolated by sequentially adding hexane, dichloromethane, and ethyl acetate to the ethanol extract of perilla leaf. For example, the compound can be isolated from the dichloromethane (DCM) fraction of ethanol extract of perilla leaves.
상기 분획온도는 4℃ 내지 120℃에서 수행될 수 있다. 또는, 상기 분획온도는 상온일 수 있다. The fractionation temperature may be carried out at 4 ℃ to 120 ℃. Alternatively, the fractionation temperature may be room temperature.
필요한 경우 당업계에 공지된 여과, 농축, 동결건조 방법이 추가적으로 사용될 수 있다. 본 발명에서 사용된 추출물 및/또는 분획물의 건조물 또는 농축물은 위와 같이 공지된 방법으로 건조 또는 농축된 것을 의미한다. If necessary, filtration, concentration, and freeze-drying methods known in the art may be additionally used. The dried product or concentrate of the extract and/or fraction used in the present invention means dried or concentrated by a known method as described above.
필요에 따라 분획과정은 1 내지 10회, 예를 들어 2 내지 5회 반복할 수 있다. If necessary, the fractionation process may be repeated 1 to 10 times, for example, 2 to 5 times.
필요에 따라 분획과정 전에 추출물의 현탁 과정을 거칠 수 있다. If necessary, a suspension process of the extract may be performed before the fractionation process.
상기 분획과정을 수행하여 수득한 분획추출물은 진공회전농축기 또는 진공건조기를 사용하여 농축한 후, 실온에서 보관할 수 있다.The fractionated extract obtained by performing the fractionation process may be concentrated using a vacuum rotary concentrator or a vacuum dryer, and then stored at room temperature.
일 구체 예에서, 상기 분리는 디클로로메탄으로 분획하여 얻어진 디클로로메탄층을 실리카젤 컬럼크로마토그래피법을 통해 분리할 수 있다. In one embodiment, in the separation, the dichloromethane layer obtained by fractionation with dichloromethane may be separated through silica gel column chromatography.
일 구체 예에서, 실리카젤 컬럼크로마토그래피법은 용매의 농도구배법(gradient method)을 통해 분리할 수 있다. In one embodiment, the silica gel column chromatography method can be separated through a solvent gradient method (gradient method).
일 구체 예에서, 상기 염은 무기산, 유기산, 무기 염기 또는 유기 염기와의 생리학적으로 허용되는 염일 수 있다. In one embodiment, the salt may be a physiologically acceptable salt with an inorganic acid, an organic acid, an inorganic base or an organic base.
일 구체 예에서, 상기 무기산은 염산, 브롬산, 황산 및 인산으로 이루어진 그룹에서 선택되는 1종 이상이며, 상기 유기산은 구연산 (citric acid), 초산, 젖산, 주석산 (tartariac acid), 말레인산, 푸마르산 (fumaric acid), 포름산, 프로피온산 (propionic acid), 옥살산, 트리플루오로아세트산, 벤조산, 글루콘산, 메탄술폰산, 글리콜산, 숙신산, 4-톨루엔술폰산, 글루탐산 또는 아스파르트산으로 이루어진 그룹에서 선택된 1종 이상일 수 있다. In one embodiment, the inorganic acid is at least one selected from the group consisting of hydrochloric acid, hydrobromic acid, sulfuric acid and phosphoric acid, and the organic acid is citric acid, acetic acid, lactic acid, tartaric acid, maleic acid, fumaric acid ( fumaric acid), formic acid, propionic acid, oxalic acid, trifluoroacetic acid, benzoic acid, gluconic acid, methanesulfonic acid, glycolic acid, succinic acid, 4-toluenesulfonic acid, glutamic acid or aspartic acid may be at least one selected from the group consisting of have.
상기 염은 약학적으로 허용 가능한 염 또는 식품학적으로 허용 가능한 염일 수 있다. 용어 "약학적으로 허용가능한 염" 또는 "식품학적으로 허용가능한 염"은 일반적으로 안전하며, 무독성이고, 생물학적으로도 다른 측면으로도 부적합하지 않아 약학적 및 식품학적 조성물의 제조에 사용가능함을 말한다. The salt may be a pharmaceutically acceptable salt or a food acceptable salt. The term "pharmaceutically acceptable salt" or "food acceptable salt" refers to generally safe, non-toxic, not biologically or otherwise unsuitable for use in the manufacture of pharmaceutical and food pharmaceutical compositions. .
상기 화학식 1의 화합물은 시험관적으로 합성되거나 생약에서 추출될 수 있다. 생약에서 추출할 경우 자소엽으부터 분리 추출할 수 있다.The compound of
상기 화학식 1의 화합물은 토멘트산 (tormentic acid)으로 지칭될 수 있다. The compound of
상기 화학식 1로 표시되는 토멘트산 화합물 또는 그의 염은 세포의 분화 조절에 관여하여 Th17 관련 사이토카인 및 전사인자인 IL-17A 발현을 감소시킬 수 있다. The tomentic acid compound represented by
Th17 세포는 점막 표면에 축적되고 숙주를 박테리아 및 곰팡이 감염으로부터 보호하는 필수 T 세포 하위 집합이다. 또한, 보호 면역 기능 외에도 자가면역 염증의 중요한 이펙터(effector) 역할을 한다. Th17 세포는 IL-17A, IL-17F, IL-21, 및 IL-22 사이토카인의 분비를 특징으로 한다. Th17 세포가 조절되지 않거나 부적절한 활성화는 여러가지 염증 병리에서 중요한 역할을 한다.Th17 cells are an essential T cell subset that accumulates on mucosal surfaces and protects the host from bacterial and fungal infections. In addition to its protective immune function, it also serves as an important effector of autoimmune inflammation. Th17 cells are characterized by secretion of IL-17A, IL-17F, IL-21, and IL-22 cytokines. Unregulated or inappropriate activation of Th17 cells plays an important role in several inflammatory pathologies.
상기 화학식 1로 표시되는 토멘트산 화합물 또는 그의 염은 IL-17의 생성을 억제하고, 보다 구체적으로는 Th17의 분극화 (polarization)를 억제하여 IL-17의 발현을 효과적으로 억제할 수 있다. 이에 따라 상기 화합물 또는 그의 염을 유효성분으로 포함하는 조성물은 자가면역질환 예방, 개선, 또는 치료에 이용될 수 있다. The tomentic acid compound represented by
본 명세서에서 사용된 용어 “T 도움 17 세포 (Th17, Th17 cells, T helper 17 cells)”는 염증 전 도움 T 세포 중에서 인터루킨17 (IL-17)을 생성하는 집단을 말한다. 이들은 조절 T 세포와 관련되며, Th17s을 분화시켜 실제 조절 T세포 분화를 억제하는 신호들과 관련된다. Th17s는 발달상에 있어서 Th1, Th2와는 구별된다. Th17 세포는 점막 장벽을 유지하는데 중요한 역할을 하며, 점막 표면에서 병원체를 없애는데 기여하지만, 또한 자가면역 질환과 염증성 질병과 연관된다. 점막 표면에서 Th17 세포가 줄어드는 것은 만성 염증과 미생물이 전이되는 것 과도 연관된다.As used herein, the term “
자소엽 추출물로부터 분리한 화학식 1로 표시되는 화합물 또는 이의 약학적으로 허용 가능한 염은 자가면역질환 예방, 개선 또는 치료에 탁월한 용도를 제공한다. The compound represented by
상기 약학적 조성물 중의 화학식 1의 화합물은 이의 유도체, 이성질체, 약학적으로 허용가능한 염 또는 용매화물로 제공될 수 있다. The compound of
상기 유도체 (derivative)는 상기 화합물의 구조 일부를 다른 원자나 원자단으로 치환하여 얻어지는 화합물을 말한다. 용어 "치환"은 유기 화합물 중의 하나 이상의 수소 원자를 다른 원자단으로 치환하여 유도체를 형성한 경우 수소 원자 대신에 도입되는 것을 말하고, "치환기"는 도입된 원자단을 말한다. 치환기는 예를 들면, 히드록시기, 할로겐 원자(예, 불소(F), 염소(Cl), 브롬(Br), 및 요오드(I)), C2 내지 C10 알케닐기, C2 내지 C10 알키닐기, C1 내지 C10 헤테로알킬기, C6 내지 C10 아릴기, C6 내지 C10 헤테로아릴기, C1 내지 C10의 알콕시, 니트로기, 시아노기, 아미노기, 카르복실기나 그의 염, 술포닐기, 술파모일(sulfamoyl)기, 술폰산기나 그의 염, 인산이나 그의 염, 또는 이들의 조합일 수 있다.The derivative refers to a compound obtained by substituting a part of the structure of the compound with another atom or group of atoms. The term "substitution" refers to introduced instead of a hydrogen atom when a derivative is formed by substituting one or more hydrogen atoms in an organic compound with another atomic group, and "substituent" refers to an introduced atomic group. The substituent is, for example, a hydroxyl group, a halogen atom (eg, fluorine (F), chlorine (Cl), bromine (Br), and iodine (I)), a C 2 to C 10 alkenyl group, a C 2 to C 10 alkynyl group. , C 1 to C 10 heteroalkyl group, C 6 to C 10 aryl group, C 6 to C 10 heteroaryl group, C 1 to C 10 alkoxy, nitro group, cyano group, amino group, carboxyl group or a salt thereof, sulfonyl group, It may be a sulfamoyl group, a sulfonic acid group or a salt thereof, phosphoric acid or a salt thereof, or a combination thereof.
상기 이성질체는 구조 이성질체 또는 입체이성질체일 수 있다.The isomers may be structural isomers or stereoisomers.
상기 용매화물 (solvate)은 유기 또는 무기 용매에 용매화된 화합물을 말한다. 상기 용매화물은 예를 들어, 수화물이다.The solvate refers to a compound solvated in an organic or inorganic solvent. The solvate is, for example, a hydrate.
일 구체 예에서, 상기 약학적 조성물은 희석제 또는 담체를 더 포함할 수 있다. 상기 희석제 또는 담체는 부형제, 붕해제, 결합제, 활택제, 또는 그 조합일 수 있다. 상기 부형제는 미결정 셀룰로오스, 유당, 또는 저치환도 히드록시셀룰로오스 등으로 예시 될 수 있으나, 이에 한정되는 것은 아니다. 상기 붕해제는 전분글리콜산 나트륨, 또는 무수인산일수소 칼슘 등으로 예시 될 수 있으나, 이에 한정되는 것은 아니다. 상기 결합제는 폴리비닐피롤리돈, 저치환도 히드록시프로필셀룰로오스, 또는 히드록시프로필셀룰로오스 등으로 예시 될 수 있으나, 이에 한정되는 것은 아니다. 상기 활택제는 스테아린산 마그네슘, 이산화규소, 또는 탈크 등으로 예시 될 수 있으나, 이에 한정되는 것은 아니다.In one embodiment, the pharmaceutical composition may further include a diluent or carrier. The diluent or carrier may be an excipient, a disintegrant, a binder, a lubricant, or a combination thereof. The excipient may be exemplified by microcrystalline cellulose, lactose, or low-substituted hydroxycellulose, but is not limited thereto. The disintegrant may be exemplified by sodium starch glycolate, or anhydrous calcium monohydrogen phosphate, but is not limited thereto. The binder may be exemplified by polyvinylpyrrolidone, low-substituted hydroxypropyl cellulose, or hydroxypropyl cellulose, but is not limited thereto. The lubricant may be exemplified by magnesium stearate, silicon dioxide, or talc, but is not limited thereto.
상기 희석제 또는 담체는 조성물 100 중량부당 예컨대 0.001 내지 90 중량부의 범위에서 적절하게 선택될 수 있다.The diluent or carrier may be appropriately selected, for example, in the range of 0.001 to 90 parts by weight per 100 parts by weight of the composition.
일 구체 예에서, 경구형 제제 또는 비경구형 제제로 제형화될 수 있다. In one embodiment, it may be formulated as an oral preparation or a parenteral preparation.
일 구체 예에서, 상기 경구형 제제는 정제, 캡슐제, 환제, 산제, 액제, 건조시럽제, 과립제, 현탁화제 또는 시럽제으로 예시될 수 있으나 이에 한정되는 것은 아니다. 상기 비경구형 제제는 크림제, 로션제, 연고제, 액제, 겔제, 카타플라스마제, 패취제, 에어로솔제, 유동엑스제, 엘릭서제, 침제, 향낭, 주사제, 피부 유화제, 피부 현탁액, 경피전달성 패치, 약물 함유 붕대 등으로 예시 될 수 있으나, 이에 한정되는 것은 아니다.In one embodiment, the oral formulation may be exemplified as a tablet, capsule, pill, powder, liquid, dry syrup, granule, suspending agent or syrup, but is not limited thereto. The parenteral formulations include creams, lotions, ointments, liquids, gels, cataplasmas, patches, aerosols, fluid extracts, elixirs, needles, sachets, injections, skin emulsifiers, skin suspensions, transdermal delivery patches, It may be exemplified as a drug-containing bandage, but is not limited thereto.
상기 조성물의 투여는 당업계에 알려진 방법에 의하여 투여될 수 있다. 예를 들면, 정맥내, 근육내, 경구, 경피 (transdermal), 점막, 코안 (intranasal), 기관내 (intratracheal) 또는 피하 투여와 같은 경로로, 임의의 수단에 의하여 개체로 직접적으로 투여될 수 있다. 상기 투여는 전신적으로 또는 국부적으로 투여될 수 있다. Administration of the composition may be administered by a method known in the art. For example, it can be administered directly to a subject by any means, such as intravenous, intramuscular, oral, transdermal, mucosal, intranasal, intratracheal or subcutaneous administration. . The administration may be systemically or locally.
다른 일 양상은, 자소엽을 50 %(v/v) 내지 100 %(v/v) 에탄올로 추출하는 단계;In another aspect, extracting the perilla leaves with 50% (v/v) to 100% (v/v) ethanol;
상기 단계로부터 얻어진 에탄올 추출물을 30 %(v/v) 내지 99 %(v/v) 디클로로메탄으로 분획하는 단계; 및 fractionating the ethanol extract obtained from the above step with 30% (v/v) to 99% (v/v) dichloromethane; and
상기 단계로부터 얻어진 디클로로메탄 분획물을 실리카젤 컬럼크로마토그래피법으로 분리하여 상기 화학식 1의 화합물을 얻는 단계;를 포함하는, 상기 자가면역질환 예방 또는 치료용 약학적 조성물의 제조방법을 제공한다.It provides a method for preparing a pharmaceutical composition for preventing or treating autoimmune diseases, including; obtaining the compound of
다른 일 양상은, 자소엽 추출물로부터 분리된 상기 화학식 1로 표시되는 화합물 또는 그의 염을 유효성분으로 포함하는 자가면역질환 예방 또는 치료용 식품용 조성물을 제공한다. Another aspect provides a food composition for preventing or treating autoimmune diseases, comprising the compound represented by
상기 식품용 조성물은 예를 들어 자가면역질환을 앓고 있는 환자 또는 자가면역질환을 앓을 수 있는 사람에 대한 의약품, 보조제, 건강 식품 또는 기능성 식품으로 이용될 수 있다. 상기 식품의 종류에는 특별한 제한은 없다. 상기 물질을 첨가할 수 있는 식품의 예로는 우유, 요플레 등의 각종 낙농제품, 음료수, 차, 드링크제, 알콜 음료 및 비타민 복합제 등의 식음료, 빵, 쵸코렛, 캔디류, 과자류 등의 스낵류를 포함하여, 통상적인 의미에서의 식품을 모두 포함한다.The composition for food may be used, for example, as a pharmaceutical, supplement, health food or functional food for a patient suffering from an autoimmune disease or a person who may suffer from an autoimmune disease. There is no particular limitation on the type of the food. Examples of foods to which the above substances can be added include various dairy products such as milk and yogurt, beverages, tea, drinks, alcoholic beverages and vitamin complexes, and snacks such as bread, chocolate, candy, and confectionery. It includes all foods in the sense of phosphorus.
상기 식품 조성물은 보조식품, 건강기능식품으로도 제공될 수 있다. The food composition may be provided as a supplement or a health functional food.
또 다른 일 양상은 자소엽 추출물로부터 분리된 상기 화학식 1로 표시되는 화합물 또는 그의 염을 유효성분으로 포함하는 자가면역질환을 예방, 개선 또는 치료하기 위한 방법을 제공한다. Another aspect provides a method for preventing, improving or treating an autoimmune disease comprising the compound represented by
본 명세서에서 사용되는 용어 "예방"은 질환 또는 질병을 보유하고 있다고 진단된 적은 없으나, 이러한 질환 또는 질병에 걸리기 쉬운 경향이 있는 개체에서 질환 또는 질병의 발생을 억제하는 것을 의미한다.As used herein, the term "prevention" refers to inhibiting the development of a disease or disorder in an individual who has not been diagnosed with the disease or disease, but is prone to the disease or disease.
본 명세서에서 사용되는 용어 "치료"는 개체에서 (a) 질환 또는 질병의 발전의 억제 (b) 질환 또는 질병의 경감 및 (c) 질환 또는 질환의 제거를 의미한다.As used herein, the term “treatment” refers to (a) inhibiting the development of a disease or disorder in a subject, (b) alleviating the disease or disorder, and (c) eliminating the disease or disorder.
본 명세서에서 사용되는 용어 "개선"은 개체에서 질환 또는 질병의 증세가 호전되는 모든 행위를 의미한다.As used herein, the term “improvement” refers to any action in which a disease or symptom of a disease is improved in an individual.
본 명세서에서 사용되는 용어 "개체"는 본 발명의 상기 조성물을 투여하여 증상이 호전될 수 있는 질환을 가진 인간을 포함한 원숭이, 소, 말, 돼지, 양, 개, 고양이, 래트, 마우스, 침팬지 등의 포유동물을 의미한다.As used herein, the term "individual" refers to monkeys, cows, horses, pigs, sheep, dogs, cats, rats, mice, chimpanzees, etc. means a mammal of
본 명세서에서 사용된 용어 "유효성분으로 포함"은 자소엽 추출물로부터 분리한 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물의 효능 또는 활성을 달성하는 데 충분한 양을 포함하는 것을 의미한다. 예를 들어, 자가면역질환 예방 또는 치료용 약학적 조성물 내 유효성분의 함량은 0.001 중량% 내지 99.9 중량%, 0.1 중량% 내지 99 중량% 또는 1 중량% 내지 50 중량%일 수 있으나, 이에 한정되는 것은 아니며, 조성물의 사용태양 및 사용방법에 따라 바람직한 함량으로 적절히 조절하여 사용될 수 있다.As used herein, the term "included as an active ingredient" means to include an amount sufficient to achieve the efficacy or activity of the compound represented by
일 구체 예에서, 자소엽 추출물로부터 분리한 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 약학적 조성물 전체 중량을 기초로 1 내지 80 중량%의 양으로 포함될 수 있으며, 용매화물 또는 약학적으로 허용가능한 염 형태로 제공될 수도 있다. In one embodiment, the compound represented by
일 구체 예에서, 자소엽 추출물로부터 분리한 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 식품 조성물 전체 중량을 기초로 1 내지 80 중량%의 양으로 포함될 수 있으며, 용매화물 또는 식품학적으로 허용가능한 염 형태로 제공될 수도 있다. In one embodiment, the compound represented by
또한, 조성물 중에서는 상기 유효성분 이외에 공지의 자가면역질환 치료제를 추가적으로 포함할 수 있다.In addition, the composition may additionally include a known therapeutic agent for autoimmune diseases in addition to the active ingredient.
상기 조성물 중 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 약학적으로 또는 식품학적으로 유효한 함량으로 포함될 수 있다. 예를 들어, 상기 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 조성물 중 0.001 내지 1000 nM의 농도로 존재할 수 있다. 예를 들어, 상기 조성물 중 5 nM, 10 nM, 25 nM, 30nM, 40 nM, 50 nM, 60 nM, 75 nM, 100 nM, 또는 이들 수치를 상한 또는 하한으로 하는 범위로 존재할 수 있다. 예를 들어, 상기 조성물 중 1 내지 10 M의 농도로 존재할 수 있다. In the composition, the compound represented by
또는 상기 조성물 중 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 0.001 내지 200 ㎍/mL, 예를 들어 0.5, 1, 2, 4, 5, 7, 8, 10, 15, 20, 30, 50, 100, 200 ㎍/mL 또는 이들을 상한 또는 하한으로 하는 범위 예컨대 0.5 내지 30 ㎍/mL, 1 내지 20 ㎍/mL, 4 내지 15 ㎍/mL, 7 내지 10 ㎍/mL, 0.1 내지 100 ㎍/mL 일 수 있다. Or in the composition, the compound represented by
또는 상기 조성물 중 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 0.1 ㎍/mL 이상으로 포함될 수 있다. Alternatively, the compound represented by
예를 들어, 상기 조성물 중 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 자가면역질환 예방, 치료, 또는 개선을 위해 필요한 1일 투여량의 전부, 1/2, 또는 1/3의 양으로 포함될 수 있다. For example, in the composition, the compound represented by
또는 상기 조성물 중 자소엽 에탄올 추출물 또는 이로부터 분리된 디클로로메탄 분획물은 0.001 내지 100 ㎍/mL, 예를 들어 0.5, 1, 2, 4, 5, 7, 8, 10, 15, 20, 30 ㎍/mL 또는 이들을 상한 또는 하한으로 하는 범위 예컨대 0.5 내지 30 ㎍/mL , 1 내지 20 ㎍/mL , 4 내지 15 ㎍/mL , 7 내지 10 ㎍/mL 일 수 있다. or 0.001 to 100 μg/mL, for example, 0.5, 1, 2, 4, 5, 7, 8, 10, 15, 20, 30 μg/mL of perilla leaf ethanol extract or the dichloromethane fraction isolated therefrom in the composition mL or a range using these as upper or lower limits, such as 0.5 to 30 µg/mL, 1 to 20 µg/mL, 4 to 15 µg/mL, and 7 to 10 µg/mL.
또는 상기 조성물 중 자소엽 에탄올 추출물 또는 이로부터 분리된 디클로로메탄 분획물은 0.1 ㎍/mL 이상으로 포함될 수 있다. Alternatively, the ethanol extract of perilla leaf or the dichloromethane fraction separated therefrom in the composition may be included in an amount of 0.1 μg/mL or more.
상기 조성물은 약학적으로 또는 식품학적으로 허용가능한 첨가제 또는 담체를 이용하여 제제화함으로써 단위 용량 형태로 제조되거나 또는 다용량 용기 내에 내입시켜 제조될 수 있다. The composition may be prepared in a unit dose form by formulating using a pharmaceutically or food acceptable additive or carrier, or may be prepared by internalizing in a multi-dose container.
상기 조성물의 적합한 투여량은 제제화 방법, 투여 방식, 환자의 연령, 체중, 성, 병적 상태, 음식, 투여 시간, 투여 경로, 배설 속도 및 반응 감응성과 같은 요인들에 의해 다양하며, 보통으로 숙련된 의사 등은 소망하는 치료, 예방 또는 개선에 효과적인 투여량을 용이하게 결정 및 처방할 수 있다. 일 구체 예에 따르면, 상기 조성물의 1일 투여량은 0.001 내지 10 g/㎏일 수 있다.A suitable dosage of the composition varies depending on factors such as formulation method, administration mode, age, weight, sex, pathological condition, food, administration time, administration route, excretion rate, and response sensitivity of the patient, usually skilled in the art. A physician or the like can readily determine and prescribe an effective dosage for the desired treatment, prevention or improvement. According to one embodiment, the daily dose of the composition may be 0.001 to 10 g / kg.
예를 들어, 자가면역질환 치료용 약학적 조성물의 투여량은 유효성분의 흡수도, 불활성률 및 병용되는 약물을 고려하여 결정할 수 있으며, 1일 유효성분을 기준으로 하였을 때 0.1 mg/kg(체중) 내지 500 mg/kg(체중), 0.1 mg/kg(체중) 내지 400 mg/kg(체중) 또는 1 mg/kg(체중) 내지 300 mg/kg(체중)으로 투여할 수 있으며, 1회 또는 수회로 나누어 투여할 수 있으나, 이에 한정되는 것은 아니다.For example, the dosage of the pharmaceutical composition for the treatment of autoimmune diseases may be determined in consideration of the absorption of the active ingredient, the inactivation rate, and the drug used in combination, and 0.1 mg/kg (body weight) based on the daily active ingredient. ) to 500 mg/kg (body weight), 0.1 mg/kg (body weight) to 400 mg/kg (body weight), or 1 mg/kg (body weight) to 300 mg/kg (body weight), and may be administered once or It can be administered in several divided doses, but is not limited thereto.
예를 들어, 자소엽 에탄올 추출물, 이의 디클로로메탄 분획물, 또는 이로부터 분리한 화학식 1로 표시되는 화합물, 이의 유도체, 또는 이들의 혼합물은 10 내지 100 mg/kg(체중), 20 내지 80 mg/kg(체중), 또는 25 내지 50 mg/kg(체중)으로 투여될 수 있다. For example, an ethanol extract of perilla leaf, a dichloromethane fraction thereof, or a compound represented by
이하 본 발명을 실시예를 통하여 보다 상세하게 설명한다. 그러나, 이들 실시예는 본 발명을 예시적으로 설명하기 위한 것으로 본 발명의 범위가 이들 실시예에 한정되는 것은 아니다.Hereinafter, the present invention will be described in more detail through examples. However, these examples are for illustrative purposes of the present invention, and the scope of the present invention is not limited to these examples.
실시예 1. 자소엽 에탄올 추출물의 제조 Example 1. Preparation of perilla ethanol extract
자소엽을 6 kg (국내산, 영천)을 구매하여 100% 에탄올로 추출하였다. 에탄올 추출물 650 g을 수득 하였다. 이 과정을 3번 반복 하고, 농축액은 사용할 때까지 4℃에서 보관하였다. 6 kg of perilla leaves (from Korea, Yeongcheon) were purchased and extracted with 100% ethanol. 650 g of ethanol extract were obtained. This process was repeated 3 times, and the concentrate was stored at 4°C until use.
실시예 2. 자소엽 에탄올 추출물로부터 분획물의 제조Example 2. Preparation of fractions from perilla leaf ethanol extract
실시예 1에서 제조된 자소엽 에탄올 추출물을 극성 차이를 이용하여 섞이지 않는 용매로 분획하였다. 구체적으로 상기 에탄올 추출물을 n-헥산, 디클로로메탄 (DCM), 에틸아세테이트 (EtOAc), 부탄올 및 물을 이용하여 극성별로 분획을 진행하여 헥산 층, DCM 층, EtOAc 층, 부탄올층 및 물층을 얻었다. 이 과정을 3번 반복 하고, 농축액은 사용할 때까지 4℃에서 보관하였다. The perilla leaf ethanol extract prepared in Example 1 was fractionated with an immiscible solvent using the difference in polarity. Specifically, the ethanol extract was fractionated by polarity using n-hexane, dichloromethane (DCM), ethyl acetate (EtOAc), butanol and water to obtain a hexane layer, a DCM layer, an EtOAc layer, a butanol layer and a water layer. This process was repeated 3 times, and the concentrate was stored at 4°C until use.
도 1은 자소엽 추출물의 용매 분획 과정 (scheme)을 나타낸다. 1 shows the solvent fractionation process (scheme) of perilla leaf extract.
보다 구체적으로 도 1은 자소엽 에탄올 추출물의 n-헥산, 디클로로메탄 (DCM), 에틸아세테이트 (EtOAc), 부탄올 및 물을 이용한 용매 분획 과정을 나타낸다. More specifically, FIG. 1 shows a solvent fractionation process using n-hexane, dichloromethane (DCM), ethyl acetate (EtOAc), butanol and water of an ethanol extract of perilla leaf.
비교예 1. 천년초 열매, 천년초 줄기, 구절초, 및 녹차의 에탄올 추출물 제조Comparative Example 1. Preparation of ethanol extracts of cheonnyeoncho fruit, cheonnyeoncho stem, gujeolcho, and green tea
실시예 1에 기재된 자소엽 에탄올 추출물의 제조 방법과 동일한 방법으로 천년초 열매, 천년초 줄기, 구절초, 및 녹차로부터 각 에탄올 추출물을 수득하였다. Each ethanol extract was obtained from the fruit of cheonnyeoncho, the stem of cheonnyeoncho, the gujeolcho, and green tea in the same manner as the method for preparing the ethanol extract of perilla leaf described in Example 1.
시험예 1. 실시예 1 및 비교예 1에서 제조한 에탄올 추출물의 독성 평가 및 IL-17A의 발현량 측정Test Example 1. Evaluation of toxicity of ethanol extracts prepared in Example 1 and Comparative Example 1 and measurement of IL-17A expression level
실시예 1에서 수득한 자소엽 에탄올 추출물과 비교예 1에서 수득한 천년초 열매, 천년초 줄기, 구절초, 및 녹차의 각 에탄올 추출물을 이용하여 독성 평가 및 IL-17A의 발현량을 측정하였다. Toxicity evaluation and IL-17A expression levels were measured using the ethanol extract of perilla leaf obtained in Example 1 and the ethanol extracts of perilla leaf obtained in Comparative Example 1, stem, gujeolcho, and green tea.
(1) 독성 평가 (세포 활성 측정) (1) Toxicity evaluation (cell activity measurement)
B6 마우스 6주령에서 췌장을 꺼낸 후 CD4-beads를 이용하여 MACS positive separation으로 CD4+ T 세포만을 분리하였고, 96-multi well plate에 5 x 105 세포를 seeding하고 5% CO2 인큐베이터에서 배양 하였다. 배양된 세포에 자소엽, 천년초 열매, 천년초 줄기, 및 구절초의 각 에탄올 추출물 (2, 5, 10 ㎍/mL )을 각각 처리한 다음, 1일간 배양한 후 MTT를 추가하여 37℃에서 4시간 배양하였다. 이후 0.04N HCl in isopropanol 100 ul를 넣어 formazan을 녹여낸 후 570 nm에서 microplate reader (Emax, Molecular Devices)를 이용하여 흡광도를 측정하여 세포활성을 측정하였다. 대조군은 DMSO 처리군으로 하였다.After removing the pancreas from B6 mice at 6 weeks of age, using CD4-beads, only CD4 + T cells were isolated by MACS positive separation, 5 x 10 5 cells were seeded in a 96-multi well plate, and cultured in a 5% CO 2 incubator. The cultured cells were treated with each ethanol extract (2, 5, 10 μg/mL ) of perilla leaf, chrysanthemum stem, and gujeolcho, and then cultured for 1 day, then added MTT and cultured at 37°C for 4 hours. did. After dissolving formazan by adding 100 ul of 0.04N HCl in isopropanol, absorbance was measured at 570 nm using a microplate reader (Emax, Molecular Devices) to measure cell activity. The control group was the DMSO-treated group.
도 2A는 자소엽, 천년초 열매, 천년초 줄기, 및 구절초의 각 에탄올 추출물의 독성 평가에 따른 세포 생존률(%)를 나타낸다.Figure 2A shows the cell viability (%) according to the toxicity evaluation of each ethanol extract of perilla leaf, fruit of cheonnyeoncho, stem of ch.
보다 구체적으로 도 2A는 상기 각 에탄올 추출물을 2, 5, 10 ㎍/mL 로 농도를 달리하여 측정한 독성 평가 결과를 나타낸다. More specifically, Figure 2A shows the toxicity evaluation results measured by varying the concentration of each ethanol extract to 2, 5, 10 ㎍ / mL.
도 2A에서 보는 바와 같이 각 에탄올 추출물은 세포 독성을 보이지 않았다. As shown in Figure 2A, each ethanol extract did not show cytotoxicity.
(2) IL-17A 발현률(%) 측정 (IL-17A 억제 효과 측정) (2) IL-17A expression rate (%) measurement (IL-17A inhibitory effect measurement)
B6 마우스 6주령에서 췌장을 꺼낸 후 CD4-beads를 이용하여 MACS positive separation으로 CD4+ T 세포만을 분리하였고, 분리한 CD4+ T 세포를 anti-CD3, CD28 (각 1 μg/ml) 항체를 코팅한 12-multi well plate에 1.2 x 106세포를 seeding하고 Th17으로의 분화를 위하여 IL-6, TGF-β를 각각 25 ng/ml 및 2.5 ng/ml 의 농도로 처리하였다. 배양된 세포에 자소엽, 천년초 열매, 천년초 줄기, 구절초, 및 녹차의 각 에탄올 추출물 (5, 10 ㎍/mL )을 처리한 다음, 1-3일간 배양한 후 CD4-APC와 IL-17A-PE intracellular staining kit로 염색한 후 FACS로 IL-17A 발현량을 측정하였다. 대조군은 DMSO 처리군으로 하였다.After removing the pancreas from B6 mice at 6 weeks of age, only CD4 + T cells were isolated by MACS positive separation using CD4-beads. -1.2
도 2B는 자소엽, 천년초 열매, 천년초 줄기, 구절초, 및 녹차의 각 에탄올 추출물의 IL-17A 발현률(%)을 나타낸다. Figure 2B shows the IL-17A expression rate (%) of each ethanol extract of perilla, cheonnyeoncho fruit, cheonnyeoncho stem, gujeolcho, and green tea.
보다 구체적으로 도 2B는 상기 각 에탄올 추출물을 5, 10 ㎍/mL 로 농도를 달리하여 측정한 IL-17A 발현률(%)을 나타낸다.More specifically, Figure 2B shows the IL-17A expression rate (%) measured by varying the concentration of each of the ethanol extracts at 5 and 10 μg/mL.
도 2B에서 보는 바와 같이 자소엽 에탄올 추출물은 5, 10 ㎍/mL 농도에서 모두 IL-17A 발현을 효과적으로 억제하였다. As shown in FIG. 2B , the ethanol extract of perilla leaves effectively inhibited IL-17A expression at concentrations of 5 and 10 μg/mL.
시험예 2. 실시예 2에서 제조한 자소엽 분획물의 독성 평가 및 IL-17A 발현량의 측정 Test Example 2. Evaluation of toxicity of the perilla leaf fraction prepared in Example 2 and measurement of IL-17A expression level
실시예 2에서 자소엽 에탄올 추출물로부터 수득한 헥산 분획물 (HEX FR.), 디클로로메탄 분획물 (DCM FR.), 에틸아세테이트 분획물 (EA FR.), 부탄올 분획물 (BuOH FR.), 물 분획물 (Water FR.)을 이용하여 독성 평가 및 IL-17A의 발현량을 측정하였다.A hexane fraction (HEX FR.), a dichloromethane fraction (DCM FR.), an ethyl acetate fraction (EA FR.), a butanol fraction (BuOH FR.), a water fraction (Water FR) obtained from the ethanol extract of perilla leaf in Example 2 .) was used to evaluate toxicity and measure the expression level of IL-17A.
(1) 독성 평가 (세포 활성 측정) (1) Toxicity evaluation (cell activity measurement)
B6 마우스 6주령에서 췌장을 꺼낸 후 CD4-beads를 이용하여 MACS positive separation으로 CD4+ T 세포만을 분리하였고, 96-multi well plate에 5 x 105 세포를 seeding하고 5% CO2 인큐베이터에서 배양 하였다. 배양된 세포에 자소엽 에탄올 추출물의 헥산, 디클로로메탄, 에틴아세테이트, 부탄올, 물 분획물을 각각 10, 20, 50, 100 ㎍/mL 의 농도로 처리한 다음, 1일간 배양한 후 MTT를 추가하여 37℃에서 4시간 배양하였다. 이후 0.04N HCl in isopropanol 100 ul를 넣어 formazan을 녹여낸 후 570 nm에서 microplate reader (Emax, Molecular Devices)를 이용하여 흡광도를 측정하여 세포활성을 측정하였다. 대조군은 DMSO 처리군으로 하였다.After removing the pancreas from B6 mice at 6 weeks of age, using CD4-beads, only CD4 + T cells were isolated by MACS positive separation, 5 x 10 5 cells were seeded in a 96-multi well plate, and cultured in a 5% CO 2 incubator. The cultured cells were treated with hexane, dichloromethane, ethin acetate, butanol, and water fractions of perilla leaf ethanol extract at concentrations of 10, 20, 50, and 100 μg/mL, respectively, and then cultured for 1 day and then added with MTT. Incubated at ℃ for 4 hours. After dissolving formazan by adding 100 ul of 0.04N HCl in isopropanol, absorbance was measured at 570 nm using a microplate reader (Emax, Molecular Devices) to measure cell activity. The control group was the DMSO-treated group.
도 3A는 자소엽 헥산 분획물 (HEX FR.), 디클로로메탄 분획물 (DCM FR.), 에틸아세테이트 분획물 (EA FR.), 부탄올 분획물 (BuOH FR.), 물 분획물 (Water FR.)의 독성 평가에 따른 세포 생존률(%)를 나타낸다. Figure 3A shows the toxicity evaluation of perilla hexane fraction (HEX FR.), dichloromethane fraction (DCM FR.), ethyl acetate fraction (EA FR.), butanol fraction (BuOH FR.), water fraction (Water FR.) Cell viability (%) is shown.
보다 구체적으로 도 3A는 상기 각 자소엽 분획물을 10, 20, 50, 100 ㎍/mL 로 농도를 달리하여 측정한 독성 평가 결과를 나타낸다. More specifically, FIG. 3A shows the results of toxicity evaluation measured by varying concentrations of each of the perilla fractions at 10, 20, 50, and 100 μg/mL.
(2) IL-17A 발현률(%) 측정 (IL-17A 억제 효과 측정) (2) IL-17A expression rate (%) measurement (IL-17A inhibitory effect measurement)
B6 마우스 6주령에서 췌장을 꺼낸 후 CD4-beads를 이용하여 MACS positive separation으로 CD4+ T 세포만을 분리하였고, 분리한 CD4+ T 세포를 anti-CD3, CD28 (각 1 μg/ml) 항체를 코팅한 12-multi well plate에 1.2 x 106세포를 seeding하고 Th17으로의 분화를 위하여 IL-6, TGF-β를 각각 25 ng/ml 및 2.5 ng/ml 의 농도로 처리하였다. 배양된 세포에 자소엽 에탄올 추출물의 헥산, 디클로로메탄, 에틴아세테이트, 부탄올, 물 분획물을 각각 10, 20, 50, 100 ㎍/mL 의 농도로 처리한 다음, 1-3일간 배양한 후 CD4-APC와 IL-17A-PE intracellular staining kit로 염색한 후 FACS로 IL-17A 발현량을 측정하였다. 대조군은 DMSO 처리군으로 하였다.After removing the pancreas from B6 mice at 6 weeks of age, only CD4 + T cells were isolated by MACS positive separation using CD4-beads. -1.2
도 3B는 자소엽 헥산 분획물 (HEX FR.), 디클로로메탄 분획물 (DCM FR.), 에틸아세테이트 분획물 (EA FR.), 부탄올 분획물 (BuOH FR.), 물 분획물 (Water FR.)의 IL-17A 발현률(%)을 나타낸다. Figure 3B shows IL-17A of perilla hexane fraction (HEX FR.), dichloromethane fraction (DCM FR.), ethyl acetate fraction (EA FR.), butanol fraction (BuOH FR.), water fraction (Water FR.) Expression rate (%) is shown.
보다 구체적으로 도 3B 상기 각 자소엽 분획물을 10, 20, 50, 100 ㎍/mL 로 농도를 달리하여 측정한 IL-17A 발현률(%)을 나타낸다. More specifically, FIG. 3B shows the IL-17A expression rate (%) measured by varying concentrations of 10, 20, 50, and 100 μg/mL of each perilla fraction.
도 3B에서 보는 바와 같이, 자소엽 디클로로메탄 분획물은 IL-17A 발현을 특히 효과적으로 억제하였다.As shown in FIG. 3B , the perilla dichloromethane fraction particularly effectively inhibited IL-17A expression.
시험예 3. 실시예 2에서 제조한 자소엽 디클로로메탄 분획물의 독성 평가 및 IL-17A 발현량의 측정 Test Example 3. Toxicity evaluation and IL-17A expression level of dichloromethane fraction from perilla leaf prepared in Example 2
실시예 2에서 자소엽 에탄올 추출물로부터 수득한 디클로로메탄 분획물 (DCM FR.)을 이용하여 농도를 달리하여 독성 평가 및 IL-17A의 발현량을 측정하였다.In Example 2, the dichloromethane fraction (DCM FR.) obtained from the ethanol extract of perilla leaf was used at different concentrations to evaluate toxicity and measure the expression level of IL-17A.
(1) 독성 평가 (세포 활성 측정) (1) Toxicity evaluation (cell activity measurement)
배양된 세포에 자소엽 에탄올 추출물로부터 수득한 디클로로메탄 분획물을 1, 5 및 10 ㎍/mL 농도로 처리하여 시험예 2의 독성 평가와 동일한 방법으로 측정하였다. The cultured cells were treated with the dichloromethane fraction obtained from the ethanol extract of perilla leaflet at concentrations of 1, 5 and 10 μg/mL, and measured in the same manner as in the toxicity evaluation of Test Example 2.
도 4A는 자소엽 디클로로메탄 (DCM) 분획물의 독성 평가에 따른 세포 생존률(%)를 나타낸다. Figure 4A shows the cell viability (%) according to the toxicity assessment of the perilla dichloromethane (DCM) fraction.
보다 구체적으로 도 4A는 대조군(100% 자소엽 에탄올 추출물, 10 ㎍/mL )과 1, 5 및 10 ㎍/mL 농도의 자소엽 디클로로메탄 분획물 (DCM FR.)을 이용하여 측정한 독성 평가 결과를 나타낸다.More specifically, FIG. 4A shows the toxicity evaluation results measured using the control (100% perilla ethanol extract, 10 μg/mL) and the perilla dichloromethane fraction (DCM FR.) at concentrations of 1, 5 and 10 μg/mL. indicates.
도 4A에서 보는 바와 같이 자소엽 디클로로메탄 분획물은 1, 5 및 10 ㎍/mL 농도에서 모두 세포 독성을 보이지 않았다. As shown in FIG. 4A , the perilla dichloromethane fraction showed no cytotoxicity at concentrations of 1, 5, and 10 μg/mL.
(2) IL-17A 발현률(%) 측정 (IL-17A 억제 효과 측정) (2) IL-17A expression rate (%) measurement (IL-17A inhibitory effect measurement)
배양된 세포에 자소엽 에탄올 추출물로부터 수득한 디클로로메탄 분획물을 1, 5 및 10 ㎍/mL 농도로 처리하여 시험예 2의 IL-17A 발현률(%) 측정과 동일한 방법으로 측정하였다. The cultured cells were treated with the dichloromethane fraction obtained from the perilla ethanol extract at concentrations of 1, 5, and 10 μg/mL, and measured in the same manner as in Test Example 2 for measuring the IL-17A expression rate (%).
IL-6, TGF-β만 추가하여 분화를 최대한 유도한 경우를 Th17로 하였다. The case where differentiation was maximally induced by adding only IL-6 and TGF-β was designated as Th17.
도 4B는 대조군, Th17, 자소엽 에탄올 추출물 10 ㎍/mL (양성대조군)과 자소엽 디클로로메탄 분획물 (DCM FR.)을 이용하여 측정한 IL-17A의 발현량 측정 결과를 나타낸다.FIG. 4B shows the results of measuring the expression level of IL-17A measured using the control group, Th17, 10 μg/mL of perilla ethanol extract (positive control), and perilla dichloromethane fraction (DCM FR.).
보다 구체적으로 도 4B는 자소엽 디클로로메탄 분획물 (DCM FR.)을 0.1, 1, 5, 10 ㎍/mL 로 농도를 달리하여 측정한 IL-17A의 발현량 측정 결과를 나타낸다.More specifically, FIG. 4B shows the results of measuring the expression level of IL-17A measured by varying concentrations of the perilla dichloromethane fraction (DCM FR.) at 0.1, 1, 5, and 10 μg/mL.
도 4B에서 보는 바와 같이, 자소엽 디클로로메탄 분획물은 0.1 ㎍/mL 이상 농도에서 모두 IL-17A 발현을 효과적으로 억제하였다.As shown in FIG. 4B , the dichloromethane fraction of perilla leaves effectively inhibited IL-17A expression at concentrations of 0.1 μg/mL or more.
실시예 3. 자소엽 디클로로메탄 서브 분획물의 분리Example 3. Separation of perilla dichloromethane sub-fractions
실시예 2의 방법으로 자소엽 에탄올 추출물로부터 얻은 디클로로메탄 분획물 으로부터 활성 성분 유래 분리 (bioassay-guided isolation) 방법을 이용하여 활성 성분의 분리를 진행하였다. 먼저 자소엽 디클로로메탄 분획물을 Silica Open Column Chromatography (chloroform : methanol = 100 : 1 ~ 50 : 1 ~ 20 : 1 ~ 10 : 1 ~ 5 : 5 ~ 0 : 1)를 실시하여 7개의 분획 (fraction)으로 나누고, 각 분획들의 활성을 확인하였다. The active ingredient was separated from the dichloromethane fraction obtained from the ethanol extract of perilla leaf in the method of Example 2 using a bioassay-guided isolation method. First, Silica Open Column Chromatography (chloroform : methanol = 100 : 1 ~ 50 : 1 ~ 20 : 1 ~ 10 : 1 ~ 5: 5 ~ 0 : 1) was performed on the perilla dichloromethane fraction into 7 fractions. divided, and the activity of each fraction was confirmed.
도 5는 자소엽 디클로로메탄 (DCM) 각 서브 분획물의 IL-17A 발현률(%)을 나타낸다. 5 shows the IL-17A expression rate (%) of each sub-fraction of perilla dichloromethane (DCM).
그 결과 대체적으로 IL-17 발현 억제 활성이 높은 4번 fraction (PFD4)을 선택하였다. As a result, fraction 4 (PFD4) having high IL-17 expression inhibition activity was selected.
실시예 4. 자소엽 디클로로메탄 분획물로부터 활성 성분의 분리Example 4. Separation of active ingredient from perilla dichloromethane fraction
(1) 자소엽 DCM 분획물로부터 활성 성분의 분리 (1) Separation of active ingredient from perilla DCM fraction
실시예 3의 방법으로 얻은 자소엽 디클로로메탄 분획물의 4번 분획 (PFD4) 선택하여 계속하여 유효성분을 분리하였다.The active ingredient was separated by selecting fraction 4 (PFD4) of the dichloromethane fraction of perilla leaf obtained in the method of Example 3.
PFD4 를 실리카젤을 고정상으로 사용한 오픈 컬럼크로마토그래피(chloroform : methanol = 100 : 1 ~ 20 : 1 ~ 1 : 1 ~ 0 : 1)에 적용하여 얻은 6개의 서브 분획 (subfraction) 중 얻었다. 이 중 가장 양이 많은 PFD4-2층을 선택하여 Silica Open Column Chromatography (chloroform : methanol = 100 : 1 ~ 0 : 1)를 실시하여 다시 7개의 서브 분획 (subfraction)을 확보하고 이 중 PFD4-2-5층(232 mg)을 선택하여 Silica Open Column Chromatography (chloroform : acetone = 4.5 : 1 ~ 3 : 1 ~ 1 : 1 ~ 0 : 1, methanol 100%)를 실시하였으며 그 결과 6번 분획 (4-2-5-6)의 단일물질을 활성 성분으로 확보하였다. PFD4 was obtained from six subfractions obtained by applying open column chromatography (chloroform: methanol = 100: 1 to 20: 1 to 1: 1 to 0: 1) using silica gel as a stationary phase. Silica Open Column Chromatography (chloroform: methanol = 100: 1 to 0: 1) was performed by selecting the PFD4-2 layer with the highest amount among them to obtain 7 sub-fractions, and among them, PFD4-2- Silica Open Column Chromatography (chloroform : acetone = 4.5 : 1 ~ 3 : 1 ~ 1 : 1 ~ 0 : 1,
도 6는 PFD4-2 서브 분획물 (subfraction)의 TLC 결과를 나타낸다. 6 shows the TLC results of the PFD4-2 subfraction.
(2) 자소엽 DCM 분획물로부터 분리된 활성 성분의 화합물 동정 (2) Identification of the active ingredient isolated from the perilla DCM fraction
도 7A는 PFD4-2-5-6의 1H-NMR 스펙트럼(400MHz, CD3OD)를 나타낸다. 7A shows 1 H-NMR spectrum (400 MHz, CD 3 OD) of PFD4-2-5-6.
도 7B는 PFD4-2-5-6의 13C-NMR 스펙트럼(100MHz, CD3OD)를 나타낸다. 7B shows the 13 C-NMR spectrum (100 MHz, CD 3 OD) of PFD4-2-5-6.
분리된 활성 성분인 화합물 1의 1H-NMR, 13C-NMR 결과를 문헌과 비교하여 토멘트산 (tormentic acid)으로 화합물 구조를 각각 동정하였다. The 1 H-NMR and 13 C-NMR results of the isolated active ingredient,
화합물 1 - White powder; C30H48O5 MS m/z 489 [M+H]+; 1H NMR (500 MHz, Pyridine-d5): δ 5.52 (1H, brs, H-12), 4.04 (1H, ddd, J=10.5, 9.5, 4.5 Hz, H-2), 3.32 (1H, d, J=9.5 Hz, H-3), 3.06 (1H, ddd, J=13.5, 12.5, 4.5 Hz, H-16), 2.98 (1H, s, H-18), 1.65 (3H, s, Me-27), 1.37 (3H, s, Me-29), 1.20 (3H, s, Me-23), 1.05 (3H, d, J=6.0 Hz, Me-30), 1.04 (3H, s, Me-26), 1.01 (3H, s, Me-24), 0.93 (3H, s, Me-25); 13C NMR (125 MHz, Pyridine-d5): δ 180.4 (C-28), 144.6 (C-13), 127.7 (C-12), 83.6 (C-3), 72.4 (C-19), 68.3 (C-2), 55.7 (C-5), 54.3 (C-18), 48.5 (C-17), 48.1 (C-9), 48.0 (C-1), 42.6 (C-20), 42.1 (C-14), 40.1 (C-8), 39.8 (C-4), 38.5 (C-10, C-22), 33.2 (C-7), 29.2 (C-23), 29.1 (C-15), 26.8 (C-29), 26.7 (C-21), 26.1 (C-16), 24.6 (C-27), 24.5 (C-11), 18.9 (C-6), 17.5 (C-24), 17.1 (C-26), 16.7 (C-25), 16.4 (C-30). Compound 1 - White powder; C 30 H 48 O 5 MS m/z 489 [M+H] + ; 1 H NMR (500 MHz, Pyridine- d5 ): δ 5.52 (1H, brs, H-12), 4.04 (1H, ddd, J =10.5, 9.5, 4.5 Hz, H-2), 3.32 (1H, d, J =9.5 Hz, H-3), 3.06 (1H, ddd, J =13.5, 12.5, 4.5 Hz, H-16), 2.98 (1H, s, H-18), 1.65 (3H, s, Me-27) ), 1.37 (3H, s, Me-29), 1.20 (3H, s, Me-23), 1.05 (3H, d, J =6.0 Hz, Me-30), 1.04 (3H, s, Me-26) , 1.01 (3H, s, Me-24), 0.93 (3H, s, Me-25); 13 C NMR (125 MHz, Pyridine- d5 ): δ 180.4 (C-28), 144.6 (C-13), 127.7 (C-12), 83.6 (C-3), 72.4 (C-19), 68.3 ( C-2), 55.7 (C-5), 54.3 (C-18), 48.5 (C-17), 48.1 (C-9), 48.0 (C-1), 42.6 (C-20), 42.1 (C) -14), 40.1 (C-8), 39.8 (C-4), 38.5 (C-10, C-22), 33.2 (C-7), 29.2 (C-23), 29.1 (C-15), 26.8 (C-29), 26.7 (C-21), 26.1 (C-16), 24.6 (C-27), 24.5 (C-11), 18.9 (C-6), 17.5 (C-24), 17.1 (C-26), 16.7 (C-25), 16.4 (C-30).
도 7C는 자소엽 디클로로메탄 분획물로부터 활성 성분으로 분리한 화합물인 토멘트산의 구조를 나타낸다. Fig. 7C shows the structure of tomentic acid, a compound isolated as an active ingredient from a dichloromethane fraction of perilla leaves.
도 8은 자소엽 에탄올 추출물의 디클로로메탄 분획물로부터 토멘트산의 분리 과정을 나타낸다. 8 shows the separation process of tomentic acid from the dichloromethane fraction of perilla leaf ethanol extract.
시험예 4. Th17 억제 효과의 평가 Test Example 4. Evaluation of the Th17 inhibitory effect
자소엽에서 분리한 PFD 4-2-5-6 (토멘트산), PFD 2-3-2-2 (우르솔산), 표준품으로 구입한 토멘트산 (tormentic acid)과 별도로 구입한 로즈마린산 (Rosmarinic acid)을 이용하여 Th17 억제 효과를 측정하였다. PFD 4-2-5-6 (tormentic acid), PFD 2-3-2-2 (ursolic acid) isolated from perilla leaves, tormentic acid purchased as a standard product, and rosmarinic acid purchased separately acid) to measure the Th17 inhibitory effect.
IL-6, TGF-β으로 분화한 세포에 PFD 4-2-5-6, PFD 2-3-2-2, 표준품 토멘트산 또는 로즈마린산을 처리한 후 IL-17A 발현량을 측정하여 Th17 분화 억제 정도를 평가하였다. Cells differentiated with IL-6 and TGF-β were treated with PFD 4-2-5-6, PFD 2-3-2-2, standard product tomentic acid or rosmarinic acid, and then IL-17A expression was measured to differentiate Th17. The degree of inhibition was evaluated.
도 9 및 도 10에서 Th0는 분화를 위한 IL-6, TGF-β를 처리하지 않은 군을 지칭한다. 또한, 도 9 및 도 10에서 Th17은 IL-6, TGF-β만 추가하여 분화를 최대한 군을 지칭한다.In FIGS. 9 and 10 , Th0 refers to a group not treated with IL-6 and TGF-β for differentiation. In addition, in FIGS. 9 and 10, Th17 refers to a group that maximizes differentiation by adding only IL-6 and TGF-β.
도 9은 자소엽에서 분리한 PFD 4-2-5-6 (토멘트산)과 로즈마린산을 이용하여 측정한 IL-17A 발현률(%)을 나타낸다. 자소엽의 DCM층에 가장 많은 함유랑을 차지하는 로즈마린산은 추출물 표준화를 위한 지표성분으로 활용하기 위해 그 효과를 함께 측정하였다.9 shows the IL-17A expression rate (%) measured using PFD 4-2-5-6 (tomic acid) and rosmarinic acid isolated from perilla leaflets. The effect of rosmarinic acid, which occupies the most content in the DCM layer of perilla leaf, was measured together to be used as an index component for extract standardization.
보다 구체적으로 도 9은 자소엽에서 분리한 PFD 4-2-5-6 (토멘트산)과 별도로 Sigma에서 구입한 로즈마린산을 각각 1, 5, 10 ㎍/mL 농도로 하여 측정한 IL-17A 발현률(%)을 나타낸다. More specifically, FIG. 9 shows IL-17A expression rates measured by using rosmarinic acid purchased from Sigma at concentrations of 1, 5, and 10 μg/mL, respectively, separately from PFD 4-2-5-6 (tomentic acid) isolated from perilla leaflets. (%) is shown.
도 9로부터 자소엽에서 분리한 토멘트산과 로즈마린산이 IL-17A 발현을 억제함을 확인하였고, 이로부터 Th17 억제 효능을 확인할 수 있었다. From Fig. 9, it was confirmed that tomentic acid and rosmarinic acid isolated from perilla leaf inhibit IL-17A expression, thereby confirming the Th17 inhibitory effect.
도 10은 자소엽 에탄올 추출물, 자소엽으로부터 분리한 PFD 4-2-5-6 (토멘트산), 토멘트산 표준품 (토멘트산, Core Sciences에서 구입), 및 PFD 2-3-2-2 (우르솔산)을 이용하여 측정한 Th17A 발현률(%)을 나타낸다.10 shows an ethanol extract of perilla leaves, PFD 4-2-5-6 isolated from perilla leaves (tomentic acid), tomentic acid standard (tomentic acid, purchased from Core Sciences), and PFD 2-3-2- The expression rate (%) of Th17A measured using 2 (ursolic acid) is shown.
보다 구체적으로 도 10은 5, 10, 20, 50 ㎍/mL 의 자소엽 에탄올 추출물, 1, 2, 5 ㎍/mL 의 자소엽에서 분리한 PFD 4-2-5-6 (토멘트산), 1, 2, 5 ㎍/mL 의 토멘트산 (tormentic acid) 표준품, 0.5, 1, 2 ㎍/mL 의 자소엽에서 분리한 PFD 2-3-2-2 (우르솔산)을 이용하여 측정한 IL-17A 발현률(%)을 나타낸다. More specifically, FIG. 10 shows ethanol extracts of perilla leaves at 5, 10, 20, and 50 µg/mL, PFD 4-2-5-6 (tomenic acid) isolated from perilla leaves at 1, 2, and 5 µg/mL; IL measured using PFD 2-3-2-2 (ursolic acid) isolated from perilla leaflets at 1, 2, 5 μg/mL tormentic acid standard, and 0.5, 1, 2 μg/mL -17A expression rate (%) is shown.
도 10로부터 자소엽 에탄올 추출물로부터 분리한 토멘트산 (PFD 4-2-5-6)이 IL-17A 발현을 억제함을 확인하였고, 이로부터 Th17 억제 효능을 확인할 수 있었다. From FIG. 10, it was confirmed that tomentic acid (PFD 4-2-5-6) isolated from the ethanol extract of perilla leaf inhibited IL-17A expression, thereby confirming the Th17 inhibitory effect.
자소엽에서 분리한 PFD 4-2-5-6 (토멘트산)은 10 ㎍/mL , 표준품으로 구매한 토멘트산은 5 및 10 ㎍/mL 에서 유의한 IL-17A 발현을 억제 효과를 보이며 억제 비율에 대한 scale이 크게 상이하지 않아 자소엽에서 분리한 PFD 4-2-5-6 과 표준품으로 구매한 토멘트산이 동등한 정도의 효능을 보임을 확인하였다. PFD 4-2-5-6 (tomentic acid) isolated from perilla leaf showed significant inhibitory effect and suppressed IL-17A expression at 10 μg/mL and at 5 and 10 μg/mL of tomentic acid purchased as standard. It was confirmed that PFD 4-2-5-6 isolated from perilla leaf and tomentic acid purchased as a standard product showed the same level of efficacy as the scale for the ratio was not significantly different.
시험예 5. 덱스트란 설페이트 나트륨 (dextran sulfate sodium, DSS) 유발 염증성 장염 모델에서 자소엽으로부터 분리된 토멘트산의 효과 측정Test Example 5. Determination of the effect of tomentic acid isolated from perilla lobules in dextran sulfate sodium (DSS)-induced inflammatory enteritis model
7주령의 C57BL/6 (male) 생쥐를 오리엔트바이오에서 구매하여 SPF 컨디션에서 순화과정을 거쳤다 ((IACUC number: #202000120). 장염증 유발을 위해 2.5% DSS 함유한 음용수를 7일간 제공하였으며, 물 소비량을 매일 체크하였다 (6마리씩 6 그룹으로 분리하여 실험함). Seven-week-old C57BL/6 (male) mice were purchased from Orient Bio and acclimatized in SPF condition ((IACUC number: #202000120). To induce intestinal inflammation, drinking water containing 2.5% DSS was provided for 7 days, and water Consumption was checked daily (tested by dividing 6 animals into 6 groups).
비히클 (vehicle, 콘 오일) 처리군을 음성 대조군으로 하였다. 또한, DSS만 처리한 군 (DSS 유발 및 약물 미 처리군)을 양상 대조군으로 하였다. The vehicle (vehicle, corn oil) treated group was used as a negative control. In addition, a group treated with only DSS (DSS-induced and no drug) was used as a modality control group.
DSS 및 자소엽 에탄올 추출물 50 mg/kg/day 처리군, DSS 및 토멘토산 25 mg/kg/day 처리군, DSS 및 토멘토산 50 mg/kg/day 처리군, DSS 및 메살라진 (mesalazine) (50 mg/kg/day p.o.) 처리군을 시험군으로 하였다. DSS and
7일 후 2.5% DSS 포함 물은 물로 대체하고 1일 후에 (8일째) 동물을 희생하여, 비장 (Spleen), 장간막림프절(mesenteric lymph nodes, MLN) 및 창자 (intestine)를 적출하여 실험하였다.After 7 days, water containing 2.5% DSS was replaced with water, and after 1 day (day 8), the animals were sacrificed, and the spleen, mesenteric lymph nodes (MLN) and intestines were extracted and tested.
도 11은 DSS 유발 염증성 장염 모델에 비히클, 자소엽 에탄올 추출물, 자소엽 추출물로부터 분리한 토멘트산, 그리고 메살라진의 처치 과정을 나타낸다. 11 shows the treatment process of vehicle, perilla ethanol extract, tomentic acid isolated from perilla extract, and mesalazine in a DSS-induced inflammatory enteritis model.
도 12A 및 12B는 DSS 유발 염증성 장염 동물 모델에서 자소엽 에탄올 추출물, 토멘트산, 메살라진 처치 후 장의 길이 변화를 측정한 결과를 나타낸다. 12A and 12B show the results of measuring changes in the length of the intestine after treatment with perilla ethanol extract, tomentic acid, and mesalazine in an animal model of DSS-induced inflammatory enteritis.
도 12A는 비히클 처리군 (Control), DSS 유발 및 약물 미처리 군 (DSS), DSS 및 자소엽 에탄올 추출물 50 mg/kg/day 처리군 (P.F extracts 50 mg/kg), DSS 및 토멘토산 25 mg/kg/day 처리군 (Tormentic acid 25 mg/kg), DSS 및 토멘토산 50 mg/kg/day 처리군 (Tormentic acid 50 mg/kg), DSS 및 메살라진 (mesalazine) 50 mg/kg/day 처리군 (Mesalazine 50 mg/kg)을 처치 후 장의 길이 변화를 측정한 결과를 나타낸다. 또한, 도 12B는 이를 그래프로 표현한 것이다. 12A is a vehicle-treated group (Control), DSS-induced and drug-untreated group (DSS), DSS and
장염증이 심할수록 장의 길이가 짧아지며, 대조군 (Control)에 가까울수록 장염증이 개선된 것을 의미한다.The more severe the intestinal inflammation, the shorter the length of the intestine, and the closer to the control, the better the intestinal inflammation.
도 12A 및 도 12B에서 보는 바와 같이, DSS만 처리한 군 (DSS)은 비히클 처리군 (Control)에 비해 장의 길이가 현저히 줄어든 반면에 토멘트산 25 mg/kg를 투여한 생쥐의 경우 DSS에 의한 장 길이 감소가 현저히 억제되었다.As shown in FIGS. 12A and 12B , the DSS-treated group (DSS) significantly reduced the length of the intestine compared to the vehicle-treated group (Control). The decrease in intestinal length was significantly suppressed.
또한, 도 12A 및 도 12B에서 보는 바와 같이, 자소엽 추출물로부터 분리한 토멘트산이 DSS에 의해 유발된 염증성 장염으로 인한 장의 길이 감소를 유의미하게 억제하였다. In addition, as shown in FIGS. 12A and 12B , tomentic acid isolated from the perilla leaf extract significantly inhibited the decrease in the length of the intestine due to inflammatory enteritis induced by DSS.
도 13A 및 13B는 DSS 유발 염증성 장염 동물 모델에서 장의 조직학적 변화를 나타낸다. 13A and 13B show histological changes in the intestine in an animal model of DSS-induced inflammatory enteritis.
보다 구체적으로 도 13A는 생쥐에서 장(colon)의 조직학적 사진을 H&E 염색법으로 측정한 결과를 나타낸다. 비히클 처리군 (Control) 에 비해 DSS 처리군의 점막층 (mucosa layer)이 파괴된 것을 관찰할 수 있는데, 반면 토멘트산 25 mg/kg를 함께 처리한 군에서는 약간의 부종 (edema)이 관찰되나 DSS 처리군보다 점막층의 파괴가 현저히 개선되었다.More specifically, FIG. 13A shows the results of measuring histological photographs of the colon in mice by H&E staining. It can be observed that the mucosa layer of the DSS-treated group is destroyed compared to the vehicle-treated group (Control). On the other hand, a slight edema is observed in the group treated with tomentic acid 25 mg/kg, but DSS The destruction of the mucosal layer was significantly improved compared to the treatment group.
또한, 도 13B는 염색한 조직의 병리학적인 병증의 심각도를 수치로 표시한 것 것이다.In addition, Figure 13B is a numerical representation of the severity of the pathological condition of the stained tissue.
도 13A 및 13B는 자소엽으로부터 분리된 토멘트산이 DSS에 의해 유발된 장의 조직학적 변화를 유의미하게 억제함을 나타낸다. 13A and 13B show that tomentic acid isolated from perilla lobules significantly inhibited DSS-induced histological changes in the intestine.
또한 토멘트산 25 mg/kg 또는 50 mg/kg 처리 군에서 DSS에 의해 유발된 장의 조직학적 변화가 메살라진 50 mg/kg 투여군 보다도 더 억제됨을 나타낸다. It also shows that the histological changes of the intestine induced by DSS in the 25 mg/kg or 50 mg/kg treatment group of tomentic acid are more inhibited than in the
시험예 6. 사이토카인 발현 억제 평가Test Example 6. Cytokine expression inhibition evaluation
도 14A, 14B, 14C는 각각 실험생쥐의 비장 (Spleen), 장간막림프절 (mesenteric lymph nodes, MLN), 점막 고유층 백혈구 (lamina propria leukocytes, LPL)에서 분리한 CD4+ IL-17+ 세포 발현률(%)을 나타낸다. 14A, 14B, and 14C show the expression rate (%) of CD4 + IL-17 + cells isolated from the spleen, mesenteric lymph nodes (MLN), and lamina propria leukocytes (LPL) of experimental mice, respectively. ) is indicated.
즉, 각각 실험생쥐의 비장, MLN, LPL 에서 CD4+ T세포를 분리한 후 PMA, ionomycin 그리고 Golgi-plug 로 4시간 자극 (stimulation) 한 후 CD4+IL-17A+를 유세포 분석기 (flow cytometry)로 분석한 것이다.That is, after separating CD4 + T cells from the spleen, MLN, and LPL of mice, respectively, stimulation with PMA, ionomycin, and Golgi-plug for 4 hours, CD4 + IL-17A + was analyzed by flow cytometry. it will be analyzed
도 14A, 14B, 14C로부터 DSS에 의해 유도된 염증성 장염 개선효과는 IL-17과 같은 사이토카인 발현 억제에 기인한 것으로 판단된다. From Figures 14A, 14B, and 14C, it is judged that the improvement effect of DSS-induced inflammatory enteritis is due to inhibition of the expression of cytokines such as IL-17.
통계분석 statistical analysis
모든 자료와 도면은 평균 ± 표준 편차로 표현된다. All data and figures are expressed as mean ± standard deviation.
본 연구는 산업통상자원부와 한국산업기술진흥원이 지원하는 광역협력권산업 육성사업으로 수행된 연구결과 입니다(P0004697). This study is the result of a research conducted as a regional cooperation area industry promotion project supported by the Ministry of Trade, Industry and Energy and the Korea Institute for Advancement of Technology (P0004697).
본 발명이 속하는 기술 분야에서 통상의 지식을 가진 자는 본 발명이 본 발명의 본질적인 특성에서 벗어나지 않는 범위에서 변형된 형태로 구현될 수 있음을 이해할 수 있을 것이다. 그러므로, 상기 개시된 실시예들은 한정적인 관점이 아니라 설명적인 관점에서 고려되어야 한다. 본 발명의 범위는 전술한 설명이 아니라 특허청구범위에 나타나 있으며, 그와 동등한 범위 내에 있는 모든 차이점은 본 발명에 포함된 것으로 해석되어야 할 것이다.Those of ordinary skill in the art to which the present invention pertains will understand that the present invention may be implemented in a modified form without departing from the essential characteristics of the present invention. Therefore, the disclosed embodiments are to be considered in an illustrative rather than a restrictive sense. The scope of the present invention is indicated in the claims rather than the foregoing description, and all differences within the scope equivalent thereto should be construed as being included in the present invention.
Claims (14)
[화학식 1]
.A pharmaceutical composition for preventing or treating autoimmune diseases, comprising as an active ingredient a compound represented by the following formula (1) or a salt thereof isolated from the perilla leaf extract:
[Formula 1]
.
상기 단계로부터 얻어진 에탄올 추출물을 30 %(v/v) 내지 99 %(v/v) 디클로로메탄으로 분획하는 단계; 및
상기 단계로부터 얻어진 디클로로메탄 분획물을 실리카젤 컬럼크로마토그래피법으로 분리하여 청구항 1의 화학식 1의 화합물을 얻는 단계;를 포함하는
청구항 1에 따른 자가면역질환 예방 또는 치료용 약학적 조성물의 제조방법. extracting the perilla leaves with 50% (v/v) to 100% (v/v) ethanol;
fractionating the ethanol extract obtained from the above step with 30% (v/v) to 99% (v/v) dichloromethane; and
Separating the dichloromethane fraction obtained from the above step by silica gel column chromatography to obtain the compound of Formula 1 of claim 1;
A method for preparing a pharmaceutical composition for preventing or treating autoimmune diseases according to claim 1.
[화학식 1]
.
A food composition for preventing or treating autoimmune diseases, comprising as an active ingredient a compound represented by the following formula (1) or a salt thereof isolated from the perilla leaf extract:
[Formula 1]
.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020210056874A KR20220149352A (en) | 2021-04-30 | 2021-04-30 | Composition for preventing or treating autoimmune disease comprising compound isolated from Paeonia lactiflora extract as effective component |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020210056874A KR20220149352A (en) | 2021-04-30 | 2021-04-30 | Composition for preventing or treating autoimmune disease comprising compound isolated from Paeonia lactiflora extract as effective component |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220149352A true KR20220149352A (en) | 2022-11-08 |
Family
ID=84041526
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020210056874A KR20220149352A (en) | 2021-04-30 | 2021-04-30 | Composition for preventing or treating autoimmune disease comprising compound isolated from Paeonia lactiflora extract as effective component |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR20220149352A (en) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101970457B1 (en) | 2017-08-31 | 2019-04-19 | 단국대학교 천안캠퍼스 산학협력단 | Pharmaceutical Composition Comprising Fraxinus rhynchophylla Extract for Prevention or Treatment of Autoimmune Disease |
-
2021
- 2021-04-30 KR KR1020210056874A patent/KR20220149352A/en not_active Application Discontinuation
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101970457B1 (en) | 2017-08-31 | 2019-04-19 | 단국대학교 천안캠퍼스 산학협력단 | Pharmaceutical Composition Comprising Fraxinus rhynchophylla Extract for Prevention or Treatment of Autoimmune Disease |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101567633B1 (en) | Composition for treatment or prevention of inflammatory skin diseases comprising unripe Citurs unshiu extract, or synephrine or salts thereof | |
| US20150174186A1 (en) | Pharmaceutical composition for preventing or treating stat3-mediated disease, comprising salvia plebeia r. br. extract or fraction thereof as active ingredient | |
| KR20130142696A (en) | Composition comprising protaetia brevitarsis for preventing and treating inflammatory disorder | |
| JP2008531584A (en) | Composition comprising the genus Matabia and method of using the same | |
| KR20160044807A (en) | Composition comprising extracts or fractions of Justicia genus | |
| KR102124986B1 (en) | Composition for prevention or treatment of muscular disorder or improvement of muscular functions comprising Leonurus japonicus extract or leonurine | |
| JP3968405B2 (en) | Antiallergic agent | |
| US9445987B2 (en) | Ceramide production enhancer and moisturizer | |
| WO2014098512A1 (en) | Pharmaceutical composition comprising fucosterol, as active ingredient, for preventing or treating neurodegenerative diseases | |
| JP2009513626A (en) | An extract of a plant of the genus Yamaceae, and a composition for preventing or treating peripheral neuropathy containing the same | |
| JP6062065B2 (en) | Alpinia species extract for the treatment of irritable bowel syndrome | |
| KR101497109B1 (en) | Composition for preventing, improving, or treating a disease controlled by PPAR action | |
| EP3804728A1 (en) | Composition comprising inotodiol compound as effective ingredient for prevention or treatment of allergy disease | |
| KR102348782B1 (en) | Composition for preventing or treating renal disease comprising Zizyphus jujuba MILL extract | |
| KR20220149352A (en) | Composition for preventing or treating autoimmune disease comprising compound isolated from Paeonia lactiflora extract as effective component | |
| KR20060102620A (en) | Composition containing gentianae macrophyllae radix extract for treatment hypersensitive skin disease | |
| KR101503583B1 (en) | Compositions for anti-obesity comprising extract of Vitis amurensis ruprecht | |
| KR101385191B1 (en) | Use of Cichorium intybus extracts for preventing, treating improving muscular atrophy | |
| KR101332074B1 (en) | Composition Comprising Esculetin for Inhibition of Bone Loss | |
| JP2017052750A (en) | Novel ellagitannins and agents for oral applications | |
| KR101862135B1 (en) | Novel diynoic acid compound and pharmaceutical composition for preventing or treating bone diseases comprising the same | |
| KR101752233B1 (en) | Compositions containing extracts of Plectranthus hadiensis var. tomentosus (Benth. ex E. Mey.) Codd, fractions or isolated compounds isolated therefrom for prevention and treatment of allergy | |
| JP2021066673A (en) | Allergic rhinitis symptom inhibitor | |
| CN111246849A (en) | Composition for enhancing learning and memory ability | |
| KR101356213B1 (en) | Composition for preventing or treating allergy comprising nodakenin |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal |