KR20220032607A - 항암제를 스크리닝하는 방법 및 췌장암 치료를 위한 키나아제 억제제의 조합 의약 - Google Patents
항암제를 스크리닝하는 방법 및 췌장암 치료를 위한 키나아제 억제제의 조합 의약 Download PDFInfo
- Publication number
- KR20220032607A KR20220032607A KR1020227004728A KR20227004728A KR20220032607A KR 20220032607 A KR20220032607 A KR 20220032607A KR 1020227004728 A KR1020227004728 A KR 1020227004728A KR 20227004728 A KR20227004728 A KR 20227004728A KR 20220032607 A KR20220032607 A KR 20220032607A
- Authority
- KR
- South Korea
- Prior art keywords
- inhibitor
- gene
- nucleic acid
- uas
- test substance
- Prior art date
Links
- 206010061902 Pancreatic neoplasm Diseases 0.000 title claims abstract description 67
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 title claims abstract description 67
- 201000002528 pancreatic cancer Diseases 0.000 title claims abstract description 67
- 208000008443 pancreatic carcinoma Diseases 0.000 title claims abstract description 67
- 229940043355 kinase inhibitor Drugs 0.000 title claims abstract description 62
- 239000003757 phosphotransferase inhibitor Substances 0.000 title claims abstract description 62
- 238000000034 method Methods 0.000 title claims abstract description 28
- 239000002246 antineoplastic agent Substances 0.000 title claims abstract description 22
- 238000012216 screening Methods 0.000 title claims abstract description 16
- 229940000425 combination drug Drugs 0.000 title claims description 10
- 241000255581 Drosophila <fruit fly, genus> Species 0.000 claims abstract description 65
- 241000255588 Tephritidae Species 0.000 claims abstract description 62
- 239000000126 substance Substances 0.000 claims abstract description 58
- 238000012360 testing method Methods 0.000 claims abstract description 54
- 230000014509 gene expression Effects 0.000 claims abstract description 53
- 230000004083 survival effect Effects 0.000 claims abstract description 52
- 108700025694 p53 Genes Proteins 0.000 claims abstract description 30
- 101150060022 med gene Proteins 0.000 claims abstract description 29
- 101150045048 Ras85D gene Proteins 0.000 claims abstract description 28
- 239000003814 drug Substances 0.000 claims abstract description 28
- 108090000257 Cyclin E Proteins 0.000 claims abstract description 26
- 230000037430 deletion Effects 0.000 claims abstract description 16
- 238000012217 deletion Methods 0.000 claims abstract description 16
- 230000002018 overexpression Effects 0.000 claims abstract description 11
- 230000001629 suppression Effects 0.000 claims abstract description 9
- 239000003112 inhibitor Substances 0.000 claims description 151
- 108020004707 nucleic acids Proteins 0.000 claims description 59
- 102000039446 nucleic acids Human genes 0.000 claims description 59
- 150000007523 nucleic acids Chemical class 0.000 claims description 59
- 108091027967 Small hairpin RNA Proteins 0.000 claims description 51
- 239000004055 small Interfering RNA Substances 0.000 claims description 50
- 239000002829 mitogen activated protein kinase inhibitor Substances 0.000 claims description 41
- 102100040959 Tyrosine-protein kinase FRK Human genes 0.000 claims description 38
- 239000002773 nucleotide Substances 0.000 claims description 33
- 125000003729 nucleotide group Chemical group 0.000 claims description 33
- 229960004066 trametinib Drugs 0.000 claims description 33
- LIRYPHYGHXZJBZ-UHFFFAOYSA-N trametinib Chemical group CC(=O)NC1=CC=CC(N2C(N(C3CC3)C(=O)C3=C(NC=4C(=CC(I)=CC=4)F)N(C)C(=O)C(C)=C32)=O)=C1 LIRYPHYGHXZJBZ-UHFFFAOYSA-N 0.000 claims description 33
- 229940124647 MEK inhibitor Drugs 0.000 claims description 32
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Natural products NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims description 29
- 150000001413 amino acids Chemical group 0.000 claims description 20
- 239000004471 Glycine Substances 0.000 claims description 18
- 235000003704 aspartic acid Nutrition 0.000 claims description 18
- CKLJMWTZIZZHCS-REOHCLBHSA-N aspartic acid group Chemical group N[C@@H](CC(=O)O)C(=O)O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 claims description 18
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 claims description 18
- 238000009395 breeding Methods 0.000 claims description 17
- 230000001488 breeding effect Effects 0.000 claims description 17
- 108090000623 proteins and genes Proteins 0.000 claims description 17
- 230000005764 inhibitory process Effects 0.000 claims description 15
- 235000013305 food Nutrition 0.000 claims description 14
- 108010001515 Galectin 4 Proteins 0.000 claims description 13
- 102000003909 Cyclin E Human genes 0.000 claims description 10
- 235000013601 eggs Nutrition 0.000 claims description 9
- 235000005911 diet Nutrition 0.000 claims description 8
- 230000037213 diet Effects 0.000 claims description 8
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 claims description 7
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical group SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 claims description 6
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical group CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims description 6
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Chemical group CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims description 6
- 235000018417 cysteine Nutrition 0.000 claims description 6
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Chemical group SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 claims description 6
- 239000011435 rock Substances 0.000 claims description 6
- 235000014393 valine Nutrition 0.000 claims description 6
- 239000004474 valine Chemical group 0.000 claims description 6
- 235000018102 proteins Nutrition 0.000 claims description 4
- 102000004169 proteins and genes Human genes 0.000 claims description 4
- 230000000384 rearing effect Effects 0.000 claims description 3
- 241000255925 Diptera Species 0.000 description 58
- 108090000433 Aurora kinases Proteins 0.000 description 31
- 102000003989 Aurora kinases Human genes 0.000 description 31
- 108020004414 DNA Proteins 0.000 description 28
- 210000004027 cell Anatomy 0.000 description 27
- 206010028980 Neoplasm Diseases 0.000 description 26
- 102200006539 rs121913529 Human genes 0.000 description 22
- 230000035772 mutation Effects 0.000 description 17
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 15
- 108091000080 Phosphotransferase Proteins 0.000 description 14
- 201000011510 cancer Diseases 0.000 description 13
- 238000003197 gene knockdown Methods 0.000 description 12
- 102100039556 Galectin-4 Human genes 0.000 description 10
- 241001465754 Metazoa Species 0.000 description 10
- 102000020233 phosphotransferase Human genes 0.000 description 10
- 206010064571 Gene mutation Diseases 0.000 description 9
- 239000012634 fragment Substances 0.000 description 9
- 230000000694 effects Effects 0.000 description 8
- 230000002779 inactivation Effects 0.000 description 8
- 238000011161 development Methods 0.000 description 7
- 230000018109 developmental process Effects 0.000 description 7
- 229940079593 drug Drugs 0.000 description 7
- 238000002360 preparation method Methods 0.000 description 7
- 239000013598 vector Substances 0.000 description 7
- 101000584612 Homo sapiens GTPase KRas Proteins 0.000 description 6
- 241000699670 Mus sp. Species 0.000 description 6
- 230000000692 anti-sense effect Effects 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 101000721661 Homo sapiens Cellular tumor antigen p53 Proteins 0.000 description 5
- 101000621390 Homo sapiens Wee1-like protein kinase Proteins 0.000 description 5
- 102000004232 Mitogen-Activated Protein Kinase Kinases Human genes 0.000 description 5
- 108090000744 Mitogen-Activated Protein Kinase Kinases Proteins 0.000 description 5
- 108091034117 Oligonucleotide Proteins 0.000 description 5
- 102100023037 Wee1-like protein kinase Human genes 0.000 description 5
- 230000032823 cell division Effects 0.000 description 5
- 230000004663 cell proliferation Effects 0.000 description 5
- 210000000349 chromosome Anatomy 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 239000008194 pharmaceutical composition Substances 0.000 description 5
- 230000008685 targeting Effects 0.000 description 5
- 101150041972 CDKN2A gene Proteins 0.000 description 4
- 102100025064 Cellular tumor antigen p53 Human genes 0.000 description 4
- 108010009392 Cyclin-Dependent Kinase Inhibitor p16 Proteins 0.000 description 4
- 102000009508 Cyclin-Dependent Kinase Inhibitor p16 Human genes 0.000 description 4
- 102100030708 GTPase KRas Human genes 0.000 description 4
- 241000282412 Homo Species 0.000 description 4
- 108091081021 Sense strand Proteins 0.000 description 4
- 230000037396 body weight Effects 0.000 description 4
- 210000002919 epithelial cell Anatomy 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 230000003278 mimic effect Effects 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 108700042657 p16 Genes Proteins 0.000 description 4
- 230000009261 transgenic effect Effects 0.000 description 4
- BKWJAKQVGHWELA-UHFFFAOYSA-N 1-[6-(2-hydroxypropan-2-yl)-2-pyridinyl]-6-[4-(4-methyl-1-piperazinyl)anilino]-2-prop-2-enyl-3-pyrazolo[3,4-d]pyrimidinone Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1NC1=NC=C2C(=O)N(CC=C)N(C=3N=C(C=CC=3)C(C)(C)O)C2=N1 BKWJAKQVGHWELA-UHFFFAOYSA-N 0.000 description 3
- 108020004705 Codon Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- -1 FRK Proteins 0.000 description 3
- 108091054455 MAP kinase family Proteins 0.000 description 3
- 102000043136 MAP kinase family Human genes 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 101710143112 Mothers against decapentaplegic homolog 4 Proteins 0.000 description 3
- 102000049937 Smad4 Human genes 0.000 description 3
- 108020004459 Small interfering RNA Proteins 0.000 description 3
- 229950009557 adavosertib Drugs 0.000 description 3
- 229940041181 antineoplastic drug Drugs 0.000 description 3
- 230000006907 apoptotic process Effects 0.000 description 3
- 230000003833 cell viability Effects 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 239000003623 enhancer Substances 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 231100000225 lethality Toxicity 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 210000004881 tumor cell Anatomy 0.000 description 3
- WPHKIQPVPYJNAX-UHFFFAOYSA-N 1-[4-[4-amino-7-[1-(2-hydroxyethyl)pyrazol-4-yl]thieno[3,2-c]pyridin-3-yl]phenyl]-3-(3-fluorophenyl)urea Chemical compound C1=2SC=C(C=3C=CC(NC(=O)NC=4C=C(F)C=CC=4)=CC=3)C=2C(N)=NC=C1C=1C=NN(CCO)C=1 WPHKIQPVPYJNAX-UHFFFAOYSA-N 0.000 description 2
- GKHIVNAUVKXIIY-UHFFFAOYSA-N 2-[3-[4-(1h-indazol-5-ylamino)quinazolin-2-yl]phenoxy]-n-propan-2-ylacetamide Chemical compound CC(C)NC(=O)COC1=CC=CC(C=2N=C3C=CC=CC3=C(NC=3C=C4C=NNC4=CC=3)N=2)=C1 GKHIVNAUVKXIIY-UHFFFAOYSA-N 0.000 description 2
- ZLHFILGSQDJULK-UHFFFAOYSA-N 4-[[9-chloro-7-(2-fluoro-6-methoxyphenyl)-5H-pyrimido[5,4-d][2]benzazepin-2-yl]amino]-2-methoxybenzoic acid Chemical compound C1=C(C(O)=O)C(OC)=CC(NC=2N=C3C4=CC=C(Cl)C=C4C(=NCC3=CN=2)C=2C(=CC=CC=2F)OC)=C1 ZLHFILGSQDJULK-UHFFFAOYSA-N 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- NRSGWEVTVGZDFC-UHFFFAOYSA-N 6-chloro-4-n-[3,5-difluoro-4-[(3-methyl-1h-pyrrolo[2,3-b]pyridin-4-yl)oxy]phenyl]pyrimidine-2,4-diamine Chemical compound C=12C(C)=CNC2=NC=CC=1OC(C(=C1)F)=C(F)C=C1NC1=CC(Cl)=NC(N)=N1 NRSGWEVTVGZDFC-UHFFFAOYSA-N 0.000 description 2
- 206010006187 Breast cancer Diseases 0.000 description 2
- 208000026310 Breast neoplasm Diseases 0.000 description 2
- 101150032848 CycE gene Proteins 0.000 description 2
- 108010024986 Cyclin-Dependent Kinase 2 Proteins 0.000 description 2
- 102100036239 Cyclin-dependent kinase 2 Human genes 0.000 description 2
- 108700020954 Drosophila CycE Proteins 0.000 description 2
- 108700035323 Drosophila a Proteins 0.000 description 2
- 101000687968 Homo sapiens Membrane-associated tyrosine- and threonine-specific cdc2-inhibitory kinase Proteins 0.000 description 2
- 101000835893 Homo sapiens Mothers against decapentaplegic homolog 4 Proteins 0.000 description 2
- 101000669917 Homo sapiens Rho-associated protein kinase 1 Proteins 0.000 description 2
- 101000669921 Homo sapiens Rho-associated protein kinase 2 Proteins 0.000 description 2
- 101001059454 Homo sapiens Serine/threonine-protein kinase MARK2 Proteins 0.000 description 2
- 101000621401 Homo sapiens Wee1-like protein kinase 2 Proteins 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 102100024262 Membrane-associated tyrosine- and threonine-specific cdc2-inhibitory kinase Human genes 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- 208000008900 Pancreatic Ductal Carcinoma Diseases 0.000 description 2
- 108010029485 Protein Isoforms Proteins 0.000 description 2
- 102000001708 Protein Isoforms Human genes 0.000 description 2
- 102000001253 Protein Kinase Human genes 0.000 description 2
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 2
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 2
- 102100039313 Rho-associated protein kinase 1 Human genes 0.000 description 2
- 102100039314 Rho-associated protein kinase 2 Human genes 0.000 description 2
- 101150019443 SMAD4 gene Proteins 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- 102100028904 Serine/threonine-protein kinase MARK2 Human genes 0.000 description 2
- 101150080074 TP53 gene Proteins 0.000 description 2
- 102100023040 Wee1-like protein kinase 2 Human genes 0.000 description 2
- 230000002159 abnormal effect Effects 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 229950009447 alisertib Drugs 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 108010062796 arginyllysine Proteins 0.000 description 2
- 229910002056 binary alloy Inorganic materials 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 230000008034 disappearance Effects 0.000 description 2
- 239000013604 expression vector Substances 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- GLDSKRNGVVYJAB-DQSJHHFOSA-N hesperadin Chemical compound C12=CC(NS(=O)(=O)CC)=CC=C2NC(=O)\C1=C(C=1C=CC=CC=1)/NC(C=C1)=CC=C1CN1CCCCC1 GLDSKRNGVVYJAB-DQSJHHFOSA-N 0.000 description 2
- 230000006801 homologous recombination Effects 0.000 description 2
- 238000002744 homologous recombination Methods 0.000 description 2
- 102000049555 human KRAS Human genes 0.000 description 2
- 102000045603 human SMAD4 Human genes 0.000 description 2
- 208000003906 hydrocephalus Diseases 0.000 description 2
- 229950000568 ilorasertib Drugs 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 230000003902 lesion Effects 0.000 description 2
- 230000013011 mating Effects 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- DOBKQCZBPPCLEG-UHFFFAOYSA-N n-benzyl-2-(pyrimidin-4-ylamino)-1,3-thiazole-4-carboxamide Chemical compound C=1SC(NC=2N=CN=CC=2)=NC=1C(=O)NCC1=CC=CC=C1 DOBKQCZBPPCLEG-UHFFFAOYSA-N 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 210000000277 pancreatic duct Anatomy 0.000 description 2
- 201000008129 pancreatic ductal adenocarcinoma Diseases 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 239000003186 pharmaceutical solution Substances 0.000 description 2
- 238000010837 poor prognosis Methods 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 108060006633 protein kinase Proteins 0.000 description 2
- ZFLJHSQHILSNCM-UHFFFAOYSA-N reversine Chemical compound C1CCCCC1NC1=NC(NC=2C=CC(=CC=2)N2CCOCC2)=NC2=C1N=CN2 ZFLJHSQHILSNCM-UHFFFAOYSA-N 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 235000000891 standard diet Nutrition 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 230000002103 transcriptional effect Effects 0.000 description 2
- KGWWHPZQLVVAPT-STTJLUEPSA-N (2r,3r)-2,3-dihydroxybutanedioic acid;6-(4-methylpiperazin-1-yl)-n-(5-methyl-1h-pyrazol-3-yl)-2-[(e)-2-phenylethenyl]pyrimidin-4-amine Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O.C1CN(C)CCN1C1=CC(NC2=NNC(C)=C2)=NC(\C=C\C=2C=CC=CC=2)=N1 KGWWHPZQLVVAPT-STTJLUEPSA-N 0.000 description 1
- ROFMCPHQNWGXGE-SFHVURJKSA-N (3s)-n-[2-[2-(dimethylamino)ethoxy]-4-(1h-pyrazol-4-yl)phenyl]-6-methoxy-3,4-dihydro-2h-chromene-3-carboxamide Chemical compound O=C([C@@H]1COC2=CC=C(C=C2C1)OC)NC(C(=C1)OCCN(C)C)=CC=C1C=1C=NNC=1 ROFMCPHQNWGXGE-SFHVURJKSA-N 0.000 description 1
- FAYAUAZLLLJJGH-UHFFFAOYSA-N 1-(3-chlorophenyl)-3-[5-[2-(4-thieno[3,2-d]pyrimidinylamino)ethyl]-2-thiazolyl]urea Chemical compound ClC1=CC=CC(NC(=O)NC=2SC(CCNC=3C=4SC=CC=4N=CN=3)=CN=2)=C1 FAYAUAZLLLJJGH-UHFFFAOYSA-N 0.000 description 1
- GDVRVPIXWXOKQO-UHFFFAOYSA-N 1-[(3-hydroxyphenyl)methyl]-3-(4-pyridin-4-yl-1,3-thiazol-2-yl)urea Chemical compound OC1=CC=CC(CNC(=O)NC=2SC=C(N=2)C=2C=CN=CC=2)=C1 GDVRVPIXWXOKQO-UHFFFAOYSA-N 0.000 description 1
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- QFWCYNPOPKQOKV-UHFFFAOYSA-N 2-(2-amino-3-methoxyphenyl)chromen-4-one Chemical compound COC1=CC=CC(C=2OC3=CC=CC=C3C(=O)C=2)=C1N QFWCYNPOPKQOKV-UHFFFAOYSA-N 0.000 description 1
- GFMMXOIFOQCCGU-UHFFFAOYSA-N 2-(2-chloro-4-iodoanilino)-N-(cyclopropylmethoxy)-3,4-difluorobenzamide Chemical compound C=1C=C(I)C=C(Cl)C=1NC1=C(F)C(F)=CC=C1C(=O)NOCC1CC1 GFMMXOIFOQCCGU-UHFFFAOYSA-N 0.000 description 1
- RWEVIPRMPFNTLO-UHFFFAOYSA-N 2-(2-fluoro-4-iodoanilino)-N-(2-hydroxyethoxy)-1,5-dimethyl-6-oxo-3-pyridinecarboxamide Chemical compound CN1C(=O)C(C)=CC(C(=O)NOCCO)=C1NC1=CC=C(I)C=C1F RWEVIPRMPFNTLO-UHFFFAOYSA-N 0.000 description 1
- QYKHWEFPFAGNEV-UHFFFAOYSA-N 2-[4-[6-chloro-2-[4-(dimethylamino)phenyl]-1h-imidazo[4,5-b]pyridin-7-yl]piperazin-1-yl]-n-(1,3-thiazol-2-yl)acetamide Chemical compound C1=CC(N(C)C)=CC=C1C(NC1=NC=C2Cl)=NC1=C2N1CCN(CC(=O)NC=2SC=CN=2)CC1 QYKHWEFPFAGNEV-UHFFFAOYSA-N 0.000 description 1
- RHGZQGXELRMGES-UHFFFAOYSA-N 2-[ethyl-[[5-[[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]amino]-1,2-thiazol-3-yl]methyl]amino]-2-methylpropan-1-ol Chemical compound S1N=C(CN(CC)C(C)(C)CO)C=C1NC1=NC(C)=CN2C1=NC=C2C1=CNN=C1 RHGZQGXELRMGES-UHFFFAOYSA-N 0.000 description 1
- RCLQNICOARASSR-SECBINFHSA-N 3-[(2r)-2,3-dihydroxypropyl]-6-fluoro-5-(2-fluoro-4-iodoanilino)-8-methylpyrido[2,3-d]pyrimidine-4,7-dione Chemical compound FC=1C(=O)N(C)C=2N=CN(C[C@@H](O)CO)C(=O)C=2C=1NC1=CC=C(I)C=C1F RCLQNICOARASSR-SECBINFHSA-N 0.000 description 1
- OCUQMWSIGPQEMX-UHFFFAOYSA-N 3-[3-[N-[4-[(dimethylamino)methyl]phenyl]-C-phenylcarbonimidoyl]-2-hydroxy-1H-indol-6-yl]-N-ethylprop-2-ynamide Chemical compound CCNC(=O)C#CC1=CC2=C(C=C1)C(=C(N2)O)C(=NC3=CC=C(C=C3)CN(C)C)C4=CC=CC=C4 OCUQMWSIGPQEMX-UHFFFAOYSA-N 0.000 description 1
- QTBWCSQGBMPECM-UHFFFAOYSA-N 3-[4-[4-[2-[3-[(dimethylamino)methyl]phenyl]-1H-pyrrolo[2,3-b]pyridin-4-yl]-1-ethyl-3-pyrazolyl]phenyl]-1,1-dimethylurea Chemical compound N=1N(CC)C=C(C=2C=3C=C(NC=3N=CC=2)C=2C=C(CN(C)C)C=CC=2)C=1C1=CC=C(NC(=O)N(C)C)C=C1 QTBWCSQGBMPECM-UHFFFAOYSA-N 0.000 description 1
- WGPXKFOFEXJMBD-UHFFFAOYSA-N 3-[N-[3-[(dimethylamino)methyl]phenyl]-C-phenylcarbonimidoyl]-2-hydroxy-1H-indole-6-carboxamide Chemical compound CN(C)CC1=CC(=CC=C1)N=C(C2=CC=CC=C2)C3=C(NC4=C3C=CC(=C4)C(=O)N)O WGPXKFOFEXJMBD-UHFFFAOYSA-N 0.000 description 1
- ZGXOBLVQIVXKEB-UHFFFAOYSA-N 3-[N-[3-[(dimethylamino)methyl]phenyl]-C-phenylcarbonimidoyl]-2-hydroxy-N,N-dimethyl-1H-indole-6-carboxamide Chemical compound CN(C)CC1=CC(=CC=C1)N=C(C2=CC=CC=C2)C3=C(NC4=C3C=CC(=C4)C(=O)N(C)C)O ZGXOBLVQIVXKEB-UHFFFAOYSA-N 0.000 description 1
- GFLQCBTXTRCREJ-UHFFFAOYSA-N 3-[[4-[6-bromo-2-[4-(4-methylpiperazin-1-yl)phenyl]-1h-imidazo[4,5-b]pyridin-7-yl]piperazin-1-yl]methyl]-5-methyl-1,2-oxazole Chemical compound C1CN(C)CCN1C1=CC=C(C=2NC3=C(N4CCN(CC5=NOC(C)=C5)CC4)C(Br)=CN=C3N=2)C=C1 GFLQCBTXTRCREJ-UHFFFAOYSA-N 0.000 description 1
- JTVBXQAYBIJXRP-SNVBAGLBSA-N 4-[(1R)-1-aminoethyl]-N-(1H-pyrrolo[2,3-b]pyridin-4-yl)benzamide Chemical compound C1=CC([C@H](N)C)=CC=C1C(=O)NC1=CC=NC2=C1C=CN2 JTVBXQAYBIJXRP-SNVBAGLBSA-N 0.000 description 1
- KDKUVYLMPJIGKA-UHFFFAOYSA-N 4-[[5-amino-1-[(2,6-difluorophenyl)-oxomethyl]-1,2,4-triazol-3-yl]amino]benzenesulfonamide Chemical compound N=1N(C(=O)C=2C(=CC=CC=2F)F)C(N)=NC=1NC1=CC=C(S(N)(=O)=O)C=C1 KDKUVYLMPJIGKA-UHFFFAOYSA-N 0.000 description 1
- HHFBDROWDBDFBR-UHFFFAOYSA-N 4-[[9-chloro-7-(2,6-difluorophenyl)-5H-pyrimido[5,4-d][2]benzazepin-2-yl]amino]benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1NC1=NC=C(CN=C(C=2C3=CC=C(Cl)C=2)C=2C(=CC=CC=2F)F)C3=N1 HHFBDROWDBDFBR-UHFFFAOYSA-N 0.000 description 1
- BPVZKUXLOLRECL-UHFFFAOYSA-N 4-chloro-1-piperidin-4-yl-n-(5-pyridin-2-yl-1h-pyrazol-4-yl)pyrazole-3-carboxamide Chemical compound ClC1=CN(C2CCNCC2)N=C1C(=O)NC=1C=NNC=1C1=CC=CC=N1 BPVZKUXLOLRECL-UHFFFAOYSA-N 0.000 description 1
- GPSZYOIFQZPWEJ-UHFFFAOYSA-N 4-methyl-5-[2-(4-morpholin-4-ylanilino)pyrimidin-4-yl]-1,3-thiazol-2-amine Chemical compound N1=C(N)SC(C=2N=C(NC=3C=CC(=CC=3)N3CCOCC3)N=CC=2)=C1C GPSZYOIFQZPWEJ-UHFFFAOYSA-N 0.000 description 1
- WKDACQVEJIVHMZ-UHFFFAOYSA-N 5-(3-ethylsulfonylphenyl)-3,8-dimethyl-n-(1-methylpiperidin-4-yl)-9h-pyrido[2,3-b]indole-7-carboxamide Chemical compound CCS(=O)(=O)C1=CC=CC(C=2C=3C4=CC(C)=CN=C4NC=3C(C)=C(C(=O)NC3CCN(C)CC3)C=2)=C1 WKDACQVEJIVHMZ-UHFFFAOYSA-N 0.000 description 1
- XXSSGBYXSKOLAM-UHFFFAOYSA-N 5-bromo-n-(2,3-dihydroxypropoxy)-3,4-difluoro-2-(2-fluoro-4-iodoanilino)benzamide Chemical compound OCC(O)CONC(=O)C1=CC(Br)=C(F)C(F)=C1NC1=CC=C(I)C=C1F XXSSGBYXSKOLAM-UHFFFAOYSA-N 0.000 description 1
- AKJBLKUZXRMECW-UHFFFAOYSA-N 6-chloro-7-[4-[(4-chlorophenyl)methyl]piperazin-1-yl]-2-(1,3-dimethylpyrazol-4-yl)-1h-imidazo[4,5-b]pyridine Chemical compound CC1=NN(C)C=C1C(NC1=NC=C2Cl)=NC1=C2N1CCN(CC=2C=CC(Cl)=CC=2)CC1 AKJBLKUZXRMECW-UHFFFAOYSA-N 0.000 description 1
- IPEXHQGMTHOKQV-UHFFFAOYSA-N 6-piperidin-4-yloxy-2h-isoquinolin-1-one Chemical compound C=1C=C2C(=O)NC=CC2=CC=1OC1CCNCC1 IPEXHQGMTHOKQV-UHFFFAOYSA-N 0.000 description 1
- GBJVVSCPOBPEIT-UHFFFAOYSA-N AZT-1152 Chemical compound N=1C=NC2=CC(OCCCN(CC)CCOP(O)(O)=O)=CC=C2C=1NC(=NN1)C=C1CC(=O)NC1=CC=CC(F)=C1 GBJVVSCPOBPEIT-UHFFFAOYSA-N 0.000 description 1
- 206010073363 Acinar cell carcinoma of pancreas Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- WKOBSJOZRJJVRZ-FXQIFTODSA-N Ala-Glu-Glu Chemical compound [H]N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(O)=O WKOBSJOZRJJVRZ-FXQIFTODSA-N 0.000 description 1
- VGPWRRFOPXVGOH-BYPYZUCNSA-N Ala-Gly-Gly Chemical compound C[C@H](N)C(=O)NCC(=O)NCC(O)=O VGPWRRFOPXVGOH-BYPYZUCNSA-N 0.000 description 1
- NINQYGGNRIBFSC-CIUDSAMLSA-N Ala-Lys-Ser Chemical compound NCCCC[C@H](NC(=O)[C@@H](N)C)C(=O)N[C@@H](CO)C(O)=O NINQYGGNRIBFSC-CIUDSAMLSA-N 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- DXQIQUIQYAGRCC-CIUDSAMLSA-N Arg-Asp-Gln Chemical compound C(C[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)N[C@@H](CCC(=O)N)C(=O)O)N)CN=C(N)N DXQIQUIQYAGRCC-CIUDSAMLSA-N 0.000 description 1
- MZRBYBIQTIKERR-GUBZILKMSA-N Arg-Glu-Gln Chemical compound [H]N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(O)=O MZRBYBIQTIKERR-GUBZILKMSA-N 0.000 description 1
- OHYQKYUTLIPFOX-ZPFDUUQYSA-N Arg-Glu-Ile Chemical compound [H]N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(O)=O OHYQKYUTLIPFOX-ZPFDUUQYSA-N 0.000 description 1
- HQIZDMIGUJOSNI-IUCAKERBSA-N Arg-Gly-Arg Chemical compound N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(O)=O HQIZDMIGUJOSNI-IUCAKERBSA-N 0.000 description 1
- MJINRRBEMOLJAK-DCAQKATOSA-N Arg-Lys-Asp Chemical compound OC(=O)C[C@@H](C(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)CCCN=C(N)N MJINRRBEMOLJAK-DCAQKATOSA-N 0.000 description 1
- KZXPVYVSHUJCEO-ULQDDVLXSA-N Arg-Phe-Lys Chemical compound NC(=N)NCCC[C@H](N)C(=O)N[C@H](C(=O)N[C@@H](CCCCN)C(O)=O)CC1=CC=CC=C1 KZXPVYVSHUJCEO-ULQDDVLXSA-N 0.000 description 1
- JGIAYNNXZKKKOW-KKUMJFAQSA-N Asn-His-Phe Chemical compound C1=CC=C(C=C1)C[C@@H](C(=O)O)NC(=O)[C@H](CC2=CN=CN2)NC(=O)[C@H](CC(=O)N)N JGIAYNNXZKKKOW-KKUMJFAQSA-N 0.000 description 1
- FODVBOKTYKYRFJ-CIUDSAMLSA-N Asn-Lys-Cys Chemical compound C(CCN)C[C@@H](C(=O)N[C@@H](CS)C(=O)O)NC(=O)[C@H](CC(=O)N)N FODVBOKTYKYRFJ-CIUDSAMLSA-N 0.000 description 1
- NECWUSYTYSIFNC-DLOVCJGASA-N Asp-Ala-Phe Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 NECWUSYTYSIFNC-DLOVCJGASA-N 0.000 description 1
- JNNVNVRBYUJYGS-CIUDSAMLSA-N Asp-Leu-Ala Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(O)=O JNNVNVRBYUJYGS-CIUDSAMLSA-N 0.000 description 1
- RVMXMLSYBTXCAV-VEVYYDQMSA-N Asp-Pro-Thr Chemical compound [H]N[C@@H](CC(O)=O)C(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)O)C(O)=O RVMXMLSYBTXCAV-VEVYYDQMSA-N 0.000 description 1
- 102000004000 Aurora Kinase A Human genes 0.000 description 1
- 108090000461 Aurora Kinase A Proteins 0.000 description 1
- 102100032306 Aurora kinase B Human genes 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 101150012716 CDK1 gene Proteins 0.000 description 1
- LMMJFBMMJUMSJS-UHFFFAOYSA-N CH5126766 Chemical compound CNS(=O)(=O)NC1=NC=CC(CC=2C(OC3=CC(OC=4N=CC=CN=4)=CC=C3C=2C)=O)=C1F LMMJFBMMJUMSJS-UHFFFAOYSA-N 0.000 description 1
- 101100356682 Caenorhabditis elegans rho-1 gene Proteins 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 208000037051 Chromosomal Instability Diseases 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 108050006400 Cyclin Proteins 0.000 description 1
- 102000016736 Cyclin Human genes 0.000 description 1
- 102000002427 Cyclin B Human genes 0.000 description 1
- 108010068150 Cyclin B Proteins 0.000 description 1
- LBSKYJOZIIOZIO-DCAQKATOSA-N Cys-Lys-Met Chemical compound CSCC[C@@H](C(=O)O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CS)N LBSKYJOZIIOZIO-DCAQKATOSA-N 0.000 description 1
- 241000255601 Drosophila melanogaster Species 0.000 description 1
- 108700008634 Drosophila p53 Proteins 0.000 description 1
- 108700004685 Drosophila y Proteins 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 208000001976 Endocrine Gland Neoplasms Diseases 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 230000010190 G1 phase Effects 0.000 description 1
- 230000020172 G2/M transition checkpoint Effects 0.000 description 1
- RFWVETIZUQEJEF-UHFFFAOYSA-N GDC-0623 Chemical compound OCCONC(=O)C=1C=CC2=CN=CN2C=1NC1=CC=C(I)C=C1F RFWVETIZUQEJEF-UHFFFAOYSA-N 0.000 description 1
- 102000013446 GTP Phosphohydrolases Human genes 0.000 description 1
- 108091006109 GTPases Proteins 0.000 description 1
- INKFLNZBTSNFON-CIUDSAMLSA-N Gln-Ala-Arg Chemical compound NC(=O)CC[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCN=C(N)N)C(O)=O INKFLNZBTSNFON-CIUDSAMLSA-N 0.000 description 1
- SNLOOPZHAQDMJG-CIUDSAMLSA-N Gln-Glu-Glu Chemical compound NC(=O)CC[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(O)=O SNLOOPZHAQDMJG-CIUDSAMLSA-N 0.000 description 1
- LWYUQLZOIORFFJ-XKBZYTNZSA-N Glu-Thr-Cys Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CS)C(=O)O)NC(=O)[C@H](CCC(=O)O)N)O LWYUQLZOIORFFJ-XKBZYTNZSA-N 0.000 description 1
- KIEICAOUSNYOLM-NRPADANISA-N Glu-Val-Ala Chemical compound [H]N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C)C(O)=O KIEICAOUSNYOLM-NRPADANISA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- BHPQOIPBLYJNAW-NGZCFLSTSA-N Gly-Ile-Pro Chemical compound CC[C@H](C)[C@@H](C(=O)N1CCC[C@@H]1C(=O)O)NC(=O)CN BHPQOIPBLYJNAW-NGZCFLSTSA-N 0.000 description 1
- JPVGHHQGKPQYIL-KBPBESRZSA-N Gly-Phe-Leu Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@@H](NC(=O)CN)CC1=CC=CC=C1 JPVGHHQGKPQYIL-KBPBESRZSA-N 0.000 description 1
- DNVDEMWIYLVIQU-RCOVLWMOSA-N Gly-Val-Asp Chemical compound NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(O)=O)C(O)=O DNVDEMWIYLVIQU-RCOVLWMOSA-N 0.000 description 1
- 101000798306 Homo sapiens Aurora kinase B Proteins 0.000 description 1
- 101000980932 Homo sapiens Cyclin-dependent kinase inhibitor 2A Proteins 0.000 description 1
- 101100086477 Homo sapiens KRAS gene Proteins 0.000 description 1
- KIMHKBDJQQYLHU-PEFMBERDSA-N Ile-Glu-Asp Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)N[C@@H](CC(=O)O)C(=O)O)N KIMHKBDJQQYLHU-PEFMBERDSA-N 0.000 description 1
- DFFTXLCCDFYRKD-MBLNEYKQSA-N Ile-Gly-Thr Chemical compound CC[C@H](C)[C@@H](C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)O)N DFFTXLCCDFYRKD-MBLNEYKQSA-N 0.000 description 1
- OUUCIIJSBIBCHB-ZPFDUUQYSA-N Ile-Leu-Asp Chemical compound CC[C@H](C)[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(O)=O OUUCIIJSBIBCHB-ZPFDUUQYSA-N 0.000 description 1
- NZGTYCMLUGYMCV-XUXIUFHCSA-N Ile-Lys-Arg Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCN=C(N)N)C(=O)O)N NZGTYCMLUGYMCV-XUXIUFHCSA-N 0.000 description 1
- 108010065920 Insulin Lispro Proteins 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- 101150105104 Kras gene Proteins 0.000 description 1
- 239000005551 L01XE03 - Erlotinib Substances 0.000 description 1
- AUBMZAMQCOYSIC-MNXVOIDGSA-N Leu-Ile-Gln Chemical compound [H]N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(O)=O AUBMZAMQCOYSIC-MNXVOIDGSA-N 0.000 description 1
- PDQDCFBVYXEFSD-SRVKXCTJSA-N Leu-Leu-Asp Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(O)=O PDQDCFBVYXEFSD-SRVKXCTJSA-N 0.000 description 1
- AAKRWBIIGKPOKQ-ONGXEEELSA-N Leu-Val-Gly Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](C(C)C)C(=O)NCC(O)=O AAKRWBIIGKPOKQ-ONGXEEELSA-N 0.000 description 1
- KPJJOZUXFOLGMQ-CIUDSAMLSA-N Lys-Asp-Asn Chemical compound C(CCN)C[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)N[C@@H](CC(=O)N)C(=O)O)N KPJJOZUXFOLGMQ-CIUDSAMLSA-N 0.000 description 1
- IRRZDAIFYHNIIN-JYJNAYRXSA-N Lys-Gln-Tyr Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(O)=O IRRZDAIFYHNIIN-JYJNAYRXSA-N 0.000 description 1
- NDORZBUHCOJQDO-GVXVVHGQSA-N Lys-Gln-Val Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(O)=O NDORZBUHCOJQDO-GVXVVHGQSA-N 0.000 description 1
- GQZMPWBZQALKJO-UWVGGRQHSA-N Lys-Gly-Arg Chemical compound [H]N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(O)=O GQZMPWBZQALKJO-UWVGGRQHSA-N 0.000 description 1
- 238000000719 MTS assay Methods 0.000 description 1
- 231100000070 MTS assay Toxicity 0.000 description 1
- 241000282560 Macaca mulatta Species 0.000 description 1
- 238000000585 Mann–Whitney U test Methods 0.000 description 1
- DRXODWRPPUFIAY-DCAQKATOSA-N Met-Asn-Lys Chemical compound CSCC[C@H](N)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H](C(O)=O)CCCCN DRXODWRPPUFIAY-DCAQKATOSA-N 0.000 description 1
- FXBKQTOGURNXSL-HJGDQZAQSA-N Met-Thr-Glu Chemical compound CSCC[C@H](N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@H](C(O)=O)CCC(O)=O FXBKQTOGURNXSL-HJGDQZAQSA-N 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 101600097262 Monodelphis domestica Cyclin-dependent kinase inhibitor 2A (isoform 1) Proteins 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- IKMDFBPHZNJCSN-UHFFFAOYSA-N Myricetin Chemical compound C=1C(O)=CC(O)=C(C(C=2O)=O)C=1OC=2C1=CC(O)=C(O)C(O)=C1 IKMDFBPHZNJCSN-UHFFFAOYSA-N 0.000 description 1
- 101150092630 Myt1 gene Proteins 0.000 description 1
- AKSIZPIFQAYJGF-UHFFFAOYSA-N N-(2-chlorophenyl)-4-[[2-[4-[2-(4-ethyl-1-piperazinyl)-2-oxoethyl]anilino]-5-fluoro-4-pyrimidinyl]amino]benzamide Chemical compound C1CN(CC)CCN1C(=O)CC(C=C1)=CC=C1NC1=NC=C(F)C(NC=2C=CC(=CC=2)C(=O)NC=2C(=CC=CC=2)Cl)=N1 AKSIZPIFQAYJGF-UHFFFAOYSA-N 0.000 description 1
- OLIIUAHHAZEXEX-UHFFFAOYSA-N N-(6-fluoro-1H-indazol-5-yl)-6-methyl-2-oxo-4-[4-(trifluoromethyl)phenyl]-3,4-dihydro-1H-pyridine-5-carboxamide Chemical compound C1C(=O)NC(C)=C(C(=O)NC=2C(=CC=3NN=CC=3C=2)F)C1C1=CC=C(C(F)(F)F)C=C1 OLIIUAHHAZEXEX-UHFFFAOYSA-N 0.000 description 1
- VIUAUNHCRHHYNE-JTQLQIEISA-N N-[(2S)-2,3-dihydroxypropyl]-3-(2-fluoro-4-iodoanilino)-4-pyridinecarboxamide Chemical compound OC[C@@H](O)CNC(=O)C1=CC=NC=C1NC1=CC=C(I)C=C1F VIUAUNHCRHHYNE-JTQLQIEISA-N 0.000 description 1
- GCIKSSRWRFVXBI-UHFFFAOYSA-N N-[4-[[4-(4-methyl-1-piperazinyl)-6-[(5-methyl-1H-pyrazol-3-yl)amino]-2-pyrimidinyl]thio]phenyl]cyclopropanecarboxamide Chemical compound C1CN(C)CCN1C1=CC(NC2=NNC(C)=C2)=NC(SC=2C=CC(NC(=O)C3CC3)=CC=2)=N1 GCIKSSRWRFVXBI-UHFFFAOYSA-N 0.000 description 1
- XKFTZKGMDDZMJI-HSZRJFAPSA-N N-[5-[(2R)-2-methoxy-1-oxo-2-phenylethyl]-4,6-dihydro-1H-pyrrolo[3,4-c]pyrazol-3-yl]-4-(4-methyl-1-piperazinyl)benzamide Chemical compound O=C([C@H](OC)C=1C=CC=CC=1)N(CC=12)CC=1NN=C2NC(=O)C(C=C1)=CC=C1N1CCN(C)CC1 XKFTZKGMDDZMJI-HSZRJFAPSA-N 0.000 description 1
- 108010079364 N-glycylalanine Proteins 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- MPFGIYLYWUCSJG-AVGNSLFASA-N Phe-Glu-Asp Chemical compound OC(=O)C[C@@H](C(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](N)CC1=CC=CC=C1 MPFGIYLYWUCSJG-AVGNSLFASA-N 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- VPVHXWGPALPDGP-GUBZILKMSA-N Pro-Asn-Arg Chemical compound [H]N1CCC[C@H]1C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O VPVHXWGPALPDGP-GUBZILKMSA-N 0.000 description 1
- 241000382353 Pupa Species 0.000 description 1
- 108010003201 RGH 0205 Proteins 0.000 description 1
- 101150111584 RHOA gene Proteins 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 230000018199 S phase Effects 0.000 description 1
- 102000001332 SRC Human genes 0.000 description 1
- 108060006706 SRC Proteins 0.000 description 1
- HRNQLKCLPVKZNE-CIUDSAMLSA-N Ser-Ala-Leu Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(O)=O HRNQLKCLPVKZNE-CIUDSAMLSA-N 0.000 description 1
- WTUJZHKANPDPIN-CIUDSAMLSA-N Ser-Ala-Lys Chemical compound C[C@@H](C(=O)N[C@@H](CCCCN)C(=O)O)NC(=O)[C@H](CO)N WTUJZHKANPDPIN-CIUDSAMLSA-N 0.000 description 1
- IYCBDVBJWDXQRR-FXQIFTODSA-N Ser-Ala-Met Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCSC)C(O)=O IYCBDVBJWDXQRR-FXQIFTODSA-N 0.000 description 1
- AXKJPUBALUNJEO-UBHSHLNASA-N Ser-Trp-Asn Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC1=CNC2=C1C=CC=C2)C(=O)N[C@@H](CC(N)=O)C(O)=O AXKJPUBALUNJEO-UBHSHLNASA-N 0.000 description 1
- FGBLCMLXHRPVOF-IHRRRGAJSA-N Ser-Tyr-Arg Chemical compound [H]N[C@@H](CO)C(=O)N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O FGBLCMLXHRPVOF-IHRRRGAJSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- TYVAWPFQYFPSBR-BFHQHQDPSA-N Thr-Ala-Gly Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C)C(=O)NCC(O)=O TYVAWPFQYFPSBR-BFHQHQDPSA-N 0.000 description 1
- XVNZSJIKGJLQLH-RCWTZXSCSA-N Thr-Arg-Met Chemical compound C[C@H]([C@@H](C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CCSC)C(=O)O)N)O XVNZSJIKGJLQLH-RCWTZXSCSA-N 0.000 description 1
- AQAMPXBRJJWPNI-JHEQGTHGSA-N Thr-Gly-Glu Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(O)=O AQAMPXBRJJWPNI-JHEQGTHGSA-N 0.000 description 1
- ZBKDBZUTTXINIX-RWRJDSDZSA-N Thr-Ile-Gln Chemical compound [H]N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(O)=O ZBKDBZUTTXINIX-RWRJDSDZSA-N 0.000 description 1
- 208000024770 Thyroid neoplasm Diseases 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- 108700019146 Transgenes Proteins 0.000 description 1
- 108010078814 Tumor Suppressor Protein p53 Proteins 0.000 description 1
- 102000015098 Tumor Suppressor Protein p53 Human genes 0.000 description 1
- ILTXFANLDMJWPR-SIUGBPQLSA-N Tyr-Ile-Glu Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CCC(=O)O)C(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)N ILTXFANLDMJWPR-SIUGBPQLSA-N 0.000 description 1
- FMXFHNSFABRVFZ-BZSNNMDCSA-N Tyr-Lys-Leu Chemical compound [H]N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(O)=O FMXFHNSFABRVFZ-BZSNNMDCSA-N 0.000 description 1
- BBSPTGPYIPGTKH-JYJNAYRXSA-N Tyr-Met-Arg Chemical compound CSCC[C@@H](C(=O)N[C@@H](CCCN=C(N)N)C(=O)O)NC(=O)[C@H](CC1=CC=C(C=C1)O)N BBSPTGPYIPGTKH-JYJNAYRXSA-N 0.000 description 1
- PWKMJDQXKCENMF-MEYUZBJRSA-N Tyr-Thr-Leu Chemical compound [H]N[C@@H](CC1=CC=C(O)C=C1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(O)=O PWKMJDQXKCENMF-MEYUZBJRSA-N 0.000 description 1
- 101710089880 Tyrosine-protein kinase FRK Proteins 0.000 description 1
- BYOHPUZJVXWHAE-BYULHYEWSA-N Val-Asn-Asn Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)N[C@@H](CC(=O)N)C(=O)O)N BYOHPUZJVXWHAE-BYULHYEWSA-N 0.000 description 1
- JLFKWDAZBRYCGX-ZKWXMUAHSA-N Val-Asn-Ser Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CC(=O)N)C(=O)N[C@@H](CO)C(=O)O)N JLFKWDAZBRYCGX-ZKWXMUAHSA-N 0.000 description 1
- VLOYGOZDPGYWFO-LAEOZQHASA-N Val-Asp-Glu Chemical compound CC(C)[C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(O)=O VLOYGOZDPGYWFO-LAEOZQHASA-N 0.000 description 1
- SYOMXKPPFZRELL-ONGXEEELSA-N Val-Gly-Lys Chemical compound CC(C)[C@@H](C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)O)N SYOMXKPPFZRELL-ONGXEEELSA-N 0.000 description 1
- LKUDRJSNRWVGMS-QSFUFRPTSA-N Val-Ile-Asp Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CC(=O)O)C(=O)O)NC(=O)[C@H](C(C)C)N LKUDRJSNRWVGMS-QSFUFRPTSA-N 0.000 description 1
- KTEZUXISLQTDDQ-NHCYSSNCSA-N Val-Lys-Asp Chemical compound CC(C)[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(=O)O)C(=O)O)N KTEZUXISLQTDDQ-NHCYSSNCSA-N 0.000 description 1
- LJSZPMSUYKKKCP-UBHSHLNASA-N Val-Phe-Ala Chemical compound CC(C)[C@H](N)C(=O)N[C@H](C(=O)N[C@@H](C)C(O)=O)CC1=CC=CC=C1 LJSZPMSUYKKKCP-UBHSHLNASA-N 0.000 description 1
- WANVRBAZGSICCP-SRVKXCTJSA-N Val-Pro-Met Chemical compound CSCC[C@H](NC(=O)[C@@H]1CCCN1C(=O)[C@@H](N)C(C)C)C(O)=O WANVRBAZGSICCP-SRVKXCTJSA-N 0.000 description 1
- AEFJNECXZCODJM-UWVGGRQHSA-N Val-Val-Gly Chemical compound CC(C)[C@H]([NH3+])C(=O)N[C@@H](C(C)C)C(=O)NCC([O-])=O AEFJNECXZCODJM-UWVGGRQHSA-N 0.000 description 1
- OURRXQUGYQRVML-AREMUKBSSA-N [4-[(2s)-3-amino-1-(isoquinolin-6-ylamino)-1-oxopropan-2-yl]phenyl]methyl 2,4-dimethylbenzoate Chemical compound CC1=CC(C)=CC=C1C(=O)OCC1=CC=C([C@@H](CN)C(=O)NC=2C=C3C=CN=CC3=CC=2)C=C1 OURRXQUGYQRVML-AREMUKBSSA-N 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 239000012635 anticancer drug combination Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 108010013835 arginine glutamate Proteins 0.000 description 1
- 108010068380 arginylarginine Proteins 0.000 description 1
- 108010040443 aspartyl-aspartic acid Proteins 0.000 description 1
- 108010047857 aspartylglycine Proteins 0.000 description 1
- 239000005441 aurora Substances 0.000 description 1
- 229950005645 barasertib Drugs 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229950003054 binimetinib Drugs 0.000 description 1
- ACWZRVQXLIRSDF-UHFFFAOYSA-N binimetinib Chemical compound OCCONC(=O)C=1C=C2N(C)C=NC2=C(F)C=1NC1=CC=C(Br)C=C1F ACWZRVQXLIRSDF-UHFFFAOYSA-N 0.000 description 1
- 238000010170 biological method Methods 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 235000011148 calcium chloride Nutrition 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 108010079058 casein hydrolysate Proteins 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 230000022131 cell cycle Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000009087 cell motility Effects 0.000 description 1
- 230000033077 cellular process Effects 0.000 description 1
- 210000003793 centrosome Anatomy 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229960002271 cobimetinib Drugs 0.000 description 1
- RESIMIUSNACMNW-BXRWSSRYSA-N cobimetinib fumarate Chemical compound OC(=O)\C=C\C(O)=O.C1C(O)([C@H]2NCCCC2)CN1C(=O)C1=CC=C(F)C(F)=C1NC1=CC=C(I)C=C1F.C1C(O)([C@H]2NCCCC2)CN1C(=O)C1=CC=C(F)C(F)=C1NC1=CC=C(I)C=C1F RESIMIUSNACMNW-BXRWSSRYSA-N 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000009402 cross-breeding Methods 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 230000003436 cytoskeletal effect Effects 0.000 description 1
- 210000004292 cytoskeleton Anatomy 0.000 description 1
- 229950002966 danusertib Drugs 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- FSXRLASFHBWESK-UHFFFAOYSA-N dipeptide phenylalanyl-tyrosine Natural products C=1C=C(O)C=CC=1CC(C(O)=O)NC(=O)C(N)CC1=CC=CC=C1 FSXRLASFHBWESK-UHFFFAOYSA-N 0.000 description 1
- 238000011038 discontinuous diafiltration by volume reduction Methods 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 229940121647 egfr inhibitor Drugs 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 201000011523 endocrine gland cancer Diseases 0.000 description 1
- 230000008556 epithelial cell proliferation Effects 0.000 description 1
- 229960001433 erlotinib Drugs 0.000 description 1
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 description 1
- NGOGFTYYXHNFQH-UHFFFAOYSA-N fasudil Chemical compound C=1C=CC2=CN=CC=C2C=1S(=O)(=O)N1CCCNCC1 NGOGFTYYXHNFQH-UHFFFAOYSA-N 0.000 description 1
- 229960002435 fasudil Drugs 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 230000000855 fungicidal effect Effects 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- 230000005861 gene abnormality Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- VPZXBVLAVMBEQI-UHFFFAOYSA-N glycyl-DL-alpha-alanine Natural products OC(=O)C(C)NC(=O)CN VPZXBVLAVMBEQI-UHFFFAOYSA-N 0.000 description 1
- 108010078326 glycyl-glycyl-valine Proteins 0.000 description 1
- 102000051323 human CDKN2A Human genes 0.000 description 1
- 102000048958 human TP53 Human genes 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 208000013403 hyperactivity Diseases 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 230000006742 locomotor activity Effects 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 108010005942 methionylglycine Proteins 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 230000011278 mitosis Effects 0.000 description 1
- 230000006618 mitotic catastrophe Effects 0.000 description 1
- 208000022669 mucinous neoplasm Diseases 0.000 description 1
- 229940116852 myricetin Drugs 0.000 description 1
- PCOBUQBNVYZTBU-UHFFFAOYSA-N myricetin Natural products OC1=C(O)C(O)=CC(C=2OC3=CC(O)=C(O)C(O)=C3C(=O)C=2)=C1 PCOBUQBNVYZTBU-UHFFFAOYSA-N 0.000 description 1
- 235000007743 myricetin Nutrition 0.000 description 1
- BCSBXWKRZUPFHW-UHFFFAOYSA-N n-(12-cyanoindolizino[2,3-b]quinoxalin-2-yl)thiophene-2-carboxamide Chemical compound C1=CN(C2=NC3=CC=CC=C3N=C2C=2C#N)C=2C=C1NC(=O)C1=CC=CS1 BCSBXWKRZUPFHW-UHFFFAOYSA-N 0.000 description 1
- OBWNXGOQPLDDPS-UHFFFAOYSA-N n-(2,6-diethylphenyl)-3-[[4-(4-methylpiperazin-1-yl)benzoyl]amino]-4,6-dihydro-1h-pyrrolo[3,4-c]pyrazole-5-carboxamide Chemical compound CCC1=CC=CC(CC)=C1NC(=O)N1CC(C(NC(=O)C=2C=CC(=CC=2)N2CCN(C)CC2)=NN2)=C2C1 OBWNXGOQPLDDPS-UHFFFAOYSA-N 0.000 description 1
- BRKWREZNORONDU-UHFFFAOYSA-N n-(2-aminophenyl)-6-(7-methoxyquinolin-4-yl)oxynaphthalene-1-carboxamide Chemical compound C=1C=NC2=CC(OC)=CC=C2C=1OC(C=C1C=CC=2)=CC=C1C=2C(=O)NC1=CC=CC=C1N BRKWREZNORONDU-UHFFFAOYSA-N 0.000 description 1
- RDSACQWTXKSHJT-NSHDSACASA-N n-[3,4-difluoro-2-(2-fluoro-4-iodoanilino)-6-methoxyphenyl]-1-[(2s)-2,3-dihydroxypropyl]cyclopropane-1-sulfonamide Chemical compound C1CC1(C[C@H](O)CO)S(=O)(=O)NC=1C(OC)=CC(F)=C(F)C=1NC1=CC=C(I)C=C1F RDSACQWTXKSHJT-NSHDSACASA-N 0.000 description 1
- YOVNFNXUCOWYSG-UHFFFAOYSA-N n-[3-[2-(4-amino-1,2,5-oxadiazol-3-yl)-1-ethylimidazo[4,5-c]pyridin-6-yl]oxyphenyl]-4-(2-morpholin-4-ylethoxy)benzamide Chemical compound C1=C2N(CC)C(C=3C(=NON=3)N)=NC2=CN=C1OC(C=1)=CC=CC=1NC(=O)C(C=C1)=CC=C1OCCN1CCOCC1 YOVNFNXUCOWYSG-UHFFFAOYSA-N 0.000 description 1
- IVUGFMLRJOCGAS-UHFFFAOYSA-N n-[4-[3-(2-aminopyrimidin-4-yl)pyridin-2-yl]oxyphenyl]-4-(4-methylthiophen-2-yl)phthalazin-1-amine Chemical compound CC1=CSC(C=2C3=CC=CC=C3C(NC=3C=CC(OC=4C(=CC=CN=4)C=4N=C(N)N=CC=4)=CC=3)=NN=2)=C1 IVUGFMLRJOCGAS-UHFFFAOYSA-N 0.000 description 1
- FYNMINFUAIDIFL-UHFFFAOYSA-N n-[6-methyl-5-[5-morpholin-4-yl-6-(oxan-4-yloxy)pyridin-3-yl]pyridin-3-yl]-3-(trifluoromethyl)benzamide Chemical compound C1=C(C=2C=C(C(OC3CCOCC3)=NC=2)N2CCOCC2)C(C)=NC=C1NC(=O)C1=CC=CC(C(F)(F)F)=C1 FYNMINFUAIDIFL-UHFFFAOYSA-N 0.000 description 1
- 229950009210 netarsudil Drugs 0.000 description 1
- 201000011519 neuroendocrine tumor Diseases 0.000 description 1
- 239000002547 new drug Substances 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 238000011580 nude mouse model Methods 0.000 description 1
- 230000009437 off-target effect Effects 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 201000010287 pancreatic acinar cell adenocarcinoma Diseases 0.000 description 1
- 208000030352 pancreatic acinar cell carcinoma Diseases 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229950002592 pimasertib Drugs 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 108010079317 prolyl-tyrosine Proteins 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 102000016914 ras Proteins Human genes 0.000 description 1
- 102000027426 receptor tyrosine kinases Human genes 0.000 description 1
- 108091008598 receptor tyrosine kinases Proteins 0.000 description 1
- 229950008933 refametinib Drugs 0.000 description 1
- 230000022983 regulation of cell cycle Effects 0.000 description 1
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- QSKQVZWVLOIIEV-NSHDSACASA-N ripasudil Chemical compound C[C@H]1CNCCCN1S(=O)(=O)C1=CC=CC2=CN=CC(F)=C12 QSKQVZWVLOIIEV-NSHDSACASA-N 0.000 description 1
- 229950007455 ripasudil Drugs 0.000 description 1
- 229950010746 selumetinib Drugs 0.000 description 1
- CYOHGALHFOKKQC-UHFFFAOYSA-N selumetinib Chemical compound OCCONC(=O)C=1C=C2N(C)C=NC2=C(F)C=1NC1=CC=C(Br)C=C1Cl CYOHGALHFOKKQC-UHFFFAOYSA-N 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 108010087686 src-Family Kinases Proteins 0.000 description 1
- 102000009076 src-Family Kinases Human genes 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 201000002510 thyroid cancer Diseases 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 229950000185 tozasertib Drugs 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 230000016596 traversing start control point of mitotic cell cycle Effects 0.000 description 1
- 229910021642 ultra pure water Inorganic materials 0.000 description 1
- 239000012498 ultrapure water Substances 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 108700026220 vif Genes Proteins 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5082—Supracellular entities, e.g. tissue, organisms
- G01N33/5085—Supracellular entities, e.g. tissue, organisms of invertebrates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/0004—Screening or testing of compounds for diagnosis of disorders, assessment of conditions, e.g. renal clearance, gastric emptying, testing for diabetes, allergy, rheuma, pancreas functions
- A61K49/0008—Screening agents using (non-human) animal models or transgenic animal models or chimeric hosts, e.g. Alzheimer disease animal model, transgenic model for heart failure
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/033—Rearing or breeding invertebrates; New breeds of invertebrates
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/033—Rearing or breeding invertebrates; New breeds of invertebrates
- A01K67/0333—Genetically modified invertebrates, e.g. transgenic, polyploid
- A01K67/0337—Genetically modified Arthropods
- A01K67/0339—Genetically modified insects, e.g. Drosophila melanogaster, medfly
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4409—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 4, e.g. isoniazid, iproniazid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/43504—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from invertebrates
- C07K14/43563—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from invertebrates from insects
- C07K14/43577—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from invertebrates from insects from flies
- C07K14/43581—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from invertebrates from insects from flies from Drosophila
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/15—Medicinal preparations ; Physical properties thereof, e.g. dissolubility
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5011—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics for testing antineoplastic activity
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/05—Animals comprising random inserted nucleic acids (transgenic)
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/07—Animals genetically altered by homologous recombination
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/15—Animals comprising multiple alterations of the genome, by transgenesis or homologous recombination, e.g. obtained by cross-breeding
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/70—Invertebrates
- A01K2227/706—Insects, e.g. Drosophila melanogaster, medfly
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/0331—Animal model for proliferative diseases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y306/00—Hydrolases acting on acid anhydrides (3.6)
- C12Y306/05—Hydrolases acting on acid anhydrides (3.6) acting on GTP; involved in cellular and subcellular movement (3.6.5)
- C12Y306/05002—Small monomeric GTPase (3.6.5.2)
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Biotechnology (AREA)
- Epidemiology (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Organic Chemistry (AREA)
- Urology & Nephrology (AREA)
- Biochemistry (AREA)
- Hematology (AREA)
- Pathology (AREA)
- Toxicology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Insects & Arthropods (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Tropical Medicine & Parasitology (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Food Science & Technology (AREA)
- Biodiversity & Conservation Biology (AREA)
- Animal Husbandry (AREA)
- Cell Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Rheumatology (AREA)
Abstract
본 발명은 a) 변이형 Ras85D의 발현, b) p53 유전자의 결실 또는 발현 억제, c) Cyclin E 유전자의 과발현, 및 d) Med 유전자의 결실 또는 발현 억제의 특징을 갖는 초파리에 시험 물질을 섭취시키고 그 생존율을 피험물질을 섭취하지 않는 초파리의 생존율과 비교함으로써 항암제를 스크리닝하는 방법에 관한 것이다. 본 발명은 또한 췌장암의 치료를 위한 2종 이상의 키나아제 억제제의 조합 의약, 및 상기 조합 의약에 사용하기 위한 키나아제 억제제에 관한 것이다.
Description
본 발명은 췌장암에 대한 항암제를 스크리닝하는 방법, 췌장암 치료를 위한 2 종 이상의 키나아제 억제제의 조합 의약, 및 상기 조합 의약에 사용하기 위한 키나아제 억제제에 관한 것이다.
췌장암은 가장 치료하기 어려운 암 중 하나이다. 현재, 췌장암은 암 사인의 4위이지만, 앞으로 10년간 2위로 부상할 것으로 예상되고 있어 큰 사회 문제가 될 우려가 있다.
췌장암은 그 중 90% 이상이 췌관에 발생하는 췌관암이며, 발병해도 자각증상이 없는 것이 특징이다. 이 때문에 환자가 진찰의 기회를 벗어나, 진찰시에는 이미 암세포가 다른 장기로 전이되어 버리는 경우가 많다. 전이는 심각한 예후 불량을 초래하기 때문에, 췌장암 환자의 생존율은 암종 중에서 최저 수준에 있어, 췌장암의 예방이나 치료법의 개발이 오랫동안 매우 중요한 과제로 여겨지고 있다.
그러나, 췌장암은 매우 높은 약물 치료 저항성을 나타내는 것으로 알려져 있고, 신약의 개발은 매우 난항하고 있다. 몇 안되는 인가약인 대사 길항제 젬시타빈이나 EGFR 억제제 에를로티닙 등도 효과가 충분하지 않고, 독성이 우려되는 등의 문제가 지적되고 있다.
췌장암에서는, 4종류의 유전자 변이, 즉 KRAS 유전자 변이에 의한 KRAS 활성화, TP53 유전자 변이에 의한 TP53 불활성화, CDKN2A 유전자 변이에 의한 CDKN2A 불활성화 및 SMAD4 유전자 변이에 의한 SMAD4 불활성화가 자주 발생하며, 가장 예후가 불량한 췌장암 환자는 상기 4개의 유전자 변이 모두를 갖는 것으로 알려져있다 (비 특허 문헌 1). 따라서, 상기 4개의 유전자 변이를 갖는 모델 동물 및 이것을 사용한 치료법의 연구는 췌장암 치료법의 개발에 중요한 의의를 갖는다. 그러나 현재까지 이 4개의 유전자 이상을 모방한 동물 모델은 만들어지지 않았고, 연구의 큰 장애가 되고 있다.
최근, 모델 동물로서 초파리(Drosophila)의 이용에 관심을 모으고 있다. 초파리는 포유류와의 유전 보존도가 높고(예를 들어, 인간 질환의 이상 유전자의 75 % 이상이 파리에도 존재), 포유류에 기능적으로 대응하는 체내 구조 (상피 구조, 주요 장기 등)를 가지며, 유전학 분석 도구가 충실하고(거의 전체 유전자의 siRNA 넉다운 계통이나 변이체가 입수 가능하다), 매우 빠르고 저렴한 사육이 가능하다(다음 세대를 10일에 생산할 수 있고, 사육비는 마우스의 약 1/1000으로 해결된다)는 것과 같은, 모델 동물로서 유익한 특질을 갖추고 있다.
본 발명자들은, 갑상선 수양암과 관련된 수용체 티로신 키나아제인 RET의 변이형을 발현하는 초파리(ptc>dRetM955T)를 모델 동물로 한 갑상선 수양암에 관여하는 키나아제의 탐색 및 이 키나아제를 타깃으로 하는 항암제의 스크리닝에 대해 보고한 바 있다(특허문헌 1, 비특허문헌 2~4). ptc>dRetM955T는 초파리에서 외래 유전자를 강제 발현시킬 수 있는 바이너리 시스템인 gal4-UAS 시스템 및 ptc 프로모터를 이용하여, RET 변이체가 유충의 선원기의 국한된 상피 세포 내에서 발현되도록 개변된 초파리이며, 종양과 같은 병변을 일으켜 성충에 이르지 않고 전체 개체가 사망한다는 성질을 나타낸다.
이처럼 초파리를 모델 동물로 하는 암 치료법의 개발은 유효한 수단이지만, ptc>dRetM955T는 갑상선 수양암의 모델 동물이기 때문에 췌장암에 대한 치료법을 탐구하기 위해서는 췌장암 모델 동물을 새로 만들 필요가 있다.
Qian et al., JAMA Oncol. 2018; 4(3): e173420.
Sonoshita et al., Curr. Top. Dev. Biol. 2017; 121:287-309.
Sonoshita et al., Nat. Chem. Biol. 2018; 14(3): 291-298.
Ung, Sonoshita et al., PLoS Comput. Biol. 2019; 15(4): e1006878.
인간의 췌장암으로 확인된 4종류의 돌연변이 유전자 중 CDKN2A 유전자는 초파리에 존재하지 않는다. 따라서, 췌장암의 초파리 모델은, 갑상선 수양암의 초파리 모델과 같이, 인간 췌장암에서 인정되는 유전자 변이를 그대로 초파리로 재현하는 것에 의해 제작할 수 없다. 본 발명은 췌장암의 모델 동물이 될 수 있는 초파리의 창출, 이를 이용한 췌장암의 새로운 치료 수단의 탐색 방법, 및 췌장암의 치료에 사용하기 위한 의약의 제공을 목적으로 한다.
본 발명자들은 인간의 췌장암과 관련된 4 종류의 유전자 변이에 상당하는 특징을 갖는 초파리를 창출하고, 이것을 이용한 스크리닝에 의해, 복수 종류의 키나아제 억제제의 조합이 췌장암 치료에 효과적임을 발견하고, 하기 발명을 완성하였다.
(1) 하기 a)~d):
a) 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산, 발린 또는 시스테인으로 치환된 변이형 Ras85D의 발현,
b) p53 유전자의 결실 또는 발현 억제,
c) Cyclin E 유전자의 과발현 및
d) Med 유전자의 결실 또는 발현 억제
의 특징을 가진 초파리에 피험물질을 섭취시키는 단계; 피험물질을 섭취한 초파리의 생존율을 측정하는 단계; 및 피험물질을 섭취한 초파리의 생존율이 피험물질을 섭취하지 않은 초파리의 생존율보다 높은 경우, 당해 피험물질을 항암제의 후보 물질로서 선발하는 단계를 포함하는 항암제를 스크리닝하는 방법.
(2) 변이형 Ras85D는 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 단백질이며, p53 유전자의 발현 억제는 p53 유전자의 발현을 억제하는 핵산의 도입에 의해 수행되고, Cyclin E의 과발현은 Cyclin E를 코딩하는 핵산의 도입에 의해 수행되며, Med 유전자의 발현 억제는 Med 유전자의 발현을 억제하는 핵산의 도입에 의해 수행되는 (1)에 기재된 방법.
(3) 초파리가, 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 변이형 Ras85D를 코드하는 핵산, p53 유전자에 대한 넉다운 핵산, Cyclin E 유전자를 코드하는 핵산 및 Med 유전자에 대한 넉다운 핵산이 도입된 초파리인 (1)에 기재된 방법.
(4) 하기 a')~d'):
a') UAS 서열의 하류에 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 변이형 Ras85D를 코딩하는 염기 서열을 갖는 핵산,
b') UAS 서열의 하류에 p53 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산,
c') UAS 서열의 하류에 Cyclin E 유전자를 코딩하는 염기 서열을 갖는 핵산 및
d') UAS 서열의 하류에 Med 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산
이 도입된 초파리와 gal4 유전자가 도입된 초파리와의 교배에 의해 태어난 알을 피험물질을 함유하는 먹이상에서 사육하는 단계; 및 피험물질을 함유하는 먹이상에서 사육한 초파리의 생존율이, 피험물질을 함유하지 않는 먹이상에서 사육한 초파리의 생존율보다 높은 경우, 당해 피험물질을 항암제의 후보물질로 선택하는 단계를 포함하는 항암제를 스크리닝하는 방법.
(5) 초파리의 사육 온도를 조절함으로써, 피험물질을 섭취하지 않는 초파리 또는 피험물질을 함유하지 않는 먹이상에서 사육한 초파리의 생존율을 제어하는, (1)~(4) 중 어느 한 항 에 기재된 방법.
(6) 하기 a)~d):
a) 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산, 발린 또는 시스테인으로 치환된 변이형 Ras85D의 발현,
b) p53 유전자의 결실 또는 발현 억제,
c) Cyclin E 유전자의 과발현 및
d) Med 유전자의 결실 또는 발현 억제
의 특징을 가진 초파리.
(7) 하기 a')~d'):
a') UAS 서열의 하류에 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 변이형 Ras85D를 코딩하는 염기 서열을 갖는 핵산,
b') UAS 서열의 하류에 p53 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산,
c') UAS 서열의 하류에 Cyclin E 유전자를 코딩하는 염기 서열을 갖는 핵산 및
d') UAS 서열의 하류에 Med 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산
이 도입된, (6)에 기재된 초파리.
(8) 췌장암의 치료를 위한 MEK 억제제, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택되는 적어도 2종의 키나아제 억제제의 조합 의약.
(9) 췌장암의 치료를 위한 MEK 억제제와, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군에서 선택되는 적어도 1종의 키나아제 억제제의 조합 의약 .
(10) MEK 억제제가 트라메티닙 인 (8) 또는 (9)에 기재된 조합 의약.
(11) FRK 억제제가 AD80이고, WEE 억제제가 아다보셀티브이고, AURK 억제제가 알리서팁 또는 BI-831266인, (8) 내지 (10) 중 어느 한 항의 조합 의약.
(12) 췌장암의 치료에 있어서 MEK 억제제와 조합하기 위한, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택되는 키나아제 억제제.
(13) MEK 억제제가 트라메티닙인 (12)에 기재된 키나아제 억제제.
(14) FRK 억제제가 AD80이고, WEE 억제제가 아다보셀티브이고, AURK 억제제가 알리서팁 또는 BI-831266 인 (12) 또는 (13)에 기재된 키나아제 억제제.
(15) 췌장암의 치료에 있어서 FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어지는 군으로부터 선택되는 적어도 1종의 키나아제 억제제와 조합하기 위한 MEK 억제제.
(16) 트라메티닙인 (15)에 기재된 MEK 억제제.
(17) FRK 억제제가 AD80이고, WEE 억제제가 아다보셀티브이고, AURK 억제제가 알리서팁 또는 BI-831266 인 (15) 또는 (16)에 기재된 MEK 억제제.
본 발명에 의하면, 인간의 췌장암과 관련된 4종류의 유전자 변이에 상당하는 특징을 갖는 초파리를 제작할 수 있고, 이 초파리를 췌장암 모델 동물로서 사용함으로써, 췌장암에 대하여 치료 효과를 얻을 수 있는 물질을 효율적이고 저렴한 비용으로 탐색할 수 있다. 또한, 특정 키나아제 억제제의 2종 이상의 조합이 췌장암 치료제로서 제공될 수 있다.
[도 1] 대조파리(ptc>GFP), 췌장암세포에 빈번한 변이형 Ras85D를 발현하는 초파리(1-hit파리) 및 췌장암세포에 빈번한 4개의 유전자 돌연변이를 모방한 초파리(4-hit 파리)의 유충의 선원기를 형광 현미경으로 관찰한 이미지이다.
[도 2] 4-hit 파리에 키나아제 유전자의 헤테로 접합성 돌연변이를 도입하여 키나아제 헤테로 접합성 돌연변이 4-hit 파리를 생성하는 프로토콜의 개략을 나타낸 도이다.
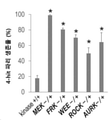
[도 3] MEK, FRK, WEE, ROCK 또는 AURK의 이형 접합성 돌연변이를 갖는 4-hit 파리의 생존율을 나타내는 그래프이다.
[도 4] MEK 억제제(트라메티닙), FRK 억제제(AD80), WEE 억제제(MK-1775), ROCK 억제제(Y-27632) 및 AURK 억제제(BI-831266) 단독으로 또는 MEK 억제제와 다른 4개의 키나아제 억제제의 조합을 섭취했을 때의 4-hit 파리(non-GFP)의 생존율을 나타내는 그래프이다. *p<0.01.
[도 5] 제1화합물로서의 MEK 억제제(트라메티닙)와, 제2화합물로서의 FRK 억제제(AD80), WEE 억제제(MK-1775), 또는 AURK 억제제(알리서팁, BI-831266)의 조합의 존재하에서 배양한 인간 췌장암 세포(MIAPaCa-2 세포)의 상대적 세포수를 나타내는 그래프이다. *, 제2화합물 없음 (0 nM)에 비해 유의하게 감소 (p<0.05). #, 트라메티닙 없음 (0 nM)에 비해 유의하게 감소 (p<0.05).
[도 6] 22~29℃에서 사육했을 때의 4-hit 파리(non-GFP)의 생존율을 나타내는 그래프이다.
[도 7A] MEK 억제제 (트라메티닙) 및 AURK 억제제 (BI-831266)를 각각 단독으로 또는 조합하여 경구 투여한 담암 마우스에서의 종양 부피의 시간 경과에 따른 변화를 나타내는 그래프이다. *p<0.05, **p<0.01(모두 투여 21일째의 Mann-Whitney U test). NS, not significant (유의차 없음). 오차 막대는 8마리의 표준 편차를 나타낸다.
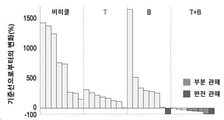
[도 7B] MEK 억제제 (트라메티닙) 및 AURK 억제제 (BI-831266)를 각각 단독으로 또는 조합하여 경구 투여한 담암 마우스에서의 투여 21 일째의 종양 체적을 투여 개시시의 종양 체적과 비교한 변화율을 나타내는 워터폴 플롯이다. 하나의 막대는 한 마리의 마우스의 종양 부피 변화율을 나타낸다.
[도 2] 4-hit 파리에 키나아제 유전자의 헤테로 접합성 돌연변이를 도입하여 키나아제 헤테로 접합성 돌연변이 4-hit 파리를 생성하는 프로토콜의 개략을 나타낸 도이다.
[도 3] MEK, FRK, WEE, ROCK 또는 AURK의 이형 접합성 돌연변이를 갖는 4-hit 파리의 생존율을 나타내는 그래프이다.
[도 4] MEK 억제제(트라메티닙), FRK 억제제(AD80), WEE 억제제(MK-1775), ROCK 억제제(Y-27632) 및 AURK 억제제(BI-831266) 단독으로 또는 MEK 억제제와 다른 4개의 키나아제 억제제의 조합을 섭취했을 때의 4-hit 파리(non-GFP)의 생존율을 나타내는 그래프이다. *p<0.01.
[도 5] 제1화합물로서의 MEK 억제제(트라메티닙)와, 제2화합물로서의 FRK 억제제(AD80), WEE 억제제(MK-1775), 또는 AURK 억제제(알리서팁, BI-831266)의 조합의 존재하에서 배양한 인간 췌장암 세포(MIAPaCa-2 세포)의 상대적 세포수를 나타내는 그래프이다. *, 제2화합물 없음 (0 nM)에 비해 유의하게 감소 (p<0.05). #, 트라메티닙 없음 (0 nM)에 비해 유의하게 감소 (p<0.05).
[도 6] 22~29℃에서 사육했을 때의 4-hit 파리(non-GFP)의 생존율을 나타내는 그래프이다.
[도 7A] MEK 억제제 (트라메티닙) 및 AURK 억제제 (BI-831266)를 각각 단독으로 또는 조합하여 경구 투여한 담암 마우스에서의 종양 부피의 시간 경과에 따른 변화를 나타내는 그래프이다. *p<0.05, **p<0.01(모두 투여 21일째의 Mann-Whitney U test). NS, not significant (유의차 없음). 오차 막대는 8마리의 표준 편차를 나타낸다.
[도 7B] MEK 억제제 (트라메티닙) 및 AURK 억제제 (BI-831266)를 각각 단독으로 또는 조합하여 경구 투여한 담암 마우스에서의 투여 21 일째의 종양 체적을 투여 개시시의 종양 체적과 비교한 변화율을 나타내는 워터폴 플롯이다. 하나의 막대는 한 마리의 마우스의 종양 부피 변화율을 나타낸다.
인간 췌장암을 모방한 초파리
본 발명의 제1 양태는, 하기 a) 내지 d):
a) 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산, 발린 또는 시스테인으로 치환된 변이형 Ras85D의 발현,
b) p53 유전자의 결실 또는 발현 억제,
c) Cyclin E 유전자의 과발현 및
d) Med 유전자의 결실 또는 발현 억제
의 특징을 가진 초파리에 관한 것이다.
Ras85D 단백질은 인간 KRAS의 초파리에서의 오르쏘로그(ortholog)이며, 그 아미노산 서열 (서열번호 1)은 NCBI에 액세스 번호 NP_476699.1로, 이것을 코딩하는 염기 서열은 NCBI에 액세스 번호 NM_057351.5로서 각각 등록되어 있다.
인간 KRAS 유전자 엑손 2의 코돈 12에서의 돌연변이는 KRAS의 활성화를 초래하는 암 유도성 돌연변이로 알려져 있으며, 췌장암 세포에서도 자주 관찰되고 있다. 변이형 Ras85D는 Ras85D에 인간 KRAS의 암 유도성 돌연변이에 상당하는 돌연변이를 도입한 것, 구체적으로는 서열번호 1에 나타내는 아미노산 서열의 12번째 글리신이 아스파르트산, 발린 또는 시스테인으로 치환되어 활성화 KRAS로서 기능한다. 초파리에서 변이형 Ras85D를 코딩하는 유전자의 강제 발현은 인간 활성화 KRAS가 초래하는 것과 유사한 상황을 초파리에서 모방할 수 있다고 믿어진다.
초파리의 p53은 인간 TP53의 오르쏘로그이며, 이것을 코딩하는 염기 서열은 NCBI에 수탁 번호 NM_206545.2로 등록되어 있다. 인간에서 TP53 유전자의 변이에 의한 p53의 기능 저하가 암의 발생과 진전을 촉진하는 것으로 알려져 있으며, 췌장암 세포에서도 p53 변이는 빈번히 관찰되고 있다. 초파리에서 p53 유전자의 기능적 발현의 억제, 예를 들어 p53 유전자의 결실 또는 발현 억제는 인간 불활성화 p53이 초래하는 것과 유사한 상황을 초파리에서 모방하는 것을 가능하게 하는 것으로 생각된다.
사이클린 의존성 키나아제 억제 2A (cyclin-dependent kinase inhibitor 2A, CDKN2A)는 P16이라고도 불리는 세포주기의 조절에 관여하는 단백질이다. CDKN2A 유전자의 돌연변이에 의한 CDKN2A의 불활성화는 다양한 암의 발생과 관련되어 있는 것으로 알려져 있으며, 췌장암 세포에서도 자주 관찰되고 있다. 초파리에는 인간 CDKN2A의 오르쏘로그가 존재하지 않기 때문에, 본 발명에서는 CDKN2A 유전자 변이 대신에 초파리 Cyclin E의 과발현이 사용된다. Cyclin E는 세포주기에서 G1기의 진행 및 S기로의 이행을 제어하는 인자이며, cyclin dependent kinase 2 (CDK2)와 결합하여 이것을 활성화하는 것으로 알려져 있다. 초파리에서 Cyclin E의 과발현은 CDKN2A 불활성화를 기능적으로 대체하고 CDKN2A 불활성화로 인한 것과 유사한 상황을 초파리에서 모방하는 것으로 보고되었다 (Datar et al. EMBO J . 19:4543, 2000). 초파리의 Cyclin E를 코딩하는 염기 서열은 NCBI에서 수탁 번호 NP_476959.1로 등록되어 있다.
Med(Mothers against decapentaplegic)는 인간 SMAD4의 초파리에서의 오르쏘로그이며, 이것을 코딩하는 염기서열은 NCBI에 엑세스 번호 NM_079871.4로서 등록되어 있다. 인간에서, SMAD4는 세포 증식을 억제적으로 조절하는 TGF-β 신호전달에 관여한다. SMAD4 유전자의 돌연변이에 의한 SMAD4 불활성화는 암의 발생과 관련이 있다고 지적되고 있으며, 췌장암 세포에서 자주 관찰되고 있다. 초파리에서 Med 유전자의 기능적 발현의 억제, 예를 들어 Med 유전자의 결실 또는 발현 억제는 인간 불활성화 SMAD4가 초래하는 것과 유사한 상황을 초파리에서 모방하는 것을 가능하게 하는 것으로 생각된다.
본 발명에 있어서, 유전자에의 돌연변이 도입, 유전자의 결실 및 발현 억제는, 당업계에서 일반적으로 사용되는 분자 생물적 방법을 이용하여 행할 수 있다.
바람직한 구체예에서, 초파리는 변이형 Ras85D가 12번째 글리신이 아스파르트산으로 치환된 것(RasG12D로 나타낸다)이며, p53 유전자의 발현 억제가 p53 유전자의 발현을 억제하는 핵산의 도입에 의해 수행되고, Cyclin E의 과발현은 Cyclin E를 코딩하는 핵산의 도입에 의해 수행되고, Med 유전자의 발현 억제는 Med 유전자의 발현을 억제하는 핵산의 도입에 의해 수행되는 초파리이다.
본 발명에 있어서 이용할 수 있는 유전자의 발현을 억제하는 핵산으로서는, 안티센스 핵산이나 siRNA와 같은 넉다운 핵산(안티센스 핵산, siRNA, 그 전구체인 shRNA, 또는 shRNA를 코드하는 shDNA 등)을 들 수 있다. 넉다운 핵산은 표적 유전자의 염기 서열에 기초하여 표적 유전자에 특이적이고 오프타겟 효과가 낮아지도록 적절히 설계될 수 있다. 보다 바람직한 실시 양태에서, 초파리는 RasG12D를 코딩하는 핵산, p53 유전자에 대한 넉다운 핵산, Cyclin E 유전자를 코딩하는 핵산 및 Med 유전자에 대한 넉다운 핵산이 도입된 초파리이다. 이 4개의 핵산은 모두가 1개의 제어 서열 하에 존재하도록 구성될 수 있거나, 또는 각각이 서로 다른 제어 서열 하에 존재하도록 구성될 수 있다.
상기 4개의 핵산은, 이들의 발현의 타이밍이나 정도를 제어 가능하게 하는 제어계를 수반하여 초파리의 게놈에 혼입되는 것이 바람직하다. 이것을 실현하기 위해, 전형적으로 gal4-UAS 시스템이 이용된다. gal4-UAS 시스템은 효모의 전사 활성화 인자 gal4와 그 표적 서열인 UAS(Upstream activating sequence)를 조합한 유전자의 강제 발현을 유도하는 바이너리 시스템이다. 예를 들어, UAS의 하류에 상기 4개의 핵산을 배치한 컨스트럭트가 게놈에 혼입된 초파리를, gal4 단백질을 발현하는 초파리(gal4 드라이버 계통)와 교배함으로써 얻어진 F1의 초파리는, gal4 단백질의 발현 패턴에 따라 상기 4개의 핵산의 발현을 조절할 수 있는 초파리이다. gal4-UAS 시스템에서는 온도에 따라 gal4 단백질의 전사능이 변화하기 때문에 초파리의 사육 온도를 조절함으로써 gal4 단백질의 활성을 제어하고, 상기 4개의 핵산의 발현 수준을 제어할 수 있다. 또한, 이 F1의 초파리에서 상기 4 개의 핵산의 발현 정도는 gal4의 발현을 제어하는 프로모터/인핸서 영역의 활성을 갖는 세포 종 및 조직 및 이들 부위에서의 프로모터/인핸서 영역의 활성의 강도에 의해 또한 다를 수 있다. 따라서, F1을 생성하기 위한 부모인 gal4 드라이버 계통에서 gal4 발현을 제어하는 프로모터/인핸서 영역을 적절히 설정함으로써도 상기 4개의 핵산의 발현 수준을 제어할 수 있으며, 이들은 모두 당업자의 실행 능력의 범위 내이다.
초파리 게놈에서, 상기 4개의 핵산이 혼입되는 위치에 특별히 제한은 없지만, 상염색체인 제2 염색체 또는 제3 염색체에 혼입되는 것이 바람직하다.
더욱 바람직한 실시형태에 있어서, 초파리는, 하기 a')~d'):
a') UAS 서열의 하류에 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 변이형 Ras85D를 코딩하는 염기 서열을 갖는 핵산,
b') UAS 서열의 하류에 p53 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산,
c') UAS 서열의 하류에 Cyclin E 유전자를 코딩하는 염기 서열을 갖는 핵산 및
d') UAS 서열의 하류에 Med 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산
이 도입된 초파리이다.
a) 내지 d)의 특징을 갖는 초파리의 제작은, 비특허문헌 2 내지 4에 기재된 ptc>dRetM955T 의 제작을 참고로 하여 실시할 수 있다. 제작 프로토콜의 일례의 개략을 이하 (i) 내지 (iii)에 나타내지만, 제작 방법 및 초파리는 하기 예에 한정되지 않는다.
(i) 변이형 Ras85D를 코딩하는 염기서열과 p53 유전자에 대한 shRNA를 코딩하는 염기서열을 UAS의 제어하에 재조합한 초파리용 발현 벡터를 이용하여 초파리 게놈을 개변하여 형질전환파리 1을 생성한다.
(ii) Cyclin E 유전자의 염기서열과 Med 유전자에 대한 shRNA를 코딩하는 염기서열을 UAS의 제어하에 재조합한 초파리용 발현 벡터를 이용하여 초파리 게놈을 개변하여 형질전환파리 2를 제작한다.
(iii) 형질전환파리 1과 2를 교배하여 형질전환파리 3을 만들어 내고, 이와 gal4 드라이버 계통을 교배하여 a)~d)의 특징을 가지는 모델 초파리를 제작한다.
a)~d)의 특징을 갖는 초파리에서는, 세포의 이상 증식이나 유주능이 항진된 종양 세포가 발생한다. 이들 현상은 인간 췌장암의 형질이 재현된 결과라고 생각되기 때문에, a)~d)의 특징을 가지는 초파리는 인간 췌장암의 모델로서 이용 가능하다. 또, 이 초파리와, 임의의 유전자의 대립유전자의 한쪽에 결실 등의 변이를 도입하여 당해 유전자의 기능을 저하시킨 이종접합성 변이 초파리를 교배하여 얻어지는 F1의 형질이나 생존율을 조사함으로써, a) 내지 d)의 특징을 갖는 초파리가 나타내는 인간 췌장암형질의 형질에 영향을 주는 유전자의 탐색을 실시할 수도 있다.
항암제의 스크리닝 방법
본 발명은 상기 인간 췌장암 모방 초파리, 즉 상기 a) 내지 d)의 특징을 갖는 초파리에 피험물질을 섭취시키는 단계; 피험물질을 섭취한 초파리의 생존율을 측정하는 단계; 피험물질을 섭취한 초파리의 생존율이 피험물질을 섭취하지 않는 초파리의 생존율보다 높은 경우, 당해 피험물질을 항암제의 후보 물질로 선발하는 단계를 포함하는 항암제를 스크리닝하는 방법을, 다른 양태로서 제공한다.
항암제의 스크리닝 방법은 상기 인간 췌장암 모방 초파리, 즉 상기 a) 내지 d)의 특징을 갖는 초파리에 피험물질을 섭취시키는 단계를 포함한다. 이 단계는 전형적으로 a) 내지 d)의 특징을 갖는 초파리에 피험물질을 함유하는 먹이를 섭취시킴으로써 수행될 수 있다. 당해 먹이는, 적당량의 피험물질을 함유하는 것 이외에는, 통상의 초파리 먹이를 조제하는 방법 및 재료를 사용하여 조제할 수 있다. 피험물질의 양이나 다른 재료와의 혼합 방법은, 피험물질의 물성이나 기대되는 유효 농도 등에 따라 적절히 조절하면 된다. 또한, 먹이를 섭취시키는 기간은, 초파리가 유충인 기간, 즉 초파리가 알로부터 부화하고 번데기까지 상당하는 기간이면 된다. 이 단계에서 초파리는 원하는 생존율을 얻기 위해 후술하는 바와 같이 사육온도가 조절되고, 먹이가 건조하지 않을 정도로 습도가 유지되는 한, 실험동물로서 초파리를 사육할 때 통상 사용되는 조건하에서 사육하면 된다.
이 단계의 바람직한 예 중 하나는 피험물질을 함유한 먹이 상에 상기 a) ~ d)의 특징을 갖는 초파리 알을 놓고 부화된 유충에게 먹이 당 피험물질을 섭취시키는 단계이다. 또 다른 바람직한 예는 피험물질을 함유하는 먹이 상에 상기 a) 내지 d)의 특징을 갖는 초파리 유충을 놓고 먹이 당 피험물질을 섭취시키는 단계이다.
항암제의 스크리닝 방법은, 피험물질을 섭취한 초파리의 생존율을 측정하는 단계, 및 피험물질을 섭취한 초파리의 생존율이, 피험물질을 섭취하지 않는 초파리의 생존율보다 높은 경우, 해당 시험 물질을 항암제의 후보 물질로서 선택하는 단계를 포함한다. 생존율은 번데기로부터 우화한 개체의 수를 번데기의 총수로 나눔으로써 산출할 수 있다.
상기 a) 내지 d)의 특징을 갖는 초파리에서는, 세포의 이상 증식이나 유주능이 항진된 종양 세포가 발생하여, 생존율이 저하된다. 또한, gal4-UAS 시스템이 이용되고 있는 경우, 사육 온도를 16~29℃의 범위 내에서 상승시키면, 이 파리의 유충이 번데기로부터 우화하지 않고 사망할 확률은 상승하고, 예를 들어 실시예 3 및 5에 기재된 Ser-gal4;UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 4-hit 파리(non-GFP)의 경우, 25℃ 이상에서는 생존율은 실질적으로 0%가 된다. 따라서 피험물질을 섭취시켜 사육한 초파리의 생존율이 피험물질을 섭취하지 않고 같은 조건 하에서 사육한 초파리의 생존율보다 높은 경우, 예를 들면 피험물질을 섭취시키지 않고 사육한 초파리의 생존율이 0%인 것에 대해, 피험물질을 섭취시켜 사육한 초파리의 생존율이 0%를 상회하는 경우에는, 해당 물질은 a)~d)의 특징을 가지는 초파리가 나타내는 인간 췌장이 이러한 형질의 발현을 억제하는 작용을 갖는 것으로 추측되기 때문에, 당해 물질을 췌장암에 대한 항암제의 후보 물질로서 선발할 수 있다.
gal4-UAS 시스템을 이용한 상기 a) 내지 d)의 특징을 갖는 초파리에서는, 사육 온도를 조절하여 상기 4개의 핵산의 발현 수준을 제어함으로써, 그 생존율을 제어할 수 있다. 예를 들면 실시예 3 및 5에 기재된 Ser-gal4;UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 4-hit 파리(non-GFP)는, 25℃ 이상에서 사육하면 그 생존율은 실질적으로 0%이지만, 22~24℃에서 사육하면 생존율을 10~20% 정도까지 상승시킬 수 있다. 22~24℃의 사육 온도 하에서 본 스크리닝 방법을 실시하여 선발된 피험물질은 25℃ 이상의 사육 온도 하에서 본 스크리닝 방법을 실시하여 선발된 피험물질과 비교하여 비교적 완만한 항암 작용을 갖는 것으로 기대할 수 있다.
본 스크리닝 방법의 바람직한 실시형태는, 하기 a')~d'):
a') UAS 서열의 하류에 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 변이형 Ras85D를 코딩하는 염기 서열을 갖는 핵산,
b') UAS 서열의 하류에 p53 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산,
c') UAS 서열의 하류에 Cyclin E 유전자를 코딩하는 염기 서열을 갖는 핵산 및
d') UAS 서열의 하류에 Med 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산
이 도입된 초파리와 gal4 유전자가 도입된 초파리와의 교배에 의해 태어난 알을 피험물질을 함유하는 먹이 상에서 사육하는 단계; 피험물질을 함유하는 먹이상에서 사육한 초파리의 생존율을 측정하는 단계; 피험물질을 함유하는 먹이 상에서 사육한 초파리의 생존율이, 피험물질을 함유하지 않는 먹이 상에서 사육한 초파리의 생존율보다 높은 경우, 당해 피험물질을 항암제의 후보물질로서 선발하는 단계를 포함하는 항암제를 스크리닝하는 방법이다.
조합 의약
본 발명의 또 다른 실시 양태는 췌장암 치료를 위한 MEK 억제제, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택된 2 종 이상의 키나아제 억제제 조합 의약에 관한 것이다.
MEK (MAPK (마이토젠 활성화 단백질 키나아제) / ERK (세포 외 신호 제어 키나아제) 키나아제)는 MAPK 캐스케이드를 구성하는 단백질 키나아제의 일종이다. MAPK 캐스케이드는 세포 증식, 성장, 분화 및 세포 사멸과 같은 다양한 세포 과정을 제어하는 복잡한 신호 전달 네트워크를 형성한다. MEK를 억제함으로써 세포 증식이 정지하여 아폽토시스가 유도되기 때문에, MEK는 항암제의 표적 분자로서 주목받고 있으며, 다양한 MEK 억제제가 보고되고 있다.
본 발명에서 사용되는 MEK 억제제의 예로는 트라메티닙(Trametinib), 코비메티닙(Cobimetinib), 비니메티닙(Binimetinib), 셀루메티닙(Selumetinib), 피마서팁(pimasertib), 밀다메티닙(Mirdametinib), 레파메티닙(Refametinib), PD184352, PD98059, BIX02189, BIX02188, TAK-733, AZD8330, PD318088, 미리세틴(Myricetin), BI-847325, GDC-0623, Ro 5126766, PD198306, RO4987655, HI TOPK 032 등을 들 수 있다.
FRK(Fyn related kinase, RAK라고도 불린다)는, SRC 서브패밀리 멤버에 속하는, 핵 내에 존재하는 비수용체형 티로신 키나아제이며, 유방암 세포나 신장암 세포에 있어서의 발현 상승이 알려져 있다.
본 발명에서 사용되는 FRK 억제제의 예로는 AD80, RAF709 등을 들 수 있다.
AURORA 키나아제 (AURK)는 세포 분열을 조절하는 세린/트레오닌 키나아제이며, 세포 분열 단계에서 중심체의 분리 및 양극 스핀들의 형성에 관여하는 것으로 알려져 있다. AURK-A, AURK-B, AURK-C의 3종의 이소형이 존재하며, 이들은 C-말단 키나아제 도메인에서 높은 상동성을 갖는다. AURK는 많은 암세포에서 고발현하고 있기 때문에 항암제의 표적 분자로서 주목받고 있으며, 다양한 AURK 억제제가 보고되고 있다.
본 발명에서 사용되는 AURK 억제제의 예로는 알리서팁(Alisertib, AURK-A 억제제), BI-831266(AURK-B 억제제), 바라서팁(Barasertib, AURK-B 억제제), 토자서팁(Tozasertib, AURK-A 선택성이 높은 범 AURK 억제제), 다누서팁(Danusertib, 범 AURK 억제제), CCT137690 (범 AURK 억제제) CCT129202 (AURK-A 선택성이 높은 범 AURK 억제제), CCT241736 (AURK-A , B 억제제), SNS-314 (일반 AURK 억제제), 헤스페라딘 (Hesperadin, AURK-B 억제제), MK-5108 (AURK-A 억제제), MLN8054 (AURK-A 억제제), ZM 447439 (AURK-A, B 억제제), PF03814735 (AURK-A, B 억제제), AT9283 (AURK-A, B 억제제), GSK1070916 (AURK-B, C 억제제), PHA-680632 (AURK-A 선택 고성능 일반 AURK 억제제), 리버신 (Reversine, 일반 AURK 억제제), CYC116 (AURK-A, B 억제제), ENMD-2076 (AURK-A 억제제), TAK-901 (AURK-A, B 억제제), AMG 900 (일반 AURK 억제제), MK-8745 (AURK-A 억제제), JNJ-7706621 (AURK-A, B 억제제), SCH-1473759 (AURK-A, B 억제제), 일로라서팁 (Ilorasertib, AURK-B, C 선택성이 높은 범 AURK 억제제), TCS7010 (AURK-A 억제제), LY3295668 (AURK-A 억제제), BI-811283 (AURK-B 억제제), 키아우라닙(Chiauranib, AURK-B 억제제), NMI-900 (AURK-B, C 억제제) 등을 들 수 있다.
WEE 키나아제는 CDK-1/cyclin B 복합체의 인산화에 의한 불활성화를 통해 세포 분열을 음으로 제어하는 핵내 티로신 키나아제이며, WEE1(WEE1A), WEE2(WEE1B) 및 Myt1(PKMYT1) 세 가지 유형이 있다. WEE1은 유사분열의 G2/M 체크포인트에서 중요한 역할을 담당하고 있으며, MYT1과 공동으로 세포를 G2-M arrest로 이행시키는 기능을 가진다. 암세포에서 WEE1 억제는 G1 체크포인트를 불활성화시켜 염색체 불안정성을 일으키고 결국 분열기 세포사멸(mitotic catastrophe)로 이어지기 때문에 WEE 키나아제, 특히 WEE1은 항암제의 표적 분자로 주목받고 있다.
본 발명에 있어서 사용되는 WEE 억제제의 예로서는, 아다보서팁(Adavosertib, MK-1775 또는 AZD1775라고도 불린다), PD0166285, PD407824 등을 들 수 있다.
ROCK(Rho-associated protein kinase)는, 세포골격을 제어하는 세린/트레오닌 키나아제이며, ROCK1과 ROCK2의 2종류의 이소형이 존재한다. ROCK은 저분자 GTPase RhoA의 하류 표적이며, 수많은 기질을 인산화하여 세포운동, 세포극성, 세포접착, 세포분열, 아폽토시스, 전사제어 등 다양한 생명 기능에 관여하고 있기 때문에 항암제를 포함한 각종 의약의 표적 분자로서 주목받고 있으며, 다양한 ROCK 억제제가 보고되고 있다.
본 발명에서 사용되는 ROCK 억제제의 예로는 Y-27632(ROCK1 억제제), 파스딜(Fasudil, ROCK2 억제제), 아자인돌 1(Azaindole 1, 범 ROCK 억제제), AT13148(범 ROCK 억제제), 티아조비빈(Thiazovivin), 네타수딜(Netarsudil), 리파수딜(Ripasudil), 크로만 1(Chroman 1), GSK429286A, RKI-1447, GSK269962A, Y-39983, KD025, SAR407899, BDP5290, SB-7720 CMPD101, SLx-2119 등을 들 수 있다.
본 실시 양태의 조합 의약은 전술한 키나아제 억제제 중 적어도 2 종, 즉 MEK 억제제, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택되는 적어도 2 종 키나아제 억제제의 조합을 포함하는 약제이다. 「적어도 2종의 키나아제 억제제의 조합」은, 2종의 키나아제 억제제의 조합, 3종의 키나아제 억제제의 조합, 4종의 키나아제 억제제의 조합, 5종 모두의 키나아제 억제제의 조합을 포함한다. 이 용어는 동종의 키나아제 억제제의 2종 이상의 조합, 예를 들어 MEK 억제제로 분류되는 2종 이상의 키나아제 억제제의 조합을 포함하지 않는다. 따라서, 예를 들면 「2종의 키나아제 억제제의 조합」은 MEK 억제제와 FRK 억제제, MEK 억제제와 WEE 억제제, MEK 억제제와 AURK 억제제, MEK 억제제와 ROCK 억제제, FRK 억제제 와 WEE 억제제, FRK 억제제와 AURK 억제제, FRK 억제제와 ROCK 억제제, WEE 억제제와 AURK 억제제, WEE 억제제와 ROCK 억제제, 및 AURK 억제제와 ROCK 억제제의 각 조합을 의미한다.
또한, 조합을 구성하는 각 억제제는 하나의 화합물에 한정되지 않는다. 예를 들어, MEK 억제제와 FRK 억제제의 조합은 하나의 MEK 억제제와 하나의 FRK 억제제의 조합에 한정되지 않고, 하나의 MEK 억제제와 둘 이상의 FRK 억제제의 조합, 둘 이상의 MEK 억제제와 하나의 FRK 억제제의 조합, 및 둘 이상의 MEK 억제제와 둘 이상의 FRK 억제제의 조합이 포함된다.
본 양태의 조합 의약은 상기 5종류의 키나아제 억제제 중 2종 이상의 키나아제 억제제로 구성되는 임의의 조합을 포함할 수 있다. 특정 실시양태에서, 조합물은 MEK 억제제인 트라메티닙, FRK 억제제인 AD80, WEE 억제제인 아다보서팁 및 AURK 억제제인 알리서팁 및 BI-831266으로 이루어진 군으로부터 선택되는 적어도 2종의 키나아제 억제제의 조합이다. 또한, 조합은 MEK 억제제와 다른 4종의 키나아제 억제제로부터 선택되는 적어도 1종의 키나아제 억제제의 조합일 수 있다. 다른 실시양태에서, 조합물은 MEK 억제제인 트라메티닙, FRK 억제제인 AD80, WEE 억제제인 아다보서팁 및 AURK 억제제인 알리셀티브 및 BI-831266으로 이루어진 군으로부터 선택되는 적어도 하나 종의 키나아제 억제제와의 조합이다.
조합 의약에 포함되는 2종 이상의 키나아제 억제제는 그 필요성, 즉 췌장암의 치료가 요구되는 대상에게 함께 또는 개별적으로, 동시에 또는 순차적으로 투여된다. 조합 의약은, 2종 이상의 키나아제 억제제를 함께 함유하는 제제의 형태여도 되고, 각각의 키나아제 억제제의 별개의 제제를 조합한 형태여도 된다. 조합 의약이 별개의 제형의 조합인 경우, 각각의 제제의 투여 순서 및 투여 시기는 특별히 제한되지 않고, 동시에 투여될 수도 있고, 시간을 두고 상이한 시간에 또는 상이한 날에 투여될 수도 있다.
상기 조합 의약에 사용되는 것으로 의도된 개별 키나아제 억제제도 본 발명의 또 다른 실시 양태이다.
상기 조합 의약은 췌장암의 치료를 위해 사용될 수 있다. 본원에서 용어 "치료"는 질환의 치유 또는 일시적인 관해를 목적으로 하는 의학적으로 허용되는 모든 유형의 치료적 개입을 포함한다. 즉, 췌장암의 치료는 췌장암 진행의 지연 또는 정지, 병변의 퇴축 또는 소실, 재발의 방지 등을 포함하는 다양한 목적의 의학적으로 허용되는 개입을 포함한다.
상기 조합된 의약은 췌장암을 앓고 있는 대상, 예를 들어 마우스, 래트, 햄스터, 기니피그를 포함하는 설치류, 인간, 침팬지, 히말라야 원숭이를 포함한 영장류, 돼지, 소, 염소, 말, 양을 포함한 가축, 개, 고양이를 포함한 애완 동물과 같은 포유 동물에게 투여된다. 바람직한 대상은 인간이다.
치료되는 췌장암으로서는, 외분비 종양, 예를 들면 침윤성 췌관암, 췌선방세포암, 췌관 내 유두 점액성 종양 등, 및 내분비 종양, 예를 들면 신경 내분비 종양 등을 들 수 있다.
조합 의약에서의 개별 키나아제 억제제의 양은 조합을 구성하는 다른 키나아제 억제제와 조합될 때 췌장암을 치료할 수 있는 양이면 되고, 일반적으로 단독으로 사용되는 경우 양과 동등하거나 이것보다 적다. 개별 키나아제 억제제를 단독으로 사용하는 경우의 양과 동등한 양으로 포함하는 조합 의약은, 췌장암에 대한 보다 강력한 효과를 발휘하고, 보다 단기간에, 또는 단독으로 사용해도 효과를 확인할 수 없었던 대상에서 췌장암을 치료할 수 있다. 또한 개별 키나아제 억제제를 단독으로 사용하는 경우의 양보다 적은 양으로 포함하는 조합 의약은 췌장암에 대한 효과를 유지하면서 개별 키나아제 억제제의 양을 줄일 수 있다는 이점이 있다.
상기 조합 의약 및 조합 의약을 위한 키나아제 억제제는 각각 키나아제 억제제 이외의 약물, 완충제, 항산화제, 보존제, 단백질, 친수성 폴리머, 아미노산, 킬레이트화제, 비이온성 계면 활성제, 부형제, 안정화제, 담체 등의 약학적으로 허용가능한 성분을 포함하는 약학 조성물의 형태로 사용될 수 있다. 약학적으로 허용가능한 성분은 당업자에게 잘 알려져 있으며, 당업자가 통상의 실시 능력의 범위 내에서, 예를 들면 제17개정 일본 약국 기타 규격서에 기재된 성분으로부터 제제의 형태에 따라 적절히 선택하여 사용할 수 있다.
약제학적 조성물은 유효량의 개별 키나아제 억제제를 함유한다. 본원에서 유효량은 상기 기재된 바와 같이, 조합을 구성하는 다른 키나아제 억제제와 조합될 때 암을 치료할 수 있는 양이다. 유효량은 조합되는 개개의 키나아제 억제제의 종류나 비율, 용법, 대상의 연령, 질환의 상태 등의 조건에 따라 적절히 결정된다.
의약 조성물의 투여 형태는 임의이지만, 경구제(정제, 캡슐제, 산제, 과립제, 세립제, 환제, 현탁제, 유제, 액제, 시럽제 등) 및 비경구 제제(주사 제제, 점적제, 경장제, 경피제 등)의 형태를 바람직한 예로서 들 수 있다. 또한, 의약 조성물의 투여 경로는 특별히 제한되지 않지만, 비경구 제제인 경우는, 예를 들면 혈관내 투여(바람직하게는 정맥내 투여), 복강내 투여, 장관내 투여, 피하 투여, 표적 부위에의 국소 투여 등을 들 수 있다. 바람직한 실시 양태에서, 약학 조성물은 경구 투여 또는 정맥 내 투여에 의해 투여된다.
암 치료 방법
본 발명은 또한 MEK 억제제, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택된 2종 이상의 유효량의 키나아제 억제제의 조합을 함께 또는 개별적으로, 동시에 또는 순차적으로, 필요로 하는 대상에게 투여하는 것을 포함하는, 췌장암의 치료 방법이 또 다른 양태로서 제공된다.
이하의 실시예에 의해 본 발명을 더욱 상세하게 설명하지만, 본 발명은 이들에 한정되는 것은 아니다.
[실시예]
실시예 1: 인간 췌장암 초파리 모델의 작출
Drosophila w- (Bloomington Drosophila Stock Center)에서 통상적인 방법으로 게놈 DNA를 추출하였다. 이 게놈 DNA를 주형으로 하여, Ras85D 유전자를 증폭하도록 설계된 프라이머 DNA를 사용하여 PCR을 행하여, Ras85D 유전자의 염기 서열을 포함하는 DNA 단편을 얻었다. 또한, Ras85D의 아미노산 서열의 12번째의 글리신을 코드하는 코돈을 아스파르트산을 코드하는 코돈으로 치환하기 위한 부위 특이적 변이 도입용 프라이머 DNA를 설계, 합성하고, 상기 DNA 단편을 주형으로 한 PCR을 수행하여 Ras85D 변이체 (RasG12D)를 코딩하는 DNA 단편을 제조하였다. 이 DNA 단편을 초파리의 넉다운용 벡터인 pWALIUM 벡터(Harvard Medical School)에 삽입하여 pWALIUM.UAS-RasG12D 벡터를 제작하였다. 이것을 초파리 y1w67c23;P{CaryP}attP2에 마이크로 인젝션하고, 상동 재조합에 의해 3번 염색체 L영역에 RasG12D 를 코드하는 DNA가 삽입된 UAS- RasG12D 파리를 생성하였다.
또한, RasG12D를 코딩하는 DNA 단편과 함께 p53 유전자 넉다운 서열(센스 가닥 TGCTGAAGCAATAACCACCGA(서열번호 2), 헤어핀 루프 TAGTTATATTCAAGCATA(서열번호 6) 및 안티센스 가닥 TCGGTGGTTATTGCTTCAGCA(서열번호 3)를 연결한 서열)을 포함하는 DNA 단편을 pWALIUM 벡터에 삽입하여 pWALIUM.UAS-RasG12D, UAS-p53shRNA 벡터를 제조하였다. 이것을 마찬가지로 초파리 y1w67c23;P{CaryP}attP2에 마이크로 인젝션함으로써, 3번 염색체 L 영역에 RasG12D를 코드하는 DNA 및 p53 유전자에 대한 shRNA가 삽입된 UAS-RasG12D, UAS-p53shRNA 파리를 제작하였다.
또한, Drosophila w-의 게놈 DNA를 주형으로서 Cyclin E (CycE) 유전자를 증폭하도록 설계된 프라이머 DNA를 사용하여 PCR을 행하여 CycE 유전자의 염기 서열을 포함하는 DNA 단편을 얻었다. 이 DNA 단편을 Med 유전자 넉다운 서열 (센스 가닥 TTCAGTGCGATGAACATTGCT (서열번호 4), 헤어핀 루프 TAGTTATATTCAAGCATA (서열번호 6) 및 안티센스 가닥 AGCAATGTTCATCGCACTGAA (서열번호 5)가 연결된 서열)을 포함하는 DNA 단편과 함께 pWALIUM 벡터에 삽입하여 pWALIUM.UAS-CycE, UAS-MedshRNA 벡터를 제조하였다. 이것을 초파리 PBac{yellow[+]-attP-9A}VK00027에 마이크로 인젝션하고, 상동 재조합에 의해 3 번 염색체 R 영역에 CycE 유전자를 코딩하는 DNA 및 Med 유전자에 대한 shRNA가 삽입 된 UAS-CycE,UAS-MedshRNA 파리를 제작하였다.
이어서, UAS-RasG12D,UAS-p53shRNA 파리와 UAS-CycE,UAS-MedshRNA 파리를 25에서 3일간 교배하여, UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 파리를 생성하였다.
UAS-RasG12D 파리 및 UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 파리 각각을 ptc-gal4,UAS-GFP 파리(ptc>GFP 파리, Bloomington Drosophila Stock Center)와 25에서 3일간 교배하여 ptc>GFP; UAS-RasG12D 파리(1-hit 파리(ptc>GFP)로 표시) 및 ptc>GFP; UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 파리(4-hit 파리(ptc>GFP)로 표시)를 제작하였다. 이들 파리에서, ptc 프로모터의 제어하에 선원기의 제한된 상피 세포에서 도입유전자의 발현이 유도된다.
1-hit 파리(ptc>GFP), 4-hit 파리(ptc>GFP) 및 대조군인 ptc>GFP 파리의 3령 유충의 선원기를 형광 현미경으로 관찰한 이미지를 도 1에 나타낸다. 대조군에서는 약 10 세포의 폭의 단일 층 상피 세포에서 GFP의 발현이 관찰되었다 (왼쪽에서 두 번째 및 중앙 이미지). 1-hit 파리(ptc>GFP)에서는 보다 넓은 폭으로 GFP 발현 세포가 관찰되었다(오른쪽에서 2번째의 이미지. 이 경향은 4-hit 파리(ptc>GFP)에서는 더욱 현저해진다(오른쪽에서 1 두 번째 이미지), 또한 원래의 영역에서 이탈한 유주능이 항진된 종양 세포(도면에서 화살표로 표시)의 출현이 확인되었다.
또, 1-hit 파리(ptc>GFP) 및 4-hit 파리(ptc>GFP)를 생성하기 위한 교배를 실시했을 때, 교배 후의 모 파리에 먹이상에서 2일간 산란시켜, 바이알당 20 ~ 50개의 알을 얻었다. 이것을 16℃에서 25일간 사육한 후, 우화한 개체의 수를 번데기의 총수로 나누어, 생존율을 산출하였다. 대조군의 ptc>GFP 파리의 생존율은 100 %였지만, 1-hit 파리 (ptc>GFP)의 생존율은 55 %이며, 4-hit 파리 (ptc>GFP)의 생존율은 0%, 즉 치사였다.
이러한 결과로부터, RasG12D의 발현에 의해 선원기 상피 세포의 증식이 항진하는 것, RasG12D 의 발현에 더하여 p53의 넉다운, CycE의 발현 항진 및 Med 유전자의 넉다운을 유도하면 선원기 상피 세포의 증식이 더욱 항진하고, 또 유주능도 항진하는 것이 확인되었고, 4-hit 파리는 인간 췌장암 초파리 모델이 될 수 있는 것으로 나타났다.
실시예 2: 4-hit 파리의 생존율에 영향을 미치는 키나아제 유전자의 탐색
Sonoshita et al. (Curr. Top. Dev. Biol., 2017, 121, 287-309)의 방법에 따라, 도 2에 나타낸 바와 같이 교배를 실시하여, 4-hit 파리의 생존율에 영향을 주는 키나아제 유전자의 탐색을 행하였다. 구체적으로는, 실시예 1에서 제작한 UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 파리를 SM5tubgal80-TM6B 밸런서 파리(Dr. Ross Cagan, Icahn School of Medicine at Mount Sinai, NY,)와 교배하여 UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA/SM5tubgal80-TM6B 파리를 제작하였다. 이어서 이것을 Ser>GFP 파리(Bloomington Drosophila Stock Center)와 교배하여 Ser>GFP;UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA/SM5tubgal80-TM6B 파리를 생성하였다.
또한 Bloomington Drosophila Stock Center (미국)에서 파리 전체 퀴놈 중 키나아제의 헤테로 접합 돌연변이 계통에서 이용 가능한 220 계통을 입수하고, 이들 각각을 27℃에서 3 일간 Ser>GFP;UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA/SM5tubgal80-TM6B 파리와 교배하여 키나아제 이형 접합 돌연변이 4-hit 파리 알을 얻었다. 대조군으로서, w- 파리를 Ser>GFP;UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA/SM5tubgal80-TM6B 파리와 교배하여 키나아제 야생형 4-hit 파리 알을 얻었다. 이들 파리를 27℃에서 13일간 사육한 후, 우화한 개체의 수를 번데기의 총수로 나누어, 생존율을 산출하였다.
파리 키나아제 유전자의 완전한 검색 결과, RAS 경로 인자 MEK, SRC 패밀리 키나아제 FRK, 세포 분열 제어 인자군 WEE 및 AURORA, 및 세포 골격 제어 인자 ROCK 각각의 헤테로접합성 변이가 4-hit 파리의 치사성을 억제하는 것으로 밝혀졌다 (도 3). 이들 헤테로접합성 돌연변이 파리의 생존율을 도 3에 나타낸다. 이것은 MEK 억제제, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제의 사용이 4-hit 파리의 생존율을 높이는 데 효과적일 수 있음을 시사한다.
실시예 3: 4-hit 파리의 생존율에 대한 키나아제 억제제의 약효 평가
트라메티닙(MEK 억제제), 아다보셀티브(MK-1775라고도 하는, WEE1 억제제), AD80(FRK 억제제), Y-27632(ROCK 억제제), 알리서팁(AURKA 억제제, 이상은 MedChem Express에서 구입), BI-831266(AURKB 억제제, Boehringer Ingelheim에서 양도)을 DMSO(SIGMA)에 용해시키고 -20℃에서 보관하였다.
아가(Wako), brewers' yeast(MPBio), 효모 추출물(Sigma Aldrich), bacto casitone (BD), 수크로스 (Wako), 글루코스 (Wako), MgCl2 (Wako), CaCl2 (Wako), 프로피온산 (Wako), 곰팡이 억제제(95% 에탄올 중의 10% 메틸-4-하이드록시 벤조에이트; Wako)를 초순수에 용해시켜 표준 먹이를 제작하였다. 이것을 50℃로 보온하면서, DMSO에 용해한 키나아제 억제제(트라메티닙 단독, 또는 트라메티닙과 다른 키나아제 억제제의 조합)를 첨가 혼합하고, 냉각하여 약 먹이를 조제하였다. 각 화합물의 먹이 중 최종 농도는 트라메티닙 1μM, 아다보셀티브 100μM, AD80 50μM, Y-27632 10μM, BI-831266 100μM로 하였다.
실시예 1에서 제작한 UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 파리를 Ser-gal4 파리(Bloomington Drosophila Stock Center)와 교배한 후, 부모 파리에 표준 먹이 또는 약 먹이상에서 2일간 산란 바이알 당 20-50 개의 Ser-gal4;UAS-RasG12D,UAS-p53shRNA,UAS-CycE,UAS-MedshRNA 4-hit 파리 (non-GFP)의 알을 얻었다. 이것을 25℃에서 13일간 사육한 후, 우화한 개체의 수를 번데기의 총수로 나누어, 각 먹이상에서 사육한 4-hit 파리(non-GFP)의 생존율을 산출하였다.
트라메티닙은 단독으로 4-hit 파리(non-GFP)의 생존율을 20% 향상시켰다. 또 다른 키나아제 억제제는 단독으로는 4-hit 파리(non-GFP)의 생존율을 변화시키지 않았지만, 트라메티닙과 조합하면 트라메티닙 단독보다 생존율을 향상시켰기 때문에 트라메티닙과 다른 키나아제 억제제와의 상승 효과의 존재가 제안되었다 (도 4).
실시예 4: 인간 췌장암 세포를 이용한 키나아제 억제제의 약효 평가
인간 췌장암 세포주(MIAPaCa-2)는 국립 연구개발법인이화학연구소 바이오자원연구센터에서 구입하여, Dulbecco's Modified Eagle's Medium (nakalai tesque)에 10% 소태아혈청(gibco)과 1% 페니실린-스트렙토마이신 (nakalai tesque)를 첨가한 배지를 사용하고, 5% CO2 존재하, 37℃에서 배양하였다.
트라메티닙(DMSO만, 1μM, 300μM), 아다보서팁(300μM, 1mM), AD80(30μM, 3mM), 알리서팁(30μM, 1mM), BI-831266(3μM, 3mM)을 각각 조제하고, 100배로 희석하여 약제액으로 하였다.
MIAPaCa-2 세포를 96 웰 플레이트에 1,000 세포/웰 파종하였다(100 μL 배지 중). 1일 배양 후, 트라메티닙 단독 또는 트라메티닙과 다른 키나아제 억제제의 조합된 약제액을 10㎕씩 96웰 플레이트의 세포에 첨가하였다(DMSO의 최종 농도 0.2%). 각 조합을 5 웰씩 시험하였다. 약제액 첨가 후, 5% CO2 존재하, 37℃에서 72시간 배양한 후, MTS 어세이(CellTiter96(등록상표), Promega)을 사용하여 세포 생존율을 측정하였다. 생존율은 대조군(용매만)에 대한 비율로 표기하였다.
트라메티닙은 단독으로 세포 생존율을 용량 의존적으로 감소시켰다. 트라메티닙을 아다보서팁, AD80, 알리서팁, BI-831266의 각각과 조합하면, 어느 조합에 있어서도 트라메티닙 단독보다 세포 생존율이 크게 감소했기 때문에, 트라메티닙과 다른 키나아제 억제제의 상승효과의 존재가 제안되었다 (도 5).
실시예 5: 4-hit 파리의 치사성의 온도 의존성 평가
실시예 3에서 제작한 4-hit 파리(non-GFP)를, 22, 24, 25, 27, 29℃의 각 온도에서 사육한 바, 온도 상승과 함께 생존율은 저하하고, 25℃ 이상에서 치사가 되었다(도 6).
실시예 6: 담암 마우스를 이용한 키나아제 억제제의 약효 평가
BALB/c-nu/nu 면역결핍 누드 마우스(6주령, specific pathogen-free 사육)에 마취를 실시하고, 그 피하에 5×106 개의 MIA PaCa-2 세포를 이식하였다. 종양 체적(장경×단경×단경/2)을 계측하면서 사육을 계속하고, 이것이 100 mm3에 도달한 시점에서 4군(n=8)으로 나누었다. 각 그룹에 용매(5% DMSO), 트라메티닙(1 mg/kg 체중/일), BI-831266(10 mg/kg 체중/일), 또는 트라메티닙(1 mg/kg 체중/일) 및 BI -831266(10 mg/kg 체중/일)을 1주일에 5일 동안 경구 투여하고, 종양 부피를 시간 경과에 따라 측정하였다.
트라메티닙과 BI-831266의 조합 투여군(T+B군)에서는 트라메티닙 단독 투여군(T군) 및 BI-831266 단독 투여군(B군)과 비교하여 종양 체적 평균치의 증가가 현저히 억제되었다 (도 7A). 개별 마우스에서 볼 때, 조합 투여군에서는 부분 관해(30% 이상의 종양 체적 축소) 또는 완전 관해(종양 소실)에 이르는 증례가 많이 인정되었지만, 용매 투여군 및 트라메티닙 단독 투여 그룹에서 부분적인 관해 또는 완전한 관해는 관찰되지 않았고, BI-831266 투여군에서 단지 하나의 완전한 관해만이 발견되었다 (도 7B). 이러한 결과로부터, 트라메티닙과 BI-831266의 조합은 마우스에 이식된 인간 췌장암 세포에 대해 상승적인 세포 증식 억제 효과를 나타내고, 그 효과에는 개체차가 적다는 것이 확인되었다.
[배열표 프리텍스트]
서열번호 1 Ras85D의 아미노산 서열
서열번호 2 p53 유전자를 표적으로 하는 shRNA의 센스 가닥을 코딩하는 DNA의 염기 서열
서열번호 3 p53 유전자를 표적으로 하는 shRNA의 안티센스 가닥을 코딩하는 DNA의 염기 서열
서열번호 4 Med 유전자를 표적으로 하는 shRNA의 센스 가닥을 코딩하는 DNA의 염기 서열
서열번호 5 Med 유전자를 표적으로 하는 shRNA의 안티센스 가닥을 코딩하는 DNA의 염기 서열
서열번호 6 shRNA 헤어핀 루프를 코딩하는 DNA의 염기 서열
SEQUENCE LISTING
<110> National University Corporation Hokkaido University
<120> Method for screening anticancer agent, and combination of kinase
inhibitors for treating pancreatic cancer
<130> P19HU10WO
<160> 6
<170> PatentIn version 3.5
<210> 1
<211> 189
<212> PRT
<213> Drosophila melanogaster
<400> 1
Met Thr Glu Tyr Lys Leu Val Val Val Gly Ala Gly Gly Val Gly Lys
1 5 10 15
Ser Ala Leu Thr Ile Gln Leu Ile Gln Asn His Phe Val Asp Glu Tyr
20 25 30
Asp Pro Thr Ile Glu Asp Ser Tyr Arg Lys Gln Val Val Ile Asp Gly
35 40 45
Glu Thr Cys Leu Leu Asp Ile Leu Asp Thr Ala Gly Gln Glu Glu Tyr
50 55 60
Ser Ala Met Arg Asp Gln Tyr Met Arg Thr Gly Glu Gly Phe Leu Leu
65 70 75 80
Val Phe Ala Val Asn Ser Ala Lys Ser Phe Glu Asp Ile Gly Thr Tyr
85 90 95
Arg Glu Gln Ile Lys Arg Val Lys Asp Ala Glu Glu Val Pro Met Val
100 105 110
Leu Val Gly Asn Lys Cys Asp Leu Ala Ser Trp Asn Val Asn Asn Glu
115 120 125
Gln Ala Arg Glu Val Ala Lys Gln Tyr Gly Ile Pro Tyr Ile Glu Thr
130 135 140
Ser Ala Lys Thr Arg Met Gly Val Asp Asp Ala Phe Tyr Thr Leu Val
145 150 155 160
Arg Glu Ile Arg Lys Asp Lys Asp Asn Lys Gly Arg Arg Gly Arg Lys
165 170 175
Met Asn Lys Pro Asn Arg Arg Phe Lys Cys Lys Met Leu
180 185
<210> 2
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> synthesized oligonucleotide
<400> 2
tgctgaagca ataaccaccg a 21
<210> 3
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> synthesized oligonucleotide
<400> 3
tcggtggtta ttgcttcagc a 21
<210> 4
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> synthesized oligonucleotide
<400> 4
ttcagtgcga tgaacattgc t 21
<210> 5
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> synthesized oligonucleotide
<400> 5
agcaatgttc atcgcactga a 21
<210> 6
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> synthesized oligonucleotide
<400> 6
tagttatatt caagcata 18
Claims (17)
- 하기 a)~d):
a) 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산, 발린 또는 시스테인으로 치환된 변이형 Ras85D의 발현,
b) p53 유전자의 결실 또는 발현 억제,
c) Cyclin E 유전자의 과발현 및
d) Med 유전자의 결실 또는 발현 억제
의 특징을 가지는 초파리에 피험물질을 섭취시키는 단계,
피험물질을 섭취한 초파리의 생존율을 측정하는 단계 및
피험물질을 섭취한 초파리의 생존율이 피험물질을 섭취하지 않는 초파리의 생존율보다 높은 경우, 당해 피험물질을 항암제의 후보 물질로 선발하는 단계를 포함하는 항암제를 스크리닝하는 방법. - 제 1 항에 있어서,
변이형 Ras85D는 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 단백질이며,
p53 유전자의 발현 억제는 p53 유전자의 발현을 억제하는 핵산의 도입에 의해 수행되고,
Cyclin E의 과발현은 Cyclin E를 코딩하는 핵산의 도입에 의해 수행되며,
Med 유전자의 발현 억제는 Med 유전자의 발현을 억제하는 핵산의 도입에 의해 수행되는 방법. - 제1항에 있어서,
초파리는 서열번호 1의 아미노산 서열의 12 번째 글리신이 아스파르트 산으로 치환된 변이형 Ras85D를 코딩하는 핵산, p53 유전자에 대한 넉다운 핵산, Cyclin E 유전자를 코딩하는 핵산 및 Med 유전자에 대한 넉다운 핵산이 도입된 초파리인 방법. - 하기 a')~d'):
a') UAS 서열의 하류에 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 변이형 Ras85D를 코딩하는 염기 서열을 갖는 핵산,
b') UAS 서열의 하류에 p53 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산,
c ') UAS 서열의 하류에 Cyclin E 유전자를 코딩하는 염기 서열을 갖는 핵산 및
d') UAS 서열의 하류에 Med 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산
이 도입된 초파리와 gal4 유전자가 도입된 초파리와의 교배에 의해 태어난 알을, 피험물질을 함유하는 먹이 상에서 사육하는 단계,
피험물질을 함유한 먹이 상에서 사육한 초파리의 생존율을 측정하는 단계, 및
피험물질을 함유한 먹이 상에서 사육한 초파리의 생존율이, 피험물질을 함유하지 않는 먹이 상에서 사육한 초파리의 생존율보다 높은 경우, 당해 피험물질을 항암제의 후보물질로서 선발하는 단계를 포함하는 항암제를 스크리닝하는 방법. - 제 1 항 내지 제 4 항 중 어느 한 항에 있어서, 초파리의 사육 온도를 조절함으로써 피험물질을 섭취하지 않는 초파리 또는 피험물질을 함유하지 않는 먹이로 사육한 초파리의 생존율을 제어하는 방법.
- 아래 a)~d):
a) 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산, 발린 또는 시스테인으로 치환된 변이형 Ras85D의 발현,
b) p53 유전자의 결실 또는 발현 억제,
c) Cyclin E 유전자의 과발현 및
d) Med 유전자의 결실 또는 발현 억제
의 특징을 가진 초파리. - 제6항에 있어서,
아래 a')~d'):
a') UAS 서열의 하류에 서열번호 1의 아미노산 서열의 12번째 글리신이 아스파르트산으로 치환된 변이형 Ras85D를 코딩하는 염기 서열을 갖는 핵산,
b') UAS 서열의 하류에 p53 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산,
c ') UAS 서열의 하류에 Cyclin E 유전자를 코딩하는 염기 서열을 갖는 핵산 및
d') UAS 서열의 하류에 Med 유전자에 대한 shRNA를 코딩하는 염기 서열을 갖는 핵산
이 도입된 초파리. - 췌장암의 치료를 위한 MEK 억제제, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택되는 적어도 2종의 키나아제 억제제의 조합 의약.
- 췌장암의 치료를 위한 MEK 억제제와, FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택되는 적어도 1종의 키나아제 억제제의 조합 의약.
- 제8항 또는 제9항에 있어서, MEK 억제제가 트라메티닙인 조합 의약.
- 제8항 내지 제10항 중 어느 한 항에 있어서, FRK 억제제가 AD80이고, WEE 억제제가 아다보셀티브이고, AURK 억제제가 알리서팁 또는 BI-831266인 조합 의약.
- 췌장암의 치료에 있어서 MEK 억제제와 조합하기 위한 FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택되는 키나아제 억제제.
- 제12항에 있어서, MEK 억제제가 트라메티닙인 키나아제 억제제.
- 제12항 또는 제13항에 있어서, FRK 억제제가 AD80이고, WEE 억제제가 아다보셀티브이고, AURK 억제제가 알리서팁 또는 BI-831266인 키나아제 억제제.
- 췌장암의 치료에 있어서 FRK 억제제, WEE 억제제, AURK 억제제 및 ROCK 억제제로 이루어진 군으로부터 선택되는 적어도 1종의 키나아제 억제제와 조합하기 위한, MEK 억제제.
- 제15항에 있어서, 트라메티닙인, MEK 억제제.
- 제15항 또는 제16항에 있어서, FRK 억제제가 AD80이고, WEE 억제제가 아다보셀티브이고, AURK 억제제가 알리서팁 또는 BI-831266 인 MEK 억제제.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2020-032112 | 2020-02-27 | ||
| JP2020032112 | 2020-02-27 | ||
| PCT/JP2021/007651 WO2021172582A1 (ja) | 2020-02-27 | 2021-03-01 | 抗がん剤をスクリーニングする方法及び膵がんの治療のためのキナーゼ阻害剤の組み合わせ医薬 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220032607A true KR20220032607A (ko) | 2022-03-15 |
Family
ID=77491650
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227004728A KR20220032607A (ko) | 2020-02-27 | 2021-03-01 | 항암제를 스크리닝하는 방법 및 췌장암 치료를 위한 키나아제 억제제의 조합 의약 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20220387630A1 (ko) |
| EP (1) | EP4115907A4 (ko) |
| JP (1) | JPWO2021172582A1 (ko) |
| KR (1) | KR20220032607A (ko) |
| CN (1) | CN114207437B (ko) |
| AU (1) | AU2021226119B2 (ko) |
| CA (1) | CA3151403A1 (ko) |
| WO (1) | WO2021172582A1 (ko) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019528279A (ja) | 2016-08-17 | 2019-10-10 | アイカーン スクール オブ メディシン アット マウント サイナイ | キナーゼ阻害物質化合物、組成物、及びがんの治療方法 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101896227A (zh) * | 2007-12-12 | 2010-11-24 | 阿斯利康(瑞典)有限公司 | 包含mek抑制剂和极光激酶抑制剂的组合 |
| US20110319415A1 (en) * | 2008-08-18 | 2011-12-29 | Universit+e,uml a+ee t zu K+e,uml o+ee ln | Susceptibility to HSP90-Inhibitors |
| TW201316991A (zh) * | 2011-06-03 | 2013-05-01 | Millennium Pharm Inc | Mek抑制劑與奧諾拉(aurora)a激酶選擇性抑制劑之組合 |
| JP6342805B2 (ja) * | 2011-09-02 | 2018-06-13 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 置換ピラゾロ[3,4−d]ピリミジンおよびその用途 |
| WO2015026860A1 (en) * | 2013-08-20 | 2015-02-26 | Tosk, Inc. | Non-mammalian ras transgenic animal model |
| US9629851B2 (en) * | 2013-09-20 | 2017-04-25 | Stitching Het Nederlands Kanker Institut—Antoni Van Leeuwenhoek Ziekenhuis | ROCK in combination with MAPK pathway |
| US10335494B2 (en) * | 2013-12-06 | 2019-07-02 | Millennium Pharmaceuticals, Inc. | Combination of aurora kinase inhibitors and anti-CD30 antibodies |
| WO2017117344A1 (en) * | 2015-12-30 | 2017-07-06 | Icahn School Of Medicine At Mount Sinai | Fly avatars for cancer and uses thereof |
| WO2018183891A1 (en) * | 2017-03-31 | 2018-10-04 | Cascadian Therapeutics | Combinations of chk1- and wee1 - inhibitors |
| JP7309614B2 (ja) * | 2017-05-02 | 2023-07-18 | ノバルティス アーゲー | 組み合わせ療法 |
| JP2019206516A (ja) * | 2018-05-23 | 2019-12-05 | 国立大学法人高知大学 | 膵癌細胞の浸潤転移抑制剤 |
| WO2020010280A1 (en) * | 2018-07-06 | 2020-01-09 | Memorial Sloan Kettering Cancer Center | Combination therapy with mek inhibitor and cdk4/6 inhibitor to treat pancreatic cancer |
| CN110295233B (zh) * | 2019-07-08 | 2023-04-25 | 深圳开悦生命科技有限公司 | DHX33基因作为Ras驱动的癌症分子靶点的应用 |
-
2021
- 2021-03-01 JP JP2022503384A patent/JPWO2021172582A1/ja active Pending
- 2021-03-01 AU AU2021226119A patent/AU2021226119B2/en active Active
- 2021-03-01 CN CN202180004873.8A patent/CN114207437B/zh active Active
- 2021-03-01 CA CA3151403A patent/CA3151403A1/en active Pending
- 2021-03-01 WO PCT/JP2021/007651 patent/WO2021172582A1/ja unknown
- 2021-03-01 US US17/635,820 patent/US20220387630A1/en active Pending
- 2021-03-01 EP EP21761537.6A patent/EP4115907A4/en active Pending
- 2021-03-01 KR KR1020227004728A patent/KR20220032607A/ko not_active Application Discontinuation
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019528279A (ja) | 2016-08-17 | 2019-10-10 | アイカーン スクール オブ メディシン アット マウント サイナイ | キナーゼ阻害物質化合物、組成物、及びがんの治療方法 |
Non-Patent Citations (4)
| Title |
|---|
| Qian et al., JAMA Oncol. 2018; 4(3): e173420. |
| Sonoshita et al., Curr. Top. Dev. Biol. 2017; 121:287-309. |
| Sonoshita et al., Nat. Chem. Biol. 2018; 14(3): 291-298. |
| Ung, Sonoshita et al., PLoS Comput. Biol. 2019; 15(4): e1006878. |
Also Published As
| Publication number | Publication date |
|---|---|
| CN114207437B (zh) | 2024-05-28 |
| AU2021226119B2 (en) | 2024-04-18 |
| WO2021172582A1 (ja) | 2021-09-02 |
| CA3151403A1 (en) | 2021-09-02 |
| AU2021226119A1 (en) | 2022-03-24 |
| EP4115907A4 (en) | 2024-07-03 |
| JPWO2021172582A1 (ko) | 2021-09-02 |
| US20220387630A1 (en) | 2022-12-08 |
| EP4115907A1 (en) | 2023-01-11 |
| CN114207437A (zh) | 2022-03-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Issa et al. | Therapeutic implications of menin inhibition in acute leukemias | |
| Falcicchia et al. | Seizure-suppressant and neuroprotective effects of encapsulated BDNF-producing cells in a rat model of temporal lobe epilepsy | |
| Wu et al. | Activity of the type II JAK2 inhibitor CHZ868 in B cell acute lymphoblastic leukemia | |
| Bruchas et al. | Stress-induced p38 mitogen-activated protein kinase activation mediates κ-opioid-dependent dysphoria | |
| Vitucci et al. | Cooperativity between MAPK and PI3K signaling activation is required for glioblastoma pathogenesis | |
| Fu et al. | Regulation of postsynaptic signaling in structural synaptic plasticity | |
| Taneja et al. | Transgenic and knockout mice models to reveal the functions of tumor suppressor genes | |
| Chen et al. | The type 1 equilibrative nucleoside transporter regulates anxiety‐like behavior in mice | |
| WO2003026576A2 (en) | Induction of brown adipocytes by transcription factor nfe2l2 | |
| Bihannic et al. | Insights into cerebellar development and medulloblastoma | |
| CN107530433A (zh) | 针对具有braf基因突变的细胞的细胞死亡诱导试剂、该细胞的增殖抑制试剂及用于治疗由该细胞的增殖异常导致的疾病的医药组合物 | |
| Stavarache et al. | The tumor suppressor PTEN regulates motor responses to striatal dopamine in normal and Parkinsonian animals | |
| Padhye et al. | Targeting CDK4 overcomes EMT-mediated tumor heterogeneity and therapeutic resistance in KRAS-mutant lung cancer | |
| DK3066199T3 (en) | SNORNA, COMPOSITIONS AND APPLICATIONS | |
| Zhu et al. | TAOK1 positively regulates TLR4-induced inflammatory responses by promoting ERK1/2 activation in macrophages | |
| Kantarci et al. | The Warburg Effect and lactate signaling augment Fgf-MAPK to promote sensory-neural development in the otic vesicle | |
| CN105636434A (zh) | 非哺乳类ras转基因动物模型 | |
| Hutter et al. | Differential roles of miR‐15a/16‐1 and miR‐497/195 clusters in immune cell development and homeostasis | |
| US11077110B2 (en) | Compositions and methods for treating and preventing metabolic disorders | |
| Fukuda et al. | Augmented growth hormone secretion and Stat3 phosphorylation in an aryl hydrocarbon receptor interacting protein (AIP)-disrupted somatotroph cell line | |
| KR20220032607A (ko) | 항암제를 스크리닝하는 방법 및 췌장암 치료를 위한 키나아제 억제제의 조합 의약 | |
| US20160128311A1 (en) | Screen and use of therapeutics for pancreatic ductal adenocarcinoma | |
| Denton et al. | Drosophila as a model to understand autophagy deregulation in human disorders | |
| ES2331800T3 (es) | Utilizacion de inhibidores de tirosina-quinasa para el tratamiento de la diabetes. | |
| KR20150099125A (ko) | microRNA-30b, microRNA-133a 또는 microRNA-202-5p의 억제제를 포함하는 항암용 약학적 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal |