KR20200070091A - Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof - Google Patents
Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof Download PDFInfo
- Publication number
- KR20200070091A KR20200070091A KR1020190130504A KR20190130504A KR20200070091A KR 20200070091 A KR20200070091 A KR 20200070091A KR 1020190130504 A KR1020190130504 A KR 1020190130504A KR 20190130504 A KR20190130504 A KR 20190130504A KR 20200070091 A KR20200070091 A KR 20200070091A
- Authority
- KR
- South Korea
- Prior art keywords
- nanolipid
- transporter
- lipid
- polypeptide
- present
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/55—Phosphorus compounds
- A61K8/553—Phospholipids, e.g. lecithin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/64—Proteins; Peptides; Derivatives or degradation products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0014—Skin, i.e. galenical aspects of topical compositions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/5123—Organic compounds, e.g. fats, sugars
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5192—Processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/41—Particular ingredients further characterized by their size
- A61K2800/413—Nanosized, i.e. having sizes below 100 nm
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/40—Chemical, physico-chemical or functional or structural properties of particular ingredients
- A61K2800/56—Compounds, absorbed onto or entrapped into a solid carrier, e.g. encapsulated perfumes, inclusion compounds, sustained release forms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/80—Process related aspects concerning the preparation of the cosmetic composition or the storage or application thereof
- A61K2800/805—Corresponding aspects not provided for by any of codes A61K2800/81 - A61K2800/95
Abstract
Description
본 발명은 생리활성 물질 봉입을 위한 나노지질전달체 및 이의 제조방법에 관한 것으로, 보다 상세하게는 나노 입자 안정성이 우수하고 수용성 약물의 봉입이 향상된 입자성 나노지질전달체에 관한 것이다.The present invention relates to a nanolipid transporter for encapsulating a bioactive material and a method for manufacturing the same, and more particularly, to a particulate nanolipid transporter having excellent nanoparticle stability and improved encapsulation of a water-soluble drug.
인체 내에 약물을 효율적으로 전달할 수 있는 약물전달 시스템의 개발은 그 중요성이 증가하고 있다. 약물전달시스템 중 약물을 마이크로 또는 나노 크기의 전달체에 봉입하여 활용하는 기술은 주사용, 경구용 또는 경피용 등으로 다양하게 활용될 수 있으며, 대표적인 기술로는 에멀젼, 리포좀, 마이크로 입자 또는 나노입자형태의 구조체를 들 수 있다.The importance of developing a drug delivery system capable of efficiently delivering drugs in the human body is increasing. Among the drug delivery systems, the technology of encapsulating and using the drug in a micro or nano-sized carrier can be variously used for injection, oral or transdermal use, and representative technologies include emulsions, liposomes, microparticles, or nanoparticles. The structure of the.
에멀젼은 오일액적에 약물을 봉입시키고 이를 양친성 계면활성제를 이용하여 분산시킨 구조체로서 난용성 약물의 용해에 매우 효과적이나 물리적 안정성이 낮다. 리포좀은 콜로이드성 나노전달체로서 혈중에서 오랜 시간 순환할 수 있고 생체적합성이며 생리활성물질의 독성을 줄여주는 장점이 있으나 대식세포의 식작용에 의한 손실 가능성이 높고, 콜로이드적으로 불안정한 단점이 있다. 또한, 고분자 마이크로 입자 또는 나노 입자는 약물의 방출 조절, 타게팅 등에 유리하며 원하는 입자 크기로 조절하여 다양한 형태의 입자를 제조할 수 있는 장점은 있으나 세포 독성이 존재하고, 유기 용매의 사용에 따른 용매의 제거 문제 및 대량 생산이 쉽지 않은 단점이 있다.The emulsion is a structure in which a drug is enclosed in an oil droplet and dispersed using an amphiphilic surfactant, which is very effective in dissolving poorly soluble drugs, but has low physical stability. Liposomes are colloidal nanocarriers, which can circulate in the blood for a long time, have biocompatibility, and reduce the toxicity of bioactive substances, but have a high probability of loss due to phagocytosis of macrophages and colloidally unstable disadvantages. In addition, polymer microparticles or nanoparticles are advantageous for controlling drug release, targeting, etc., and have the advantage of producing various types of particles by controlling to a desired particle size. There are drawbacks and disadvantages that mass production is not easy.
최근, 상기와 같은 약물전달 시스템의 단점을 극복한 고상지질 나노입자(solid lipid nanoparticle)가 새로운 구조체로서 활발히 연구되고 있다. 고상지질 나노입자는 상온에서 고체상태인 지질을 활용하여 약물을 봉입하고 구형의 입자를 제조하여 고체 지질 내부에 약물의 봉입되는 형태로 존재하는 구조체이다. 고상지질 나노입자는 고형의 지질의 온도를 높여 소수성 약물과 혼합 후 계면활성제를 통해 입자를 형성하면서 수상에서 냉각시키기 때문에 소수성 약물을 봉입하기에는 유리하나, 펩타이드와 같은 친수성 약물은 20-30%로 매우 낮은 봉입률을 보이는 단점이 있다. 상기와 같은 문제의 극복을 위해 친수성 약물을 소수성으로 결합시키거나, 에멀젼 형태로 제조하는 방법, 액정상태의 지질 등을 결합시키는 방법 등이 연구되었으나, 봉입율의 현저한 향상은 이루어지지 않았을 뿐만 아니라, 대량생산이 어려운 문제가 남아있다.Recently, solid lipid nanoparticles that overcome the disadvantages of the drug delivery system as described above have been actively studied as a new structure. Solid lipid nanoparticles are structures that exist in the form of encapsulating the drug inside the solid lipid by encapsulating the drug using solid lipids at room temperature and producing spherical particles. Solid lipid nanoparticles increase the temperature of solid lipids, mix with hydrophobic drugs, form particles through a surfactant and cool in the water phase, so it is advantageous to encapsulate hydrophobic drugs, but hydrophilic drugs such as peptides are very high at 20-30%. It has the disadvantage of showing a low encapsulation rate. In order to overcome the above problems, a method of binding a hydrophilic drug with hydrophobicity, a method of preparing in an emulsion form, a method of binding a lipid in a liquid crystal state, etc. has been studied, but not only a significant improvement in the encapsulation rate has not been achieved, The problem remains that mass production is difficult.
약물 전달 경로 중 피부에 비침습적으로 전달하는 방법으로는 크게 두 가지로 경피전달경로(transdermal delivery)와 모낭전달경로(hair follicle delivery)를 들 수 있다. 최근까지의 연구 결과, 전달체의 크기를 나노화하였을 때, 각질 세포 사이를 통과하여 진피로 흡수되는 확률이 마이크로 또는 그 이상의 크기를 가진 전달체 대비 훨씬 높은 것으로 나타났다. 대표적인 경피 전달체로는 인지질로 약물을 봉입하는 리포좀을 들 수 있으며, 약물 전달, 화장품 분야에서 많이 활용되고 있으나, 상기 경피 전달체는 경피에서의 전달 능력이 이론보다 현저히 낮은 경향을 보이며, 콜로이드성 전달체로 안정성이 매우 낮은 단점이 존재하기 때문에 이에 대한 해결이 절실한 상황이다.There are two methods of non-invasive delivery to the skin among drug delivery routes, transdermal delivery and hair follicle delivery. As a result of studies until recently, when nanosized the size of a carrier, the probability of passing through keratinocytes to the dermis is much higher than that of a carrier having a micro or larger size. Representative transdermal delivery systems include liposomes that encapsulate drugs with phospholipids, and are widely used in drug delivery and cosmetics, but the transdermal delivery system shows a remarkably lower tendency in transdermal delivery than the theory, and is a colloidal delivery system. Since there is a disadvantage that stability is very low, the solution to this problem is urgent.
종래의 고상지질 나노입자가 수용성 생리활성물질에 대해 낮은 봉입 효율을 가져 주로 지용성 생리활성물질의 전달체로만 사용된 것과 달리, 본 발명의 목적은 나노지질전달체를 수용성 생리활성물질의 전달체로 사용하고 수용성 생리활성물질의 봉입 효율을 현저하게 향상시키기 위한 것이다.Unlike conventional solid lipid nanoparticles, which have low encapsulation efficiency for water-soluble physiologically active substances and are mainly used only as carriers for fat-soluble bioactive substances, the object of the present invention is to use nanolipid carriers as carriers for water-soluble bioactive substances and It is intended to significantly improve the encapsulation efficiency of bioactive materials.
본 발명의 다른 목적은 수용성 생리활성물질을 봉입하더라도 낮은 안정성으로 인해 고상지질 나노입자의 구조가 붕괴되어 생리활성물질이 빠르게 방출되는 문제를 해결하고, 안정적으로 수용성 생리활성물질을 봉입할 수 있는 나노지질전달체를 제공하고, 수분산액 상태에서 장시간 안정적으로 콜로이드 안정성을 가질 수 있는 나노지질전달체를 제공하는 것이다.Another object of the present invention is to solve the problem that the structure of the solid lipid nanoparticles is collapsed due to low stability even if the water-soluble physiologically active material is encapsulated, and it is possible to stably encapsulate the water-soluble physiologically active material. It is to provide a lipid transporter and a nanolipid transporter that can stably have colloidal stability for a long time in an aqueous dispersion state.
본 발명의 다른 목적은 피부에 처리시 모낭에 대해 특이적으로 흡수효율이 뛰어난 고상지질 나노입자를 제공하는 것이다.Another object of the present invention is to provide solid lipid nanoparticles with excellent absorption efficiency specifically for hair follicles when treated on skin.
본 발명에 따른 생리활성물질이 봉입된 나노지질전달체의 제조방법은 생리활성물질 및 친수성 고분자를 포함하는 친수성 고분자 복합체 수용액을 생성하는 단계; 상기 친수성 복합체 수용액을 인지질 용액에 투입하여 콜로이드 용액을 생성하는 단계; 지질에 상기 콜로이드 용액을 투입하여 유중수 분산액을 생성하는 단계; 및 상기 유중수 분산액을 계면활성제를 포함하는 수용액에 투입하고 균질화하여 나노지질전달체를 생성하는 단계;를 포함한다.A method of manufacturing a nanolipid transporter encapsulated with a physiologically active material according to the present invention comprises the steps of: generating an aqueous solution of a hydrophilic polymer complex comprising a bioactive material and a hydrophilic polymer; Generating a colloidal solution by introducing the aqueous hydrophilic complex solution into a phospholipid solution; Generating a water-in-oil dispersion by adding the colloidal solution to lipids; And adding the water-in-oil dispersion to an aqueous solution containing a surfactant and homogenizing to generate a nanolipid transporter.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 생리활성물질은 펩타이드계 화합물을 포함할 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the bioactive material may include a peptide-based compound.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 생리활성물질은 수용액 내에서 양 또는 음의 전하를 가질 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the bioactive material may have a positive or negative charge in an aqueous solution.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 친수성 고분자는 음이온성 또는 양이온성 고분자를 포함하며, 상리 생리물질과 상이한 전하를 가지는 것일 수 있다. In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the hydrophilic polymer may include anionic or cationic polymers, and may have different charges from upper physiological substances .
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 친수성 고분자 복합체 수용액은 하이드로겔 특성을 나타낼 수 있다.In the method of manufacturing a nanolipid transporter according to an example of the present invention, the aqueous hydrophilic polymer composite solution may exhibit hydrogel properties.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 지질은 서로 다른 융점을 가지는 2 이상의 지질을 포함할 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the lipid may include two or more lipids having different melting points.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 지질 혼합액은 상온에서 고상인 제1지질 및 상온에서 액상인 제2지질을 포함할 수 있다.In the method of manufacturing a nanolipid transporter according to an example of the present invention, the lipid mixture may include a first lipid that is solid at room temperature and a second lipid that is liquid at room temperature.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 유중수 분산액은 지질을 가온하여 용액상을 형성한 후 상기 콜로이드 용액을 혼합하여 제조될 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the water-in-oil dispersion may be prepared by mixing the colloidal solution after heating the lipid to form a solution phase.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 계면활성제는 지방족 글리세릴계 화합물을 포함할 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the surfactant may include an aliphatic glyceryl-based compound.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 인지질 용액의 용매는 알코올을 포함할 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the solvent of the phospholipid solution may include alcohol.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 콜로이드 용액은 에토좀 콜로이드를 포함할 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the colloidal solution may include an ethosomal colloid.
본 발명의 일 예에 따른 나노지질전달체의 제조방법에서, 상기 나노지질전달체를 생성하는 단계는 고압유화 단계를 더 포함할 수 있다.In the method of manufacturing a nanolipid transporter according to an embodiment of the present invention, the step of generating the nanolipid transporter may further include a high pressure emulsification step.
또한, 본 발명에 따른 나노지질전달체는 생리활성물질 및 친수성 고분자를 함유하는 친수성 고분자 복합체를 포함하는 코어부; 및 상기 코어의 표면 상에 위치하며 지질을 포함하는 쉘부;를 포함하고, 상기 코어부는 인지질을 더 포함한다.In addition, the nanolipid transporter according to the present invention includes a core portion including a hydrophilic polymer complex containing a bioactive material and a hydrophilic polymer; And a shell portion located on the surface of the core and including lipids. The core portion further includes phospholipids.
본 발명의 일 예에 따른 나노지질전달체에서, 상기지질 및 인지질은 중량비로 100:0.1 내지 100:50으로 포함될 수 있다.In the nanolipid transporter according to an embodiment of the present invention, the lipid and phospholipid may be included in a weight ratio of 100:0.1 to 100:50.
본 발명의 일 예에 따른 나노지질전달체에서, 상기 생리활성물질 및 친수성 고분자는 중량비로 2000:1 내지 20:1으로 포함될 수 있다.In the nanolipid transporter according to an embodiment of the present invention, the bioactive material and the hydrophilic polymer may be included in a weight ratio of 2000:1 to 20:1.
본 발명의 일 예에 따른 나노지질전달체에서, 상기 나노지질전달체는 20 nm 내지 1000 nm의 평균 입경을 가지며 하기 관계식 1을 만족할 수 있다.In the nanolipid transporter according to an embodiment of the present invention, the nanolipid transporter has an average particle diameter of 20 nm to 1000 nm and may satisfy the following relational expression 1.
[관계식 1][Relationship 1]
|T0-T20|/T0< 0.2|T 0 -T 20 |/T 0 <0.2
(상기 관계식 1에서 T0는 나노지질전달체 1중량% 수분산액의 제조 후 500 nm 파장에서 측정된 투과도를 의미하며, T20은 나노지질전달체 1중량% 수분산액을 45℃에서 20일 방치 후 500 nm 파장에서 측정된 투과도를 의미한다.)(In the above equations 1 T 0 after the production of nano-lipid delivery system of 1% aqueous dispersion by weight means a permeability measured at 500 nm wavelength, and, T 20 are 500 then the nano-lipid delivery system of 1% aqueous dispersion by weight to stand at 45
또한, 본 발명은 상기 나노지질전달체를 포함하는 화장료 조성물을 제공한다.In addition, the present invention provides a cosmetic composition comprising the nanolipid transporter.
본 발명의 일 예에 따른 화장료 조성물은 모낭 타게팅 특성을 가질 수 있으며 경피흡수용화장료 조성물일 수 있다.The cosmetic composition according to an embodiment of the present invention may have follicle targeting properties and may be a transdermal absorption cosmetic composition.
또한, 본 발명은 상기 나노지질전달체를 피부에 처리하는 단계를 포함하는, 생리활성물질이 봉입된 나노지질전달체의 모낭 타게팅 전달방법을 제공한다.In addition, the present invention provides a method for delivering follicular targeting of a nanolipid transporter encapsulated with a bioactive substance, comprising the step of treating the nanolipid transporter on the skin.
본 발명에 따른 나노지질전달체는 수용성 생리활성물질을 내부에 고함량으로 봉입하여 수용성 생리활성물질의 전달체로 바람직하게 사용될 수 있다.The nanolipid transporter according to the present invention can be preferably used as a carrier of a water-soluble bioactive material by encapsulating the water-soluble bioactive material with a high content therein.
또한, 본 발명에 따른 나노지질전달체는 수용성 생리활성물질을 안정적으로 봉입할 수 있으며, 수분산액 상태에서 장시간 안정적으로 콜로이드 안정성을 가질 수 있다.In addition, the nanolipid transporter according to the present invention can stably encapsulate a water-soluble physiologically active substance, and can have colloidal stability stably for a long time in an aqueous dispersion state.
또한, 본 발명에 따른 나노지질전달체는 피부에 처리시 모낭에 대해 특이적으로 흡수율이 뛰어나고, 비교적 간단한 제조방법으로 대량생산이 가능하여 모낭에 생리활성물질을 전달하기 위한 약학 조성물 또는 화장료 조성물로 바람직하게 사용될 수 있다.In addition, the nanolipid transporter according to the present invention has a particularly excellent absorption rate for hair follicles when treated on the skin, and is capable of mass production in a relatively simple manufacturing method, and thus is preferable as a pharmaceutical composition or cosmetic composition for delivering a physiologically active substance to the hair follicle. Can be used.
도 1은 본 발명의 일 예에 따른 생리활성물질이 봉입된 나노지질전달체의 구조에 대한 모식도를 나타낸 것이다.
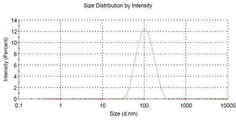
도 2는 본 발명의 일 예에 따라 제조된 나노지질전달체의 입자크기를 측정한 결과를 도시한 것이다.
도 3은 본 발명의 일 예에 따른 나노지질전달체 분산액(고형분 6.5 중량%)의 30일간 안정성 실험 후 샘플을 촬영한 결과 도시한 것이다.
도 4는 본 발명의 일 예에 따른 나노지질전달체를 bio-TEM으로 측정한 결과를 도시한 것이다.
도 5는 본 발명의 일 예에 따른 나노지질전달체를 형광처리하고 피부모낭에 흡수된 나노지질전달체를 공초점 형광 측정한 결과 도시한 것이다.
도 6은 본 발명의 일 예에 따른 나노지질전달체가 모낭에 타게팅되어 흡수된 시험 결과를 도시한 것이다.1 shows a schematic diagram of the structure of a nanolipid transporter in which a bioactive material is encapsulated according to an example of the present invention.
Figure 2 shows the results of measuring the particle size of the nanolipid transporter prepared according to an example of the present invention.
Figure 3 shows the results of taking a sample after a 30-day stability test of the nanolipid transporter dispersion (solid content 6.5% by weight) according to an example of the present invention.
Figure 4 shows the results of measuring the nanolipid transporter according to an embodiment of the present invention by bio-TEM.
FIG. 5 shows the results of confocal fluorescence measurement of the nanolipid transporter absorbed by the skin follicle and fluorescent treatment of the nanolipid transporter according to an embodiment of the present invention.
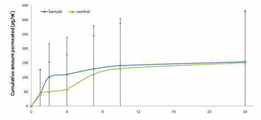
Figure 6 shows the results of the test is absorbed by targeting the nano-lipid transporter in the hair follicle according to an embodiment of the present invention.
이하 첨부한 도면들을 참조하여 본 발명을 상세히 설명한다. 다음에 소개되는 도면들은 당업자에게 본 발명의 사상이 충분히 전달될 수 있도록 하기 위해 예로서 제공되는 것이다. 따라서 본 발명은 이하 제시되는 도면들에 한정되지 않고 다른 형태로 구체화될 수도 있으며, 이하 제시되는 도면들은 본 발명의 사상을 명확히 하기 위해 과장되어 도시될 수 있다. Hereinafter, the present invention will be described in detail with reference to the accompanying drawings. The drawings introduced below are provided as examples in order to sufficiently convey the spirit of the present invention to those skilled in the art. Therefore, the present invention is not limited to the drawings presented below and may be embodied in other forms, and the drawings presented below may be exaggerated to clarify the spirit of the present invention.
본 발명의 명세서에서 사용되는 기술 용어 및 과학 용어에 있어서 다른 정의가 없다면, 이 발명이 속하는 기술 분야에서 통상의 지식을 가진 자가 통상적으로 이해하고 있는 의미를 가지며, 하기의 설명 및 첨부 도면에서 본 발명의 요지를 불필요하게 흐릴 수 있는 공지 기능 및 구성에 대한 설명은 생략한다.Unless otherwise defined in the technical terms and scientific terms used in the specification of the present invention, those skilled in the art to which the present invention pertains have the meanings commonly understood, and the present invention in the following description and accompanying drawings Descriptions of well-known functions and configurations that may unnecessarily obscure the subject matter are omitted.
또한 본 발명의 명세서에서 사용되는 단수 형태는 문맥에서 특별한 지시가 없는 한 복수 형태도 포함하는 것으로 의도할 수 있다. Also, the singular form used in the specification of the present invention may be intended to include the plural form unless otherwise specified in the context.
또한 본 발명의 명세서에서 특별한 언급 없이 사용된 단위는 중량을 기준으로 하며, 일 예로 % 또는 비의 단위는 중량% 또는 중량비를 의미한다.In addition, in the specification of the present invention, the units used without specific reference are based on weight, and for example, units of% or ratio mean weight percent or weight ratio.
또한 본 발명의 명세서에서 다른 정의가 없는 한, 중합체의 분자량은 중량평균 분자량을 의미한다.Also, unless otherwise defined in the specification of the present invention, the molecular weight of the polymer means the weight average molecular weight.
또한 본 발명의 명세서에서 다른 정의가 없는 한, 입자의 평균입경은 입도 분석기를 통해 얻어진 D50을 의미한다.Also, unless otherwise defined in the specification of the present invention, the average particle diameter of the particles means D50 obtained through a particle size analyzer.
또한 본 발명의 명세서에서, “포함한다”는 표현은 “구비한다”, “함유한다”, “가진다” 또는 “특징으로 한다” 등의 표현과 등가의 의미를 가지는 개방형 기재이며, 추가로 열거되어 있지 않은 요소, 재료 또는 공정을 배제하지 않는다. 또한 “실질적으로…로 구성된다”는 표현은 특정된 요소, 재료 또는 공정과 함께 열거되어 있지 않은 다른 요소, 재료 또는 공정이 발명의 적어도 하나의 기본적이고 신규한 기술적 사상에 허용할 수 없을 만큼의 현저한 영향을 미치지 않는 양으로 존재할 수 있는 것을 의미한다. 또한 “구성된다”는 표현은 기재된 요소, 재료 또는 공정만이 존재하는 것을 의미한다.In addition, in the specification of the present invention, the expression “includes” is an open description having the meaning equivalent to expressions such as “have”, “contains”, “haves” or “makes a feature”, and is additionally listed. It does not exclude elements, materials or processes that are not present. Also, “actually… The phrase “consisting of” means that a specified element, material, or process, along with other elements, materials, or processes not listed, does not have an unacceptably significant effect on at least one basic and novel technical idea of the invention. It means that it can exist in quantity. Also, the expression “consisting of” means that only the elements, materials, or processes described are present.
또한 본 발명의 명세서에서 하이드로겔은 물을 용매로 하여 팽윤성을 가지는 친수성 중합체를 포함하는 고체 물질을 의미하며, 고점성을 가져 실질적으로 변형이 되지 않거나 낮은 유동성을 가지는 것을 의미한다. In addition, in the specification of the present invention, a hydrogel means a solid material including a hydrophilic polymer having swelling property using water as a solvent, and has high viscosity, which means that it is substantially unmodified or has low fluidity.
이하 본 발명에 따른 생리활성물질이 봉입된 나노지질전달체의 제조방법에 대해 상세히 설명한다.Hereinafter, a method of manufacturing a nanolipid transporter encapsulated with a bioactive material according to the present invention will be described in detail.
본 발명은 생리활성물질 및 친수성 고분자를 포함하는 친수성 고분자 복합체 수용액을 생성하는 단계; 상기 친수성 복합체 수용액을 인지질 용액에 투입하여 콜로이드 용액을 생성하는 단계; 지질에 상기 콜로이드 용액을 투입하여 유중수 분산액을 생성하는 단계; 및 상기 유중수 분산액을 계면활성제를 포함하는 수용액에 투입하고 균질화하여 나노지질전달체를 생성하는 단계; 를 포함하는, 생리활성물질이 봉입된 나노지질전달체의 제조방법을 제공한다.The present invention comprises the steps of producing an aqueous solution of a hydrophilic polymer complex comprising a bioactive material and a hydrophilic polymer; Generating a colloidal solution by introducing the aqueous hydrophilic complex solution into a phospholipid solution; Generating a water-in-oil dispersion by adding the colloidal solution to lipids; And adding the water-in-oil dispersion to an aqueous solution containing a surfactant and homogenizing to generate a nanolipid transporter; It provides a method for producing a nanolipid transporter containing a bioactive material containing.
상기 생리활성물질 및 친수성 고분자를 포함하는 친수성 고분자 복합체 수용액을 생성하는 단계에서, 상기 생리활성물질은 화장품용 생리활성물질이나 의약용 생리활성물질 등 그 범위에 제한을 두지 않으며, 바람직하게 수용성생리활성물질일 수 있다. 수용성 생리활성물질은 생리활성 효과가 있는 모든 물질이 가능하나, 본 발명에 따른 일 구체예로는 펩타이드를 들 수 있으며, 이하 설명에는 구체적으로 펩타이드를 생리활성물질로 설명하고자 하나 이에 한정되는 것은 아니다.In the step of producing an aqueous solution of a hydrophilic polymer complex containing the bioactive substance and the hydrophilic polymer, the bioactive substance is not limited to a range such as a bioactive substance for cosmetics or a bioactive substance for medicine, preferably water-soluble physiological activity It can be a substance. The water-soluble physiologically active substance may be any substance having a physiologically active effect, but one embodiment of the present invention may include a peptide, and the following description specifically describes the peptide as a physiologically active substance, but is not limited thereto. .
상기 펩타이드계 화합물은 일예로, 2 내지 1000, 좋게는 2 내지 100개, 더욱 좋게는 2 내지 10개의 아미노산을 포함할 수 있으나 이에 한정하는 것은 아니다.The peptide-based compound may include, for example, 2 to 1000, preferably 2 to 100, and more preferably 2 to 10 amino acids, but is not limited thereto.
상기 펩타이드계 화합물에서 펩타이드는 2 이상의 아미노산이 공유결합으로 연결된 물질로서, 세포막을 통해 흡수됨으로써 세포 및 조직에 생리활성을 나타내게 된다. 펩타이드의 구체적인 예로는, 커퍼펩타이드(copper peptide, GHK-Cu), 알라닌/히스티딘/라이신 폴리펩타이드 커퍼 에이치씨엘(alanine/histidine/lysine polypeptide copper HCl), 아세틸데카펩타이드-3, 아세틸올리고펩타이드-2 아마이드, 아세틸테트라펩타이드-2, 아세틸테트라펩타이드-3, 아세틸테트라펩타이드-5, 아세틸테트라펩타이드-9, 아세틸테트라펩타이드-11, 아세틸테트라펩타이드-15, 아세틸테트라펩타이드-17, 아세틸테트라펩타이드-22, 아세틸테트라펩타이드-40, 아세틸트라이펩타이드-1, 아세틸펜타펩타이드-1, 아세틸펜타펩타이드-55아마이드, 아세틸헥사펩타이드-1, 아세틸헥사펩타이드-8, 아세틸헥사펩타이드-22, 아세틸헥사펩타이드-30, 아세틸헥사펩타이드-37, 아세틸헥사펩타이드-38, 아세틸헥사펩타이드-39, 아세틸헥사펩타이드-49, 아세틸헥사펩타이드-51아마이드, 아세틸헵타펩타이드-4, 아세틸헵타펩타이드-9, 팔미토일테트라펩타이드-3, 팔미토일테트라펩타이드-7, 팔미토일펜타펩타이드-3, 팔미토일펜타펩타이드-4, 팔미토일펜타펩타이드-5, 팔미토일트리펩타이드-1, 팔미토일트리펩타이드-5, 팔미토일트리펩타이드-8, 팔미토일트리펩타이드-29, 팔미토일트리펩타이드-36, 팔미토일트리펩타이드-38, 팔미토일트리펩타이드-40, 팔미토일헥사펩타이드-12, 팔미토일헥사펩타이드-14, 팔미토일헥사펩타이드-15, 팔미토일헥사펩타이드-56, 팔미토일헵타펩타이드-5, 커퍼트리펩타이드-1, 올리고펩타이드-1, 올리고펩타이드-2, 올리고펩타이드-3, 올리고펩타이드-4, 올리고펩타이드-5, 올리고펩타이드-6, 올리고펩타이드-7, 올리고펩타이드-11, 올리고펩타이드-14, 올리고펩타이드-18, 올리고펩타이드-20, 올리고펩타이드-24, 올리고펩타이드-27, 올리고펩타이드-28, 올리고펩타이드-29, 올리고펩타이드-30, 올리고펩타이드-31, 올리고펩타이드-32, 올리고펩타이드-34, 올리고펩타이드-41, 올리고펩타이드-42, 올리고펩타이드-50, 올리고펩타이드-51, 올리고펩타이드-52, 올리고펩타이드-54, 올리고펩타이드-55, 올리고펩타이드-57, 올리고펩타이드-58, 올리고펩타이드-59, 올리고펩타이드-61, 올리고펩타이드-62, 올리고펩타이드-66, 올리고펩타이드-68, 올리고펩타이드-70, 올리고펩타이드-71, 올리고펩타이드-72, 올리고펩타이드-73, 올리고펩타이드-74, 올리고펩타이드-75, 올리고펩타이드-76, 올리고펩타이드-79, 올리고펩타이드-86, 올리고펩타이드-88, 올리고펩타이드-92, 알에이치-올리고펩타이드-1, 알에이치-올리고펩타이드-2, 알에이치-올리고펩타이드-4, 알에이치-올리고펩타이드-33, 트리펩타이드-1, 트리펩타이드-2, 트리펩타이드-3, 트리펩타이드-29, 트리펩타이드-31, 트리펩타이드-32, 트리펩타이드-47, 트리펩타이드-48, 트리펩타이드-56, 테트라펩타이드-3, 테트라펩타이드-4, 테트라펩타이드-7, 테트라펩타이드-14, 테트라펩타이드-21, 테트라펩타이드-26, 테트라펩타이드-30, 테트라펩타이드-32, 테트라펩타이드-42, 테트라펩타이드-44, 테트라펩타이드-51, 테트라펩타이드-56, 테트라펩타이드-57, 테트라펩타이드-58, 테트라펩타이드-59, 니코티노일헥사펩타이드-44, 니코티노일헥사펩타이드-45, 니코티노일헥사펩타이드-56, 니코티노일다이펩타이드-22, 니코티노일다이펩타이드-23, 니코티노일다이펩타이드-24, 니코티노일다이펩타이드-26, 니코티노일트라이펩타이드-1, 니코티노일트라이펩타이드-35, 니코티노일트라이펩타이드-47, 니코티노일트라이펩타이드-48, 니코티노일옥타펩타이드-9, 니코티노일펜타펩타이드-20, 니코티노일펜타펩타이드-33, 갈로일노나펩타이드-11, 갈로일테트라펩타이드-19, 갈로일트라이펩타이드-47, 갈로일트라이펩타이드-48, 갈로일트리펩타이드-35, 갈로일트리펩타이드-7, 갈로일펜타펩타이드-33, 갈로일헥사펩타이드-44, 디갈로일테트라펩타이드-19, 데카펩타이드-2, 데카펩타이드-4, 데카펩타이드-6, 데카펩타이드-10, 데카펩타이드-11, 데카펩타이드-12, 데카펩타이드-15, 데카펩타이드-16, 데카펩타이드-18, 데카펩타이드-19, 데카펩타이드-20, 데카펩타이드-23, 데카펩타이드-25, 데카펩타이드-28, 데카펩타이드-31, 레티노일트리펩타이드-1, 레티노일트리펩타이드-35, 레티노일펜타펩타이드-4, 망가니즈트리펩타이드-1, 메발로노일펜타펩타이드-37, 메발로노일펜타펩타이드-39, 메발로노일트리펩타이드-1, 메발로노일트리펩타이드-35, 메발로노일테트라펩타이드-36, 미리스토일테트라펩타이드-6, 미리스토일테트라펩타이드-8, 미리스토일테트라펩타이드-34, 미리스토일트라이펩타이드-31, 미리스토일펜타펩타이드-8, 미리스토일펜타펩타이드-9, 미리스토일펜타펩타이드-17, 바이오티노일테트라펩타이드-51, 바이오티노일트리펩타이드-1, 바이오티노일트리펩타이드-35, 바이오티노일펜타펩타이드-4, 발프로오일올리고펩타이드-33, 카페오일데카펩타이드-17, 카페오일올리고펩타이드-77, 카페오일트라이펩타이드-1, 카페오일트라이펩타이드-7, 카페오일트라이펩타이드-35, 카페오일펜타펩타이드-20, 카페오일펜타펩타이드-27, 카페오일헥사펩타이드-48, 카페오일헥사펩타이드-50, 카페오일헥사펩타이드-56, 카페오일헥사펩타이드-65, 카페오일헵타펩타이드-11, 에스에이치-폴리펩타이드-1, 에스에이치-폴리펩타이드-2, 에스에이치-폴리펩타이드-3, 에스에이치-폴리펩타이드-4, 에스에이치-폴리펩타이드-5, 에스에이치-폴리펩타이드-6, 에스에이치-폴리펩타이드-7, 에스에이치-폴리펩타이드-8, 에스에이치-폴리펩타이드-9, 에스에이치-폴리펩타이드-10, 에스에이치-폴리펩타이드-11, 에스에이치-폴리펩타이드-13, 에스에이치-폴리펩타이드-15, 에스에이치-폴리펩타이드-16, 에스에이치-폴리펩타이드-17, 에스에이치-폴리펩타이드-18, 에스에이치-폴리펩타이드-19, 에스에이치-폴리펩타이드-22, 에스에이치-폴리펩타이드-25, 에스에이치-폴리펩타이드-26, 에스에이치-폴리펩타이드-28, 에스에이치-폴리펩타이드-29, 에스에이치-폴리펩타이드-31, 에스에이치-폴리펩타이드-33, 에스에이치-폴리펩타이드-34, 에스에이치-폴리펩타이드-35, 에스에이치-폴리펩타이드-36, 에스에이치-폴리펩타이드-37, 에스에이치-폴리펩타이드-38, 에스에이치-폴리펩타이드-39, 에스에이치-폴리펩타이드-40, 에스에이치-폴리펩타이드-41, 에스에이치-폴리펩타이드-42, 에스에이치-폴리펩타이드-43, 에스에이치-폴리펩타이드-44,에스에이치-폴리펩타이드-45, 에스에이치-폴리펩타이드-46, 에스에이치-폴리펩타이드-50, 에스에이치-폴리펩타이드-53, 에스에이치-폴리펩타이드-54, 에스에이치-폴리펩타이드-55, 에스에이치-폴리펩타이드-56, 에스에이치-폴리펩타이드-58, 에스에이치-폴리펩타이드-59, 에스에이치-폴리펩타이드-60, 에스에이치-폴리펩타이드-62, 에스에이치-폴리펩타이드-64, 에스에이치-폴리펩타이드-66, 에스에이치-폴리펩타이드-70, 에스에이치-폴리펩타이드-71, 에스에이치-폴리펩타이드-74, 에스에이치-폴리펩타이드-78, 에스에이치-폴리펩타이드-81, 에스에이치-폴리펩타이드-85, 알에이치-폴리펩타이드-1, 알에이치-폴리펩타이드-2, 알에이치-폴리펩타이드-3, 알에이치-폴리펩타이드-4, 알에이치-폴리펩타이드-5, 알에이치-폴리펩타이드-6, 알에이치-폴리펩타이드-7, 알에이치-폴리펩타이드-8, 알에이치-폴리펩타이드-9, 알에이치-폴리펩타이드-10, 알에이치-폴리펩타이드-11, 알에이치-폴리펩타이드-13, 알에이치-폴리펩타이드-14, 알에이치-폴리펩타이드-15, 알에이치-폴리펩타이드-22, 알에이치-폴리펩타이드-26, 알에이치-폴리펩타이드-28, 알에이치-폴리펩타이드-33, 알에이치-폴리펩타이드-51, 알에이치-폴리펩타이드-53, 알에이치-폴리펩타이드-58, 알에이치-폴리펩타이드-59, 알에이치-폴리펩타이드-60, 알에이치-폴리펩타이드-62, 알에이치-폴리펩타이드-64, 알에이치-폴리펩타이드-66, 알에이치-폴리펩타이드-67, 노나펩타이드-1, 노나펩타이드-10, 노나펩타이드-11, 노나펩타이드-16, 노나펩타이드-18, 노나펩타이드-19, 귀리펩타이드, 대두폴리펩타이드, 다이펩타이드-1, 다이펩타이드-15, 밀펩타이드, 살리실로일옥타펩타이드-9, 살리실로일펜타펩타이드-33, 시키모일노나펩타이드-11, 시키모일펜타펩타이드-33, 시키모일헥사펩타이드-48, 아젤라오일옥타펩타이드-9, 아젤라오일트리펩타이드-1, 아젤라오일펜타펩타이드-37, 완두콩펩타이드, 우르솔로일테트라펩타이드-37, 우르솔로일트리펩타이드-1, 우르솔로일트리펩타이드-35, 우르솔로일펜타펩타이드-4, 치옥토일트리펩타이드-1, 치옥토일트리펩타이드-35, 치옥토일펜타펩타이드-4, 커퍼팔미토일헥타펩타이드-14, 카프로오일테트라펩타이드-3, 카프릴로일다이펩타이드-17, 카프릴로일헵타펩타이드-33, 퀴노일트리펩타이드-1, 퀴노일트리펩타이드-7, 퀴노일트리펩타이드-35, 코코일펜타펩타이드-9, 쿠마로일노나펩타이드-29, 쿠마로일디펩타이드-3, 펜타펩타이드-3, 펜타펩타이드-13, 펜타펩타이드-18, 펜타펩타이드-20, 펜타펩타이드-27, 펜타펩타이드-28, 펜타펩타이드-31, 펜타펩타이드-36, 펜타펩타이드-37, 펜타펩타이드-44, 펜타펩타이드-45, 펜타펩타이드-46, 펜타펩타이드-48, 펜타펩타이드-54, 펜타펩타이드-56, 펜타펩타이드-57, 헥사펩타이드-2, 헥사펩타이드-3, 헥사펩타이드-9, 헥사펩타이드-10, 헥사펩타이드-11, 헥사펩타이드-12, 헥사펩타이드-17, 헥사펩타이드-33, 헥사펩타이드-42, 헥사펩타이드-43, 헥사펩타이드-47, 헥사펩타이드-57, 헥사펩타이드-61, 헥사펩타이드-62, 헥사펩타이드-63, 헥사펩타이드-65, 헵타펩타이드-10, 헵타펩타이드-12, 헵타펩타이드-13, 헵타펩타이드-16, 헵타펩타이드-22, 헵타펩타이드-36, 헵타펩타이드-37, 헵타펩타이드-38, 헵타펩타이드-39, 헵타펩타이드-40, 효모폴리펩타이드, 페룰로일올리고펩타이드-33, 트라넥사모일다이펩타이드-22, 코질카복시다이펩타이드-23, 옥타펩타이드-2, 옥타펩타이드-7, 옥타펩타이드-8, 옥타펩타이드-10, 옥타펩타이드-11, 옥타펩타이드-15 등을 들 수 있으나, 이에 한정하는 것은 아니다.In the peptide-based compound, a peptide is a substance in which two or more amino acids are covalently linked, and is absorbed through a cell membrane, thereby exhibiting physiological activity in cells and tissues. Specific examples of the peptides include copper peptide (GHK-Cu), alanine/histidine/lysine polypeptide copper HCl, acetyldecapeptide-3, and acetyloligopeptide-2 amide , Acetyltetrapeptide-2, acetyltetrapeptide-3, acetyltetrapeptide-5, acetyltetrapeptide-9, acetyltetrapeptide-11, acetyltetrapeptide-15, acetyltetrapeptide-17, acetyltetrapeptide-22, acetyl Tetrapeptide-40, acetyltripeptide-1, acetylpentapeptide-1, acetylpentapeptide-55amide, acetylhexapeptide-1, acetylhexapeptide-8, acetylhexapeptide-22, acetylhexapeptide-30, acetylhexa Peptide-37, acetylhexapeptide-38, acetylhexapeptide-39, acetylhexapeptide-49, acetylhexapeptide-51amide, acetylheptapeptide-4, acetylheptapeptide-9, palmitoyltetrapeptide-3, palmitoyl Tetrapeptide-7, palmitoylpentapeptide-3, palmitoylpentapeptide-4, palmitoylpentapeptide-5, palmitoyltripeptide-1, palmitoyltripeptide-5, palmitoyltripeptide-8, palmitoyltri Peptide-29, palmitoyl tripeptide-36, palmitoyl tripeptide-38, palmitoyl tripeptide-40, palmitoylhexapeptide-12, palmitoylhexapeptide-14, palmitoylhexapeptide-15, palmitoylhexapeptide -56, palmitoyl hepta peptide-5, copper tripeptide-1, oligopeptide-1, oligopeptide-2, oligopeptide-3, oligopeptide-4, oligopeptide-5, oligopeptide-6, oligopeptide-7 , Oligopeptide-11, oligopeptide-14, oligopeptide-18, oligopeptide-20, oligopeptide-24, oligopeptide-27, oligopeptide-28, oligopeptide-29, oligopeptide-30, oligopeptide-31 , Oligopeptide-32, oligopeptide-34, oligopeptide-41, oligopeptide-42, oligopeptide DE-50, oligopeptide-51, oligopeptide-52, oligopeptide-54, oligopeptide-55, oligopeptide-57, oligopeptide-58, oligopeptide-59, oligopeptide-61, oligopeptide-62, oligo Peptide-66, oligopeptide-68, oligopeptide-70, oligopeptide-71, oligopeptide-72, oligopeptide-73, oligopeptide-74, oligopeptide-75, oligopeptide-76, oligopeptide-79, oligo Peptide-86, oligopeptide-88, oligopeptide-92, R-oligopeptide-1, R-oligopeptide-2, R-oligopeptide-4, R-oligopeptide-33, tripeptide-1 , Tripeptide-2, tripeptide-3, tripeptide-29, tripeptide-31, tripeptide-32, tripeptide-47, tripeptide-48, tripeptide-56, tetrapeptide-3, tetrapeptide-4 , Tetrapeptide-7, tetrapeptide-14, tetrapeptide-21, tetrapeptide-26, tetrapeptide-30, tetrapeptide-32, tetrapeptide-42, tetrapeptide-44, tetrapeptide-51, tetrapeptide-56 , Tetrapeptide-57, tetrapeptide-58, tetrapeptide-59, nicotinoyl hexapeptide-44, nicotinoyl hexapeptide-45, nicotinoyl hexapeptide-56, nicotinoyl dipeptide-22, nicotino One dipeptide-23, nicotinoyl dipeptide-24, nicotinoyl dipeptide-26, nicotinoyl tripeptide-1, nicotinoyl tripeptide-35, nicotinoyl tripeptide-47, nicotinoyl tripeptide Peptide-48, Nicotinoyloctapeptide-9, Nicotinoylpentapeptide-20, Nicotinoylpentapeptide-33, Galoylnonapeptide-11, Galoyltetrapeptide-19, Galoyltripeptide-47, Gallo Iltripeptide-48, Galoyltripeptide-35, Galoyltripeptide-7, Galoylpentapeptide-33, Galoylhexapeptide-44, Digaloyltetrapeptide-19, Decapeptide-2, Decapeptide- 4, decapeptide-6, decapeptide -10, decapeptide-11, decapeptide-12, decapeptide-15, decapeptide-16, decapeptide-18, decapeptide-19, decapeptide-20, decapeptide-23, decapeptide-25, decapeptide -28, decapeptide-31, retinoyl tripeptide-1, retinoyl tripeptide-35, retinoylpentapeptide-4, manganese tripeptide-1, mevalonoylpentapeptide-37, mevalonoylpentapeptide- 39, mevalonoyl tripeptide-1, mevalonoyl tripeptide-35, mevalonoyl tetrapeptide-36, myristoyltetrapeptide-6, myristoyltetrapeptide-8, myristoyltetrapeptide-34, Myristoyl tripeptide-31, myristoylpentapeptide-8, myristoylpentapeptide-9, myristoylpentapeptide-17, biotinoyl tetrapeptide-51, biotinoyl tripeptide-1, biotino Iltripeptide-35, biotinoyl pentapeptide-4, valpro oil oligopeptide-33, cafe oil decapeptide-17, cafe oil oligopeptide-77, cafe oil tripeptide-1, cafe oil tripeptide-7, Cafe oil tripeptide-35, cafe oil pentapeptide-20, cafe oil pentapeptide-27, cafe oil hexapeptide-48, cafe oil hexapeptide-50, cafe oil hexapeptide-56, cafe oil hexapeptide-65, cafe Oil Heptapeptide-11, S-polypeptide-1, S-polypeptide-2, S-polypeptide-3, S-polypeptide-4, S-polypeptide-5, S-polypeptide-6, S- Polypeptide-7, S-polypeptide-8, S-polypeptide-9, S-polypeptide-10, S-polypeptide-11, S-polypeptide-13, S-polypeptide-15, S-poly Peptide-16, S-polypeptide-17, S-polypeptide-18, S-polypeptide-19, S-polypeptide-22, S-polypeptide-25, S-polypeptide-26, S-polypeptide -28, S-Polypeptide D-29, S-polypeptide-31, S-polypeptide-33, S-polypeptide-34, S-polypeptide-35, S-polypeptide-36, S-polypeptide-37, S-polypeptide -38, S-polypeptide-39, S-polypeptide-40, S-polypeptide-41, S-polypeptide-42, S-polypeptide-43, S-polypeptide-44,S-polypeptide- 45, S-polypeptide-46, S-polypeptide-50, S-polypeptide-53, S-polypeptide-54, S-polypeptide-55, S-polypeptide-56, S-polypeptide-58 , S-polypeptide-59, S-polypeptide-60, S-polypeptide-62, S-polypeptide-64, S-polypeptide-66, S-polypeptide-70, S-polypeptide-71, S-polypeptide-74, S-polypeptide-78, S-polypeptide-81, S-polypeptide-85, R-polypeptide-1, R-polypeptide-2, R-polypeptide- 3, R-polypeptide-4, R-polypeptide-5, R-polypeptide-6, R-polypeptide-7, R-polypeptide-8, R-polypeptide-9, R-polypeptide-10, R-polypeptide-11, R-polypeptide-13, R-polypeptide-14, R-polypeptide-15, R-polypeptide-22, R-H -Polypeptide-26, R-polypeptide-28, R-polypeptide-33, R-polypeptide-51, R-polypeptide-53, R-poly-peptide-58, R-poly Peptide-59, R-polypeptide-60, R-polypeptide-62, R-polypeptide-64, R-polypeptide-66, R-polypeptide-67, nonapeptide-1, nona Peptide-10, Nonapeptide- 11, nonapeptide-16, nonapeptide-18, nonapeptide-19, oat peptide, soybean polypeptide, dipeptide-1, dipeptide-15, wheat peptide, salicyloyl octapeptide-9, salicyloyl pentapeptide -33, Shikimoyl nonapeptide-11, Shikimoyl pentapeptide-33, Shikimoyl hexapeptide-48, Azela oil octapeptide-9, Azela oil tripeptide-1, Azela oil pentapeptide-37, Pea peptide, Ursolo Iltetrapeptide-37, ursoloyl tripeptide-1, ursoloyl tripeptide-35, ursoloyl pentapeptide-4, thiotoyl tripeptide-1, thiotoyl tripeptide-35, thiotoyl penta Peptide-4, Copper Palmitoyl Hepteptide-14, Caproyl Tetrapeptide-3, Capryloyl Dipeptide-17, Capryloyl Heptapeptide-33, Quinoyl Tripeptide-1, Quinoyl Tripeptide-7, Qui Noyl tripeptide-35, cocoyl pentapeptide-9, couromayl nonapeptide-29, couromayl dipeptide-3, pentapeptide-3, pentapeptide-13, pentapeptide-18, pentapeptide-20, pentapeptide -27, pentapeptide-28, pentapeptide-31, pentapeptide-36, pentapeptide-37, pentapeptide-44, pentapeptide-45, pentapeptide-46, pentapeptide-48, pentapeptide-54, pentapeptide -56, pentapeptide-57, hexapeptide-2, hexapeptide-3, hexapeptide-9, hexapeptide-10, hexapeptide-11, hexapeptide-12, hexapeptide-17, hexapeptide-33, hexapeptide -42, hexapeptide-43, hexapeptide-47, hexapeptide-57, hexapeptide-61, hexapeptide-62, hexapeptide-63, hexapeptide-65, heptapeptide-10, heptapeptide-12, heptapeptide -13, heptapeptide-16, heptapeptide-22, heptapeptide-36, heptapeptide-37, heptapeptide-38, heptapeptide-39, heptapeptide-40, yeast polypeptide, feruloyl oligopeptide-33, Tranexamoyl dipeptide-22, cozylcarboxydipeptide-23, octapeptide-2, octapeptide- 7, octapeptide-8, octapeptide-10, octapeptide-11, octapeptide-15, and the like, but are not limited thereto.
또한 상기 생리활성물질은 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 수용액 내에서 양 또는 음의 전하를 가질 수 있다.In addition, the bioactive material is not limited as long as it does not inhibit the object of the present invention, but may have a positive or negative charge in an aqueous solution.
수용액 내에서 양의 전하를 갖는 양이온성 펩타이드는 양이온성 아미노산을 다수 포함하고 있어, 펩타이드의 pKa가 5 이상, 구체적으로 6 이상, 더욱 구체적으로 8 이상인 펩타이드를 의미할 수 있다. 보다 구체적으로, 상기 양의 전하는 pH 7의 중성 수용액에서 측정된 것을 의미한다. 상기 양이온성 펩타이드는 바람직하게 H, K, R을 펩타이드 서열에서 다수 포함하는 것일 수 있다. 바람직하게 상기 양이온성 펩타이드는 H, K 및 R으로 이루어지는 군에서 선택되는 아미노산을 2 이상 포함하는 것일 수 있으며 양이온성 펩타이드를 구성하는 1차 서열 중 양이온성 아미노산의 비율이 20% 이상, 바람직하게 30%, 보다 바람직하게 50% 이상일 수 있다.A cationic peptide having a positive charge in an aqueous solution contains a large number of cationic amino acids, and may refer to a peptide having a pKa of 5 or more, specifically 6 or more, and more specifically 8 or more. More specifically, the amount of the charge means that measured in a neutral aqueous solution of pH 7. The cationic peptide may preferably include a large number of H, K, R in the peptide sequence. Preferably, the cationic peptide may include two or more amino acids selected from the group consisting of H, K and R, and the proportion of cationic amino acids in the primary sequence constituting the cationic peptide is 20% or more, preferably 30 %, more preferably 50% or more.
수용액 내에서 음의 전하를 갖는 음이온성 펩타이드는 음이온성 아미노산을 다수 포함하고 있어, 펩타이드의 pKa가 5 이하, 구체적으로 4 이하인 펩타이드를 의미할 수 있다. 보다 구체적으로, 상기 음의 전하는 pH 7의 중성 수용액에서 측정된 것을 의미한다. 상기 음이온성 펩타이드는 바람직하게 D 및 E를 펩타이드 서열에서 다수 포함하는 것일 수 있다. 바람직하게 상기 음이온성 펩타이드는 D 및 E으로 이루어지는 군에서 선택되는 아미노산을 2 이상 포함하는 것일 수 있으며, 음이온성 펩타이드를 구성하는 1차 서열 중 음이온성 아미노산의 비율이 20% 이상, 바람직하게 30%, 보다 바람직하게 50% 이상일 수 있다.The anionic peptide having a negative charge in the aqueous solution contains a large number of anionic amino acids, and may mean a peptide having a pKa of 5 or less, specifically 4 or less. More specifically, the negative charge means measured in a neutral aqueous solution of pH 7. The anionic peptide may preferably include a plurality of D and E in the peptide sequence. Preferably, the anionic peptide may include two or more amino acids selected from the group consisting of D and E, and the proportion of anionic amino acids in the primary sequence constituting the anionic peptide is 20% or more, preferably 30%. , More preferably 50% or more.
상기 친수성 고분자는 중량평균분자량 10,000 이상, 구체적으로 50,000 이상, 보다 구체적으로 100,000 이상 5,000,000 이하일 수 있으나 이에 제한받지 않는다.The hydrophilic polymer may have a weight average molecular weight of 10,000 or more, specifically 50,000 or more, and more specifically 100,000 or more and 5,000,000 or less.
상기 친수성 고분자는 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 음이온성 또는 양이온성 고분자를 포함하며, 상리 생리물질과 상이한 전하를 가지는 것일 수 있다.The hydrophilic polymer is not limited as long as it does not inhibit the object of the present invention, but includes an anionic or cationic polymer, and may have a different charge from a physiological substance.
상기 음이온성 고분자에 포함되는 음이온기의 종류로는 일예로 카르복실기, 술폰산기, 황산에스테르기, 인산기 등을 들 수 있으나, 이에 한정하는 것은 아니다. 상기 음이온성 고분자는 합성 고분자, 당류계 고분자, 폴리아미노산계 고분자 및 그 유도체일 수 있다. 음이온성 고분자의 구체적인 일 예로 폴리글루탐산(Polyglutamic acid), 폴리아크릴산(Polyacrylic acid), 카보머(Carbomer), 알긴산(Alginate), 카라기난(Carrageenan), 히알루론산(Hyaluronic acid), 폴리스타이렌술폰산염(Poly(styrene sulfonate)), 카복시메틸셀룰로스(Carboxymethylcellulose), 셀룰로오스황산염(Cellulose sulfate), 덱스트란황산염(Dextran sulfate), 헤파린(Heparin), 펙틴, 헤파린황산염(Heparin sulfate), 폴리메틸렌코구아니딘(Poly(methylene-co-guanidine)) 및 콘드로이틴황산염(Condroitin sulfate)으로 구성된 군에서 선택될 수 있으나 이에 한정하는 것은 아니다.Examples of the types of anionic groups included in the anionic polymer include, but are not limited to, carboxyl groups, sulfonic acid groups, sulfate ester groups, phosphoric acid groups, and the like. The anionic polymer may be a synthetic polymer, a saccharide polymer, a polyamino acid polymer, and derivatives thereof. Specific examples of anionic polymers include polyglutamic acid, polyacrylic acid, carbomer, alginate, carrageenan, hyaluronic acid, polystyrene sulfonate styrene sulfonate), carboxymethylcellulose, Cellulose sulfate, Dextran sulfate, Heparin, Pectin, Heparin sulfate, Polymethylenecoguanidine (Poly(methylene- co-guanidine)) and chondroitin sulfate, but is not limited thereto.
상기 양이온성 고분자에 포함되는 양이온기의 종류로는 일예로 1차 아미노기, 2차 아미노기, 3차 아미노기, 설포늄기 또는 포스포늄기 등을 들 수 있으나, 이에 한정하는 것은 아니다. 상기 양이온성 고분자는 합성 고분자, 당류계 고분자, 폴리아미노산계 고분자 및 그 유도체일 수 있다. 양이온성 고분자의 구체적인 일 예로 폴리에틸렌이민, 폴리라이신, 폴리히스티딘, 폴리아르기닌, Polyquaternium-10 및 키토산으로 구성된 군에서 선택될 수 있으나 이에 한정하는 것은 아니다.Examples of cationic groups included in the cationic polymer include primary amino groups, secondary amino groups, tertiary amino groups, sulfonium groups or phosphonium groups, but are not limited thereto. The cationic polymer may be a synthetic polymer, a saccharide polymer, a polyamino acid polymer, and derivatives thereof. Specific examples of the cationic polymer may be selected from the group consisting of polyethyleneimine, polylysine, polyhistidine, polyarginine, Polyquaternium-10 and chitosan, but is not limited thereto.
상기 친수성 고분자 복합체 수용액은 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 하이드로겔(hydrogel) 특성을 나타낼 수 있다. 하이드로겔은 수화겔이라고도 하며, 수용성 고분자가 수소결합, 반데르 발스 힘, 소수성 상호작용 또는 고분자의 결정 또는 화학적 공유결합에 의해 고점성을 가진 수화된 중합체를 의미하며, 수상에서 상당한 양의 수분을 함유할 수 있는 특성을 갖는다. 상기 하이드로겔은 상술한 바와 같은 다양한 음이온성 또는 양이온성 고분자로부터 생성될 수 있으며, 여러 가지 화학적 조성을 가질 수 있으며 공중합체 또는 치환된 유도체의 구조를 가질 수도 있다.The aqueous hydrophilic polymer composite solution is not limited as long as it does not inhibit the object of the present invention, but may exhibit hydrogel properties. Hydrogel, also called hydrogel, refers to a hydrated polymer in which the water-soluble polymer is highly viscous by hydrogen bonding, van der Waals forces, hydrophobic interactions, or crystal or chemical covalent bonding of the polymer, and contains a significant amount of water in the water phase It has the ability to do it. The hydrogel may be produced from various anionic or cationic polymers as described above, may have various chemical compositions and may also have a structure of a copolymer or a substituted derivative.
보다 구체적으로, 생리활성물질로 양이온성 펩타이드가 선택되고 친수성 고분자로서 음이온성 고분자가 선택될 경우 상기 음이온성 고분자와 양이온성 펩타이드는 이온 복합체(ionic complex)를 형성할 수 있으며, 양이온성 펩타이드가 음이온성 고분자에 의해 안정적으로 수상에서 복합체의 형태로 존재할 수 있다. 바람직하게, 양이온성 펩타이드가 2 이상의 양이온성 잔기를 포함할 경우 음이온성 고분자의 음이온기와 2 이상의 이온 결합을 형성함으로써 물리적 가교점을 형성할 수 있어 수상에 포함되어 있는 음이온성 고분자와 양이온성 펩타이드는 보다 고점성의 하이드로겔 특성을 나타낼 수 있다. 마찬가지로 생리활성물질로 음이온성 펩타이드가 선택되고 친수성 고분자로서 양이온성 고분자가 선택될 경우 상기 양이온성 고분자와 음이온성 펩타이드는 이온 복합체(ionic complex)를 형성할 수 있으며, 음이온성 펩타이드가 양이온성 고분자에 의해 안정적으로 수상에서 복합체의 형태로 존재할 수 있다. 바람직하게, 음이온성 펩타이드가 2 이상의 음이온성 잔기를 포함할 경우 양이온성 고분자의 양이온기와 2 이상의 이온 결합을 형성함으로써 물리적 가교점을 형성할 수 있어 수상에 포함되어 있는 양이온성 고분자와 음이온성 펩타이드는 보다 고점성의 하이드로겔 특성을 나타낼 수 있다.More specifically, when a cationic peptide is selected as a bioactive material and an anionic polymer is selected as a hydrophilic polymer, the anionic polymer and the cationic peptide can form an ionic complex, and the cationic peptide is anionic It can stably exist in the form of a complex in the aqueous phase by the sex polymer. Preferably, when the cationic peptide contains two or more cationic residues, the physical cross-linking point can be formed by forming two or more ionic bonds with the anionic group of the anionic polymer, so that the anionic polymer and cationic peptide included in the aqueous phase are It can exhibit more viscous hydrogel properties. Similarly, when an anionic peptide is selected as a bioactive material and a cationic polymer is selected as a hydrophilic polymer, the cationic polymer and anionic peptide may form an ionic complex, and the anionic peptide is added to the cationic polymer. It can stably exist in the form of a complex in the aqueous phase. Preferably, when the anionic peptide contains two or more anionic residues, a physical crosslinking point can be formed by forming two or more ionic bonds with the cationic polymer's cationic polymer, so that the cationic polymer and anionic peptide included in the aqueous phase are It can exhibit more viscous hydrogel properties.
양이온성 펩타이드의 양이온 잔기의 총 몰수는 음이온성 고분자의 음이온 잔기의 총 몰수 대비 동일하거나 더 많을 수 있으며, 바람직하게는 상기 양이온 잔기의 총 몰수가 상기 음이온 잔기의 몰수보다 더 많은 것이 좋을 수 있고, 비한정적인 일 예로 10 내지 100배 더 많을 수 있다. 마찬가지로 음이온성 펩타이드의 음이온 잔기의 총 몰수와 양이온성 고분자의 양이온 잔기의 총 몰수에 대한 관계는 앞서와 동일하므로 상세한 설명은 생략한다.The total number of moles of cation residues of the cationic peptide may be the same or more than the total number of moles of anion residues of the anionic polymer, preferably, the total number of moles of the cation residues may be greater than the number of moles of the anion residues, As a non-limiting example, it may be 10 to 100 times more. Similarly, since the relationship between the total number of moles of anionic residues of anionic peptides and the total number of moles of cationic residues of cationic polymers is the same as above, detailed descriptions are omitted.
상기 친수성 고분자 복합체 수용액의 제조시 용매인 물에 대해 생리활성물질은 0.01 중량% 내지 50 중량%, 구체적으로 0.1 중량% 내지 20 중량%, 보다 구체적으로 0.5 중량% 내지 10 중량%의 범위로 포함될 수 있다. 또한 용매인 물에 대해 친수성 고분자는 0.0001 중량% 내지 1 중량%, 구체적으로 0.001 중량% 내지 0.1 중량%, 보다 구체적으로 0.005 중량% 내지 0.05 중량%,일 수 있으나 이에 제한받지 않는다.When preparing the aqueous solution of the hydrophilic polymer composite, the bioactive substance with respect to water as a solvent may be included in a range of 0.01% to 50% by weight, specifically 0.1% to 20% by weight, and more specifically 0.5% to 10% by weight. have. In addition, the hydrophilic polymer with respect to water as a solvent may be 0.0001 wt% to 1 wt%, specifically 0.001 wt% to 0.1 wt%, more specifically 0.005 wt% to 0.05 wt%, but is not limited thereto.
상술한 바와 같은 함량범위로 물, 생리활성물질 및 친수성 고분자를 포함하는 친수성 고분자 복합체 수용액을 생성한 후, 상기 친수성 고분자 복합체 수용액은 인지질 용액에 투입되어 콜로이드 용액을 생성한다.After producing an aqueous hydrophilic polymer composite solution containing water, a physiologically active substance and a hydrophilic polymer in the content range as described above, the aqueous hydrophilic polymer composite aqueous solution is introduced into a phospholipid solution to produce a colloidal solution.
상기 콜로이드 용액을 생성하는 단계에서, 상기 하이드로겔 특성을 나타내는 친수성 고분자복합체 수용액을 인지질 용액에 투입함으로써, 상기 인지질 용액이 친수성 고분자 복합체 수용액에 수화되어 수화 액정상을 형성할 수 있다.In the step of generating the colloidal solution, the aqueous solution of the hydrophilic polymer complex exhibiting the hydrogel characteristic is introduced into the phospholipid solution, whereby the phospholipid solution can be hydrated in the aqueous solution of the hydrophilic polymer complex to form a hydrated liquid crystal phase.
상기 인지질은 천연 인지질 및 합성 지질에서 선택될 수 있다. 천연 인지질은 난황 레시틴 (포스파티딜콜린), 대두 레시틴, 수첨 레시틴(hydrogenated lecithin), 리조레시틴 (Lysolecithin), 스핑고마이엘린 (Sphingomyelin), 포스파티딘산, 포스파티딜세린, 포스파티딜 글리세롤, 포스파티딜이노시톨, 포스파티딜에탄올아민, 디포스파티딜글리세롤, 카르디오리핀 (Cardiolipin) 및 플라즈마로겐으로 구성된 군에서 선택된 적어도 하나의 물질일 수 있으며, 합성 지질은 디세틸포스페이트, 디스테아로일포스파티딜콜린, 디올레오일포스파티딜에탄올아민, 디팔미토일포스파티딜콜린, 디팔미토일포스파티딜에탄올아민, 디팔미토일포스파티딜세린, 엘레오스테아로일포스파티딜콜린, 엘레오스테아로일포스파티딜에탄올아민 및 엘레오스테아로일포스파티딜세린으로 구성된 군에서 선택된 적어도 하나의 물질일 수 있으나, 이에 한정하는 것은 아니다.The phospholipid can be selected from natural phospholipids and synthetic lipids. Natural phospholipids are egg yolk lecithin (phosphatidylcholine), soybean lecithin, hydrogenated lecithin, lysolecithin, sphingomyelin, phosphatidic acid, phosphatidylserine, phosphatidyl glycerol, phosphatidyl inositol, phosphatidyl inositol, phosphatidyl inositol, Diphosphatidylglycerol, cardiolipin (Cardiolipin) and may be at least one substance selected from the group consisting of plasma, synthetic lipids are disetyl phosphate, distearoylphosphatidylcholine, dioleoyl phosphatidylethanolamine, dipalmitoyl Phosphatidylcholine, dipalmitoylphosphatidylethanolamine, dipalmitoylphosphatidylserine, eleostearoylphosphatidylcholine, eleostearoylphosphatidylethanolamine and eleostearoylphosphatidylserine, but may be at least one substance selected from the group consisting of It is not done.
상기 인지질 용액의 용매는 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 알코올을 포함할 수 있으며, 본 발명에서 상기 알코올은 탄소수 1 내지 4의 저급 알코올로부터 선택될 수 있으나 이에 한정하는 것은 아니다. 상기 저급 알코올의 일예로, 메탄올, 에탄올, 프로판올, 부탄올 등일 수 있으며, 보다 바람직하게 에탄올이 선택될 수 있다. 저급 알코올을 선택함으로써 피부의 지질막을 유연하게 하고, 나노지질전달체의 흡수율을 증진할 수 있어 바람직하다.The solvent of the phospholipid solution is not limited as long as it does not impair the object of the present invention, but may include alcohol, and in the present invention, the alcohol may be selected from lower alcohols having 1 to 4 carbon atoms, but is not limited thereto. As an example of the lower alcohol, methanol, ethanol, propanol, butanol, and the like, more preferably, ethanol may be selected. It is preferable to select a lower alcohol to soften the lipid film of the skin and enhance the absorption rate of the nanolipid transporter.
상기 인지질 용액의 용매인 알코올에 대해 인지질은 0.1 중량% 내지 50 중량%, 구체적으로 1 중량% 내지 40 중량%, 보다 구체적으로 10 중량% 내지 30 중량%의 범위로 포함될 수 있다.The phospholipid may be included in a range of 0.1% to 50% by weight, specifically 1% to 40% by weight, and more specifically 10% to 30% by weight with respect to alcohol as a solvent of the phospholipid solution.
상기 인지질 용액과 친수성 고분자 복합체 수용액은 중량비로 1:0.1 내지 1:10 일 수 있으며, 구체적으로 1:0.2 내지 1:5, 보다 구체적으로 1:0.5 내지 1:2의 범위로 포함될 수 있다. 바람직하게는 인지질 용액과 친수성 고분자 복합체 수용액을 중량비로 1:0.9 내지 1:1로 혼합하는 것일 수 있다. 상기 중량 혼합비에서 친수성 고분자 복합체 수용액에 포함되어 있던 물에 의해 인지질이 수화되어 수화액정상을 바람직하게 형성할 수 있다.The phospholipid solution and the aqueous solution of the hydrophilic polymer composite may be 1:0.1 to 1:10 by weight, specifically 1:0.2 to 1:5, and more specifically 1:0.5 to 1:2. Preferably, the phospholipid solution and the hydrophilic polymer composite aqueous solution may be mixed in a weight ratio of 1:0.9 to 1:1. Phospholipids are hydrated by the water contained in the hydrophilic polymer composite aqueous solution at the above weight mixing ratio to form a hydrated liquid phase.
구체적으로 예를 들어, 상기 인지질 에탄올 용액과 친수성 고분자 복합체 수용액이 혼합됨에 따라 인지질 용액에 포함되어 있는 에탄올과 친수성 고분자 복합체 수용액에 포함되어 있는 물이 서로 혼합된다. 상기 인지질 용액에서 인지질은 에탄올 용매 내에 균일한 용액을 형성하고 있지만 물과 혼합됨에 따라 점차 수화되고 액정상을 형성하여 에토좀 콜로이드의 구조를 형성할 수 있다.Specifically, for example, as the phospholipid ethanol solution and the hydrophilic polymer composite aqueous solution are mixed, the ethanol contained in the phospholipid solution and the water contained in the hydrophilic polymer composite aqueous solution are mixed with each other. In the phospholipid solution, the phospholipid forms a uniform solution in an ethanol solvent, but gradually mixes with water to form a liquid crystal phase to form a structure of an ethosome colloid.
상기 에토좀은 리포좀보다 피부 흡수 효과를 높이기 위한 약물전달체로서 리포좀보다 막을 좀 더 유연하게 변형이 쉬운 상태로 각질세포 사이의 좁은 틈을 더 잘 통과할 수 있으며, 피부 투과 증진제의 역할을 할 수 있는 에탄올에 인지질을 용해시켜 제조된다. 상기 에탄올은 지질의 극성 머리 부분과 작용하여 계면장력을 감소시킴으로써, 각질층 안에 존재하는 지질 막의 계면장력을 감소시키며, 베지클 자체의 막을 유연하게 만들 수 있다. 이로부터 에토좀은 피부 내부로 생리활성물질을 더욱 효과적으로 피부 장벽을 통과하여 전달할 수 있어 바람직하다.The ethosome is a drug delivery system for enhancing the skin absorption effect than the liposome, and can more easily pass through a narrow gap between keratinocytes with a more flexible and easily deformable membrane than the liposome, and can act as a skin penetration enhancer. It is prepared by dissolving phospholipids in ethanol. The ethanol acts with the polar head portion of the lipid to reduce the interfacial tension, thereby reducing the interfacial tension of the lipid membrane present in the stratum corneum and making the membrane of the vesicle itself flexible. Etosome from this is preferable because it can deliver the bioactive substance through the skin barrier more effectively into the skin.
상기 친수성 복합체 수용액을 인지질 용액에 투입하여 콜로이드 용액이 생성된 후, 상기 콜로이드 용액은 지질에 투입되어 유중수(water-in-oil) 분산액을 생성할 수 있다.After the colloidal solution is generated by injecting the aqueous hydrophilic complex solution into a phospholipid solution, the colloidal solution may be introduced into a lipid to generate a water-in-oil dispersion.
상기 지질에 상기 콜로이드 용액을 투입하여 유중수 분산액을 생성하는 단계에서, 상기 지질은 물과 혼화성이 없는 지방족 탄화수소를 포함하는 화합물일 수 있으며, 상기 콜로이드 용액을 지질에 투입하여, 지질이 연속상을 형성하고 상기 콜로이드 용액이 분산상을 형성하는 유중수 분산액을 생성한다. 보다 구체적으로 상기 지질은 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 서로 다른 융점을 가지는 2 이상의 지질을 포함하는 지질 혼합액일 수 있으나 이에 한정하는 것은 아니다.In the step of generating the water-in-oil dispersion by adding the colloidal solution to the lipid, the lipid may be a compound containing an aliphatic hydrocarbon that is not miscible with water, and the colloidal solution is introduced into the lipid, so that the lipid is a continuous phase. And a water-in-oil dispersion in which the colloidal solution forms a dispersed phase. More specifically, the lipid is not limited as long as it does not inhibit the object of the present invention, but may be a lipid mixed solution containing two or more lipids having different melting points, but is not limited thereto.
상기 지질 혼합액은 상온에서 고상인 제1지질 및 상온에서 액상인 제2지질을 포함할 수 있으며, 상온에서 고상인 제1지질의 일예로는 Apifil(PEG-8 Beeswax), Beeswax, Carnauba wax 2442 L(Copernicia Cerifera wax), Compritol ATO(Glyceryl Behenate), Cutina CP(Cetyl Palmitate), Dynasan(Trimyristin), 글리세릴스테아레이트, 글리세릴스테아레이트/말레이트, 글리세릴스테아레이트/아세테이트, 스테아릭에씨드, 세틸팔미테이트, 트리스테아린 등에서 선택된 적어도 하나의 물질일 수 있으나 이에 한정하는 것은 아니다, 상온에서 액상인 제2지질의 일예로는 카프릴릭/카프릴트라이글리세라이드, 파라핀 오일, 올레익에씨드, 스쿠아렌, 옥틸도데칸올, 아이소프로필미리스테이트, 토코페롤, 에톡시다이글라이콜, 디세틸포스페이트으로구성된 군에서 선택된 적어도 하나의 물질일 수 있으나 이에 한정하는 것은 아니다.The lipid mixture may include a first lipid that is solid at room temperature and a second lipid that is liquid at room temperature. Examples of the first lipid that is solid at room temperature include Apifil (PEG-8 Beeswax), Beeswax, and Carnauba wax 2442 L (Copernicia Cerifera wax), Compritol ATO (Glyceryl Behenate), Cutina CP (Cetyl Palmitate), Dynasan (Trimyristin), Glyceryl stearate, Glyceryl stearate/maleate, Glyceryl stearate/acetate, Stearic acid, It may be at least one substance selected from cetyl palmitate, tristearin, and the like, but is not limited thereto. Examples of the second lipid that is liquid at room temperature include caprylic/capryl triglyceride, paraffin oil, oleic acid, It may be at least one material selected from the group consisting of squaene, octyldodecanol, isopropyl myristate, tocopherol, ethoxydiglycol, and dicetyl phosphate, but is not limited thereto.
상기 고상인 제1지질과 액상인 제2지질의 혼합 비율은 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 1:0.05 내지 1:20, 구체적으로 1:0.1 내지 1:10, 더욱 구체적으로 1:0.5 내지 1:5의 중량비로 혼합될 수 있다. 바람직하게는 고상인 제1지질과 액상지질의 혼합 비율은 1:0.8 내지 1:1.2의 중량비일 수 있으며, 상기 범위에서 나노지질전달체의 코어부가 안정적으로 형성될 수 있어 바람직하다.The mixing ratio of the first lipid in the solid phase and the second lipid in the liquid phase is not limited as long as it does not impair the object of the present invention, but is 1:0.05 to 1:20, specifically 1:0.1 to 1:10, and more specifically 1 It can be mixed in a weight ratio of :0.5 to 1:5. Preferably, the mixing ratio of the solid first lipid and the liquid lipid may be a weight ratio of 1:0.8 to 1:1.2, and the core portion of the nanolipid transporter can be stably formed in the above range, which is preferable.
상온에서 고상인 제1지질과 상온에서 액상인 제2지질이 혼합된 지질 혼합액을 유상으로 포함함에 따라 균질화시 높은 에너지를 가하지 않고서도 작은 입경의 나노지질전달체를 형성할 수 있으며 코어부가 쉘부 내에 보다 안정적으로 봉입될 수 있다. 또한, 코어부에 해당하는 생리활성물질 및 친수성 고분자를 함유하는 친수성 고분자 복합체와 쉘부에 해당하는 지질 혼합액이 유동성 있는 오일-물 계면을 형성하며, 인지질에 의한 수화 액정상이 상기 오일-물 계면에 배치되어 계면을 매우 효과적으로 안정화시킬 수 있다. 고상의 지질만 사용하는 경우 유동성 있는 오일-물 계면을 형성하기보다 상온에서 소수성 고체-물 계면을 형성하기 때문에 인지질에 의한 수화 액정상이 상기 소수성 고체-물 계면에 존재하더라도 계면의 안정화 효과는 다소 떨어질 수 있다.As the lipid mixture containing the first lipid, which is solid at room temperature and the second lipid, which is liquid at room temperature, is included as an oil phase, a nano-lipid transporter having a small particle size can be formed without adding high energy during homogenization. It can be stably sealed. In addition, a hydrophilic polymer composite containing a physiologically active substance corresponding to the core portion and a hydrophilic polymer and a lipid mixture liquid corresponding to the shell portion form a fluid oil-water interface, and a hydrated liquid crystal phase by phospholipids is disposed at the oil-water interface. It can stabilize the interface very effectively. When only solid lipids are used, the hydrophobic solid-water interface is formed at room temperature rather than forming a fluid oil-water interface, so even if the hydrated liquid crystal phase by phospholipids is present at the hydrophobic solid-water interface, the stabilization effect of the interface is somewhat inferior. Can be.
상기 지질과 상기 콜로이드 용액은 중량비로 1:1 내지 1:0.01일 수 있으며, 구체적으로 1:0.8 내지 1:0.1, 보다 구체적으로 1:0.7 내지 1:0.3의 범위로 포함될 수 있으나 이에 제한받지 않는다.The lipid and the colloidal solution may be 1:1 to 1:0.01 by weight, specifically 1:0.8 to 1:0.1, and more specifically 1:0.7 to 1:0.3, but are not limited thereto. .
상기 유중수 분산액은 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 지질을 가온하여 용액상을 형성한 후 상기 콜로이드 용액을 혼합하여 제조될 수 있다. 상기 지질 가온시 온도는 지질의 종류, 분자량, 함량 등에 따라 선택될 수 있으며, 바람직하게, 지질이 액상으로 변환되는 융해점 이상의 온도일 수 있다. 일예로 50 내지 100℃, 좋게는 60 내지 95 ℃, 더욱 좋게는 70 내지 90 ℃ 범위일 수 있으나, 이에 한정하는 것은 아니다.The water-in-oil dispersion is not limited unless it inhibits the object of the present invention, but can be prepared by mixing the colloidal solution after heating the lipid to form a solution phase. When the lipid is heated, the temperature may be selected according to the type, molecular weight, and content of the lipid, and preferably, may be a temperature above a melting point at which the lipid is converted into a liquid phase. For example, it may be in the range of 50 to 100°C, preferably 60 to 95°C, more preferably 70 to 90°C, but is not limited thereto.
상기 지질에 상기 콜로이드 용액을 투입하여 유중수 분산액이 생성된 후, 상기 유중수 분산액은 계면활성제를 포함하는 수용액에 투입되고 균질화되어 나노지질전달체를 생성할 수 있다.After adding the colloidal solution to the lipid to generate a water-in-oil dispersion, the water-in-oil dispersion is introduced into an aqueous solution containing a surfactant and homogenized to produce a nanolipid transporter.
상기 유중수 분산액을 상기 계면활성제를 포함하는 수용액에 투입하고 균질화하여 나노지질전달체를 생성하는 단계에서, 상기 계면활성제는 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 지방족 글리세릴계 화합물을 포함할 수 있다.In the step of generating a nanolipid transporter by introducing the water-in-oil dispersion into an aqueous solution containing the surfactant and homogenizing the surfactant, the surfactant is not limited, but may include an aliphatic glyceryl-based compound. have.
바람직하게 상기 계면활성제의 HLB는 10 이상일 수 있다. HLB값(Hydrophile-Lipophile Balance, 친수성 친유성 밸런스)은 계면활성제의 친수성 물질 및 친유성 물질에 대한 친화성 정도를 나타내는 값으로, HLB 값이 0에 가까워질수록 친유성을 나타내며, 40에 가까워질수록 친수성을 나타낸다. 본 발명의 실시예에 따른 계면활성제는 HLB 값이 10 이상일 수 있으며, 좋게는 10 내지 25, 더욱 좋게는 12 내지 20인 지방족 글리세릴계 화합물을 사용할 수 있으나, 이에 한정하는 것은 아니다. 상기 범위에서, 나노지질전달체 형성시 수분산액의 안정성이 향상되고, 수분산액이 보다 균질화되는 효과를 얻을 수 있어 바람직하다.Preferably, the HLB of the surfactant may be 10 or more. The HLB value (Hydrophile-Lipophile Balance) is a value indicating the degree of affinity of the 활성제surfactant to the hydrophilic substance and 유ophilic substance, and as the HLB value approaches 0, it exhibits lipophilicity and approaches 40 Shows hydrophilicity. The surfactant according to the embodiment of the present invention may have an HLB value of 10 or more, preferably 10 to 25, more preferably an aliphatic glyceryl-based compound having 12 to 20, but is not limited thereto. In the above range, the stability of the aqueous dispersion is improved when the nanolipid transporter is formed, and an effect that the aqueous dispersion is more homogenized can be obtained, which is preferable.
상기 지방족 글리세릴계 화합물 계면활성제는 폴리글리세릴 비이온계 계면활성제일 수 있으며, 구체적인 일예로, 폴리글리세릴 지방산 에스테르계 화합물, 폴리글리세릴 지방족 에테르계 화합물, 폴리글리세릴 소르비탄 지방산 에스테르 및 이들 중 둘 이상의 배합물 등으로 이루어진 군으로부터 선택되는 어느 하나 이상을 들 수 있다.보다 구체적인 일 예로 폴리글리세릴-4 카프릴레이트/카프레이트, 폴리글리세릴-5 카프릴레이트/카프레이트, 폴리글리세릴-6 카프릴레이트/카프레이트, 폴리글리세릴-7 카프릴레이트/카프레이트, 폴리글리세릴-8 카프릴레이트/카프레이트, 폴리글리세릴-9 카프릴레이트/카프레이트, 폴리글리세릴-10 카프릴레이트/카프레이트, 폴리글리세릴-4 카프레이트, 폴리글리세릴-5 카프레이트, 폴리글리세릴-6 카프레이트, 폴리글리세릴-7 카프레이트, 폴리글리세릴-8 카프레이트, 폴리글리세릴-9 카프레이트, 폴리글리세릴-10 카프레이트, 폴리글리세릴-4 라우레이트, 폴리글리세릴-5 라우레이트, 폴리글리세릴-6 라우레이트, 폴리글리세릴-7 라우레이트, 폴리글리세릴-8 라우레이트, 폴리글리세릴-9 라우레이트, 폴리글리세릴-10 라우레이트, 폴리글리세릴-6 코코에이트, 폴리글리세릴-7 코코에이트, 폴리글리세릴-8 코코에이트, 폴리글리세릴-9 코코에이트, 폴리글리세릴-10 코코에이트, 폴리글리세릴-11 코코에이트, 폴리글리세릴-12 코코에이트, 폴리글리세릴-6 미리스테이트, 폴리글리세릴-7 미리스테이트, 폴리글리세릴-8 미리스테이트, 폴리글리세릴-9 미리스테이트, 폴리글리세릴-10 미리스테이트, 폴리글리세릴-11 미리스테이트, 폴리글리세릴-12 미리스테이트, 폴리글리세릴-10 올레에이트, 폴리글리세릴-11 올레에이트, 폴리글리세릴-12 올레에이트, 폴리글리세릴-10 스테아레이트, 폴리글리세릴-11 스테아레이트, 폴리글리세릴-12 스테아레이트, 및 이들 중 둘 이상의 배합물로 이루어진 군으로부터 선택되는 하나 이상을 포함할 수 있으나 이에 한정하는 것은 아니다.The aliphatic glyceryl-based compound surfactant may be a polyglyceryl nonionic surfactant, and specific examples thereof include polyglyceryl fatty acid ester-based compounds, polyglyceryl aliphatic ether-based compounds, polyglyceryl sorbitan fatty acid esters, and among them. And any one or more selected from the group consisting of two or more combinations. More specific examples include polyglyceryl-4 caprylate/caprate, polyglyceryl-5 caprylate/caprate, polyglyceryl- 6 Caprylate/caprate, polyglyceryl-7 caprylate/caprate, polyglyceryl-8 caprylate/caprate, polyglyceryl-9 caprylate/caprate, polyglyceryl-10 ka Prilate/caprate, polyglyceryl-4 caprate, polyglyceryl-5 caprate, polyglyceryl-6 caprate, polyglyceryl-7 caprate, polyglyceryl-8 caprate, polyglyceryl- 9 Caprate, polyglyceryl-10 caprate, polyglyceryl-4 laurate, polyglyceryl-5 laurate, polyglyceryl-6 laurate, polyglyceryl-7 laurate, polyglyceryl-8 laur Rate, polyglyceryl-9 laurate, polyglyceryl-10 urarate, polyglyceryl-6 cocoate, polyglyceryl-7 cocoate, polyglyceryl-8 cocoate, polyglyceryl-9 cocoate, Polyglyceryl-10 cocoate, polyglyceryl-11 cocoate, polyglyceryl-12 cocoate, polyglyceryl-6 myristate, polyglyceryl-7 myristate, polyglyceryl-8 myristate, polyglyceryl Reel-9 myristate, polyglyceryl-10 myristate, polyglyceryl-11 myristate, polyglyceryl-12 myristate, polyglyceryl-10 oleate, polyglyceryl-11 oleate, polyglyceryl- 12 oleate, polyglyceryl-10 stearate, polyglyceryl-11stearate, polyglyceryl-12stearate, and one or more selected from the group consisting of combinations of two or more of them. It is not.
상기 계면활성제는 수용액 내에 0.01 중량% 내지 15 중량%, 구체적으로 0.1 중량% 내지 10 중량%, 보다 구체적으로 0.5 중량% 내지 5중량%일 수 있으나, 이에 제한받지 않는다.The surfactant may be 0.01% to 15% by weight in aqueous solution, specifically 0.1% to 10% by weight, and more specifically 0.5% to 5% by weight, but is not limited thereto.
상기 계면활성제를 포함하는 수용액은 알코올을 바람직하게 더 포함할 수 있으며, 상기 알코올은 탄소수 1 내지 4의 저급 알코올로부터 선택될 수 있고, 바람직하게 에탄올일 수 있으나 이에 한정하는 것은 아니다. 상기 알코올이 물과 혼합될 경우 물-알코올 공용매를 형성하며 상기 계면활성제가 상기 공용매에 용해된 형태를 가진다. 상기 물-알코올 공용매에서 물과 알코올의 혼합비는 중량기준으로 10:1 내지 10:10, 구체적으로 10:5 내지 10:9일 수 있다. 물-알코올 공용매를 사용함에 따라 균질화시 낮은 에너지에서도 보다 작은 입경의 나노지질전달체가 얻어질 수 있으며 높은 분산 안정성을 가질 수 있는 점에서 바람직하다.The aqueous solution containing the surfactant may further include alcohol, and the alcohol may be selected from lower alcohols having 1 to 4 carbon atoms, preferably ethanol, but is not limited thereto. When the alcohol is mixed with water, a water-alcohol co-solvent is formed and the surfactant has a form dissolved in the co-solvent. The mixing ratio of water and alcohol in the water-alcohol co-solvent may be 10:1 to 10:10 by weight, specifically 10:5 to 10:9. The use of a water-alcohol co-solvent is preferred in that it is possible to obtain a nanolipid transporter having a smaller particle size even at low energy during homogenization and to have high dispersion stability.
상기 균질화하는 단계는 상기 나노지질전달체를 호모 믹서로 500 rpm 이상, 좋게는 3,000 ~ 5,000 RPM으로5분 이상, 좋게는 10분 내지 20분간 균질화하는것일 수 있다.The homogenizing step may be to homogenize the nanolipid transporter with a homo mixer at 500 rpm or more, preferably 3,000 to 5,000 RPM for 5 minutes or more, and preferably 10 to 20 minutes.
상기 나노지질전달체를 생성하는 단계는 균질화를 위해 바람직하게 고압유화 단계를 더 포함할 수 있다. 상기 고압유화 단계를 거침으로써, 비교적 높은 함량의 생리활성물질을 함유하면서도 투명 또는 현탁 액상의 외관을 갖고 있으며, 상기 투명 또는 현탁 액상을 피부 또는 모낭 등에 도포시 에멀젼을 도포한 것과 같이 흡수되는 차별된 사용감을 제공할 수 있으며, 모낭에 특이적으로 우수한 흡수 특성을 나타낼 수 있어 바람직하다.The step of generating the nanolipid transporter may further include a high pressure emulsification step, preferably for homogenization. By going through the high-pressure emulsification step, it contains a relatively high content of physiologically active substances, yet has the appearance of a transparent or suspended liquid, and is differentiated from being absorbed as when applying the transparent or suspended liquid to the skin or hair follicles as an emulsion. It is preferable because it can provide a feeling of use and can exhibit excellent absorption characteristics specifically for hair follicles.
보다 구체적으로, 고압유화 단계는 고압유화기로 100 bar 이상, 좋게는 100 ~ 1500 bar, 더욱 좋게는 500 ~ 1500 bar 압력으로 1회 이상, 좋게는 2 내지 5회 통과시켜 추가로 균질화하는 단계를 포함할 수 있다. 상기 단계를 거침으로써, 균일한 나노 입자의 형성이 보다 용이하게 이루어질 수 있으며, 나노지질전달체를 대용량으로 생산하는데 유리하다.More specifically, the high-pressure emulsification step includes a further homogenization by passing at least one time, preferably 2 to 5 times, at a pressure of 100 bar or more, preferably 100 to 1500 bar, more preferably 500 to 1500 bar, with a high pressure emulsifier. can do. By going through the above steps, uniform nanoparticles can be formed more easily, and it is advantageous to produce a nanolipid transporter in a large capacity.
이하 본 발명의 생리활성물질이 봉입된 나노지질전달체에 대해 상세히 설명한다.Hereinafter will be described in detail with respect to the nanolipid transporter encapsulated bioactive material of the present invention.
도 1을 참조하여 설명하면, 도 1은 본 발명에 따른 나노지질전달체의 일 예에 대한 모식도를 도시한 것으로, 본 발명에 따른 나노지질전달체는 생리활성물질 및 친수성 고분자를 함유하는 친수성 고분자 복합체를 포함하는 코어부; 및 상기 코어의 표면 상에 위치하며 지질을 포함하는 쉘부;를 포함한다.Referring to FIG. 1, FIG. 1 shows a schematic diagram of an example of a nanolipid transporter according to the present invention, wherein the nanolipid transporter according to the present invention comprises a hydrophilic polymer complex containing a bioactive substance and a hydrophilic polymer. Core portion comprising; And a shell portion located on the surface of the core and including lipids.
또한 상기 코어부는 인지질을 더 포함한다. 상기 코어부에 포함되는 친수성 고분자 복합체는 지질과 계면을 형성하며, 상기 계면에는 인지질에 의한 수화 액정상이 상기 계면에 배치되어 계면을 매우 효과적으로 안정화시킬 수 있다. 이에 따라 코어부에 포함되는 생리활성물질은 외부로 쉽게 용출되지 않을 수 있으며, 제조공정중 균질화 또는 고압유화단계에서도 외상인 수용액 상으로 용출되지 않을 뿐만 아니라 수분산액 상태로 존재할 때에도 안정적으로 쉘부 내에 봉입되어 존재할 수 있다.In addition, the core portion further includes phospholipids. The hydrophilic polymer composite included in the core portion forms an interface with lipids, and a hydrated liquid crystal phase by phospholipids is disposed on the interface to stabilize the interface very effectively. Accordingly, the physiologically active substance contained in the core portion may not be easily eluted to the outside, and is not eluted into the aqueous solution phase as a trauma in the homogenization or high-pressure emulsification step during the manufacturing process, and is stably enclosed in the shell portion even when present in the form of an aqueous dispersion. Can exist.
상기 생리활성물질은 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 상기 나노지질전달체에서 0.0001 ~ 20중량%, 좋게는 0.005 ~ 10 중량%, 더욱 좋게는 0.002 ~ 3 중량%, 가장 좋게는 0.001 ~ 1 중량%일 수 있다.The bioactive material is not limited as long as it does not interfere with the object of the present invention, but 0.0001 to 20% by weight, preferably 0.005 to 10% by weight, more preferably 0.002 to 3% by weight, most preferably 0.001 to It may be 1% by weight.
상기 생리활성물질 및 친수성 고분자를 함유하는 친수성 고분자 복합체는 생리활성물질 및 친수성 고분자가 2000:1 내지 20:1, 구체적으로 1000:1 내지 40:1의 중량비로 결합될 수 있으며, 상기 범위에서 생리활성물질의 봉입 효율이 향상될 수 있어 바람직하다.In the hydrophilic polymer complex containing the bioactive material and hydrophilic polymer, the bioactive material and hydrophilic polymer may be combined in a weight ratio of 2000:1 to 20:1, specifically 1000:1 to 40:1, and physiological in the above range. It is preferable because the encapsulation efficiency of the active material can be improved.
상기지질 및 인지질은 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 중량비로 100:0.1 내지 100:50, 구체적으로 100:0.5 내지 100: 25, 더욱 구체적으로 100:1 내지 100:10로 포함될 수 있다.The lipids and phospholipids are not limited as long as they do not inhibit the object of the present invention, but may be included in a weight ratio of 100:0.1 to 100:50, specifically 100:0.5 to 100:25, and more specifically 100:1 to 100:10. have.
상기 나노지질전달체는 본 발명의 목적을 저해하지 않는 한 제한되지 않으나 20 nm 내지 1000 nm, 구체적으로 40 내지 700 nm, 더욱 구체적으로 50 내지 500 nm의 평균 입경을 가지며 하기 관계식 1을 만족하는 것일 수 있다.The nanolipid transporter is not limited as long as it does not inhibit the object of the present invention, but may have an average particle diameter of 20 nm to 1000 nm, specifically 40 to 700 nm, more specifically 50 to 500 nm, and satisfy the following relational expression (1) have.
[관계식 1][Relationship 1]
|T0-T20|/T0< 0.2|T 0 -T 20 |/T 0 <0.2
(상기 관계식 1에서 T0는 나노지질전달체 1중량% 수분산액의 제조 후 500 nm 파장에서 측정된 투과도를 의미하며, T20은 나노지질전달체 1중량% 수분산액을 45℃에서20일 방치 후 500 nm 파장에서 측정된 투과도를 의미한다.)(In the relational formula 1, T 0 means the transmittance measured at 500 nm wavelength after the preparation of the 1% by weight aqueous dispersion of the nanolipid transporter, T 20 is 500% after leaving the 1% by weight aqueous dispersion of the nanolipid transporter at 45°C for 20 days. It means transmittance measured at nm wavelength.)
본 발명에 따른 나노지질전달체는 구체적으로 상기 관계식 1로 정의되는 분산 안정성의 값이 0.1 미만의 값을 가질 수 있다. 즉 상기 나노지질전달체가 우수한 분산 안정성을 가지며 나노지질전달체의 변색 또는 층분리가 발생하지 않고, 장시간 방치시에도 응집 현상으로 인해 안정성이 떨어지는 문제 등이 발생하지 않는다.The nanolipid transporter according to the present invention may have a value of dispersion stability, specifically defined by the relational expression 1, below 0.1. That is, the nanolipid transporter has excellent dispersion stability, and discoloration or layer separation of the nanolipid transporter does not occur, and even when it is left for a long time, problems such as poor stability due to aggregation phenomenon do not occur.
또한, 본 발명은 상기 나노지질전달체를 포함하는 화장료 조성물을 제공한다.In addition, the present invention provides a cosmetic composition comprising the nanolipid transporter.
본 발명에서 상기 화장료 조성물은 제한되지는 않으나 용액, 현탁액, 유탁액, 페이스트, 겔, 크림, 로션, 파우더, 비누, 오일, 분말 파운데이션, 유탁액 파운데이션, 왁스 파운데이션 및 스프레이로 구성된 군으로부터 선택되는 어느 하나의 제형일 수 있다.In the present invention, the cosmetic composition is not limited, but any one selected from the group consisting of solutions, suspensions, emulsions, pastes, gels, creams, lotions, powders, soaps, oils, powder foundations, emulsion foundations, wax foundations and sprays It may be one formulation.
상기 화장료 조성물은 유효 성분으로서 상기 나노지질전달체 이외에 화장품에 통상적으로 이용되는 성분들을 포함할 수 있으며, 예컨대 항산화제, 안정화제, 용해화제, 비타민, 안료 및 향료와 같은 통상적인 보조제, 그리고 담체를 포함할 수 있다.The cosmetic composition may include ingredients commonly used in cosmetics in addition to the nanolipid transporter as an active ingredient, and include, for example, antioxidants, stabilizers, solubilizers, conventional adjuvants such as vitamins, pigments and fragrances, and carriers can do.
한편, 상기 화장료 조성물은 당업계에서 통상적으로 제조되는 어떠한 제형으로도 제조될 수 있으며, 예를 들어, 용액, 현탁액, 유탁액, 페이스트, 겔, 크림, 로션, 파우더, 비누, 계면활성제-함유 클린싱, 오일, 분말 파운데이션, 유탁액 파운데이션, 왁스 파운데이션 및 스프레이 등으로 제형화될 수 있다. 다만, 이에 반드시 한정되는 것은 아니다. 더욱 상세하게는, 유연 화장수, 수렴 화장수, 영양 화장수, 영양 크림, 마사지 크림, 에센스, 팩, 스프레이 또는 파우더의 제형으로 제조될 수 있다.On the other hand, the cosmetic composition may be prepared in any formulation conventionally prepared in the art, for example, solution, suspension, emulsion, paste, gel, cream, lotion, powder, soap, surfactant-containing cleaning , Oil, powder foundation, emulsion foundation, wax foundation and spray. However, it is not necessarily limited thereto. More specifically, it can be prepared in the form of flexible lotion, converging lotion, nutrition lotion, nutrition cream, massage cream, essence, pack, spray or powder.
상기 화장료 조성물의 제형이 페이스트, 크림 또는 겔인 경우에는 담체 성분으로서 동물성유, 식물성유, 왁스, 파라핀, 전분, 트라칸트, 셀룰로오스 유도체, 폴리에틸렌 글리콜, 실리콘, 벤토나이트, 실리카, 탈크 또는 산화아연 등이 이용될 수 있다.When the formulation of the cosmetic composition is a paste, cream or gel, animal oil, vegetable oil, wax, paraffin, starch, tracant, cellulose derivative, polyethylene glycol, silicone, bentonite, silica, talc or zinc oxide are used as carrier components. Can be.
또한, 본 발명의 화장품의 제형이 파우더 또는 스프레이인 경우에는 담체 성분으로서 락토스, 탈크, 실리카, 알루미늄 히드록시드, 칼슘 실리케이트 또는 폴리아미드 파우더가 이용될 수 있고, 특히 스프레이인 경우에는 추가적으로 클로로플루오로히드로카본,프로판/부탄 또는 디메틸 에테르와 같은 추진체를 포함할 수 있다.In addition, when the formulation of the cosmetic product of the present invention is a powder or a spray, lactose, talc, silica, aluminum hydroxide, calcium silicate or polyamide powder may be used as a carrier component, and particularly in the case of a spray, additionally chlorofluoro Propellants such as hydrocarbon, propane/butane or dimethyl ether.
또한, 본 발명의 화장품의 제형이 용액 또는 유탁액인 경우에는 담체 성분으로서 용매, 용해화제 또는 유탁화제가 이용되고, 예컨대 물, 에탄올, 이소프로판올, 에틸 카보네이트, 에틸 아세테이트, 벤질 알코올, 벤질 벤조에이트, 프로필렌 글리콜, 1,3-부틸글리콜오일, 글리세롤 지방족 에스테르, 폴리에틸렌 글리콜 또는 소르비탄의 지방산 에스테르가 사용될 수 있다.Further, when the formulation of the cosmetic product of the present invention is a solution or emulsion, a solvent, solubilizer or emulsifier is used as a carrier component, such as water, ethanol, isopropanol, ethyl carbonate, ethyl acetate, benzyl alcohol, benzyl benzoate, Propylene glycol, 1,3-butylglycol oil, glycerol aliphatic esters, polyethylene glycol or fatty acid esters of sorbitan can be used.
또한, 본 발명의 화장품의 제형이 현탁액인 경우에는 담체 성분으로서 물, 에탄올 또는 프로필렌 글리콜과 같은 액상의 희석제, 에톡실화이소스테아릴 알코올, 폴리옥시에틸렌 소르비톨 에스테르 및 폴리옥시에틸렌 소르비탄 에스테르와 같은 현탁제, 미소결정성 셀룰로오스, 알루미늄 메타히드록시드, 벤토나이트, 아가 또는 트라칸트 등이 사용될 수 있다.In addition, when the formulation of the cosmetic product of the present invention is a suspension, liquid diluents such as water, ethanol or propylene glycol as carrier components, suspensions such as ethoxylated isostearyl alcohol, polyoxyethylene sorbitol ester and polyoxyethylene sorbitan ester Agents, microcrystalline cellulose, aluminum metahydroxide, bentonite, agar or trakant, etc. can be used.
바람직한 일 예로, 상기 나노지질전달체를 포함하는 화장료 조성물은 모낭에 대해 타게팅 특성을 가지는 경피 흡수용 화장료 조성물일 수 있다.As a preferred example, the cosmetic composition comprising the nanolipid transporter may be a cosmetic composition for transdermal absorption having targeting properties for hair follicles.
상기 나노지질전달체는 쉘부가 지질을 포함하기 때문에 모낭에 대해 친화도가 매우 뛰어나며 수십 내지 수백 nm의 입경을 가지기 때문에 모낭에 특이적으로 우수한 흡수능력을 가져 우수한 타게팅 특성을 가질 수 있다. 이러한 모낭 타게팅 특성에 의해 피부에 처리된 나노지질전달체는 모낭의 헤어를 따라 모낭 중심에 집중적으로 축적될 수 있으며, 모낭 내부에서 진피쪽으로 흡수될 수 있다. 진피에 흡수된 나노지질전달체는 코어부에 포함되어 있는 생리활성물질을 방출함으로써 생리활성물질을 통한 치료 또는 개선 효과를 부여할 수 있다.The nanolipid transporter has excellent affinity for hair follicles because the shell portion contains lipids, and has a particle size of tens to hundreds of nm, so it can have excellent targeting properties by having excellent absorption capacity specifically for hair follicles. Due to these hair follicle targeting properties, the nanolipid transporter treated on the skin can be intensively accumulated in the center of the hair follicle along the hair follicle, and can be absorbed from the inside of the hair follicle to the dermis. The nanolipid transporter absorbed by the dermis can impart a treatment or improvement effect through the bioactive material by releasing the bioactive material contained in the core.
비한정적인 일 예로, 상기 나노지질전달체를 포함하는 경피 흡수용 화장료 조성물은 두피에 처리하여 모낭으로 타게팅할 수 있다. 상기 처리는 스프레이나 도포와 같은 통상적인 공지의 수단을 포함할 수 있으며, 손이나 도포기구를 통해 도포함으로서 나노지질전달체가 두피에 존재하는 모낭으로 타게팅될 수 있으며, 모낭 타게팅을 통해 생리활성물질을 두피에 공급하여 발모 및 탈모 방지의 우수한 효과를 얻을 수 있다. As a non-limiting example, the cosmetic composition for transdermal absorption containing the nanolipid transporter may be targeted to the hair follicles by treating the scalp. The treatment may include conventionally known means, such as spraying or application, and nano-lipid transporters may be targeted to the hair follicles present on the scalp as a dosing device through a hand or an application device, and bioactive substances may be targeted through the targeting of the hair follicles. It can be supplied to the scalp to obtain an excellent effect of preventing hair growth and hair loss.
즉 탈모방지, 발모 또는 제모 등의 목적을 위해, 모낭이 많이 분포한 두피 조직에서는 경피 전달보다는 모낭으로 효율적으로 전달되는 전달체를 매우 필요로 하고 있으며, 또한 모낭은 혈액과 가장 빠르게 연결될 수 있는 조직이다. 본 발명에 따른 나노지질전달체는 리포좀과 같은 콜로이드성 전달체보다 고형지질 나노입자와 같은 입자성을 가지기 때문에 모낭에 처리시 더욱 빠르고 효과적인 개선 효과를 얻을 수 있다.In other words, for the purpose of preventing hair loss, hair growth, or hair removal, scalp tissue with a large distribution of hair follicles requires a delivery agent that is efficiently delivered to the hair follicle rather than transdermal delivery, and the hair follicle is the tissue that can be quickly connected to blood. . Since the nanolipid transporter according to the present invention has the same graininess as the solid lipid nanoparticles than the colloidal transporter such as liposomes, it is possible to obtain a faster and more effective improvement effect when treating the hair follicles.
이하, 본 발명의 내용을 실시예를 통하여 보다 구체적으로 설명한다. 실시예는 본 발명을 보다 구체적으로 설명하기 위한 것일 뿐, 본 발명의 권리범위가 이들에 의해 한정되는 것은 아니다.Hereinafter, the contents of the present invention will be described in more detail through examples. The examples are only intended to illustrate the present invention in more detail, and the scope of the present invention is not limited by them.
[실시예 1] 나노지질전달체(Nano Lipid Carriers; NLC)의 제조[Example 1] Preparation of Nano Lipid Carriers (NLC)
하기와 같은 제조 방법을 통해 나노지질전달체 100g이 되도록 제조하였다.It was prepared so that the nanolipid transporter 100g through the following manufacturing method.
펩타이드로서 커퍼 트리펩타이드-1(Copper TriPeptide-1, CTP)와 알라닌/히스티딘/라이신 폴리펩타이드 커퍼 에이치씨엘(Alanine/Histidine/Lysine Polypeptide Copper HCl, ATP)을 정제수에 첨가한 후 용해하여 펩타이드 수용액을 제조하였다. 상기 펩타이드는 전체 나노지질전달체 분산액에서 0.0225 중량%가 되도록 하였다.As a peptide, Copper TriPeptide-1 (CTP) and Alanine/Histidine/Lysine Polypeptide Copper HCl (ATP) are added to purified water and dissolved to prepare a peptide aqueous solution. Did. The peptide was made to be 0.0225% by weight in the total nanolipid transporter dispersion.
용해된 펩타이드 수용액에 0.1중량%카보머(Carbomer) 수용액을 첨가하고, 70℃ 환경에서 자석교반을 통해 500RPM으로 분산시켰다. 제조 후 카보머는 전체 나노지질전달체 수분산액에서 0.000125 중량%가 되도록 하였다. 상기 과정을 통해 펩타이드-하이드로겔 형태의 친수성 고분자 복합체 수용액을 제조하였다.A 0.1 wt% Carbomer aqueous solution was added to the dissolved peptide aqueous solution, and dispersed at 500 RPM through magnetic stirring at 70°C. After preparation, the carbomer was set to 0.000125% by weight in the total nanolipid transporter dispersion. Through the above process, an aqueous solution of a hydrophilic polymer complex in the form of a peptide-hydrogel was prepared.
인지질 용액을 제조하기 위해 수첨 레시틴(하이드로제네이티드레시틴, Hydrogenated Lecithin)을 에탄올에 용해하여 제조하였다. 상세하게, 인지질 용액에 사용되는 에탄올은 나노지질전달체 수분산액의 0.8중량%이 되도록 준비하였고, 상기 수첨 레시틴을 상기 에탄올에 투입하고 70℃ 온도에서 500RPM으로 교반하여 완전히 용해시킨 후 투명한 인지질 용액을 제조하였다.To prepare a phospholipid solution, hydrogenated lecithin (hydrogenated lecithin) was prepared by dissolving in ethanol. In detail, ethanol used in the phospholipid solution was prepared to be 0.8% by weight of the aqueous dispersion of nanolipid transporter, and the hydrolyzed lecithin was added to the ethanol and stirred at 500RPM at 70°C to completely dissolve to prepare a transparent phospholipid solution. Did.
상기 과정을 통해 제조한 인지질 용액에 미리 제조한 펩타이드-하이드로겔 형태의 친수성 고분자 복합체 수용액을 첨가하여 5분, 700RPM으로 골고루 혼합시키면서 인지질 용액에 수화시켜 수화액정상으로 제조하여 나노지질전달체에 봉입될 코어부를 형성하였다.To the phospholipid solution prepared through the above process, the aqueous solution of the hydrophilic polymer complex in the form of a pre-prepared peptide-hydrogel is added and mixed evenly at 700 RPM for 5 minutes, hydrated in a phospholipid solution to prepare a hydrated liquid to be encapsulated in the nanolipid transporter. A core portion was formed.
이어서, 고상인 제1지질인 글리세릴 디스테아레이트(Glyceryl distearate)와 액상인 제2지질인 카프릴릭/카프릭 트라이글리세라이드(Caprylic/capric triglyceride)를 70℃에서 500rpm으로 교반하여 용해시켜 투명한 용액 상으로 만들었다. 투명한 용액 상의 상기 지질 혼합액에 수화액정상 형태의 코어부를 포함하는 용액을 첨가하여 70℃에서 700RPM으로 10분간 교반하여 유중수 분산액을 제조하였다.Subsequently, the solid first lipid, glyceryl distearate, and the liquid second lipid, caprylic/capric triglyceride, were dissolved by stirring at 70° C. at 500 rpm for clarity. Made into solution phase. A solution containing a core portion in the form of a hydrated liquid was added to the lipid mixture on a transparent solution, and stirred at 700°C for 10 minutes at 70° C. to prepare a water-in-oil dispersion.
계면활성제로 HLB가 15.9인 폴리글리세릴-10 올리에이트(Polyglyceryl-10 oleate)가 용해되어있는 정제수/에탄올 혼합액에 상기 유중수 분산액을 첨가하면서 Homodisperser(Model 2.5, PRIMIX)로 2,000rpm, 15분간 교반하였다. 이 때 계면활성제와 혼합되는 에탄올은 전체 나노지질전달체 수분산액의 40 중량%가 되도록 혼합하였다.While stirring the water-in-oil dispersion in purified water/ethanol mixture in which polyglyceryl-10 oleate having a HLB of 15.9 as a surfactant was dissolved, stirring was performed at 2,000 rpm for 15 minutes with a Homodisperser (Model 2.5, PRIMIX). Did. At this time, the ethanol mixed with the surfactant was mixed to be 40% by weight of the total aqueous dispersion of nanolipids.
교반이 끝난 용액은 호모믹서를 통해 5,000rpm으로 20분간 진행하여 더 균질화한후, 고압유화를 위해 고압유화기(Microfluidics, M-110P 마이크로플루다이져)를 이용하였고, 압력 조건 1,000bar, 통과횟수 3회로 하여 추가적인 균질화를 수행하였다. 이후, 균질화가 끝난 용액을 상온에서 천천히 냉각하여 최종적으로 나노지질전달체 수분산액을 제조하였고, 나노지질전달체 수분산액에 포함되는 구성성분의 함량은 표 1에 기재하였다.The stirred solution was further homogenized by proceeding with a homomixer at 5,000 rpm for 20 minutes, and then a high pressure emulsifier (Microfluidics, M-110P microfluidizer) was used for high pressure emulsification. Additional homogenization was performed in 3 runs. Subsequently, the homogenized solution was slowly cooled at room temperature to finally prepare a nanolipid transporter dispersion, and the contents of the components included in the nanolipid transporter dispersion are listed in Table 1.
[실시예 2][Example 2]
실시예 1에서 계면활성제를 용해시킨 용액의 에탄올 함량을 1/5로 줄여 전체 나노지질전달체의 8%가 되도록 하는 것을 제외하고 나머지 과정은 동일하게 하여 나노지질전달체 수분산액을 제조하였다. 나노지질전달체 수분산액에 포함되는 구성성분의 함량은 표 1에 기재하였다.In Example 1, the ethanol content of the solution in which the surfactant was dissolved was reduced to 1/5 to make 8% of the total nanolipid transporter, and the rest of the procedure was the same to prepare an aqueous dispersion of nanolipid transporter. The contents of the components included in the aqueous dispersion of nanolipid transporters are listed in Table 1.
[실시예 3][Example 3]
실시예 1에서 카보머의 첨가량을 4배로 늘려 전체 나노지질전달체의 0.0005 중량%가 되도록 한 것을 제외하고 나머지 과정은 동일하게 하여 나노지질전달체 수분산액을 제조하였다. 나노지질전달체 수분산액에 포함되는 구성성분의 함량은 표 1에 기재하였다.In Example 1, the amount of addition of carbomer was increased to 4 times to make 0.0005% by weight of the total nanolipid transporter, and the rest of the procedure was the same to prepare a nanolipid transporter dispersion. The contents of the components included in the aqueous dispersion of nanolipid transporters are listed in Table 1.
[실시예 4][Example 4]
실시예 1에서 액상인 제2지질인 카프릴릭/카프릭 트라이글리세라이드의 함량을 1/2로 줄여 전체 나노지질전달체의 0.9375 중량%가 되도록 한 것을 제외하고 나머지 과정은 동일하게 하여 나노지질전달체 수분산액을 제조하였다. 나노지질전달체 수분산액에 포함되는 구성성분의 함량은 표 1에 기재하였다.In Example 1, the rest of the procedure was the same as that of the nanolipid transporter, except that the content of the second lipid, caprylic/capric triglyceride, was reduced to 1/2 to make 0.9375% by weight of the total nanolipid transporter. An aqueous dispersion was prepared. The contents of the components included in the aqueous dispersion of nanolipid transporters are listed in Table 1.
하기 표 1은 전술한 실시예 1 내지 실시예 4의 조성비 및 고압유화에 의한 균질화 여부를 나타낸 것이다.Table 1 below shows the composition ratios of Examples 1 to 4 and the homogenization by high pressure emulsification.
[실시예 5][Example 5]
실시예 1에서 고압유화 균질화과정을 생략한 것을 제외하고 나머지 과정은 동일하게 하여 나노지질전달체 수분산액을 제조하였다.In Example 1, except for omitting the high pressure emulsification homogenization process, the rest of the procedure was the same to prepare a nanolipid transporter dispersion.
[비교예 1][Comparative Example 1]
실시예 1에서 하이드로겔인 카보머를 첨가하지 않고 나머지 과정은 동일하게 하여 나노지질전달체 수분산액을 제조하였다.In Example 1, the hydrogel, a carbomer, was not added, and the rest of the procedure was the same to prepare a nanolipid transporter dispersion.
[비교예 2][Comparative Example 2]
실시예 2에서 계면활성제인 폴리글리세릴-10 올리에이트 대신 솔비탄 팔미테이트(Sorbitan Palmitate)를 사용한 것을 제외하고 나머지 과정은 동일하게 하여 나노지질전달체 수분산액을 제조하였다.In Example 2, except for using sorbitan palmitate (Sorbitan Palmitate) instead of the surfactant polyglyceryl-10 oleate, the rest of the procedure was the same to prepare a nanolipid aqueous dispersion.
아래 표 2는 전술한 실시예 5, 비교예 1 및 비교예 2에 대한 조성비 및 균질화여부이다.Table 2 below shows the composition ratio and homogenization of Example 5, Comparative Example 1 and Comparative Example 2 described above.
[비교예 3][Comparative Example 3]
실시예 1의 인지질 용액 중 인지질을 함유하지 않고 에탄올 용액을 사용한 것만 제외하고 나머지 과정은 동일하게 하여 나노지질전달체를 제조하였다.In the phospholipid solution of Example 1, a nanolipid transporter was prepared in the same manner as the rest of the procedure, except that the ethanol solution was used without containing the phospholipid.
[비교예 4][Comparative Example 4]
실시예 1의 지질 혼합액에서 액상인 제2지질을 사용하지 않고 고상인 제1지질만을 3.75 중량% 사용하는 것을 제외하고 나머지 과정은 동일하게 하여 나노지질전달체를 제조하였다.In the lipid mixture of Example 1, a nanolipid transporter was prepared in the same manner as the rest of the procedure, except that 3.75% by weight of the solid first lipid was not used and the liquid second lipid was not used.
[비교예 5][Comparative Example 5]
실시예 1의 지질 혼합액에서 고상인 제1지질을 사용하지 않고 액상인 제2지질만을 3.75 중량% 사용하는 것을 제외하고 나머지 과정은 동일하게 하여 나노지질전달체를 제조하였다.A nanolipid transporter was prepared in the same manner as the rest of the procedure, except that 3.75% by weight of the second lipid in the liquid phase was not used in the lipid mixture of Example 1 without using the solid first lipid.
상기 실시예 및 비교예 각 실험군에 대해 하기와 같이 조성물의 특성을 평가하였다. The properties of the composition were evaluated as follows for each of the experimental and comparative examples.
[시험예 1] 제형조성비 및 고압균질에 따른 나노지질전달체입자 크기 및 투과도 측정[Test Example 1] Measurement of nanolipid transporter particle size and permeability according to formulation composition ratio and high pressure homogeneity
상기 실시예 및 비교예로부터 제조된 나노지질전달체의 평균 입자 크기를 분석하기 위해 나노입자 분석기(Zetasizer Nano ZS, Malvern Instruments)로 입자크기를 측정하였으며, 나노지질전달체 제조 후 500 nm에서 측정된 투과도 To 및 45 ℃에서 30일 방치 후 500 nm 파장에서 측정한 투과도로부터 하기 관계식1에 의해 계산된 장기 안정성 값을 계산하여 그 결과를 표 3에 나타내었다.In order to analyze the average particle size of the nanolipid transporter prepared from the Examples and Comparative Examples, the particle size was measured with a nanoparticle analyzer (Zetasizer Nano ZS, Malvern Instruments), and the transmittance measured at 500 nm after preparation of the nanolipid transporter To And after standing for 30 days at 45 ℃ to calculate the long-term stability value calculated by the following equation 1 from the transmittance measured at 500 nm wavelength are shown in Table 3.
[관계식 1] [Relationship 1]
|T0-T20|/T0< 0.2|T 0 -T 20 |/T 0 <0.2
(상기 관계식 1에서 T0는 나노지질전달체 1중량% 수분산액의 제조 후 500 nm 파장에서 측정된 투과도를 의미하며, T20은 나노지질전달체 1중량% 수분산액을 45℃에서 20일 방치 후 500 nm 파장에서 측정된 투과도를 의미한다.)(In the above equations 1 T 0 after the production of nano-lipid delivery system of 1% aqueous dispersion by weight means a permeability measured at 500 nm wavelength, and, T 20 are 500 then the nano-lipid delivery system of 1% aqueous dispersion by weight to stand at 45 ℃ 20 il It means transmittance measured at nm wavelength.)
도 2는 실시예 2의 입자 크기를 분석한 결과를 나타낸 것이다. Figure 2 shows the results of analyzing the particle size of Example 2.
실시예 1 내지 실시예 4의 경우 대략 300nm 이하의 입자크기를 갖는 것을 확인하였으며,장기 분산 안정성 역시 우수하였다. 실시예 5의 경우 고압유화에 의한 균질화를 수행하지 않음에 따라 외관이 탁한 현탁액이 얻어졌고 평균 입경 5 ㎛ 이상의 입경을 나타냈고, 큰 입경을 가짐에 따라 분산 안정성도 좋지 않았다.For Examples 1 to 4, it was confirmed to have a particle size of approximately 300 nm or less, and long-term dispersion stability was also excellent. In the case of Example 5, a suspension having a cloudy appearance was obtained as a result of not homogenizing by high-pressure emulsification, an average particle size of 5 µm or more was observed, and dispersion stability was not good as it had a large particle size.
반면, 비교예 1, 2, 4 및 5의 경우 초기 입경이 다소 큰 나노입자가 얻어졌을 뿐만 아니라 장기 분산 안정성도 좋지 않은 것으로 나타나 화장료 조성물 용도의 나노지질전달체로 활용하기 어려운 것을 확인할 수 있었다. 비교예 3의 경우 초기 입경은 다소 큰 나노입자가 얻어졌지만 장기 분산 안정성은 다른 비교예에 비해 우수한 것으로 나타났다.On the other hand, in Comparative Examples 1, 2, 4, and 5, it was confirmed that nanoparticles having a slightly larger initial particle size were obtained, and that long-term dispersion stability was also poor, and thus it was difficult to utilize them as nanolipid transporters for cosmetic compositions. In the case of Comparative Example 3, nanoparticles having a slightly larger initial particle size were obtained, but long-term dispersion stability was found to be superior to that of other Comparative Examples.
[시험예 2] 나노지질전달체 안정성 분석[Test Example 2] Nano lipid transport stability analysis
상기 실시예 및 비교예를 통해 제조된 나노지질전달체 용액에 대한 안정성을 측정하였다. 제조된 나노지질전달체의 특정 조건에서 시간 경과에 따른 변색, 층분리 등을 확인하기 위한 안정성을 측정하였다. 장기 분산 안정성을 측정하기 위해 각각의 나노지질전달체 수분산액을 45℃가 유지되는 항온 챔버에 배치하였다.Stability was measured for the nanolipid transporter solution prepared through the above Examples and Comparative Examples. Stability was measured to confirm discoloration, layer separation, etc. over time, under specific conditions of the prepared nanolipid transporter. In order to measure long-term dispersion stability, each nanolipid carrier aqueous dispersion was placed in a constant temperature chamber at which 45°C was maintained.
상기 항온 챔버에 배치한 나노지질전달체 수분산액을 1일, 10일, 20일, 30일 경과시점을 기준으로 형태 변화를 육안으로 관찰하였다.The change in morphology was visually observed based on the elapsed time of 1 day, 10 days, 20 days, and 30 days of the dispersion of the nanolipid transporter placed in the constant temperature chamber.
시간 경과에 따른 나노지질전달체 용액의 응집, 침전 등을 확인한 결과는 표 4와 같고, 도 3은 안정성 실험을 통해 30일 경과된 실시예 1과 비교예 1을 촬영한 사진이다.The results of confirming the aggregation, precipitation, etc. of the nanolipid transporter solution over time are as shown in Table 4, and FIG. 3 is a photograph of Example 1 and Comparative Example 1, which has passed 30 days through the stability experiment.
상기 표 4의 결과를 살펴보면, 실시예 1의 경우 30일까지도 안정된 분산 안정성을 보였으며, 실시예 2 내지 4의 경우 20일까지는 안정된 분산 안정성을 나타냈지만 30일부터는 일부 응집이 되는 현상이 발견되었다. 한편 실시예 5의 경우 초기 입경이 큰 마이크로 입자가 생성되었기 때문에 10일부터 침전되는 현상이 나타났다.Looking at the results of Table 4, Example 1 showed stable dispersion stability up to 30 days, and Examples 2 to 4 showed stable dispersion stability up to 20 days, but some aggregation was observed from 30 days. . On the other hand, in the case of Example 5, since a micro particle having a large initial particle size was generated, a phenomenon of sedimentation was observed from the 10th.
반면, 비교예 1, 2, 4 및 5의 10일 이후부터 침전이나 응집 현상이 심각하게 발생하였으며, 비교예 3의 경우 30일부터 응집되는 현상이 발견되었다On the other hand, precipitation or aggregation occurred seriously after 10 days of Comparative Examples 1, 2, 4 and 5, and in the case of Comparative Example 3, aggregation was observed from 30 days.
[시험예 3] 나노지질전달체 내 생리활성성분의 봉입효율 측정[Test Example 3] Measurement of encapsulation efficiency of bioactive components in nanolipid transporters
상기 실시예 및 비교예로부터 제조된 나노지질전달체 용액을 각각 원심분리기를 통해 4℃, 80,000RPM으로 30분 동안 원심분리시켜 상층액과 침전물을 분리하였다. 이후 상층액을 채취하여 미봉입된 펩타이드의 농도를 측정하여 계산하였으며, 미봉입 펩타이드와 봉입효율의 계산방법은 아래 관계식 2로부터 구할 수 있다.The nanolipid transporter solutions prepared from the above Examples and Comparative Examples were centrifuged at 4°C and 80,000 RPM for 30 minutes through a centrifuge to separate the supernatant and precipitate. Subsequently, the supernatant was collected and calculated by measuring the concentration of the unencapsulated peptide, and the calculation method of the unencapsulated peptide and encapsulation efficiency can be obtained from Equation 2 below.
[관계식 2][Relationship 2]
EEFree = (WTotal-WFree)/WTotal x 100EE Free = (W Total -W Free )/W Total x 100
상기 관계식 2에서 EEFree는 표준물질(펩타이드) 봉입효율을 의미하고, WTotal는 전체 표준물질 농도를 의미하며, WFree는 미봉입 표준물질 농도를 의미한다. 아래 표 5는 실험 결과로 나타난 봉입 효율을 수치로 나타낸 것이다.In Equation 2, EE Free means the standard (peptide) encapsulation efficiency, W Total means the total standard concentration, and W Free means the unenclosed standard concentration. Table 5 below shows the encapsulation efficiency as a result of the experiment.
상기 표 5의 결과로부터, 본 발명의 실시예 1 내지 실시예5에서는 봉입효율이 89% 이상 우수하게 나타난 반면, 비교예 1 내지 5의 경우 봉입효율이 현저하게 낮은 것으로 나타났다.From the results of Table 5, in Examples 1 to 5 of the present invention, the encapsulation efficiency was excellent over 89%, whereas in Comparative Examples 1 to 5, the encapsulation efficiency was remarkably low.
[시험예 4] bio-TEM를 이용한 모낭특이적 나노지질전달체 입자 측정[Test Example 4] Measurement of follicle-specific nanolipid transporter particles using bio-TEM
실시예 1에서 생성된 나노지질전달체를 Bio-TEM(Bio-Transmission Electron Microscope, HITACHI H-7650)으로 측정하는 실험을 진행하였다. 샘플 용액은 극저온(cryo) 처리를 통해 200 메쉬(mesh)그리드로 샘플링하여 측정하였다.The experiment of measuring the nanolipid transporter produced in Example 1 with Bio-TEM (Bio-Transmission Electron Microscope, HITACHI H-7650) was performed. The sample solution was measured by sampling with a 200 mesh grid through cryo treatment.
Bio-TEM으로 이미지화된 입자의 측정 결과는 도 4에 도시하였다. 도 4은 그리드에 안착된 나노지질전달체를 측정한 이미지로, 이로부터 확인할 수 있는 바와 같이, 상기 나노지질전달체는 약 100nm의 균일하고 고형화된 입자형태로 형성되어 있음을 확인할 수 있다.The measurement results of the particles imaged with Bio-TEM are shown in FIG. 4. FIG. 4 is an image of a nanolipid transporter mounted on a grid, and as can be seen from this, it can be seen that the nanolipid transporter is formed in a uniform and solid particle form of about 100 nm.
[시험예 5] 공초점 레이저 스캐닝 현미경(Confocal laser scanning microscope)을 이용한 모낭특이적 나노지질전달체 흡수 거동 측정[Test Example 5] Measurement of follicle-specific nanolipid transporter absorption behavior using a confocal laser scanning microscope
실시예 1에서 제조된 나노지질전달체에 형광물질인 Fluorescein isothiocyanate(FITC)처리하여 피부에 흡수되어있는 거동을 관찰하는 실험을 진행하였다.The nano lipid transporter prepared in Example 1 was treated with a fluorescent substance, Fluorescein isothiocyanate (FITC), and experiments were performed to observe the absorption of the skin.
흡수실험을 위해 MicroPig membrane을 사용하였고, 상기 MicroPig membrane은 액체질소로 냉동시킨 후 정밀 박절기를 통해 8um로 박절시켰다. 박절시킨 조직은 슬라이드글라스에 옮긴 후 Mouting 시약을 도포한 후 공초점현미경으로 관찰하였다.A MicroPig membrane was used for the absorption experiment, and the MicroPig membrane was frozen with liquid nitrogen and then sliced to 8um through a precision grinder. The crushed tissue was transferred to a slide glass and then observed by a confocal microscope after applying the Mouting reagent.
도 5는 박절된 조직내에 FITC처리되어있는 나노지질전달체가 흡수되어있는 형상을 이미지화한 것으로, 전반적으로 모낭의 헤어를 따라 나노지질전달체가 흡수되어있는 것을 확인할 수 있으며, 서서히 모낭내부에서 진피쪽으로 나노지질전달체가 흡수되고 있는 것을 확인할 수 있었다.FIG. 5 is an image of the shape in which the FITC-treated nanolipid transporter is absorbed in the ruptured tissue, and it can be seen that the nanolipid transporter is absorbed along the hair of the hair follicle, and gradually moves from the inside of the hair follicle to the dermis. It was confirmed that the lipid transporter was being absorbed.
[시험예 6] 나노지질전달체 피부흡수력 실험[Test Example 6] Nanolipid transporter skin absorption capacity test
실시예 1의 나노지질전달체와 생리활성물질 수용액을 피부투과장치(Franz Diffusion Cell)에 고정되어있는 Micropig Membrane에 각각 도포하여 나노지질전달체의 흡수량을 확인하였다.The nanolipid transporter of Example 1 and the physiologically active substance aqueous solution were respectively applied to a micropig membrane fixed to a skin diffusion device (Franz Diffusion Cell) to confirm the absorption amount of the nanolipid transporter.
인공피부를 투과한 나노지질전달체를 전처리를 수행하였다. 구체적으로, 인공피부를 투과한 나노지질전달체를 파괴하기 위해 에탄올 2.5ml와 클로로포름 2ml, 정제수 0.5ml에 시료 1ml를 첨가하여 voltexing후, 4000 rpm으로 10분간 원심분리하여 상층액만 추출하였다. 상기 전처리된 나노지질전달체로부터 유효성분을 추출하여 HPLC를 통해 함량 분석을 진행하였다. The nanolipid transporter that penetrated the artificial skin was pretreated. Specifically, 1 ml of the sample was added to 2.5 ml of ethanol, 2 ml of chloroform, and 0.5 ml of purified water to destroy the nanolipid transporter that penetrated the artificial skin, followed by voltexing, and centrifuged at 4000 rpm for 10 minutes to extract only the supernatant. The active ingredient was extracted from the pre-treated nanolipid transporter and content analysis was performed through HPLC.
HPLC를 통한 함량 분석 결과는 표 6, 표 7 및 도 6에 도시하였다. 구체적으로 표 6은 각 시간대별 흡수량을 나타내고 있다.Content analysis results through HPLC are shown in Table 6, Table 7 and FIG. 6. Specifically, Table 6 shows the absorption amount for each time zone.
도 6은 실시예 1의 나노지질전달체와 생리활성물질 수용액의 시간대별 흡수된 함량을 분석한 그래프로, 각 시간대별로 나노지질전달체를 도포한 실험군에서 높은 흡수율과 빠른 흡수 시간대를 갖는 것을 확인하였다. 특히 최초 투여 후 2시간 경과시에는 대조군 대비 2배 가까이 빠른 누적 투과량을 나타내어, 최초 투여시 즉각적인 투여 효과를 나타내는 새로운 효과를 발견하였다.FIG. 6 is a graph analyzing the absorbed content of the nanolipid transporter of Example 1 and the aqueous solution of physiologically active substances over time, and was confirmed to have a high absorption rate and a fast absorption time zone in the experimental group coated with the nanolipid transporter for each time zone. Particularly, 2 hours after the first administration, a cumulative permeation amount was almost twice as fast as the control group, and a new effect was found, indicating an immediate administration effect upon the first administration.
상기 결과로부터 본 발명을 통한 나노지질전달체는 장기간동안 생리활성물질이 외부로 유출되지 않고 안정적인 구조를 유지할 수 있으며, 생리활성물질의 봉입 효율이 대조군 대비 현저히 우수할 뿐만 아니라, 피부 투여시 누적 투과량이 생리활성물질을 직접 투여한 경우 대비 약 36% 이상 높고, 모낭에 투여시 일반 피부 대비 2배 이상으로 현저히 높은 투과 속도를 갖는 것을 확인하였다. 이로부터, 본 발명의 나노지질전달체의 모낭 타게팅약물 전달체로서의 우수한 효과를 가지는 것을 확인하였다.From the above results, the nanolipid transporter through the present invention can maintain a stable structure without spilling physiologically active substances to the outside for a long period of time, and the encapsulation efficiency of the physiologically active substances is not only excellent compared to the control group, but also the cumulative permeation amount during skin administration It was confirmed that the physiologically active substance was about 36% higher than the direct administration, and when administered to the hair follicles, it had a remarkably high permeation rate twice or more compared to normal skin. From this, it was confirmed that the nanolipid delivery system of the present invention has an excellent effect as a follicle targeting drug delivery system.
Claims (5)
상기 코어의 표면 상에 위치하며 지질을 포함하는 쉘부;를 포함하고, 상기 코어부는 인지질을 더 포함하는 나노지질전달체.A core portion comprising a hydrophilic polymer complex containing a bioactive substance and a hydrophilic polymer; And
Located on the surface of the core and the shell portion containing a lipid; includes, the core portion nanolipid transporter further comprises a phospholipid.
상기 지질 및 인지질은 중량비로 100:0.1 내지 100:50으로 포함되는, 나노지질전달체.According to claim 1,
The lipid and phospholipids are included in a weight ratio of 100:0.1 to 100:50, nanolipid transporter.
상기 생리활성물질 및 친수성 고분자는 중량비로 2000:1 내지 20:1으로 포함되는, 나노지질전달체.According to claim 1,
The bioactive material and the hydrophilic polymer are contained in a weight ratio of 2000:1 to 20:1, nanolipid transporter.
상기나노지질전달체는 20 nm 내지 1000 nm의 평균 입경을 가지며 하기 관계식 1을 만족하는, 나노지질전달체.
[관계식 1]
|T0-T20|/T0< 0.2
(상기 관계식 1에서 T0는 나노지질전달체 1중량% 수분산액의 제조 후 500 nm 파장에서 측정된 투과도를 의미하며, T20은 나노지질전달체 1중량% 수분산액을 45℃에서 20일 방치 후 500 nm 파장에서 측정된 투과도를 의미한다.)According to claim 1,
The nanolipid transporter has an average particle diameter of 20 nm to 1000 nm, and satisfies the following relationship 1, nanolipid transporter.
[Relationship 1]
|T 0 -T 20 |/T 0 <0.2
(In the above equations 1 T 0 after the production of nano-lipid delivery system of 1% aqueous dispersion by weight means a permeability measured at 500 nm wavelength, and, T 20 are 500 then the nano-lipid delivery system of 1% aqueous dispersion by weight to stand at 45 ℃ 20 il It means transmittance measured at nm wavelength.)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020190130504A KR102190935B1 (en) | 2019-10-21 | 2019-10-21 | Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020190130504A KR102190935B1 (en) | 2019-10-21 | 2019-10-21 | Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020180157119A Division KR102037354B1 (en) | 2018-12-07 | 2018-12-07 | Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20200070091A true KR20200070091A (en) | 2020-06-17 |
| KR102190935B1 KR102190935B1 (en) | 2020-12-15 |
Family
ID=71405879
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020190130504A KR102190935B1 (en) | 2019-10-21 | 2019-10-21 | Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102190935B1 (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102510870B1 (en) * | 2022-12-14 | 2023-03-17 | 유스킨컴퍼니 주식회사 | Composition for promoting hair growth containing peptides |
| KR102653697B1 (en) * | 2024-01-08 | 2024-04-03 | 주식회사 비스코스 | Composition for improving scalp and hair loss and manufacturing thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101054731B1 (en) | 2004-06-16 | 2011-08-05 | (주)아모레퍼시픽 | Nanoparticles comprising finasteride, a poorly soluble hair growth and hair growth bioactive substance, and an external composition for skin containing the same |
| KR101377710B1 (en) | 2012-02-02 | 2014-03-21 | 강원대학교산학협력단 | Cubic phase nanoparticles enhancing the hair growth-promoting efficacies of herbal extracts and method for preparing the same |
| KR101810160B1 (en) | 2017-06-30 | 2018-01-25 | 주식회사 셀리제코스메틱 | Generating method for ethosome with bioactive compounds, ethosome and cosmetic composition including ethosome |
-
2019
- 2019-10-21 KR KR1020190130504A patent/KR102190935B1/en active IP Right Grant
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101054731B1 (en) | 2004-06-16 | 2011-08-05 | (주)아모레퍼시픽 | Nanoparticles comprising finasteride, a poorly soluble hair growth and hair growth bioactive substance, and an external composition for skin containing the same |
| KR101377710B1 (en) | 2012-02-02 | 2014-03-21 | 강원대학교산학협력단 | Cubic phase nanoparticles enhancing the hair growth-promoting efficacies of herbal extracts and method for preparing the same |
| KR101810160B1 (en) | 2017-06-30 | 2018-01-25 | 주식회사 셀리제코스메틱 | Generating method for ethosome with bioactive compounds, ethosome and cosmetic composition including ethosome |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102510870B1 (en) * | 2022-12-14 | 2023-03-17 | 유스킨컴퍼니 주식회사 | Composition for promoting hair growth containing peptides |
| KR102653697B1 (en) * | 2024-01-08 | 2024-04-03 | 주식회사 비스코스 | Composition for improving scalp and hair loss and manufacturing thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102190935B1 (en) | 2020-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102037354B1 (en) | Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof | |
| Elnaggar et al. | Lecithin-based nanostructured gels for skin delivery: an update on state of art and recent applications | |
| EP1410790B1 (en) | Submicron-liposome containing triterpenoid and a method for preparing the same | |
| JP4758915B2 (en) | Multilamellar liposome and production method thereof | |
| US5665379A (en) | Lipid particle forming matrix, preparation and use thereof | |
| JP4237446B2 (en) | Method for stabilizing nano-emulsified particles using tocopherol derivative and skin external preparation composition containing nano-emulsified particles | |
| S Duttagupta et al. | Cubosomes: innovative nanostructures for drug delivery | |
| KR100921959B1 (en) | Multi-Emulsified Vesicles Comprising a Multi Lamellar Liposome and Phospholipid Monolayer Nanoliposomes | |
| JP3599114B2 (en) | Phospholipid- and fluorocarbon-containing cosmetics | |
| EP0514506B1 (en) | Lipid formulation system | |
| KR102190935B1 (en) | Nano-lipid carrier for encapsulation of physiologically active substance and preparation method thereof | |
| KR20130011800A (en) | O/w emulsion having skin lipid and cosmetic composition comprising the same | |
| JP2009173610A (en) | Protein nanoparticles | |
| JP2008179551A (en) | Preparation for percutaneous absorption | |
| Awasthi et al. | Frontier lipid-based carrier systems for drug targeting: A laconic review on niosomes | |
| KR20120114730A (en) | Microemulsion as a transdermal delivery system comprising gamma oryzanol | |
| JP3834563B2 (en) | Method for producing stable nano-emulsified particles using arbutin and cosmetic composition containing nano-emulsified particles | |
| KR102632679B1 (en) | Hyaluronic Acid Loading Nano Particle Complex And A Method For Preparing The Same | |
| Hu et al. | Current advances in sustained-release injectable preparations | |
| WO2024090548A1 (en) | Hydroxyapatite-particle-containing material, liposome having enclosed hydroxyapatite, and liposome-containing composition | |
| KR102611802B1 (en) | A hybrid multilamellar nanostructure of insulin-like growth factor 1 and liposome and a preparation method of the same | |
| KR102266329B1 (en) | Nano-liposome Comprising Idebenone and Bisabolol | |
| Kaushik et al. | Nanostructured Lipids as a Bioactive Compound Carrier | |
| KR100690103B1 (en) | Method for preparing phytosphingosine liposome composition | |
| Carrier et al. | Nanostructured Lipids as |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |