KR20190066037A - 샘플을 테스트하기 위한 분석 시스템 및 방법 - Google Patents
샘플을 테스트하기 위한 분석 시스템 및 방법 Download PDFInfo
- Publication number
- KR20190066037A KR20190066037A KR1020197012881A KR20197012881A KR20190066037A KR 20190066037 A KR20190066037 A KR 20190066037A KR 1020197012881 A KR1020197012881 A KR 1020197012881A KR 20197012881 A KR20197012881 A KR 20197012881A KR 20190066037 A KR20190066037 A KR 20190066037A
- Authority
- KR
- South Korea
- Prior art keywords
- sensor
- nucleic acid
- capture
- target
- assay
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 72
- 238000012360 testing method Methods 0.000 title claims abstract description 51
- 238000004458 analytical method Methods 0.000 title claims description 138
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 251
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 251
- 150000007523 nucleic acids Chemical group 0.000 claims abstract description 190
- 238000003556 assay Methods 0.000 claims abstract description 98
- 108091023037 Aptamer Proteins 0.000 claims abstract description 89
- 238000002731 protein assay Methods 0.000 claims abstract description 76
- 238000007826 nucleic acid assay Methods 0.000 claims abstract description 68
- 239000012472 biological sample Substances 0.000 claims abstract description 7
- 239000000523 sample Substances 0.000 claims description 161
- 238000011156 evaluation Methods 0.000 claims description 118
- 239000012491 analyte Substances 0.000 claims description 86
- 239000012530 fluid Substances 0.000 claims description 85
- 238000006243 chemical reaction Methods 0.000 claims description 78
- 230000003321 amplification Effects 0.000 claims description 55
- 238000003199 nucleic acid amplification method Methods 0.000 claims description 55
- 238000001514 detection method Methods 0.000 claims description 54
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 42
- 238000004925 denaturation Methods 0.000 claims description 36
- 230000036425 denaturation Effects 0.000 claims description 36
- 108020004707 nucleic acids Proteins 0.000 claims description 16
- 102000039446 nucleic acids Human genes 0.000 claims description 16
- 108091032973 (ribonucleotides)n+m Proteins 0.000 claims description 12
- 230000001351 cycling effect Effects 0.000 claims description 11
- 230000008878 coupling Effects 0.000 claims description 3
- 238000010168 coupling process Methods 0.000 claims description 3
- 238000005859 coupling reaction Methods 0.000 claims description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 52
- 239000000047 product Substances 0.000 description 46
- 238000005259 measurement Methods 0.000 description 42
- 239000007788 liquid Substances 0.000 description 31
- 238000010438 heat treatment Methods 0.000 description 29
- 239000000758 substrate Substances 0.000 description 28
- 238000009396 hybridization Methods 0.000 description 24
- 239000000126 substance Substances 0.000 description 24
- 230000000694 effects Effects 0.000 description 19
- 239000000275 Adrenocorticotropic Hormone Substances 0.000 description 18
- 102400000739 Corticotropin Human genes 0.000 description 18
- 101800000414 Corticotropin Proteins 0.000 description 18
- IDLFZVILOHSSID-OVLDLUHVSA-N corticotropin Chemical compound C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(O)=O)NC(=O)[C@@H](N)CO)C1=CC=C(O)C=C1 IDLFZVILOHSSID-OVLDLUHVSA-N 0.000 description 18
- 229960000258 corticotropin Drugs 0.000 description 18
- 238000002156 mixing Methods 0.000 description 18
- 239000007789 gas Substances 0.000 description 17
- 239000000463 material Substances 0.000 description 14
- 150000003431 steroids Chemical class 0.000 description 14
- 108020004414 DNA Proteins 0.000 description 13
- 238000002848 electrochemical method Methods 0.000 description 13
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 12
- 230000008569 process Effects 0.000 description 12
- 238000001035 drying Methods 0.000 description 11
- 239000000243 solution Substances 0.000 description 11
- 239000003298 DNA probe Substances 0.000 description 9
- PLIKAWJENQZMHA-UHFFFAOYSA-N 4-aminophenol Chemical compound NC1=CC=C(O)C=C1 PLIKAWJENQZMHA-UHFFFAOYSA-N 0.000 description 8
- 229940088597 hormone Drugs 0.000 description 8
- 239000005556 hormone Substances 0.000 description 8
- 238000002844 melting Methods 0.000 description 8
- 230000008018 melting Effects 0.000 description 8
- 239000011534 wash buffer Substances 0.000 description 8
- 102000004190 Enzymes Human genes 0.000 description 7
- 108090000790 Enzymes Proteins 0.000 description 7
- 239000002299 complementary DNA Substances 0.000 description 7
- 239000003550 marker Substances 0.000 description 7
- 239000012723 sample buffer Substances 0.000 description 7
- 238000011144 upstream manufacturing Methods 0.000 description 7
- 239000000427 antigen Substances 0.000 description 6
- 108091007433 antigens Proteins 0.000 description 6
- 102000036639 antigens Human genes 0.000 description 6
- 229960002685 biotin Drugs 0.000 description 6
- 235000020958 biotin Nutrition 0.000 description 6
- 239000011616 biotin Substances 0.000 description 6
- 239000000872 buffer Substances 0.000 description 6
- 201000010099 disease Diseases 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 244000052769 pathogen Species 0.000 description 6
- 238000005406 washing Methods 0.000 description 6
- 102000053602 DNA Human genes 0.000 description 5
- 241001465754 Metazoa Species 0.000 description 5
- 108020004682 Single-Stranded DNA Proteins 0.000 description 5
- 238000004140 cleaning Methods 0.000 description 5
- 238000005086 pumping Methods 0.000 description 5
- 150000003384 small molecules Chemical class 0.000 description 5
- ZYPZVOKVDNSKLP-UHFFFAOYSA-N tris(4-aminophenyl) phosphate Chemical compound C1=CC(N)=CC=C1OP(=O)(OC=1C=CC(N)=CC=1)OC1=CC=C(N)C=C1 ZYPZVOKVDNSKLP-UHFFFAOYSA-N 0.000 description 5
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 4
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 4
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 4
- 108091034117 Oligonucleotide Proteins 0.000 description 4
- 108010090804 Streptavidin Proteins 0.000 description 4
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 239000013642 negative control Substances 0.000 description 4
- 238000003752 polymerase chain reaction Methods 0.000 description 4
- 239000013641 positive control Substances 0.000 description 4
- 238000007725 thermal activation Methods 0.000 description 4
- 108020003215 DNA Probes Proteins 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- -1 and / Proteins 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 238000003891 environmental analysis Methods 0.000 description 3
- 230000007613 environmental effect Effects 0.000 description 3
- 235000021317 phosphate Nutrition 0.000 description 3
- 238000006479 redox reaction Methods 0.000 description 3
- 150000003839 salts Chemical class 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 2
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 2
- 238000012408 PCR amplification Methods 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000003750 conditioning effect Effects 0.000 description 2
- 238000000835 electrochemical detection Methods 0.000 description 2
- 238000011049 filling Methods 0.000 description 2
- 238000011010 flushing procedure Methods 0.000 description 2
- 238000003018 immunoassay Methods 0.000 description 2
- 229910001629 magnesium chloride Inorganic materials 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 239000005445 natural material Substances 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 150000002903 organophosphorus compounds Chemical class 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 210000003296 saliva Anatomy 0.000 description 2
- 238000005070 sampling Methods 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 210000002700 urine Anatomy 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 108020004635 Complementary DNA Proteins 0.000 description 1
- 102100034343 Integrase Human genes 0.000 description 1
- 230000010802 Oxidation-Reduction Activity Effects 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 238000010170 biological method Methods 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 238000004820 blood count Methods 0.000 description 1
- 238000007664 blowing Methods 0.000 description 1
- 238000010804 cDNA synthesis Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 235000019878 cocoa butter replacer Nutrition 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 229940127121 immunoconjugate Drugs 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 229910000510 noble metal Inorganic materials 0.000 description 1
- 239000002777 nucleoside Substances 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 230000002572 peristaltic effect Effects 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 239000002574 poison Substances 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 238000007781 pre-processing Methods 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000011535 reaction buffer Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- 150000003573 thiols Chemical class 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000017105 transposition Effects 0.000 description 1
- 239000001226 triphosphate Substances 0.000 description 1
- 235000011178 triphosphate Nutrition 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502761—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip specially adapted for handling suspended solids or molecules independently from the bulk fluid flow, e.g. for trapping or sorting beads, for physically stretching molecules
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
- C12Q1/6825—Nucleic acid detection involving sensors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/28—Electrolytic cell components
- G01N27/30—Electrodes, e.g. test electrodes; Half-cells
- G01N27/327—Biochemical electrodes, e.g. electrical or mechanical details for in vitro measurements
- G01N27/3275—Sensing specific biomolecules, e.g. nucleic acid strands, based on an electrode surface reaction
- G01N27/3277—Sensing specific biomolecules, e.g. nucleic acid strands, based on an electrode surface reaction being a redox reaction, e.g. detection by cyclic voltammetry
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54366—Apparatus specially adapted for solid-phase testing
- G01N33/54373—Apparatus specially adapted for solid-phase testing involving physiochemical end-point determination, e.g. wave-guides, FETS, gratings
- G01N33/5438—Electrodes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0627—Sensor or part of a sensor is integrated
- B01L2300/0636—Integrated biosensor, microarrays
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0819—Microarrays; Biochips
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/18—Means for temperature control
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L7/00—Heating or cooling apparatus; Heat insulating devices
- B01L7/52—Heating or cooling apparatus; Heat insulating devices with provision for submitting samples to a predetermined sequence of different temperatures, e.g. for treating nucleic acid samples
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Analytical Chemistry (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- Hematology (AREA)
- Biochemistry (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pathology (AREA)
- Zoology (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Urology & Nephrology (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- General Physics & Mathematics (AREA)
- Clinical Laboratory Science (AREA)
- Dispersion Chemistry (AREA)
- Biophysics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Electrochemistry (AREA)
- Cell Biology (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Fluid Mechanics (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Automatic Analysis And Handling Materials Therefor (AREA)
Abstract
Description
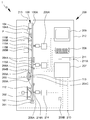
도 1은 제안된 분석 디바이스 및 분석 디바이스에 수용되는 제안된 카트리지를 포함하는 제안된 분석 시스템의 개략도;
도 2는 카트리지의 개략도;
도 3은 분석 시스템 및/또는 카트리지의 센서 장치의 개략 정면도;
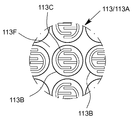
도 4는 센서 장치의 센서 필드를 도시하는 도 3의 확대 상세도;
도 5는 센서 장치의 개략 배면도;
도 6은 센서 장치 및 더욱 멀리 이동된 센서 커버를 포함하는 분석 시스템 및/또는 카트리지의 센서 배열의 개략 단면도;
도 7은 센서 커버가 하강된, 도 6에 따른 센서 배열의 개략 단면도;
도 8은 단백질 분석 평가가 수행된 후의 센서 배열의 개략 단면도;
도 9는 핵산 분석이 수행되는 동안 센서 배열의 개략 단면도;
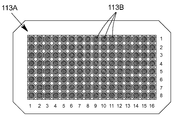
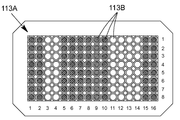
도 10a는 센서 장치의 센서 어레이의 센서 필드의 점유의 개략도;
도 10b는 센서 필드의 형광 측정의 도 10a에 대응하는 개략도;
도 10c는 센서 필드의 다른 형광 측정의 도 10a에 대응하는 개략도;
도 11a는 센서 어레이의 제1 전기 화학적 측정의 그래프;
도 11b는 센서 어레이의 제2 전기 화학적 측정의 그래프;
도 11c는 센서 어레이의 제3 전기 화학적 측정의 그래프; 및
도 12는 상이한 포획 분자들를 포함하는 센서 배열의 도 6에 대응하는 개략 단면도.
101 : 본체 102 : 커버
103 : 유체 시스템 104 : 수용 캐비티
104A : 연결부 104B : 입구
104C : 출구 104D : 중간 연결부
105 : 계량 캐비티 105A : 제1 계량 캐비티
105B : 제2 계량 캐비티 106(A-G) : 중간 캐비티
107 : 혼합 캐비티 108(A-E) : 저장 캐비티
109 : 반응 캐비티 109A : 제1 반응 캐비티
109B : 제2 반응 캐비티 109C : 제3 반응 캐비티
110 : 중간 온도 제어 캐비티 110A : 입구
110B : 출구 111 : 수집 캐비티
112 : 펌프 장치 113 : 센서 장치
113A : 센서 어레이 113B : 센서 필드
113C : 전극 113D : 지지부
113E : 접촉부 113F : 층
114 : 채널 114A : 바이패스
115 : 밸브 115A : 초기 폐쇄 밸브
115B : 초기 개방 밸브 116 : 센서 부분
117 : 센서 커버 118 : 센서 구획
119 : 입구 120 : 출구
200 : 분석 디바이스 201 : 리셉터클
202 : 펌프 드라이브 203 : 연결 장치
203A : 연결 요소 204 : 온도 제어 장치
204A : 반응 온도 제어 장치 204B : 중간 온도 제어 장치
204C : 센서 온도 제어 장치 205 : (밸브) 액튜에이터
205A : 115A를 위한 (밸브) 액튜에이터
205B : 115B를 위한 (밸브) 액튜에이터 206 : 센서
206A : 유체 센서 206B : 다른 센서
207 : 제어 장치 208 : 입력 장치
209 : 디스플레이 장치 210 : 인터페이스
211 : 전력 공급부 211A : 연결부
212 : 하우징 213 : 개구
214 : 가압 가스 공급부 214A : 연결 요소
B : 결합제 D : 검출기 분자
F(1-5) : 액체 시약 FP : 포획 단백질
FN(1-2) : 포획 핵산 서열 L : 라벨
P : 샘플 S(1-10) : 건조 시약
SA : 제1 물질 SP : 제2 물질
SU : 기재 ZP(1-2) : 표적 단백질
ZN(1-2) : 표적 핵산 서열
Claims (31)
- 분석 시스템(1)이 복수의 채널(114)을 가지는 유체 시스템(103), 및 샘플(P)의 피분석물들을 결합하기 위한 포획 분자들을 포함하는 센서 장치(113)를 포함하며,
상기 센서 장치(113)는 복수의 센서 필드(113B)들 및/또는 전극(113C)들을 가지는 센서 어레이(113A)를 가지는, 특히 생물학적 샘플(P)을 테스트하기 위한 분석 시스템(1)에 있어서,
상기 센서 어레이(113A)에는 포획 단백질(FP)들, 포획 앱타머(FA)들 및/또는 포획 핵산 서열(FN)들로 이루어진 선택 그룹으로부터의 적어도 2개의 형태으로부터 선택된 포획 분자들이 제공되며, 및/또는
상기 센서 어레이(113A)는 제1 그룹의 포획 분자(FP, FA)들 및 제2 그룹의 포획 분자(FN)들을 포함하고, 상기 제1 그룹의 포획 분자(FP, FA)들은 피분석물들을 결합하기 위하여 열적으로 활성화될 수 있거나, 또는 온도 제어 장치(204B, 204C)에 의해 피분석물들의 결합을 방지하기 위해 열적으로 비활성화되고 및/또는 변성될 수 있는 것을 특징으로 하는 분석 시스템. - 제1항에 있어서, 상기 분석 시스템(1)은 상기 표적 핵산 서열(FN)들을 증폭시키기 위한 적어도 하나의 반응 캐비티(109)를 포함하는 것을 특징으로 하는 분석 시스템.
- 제2항에 있어서, 상기 분석 시스템(1)은 상기 반응 캐비티(109)를 지나서 상기 샘플(P) 또는 상기 표적 단백질(ZP)들의 일부를 전도하기 위하여 상기 반응 캐비티(109) 주위의 바이패스(114A)를 포함하는 것을 특징으로 하는 분석 시스템.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 상기 센서 장치(113)는 상기 포획 분자들에 결합된 피분석물들을 전기 화학적으로 검출하기 위해 설계되는 것을 특징으로 하는 분석 시스템.
- 제4항에 있어서, 모든 또는 일부 센서 필드(113B)들 및/또는 전극(113C)들에는 포획 단백질(FP)들, 포획 앱타머(FA)들 및/또는 포획 핵산 서열(FN)들로 이루어진 선택 그룹으로부터의 적어도 2개의 형태으로부터 선택된 포획 분자들이 각각 제공되는 것을 특징으로 하는 분석 시스템.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 상기 분석 시스템(1) 및/또는 상기 센서 장치(113)는 단백질 분석 평가, 핵산 분석 평가 및/또는 앱타머 분석 평가를 특히 순차적으로 수행하기 위해 설계되는 것을 특징으로 하는 분석 시스템.
- 제1항 내지 제6항 중 어느 한 항에 있어서, 상기 분석 시스템(1)은 상기 포획 분자들을 온도 제어하기 위한 온도 제어 장치(204B, 204C)를 포함하는 것을 특징으로 하는 분석 시스템.
- 제7항에 있어서, 상기 분석 시스템(1) 및/또는 상기 온도 제어 장치(204B, 204C)는 바람직하게 40℃ 보다 높은 온도 및/또는 70℃보다 낮은 온도에서 하이브리드화된 표적 단백질(ZP)들 및/또는 포획 단백질(FP)들을 변성시키도록 설계되는 것을 특징으로 하는 분석 시스템.
- 제7항 또는 제8항에 있어서, 상기 분석 시스템(1) 및/또는 상기 온도 제어 장치(204B, 204C)는 바람직하게 90℃ 보다 높은 온도 및/또는 110℃보다 낮은 온도에서, 결합된 포획 핵산 서열(FN)들 및 표적 핵산 서열(FN)들을 서로로부터 분리하도록, 및/또는 상기 포획 앱타머(FA)들을 작동 및/또는 폴딩하도록 설계되는 것을 특징으로 하는 분석 시스템.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 상기 분석 시스템(1)은 상기 샘플(P)을 수용하기 위한 카트리지(100), 및 상기 카트리지(100)를 수용하기 위한 분석 디바이스(200)를 포함하는 것을 특징으로 하는 분석 시스템.
- 제10항에 있어서, 상기 카트리지(100)는 상기 센서 장치(113) 및/또는 반응 캐비티(109)를 포함하는 것을 특징으로 하는 분석 시스템.
- 제10항 또는 제11항에 있어서, 상기 분석 디바이스(200)는 상기 온도 제어 장치(204B, 204C)를 포함하는 것을 특징으로 하는 분석 시스템.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 상기 일부 또는 모든 센서 필드(113B) 및/또는 전극(113C)은 상기 제1 그룹의 포획 분자(FP, FA)들 및 상기 제2 그룹의 포획 분자(FN)들을 각각 포함하는 것을 특징으로 하는 분석 시스템.
- 샘플(P)의 피분석물들이 센서 장치(113)의 포획 분자들에 결합되고, 결합된 피분석물들이 상기 센서 장치(113)에 의해 검출되거나 또는 식별되는, 특히 생물학적 샘플(P)을 테스트하는 방법에 있어서,
단백질 분석 평가, 핵산 분석 평가 및/또는 앱타머 분석 평가로 이루어진 선택 그룹으로부터의 적어도 2개의 분석 평가로부터 선택된 복수의 분석 평가는 상기 센서 장치(113)의 공통 센서 어레이(113A)에서 상기 센서 장치(113)에 의해 수행되며, 및/또는
상기 샘플(P)의 피분석물들로서 표적 단백질(ZP)들 및 표적 핵산 서열(ZN)들 모두는 상기 센서 장치(113)의 공통 센서 어레이(113A)에서 대응하는 포획 분자들에 결합되고 검출되거나 또는 식별되는 것을 특징으로 하는 방법. - 제14항에 있어서, 상기 샘플(P)은 카트리지(100)에 수용되고 부분들로 분할되며, 단백질 분석 평가, 핵산 분석 평가 및/또는 앱타머 분석 평가로 이루어진 선택 그룹으로부터의 적어도 2개의 분석 평가로부터 선택된 복수의 분석 평가는 동일한 카트리지(100) 및/또는 센서 장치(113)에서 수행되는 것을 특징으로 하는 방법.
- 제14항 또는 제15항에 있어서, 포획 분자(FP, FA)들의 그룹은 피분석물들을 결합할 수 있도록 열적으로 활성화되거나, 또는 어떠한 피분석물도 결합하지 않도록 열적으로 비활성화되고 및/또는 변성되는 것을 특징으로 하는 방법.
- 제16항에 있어서, 하나의 분석 평가는 포획 분자(FP, FA)들의 그룹에 의해 수행되고, 다른 분석 평가는 다른 포획 분자(FN)들의 다른 그룹에 의해 수행되는 것을 특징으로 하는 방법.
- 제14항 내지 제17항 중 어느 한 항에 있어서, 상기 단백질 분석 평가는 상기 핵산 분석 평가 전에 수행되는 것을 특징으로 하는 방법.
- 제14항 내지 제18항 중 어느 한 항에 있어서, 상기 핵산 분석 평가는 상기 앱타머 분석 평가 전에 수행되는 것을 특징으로 하는 방법.
- 제14항 내지 제19항 중 어느 한 항에 있어서, 상기 단백질 분석 평가, 상기 핵산 분석 평가 및/또는 상기 앱타머 분석 평가는 상기 센서 장치(113)의 공통 센서 어레이(113A)에서 수행되는 것을 특징으로 하는 방법.
- 제14항 내지 제20항 중 어느 한 항에 있어서, 특히 상기 단백질 분석 평가 동안, 상기 표적 피분석물들 및/또는 표적 단백질(ZP)들은 복수의 채널(114)을 가지는 유체 시스템(103)을 통해 상기 센서 장치(113)에 공급되는 것을 특징으로 하는 방법.
- 제14항 내지 제21항 중 어느 한 항에 있어서, 특히 상기 단백질 분석 평가 동안, 상기 표적 피분석물들 및/또는 표적 단백질(ZP)들은 포획 분자들로서 대응하는 포획 단백질(FP)들에 결합되는 것을 특징으로 하는 방법.
- 제14항 내지 제22항 중 어느 한 항에 있어서, 특히 단백질 분석 평가 동안, 상기 표적 피분석물들 및/또는 표적 단백질(ZP)들은 전기 화학적으로 및/또는 산화환원 사이클링에 의해 식별되거나 또는 검출되는 것을 특징으로 하는 방법.
- 제14항 내지 제23항 중 어느 한 항에 있어서, 서로 결합되는 상기 포획 단백질(FP)들 및 표적 피분석물들 및/또는 표적 단백질(ZP)들은 검출 후에 및/또는 상기 단백질 분석 평가가 수행된 후에 열의 추가에 의해 변성되는 것을 특징으로 하는 방법.
- 제14항 내지 제24항 중 어느 한 항에 있어서, 서로 결합되는 상기 포획 단백질(FP)들 및 표적 피분석물들 및/또는 표적 단백질(ZP)들은 검출 후에 및/또는 상기 단백질 분석 평가가 수행된 후에 상기 센서 장치(113)로부터 제거되는 것을 특징으로 하는 방법.
- 제14항 내지 제25항 중 어느 한 항에 있어서, 상기 센서 장치(113)는 특히 바람직하게 40℃ 보다 높은 온도 및/또는 70℃보다 낮은 온도에서, 특히 서로 결합된 상기 포획 단백질(FP)들 및 표적 피분석물들 및/또는 표적 단백질(ZP)들을 변성시키기 위하여, 상기 단백질 분석 평가가 수행된 후에 가열되는 것을 특징으로 하는 방법.
- 제14항 내지 제26항 중 어느 한 항에 있어서, 특히 상기 핵산 분석 평가 동안, 상기 표적 핵산 서열(ZN)들, 특히 표적 DNA 서열들 또는 표적 RNA 서열들은 증폭 반응, 특히 PCR에 의해 반응 캐비티(109)에서 증폭되는 것을 특징으로 하는 방법.
- 제14항 내지 제27항 중 어느 한 항에 있어서, 상기 표적 핵산 서열(ZN)들은 복수의 채널(114)을 가지는 유체 시스템(103)을 통해 상기 센서 장치(113)에 공급되는 것을 특징으로 하는 방법.
- 제14항 내지 제28항 중 어느 한 항에 있어서, 상기 표적 핵산 서열(ZN)들은 포획 분자들로서 상기 대응하는 포획 핵산 서열(FN)들에 결합되는 것을 특징으로 하는 방법.
- 제14항 내지 제29항 중 어느 한 항에 있어서, 상기 표적 핵산 서열(ZN)들은 전기 화학적으로 및/또는 산화환원 사이클링에 의해 식별되거나 또는 검출되는 것을 특징으로 하는 방법.
- 제14항 내지 제30항 중 어느 한 항에 있어서, 복수의 표적 단백질(ZP) 및 복수의 표적 핵산 서열(ZN)은 센서 장치(113) 및/또는 상기 센서 어레이(113A)의 공통 센서 필드(113B)에 있는, 특히 상기 센서 장치(113) 및/또는 상기 센서 어레이(113A)의 공통 전극(113C) 상의 상기 대응하는 포획 분자들에 바람직하게 순차적으로 결합되며, 바람직하게 순차적으로 검출되거나 또는 식별되는 것을 특징으로 하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP16020373 | 2016-10-07 | ||
| EP16020373.3 | 2016-10-07 | ||
| PCT/EP2017/025281 WO2018065104A1 (en) | 2016-10-07 | 2017-10-05 | Analysis system and method for testing a sample |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20190066037A true KR20190066037A (ko) | 2019-06-12 |
Family
ID=57132954
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020197012881A KR20190066037A (ko) | 2016-10-07 | 2017-10-05 | 샘플을 테스트하기 위한 분석 시스템 및 방법 |
Country Status (8)
| Country | Link |
|---|---|
| US (2) | US10597703B2 (ko) |
| EP (1) | EP3523030B1 (ko) |
| JP (1) | JP2019536441A (ko) |
| KR (1) | KR20190066037A (ko) |
| CN (1) | CN110114145B (ko) |
| BR (1) | BR112019007081A2 (ko) |
| CA (1) | CA3037217A1 (ko) |
| WO (1) | WO2018065104A1 (ko) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111108217A (zh) * | 2017-09-29 | 2020-05-05 | 勃林格殷格翰维特梅迪卡有限公司 | 用于测试样品的传感器装置和方法 |
| MX2020006327A (es) | 2017-12-20 | 2020-09-17 | Boehringer Ingelheim Vetmedica Gmbh | Deteccion de vacunas vivas modificadas contra el virus de la gripe porcina. |
| WO2021067779A1 (en) * | 2019-10-04 | 2021-04-08 | University Of Cincinnati | Shelf-stable, ready-to-use, electrochemical aptamer sensors |
| WO2022128917A1 (en) | 2020-12-14 | 2022-06-23 | Boehringer Ingelheim Vetmedica Gmbh | Analysis system and method for testing a sample |
| WO2023210026A1 (en) * | 2022-04-26 | 2023-11-02 | The University Of Tokyo | Sensor |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5096669A (en) | 1988-09-15 | 1992-03-17 | I-Stat Corporation | Disposable sensing device for real time fluid analysis |
| WO2000034521A1 (en) * | 1998-12-08 | 2000-06-15 | Boston Probes, Inc. | Methods, kits and compositions for the identification of nucleic acids electrostatically bound to matrices |
| CA2358699A1 (en) * | 1999-01-25 | 2000-07-27 | Ut-Battelle, Llc | Advanced multifunctional/multispectral biosensor devices and methods of use |
| US6942771B1 (en) * | 1999-04-21 | 2005-09-13 | Clinical Micro Sensors, Inc. | Microfluidic systems in the electrochemical detection of target analytes |
| AT410444B (de) | 2001-03-02 | 2003-04-25 | Oesterr Forsch Seibersdorf | Verfahren zur detektion von nukleinsäuremolekülen |
| DE10111457B4 (de) | 2001-03-09 | 2006-12-14 | Siemens Ag | Diagnoseeinrichtung |
| EP1439910A2 (en) | 2001-07-26 | 2004-07-28 | Motorola, Inc. | System and methods for mixing within a microfluidic device |
| DE502004003698D1 (de) | 2003-05-13 | 2007-06-14 | Siemens Ag | Schaltkreisanordnung zur potentialkonstanthaltung an einem biosensor und zur digitalisierung des messstroms |
| EP1712916A4 (en) * | 2003-12-26 | 2008-07-23 | Matsushita Electric Ind Co Ltd | DEVICE FOR THE DISTINCTION OF BIOLOGICAL SAMPLES, METHOD FOR THE DISTINCTION OF BIOLOGICAL SAMPLES AND PLATE FOR THE DISTINCTION OF BIOLOGICAL SAMPLES |
| DK1883474T3 (da) | 2005-05-25 | 2021-06-21 | Boehringer Ingelheim Vetmedica Gmbh | System til integreret og automatiseret dna- eller proteinanalyse og fremgangsmåde til at drive et sådan system |
| DE102005059535B4 (de) | 2005-12-13 | 2010-01-14 | Siemens Ag | Vorrichtung und Verfahren zur Durchführung eines Nukleinsäure-Tests, sowie Verfahren zur Herstellung einer solchen Vorrichtung |
| GB2436616A (en) | 2006-03-29 | 2007-10-03 | Inverness Medical Switzerland | Assay device and method |
| WO2008147382A1 (en) | 2006-09-27 | 2008-12-04 | Micronics, Inc. | Integrated microfluidic assay devices and methods |
| EP1947197A1 (en) | 2007-08-24 | 2008-07-23 | Siemens Aktiengesellschaft, A German Corporation | Method for the amplification of at least one nucleic acid |
| US8741815B2 (en) | 2008-02-19 | 2014-06-03 | Intelligent Bio Systems, Inc. | Methods and devices for amplification of nucleic acid |
| NZ595174A (en) * | 2009-03-13 | 2013-04-26 | Univ California | Prebiotic galacto oligosaccharides used to stimulate growth or colonisation of beneficial bifidobacterium bacteria in gut |
| US10022696B2 (en) | 2009-11-23 | 2018-07-17 | Cyvek, Inc. | Microfluidic assay systems employing micro-particles and methods of manufacture |
| DE102011015184B4 (de) | 2010-06-02 | 2013-11-21 | Thinxxs Microtechnology Ag | Vorrichtung für den Transport kleiner Volumina eines Fluids, insbesondere Mikropumpe oder Mikroventil |
| EP3644058A1 (en) * | 2010-10-14 | 2020-04-29 | Meso Scale Technologies, LLC | Reagent storage in an assay device |
| US8614087B2 (en) * | 2011-05-02 | 2013-12-24 | Ibis Biosciences, Inc. | Multiple-analyte assay device and system |
| US20130067525A1 (en) | 2011-09-09 | 2013-03-14 | Pct International, Inc. | Service provisioning device with integrated cable modem |
| WO2013067525A2 (en) * | 2011-11-04 | 2013-05-10 | President And Fellows Of Harvard College | Self-regulating chemo-mechano-chemical systems |
| US20130203057A1 (en) | 2012-01-20 | 2013-08-08 | Biohelix Corporation | Step-wise detection of multiple target sequences in isothermal nucleic acid amplification reactions |
| WO2013161964A1 (ja) * | 2012-04-27 | 2013-10-31 | キリンホールディングス株式会社 | リガンドを高感度に検出する核酸分子並びに該核酸分子のスクリーニング方法および該核酸分子の感度の最適化方法 |
| US9217179B2 (en) * | 2012-05-24 | 2015-12-22 | The Governing Council Of The University Of Toronto | Systems and methods for multiplexed electrochemical detection |
| US9624532B2 (en) * | 2013-02-05 | 2017-04-18 | Neil Gordon | Ultra-sensitive detection of extremely low level biological analytes using electrochemical signal amplification and biosensor |
| KR102557135B1 (ko) * | 2013-03-11 | 2023-07-19 | 큐 헬스 인코퍼레이티드 | 분석물의 검출 및 정량을 위한 시스템 및 방법 |
| WO2015054546A1 (en) * | 2013-10-10 | 2015-04-16 | Song Diagnostic Research Llc. | Improved lateral flow assays |
| GB201320071D0 (en) | 2013-11-13 | 2013-12-25 | Univ Leuven Kath | Monitoring multiplex DNA amplification |
-
2017
- 2017-10-05 JP JP2019518541A patent/JP2019536441A/ja not_active Ceased
- 2017-10-05 US US15/725,332 patent/US10597703B2/en not_active Expired - Fee Related
- 2017-10-05 WO PCT/EP2017/025281 patent/WO2018065104A1/en unknown
- 2017-10-05 BR BR112019007081A patent/BR112019007081A2/pt not_active Application Discontinuation
- 2017-10-05 KR KR1020197012881A patent/KR20190066037A/ko not_active Application Discontinuation
- 2017-10-05 CN CN201780061349.8A patent/CN110114145B/zh not_active Expired - Fee Related
- 2017-10-05 CA CA3037217A patent/CA3037217A1/en not_active Abandoned
- 2017-10-05 EP EP17784848.8A patent/EP3523030B1/en active Active
-
2020
- 2020-02-07 US US16/784,446 patent/US10988799B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US10988799B2 (en) | 2021-04-27 |
| US20200172965A1 (en) | 2020-06-04 |
| EP3523030B1 (en) | 2021-05-05 |
| BR112019007081A2 (pt) | 2019-07-09 |
| US20180100188A1 (en) | 2018-04-12 |
| CN110114145B (zh) | 2022-08-09 |
| EP3523030A1 (en) | 2019-08-14 |
| WO2018065104A1 (en) | 2018-04-12 |
| JP2019536441A (ja) | 2019-12-19 |
| CA3037217A1 (en) | 2018-04-12 |
| US10597703B2 (en) | 2020-03-24 |
| CN110114145A (zh) | 2019-08-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10988799B2 (en) | Analysis system and method for testing a sample | |
| US20200164372A1 (en) | Analysis system for testing a sample | |
| CN109789412B (zh) | 用于检测样品的分析系统及方法 | |
| JP2019537705A5 (ko) | ||
| US10604792B2 (en) | Method and analysis system for testing a sample | |
| US11268134B2 (en) | Sensor apparatus and method for testing a sample | |
| US10953403B2 (en) | Method and analysis system for testing a sample | |
| WO2022128917A1 (en) | Analysis system and method for testing a sample | |
| EP3673083B1 (en) | Analysis system with cartridge and method for testing a sample |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20190503 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20200731 Comment text: Request for Examination of Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20220926 Patent event code: PE09021S01D |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20221129 Comment text: Decision to Refuse Application Patent event code: PE06012S01D Patent event date: 20220926 Comment text: Notification of reason for refusal Patent event code: PE06011S01I |