KR20170086455A - Preparation method of polyimide film, and the polyimide film thereby - Google Patents
Preparation method of polyimide film, and the polyimide film thereby Download PDFInfo
- Publication number
- KR20170086455A KR20170086455A KR1020170092009A KR20170092009A KR20170086455A KR 20170086455 A KR20170086455 A KR 20170086455A KR 1020170092009 A KR1020170092009 A KR 1020170092009A KR 20170092009 A KR20170092009 A KR 20170092009A KR 20170086455 A KR20170086455 A KR 20170086455A
- Authority
- KR
- South Korea
- Prior art keywords
- polyimide
- polyamic acid
- polyimide film
- solution
- dianhydride
- Prior art date
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B29—WORKING OF PLASTICS; WORKING OF SUBSTANCES IN A PLASTIC STATE IN GENERAL
- B29D—PRODUCING PARTICULAR ARTICLES FROM PLASTICS OR FROM SUBSTANCES IN A PLASTIC STATE
- B29D7/00—Producing flat articles, e.g. films or sheets
- B29D7/01—Films or sheets
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J5/00—Manufacture of articles or shaped materials containing macromolecular substances
- C08J5/18—Manufacture of films or sheets
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L79/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing nitrogen with or without oxygen or carbon only, not provided for in groups C08L61/00 - C08L77/00
- C08L79/04—Polycondensates having nitrogen-containing heterocyclic rings in the main chain; Polyhydrazides; Polyamide acids or similar polyimide precursors
- C08L79/08—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Materials Engineering (AREA)
- Mechanical Engineering (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
Abstract
본 발명은 폴리아믹산 용액을 비교적 저온에서 이미드화 함으로써 무색·투명한 폴리이미드를 제조한 다음, 또한 상기 폴리이미드를 사용하여 무색·투명할 뿐만 아니라 유연하여 디스플레이 용도로 사용될 수 있는 폴리이미드 필름을 제조하기 위한 폴리이미드 필름 제조방법 및 이를 통하여 제조된 폴리이미드 필름에 관한 발명으로서, (a) 다이안하이드라이드(dianhydride)와 다이아민(diamine)을 용매에 넣고 교반하여 폴리아믹산(polyamic aicd) 용액을 제조하는 단계; (b) 상기 제조된 폴리아믹산 용액에 화학적 탈수제 및 촉매를 첨가하는 단계; (c) 상기 폴리아믹산 용액을 20 내지 80℃에서 이미드화 반응시켜 폴리이미드 용액을 제조하는 단계; (d) 상기 제조된 폴리이미드 용액을 기판에 도포하는 단계; 및 (e) 상기 도포된 폴리이미드 용액을 건조하여 폴리이미드 필름을 제조하는 단계; 를 포함한다. The present invention relates to a process for producing a polyimide film by colorless and transparent polyimide by imidizing the polyamic acid solution at a relatively low temperature and then using the polyimide to form a polyimide film which is colorless and transparent as well as flexible and can be used for display purposes The present invention relates to a process for producing a polyimide film and a polyimide film produced by the process, which comprises the steps of: (a) preparing a solution of polyamic acid by adding dianhydride and diamine into a solvent, step; (b) adding a chemical dehydrating agent and a catalyst to the prepared polyamic acid solution; (c) preparing a polyimide solution by imidizing the polyamic acid solution at 20 to 80 캜; (d) applying the prepared polyimide solution to a substrate; And (e) drying the applied polyimide solution to produce a polyimide film; .
Description
본 발명은 폴리이미드 필름의 제조방법 및 이를 통하여 제조된 폴리이미드 필름에 관한 것이다. The present invention relates to a process for producing a polyimide film and a polyimide film produced thereby.
고내열성 고분자 재료는 첨단 기술의 발달에 따라 제품의 소형 경박화, 고성능화, 고신뢰화를 위한 필수적인 소재로서 필름, 성형품, 섬유, 도료, 접착제 및 복합재 등의 형태로 우주, 항공, 전기/전자, 자동차 및 정밀기기 등 광범위한 산업분야에 이용되고 있다. High heat-resistant polymer materials are essential materials for miniaturization, high performance, and high reliability of products in accordance with the development of advanced technology. They are used in the form of film, molded product, fiber, paint, adhesive and composite materials. And precision instruments.
이들 중 필름은 전자 재료와 패키징(packaging) 재료로 개발되어 왔으며 이들을 분류하면 폴리에스터 필름을 중심으로 한 일반 목적 엔지니어링 플라스틱 필름, 고내열, 내화학성 및 전기적 특성이 우수하여 유연회로기판 등으로 사용되는 폴리이미드(polyimide, PI) 필름, 고탄성 특성을 갖는 아라미드 필름 및 불소 필름, 슈퍼엔지니어링 열가소성 필름 등으로 나눌 수 있고, 또한 이들은 내열성 및 용도에 따라 다양한 목적의 특수 필름으로 분류할 수 있다. 이들 재료의 사용은 IT 산업의 발달에 따라 꾸준한 증가 추세에 있다. Among them, films have been developed as electronic materials and packaging materials. These types of films are general-purpose engineering plastic films mainly composed of polyester films, and have excellent heat resistance, chemical resistance, and electrical properties. A polyimide (PI) film, an aramid film having high elasticity properties, a fluorine film, and a super engineering thermoplastic film, and they can be classified into special films for various purposes depending on their heat resistance and applications. The use of these materials is steadily increasing with the development of the IT industry.
상기 재료 중 폴리이미드는 이미드 고리의 화학적 안정성을 기초로 하여 우수한 기계적 강도, 내화학성, 내후성, 내열성을 가진다. 뿐만 아니라 합성이 용이하고, 박막형 필름을 만들 수 있으며, 경화를 위한 가교기가 필요 없는 장점을 가지고 있다. 또한 뛰어난 전기적 특성으로 인해 미소전자 분야, 광학 분야 등에 이르기까지 고기능성 고분자 재료로 각광받고 있다. Among these materials, the polyimide has excellent mechanical strength, chemical resistance, weather resistance, and heat resistance based on the chemical stability of the imide ring. In addition, it is easy to synthesize, can form a thin film film, and has the advantage of not requiring a crosslinking agent for curing. In addition, due to its excellent electrical properties, it is attracting attention as a highly functional polymer material ranging from microelectronics and optical fields.
최근 디스플레이 분야에서 제품의 경량화 및 소형화가 중요시 되고 있으나 현재 사용되고 있는 유리 기판의 경우 무겁고 잘 깨지며 연속공정이 어렵다는 단점이 있다. 이 때문에 유리 기판을 대체하여 가볍고 유연하며 연속공정이 가능한 장점을 갖는 폴리이미드 기판을 유연한 디스플레이 제작에 활용하기 위한 연구가 진행되고 있다. In recent years, weight reduction and miniaturization of products have been emphasized in the field of display, but currently used glass substrates are heavy and broken, and continuous process is difficult. For this reason, studies are underway to utilize a polyimide substrate, which has advantages of being light, flexible, and continuous process in place of a glass substrate, in the production of a flexible display.
폴리이미드의 일반적인 합성방법은 다이안하이드라이드(dianhydride)와 다이아민(diamine)의 반응에 의하여 전구체인 폴리아믹산(polyamic acid)을 먼저 합성하고 다음 단계에서 폴리아믹산을 이미드화시키는 2단계로 구성되는데, 상기 폴리아믹산 합성은 용매에 용해된 다이아민과 다이안하이드라이드가 개환, 중부가 반응을 일으켜 폴리아믹산을 제조하는 것이고, 이때 사용되는 반응 용매는 N,N-다이메틸아세트아마이드, N,N-다이메틸포름아마이드, N-메틸-2-피롤리돈, 메타-크레졸 등의 극성 유기 용매가 주가 된다. 한편, 상기 합성한 폴리아믹산은 화학적 방법 또는 열적 방법을 통하여 탈수 및 폐환 반응시킴으로써 이미드화하여 폴리이미드를 만든다. The general synthesis method of polyimide is composed of two steps of synthesizing the precursor polyamic acid by the reaction of dianhydride and diamine and then imidizing the polyamic acid in the next step. The synthesis of the polyamic acid is a process in which a diamine and a dianhydride dissolved in a solvent are opened to produce a polyamic acid by the action of a middle part, and the reaction solvent used is N, N -dimethylacetamide, N, Polar organic solvents such as methyl formamide, N -methyl-2-pyrrolidone, and meta-cresol are predominant. On the other hand, the synthesized polyamic acid is imidized by a dehydration and ring-closing reaction through a chemical method or a thermal method to produce a polyimide.
화학적 이미드화 방법은 전구체인 폴리아믹산 용액에 무수 아세트산 등의 산무수물로 대표되는 화학 탈수제와 피리딘 등의 3급 아민류로 대표되는 이미드화 촉매를 투입하여 160℃이상에서 가열하는 방법이다. 한편 열적 이미드화 방법은 전구체인 폴리아믹산 용액을 기판에 도포하고 용매를 증발시킨 후 화학 탈수제 및 촉매 없이 250∼350 ℃로 가열하여 열적으로 이미드화 하는 방법이다.The chemical imidization method is a method in which a chemical dehydrating agent represented by an acid anhydride such as acetic anhydride and an imidation catalyst represented by a tertiary amine such as pyridine are added to a polyamic acid solution as a precursor and heated at 160 ° C or higher. On the other hand, the thermal imidization method is a method in which a polyamic acid solution as a precursor is applied to a substrate, the solvent is evaporated, and the film is thermally imidized by heating to 250 to 350 ° C without a chemical dehydrating agent and a catalyst.
상기와 같은 종래의 폴리아믹산 이미드화 반응을 통하여 제조된 폴리이미드 및 이를 포함하는 필름은 노란색 내지 갈색을 띄는 경향이 있고 용해도 및 유연성이 부족하여 디스플레이 용도로 사용하기에 부적합한 문제점이 있었다. 이에, 폴리이미드의 무색·투명성과 용해도를 향상시키기 위하여 종래 기술에서는 다이안하이드라이드 또는 다이아민 화합물로서 불소기가 함유된 구조 또는 지방족 구조 등을 가진 화합물을 사용해 왔다. 그러나 이러한 경우에도 디스플레이 용도로 사용할 수 있을 정도의 무색·투명성을 가진 폴리이미드를 제조하기에 어려움이 있었다.The polyimide prepared through the conventional polyamic acid imidization reaction as described above and the film containing the same tend to be yellow to brown, and have insufficient solubility and flexibility to be used for display purposes. Therefore, in order to improve colorlessness, transparency and solubility of polyimide, a compound having a structure containing a fluorine group or an aliphatic structure as a dianhydride or a diamine compound has been used in the prior art. However, even in such a case, it has been difficult to produce polyimide having colorlessness and transparency enough to be used for display purposes.
본 발명의 발명자들은, 종래의 기술로 합성된 폴리이미드가 착색과 함께 낮은 투명도 및 용해도를 나타내는 원인을 분석한 결과, 160 내지 350℃의 고온에서 이루어지는 이미드화 반응이 큰 영향을 주는 것을 발견하였다. The inventors of the present invention have found that the polyimide synthesized by the conventional technique exhibits low transparency and solubility as well as coloration and has a great influence on the imidization reaction at a high temperature of 160 to 350 ° C.
이에, 본 발명은 상기와 같은 문제점을 해결하기 위하여 폴리아믹산을 비교적 저온에서 이미드화 함으로써 무색·투명한 폴리이미드 필름을 제조하는 방법을 제공한다. Accordingly, the present invention provides a method for producing a colorless transparent polyimide film by imidizing polyamic acid at a relatively low temperature in order to solve the above problems.
상기와 같은 과제 해결을 위한 본 발명의 일실시예에서는 (a) 다이안하이드라이드(dianhydride)와 다이아민(diamine)을 용매에 넣고 교반하여 폴리아믹산(polyamic aicd) 용액을 제조하는 단계; (b) 상기 제조된 폴리아믹산 용액에 화학적 탈수제 및 촉매를 첨가하는 단계; (c) 상기 폴리아믹산 용액을 20 내지 80℃에서 이미드화 반응시켜 폴리이미드 용액을 제조하는 단계; (d) 상기 제조된 폴리이미드 용액을 기판에 도포하는 단계; 및 (e) 상기 도포된 폴리이미드 용액을 건조하여 폴리이미드 필름을 제조하는 단계; 를 포함하는 폴리이미드 필름 제조방법을 제공한다.According to an embodiment of the present invention, there is provided a method of manufacturing a polyamic acid solution, comprising: (a) preparing a solution of polyamic acid by adding dianhydride and diamine in a solvent; (b) adding a chemical dehydrating agent and a catalyst to the prepared polyamic acid solution; (c) preparing a polyimide solution by imidizing the polyamic acid solution at 20 to 80 캜; (d) applying the prepared polyimide solution to a substrate; And (e) drying the applied polyimide solution to produce a polyimide film; And a method for producing the polyimide film.
본 발명의 또 다른 일실시예에서는, 상기 방법에 따라 제조된 폴리이미드 필름으로서, 상기 폴리이미드 필름의 황색 지수(Yellow Index)는 5 이하인 폴리이미드 필름을 제공한다.In another embodiment of the present invention, there is provided a polyimide film produced by the above method, wherein the polyimide film has a Yellow Index of 5 or less.
본 발명의 또 다른 일실시예에서는, 상기 방법에 따라 제조된 폴리이미드 필름으로서, 상기 폴리이미드 필름은 20 ㎛ 두께에서 파장 450 ㎚의 빛에 대하여 90% 이상의 광투과율을 나타내는 폴리이미드 필름을 제공한다.In another embodiment of the present invention, there is provided a polyimide film produced by the above method, wherein the polyimide film exhibits a light transmittance of 90% or more with respect to light having a wavelength of 450 nm at a thickness of 20 탆 .
또한, 본 발명의 또 다른 일실시예에서는, 상기 폴리이미드 필름을 포함하는 디스플레이를 제공한다. Further, in another embodiment of the present invention, there is provided a display comprising the polyimide film.
본 발명에 따른 폴리이미드 필름 제조방법에 따라 제조되는 폴리이미드 필름은 종래의 기술에 따라 제조된 폴리이미드 필름과는 달리 무색·투명하며 유기용매에 대한 용해도가 우수하다.The polyimide film produced according to the process for producing a polyimide film according to the present invention is colorless, transparent and excellent in solubility in an organic solvent, unlike the polyimide film produced according to the prior art.
또한, 상기 제조된 폴리이미드 필름은 무색·투명할 뿐만 아니라 유연하여 디스플레이 용도로 사용될 수 있다.In addition, the polyimide film is not only colorless and transparent but also flexible and can be used for display purposes.
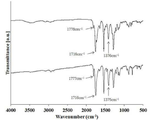
도 1은 본 발명의 실시예 1과 실시예 2에 따른 4,4’-옥시다이프탈릭 안하이드라이드와 2,2-비스(4-아미노페닐)헥사플루오로프로판 폴리이미드의 FT-IR 스펙트럼을 나타낸 것이다.
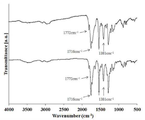
도 2는 본 발명의 실시예 3과 실시예 4에 따른 1,2,4,5-싸이클로헥산테트라카르복실릭 다이안하이드라이드 와 4,4’-다이아미노다이페닐메테인 폴리이미드의 FT-IR 스펙트럼을 나타낸 것이다.
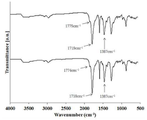
도 3은 본 발명의 실시예 5와 실시예 6에 따른 파이로멜리틱 다이안하이드라이드 와 4,4’-메틸렌비스(싸이클로헥실아민) 폴리이미드의 FT-IR 스펙트럼을 나타낸 것이다.
도 4는 본 발명의 실시예 7과 실시예 8에 따른 1,2,3,4-싸이클로펜탄테트라카르복실릭 다이안하이드라이드와 1,4-다이아미노싸이클로헥산 폴리이미드의 FT-IR 스펙트럼을 나타낸 것이다.
도 5는 비교예 1과 비교예 2에 따른 1.2.3.4-싸이클로뷰탄테트라카르복실릭 다이안하이드라이드와 3,3’,4,4’-벤조 피논테트라카르복실릭 다이안하이드라이드와 2,2-비스(4-아미노페닐)헥사플루오로프로판 폴리이미드의 FT-IR 스펙트럼을 나타낸 것이다.
도 6은 본 발명의 실시예 1과 실시예 2에 따른 4,4’-옥시다이프탈릭 안하이드라이드와 2,2-비스(4-아미노페닐)헥사플루오로프로판 폴리이미드 필름의 UV-vis 투과 스펙트럼이다.
도 7은 본 발명의 실시예 3과 실시예 4에 따른 1,2,4,5-싸이클로헥산테트라카르복실릭 다이안하이드라이드 와 4,4’-다이아미노다이페닐메테인 폴리이미드 필름의 UV-vis 투과 스펙트럼이다.
도 8은 본 발명의 실시예 5와 실시예 6에 따른 파이로멜리틱 다이안하이드라이드 와 4,4’-메틸렌비스(싸이클로헥실아민) 폴리이미드 필름의 UV-vis 투과 스펙트럼이다.
도 9는 본 발명의 실시예 7과 실시예 8에 따른 1,2,3,4-싸이클로펜탄테트라카르복실릭 다이안하이드라이드와 1,4-다이아미노싸이클로헥산 폴리이미드 필름의 UV-vis 투과 스펙트럼이다.
도 10은 비교예 1과 비교예 2에 따른 1.2.3.4-싸이클로뷰탄테트라카르복실릭 다이안하이드라이드와 3,3’,4,4’-벤조 피논테트라카르복실릭 다이안하이드라이드와 2,2-비스(4-아미노페닐)헥사플루오로프로판 폴리이미드 필름의 UV-vis 투과 스펙트럼이다.
도 11은 실시예 1 내지 8, 비교예 1 및 비교예 2에 따른 폴리이미드 필름의 사진이다. 1 shows the FT-IR spectrum of 4,4'-oxydiphthalic anhydride and 2,2-bis (4-aminophenyl) hexafluoropropane polyimide according to Example 1 and Example 2 of the present invention Lt; / RTI >
2 is a graph showing the FT-IR spectrum of 1,2,4,5-cyclohexanetetracarboxylic dianhydride and 4,4'-diaminodiphenylmethane polyimide according to Example 3 and Example 4 of the present invention. Lt; / RTI >
3 shows FT-IR spectra of pyromellitic dianhydride and 4,4'-methylene bis (cyclohexylamine) polyimide according to Example 5 and Example 6 of the present invention.
4 shows FT-IR spectra of 1,2,3,4-cyclopentane tetracarboxylic dianhydride and 1,4-diaminocyclohexane polyimide according to Example 7 and Example 8 of the present invention will be.
FIG. 5 is a graph showing the relationship between the content of 1,2,3,4-cyclobutane tetracarboxylic dianhydride and 3,3 ', 4,4'-benzopinone tetracarboxylic dianhydride and 2,2- FT-IR spectrum of bis (4-aminophenyl) hexafluoropropane polyimide.
Fig. 6 is a graph showing the UV-vis spectra of 4,4'-oxydiphthalic anhydride and 2,2-bis (4-aminophenyl) hexafluoropropane polyimide film according to Example 1 and Example 2 of the present invention. Transmission spectrum.
7 is a graph showing the results of measurement of UV-vis spectra of 1,2,4,5-cyclohexanetetracarboxylic dianhydride and 4,4'-diaminodiphenylmethane polyimide film according to Example 3 and Example 4 of the present invention, vis transmission spectrum.
8 is a UV-vis transmission spectrum of pyromellitic dianhydride and 4,4'-methylene bis (cyclohexylamine) polyimide film according to Example 5 and Example 6 of the present invention.
9 shows the UV-vis transmission spectrum of 1,2,3,4-cyclopentane tetracarboxylic dianhydride and 1,4-diaminocyclohexane polyimide film according to Example 7 and Example 8 of the present invention to be.
FIG. 10 is a graph showing the results obtained by comparing the content of 1,2,3,4-cyclobutane tetracarboxylic dianhydride and 3,3 ', 4,4'-benzopinone tetracarboxylic dianhydride and 2,2- UV-vis transmission spectrum of bis (4-aminophenyl) hexafluoropropane polyimide film.
11 is a photograph of a polyimide film according to Examples 1 to 8, Comparative Example 1 and Comparative Example 2.
본 발명은 다이안하이드라이드 화합물과 다이아민 화합물로부터 합성된 폴리아믹산을 상대적인 저온 조건에서 이미드화 반응시켜 폴리이미드 용액을 제조한 다음, 이를 이용하여 폴리이미드 필름을 제조하는 방법에 관한 것이다. The present invention relates to a method for producing a polyimide film by preparing a polyimide solution by imidizing a polyamic acid synthesized from a dianhydride compound and a diamine compound at a relatively low temperature condition.
상기 방법으로 제조된 폴리이미드 필름은 무색·투명하고, 유연성이 뛰어나 디스플레이에 활용되기에 적합하다. The polyimide film produced by the above method is colorless, transparent, and excellent in flexibility, and is suitable for use in a display.
이하, 본 발명을 더욱 상세히 설명한다. Hereinafter, the present invention will be described in more detail.
폴리이미드 필름의 제조Production of polyimide film
본 발명의 목적을 달성하기 위한 일실시예에서 (a) 다이안하이드라이드(dianhydride)와 다이아민(diamine)을 용매에 넣고 교반하여 폴리아믹산(polyamic acid) 용액을 제조하는 단계; (b) 상기 제조된 폴리아믹산 용액에 화학적 탈수제 및 촉매를 첨가하는 단계; (c) 상기 폴리아믹산 용액을 20 내지 80℃에서 이미드화 반응시켜 폴리이미드 용액을 제조하는 단계; (d) 상기 제조된 폴리이미드 용액을 기판에 도포하는 단계; 및 (e) 상기 도포된 폴리이미드 용액을 건조하여 폴리이미드 필름을 제조하는 단계; 를 포함하는 폴리이미드 필름 제조방법을 제공한다. (A) preparing a polyamic acid solution by adding dianhydride and diamine in a solvent and stirring the mixture; (b) adding a chemical dehydrating agent and a catalyst to the prepared polyamic acid solution; (c) preparing a polyimide solution by imidizing the polyamic acid solution at 20 to 80 캜; (d) applying the prepared polyimide solution to a substrate; And (e) drying the applied polyimide solution to produce a polyimide film; And a method for producing the polyimide film.
본 발명의 또 다른 일실시예에서는 상기 (a)단계에서 제조되는 폴리아믹산 용액을 재침전, 여과 및 건조하는 과정을 순차적으로 거쳐 폴리아믹산 분말을 제조하고, 폴리아믹산 분말을 용매에 용해시켜 폴리아믹산 용액을 제조하여 상기 (b)단계로 이행하는 단계를 더 포함할 수 있다. In another embodiment of the present invention, the polyamic acid solution prepared in step (a) is subjected to re-precipitation, filtration and drying in order to prepare a polyamic acid powder, and the polyamic acid powder is dissolved in a solvent to form a polyamic acid And the step (b) may be further carried out.
본 발명의 또 다른 일실시예에서는 상기 (c)단계에서 제조되는 폴리이미드 용액을 재침전, 여과 및 건조하는 과정을 순차적으로 거쳐 폴리이미드 분말을 제조하고, 폴리이미드 분말을 용매에 용해시켜 폴리이미드 용액을 제조하여 상기 (d)단계로 이행하는 단계를 더 포함할 수 있다. In another embodiment of the present invention, the polyimide powder is prepared by sequentially repeating the steps of reprecipitating, filtering and drying the polyimide solution prepared in the step (c), dissolving the polyimide powder in a solvent, And then proceeding to step (d).
우선, 다이안하이드라이드와 다이아민을 용매에 넣고 교반하여 폴리아믹산 용액을 제조한다(단계 a).First, dianhydride and diamine are added to a solvent and stirred to prepare a polyamic acid solution (step a).
상기 폴리아믹산은 폴리이미드 전구체로서, 치환 또는 비치환된 1종 이상의 다이안하이드라이드와 치환 또는 비치환된 1종 이상의 다이아민 간의 반응으로부터 합성된 것일 수 있다. The polyamic acid may be a polyimide precursor which is synthesized from a reaction between one or more substituted or unsubstituted dianhydrides and one or more substituted or unsubstituted diamines.
본 발명의 일실시예에서 상기 치환 또는 비치환된 1종 이상의 다이안하이드라이드는 방향족 또는 지방족 다이안하이드라이드일 수 있다.In one embodiment of the present invention, the substituted or unsubstituted at least one dianhydride may be an aromatic or aliphatic dianhydride.
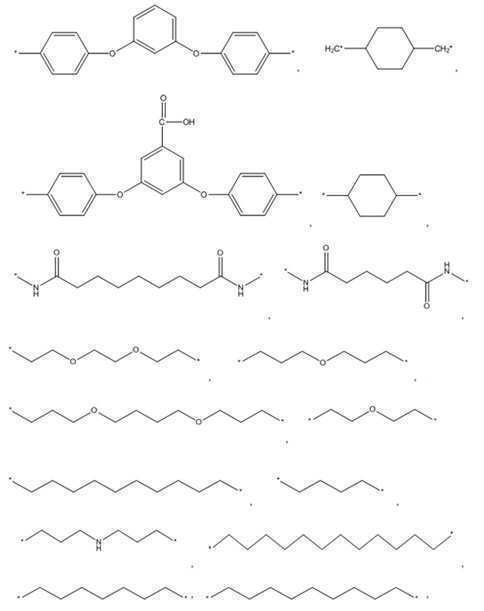
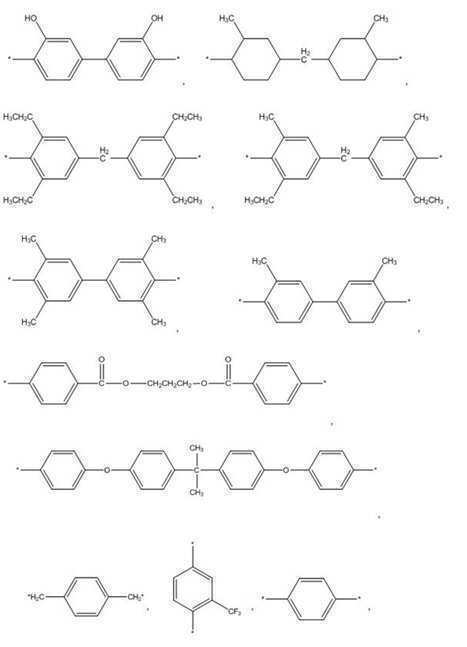
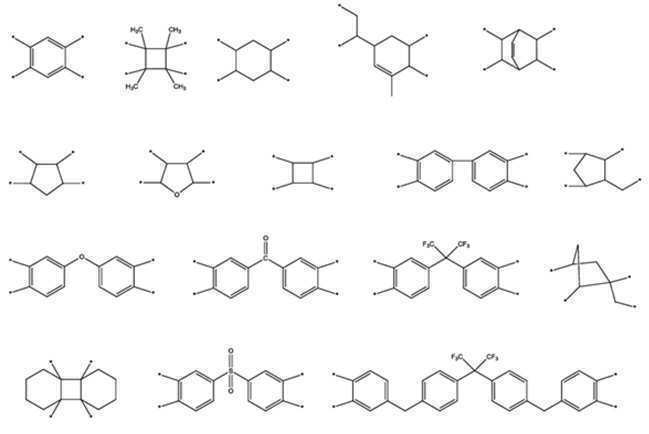
한편, 본 발명의 일실시예에서 상기 다이안하이드라이드는 하기 화학식 1의 화합물을 포함할 수 있다. Meanwhile, in one embodiment of the present invention, the dianhydride may include a compound represented by the following formula (1).
<화학식 1>≪ Formula 1 >
(상기 화학식 1에서 R1은 아래의 화합물(R 1 in the
로 이루어지는 군에서 선택된다.) . ≪ / RTI >
한편, 본 발명의 일실시예에서 상기 치환 또는 비치환된 1종 이상의 다이아민은 방향족 또는 지방족 다이아민일 수 있다.In one embodiment of the present invention, the substituted or unsubstituted diamines may be aromatic or aliphatic diamines.
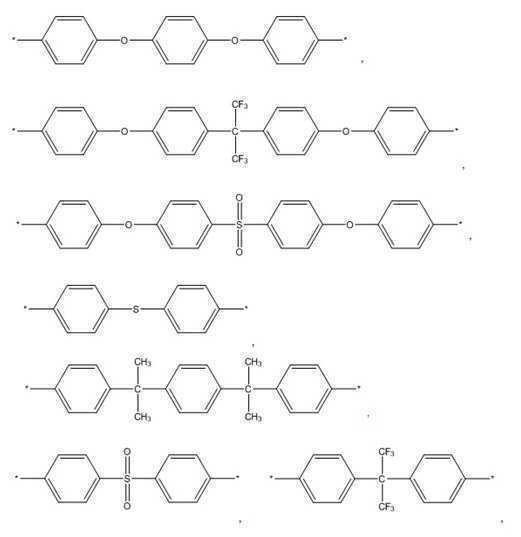
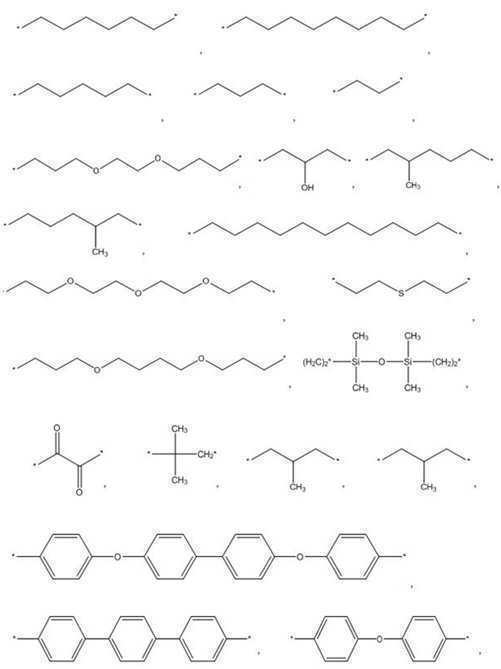
한편, 본 발명의 일실시예에서 상기 다이아민은 하기 화학식 2의 화합물을 포함할 수 있다. Meanwhile, in one embodiment of the present invention, the diamine may include a compound represented by the following formula (2).
<화학식 2> (2)
(상기 화학식 2에서 R2는 아래의 화합물(Wherein R < 2 > represents the following compound
로 이루어지는 군에서 선택된다.) . ≪ / RTI >
한편, 상기 다이안하이드라이드와 다이아민을 반응시켜 폴리아믹산 용액을 제조하는 용매; 상기 폴리아믹산 분말이 용해되는 용매; 및 상기 폴리이미드 분말이 용해되는 용매는 유기 용매일 수 있으며, 예를 들어 N-메틸-2-피롤리돈, N,N-다이메틸아세트아미드, N,N-다이메틸포름아미드, N-비닐피롤리돈, N-메틸카프로락탐, 디메틸술폭시드, 테트라메틸요소, 피리딘, 디메틸술폰, 헥사메틸술폭시드, 메타-크레졸, 감마-부티로락톤, 에틸셀로솔브, 부틸셀로솔브, 에틸카르비톨, 부틸카르비톨, 에틸카르비톨 아세테이트, 부틸카르비톨 아세테이트, 에틸렌글리콜, 젖산에틸, 젖산부틸, 시클로헥사논, 시클로펜타논, 헥산(노말헥산, 이소헥산, 시클로헥산), 펜탄, 헵탄, 벤젠, 톨루엔, 자일렌, 메탄올, 에탄올, 프로판올(노말프로판올, 이소프로판올), 부탄올(노말-, 이소-, 터셔리-), 시클로헥사놀, 옥탄올, 벤질알콜, 아세톤, 메틸에틸케톤, 메틸부틸케톤, 초산메틸, 초산에틸, 디에틸에테르, 이소프로필에테르, 테트라하이드로퓨란, 클로로포름, 다이옥세인, 디에틸포름아미드, 설포레인, 개미산, 초산, 프로피온산, 아세트나이트라일 및 테트랄린으로 이루어진 군에서 선택되는 1종의 단일 용매 또는 2종 이상의 혼합 용매일 수 있다. On the other hand, a solvent for preparing a polyamic acid solution by reacting the dianhydride with diamine; A solvent in which the polyamic acid powder is dissolved; And a solvent to which the polyimide powder may be dissolved in an organic daily, for example, N - methyl-2-pyrrolidone, N, N - dimethyl acetamide, N, N - dimethyl-formamide, N - vinyl But are not limited to, pyrrolidone, N -methylcaprolactam, dimethylsulfoxide, tetramethylurea, pyridine, dimethylsulfone, hexamethylsulfoxide, meta-cresol, gamma-butyrolactone, ethylcellosolve, Butanol, cyclohexane, hexane, hexane, heptane, cyclohexane, cyclohexanone, cyclohexanone, cyclohexanone, cyclohexanone, cyclohexane, , Butanol (normal-, iso-, tertiary-), cyclohexanol, octanol, benzyl alcohol, acetone, methyl ethyl ketone, methyl butyl ketone , Methyl acetate, ethyl acetate, diethyl ether, iso One single solvent selected from the group consisting of propyl ether, tetrahydrofuran, chloroform, dioxane, diethylformamide, sulfolane, formic acid, acetic acid, propionic acid, acetonitrile and tetralin or a mixture of two or more It can be used every day.
본 발명의 일실시예에서 상기 (a)단계는 0 내지 30℃의 반응 온도에서 진행될 수 있다. 반응 온도가 0℃ 미만일 경우는 반응 속도가 느려 폴리이미드 제조공정에 지장을 초래하며, 30℃가 넘을 경우는 폴리아믹산의 생성에 따른 발열 현상 때문에 반응온도가 급격히 상승하여 분자량이 낮아질 수 있다.In one embodiment of the present invention, the step (a) may be carried out at a reaction temperature of 0 to 30 ° C. If the reaction temperature is less than 0 ° C, the reaction rate is low, which may interfere with the polyimide production process. If the reaction temperature is more than 30 ° C, the reaction temperature may rapidly increase due to the exothermic reaction due to the production of polyamic acid.
본 발명의 일실시예에서 상기 (a)단계는 1 내지 48시간 동안 진행될 수 있으며, 보다 상세하게는 6 내지 36시간 진행될 수 있다. 반응 시간이 1시간 미만인 경우에는 중합 반응이 충분히 진행되지 않아 분자량이 너무 낮을 수 있으며 48시간 이후에는 폴리아믹산의 겔화가 일어날 수 있다.In one embodiment of the present invention, the step (a) may be carried out for 1 to 48 hours, more specifically 6 to 36 hours. If the reaction time is less than 1 hour, the polymerization reaction may not proceed sufficiently and the molecular weight may be too low, and after 48 hours, gelation of the polyamic acid may occur.
한편, 본 발명의 일실시예에서는 상기 반응 후에 제조되는 폴리아믹산 용액을 재침전, 여과 및 건조하는 과정이 더 포함될 수 있다. 상기 건조 후 제조되는 폴리아믹산 분말은 용매에 용해시켜 다시 폴리아믹산 용액으로 제조될 수 있다.In an embodiment of the present invention, the polyamic acid solution prepared after the reaction may be further subjected to a re-precipitation, filtration and drying process. The polyamic acid powder prepared after drying may be dissolved in a solvent and then be made into a polyamic acid solution.
상기 재침전 및 여과 시 사용되는 용매는 예를 들어, 물, 메탄올, 에탄올, 아이소프로판올, n-뷰탄올, n-헥세인, 아세톤, 에테르, 에틸 아세테이트, 테트라하이드로퓨란 및 클로로폼으로 이루어지는 군에서 선택되는 1종의 단일 용매 또는 2종이상의 혼합 용매일 수 있다. The solvent used in the reprecipitation and filtration is, for example, water, methanol, ethanol, isopropanol, n-butanol, n-hexane, acetone, ether, ethyl acetate, tetrahydrofuran and chloroform It may be one single solvent selected or two or more mixing days.
한편, 상기 건조 과정은 20 내지 80℃ 온도 범위 내에서 진행될 수 있으며, 상세하게는 30 내지 80℃, 더욱 상세하게는 40 내지 60℃ 온도 범위 내에서 진행될 수 있다. 상기 건조 온도가 20℃ 미만인 경우 건조에 오랜 시간이 걸리며 사용한 용매가 잔류할 수 있는 문제점이 있고, 80℃를 초과하는 경우 폴리이미드의 색이 진하게 될 수 있는 문제점이 있다. Meanwhile, the drying process may be performed at a temperature ranging from 20 to 80 ° C, more specifically, at a temperature ranging from 30 to 80 ° C, and more specifically, a temperature range of 40 to 60 ° C. If the drying temperature is lower than 20 ° C, it takes a long time to dry and the used solvent may remain. If the drying temperature exceeds 80 ° C, the color of the polyimide may become dark.
한편, 상기 건조 과정은 1 기압(1013 hPa) 이하에서 진행될 수 있으며, 상세하게는 0.9 내지 0.001 기압(910 hPa 내지 1 hPa), 보다 상세하게는 0.7 내지 0.01 기압(710 hPa 내지 10 hPa)범위 내에서 진행될 수 있다. On the other hand, the drying process may be performed at a pressure of 1 atm (1013 hPa) or less, more specifically, at a pressure of 0.9 to 0.001 atmospheres (910 hPa to 1 hPa), more specifically 0.7 to 0.01 atmospheres (710 hPa to 10 hPa) Lt; / RTI >
다음으로 상기 폴리아믹산 용액에 화학적 탈수제와 촉매를 첨가한다(단계 b).Next, a chemical dehydrating agent and a catalyst are added to the polyamic acid solution (step b).
상기 화학적 탈수제와 촉매는 폴리아믹산 용액 내에서 이미드화 반응을 진행시키기 위한 것이다.The chemical dehydrating agent and the catalyst are for carrying out the imidization reaction in the polyamic acid solution.
상기 화학적 탈수제는 예를 들어, 무수 아세트산, 무수 프로피온산, 무수 부티르산, 무수 벤조산, 무수 아디프산, 무수 이소프탈산, 프탈릭 무수물 및 트리멜리틱 무수물로 이루어지는 군에서 선택되는 1종 또는 2종 이상일 수 있다.The chemical dehydrating agent may be one or more selected from the group consisting of acetic anhydride, anhydrous propionic acid, anhydrous butyric acid, anhydrous benzoic acid, anhydrous adipic acid, anhydrous isophthalic acid, phthalic anhydride and trimellitic anhydride. have.
한편, 상기 촉매는 트라이메틸아민, 트라이에틸아민, 메틸피롤리딘, N,N-다이메틸헥실아민, 이미다졸, 1,2-다이메틸이미다졸, N-메틸이미다졸, N-벤질-2-메틸이미다졸, 2-메틸이미다졸, 2-에틸-4-메틸이미다졸, 5-메틸벤즈이미다졸, N-벤질-2-메틸이미다졸, 이소퀴놀린, 3,5-다이메틸피리딘, 3,4-다이메틸피리딘, 2,5-다이메틸피리딘, 2,4-다이메틸피리딘 및 4-n-프로필피리딘으로 이루어지는 군에서 선택되는 1종 또는 2종 이상일 수 있다. On the other hand, the catalyst is trimethyl amine, triethyl amine, methyl-pyrrolidine, N, N - dimethyl-cyclohexyl amine, imidazole, 1,2-dimethyl-imidazole, N - methylimidazole, N - benzyl Methylimidazole, 2-methylimidazole, N -benzyl-2-methylimidazole, isoquinoline, 3,5 May be one or more selected from the group consisting of dimethylpyridine, 3,4-dimethylpyridine, 2,5-dimethylpyridine, 2,4-dimethylpyridine and 4-n-propylpyridine.
본 발명의 일실시예에서 상기 화학적 탈수제 및 촉매는 각각 폴리아믹산 반복 단위에 대하여 동일 내지 50배의 몰 비, 상세하게는 2 내지 40배의 몰 비, 더 상세하게는 5 내지 30배의 몰 비로 첨가될 수 있다. 상기 화학적 탈수제 및 촉매의 양을 폴리아믹산 반복 단위에 대하여 1배의 몰 비 미만으로 하는 경우 이미드화 반응이 충분히 진행될 수 없을 만큼 반응 속도가 느려 폴리이미드 제조가 사실상 어려워지고, 50배의 몰 비 초과인 경우에는 잔류하는 탈수제와 촉매로 인하여 폴리이미드의 물성이 떨어지는 문제점이 있다. In one embodiment of the present invention, the chemical dehydrating agent and the catalyst each have a molar ratio of the same to 50 times the polyamic acid repeating unit, specifically 2 to 40 times, more specifically 5 to 30 times Can be added. When the amounts of the chemical dehydrating agent and the catalyst are less than 1 times the molar ratio of the polyamic acid repeating units, the reaction rate is so low that the imidization reaction can not proceed sufficiently, There is a problem that the physical properties of the polyimide deteriorate due to the residual dehydrating agent and the catalyst.
다음으로, 상기 용매에 용해된 폴리아믹산을 20 내지 80℃에서 이미드화 반응시키는 단계를 거치면 폴리이미드 용액이 제조된다(단계 c). Next, the polyimide solution dissolved in the solvent is imidized at 20 to 80 캜 to prepare a polyimide solution (step c).
종래 기술에서는 폴리아믹산의 이미드화 반응 시 160 내지 350℃의 비교적 고온에서 반응이 진행되었는데, 이 경우 제조되는 폴리이미드를 이용하여 제조된 폴리이미드 필름은 노란색 또는 갈색으로 무색·투명성이 요구되는 디스플레이에 적용하기 어려운 문제점이 있었다. In the prior art, the reaction proceeded at a relatively high temperature of 160 to 350 DEG C in the imidization reaction of the polyamic acid. In this case, the polyimide film prepared using the polyimide produced was yellow or brown, There is a problem that it is difficult to apply.
반면, 본 발명에서는 종래의 기술 대비 상대적인 저온에서 폴리아믹산의 이미드화 반응을 진행시킴으로써 상기 제조된 폴리이미드를 이용하여 폴리이미드 필름 제조 시 무색·투명한 폴리이미드 필름을 얻을 수 있는 장점이 있다. On the other hand, in the present invention, there is an advantage that a colorless transparent polyimide film can be obtained when the polyimide film is produced by proceeding the imidization reaction of the polyamic acid at a relatively low temperature as compared with the conventional technique.
상기와 같이 무색·투명한 폴리이미드 필름을 구현하기 위하여 폴리이미드 제조 시 이미드화 반응은 20 내지 80℃의 온도 범위에서 진행될 수 있고, 더욱 상세하게는 25 내지 60℃의 온도 범위에서 진행될 수 있다. In order to realize a colorless and transparent polyimide film as described above, the imidization reaction may be carried out at a temperature of 20 to 80 ° C, and more specifically, at a temperature of 25 to 60 ° C.
상기 폴리아믹산의 이미드화 반응 온도가 20℃ 미만인 경우 이미드화 반응 속도가 지나치게 느려지므로 이미드화 반응이 충분하게 진행될 수 없어 폴리이미드 제조가 어렵다. 상기 반응 온도가 80℃를 초과하는 경우 최종적으로 제조되는 폴리이미드 필름이 20㎛ 두께에서 파장 450㎚의 빛에 대하여 90% 이하의 광투과율을 나타내고, 황색 지수(Yellow Index)는 10이상으로 증가하여 디스플레이 용도로 사용하기에 부적합해진다. If the imidization reaction temperature of the polyamic acid is less than 20 캜, the imidization reaction rate becomes too slow, so that the imidization reaction can not proceed sufficiently and polyimide production is difficult. When the reaction temperature exceeds 80 ° C, the finally prepared polyimide film exhibits a light transmittance of 90% or less with respect to light having a wavelength of 450 nm at a thickness of 20 μm, and the Yellow Index increases to 10 or more Which makes it unsuitable for use as a display.
본 발명의 일실시예에서, 상기 이미드화 반응은 10분 내지 72시간 동안 진행되는 것일 수 있으며, 상세하게는 6 내지 48시간, 더욱 상세하게는 12 내지 24시간 동인 진행되는 것일 수 있다. 상기 반응 시간이 10분 미만인 경우 이미드화 반응이 잘 진행되지 않으며, 72시간을 초과하는 경우 겔화(gelation)가 진행될 수 있다. In one embodiment of the present invention, the imidization reaction may be carried out for 10 minutes to 72 hours, in particular 6 to 48 hours, more particularly 12 to 24 hours. If the reaction time is less than 10 minutes, the imidization reaction does not progress well, and if the reaction time exceeds 72 hours, gelation may proceed.
다음으로, 상기 일련의 과정을 통하여 제조되는 폴리이미드 용액을 기판에 도포한다(단계 d).Next, the polyimide solution prepared through the series of steps is applied to the substrate (step d).
본 발명의 일실시예에서, 상기 단계 (c)를 통하여 제조된 폴리이미드 용액을 그대로 기판에 도포하여 폴리이미드 필름을 제조할 수 있다. In one embodiment of the present invention, the polyimide solution prepared through step (c) may be directly applied to a substrate to produce a polyimide film.
한편, 본 발명의 또 다른 일실시예에서, 상기 단계 (c)를 통하여 제조된 폴리이미드 용액을 재침전, 여과 및 건조한 다음, 상기 건조에 의해 얻어진 폴리이미드 분말을 용매에 용해시켜 폴리이미드 용액을 제조하고, 상기 제조된 폴리이미드 용액을 기판에 도포하여 폴리이미드 필름으로 제조할 수도 있다.Meanwhile, in another embodiment of the present invention, the polyimide solution prepared through the step (c) is re-precipitated, filtered and dried, and then the polyimide powder obtained by the drying is dissolved in a solvent to prepare a polyimide solution And the polyimide solution may be applied to a substrate to produce a polyimide film.
상기 재침전 및 여과 시 사용되는 용매는 예를 들어, 물, 메탄올, 에탄올, 아이소프로판올, n-뷰탄올, n-헥세인, 아세톤, 에테르, 에틸 아세테이트, 테트라하이드로퓨란 및 클로로폼으로 이루어지는 군에서 선택되는 1종의 단일 용매 또는 2종 이상의 혼합 용매일 수 있다. The solvent used in the reprecipitation and filtration is, for example, water, methanol, ethanol, isopropanol, n-butanol, n-hexane, acetone, ether, ethyl acetate, tetrahydrofuran and chloroform May be selected from a single solvent or a mixture of two or more solvents.
한편, 상기 건조 과정은 20 내지 80℃ 온도 범위 내에서 진행될 수 있으며, 상세하게는 30 내지 80℃, 더욱 상세하게는 40 내지 60℃ 온도 범위 내에서 진행될 수 있다. 상기 건조 온도가 20℃ 미만인 경우 건조에 오랜 시간이 걸리며 사용한 용매가 잔류할 수 있는 문제점이 있고, 80℃를 초과하는 경우 폴리이미드의 색이 진하게 될 수 있는 문제점이 있다. Meanwhile, the drying process may be performed at a temperature ranging from 20 to 80 ° C, more specifically, at a temperature ranging from 30 to 80 ° C, and more specifically, a temperature range of 40 to 60 ° C. If the drying temperature is lower than 20 ° C, it takes a long time to dry and the used solvent may remain. If the drying temperature exceeds 80 ° C, the color of the polyimide may become dark.
한편, 상기 건조 과정은 1 기압(1013 hPa) 이하에서 진행될 수 있으며, 상세하게는 0.9 내지 0.001 기압(910 hPa 내지 1 hPa), 보다 상세하게는 0.7 내지 0.01 기압(710 hPa 내지 10 hPa)범위 내에서 진행될 수 있다. 한편, 상기 폴리이미드 용액에는 필요에 따라 젖음성 향상제 등의 첨가제를 소량 첨가할 수도 있으며, 이 경우 첨가제는 폴리이미드 용액 전체 중량 대비 0.001 내지 5wt%로 첨가될 수 있고, 더욱 상세하게는 0.01 내지 2wt%로 첨가될 수 있다. On the other hand, the drying process may be performed at a pressure of 1 atm (1013 hPa) or less, more specifically, at a pressure of 0.9 to 0.001 atmospheres (910 hPa to 1 hPa), more specifically 0.7 to 0.01 atmospheres (710 hPa to 10 hPa) Lt; / RTI > If necessary, additives such as a wettability improver may be added to the polyimide solution. In this case, the additive may be added in an amount of 0.001 to 5 wt% relative to the total weight of the polyimide solution, more specifically 0.01 to 2 wt% Lt; / RTI >
한편, 상기 폴리이미드 분말을 용해시키는 용매는 N-메틸-2-피롤리돈(NMP), N,N-다이메틸아세트아미드, N,N-다이메틸포름아미드, N-비닐피롤리돈, N-메틸카프로락탐, 디메틸술폭시드, 테트라메틸요소, 피리딘, 디메틸술폰, 헥사메틸술폭시드, 메타-크레졸, 감마-부티로락톤, 에틸셀로솔브, 부틸셀로솔브, 에틸카르비톨, 부틸카르비톨,에틸카르비톨 아세테이트, 부틸카르비톨 아세테이트, 에틸렌글리콜, 젖산에틸, 젖산부틸, 시클로헥사논, 시클로펜타논, 헥산(노말헥산, 이소헥산, 시클로헥산), 펜탄, 헵탄, 벤젠, 톨루엔, 자일렌, 메탄올, 에탄올, 프로판올(노말프로판올, 이소프로판올), 부탄올(노말-, 이소-, 터셔리-), 시클로헥사놀, 옥탄올, 벤질알콜, 아세톤, 메틸에틸케톤, 메틸부틸케톤, 초산메틸, 초산에틸, 디에틸에테르, 이소프로필에테르, 테트라하이드로퓨란, 클로로포름, 다이옥세인, 디에틸포름아미드, 설포레인, 개미산, 초산, 프로피온산, 아세트나이트라일 및 테트랄린으로 이루어지는 군에서 선택되는 하나 이상의 용매일 수 있다. The solvent for dissolving the polyimide powder may include N -methyl-2-pyrrolidone (NMP), N, N -dimethylacetamide, N, N -dimethylformamide, N -vinylpyrrolidone, N -Methyl caprolactam, dimethyl sulfoxide, tetramethyl urea, pyridine, dimethyl sulfone, hexamethyl sulfoxide, meta-cresol, gamma-butyrolactone, ethyl cellosolve, butyl cellosolve, ethyl carbitol, butyl carbitol , Ethyl carbitol acetate, butyl carbitol acetate, ethylene glycol, ethyl lactate, butyl lactate, cyclohexanone, cyclopentanone, hexane (normalhexane, isohexane, cyclohexane), pentane, heptane, benzene, toluene, , Methanol, ethanol, propanol (normal propanol, isopropanol), butanol (normal-, iso-, tertiary-), cyclohexanol, octanol, benzyl alcohol, acetone, methyl ethyl ketone, methyl butyl ketone, Ethyl, diethyl ether, isopropyl ether, tetra One or more solvents selected from the group consisting of chloroform, chloroform, dioxane, diethylformamide, sulfolane, formic acid, acetic acid, propionic acid, acetonitrile and tetralin can be used.
한편, 상기 폴리이미드는 제조되는 폴리이미드 용액의 전체 중량 대비 1 내지 90wt%가 되도록 용해시킨다. On the other hand, the polyimide is dissolved in an amount of 1 to 90 wt% based on the total weight of the polyimide solution to be produced.
한편, 상기 과정에서 도포 방법은 예를 들어, 스핀도포법, 침지법, 프렉소 인쇄법, 잉크젯 인쇄법, 분사법, 포팅법, 스크린 인쇄법 등이 사용될 수 있다. 또한, 이들 방법 중 필요에 따라 10 ㎛ 이상의 두꺼운 막을 얻기 위해서는 바코트 도포법, 슬릿코팅 도포법, 스크린 인쇄법, 스핀 도포법 등이 사용될 수도 있다. Meanwhile, in the above process, for example, a spin coating method, a dipping method, a flexographic printing method, an inkjet printing method, a spraying method, a potting method, a screen printing method and the like can be used. In order to obtain a thick film having a thickness of 10 탆 or more among these methods, a bar coating method, a slit coating method, a screen printing method, a spin coating method, or the like may be used.
다음으로, 상기 기판에 도포된 폴리이미드 용액의 용매를 증발시켜 폴리이미드 필름을 제조한다(단계 e).Next, the polyimide film is prepared by evaporating the solvent of the polyimide solution applied to the substrate (step e).
본 발명의 일실시예에서, 상기 도포된 폴리이미드 용액에서 20 내지 100℃에서 용매를 증발시켜 폴리이미드 필름을 제조한다. 더욱 상세하게는 25 내지 60℃에서 용매를 증발시킨다. 용매 증발 온도가 20℃ 미만이면 용매 증발 시간이 너무 많이 소요되며, 100℃ 이상이면 폴리이미드가 착색될 수 있다. In one embodiment of the present invention, the polyimide film is prepared by evaporating the solvent at 20 to 100 DEG C in the applied polyimide solution. More specifically, the solvent is evaporated at 25 to 60 占 폚. If the evaporation temperature of the solvent is less than 20 캜, the evaporation time of the solvent is excessively long, and if it is 100 캜 or more, the polyimide may be colored.
상기 용매를 증발시키는 단계는 1 기압 이하에서 진행되는 것이 바람직하다.The step of evaporating the solvent preferably proceeds at 1 atm or less.
상기 일련의 과정을 거치면 폴리이미드 필름이 제조된다. 본 발명에 따라 제조되는 폴리이미드 필름은 무색·투명하며 유연하다. 특히, 상기 폴리이미드 필름의 황색 지수(Yellow Index)는 5 이하이며, 20 ㎛ 두께에서 파장 450㎚의 빛에 대하여 90% 이상의 광투과율을 나타낸다. 또한, 상기 폴리이미드 필름의 폴리이미드는 전방향족 폴리이미드, 부분지방족 폴리이미드, 또는 전지방족 폴리이미드일 수 있다. The polyimide film is produced through the above-described series of processes. The polyimide film produced according to the present invention is colorless, transparent and flexible. In particular, the yellow index of the polyimide film is 5 or less, and the light transmittance is 90% or more with respect to light having a wavelength of 450 nm at a thickness of 20 탆. The polyimide of the polyimide film may be a wholly aromatic polyimide, a partially aliphatic polyimide, or a prealiphatic polyimide.
한편, 본 발명에 따라 제조되는 폴리이미드 필름은 상기와 같은 특징에 의해 우주, 항공, 전기/전자, 반도체, 투명/유연 디스플레이, 액정 배향막, 자동차, 정밀기기, 패키징, 의료용 소재, 분리막, 연료전지, 2차전지 등 광범위한 산업분야에서 활용될 수 있다. Meanwhile, the polyimide film produced according to the present invention can be applied to various fields such as space, aviation, electric / electronic, semiconductor, transparent / flexible display, liquid crystal alignment film, automobile, precision instrument, packaging, , Secondary batteries, and the like.
이하, 본 발명의 실시예 및 비교예를 통해 본 발명을 보다 상세히 설명한다. 다만, 하기 실시예 및 비교예는 본 발명의 이해를 돕기 위한 것이고 본 발명의 권리범위를 이로 한정하는 것을 의도하지 않는다. Hereinafter, the present invention will be described in more detail with reference to Examples and Comparative Examples. It should be understood, however, that the following examples and comparative examples are intended to assist the understanding of the present invention and are not intended to limit the scope of the present invention thereto.
실시예Example
실시예 1: 전 방향족 폴리이미드 필름 제조Example 1: Preparation of wholly aromatic polyimide film
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈(NMP) 184 mL을 넣고 4,4’-옥시다이프탈릭 안하이드라이드 15.510g (0.05mol)과 2,2-비스(4-아미노페닐)헥사플루오로프로판 16.713g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.184 mL of N -methyl-2-pyrrolidone (NMP) was added to a 500-mL two-necked round bottom flask substituted with nitrogen gas, and 15.510 g (0.05 mol) of 4,4'-oxydiphthalic anhydride and 2 And 16.713 g (0.05 mol) of 2-bis (4-aminophenyl) hexafluoropropane were added thereto, followed by reaction at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 5배에 해당하는 몰 수의 무수 아세트산 25.522g (0.25mol)과 피리딘 19.775g (0.25mol)을 넣고 20℃에서 24시간 교반시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 전방향족 폴리이미드를 합성하였다.Next, 25.522 g (0.25 mol) of acetic anhydride and 19.775 g (0.25 mol) of pyridine were added to the solution, and the mixture was stirred at 20 ° C for 24 hours, Reprecipitated. After filtration, the filtrate was washed with 100 mL of water and 100 mL of methanol, followed by vacuum drying to synthesize a wholly aromatic polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 1)에서는 1778cm- 1와 1716cm-1에서 이미드기의 C=O 흡수띠, 1376cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 22㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 6).In the infrared absorption spectrum (Fig. 1) of the synthesized polymers 1778cm - 1 and 1716cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1376cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 90% or more at 450 nm (FIG. 6).
실시예 2: 전 방향족 폴리이미드의 필름 제조Example 2: Production of film of wholly aromatic polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 184 mL을 넣고 4,4’-옥시다이프탈릭 안하이드라이드 15.510g (0.05mol)과 2,2-비스(4-아미노페닐)헥사플루오로프로판 16.713g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.184 mL of N -methyl-2-pyrrolidone was added to a 500-mL two-necked round bottom flask substituted with nitrogen gas, and 15.510 g (0.05 mol) of 4,4'-oxydiphthalic anhydride and 2,2- 16.713 g (0.05 mol) of bis (4-aminophenyl) hexafluoropropane was added and reacted at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 5배에 해당하는 몰 수의 무수 아세트산 25.522g (0.25mol)과 피리딘 19.775g (0.25mol)을 넣고 80℃에서 24시간 교반시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올100 mL로 세척 후 진공 건조하여 전방향족 폴리이미드를 합성하였다.. Next, 25.522 g (0.25 mol) of acetic anhydride and 19.775 g (0.25 mol) of pyridine were added to the solution, and the mixture was stirred at 80 ° C. for 24 hours, Reprecipitated. After filtration, the filtrate was washed with 100 mL of water and 100 mL of methanol and vacuum-dried to synthesize a wholly aromatic polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 1)에서는 1777cm- 1와 1716cm-1에서 이미드기의 C=O 흡수띠, 1375cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 27㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 6).In the infrared absorption spectrum (Fig. 1) of the synthesized polymers 1777cm - 1 and 1716cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1375cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 450 nm at 90% or more (Fig. 6).
실시예 3: 부분지방족 폴리이미드의 필름 제조Example 3: Production of film of partially aliphatic polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 190 mL을 넣고 1,2,4,5-싸이클로헥산테트라카르복실릭 다이안하이드라이드 11.208g (0.05mol)과 4,4’-다이아미노다이페닐메테인 9.913g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.190 mL of N -methyl-2-pyrrolidone was added to a 500-mL two-neck round bottom flask substituted with nitrogen gas, and 11208 g (0.05 mol) of 1,2,4,5-cyclohexanetetracarboxylic dianhydride, And 9.913 g (0.05 mol) of 4,4'-diaminodiphenylmethane were placed and reacted at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 20배에 해당하는 몰 수의 무수 아세트산 102.09g (1.0mol)과 피리딘 79.1g (1.0mol)을 넣고 40℃에서 24시간 교반 시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 부분지방족 폴리이미드를 합성하였다. Next, 102.09 g (1.0 mol) of acetic anhydride and 79.1 g (1.0 mol) of pyridine were added to the solution in an amount corresponding to 20 times the number of repeating units of polyamic acid, and the mixture was stirred at 40 ° C for 24 hours, Reprecipitated. After filtration, the mixture was washed with 100 mL of water and 100 mL of methanol, followed by vacuum drying to synthesize a partially aliphatic polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 2)에서는 1783cm- 1와 1719cm-1에서 이미드기의 C=O 흡수띠, 1379cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 26㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 7).In the infrared absorption spectrum of the synthesized polymer (Fig. 2) 1783cm - 1 and 1719cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1379cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 450 nm at 90% or more (Fig. 7).
실시예 4: 부분지방족 폴리이미드의 필름 제조Example 4: Production of film of partially aliphatic polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 190 mL을 넣고 1,2,4,5-싸이클로헥산테트라카르복실릭 다이안하이드라이드 11.208g (0.05mol)과 4,4’-다이아미노다이페닐메테인 9.913g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.190 mL of N -methyl-2-pyrrolidone was added to a 500-mL two-neck round bottom flask substituted with nitrogen gas, and 11208 g (0.05 mol) of 1,2,4,5-cyclohexanetetracarboxylic dianhydride, And 9.913 g (0.05 mol) of 4,4'-diaminodiphenylmethane were placed and reacted at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 40배에 해당하는 몰 수의 무수 아세트산 204.18g (2.0mol)과 피리딘 158.2g (2.0mol)을 넣고 40℃에서 24시간 교반 시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 부분지방족 폴리이미드를 합성하였다.Next, 204.18 g (2.0 mol) of acetic anhydride corresponding to 40 times the number of moles of the repeating unit of the polyamic acid was added to the solution, and 158.2 g (2.0 mol) of pyridine was added to the solution. The solution was stirred at 40 ° C for 24 hours, Reprecipitated. After filtration, the mixture was washed with 100 mL of water and 100 mL of methanol, followed by vacuum drying to synthesize a partially aliphatic polyimide.
상기 합성된 중합체의 적외선흡수스펙트럼(도 2)에서는 1781cm- 1와 1720cm-1에서 이미드기의 C=O 흡수띠, 1378cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 23㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 7).In the infrared absorption spectrum (Fig. 2) of the synthesized polymers 1781cm - 1 and 1720cm -1 in the already C = O absorption band of in deugi, 1378cm -1 The absorption band of CN already deugi was observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 450 nm at 90% or more (Fig. 7).
실시예 5: 부분지방족 폴리이미드의 필름 제조Example 5: Production of film of partially aliphatic polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 192 mL을 넣고 파이로멜리틱 다이안하이드라이드 10.910g (0.05mol) 과 4,4’-메틸렌비스(싸이클로헥실아민) 10.518g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.192 mL of N -methyl-2-pyrrolidone was added to a 500-mL 2-necked round bottom flask substituted with nitrogen gas, and 10.910 g (0.05 mol) of pyromellitic dianhydride and 4,4'-methylenebis Hexylamine) was added thereto, followed by reaction at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 5배에 해당하는 몰 수의 무수 벤조산 56.558g (0.25mol)과 1,2-다이메틸이미다졸 24.032g (0.25mol)을 넣고 40℃에서 24시간 교반 시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 부분지방족 폴리이미드를 합성하였다.Next, 56.558 g (0.25 mol) of anhydrous benzoic acid and 24.032 g (0.25 mol) of 1,2-dimethylimidazole corresponding to 5 times the number of repeating units of the polyamic acid were added to the solution, After stirring for a time, re-precipitation was performed using water. After filtration, the mixture was washed with 100 mL of water and 100 mL of methanol, followed by vacuum drying to synthesize a partially aliphatic polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 3)에서는 1772cm- 1와 1716cm-1에서 이미드기의 C=O 흡수띠, 1381cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 28㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 8).In the infrared absorption spectrum of the synthesized polymer (Fig. 3) 1772cm - 1 and 1716cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1381cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 450 nm at 90% or more (Fig. 8).
실시예 6: 부분지방족 폴리이미드의 필름 제조Example 6: Film Production of Partial Aliphatic Polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 192 mL을 넣고 파이로멜리틱 다이안하이드라이드 10.910g (0.05mol) 과 4,4’-메틸렌비스(싸이클로헥실아민) 10.518g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.192 mL of N -methyl-2-pyrrolidone was added to a 500-mL 2-necked round bottom flask substituted with nitrogen gas, and 10.910 g (0.05 mol) of pyromellitic dianhydride and 4,4'-methylenebis Hexylamine) was added thereto, followed by reaction at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 5배에 해당하는 몰 수의 무수 프로피온산 32.535g (0.25mol)과 트라이메틸아민 14.778g (0.25mol)을 넣고 40℃에서 24시간 교반 시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 부분지방족 폴리이미드를 합성하였다.Next, 32.535 g (0.25 mol) of anhydrous propionic acid and 14.778 g (0.25 mol) of trimethylamine corresponding to 5 times the number of repeating units of the polyamic acid were added to the solution, stirred at 40 ° C for 24 hours, Lt; / RTI > After filtration, the mixture was washed with 100 mL of water and 100 mL of methanol, followed by vacuum drying to synthesize a partially aliphatic polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 3)에서는 1772cm- 1와 1716cm-1에서 이미드기의 C=O 흡수띠, 1381cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 27㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 8).In the infrared absorption spectrum of the synthesized polymer (Fig. 3) 1772cm - 1 and 1716cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1381cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 450 nm at 90% or more (Fig. 8).
실시예 7: 전지환식 폴리이미드의 필름 제조Example 7: Film production of battery cyclic polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 146 mL을 넣고 1,2,3,4-싸이클로펜탄테트라카르복실릭 다이안하이드라이드 10.507g (0.05mol) 과 1,4-다이아미노싸이클로헥산 5.709g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.Into a 500-mL 2-necked round bottom flask substituted with nitrogen gas, 146 mL of N -methyl-2-pyrrolidone was added, and 10.507 g (0.05 mol) of 1,2,3,4-cyclopentanetetracarboxylic dianhydride was added thereto. And 5.709 g (0.05 mol) of 1,4-diaminocyclohexane were added thereto, and reacted at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 5배에 해당하는 몰 수의 무수 아세트산 25.522g (0.25mol)과 피리딘 19.775g (0.25mol)을 넣고 40℃에서 1시간 교반 시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 전지방족 폴리이미드를 합성하였다.Next, 25.522 g (0.25 mol) of acetic anhydride and 19.775 g (0.25 mol) of pyridine were added to the solution, and the mixture was stirred at 40 ° C for 1 hour, Reprecipitated. After filtration, the filtrate was washed with 100 mL of water and 100 mL of methanol, followed by vacuum drying to synthesize all aliphatic polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 4)에서는 1775cm- 1와 1719cm-1에서 이미드기의 C=O 흡수띠, 1387cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 25㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 9).In the infrared absorption spectrum (Fig. 4) of the synthesized polymers 1775cm - 1 and 1719cm -1 in the already C = O absorption band of in deugi, 1387cm -1 The absorption band of CN already deugi was observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 450 nm at 90% or more (FIG. 9).
실시예 8: 전지환식 폴리이미드의 필름 제조Example 8: Film production of battery cyclic polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 146 mL을 넣고 1,2,3,4-싸이클로펜탄테트라카르복실릭 다이안하이드라이드 10.507g (0.05mol) 과 1,4-다이아미노싸이클로헥산 5.709g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.Into a 500-mL 2-necked round bottom flask substituted with nitrogen gas, 146 mL of N -methyl-2-pyrrolidone was added, and 10.507 g (0.05 mol) of 1,2,3,4-cyclopentanetetracarboxylic dianhydride was added thereto. And 5.709 g (0.05 mol) of 1,4-diaminocyclohexane were added thereto, and reacted at 0 to 25 ° C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 5배에 해당하는 몰 수의 무수 아세트산 25.522g (0.25mol)과 피리딘 19.775g (0.25mol)을 넣고 40℃에서 48시간 교반 시킨 후 물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 전지방족 폴리이미드를 합성하였다.Then 25.522 g (0.25 mol) of acetic anhydride and 19.775 g (0.25 mol) of pyridine were added to the solution, and the mixture was stirred at 40 ° C for 48 hours, Reprecipitated. After filtration, the filtrate was washed with 100 mL of water and 100 mL of methanol, followed by vacuum drying to synthesize all aliphatic polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 4)에서는 1774cm- 1와 1718cm-1에서 이미드기의 C=O 흡수띠, 1387cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 5이하이며, 450㎚에서 90%이상의 광투과율을 나타내는 23㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 9).In the infrared absorption spectrum of the synthesized polymer (Fig. 4) 1774cm - 1 and 1718cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1387cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 5 or less and a light transmittance of 450 nm at 90% or more (Fig. 9).
비교예 1: 공중합체 폴리이미드의 필름 제조Comparative Example 1: Film Production of Copolymer Polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 267 mL을 넣고 1.2.3.4-싸이클로뷰탄테트라카르복실릭 다이안하이드라이드 4.903g (0.025mol) 과 3,3’,4,4’-벤조 피논테트라카르복실릭 다이안하이드라이드 8.056g (0.025mol)과 2,2-비스(4-아미노페닐)헥사플루오로프로판 16.713g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다.To a 500-mL 2-neck round bottom flask substituted with nitrogen gas was added 267 mL of N -methyl-2-pyrrolidone, and 4.903 g (0.025 mol) of 1,2,3,4-cyclobutane tetracarboxylic dianhydride and 3,3 (0.025 mol) of 4,4'-benzophenone tetracarboxylic dianhydride and 16.713 g (0.05 mol) of 2,2-bis (4-aminophenyl) hexafluoropropane. C for 24 hours to synthesize polyamic acid.
다음으로 상기 용액에 폴리아믹산의 반복단위에 대해 2배에 해당하는 몰 수의 무수 아세트산 10.209g (0.1 mol)과 피리딘 7.91g (0.1mol)을 넣고 160℃에서 12시간 환류 시킨 후 상온까지 온도를 내린 후 과량의 얼음물을 사용하여 재침전을 하였다. 여과 후 물 100mL와 메탄올 100mL로 세척 후 진공 건조하여 공중합체 폴리이미드를 합성하였다.Next, 10.209 g (0.1 mol) of acetic anhydride and 7.91 g (0.1 mol) of pyridine were added to the solution in an amount corresponding to twice the repeating unit of the polyamic acid, and the mixture was refluxed at 160 ° C. for 12 hours, And then reprecipitated using an excessive amount of ice water. Filtered, washed with 100 mL of water and 100 mL of methanol, and vacuum-dried to synthesize a copolymer polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 5)에서는 1778cm- 1와 1719cm-1에서 이미드기의 C=O 흡수띠, 1380cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 56이며, 450㎚에서 90%이하의 광투과율을 나타내는 28㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 10).In the infrared absorption spectrum of the synthesized polymer (Fig. 5) 1778cm - 1 and 1719cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1380cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 56 and a light transmittance of 450 nm at 90% or less (Fig. 10).
비교예 2: 공중합체 폴리이미드의 필름 제조Comparative Example 2: Film production of copolymer polyimide
질소 가스로 치환한 500-mL 2구 둥근바닥 플라스크에 N-메틸-2-피롤리돈 277 mL을 넣고 1.2.3.4-싸이클로뷰탄테트라카르복실릭 다이안하이드라이드 4.903g (0.025mol) 과 3,3’,4,4’-벤조 피논테트라카르복실릭 다이안하이드라이드 8.056g (0.025mol)과 2,2-비스(4-아미노페닐)헥사플루오로프로판 16.713g (0.05mol)을 넣은 후 0 ~ 25℃에서 24시간 반응시켜 폴리아믹산을 합성하였다. N -methyl-2-pyrrolidone (277 mL) was added to a 500-mL two-neck round bottom flask substituted with nitrogen gas, and 4.903 g (0.025 mol) of 1.2.3.4-cyclobutane tetracarboxylic dianhydride and 3,3 (0.025 mol) of 4,4'-benzophenone tetracarboxylic dianhydride and 16.713 g (0.05 mol) of 2,2-bis (4-aminophenyl) hexafluoropropane. C for 24 hours to synthesize polyamic acid.
다음으로 상기 합성된 폴리아믹산 용액을 250 ~ 300℃로 오븐 또는 핫플레이트로 단계별로 승온하여 12시간 동안 가열하는 방법을 사용하여 폴리이미드를 수득하였다.Next, the synthesized polyamic acid solution was heated at 250 to 300 ° C in an oven or hot plate stepwise and heated for 12 hours to obtain polyimide.
상기 합성된 중합체의 적외선 흡수 스펙트럼(도 5)에서는 1777cm- 1와 1718cm-1에서 이미드기의 C=O 흡수띠, 1381cm-1에서 이미드기의 C-N 흡수띠가 관찰되었다. 상기 합성된 중합체를 NMP에 용해시켜 황색 지수가 67이며, 450㎚에서 90%이하의 광투과율을 나타내는 21㎛ 두께의 폴리이미드 필름을 얻을 수 있었다(도 10). In the infrared absorption spectrum of the synthesized polymer (Fig. 5) 1777cm - 1 and 1718cm - is already in the C = O absorption band deugi in 1, already CN absorption band of deugi at 1381cm -1 were observed. The synthesized polymer was dissolved in NMP to obtain a polyimide film having a yellow index of 67 and a light transmittance of 450 nm at 90% or less (FIG. 10).
반응 온도Imidated
반복 단위에 대한 촉매 및 탈수제의 몰 비Polyamic acid
The molar ratio of the catalyst and the dehydrating agent to the repeating unit
안함use
Do not
이미다졸1,2-dimethyl
Imidazole
메틸아민try
Methylamine
아세트산myriad
Acetic acid
아세트산myriad
Acetic acid
아세트산myriad
Acetic acid
아세트산myriad
Acetic acid
벤조산myriad
Benzoic acid
프로피온산myriad
Propionic acid
아세트산myriad
Acetic acid
아세트산myriad
Acetic acid
아세트산myriad
Acetic acid
시간Imidated
time
(450nm)Permeability
(450 nm)
대한 용해도To an organic solvent of polyimide
Solubility in water
깨짐film
fracture
폴리이미
드의 열분
해 온도Synthesized
Polyimide
Heat
Sun temperature
폴리이미
드분자량Synthesized
Polyimide
De molecular weight
상기 표 1에서 확인할 수 있듯이 실시예 1 내지 8에서는 이미드화 반응이 20 내지 80℃ 온도 범위 내에서 수행되었으며 상기 방법으로 얻어진 폴리이미드는 유기 용매에 대한 용해성이 좋다. 상기 폴리이미드를 이용하여 두께가 20 ~ 30㎛ 범위 내인 폴리이미드 필름을 제작하여 특성을 평가한 결과 파장 450㎚에서의 투과도가 90% 이상, 황색 지수 5이하의 무색·투명하며 유연한 필름이 얻어지는 것을 확인할 수 있었다.As shown in Table 1, in Examples 1 to 8, the imidization reaction was carried out within a temperature range of 20 to 80 ° C, and the polyimide obtained by the above method had good solubility in an organic solvent. A polyimide film having a thickness in the range of 20 to 30 mu m was produced using the polyimide to evaluate the characteristics thereof. As a result, a colorless, transparent and flexible film having a transmittance of 90% or more at a wavelength of 450 nm and a yellow index of 5 or less was obtained I could confirm.
이에 비하여 비교예 1과 비교예 2에서는 이미드화 반응이 160℃ 이상에서 수행되었고, 상기 방법으로 얻어진 폴리이미드를 이용하여 두께가 20 ~ 30㎛ 범위 내인 폴리이미드 필름을 제작하여 특성을 평가한 결과 파장 450㎚에서의 투과도가 80%이하, 황색 지수 50 이상의 필름이 얻어지는 것을 확인할 수 있었다. On the other hand, in Comparative Examples 1 and 2, the imidization reaction was carried out at 160 ° C. or higher. A polyimide film having a thickness in the range of 20 to 30 μm was produced using the polyimide obtained by the above- It was confirmed that a film having a transmittance at 450 nm of 80% or less and a yellow index of 50 or more was obtained.
Claims (14)
(b) 상기 제조된 폴리아믹산 용액에 화학적 탈수제 및 촉매를 첨가하되, 상기 화학적 탈수제 및 촉매는 각각 폴리아믹산 반복 단위에 대하여 동일 내지 50배의 몰비로 첨가되는 단계;
(c) 상기 폴리아믹산 용액을 25 내지 60℃에서 이미드화 반응시켜 폴리이미드 용액을 제조하는 단계;
(d) 상기 제조된 폴리이미드 용액을 기판에 도포하는 단계; 및
(e) 상기 도포된 폴리이미드 용액을 20 내지 100℃의 온도 범위 및 1 기압 이하의 조건에서 건조하여 폴리이미드 필름을 제조하는 단계; 를 포함하고,
상기 다이안하이드라이드는 치환 또는 비치환된 1종 이상의 다이안하이드라이드이고, 상기 다이아민은 치환 또는 비치환된 1종 이상의 다이아민인,
폴리이미드 필름 제조방법.
(a) preparing a polyamic acid solution by mixing dianhydride and diamine in a solvent;
(b) adding a chemical dehydrating agent and a catalyst to the prepared polyamic acid solution, wherein the chemical dehydrating agent and the catalyst are added at the same to 50-fold molar ratio with respect to the polyamic acid repeating unit;
(c) preparing a polyimide solution by imidizing the polyamic acid solution at 25 to 60 캜;
(d) applying the prepared polyimide solution to a substrate; And
(e) drying the applied polyimide solution at a temperature in the range of 20 to 100 캜 and at a pressure of 1 atm or less to produce a polyimide film; Lt; / RTI >
Wherein said dianhydride is at least one substituted or unsubstituted dianhydride, said diamine being at least one substituted or unsubstituted diamine,
A method for producing a polyimide film.
상기 (a)단계에서 제조되는 폴리아믹산 용액을 재침전, 여과 및 건조하는 과정을 순차적으로 거쳐 폴리아믹산 분말을 제조하고, 상기 폴리아믹산 분말을 용매에 용해시켜 폴리아믹산 용액을 제조하여 상기 (b)단계로 이행하는 폴리이미드 필름 제조방법.
The method according to claim 1,
The polyamic acid solution is prepared by sequentially preparing the polyamic acid solution prepared in step (a) by re-precipitation, filtration and drying, and dissolving the polyamic acid powder in a solvent to prepare a polyamic acid solution. Wherein the polyimide film is a polyimide film.
상기 (c)단계에서 제조되는 폴리이미드 용액을 재침전, 여과 및 건조하는 과정을 순차적으로 거쳐 폴리이미드 분말을 제조하고, 상기 폴리이미드 분말을 용매에 용해시켜 폴리이미드 용액을 제조하여 상기 (d)단계로 이행하는 폴리이미드 필름 제조방법.
The method according to claim 1,
The polyimide solution prepared in step (c) is re-precipitated, filtered and dried to prepare a polyimide powder. The polyimide powder is dissolved in a solvent to prepare a polyimide solution. Wherein the polyimide film is a polyimide film.
상기 다이안하이드라이드는 방향족 또는 지방족 다이안하이드라이드인 폴리이미드 필름 제조방법.
The method according to claim 1,
Wherein the dianhydride is an aromatic or aliphatic dianhydride.
상기 다이안하이드라이드는 하기의 화학식 1의 다이안하이드라이드인 폴리이미드 필름 제조방법.
<화학식 1>
(상기 화학식 1에서 R1은 아래의 화합물
로 이루어지는 군에서 선택된다.)
5. The method of claim 4,
Wherein the dianhydride is a dianhydride of the following formula (1).
≪ Formula 1 >
(R 1 in the formula 1 is a compound of the following
. ≪ / RTI >
상기 다이아민은 방향족 또는 지방족 다이아민인 폴리이미드 필름 제조방법.
The method according to claim 1,
Wherein the diamine is an aromatic or aliphatic diamine.
상기 다이아민은 하기의 화학식 2의 다이아민인 폴리이미드 필름 제조방법.
<화학식 2>
(상기 화학식 2에서 R2는 아래의 화합물
로 이루어지는 군에서 선택된다.)
The method according to claim 6,
Wherein the diamine is a diamine of the following formula (2).
(2)
(Wherein R < 2 > represents the following compound
. ≪ / RTI >
상기 용매는 N-메틸-2-피롤리돈, N,N-다이메틸아세트아미드, N,N-다이메틸포름아미드, N-비닐피롤리돈, N-메틸카프로락탐, 디메틸술폭시드, 테트라메틸요소, 피리딘, 디메틸술폰, 헥사메틸술폭시드, 메타-크레졸, 감마-부티로락톤, 에틸셀로솔브, 부틸셀로솔브, 에틸카르비톨, 부틸카르비톨, 에틸카르비톨 아세테이트, 부틸카르비톨 아세테이트, 에틸렌글리콜, 젖산에틸, 젖산부틸, 시클로헥사논, 시클로펜타논, 헥산(노말헥산, 이소헥산, 시클로헥산), 펜탄, 헵탄, 벤젠, 톨루엔, 자일렌, 메탄올, 에탄올, 프로판올(노말프로판올, 이소프로판올), 부탄올(노말-, 이소-, 터셔리-), 시클로헥사놀, 옥탄올, 벤질알콜, 아세톤, 메틸에틸케톤, 메틸부틸케톤, 초산메틸, 초산에틸, 디에틸에테르, 이소프로필에테르, 테트라하이드로퓨란, 클로로포름, 다이옥세인, 디에틸포름아미드, 설포레인, 개미산, 초산, 프로피온산, 아세트나이트라일 및 테트랄린으로 이루어지는 군에서 선택되는 1종의 단일 용매 또는 2종 이상의 혼합 용매인 폴리이미드 필름 제조방법.
4. The method according to any one of claims 1 to 3,
The solvent may be N -methyl-2-pyrrolidone, N, N -dimethylacetamide, N, N -dimethylformamide, N -vinylpyrrolidone, N -methylcaprolactam, dimethylsulfoxide, tetramethylurea, pyridine, dimethylsulfone, hexamethylsulfoxide, meta-cresol, gamma-butyrolactone, Butyl cellosolve, ethyl carbitol, butyl carbitol, ethyl carbitol acetate, butyl carbitol acetate, ethylene glycol, ethyl lactate, butyl lactate, cyclohexanone, cyclopentanone, hexane (normal hexane, (Isopropanol, isopropanol), butanol (normal-, iso-, tertiary-), cyclohexanol, octanol, cyclohexane, cyclohexane, cyclohexane, cyclohexane, pentane, heptane, benzene, toluene, xylene, methanol, ethanol, Benzyl alcohol, acetone, methyl ethyl ketone, methyl butyl ketone, methyl acetate, ethyl acetate, diethyl ether, isopropyl ether, tetrahydrofuran, chloroform, dioxane, diethylformamide, sulfolane, formic acid, , Acetone The Tra days and a method of producing a polyimide film tetralin in one single solvent or a mixed solvent of two or more of the species selected from the group consisting of.
상기 (a)단계는 0 내지 30℃의 온도에서 진행되는 폴리이미드 필름 제조방법.
The method according to claim 1,
Wherein the step (a) is performed at a temperature of 0 to 30 캜.
상기 (a)단계는 1 내지 48시간 동안 진행되는 폴리이미드 필름 제조방법.
The method according to claim 1,
Wherein the step (a) is performed for 1 to 48 hours.
상기 화학적 탈수제는 무수 아세트산, 무수 프로피온산, 무수 부티르산, 무수 벤조산, 무수 아디프산, 무수 이소프탈산, 프탈릭 무수물 및 트리멜리틱 무수물로 이루어지는 군에서 선택되는 1종 또는 2종 이상의 탈수제인 폴리이미드 필름 제조방법.
The method according to claim 1,
Wherein the chemical dehydrating agent is at least one dehydrating agent selected from the group consisting of acetic anhydride, anhydrous propionic acid, anhydrous butyric acid, anhydrous benzoic acid, anhydrous adipic acid, anhydrous isophthalic acid, phthalic anhydride and trimellitic anhydride. Gt;
상기 촉매는 트라이메틸아민, 트라이에틸아민, 메틸피롤리딘, N,N-다이메틸헥실아민, 이미다졸, 1,2-다이메틸이미다졸, N-메틸이미다졸, N-벤질-2-메틸이미다졸, 2-메틸이미다졸, 2-에틸-4-메틸이미다졸, 5-메틸벤즈이미다졸, N-벤질-2-메틸이미다졸, 이소퀴놀린, 3,5-다이메틸피리딘, 3,4-다이메틸피리딘, 2,5-다이메틸피리딘, 2,4-다이메틸피리딘 및 4-n-프로필피리딘으로 이루어지는 군에서 선택되는 1종 또는 2종 이상의 촉매인 폴리이미드 필름 제조방법.
The method according to claim 1,
The catalyst may be selected from the group consisting of trimethylamine, triethylamine, methylpyrrolidine, N, N -dimethylhexylamine, imidazole, 1,2-dimethylimidazole, N -methylimidazole, N- Methylimidazole, N -benzyl-2-methylimidazole, isoquinoline, 3,5-di-methylimidazole, A polyimide film which is at least one catalyst selected from the group consisting of methyl pyridine, 3,4-dimethylpyridine, 2,5-dimethylpyridine, 2,4-dimethylpyridine and 4-n- Gt;
상기 (c) 단계는 10 분 내지 72시간 동안 진행되는 폴리이미드 필름 제조방법.
The method according to claim 1,
Wherein the step (c) is performed for 10 minutes to 72 hours.
상기 (d) 단계의 폴리이미드 용액 내의 폴리이미드는 전체 용액 중량 대비 1 내지 90wt%인 폴리이미드 필름 제조방법. The method according to claim 1,
Wherein the polyimide in the polyimide solution in step (d) is 1 to 90 wt% based on the total weight of the solution.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020170092009A KR20170086455A (en) | 2017-07-20 | 2017-07-20 | Preparation method of polyimide film, and the polyimide film thereby |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020170092009A KR20170086455A (en) | 2017-07-20 | 2017-07-20 | Preparation method of polyimide film, and the polyimide film thereby |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020160110800A Division KR20160105378A (en) | 2016-08-30 | 2016-08-30 | Preparation method of polyimide film, and the polyimide film thereby |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020170133779A Division KR20170118662A (en) | 2017-10-16 | 2017-10-16 | Preparation method of polyimide film, and the polyimide film thereby |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170086455A true KR20170086455A (en) | 2017-07-26 |
Family
ID=59427228
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020170092009A KR20170086455A (en) | 2017-07-20 | 2017-07-20 | Preparation method of polyimide film, and the polyimide film thereby |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR20170086455A (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210059404A (en) * | 2019-11-15 | 2021-05-25 | 에스케이씨 주식회사 | Polyimide-based film, cover window and display device comprising same |
-
2017
- 2017-07-20 KR KR1020170092009A patent/KR20170086455A/en not_active Application Discontinuation
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20210059404A (en) * | 2019-11-15 | 2021-05-25 | 에스케이씨 주식회사 | Polyimide-based film, cover window and display device comprising same |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101714980B1 (en) | Preparation method of polyimide using water as a dispersion medium | |
| JPH0211615B2 (en) | ||
| KR102198357B1 (en) | Preparation method for polyimide | |
| CN112334511A (en) | Polyimide resin and method for producing same, and polyimide film and method for producing same | |
| KR102050660B1 (en) | Preparation method for polyimide | |
| KR101548877B1 (en) | Preparation method for polyimide from salt of monomer and the polyimide thereby | |
| US20100228002A1 (en) | Self-crosslinking polyamic acid, self-crosslinking polyimide, method of manufacturing self-crosslinking polyimide, and self-crosslinking polyimide film including the self-crosslinking polyimide | |
| KR101755251B1 (en) | Method for recycling water in the preparation of polyimide using water as a dispersion medium | |
| KR101838333B1 (en) | Polyimide-based film and mehtod for preparing same | |
| KR102261849B1 (en) | Preparation method of polyamideimide copolymers | |
| KR20160105378A (en) | Preparation method of polyimide film, and the polyimide film thereby | |
| KR102219892B1 (en) | Manufacturing method of polyimide powder and polyimide power manufactured by the same | |
| KR101787807B1 (en) | Polyimide-based film and mehtod for preparing same | |
| KR20150141839A (en) | Preparation method of polyimide using water as a dispersion medium | |
| JPS60188427A (en) | Novel polyimide resin and its production | |
| KR101728823B1 (en) | The manufacturing method of polyimide | |
| EP1408067A1 (en) | Colorless and transparent polyimidesilicone resin having thermosetting functional groups | |
| KR20130078307A (en) | Polyimide film and method for preparing same | |
| KR20160013772A (en) | Preparation method of polyimide film, and the polyimide film thereby | |
| KR20170086455A (en) | Preparation method of polyimide film, and the polyimide film thereby | |
| KR100519652B1 (en) | Polyamic acid random copolymer and Polyimide random copolymer | |
| KR101709378B1 (en) | Preparation method of polyimide under high pressure | |
| KR20170100794A (en) | Polyamic acid, Polyimide Resin, Polyimide Film and Display Device Comprising Thereof | |
| KR101692137B1 (en) | Preparation method for polyimide powder and polyimide product from water soluble polyamic acid | |
| KR20170118662A (en) | Preparation method of polyimide film, and the polyimide film thereby |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| A107 | Divisional application of patent | ||
| E601 | Decision to refuse application |