KR20150050090A - 마이크로웨이브 조사에 의해 유효 성분 함량이 증가된 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 조성물, 건강기능식품용 조성물, 및 개체의 신장 독성을 억제하는 방법 - Google Patents
마이크로웨이브 조사에 의해 유효 성분 함량이 증가된 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 조성물, 건강기능식품용 조성물, 및 개체의 신장 독성을 억제하는 방법 Download PDFInfo
- Publication number
- KR20150050090A KR20150050090A KR1020130131500A KR20130131500A KR20150050090A KR 20150050090 A KR20150050090 A KR 20150050090A KR 1020130131500 A KR1020130131500 A KR 1020130131500A KR 20130131500 A KR20130131500 A KR 20130131500A KR 20150050090 A KR20150050090 A KR 20150050090A
- Authority
- KR
- South Korea
- Prior art keywords
- extract
- panax
- composition
- microwave irradiation
- renal toxicity
- Prior art date
Links
- 0 C[C@](CCC=C(C)C)(C(CC1)C(C(C2)O)[C@]1(C)[C@](C)(CC1*)C2[C@@](C)(CC2)C1C(C)(C)C2O)O Chemical compound C[C@](CCC=C(C)C)(C(CC1)C(C(C2)O)[C@]1(C)[C@](C)(CC1*)C2[C@@](C)(CC2)C1C(C)(C)C2O)O 0.000 description 3
Images
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L19/00—Products from fruits or vegetables; Preparation or treatment thereof
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L3/00—Preservation of foods or foodstuffs, in general, e.g. pasteurising, sterilising, specially adapted for foods or foodstuffs
- A23L3/005—Preservation of foods or foodstuffs, in general, e.g. pasteurising, sterilising, specially adapted for foods or foodstuffs by heating using irradiation or electric treatment
- A23L3/01—Preservation of foods or foodstuffs, in general, e.g. pasteurising, sterilising, specially adapted for foods or foodstuffs by heating using irradiation or electric treatment using microwaves or dielectric heating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/25—Araliaceae (Ginseng family), e.g. ivy, aralia, schefflera or tetrapanax
- A61K36/258—Panax (ginseng)
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Nutrition Science (AREA)
- Food Science & Technology (AREA)
- Polymers & Plastics (AREA)
- Mycology (AREA)
- Biotechnology (AREA)
- Alternative & Traditional Medicine (AREA)
- Botany (AREA)
- Medical Informatics (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicines Containing Plant Substances (AREA)
Abstract
본 발명은 파낙스속 식물 또는 그 추출물을 마이크로웨이브 반응시켜 얻어진 진세노사이드 Rg3, Rk1 및 Rg5 및 비진세노사이드 성분이 함유된 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 약학 조성물, 건강기능식품용 조성물 및 개체의 신장 독성을 억제하는 방법을 제공한다.
Description
본 발명은 가공 파낙스속 식물 추출물에 관한 것으로, 보다 구체적으로는 파낙스속 식물 추출물을 가공처리하여 증가된 양의 진세노사이드 Rg3, Rk1 및 Rg5 및 비진세노사이드 성분이 함유된 가공 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 조성물, 건강기능식품용 조성물 및 개체의 신장 독성을 억제하기 위한 방법에 관한 것이다.
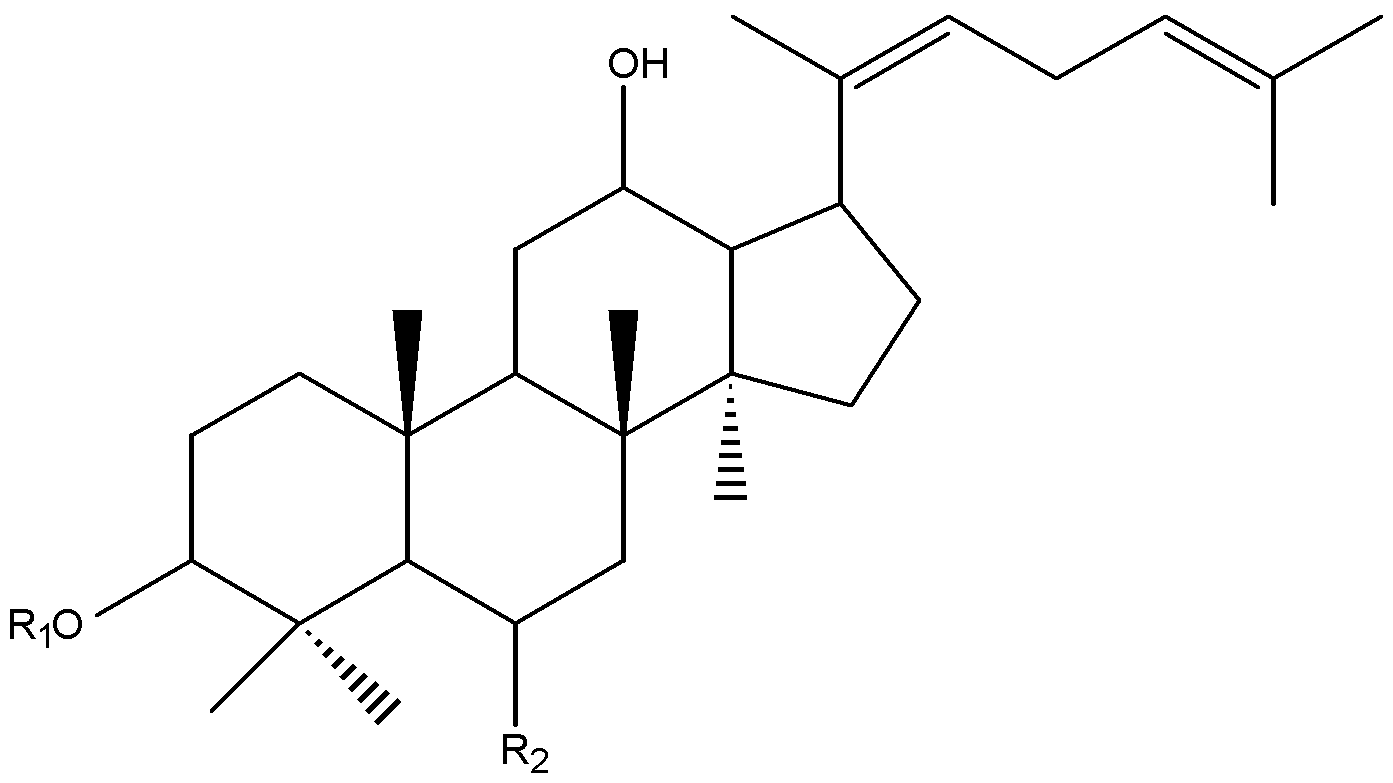
인삼(Panax ginseng)은 식물 분류학상 파낙스(Panax)속 오가피과(Araliaceae)에 속하는 다년생 식물로서, 인삼과 유사한 효능을 갖는 파낙스속 식물로는 화기삼(Panax quinquefolia), 전칠삼(삼칠, Panax notoginseng), 죽절삼(Panax japonica), 삼엽삼(Panax trifolia), 히말라야삼(Panax pseudoginseng), 베트남삼(Panax vietnamensis) 등이 있다. 이러한 파낙스속 식물에는 전분 등의 탄수화물(60-70%), 단백질과 아미노산 등의 함질소화합물(12-16%), 폴리아세틸렌과 페놀계 화합물을 포함하는 지용성 성분(1%) 그리고 비타민 및 무기질 성분(4-6%) 등이 함유되어 있으며, 다른 식물과는 달리 담마란(dammarane) 골격에 1-4개의 당이 결합되어 있는 담마란계 사포닌 (3-6%)을 공통으로 함유하고 있다. 특히 인삼에 함량이 높은 사포닌은 진세노사이드 Rb1, Rb2, Rc, Rd, Rg1, Re 등이며, 이러한 사포닌 성분들은 다양한 약효를 나타내는데 그 구조에 따라 약효의 종류와 강도가 매우 다르다. 파낙스속 식물의 담마란계 사포닌은 프로토파낙사디올 (protopanaxadiol: PPD) 또는 프로토파낙사트리올 (protopanaxatriol: PPT)을 모핵으로 가지며, 식 1과 같이 표시될 수 있다.
식 1 중 R1, R2, 및 R3에 따라 담마란계 사포닌은 다음과 같이 분류될 수 있다.
| 그룹 | 진세노사이드 | R1 | R2 | R3 |
| 프로토파낙사디올 | Ra1 | -Glc-Glc | -H | -Glc-Ara(pyr)-Xyl |
| Ra2 | -Glc-Glc | -H | -Glc-Ara(fur)-Xyl | |
| Ra3 | -Glc-Glc | -H | -Glc-Glc-Xyl | |
| Rb1 | -Glc-Glc | -H | -Glc-Glc | |
| Rb2 |
-Glc-Glc | -H | -Glc-Ara(pyr) | |
| Rb3 | -Glc-Glc | -H | -Glc-Xyl | |
| Rc | -Glc-Glc | -H | -Glc-Ara(fur) | |
| Rd | -Glc-Glc | -H | -Glc | |
| Rg3(20-R,S) | -Glc-Glc | -H | -H | |
| Rh2(20-R,S) | -Glc | -H | -H | |
| Rs1 | -Glc-Glc-Ac | -H | -Glc-Ara(pyr) | |
| Rs2 | -Glc-Glc-Ac | -H | -Glc-Ara(fur) | |
| Rs3 | -Glc-Glc-Ac | -H | -H | |
| malonyl-Rb1 | -Glc-Glc-malonyl | -H | -Glc-Glc | |
| malonyl-Rc | -Glc-Glc-malonyl | -H | -Glc-Ara(fur) | |
| malonyl-Rd | -Glc-Glc-malonyl | -H | -Glc | |
| pseudoginsenoside F2 | -Glc | -H | -Glc | |
| notoginsenoside Fe | -Glc | -H | -Glc-Ara(fur) | |
| 프로토파낙사트리올 | Re | -H | -OGlc-Rha | -Glc |
| Ff | -H | -OGlc-Glc | -H | |
| Rg1 | -H | -OGlc | -Glc | |
| Rg2(20-R,S) | -H | -OGlc-Rha | -H | |
| Rh1(20-R,S) | -H | -OGlc | -H | |
| notoginsenoside R1 | -H | -OGlc-Xyl | -Glc | |
| notoginsenoside R2 | -H | -OGlc-Xyl | -H | |
| pseudoginsenoside F1 | -H | -OH | -Glc | |
| pseudoginsenoside F8 | -Glc-GlcAc | -OH | -Glc-Glc | |
| pseudoginsenoside F3 | -H | -OH | -Glc-Ara(pyr) | |
| Rh4 | -H | -OGlc | -methyl |
Rg5와 Rk1은 각각 식 2 및 식 3으로 표시될 수 있는 화합물로서, 식 중 R1은 -Glc-Glc이고, R2는 -H이다.
진세노사이드 Rg5는 항산화효과, 항암효과, 항암제의 부작용인 면역력 저하 및 항암제 내성 억제 효과, 뇌기능 및 인지기능 개선효과, 혈관이완 효과, 혈소판 응집억제 효과, 피부염/건선 개선 효과, 항염증 효과가 있는 것으로 알려져 있다. 진세노사이드 Rk1은 주로 항암효과가 알려져 있으며, 혈관이완 효과, 혈소판 응집억제 효과, 뇌기능 및 인지기능 개선효과가 있는 것으로 알려져 있다.
프로토파낙사디올계 진세노사이드인 Rb1과 Rb2는 20번 위치에서 -Glc-Glc 또는 -Glc-Ara(pyr)의 이탈에 의하여 20(S)-Rg3 또는 20(R)-Rg3가 생성될 수 있다. 또한, 20(S)-Rg3 또는 20(R)-Rg3는 20번 위치에서 H2O의 이탈에 의하여 Rg5 및 Rk1이 생성될 수 있다.
신장은 혈액 속의 노폐물을 걸러내어 뇨의 형태로 내보내는 척추동물의 배설기관이다. 신장 독성을 일으키는 독성물질은 매우 다양하다. 신장 독성을 일으키는 것으로 알려진 화학물질에는 펜아세틴, 아스피린, 인도메타신 등의 비스테로이드성 해열 진통 소염제 퓨로마이신, 다우노마이신, 시클로포스파미드, 페니실라민, 아드리아마이신, 씨스플라틴 등의 항암제, 면역억제제, 아미카신, 겐타마이신, 카나마이신, 네오마이신, 시소마이신, 스트렙토마이신, 토브라마이신 등의 아미노글라이코사이드계 항생제, 세팔로스포린계 항생제, 이미페넴, 멜로페넴 등 카바페넴계 항생제, 카드뮴, 납, 수은, 크롬 등의 중금속 및 무기?유기중금속 화합물, 클로로포름, D-세린, 설폰아미드, 2-브로모에틸렌, 하이드로브로마이드 등의 화합물 또는 오카라톡신, 시트리닌과 같은 곰팡이 독소 등이 있으며, 대부분이 화학물질 또는 의약품에 있어서 신장 독성을 일으키는 정확한 기전이 밝혀지지 않은 경우가 많다.
신장이 독성물질의 표적이 되는 이유는, 정상적인 성인의 경우 하루에 약 180L의 혈액을 여과시킴에 따라 많은 혈류량이 흐르기 때문에 혈액에 수반된 독성물질이 축적될 가능성이 높기 때문이다. 또한 뇨의 생성 과정에 있어서, 뇨가 일시적으로 신장에 저장되기 때문에 독성물질이 농축되어 표적이 되기 때문이다.
이러한 신장 독성에 따른 질환의 예방 또는 치료를 위한 다수의 합성 제제가 개발되어 있으나, 인체에 장기간 적용시 부작용의 발생 가능성 등 안정성에 대한 문제로 인하여 천연물로부터 유래되는 제제의 중요성이 부각되고 있는 현실이다.
이에 본 발명자들은 마이크로웨이브 조사에 의해 유효 성분의 함량이 증가된 파낙스속 식물 추출물이 신장 질환의 예방 또는 치료에 효과를 가진다는 것을 발견하고, 본 발명을 완성하게 되었다.
일 양상은 신장 독성을 억제하기 위한 조성물을 제공하는 것이다.
다른 양상은 건강기능식품용 조성물을 제공하는 것이다.
다른 양상은 개체의 신장 독성을 억제하는 방법을 제공하는 것이다.
일 양상은 파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 진세노사이드 Rg3, Rk1 및 Rg5 및 비진세노사이드 성분이 함유된 파낙스속 식물 추출물을 활성 성분으로 함유하는 신장 독성을 억제하기 위한 조성물을 제공한다.
상기 조성물은 파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 진세노사이드 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상, 예를 들면, 95% 내지 100%, 98% 내지 100%, 90% 내지 100%, 또는 100% 포함하는 파낙스속 식물 추출물 (이하 '마이크로웨이브 조사된 식물 추출물'이라고도 함)을 함유할 수 있다. 또한, 상기 마이크로웨이브 조사 가공물은 진세노사이드 (Rg5 + Rk1)/(Rg3)의 비율이 현저히 높으며, 예를 들면, (Rg5+Rk1)/(Rg3)가 2 이상, 3 이상, 4 이상 또는 5 이상일 수 있다.
상기 추출물은 폴리스티렌 수지에 흡착성 물질인 것일 수 있다. 폴리스티렌 수지는 상대적으로 큰 표면적 (전형적으로 450-900 m2g), 높은 다공성 (porosity) (포어 부피, 전형적으로 0.6-1.8ml/G) 및 큰 평균 포어 크기 (전형적으로 100-800A)을 갖고 있어, 거친 입자 크기 (전형적으로 20-60 메쉬, wet)와 조합되어 높은 추출물 흐름 속도 (extract flow rate)와 표적 화합물의 보류 (retention)를 위한 큰 능력 (capacity)를 제공한다. 따라서, 소수성기의 소수성이 큰 유기 화합물, 예를 들면, 진세노사이드, 지용성 비타민, 항생물질, 효소 및 페놀성 화합물 등이 잘 흡착될 수 있다. 상기 폴리스티렌 수지는 DIAIONTM HP 20 수지일 수 있다. DIAIONTM HP 20 수지는 폴리스티렌 수지로서, 입자의 표면이 소수성 (hydrophobic)을 띠고 있어서 유기물이 흡착될 때 유기 분자 중의 소수성기가 흡착된다. 예를 들면, 폴리스티렌 수지로 충전된 크로마토그래피 칼럼에 파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 추출물을 흘려주어 소수성 물질을 상기 수지에 결합시킨 후, 용매로 용출하여 얻어진 물질인 것일 수 있다. 용출에 사용되는 용매는 물, 알콜 또는 그 조합에 의하여 추출된 것일 수 있다. 상기 알콜은 C1 내지 C10의 하나이상의 -OH기를 갖는 화합물일 수 있다. 상기 알콜은 C1 내지 C4의 알콜일 수 있다. 상기 알콜은 메탄올, 에탄올, 프로판올, 부탄올, 또는 그 조합인 것일 수 있다.
상기 비진세노사이드 성분은 항산화 활성을 갖는 것일 수 있다. 상기 추출물은 원료 인삼에 비해 비진세노사이드, 예를 들면 항산화 성분 함량이 2배 이상, 3배 이상, 4배 이상 또는 5배 이상 함유된 것일 수 있다.
상기 마이크로웨이브 조사는 파낙스속 식물 또는 파낙스속 식물 추출물에 마이크로웨이브를 조사하여 가열하는 열적 반응(thermal reaction)을 의미한다. 마이크로웨이브는 1m 내지 1mm의 파장을 갖는 라디오파, 또는 300MHz 내지 300GHz의 주파수를 갖는 라디오일 수 있다. 마이크로웨이브에 의한 가열은 반응물의 양이나 상태 등에 따라 달라질 수 있다. 마이크로웨이브 조사는 150℃ 내지 190℃, 예를 들면, 160℃ 내지 190℃, 170℃ 내지 190℃, 180℃ 내지 190℃, 150℃ 내지 180℃, 150℃ 내지 170℃, 150℃ 내지 160℃, 170℃ 내지 180℃, 또는 160℃ 내지 170℃에서 수행될 수 있다. 또한, 마이크로웨이브 조사는 30 분 내지 90 분, 30 분 내지 80 분, 30분 내지 70 분, 30분 내지 60 분, 30 분 내지 50, 30 분 내지 40 분,40 분 내지 90 분, 50 분 내지 90 분, 60분 내지 90 분, 70분 내지 90 분, 80 분 내지 90, 50 분 내지 80 분, 60 분 내지 80 분, 70 분 내지 80 분, 또는 50 분 내지 70 분 동안 수행할 수 있다. 마이크로웨이브 조사는 가압하에서, 예를 들면, 1 기압 내지 100기압, 2 기압 내지 100기압, 5 기압 내지 100기압, 7 기압 내지 100기압, 10 기압 내지 100기압, 15 기압 내지 100기압, 1 기압 내지 80기압, 2 기압 내지 80기압, 5 기압 내지 80기압, 7 기압 내지 80기압, 10 기압 내지 80기압, 15 기압 내지 80기압, 1 기압 내지 50기압, 2 기압 내지 50기압, 5 기압 내지 50기압, 7 기압 내지 50기압, 10 기압 내지 50기압, 15 기압 내지 50기압, 1 기압 내지 30기압, 2 기압 내지 30기압, 5 기압 내지 30기압, 7 기압 내지 30기압, 10 기압 내지 30기압, 또는 15 기압 내지 30기압의 압력하에서 수행되는 것일 수 있다. 마이크로웨이브 조사는 중성 용액, 예를 들면, 수성 용액 중에서 조사되는 것일 수 있다. 마이크로웨이브의 출력은 특별히 한정되는 것은 아니며, 반응물의 양에 따라 적절히 증감될 수 있고 예를 들어 50 내지 1000 W, 예를 들면, 100 내지 700W의 마이크로웨이브가 사용될 수 있다. 상기 마이크로웨이브 조사 조건은 특별히 한정되는 것은 아니며, 마이크로웨이브 조사에 의해 진세노사이드 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상 함유되도록 하는 임의의 반응 조건을 포함할 수 있다. 또한, (Rg5 + Rk1)/(Rg3)의 비율이 2 이상, 3이상, 4이상 또는 5 이상이 되도록 할 수 있는 임의의 반응을 포함할 수 있다. 상기 마이크로웨이브 조사의 생성물은 그대로 사용될 수도 있으나, 건조물 또는 동결건조물로서 함유될 수도 있다. 일 구체예에서, 마이크로웨이브 조사는 파낙스속 식물 또는 파낙스속 식물 추출물을 포함하는 수성 용액에 대하여, 30분 내지 90 분 동안 150 내지 190℃에서 가압하에서 예를 들면 1 기압 내지 100기압, 2 기압 내지 100기압, 5 기압 내지 100기압, 7 기압 내지 100기압, 10 기압 내지 100기압, 15 기압 내지 100기압, 1 기압 내지 80기압, 2 기압 내지 80기압, 5 기압 내지 80기압, 7 기압 내지 80기압, 10 기압 내지 80기압, 15 기압 내지 80기압, 1 기압 내지 50기압, 2 기압 내지 50기압, 5 기압 내지 50기압, 7 기압 내지 50기압, 10 기압 내지 50기압, 15 기압 내지 50기압, 1 기압 내지 30기압, 2 기압 내지 30기압, 5 기압 내지 30기압, 7 기압 내지 30기압, 10 기압 내지 30기압, 또는 15 기압 내지 30기압에서 수행되는 것일 수 있다.
상기 파낙스속 식물은 진세노사이드 Rb1, Rb2, Re, Rg1, Rc, 및 Rd 중 하나이상을 포함하는 것일 수 있다. 이러한 파낙스속 식물로는 인삼(Panax ginseng), 화기삼(Panax quinquefolia), 전칠삼(Panax notoginseng), 죽절삼(Panax japonica), 삼엽삼(Panax trifolia), 히말라야삼(Panax pseudoginseng), 베트남삼(Panax vietnamensis), 이들의 배양근, 열처리 또는 효소처리 가공물, 또는 이들의 조합이 이용될 수 있다. 상기 열처리 가공물은 홍삼, 흑삼을 포함한다. 바람직하게는 인삼이 사용될 수 있다.
상기 마이크로웨이브 조사의 반응물에 해당하는 파낙스속 식물 추출물은 진세노사이드 Rb1, Rb2, Rc, 및 Rd 중 하나이상을 포함하는 임의의 파낙스속 식물의 추출물일 수 있다. 또한, Re, 및/또는 Rg1을 더 포함하는 것일 수 있다. 파낙스속 식물 추출물은 조추출물일 수도 있으며 추가적인 용매 분획이나 크로마토그래피에 의해 정제된 정제물일 수도 있다. 예를 들어 파낙스속 식물의 물, C1-C4 알콜, 또는 이들의 혼합물의 조추출물; 그 조추출물의 n-헥산, 메틸렌클로라이드, 에틸아세테이트, 부탄올 또는 이들의 혼합물의 용매 분획물; 또는 그 용매 분획물의 정제물일 수 있다.
상기 물, C1-C4 알콜, 또는 이들의 혼합물의 조추출물은 예를 들면, 메탄올 또는 에탄올의 조추출물일 수 있다. 추출 시 용매를 식물 분량의 약 5 내지 15배 첨가하여 추출하는 것, 예를 들면, 약 10 배 첨가하여 추출하는 것일 수 있다. 상기 용매를 가한 후 가열 추출, 초음파 추출, 환류 추출 등의 통상의 방법으로 추출할 수 있으며, 바람직하게는 초음파 추출이 이용될 수 있다. 추출시 용매의 온도는 약 50 ~ 200℃, 예를 들면, 120℃일 수 있으나 이에 한정하지 않는다. 또한, 추출시간은 약 2 ~ 4 시간, 예를 들면 약 3 시간일 수 있으나 이에 한정되지 않는다. 아울러, 추출 회수는 1 내지 5 회, 예를 들면 3 회 반복 추출하는 것일 수 있으나 이에 한정되는 것은 아니다. 이러한 방법에 의하여 얻어진 조추출물을 상기 파낙스속 식물 추출물로서 사용할 수도 있으나, 상기 조추출물을 추가적으로 유기용매로 추출한 용매분획물이 이용될 수도 있다. 상기 유기용매 분획물은 상기 조추출물을 메틸렌클로라이드, 헥산, 에틸아세테이트, 부탄올, 또는 이들의 혼합물 등으로 추출한 분획물일 수 있으나, 이에 한정되지 않는다.
상기 유기 용매 분획물을 더욱 정제한 정제물을 상기 파낙스속 식물 추출물로서 사용할 수도 있으며, 예를 들어 칼럼 크로마토그래피에 의해 진세노사이드 Rb1, Rb2, Re, Rg1, Rc, 및 Rd 중 하나이상을 더욱 정제할 수 있다.
상기한 마이크로웨이브 조사 가공물은 얻어진 추출물 중 진세노사이드 총 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상, 95%이상, 또는 98%이상 함유된 것일 수 있다. 상기 진세노사이드 총 중량은 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5 또는 Re, Rg1, Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량일 수 있다. 상기한 마이크로웨이브 조사 가공물은 용매에 의하여 추출된 것으로서, 분획되지 않은 상태의 것일 수 있다.
상기 조성물은 파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 진세노사이드 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상 함유된 파낙스속 식물 추출물을 1mg 내지 1000mg, 10mg 내지 1000mg, 50mg 내지 1000mg, 100mg 내지 1000mg, 500mg 내지 1000mg, 1mg 내지 500mg, 1mg 내지 100mg, 1mg 내지 50mg, 1mg 내지 20mg, 1mg 내지 10mg, 10mg 내지 1000mg, 10mg 내지 500mg, 10mg 내지 100mg, 10mg 내지 50mg, 또는 10mg 내지 20mg 포함하는 것일 수 있다. 상기 마이크로웨이브 조사된 식물 추출물은 mg 당 Rg3, Rk1 및 Rg5을 0.9mg이상 포함하는 것일 수 있다.
상기 신장 독성은 약제를 개체 투여하는 것에 의하여 야기된 것일 수 있다. 상기 약제는 펜아세틴, 아스피린, 인도메타신과 같은 비스테로이드성 항염증제, 푸로마이신, 다우노마이신, 시클로포스파미드, 페니실라민, 아드리아마이신, 시스플라틴과 같은 항암제, 면역억제제, 아미카신, 겐타마이신, 카나마이신, 네오마이신, 시소마이신, 스트렙토마이신, 토브라마이신과 같은 아미노글리코시드게 항생제, 세팔로스포린계 항생제, 또는 이미페넴, 멜로페넴과 같은 카바페넴계 항생제일 수 있다. 상기 개체는 포유동물, 예를 들면 사람일 수 있다.
상기 신장 독성은 신장 세포 손상일 수 있다. 상기 신장 세포 손상은 산화적 스트레스로부터 야기되는 것일 수 있다. 상기 신장 독성은 신장 세포 손상으로부터 야기되는 신장 질환일 수 있다. 상기 신장 질환은 신장염, 신우염, 신증후군, 신장암, 급성신우신염, 만성신우신염, 신장결핵, 요로감염증, 요로결석, 요관결석, 급성신부전, 만성신부전 또는 당뇨병성신증, 만성사구체신염, 급성진행성신염, 네프로제증후군, 소상사구체경화증, 막성신증 또는 막성증식성사구체신염을 포함한다.
본 발명에 따른 약학 조성물은 당해 기술분야에 공지되어 있는 통상적인 약제학적 제형으로 제제화될 수 있다. 상기 약제학적 제형은 경구 투여제제, 주사제, 좌제, 경피 투여제제, 및 경비 투여제제를 포함하지만, 이에 한정되지 않는 임의의 제형으로 제제화되어 투여될 수도 있으나, 바람직하게는 액제, 유제, 현탁제, 엑스제, 또는 시럽제와 같은 액상 제제 및 산제, 과립제, 정제, 캡슐제, 또는 환제와 같은 고형 제제를 포함한 경구 투여용 제형으로 제제화될 수 있다.
상기 각각의 제형으로 제제화 시, 각각의 제형의 제조에 필요한 약제학적으로 허용 가능한 부형제 또는 첨가제를 부가하여 제조할 수 있다. 대표적으로 경구 투여용 고형 제제로 제제화 시 상기 부형제로서 희석제, 활택제, 결합제, 붕해제, 감미제, 안정제, 및 방부제 중에서 1 종 이상을 선택하여 사용할 수 있다. 상기 부형제는 약제학적으로 허용 가능한 것은 모두 가능하며, 구체적으로 희석제로는 유당, 옥수수 전분, 대두유, 미정질 셀룰로오스, 또는 만니톨, 활택제로는 스테아린산 마그네슘 또는 탈크, 결합제로는 폴리비닐피롤리돈 또는 히드록시프로필셀룰로오스가 바람직하다. 또한, 붕해제로는 카르복시메틸셀룰로오스 칼슘, 전분글리콜산나트륨, 폴라크릴린칼륨, 또는 크로스포비돈이 바람직하다. 경구 투여용 액상 제제로 제제화 시 흔히 사용되는 단순 희석제인 물, 리퀴드 파라핀 이외에 여러 가지 부형제, 예를 들면 습윤제, 감미제, 방향제 및 보존제 등이 포함될 수 있다. 상기 감미제로는 백당, 과당, 솔비톨, 또는 아스파탐, 안정제로는 카르복시메틸셀룰로오스나트륨, 베타-사이클로덱스트린, 백납, 또는 잔탄검, 보존제로는 파라옥시안식향산메틸, 파라옥시안식향산프로필, 또는 솔빈산칼륨이 바람직하다. 또한, 고형 및 액상 경구제제의 첨가제로는 향료, 비타민류, 및 항산화제 중에서 1 종 이상을 선택하여 사용할 수 있다. 상기 성분 이외에도 공지의 첨가제로서 미각을 돋구기 위하여, 매실향, 레몬향, 파인애플향, 허브향 등의 천연향료, 천연과즙, 클로로필린, 플라보노이드 등의 천연색소, 과당, 벌꿀, 당알코올, 설탕과 같은 감미성분, 또는 구연산, 구연산 나트륨과 같은 산미제를 혼합하여 사용할 수도 있다.
상기 통상적인 약제학적 제형은 당해 기술분야에 공지되어 있는 통상적인 방법에 따라 당업자가 적절한 제조할 수 있다.
본 발명에 따른 약학 조성물은 유효성분으로서 성인을 기준으로 1 일 총 투여량이 상기 마이크로웨이브 조사 가공물을 약 0.01 mg/kg 내지 10 g/kg, 바람직하게는 약 1 mg/kg 내지 1 g/kg이 되도록 임의로 수회 나누어서 투여할 수 있다. 상기 투여량은 투여 경로, 질병의 진행 정도, 성별, 나이, 체중 등에 따라, 또는 전문가의 임상적 판단에 따라 적절히 증감될 수 있다. 상기 본 발명에 따른 약학 조성물은 면역력 저하 및 항암제 내성에서 선택된 항암제 부작용 개선, 항산화, 항암, 항염증, 뇌기능 또는 인지기능 개선, 혈관이완, 혈소판 응집억제, 피부염 개선, 또는 건선 개선 효과를 위해 단독으로, 또는 수술, 호르몬 치료, 화학 치료 및 생물학적 반응 조절제를 사용하는 방법들과 병용하여 사용할 수 있다.
다른 양상은 파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 진세노사이드 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상 함유된 파낙스속 식물 추출물을 활성 성분으로 함유하는 건강기능식품용 조성물을 제공한다.
파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 진세노사이드 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상 함유된 파낙스속 식물 추출물에 대하여는 상기한 바와 같다.
상기 본 발명에 따른 건강기능식품용 조성물은 당해 기술분야에 공지되어 있는 통상적인 건강기능식품의 제형으로 제제화될 수 있다.
상기 건강기능식품은 예를 들어 산제, 과립제, 정제, 환제, 캅셀제, 현탁액, 유제, 시럽제, 침제, 액제, 엑스제 등의 일반적인 제형으로 제조될 수도 있고, 육류, 소세지, 빵, 쵸코렛, 캔디류, 스넥류, 과자류, 피자, 라면, 기타 면류, 껌류, 젤리, 아이스크림류를 포함한 낙농제품, 각종 스프, 음료수, 차, 드링크제, 알콜 음료 및 비타민 복합제 등의 임의의 건강식품 형태로 제조될 수도 있다. 상기 건강식품의 제제화를 위해 식품학적으로 허용 가능한 담체 또는 첨가제를 사용할 수 있으며, 제조하고자 하는 제형의 제조에 당해 기술분야에서 사용 가능한 것으로 공지되어 있는 임의의 담체 또는 첨가제가 이용될 수 있다. 상기 첨가제로서 각종 영양제, 비타민, 전해질, 풍미제, 착색제, 펙트산 및 그의 염, 알긴산 및 그의 염, 유기산, 보호성 콜로이드 증점제, pH 조절제, 안정화제, 방부제, 글리세린, 알콜, 탄산 음료에 사용되는 탄산화제 등을 함유할 수 있다. 그 이외에도 천연 과일쥬스, 과일쥬스 음료 및 야채 음료의 제조를 위한 과육을 함유할 수 있다. 이러한 첨가제 성분은 독립적으로 또는 조합하여 사용할 수 있으며, 첨가제의 비율은 크게 중요하진 않지만 본 발명의 조성물 100 중량부당 0.01 ~ 0.1 중량부의 범위에서 선택될 수 있다.
상기 건강기능식품용 조성물 중의 상기 마이크로웨이브 조사 가공물의 함량은 사용 목적(예방 또는 개선)에 따라 적합하게 결정될 수 있다. 일반적으로, 전체 식품 중량의 0.01 내지 15 중량%로 포함할 수 있으며, 음료로서 제조될 경우 100 mL를 기준으로 0.02 내지 10 g, 바람직하게는 0.3 내지 1 g의 비율로 함유할 수 있다.
상기 음료는 상기 활성성분 이외의 다른 성분을 더 포함할 수 있으며, 통상적으로 음료에 사용되는 다양한 향미제 또는 천연 탄수화물 등을 더 함유할 수 있다. 상기 천연 탄수화물로는 단당류(예: 포도당, 과당 등), 이당류(예: 말토즈, 수크로즈 등), 다당류(예: 덱스트린, 시클로덱스트린 등)와 같은 통상적인 당 및 자일리톨, 소르비톨, 에리트리톨 등의 당알콜이 함유될 수 있다. 또한, 향미제로서 천연 향미제(예: 타우마틴, 스테비아 추출물 등) 및 합성 향미제(예: 사카린, 아스파탐 등)를 함유할 수 있다. 상기 천연 탄수화물의 비율은 음료 100 mL당 일반적으로 약 1 내지 20g, 바람직하게는 약 5 내지 12g으로 함유되는 것이 바람직하다.
다른 양상은 상기한 신장 독성을 억제하기 위한 조성물을 개체에 투여하는 단계를 포함하는, 개체의 신장 독성을 억제하는 방법을 제공한다.
상기 개체는 사람을 포함한 포유동물일 수 있다. 상기 투여는 경구, 정맥, 경피, 및 경비 투여하는 것일 수 있다.
상기 방법은 신장 독성을 유발하는 약제를 개체에 투여하는 단계를 더 포함하는 것일 수 있다. 상기 약제는 상기 신장 독성을 억제하기 위한 조성물을 투여하기 전, 동시 또는 후에 투여되는 것일 수 있다. 신장 독성을 유발하는 약제는 상기한 바와 같다.
일 양상에 따른 신장 독성을 억제하기 위한 조성물에 의하면, 진세노사이드에 대한 현저하게 높은 Rg5+Rk1+Rg3의 비율을 갖고 있어서 효율적으로 개체의 신장 독성을 억제하는데 사용될 수 있다.
다른 양상에 따른 건강기능식품용 조성물에 의하면, 효율적으로 개체의 신장 독성을 억제할 수 있다.
다른 양상에 따른 개체의 신장 독성을 억제하는 방법에 의하면, 개체의 신장 독성을 효율적으로 억제할 수 있다.
도 1은 원료 인삼의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
도 2는 정관장 홍삼정플러스TM의 단순 동결건조물 중의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
도 3은 인삼 추출물을 150℃, 100W에서 60분간 마이크로웨이브 가공 처리한 마이크로웨이브 조사 가공물 중의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
도 4는 원료 인삼 추출물, 정관장 홍삼정플러스TM 및 마이크로웨이브 조사 가공물 추출물의 DPPH 라디칼 소거능을 비교한 결과를 도시한 그래프이다.
도 5는 마이크로웨이브 조사 가공물 추출물로부터 분리된 HP-20수지 비흡착 성분, HP-20수지 흡착 성분 및 진세노사이드 성분의 DPPH 라디칼 소거능을 측정한 결과를 도시한 그래프이다.
도 6는 원료 인삼 추출물, 정관장 홍삼정플러스TM, 마이크로웨이브 조사 가공물 추출물 및 마이크로웨이브 조사 가공물 추출물로부터 분리된 HP-20수지 비흡착 성분, HP-20수지 흡착 성분 및 진세노사이드 성분의 환원력을 비교한 결과를 도시한 그래프이다.
도 7은 인삼추출물을 투여한 후, 혈액 중의 크레아티닌 측정 결과를 그래프로 나타낸 것이다. (Vehicle: 정상군, Cisplatin: 시스플라틴 투여군, Cisplatin+실시예1: 시스플라틴+실시예 1 투여군, Cisplatin+비교예1: 시스플라틴+비교예 1 투여군, Cisplatin+실시예2: 시스플라틴+실시예 2 투여군)
도 8은 인삼추출물을 투여한 후, 신장조직의 변화를 비교한 것이다. (Vehicle: 정상군, Cisplatin: 시스플라틴 투여군, Cisplatin+실시예1: 시스플라틴+실시예1 투여군, Cisplatin+비교예1: 시스플라틴+비교예1 투여군, Cisplatin+실시예2: 시스플라틴+실시예 2 투여군)
도 9는 마이크로웨이브 가공인삼 추출물을 투여한 후, 체중과 사료 및 물 섭취량의 변화를 비교한 것이다. (Vehicle: 정상군, 실시예2: 실시예 2 투여군)
도 10 마이크로웨이브 가공인삼 추출물을 투여한 후, 혈액 중의 크레아티닌과 ALT 수치를 측정한 결과를 그래프로 나타낸 것이다. (Vehicle: 정상군, 실시예2: 실시예 2 투여군)
도 2는 정관장 홍삼정플러스TM의 단순 동결건조물 중의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
도 3은 인삼 추출물을 150℃, 100W에서 60분간 마이크로웨이브 가공 처리한 마이크로웨이브 조사 가공물 중의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
도 4는 원료 인삼 추출물, 정관장 홍삼정플러스TM 및 마이크로웨이브 조사 가공물 추출물의 DPPH 라디칼 소거능을 비교한 결과를 도시한 그래프이다.
도 5는 마이크로웨이브 조사 가공물 추출물로부터 분리된 HP-20수지 비흡착 성분, HP-20수지 흡착 성분 및 진세노사이드 성분의 DPPH 라디칼 소거능을 측정한 결과를 도시한 그래프이다.
도 6는 원료 인삼 추출물, 정관장 홍삼정플러스TM, 마이크로웨이브 조사 가공물 추출물 및 마이크로웨이브 조사 가공물 추출물로부터 분리된 HP-20수지 비흡착 성분, HP-20수지 흡착 성분 및 진세노사이드 성분의 환원력을 비교한 결과를 도시한 그래프이다.
도 7은 인삼추출물을 투여한 후, 혈액 중의 크레아티닌 측정 결과를 그래프로 나타낸 것이다. (Vehicle: 정상군, Cisplatin: 시스플라틴 투여군, Cisplatin+실시예1: 시스플라틴+실시예 1 투여군, Cisplatin+비교예1: 시스플라틴+비교예 1 투여군, Cisplatin+실시예2: 시스플라틴+실시예 2 투여군)
도 8은 인삼추출물을 투여한 후, 신장조직의 변화를 비교한 것이다. (Vehicle: 정상군, Cisplatin: 시스플라틴 투여군, Cisplatin+실시예1: 시스플라틴+실시예1 투여군, Cisplatin+비교예1: 시스플라틴+비교예1 투여군, Cisplatin+실시예2: 시스플라틴+실시예 2 투여군)
도 9는 마이크로웨이브 가공인삼 추출물을 투여한 후, 체중과 사료 및 물 섭취량의 변화를 비교한 것이다. (Vehicle: 정상군, 실시예2: 실시예 2 투여군)
도 10 마이크로웨이브 가공인삼 추출물을 투여한 후, 혈액 중의 크레아티닌과 ALT 수치를 측정한 결과를 그래프로 나타낸 것이다. (Vehicle: 정상군, 실시예2: 실시예 2 투여군)
이하, 본 발명을 하기 실시예에 의해 더욱 구체적으로 설명한다. 그러나, 이들 실시예는 본 발명에 대한 이해를 돕기 위한 것일 뿐, 어떤 의미로든 본 발명의 범위가 이들에 의해 제한되는 것은 아니다.
실시예
1: 인삼 추출물의 제조
인삼 (Panax ginseng) 뿌리는 금산 인삼시장 한약재상에서 구입하여 사용하였다. 세절된 분말 인삼 뿌리 200 g에 50% 에탄올 1.5 L를 넣고 70℃에서 3시간 환류 추출하여 50% 에탄올 추출물을 수득하고, 수득한 50% 에탄올 추출물을 감압 하에서 용매를 증발 건조하여 진세노사이드 Rb1, Rb2, Rc, Rd, Rg1, 및 Re를 포함하는 건조 추출물 27 g을 수득하였다.
실시예
2: 마이크로웨이브를 이용한 가공 인삼 추출물의 제조
실시예 1에서 얻어진 50% 에탄올 추출물을 열처리 가공하였다. 구체적으로는, 인삼 건조 추출물 200 mg을 미국 CEM사에서 제조된 마이크로웨이브 조사기 (모델번호 908005)의 10 mL 용기 중의 물 1 mL 중에 첨가하고 용기를 밀봉한 상태에서 약 150℃로 100W (주파수 2455 MHz)에서 60분 동안 마이크로웨이브 조사시킨 후, 동결건조하여 마이크로웨이브 조사된 가공물을 수득하였다. 마이크로웨이브 조사시 압력은 20 기압이었다.
실시예
3-6: 마이크로웨이브 조사된 인삼 가공물의 유효성분 함유 분획 제조
실시예 2에서 얻어진 마이크로웨이브 조사된 인삼 가공물 3g에 5배 용적의 물을 가하여 충분히 희석시킨 후, 물로 평형화된 비극성 흡착 수지인 DIAIONTM HP 20 수지 (Samchun Chemicals)가 충진된 칼럼을 통과시켜 사포닌 성분을 흡착시켰다. DIAIONTM HP 20 수지는 폴리스티렌 수지로서, 입자의 표면이 소수성 (hydrophobic)을 띠고 있어서 유기물이 흡착될 때 유기 분자 중의 소수성기가 흡착된다. 폴리스티렌 수지는 상대적으로 큰 표면적 (전형적으로 450-900 m2g), 높은 다공성 (porosity) (포어 부피, 전형적으로 0.6-1.8ml/G) 및 큰 평균 포어 크기 (전형적으로 100-800A)을 갖고 있어, 거친 입자 크기 (전형적으로 20-60 메쉬, wet)와 조합되어 높은 추출물 흐름 속도 (extract flow rate)와 표적 화합물의 보류 (retention)를 위한 큰 능력 (capacity)를 제공한다. 따라서, 소수성기의 소수성이 큰 유기 화합물, 예를 들면, 진세노사이드, 지용성 비타민, 항생물질, 효소 및 페놀성 화합물 등이 잘 흡착될 수 있다.
다음으로, 상기 수지 용적의 약 5배의 증류수를 상기 칼럼을 통하여 흘려주어 얻어진 수용성 성분을 모아 동결건조하여 HP-20 수지 비흡착 수용성 성분 2.7g을 수득하였다 (실시예 3). 수용성 성분이 제거되고 HP-20 수지 흡착 성분, 예를 들면, 소수성 사포닌계 성분과 항산화 성분이 흡착되어 있는 수지에 상기 수지의 5 내지 10 배 부피의 50 내지 100 v/v% 에탄올을 상기 칼럼에 통과시켜 용출시키고, 건조하여 유효 성분 함유 분획 0.3g을 얻었다 (실시예 4).
위 실시예 4의 유효성분 함유 분획을 헥산 : 에틸아세테이트(10:1) 3 ml에 녹인 후, 헥산: 에틸아세테이트=10: 1로 평형화된 실리카겔 컬럼 (Merck, TA1524185)에 흘려준 후, 헥산 : 에틸아세테이트(10:1-> 5:1-> 1:1) 용매 조건하에서 용출하여, 진세노사이드 Rg3, Rg5 및 Rk1 함유 분획만을 분취하고 수집, 농축하였다.
진세노사이드 Rg3의 함량이 50% 이상인 분획물을 반분취 (semi-preparative) HPLC (Phenomenex, Luna 10μ C18(2) 100A, 250x20mm)를 이용하여, Gilson HPLC system과 UV/VIS-151 detector를 사용하고, 이동상 (water : CH3CN)을 40 : 60로부터 시작하여 40분 후 0 : 100이 되도록 용출하여 10 mg의 순수한 진세노사이드 Rg3를 수득하였다 (실시예 5).
다음으로 진세노사이드 Rg5 및 Rk1의 함량이 50% 이상인 분획물을 반분취 HPLC (Phenomenex, Luna 10μ C18(2) 100A, 250x20mm)를 이용하여, Gilson HPLC system과 UV/VIS-151 detector를 사용하고, 이동상 (water : CH3CN)을 40 : 60로부터 시작하여 40분 후 0 : 100이 되도록 용출하여 20 mg의 순수한 진세노사이드 Rg5 및 Rk1 혼합물을 수득하였다 (실시예 6).
비교예
1: 정관장
홍삼정플러스
TM
동결 건조물의 제조
실시예 2에 의해 제조된 마이크로웨이브 조사 생성물과 기존의 열처리 가공 인삼과의 성분차이를 비교하기 위해 다음과 같이 정관장 홍삼정플러스TM 동결 건조물과 단순 열처리 가공 인삼추출물을 제조하였다. 시중에서 판매 중인 정관장 홍삼정 플러스TM 홍삼농축액을 동결건조하여 정관장 홍삼 추출물의 동결 건조물 (비교예 1)을 수득하였다.
실험예
1: 인삼 추출물 및 분획의
진세노사이드
분석
(1) 실험 방법
진세노사이드 20(S)-Rg3, 20(R)-Rg3, Rg5, 및 Rk1 표준액을 대조군으로 하여 문헌의 방법 (Kwon et al., J. Chromatogr . A, 921(2), pp335-339, 2001)에 기재된 바에 따라 HPLC로, 실시예 1-6 및 비교예 1에서 얻어진 가공 인삼 추출물 각각의 사포닌 성분을 분석하였다. 사포닌 분석은 3회 반복하여 재현성을 확인하였다.
용출 용매인 A는 15:80:5 비율(v/v/v)의 아세토니트릴: 물: 아세트산이고 용출용매 B는 80:20 비율(v/v)의 아세토니트릴:물이며, 용출용매 A와 B는 0.45㎛ 막 필터 (membrane filter)를 통해 필터링한 후 2개의 펌프를 이용하여 각각 펌핑하여 사용하였다. 상기 표준용액 10 ㎕를 시린지를 이용하여 분리 컬럼인 역상 컬럼 (C18, 4.6 X 150 mm)에 주입시키고, 100 부피%의 A, 0부피%의 B의 조성을 갖는 용출용매를 1㎖/분의 유속으로 흘렸다. 그 후, 용출용매 A의 부피%를 70% (6분), 50% (18분), 0% (30분)로 점차적으로 변화시켰고 상기 조성을 7분 동안 유지시켰다. 상기 과정 후 컬럼에서 분리된 각 성분을 증기화광산란 검출기 (ELSD)를 통하여 분석하였다.
(2) 실험 결과
실험 결과, 인삼 추출물에 대해 HPLC 분석에 의해 컬럼에서 분리된 각 성분을 증기화광산란 검출기(ELSD)를 통하여 분석한 결과 도 1 내지 3의 피크를 얻었다.
도 1은 원료 인삼의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
도 2는 정관장 홍삼정플러스TM의 단순 동결건조물 중의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
도 3은 인삼 추출물을 150℃, 100W에서 60분간 마이크로웨이브 가공 처리한 마이크로웨이브 조사 가공물 중의 진세노사이드 성분을 분석한 HPLC 크로마토그램이다.
또한, 얻어진 HPLC 크로마토그램에서 얻어진 각각의 진세노사이드 함량을 계산한 결과를 표 2 및 표 3에 정리하였다.
| 구분 | Re+Rg1 | Rb1 | Rc | Rb2 | Rd | 20(S)Rg3 | 20(R)Rg3 | Rk1 | Rg5 | (RG5+RK1)/Rg3 |
| 실시예1 | 114.4±10.5 | 158±15.0 | 93.9±10.1 | 74.2±6.8 | 8.1±1.2 | - | - | - | - | - |
| 비교예1 | 6.5±0.8 | 12.4±1.5 | 1.9 ±0.7 |
4.5±0.8 | 1.6±0.6 | 2.5±0.8 | 1.3± 0.6 |
1.3± 0.9 |
2.2± 0.9 |
0.9 |
| 실시예2 | - | - | - | 8.6±1.4 | - | 60.6±11.7 | 44.0±4.3 | 150.5±12.8 | 275.1±1.8 | 4.1 |
| 실시예4 | - | - | - | - | - | 106.8±20.6 | 116.3±7.5 | 227.6±6.2 | 358.2±6.1 | 2.6 |
| 구분 | Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대한 Rg3, Rk1 및 Rg5 함량(%) | Re,Rg1,Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대한 Rg3, Rk1 및 Rg5 함량(%) |
| 실시예1 | 0 | 0 |
| 비교예1 | 26.35 | 21.35 |
| 실시예2 | 98.40 | 98.40 |
| 실시예4 | 100 | 100 |
표 2에서 각 숫자는 mg 추출물 당 μg을 나타낸다. 표 2에서, 주요 진세노사이드인 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5 또는 Re,Rg1,Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대한 Rg3 (20(S)+20(R)), Rg5 및 Rk1의 함량을 계산하여 보면, 표 3과 같다.
도 1-2, 표 2 및 3에 나타난 바와 같이, 인삼에 함유되어 있는 주요 진세노사이드인 Rb1, Rb2, Rc, Rd, Rg1, 및 Re는 홍삼 가공에 의해 20번 위치의 배당체인 글루코스가 이탈되고, 이어서 20번 위치에서 탈수반응이 일어나 Rg3, Rg5 및 Rk1로 변환되었음을 알 수 있었다 (도 2와 3의 비교). 또한, 완전히 배당체가 이탈되지 않고 남아있는 백삼의 진세노사이드가 8분에서 14분 사이에서 검출되었다.
표 2의 실시예 2에 나타난 바와 같이, 150℃ 및 20기압에서 마이크로웨이브 조사한 경우, 진세노사이드 Rg3, Rk1, 및 Rg5의 함량은 90% 이상으로 예기치 않게 현저하게 증가하였으며, (Rg5 + Rk1)/(Rg3)의 비율도 3.0 이상으로서 예기치 않게 증가하였다. Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5 또는 Re,Rg1,Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대한 Rg3, Rk1, 및 Rg5의 함량은 단순 열처리 가공 백삼보다 200% 이상 현저히 증가한 값이다.
상기 결과에 따르면, 인삼의 추출물 또는 인삼 자체를 마이크로웨이브 조사 시, 인삼의 주요 진세노사이드인 Rb1, Rb2, Rc, Rd, 및 Re을 약효가 우수한 진세노사이드인 Rg3, Rg5, 및 Rk1로 더욱 효율적으로 변환시킬 수 있었다. 예를 들면, 진세노사이드 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5 또는 Rg1, Re, Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상 함유된 마이크로웨이브 조사 가공물이 얻어졌다. 특히 진세노사이드 (Rg5 + Rk1)/(Rg3)의 비율이 지금까지 개발된 단순 열처리 가공법에 비해 현저히 높다는 것을 알 수 있다.
실험예
2: 인삼 추출물,
분획물
및 성분의
항산화능
평가
(1) 실험 방법
각 인삼 추출물, 분획물, 및 성분에 대해 DPPH (2-2-diphenyl-1-picrylhydrazyl) 라디컬 소거활성을 측정하였다. DPPH 라디칼 소거효과 시험에서 DPPH는 안정한 자유 라디칼로서 그것의 비공유전자로 인해 517nm 부근에서 최대 흡수치를 나타내며, 전자 또는 수소를 받으면 517nm부근에서 흡광도가 감소하게 되므로, 이러한 흡광도 감소율을 측정함으로서 항산화 활성 및 활성 산소를 비롯한 다른 라디칼에 대한 소거 활성을 평가할 수 있다 (Hatano et al., Chem. Pharm. Bull., 38(5), pp1224-1229, 1990).
10, 50, 100, 및 250 ug/mL의 농도로 조제된 각 인삼 추출물, 분획물, 및 성분 100uL에 60uM의 DPPH(2-2-diphenyl-1-picrylhydrazyl) 100 uL를 넣고 교반한 후 30분간 방치한 다음 540nm에서 흡광도를 측정하였다. 항산화활성 즉 전자공여능은 아무것도 처리하지 않은 대조군과 비교한 인삼 추출물에 의한 흡광도 감소율을 측정하여 확인하였다.
(2) 실험 결과
각 인삼 추출물, 분획물, 및 성분에 대해 DPPH 라디칼 소거활성을 측정하였다. 그 결과를 도 4-5에 나타내었다.
도 4는 원료 인삼 추출물, 정관장 홍삼정플러스TM 및 마이크로웨이브 조사 가공물 추출물의 DPPH 라디칼 소거능을 비교한 결과를 도시한 그래프이다.
도 5는 마이크로웨이브 조사 가공물 추출물로부터 분리된 HP-20 수지 비흡착 성분, HP-20 수지 흡착 성분 및 진세노사이드 성분의 DPPH 라디칼 소거능을 측정한 결과를 도시한 그래프이다.
도 4에 따르면, 원료 인삼의 활성산소 소거능력이 미약하였으나 홍삼정플러스TM 추출물은 원료 인삼에 비해 농도 의존적으로 DPPH 라디칼 소거능이 다소 향상되었다 (IC50=218 ug/mL). 이에 반해, 마이크로웨이브가공 인삼 추출물은 농도 의존적으로 탁월한 DPPH 라디칼 소거능을 나타냈으며, IC50 수치는 90 ug/mL로 정관장홍삼 보다 2배 이상 향상되었다. 다음으로, 도 5에 따르면, HP-20수지 흡착 성분은 HP-20수지 비흡착 성분 및 진세노사이드 성분과 비교하여 농도 의존적으로 탁월한 DPPH 라디칼 소거능을 나타내어 HP-20수지에 흡착되는 성분 중에 진세노사이드 보다 강한 항산화 효과를 나타내는 물질이 함유되어 있음이 확인되었다.
따라서, 본 발명에 따른 조성물은 탁월한 전자공여능을 갖는 것으로 확인되었다.
실험예
3: 인삼 추출물, 분획 및 성분의 환원력 비교
물질의 환원력은 산화를 환원시키는 의미로 항산화 효과와 유사한 의미로 사용된다.
(1) 실험 방법
인삼 추출물, 분획 및 성분의 환원력은 Folin-Denis 방법에 따라 Folin-Ciocalteu 시약(Sigma-Aldrich)을 사용하여 측정되었다(Zhang et al., J. Appl. Phycol,, 18, pp445-450, 2006). 건조된 샘플 시료를 물에 녹여 1mg/mL 농도로 만든 후에, 이를 20 ul를 취하고, 여기에 Folin-Ciocalteu 시약 20 ul, 증류수 60 ul를 가하였다. 상온에 5분간 방치한 다음 20% Na2CO3 100 ul를 가하고 다시 상온에서 30 분간 방치한 후, Spectrophotometer (BioTek Instruments, USA)를 이용하여 734 nm에서 반응액의 흡광도 값을 측정하였다. 표준물질로 gallic acid (Sigma-Aldrich)를 사용하였고, gallic acid 검량선을 이용하여 환원력을 mg GAE (gallic acid equivalent)/g 추출물로 표현하였다.
(2) 실험 결과
각 인삼 추출물, 분획 및 성분에 대해 환원력을 비교하였다. 그 결과를 도 6에 나타내었다.
도 6은 원료 인삼 추출물, 정관장 홍삼정플러스TM, 마이크로웨이브 조사 가공물 추출물 및 마이크로웨이브 조사 가공물 추출물로부터 분리된 HP-20수지 비흡착 성분, HP-20수지 흡착 성분 및 진세노사이드 성분의 환원력을 비교한 결과를 도시한 그래프이다.
도 6에 따르면, 원료 인삼 추출물과 비교하여 정관장 홍삼정플러스TM는 현저하게 강한 환원력을 보였으나, 마이크로웨이브 조사 가공물 추출물은 홍삼정플러스TM 보다 약 2배 더 강한 환원력을 보였다. 다음으로 마이크로웨이브 조사 가공물 추출물 중 HP-20수지 흡착 성분은 HP-20수지 비흡착 성분 및 진세노사이드 성분과 비교하여 탁월한 환원력을 나타냄이 확인되었다.
따라서, 본 발명에 따른 조성물은 탁월한 환원력을 갖는 것으로 확인되었다.
실험예
4: 인삼 추출물, 분획 및 성분의
In
vitro
신장 독성 보호 효과 평가
(1) 실험 방법
문헌에 보고된 방법 (Yokozawa et al., J. Pharm. Pharmacol,, 51, pp1325-1331, 1999)을 참조하여 신장세포 LLC-PK1 (ATCC CL-101TM)를 사용하여 신장 독성에 대한 보호 효과를 다음과 같이 평가하였다.
먼저, LLC-PK1 세포를 10% 소태아 혈청 (fetal bovine serum;Gibco BRL Life Technologies), 페니실린 G 100 유닛/ml (Gibco BRL Life Technologies) 및 스트렙토마이신 (streptomycin; Gibco BRL Life Technologies) 100 ug/ml를 가한 DMEM (Cellgro, Manassas, VA,USA) 배지를 사용하여 37℃로 유지된 95% 공기/5% 이산화탄소 배양기에서 배양하였다. 배양된 LLC-PK1 세포를 96-웰 배양 플레이트의 100ul를 포함한 각 웰에 104 개씩 도입하고 22 시간 동안 세포가 안정되도록 하였다. 그 후, 인삼 추출물, 분획 및 성분을 지정된 농도가 되도록 첨가하고, 2시간 뒤 라디칼 발생 시약인 배지에 녹인 250uM 시스플라틴 (cisplatin)을 0.1ml씩 첨가하여 24 시간 배양한 후 10 ㎕의 CCK-8 (CCK-8, Dojindo Laboratories, Japan) 시약을 각 웰에 첨가 후, 37℃에서 배양하였다. 1 시간 후 BIO-TEK (Winooski, VT, USA) 마이크로플레이트 리더 (microplate reader)에서 450 nm 검출 파장을 이용하여 흡광도를 측정하여 세포의 생존율을 측정하였다.
(2) 실험 결과
하기 표 4는 시스플라틴 처리한 신장 상피세포인 LLC-PK1 세포에 대한 각 인삼 샘플의 효과를 나타낸다. LLC-PK1 세포수는 250 uM 시스플라틴 처리로 시스플라틴 비처리군의 50% 이하로 감소하였다. 각 인삼 샘플들은 이런 세포 손상을 억제하는 것으로 나타났다. 원료 인삼과 홍삼정플러스TM은 250 uM 시스플라틴 처리로 감소된 세포 생존율을 농도 의존적으로 유의적으로 증가시켰으며, 마이크로웨이브 가공인삼 추출물은 250 ug/mL의 농도에서 원료 인삼과 홍삼보다 효과적으로 78.5%까지 유의적으로 세포의 생존율을 증가시켰다. 특히,
마이크로웨이브 조사 가공물 추출물 중 HP-20수지 흡착 성분은 250 ug/mL의 농도에서 세포의 생존율을 82.6%까지 증가시켜 가장 우수한 효과를 보였으며, HP-20수지 비흡착 성분과 비교하여 탁월한 신장세포보호 효과를 나타내었다. 다음으로 HP-20수지 흡착 성분으로부터 분리된 진세노사이드 Rg3와 Rg5 및 Rk1 또한 250 ug/mL의 농도에서 세포의 생존율을 각각 78.9 와 76.7%까지 회복시켰다. 따라서 본 발명에 따른 조성물은 탁월한 신장보호 효능을 갖는 것으로 확인되었으며 이러한 효과는 HP-20수지에 흡착되는 진세노사이드와 비진세노사이드 성분에 의한 것으로 여겨진다.
| 구분 | 농도 (μg/mL) | 세포생존율 (%) |
| 실시예1 | 0 | 50.1±2.8 |
| 50 | 50.5±3.3 | |
| 100 | 59.7±4.8 | |
| 250 | 61.2±1.8a | |
| 500 | 64.6±3.3a | |
| 비교예2 | 0 | 50.1±2.8 |
| 50 | 52.0±5.1 | |
| 100 | 49.9±3.0 | |
| 250 | 56.9±4.2 | |
| 500 | 61.1±5.2a | |
| 실시예2 | 0 | 39.5±1.2 |
| 50 | 48.6±7.6 | |
| 100 | 52.7±6.3a | |
| 250 | 71.1±6.8a | |
| 500 | 78.5±7.0a | |
| 실시예3 | 0 | 35.5±1.3 |
| 50 | 43.1±1.2a | |
| 100 | 43.9±2.1a | |
| 250 | 49.8±2.0a | |
| 실시예4 | 0 | 35.5±1.3 |
| 50 | 60.9±0.5a | |
| 100 | 81.2±1.2a | |
| 250 | 82.6±6.7a | |
| 실시예5 | 0 | 40.1±2.7 |
| 50 | 57.1±2.2a | |
| 100 | 69.0±1.1a | |
| 250 | 78.2±2.8a | |
| 실시예6 | 0 | 40.1±2.7 |
| 50 | 46.9±1.1a | |
| 100 | 57.6±2.2a | |
| 250 | 76.7±1.7a |
* a는 통계적 유의성을 나타내는 것으로서, p<0.001 vs 시스플라틴 처리 표준 수치이다.
이상의 결과로부터, 마이크로웨이브 가공인삼 추출물은 시스플라틴에 대한 신장세포 손상을 효과적으로 보호함을 알 수 있었으며. 이런 결과들은 마이크로웨이브 가공인삼 추출물의 진세노사이드 성분과 비진세노사이드 항산화 성분들이 산화적 스트레스로부터 야기되는 신장세포 손상을 보호해줄 수 있다는 것을 의미한다.
실험예
5: 인삼 추출물의 인 비보 신장 독성 보호 효과 평가
(1) 실험 방법
문헌에 보고된 방법 (Ahn et al., Korean J. Anesthesiol., 52, pp318-327, 2007)을 참조하여 C57BL/6 숫쥐를 사용하여 시스플라틴의 신장 독성에 대한 보호 효과를 다음과 같이 평가하였다.
실험동물은 체중 25 g 내외의 C57BL/6 숫쥐를 사용하였다. 시스플라틴 신장 독성을 유발하기 위하여 복강 내로 시스플라틴 16 mg/kg를 1회 주사하였다. 시스플라틴 주사 7 일 전부터 그리고 3 일후까지 총 10 일간 각 인삼추출물을 200 mg/kg 체중의 농도로 경구 투여하였다.
10 일간의 각 인삼추출물 투여가 끝난 후, 신장기능을 측정하기 위해 마취 하에 개복 후 혈액을 채취하여 혈청 크레아티닌을 측정하였다. 혈중 크레아티닌 농도는 크레아티닌 (creatinine) 시약 (Roche, USA)으로 Hitachi modular(Japan) 기기를 사용하여 Rate blank Jaffe Kinetic 방법으로 측정하였고, 신장의 조직학적 회복이 이루어지는지 확인하기 위해 문헌의 방법을 참조로 PAS 염색을 실시하였다 (Ahn et al., Korean J. Anesthesiol., 52, pp318-327, 2007).
(2) 실험 결과
인삼 추출물을 샘플로서 사용하여 실험한 결과를 도 7에 나타내었다.
도 7은 인삼추출물을 투여한 후, 혈액 중의 크레아티닌 측정 결과를 그래프로 나타낸 것이다. (Vehicle: 정상군, Cisplatin: 시스플라틴 투여군, Cisplatin+실시예1: 시스플라틴+실시예 1 투여군, Cisplatin+비교예1: 시스플라틴+비교예 1 투여군, Cisplatin+실시예2: 시스플라틴+실시예 2 투여군)
도 8은 인삼추출물을 투여한 후, 신장조직의 변화를 비교한 것이다. (Vehicle: 정상군, Cisplatin: 시스플라틴 투여군, Cisplatin+실시예1: 시스플라틴+실시예1 투여군, Cisplatin+비교예1: 시스플라틴+비교예1 투여군, Cisplatin+실시예2: 시스플라틴+실시예 2 투여군)
도 7에 따르면, 시스플라틴 투여에 의해 크레아티닌 혈액농도는 정상군의 1.7배로 증가하였으나 원료 인삼과 홍삼정플러스TM 투여에 의한 효과는 미미하였다. 그러나 시스플라틴을 마이크로웨이브 가공 인삼 추출물과 함께 투여한 군의 크레아티닌 혈액농도는 시스플라틴 투여군에 비하여 약 30% 감소하여 정상군의 농도를 나타내는 것을 확인하였다.
도 8에 따르면, 정상군에서는 조직학적 이상소견이 관찰되지 않았으나 시스플라틴 투여에 의해 신장조직 뇨세관 괴사에 의한 세포손상 부위가 증가하였다. 시스플라틴과 원료 인삼 또는 홍삼정플러스TM 투여에 의한 보호효과는 미미하였으나, 시스플라틴을 마이크로웨이브 가공 인삼 추출물과 함께 투여한 군에서는 이러한 세포손상 부위가 정상군의 수준으로 감소되는 것을 확인하였다.
상기 결과에 따르면, 마이크로웨이브 가공 인삼 추출물은 시스플라틴에 의해 유도된 신장기능의 감소를 효과적으로 개선함을 알 수 있었으며, 이런 결과들은 마이크로웨이브 가공 인삼 추출물이 신장손상을 보호해줄 수 있다는 것을 의미한다.
실험예 5: 마이크로웨이브 가공 인삼 추출물의 급성경구독성에 대한 안전성 평가
(1) 실험 방법
연령이 5 내지 6 주령 된 시험용 마우스 (BALB/c, 수컷)를 사용하였으며 개체 간 체중 차이는 평균체중의 ±20%를 넘지 않도록 하였다. 시험에 사용할 개체는 시험 시작 전 최소 5일 이상 실험실에서 순화시킨 건강한 동물 중에서 무작위로 선정하였다. 사육실은 온도가 22℃, 습도가 30 내지 70%가 유지되도록 하였다. 조명은 명/암이 12/12시간이 되도록 조절하며, 시료와 물을 적절히 공급하였다. 시험물질인 마이크로웨이브 가공인삼 추출물은 물에 용해시켜 사용하였다. 마이크로웨이브 가공인삼 추출물을 2000 mg/kg의 농도로 1회 투여 후, 15일간 체중, 사료/물 섭취량을 측정하였다. 실험 종료일에 마취 하에 부검하여 신장과 간장의 무게를 측정하고, 신장과 간장기능의 평가를 위해 혈청 ALT와 크레아티닌 농도를 측정하였다.
(2) 실험 결과
도 9는 마이크로웨이브 가공인삼 추출물을 투여한 후, 체중과 사료 및 물 섭취량의 변화를 비교한 것이다. (Vehicle: 정상군, 실시예2: 실시예 2 투여군)
도 10 마이크로웨이브 가공인삼 추출물을 투여한 후, 혈액 중의 크레아티닌과 ALT 수치를 측정한 결과를 그래프로 나타낸 것이다. (Vehicle: 정상군, 실시예2: 실시예 2 투여군)
마이크로웨이브 가공인삼 추출물 2000 mg/kg를 경구 투여 한 후 15일간 사망하거나 이상행동을 보인 개체는 없었으며, 도 9의 결과와 같이 정상군과 동일한 체중증가와 사료 및 물 섭취량을 보였다. 다음으로 도 10의 결과와 같이 마이크로웨이브 가공인삼 추출물의 경구투여 15일 후 부검한 실험동물의 신장과 간장의 무게는 대조군과 변화가 없었다. 또한 도 10의 결과와 같이 신장과 간장의 기능을 나타내는 지표인 혈액 중의 크레아티닌과 ALT 수치는 마이크로웨이브 가공인삼 추출물 투여군에서 대조군과 변화 없는 수치를 나타냈다. 이상의 결과와 같이 실험동물을 이용한 급성경구독성 실험에서, 마이크로웨이브 가공인삼 추출물 2000 mg/kg은 독성을 나타내지 않았다.
제제예
1: 약학적 제제의 제조
1. 산제의 제조
활성성분
2 g
유당 1 g
상기의 성분을 혼합하고 기밀포에 충진하여 산제를 제조하였다.
2. 정제의 제조
활성성분 100 ㎎
옥수수전분 100 ㎎
유 당 100 ㎎
스테아린산 마그네슘 2 ㎎
상기의 성분을 혼합한 후, 통상의 정제의 제조방법에 따라서 타정하여 정제를 제조하였다.
3. 캡슐제의 제조
활성성분
100 ㎎
옥수수전분 100 ㎎
유 당 100 ㎎
스테아린산 마그네슘 2 ㎎
상기의 성분을 혼합한 후, 통상의 캡슐제의 제조방법에 따라서 젤라틴 캡슐에 충전하여 캡슐제를 제조하였다.
4. 환의 제조
활성성분
1 g
유당 1.5 g
글리세린 1 g
자일리톨 0.5 g
상기의 성분을 혼합한 후, 통상의 방법에 따라 1 환 당 4 g이 되도록 제조하였다.
5. 과립의 제조
활성성분
150 ㎎
대두 추출물 50 ㎎
포도당 200 ㎎
전분 600 ㎎
상기의 성분을 혼합한 후, 30% 에탄올 100 ㎎을 첨가하고 60℃에서 건조하여 과립을 형성한 후 포에 충진하였다.
제제예
2: 건강식품의 제조
1. 토마토 케찹 및 소스의 제조
활성성분 0.2~1.0 중량부를 토마토 케찹 또는 소스에 첨가하여 건강 증진용 토마토 케찹 또는 소스를 제조하였다.
2. 밀가루 식품의 제조
활성성분 0.5~5.0 중량부를 밀가루에 첨가하고, 이 혼합물을 이용하여 빵, 케이크, 쿠키, 크래커 및 면류를 제조하여 건강 증진용 식품을 제조하였다.
3. 스프 및 육즙(gravies)의 제조
활성성분 0.1~5.0 중량부를 스프 및 육즙에 첨가하여 건강 증진용 육가공 제품, 면류의 수프 및 육즙을 제조하였다.
4. 그라운드 비프(ground beef)의 제조
활성성분 10 중량부를 그라운드 비프에 첨가하여 건강 증진용 그라운드 비프를 제조하였다.
5. 유제품(dairy products)의 제조
활성성분 5~10 중량부를 우유에 첨가하고, 상기 우유를 이용하여 버터 및 아이스크림과 같은 다양한 유제품을 제조하였다.
6. 선식의 제조
현미, 보리, 찹쌀, 율무를 공지의 방법으로 알파화시켜 건조시킨 것을 배전한 후 분쇄기로 입도 60 메쉬의 분말로 제조하였다. 검정콩, 검정깨, 들깨도 공지의 방법으로 쪄서 건조시킨 것을 배전한 후 분쇄기로 입도 60 메쉬의 분말로 제조하였다. 활성성분을 진공 농축기에서 감압농축하고, 분무, 열풍건조기로 건조하여 얻은 건조물을 분쇄기로 입도 60 메쉬로 분쇄하여 건조분말을 얻었다.
상기에서 제조한 곡물류, 종실류 및 실시예<1-2>의 추출물의 건조분말을 다음의 비율로 배합하여 제조하였다.
곡물류(현미 30 중량부, 율무 15 중량부, 보리 20 중량부),
종실류(들깨 7 중량부, 검정콩 8 중량부, 검정깨 7 중량부),
실시예<1-2>의 추출물에서 분리한 화합물의 건조분말(3 중량부),
영지(0.5 중량부),
지황(0.5 중량부)
제제예
3 :
건강음료의
제조
1. 건강 드링크의 제조
활성성분
1000 ㎎
구연산 1000 ㎎
올리고당 100 g
매실농축액 2 g
타우린 1 g
정제수를 가하여 전체 900 ㎖
통상의 건강음료 제조방법에 따라 상기의 성분을 혼합한 다음, 약 1시간 동안 85?에서 교반 가열한 후, 만들어진 용액을 여과하여 멸균된 2 l용기에 취득하여 밀봉 멸균한 뒤 냉장 보관한 다음 본 발명의 건강음료 조성물 제조에 사용한다.
상기 조성비는 비교적 기호 음료에 적합한 성분을 바람직한 실시예로 혼합 조성하였지만, 수요계층, 수요국가, 사용 용도 등 지역적, 민족적 기호도에 따라서 그 배합비를 임의로 변형 실시하여도 무방하다.
2. 야채쥬스의 제조
활성성분 5 g을 토마토 또는 당근 쥬스 1,000 ㎖에 가하여 건강 증진용 야채쥬스를 제조하였다.
3. 과일쥬스의 제조
활성성분 1 g을 사과 또는 포도 쥬스 1,000㎖ 에 가하여 건강 증진용 과일쥬스를 제조하였다.
이상으로 본 발명 내용의 특정한 부분을 상세히 기술하였는바, 당업계의 통상의 지식을 가진 자에게 있어서, 이러한 구체적 기술은 단지 바람직한 실시양태일 뿐이며, 이에 의해 본 발명의 범위가 제한되는 것이 아닌 점은 명백할 것이다. 따라서 본 발명의 실질적인 범위는 첨부된 청구항들과 그것들의 등가물에 의하여 정의된다고 할 것이다.
Claims (17)
- 파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 진세노사이드 Rg3, Rk1 및 Rg5 및 비진세노사이드 성분이 함유된 파낙스속 식물 추출물을 활성 성분으로 함유하는 신장 독성을 억제하기 위한 조성물.
- 청구항 1에 있어서, 상기 추출물은 폴리스티렌 수지에 흡착성 물질인 것인 조성물.
- 청구항 1에 있어서, 상기 추출물은 비진세노사이드 성분이 원료 인삼에 대하여 2배이상 함유된 것인 조성물.
- 청구항 1에 있어서, 상기 추출물은 Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상 함유되어 있는 것인 조성물.
- 청구항 1에 있어서, 상기 추출물은 파낙스속 식물을 마이크로웨이브 조사한 후 용매를 사용하여 추출된 것인 조성물.
- 청구항 1에 있어서, 상기 추출물은 진세노사이드 (Rg5 + Rk1)/(Rg3)의 비율이 2 이상인 조성물.
- 청구항 1에 있어서, 상기 추출물은 진세노사이드 Re, Rg1, Rb1, Rc, Rb2, Rd, Rg3, Rk1 및 Rg5의 중량에 대하여 Rg3, Rk1 및 Rg5가 90%이상 함유된 것인 조성물.
- 청구항 1에 있어서, 상기 마이크로웨이브 조사는 가압하에서 150℃ 내지 190℃에서 30분 내지 90 분 동안 수행하는 것인 조성물.
- 청구항 1에 있어서, 상기 마이크로웨이브 조사는 2 기압 내지 100 기압하에서 수행하는 것인 조성물.
- 청구항 1에 있어서, 상기 파낙스속 식물은 고려인삼(Panax ginseng), 화기삼(Panax quinquefolia), 전칠삼(Panax notoginseng), 죽절삼(Panax japonica), 삼엽삼(Panax trifolia), 히말라야삼(Panax pseudoginseng), 베트남삼(Panax vietnamensis), 이들의 배양근, 이들의 열처리 또는 효소처리 가공물, 또는 이들의 조합인 것인 조성물.
- 청구항 1에 있어서, 상기 마이크로웨이브 조사는 가압하에서 150℃ 내지 190℃에서 30분 내지 90 분 동안 이루어지는 것인 조성물.
- 청구항 11에 있어서, 상기 마이크로웨이브 조사는 2 기압 내지 100 기압하에서 이루어는 것인 조성물.
- 청구항 1에 있어서, 상기 신장 독성은 시스플라틴 또는 그 유사체의 투여에 의하여 야기되는 신장 독성인 것인 조성물.
- 파낙스속 식물 또는 그 추출물을 마이크로웨이브 조사하여 얻어진 진세노사이드 Rg3, Rk1 및 Rg5 및 비진세노사이드 성분이 함유된 파낙스속 식물 추출물을 활성 성분으로 함유하는 건강기능식품용 조성물.
- 청구항 1 내지 13 중 어느 하나의 조성물을 개체에 투여하는 단계;를 포함하는, 개체의 신장 독성을 억제하는 방법.
- 청구항 15에 있어서, 신장 독성을 유발하는 약제를 개체에 투여하는 단계를 더 포함하는 것인 방법.
- 청구항 16에 있어서, 상기 약제는 상기 신장 독성을 억제하기 위한 조성물을 투여하기 전, 동시 또는 후에 투여되는 것인 방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020130131500A KR20150050090A (ko) | 2013-10-31 | 2013-10-31 | 마이크로웨이브 조사에 의해 유효 성분 함량이 증가된 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 조성물, 건강기능식품용 조성물, 및 개체의 신장 독성을 억제하는 방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020130131500A KR20150050090A (ko) | 2013-10-31 | 2013-10-31 | 마이크로웨이브 조사에 의해 유효 성분 함량이 증가된 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 조성물, 건강기능식품용 조성물, 및 개체의 신장 독성을 억제하는 방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150050090A true KR20150050090A (ko) | 2015-05-08 |
Family
ID=53388045
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020130131500A KR20150050090A (ko) | 2013-10-31 | 2013-10-31 | 마이크로웨이브 조사에 의해 유효 성분 함량이 증가된 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 조성물, 건강기능식품용 조성물, 및 개체의 신장 독성을 억제하는 방법 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR20150050090A (ko) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108403741A (zh) * | 2018-04-18 | 2018-08-17 | 佛山市飞程信息技术有限公司 | 一种微波辅助提取人参皂苷的方法 |
| KR20210155691A (ko) * | 2020-06-16 | 2021-12-23 | 한국과학기술연구원 | 연속식 마이크로웨이브 조사에 의해 테트라히드로칸나비놀의 함량비율이 증가된 칸나비스속 식물 추출물의 제조방법, 및 그 칸나비스속 식물 추출물을 포함하는 조성물 |
-
2013
- 2013-10-31 KR KR1020130131500A patent/KR20150050090A/ko active Search and Examination
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN108403741A (zh) * | 2018-04-18 | 2018-08-17 | 佛山市飞程信息技术有限公司 | 一种微波辅助提取人参皂苷的方法 |
| KR20210155691A (ko) * | 2020-06-16 | 2021-12-23 | 한국과학기술연구원 | 연속식 마이크로웨이브 조사에 의해 테트라히드로칸나비놀의 함량비율이 증가된 칸나비스속 식물 추출물의 제조방법, 및 그 칸나비스속 식물 추출물을 포함하는 조성물 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102070297B1 (ko) | 마이크로웨이브 조사에 의해 진세노사이드 알지3, 알지5 및 알케이1의 함량비율이 증가된 파낙스속 식물 추출물, 그 제조방법, 및 그 가공 파낙스속 식물 추출물을 포함하는 조성물 | |
| Lin et al. | Cordyceps as an herbal drug | |
| US20130178436A1 (en) | Composition for preventing, improving, or treating renal disease including maillard browning reaction products of panax species plant extract | |
| Gasparrini et al. | The efficacy of berries against lipopolysaccharide-induced inflammation: A review | |
| US20100112101A1 (en) | Bio-availability/bio-efficacy enhancing activity of stevia rebaudiana and extracts and fractions and compounds thereof | |
| KR101579219B1 (ko) | 복합 추출물을 포함하는 대장염 예방, 개선 또는 치료용 조성물 | |
| KR101776179B1 (ko) | 진세노사이드 20(s)-알지3 또는 진세노사이드 20(r)-알지3의 함량비율이 증가된 가공 파낙스속 식물 추출물, 그 제조방법, 및 그 가공 파낙스속 식물 추출물을 포함하는 조성물 | |
| KR101209574B1 (ko) | 이고들빼기로부터 분리한 화합물을 유효성분으로 함유하는 간 기능 개선용 약학적 조성물 및 간 기능 개선용 건강기능 식품조성물 | |
| Zhou et al. | Phytochemicals as potential target on thioredoxin-interacting protein (TXNIP) for the treatment of cardiovascular diseases | |
| KR101831981B1 (ko) | 상동나무 추출물 또는 이의 분획물을 유효성분으로 함유하는 암의 예방, 개선 또는 치료용 조성물 | |
| KR20150050090A (ko) | 마이크로웨이브 조사에 의해 유효 성분 함량이 증가된 파낙스속 식물 추출물을 포함하는 신장 독성을 억제하기 위한 조성물, 건강기능식품용 조성물, 및 개체의 신장 독성을 억제하는 방법 | |
| EP3025721B1 (en) | Pharmaceutical composition for preventing or treating asthma comprising pistacia weinmannifolia j. poiss. ex franch extract or fraction thereof | |
| KR101455177B1 (ko) | 파낙스속 식물 추출물의 마이얄형 갈색화 반응 생성물을 포함하는 신장질환의 예방, 개선 또는 치료용 조성물 | |
| KR101537856B1 (ko) | 인삼 유래의 진세노사이드 Rb1의 함량이 증강된 추출 분획물을 유효성분으로 함유하는 비알코올성 지방간증의 예방 및 치료용 약제학적 조성물 | |
| KR101496155B1 (ko) | 진세노사이드 알지5 또는 진세노사이드 알케이1의 함량비율이 증가된 가공 파낙스속 식물 추출물, 그 제조방법, 및 그 가공 파낙스속 식물 추출물을 포함하는 조성물 | |
| KR101520388B1 (ko) | 마이크로웨이브 조사에 의해 진세노사이드 알에스3, 알에스4 및 알에스5의 함량비율이 증가된 파낙스속 식물 추출물, 그 식물 추출물을 포함하는 조성물 및 진세노사이드 함량이 증가된 파낙스속 식물 추출물의 제조방법 | |
| KR101400782B1 (ko) | 진세노사이드 20(s)-알지3 또는 진세노사이드 20(r)-알지3의 함량비율이 증가된 가공 파낙스속 식물 추출물, 그 제조방법, 및 그 가공 파낙스속 식물 추출물을 포함하는 조성물 | |
| KR101794924B1 (ko) | 퉁퉁마디 유래 비알코올성 지방간 질환 예방 또는 치료용 이소람네틴의 분리방법 | |
| KR20200107524A (ko) | 인삼 추출물의 분획물을 포함하는 간질환 예방 또는 치료용 약학적 조성물 | |
| KR101454336B1 (ko) | 관절염 예방 및 치료를 위한 조성물 | |
| KR20140129752A (ko) | 혈중 콜레스테롤 농도 저하 활성을 갖는 초고압 양파 추출물의 제조방법 및 그 양파 추출물을 유효성분으로 약학조성물 또는 건강기능식품 조성물 | |
| KR102392292B1 (ko) | 페오니플로린을 포함하는 악액질 및 근손실 예방 또는 치료용 조성물 | |
| KR101241338B1 (ko) | 편축 추출물을 유효성분으로 함유하는 지질 관련 심혈관 질환 또는 비만의 예방 및 치료용 조성물 | |
| KR20230057661A (ko) | 인삼 추출물의 사포닌 분획물을 포함하는 신경퇴행성 질환의 예방 또는 치료용 약학적 조성물 | |
| Boro et al. | Herbal Medicine and Plants in the Treatment of Leukemia |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| AMND | Amendment |