KR20100097098A - Methods and compounds for treating retinol-related diseases - Google Patents
Methods and compounds for treating retinol-related diseases Download PDFInfo
- Publication number
- KR20100097098A KR20100097098A KR1020107009129A KR20107009129A KR20100097098A KR 20100097098 A KR20100097098 A KR 20100097098A KR 1020107009129 A KR1020107009129 A KR 1020107009129A KR 20107009129 A KR20107009129 A KR 20107009129A KR 20100097098 A KR20100097098 A KR 20100097098A
- Authority
- KR
- South Korea
- Prior art keywords
- alkyl
- compound
- optionally substituted
- formula
- butyl
- Prior art date
Links
- 0 *c1cc(O)c(*C*N)cc1 Chemical compound *c1cc(O)c(*C*N)cc1 0.000 description 5
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/167—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the nitrogen of a carboxamide group directly attached to the aromatic ring, e.g. lidocaine, paracetamol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
Abstract
혈청 레티놀 수준을 감소시키는 화합물은 시각 사이클 과정 중에 축적되는 노폐물의 과잉생산과 관련이 있는 안과적 병상을 치료하는데 사용된다. 본 발명자들은 예를 들어 황반 변성 및 이영양을 치료하거나 이러한 안과적 병상과 관련이 있는 증상을 완화시키는 방법, 화합물 및 조성물을 기술한다.Compounds that reduce serum retinol levels are used to treat ophthalmic conditions that are associated with overproduction of waste products that accumulate during the visual cycle process. We describe for example methods, compounds and compositions for treating macular degeneration and dystrophies or for alleviating the symptoms associated with such ocular conditions.
Description
관련 출원의 상호 참조Cross Reference of Related Application
본 출원은 2007년 9월 27일 출원된 레티놀 관련 질환을 치료하기 위한 방법 및 화합물이라는 명칭의 미국 가출원 제60/975,765호의 이점을 청구하며, 그의 개시내용은 전체적으로 본원에 참고로 포함된다.This application claims the benefit of US Provisional Application No. 60 / 975,765, entitled Methods and Compounds for Treating Retinol Related Diseases, filed September 27, 2007, the disclosure of which is incorporated herein by reference in its entirety.
본원에 기술된 방법 및 조성물은 대상에서 혈청 레티놀, 레티놀 결합 단백질(RBP) 및/또는 트랜스티레틴(TTR)의 활성 또는 이용가능성(availability)을 조절함으로써, 대상에서 레티놀 관련 질환을 치료하기 위한 것이다.The methods and compositions described herein are for treating retinol related diseases in a subject by modulating the activity or availability of serum retinol, retinol binding protein (RBP) and / or transthyretin (TTR) in the subject. .
레티노이드는 정상적인 성장, 발육, 면역, 생식, 시력 및 기타 생리적 과정의 유지에 필수적이다. 이와는 반대로, 레티노이드의 비정상적인 생산 또는 가공 과정은 질환의 발현과 상관성이 있다.Retinoids are essential for the maintenance of normal growth, development, immunity, reproduction, vision and other physiological processes. In contrast, abnormal production or processing of retinoids correlates with the manifestation of the disease.
예를 들어, 세계 어린이 중 1억 명 이상이 비타민 A 결핍으로 인하여 시력상실은 물론, 사망에까지 이르고 있다. 표적 기관 및 조직, 예를 들어 눈에 과량의 비타민 A가 축적되게 되면, 황반 변성을 비롯한 다수의 망막 질환에서 실명을 초래할 수도 있다. 일반적으로 유리체망막 질환이라 불리는 다수의 병상들(예를 들어, 망막증, 황반 변성 및 이영양)은 안구의 뒷부분에 존재하는 유리체 및 망막에 영향을 미친다. 황반 변성은 미국내 55세 이상의 인구에 있어서 실명의 주요 원인이 되는 안질환의 일군으로서, 현재 미국인 중 1 천만 명 이상이 이 병을 앓고 있다. 몇몇 연구 결과에 따르면, 이 질환의 유행성으로 판단하건대, 향후 10년에 걸쳐서 발생할 황반 변성 발병 환자의 수는 6 배 정도 증가할 것으로 예측하고 있다. 연령 관련 황반 변성 또는 이영양은, 특히 쇠약성 질환(debilitating disease)이며, 시력을 점점 상실시키고 마침내는 중심부 시력(central vision)의 심각한 손상을 초래하게 된다.For example, more than 100 million of the world's children are suffering from vitamin A deficiency and death. Accumulation of excess vitamin A in target organs and tissues, such as the eye, can also lead to blindness in many retinal diseases, including macular degeneration. Many pathologies commonly referred to as vitreoretinal diseases (eg, retinopathy, macular degeneration and dystrophies) affect the vitreous and retina that are present at the back of the eye. Macular degeneration is a group of eye diseases that are the leading cause of blindness in the population over the age of 55 in the United States, with more than 10 million Americans now suffering from this disease. According to some studies, judging from the epidemic of the disease, the number of patients with macular degeneration over the next decade will increase by six times. Age-related macular degeneration or dystrophy is a particularly debilitating disease, which leads to progressive loss of vision and eventually to severe damage to central vision.
연령 관련 황반 변성의 두 가지 범주로 습성 형태와 건성 형태가 있다. 모든 경우의 약 90%를 차지하는 건성 형태의 황반 변성은 또한 위축성(atropic), 비삼출성(nonexudative) 또는 드루제노이드(drusenoid) 황반 변성으로도 알려져 있다. 건성 형태의 황반 변성의 경우, 드루젠은 전형적으로 망막내 RPE 조직 아래에 축적된다. 그 후, 드루젠이 황반에서 광수용체의 기능을 방해하면 시력 상실이 일어날 수 있다. 그 결과, 이러한 형태의 황반 변성은 수 년에 걸쳐 점진적인 시력 상실을 초래한다.There are two categories of age-related macular degeneration: wet and dry. Dry form of macular degeneration, which accounts for about 90% of all cases, is also known as atropic, nonexudative or drusenoid macular degeneration. In the dry form of macular degeneration, drusen typically accumulates under RPE tissue in the retina. Thereafter, vision loss can occur if drusen interferes with the function of the photoreceptor in the macula. As a result, this form of macular degeneration results in gradual loss of vision over the years.
경우의 약 10%를 차지하는 습성 형태의 황반 변성은 또한 맥락막 혈관신생, 망막하 혈관신생, 삼출성 또는 원반형 변성이라고도 알려져 있다. 습성 형태의 황반 변성에서, 비정상적 혈관 성장이 황반 아래에서 형성될 수 있으며; 이들 혈관이 혈액을 누출시키고 체액을 황반으로 유입시켜 광수용체 세포를 손상시킬 수 있다. 연구에 따르면, 건성 형태의 황반 변성은 습성 형태의 황반 변성을 유발시킬 수 있는 것으로 나타났다. 습성 형태의 황반 변성은 신속하게 진행하여 중심 시력에 심각한 손상을 야기할 수 있다.Macular degeneration in wet form, which accounts for about 10% of cases, is also known as choroidal neovascularization, subretinal angiogenesis, exudative or discoid degeneration. In wet form of macular degeneration, abnormal blood vessel growth may form below the macular; These blood vessels can leak blood and enter body fluids into the macula, damaging photoreceptor cells. Studies have shown that dry macular degeneration can lead to wet macular degeneration. Wet form macular degeneration can proceed rapidly and cause serious damage to central vision.
본원에는 인간 대상 또는 환자에서 레티놀 관련 질환을 치료하기 위한 방법, 화합물 및 조성물이 기술되어 있다. 이러한 질환으로는 건성 형태의 황반 변성, 지도형 위축 및/또는 광수용체 변성을 비롯한 황반 변성, 황반 이영양 및 망막 이영양이 있다. 또한, 본원에는 인간 대상 또는 환자에서 과다레티놀혈증(hyperretinolemia)(과량의 혈청 레티놀 수준)을 치료하기 위한 방법, 화합물 및 조성물이 기술되어 있다. 또한, 본원에는 인간 대상 또는 환자에서 혈청 레티놀, 혈청 RBP(레티놀 결합 단백질) 및/또는 혈청 TTR(트랜스티레틴(transthyretin))의 수준을 저하시키기 위한 방법, 화합물 및 조성물이 기술되어 있다. 또한, 본원에는 환자 신체에서 혈청 레티놀의 수준을 저하시키도록 유리체망막 질환을 치료하기 위한 방법, 화합물 및 조성물이 기술되어 있다. 일부 구체예에서, 유리체망막 질환은 황반 변성, 황반 이영양 및 망막 이영양이다. 일부 구체예에서, 유리체망막 질환은 건성 형태의 황반 변성, 광수용체 변성, 지도형 위축, 황반 이영양, 당뇨병성 망막병증, 습성 형태의 황반 변성, 미숙아 망막병증 및/또는 색소성 망막염이다.Described herein are methods, compounds, and compositions for treating retinol related diseases in human subjects or patients. Such diseases include macular degeneration, macular dystrophy and retinal dystrophy, including dry form of macular degeneration, superficial atrophy and / or photoreceptor degeneration. Also described herein are methods, compounds, and compositions for treating hyperretinolemia (excess serum retinol levels) in human subjects or patients. Also described herein are methods, compounds and compositions for lowering levels of serum retinol, serum RBP (retinol binding protein) and / or serum TTR (transthyretin) in human subjects or patients. Also described herein are methods, compounds, and compositions for treating vitreoretinal diseases to lower the level of serum retinol in a patient's body. In some embodiments, the vitreoretinal disease is macular degeneration, macular dystrophy and retinal dystrophy. In some embodiments, the vitreoretinal disease is dry form macular degeneration, photoreceptor degeneration, superficial atrophy, macular dystrophy, diabetic retinopathy, wet form macular degeneration, prematurity retinopathy and / or pigmented retinitis.
하나의 일면으로는, 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제를 포함하는 약제학적 조성물이다:In one aspect, a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 네오펜틸, sec-펜틸, 이소펜틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, neopentyl, sec-pentyl, isopentyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체(bioisostere), -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisostere,-(C = O) -NR 1 R, NR 1- (C═O) —R, — (C 1 -C 7 ) alkyl- (C═O) -OR or-(C 1 -C 7 ) alkyl- (C═O) -NR 1 R Is;
R은 H 또는 이고;R is H or ego;
G는 -OR1, -(C1-C6)알킬, -(C1-C6)알킬-OR1, 할로겐, -CO2R1, -(C1-C6)알킬-CO2R1, NHR1, -(C1-C6)알킬-NHR1, -(C=O)NHR1, -(C1-C6)알킬-(C=O)NHR1, -NHR1(C=O)R1, -(C1-C6)알킬-NHR1(C=O)R1이며;G is -OR 1 ,-(C 1 -C 6 ) alkyl,-(C 1 -C 6 ) alkyl-OR 1 , halogen, -CO 2 R 1 ,-(C 1 -C 6 ) alkyl-CO 2 R 1 , NHR 1 ,-(C 1 -C 6 ) alkyl-NHR 1 ,-(C = O) NHR 1 ,-(C 1 -C 6 ) alkyl- (C = O) NHR 1 , -NHR 1 (C ═O) R 1 , — (C 1 -C 6 ) alkyl-NHR 1 (C═O) R 1 ;
R1은 H 또는 (C1-C6)알킬이고;R 1 is H or (C 1 -C 6 ) alkyl;
X는 할로겐이다. 하나의 구체예에서, 약제학적 조성물은 일반식 (I)의 화합물을 전신적 투여하기 위한 경구적인 약제학적 조성물이다.X is halogen. In one embodiment, the pharmaceutical composition is an oral pharmaceutical composition for systemic administration of a compound of formula (I).
하나의 구체예로는, 하기 일반식 (II)의 구조를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제를 포함하는 약제학적 조성물이다:In one embodiment, there is provided a compound having the structure of Formula (II): or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H 또는 이며;R is H or Is;
G는 -OR1, -(C1-C6)알킬, -(C1-C6)알킬-OR1, 할로겐, -CO2R1, -(C1-C6)알킬-CO2R1, NHR1, -(C1-C6)알킬-NHR1, -(C=O)NHR1, -(C1-C6)알킬-(C=O)NHR1, -NHR1(C=O)R1, -(C1-C6)알킬-NHR1(C=O)R1이고;G is -OR 1 ,-(C 1 -C 6 ) alkyl,-(C 1 -C 6 ) alkyl-OR 1 , halogen, -CO 2 R 1 ,-(C 1 -C 6 ) alkyl-CO 2 R 1 , NHR 1 ,-(C 1 -C 6 ) alkyl-NHR 1 ,-(C = O) NHR 1 ,-(C 1 -C 6 ) alkyl- (C = O) NHR 1 , -NHR 1 (C ═O) R 1 , — (C 1 -C 6 ) alkyl-NHR 1 (C═O) R 1 ;
R1은 H 또는 (C1-C6)알킬이다. 하나의 구체예에서, 약제학적 조성물은 일반식 (II)의 화합물을 전신적 투여하기 위한 경구적인 약제학적 조성물이다.R 1 is H or (C 1 -C 6 ) alkyl. In one embodiment, the pharmaceutical composition is an oral pharmaceutical composition for systemic administration of a compound of formula (II).
또 다른 구체예로는, A가 O인 일반식 (II)의 구조를 가진 화합물을 포함하는 약제학적 조성물이다. 추가의 구체예로는, B가 -(CH2)n이고 n이 1-6이거나, B가 -(C3-C8)사이클로알킬인 일반식 (II)의 구조를 가진 화합물을 포함하는 약제학적 조성물이다. 또 다른 추가의 구체예로는, E가 (C=O)-OR, 카르복시산 생물동배체, -(C=O)-NR1R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R인 일반식 (II)의 구조를 가진 화합물을 포함하는 약제학적 조성물이다. 하나의 구체예로는, A가 O이고, B가 (C3-C8)사이클로알킬이며, E가 (C=O)-OR이고, R이 H인 일반식 (II)의 구조를 가진 화합물을 포함하는 약제학적 조성물이다. 추가의 구체예에서, B는 사이클로헥실이고, R은 H이다. 또 다른 추가의 구체예에서, B는 사이클로펜틸이고, R은 H이다. 또 다른 추가의 구체예로는, 구조 를 가진 화합물이다. 또 다른 구체예로는, 구조 를 가진 화합물이다.In another embodiment is a pharmaceutical composition comprising a compound having the structure of Formula (II) wherein A is O. In a further embodiment, a medicament comprising a compound having the structure of formula (II) wherein B is-(CH 2 ) n and n is 1-6 or B is-(C 3 -C 8 ) cycloalkyl Pharmaceutical composition. In yet another embodiment, E is (C═O) —OR, a carboxylic acid bioisotope, — (C═O) —NR 1 R, — (C 1 -C 7 ) alkyl- (C═O) A pharmaceutical composition comprising a compound having the structure of Formula (II) wherein -OR or-(C 1 -C 7 ) alkyl- (C═O) —NR 1 R. In one embodiment, a compound having the structure of Formula (II) wherein A is O, B is (C 3 -C 8 ) cycloalkyl, E is (C═O) —OR, and R is H It is a pharmaceutical composition comprising a. In a further embodiment, B is cyclohexyl and R is H. In yet further embodiments, B is cyclopentyl and R is H. In still further embodiments, the structure It is a compound having. In another embodiment, the structure It is a compound having.
하나의 구체예로는, R이 인 일반식 (II)의 구조를 가진 화합물을 포함하는 약제학적 조성물이다.In one embodiment, R is A pharmaceutical composition comprising a compound having the structure of phosphorus general formula (II).
또 다른 구체예로는, E가 (C=O)-OR인 일반식 (II)의 구조를 가진 화합물을 포함하는 약제학적 조성물이다. 추가의 구체예로는, R이 H인 일반식 (II)의 구조를 가진 화합물을 포함하는 약제학적 조성물이다. 또 다른 추가의 구체예로는, 5-(2-tert-부틸-4-클로로페녹시)-N-(4-하이드록시페닐)펜탄아미드, 7-(2-tert-부틸-4-클로로페녹시)-N-(4-하이드록시페닐)헵탄아미드, 4-(5-(2-tert-부틸-4-클로로페녹시)펜탄아미도)벤조산, 4-(3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로펜탄아미도)벤조산, 5-(2-tert-부틸-4-클로로페녹시)펜탄산, 4-(2-tert-부틸-4-클로로페녹시)부탄산, 2-(3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로펜틸)아세트산, 7-(2-tert-부틸-4-클로로페녹시)헵탄산, 4-(5-(2-tert-부틸-4-클로로페녹시)펜탄아미도)벤자미드, 3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로헥산카르복시산, 3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로펜탄카르복시산, 3-((2-tert-부틸-4-클로로페닐아미노)메틸)사이클로펜탄아미드, 4-(3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로펜탄카르복사미도)벤조산 및 5-(2-tert-부틸-4-클로로페닐티오)펜탄산으로 이루어진 그룹 중에서 선택된 일반식 (I)의 화합물을 포함하는 조성물이다.In another embodiment is a pharmaceutical composition comprising a compound having the structure of Formula (II) wherein E is (C═O) —OR. In a further embodiment is a pharmaceutical composition comprising a compound having the structure of formula (II) wherein R is H. In yet further embodiments, 5- (2-tert-butyl-4-chlorophenoxy) -N- (4-hydroxyphenyl) pentanamide, 7- (2-tert-butyl-4-chlorophenoxy C) -N- (4-hydroxyphenyl) heptanamide, 4- (5- (2-tert-butyl-4-chlorophenoxy) pentaneamido) benzoic acid, 4- (3-((2-tert- Butyl-4-chlorophenoxy) methyl) cyclopentaneamido) benzoic acid, 5- (2-tert-butyl-4-chlorophenoxy) pentanoic acid, 4- (2-tert-butyl-4-chlorophenoxy) Butanoic acid, 2- (3-((2-tert-butyl-4-chlorophenoxy) methyl) cyclopentyl) acetic acid, 7- (2-tert-butyl-4-chlorophenoxy) heptanoic acid, 4- ( 5- (2-tert-butyl-4-chlorophenoxy) pentaneamido) benzamide, 3-((2-tert-butyl-4-chlorophenoxy) methyl) cyclohexanecarboxylic acid, 3-((2- tert-butyl-4-chlorophenoxy) methyl) cyclopentanecarboxylic acid, 3-((2-tert-butyl-4-chlorophenylamino) methyl) cyclopentanamide, 4- (3-((2-tert-butyl 4-chlorophenoxy) methyl) cyclopentanecarboxamido) benzoic acid 5- (2-tert- butyl-4-chlorophenylthio) a composition comprising a compound of formula (I) selected from the group consisting of pentanoic acid.
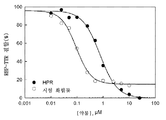
하나의 구체예로는, 억제의 IC5O이 약 5 μM 미만인, 레티놀-레티놀 결합 단백질-트랜스티레틴 복합체 형성을 억제하는 일반식 (I)의 화합물을 포함하는 약제학적 조성물이다. 추가의 구체예로는, 억제의 IC50이 약 1 μM 미만인 일반식 (I)의 화합물을 포함하는 약제학적 조성물이다. 또 다른 구체예로는, 시토크롬 P450을 약 50% 미만으로 억제하는 일반식 (I)의 화합물을 포함하는 약제학적 조성물이다. 또 다른 추가의 구체예로는, 시토크롬 P450을 약 10% 미만으로 억제하는 일반식 (I)의 화합물을 포함하는 약제학적 조성물이다. 또 다른 구체예로는, 유리체망막 질환을 치료하는데 사용되는 일반식 (I)의 화합물을 포함하는 약제학적 조성물이다. 추가의 구체예로는, 유리체망막 질환이 건성 형태의 황반 변성, 광수용체 변성, 지도형 위축, 황반 이영양, 당뇨병성 망막병증, 습성 형태의 황반 변성, 미숙아 망막병증 및 색소성 망막염으로 이루어진 그룹 중에서 선택되는, 일반식 (I)의 화합물을 포함하는 약제학적 조성물이다.In one embodiment is a pharmaceutical composition comprising a compound of formula (I) that inhibits the retinol-retinol binding protein-transtyretin complex formation, wherein the IC 50 of inhibition is less than about 5 μM. In a further embodiment is a pharmaceutical composition comprising a compound of formula (I) wherein the IC 50 of inhibition is less than about 1 μM. In another embodiment is a pharmaceutical composition comprising a compound of formula (I) that inhibits cytochrome P 450 to less than about 50%. In yet another embodiment is a pharmaceutical composition comprising a compound of formula (I) that inhibits cytochrome P 450 to less than about 10%. In another embodiment is a pharmaceutical composition comprising a compound of formula (I) for use in treating a vitreoretinal disease. In a further embodiment, the vitreoretinal disease is a group consisting of macular degeneration of the dry form, photoreceptor degeneration, superficial atrophy, macular dystrophy, diabetic retinopathy, macular degeneration of the wet form, prematurity retinopathy and retinitis pigmentosa. It is a pharmaceutical composition containing the compound of general formula (I) selected from.
하나의 일면으로는, 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제 또는 담체를 포함하는 약제학적 조성물이다:In one aspect, a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients or carriers:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 네오펜틸, sec-펜틸, 이소펜틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, neopentyl, sec-pentyl, isopentyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 약제학적 조성물은 일반식 (I)의 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물이다.X is halogen. In one embodiment, the pharmaceutical composition is an oral pharmaceutical composition for systemic administration of a compound of formula (I).
하나의 구체예로는, 하기 일반식 (II)의 구조를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제 또는 담체를 포함하는 약제학적 조성물이다:In one embodiment, there is provided a compound having the structure of Formula (II): or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients or carriers:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, (C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl, (C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 약제학적 조성물은 일반식 (II)의 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물이다.R is H, optionally substituted aryl or optionally substituted heteroaryl. In one embodiment, the pharmaceutical composition is an oral pharmaceutical composition for systemic administration of a compound of formula (II).
하나의 구체예로는, A가 O이고, B가 (C3-C8)사이클로알킬이며, E가 (C=O)-OR이고, R이 H인 일반식 (II)의 구조를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제 또는 담체를 포함하는 약제학적 조성물이다. 추가의 구체예로는, A가 O이고, B가 사이클로헥실이며, R이 H인 일반식 (II)의 구조를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제 또는 담체를 포함하는 약제학적 조성물이다. 또 다른 추가의 구체예로는, A가 O이고, B가 사이클로펜틸이며, R이 H인 일반식 (II)의 구조를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제 또는 담체를 포함하는 약제학적 조성물이다. 또 다른 추가의 구체예로는, 구조 를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제 또는 담체를 포함하는 약제학적 조성물이다. 또 다른 구체예로는, 구조 를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물; 및 약제학적으로 허용가능한 부형제 또는 담체를 포함하는 약제학적 조성물이다.In one embodiment, a compound having the structure of Formula (II) wherein A is O, B is (C 3 -C 8 ) cycloalkyl, E is (C═O) —OR, and R is H Or active metabolites or pharmaceutically acceptable prodrugs, salts or solvates thereof; And pharmaceutically acceptable excipients or carriers. In a further embodiment, a compound having the structure of formula (II) wherein A is O, B is cyclohexyl, and R is H, or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof ; And pharmaceutically acceptable excipients or carriers. In yet another embodiment, a compound having the structure of formula (II) wherein A is O, B is cyclopentyl, and R is H, or an active metabolite or pharmaceutically acceptable prodrug, salt or Solvates; And pharmaceutically acceptable excipients or carriers. In still further embodiments, the structure A compound having or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients or carriers. In another embodiment, the structure A compound having or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients or carriers.
또 다른 구체예로는, 포유동물에서 혈청 레티놀 또는 안조직 레티놀 수준 또는 활성을 조절하는데 충분한 양으로 일반식 (I)의 화합물을 포함하는 약제학적 조성물이다.In another embodiment is a pharmaceutical composition comprising a compound of formula (I) in an amount sufficient to modulate serum retinol or ocular retinol levels or activity in a mammal.
하나의 일면으로는, 환자에게 치료학적 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하여, 이를 필요로 하는 환자에서 건성 형태의 황반 변성, 광수용체 변성, 지도형 위축, 황반 이영양, 당뇨병성 망막병증, 습성 형태의 황반 변성, 미숙아 망막병증 또는 색소성 망막염을 치료하는 방법이다:In one aspect, the method comprises administering to a patient a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof, Treatment of dry macular degeneration, photoreceptor degeneration, superficial atrophy, macular dystrophies, diabetic retinopathy, wet macular degeneration, prematurity retinopathy or pigment retinopathy in patients:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 환자에게 치료학적 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하여, 이를 필요로 하는 환자에서 건성 형태의 황반 변성, 광수용체 변성, 지도형 위축, 황반 이영양, 당뇨병성 망막병증, 습성 형태의 황반 변성, 미숙아 망막병증 또는 색소성 망막염을 치료하는 방법이다:In one embodiment, there is a need for administering to a patient a therapeutically effective amount of a compound of formula (II): or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof, Treatment of dry form macular degeneration, photoreceptor degeneration, superficial atrophy, macular dystrophies, diabetic retinopathy, wet form macular degeneration, prematurity retinopathy, or pigmented retinitis
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 일면으로는, 포유동물에서 레티놀 결합 단백질 수준 또는 활성을 조절하는 치료학적 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에게 투여하는 단계를 포함하여, 유리체망막 질환을 치료하는 방법이다:In one aspect, a mammal is provided with a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof that modulates retinol binding protein levels or activity in a mammal. A method of treating vitreoretinal disease, comprising administering to an animal:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 포유동물에서 레티놀 결합 단백질 수준 또는 활성을 조절하는 치료학적 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에게 투여하는 단계를 포함하여, 유리체망막 질환을 치료하는 방법이다:In one embodiment, there is provided a therapeutically effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof that modulates retinol binding protein levels or activity in a mammal. A method of treating vitreoretinal disease, comprising administering to a mammal:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, (C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl, (C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
또 다른 구체예로는, 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 포유동물에게 투여하는 단계를 포함하며, 레티놀 결합 단백질이 RBP4인 유리체망막 질환을 치료하는 방법이다. 추가의 구체예로는, 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 포유동물에 투여하는 단계를 포함하여, 건성 형태의 황반 변성, 광수용체 변성, 지도형 위축, 황반 이영양, 당뇨병성 망막병증, 습성 형태의 황반 변성, 미숙아 망막병증 및 색소성 망막염인 유리체망막 질환을 치료하는 방법이다.In another embodiment is a method of treating a vitreoretinal disease wherein a therapeutically effective amount of a compound of Formula (I) or (II) is administered to a mammal, wherein the retinol binding protein is RBP4. In a further embodiment, the method comprises administering to a mammal a therapeutically effective amount of a compound of formula (I) or (II) in dry form macular degeneration, photoreceptor degeneration, geographic atrophy, macular dystrophy , Diabetic retinopathy, wet form macular degeneration, prematurity retinopathy and pigmented retinitis.
하나의 일면으로, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 조절하는 치료학적 유효량의 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다:In one aspect, a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvent thereof, that modulates serum retinol binding protein or transthyretin level or activity in a mammal A method of lowering serum retinol binding protein or transthyretin level or activity in a mammal, comprising administering a cargo:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 일면으로, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 조절하는 치료학적 유효량의 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다:In one aspect, a therapeutically effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvent thereof that modulates serum retinol binding protein or transthyretin level or activity in a mammal A method of lowering serum retinol binding protein or transthyretin level or activity in a mammal, comprising administering a cargo:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, (C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl, (C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
또 다른 구체예로는, 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하며, 혈청 레티놀 결합 단백질이 RBP4인, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다. 하나의 구체예로는, 포유동물에서 레티놀 결합 단백질 또는 트랜스티레틴의 전사를 억제하는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다. 추가의 구체예로는, 포유동물에서 레티놀 결합 단백질 또는 트랜스티레틴의 전사를 억제하는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다. 또 다른 구체예로는, 레티놀 결합 단백질에 대한 레티놀의 결합을 억제하는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다. 하나의 구체예로는, 트랜스티렌에 대한 레티놀 결합 단백질의 결합을 억제하는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다. 또 다른 구체예로는, 포유동물에서 레티놀 결합 단백질 또는 트랜스티레틴 제거율을 증가시키는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 저하시키는 방법이다.In another embodiment, the method comprises administering a therapeutically effective amount of a compound of Formula (I) or (II), wherein the serum retinol binding protein or transthyretin level in a mammal wherein the serum retinol binding protein is RBP4. Or a method of lowering activity. In one embodiment, the method comprises administering a therapeutically effective amount of a compound of formula (I) or (II) to inhibit the transcription of a retinol binding protein or transthyretin in a mammal, the serum retinol in the mammal A method of lowering binding protein or transthyretin level or activity. In a further embodiment, the method comprises administering a therapeutically effective amount of a compound of formula (I) or (II) to inhibit the transcription of a retinol binding protein or transthyretin in a mammal, wherein the serum retinol in the mammal is A method of lowering binding protein or transthyretin level or activity. In another embodiment, the method comprises administering a therapeutically effective amount of a compound of Formula (I) or (II) to inhibit the binding of retinol to a retinol binding protein, wherein the serum retinol binding protein or trans in a mammal. It is a method of lowering tyretin level or activity. In one embodiment, the method comprises administering a therapeutically effective amount of a compound of formula (I) or (II) to inhibit the binding of a retinol binding protein to transtiren, or the serum retinol binding protein in a mammal. It is a method of lowering transthyretin level or activity. In another embodiment, serum retinol binding in a mammal, comprising administering a therapeutically effective amount of a compound of formula (I) or (II) to increase the retinol binding protein or transthyretin removal rate in the mammal. A method of lowering protein or transthyretin levels or activity.
하나의 일면으로는, 치료학적 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에게 투여하는 단계를 포함하여, 포유동물에서 레티놀 관련 질환을 치료하는 방법이다:In one aspect, there is provided a method of treating a mammal in a mammal comprising administering to the mammal a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof: Here's how to treat retinol-related diseases:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 치료학적 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하여, 포유동물에서 레티놀 관련 질환을 치료하는 방법이다:In one embodiment, retinol-associated in a mammal comprises administering a therapeutically effective amount of a compound of formula (II): or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof Here's how to treat a disease:
상기 식에서,Where
A는 O, NH 또는 S이고; A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
또 다른 구체예로는, 포유동물에게 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 포유동물에서 레티놀 관련 질환을 치료하는 방법이며, 여기서 레티놀 관련 질환은 골형성과다증, 특발성 두개내 고혈압, 아밀로이드증, 알츠하이머 질환 및 알스트롬-할그렌 증후군이다.In another embodiment, a method of treating a retinol related disease in a mammal comprising administering to the mammal a therapeutically effective amount of a compound of formula (I) or (II), wherein the retinol related disease is Hyperostosis, idiopathic intracranial hypertension, amyloidosis, Alzheimer's disease and Alstrom-Halgren syndrome.
하나의 일면으로는, 시각 사이클에서 효소 또는 단백질의 활성을 직접적으로 조절하지 않는 치료학적 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에게 투여하는 단계를 포함하여, 건성 형태의 연령 관련 황반 변성을 가진 포유동물에서 혈청 레티놀 수준을 감소시키는 방법이다:In one aspect, a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof, which does not directly modulate the activity of an enzyme or protein in the visual cycle: A method of reducing serum retinol levels in a mammal with dry form of age related macular degeneration, comprising administering to the mammal:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 시각 사이클에서 효소 또는 단백질의 활성을 직접적으로 조절하지 않는 치료학적 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하여, 건성 형태의 연령 관련 황반 변성을 가진 포유동물에서 혈청 레티놀 수준을 감소시키는 방법이다:In one embodiment, a therapeutically effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvent thereof, which does not directly modulate the activity of an enzyme or protein in the visual cycle A method of reducing serum retinol levels in a mammal with dry form of age related macular degeneration, comprising administering a cargo:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예예서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
또 다른 구체예로는, 시각 사이클에서 효소 또는 단백질을 직접적으로 억제 또는 결합하지 않는 일반식 (I) 또는 (II)의 화합물을 포유동물에게 투여하는 단계를 포함하여, 건성 형태의 연령 관련 황반 변성을 가진 포유동물에서 혈청 레티놀 수준을 감소시키는 방법이다.In another embodiment, age-related macular degeneration in dry form, comprising administering to a mammal a compound of formula (I) or (II) that does not directly inhibit or bind an enzyme or protein in the visual cycle. To reduce serum retinol levels in mammals with
추가의 구체예로는, 로돕신 재생률에 영향을 미치지 않는 일반식 (I) 또는 (II)의 화합물을 포유동물에게 투여하는 단계를 포함하여, 건성 형태의 연령 관련 황반 변성을 가진 포유동물에서 혈청 레티놀 수준을 감소시키는 방법이다.In a further embodiment, serum retinol in a mammal having dry form of age-related macular degeneration, comprising administering to the mammal a compound of formula (I) or (II) that does not affect rhodopsin regeneration rate. It is a way to reduce the level.
또 다른 구체예로는, 지연된 암순응을 악화시키지 않는 일반식 (I) 또는 (II)의 화합물을 포유동물에게 투여하는 단계를 포함하여, 건성 형태의 연령 관련 황반 변성을 가진 포유동물에서 혈청 레티놀 수준을 감소시키는 방법이다.In another embodiment, serum retinol levels in a mammal having dry form of age-related macular degeneration, comprising administering to the mammal a compound of Formula (I) or (II) that does not worsen delayed dark adaptation. It is a way to reduce.
또 다른 추가의 구체예로는, 지도형 위축 또는 광수용체 변성의 확산을 제한하는 일반식 (I) 또는 (II)의 화합물을 포유동물에게 투여하는 단계를 포함하여, 건성 형태의 연령 관련 황반 변성을 가진 포유동물에서 혈청 레티놀 수준을 감소시키는 방법이다.In still further embodiments, dry age-related macular degeneration, comprising administering to a mammal a compound of formula (I) or (II) that limits the spread of geographic atrophy or photoreceptor degeneration To reduce serum retinol levels in mammals with
하나의 일면으로는, 포유동물에게 치료학적 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하여, 과다레티놀혈증을 치료하는 방법이다:In one aspect, hyperretinolemia, comprising administering to a mammal a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof: Here's how to cure:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
또 다른 구체예에서, 치료학적 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물 또는 용매화물을 투여하는 단계를 포함하여 과다레티놀혈증을 치료하는 방법이다:In another embodiment is a method of treating hyperretinolemia comprising administering a therapeutically effective amount of a compound of Formula (II): or an active metabolite or pharmaceutically acceptable prodrug or solvate thereof:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
추가의 구체예로는, 포유동물에게 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 유리체망막 질환과 관련이 있는 과다레티놀혈증을 치료하는 방법이다.In a further embodiment, there is a method of treating hyperretinolemia associated with vitreoretinal disease, comprising administering a compound of formula (I) or (II) to a mammal.
또 다른 구체예로는, 포유동물에게 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 당뇨병 또는 알츠하이머 질환과 관련된 과다레티놀혈증을 치료하는 방법이다.In another embodiment is a method of treating hyperretinolemia associated with diabetes or Alzheimer's disease, comprising administering a compound of formula (I) or (II) to a mammal.
하나의 일면으로는, 포유동물에게 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하며, 하기 일반식 (I)의 화합물이 레티놀-레티놀 결합 단백질-트랜스티레틴 복합체 형성을 억제하고, IC5O 억제가 약 5 μM 미만인, 포유동물에서 레티놀 관련 질환을 치료하는 방법이다:In one aspect, the method comprises administering to a mammal an effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof, wherein ) Is a method of treating retinol related diseases in mammals, wherein the retinol-retinol binding protein-transtyretin complex formation is inhibited and the IC 5O inhibition is less than about 5 μM:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, an effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 포유동물에게 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 투여하는 단계를 포함하며, 하기 일반식 (II)의 화합물이 레티놀-레티놀 결합 단백질-트랜스티레틴 복합체 형성을 억제하고, IC5O 억제가 약 5 μM 미만인, 포유동물에서 레티놀 관련 질환을 치료하는 방법이다:In one embodiment, the method comprises administering to a mammal an effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof, wherein Is a method of treating retinol related diseases in mammals wherein the compound of II) inhibits retinol-retinol binding protein-transtyretin complex formation and IC 5O inhibition is less than about 5 μM:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, an effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 포유동물에게 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하며, 상기 일반식 (I) 또는 (II)의 화합물이 레티놀-레티놀 결합 단백질-트랜스티레틴 복합체 형성을 억제하고, IC5O 억제가 약 1 μM 미만인, 포유동물에서 레티놀 관련 질환을 치료하는 방법이다.In one embodiment, the method comprises administering to a mammal an effective amount of a compound of formula (I) or (II), wherein the compound of formula (I) or (II) is a retinol-retinol binding protein- A method of treating retinol related diseases in mammals that inhibits the formation of transtyretin complexes and wherein IC 50 inhibition is less than about 1 μM.
또 다른 구체예로는, 포유동물에게 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하며, 상기 일반식 (I) 또는 (II)의 화합물이 레티놀-레티놀 결합 단백질-트랜스티레틴 복합체 형성을 억제하고, 상기 일반식 (I) 또는 (II)의 화합물이 시토크롬 P450을 약 50% 미만으로 추가로 억제하는, 포유동물에서 레티놀 관련 질환을 치료하는 방법이다.In another embodiment, the method comprises administering to a mammal an effective amount of a compound of formula (I) or (II), wherein the compound of formula (I) or (II) is a retinol-retinol binding protein- A method of treating retinol-related diseases in a mammal, wherein the composition of the formula (I) or (II) further inhibits cytochrome P 450 by less than about 50%.
또 다른 구체예로는, 포유동물에게 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하며, 상기 일반식 (I) 또는 (II)의 화합물이 레티놀-레티놀 결합 단백질-트랜스티레틴 복합체 형성을 억제하고, 상기 일반식 (I) 또는 (II)의 화합물이 시토크롬 P450을 약 10% 미만으로 추가로 억제하는, 포유동물에서 레티놀 관련 질환을 치료하는 방법이다.In another embodiment, the method comprises administering to a mammal an effective amount of a compound of formula (I) or (II), wherein the compound of formula (I) or (II) is a retinol-retinol binding protein- A method of treating retinol-related diseases in a mammal, wherein the composition of the formula (I) or (II) further inhibits cytochrome P 450 by less than about 10%.
하나의 일면으로는, 포유동물에서 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 조절하는 치료학적 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에게 투여하는 단계를 포함하여, 포유동물에서 I형 또는 II형 당뇨병을 치료하는 방법이다:In one aspect, a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt thereof, which modulates retinol binding protein or transthyretin level or activity in a mammal, or A method of treating Type I or Type II diabetes in a mammal, comprising administering a solvate to the mammal:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 포유동물에서 레티놀 결합 단백질 또는 트랜스티레틴 수준 또는 활성을 조절하는 치료학적 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에게 투여하는 단계를 포함하여, 포유동물에서 I형 또는 II형 당뇨병을 치료하는 방법이다:In one embodiment, a therapeutically effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt thereof, that modulates retinol binding protein or transthyretin level or activity in a mammal Or administering a solvate to the mammal, the method of treating type I or type II diabetes in a mammal:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 일면으로는, 치료학적 유효량의 일반식 (I)의 화합물 및 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 또는 안조직 레티놀 수준을 감소시키는 방법이다:In one aspect, a method of treating a mammal in a mammal, comprising administering to the mammal a therapeutically effective amount of a compound of formula (I) and / or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof A method of reducing serum retinol or ocular retinol levels is:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X는 할로겐이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (I)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.X is halogen. In one embodiment, a therapeutically effective amount of a compound of formula (I) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
하나의 구체예로는, 치료학적 유효량의 일반식 (II)의 화합물 및 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포유동물에 투여하는 단계를 포함하여, 포유동물에서 혈청 레티놀 또는 안조직 레티놀 수준을 감소시키는 방법이다:In one embodiment, the method comprises administering to a mammal a therapeutically effective amount of a compound of formula (II) and / or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof To reduce serum retinol or ocular retinol levels in:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다. 하나의 구체예에서, 치료학적 유효량의 일반식 (II)의 화합물은 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물의 형태로 제공된다.R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl. In one embodiment, a therapeutically effective amount of a compound of formula (II) is provided in the form of an oral pharmaceutical composition for systemic administration of the compound.
또 다른 구체예로는, 포유동물에게 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하며, 포유동물이 인간인, 포유동물에서 혈청 레티놀 또는 안조직 레티놀 수준을 감소시키는 방법이다.In another embodiment, the method comprises administering to a mammal an effective amount of a compound of Formula (I) or (II), wherein the mammal is a human that reduces serum retinol or ocular retinol levels. It is a way.
추가의 구체예로는, 포유동물에게 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하며, 혈청 레티놀 또는 안조직 레티놀 수준을 적어도 20%까지 감소시키는, 포유동물에서 혈청 레티놀 또는 안조직 레티놀 수준을 감소시키는 방법이다.A further embodiment comprises administering to the mammal an effective amount of a compound of Formula (I) or (II) and reducing serum retinol or ocular retinol levels by at least 20%. Retinol or eye tissue retinol levels are reduced.
또 다른 추가의 구체예로는, 포유동물에게 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하고, 산화질소 생산 유도제, 항염증제, 생리학적으로 허용가능한 항산화제, 생리학적으로 허용가능한 미네랄, 음하전 인지질, 카로테노이드, 스타틴, 혈관신생 억제 약물, 매트릭스 금속단백분해효소 억제제, 레스베라트롤 및 다른 트랜스-스틸벤 화합물 및 13-시스-레티노산으로 이루어진 그룹 중에서 선택된 적어도 하나의 부가적인 제제를 투여하는 단계를 추가로 포함하여, 포유동물에서 혈청 레티놀 또는 안조직 레티놀 수준을 감소시키는 방법이다.Still further embodiments include administering to a mammal an effective amount of a compound of Formula (I) or (II), the method comprising inducing nitric oxide production inducing agents, anti-inflammatory agents, physiologically acceptable antioxidants, physiological At least one additional agent selected from the group consisting of acceptable minerals, negatively charged phospholipids, carotenoids, statins, angiogenesis inhibitors, matrix metalloproteinase inhibitors, resveratrol and other trans-stilbene compounds and 13-cis-retinoic acid A method for reducing serum retinol or ocular retinol levels in a mammal, further comprising administering a.
하나의 일면으로는, 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포함하는 조성물이다:In one aspect, there is a composition comprising a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며, 단 -(C2-C7)헤테로알킬이 질소 원자, -C(=O)-, -S-, -S(=O)-, -S(=O)2-, -NR1(C=O)-, -(C=O)NR1-, S(=O)2NR1-, -NR1S(=O)2, -0(C=O)NR1-, -NR1(C=O)O-, -0(C=O)O-, -NR1(C=O)NR1-, -(C=O)O-, -0(C=O)-을 함유할 수 없고;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl, provided that-(C 2 -C 7 ) heteroalkyl is a nitrogen atom, -C (= O)-, -S-, -S (= O)-, -S (= O) 2- , -NR 1 (C = O)-,-(C = O) NR 1- , S (= O) 2 NR 1- , -NR 1 S (= O) 2 , -0 (C = O) NR 1- , -NR 1 (C = O) O-, -0 (C = O) O- , -NR 1 (C═O) NR 1 —, — (C═O) O—, —0 (C═O) — may not contain;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이며;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 헤테로아릴, 치환된 헤테로아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -0-C(O)NR2R3, -NR2R3(C=O)OR1, -SO2NR2R3이고, 단 헤테로아릴은 질소 원자를 함유할 수 없으며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -
R2 및 R3는 각각 독립적으로 H, C1-C6알킬 및 C3-C6 사이클로알킬 중에서 선택되고;R 2 and R 3 are each independently H, C 1 -C 6 alkyl and C 3 -C 6 Selected from cycloalkyl;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이며, 단 B가 -S-인 경우 R은 피리미딘일 수 없고; B가 -(C2-C7)알킬인 경우 R은 이미다졸일 수 없으며;R is H, optionally substituted aryl or optionally substituted heteroaryl, provided that when B is -S-, R cannot be pyrimidine; When B is-(C 2 -C 7 ) alkyl R cannot be imidazole;
R1은 H 또는 (C1-C6)알킬이고;R 1 is H or (C 1 -C 6 ) alkyl;
X는 할로겐이며,X is halogen,
단 E는 일 수 없다.Where E is Cannot be
하나의 구체예로는, 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 포함하는 조성물이다:In one embodiment is a composition comprising a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며; 단, -(C2-C7)헤테로알킬은 질소 원자, -C(=O)-, -S-, -S(=O)-, -S(=O)2-, -NR1(C=O)-, -(C=O)NR1-, S(=O)2NR1-, -NR1S(=O)2, -0(C=O)NR1-, -NR1(C=O)O-, -0(C=O)O-, -NR1(C=O)NR1-, -(C=O)O-, -0(C=O)-를 함유할 수 없고;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl; Provided that-(C 2 -C 7 ) heteroalkyl is a nitrogen atom, -C (= O)-, -S-, -S (= O)-, -S (= O) 2- , -NR 1 (C = O)-,-(C = O) NR 1- , S (= O) 2 NR 1- , -NR 1 S (= O) 2 , -0 (C = O) NR 1- , -NR 1 ( May contain C═O) O—, —0 (C═O) O—, —NR 1 (C═O) NR 1 —, — (C═O) O—, —0 (C═O) — No;
D는 tert-부틸이며;D is tert-butyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -O-C(O)NR2R3, -NR2R3(C=O)OR1, -SO2NR2R3이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -
R2 및 R3는 각각 독립적으로 H, C1-C6 알킬 및 C3-C6 사이클로알킬 중에서 선택되며;R 2 and R 3 are each independently H, C 1 -C 6 Alkyl and C 3 -C 6 Selected from cycloalkyl;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고, 단 B가 -S-인 경우 R은 피리미딘일 수 없으며; B가 -(C2-C7)알킬인 경우 R은 이미다졸일 수 없고;R is H, optionally substituted aryl or optionally substituted heteroaryl, provided that when B is -S-, R cannot be pyrimidine; When B is-(C 2 -C 7 ) alkyl R cannot be imidazole;
R1은 H 또는 (C1-C6)알킬이며;R 1 is H or (C 1 -C 6 ) alkyl;
X는 Cl이고;X is Cl;
단, 일반식 (I)의 화합물은 다이머일 수 없다.However, the compound of general formula (I) cannot be a dimer.
약제학적 조성물은 하기 일반식 (I)의 화합물 및 약제학적으로 허용가능한 담체 또는 부형제를 포함한다:The pharmaceutical composition comprises a compound of formula (I) and a pharmaceutically acceptable carrier or excipient:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며; 단, -(C2-C7)헤테로알킬은 질소 원자, -C(=O)-, -S-, -S(=O)-, -S(=O)2-, -NR1(C=O)-, -(C=O)NR1-, S(=O)2NR1-, -NR1S(=O)2, -0(C=O)NR1-, -NR1(C=O)O-, -0(C=O)O-, -NR1(C=O)NR1-, -(C=O)O-, -0(C=O)-를 함유할 수 없고;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl; Provided that-(C 2 -C 7 ) heteroalkyl is a nitrogen atom, -C (= O)-, -S-, -S (= O)-, -S (= O) 2- , -NR 1 (C = O)-,-(C = O) NR 1- , S (= O) 2 NR 1- , -NR 1 S (= O) 2 , -0 (C = O) NR 1- , -NR 1 ( May contain C═O) O—, —0 (C═O) O—, —NR 1 (C═O) NR 1 —, — (C═O) O—, —0 (C═O) — No;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이며;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -O-C(O)NR2R3, -NR2R3(C=O)OR1, -SO2NR2R3이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -
R2 및 R3는 각각 독립적으로 H, C1-C6 알킬 및 C3-C6 사이클로알킬 중에서 선택되며;R 2 and R 3 are each independently H, C 1 -C 6 Alkyl and C 3 -C 6 Selected from cycloalkyl;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고, 단 B가 -S-인 경우 R은 피리미딘일 수 없으며; B가 -(C2-C7)알킬인 경우 R은 이미다졸일 수 없고;R is H, optionally substituted aryl or optionally substituted heteroaryl, provided that when B is -S-, R cannot be pyrimidine; When B is-(C 2 -C 7 ) alkyl R cannot be imidazole;
R1은 H 또는 (C1-C6)알킬이며;R 1 is H or (C 1 -C 6 ) alkyl;
X는 할로겐이고;X is halogen;
단, 일반식 (I)의 화합물은 다이머일 수 없다. 하나의 구체예에서, 약제학적 조성물은 일반식 (I)의 화합물의 전신적 투여를 위한 경구적인 약제학적 조성물이다.However, the compound of general formula (I) cannot be a dimer. In one embodiment, the pharmaceutical composition is an oral pharmaceutical composition for systemic administration of a compound of formula (I).
일부 구체예로는, E가 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R인 조성물이다. 다른 구체예로는, X가 Cl이고, D가 이소프로필, tert-부틸 또는 사이클로프로필인 조성물이다. 추가의 구체예로는, D가 tert-부틸이고 X가 Cl인 조성물이다. 일부 구체예로는, B가 -(CH2)n이고 n이 1-6이거나, B가 -(C3-C8)사이클로알킬인 조성물이다. 일부 구체예로는 A가 0인 조성물이다. 다른 구체예로는 A가 NH 또는 S인 조성물이다.In some embodiments, E is (C═O) —OR, —0- (C═O) —R, — (C═O) —R, —OR, carboxylic acid bioisotope, — (C═O) -NR 1 R, NR 1- (C═O) —R; - (C 1 -C 7) alkyl, - (C = O) -OR, or - is a (C = O) -NR 1 R composition - (C 1 -C 7) alkyl. In another embodiment, a composition wherein X is Cl and D is isopropyl, tert-butyl or cyclopropyl. In further embodiments are compositions wherein D is tert-butyl and X is Cl. In some embodiments, a composition wherein B is — (CH 2 ) n and n is 1-6 or B is — (C 3 -C 8 ) cycloalkyl. In some embodiments is a composition where A is zero. In another embodiment is a composition wherein A is NH or S.
일부 구체예로는, 포유동물에게 치료학적 유효량의 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물의 조성물을 투여하는 단계를 포함하는, 본원에 개시된 치료 방법이다:In some embodiments, herein comprising administering to a mammal a therapeutically effective amount of a compound of formula (I) or an active metabolite or composition of a pharmaceutically acceptable prodrug, salt or solvate The disclosed methods of treatment are:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며; 단 -(C2-C7)헤테로알킬은 질소 원자, -C(=O)-, -S-, -S(=O)-, -S(=O)2-, -NR1(C=O)-, -(C=O)NR1-, S(=O)2NR1-, -NR1S(=O)2, -0(C=O)NR1-, -NR1(C=O)O-, -0(C=O)O-, -NR1(C=O)NR1-, -(C=O)O-, -0(C=O)-을 함유할 수 없고;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl; Provided that-(C 2 -C 7 ) heteroalkyl is a nitrogen atom, -C (= 0)-, -S-, -S (= 0)-, -S (= 0) 2- , -NR 1 (C = O)-,-(C = O) NR 1- , S (= O) 2 NR 1- , -NR 1 S (= O) 2 , -0 (C = O) NR 1- , -NR 1 (C Cannot contain -O-, -0 (C = O) O-, -NR 1 (C = O) NR 1 -,-(C = O) O-, -0 (C = O)- ;
D는 tert-부틸이며;D is tert-butyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -O-C(O)NR2R3, -NR2R3(C=O)OR1, -SO2NR2R3이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -
R2 및 R3는 각각 독립적으로 H, C1-C6 알킬 및 C3-C6 사이클로알킬 중에서 선택되며;R 2 and R 3 are each independently H, C 1 -C 6 Alkyl and C 3 -C 6 cycloalkyl;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고, 단 B가 -S-인 경우 R은 피리미딘일 수 없고; B가 -(C2-C7)알킬인 경우 R은 이미다졸일 수 없으며;R is H, optionally substituted aryl or optionally substituted heteroaryl, provided that when B is -S-, R cannot be pyrimidine; When B is-(C 2 -C 7 ) alkyl R cannot be imidazole;
R1은 H 또는 (C1-C6)알킬이고;R 1 is H or (C 1 -C 6 ) alkyl;
X는 Cl이며; 단 일반식 (I)의 화합물은 다이머일 수 없다.X is Cl; Provided that the compound of formula (I) may not be a dimer.
하나의 일면으로는, 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물이다:In one aspect, a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
상기 식에서,Where
A는 O이고;A is O;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며; 단 -(C2-C7)헤테로알킬은 질소 원자, -C(=0)-, -S-, -S(=0)-, -S(=0)2-, -NR1(C=O)-, -(C=O)NR1-, S(=O)2NR1-, -NR1S(=O)2, -0(C=O)NR1-, -NR1(C=O)O-, -0(C=O)O-, -NR1(C=O)NR1-, -(C=O)O-, -0(C=O)-을 함유할 수 없고;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl; Provided that-(C 2 -C 7 ) heteroalkyl is a nitrogen atom, -C (= 0)-, -S-, -S (= 0)-, -S (= 0) 2- , -NR 1 (C = O)-,-(C = O) NR 1- , S (= O) 2 NR 1- , -NR 1 S (= O) 2 , -0 (C = O) NR 1- , -NR 1 (C Cannot contain -O-, -0 (C = O) O-, -NR 1 (C = O) NR 1 -,-(C = O) O-, -0 (C = O)- ;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이며;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -O-C(O)NR2R3, -NR2(C=O)OR1 또는 -SO2NR2R3이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -
R2 및 R3는 각각 독립적으로 H, C1-C6 알킬 및 C3-C6 사이클로알킬 중에서 선택되며;R 2 and R 3 are each independently H, C 1 -C 6 Alkyl and C 3 -C 6 cycloalkyl;
R은 H, -(C2-C7)알킬, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고, 단 B가 -S-인 경우 R은 피리미딘일 수 없으며; B가 -(C2-C7)알킬인 경우 R은 이미다졸일 수 없고;R is H,-(C 2 -C 7 ) alkyl, optionally substituted aryl or optionally substituted heteroaryl, provided that when B is -S-, R cannot be pyrimidine; When B is-(C 2 -C 7 ) alkyl R cannot be imidazole;
R1은 H 또는 (C1-C6)알킬이며;R 1 is H or (C 1 -C 6 ) alkyl;
X는 할로겐이다.X is halogen.
일부 구체예로는, B가 -(CH2)n이고 n이 1-6이거나 B가 -(C3-C8)사이클로알킬인 일반식 (I)의 화합물이다. 다른 구체예에서, E는 (C=O)-OR, 카르복시산 생물동배체, -(C=O)-NR1R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이다. 추가의 구체예로는, D가 이소프로필, tert-부틸 또는 사이클로프로필인 일반식 (I)의 화합물이다. 일부 구체예에서, X는 Cl이고, D는 tert-부틸이다.In some embodiments is a compound of Formula (I) wherein B is — (CH 2 ) n and n is 1-6 or B is — (C 3 -C 8 ) cycloalkyl. In another embodiment, E is (C═O) —OR, a carboxylic acid bioisotope, — (C═O) —NR 1 R, — (C 1 -C 7 ) alkyl- (C═O) —OR or — (C 1 -C 7 ) alkyl- (C═O) -NR 1 R. In a further embodiment is a compound of formula (I) wherein D is isopropyl, tert-butyl or cyclopropyl. In some embodiments, X is Cl and D is tert-butyl.
다른 일면으로는, 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물이다:In another embodiment, a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
상기 식에서,Where
A는 NH 또는 S이고;A is NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며; B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -O-C(O)NR2R3, -NR2(C=O)OR1 또는 -SO2NR2R3이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -
R2 및 R3는 각각 독립적으로 H, C1-C6 알킬 및 C3-C6 사이클로알킬 중에서 선택되고;R 2 and R 3 are each independently H, C 1 -C 6 Alkyl and C 3 -C 6 cycloalkyl;
R은 H, -(C2-C7)알킬, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이며;R is H,-(C 2 -C 7 ) alkyl, optionally substituted aryl or optionally substituted heteroaryl;
R1은 H 또는 (C1-C6)알킬이고;R 1 is H or (C 1 -C 6 ) alkyl;
X는 할로겐이다.X is halogen.
일부 구체예로는, B가 -(CH2)n이고 n이 1-6이거나 B가 -(C3-C8)사이클로알킬인 일반식 (I)의 화합물이다. 다른 구체예에서, E는 (C=O)-OR, 카르복시산 생물동배체, -(C=O)-NR1R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이다. 추가의 구체예로는, D가 이소프로필, tert-부틸 또는 사이클로프로필인 일반식 (I)의 화합물이다. 일부 구체예에서, X는 Cl이고, D는 tert-부틸이다.In some embodiments is a compound of Formula (I) wherein B is — (CH 2 ) n and n is 1-6 or B is — (C 3 -C 8 ) cycloalkyl. In another embodiment, E is (C═O) —OR, a carboxylic acid bioisotope, — (C═O) —NR 1 R, — (C 1 -C 7 ) alkyl- (C═O) —OR or — (C 1 -C 7 ) alkyl- (C═O) -NR 1 R. In a further embodiment is a compound of formula (I) wherein D is isopropyl, tert-butyl or cyclopropyl. In some embodiments, X is Cl and D is tert-butyl.
본원에 개시된 방법, 화합물 및 조성물의 다른 목적, 특징 및 이점은 다음의 상세한 설명으로부터 명백해질 것이다. 그러나, 상세한 설명 및 특정의 실시예는 특정의 구체예를 나타내지만 단지 예시로서 제공되는 것으로 이해되어야 한다.Other objects, features and advantages of the methods, compounds and compositions disclosed herein will become apparent from the following detailed description. However, it is to be understood that the description and the specific examples, although indicative of specific embodiments, are provided by way of illustration only.
도 1. 펜레티나이드(HPR)와 비교한 시험 화합물의 용량-반응 관계. 데이터를 통해, 시험 화합물(일반식 (I)과 일치하는 화학 구조를 가짐)이 HPR보다 대략 7배 더 강력하게 RBP4-TTR 상호작용을 방해한다는 것을 알 수 있다(각각 IC5O = 0.1 대 IC5O = 0.7).
도 2. 혈청 레티놀의 HPLC 분석. 마우스를 DMSO 또는 일반식 (I)의 구조를 가진 화합물로 처리하였다. 꼬리 정맥으로부터 전혈을 수집하여 혈청을 준비하였다. 혈청 시료를 HPLC에 의해 분석하였다. DMSO을 제공받은 마우스(패널 A) 및 시험 화합물을 제공받은 마우스(패널 B)에 대한 대표적인 크로마토그래피 추적을 도시하였다. 레티놀 피크 및 그의 흡광도 스펙트럼을 플롯으로 나타내었다.
도 3. 레티놀 및 시험 화합물의 항정 상태 혈청 농도. 일반식 (I)의 구조를 가진 시험 화합물의 일일 용량(20 ㎎/㎏/일, 복강내, DMSO중)을 마우스에 투여하였다. 처리 28 일후, 혈액 시료를 취하고 HPLC에 의한 분석을 위해 혈청을 준비하였다. 시험 화합물(280 nm에서 검출, 점선) 및 레티놀(325 nm에서 검출, 실선)의 존재를 나타내는 대표적인 크로마토그램이 제공되어 있다.
도 4. RBP4의 농도계측식 정량 및 면역탁본법 검출. DMSO(상부 패널, 1-5 레인) 또는 일반식 (I)과 일치하는 구조를 가진 시험 화합물(패널 A, 6-10 레인)로 처리한 마우스의 혈청에서 RBP4의 웨스턴 블롯 검출. 패널 A의 1-5 레인에 도시된 밴드의 픽셀 밀도를 결정하고 평균 픽셀 밀도를 100%로 취하였다. 시험 화합물로 처리한 마우스에서 RBP4의 상대적 수준을 또한 픽셀 농도계측기에 의해 결정하였다. 이들 데이터를 막대그래프로 도시하였다.
도 5. 독성 망막 형광단의 크로마토그래피 분리 및 동정. abca4 널 돌연변이 마우스(BL6/129, 6 개월령)의 아이컵으로부터 지질 가용 성분을 추출하였다. 아이컵 추출액을 온라인 흡광도(실선) 및 형광(점선) 검출과 함께 HPLC에 의해 분석하였다. 지시된 형광단(A2E 전구체 및 A2E)는 연령-일치 야생형 마우스에 존재하지 않았다.
도 6. abca4 돌연변이 마우스에서 RBP4의 유전적 조절: 혈청 레티놀, RBP4 및 독성 망막 형광단에 대한 효과. RBP4의 유전적 감소가 RPE 내에서 레티놀, RBP4 및 독성 망막 형광단의 혈청 수준을 감소시키는데 충분한지를 결정하기 위해, RBP4 및 ABCA4(RBP4+/-, ABCA4+/-)에서 이형접합 돌연변이를 발현하는 마우스 계통을 생산하였다. RBP4+/-, ABCA4+/- 마우스에서 혈청 레티놀 농도는 RBP(RBP4+/+, ABCA4-/-)의 정상 보체를 가진 마우스에 비해 50% 이상까지 감소하였다. 이와 같은 레티놀 감소의 정도는 HPR-처리 RBP4+/+, ABCA4-/- 마우스에서 관찰된 정도에 상당하였다(패널 A). 면역탁본법 분석에 의해 결정된 바와 같이, 혈청 레티놀의 감소는 RBP4의 감소와 직접적으로 상관관계가 있었다. 다양한 마우스 계통에서 RBP4의 웨스턴 블롯 동정을 패널 B에 도시하였다. 조직학적 분석을 또한 수행하였다. RBP4+/+, ABCA4+/- 마우스(패널 C), RBP4+/-, ABCA4+/-(패널 D) 및 RBP4+/+, ABCA4+/+(패널 E)로부터의 조직 절편을 형광 현미경법에 의해 분석하였다. RBP4 및 레티놀의 항정 상태 수준이 낮은 마우스에서 리포푸신 형광단(백색 화살표로 표시됨)이 유의적으로 감소되었음이 본 분석으로부터 명백해졌다.
도 7. 펜레티나이드(HPR)에 대한 시험 화합물의 용량-반응 관계. 데이터는 화학명 3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로헥산카르복시산을 가진 시험 화합물 2 및 화학명 3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로펜탄카르복시산을 가진 시험 화합물 3이 RBP4-TTR 상호작용을 방해하는데 효과적임을 나타낸다(IC50 = 0.25 - 0.70 ㎛).
도 8. 시험 화합물 및 펜레티나이드(HPR)에 대한 시토크롬 P450 억제율 프로파일. 6 개의 시토크롬 P450 동종효소의 패널을 스크리닝하여 시험 화합물(화학명 3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로헥산카르복시산을 가진 시험 화합물 2 및 화학명 3-((2-tert-부틸-4-클로로페녹시)메틸)사이클로펜탄카르복시산을 가진 시험 화합물 3) 및 HPR(본 분석에서 2 μM로 표시)과 관련이 있는 강력한 독성을 분석하였다. 데이터는 시험 화합물에 의해 시토크롬 P450 동종효소가 매우 조금 억제되었음을 나타낸다.
도 9. 시험 화합물로 처리한 후 안내 레티노이드의 정량. ATRP(대조군) 또는 ATRP+SIR-1047을 20 일동안 매일 ABCA4-/- 마우스에 투여하였다(n = 그룹당 3 마리). 최종 투여일에, 100 ㎕ 옥수수유 중 미량의 [3H]ATROL (0.32 pmol, 8 μCi)을 모든 동물에게 투여하였다. 5 시간후에 안구를 적출하였다. 본 방법에 기술된 바와 같이, 각 동물의 한쪽 눈은 레티노이드 분석을 위해 사용하였고, 다른 쪽 눈은 A2E 및 관련 형광단의 분석을 위해 사용하였다. 데이터를 통해 시험 화합물로 처리한 동물에서 [3H]ATROL 흡수의 현저한 감소를 알 수 있었다. 각각의 레티노이드 종의 분석을 통해 시각 발색단 생합성에 대한 전구체 기질(ATRE) 및 A2E 생합성에 대한 즉각적인 전구체(AT-Ox)가 유의적으로 감소되었음을 알 수 있다.
도 10. ABCA4-/- 마우스에서 총 형광단 수준을 감소시키는 시험 화합물의 효과. 도 1(상기)에 기술된 바와 같이 마우스를 처리하였다. 연구의 종료 시점에, 각 동물로부터 수득한 한쪽 안구는 총 형광단 수준을 측정하기 위해 사용하였다. 요약하면, 하나의 전체 안구를 1 ㎖ 인산염 완충 염수(50 mM Na2HPO4, 150 mM NaCl, pH 7.8)에 균질화시켰다. 균질화후, 1 ㎖ 메탄올을 첨가하고 시료를 철저히 혼합하였다. 혼합물을 실온에서 5 분동안 인큐베이션하고 2 ㎖ 헥산으로 두 번 추출하였다. 형광 측정을 위해 추출액을 약 400 ㎕로 농축하였다. 수집된 형광 스펙트럼은 비율 모드로 조작한 Spex Fluorolog-3 분광형광계(뉴저지 에디슨 소재, 조빈 아이본 호리바(Jobin Yvon Horiba))를 사용하여 수득하였다. 시료를 488 nm로 여기시키고 500-700 m에서의 방출을 감시하였다. 데이터를 통해 시험 화합물로 처리한 마우스에서 총 형광단 수준이 크게 감소하였음을 알 수 있다.
도 11. ABCA4-/- 마우스에서 A2E 및 A2E 전구체 A2PE-H2를 감소시키는 시험 화합물의 효과. 도 1(상기)에 기술된 바와 같이 마우스를 처리하였다. 연구의 종료 시점에, 각 동물로부터 수득한 한쪽 안구는 A2E 및 A2PE-H2를 측정하는데 사용되었다. 요약하면, 하나의 전체 안구를 1 ㎖ 인산염 완충 염수(50 mM Na2HPO4, 150 mM NaCl, pH 7.8)에 균질화시켰다. 균질화 이후, 1 ㎖ 메탄올을 첨가하고 시료를 철저히 혼합하였다. 혼합물을 실온에서 5 분동안 인큐베이션하고 2 ㎖ 헥산으로 두 번 추출하였다. 용매를 질소 기류하에 증발시키고, 시료 잔류물을 HPLC로 분석하기 위해 200 ㎕ 이소프로판올(IPA)에 재구성시켰다. 형광단을 1 ㎖/분의 유속으로 인지질 이동상(헥산:IPA:에탄올:25 mM 인산염 완충액:아세트산 485:376:100:37.5:0.275 v:v)을 사용하여 평형화시킨 Zorbax RX-Sil 5-㎛ 컬럼(250 x 4.6-㎜) 상에서 분리하였다. 데이터를 통해 비히클-처리 마우스에 비해 시험 화합물로 처리한 마우스에서 A2E 및 그의 전구체 둘 다를 극적으로 감소시켰음을 알 수 있다.Dose-response relationship of test compound compared to fenretinide (HPR). The data show that the test compound (having a chemical structure consistent with Formula (I)) interferes with RBP4-TTR interaction approximately seven times more strongly than HPR (
HPLC analysis of serum retinol. Mice were treated with compounds having the structure of DMSO or general formula (I). Serum was prepared by collecting whole blood from the tail vein. Serum samples were analyzed by HPLC. Representative chromatographic tracing is shown for mice receiving DMSO (Panel A) and mice receiving test compound (Panel B). Retinol peaks and their absorbance spectra are shown in plots.
Steady state serum concentrations of retinol and test compounds. Mice were administered daily doses (20 mg / kg / day, intraperitoneally, in DMSO) of test compounds having the structure of Formula (I). After 28 days of treatment, blood samples were taken and serum prepared for analysis by HPLC. Representative chromatograms are provided which show the presence of test compound (detection at 280 nm, dashed line) and retinol (detection at 325 nm, solid line).
Figure 4. Concentration quantitation and immunotaxin detection of RBP4. Western blot detection of RBP4 in the serum of mice treated with DMSO (top panel, lanes 1-5) or test compounds having a structure consistent with Formula (I) (Panel A, lanes 6-10). The pixel density of the bands shown in lanes 1-5 of Panel A was determined and the average pixel density was taken as 100%. Relative levels of RBP4 in mice treated with test compounds were also determined by pixel densitometry. These data are shown in bar graphs.
5. Chromatographic separation and identification of toxic retinal fluorophores. Lipid soluble components were extracted from the eyecup of abca4 null mutant mice (BL6 / 129, 6 months old). Eyecup extracts were analyzed by HPLC with on-line absorbance (solid line) and fluorescence (dashed line) detection. The indicated fluorophores (A2E precursor and A2E) were not present in age-matched wild type mice.
6. Genetic regulation of RBP4 in abca4 mutant mice: effects on serum retinol, RBP4 and toxic retinal fluorophores. Mouse strains expressing heterozygous mutations in RBP4 and ABCA4 (RBP4 +/-, ABCA4 +/-) to determine if genetic reduction of RBP4 is sufficient to reduce serum levels of retinol, RBP4 and toxic retinal fluorophore in RPE Produced. Serum retinol concentrations in RBP4 +/-, ABCA4 +/- mice were reduced by at least 50% compared to mice with normal complement of RBP (RBP4 + / +, ABCA4-/-). The extent of this retinol reduction corresponded to that observed in HPR-treated RBP4 + / +, ABCA4-/-mice (Panel A). As determined by immunoassay analysis, the decrease in serum retinol correlated directly with the decrease in RBP4. Western blot identification of RBP4 in various mouse strains is shown in Panel B. Histological analysis was also performed. Tissue sections from RBP4 + / +, ABCA4 +/− mice (panel C), RBP4 +/−, ABCA4 +/− (panel D) and RBP4 + / +, ABCA4 + / + (panel E) were analyzed by fluorescence microscopy. It was evident from this analysis that the lipofuscin fluorophore (indicated by the white arrow) was significantly reduced in mice with low steady state levels of RBP4 and retinol.
Dose-response relationship of test compound for fenretinide (HPR). The data were obtained from
8. Cytochrome P 450 inhibition profile for test compounds and fenretinide (HPR). A panel of six cytochrome P 450 isoenzymes was screened to test
9. Quantification of intraocular retinoids after treatment with test compounds. ATRP (control) or ATRP + SIR-1047 was administered to ABCA4-/-mice daily for 20 days (n = 3 per group). On the last day of administration, traces of [ 3 H] ATROL (0.32 pmol, 8 μCi) in 100 μl corn oil were administered to all animals. After 5 hours, the eye was taken out. As described in this method, one eye of each animal was used for retinoid analysis and the other eye was used for analysis of A2E and related fluorophores. The data showed a significant decrease in [ 3 H] ATROL uptake in animals treated with the test compound. Analysis of each retinoid species reveals a significant reduction in precursor substrate (ATRE) for visual chromophore biosynthesis and immediate precursor (AT-Ox) for A2E biosynthesis.
10. Effect of test compounds to reduce total fluorophore levels in ABCA4-/-mice. Mice were treated as described in FIG. 1 (above). At the end of the study, one eye from each animal was used to measure total fluorophore levels. In summary, one whole eye was homogenized in 1 ml phosphate buffered saline (50 mM Na 2 HPO 4 , 150 mM NaCl, pH 7.8). After homogenization, 1 ml methanol was added and the samples mixed thoroughly. The mixture was incubated at room temperature for 5 minutes and extracted twice with 2 mL hexanes. The extract was concentrated to about 400 μl for fluorescence measurements. The collected fluorescence spectra were obtained using a Spex Fluorolog-3 spectrofluorometer (Jobin Yvon Horiba, Edison, NJ) operated in ratio mode. Samples were excited at 488 nm and monitored at 500-700 m. The data show a significant decrease in total fluorophore levels in mice treated with the test compound.
11. Effect of test compound on reducing A2E and A2E precursor A2PE-H2 in ABCA4-/-mice. Mice were treated as described in FIG. 1 (above). At the end of the study, one eye from each animal was used to measure A2E and A2PE-H2. In summary, one whole eye was homogenized in 1 ml phosphate buffered saline (50 mM Na 2 HPO 4 , 150 mM NaCl, pH 7.8). After homogenization, 1 ml methanol was added and the samples mixed thoroughly. The mixture was incubated at room temperature for 5 minutes and extracted twice with 2 mL hexanes. The solvent was evaporated under a stream of nitrogen and the sample residue was reconstituted in 200 μl isopropanol (IPA) for analysis by HPLC. Zorbax RX-Sil 5-μm equilibrated with phospholipid mobile phase (hexane: IPA: ethanol: 25 mM phosphate buffer: acetic acid 485: 376: 100: 37.5: 0.275 v: v) at a flow rate of 1 ml / min. Separate on column (250 x 4.6-mm). The data show that both A2E and its precursors were dramatically reduced in mice treated with test compounds as compared to vehicle-treated mice.
참고를 위해 본원에 개시된 방법 및 조성물의 구체에 대해 상세히 설명될 것이다. 구체예의 예가 다음의 실시부에 기술되어 있다.Details of the methods and compositions disclosed herein will be described for reference. Examples of embodiments are described in the following embodiments.
흥미롭게도, 일반식 (I) 및 (II)의 화합물은 황반 변성 및 이영양을 포함하나 이들에 한정되지 않는 다양한 유리체망막 질환으로 고통받거나 이들에 걸리기 쉬운 환자들에게 이점을 제공하는데 사용된다. 일반식 (I) 및 (II)의 화합물은 이러한 환자들에게 다음의 이점 중 적어도 하나를 제공한다: 혈청 레티놀 또는 RBP 수준의 감소, 트랜스티레틴 수준의 조절, 드루젠 형성의 감소, 레티놀-레티놀-결합 단백질 복합체 형성의 감소 및 레티놀-결합 단백질-트랜스티레틴 복합체 형성의 감소. 본원에 사용된 RBP는 단백질 RBP4를 말한다.Interestingly, compounds of formulas (I) and (II) are used to provide benefits to patients suffering from or susceptible to various vitreoretinal diseases, including but not limited to macular degeneration and dystrophies. Compounds of Formulas (I) and (II) provide these patients with at least one of the following benefits: reduction in serum retinol or RBP levels, control of transthyretin levels, reduction in drusen formation, retinol-retinol Reduction of binding protein complex formation and reduction of retinol-binding protein-transtyretin complex formation. As used herein, RBP refers to protein RBP4.
습성 형태의 연령 관련 황반 변성에 대한 예방학적 치료법으로서의 일반식 (I) 및 (II)의 화합물의 용도가 또한 포함된다. 또한, 일반식 (I) 및 (II)의 화합물은 습성 형태의 연령 관련 황반 변성에 추가의 치료학적 효과를 제공하는데, 이는 이러한 화합물이 혈관신생 억제 활성을 부가적으로 가지기 때문이다.Also included is the use of the compounds of formulas (I) and (II) as prophylactic treatment for wet form of age related macular degeneration. In addition, compounds of formulas (I) and (II) provide additional therapeutic effects on wet form of age-related macular degeneration because these compounds additionally have angiogenesis inhibitory activity.
시각 사이클Visual cycle
척추동물의 망막은 두 가지 형태의 광수용체 세포인 간상체와 추상체를 가진다. 간상체는 빛이 적은 조건하에서 시각 작용을 담당한다. 추상체는 덜 민감하며, 고도의 일시적 및 공간적 판별력(spatialresolution)을 제공하고 색지각력(color perception)을 제공한다. 일광 조건하에서, 간상체 반응은 포화되어 시각은 전적으로 추상체에 의해 매개된다. 두 형태의 세포 모두 적층된 막형상 원반을 포함하는 외절이라 불리는 구조를 가진다. 시각 전달의 반응은 이들 원반의 표면에서 일어난다. 시각의 제1단계는 옵신-색소분자(로돕신)에 의한 광자 흡수이며, 이는 11-시스에서 올-트랜스로의 발색단의 이성화에 관여한다. 광감수성이 회복가능하기 전에, 생산된 올-트랜스-레티날은 망막에 인접한 세포 단층인 망막 상피세포에서 일어나는 다중-효소 과정에서 11-시스-레티날로 다시 전환되어야 한다.Vertebrate retinas have two types of photoreceptor cells: rods and abstracts. The rod is responsible for visual action under low light conditions. Abstracts are less sensitive and provide a high degree of temporal and spatial resolution and color perception. Under daylight conditions, the rod reaction is saturated so that vision is entirely mediated by the abstract. Both types of cells have a structure called extinction that includes stacked disc disks. The reaction of visual transmission takes place on the surface of these discs. The first stage of vision is photon absorption by opsin-pigment molecules (rhodosin), which is involved in the isomerization of chromophores from 11-cis to all-trans. Before the photosensitivity is recoverable, the produced all-trans-retinal must be converted back to 11-cis-retinal in a multi-enzymatic process that occurs in retinal epithelial cells, a cell monolayer adjacent to the retina.
황반 또는 망막 변성 및 이영양Macular or retinal degeneration and dystrophy
황반 변성(망막 변성이라고도 함)은 망막의 중심 부분인 황반의 퇴화를 포함하는 안질환이다. 황반 변성의 경우 중 대략 85 내지 90%는 "건성(dry)"(위축성 또는 비-혈관신생성) 형태이다. 건성 형태의 황반 변성의 경우, 망막의 퇴화는 황반 아래에 드루젠으로 알려진 작은 황색 침적물의 형성과 관련이 있으며; 또한 RPE내 리포푸신의 축적은 광수용체 변성 및 지도형 위축을 유발시킨다. 이러한 현상은 황반의 박화(thinning) 및 건성화(drying)를 유발한다. 드루젠에 의해 야기된 망막 박화의 위치 및 정도는 중심부 시력 상실 정도와 직접적으로 상관성이 있다. 드루젠으로 덮힌 광수용체 및 망막의 색소층이 변성되면 위축되어 서서히 중심부 시력이 상실된다. 결국, 망막 색소 상피 및 하부 광수용체 세포의 손상은 지도형 위축을 유발한다. 포유동물에게 상기 일반식 (I) 또는 (II)의 구조를 가진 적어도 하나의 화합물을 투여하면 포유동물의 눈에서 광수용체 변성 및/또는 지도형 위축의 형성이 감소되거나 그의 확산이 제한된다. 단지 예로서, 포유동물에게 일반식 (I) 또는 (II)의 화합물의 투여는 포유동물의 눈에서 광수용체 변성 및/또는 지도형 위축을 치료하는데 사용될 수 있다.Macular degeneration (also called retinal degeneration) is an ocular disease that involves the degeneration of the macula, the central part of the retina. Approximately 85 to 90% of cases of macular degeneration are in the "dry" (atrophic or non-angiogenic) form. In dry form of macular degeneration, retinal degeneration is associated with the formation of small yellow deposits known as drusen under the macula; The accumulation of lipofucin in RPE also leads to photoreceptor degeneration and geographic atrophy. This phenomenon causes thinning and drying of the macula. The location and extent of retinal thinning caused by drusen correlates directly with the degree of central vision loss. Degeneration of the photoreceptor covered with drusen and the pigment layer of the retina is atrophy and gradually loses central vision. As a result, damage to the retinal pigment epithelium and lower photoreceptor cells causes lead atrophy. Administering at least one compound having the structure of Formula (I) or (II) to a mammal reduces or limits the diffusion of photoreceptor degeneration and / or geographic atrophy in the mammal's eye. By way of example only, administration of a compound of formula (I) or (II) to a mammal can be used to treat photoreceptor degeneration and / or geographic atrophy in the mammal's eye.
"습성" 형태의 황반 변성의 경우, 새로운 혈관이 형성되어(즉, 혈관신생) 망막 조직, 특히 예리한 중심 시각에 관여하는 망막 부분인 황반 아래에의 혈액 공급을 향상시킨다. 이 새로운 혈관은 손상되기 쉬우며, 때때로 파괴되어 출혈을 일으키고 주위 조직을 손상시킨다. 습성 형태의 황반 변성은 전체 황반 변성의 경우 중 겨우 약 10% 정도로 발생하지만, 황반 변성 관련 실명 원인 중 약 90%를 차지한다. 혈관신생은 급속한 시력 상실 및 경우에 따라 일어날 수 있는 망막조직에의 반흔 형성 및 안내 출혈을 야기할 수 있다. 이러한 반흔 조직 및 출혈 혈액은 시야에 어둡고 왜곡된 영역을 형성하며, 법적 실명 상태에 이르게 하는 경우가 종종 있다. 습성 형태의 황반 변성은 주로 중심 시야의 왜곡으로부터 시작된다. 직선들도 굽어져 보이게 된다. 황반 변성에 걸린 많은 사람은 그들의 시야가 흐리게 보이고 맹점(암점)도 있다고 한다. 혈관 내피 성장 인자 또는 VEGF라 불리는 성장 촉진 단백질은 눈에서 상기와 같은 비정상적인 혈관 성장을 유발하기 위해 표적화되어 왔다. 이러한 결과는 VEGF를 억제하거나 차단하는 실험 약물에 대한 공격적인 연구를 가능하게 하였다. 연구에 따르면, 항-VEGF 제제는 또한 비정상적인 혈관 성장을 차단하고 방지하는데 사용될 수 있는 것으로 나타났다. 이러한 항-VEGF 제제는 VEGF 자극을 중단시키거나 억제하여 혈관이 덜 성장하도록 한다. 이러한 항-VEGF 제제는 혈관형성 억제 또는 망막하에서 혈관 성장을 유도하는 VEGF의 능력 및 혈관 누출을 차단하는데 성공적일 수 있다. 하나의 구체예에서, 포유동물에게 상기 일반식 (I) 또는 (II)의 구조를 가진 적어도 하나의 화합물을 투여하면 포유동물의 눈에서 습성 형태의 연령 관련 황반 변성의 형성이 감소되거나 그의 확산이 제한된다. 단지 예로서, 포유동물에게 일반식 (I) 또는 (II)의 화합물의 투여는 포유동물의 눈에서 습성 형태의 연령 관련 황반 변성을 치료하는데 사용된다. 마찬가지로, 상기 일반식 (I) 또는 (II)의 화합물은 맥락막 혈관신생 및 포유동물 눈의 황반 아래 비정상적인 혈관 형성을 치료하는데 사용된다. 하나의 구체예에서, 이러한 치료학적 이점은 혈청 레티놀 및 안내 레티놀 수준의 저하; 혈관신생 억제 활성 및/또는 지도형 위축의 억제와 같은 다수의 효과로부터 발생한다.In the case of “wet” form of macular degeneration, new blood vessels are formed (ie, angiogenesis) to improve blood supply to the retinal tissue, particularly the macula under which the retina is involved in keen central vision. These new blood vessels are susceptible to damage and are sometimes destroyed, causing bleeding and damaging surrounding tissues. Wet macular degeneration occurs in only about 10% of cases of macular degeneration, but accounts for about 90% of macular degeneration related blindness. Angiogenesis can lead to rapid vision loss and, optionally, scar formation and intraocular bleeding into the retinal tissue. Such scar tissue and bleeding blood form dark, distorted areas of vision and often lead to legal blindness. Macular degeneration in wet form primarily begins with distortion of the central field of view. Straight lines are also bent. Many people with macular degeneration have blurred vision and even blind spots. Growth promoter proteins called vascular endothelial growth factor or VEGF have been targeted to induce such abnormal vascular growth in the eye. These results enable aggressive research into experimental drugs that inhibit or block VEGF. Studies have shown that anti-VEGF agents can also be used to block and prevent abnormal blood vessel growth. These anti-VEGF agents stop or inhibit VEGF stimulation, allowing blood vessels to grow less. Such anti-VEGF agents may be successful in inhibiting angiogenesis or blocking vascular leakage and the ability of VEGF to induce blood vessel growth under the retina. In one embodiment, administering to the mammal at least one compound having the structure of Formula (I) or (II) reduces the formation or diffusion of wet form of age-related macular degeneration in the eye of the mammal. Limited. By way of example only, administration of a compound of formula (I) or (II) to a mammal is used to treat wet form of age related macular degeneration in the eye of a mammal. Likewise, the compounds of formula (I) or (II) are used to treat choroidal neovascularization and abnormal angiogenesis under the macular of the mammalian eye. In one embodiment, these therapeutic benefits include lowering serum retinol and intraocular retinol levels; Resulting from a number of effects, such as angiogenesis inhibitory activity and / or inhibition of directed atrophy.
스타르가르트 질환은 소아기에 발병하여 퇴행성 황반 변성으로 발현하는 황반 이영양이다. 예를 들어, 문헌[Allikmets et al., Science, 277:1805-07 (1997); Lewis et al., Am. J. Hum. Genet, 64:422-34 (1999); Stone et al., Nature Genetics, 20:328-29 (1998); Allikmets, Am. J. Hum. Gen., 67:793-799 (2000); Klevering, et al., Ophthalmology, 111:546-553 (2004)]을 참조할 수 있다. 스타르가르트 질환은 임상적으로 중심 시력의 점진적인 상실 및 황반을 덮는 RPE의 점진적인 위축을 특징으로 한다. 림 단백질(RmP, Rim Protein)에 대한 인간 ABCA4 유전자의 돌연변이가 스타르가르트 질환에 관여한다. 질환 초기의 경우, 환자는 암순응에서 지연된 모습을 보이나 간상체 기능에서는 정상적인 모습을 보인다. 조직학적으로, 스타르가르트 질환은 RPE 세포내 리포푸신 색소 과립의 침착과 연관이 있다.Stargardt's disease is macular dystrophies that occur in childhood and manifest as degenerative macular degeneration. See, eg, Allikmets et al., Science, 277: 1805-07 (1997); Lewis et al., Am. J. Hum. Genet, 64: 422-34 (1999); Stone et al., Nature Genetics, 20: 328-29 (1998); Allikmets, Am. J. Hum. Gen., 67: 793-799 (2000); Klevering, et al., Ophthalmology, 111: 546-553 (2004). Stargardt's disease is characterized by a gradual loss of central vision clinically and by progressive atrophy of the RPE covering the macula. Mutations in the human ABCA4 gene for Rim Protein (RmP) are involved in Stargardt's disease. In the early stages of the disease, the patient is delayed in cancer adaptation but normal in rod function. Histologically, Stargardt's disease is associated with the deposition of lipofuscin pigment granules in RPE cells.
AMD에서의 ABCA4 돌연변이의 유병률은 아직 불명확하지만, ABCA4에서의 돌연변이가 또한 퇴행성 색소성 망막염[참조예, 문헌(Cremers et al., Hum. Mol. Genet., 7:355-62 (1998))], 퇴행성 추상체-간상체 이영양[참조예, 상동] 및 비삼출성 연령 관련 황반 변성[참조예, 문헌(Allikmetset al., Science, 277:1805-07 (1997)); 문헌(Lewis et al., Am. J. Hum. Genet., 64:422-34 (1999))]에 관여하고 있다. 문헌[Stone et al., Nature Genetics, 20:328-29 (1998); Allikmets, Am. J. Hum. Gen., 67:793-799 (2000); Klevering, et al., Ophthalmology, 111:546-553 (2004)]을 참조할 수 있다. 이들 질환은 스타르가르트 질환과 마찬가지로 간상체의 암순응 지연과 연관이 있다. 문헌[Steinmetz et al., Brit. J. Ophthalm., 77:549-54 (1993)]을 참조할 수 있다. 또한, RPE 세포내 리포푸신 침착은 주로 AMD[문헌(Kliffenet al., Microsc. Res. Tech., 36:10622(1997))]을 참조할 수 있다] 및 일부 색소성 망막염의 경우[문헌(Bergsmaet al., Nature, 265:6267(1977))을 참조할 수 있다]에서 나타난다. 또한, 상염색체 우성 형태의 스타르가르트 질환은 ELOV4 유전자의 돌연변이에 의해 야기된다. 문헌[Karan, et al., Proc. Natl. Acad. Sci.(2005)]을 참조할 수 있다.The prevalence of ABCA4 mutations in AMD is still unclear, but mutations in ABCA4 are also degenerative pigment retinitis (see, eg, Cremers et al., Hum. Mol. Genet., 7: 355-62 (1998)). , Degenerative abstract-interlaced dystrophies [Reference, Homologous] and non-exudative age-related macular degeneration [Reference, Allikmetset al., Science, 277: 1805-07 (1997)); Lewis et al., Am. J. Hum. Genet., 64: 422-34 (1999). Stone et al., Nature Genetics, 20: 328-29 (1998); Allikmets, Am. J. Hum. Gen., 67: 793-799 (2000); Klevering, et al., Ophthalmology, 111: 546-553 (2004). These diseases, like Stargard's disease, are associated with delayed adaptation of rods. See Steinmetz et al., Brit. J. Ophthalm., 77: 549-54 (1993). In addition, lipofuscin deposition in RPE cells is mainly referred to AMD (Kliffenet al., Microsc. Res. Tech., 36: 10622 (1997)) and for some pigmented retinitis (Bergsmaet). al., Nature, 265: 6267 (1977). In addition, an autosomal dominant form of Stargardt disease is caused by mutations in the ELOV4 gene. Karan, et al., Proc. Natl. Acad. Sci. (2005).
또한, 통상적으로는 조기 발병 또는 유년성 황반 변성으로서 알려진 어린이, 청소년 또는 성인에 영향을 미치는 몇 가지 형태의 황반 변성이 존재한다. 이들 형태의 대부분은 유전적이며, 변성 대신 황반 이영양으로 보여진다. 황반 이영양의 일부 예로는 스타르가르트 질환뿐만 아니라 추상체-간상체 이영양, 각막 이영양, 푹스(Fuch's) 이영양, 소르비(Sorsby's) 황반 이영양, 베스트 질환(Best Disease) 및 유년성 망막층간분리가 포함된다.There are also several forms of macular degeneration that affect children, adolescents, or adults commonly known as early onset or juvenile macular degeneration. Most of these forms are genetic and appear to be macular dystrophies instead of degeneration. Some examples of macular dystrophies include star-gardert disease, as well as abstract-spinal dystrophies, corneal dystrophies, Fuch's dystrophies, Sorsby's macular dystrophies, Best Disease and childhood. Interretinal separation.
비타민 A 수준의 조절Regulation of vitamin A levels
비타민 A(올-트랜스 레티놀)는 생체내에서 합성될 수 없는 중요한 세포 영양분이므로 음식을 통하여 공급받아야 한다. 비타민 A라는 명칭은 일반명으로서, 레티놀의 결합 활성을 비롯한 생물학적 활성을 가지는 임의의 화합물에 붙여질 수 있다. 레티놀 1 당량(RE)은 1 ㎍의 올-트랜스 레티놀(3.33 IU) 또는 6 ㎍의 베타-카로틴(10 IU)의 특이적 생물 활성을 의미한다. 베타-카로틴, 레티놀 및 레티날(비타민 A 알데히드) 모두 효과적이고 확실한 비타민 A 활성을 갖는다. 이러한 화합물들은 각각 식물성 전구체 분자인 카로틴(카로티노이드라고 알려진 분자군의 일원)으로부터 유래한다. 각각 알데히드 말단부에 연결되어 있는 레티놀 분자 2 개로 이루어진 베타-카로틴은 또한 비타민 A의 프로비타민형이라고도 한다.Vitamin A (all-trans retinol) is an important cellular nutrient that cannot be synthesized in vivo and must be obtained from food. The name vitamin A is a generic name and can be attached to any compound having biological activity, including the binding activity of retinol. One equivalent of retinol (RE) refers to the specific biological activity of 1 μg of all-trans retinol (3.33 IU) or 6 μg of beta-carotene (10 IU). Beta-carotene, retinol and retinal (vitamin A aldehyde) all have effective and robust vitamin A activity. Each of these compounds is derived from carotene, a member of the molecular family known as carotenoids, which are plant precursor molecules. Beta-carotene, which consists of two retinol molecules, each linked to the aldehyde end, is also referred to as the provitamin form of vitamin A.
섭취된 β-카로틴은 장내 루멘에서 β-카로틴 다이옥시게나제(β-carotene dioxygenase)에 의해 절단되어 레티날로 된다. 레티날은 레틴알데히드 환원효소(NADPH 필요효소)에 의해 장내에서 레티놀로 환원된 후 팔미트산으로 에스테르화된다.Ingested β-carotene is cleaved by β-carotene dioxygenase in the intestinal lumen to be retinal. Retinal is reduced to retinol in the intestine by retinaldehyde reductase (NADPH required enzyme) and then esterified with palmitic acid.
소화된 후, 음식물 중의 레티놀은 지질 응집체가 결합되어 있는 간으로 운반된다. 문헌[Bellovino et al., Mol. Aspects Med., 24:411-20 (2003)]을 참조할 수 있다. 일단 간으로 운반되면 레티놀은 레티놀 결합 단백질(RBP)과 복합체를 형성한 다음 혈류로 분비된다. 레티놀-RBP holo-단백질은 간 외부의 표적 조직, 예를 들어 눈으로 운반되기 전에 트랜스티레틴(TTR)과 결합하여야 한다[Zanotti and Berni, Vitam. Horm., 69:271-95 (2004)]. 이것이 바로 오랜 기간 동안 혈류내에 레티놀이 잔류할 수 있도록 만들어 주는 2 차 복합체이다. TTR과 결합하면 간세포로부터 RBP가 방출되는 것을 촉진하게 되고, 그 결과 RBP-레티놀 복합체가 신장에 의해 여과되는 것을 막을 수 있다. 레티놀-RBP-TTR 복합체는 레티놀을 흡수하여 이를 다양한 세포내 과정에 이용하는 표적 조직으로 운반된다. RBP-TTR 복합체에 의해 혈류를 통하여 레티놀이 세포로 운반되는 과정은 세포 및 조직이 레티놀을 필요로 하는 주경로이다.After digestion, retinol in the food is transported to the liver where the lipid aggregates are bound. Belovino et al., Mol. Aspects Med., 24: 411-20 (2003). Once transported to the liver, retinol complexes with the retinol binding protein (RBP) and is then secreted into the bloodstream. Retinol-RBP holo-protein must bind to transthyretin (TTR) before being transported to target tissue outside the liver, such as the eye [Zanotti and Berni, Vitam. Horm., 69: 271-95 (2004). This is a secondary complex that allows retinol to remain in the bloodstream for a long time. Binding to TTR promotes the release of RBP from hepatocytes, which prevents the RBP-retinol complex from being filtered by the kidneys. The retinol-RBP-TTR complex is delivered to target tissues that absorb retinol and use it for various intracellular processes. The process of transporting retinol cells through the bloodstream by the RBP-TTR complex is the main pathway where cells and tissues require retinol.
복합체화된 레티놀-RBP-TTR 형태로부터 세포로의 레티놀 흡수는 표적 세포상에 존재하는 세포 수용체에 RBP가 결합함으로써 발생한다. 이러한 상호작용으로 인하여 RBP-수용체 복합체의 내포작용이 유발되고, 그 결과 이 복합체로부터 레티놀이 방출되거나 세포내 레티놀 결합 단백질(CRBP)과 레티놀이 결합하게 되고, 그 결과 세포에 의해 apoRBP가 혈장으로 방출된다. 다른 경로는, 레티놀이 세포내에 도입되는 대안적 메카니즘, 예를 들어 레티놀 만이 세포내에 흡수되는 대안적 메카니즘에 의한 것으로 생각된다. 참고를 위해 문헌[Blomhoff (1994)]을 참조할 수 있다.Retinol uptake into cells from the complexed retinol-RBP-TTR form occurs by binding of RBP to cellular receptors present on target cells. This interaction triggers the inclusion of the RBP-receptor complex, which results in retinol release from the complex or retinol binding to intracellular retinol binding protein (CRBP), which results in the release of apoRBP into the plasma by the cell. do. Another route is believed to be due to an alternative mechanism in which retinol is introduced into the cell, for example, an alternative mechanism in which only retinol is absorbed into the cell. See Blomhoff (1994) for reference.
본원에 기술된 방법, 화합물 및 조성물은 포유동물 대상에서 비타민 A의 수준을 조절하는데에 유용하다. 특히, 비타민 A의 수준은 포유동물에서 레티놀 결합 단백질(RBP) 및 트랜스티레틴(TTR)의 이용가능성 또는 활성을 조절함으로써 조절될 수 있다. 본원에 기술된 방법, 화합물 및 조성물은 포유동물 대상에서 RBP 및 TTR 수준 또는 활성을 조절하고, 그 결과 비타민 A의 수준을 조절한다. 대상에서 비타민 A의 수준이 증가하거나 감소하면, 표적 기관 및 조직 내에서의 레티놀 이용가능성에 영향을 미칠 수 있다. 그러므로, 레티놀 및 레티놀 유도체의 이용가능성을 조절하는 수단을 제공함으로써 표적 기관 및 조직 내에 레티놀 또는 레티놀 유도체가 국소적으로 농축되지 않거나 과량으로 농축되어 유발되는 질환의 병상을 조절할 수 있다. 또한, 본원에 기술된 치료학적 방법은 과다레티놀혈증의 치료에 사용되는데, 여기서 혈청 레티놀 수준의 과잉은 유리체망막 질환 또는 유리체망막 질환관 관련된 증상(예를 들어, 리포푸신 또는 드루젠의 형성)을 유발한다.The methods, compounds and compositions described herein are useful for modulating levels of vitamin A in mammalian subjects. In particular, the level of vitamin A can be regulated by modulating the availability or activity of retinol binding protein (RBP) and transthyretin (TTR) in mammals. The methods, compounds and compositions described herein modulate RBP and TTR levels or activity in mammalian subjects, and as a result, modulate levels of vitamin A. Increasing or decreasing the levels of vitamin A in a subject can affect the availability of retinol in target organs and tissues. Therefore, by providing a means of regulating the availability of retinol and retinol derivatives, it is possible to control the pathology of the disease caused by local or non-enriched retinol or retinol derivatives in target organs and tissues. In addition, the therapeutic methods described herein are used for the treatment of hyperretinolemia, where excess serum retinol levels are associated with symptoms related to vitreoretinal disease or vitreoretinal disease (eg, the formation of lipofucin or drusen). cause.
예를 들어, 리포푸신의 주요 형광단인 A2E는, 시각 사이클 레티노이드인 올-트랜스-레틴알데히드, A2E 전구체의 과잉 생산으로 인해, 황반 또는 망막 변성 또는 이영양, 예를 들어 연령 관련 황반 변성 및 스타르가르트 질환의 경우에 형성된다. 그러므로, 망막의 비타민 A와 올-트랜스 레틴알데히드가 감소하면 A2E 및 리포푸신 축적의 감소 및 연령 관련 황반 변성의 치료에 유리할 것이다.For example, A2E, the main fluorophore of lipofuscin, is due to overproduction of the visual cycle retinoid all-trans-retinaldehyde, A2E precursor, macular or retinal degeneration or dystrophies, eg age related macular degeneration and star It is formed in the case of Legard disease. Therefore, the reduction of vitamin A and all-trans retinaldehyde in the retina will be advantageous for the reduction of A2E and lipofucin accumulation and for the treatment of age-related macular degeneration.
따라서, apoRBP와 레티놀의 결합 또는 holo-RBP(RBP + 레티놀)와 그의 수송 단백질 TTR의 결합을 방해하거나 RBP 및 TTR의 신장 배설량을 증가시킴으로써 세포로의 레티놀 전달을 억제하는 조절자(예를 들어, 일반식 (I) 및 (II)의 화합물)는 혈청 비타민 A 수준 및 눈과 같은 표적 조직내 레티놀 및 그의 유도체의 축적을 감소시키는데 유용할 것이다.Thus, modulators that inhibit retinol delivery to cells by disrupting the binding of apoRBP and retinol or the binding of holo-RBP (RBP + retinol) and its transport protein TTR or by increasing the kidney excretion of RBP and TTR (eg, Compounds of Formulas (I) and (II)) will be useful for reducing serum vitamin A levels and accumulation of retinol and derivatives thereof in target tissues such as the eye.
유사하게, 레티놀 수송 단백질, 레티놀 결합 단백질(RBP) 및 트랜스티레틴(TTR)의 이용가능성에 영향을 주는 조절자는 혈청 비타민 A 수준, 및 눈과 같은 표적 조직내 레티놀과 그의 유도체의 축적 및 신체적 징후(physical manifestation)를 감소시키는데 유용할 것이다. 예를 들어, TTR은 드루젠 구성물의 성분으로서, 이는 곧 TTR이 연령 관련 황반 변성에 직접 관여함을 시사하는 것이다[Mullins, RF, FASEB J. 14:835-846 (2000); Pfeffer BA, et al., Molecular Vision 10:23-30 (2004)].Similarly, modulators affecting the availability of retinol transport proteins, retinol binding proteins (RBPs) and transthyretin (TTR) may include serum vitamin A levels and accumulation and physical signs of retinol and its derivatives in target tissues such as the eye. It may be useful to reduce physical manifestation. For example, TTR is a component of the drusen construct, suggesting that TTR is directly involved in age-related macular degeneration [Mullins, RF, FASEB J. 14: 835-846 (2000); Pfeffer BA, et al., Molecular Vision 10: 23-30 (2004).
포유동물에서의 RBP 및/또는 TTR 수준 또는 활성의 조절과 동일한 접근법을 통해, 대사 장애, 이를 테면 I형 또는 II형 당뇨병(비만 및/또는 비비만), IIH, 골 관련 장애, 이를 테면 골형성과다증, 단백질 오접힘(misfolding) 및 응집 질환, 이를 테면 전신성 아밀로이드증 및 알츠하이머 질환, 및 알스트롬-할그렌 증후군의 치료에서의 용도를 발견할 것으로 기대된다.Through the same approach as regulating RBP and / or TTR levels or activity in mammals, metabolic disorders such as type I or type II diabetes (obesity and / or obesity), IIH, bone related disorders such as bone formation It is expected to find use in the treatment of hyperplasia, protein misfolding and aggregation disorders, such as systemic amyloidosis and Alzheimer's disease, and Alstrom-Halgren syndrome.
따라서, 본원에 기술된 방법, 화합물 및 조성물 중 하나의 구체예는 포유동물에게 일반식 (I) 또는 일반식 (II)의 화합물 중 적어도 하나의 치료학적 유효량을 투여함으로써 포유동물에서 RBP 또는 TTR 수준 또는 활성을 조절하기 위해 제공된다.Thus, one embodiment of the methods, compounds and compositions described herein provides RBP or TTR levels in a mammal by administering to the mammal a therapeutically effective amount of at least one of the compounds of Formula (I) or Formula (II). Or to modulate activity.
레티놀 결합 단백질(Retinol binding protein ( RBPRBP ) 및 트랜스티레틴() And transthyretin ( TTRTTR ))
레티놀 결합 단백질 RBP는 단일의 폴리펩티드 사슬로 이루어진 것으로서, 분자량은 약 21 kD이다. RBP는 클론화 및 서열화되어, 그 결과 그의 아미노산 서열은 결정되어 있다[Colantuni et al., Nuc. Acids Res., 11:7769-7776 (1983)]. RBP의 3 차원 구조를 통하여, 지용성 비타민인 레티놀에 결합하여 이를 보호하도록 디자인된 이의 특화된 소수성 포켓을 밝혀내었다[Newcomer et al., EMBO J., 3:1451-1454 (1984)]. 시험관내 실험에서, 배양된 간세포는 RBP를 합성하여 분비한다는 사실을 알 수 있었다[Blaner, W.S., Endocrine Rev., 10:308-316 (1989)]. 후속 실험에서, 다수의 세포가 RBP의 mRNA를 함유한다는 사실이 입증되었는데, 이는 체내 여러 곳에서 RBP가 합성된다는 사실을 시사하는 것이다. 문헌[Blaner (1989)]을 참조할 수 있다. 간에 의해 분비되는 대부분의 RBP는 레티놀을 1:1의 몰비로 함유하며, 정상적으로 RBP가 분비되기 위해서는 레티놀과 RBP가 결합해야 한다.The retinol binding protein RBP consists of a single polypeptide chain and has a molecular weight of about 21 kD. RBP is cloned and sequenced, as a result of which the amino acid sequence is determined [Colantuni et al., Nuc. Acids Res., 11: 7769-7776 (1983). Through the three-dimensional structure of RBP, its specialized hydrophobic pockets designed to bind and protect the fat-soluble vitamin retinol were identified (Newcomer et al., EMBO J., 3: 1451-1454 (1984)). In in vitro experiments, it was found that cultured hepatocytes synthesize and secrete RBP (Blaner, W.S., Endocrine Rev., 10: 308-316 (1989)). In subsequent experiments, it was demonstrated that many cells contain mRNA of RBP, suggesting that RBP is synthesized in various places in the body. See Blancer (1989). Most of the RBP secreted by the liver contains retinol in a molar ratio of 1: 1. In order for RBP to be secreted normally, retinol and RBP must be combined.
세포내에서, RBP는 RBP가 고농도로 발견되는 곳인 소포체에 존재하는 레티놀과 견고하게 결합한다. 레티놀이 RBP에 결합하면, 소포체로부터 골지 복합체로 레티놀-RBP가 전위되기 시작하며, 이에 따라 세포로부터 레티놀-RBP가 분비된다. 간세포로부터 분비되는 RBP는 또한 간세포로부터 레티놀-RBP가 혈장내에 직접 분비되는 곳인 성세포(stellate cell)로 레티놀이 운반되는 것을 돕는다.In cells, RBP binds firmly to retinol present in the endoplasmic reticulum, where RBP is found in high concentrations. When retinol binds to RBP, retinol-RBP begins to be translocated from the endoplasmic reticulum to the Golgi complex, thereby secreting retinol-RBP from the cells. RBP secreted from hepatocytes also helps transport retinol from hepatocytes to stellate cells, where retinol-RBP is directly secreted into the plasma.
혈장내에서, 혈장 RBP의 약 95%는 트랜스티레틴(TTR)과 1:1의 몰비로 결합하는데, 여기서 혈장 비타민 A의 거의 대부분은 RBP에 결합되어 있다. TTR은 분자량이 54,980 달톤인 4 개의 동일한 서브유닛으로 이루어져 있으며, 널리 특징화된 혈장 단백질이다. X-선 회절법에 의해 추정되는 완전 3 차원 구조를 통하여, 이 단백질은 사면체 형태로 배열된 확장된 β-시트 구조를 가짐을 알 수 있다[Blake et al., J. Mol. Biol., 121:339-356 (1978)]. 2 개의 티록신 결합 위치가 존재하는 4 량체 중심부에는 통로가 존재한다. 그러나, 음의 협동성(negative cooperativity)으로 인하여, 하나의 티록신 분자만이 TTR에 정상적으로 결합하고 있는 것으로 파악된다. TTR과 RBP-레티놀의 복합체 형성 과정은 레티놀이 사구체를 통해 여과되는 것을 줄여 주어, 혈장내 레티놀과 RBP의 반감기를 약 3배 정도 증가시키는 것으로 파악된다.In plasma, about 95% of plasma RBP binds to transthyretin (TTR) in a molar ratio of 1: 1, where almost all of the plasma vitamin A is bound to RBP. TTR consists of four identical subunits with a molecular weight of 54,980 Daltons and is a well characterized plasma protein. Through the full three-dimensional structure estimated by X-ray diffraction, it can be seen that the protein has an extended β-sheet structure arranged in tetrahedral form [Blake et al., J. Mol. Biol., 121: 339-356 (1978). There is a passage in the center of the tetramer where two thyroxine binding sites exist. However, due to negative cooperativity, it is understood that only one thyroxine molecule normally binds to TTR. The complexation process of TTR and RBP-retinol reduces the filtering of retinol through glomeruli, increasing the half-life of retinol and RBP in plasma by about three times.
대상에서 On target RBPRBP 또는 or TTRTTR 결합 또는 제거율의 조절 Control of binding or removal rate
RBP에 결합한 레티놀은 눈으로 전달되기 위하여 혈류로 수송되기 전에, TTR과 복합체를 형성해야 한다. 이와 같은 2 차 복합체를 형성함으로써 레티놀은 오랫 동안 혈류내에 잔류할 수 있게 된다. TTR이 없으면, 레티놀-RBP 복합체는 소변으로 신속하게 배출된다. 이와 유사하게, RBP가 없으면, 혈류내 레티놀 운반량과 세포에의한 흡수량은 줄어들 것이다.Retinol bound to RBP must complex with TTR before being transported into the bloodstream for delivery to the eye. By forming such secondary complexes, retinol can remain in the bloodstream for a long time. Without TTR, the retinol-RBP complex is rapidly excreted in the urine. Similarly, without RBP, the retinol transport in the bloodstream and the uptake by cells will be reduced.
따라서, 본 발명에 기술된 또 다른 구체예는 RBP 또는 TTR 결합 특성 또는 제거율을 조절함으로써, 혈류내 RBP 또는 TTR이 레티놀 또는 레티놀-RBP와 복합체를 형성하는 이용가능성을 조절하는 것이다. 상기 언급된 바와 같이, TTR이 RBP holo-단백질에 결합하면, RBP와 레티놀의 제거율은 줄어든다. 따라서, RBP 또는 TTR의 이용가능성 또는 활성을 조절함으로써, 레티놀 수준이 또한 이를 필요로 하는 대상에서 조절될 것이다.Thus, another embodiment described herein is to modulate the availability of RBP or TTR in the blood stream to complex with retinol or retinol-RBP by modulating RBP or TTR binding properties or clearance. As mentioned above, when TTR binds to RBP holo-protein, the removal rate of RBP and retinol is reduced. Thus, by modulating the availability or activity of RBP or TTR, retinol levels will also be regulated in subjects in need thereof.
예를 들어, 레티놀과 RBP의 결합에 대한 길항제가 본원에 기술된 방법, 화합물 및 조성물에 사용된다. 레티놀과 RBP의 결합에 대한 길항제로는 레티놀과 RBP의 결합과 경쟁하는 일반식 (I) 또는 (II)의 화합물이 포함된다.For example, antagonists for the binding of retinol to RBP are used in the methods, compounds and compositions described herein. Antagonists for the binding of retinol to RBP include compounds of general formula (I) or (II) that compete with the binding of retinol and RBP.
본원에 언급된 바와 같이, 레티놀과 RBP의 결합을 조절하는 하나의 수단은 일반식 (I) 또는 (II)의 화합물과 경쟁적으로 결합하는 것이다. 따라서, 본원에 기술된 방법 및 조성물의 하나의 구체예는 RBP 수준 또는 활성을 조절하는 하기 일반식 (I)의 구조를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 통해 RBP 수준 또는 활성을 저하시킨다:As mentioned herein, one means of regulating the binding of retinol to RBP is to competitively bind a compound of formula (I) or (II). Thus, one embodiment of the methods and compositions described herein is a compound having a structure of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvent thereof that modulates RBP levels or activity Decreases RBP levels or activity through cargo:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl or optionally substituted heteroaryl;
X는 할로겐이다.X is halogen.
본원에 기술된 방법 및 조성물의 또 다른 구체예는 RBP 수준 또는 활성을 조절하는 하기 일반식 (II)의 구조를 가진 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 통해 RBP 수준 또는 활성을 저하시킨다:Another embodiment of the methods and compositions described herein comprises a compound having a structure of formula (II) below or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof that modulates RBP levels or activity. Decreases RBP levels or activity through:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (O = C) -R, - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H 또는 이며;R is H or Is;
G는 -OR1, -(C1-C6)알킬, -(C1-C6)알킬-OR1, 할로겐, -CO2R1, -(C1-C6)알킬-CO2R1, NHR1, -(C1-C6)알킬-NHR1, -(C=O)NHR1, -(C1-C6)알킬-(C=O)NHR1, -NHR1(C=O)R1, -(C1-C6)알킬-NHR1(C=O)R1이고;G is -OR 1 ,-(C 1 -C 6 ) alkyl,-(C 1 -C 6 ) alkyl-OR 1 , halogen, -CO 2 R 1 ,-(C 1 -C 6 ) alkyl-CO 2 R 1 , NHR 1 ,-(C 1 -C 6 ) alkyl-NHR 1 ,-(C = O) NHR 1 ,-(C 1 -C 6 ) alkyl- (C = O) NHR 1 , -NHR 1 (C ═O) R 1 , — (C 1 -C 6 ) alkyl-NHR 1 (C═O) R 1 ;
R1은 H 또는 (C1-C6)알킬이다.R 1 is H or (C 1 -C 6 ) alkyl.
조절자 활성의 검출Detection of Modulator Activity
일부 구체예에서, 본원에 기술된 화합물 및 조성물은 또한 통상의 수단을 통한 RBP 또는 TTR 이용가능성의 혼란을 검출하기 위한 분석에 사용될 수 있다. 예를 들어, 대상을 본원에 기술된 화합물 또는 조성물 중 임의의 것으로 처리하고, 통상의 분석 기술을 사용하여 RBP 또는 TTR 수준을 정량할 수 있다. 문헌[Sundaram, M., et al., Biochem. J. 362:265-271 (2002)]을 참조할 수 있다. 예를 들어, 전형적인 비경쟁적 샌드위치 분석법(sandwich assay)으로는 본원에 참고로 포함되는 미국 특허 제4,486,530호에 개시된 분석법이 있다. 이 방법에서, 샌드위치복합체, 예를 들어 면역 복합체는 분석 배지(assay medium)에서 형성된다. 이 복합체는 분석 대상물인 제1항체, 또는 분석 대상물과 제2항체에 결합하는 결합원(binding member), 또는 분석 대상물 또는 분석대상물과 제1항체의 복합체에 결합하는 결합원, 또는 결합원을 포함한다. 이어, 샌드위치 복합체가 검출되는데, 이는 시료 중 분석 대상물의 존재 및/또는 그의 양과 관련이 있다. 상기 샌드위치 복합체는 표지 복합체의 존재로 인해 검출되는데, 여기서 상기 제1항체와 제2항체 중 어느 하나 또는 둘 다, 또는 결합원은 표지 또는 표지와 결합할 수 있는 치환기를 함유한다. 예를 들어, RBP 또는 TTR 제거율의 조절을 검출하기 위한 시료는 혈장, 혈액, 대변, 조직, 점액, 눈물, 타액 또는 소변일 수 있다. 이러한 접근법에 대한 더욱 상세한 설명에 대해서는 미국 특허 제29,169호 및 제4,474,878호를 참조할 수 있으며, 상기 문헌의 관련 개시 내용은 본원에 참고로 포함된다.In some embodiments, the compounds and compositions described herein can also be used in assays to detect disruptions in RBP or TTR availability via conventional means. For example, a subject can be treated with any of the compounds or compositions described herein, and conventional assay techniques can be used to quantify RBP or TTR levels. See Sundaram, M., et al., Biochem. J. 362: 265-271 (2002). For example, typical noncompetitive sandwich assays include those disclosed in US Pat. No. 4,486,530, which is incorporated herein by reference. In this method, a sandwich complex, eg an immune complex, is formed in an assay medium. The complex includes a binding member that binds to the first antibody, or analyte, and the second antibody, or a binding agent that binds to the complex of the analyte or analyte and the first antibody, or a binding agent. do. A sandwich complex is then detected, which is related to the presence and / or amount of the analyte in the sample. The sandwich complex is detected due to the presence of a label complex, wherein either or both of the first and second antibodies, or binding agents, contain a label or a substituent capable of binding to the label. For example, a sample for detecting control of RBP or TTR clearance may be plasma, blood, stool, tissue, mucus, tears, saliva or urine. For a more detailed description of this approach, see US Pat. Nos. 29,169 and 4,474,878, the disclosures of which are incorporated herein by reference.
상기 샌드위치 측정법의 변형법에서, 적당한 매질 중의 시료는 분석 대상물에 대한 표지된 항체 또는 결합원과 접촉되고 일정 시간 동안 인큐베이션된다. 이어, 상기 매질은 분석 대상물에 대한 제2항체 또는 결합원이 결합되어 있는 지지체와 접촉된다. 인큐베이션 처리 기간후, 상기 지지체를 매질로부터 분리하여 세척함으로써 미결합 시약을 제거한다. 상기 지지체 또는 매질에 표지가 존재하는지 여부를 조사하는데, 이때 표지가 존재함은 분석 대상물의 존재 또는 그의 양과 관련이 있다. 이러한 접근법에 대한 더욱 상세한 설명에 대해서는 미국 특허 제4,098,876 호를 참조할 수 있으며, 상기 문헌의 관련 개시 내용은 본원에 참고로 포함된다.In a variation of the sandwich assay, a sample in a suitable medium is contacted with a labeled antibody or binding agent for the analyte and incubated for a period of time. The medium is then contacted with a support to which the second antibody or binding source for the analyte is bound. After the incubation period, the unbound reagent is removed by washing the support off the medium. Investigate whether a label is present on the support or medium, wherein the presence of the label is related to the presence or amount of the analyte. For a more detailed description of this approach, see US Pat. No. 4,098,876, the relevant disclosure of which is incorporated herein by reference.
일부 구체예에서, 본원에 기술된 조절자는 또한 RBP 또는 TTR 활성의 변동율을 검출하기 위한 시험관내 분석에 사용될 수 있다. 예를 들어, 조절자는 RBP, TTR 및 레티놀을 포함하는 시료에 첨가된다. 성분, 예를 들어 RBP, TTR, 레티놀 또는 조절자를 표지화하여 복합체 형성의 붕괴 여부를 검출할 수 있다. 복합체 형성 및 후속의 복합체 파괴 여부는 통상의 수단, 예를 들어 상술한 바와 같은 샌드위치 분석법을 통하여 검출 및/또는 측정될 수 있다. 또한, 다른 검출 시스템, 예를 들어 RBP-TTR-레티놀 복합체 형성에 관한 FRET 검출법도 RBP 또는 TTR 결합의 조절자를 검출하는데 사용될 수 있다. 본원에 참고로 포함되는 미국 가특허출원 제60/625,532호("Fluorescence Assay for Modulators of Retinol Binding")를 참조할 수 있다.In some embodiments, the modulators described herein can also be used in in vitro assays for detecting the rate of change in RBP or TTR activity. For example, modulators are added to samples that include RBP, TTR and retinol. Labeling of components, such as RBP, TTR, retinol or modulators, can be used to detect whether the complex formation has collapsed. Complex formation and subsequent complex destruction can be detected and / or measured through conventional means, eg, sandwich assays as described above. In addition, other detection systems, such as FRET detection methods for RBP-TTR-retinol complex formation, can also be used to detect modulators of RBP or TTR binding. See U.S.
또한, 소분자, 폴리펩티드, 핵산 및 항체가 포함되나 이들에 한정되지 않는 다른 강력한 조절자는 또한 상술한 시험관내 검출법을 이용하여 스크리닝될 수도 있다. 예를 들어, 본원에 기술된 방법 및 조성물은 소분자 라이브러리, 핵산 라이브러리, 펩티드 라이브러리 또는 항체 라이브러리를 본원에 기술된 바에 따라 스크리닝하는데 사용될 수도 있다. 라이브러리, 이를 테면 상기 개시된 조합형 라이브러리 및 기타 라이브러리를 스크리닝하는 방법은 예를 들어 미국 특허 제5,591,646호; 제5,866,341호; 및 제6,343,257호에서 찾아볼 수 있으며, 이들 문헌은 본원에 참고로 포함된다.In addition, other potent modulators, including but not limited to small molecules, polypeptides, nucleic acids, and antibodies, may also be screened using the in vitro detection methods described above. For example, the methods and compositions described herein may be used to screen small molecule libraries, nucleic acid libraries, peptide libraries or antibody libraries as described herein. Methods for screening libraries, such as the combinatorial and other libraries disclosed above, are described, for example, in US Pat. No. 5,591,646; 5,866,341; 5,866,341; And 6,343,257, which are incorporated herein by reference.
조절자 활성의 Adjuster activity 생체내In vivo 검출 detection
상술한 시험관내 방법 이외에, 일부 구체예에서, 본원에 기술된 방법 및 조성물은 또한 TTR 또는 RBP 이용가능성에 대한 조절자 활성의 생체내 검출법 및/또는 정량법과 함께 사용된다. 예를 들어, 표지된 TTR 또는 RBP는 대상에게 주사될 수 있으며, 여기서 표지된 TTR 또는 RBP의 주사전, 주사중 또는 주사후 후보 조절자가 첨가될 수 있다. 대상은 포유동물, 예를 들어 인간일 수 있지만; 다른 포유동물, 이를 테면 영장류, 말, 개, 양, 염소, 토끼, 마우스 또는 래트가 또한 추가적인 예이다. 이어, TTR 또는 RBP 이용가능성을 측정하기 위해 검출된 표지와 대상으로부터 생체 시료를 제거한다. 생체 시료로는 혈장, 혈액, 소변, 대변, 점액, 조직, 눈물또는 타액이 포함될 수 있으나 이들에 한정되지 않는다. 본원에 기술된 표지된 시약의 검출은 당업자들에 공지된 통상의 방법 중 임의의 방법을 이용하여 실시할 수 있으며, 이는 표지의 성질에 따라 달라진다. 화학발광(chemi-luminescence), 방사선표지(radiolabel) 및 다른 표지 화화합물을 감시하는 장치의 예는 그의 개시내용이 전체적으로 본원에 참고로 포함되는 미국 특허 제4,618,485호; 제5,981,202호에서 찾아볼 수 있다.In addition to the in vitro methods described above, in some embodiments, the methods and compositions described herein are also used in conjunction with in vivo detection and / or quantification of modulator activity on TTR or RBP availability. For example, labeled TTR or RBP can be injected into a subject, where candidate modulators can be added before, during or after injection of the labeled TTR or RBP. The subject may be a mammal, eg, a human; Other mammals such as primates, horses, dogs, sheep, goats, rabbits, mice or rats are also additional examples. The biological sample is then removed from the detected label and subject to determine TTR or RBP availability. Biological samples may include, but are not limited to, plasma, blood, urine, feces, mucus, tissue, tears or saliva. Detection of labeled reagents described herein can be carried out using any of the conventional methods known to those skilled in the art, depending on the nature of the label. Examples of devices for monitoring chemi-luminescence, radiolabel and other labeling compounds are described in US Pat. No. 4,618,485, the disclosure of which is incorporated herein by reference in its entirety; 5,981,202.
과다레티놀혈증Hyperretinolemia
레티놀은 지용성 황산화제 비타민이다. 적절한 수준에서 레티놀은 시력 및 골 성장에 중요하지만, 과량으로 존재하는 경우에는 문제가 될 수 있다. 과다레티놀혈증은 혈액내 레티놀의 상승적 또는 비정상적 수준의 존재이며, I형 및 II형 당뇨병, 골형성과다증, 이를 테면 미만성 특발성 골격 골형성과다증(diffuse idiopathic skeletal hyperostosis, DISH), 및 유리체망막 질환, 이를 테면 황반 변성과 같은 질환 및 병상과 관련이 있는 것으로 생각된다. 혈중 레티놀의 수준을 감소시키는 본원에 기술된 방법, 화합물 및 조성물은 이러한 질환 및 병상을 치료하는데 사용된다. 또한, 본원에 개시된 방법, 화합물 및 조성물은 표적 기관 및 조직, 이를 테면 눈에서 레티놀 이용가능성을 감소시키는데 효과적이다. 혈중 레티놀 농도를 감소시킴으로써, 간과 같은 기관에서 레티놀의 이용가능성은 레티놀-레티놀-결합 단백질 복합체의 형성 및/또는 레티놀- 레티놀-결합 단백질-트랜스티레틴 복합체의 형성을 조절할 수 있다. 하나의 구체예로는, 레티놀의 혈청 수준 또는 활성을 감소시키는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여, 과다레티놀혈증을 가진 환자를 치료하는 방법이다.Retinol is a fat-soluble sulfate agent vitamin. Retinol at an appropriate level is important for vision and bone growth, but can be a problem if present in excess. Hyperretinolemia is the presence of synergistic or abnormal levels of retinol in the blood, including type I and type II diabetes, hyperostosis, such as diffuse idiopathic skeletal hyperostosis (DISH), and vitreoretinal disease It is thought to be related to diseases and conditions such as macular degeneration. The methods, compounds, and compositions described herein that reduce levels of retinol in the blood are used to treat such diseases and conditions. In addition, the methods, compounds, and compositions disclosed herein are effective in reducing retinol availability in target organs and tissues, such as the eye. By decreasing blood retinol concentrations, the availability of retinol in organs such as the liver can regulate the formation of retinol-retinol-binding protein complexes and / or the formation of retinol-retinol-binding protein-transtyretin complexes. In one embodiment, a method of treating a patient with hyperretinolemia, comprising administering a therapeutically effective amount of a compound of Formula (I) or (II) to reduce serum levels or activity of retinol .
대사 장애Metabolic disorders
I형 및 II형 당뇨병(비만 및/또는 비비만)을 비롯한 대사 장애는 또한 비정상적인 레티놀 수준과 관련이 있다.Metabolic disorders, including type I and type II diabetes (obesity and / or obesity) are also associated with abnormal retinol levels.
I형 당뇨병(인슐린-의존성 당뇨병)Type I diabetes (insulin-dependent diabetes)
I형 당뇨병은 당뇨병 중에서도 중증에 해당한다. 치료하지 않으면, I형 당뇨병 환자에게는 케톤증 및 급속한 변성이 발병하게 된다. 주로 젊은 사람들로 구성된 당뇨병 환자 중 대략 10 내지 20%의 환자가 I형 당뇨병으로 분류된다. 소수이지만 비만이 아닌 성인들에게도 I형 당뇨병이 발병하기도 한다.Type I diabetes is severe among diabetes. If left untreated, patients with type I diabetes develop ketosis and rapid degeneration. Approximately 10 to 20% of diabetics, primarily composed of young people, are classified as type I diabetes. A small but non-obese adult may develop type I diabetes.
I형 당뇨병은 이화 질환으로서, 혈류 중 인슐린은 거의 존재하지 않고 혈장의 글루카곤 수준이 상승한 경우이다. I형 당뇨병은 자가면역성 질환인 것으로 생각되는데, 아마도 발병한 개체의 췌장 B 세포에 감염에 의하거나 유해 환경의 공격으로 발병되는 것일 수 있다. 자가면역 이론의 뒷받침으로, 인슐린과 섬세포에 대한 자가항체는 당뇨병이 발병하지 않은 개체에서와는 달리 I형 당뇨병 환자에게서 검출된다.Type I diabetes is a catabolic disease in which there is little insulin in the bloodstream and elevated levels of glucagon in plasma. Type I diabetes is thought to be an autoimmune disease, possibly caused by infection of the pancreatic B cells of the affected individual or by an attack of a harmful environment. In support of the theory of autoimmunity, autoantibodies against insulin and islet cells are detected in patients with type I diabetes, unlike individuals without diabetes.
소아에게 I형 당뇨병이 발병하게 될 경우, 레티놀 결합 단백질(RBP) 수준은 감소하고 RBP가 소변으로 배출되는 양은 증가하게 되며, 레티놀 수준은 보다 낮아진다. 문헌[Basu, TK, et al., Am. J. Clin. Nutr. 50:329-331(1989); Durbey, SW et al., Diabetes Care 20:84-89 (1997)]을 참조할 수 있다. 레티놀과 RBP 수준이 낮아지면, 이에 따라 간세포에서 RBP를 합성하는데 필수적인 인자인 아연 대사량도감소하게 된다. 문헌[Cunningham, JJ, et al., Metabolism 42:1558-1562 (1994)]을 참조할 수 있다. 이와는 반대로, I형 당뇨병 환자의 경우 토코페롤, 또는 비타민 E 수준에는 변화가 없다. 문헌[Basu, TK et al (1989)]을 참조할 수 있다.In children with type I diabetes, retinol binding protein (RBP) levels decrease, the amount of RBP released into the urine increases, and retinol levels decrease. See Basu, TK, et al., Am. J. Clin. Nutr. 50: 329-331 (1989); Durbey, SW et al., Diabetes Care 20: 84-89 (1997). Lower retinol and RBP levels also reduce zinc metabolism, an essential factor in the synthesis of RBP in hepatocytes. See Cunningham, JJ, et al., Metabolism 42: 1558-1562 (1994). In contrast, there is no change in tocopherol or vitamin E levels in patients with type I diabetes. See Basu, TK et al (1989).
간 저장 세포내 비타민 A의 수준이 증가함에도 불구하고, 레티놀의 수준은 더욱 낮아짐을 확인할 수 있다. 문헌[Tuitoek PJ, et al., Br. J. Nutr. 75: 615-622 (1996)]을 참조할 수 있다. 비타민 A 상태와 인슐린 분비와의 연관성을 입증하는 연구 결과, 인슐린 치료만이 I형 당뇨병 대상에서 감소하였던 비타민 A의 수준을 회복시킬 수 있음을 알 수 있었다[Tuitoek, PJ et al., J. Clin. Biochem. Nutr. 19:165-169 (1996)]. 이와는 반대로, 비타민 A를 영양 보충한다고 해서 비타민 A의 대사 이용가능성이 정상화될 수 있는 것은 아니다.Although the level of vitamin A in liver storage cells is increased, the level of retinol is lowered. Tuitoek PJ, et al., Br. J. Nutr. 75: 615-622 (1996). Studies demonstrating the association between vitamin A status and insulin secretion have shown that only insulin treatment can restore the level of vitamin A that has been reduced in type I diabetes patients [Tuitoek, PJ et al., J. Clin . Biochem. Nutr. 19: 165-169 (1996). Conversely, nutritional supplementation of vitamin A may not normalize the metabolic availability of vitamin A.
이러한 연구를 통하여, 비타민 A와 근육과 지방세포로 운반되는 글루코오스의 인슐린에 의한 조절 사이에는 상관성이 있음을 입증할 수 있다. 정상 인슐린 분비에 비타민 A가 필요함을 입증함으로써 추가의 연구를 통해 이러한 상관성에 힘이 실렸다. 문헌[Chertow, BS, et al., J. Clin. Invest. 79: 163-169 (1987)]을 참조할 수 있다. 레티놀은 비타민 A 결핍 관류 섬세포로부터 인슐린을 방출하는데 필요한 것으로 파악되었다. 생체내 실험을 통해, 비타민 A-결핍 래트는 글루코오스-유도성 급성 인슐린 방출 과정이 손상되었으며, 이는 비타민 A를 공급하여야만 개선되었음을 알 수 있었다. 비타민 A는 섬세포 및 인슐린-분비 세포에서 트랜스글루타미나제 활성을 촉진함으로써 인슐린을 분비시킬 수 있으며[Driscoll HK, et al., Pancreas 15:69-77 (1997)], 또한 이 비타민 A는 태아의 섬세포 분화에도 필요하고, 성인의 글루코오스 과민성(glucose intolerance)을 예방하는데도 필요할 뿐만 아니라[Matthews, KA et al., J. Nutr. 134:1958-1963 (2004)], 당뇨병 환자에서 혈중 글루코오스 수준의 조절과 인슐린 방출시 비타민 A 및 레티놀의 역할을 강화하는데도 필요하다. 레티놀 및/또는 RBP의 수준 및 활성을 조절하는 일반식 (I) 또는 (II)의 화합물을 사용하여 I형 당뇨병을 치료하기 위한 방법, 화합물 및 조성물이 본원에 개시되어 있다.These studies demonstrate that there is a correlation between vitamin A and insulin-controlled glucose transported to muscle and adipocytes. Further studies have underlined this correlation by demonstrating the need for vitamin A for normal insulin secretion. See Chertow, BS, et al., J. Clin. Invest. 79: 163-169 (1987). Retinol was found to be required to release insulin from vitamin A deficient perfusion islet cells. In vivo experiments showed that vitamin A-deficient rats impaired the glucose-induced acute insulin release process, which was improved only by feeding vitamin A. Vitamin A can secrete insulin by promoting transglutaminase activity in islet and insulin-secreting cells [Driscoll HK, et al., Pancreas 15: 69-77 (1997)], and this vitamin A is fetal Is not only required for islet cell differentiation, but also to prevent glucose intolerance in adults [Matthews, KA et al., J. Nutr. 134: 1958-1963 (2004)], which is also required to enhance the role of vitamin A and retinol in the regulation of blood glucose levels and insulin release in diabetic patients. Disclosed herein are methods, compounds, and compositions for treating type I diabetes using compounds of formula (I) or (II) that modulate the levels and activities of retinol and / or RBP.
IIII 형 당뇨병(인슐린-Type Diabetes (Insulin- 비의존성Independence 당뇨병) diabetes)
II형 당뇨병은 보다 가벼운 증상을 나타내는 당뇨병의 이종군에 해당한다. II형 당뇨병은 일반적으로 성인에게 발병하지만, 때로는 유년기에 발병할 수도 있다.Type II diabetes is a heterogeneous group of diabetes with milder symptoms. Type II diabetes usually occurs in adults, but can sometimes occur in childhood.
II형 당뇨병은 통상 혈장내 글루코오스 수준이 상승함에 따라 인슐린에 둔감해진다. II형 당뇨병 환자 중 85% 이하는 비만 환자로서, 이들은 복부에 지방이 존재하는 것과 비례하여 내인성 인슐린에 둔감하다. 인슐린 둔감(insulin insensitivity)의 원인은 인슐린 작용에 관여하는 후수용체(post-receptor)가 결핍되어 있기 때문이다. 이는 팽창된 세포 저장 데포(cellular storage depot)(예를 들어, 팽창된 지방세포 및 과영양 공급 간 및 근육 세포)와 식후 혈류로부터 영양분을 제거하는 능력의 감소와 관련되어 있다. 이후 인슐린이 과다분비되면, 세포내 인슐린 수용체도 더욱 하향조절될 수 있다. 게다가, 글루코오스 운반 단백질(예를 들어, GLUT4)도 지속적인 활성화에 따라 하향조절되어, 고혈당 증상으로 인해 환자의 병상은 더욱 악화된다.Type II diabetes is usually insensitive to insulin as glucose levels in the plasma rise. Less than 85% of patients with type II diabetes are obese and are insensitive to endogenous insulin in proportion to the presence of fat in the abdomen. The cause of insulin insensitivity is the lack of post-receptors involved in insulin action. This is associated with a decrease in the ability to remove nutrients from the expanded cellular storage depots (eg, expanded adipocytes and overnourished liver and muscle cells) and the post-prandial blood stream. If insulin is oversecreted then intracellular insulin receptors may be further downregulated. In addition, glucose transport proteins (eg, GLUT4) are also downregulated with sustained activation, which further exacerbates the patient's condition due to hyperglycemic symptoms.
I형 당뇨병 환자와는 대조적으로, II형 당뇨병 환자에게서는 RBP의 수준이 선택적으로 상승하는데, 관찰된 레티놀 수준도 상승하는 것이 보통이다. 문헌[Sasaki, H et al., "Am. J. Med. Sci. 310:177-82 (1995); Basualdo CG, et al., J. Am Coll. Nutr. 16:39-45 (1997); Abahausain, MA et al., Eur. J. Clin. Nutr. 53: 630-635 (1999)]을 참조할 수 있다. 또한, II형 당뇨병 환자의 경우, 레티노산(올-트랜스 RA 및 13-시스 RA) 수준도 감소하였다[Yamakoshi, Y et al., Biol. Pharm. Bull 25:1268-1271 (2002)]. 비타민 E(토코페롤)과 카로티노이드를 비롯한 기타 비타민의 수준, 그리고 아연, 알부민 및 TTR(비타민 A의 대사에 영향을 미치는 것으로 알려짐)의 수준은 당뇨군과 대조군 둘 다에서 변함이 없었다.In contrast to patients with type I diabetes, the level of RBP is selectively elevated in patients with type II diabetes, with elevated levels of observed retinol also common. Sasaki, H et al., “Am. J. Med. Sci. 310: 177-82 (1995); Basualdo CG, et al., J. Am Coll. Nutr. 16: 39-45 (1997); Abahausain, MA et al., Eur. J. Clin. Nutr. 53: 630-635 (1999), and retinoic acid (all-trans RA and 13-cis in patients with type II diabetes). RA) levels were also reduced [Yamakoshi, Y et al., Biol. Pharm. Bull 25: 1268-1271 (2002)] Levels of vitamin E (tocopherol) and other vitamins, including carotenoids, and zinc, albumin and TTR ( Levels of vitamin A, known to affect the metabolism of vitamin A, were unchanged in both diabetic and control groups.
이와 같은 II형 당뇨병에서 RBP 수준의 선택적 증가는 I형 당뇨병에서 RBP가 선택적으로 감소하는 것과 관련되어 있는데, 이러한 사실은 인슐린에 의한 혈중 글루코오스 수준의 조절에 있어서 RBP와 비타민 A의 역할을 뒷받침한다. 당뇨병 환자에게서 인슐린 수준이 증가하면(고인슐린분비혈증) RBP의 수준도 증가하게 된다[Basualdo et al. (1997)]. RBP 수준은 또한 환자의 고혈당증과도 관련되어 있다. 레티노이드는 인간에게서 인슐린 감수성을 상승시키는 것으로 이미 규명된 바 있다. 문헌[Hartmann, D. et al., Eur. J. Clin. Pharmacol. 42:523-8 (1992)]을 참조할 수 있다. I형 당뇨병 및 II형 당뇨병에서 RBP 수준과 인슐린 감수성이 역상관관계에 있다는 것은 곧 포유동물 대상에서 인슐린 감수성을 조절하는 치료 수단임을 말해 주는 것이다.This selective increase in RBP levels in type II diabetes is associated with the selective decrease in RBP in type I diabetes, which supports the role of RBP and vitamin A in regulating blood glucose levels by insulin. Increasing insulin levels (hyperinsulinemia) in diabetics also increases levels of RBP [Basualdo et al. (1997). RBP levels are also associated with hyperglycemia in patients. Retinoids have already been shown to increase insulin sensitivity in humans. See Hartmann, D. et al., Eur. J. Clin. Pharmacol. 42: 523-8 (1992). The inverse correlation between RBP levels and insulin sensitivity in type I diabetes and type II diabetes suggests a therapeutic tool for controlling insulin sensitivity in mammalian subjects.
레티놀 결합 단백질 4(Retinol binding protein 4 ( RBPRBP 4) 4)
레티놀 결합 단백질 4(RBP4)는 비타민 A를 수송하는 역할로 알려진, 지방세포에서 분비된 단백질이다. 연구를 통해, 혈청 RBP4 수준의 상승이 II형 당뇨병의 주요 원인인 인슐린 저항성의 발달 초기 단계를 표시하도록 도울 수 있다는 결과를 알게 되었다. 문헌[Kahn et al., 354 New Eng. J. Med. 2552-63 (2006)]을 참조할 수 있다. 또한, 마우스의 실험을 통해, RBP4 수준의 상승이 인슐린 저항성을 유발하는 것으로 제시되었다. 게다가, 혈청 RBP4 수준은 내당능 이상의 비만 또는 II형 당뇨병의 환자 및 II형 당뇨병에 대한 가족력이 농후한 비비만성 비당뇨병 환자에서 인슐린 저항성 크기와 상관관계 있다. 상승된 혈청 RBP4는 신체-질량 지수, 허리 대 엉덩이 비율, 혈청 트리글리세리드 수준 및 수축기 혈압의 증가, 및 고밀도 지단백 콜레스테롤 수준의 감소를 비롯한 대사 증후군의 구성요소와 관련이 있다.Retinol binding protein 4 (RBP4) is a protein secreted from adipocytes, known to transport vitamin A. Studies have shown that elevated serum RBP4 levels can help mark early stages of development of insulin resistance, a major cause of type II diabetes. Kahn et al., 354 New Eng. J. Med. 2552-63 (2006). In addition, experiments in mice have shown that elevated RBP4 levels cause insulin resistance. In addition, serum RBP4 levels correlate with the magnitude of insulin resistance in patients with obesity or type II diabetes with impaired glucose tolerance and in obese nondiabetic patients with a rich family history of type II diabetes. Elevated serum RBP4 is associated with components of metabolic syndrome, including body-mass index, waist-to-hip ratio, increased serum triglyceride levels and systolic blood pressure, and decreased high-density lipoprotein cholesterol levels.
또한, 연구를 통해, 혈중 RBP4의 양이 복부 장기 주변의 지방의 양을 반영하며, 이는 RBP4가 심혈관계 위험도의 바이오마커(biomarker)로서 사용될 수 있음이 제시되었다. RBP4의 수준이 증가함에 따라, "내복부 지방"의 수준은 심장 질환 및 II형 당뇨병에 대한 위험성의 증가로 이어지는데, 이는 "내복부 지방"의 증가가 심혈관계 위험도와 관련이 있기 때문이다. 또한, 연구를 통해 피하 지방 조직에서보다 내장 지방 조직(내부 기관을 둘러싸는 지방 조직)에서 RBP4의 유전자 발현이 더욱 증가하는 것으로 나타났다. 따라서, RPB4의 수준은 피하형 비만인 사람들에 비해 "내장형" 비만인 사람에게서 더 높다.In addition, studies have suggested that the amount of RBP4 in the blood reflects the amount of fat around the abdominal organs, which can be used as a biomarker of cardiovascular risk. As the level of RBP4 increases, the level of "abdominal fat" leads to an increased risk for heart disease and type II diabetes, because the increase in "abdominal fat" is associated with cardiovascular risk. In addition, studies have shown that gene expression of RBP4 is more increased in visceral adipose tissue (adipose tissue surrounding internal organs) than in subcutaneous adipose tissue. Thus, the level of RPB4 is higher in people with "built-in" obesity than those with subcutaneous obesity.
본원에는 RBP4의 과잉 혈청 수준을 감소시키는 일반식 (I) 및 (II)의 화합물이 제시된다. 하나의 구체예로는, RBP4의 혈청 수준을 감소시키는 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물이다:Provided herein are compounds of Formulas (I) and (II) that reduce excess serum levels of RBP4. In one embodiment is a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof which reduces serum levels of RBP4:
상기 식에서,Where
A는 O, NH 또는 S이고; A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H 또는 이고;R is H or ego;
G는 -OR1, -(C1-C6)알킬, -(C1-C6)알킬-OR1, 할로겐, -CO2R1, -(C1-C6)알킬-CO2R1, NHR1, -(C1-C6)알킬-NHR1, -(C=O)NHR1, -(C1-C6)알킬-(C=O)NHR1, -NHR1(C=O)R1, -(C1-C6)알킬-NHR1(C=O)이며;G is -OR 1 ,-(C 1 -C 6 ) alkyl,-(C 1 -C 6 ) alkyl-OR 1 , halogen, -CO 2 R 1 ,-(C 1 -C 6 ) alkyl-CO 2 R 1 , NHR 1 ,-(C 1 -C 6 ) alkyl-NHR 1 ,-(C = O) NHR 1 ,-(C 1 -C 6 ) alkyl- (C = O) NHR 1 , -NHR 1 (C ═O) R 1 , — (C 1 -C 6 ) alkyl-NHR 1 (C═O);
R1은 H 또는 (C1-C6)알킬이고;R 1 is H or (C 1 -C 6 ) alkyl;
X는 할로겐이다.X is halogen.
또 다른 구체예로는, RBP4의 혈청 수준을 감소시키는 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물이다:In another embodiment is a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof that reduces serum levels of RBP4:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, (C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl, (C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H 또는 이며;R is H or Is;
G는 -OR1, -(C1-C6)알킬, -(C1-C6)알킬-OR1, 할로겐, -CO2R1, -(C1-C6)알킬-CO2R1, NHR1, -(C1-C6)알킬-NHR1, -(C=O)NHR1, -(C1-C6)알킬-(C=O)NHR1, -NHR1(C=O)R1, -(C1-C6)알킬-NHR1(C=O)R1이고;G is -OR 1 ,-(C 1 -C 6 ) alkyl,-(C 1 -C 6 ) alkyl-OR 1 , halogen, -CO 2 R 1 ,-(C 1 -C 6 ) alkyl-CO 2 R 1 , NHR 1 ,-(C 1 -C 6 ) alkyl-NHR 1 ,-(C = O) NHR 1 ,-(C 1 -C 6 ) alkyl- (C = O) NHR 1 , -NHR 1 (C ═O) R 1 , — (C 1 -C 6 ) alkyl-NHR 1 (C═O) R 1 ;
R1은 H 또는 (C1-C6)알킬이다.R 1 is H or (C 1 -C 6 ) alkyl.
또 다른 구체예로는, RBP4의 혈청 수준을 감소시키는 치료학적 유효량의 하기 일반식 (I)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 환자에게 투여하는 단계를 포함하여, 환자에서 당뇨병을 치료하는 방법이다:In another embodiment, administering to the patient a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof that reduces serum levels of RBP4: Including, the method of treating diabetes in a patient:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고;R is H, optionally substituted aryl or optionally substituted heteroaryl;
X는 할로겐이다. 또 다른 구체예로는, 환자에게 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 투여하여 RBP4의 수준을 감소시키는 단계를 포함하여, 단지 예로서 황반 변성과 같은 환자의 안과적 병상을 치료하는 방법이다. 추가의 구체예로는, 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여 혈청에서 RBP4를 저하시키는 방법이다. 또 다른 추가의 구체예로는, 일반식 (I) 또는 (II)의 화합물을 투여하는 단계를 포함하여 단지 예로서 지방 조직과 같은 조직에서 RBP4를 저하시키는 방법이다.X is halogen. In another embodiment, an ophthalmic condition in a patient, such as, for example, macular degeneration, is only included by administering to the patient a therapeutically effective amount of a compound of formula (I) or (II) to reduce the level of RBP4. How to treat it. In a further embodiment, a method of lowering RBP4 in serum, including administering a compound of Formula (I) or (II). Another further embodiment is a method of lowering RBP4 in a tissue such as adipose tissue, by way of example only, comprising administering a compound of Formula (I) or (II).
하나의 구체예로는, 지방 조직에서 RBP4를 조절하는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 환자에게 투여하는 단계를 포함하여, 환자에서 I형 또는 II형 당뇨병을 치료하는 방법이다. 추가의 구체예로는, RBP4 수준의 감소가 인슐린 감작(insulin sensitization)을 증가시키도록 RBP4 수준을 감소시키는 치료학적 유효량의 일반식 (I) 또는 (II)의 화합물을 환자에게 투여하는 단계를 포함하여, I형 또는 II형 당뇨병을 치료하는 방법이다. 또 다른 구체예로는, RBP4 수준의 감소가 인슐린 감작을 증가시키도록 RBP4 수준을 감소시키는 치료학적 유효량의 하기 일반식 (II)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물, 염 또는 용매화물을 환자에게 투여하는 단계를 포함하여, 환자에서 I형 또는 II형 당뇨병을 치료하는 방법이다:In one embodiment, treating a patient with type I or type II diabetes in a patient, comprising administering to the patient a therapeutically effective amount of a compound of formula (I) or (II) that modulates RBP4 in adipose tissue. It is a way. In a further embodiment, administering to the patient a therapeutically effective amount of a compound of formula (I) or (II) that reduces RBP4 levels such that a decrease in RBP4 levels increases insulin sensitization. This is a method for treating type I or type II diabetes. In another embodiment, a therapeutically effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt thereof, wherein the RBP4 level is reduced such that a decrease in RBP4 level increases insulin sensitization Or administering a solvate to the patient, the method of treating type I or type II diabetes in the patient:
상기 식에서,Where
A는 O, NH 또는 S이고;A is O, NH or S;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, -(C3-C8)헤테로사이클로알케닐이며;B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl,-(C 3 -C 8 ) heterocycloalkenyl;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이다.R is H, optionally substituted aryl or optionally substituted heteroaryl.
특발성 Idiopathic 두개내Cranial 고혈압 ( High blood pressure ( IIHIIH ))
가성뇌종양(PTC)이라고도 알려진 IIH는 확실한 원인물질 없이 뇌를 둘러싸고 있는 체액에 높은 압력이 걸리는 병상이다. 이 병상은 대부분 가임기의 여성에게서 나타난다. 증상은 체중 증가시 시작되거나 더욱 심해진다. 통상적인 증상으로서는 치료하지 않을 경우 심각하고 영구적인 실명을 유발할 수 있는, 두통, 규칙적인 동조성 이명(pulse synchronous tinnitus) 및 시력 장애(울혈 유두)를 포함한다.IIH, also known as pseudo brain tumor (PTC), is a condition in which high pressure is applied to the fluid surrounding the brain without a clear cause. This condition is most common in women of childbearing age. Symptoms begin or worsen with weight gain. Common symptoms include headache, pulse synchronous tinnitus and vision impairment (congestive papilla), which, if untreated, can cause serious and permanent blindness.
비록 IIH의 병인에 대해서는 알려진 바 없지만, 실험 대상에 과량의 비타민 A를 투여하였을 때 나타나는 증상과 징후가 IIH에서 살펴볼 수 있는 증상과 징후와 유사한 것으로 보아, 과량의 비타민 A가 원인인 것으로 보고 있다. 연구를 통하여, IIH 환자와 대조군 모두에서 비타민 A 섭취량과 레티닐 에스테르의 농도에 별로 차이가 나지 않았음에도 불구하고, 상기 대조군보다 IIH 환자의 경우가 혈청내 레티놀 수준이 더욱 높았음을 알 수 있었다. 문헌[Jacobson, DM et al, Neurology, 54:2192-3 (1999)]을 참조할 수 있다. 본원에는, 일반식 (I) 및 (II)의 화합물을 사용하여 IIH를 치료하기 위한 방법, 화합물 및 조성물이 포함된다.Although the etiology of IIH is not known, the excess of vitamin A may be due to the similar symptoms and signs of IIH when the dose of vitamin A is administered to subjects. The study showed that serum retinol levels were higher in IIH patients than in the control group, although there were no significant differences in vitamin A intake and retinyl ester concentrations in both IIH patients and controls. See Jacobson, DM et al, Neurology, 54: 2192-3 (1999). Included herein are methods, compounds, and compositions for treating IIH using compounds of formulas (I) and (II).
골 관련 장애Bone Related Disorders
골형성과다증은 골이 과도하게 성장하는 병상이다. 이 병상은 정상의 뼈에 다수의 근골격 질환에서 살펴볼 수 있는 다량의 돌출부가 형성될 수 있다. 미만성 특발성 골격 골형성과다증(DISH)은 골형성과다증의 일종으로서, 척추동물의 체내 유동성 석회 침착 및 골형성을 특징으로 한다. DISH 환자는 방사선 촬영시 이상 현상, 즉 방사능밀집 차폐물(radiodense shield)이 척추 정면에 형성되는 현상이 관찰된다(주로 흉추에서 관찰됨). 후종인대의 골형성(ossification of posterior longitudinal ligament, OPPL)은 또한 DISH 환자에서 흔히 살펴볼 수 있는 현상으로서, 척추 인대의 골형성과다증 또는 골형성의 결과로 인해 경추가 손상된다. 골형성과다증 또는 DISH 환자에 발생하는 다른 질환으로는 척추의 급성 골절 및 가성관절증이 포함된다.Hyperplasia is a condition in which bone grows excessively. This bed can form a large amount of protrusions in the normal bone that can be seen in many musculoskeletal disorders. Diffuse idiopathic skeletal hyperplasia (DISH) is a type of hyperplasia that is characterized by fluid lime deposition and bone formation in vertebrates. In patients with DISH, abnormalities, ie, radiodense shields are formed on the front of the spine, are observed mainly on the thoracic spine. Ossification of posterior longitudinal ligament (OPPL) is also a common phenomenon in DISH patients, and the cervical spine is damaged as a result of spinal ligament hyperplasia or bone formation. Other diseases that develop in patients with hyperplasia or DISH include acute fractures of the spine and pseudojoints.
DISH와 OPLL의 병인에 대해서는 현재 밝혀진 바 없지만, 이 두 질환은 혈청내 레티놀과 RBP가 높은 수준으로 존재하는 것과 관련되어 있다. DISH와 OPLL의 병인에 비타민 A가 어떠한 역할을 할 것이라고 예측하고 있는 문헌[Kodama,T et al., In vivo 12:339-344 (1998); Kilcoyne, RF, J. Am. Acad. Dermatol. 19:212-216 (1988)]을 참조할 수 있다. 기타 연구를 통해, 골형성과다증 환자에 선천적 RBP 결핍증이 발병하면, 레티놀 수준과 RBP수준이 비정상적으로 된다는 사실을 알 수 있었다. 문헌[DeBandt, M., et al., J. Rheumatol. 22:1395-8 (1995)]을 참조할 수 있다. 의료 평가 결과, 고령의 비타민 A 과다증 환자의 경우 변성 관절 질환도 함께 발병하는 것으로 보고 되었다. 문헌[Romero,JB et al., Bull Hosp. Jt. Dis. 54:169-174 (1996)]을 참조할 수 있다. 따라서, 본원에 기술된 방법, 화합물 및 조성물은 혈청 레티놀 및 RBP의 수준을 조절하는 일반식 (I) 또는 (II)의 화합물을 사용하여, 단지 예로서 골형성과다증과 같은 골 관련 장애를 치료하는데 사용된다.The pathogenesis of DISH and OPLL is currently unknown, but these two diseases are associated with high levels of serum retinol and RBP. Predicting what role vitamin A might play in the pathogenesis of DISH and OPLL (Kodama, T et al., In vivo 12: 339-344 (1998); Kilcoyne, RF, J. Am. Acad. Dermatol. 19: 212-216 (1988). Other studies have shown that retinol and RBP levels are abnormal when congenital RBP deficiency develops in patients with hyperplasia. DeBandt, M., et al., J. Rheumatol. 22: 1395-8 (1995). According to the medical evaluation, degenerative joint disease was also reported in elderly people with vitamin A hyperactivity. See Roomero, JB et al., Bull Hosp. Jt. Dis. 54: 169-174 (1996). Thus, the methods, compounds and compositions described herein utilize compounds of the general formula (I) or (II) that modulate the levels of serum retinol and RBP, for example only to treat bone related disorders such as hyperplasia. Used.
단백질 protein 오접힘Misfolding 및 응집 질환 And flocculation disease
단백질의 오접힘 및 응집은 일반적으로 아밀로이드증, 예를 들어 알츠하이머 질환, 파킨슨 질환 및 전신 아밀로이드증이라고 알려진 몇몇 질환과 관련되어 있다. 이러한 질환들은 단백질의 2차 구조가 오접힘될 때 발병되는 것으로서, 보통 가용성 단백질은 β-시트-풍부 구조의 불용성 세포외 피브릴 침착물을 형성하는데, 이는 아밀로이드 피브릴이라고도 하며 기관의 기능 장애를 일으킨다. 20 개의 상이한 피브릴 단백질, 예를 들어 트랜스티레틴(TTR)은 인간의 아밀로이드증에서 각각 상이한 임상학적 형태로서 관찰된다.Misfolding and aggregation of proteins are commonly associated with amyloidosis, for example Alzheimer's disease, Parkinson's disease and several diseases known as systemic amyloidosis. These diseases are caused when the secondary structure of a protein is misfolded, usually soluble proteins form insoluble extracellular fibrils deposits of β-sheet-rich structures, also known as amyloid fibrils, which cause dysfunction of organs. Cause Twenty different fibril proteins, such as transthyretin (TTR), are observed as different clinical forms in human amyloidosis, respectively.
야생형 TTR 단백질은 심장조직에 TTR 피브릴이 축적되어 발생하는 산발적 장애인 노인성 전신성 아밀로이드증의 진행에 관여한다. 이와는 반대로, 돌연변이 TTR 단백질은, 침착물이 주로 주로 말초신경계 및 자율신경계와 심장에 영향을 미치는 가족성 아밀로이드 다발신경병증과 심근증과 관련되어 있다. 조직 선택적 침착에 관여하는 메카니즘은 현재 알려져 있지 않다. 아밀로이드증의 발병에 있어서, TTR은 이의 단량체 형태가 피브릴과 형성과 관련되어 있다. TTR 4량체의 안정화를 촉진시키는 화합물, 예를 들어 소분자 레스베라트롤 및 비아릴아민은 시험관내에서 아밀로이드 피브릴 형성을 억제한다. 문헌[Reixach,N. et al., PNAS 101:2817-2822 (2004)]을 참조할 수 있다.Wild type TTR protein is involved in the development of sporadic impaired senile systemic amyloidosis caused by accumulation of TTR fibrils in heart tissue. In contrast, mutant TTR proteins are associated with familial amyloid polyneuropathy and cardiomyopathy, where the deposits primarily affect the peripheral and autonomic nervous system and heart. The mechanisms involved in tissue selective deposition are currently unknown. In the development of amyloidosis, TTR is associated with fibril formation in its monomeric form. Compounds that promote stabilization of TTR tetramers, such as small molecule resveratrol and biarylamines, inhibit amyloid fibril formation in vitro. Reixach, N. et al., PNAS 101: 2817-2822 (2004).
트랜스티레틴은 또한 알츠하이머 질환에 관여하지만, 이와 같이 아밀로이드증에서 아밀로이드 피브릴을 형성하는 것과는 대조적으로, TTR은 시험관내 및 생체내에서 아밀로이드 베타 단백질을 형성하는 것을 억제한다. 문헌[Schwartzman, AL et al., Amyloid. 11: 1-9 (2004); Stein, TD and Johnson, JA, J. Neurosci. 22:7380-7388(2002)]을 참조할 수 있다. 비타민 A는 또한 시험관내에서 아밀로이드형성 억제 효과와 아밀로이드-베타 피브릴 불안정화 효과를 나타내는 것으로 파악되었다. 문헌[Ono, K., et al., Exp. Neurol. 189:380-392 (2004)]을 참조할 수 있다.Transthyretin is also involved in Alzheimer's disease, but in contrast to forming amyloid fibrils in amyloidosis, TTR inhibits the formation of amyloid beta proteins in vitro and in vivo. Schwartzman, AL et al., Amyloid. 11: 1-9 (2004); Stein, TD and Johnson, JA, J. Neurosci. 22: 7380-7388 (2002). Vitamin A has also been shown to exhibit amyloidogenic and amyloid-beta fibril destabilizing effects in vitro. See Ono, K., et al., Exp. Neurol. 189: 380-392 (2004).
낭성Cystic 섬유증 fibrosis
낭성 섬유증은 사망의 일차적 병인이 녹농균(pseudomonas aeruginosa)에 의한 재발 세균 감염증과 관련된 과잉의 폐 감염증에 기인하는 치사성 유전 질환이다. 낭성 섬유증은 낭성 섬유증 막횡단 전도 조절 유전자(cystic fibrosis transmembrane conductance regulator gene, CFTR)의 돌연변이에 의해 야기된다. 이러한 유전자의 산물은 땀, 소화액 및 점액을 생산하는데 중요한 염화물 이온 채널이다. CFTR 유전자는 7번 염색체의 q31.2 위치에 위치하며, 길이가 1,480 개의 아미노산인 단백질을 생산한다. 통상의 돌연변이 ΔF508는 단백질의 508번 위치에서 아미노산 페닐알라닌을 소실시키는 3 개의 뉴클레오타이드의 결손이다. 후속으로, ΔF508은 정상적으로는 접히지 않으며 세포에 의해 분해되는 단백질을 생산한다. 또한, CFTR 유전자에 의해 생산된 단백질은 세포질을 주변 유체에 연결하는 염화물 이온 채널로서 작용한다. CFTR 단백질의 돌연변이는 세포 바깥쪽에 염화물 이온을 포착한다. 세포질로의 염화물 이온의 배제는 나트륨 이온을 유인하고, 이러한 결합은 낭성 섬유증 개체의 땀에서 다량으로 소실되는 염을 형성한다. 일부 연구를 통해, CFTR 단백질 상실이 나트륨 및 염화물 흡수를 증가시키며, 이것이 수분의 재흡수를 증가시켜 탈수증 및 다량의 점액을 야기한다는 것이 제시되어 있다.Cystic fibrosis is the primary cause of death of pseudomonas aeruginosa ) is a lethal genetic disease caused by excess lung infections associated with recurrent bacterial infections. Cystic fibrosis is caused by mutations in the cystic fibrosis transmembrane conductance regulator gene (CFTR). The products of these genes are chloride ion channels that are important for producing sweat, digestive fluid and mucus. The CFTR gene is located at q31.2 of chromosome 7 and produces a protein of 1,480 amino acids in length. The common mutation, ΔF508, is a deletion of three nucleotides that lose the amino acid phenylalanine at position 508 of the protein. Subsequently, ΔF508 produces proteins that normally do not fold and are degraded by the cell. In addition, the protein produced by the CFTR gene acts as a chloride ion channel that connects the cytoplasm to the surrounding fluid. Mutations in the CFTR protein trap chloride ions outside the cell. The exclusion of chloride ions into the cytoplasm attracts sodium ions, and these bonds form salts that are lost in large quantities in the sweat of cystic fibrosis individuals. Some studies suggest that loss of CFTR protein increases sodium and chloride uptake, which increases resorption of moisture, leading to dehydration and large amounts of mucus.
낭성 섬유증의 치료는 다량의 점액 및 감염에 의해 야기된 폐 손상의 치료에 집중되어 있다. 반코마이신 및 토브라마이신과 같은 항생제는 폐 기능이 감퇴는 경우에 사용된다. 플루티카존과 같은 코 스테로이드는 비염을 저하시키는데 사용되어 왔다. 다른 경우에, 비폐색을 완화시키고 추가의 감염을 제한하기 위해 부비동 수술이 사용된다.The treatment of cystic fibrosis is focused on the treatment of lung damage caused by large amounts of mucus and infection. Antibiotics such as vancomycin and tobramycin are used when lung function is reduced. Nose steroids such as fluticasone have been used to reduce rhinitis. In other cases, sinus surgery is used to relieve nasal obstruction and limit further infection.
세라미드 수준의 조절은 감염 폐로부터 세균을 효과적으로 제거하는데 중요한 듯 보인다. 본원에는 세라미드 생산의 매개를 통해 부하된 세균의 제거를 돕는 일반식 (I) 또는 일반식 (II)의 화합물을 투여하는 단계를 포함하여 낭성 섬유증을 치료하는 방법이 개시되어 있다. 일부 구체예로는, 감염 폐로부터 세균의 제거를 돕는 일반식 (I) 또는 일반식 (II)의 화합물을 투여하는 단계를 포함하여 낭성 섬유증에 관련된 세균 감염증을 치료하는 방법이다. 다른 구체예에서, 세균은 그램-음성 세균이다. 추가의 구체예에서, 그램-음성 세균은 녹농균(pseudomonas aeruginosa)이다. 또 다른 구체예로는, 낭성 섬유증 관련 기관에서 세라미드 결핍증을 고치는 일반식 (I) 또는 일반식 (II)의 화합물을 투여하는 단계를 포함하여 낭성 섬유증을 치료하는 방법이다. 또 다른 구체예에서, 낭성 섬유증 관련 기관은 폐이다.Control of ceramide levels appears to be important for the effective removal of bacteria from infected lungs. Disclosed herein is a method of treating cystic fibrosis comprising administering a compound of Formula (I) or Formula (II) to aid in the removal of loaded bacteria through the mediation of ceramide production. In some embodiments, a method of treating bacterial infections associated with cystic fibrosis, comprising administering a compound of Formula (I) or Formula (II) to assist in the removal of bacteria from an infected lung. In other embodiments, the bacteria are Gram-negative bacteria. In a further embodiment, the Gram-negative bacterium is pseudomonas aeruginosa . In another embodiment, a method of treating cystic fibrosis, comprising administering a compound of Formula (I) or Formula (II) to correct ceramide deficiency in a cystic fibrosis related organ. In another embodiment, the cystic fibrosis related organ is lung.
알스트롬Alstrom -- 할그렌Hallgren 증후군 syndrome
알스트롬-할그렌 증후군(알스트롬 증후군이라고도 알려짐)은 매우 어린 시기에 어린이에게 발병하는 희귀성 상염색체 퇴행성 질환이다. 증상으로는, 추상체-간상체 이영양, 난청, 생후 첫해에 발생하는 비만증, II형 당뇨병의 진행 및 심각한 인슐린 저항성, 흑색 극세포증(피부에 어두운 반점(dark patch)이 생기는 증상), 과다성선자극성 성선기능저하증(hypergonadotrophic hypogonadism) 및 갑상연골결핍증(thyroid deficiencies)과 관련된, 유아기 실명 또는 심각한 시력 손상이 포함된다.Alstrom-Halgren's syndrome (also known as Alstrom's syndrome) is a rare autosomal degenerative disease that occurs in children at very young ages. Symptoms include: abstract-rod dystrophies, deafness, obesity in the first year of life, progression of type II diabetes and severe insulin resistance, melanoma (the appearance of dark patches on the skin), hypergonadal gonadotropia Childhood blindness or severe vision impairment, associated with hypergonadotrophic hypogonadism and thyroid deficiencies.
알스트롬 증후군과 관련된 돌연변이는 염색체 2p 위의 14.9 cM 영역에 편재되었다[Collin, GB et al., Hum. Mol. Gen. 6:213-219 (1997)]. 질환의 개개의 대증적인 증상을 치료하는 것 이외에는, 알스트롬 증후군 환자에 이용가능한 치료학적 방법은 현재 없다. 일부 구체예로는, 일반식 (I) 및 (II)의 구조를 가진 화합물을 사용하여 알스트롬-할그렌 증후군을 치료하는데 사용되는 방법, 화합물 및 조성물이다.Mutations associated with Alstrom syndrome were ubiquitous in the 14.9 cM region on chromosome 2p [Collin, GB et al., Hum. Mol. Gen. 6: 213-219 (1997). Aside from treating the individual symptomatic symptoms of the disease, there are currently no therapeutic methods available for Alstrom syndrome patients. In some embodiments are methods, compounds, and compositions used to treat Alstrom-Halgren syndrome using compounds having the structures of Formulas (I) and (II).
정의Justice
"알콕시"기는 (알킬)O-기를 말하며, 여기서 알킬은 본원에 정의된 바와 같다.An "alkoxy" group refers to a (alkyl) O- group where alkyl is as defined herein.
"알킬"기는 지방족 탄화수소기를 말한다. 알킬 부분은 "포화 알킬"기 일 수 있으며, 이는 임의의 알켄 또는 알킨 부분을 함유하지 않는다는 것을 의미한다. 알킬 부분은 또한 "불포화 알킬" 부분일 수 있으며, 이는 적어도 하나의 알켄 또는 알킨 부분을 함유한다는 것을 의미한다. "알켄" 부분은 적어도 2 개의 탄소원자 및 적어도 하나의 탄소-탄소 이중결합으로 구성된 기를 의미하고, "알킨" 부분은 적어도 2 개의 탄소원자 및 적어도 하나의 탄소-탄소 삼중결합으로 구성된 기를 의미한다. 포화되었든 불포화되었든 알킬 부분은 분지쇄형, 직쇄형 또는 환형일 수 있다."Alkyl" group refers to an aliphatic hydrocarbon group. The alkyl moiety may be a "saturated alkyl" group, meaning that it does not contain any alkene or alkyne moieties. The alkyl moiety may also be an "unsaturated alkyl" moiety, meaning that it contains at least one alkene or alkyne moiety. "Alkene" moiety means a group consisting of at least two carbon atoms and at least one carbon-carbon double bond, and an "alkyne" moiety means a group consisting of at least two carbon atoms and at least one carbon-carbon triple bond. Whether saturated or unsaturated, the alkyl moiety can be branched, straight chain or cyclic.
"알킬" 부분은 1 내지 10 개의 탄소원자를 가질 수 있다(본원에서는, "1 내지 10"과 같은 수치 범위가 각각 정수로 주어지며; 예를 들어 "1 내지 10 개의 탄소원자"는 알킬기가 최대 10 개까지 탄소원자를 포함하여, 1 개의 탄소원자, 2 개의 탄소원자, 3 개의 탄소원자 등으로 구성될 수 있음을 의미하나 제시된 정의는 또한 수치 범위가 지정되지 않은 "알킬"의 경우도 포함한다). 알킬기는 또한 1 내지 5 개의 탄소원자를 가진 "저급 알킬"일 수도 있다. 본원에 기술된 화합물의 알킬기는 "C1-C4 알킬" 또는 유사한 표기로 나타내어질 수 있다. 단지 예로서, "C1-C4 알킬"은 알킬쇄에 1 내지 4 개의 탄소원자가 존재함을 의미하며, 즉 알킬쇄는 메틸, 에틸, 프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸 및 t-부틸로 이루어진 그룹 중에서 선택된다. 전형적인 알킬기로는 메틸, 에틸, 프로필, 이소프로필, 부틸, 이소부틸, t-부틸, 펜틸, 헥실, 에테닐, 프로페닐, 부테닐, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 사이클로헥실 등이 포함되나 이들에 한정되지 않는다."Alkyl" moieties may have from 1 to 10 carbon atoms (herein, numerical ranges such as "1 to 10" are each given as an integer; for example, "1 to 10 carbon atoms" is an alkyl group of up to 10 carbon atoms). Meaning that it may consist of one carbon atom, two carbon atoms, three carbon atoms, etc., up to and including carbon atoms, but the definitions given also include "alkyl" where the numerical range is not specified). The alkyl group may also be "lower alkyl" having 1 to 5 carbon atoms. The alkyl group of the compounds described herein may be represented by "C 1 -C 4 alkyl" or similar notation. By way of example only, "C 1 -C 4 Alkyl "means that there is 1 to 4 carbon atoms in the alkyl chain, ie the alkyl chain is selected from the group consisting of methyl, ethyl, propyl, isopropyl, n-butyl, isobutyl, sec-butyl and t-butyl Typical alkyl groups include methyl, ethyl, propyl, isopropyl, butyl, isobutyl, t-butyl, pentyl, hexyl, ethenyl, propenyl, butenyl, cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, and the like. Included but not limited to these.
용어 "알케닐"은 알킬기의 처음 두 원자가 방향족기 부분이 아닌 이중결합을 형성하는 알킬기의 형태를 말한다. 즉, 알케닐기는 원자 -C(R)=C-R로 시작하며, 여기서 R은 알케닐기의 나머지 부분을 말하며, 동일하거나 상이할 수 있다. 알케닐기의 비한정적인 예로는 -CH=CH, -C(CH3)=CH, -CH=CCH3 및 -C(CH3)=CCH3가 포함된다. 알케닐 부분은 분지쇄형, 직쇄형 또는 환형(이 경우는 "사이클로알케닐" 기로도 알려져 있다)일 수 있다.The term "alkenyl" refers to the form of an alkyl group in which the first two atoms of the alkyl group form a double bond rather than an aromatic group portion. That is, the alkenyl group starts with the atom -C (R) = CR, where R refers to the remainder of the alkenyl group and can be the same or different. Non-limiting examples of alkenyl groups include -CH = CH, -C (CH 3 ) = CH, -CH = CCH 3 and -C (CH 3 ) = CCH 3 . The alkenyl moiety can be branched, straight or cyclic (also known as a "cycloalkenyl" group in this case).
"아미드"는 식 -C(O)NHR 또는 -NHC(O)R의 화학적 부분이며, 여기서 R은 알킬, 사이클로알킬, 아릴, 헤테로아릴(환 탄소를 통해 결합) 및 헤테로알리사이클릭(환 탄소를 통해 결합)으로 이루어진 그룹 중에서 선택된다. 아미드는 일반식 (I)의 화합물에 결합하여 전구약물을 형성하는 아미노산 또는 펩티드 분자일 수 있다. 본원에 기술된 화합물 위의 임의의 아민, 하이드록시 또는 카르복시 측쇄는 아미드화될 수 있다. 이러한 아미드를 제조하는 과정 및 특정 기는 당업자들에게 알려져 있으며, 본원에 참고로 포함되는 문헌[Greene and Wuts, Protective Groups in Organic Synthesis, 3rd Ed., John Wiley & Sons, New York, NY, 1999]과 같은 참고문헌 자료에서 쉽게 찾아볼 수 있다."Amide" is the chemical moiety of the formula -C (O) NHR or -NHC (O) R, wherein R is alkyl, cycloalkyl, aryl, heteroaryl (bonded via ring carbon) and heteroalicyclic (ring carbon Combined through). Amides may be amino acid or peptide molecules that bind to compounds of formula (I) to form prodrugs. Any amine, hydroxy or carboxy side chain on the compounds described herein may be amidated. Processes and specific groups for preparing such amides are known to those skilled in the art and are described herein by Greene and Wuts, Protective Groups in Organic Synthesis, 3 rd Ed., John Wiley & Sons, New York, NY, 1999].
용어 "방향족" 또는 "아릴"은 공역 파이 전자 시스템을 가진 적어도 하나의 환을 함유하는 방향족기를 말하며, 카보사이클릭 아릴(예, 페닐) 및 헤테로사이클릭 아릴(또는 "헤테로아릴" 또는 "헤테로방향족") 기(예, 피리딘) 둘 다를 포함한다. 이 용어는 모노사이클릭 또는 융합-환 폴리사이클릭(즉, 인접 쌍의 탄소원자를 공유하는 환) 기를 포함한다. 용어 "카보사이클릭"은 하나 이상의 공유적으로 폐환된 구조를 가지며, 환의 골격을 형성하는 원자가 모두 탄소원자인 화합물을 의미한다. 따라서, 용어는 카보사이클릭을, 환 골격이 탄소가 아닌 적어도 하나의 원자를 함유하는 헤테로사이클릭 환과 구분짓는다.The term “aromatic” or “aryl” refers to an aromatic group containing at least one ring having a conjugated pi electronic system, and refers to carbocyclic aryl (eg phenyl) and heterocyclic aryl (or “heteroaryl” or “heteroaromatic” ") Groups such as pyridine. The term includes monocyclic or fused-ring polycyclic (ie, rings which share adjacent pairs of carbon atoms) groups. The term "carbocyclic" refers to a compound having one or more covalently ringed structures and wherein the atoms that form the backbone of the ring are all carbon atoms. Thus, the term distinguishes carbocyclic from heterocyclic rings in which the ring backbone contains at least one atom other than carbon.
용어 "사이클로알킬"은 탄소와 수소만을 함유하며 포화, 부분 불포화 또는 완전 불포화일 수 있는 모노사이클릭 또는 폴리사이클릭 래디칼을 말한다. 사이클로알킬기는 3 내지 10 개의 환원자를 가진 기를 포함한다. 사이클로알킬 기의 예시적인 예로는 하기한 부분 등이 포함된다:The term "cycloalkyl" refers to monocyclic or polycyclic radicals containing only carbon and hydrogen and which may be saturated, partially unsaturated or fully unsaturated. Cycloalkyl groups include groups having 3 to 10 reducers. Illustrative examples of cycloalkyl groups include the following moieties, and the like:
용어 "할로" 다르게는 "할로겐"은 플루오로, 클로로, 브로모 또는 요오도를 의미한다. 바람직한 할로기는 플루오로, 클로로 및 브로모이다.The term "halo" alternatively "halogen" means fluoro, chloro, bromo or iodo. Preferred halo groups are fluoro, chloro and bromo.
용어 "헤테로알킬", "헤테로알케닐" 및 "헤테로알키닐"로는 탄소가 아닌 다른 원자, 예를 들어 산소, 질소, 황, 인 또는 이들의 조합 중에서 선택된 하나 이상의 골격쇄 원자를 가진 임의로 치환된 알킬, 알케닐 및 알키닐 래디칼이 포함된다.The terms "heteroalkyl", "heteroalkenyl" and "heteroalkynyl" refer to optionally substituted atoms having one or more skeletal chain atoms selected from atoms other than carbon, such as oxygen, nitrogen, sulfur, phosphorus or combinations thereof. Alkyl, alkenyl and alkynyl radicals are included.
용어 "헤테로아릴" 다르게는 "헤테로방향족"은 질소, 산소 및 황 중에서 선택된 하나 이상의 환 헤테로원자를 포함하는 아릴기를 말한다. N-함유 "헤테로방향족" 또는 "헤테로아릴" 부분은 환 골격원자의 적어도 하나가 질소원자인 방향족기를 말한다. 폴리사이클릭 헤테로아릴기는 융합되거나 융합되지 않을 수 있다. 헤테로아릴기의 예시적인 예로는 하기한 부분 등이 포함된다:The term “heteroaryl” alternatively “heteroaromatic” refers to an aryl group comprising one or more ring heteroatoms selected from nitrogen, oxygen and sulfur. An N-containing "heteroaromatic" or "heteroaryl" moiety refers to an aromatic group wherein at least one of the ring backbone atoms is a nitrogen atom. Polycyclic heteroaryl groups may or may not be fused. Illustrative examples of heteroaryl groups include the following moieties and the like:
용어 "부분"은 분자의 특정 분절 또는 작용기를 말한다. 화학 부분은 종종 분자에 부착되거나 그 분자내에 있는 화학적 실체로 인식된다.The term "part" refers to a specific segment or functional group of a molecule. Chemical moieties are often recognized as chemical entities attached to or within a molecule.
용어 "결합" 또는 "단일 결합"은 결합에 의해 연결된 원자가 더 큰 하부구조의 부분인 것으로 간주되는 경우, 두 원자 또는 두 부분 사이의 화학적 결합을 말한다.The term "bond" or "single bond" refers to a chemical bond between two atoms or two parts when the atoms connected by the bond are considered to be part of a larger infrastructure.
용어 "카르복시산 생물동배체"는 카르복시산 기를 대체할 수 있는 부분을 의미한다. 생물동배체는 또 다른 대체로 유사한 원자 또는 원자들의 기의 교환을 함유하며, 공간 배열, 전자 특성, 또는 카르복시산 기의 일부 다른 물리화학적 특성을 모방함으로써 유사한 생물학적 활성을 유지한다. 따라서, 예를 들어 테트라졸, 설폰산 및 설폰아미드는 카르복시산 생물동배체이다.The term "carboxylic acid bioisotope" means a moiety capable of replacing carboxylic acid groups. Bioisotopes contain exchanges of other generally similar atoms or groups of atoms and maintain similar biological activity by mimicking spatial arrangement, electronic properties, or some other physicochemical properties of carboxylic acid groups. Thus, for example, tetrazole, sulfonic acid and sulfonamide are carboxylic acid bioisotopes.
용어 "임의로 치환된"은 언급된 기가 알킬, 사이클로알킬, 아릴, 헤테로아릴, 헤테로알리사이클릭, 하이드록시, 알콕시, 아릴옥시, 머캅토, 알킬티오, 아릴티오, 시아노, 할로, 카르보닐, 티오카르보닐, 이소시아네이토, 티오시아네이토, 이소티오시아네이토, 니트로, 퍼할로알킬, 퍼플루오로알킬, 실릴 및 일- 및 이-치환된 아미노기를 포함한 아미노 및 이들의 보호된 유도체 중에서 개별적으로 및 독립적으로 선택된 하나 이상의 추가의 기(들)에 의해 치환될 수 있음을 의미한다. 보호기의 예는 상술된 문헌(Greene and Wuts)과 같은 참고문헌에서 찾아볼 수 있다.The term “optionally substituted” means that the groups mentioned are alkyl, cycloalkyl, aryl, heteroaryl, heteroalicyclic, hydroxy, alkoxy, aryloxy, mercapto, alkylthio, arylthio, cyano, halo, carbonyl, Amino and protected derivatives thereof, including thiocarbonyl, isocyanato, thiocyanato, isothiocyanato, nitro, perhaloalkyl, perfluoroalkyl, silyl and mono- and di-substituted amino groups It can be substituted by one or more additional group (s) selected individually and independently. Examples of protecting groups can be found in references such as Greene and Wuts, supra.
일부 구체예에서, 본원에 개시된 화합물은 하나 이상의 키랄 중심을 가질 수 있으며, 각 중심은 R 또는 S 배열로 존재할 수 있다. 본원에 기술된 화합물은 모든 부분입체이성질체, 거울상이성질체 및 에피머(epimeric) 형태 뿐만아니라 이들의 적절한 혼합물을 포함한다. 입체이성질체는 필요에 따라 예를 들어 키랄 크로마토그래피 컬럼에 의한 입체이성질체의 분리로 수득할 수 있다.In some embodiments, a compound disclosed herein can have one or more chiral centers, each center can exist in an R or S configuration. The compounds described herein include all diastereomeric, enantiomeric and epimeric forms as well as the appropriate mixtures thereof. Stereoisomers may be obtained, for example, by separation of the stereoisomers, for example by chiral chromatography columns.
본원에 기술된 방법 및 제형은 일반식 (I)의 구조를 가진 화합물의 N-산화물, 결정성 형태(또한 다형체로도 알려짐) 또는 약제학적으로 허용가능한 염 뿐만아니라 동일한 활성 형태를 가진 이들 화합물의 활성 대사산물의 용도를 포함한다. 일부 상황에서, 화합물은 호변이성질체로 존재한다. 모든 호변 이성질체는 본원에 개시된 화합물의 범위내에 포함된다. 또한, 본원에 개시된 화합물은 용매화되지 않거나 물, 에탄올 등과 같은 약제학적으로 허용가능한 용매로 용매화된 형태로 존재할 수도 있다. 본원에 기술된 화합물의 용매화된 형태가 또한 본원에 제시될 것으로 여겨진다.The methods and formulations described herein include N-oxides, crystalline forms (also known as polymorphs) or pharmaceutically acceptable salts of compounds having the structure of formula (I) as well as those compounds having the same active form. The use of active metabolites. In some situations, compounds exist as tautomers. All tautomers are included within the scope of the compounds disclosed herein. In addition, the compounds disclosed herein may exist in unsolvated or solvated form with a pharmaceutically acceptable solvent such as water, ethanol, and the like. It is contemplated that the solvated forms of the compounds described herein will also be presented herein.
약제학적 조성물Pharmaceutical composition
또 다른 일면은 일반식 (I) 또는 (II)의 화합물 및 약제학적으로 허용가능한 희석제, 부형제 또는 담체를 포함하는 약제학적 조성물이다.Another aspect is a pharmaceutical composition comprising a compound of formula (I) or (II) and a pharmaceutically acceptable diluent, excipient or carrier.
용어 "약제학적 조성물"은 일반식 (I)의 화합물과 다른 화학 성분, 이를 테면 담체, 안정화제, 희석제, 분산제, 현탁화제, 증점제 및/또는 부형제와의 혼합물을 말한다. 약제학적 조성물은 유기체에의 화합물의 투여를 촉진한다. 화합물의 투여 기술로는 정맥내, 경구, 에어졸, 비경구, 눈, 폐 및 국소 투여가 포함된다.The term "pharmaceutical composition" refers to a mixture of a compound of formula (I) with other chemical components, such as carriers, stabilizers, diluents, dispersants, suspending agents, thickeners and / or excipients. The pharmaceutical composition facilitates the administration of the compound to the organism. Techniques for administering the compounds include intravenous, oral, aerosol, parenteral, eye, lung and topical administration.
용어 "담체"란 세포 또는 조직으로의 화합물 도입을 촉진시키는 비교적 비독성인 화학적 화합물 또는 제제를 의미한다.The term "carrier" refers to a relatively non-toxic chemical compound or agent that promotes compound introduction into a cell or tissue.
용어 "희석제"란 관심의 대상이 되는 화합물을 전달하기 전에 이를 희석하기 위해 사용되는 화학적 화합물을 말한다. 희석제는 또한 보다 안정한 환경을 제공할 수 있기 때문에, 화합물을 안정화시키기 위해서도 사용된다. 완충액에 용해된 염(이는 또한 pH를 조절하거나 유지하기 위해 제공될 수 있다)은 희석제로서 사용되며, 인산염 완충 염수가 포함되나 이들에 한정되지 않는다.The term "diluent" refers to a chemical compound used to dilute a compound of interest before delivery. Diluents are also used to stabilize compounds, as they can provide a more stable environment. Salts dissolved in buffers (which may also be provided to adjust or maintain pH) are used as diluents, including but not limited to phosphate buffered saline.
용어 "생리학적으로 허용가능한"이란 화합물의 생물학적 활성 또는 특성을 붕괴시키지 않으면서 비독성인 물질, 이를 테면 담체 또는 희석제를 의미한다.The term "physiologically acceptable" means a non-toxic material, such as a carrier or diluent, without disrupting the biological activity or properties of the compound.
용어 "약제학적으로 허용가능한 염"이란 투여받는 유기체에 유의적인 자극을 일으키지 않으면서 생물학적 활성 또는 특성을 붕괴시키지 않는 화합물 제형을 의미한다. 하나의 구체예에서, 약제학적으로 허용가능한 염은 일반식 (I)의 화합물을 염화수소산, 브롬화수소산, 황산, 질산, 인산, 메탄설폰산, 에탄설폰산, p-톨루엔설폰산, 살리실산 등과 같은 산을 반응시켜 수득할 수 있다. 약제학적으로 허용가능한 염은 또한 일반식 (I)의 화합물을 염기와 반응시켜 암모늄염, 알칼리 금속염, 이를 테면 나트륨 염 또는 칼륨염, 알칼리 토금속염, 이를 테면 칼슘염 또는 마그네슘염, 유기염기의 염, 이를 테면 디사이클로헥실아민, N-메틸-D-글루카민, 트리스(하이드록시메틸) 메틸아민, 및 아미노산, 이를 테면 아르기닌, 리신 등과의 염을 형성함으로써 수득된다.The term "pharmaceutically acceptable salt" means a compound formulation that does not disrupt biological activity or properties without causing significant irritation to the organism to be administered. In one embodiment, the pharmaceutically acceptable salts include compounds of formula (I) such as hydrochloric acid, hydrobromic acid, sulfuric acid, nitric acid, phosphoric acid, methanesulfonic acid, ethanesulfonic acid, p-toluenesulfonic acid, salicylic acid, and the like. It can be obtained by reacting an acid. Pharmaceutically acceptable salts can also be prepared by reacting a compound of general formula (I) with a base, such as ammonium salts, alkali metal salts, such as sodium or potassium salts, alkaline earth metal salts such as calcium or magnesium salts, salts of organic bases, Such as dicyclohexylamine, N-methyl-D-glucamine, tris (hydroxymethyl) methylamine, and salts with amino acids such as arginine, lysine and the like.
본원에 기술된 화합물의 "대사산물"은 화합물이 대사될 때 형성되는 화합물의 유도체이다. 용어 "활성 대사산물"은 화합물이 대사될 때 형성되는 화합물의 생물학적 활성 유도체를 말한다. 용어 "대사되는"이란 특정 물질이 유기체에 의해 변화되는 모든 과정(가수분해 반응 및 효소에 의해 촉매되는 반응이 포함되나 이들에 한정되지 않는다)을 말한다. 따라서, 효소는 화합물에서 특정의 구조 변경을 일으킬 수 있다. 예를 들어, 시토크롬 P450은 다양한 산화 및 환원 반응을 촉매화시키는 반면, 유리딘 디포스페이트 글루쿠로닐트랜스페라제는 활성화된 글루쿠론산 분자가 방향족 알콜, 지방족 알콜, 카르복시산, 아민 및 유리 설프하이드릴기로 전이되는 것을 촉매한다. 대사에 대한 추가의 정보는 문헌[The Pharmacological Basis of Therapeutics, 9th Edition, McGraw-Hill(1996)]으로부터 입수된다.A “metabolite” of a compound described herein is a derivative of a compound that is formed when the compound is metabolized. The term "active metabolite" refers to a biologically active derivative of a compound that is formed when the compound is metabolized. The term "metabolized" refers to all processes in which a particular substance is changed by an organism, including but not limited to hydrolysis reactions and enzyme catalyzed reactions. Thus, enzymes can cause certain structural alterations in a compound. For example, cytochrome P 450 catalyzes a variety of oxidation and reduction reactions, while uridine diphosphate glucuronyltransferases can be used in the presence of activated glucuronic acid molecules such as aromatic alcohols, aliphatic alcohols, carboxylic acids, amines, and free sulfhi. Catalyze the transition to a drill. Further information on metabolism is obtained from The Pharmacological Basis of Therapeutics, 9th Edition, McGraw-Hill (1996).
일부 구체예에서, 본원에 기술된 화합물의 대사산물은 숙주에 화합물을 투여하고 숙주로부터의 조직 시료를 분석하거나, 화합물을 시험관내에서 간 세포와 배양하고 생산된 화합물을 분석함으로써 동정된다.In some embodiments, metabolites of a compound described herein are identified by administering the compound to a host and analyzing a tissue sample from the host, or incubating the compound with liver cells in vitro and analyzing the produced compound.
"전구약물"은 생체내에서 모약물로 전환되는 제제를 말한다. 전구약물은 특정 상황에서 모약물보다 투여가 용이할 수 있기 때문에, 종종 유용하다. 일부 구체예에서, 이들은 예를 들어 경구 투여에 의해 생체이용가능하나, 모약물은 그렇지 않다. 예를 들어, 전구약물은 또한 모약물보다 약제학적 조성물에서 향상된 용해성을 가진다. 전구약물의 예로는, 수-용해도가 이동성에 불리한 경우 세포막을 통한 투과를 촉진시키기 위해 에스테르("전구약물")로 투여되고, 수용해도가 유리한 세포내로 도입되면 활성 실체인 카르복시산으로 대사적으로 가수분해되는 일반식 (I)의 화합물이 포함되나 이에 한정되지 않는다. 전구약물의 추가예는 산 기에 결합된 짧은 펩티드(폴리아미노산)일 수 있으며, 이 경우 펩티드는 활성 부분을 드러내도록 대사된다."Prodrug" refers to an agent that is converted to the parent drug in vivo. Prodrugs are often useful because, in certain circumstances, they may be easier to administer than the parent drug. In some embodiments, they are bioavailable, for example by oral administration, but the parent drug is not. For example, prodrugs also have improved solubility in pharmaceutical compositions than parent drugs. Examples of prodrugs are administered as esters (“prodrugs”) to promote permeation through the cell membrane when water-solubility is disadvantageous to mobility, and metabolically hydrolyzed to the active entity carboxylic acid when introduced into cells where water solubility is favorable. Included but are not limited to compounds of formula (I) that decompose. Further examples of prodrugs may be short peptides (polyamino acids) bound to acid groups, in which case the peptides are metabolized to reveal the active moiety.
일부 구체예에서, 본원에 기술된 화합물은 그 자체로 또는 병용 요법으로 다른 활성 성분 또는 적절한 담체(들) 또는 부형제(들)와 혼합되어 있는 약제학적 조성물로 인간 환자에게 투여될 수 있다. 본 출원의 화합물의 제형화 및 투여 기술은 문헌["Remington: The Science and Practice of Pharmacy," 20th ed. (2000)]에서 찾아볼 수 있다.In some embodiments, the compounds described herein may be administered to a human patient, either by themselves or in combination therapy, in a pharmaceutical composition in admixture with other active ingredients or appropriate carrier (s) or excipient (s). Techniques for formulating and administering compounds of the present application are described in "Remington: The Science and Practice of Pharmacy," 20th ed. (2000).
투여 경로Route of administration
적절한 투여 경로로는 예를 들어 경구, 직장, 경점막, 경피, 폐내 또는 장 투여; 근육내, 피하, 정맥내, 골수내 주사, 및 경막내, 직접 뇌실내, 복강내, 비강내 또는 주사를 포함하는 비경구적 전달이 포함될 수 있다.Suitable routes of administration include, for example, oral, rectal, transmucosal, transdermal, intrapulmonary or intestinal administration; Intramuscular, subcutaneous, intravenous, intramedullary injections, and parenteral delivery, including intradural, direct intraventricular, intraperitoneal, intranasal or injection.
다르게는, 화합물은 예를 들어 화합물을 종종 데포제 또는 서방형 제형으로 기관에 직접 주입함으로써 전신적인 방식보다는 국소적으로 투여될 수도 있다. 또한, 리포좀은 기관에 의해 표적화되어 선택적으로 흡수될 것이다. 또한, 약물은 급속 방출형 제형의 형태, 지속 방출형 제형의 형태 또는 중간 방출형(intermediate release) 제형의 형태로 제공된다.Alternatively, the compound may also be administered topically rather than in a systemic manner, for example by injecting the compound directly into an organ, often in a depot or sustained release formulation. In addition, liposomes will be targeted and selectively absorbed by the organ. In addition, the drug is provided in the form of a rapid release formulation, in the form of a sustained release formulation or in the form of an intermediate release formulation.
조성물/제형Composition / Formulation
일반식 (I)의 화합물을 포함하는 약제학적 조성물은 공지된 방법 자체로, 예를 들어 통상적인 혼합, 용해, 과립화, 당의정 제조, 연화(levigating), 유화, 캡슐화, 포착화(entrapping) 또는 압축 공정에 의해 제조될 수 있다.Pharmaceutical compositions comprising a compound of formula (I) can be prepared by known methods, for example, by conventional mixing, dissolving, granulating, preparing a dragee, levigating, emulsifying, encapsulating, entrapping or It can be produced by a compression process.
예를 들어, 약제학적 조성물은 활성 화합물을 약제학적으로 사용될 수 있는 제형으로 가공하기에 용이한 부형제 및 보조제를 포함하는 하나 이상의 생리학적으로 허용가능한 담체를 사용하여 통상적인 방법으로 제형화될 수 있다. 적절한 제형은 선택한 투여 경로에 따라 달라진다.For example, pharmaceutical compositions may be formulated in a conventional manner using one or more physiologically acceptable carriers comprising excipients and auxiliaries that are easy to process the active compounds into formulations that can be used pharmaceutically. . Proper formulation is dependent upon the route of administration chosen.
일부 구체예에서, 일반식 (I) 또는 (II)의 화합물은 전신적, 이를 테면 경구적 또는 정맥내를 비롯한 다양한 방식으로 투여될 수 있다.In some embodiments, compounds of Formula (I) or (II) may be administered in a variety of ways, including systemically, such as orally or intravenously.
유용한 조성물은 또한 일반식 (I) 또는 (II)의 화합물의 용해를 돕는 가용화제를 포함할 수도 있다. 용어 "가용화제"는 일반적으로 제제의 교질 용액 또는 참 용액이 형성되도록 하는 제제를 포함한다. 허용가능한 특정의 비이온성 계면활성제, 예를 들어 폴리소르베이트 80이 허용가능한 글리콜, 폴리글리콜, 예를 들어 폴리에틸렌 글리콜 400 및 글리콜 에테르와 같이 가용화제로 유용할 수 있다.Useful compositions may also include solubilizers that aid in dissolution of the compound of formula (I) or (II). The term “solubilizer” generally includes formulations that allow a colloidal or true solution of the formulation to form. Certain acceptable nonionic surfactants such as
유용한 조성물은 또한 아세트산, 붕산, 시트르산, 락트산, 인산 및 염화수소산과 같은 산; 수산화나트륨, 인산나트륨, 붕산나트륨, 시트르산나트륨, 아세트산나트륨, 락트산나트륨 및 트리스-하이드록시메틸아미노메탄과 같은 염기; 및 시트르산염/덱스트로스, 중탄산나트륨 및 염화암모늄과 같은 완충제를 비롯한 하나 이상의 허용가능한 pH 조절제 또는 완충제를 포함할 수 있다. 이러한 산, 염기 및 완충제는 조성물의 pH를 허용가능한 범위로 유지하는데 필요한 양으로 포함된다.Useful compositions also include acids such as acetic acid, boric acid, citric acid, lactic acid, phosphoric acid and hydrochloric acid; Bases such as sodium hydroxide, sodium phosphate, sodium borate, sodium citrate, sodium acetate, sodium lactate and tris-hydroxymethylaminomethane; And one or more acceptable pH adjusting or buffering agents including buffers such as citrate / dextrose, sodium bicarbonate and ammonium chloride. Such acids, bases and buffers are included in the amounts necessary to maintain the pH of the composition in an acceptable range.
유용한 조성물은 또한 조성물의 삼투압을 허용가능한 범위로 제공하는데 필요한 양으로 하나 이상의 허용가능한 염을 포함할 수 있다. 이러한 염으로는 나트륨, 칼륨 또는 암모늄 양이온 및 염화물, 시트르산염, 아스코르브산염, 붕산염, 인산염, 중탄산염, 황산염, 티오황산염 또는 중아황산염 음이온을 가지는 것이 포함되며; 적합한 염으로는 염화나트륨, 염화칼륨, 티오황산나트륨, 중아황산나트륨 및 황산암모늄이 포함된다.Useful compositions may also include one or more acceptable salts in amounts necessary to provide osmotic pressure in the composition in an acceptable range. Such salts include those having sodium, potassium or ammonium cations and chlorides, citrates, ascorbates, borates, phosphates, bicarbonates, sulfates, thiosulfates or bisulfite anions; Suitable salts include sodium chloride, potassium chloride, sodium thiosulfate, sodium bisulfite and ammonium sulfate.
다른 유용한 조성물은 또한 세균 활성을 억제하기 위해 하나 이상의 허용가능한 보존제를 포함할 수 있다. 적합한 보존제로는 수은-함유 물질, 이를 테면 메르펜 및 티오메살; 안정화된 이산화염소; 및 사급 암모늄 화합물, 이를 테면 염화벤잘코늄, 브롬화 세틸트리메틸암모늄 및 염화 세틸피리디늄이 포함된다.Other useful compositions may also include one or more acceptable preservatives to inhibit bacterial activity. Suitable preservatives include mercury-containing materials such as merpenes and thiomesal; Stabilized chlorine dioxide; And quaternary ammonium compounds such as benzalkonium chloride, cetyltrimethylammonium bromide and cetylpyridinium chloride.
일부 구체예에서, 수성 현탁액 조성물은 일회량의 재밀봉 불가능 용기에 패킹될 수 있다. 또한, 다중회량의 재밀봉가능 용기가 사용될 수도 있으며, 이 경우에는 조성물에 보존제를 포함하는 것이 일반적이다.In some embodiments, the aqueous suspension composition may be packed in a single non-resealable container. Multiple doses of resealable containers may also be used, in which case it is common to include a preservative in the composition.
일반식 (I) 또는 (II)의 소수성 화합물에 대한 약제학적 담체는 벤질알콜, 비극성 계면활성제, 수혼화성 유기 폴리머 및 수성상을 포함하는 공용매 시스템이다. 공용매 시스템은 10% 에탄올, 10% 폴리에틸렌글리콜 300, 10% 폴리에틸렌글리콜 40 피마자유(PEG-40 피마자유)와 70% 수용액일 수 있다. 이러한 공용매 시스템은 소수성 화합물을 잘 용해시키고, 자체는 전신투여시 저독성이다. 예를 들어, 공용매 시스템의 비율은 그의 용해도 및 독성 특징을 파괴하지 않으면서 크게 달라질 수 있다. 또한, 공용매 성분의 본질이 달라질 수 있다: 예를 들어, 다른 저독성 비극성 계면활성제가 PEG-40 피마자유 대신 사용될 수 있고, 폴리에틸렌글리콜 300의 분획 크기가 달라질 수 있으며; 일부 구체예에서, 다른 생체적합성 폴리머가 폴리에틸렌글리콜, 예를 들어 폴리비닐피롤리돈을 대체할 수 있고; 다른 당 또는 폴리사카라이드가 수용액에 포함될 수 있다.Pharmaceutical carriers for the hydrophobic compounds of formula (I) or (II) are cosolvent systems comprising benzyl alcohol, nonpolar surfactants, water miscible organic polymers and aqueous phases. The cosolvent system may be 10% ethanol, 10
다르게는, 소수성 약제학적 화합물의 다른 전달 시스템이 이용될 수 있다. 리포좀 및 유제가 소수성 약물에 대한 전달 비히클 또는 담체의 예로 널리 알려져 있다. 통상적으로 독성이 더 크나, 일부 구체예에서, N-메틸피롤리돈과 같은 특정의 유기 용매가 또한 사용된다. 또한, 화합물은 예를 들어 서방형 방출 시스템, 이를 테면 치료제를 함유하는 고체 소수성 폴리머의 반투과성 매트릭스를 이용하여 전달된다. 서방형 방출 캅셀은 그의 화학적 성질에 따라 화합물을 수주 내지 100 일 동안 방출한다. 치료제의 화학적 성질 및 생물학적 안정성에 따라, 단백질 안정화를 위한 추가의 방법이 이용될 수 있다.Alternatively, other delivery systems of hydrophobic pharmaceutical compounds can be used. Liposomes and emulsions are well known as examples of delivery vehicles or carriers for hydrophobic drugs. Typically more toxic, but in some embodiments, certain organic solvents such as N-methylpyrrolidone are also used. In addition, the compounds are delivered using, for example, sustained release systems such as semipermeable matrices of solid hydrophobic polymers containing the therapeutic agent. Sustained release capsules release the compound for weeks to 100 days, depending on its chemistry. Depending on the chemical nature and biological stability of the therapeutic agent, additional methods for protein stabilization can be used.
본원에 기술된 모든 제형은 항산화제, 금속 킬레이트제, 티올 함유 화합물 및 다른 일반적인 안정화제로부터 이점을 얻을 수 있다. 이와 같은 안정화제의 예로 다음의 것들이 포함되나 이들에 한정되지 않는다: (a) 약 0.5% 내지 약 2% w/v 글리세롤, (b) 약 0.1% 내지 약 1% w/v 메티오닌, (c) 약 0.1% 내지 약 2% w/v 모노티오글리세롤, (d) 약 1 mM 내지 약 10 mM EDTA, (e) 약 0.01% 내지 약 2% w/v 아스코르브산, (f) 0.003% 내지 약 0.02% w/v 폴리소르베이트 80, (g) 0.001% 내지 약 0.05% w/v 폴리소르베이트 20, (h) 아르기닌, (i) 헤파린, (j) 덱스트란 설페이트, (k) 사이클로덱스트린, (l) 펜토산 폴리설페이트 및 기타 헤파리노이드, (m) 마그네슘 및 아연과 같은 2가 양이온; 또는 (n) 이들의 조합.All formulations described herein can benefit from antioxidants, metal chelating agents, thiol containing compounds and other common stabilizers. Examples of such stabilizers include, but are not limited to, the following: (a) about 0.5% to about 2% w / v glycerol, (b) about 0.1% to about 1% w / v methionine, (c) About 0.1% to about 2% w / v monothioglycerol, (d) about 1 mM to about 10 mM EDTA, (e) about 0.01% to about 2% w / v ascorbic acid, (f) 0.003% to about 0.02 % w /
일부 구체예에서, 일반식 (I) 또는 (II)의 화합물은 약제학적으로 적합한 카운터 이온과의 염으로도 제공될 수 있다. 일부 구체예에서, 약제학적으로 적합한 염은 염산, 황산, 아세트산, 락트산, 타르타르산, 말산, 숙신산 등이 포함되나 이들에 한정되지 않는 다수의 산으로 형성될 수 있다. 염은 상응하는 유리산 또는 염기 형태보다 수성 또는 다른 양성자성 용매에 잘 용해되는 경향을 보인다.In some embodiments, compounds of Formula (I) or (II) may also be provided as salts with pharmaceutically suitable counter ions. In some embodiments, pharmaceutically suitable salts may be formed with a number of acids, including but not limited to hydrochloric acid, sulfuric acid, acetic acid, lactic acid, tartaric acid, malic acid, succinic acid, and the like. Salts tend to dissolve better in aqueous or other protic solvents than the corresponding free acid or base forms.
경구 투여Oral administration
일부 구체예에서, 본원에 제공된 약제학적 조성물은 고체, 반고체 또는 액체 투여형으로 제공된다. 본원에 사용된 경구적 투여로는 또한 구강, 혀 및 설하 투여가 포함된다. 적합한 경구 투여형으로는 정제, 캡슐제, 환제, 트로키, 로젠지, 향제, 카세제, 환약, 약물첨가 츄잉 검, 과립제, 벌크형 산제, 발포성 또는 비발포성 산제 또는 과립제, 용액, 유액, 현탁액, 용액, 웨이퍼, 스프링클(sprinkle), 에릭시르제 및 시럽이 포함되나 이들에 한정되지 않는다. 활성 성분(들) 이외에, 일부 구체예에서, 약제학적 조성물은 결합제, 충전제, 희석제, 붕괴제, 습윤제, 윤활제, 유동화제, 착색제, 염료 이동 억제제, 감미제 및 착향제가 포함되나 이들에 한정되지 않는 하나 이상의 약제학적으로 허용가능한 담체 또는 부형제를 함유한다.In some embodiments, the pharmaceutical compositions provided herein are provided in solid, semisolid or liquid dosage forms. Oral administration as used herein also includes oral, tongue and sublingual administration. Suitable oral dosage forms include tablets, capsules, pills, troches, lozenges, flavors, cachets, pills, drug addition chewing gums, granules, bulk powders, effervescent or non-foamable powders or granules, solutions, emulsions, suspensions, Solutions include, but are not limited to, wafers, sprinkles, elixirs and syrups. In addition to the active ingredient (s), in some embodiments, the pharmaceutical composition includes, but is not limited to, binders, fillers, diluents, disintegrants, wetting agents, lubricants, glidants, colorants, dye transfer inhibitors, sweeteners, and flavoring agents. It contains one or more pharmaceutically acceptable carriers or excipients.
결합제 또는 과립화제는 정제에 대한 밀착성을 제공하여 압축 후에도 정제가 온전히 유지되도록 보증한다. 적합한 결합제 또는 과립화제로는 전분, 이를 테면 옥수수 전분, 감자 전분, 및 전호화(pre-gelatinized) 전분(예, 전분 1500); 젤라틴; 당, 이를 테면 수크로오스, 글루코오스, 덱스트로스, 당밀 및 락토오스; 천연 및 합성 검, 이를 테면 아카시아, 알긴산, 알기네이트, 주름 진두발(Irish moss)의 추출물, 판와르(Panwar) 검, 가티(ghatti) 검, 차전자 껍질의 점액(mucilage of isabgol husks), 카르복시메틸셀룰로오스, 메틸셀룰로오스, 폴리비닐피롤리돈(PVP), 비검(Veegum), 낙엽송 아라보갈락탄(larch arabogalactan), 분말 트라가캔스(트라가캔스), 및 구아 검; 셀룰로오스, 이를 테면 에틸 셀룰로오스, 셀룰로오스 아세테이트, 카르복시메틸 셀룰로오스 칼슘, 나트륨 카르복시메틸 셀룰로오스, 메틸 셀룰로오스, 하이드록시에틸셀룰로오스 (HEC), 하이드록시프로필셀룰로오스 (HPC), 하이드록시프로필 메틸 셀룰로오스 (HPMC); 미세결정성 셀룰로오스, 이를 테면 AVICEL-PH-101, AVICEL-PH-103, AVICEL RC-581, AVICEL-PH-105(펜실베니아 마커스 훅 소재 에프엠씨 코포레이션(FMC Corp.)); 및 이들의 혼합물이 포함되나 이들에 한정되지 않는다. 적합한 충전제로는 활석, 탄산칼슘, 미세결정성 셀룰로오스, 분말 셀룰로오스, 덱스트레이트, 카올린, 만니톨, 살리실산, 소르비톨, 전분, 전호화 전분 및 이들의 혼합물이 포함되나 이들에 한정되지 않는다. 일부 구체예에서, 결합제 또는 충전제는 본원에 제공된 약제학적 조성물에 약 50 내지 약 99 중량%로 존재한다.Binders or granulating agents provide adhesion to the tablets to ensure that the tablets remain intact after compression. Suitable binders or granulating agents include starch such as corn starch, potato starch, and pre-gelatinized starch (eg starch 1500); gelatin; Sugars such as sucrose, glucose, dextrose, molasses and lactose; Natural and synthetic gums such as acacia, alginic acid, alginate, extracts of Irish moss, Panwar gum, ghatti gum, mucilage of isabgol husks, carboxy Methylcellulose, methylcellulose, polyvinylpyrrolidone (PVP), veegum, larch arabogalactan, powdered tragacanth (tragacanth), and guar gum; Celluloses such as ethyl cellulose, cellulose acetate, carboxymethyl cellulose calcium, sodium carboxymethyl cellulose, methyl cellulose, hydroxyethyl cellulose (HEC), hydroxypropyl cellulose (HPC), hydroxypropyl methyl cellulose (HPMC); Microcrystalline celluloses such as AVICEL-PH-101, AVICEL-PH-103, AVICEL RC-581, AVICEL-PH-105 (FMC Corp., Marcus Hook, Pennsylvania); And mixtures thereof. Suitable fillers include, but are not limited to, talc, calcium carbonate, microcrystalline cellulose, powdered cellulose, dexrate, kaolin, mannitol, salicylic acid, sorbitol, starch, pregelatinized starch and mixtures thereof. In some embodiments, the binder or filler is present in about 50 to about 99 weight percent of the pharmaceutical composition provided herein.
적합한 희석제로는 인산칼슘, 황산칼슘, 락토오스, 소르비톨, 수크로오스, 이노시톨, 셀룰로오스, 카올린, 만니톨, 염화나트륨, 건성 전분 및 분말 당이 포함되나 이들에 한정되지 않는다. 특정 희석제, 이를 테면 만니톨, 락토오스, 소르비톨, 수크로오스 및 이노시톨은 충분한 양으로 존재하는 경우, 씹음으로써 입에서 붕해되도록 하는 일부 압축 정제에 특성을 부여한다. 일부 구체예에서, 이러한 압축 정제는 츄어블 정제로서 사용된다.Suitable diluents include, but are not limited to, calcium phosphate, calcium sulfate, lactose, sorbitol, sucrose, inositol, cellulose, kaolin, mannitol, sodium chloride, dry starch and powdered sugars. Certain diluents such as mannitol, lactose, sorbitol, sucrose and inositol, when present in sufficient amounts, characterize some compressed tablets that disintegrate in the mouth by chewing. In some embodiments, such compressed tablets are used as chewable tablets.
적합한 붕괴제로는 한천; 벤토나이트; 셀룰로오스, 이를 테면 메틸셀룰로오스 및 카르복시메틸셀룰로오스; 목제품; 천연 스펀지; 양이온 교환 수지; 알긴산; 검, 이를 테면 구아 검 및 비검(Veegum) HV; 시트러스 펄프; 가교결합 셀룰로오스, 이를 테면 크로스카르멜로스; 가교결합 중합제, 이를 테면 크로스포비돈; 가교결합 전분; 탄산칼슘; 미세결정성 셀룰로오스, 이를 테면 나트륨 전분 글리콜레이트; 폴라크린 칼륨; 전분, 이를 테면 옥수수 전분, 감자 전분, 타피오카 전분 및 전호화 전분; 점토; 알린(aligns); 및 이들의 혼합물이 포함되나 이들에 한정되지 않는다. 본원에 제공된 약제학적 조성물 중 붕괴제의 양은 제형의 형태에 따라 변화될 수 있다. 일부 구체예에서, 본원에 제공된 약제학적 조성물의 약 0.5 내지 약 15 중량% 또는 약 1 내지 약 5 중량%의 붕괴제를 함유한다.Suitable disintegrants include agar; Bentonite; Celluloses such as methylcellulose and carboxymethylcellulose; Wood products; Natural sponge; Cation exchange resins; Alginic acid; Gums such as guar gum and Veegum HV; Citrus pulp; Crosslinked celluloses such as croscarmellose; Crosslinked polymers such as crospovidone; Crosslinked starch; Calcium carbonate; Microcrystalline celluloses such as sodium starch glycolate; Polyacrine potassium; Starch such as corn starch, potato starch, tapioca starch and pregelatinized starch; clay; Aligns; And mixtures thereof. The amount of disintegrant in the pharmaceutical compositions provided herein can vary depending on the form of the formulation. In some embodiments, it contains about 0.5 to about 15 weight percent or about 1 to about 5 weight percent disintegrant of the pharmaceutical composition provided herein.
적합한 윤활제로는 스테아르산 칼슘; 스테아르산 마그네슘; 광유; 백색 광유; 글리세린; 소르비톨; 만니톨; 글리콜, 이를 테면 베헨산 글리세롤 및 폴리에틸렌 글리콜(PEG); 스테아르산; 나트륨 라우릴 설페이트; 활석; 낙화생유, 면실유, 해바라기유, 참깨유, 올리브유, 옥수수유 및 대두유를 비롯한 수소화 야채유; 아연 스테아레이트; 에틸 올레에이트; 에틸 라우레이트; 한천; 전분; 리코포듐(lycopodium); 실리카 또는 실리카 겔, 이를 테면 AEROSIL 200(메릴랜드 볼티모어 소재 더블유.알. 그레이스 코포레이션(W.R. Grace Co.)) 및 CAB-O-SIL®(메사추세츠 보스턴 소재 카보트 코포레이션(Cabot Co.)) 및 이들의 혼합물이 포함되나 이들에 한정되지 않는다. 일부 구체예에서, 본원에 제공된 약제학적 조성물은 약 0.1 내지 약 5 중량%의 윤활제를 함유한다.Suitable lubricants include calcium stearate; Magnesium stearate; Mineral oil; White mineral oil; glycerin; Sorbitol; Mannitol; Glycols such as glycerol behenate and polyethylene glycol (PEG); Stearic acid; Sodium lauryl sulfate; talc; Hydrogenated vegetable oils including peanut oil, cottonseed oil, sunflower oil, sesame oil, olive oil, corn oil and soybean oil; Zinc stearate; Ethyl oleate; Ethyl laurate; Agar; Starch; Lycopodium; Silica or silica gel such as AEROSIL 200 (WR Grace Co., Baltimore, MD) and CAB-O-SIL ® (Cabot Co., Boston, Mass.) And mixtures thereof Include but are not limited to these. In some embodiments, the pharmaceutical compositions provided herein contain about 0.1 to about 5 weight percent lubricant.
적합한 유동화제로는 콜로이드성 이산화규소, CAB-O-SIL®(메사추세츠 보스턴 소재 카보트 코포레이션(Cabot Co.)), 및 무석면 활석이 포함된다. 착색제로는 승인되고 보증된 수용성 FD&C 염료, 및 알루미나 수화물 위에 현탁된 수불용성 FD&C 염료, 및 안료 레이크(color lake) 및 이들의 혼합물 중 임의의 것이 포함된다. 안료 레이크는 중금속의 수화 산화물에 수용성 염료를 흡착시킴으로써 불용성 형태의 염료를 생산하는 조합물이다. 착향제로는 식물, 이를 테면 과일에서 추출한 천연 착향제 및 좋은 취향 감각, 이를 테면 페퍼민트 및 메틸 살리실레이트 및 페퍼민트와 같은 좋은 취향 감각을 생산하는 화합물의 합성 혼련물이 포함된다. 감미제로는 수크로오스, 락토오스, 만니톨, 시럽, 글리세린, 및 인공 감미제, 이를 테면 사카린 및 아스파탐이 포함된다. 적합한 유화제로는 젤라틴, 아카시아, 트라가캔스, 벤토나이트 및 계면활성제, 이를 테면 폴리옥시에틸렌 소르비탄 모노올레에이트(TWEEN® 20), 폴리옥시에틸렌 소르비탄 모노올레에이트 80(TWEEN® 80) 및 트리에탄올아민 올레에이트가 포함된다. 현탁화제 및 분산화제로는 나트륨 카르복시메틸셀룰로오스, 펙틴, 트라가캔스, 비검(Veegum), 아카시아, 나트륨 카보메틸셀룰로오스, 하이드록시프로필 메틸셀룰로오스 및 폴리비닐피롤리돈이 포함된다. 보존제로는 글리세린, 메틸 및 프로필 파라벤, 벤조산, 나트륨 벤조에이트 및 알코올이 포함된다. 습윤제로는 프로필렌글리콜 모노스테아레이트, 소르비탄 모노올레에이트, 디에틸렌 글리콜 모노라우레이트 및 폴리옥시에틸렌 라우릴 에테르가 포함된다. 용매로는 글리세린, 소르비톨, 에틸 알코올 및 시럽이 포함된다. 유액에 사용되는 비수성 액체의 예로는 광유 및 면실유가 포함된다. 유기산으로는 시트르산 및 타르타르산이 포함된다. 이산화탄소 원으로는 중탄산나트륨 및 탄산나트륨이 포함된다.Suitable fluidizing agents include colloidal silicon dioxide, CAB-O-SIL ® (Cabot Co., Boston, Mass.), And asbestos-free talc. Colorants include approved and certified water soluble FD & C dyes, and water insoluble FD & C dyes suspended on alumina hydrate, and any of pigment lakes and mixtures thereof. Pigment lakes are combinations that produce dyes in insoluble form by adsorbing a water soluble dye on a hydrated oxide of a heavy metal. Flavorants include natural flavors derived from plants, such as fruits, and synthetic blends of compounds that produce good taste sensations such as peppermint and methyl salicylate and peppermint. Sweetening agents include sucrose, lactose, mannitol, syrup, glycerin, and artificial sweeteners such as saccharin and aspartame. Suitable emulsifiers include gelatin, acacia, tragacanth, bentonite and surfactants such as polyoxyethylene sorbitan monooleate (TWEEN ® 20), polyoxyethylene sorbitan monooleate 80 (TWEEN ® 80) and triethanolamine Oleate is included. Suspending and dispersing agents include sodium carboxymethylcellulose, pectin, tragacanth, Veegum, acacia, sodium carbomethylcellulose, hydroxypropyl methylcellulose and polyvinylpyrrolidone. Preservatives include glycerin, methyl and propyl parabens, benzoic acid, sodium benzoate and alcohols. Wetting agents include propylene glycol monostearate, sorbitan monooleate, diethylene glycol monolaurate and polyoxyethylene lauryl ether. Solvents include glycerin, sorbitol, ethyl alcohol and syrup. Examples of non-aqueous liquids used in the emulsion include mineral oil and cottonseed oil. Organic acids include citric acid and tartaric acid. Sources of carbon dioxide include sodium bicarbonate and sodium carbonate.
일부 구체예에서, 경구적으로 사용되는 약제학적 제제로는 경구적으로 사용되는 약제학적 제제로는 젤라틴으로 만들어진 압입형(push-fit) 캅셀이 포함되며, 이들로는 단지 예로서 글리세롤 또는 솔비톨과 같은 가소제 및 젤라틴으로 제조된 밀봉 연질 캅셀; 또는 경질 겔 캅셀 또는 정제가 포함된다. 일부 구체예에서, 압입형 캅셀은 활성 성분을 락토오스와 같은 충전제, 전분과 같은 결합제 및/또는 활석 또는 마그네슘 스테아레이트와 같은 윤활제 및 임의로 안정화제와 혼합하여 함유한다. 일부 구체예에서, 연질 캅셀의 경우, 활성 화합물은 적합한 액체, 이를 테면 지방 오일, 액체 파라핀 또는 액체 폴리에틸렌글리콜에 용해 또는 현탁된다. 또한, 일부 구체예에서, 안정화제가 첨가된다. 모든 경구 투여용 제형은 이러한 투여에 적합한 투여량으로 존재하여야 한다.In some embodiments, orally used pharmaceutical preparations include orally used pharmaceutical preparations include push-fit capsules made of gelatin, which are only examples of glycerol or sorbitol, and Sealed soft capsules made of the same plasticizer and gelatin; Or hard gel capsules or tablets. In some embodiments, the indentable capsules contain the active ingredient in admixture with fillers such as lactose, binders such as starch and / or lubricants such as talc or magnesium stearate and optionally stabilizers. In some embodiments, for soft capsules, the active compounds are dissolved or suspended in suitable liquids, such as fatty oils, liquid paraffin, or liquid polyethylene glycols. In addition, in some embodiments, stabilizers are added. All oral dosage forms should be present in dosages suitable for such administration.
구강 또는 설하 투여의 경우, 일부 구체예에서, 조성물은 통상의 방식으로 제형화된 정제, 로젠지 또는 겔의 형태를 취할 수 있다.For oral or sublingual administration, in some embodiments, the composition may take the form of a tablet, lozenge or gel formulated in a conventional manner.
일부 구체예에서, 다수의 담체 및 부형제가 동일한 제형 내에서조차 몇 가지 기능을 제공하는 것으로 이해되어야 한다.In some embodiments, it should be understood that multiple carriers and excipients provide several functions even within the same formulation.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 압축 정제, 습제 정제, 츄어블 로젠지, 속용제, 다중 압축 정제 또는 장용 피복 정제, 당의정 또는 필름 피복 정제로서 제공된다. 장용 피복 정제는 위산의 작용에는 저항하지만 장에서 용해하거나 붕괴하며, 이로 인해 위의 산성 환경으로부터 활성 성분을 보호하는 물질로 코팅된 압축 정제이다. 장용 피복제로는 지방산, 지방, 페닐살리실레이트, 왁스, 쉘락, 암모니아성 쉘락 및 암모니아성 쉘락, 및 셀룰로오스 아세테이트 프탈레이트가 포함되나 이들에 한정되지 않는다. 당의정은 일부 구체예에서 불쾌한 맛 또는 향을 완전히 덮고 정제의 산화를 보호하는데 유리한 당 피복에 의한 둘러싸인 압축 정제이다. 필름 피복 정제는 수용성의 박층 또는 필름으로 덮은 압축 젱제이다. 필름 피복제로는 하이드록시에틸셀룰로오스, 나트륨 카르복시메틸셀룰로오스, 폴리에틸렌 글리콜 4000 및 셀룰로오스 아세테이트 프탈레이트가 포함되나 이들에 한정되지 않는다. 필름 코팅은 당 피복과 동일한 일반적인 특징을 부여한다. 다중 압축 정제는 층상 정제, 및 압축-피복 또는 건조-피복 정제를 비롯한 1 회 이상의 압축 사이클에 의해 제조된 압축 정제이다.In some embodiments, the pharmaceutical compositions provided herein are provided as compressed tablets, humectant tablets, chewable lozenges, rapid solvents, multiple compressed tablets or enteric coated tablets, dragees or film coated tablets. Enteric coated tablets are compressed tablets coated with a substance that resists the action of stomach acid but dissolves or disintegrates in the intestine, thereby protecting the active ingredient from the acidic environment of the stomach. Enteric coatings include, but are not limited to, fatty acids, fats, phenylsalicylates, waxes, shellac, ammonia shellac and ammonia shellac, and cellulose acetate phthalate. Dragees are, in some embodiments, enclosed compressed tablets with a sugar coating that completely covers the unpleasant taste or aroma and is beneficial in protecting the oxidation of the tablets. Film coated tablets are compression tablets covered with a water soluble thin layer or film. Film coatings include, but are not limited to, hydroxyethyl cellulose, sodium carboxymethyl cellulose,
일부 구체예에서, 정제 투여형은 분말, 결정 또는 과립 형태의 활성 성분 단독 또는 결합제, 붕괴제, 제어 방출 폴리머, 윤활제, 희석제 및/또는 착색제를 비롯한 본원에 개시된 하나 이상의 담체 또는 부형제와 함께 제공된다. 착향제 감미제는 츄어블 정제 및 로젠지의 형성에 특히 유용하다.In some embodiments, the tablet dosage form is provided with one or more carriers or excipients disclosed herein, including the active ingredient alone or as a binder, disintegrant, controlled release polymer, lubricant, diluent and / or colorant in powder, crystal or granular form. . Flavoring sweeteners are particularly useful for the formation of chewable tablets and lozenges.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 젤라틴, 메틸셀룰로오스, 전분, 또는 칼슘 알기네이트로부터 제조된 연질 또는 경질 캡슐로서 제공된다. 건식 충전 캡슐(dry-filled capsule, DFC)로도 알려진 경질 젤라틴은 두 부분으로 이루어지는데, 한 부분이 다른 부분을 덮어 활성 성분을 완전히 에워싼다. 연성 탄성 캡슐(soft elastic capsule, SEC)은, 글리세린, 소르비톨 또는 유사한 폴리올의 첨가에 의해 가소화된 부드러운 구상 쉘, 이를 테면 젤라틴 쉘이다. 일부 구체예에서, 연성 젤라틴 쉘은 미생물의 성장을 방지하는 보존제를 함유한다. 적합한 보존제는 메틸- 및 프로필-파라벤 및 소르빈산을 비롯한 본원에 기술된 것들이다. 일부 구체예에서, 본원에 제공된 액체, 반고체 및 고체 투여형은 캡슐로 캡슐화된다. 적합한 액체 및 반고체 투여형으로는 프로필렌 카보네이트, 야채유 또는 트리글리세리드 중의 현탁액 및 용액이 포함된다. 이러한 용액을 함유하는 캡슐은 예를 들어 미국 특허 제4,328,245호; 제4,409,239호; 및 제4,410,545호에 기술된 바와 같이 제조된다. 일부 구체예에서, 활성 성분(들)의 용해를 조정하거나 유지하도록 캡슐이 피복된다.In some embodiments, the pharmaceutical compositions provided herein are provided as soft or hard capsules made from gelatin, methylcellulose, starch, or calcium alginate. Hard gelatin, also known as dry-filled capsule (DFC), consists of two parts, one covering the other and completely enclosing the active ingredient. Soft elastic capsules (SECs) are soft spherical shells, such as gelatin shells, plasticized by the addition of glycerin, sorbitol or similar polyols. In some embodiments, the soft gelatin shell contains a preservative to prevent the growth of microorganisms. Suitable preservatives are those described herein, including methyl- and propyl-parabens and sorbic acid. In some embodiments, liquid, semisolid and solid dosage forms provided herein are encapsulated in a capsule. Suitable liquid and semisolid dosage forms include suspensions and solutions in propylene carbonate, vegetable oils or triglycerides. Capsules containing such solutions are described, for example, in US Pat. No. 4,328,245; No. 4,409,239; And 4,410,545. In some embodiments, the capsule is coated to adjust or maintain dissolution of the active ingredient (s).
일부 구체예에서, 본원에 제공된 약제학적 조성물은 유액, 용액, 현탁액, 에릭시르 및 시럽을 비롯한 액체 및 반고체 투여형으로 제공된다. 유액은 하나의 액체가 수중유 또는 유중수를 포함하는 또 다른 액체 전체에 작은 소구체의 형태로 분산된 2 상 시스템이다. 유액은 약제학적으로 허용가능한 비수성 액체 또는 용매, 유화제 및 보존제를 포함한다. 현탁액은 약제학적으로 허용가능한 현탁화제 및 보존제를 포함한다. 수성 알코올 용액은 약제학적으로 허용가능한 아세탈, 이를 테면 저급 알킬 알데히드의 디(저급 알킬)아세탈(용어 "저급"은 1 내지 6 개의 탄소원자를 가진 알킬을 의미한다), 예를 들어 아세트알데히드 디에틸 아세탈; 및 하나 이상의 하이드록실기를 가진 수혼화성 용매, 이를 테면 프로필렌글리콜 및 에탄올을 포함한다. 에릭시르는 투명하고 감미된 함수알코올 용액이다. 시럽은 당의 농축 수용액, 예를 들어 수크로오스이며, 또한 보존제를 함유한다. 액체 투여형의 경우, 예를 들어 폴리에틸렌글리콜의 용액은 투여에 용이하도록 평가된 충분한 양의 약제학적으로 허용가능한 액체 담체, 예를 들어 물로 희석된다.In some embodiments, the pharmaceutical compositions provided herein are provided in liquid and semisolid dosage forms, including emulsions, solutions, suspensions, elixirs, and syrups. Latex is a two-phase system in which one liquid is dispersed in the form of small globules throughout another liquid, including oil-in-water or water-in-oil. Latexes include pharmaceutically acceptable non-aqueous liquids or solvents, emulsifiers and preservatives. Suspensions include pharmaceutically acceptable suspending agents and preservatives. Aqueous alcohol solutions are pharmaceutically acceptable acetals such as di (lower alkyl) acetals of lower alkyl aldehydes (the term "lower" means alkyl having from 1 to 6 carbon atoms), for example acetaldehyde diethyl acetal ; And water miscible solvents having one or more hydroxyl groups, such as propylene glycol and ethanol. Ericsir is a clear, sweet solution of hydrous alcohol. The syrup is a concentrated aqueous solution of sugar, for example sucrose, and also contains a preservative. In the case of liquid dosage forms, for example a solution of polyethylene glycol is diluted with a sufficient amount of a pharmaceutically acceptable liquid carrier, for example water, to be evaluated for ease of administration.
다른 유용한 액체 및 반고체 투여형으로는 1,2-디메톡시메탄, 디글림, 트리글림, 테트라글림, 폴리에틸렌 글리콜-350-디메틸 에테르, 폴리에틸렌 글리콜-550-디메틸 에테르, 폴리에틸렌 글리콜-750-디메틸 에테르를 비롯한 디알킬화 모노- 또는 폴리-알킬렌 글리콜 및 본원에 제공된 활성 성분(들)을 함유하는 것들이 포함되나 이들에 한정되지 않으며, 여기서 350, 550 및 750은 폴리에틸렌 글리콜의 대략적인 평균 분자량을 말한다. 일부 구체예에서, 이들 제형은 하나 이상의 항산화제, 이를 테면 부틸화 하이드록시톨루엔(BHT), 부틸화 하이드록시아니솔(BHA), 프로필 갈레이트, 비타민 E, 하이드로퀴논, 하이드록시쿠마린, 에탄올아민, 레시틴, 세팔린, 아스코르브산, 말산, 소르비톨, 인산, 바이설파이트, 나트륨 메타비설파이트, 티오디프로피온산 및 그의 에스테르, 및 디티오카바메이트를 추가로 포함한다.Other useful liquid and semisolid dosage forms include 1,2-dimethoxymethane, diglyme, triglyme, tetraglyme, polyethylene glycol-350-dimethyl ether, polyethylene glycol-550-dimethyl ether, polyethylene glycol-750-dimethyl ether Including, but not limited to, dialkylated mono- or poly-alkylene glycols and those containing the active ingredient (s) provided herein, where 350, 550, and 750 refer to approximate average molecular weights of polyethylene glycol. In some embodiments, these formulations contain one or more antioxidants, such as butylated hydroxytoluene (BHT), butylated hydroxyanisole (BHA), propyl gallate, vitamin E, hydroquinone, hydroxycoumarin, ethanolamine , Lecithin, cephalin, ascorbic acid, malic acid, sorbitol, phosphoric acid, bisulfite, sodium metabisulfite, thiodipropionic acid and esters thereof, and dithiocarbamate.
일부 구체예에서, 경구 투여를 위한 본원에 제공된 약제학적 조성물은 또한 리포솜, 마이셀, 미세구 또는 나노계의 형태로 제공된다. 일부 구체예에서, 마이셀 투여형은 미국 특허 제6,350,458호에 기술된 바와 같이 제조된다.In some embodiments, the pharmaceutical compositions provided herein for oral administration are also provided in the form of liposomes, micelles, microspheres or nanosystems. In some embodiments, the micelle dosage form is prepared as described in US Pat. No. 6,350,458.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 액체 투여형으로 재구성될 비-기포성 및 기포성 과립제 및 분말로서 제공된다. 일부 구체예에서, 비-기포성 과립제 또는 분말에 사용되는 약제학적으로 허용가능한 담체 및 부형제로는 희석제, 감미제 및 습윤제가 포함된다. 일부 구체예에서, 기포성 과립제 또는 분말에 사용되는 약제학적으로 허용가능한 담체 및 부형제로는 이산화탄소의 공급원 및 유기산이 포함된다.In some embodiments, the pharmaceutical compositions provided herein are provided as non-bubble and foamy granules and powders to be reconstituted into liquid dosage forms. In some embodiments, pharmaceutically acceptable carriers and excipients used in non-bubble granules or powders include diluents, sweeteners, and wetting agents. In some embodiments, pharmaceutically acceptable carriers and excipients used in aerated granules or powders include sources of carbon dioxide and organic acids.
일부 구체예에서, 착색제 및 착향제는 상기 투여형 모두에 사용된다.In some embodiments, colorants and flavoring agents are used in both of the above dosage forms.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 지연-, 지속-, 펄스-, 제어-, 표적- 및 계획-방출형을 비롯한 즉시형 또는 변형 방출 투여형으로 제형화된다.In some embodiments, the pharmaceutical compositions provided herein are formulated in immediate or modified release dosage forms, including delayed-, sustained-, pulsed-, controlled-, targeted- and planned-release forms.
비경구적Parenteral 투여 administration
일부 구체예에서, 본원에 제공된 약제학적 조성물은 국소 또는 전신 투여를 위한 주사, 주입 또는 이식에 의해 비경구적으로 투여도니다. 본원에 사용된 비경구적 투여로는 정맥내, 동맥내, 복강내, 척수강내, 뇌실내, 요도내, 흉골내, 두개내, 근육내, 활막내 및 피하 투여가 포함된다.In some embodiments, the pharmaceutical compositions provided herein are administered parenterally by injection, infusion or implantation for topical or systemic administration. Parenteral administration as used herein includes intravenous, intraarterial, intraperitoneal, intrathecal, intraventricular, urethral, intrasternal, intracranial, intramuscular, intravitreal and subcutaneous administration.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 용액, 현탁액, 유액, 마이셀, 리포솜, 미세구, 나노계, 및 주사전 용액 중 현탁액 또는 용액에 적합한 고체형을 비롯한 비경구적 투여에 적합한 임의의 투여형으로 제형화된다. 일부 구체예에서, 이러한 투여형은 통상의 방법에 따라 제조된다.(예를 들어, 문헌[Remington: The Science and Practice of Pharmacy]을 참조할 수 있다).In some embodiments, the pharmaceutical compositions provided herein are any administration suitable for parenteral administration, including solid forms suitable for suspensions or solutions in solutions, suspensions, emulsions, micelles, liposomes, microspheres, nanobased, and pre-injection solutions. Formulated in the form. In some embodiments, such dosage forms are prepared according to conventional methods (see, eg, Remington: The Science and Practice of Pharmacy).
일부 구체예에서, 비경구적 투여용으로 의도된 약제학적 조성물은 수성 비히클, 수혼화성 비히클, 비수성 비히클, 항균 제제 또는 미생물의 성장 보존제, 안정화제, 용해촉진제, 등장화제, 완충제, 항산화제, 국소 마취제, 현탁화 및 분산화 제제, 습윤화 또는 유화 제제, 착화제, 금속이온봉쇄 또는 레이트 제제, 침투촉진제, 세포냉동보호제, 동결건조보호제, 증점제, pH 조정제 및 불활성 기체가 포함되나 이들에 한정되지 않는, 하나 이상의 약제학적으로 허용가능한 담체를 포함한다.In some embodiments, pharmaceutical compositions intended for parenteral administration include aqueous vehicles, water miscible vehicles, non-aqueous vehicles, antimicrobial or microbial growth preservatives, stabilizers, solubilizers, isotonic agents, buffers, antioxidants, topical Include, but are not limited to, anesthetics, suspensions and dispersing agents, wetting or emulsifying agents, complexing agents, metal ion-blocking or latent agents, penetration enhancers, cell cryoprotectants, lyophilizers, thickeners, pH adjusters and inert gases And one or more pharmaceutically acceptable carriers.
적합한 수성 비히클로는 물, 염수, 생리학적 염수 또는 인산 완충 염수(PBS), 염화나트륨 주사액, 링거 주사액, 등장성 덱스트로스 주사액, 멸균수 주사액, 덱스트로스 및 하트만 용액(lactated Ringer)이 포함되나 이들에 한정되지 않는다. 비수성 비히클로는 식물 유래 고정유, 피마자유, 옥수수유, 면실유, 올리브유, 낙화생유, 박하유, 홍화유, 참깨유, 대두유, 수소화 야채유, 수소화 대두유, 및 코코넛유 및 팜핵유의 중쇄 트리글리세리드가 포함되나 이들에 한정되지 않는다. 수혼화성 비히클로는 에탄올, 1,3-부탄디올, 액체 폴리에틸렌 글리콜(예, 폴리에틸렌 글리콜 300 및 폴리에틸렌 글리콜 400), 프로필렌글리콜, 글리세린, N-메틸-2-피롤리돈, 디메틸아세트아미드 및 디메틸 설폭시드가 포함되나 이들에 한정되지 않는다.Suitable aqueous vehicles include, but are not limited to, water, saline, physiological saline or phosphate buffered saline (PBS), sodium chloride injections, Ringer's injections, isotonic dextrose injections, sterile water injections, dextrose and Hartmann Ringer's solutions. It is not limited. Non-aqueous vehicles include plant-derived fixed oil, castor oil, corn oil, cottonseed oil, olive oil, peanut oil, peppermint oil, safflower oil, sesame oil, soybean oil, hydrogenated vegetable oil, hydrogenated soybean oil, and medium-chain triglycerides of coconut and palm kernel oils. It is not limited to these. Water-miscible vehicles include ethanol, 1,3-butanediol, liquid polyethylene glycols (
적합한 항균 제제 또는 보존제로는 페놀, 크레졸, 수은제, 벤질 알코올, 클로로부탄올, 메틸 및 프로필 p-하이드록시벤조에이트, 티메로살, 벤즈알코늄 클로라이드, 벤즈에토늄 클로라이드, 메틸- 및 프로필-파라벤 및 소르빈산이 포함되나 이들에 한정되지 않는다. 적합한 등장화제로는 염화나트륨, 글리세린 및 덱스트로스가 포함되나 이들에 한정되지 않는다. 적합한 완충제로는 포스페이트 및 시트레이트가 포함되나 이들에 한정되지 않는다. 적합한 항산화제는 비설파이트 및 나트륨 메타비설파이트를 비롯한 본원에 기술된 것들이다. 적합한 국소 마취제로는 프로카인 하이드로클로라이드가 포함되나 이에 한정되지 않는다. 적합한 현탁화 및 분산화 제제는 나트륨 카르복시메틸셀룰로오스, 하이드록시프로필 메틸셀룰로오스 및 폴리비닐피롤리돈을 비롯한 본원에 기술된 것들이다. 적합한 유화제로는 폴리옥시에틸렌 소르비탄 모노라우레이트, 폴리옥시에틸렌 소르비탄 모노올레에이트 80 및 트리에탄올아민 올레에이트를 비롯한 본원에 기술된 것들이 포함된다. 적합한 금속이온봉쇄 또는 킬레이트 제제로는 EDTA가 포함되나 이들에 한정되지 않는다. 적합한 pH 조정제로는 나트륨 하이드록시드, 염화수소산, 시트르산 및 락트산이 포함되나 이들에 한정되지 않는다. 적합한 착화제로는 α-사이클로덱스트린, β-사이클로덱스트린, 하이드록시프로필-β-사이클로덱스트린, 설포부틸에테르-β-사이클로덱스트린 및 설포부틸에테르 7-β-사이클로덱스트린 (CAPTISOL®, CyDex, Lenexa, KS)을 비롯한 사이클로덱스트린이 포함되나 이에 한정되지 않는다.Suitable antimicrobial agents or preservatives include phenol, cresol, mercury, benzyl alcohol, chlorobutanol, methyl and propyl p-hydroxybenzoate, thimerosal, benzalkonium chloride, benzethonium chloride, methyl- and propyl-paraben and Sorbic acid is included but is not limited thereto. Suitable isotonic agents include but are not limited to sodium chloride, glycerin and dextrose. Suitable buffers include, but are not limited to, phosphates and citrate. Suitable antioxidants are those described herein, including bisulfite and sodium metabisulfite. Suitable local anesthetics include but are not limited to procaine hydrochloride. Suitable suspending and dispersing agents are those described herein, including sodium carboxymethylcellulose, hydroxypropyl methylcellulose and polyvinylpyrrolidone. Suitable emulsifiers include those described herein including polyoxyethylene sorbitan monolaurate, polyoxyethylene sorbitan monooleate 80 and triethanolamine oleate. Suitable metalion blockade or chelating agents include, but are not limited to, EDTA. Suitable pH adjusting agents include, but are not limited to, sodium hydroxide, hydrochloric acid, citric acid and lactic acid. Suitable complexing agents include α-cyclodextrin, β-cyclodextrin, hydroxypropyl-β-cyclodextrin, sulfobutylether-β-cyclodextrin and sulfobutylether 7-β-cyclodextrin (CAPTISOL ® , CyDex, Lenexa, KS Cyclodextrins, including), but are not limited to these.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 단일 또는 복수 투여로 투여하기 위해 제형화된다. 단일 투여 제형은 앰플, 바이얼 또는 시린지에 충전된다. 복수 투여용 비경구 제형은 정균 또는 정진균 농도로 항균 제제를 함유해야 한다. 모든 비경구 제형은 멸균되어야 한다.In some embodiments, the pharmaceutical compositions provided herein are formulated for single or multiple administration. Single dose formulations are filled in ampoules, vials or syringes. Parenteral formulations for multiple administration should contain antimicrobial agents at bacteriostatic or bacteriostatic concentrations. All parenteral formulations must be sterile.
하나의 구체예에서, 약제학적 조성물은 즉시사용형 멸균 용액으로 제공된다. 또 다른 구체예에서, 약제학적 조성물은 사용하기 전에 비히클과 함께 재구성될, 동결건조 분말 및 피하 정제를 비롯한 멸균 가용성 건조 제품으로 제공된다. 또 다른 구체예에서, 약제학적 조성물은 즉시사용형 멸균 현탁액으로 제공된다. 또 다른 구체예에서, 약제학적 조성물은 사용하기 전에 비히클과 함께 재구성될 멸균 가용성 건조 제품으로 제공된다. 또 다른 구체예에서, 약제학적 조성물은 즉시사용형 멸균 유액으로 제공된다.In one embodiment, the pharmaceutical composition is provided in a ready-to-use sterile solution. In another embodiment, the pharmaceutical composition is provided in a sterile soluble dry product, including lyophilized powder and subcutaneous tablet, to be reconstituted with the vehicle prior to use. In another embodiment, the pharmaceutical composition is provided in a ready-to-use sterile suspension. In another embodiment, the pharmaceutical composition is provided as a sterile soluble dry product to be reconstituted with the vehicle prior to use. In another embodiment, the pharmaceutical composition is provided in a ready-to-use sterile milk.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 지연-, 지속-, 펄스-, 제어-, 표적- 및 계획-방출형을 비롯한 즉시 또는 변형 방출 투여형으로 제형화된다.In some embodiments, the pharmaceutical compositions provided herein are formulated in immediate or modified release dosage forms, including delayed-, sustained-, pulsed-, controlled-, targeted- and planned-release forms.
일부 구체예에서, 약제학적 조성물은 이식 데포제로서 투여하기 위한 고체, 반고체 또는 요변성(thixotropic) 액체인 현탁액으로서 제형화된다. 하나의 구체예에서, 본원에 제공된 약제학적 조성물은 고체형 내부 매트릭스에 분산되며, 이 고체형 내부 매트릭스는 약제학적 조성물 중의 활성 성분(들)을 확산하게 하는 외부 폴리머 막에 의해 둘러싸여 있다.In some embodiments, the pharmaceutical composition is formulated as a suspension that is a solid, semisolid or thixotropic liquid for administration as a transplant depot. In one embodiment, the pharmaceutical compositions provided herein are dispersed in a solid inner matrix, which is surrounded by an outer polymeric membrane that allows the active ingredient (s) to diffuse in the pharmaceutical composition.
적합한 내부 매트릭스로는 폴리메틸메타크릴레이트, 폴리부틸메타크릴레이트, 가소화 또는 비가소화 폴리비닐클로라이드, 가소화 나일론, 가소화 폴리에틸렌테레프탈레이트, 천연 고무, 폴리이소프렌 폴리가소부틸렌, 폴리부타디엔, 폴리에틸렌, 에틸렌-비닐아세테이트 코폴리머, 실리콘 고무, 폴리디메틸실록산, 실리콘 카보네이트 코폴리머, 친수성 폴리머, 이를 테면 아크릴산 및 메타크릴산 에스테르의 하이드로겔, 콜라겐, 가교결합 폴리비닐알코올, 및 부분 가수분해된 가교결합 폴리비닐 아세테이트가 포함된다.Suitable internal matrices include polymethylmethacrylate, polybutylmethacrylate, plasticized or unplasticized polyvinylchloride, plasticized nylon, plasticized polyethylene terephthalate, natural rubber, polyisoprene polyisobutylene, polybutadiene, polyethylene , Ethylene-vinylacetate copolymers, silicone rubbers, polydimethylsiloxanes, silicone carbonate copolymers, hydrophilic polymers such as hydrogels, collagen, crosslinked polyvinyl alcohols of acrylic and methacrylic esters, and partially hydrolyzed crosslinks Polyvinyl acetate is included.
적합한 외부 폴리머 막으로는 폴리에틸렌, 폴리프로필렌, 에틸렌/프로필렌 코폴리머, 에틸렌/에틸 아크릴레이트 코폴리머, 에틸렌/비닐아세테이트 코폴리머, 실리콘 고무, 폴리디메틸 실록산, 네오프렌 고무, 염소화 폴리에틸렌, 폴리비닐클로라이드, 비닐 아세테이트, 비닐리덴 클로라이드, 에틸렌 및 프로필렌과의 비닐클로라이드 코폴리머, 이오노머 폴리에틸렌 테레프탈레이트, 부틸 고무 에피클로로하이드린 고무, 에틸렌/비닐 알코올 코폴리머, 에틸렌/비닐 아세테이트/비닐 알코올 터폴리머 및 에틸렌/비닐 옥시에탄올 코폴리머가 포함된다.Suitable outer polymer membranes include polyethylene, polypropylene, ethylene / propylene copolymers, ethylene / ethyl acrylate copolymers, ethylene / vinylacetate copolymers, silicone rubber, polydimethyl siloxane, neoprene rubber, chlorinated polyethylene, polyvinylchloride, vinyl Vinyl chloride copolymer with acetate, vinylidene chloride, ethylene and propylene, ionomer polyethylene terephthalate, butyl rubber epichlorohydrin rubber, ethylene / vinyl alcohol copolymer, ethylene / vinyl acetate / vinyl alcohol terpolymer and ethylene / vinyl oxy Ethanol copolymers are included.
일부 구체예에서, 정맥 주사의 경우 일반식 (I) 또는 (II)의 화합물은 수용액, 바람직하게는 생리학적으로 적합한 완충액, 이를 테면 행크 용액, 링거액 또는 생리학적 식염 완충액으로 제형화된다. 경점막 투여의 경우, 침투할 장벽에 적합한 침투제가 제형에 사용된다. 다른 비경구적 주사의 경우, 일부 구체예에서, 적절한 제형은 수성 또는 비수성 용액을, 바람직하게는 생리학적으로 적합한 완충액 또는 부형제와 함께 포함한다.In some embodiments, for intravenous injection, the compounds of formula (I) or (II) are formulated in aqueous solutions, preferably in physiologically suitable buffers such as Hank's solution, Ringer's solution or physiological saline buffer. For transmucosal administration, penetrants suitable for the barrier to penetrate are used in the formulation. For other parenteral injections, in some embodiments, a suitable formulation comprises an aqueous or nonaqueous solution, preferably with a physiologically suitable buffer or excipient.
화합물은, 일부 구체예에서 주사에 의해, 예를 들어 볼루스 주사 또는 연속 주입에 의해 비경구적으로 투여하기 위해 제형화된다. 일부 구체예에서, 주사용 제형은 부가적인 보존제와 함께 단위 투여형, 예를 들어 앰플 또는 복수-투여 용기로 존재한다. 일부 구체예에서, 조성물은 유성 또는 수성 비히클 중의 현탁액, 용액 또는 유액과 같은 형태를 취하며, 현탁화, 안정화 및/또는 분산화 제제와 같은 제형화 제제를 함유한다.The compounds are formulated for parenteral administration in some embodiments by injection, for example by bolus injection or continuous infusion. In some embodiments, the injectable formulation is in unit dosage form, eg, in ampoules or in multi-dose containers, with additional preservatives. In some embodiments, the composition takes the form of a suspension, solution or emulsion in an oily or aqueous vehicle, and contains a formulation formulation, such as a suspension, stabilization and / or dispersing formulation.
비경구적 투여용 약제학적 제형으로는 수용성 형태로 활성 화합물의 수용액이 포함된다. 부가적으로, 일부 구체예에서, 활성 화합물의 현탁액이 적절한 유성 주사 현탁액으로서 제조된다. 적합한 친유성 용매 또는 비히클로는 지방 오일, 이를 테면 참깨유, 또는 합성 지방산 에스테르, 이를 테면 에틸 올레에이트 또는 트리글리세리드, 또는 리포솜이 포함된다. 수성 주사 현탁액은, 일부 구체예에서, 현탁액의 점도를 증가시키는 물질, 이를 테면 나트륨 카르복시메틸 셀룰로오스, 소르비톨 또는 덱스트란을 함유한다. 임의로, 현탁액은 또한 적합한 안정화제 또는 고농도 용액을 제조하도록 화합물의 용해도를 증가시키는 제제를 함유한다.Pharmaceutical formulations for parenteral administration include aqueous solutions of the active compounds in water-soluble form. Additionally, in some embodiments, suspensions of the active compounds are prepared as appropriate oily injection suspensions. Suitable lipophilic solvents or vehicles include fatty oils such as sesame oil, or synthetic fatty acid esters such as ethyl oleate or triglycerides, or liposomes. Aqueous injection suspensions, in some embodiments, contain substances that increase the viscosity of the suspension, such as sodium carboxymethyl cellulose, sorbitol or dextran. Optionally, the suspension also contains an agent which increases the solubility of the compound to produce a suitable stabilizer or high concentration solution.
다르게는, 활성 성분(들)은 사용전 적합한 비히클, 예를 들어 발열원-무함유 멸균수와 함께 구성하기 위한 분말형으로 존재한다. Alternatively, the active ingredient (s) are in powder form for constitution with a suitable vehicle, eg pyrogen-free sterile water, before use.
일부 구체예에서, 화합물은 코코아 버터 또는 다른 글리세리드와 같은 통상의 좌제 기제를 함유하는 직장용 조성물, 이를 테면 직장용 겔, 직장용 포말, 직장용 에어로졸, 좌제 또는 정체 관장제로 제형화된다.In some embodiments, the compounds are formulated in rectal compositions containing conventional suppository bases, such as cocoa butter or other glycerides, such as rectal gels, rectal foams, rectal aerosols, suppositories, or retention enemas.
앞서 기술된 제형 이외에, 일부 구체예에서 화합물은 데포 제제로 제형화된다. 이러한 장시간 작용하는 제형은 이식에 의하거나(예를 들어 피하 또는 근육내) 근육내 주사에 의해 투여된다. 따라서, 예를 들어 화합물은 적합한 폴리머 또는 소수성 물질(예를 들어 허용가능한 오일 중 유액으로서) 또는 이온 교환 수지와 함께 또는 난용성 유도체, 예를 들어 난용성 염으로 제형화된다.In addition to the formulations described above, in some embodiments the compound is formulated as a depot preparation. Such long acting formulations are administered by implantation (for example subcutaneously or intramuscularly) or by intramuscular injection. Thus, for example, the compounds are formulated with suitable polymers or hydrophobic materials (eg as emulsions in acceptable oils) or ion exchange resins or with poorly soluble derivatives such as poorly soluble salts.
주사가능 데포 제형은, 일부 구체예에서 생분해가능 폴리머 중에서 일반식 (I) 또는 (II)의 화합물의 미세캡슐화 매트릭스(미세캡슐 매트릭스로도 공지됨)를 형성함으로써 제조된다. 폴리머에 대한 약물의 비율 및 사용되는 특정 폴리머의 성질에 따라, 약물 방출 속도가 제어된다. 주사가능 데포 제형은 일부 구체예에서, 미세유액 또는 리포솜에 약물을 포획시킴으로써 제조된다. 단지 예로서, 후방 공막옆(posterior juxtascleral) 데포제가 일반식 (I) 또는 (II)의 구조를 가진 화합물의 투여 모드로서 사용될 수 있다. 공막은 대부분의 척추동물의 눈을 감싸고 있는 고도로 배향된 콜라겐 네트워크로 구성된 얇은 무혈관층이다. 공막은 무혈관이기 때문에, 주사된 물질이 눈으로부터 신속히 제거되거나 없어지지 않는 천연 저장 데포제로서 사용된다. 일부 구체예에서, 눈의 공막층에 투여하기 위해 사용되는 화합물의 제형은 공막층 주사에 적합한 직경이 작은 캐뉼라를 통한 주사에 의해 공막에 적용하기에 적합한 임의의 형태이다. 주사가능한 적용 형태의 예는 용액, 현탁액 또는 콜리이드성 현탁액이다.Injectable depot formulations are prepared in some embodiments by forming microencapsulation matrices (also known as microcapsule matrices) of compounds of formula (I) or (II) in biodegradable polymers. Depending on the ratio of drug to polymer and the nature of the particular polymer used, the rate of drug release is controlled. Injectable depot formulations are prepared in some embodiments by entrapping the drug in microfluidic or liposomes. By way of example only, a posterior juxtascleral depot can be used as the mode of administration of a compound having the structure of Formula (I) or (II). The sclera is a thin, avascular layer composed of a highly oriented collagen network that wraps the eyes of most vertebrates. Because the sclera is bloodless, it is used as a natural storage depot that the injected material does not quickly remove or disappear from the eye. In some embodiments, the formulation of the compound used for administration to the sclera of the eye is in any form suitable for application to the sclera by injection through a small diameter cannula suitable for scleral layer injection. Examples of injectable application forms are solutions, suspensions or colloidal suspensions.
국소 투여Topical administration
본원에 제공된 약제학적 조성물은, 일부 구체예에서 피부, 개구부 또는 점막에 국소적으로 투여된다. 본원에 사용된 국소 투여로는 진피(내), 결막, 각막내, 안내, 안과적, 귀내, 경피, 비강, 질, 요도, 호흡기 및 직장 투여가 포함된다.The pharmaceutical compositions provided herein are administered topically to the skin, openings or mucous membranes in some embodiments. Topical administration as used herein includes dermal (intra), conjunctival, corneal, intraocular, ophthalmic, ear, transdermal, nasal, vaginal, urethral, respiratory and rectal administration.
본원에 제공된 약제학적 조성물은, 일부 구체예에서 유액, 용액, 현탁액, 크림, 겔, 하이드로겔, 연고, 산포제, 드레싱, 에릭시르, 로션, 현탁액, 딩크제, 페이스트, 포말, 필름, 에어로졸, 세척제, 스프레이, 좌제, 붕대, 경피 패치제를 비롯한 국소 또는 전신 효과를 위한 국소 투여에 적합한 임의의 투여형으로 제형화된다. 일부 구체예에서, 본원에 제공된 약제학적 조성물의 국소 제형은 또한 리포솜, 마이셀, 미세구, 나노구 또는 나노입자 및 이들의 혼합물을 포함한다.The pharmaceutical compositions provided herein may, in some embodiments, be emulsions, solutions, suspensions, creams, gels, hydrogels, ointments, dispersants, dressings, elixirs, lotions, suspensions, dikes, pastes, foams, films, aerosols, It is formulated in any dosage form suitable for topical or systemic administration, including washes, sprays, suppositories, bandages, transdermal patches. In some embodiments, topical formulations of the pharmaceutical compositions provided herein also include liposomes, micelles, microspheres, nanospheres or nanoparticles and mixtures thereof.
일반식 (I) 또는 (II)의 구조를 가진 화합물을 투여하기 위한 다른 유용한 제형으로는 경피 전달 장치("패치제")가 사용된다. 이러한 경피용 패치제는 일부 구체예에서 본원의 화합물을 제어된 양으로 연속적이거나 비연속적으로 주입하기 위해 사용될 수 있다. 약제학적 제제를 전달하기 위한 경피용 패치제의 구조 및 용도의 예는 미국 특허 제5,023,252호에서 찾아볼 수 있다. 일부 구체예에서, 이러한 패치제는 연속적으로, 펄스적으로 또는 약제학적 제제의 전달 요구에 따라 제작될 수 있다. 또 다른 추가의 일부 구체예에서, 일반식 (I) 또는 (II)의 화합물의 경피 전달은 이온삼투성 패치제 등의 수단에 의해 달성된다. 경피용 패치제는 화합물의 전달을 제어할 수 있다. 일부 구체예에서, 속도-제어막을 사용하거나 화합물을 폴리머 매트릭스 또는 겔 내에 포획하여 흡수율을 느리게 조절할 수 있다. 반대로, 일부 구체예에서, 흡수촉진제를 사용하여 흡수율을 증가시킬 수 있다. 일부 구체예에서, 경피 투여에 적합한 제형은 분리된 패치제로 존재할 수 있으며, 폴리머 또는 점착제에 용해되고/용해되거나 분산된 친유성 유제 또는 수성 완충액일 수 있다.As another useful formulation for administering a compound having the structure of Formula (I) or (II), transdermal delivery devices (“patches”) are used. Such transdermal patch agents may be used in some embodiments to inject continuously or discontinuously in a controlled amount of a compound of this disclosure. Examples of the structure and use of transdermal patches for the delivery of pharmaceutical preparations can be found in US Pat. No. 5,023,252. In some embodiments, such patches can be made continuously, pulsed or as required for delivery of the pharmaceutical formulation. In yet another additional embodiment, transdermal delivery of a compound of formula (I) or (II) is achieved by means such as iontophoretic patching agents. Transdermal patch agents can control delivery of the compound. In some embodiments, the rate of absorption can be slowed by using a rate-controlling membrane or by entrapping the compound in a polymer matrix or gel. Conversely, in some embodiments, absorption accelerators may be used to increase the absorption rate. In some embodiments, formulations suitable for transdermal administration may be in separate patches and may be lipophilic emulsions or aqueous buffers dissolved and / or dispersed in a polymer or tackifier.
본원에 제공된 국소 제형에 사용하기에 적합한 약제학적으로 허용가능한 담체 및 부형제로는 수성 비히클, 수혼화성 비히클, 비수성 비히클, 항균 제제 또는 미생물의 성장 보존제, 안정화제, 용해촉진제, 등장화제, 완충제, 항산화제, 국소 마취제, 현탁화 및 분산화 제제, 습윤화 또는 유화 제제, 착화제, 금속이온봉쇄 또는 레이트 제제, 침투촉진제, 세포냉동보호제, 동결건조보호제, 증점제 및 불활성 기체가 포함되나 이들에 한정되지 않는다.Pharmaceutically acceptable carriers and excipients suitable for use in the topical formulations provided herein include aqueous vehicles, water miscible vehicles, non-aqueous vehicles, antimicrobial agents or growth preservatives, stabilizers, solubilizers, isotonic agents, buffers, Antioxidants, local anesthetics, suspending and dispersing preparations, wetting or emulsifying preparations, complexing agents, metal ion block or rate preparations, penetration enhancers, cell cryoprotectants, lyophilizers, thickeners and inert gases. Do not.
일부 구체예에서, 약제학적 조성물은 전기천공법, 이온삼투요법, 음성영동법, 초음파영동법 및 현미침법 또는 무바늘 주사법, 이를 테면 POWDERJECTTM(캘리포니아 에머리빌 소재 시론 코포레이션(Chiron Corp.)) 및 BIOJECTTM(오리건 투알라틴 소재 바이오젝트 메디컬 테크놀러지 인코포레이션(Bioject Medical Technologies Inc.))에 의해 국소적으로 투여된다.In some embodiments, the pharmaceutical compositions are electroporation, iontophoresis, negative electrophoresis, ultrasonography and microneedle or needleless injection methods such as POWDERJECT ™ (Chiron Corp., Emeryville, CA) and BIOJECT ™ (Bioject Medical Technologies Inc., Tualatin, Oregon).
일부 구체예에서, 본원에 제공된 약제학적 조성물은 연고, 크림 및 겔의 형태로 제공된다. 적합한 연고 비히클로는 유성 또는 탄화수소 비히클, 이를 테면 돈지, 벤조인지(benzoinated lard), 올리브유, 면실유 및 다른 오일, 백색 바셀린; 유화성 또는 흡수성 비히클, 이를 테면 친수성 바셀린, 하이드록시스테아린 설페이트 및 무수 라놀린; 탈수성 비히클, 이를 테면 친수성 연고; 다양한 분자량의 폴리에틸렌 글리콜을 비롯한 수용성 연고 비히클; 세틸 알코올, 글리세릴 모노스테아레이트, 라놀린 및 스테아르산을 비롯한 유중수(W/O) 유제 또는 수중유(O/W) 유제의 유제 비히클이 포함된다(상기한 문헌[The Science and Practice of Pharmacy]을 참조할 수 있다). 이들 비히클은 연화제이나 일반적으로 항산화제 및 보존제의 첨가를 필요로 한다.In some embodiments, the pharmaceutical compositions provided herein are provided in the form of ointments, creams and gels. Suitable ointment vehicles include oily or hydrocarbon vehicles such as lard, benzoinated lard, olive oil, cottonseed oil and other oils, white petrolatum; Emulsifiable or absorbent vehicles such as hydrophilic petrolatum, hydroxystealine sulfate and anhydrous lanolin; Dehydrated vehicles, such as hydrophilic ointments; Water soluble ointment vehicles including polyethylene glycols of various molecular weights; Emulsion vehicles of water-in-oil (W / O) emulsions or oil-in-water (O / W) emulsions, including cetyl alcohol, glyceryl monostearate, lanolin and stearic acid are described (The Science and Practice of Pharmacy, supra). See). These vehicles are softeners but generally require the addition of antioxidants and preservatives.
일부 구체예에서, 적합한 크림 기제는 수중유 또는 유중수이다. 일부 구체예에서, 크림 비히클은 수세성이며, 오일상, 유화제 및 수성상을 함유한다. 오일상은 또한 일반적으로 바셀린 및 지방 알코올, 이를 테면 세틸 또는 스테아릴 알코올로 구성된, "내부" 상이라고도 불린다. 수성상은 필수적이지는 않지만 주로 다량으로 오일상을 초과하며, 일반적으로 보습제를 함유한다. 크림 제형의 유화제는 비이온성, 음이온성, 양이온성 또는 양성 계면활성제를 포함한다.In some embodiments, a suitable cream base is oil-in-water or water-in-oil. In some embodiments, the cream vehicle is flushable and contains an oil phase, an emulsifier and an aqueous phase. The oil phase is also commonly referred to as the "inner" phase, consisting of petrolatum and fatty alcohols, such as cetyl or stearyl alcohol. The aqueous phase is not essential but mainly exceeds the oil phase in large quantities and generally contains a humectant. Emulsifiers in cream formulations include nonionic, anionic, cationic or amphoteric surfactants.
겔은 반고체의 현탁액 형태의 시스템이다. 단상 겔은 액체 담체 전체에 실질적으로 균일하게 분포된 유기 고분자를 함유한다. 적합한 겔화제로는 가교결합 아크릴산 폴리머, 이를 테면 카보머, 카르복시폴리알킬렌, 카보폴(Carbopol®); 친수성 폴리머, 이를 테면 폴리에틸렌 옥사이드, 폴리옥시에틸렌-폴리옥시프로필렌 코폴리머 및 폴리비닐알코올; 셀룰로오스성 폴리머, 이를 테면 하이드록시프로필 셀룰로오스, 하이드록시에틸 셀룰로오스, 하이드록시프로필 메틸셀룰로오스, 하이드록시프로필 메틸셀룰로오스 프탈레이트 및 메틸셀룰로오스; 검, 이를 테면 트라가캔스 및 크산탄 검; 나트륨 알기네이트; 및 젤라틴이 포함된다. 일부 구체예에서, 균일한 겔을 제조하기 위해, 알코올 또는 글리세린과 같은 분산제 또는 분쇄, 기계적 혼합 및/또는 교반에 의해 분산된 겔화제가 첨가된다.Gels are systems in the form of semisolid suspensions. Single-phase gels contain organic polymers that are substantially uniformly distributed throughout the liquid carrier. Suitable gelling agents include crosslinked acrylic acid polymers, Carbomer For instance, carboxy polyalkylene, Carbopol (Carbopol ®); Hydrophilic polymers such as polyethylene oxide, polyoxyethylene-polyoxypropylene copolymer and polyvinyl alcohol; Cellulosic polymers such as hydroxypropyl cellulose, hydroxyethyl cellulose, hydroxypropyl methylcellulose, hydroxypropyl methylcellulose phthalate and methylcellulose; Gums such as tragacanth and xanthan gum; Sodium alginate; And gelatin. In some embodiments, dispersants such as alcohols or glycerin are added or gelling agents dispersed by grinding, mechanical mixing and / or stirring to prepare a uniform gel.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 좌제, 질 좌제, 요도 좌제, 찜질제 또는 습포제, 페이스트, 분말, 드레싱, 크림, 석고, 피임약, 연고, 용액, 유액, 현탁액, 탐폰, 겔, 포말, 스프레이 또는 관장제의 형태로 직장 투여, 요도 투여, 질 투여 또는 질주위 투여된다. 일부 구체예에서, 이들 투여형은 상기 문헌[Remington: The Science and Practice of Pharmacy]에 개시된 바와 같은 통상의 공정을 사용하여 제조된다.In some embodiments, the pharmaceutical compositions provided herein comprise suppositories, vaginal suppositories, urethral suppositories, poultices or poultices, pastes, powders, dressings, creams, gypsum, contraceptives, ointments, solutions, emulsions, suspensions, tampons, gels, foams Rectal, urethral, vaginal or vaginal administration, in the form of a spray or enema. In some embodiments, these dosage forms are prepared using conventional processes as disclosed in Remington: The Science and Practice of Pharmacy, supra.
직장, 요도 및 질 좌제는 상온에서 고체이나 체온에서 용융 또는 연화하여 개구부내로 활성 성분(들)을 방출하는, 신체 개구부로 삽입하기 위한 고체이다. 직장 및 질 좌제에 사용되는 약제학적으로 허용가능한 담체로는 본원에 제공된 약제학적 조성물과 함께 제형화되는 경우 체온에 가까운 융점을 생성하는 강직화 제제와 같은 기제 또는 비히클; 및 비설파이트 및 나트륨 메타비설파이트를 비롯한 본원에 기술된 항산화제가 포함된다. 적합한 비히클로는 코코아 버터(테오브로마 오일), 글리세린-젤라틴, 카보왁스(폴리옥시에틸렌 글리콜), 경랍, 파라핀, 백색 및 황색 왁스, 지방산의 모노-, 디- 및 트리글리세리드의 적절한 혼합물, 하이드로겔, 이를 테면 폴리비닐 알코올, 하이드록시에틸 메타크릴레이트, 폴리아크릴산; 글리세린화 젤라틴이 포함되나 이들에 한정되지 않는다. 일부 구체예에서 다양한 비히클의 조합물이 사용된다. 직장 및 질 좌제는 일부 구체예에서, 압축 방법 또는 성형에 의해 제조된다. 직장 및 질 좌제의 전형적인 중량은 약 2 내지 약 3 g이다.Rectal, urethral, and vaginal suppositories are solids for insertion into the body openings, which melt or soften at room temperature or soften at body temperature to release the active ingredient (s) into the openings. Pharmaceutically acceptable carriers for use in rectal and vaginal suppositories include bases or vehicles, such as an upright formulation, which when formulated with the pharmaceutical compositions provided herein produce a melting point close to body temperature; And antioxidants described herein, including bisulfite and sodium metabisulfite. Suitable vehicles include cocoa butter (theobroma oil), glycerin-gelatin, carbowax (polyoxyethylene glycol), mercury, paraffin, white and yellow waxes, suitable mixtures of mono-, di- and triglycerides of fatty acids, hydrogels Such as polyvinyl alcohol, hydroxyethyl methacrylate, polyacrylic acid; Glycerylated gelatin is included, but is not limited to these. In some embodiments combinations of various vehicles are used. Rectal and vaginal suppositories are prepared in some embodiments by compression methods or molding. Typical weights of rectal and vaginal suppositories are about 2 to about 3 g.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 용액, 현탁액, 연고, 유액, 겔-형성 용액, 용액용 분말, 겔, 안내 삽입물 및 이식물의 형태로 눈에 투여된다.In some embodiments, the pharmaceutical compositions provided herein are administered to the eye in the form of solutions, suspensions, ointments, emulsions, gel-forming solutions, powders for solutions, gels, intraocular inserts and implants.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 비강내 또는 기도로의 흡입에 의해 투여된다. 일부 구체예에서, 약제학적 조성물은 가압 용기, 펌프, 스프레이, 아토마이저(atomizer), 이를 테면 전기수력학을 이용하여 미세 분무를 생성하는 아토마이저, 네뷸라이저를 단독으로 또는 적합한 분사제, 이를 테면 1,1,1,2-테트라플루오로에탄 또는 1,1,1,2,3,3,3-헵타플루오로프로판과 함께 사용하여 전달하기 위한 에어로졸 또는 용액의 형태로 제공된다. 약제학적 조성물은, 일부 구체예에서 단독 또는 락토오스 또는 인지질과 같은 불활성 담체와 함께 흡입을 위한 건조 분말; 및 점비액으로서 제공된다. 비강내 사용을 위해, 일부 구체예에서 분말은 키토산 또는 사이클로덱스트린을 비롯한 생체결합성 제제를 포함한다.In some embodiments, the pharmaceutical compositions provided herein are administered by inhalation intranasally or by airway. In some embodiments, the pharmaceutical composition may be a pressurized container, a pump, a spray, an atomizer, such as an atomizer, a nebulizer alone or a suitable propellant, such as an electrohydraulic, to produce a fine spray. It is provided in the form of an aerosol or solution for delivery using 1,1,1,2-tetrafluoroethane or 1,1,1,2,3,3,3-heptafluoropropane. The pharmaceutical composition may, in some embodiments, be a dry powder for inhalation alone or in combination with an inert carrier such as lactose or phospholipids; And nasal drops. For intranasal use, in some embodiments the powder comprises biobinding agents including chitosan or cyclodextrins.
일부 구체예에서, 가압 용기, 펌프, 스프레이, 아토마이저 및 네뷸라이저에 사용하기 위한 용액 또는 현탁액은 에탄올, 수성 에탄올, 또는 본원에 제공된 활성 성분(들)의 방출을 분산화, 가용화 또는 확장화하기 위한 적합한 다른 제제, 용매로서 분사제; 및/또는 계면활성제, 이를 테면 소르비탄 트리올레에이트, 올레산 또는 올리고락트산을 함유하도록 제형화된다.In some embodiments, solutions or suspensions for use in pressurized vessels, pumps, sprays, atomizers and nebulizers are used to disperse, solubilize or expand the release of ethanol, aqueous ethanol, or the active ingredient (s) provided herein. Other suitable agents, propellants as solvents; And / or surfactants such as sorbitan trioleate, oleic acid or oligolactic acid.
일부 구체예에서, 본원에 제공된 약제학적 조성물은 흡입에 의한 투여에 적합한 크기, 이를 테면 50 마이크로미터 이하, 또는 약 10 마이크로미터 이하로 미분화된다. 이러한 크기의 입자는, 일부 구체예에서 분쇄 방법, 이를 테면 와류식 제트밀(spiral jet milling), 유동상(fluid bed) 제트밀, 나노입자 형성을 위한 초임계 유체 처리공정, 고압 균질화 또는 스프레이 건조를 사용하여 제조된다.In some embodiments, the pharmaceutical compositions provided herein are micronized to a size suitable for administration by inhalation, such as 50 micrometers or less, or about 10 micrometers or less. Particles of this size may, in some embodiments, be pulverized, such as spiral jet milling, fluid bed jet mills, supercritical fluid processing for nanoparticle formation, high pressure homogenization or spray drying. It is prepared using.
일부 구체예에서, 흡입기 또는 취입기에 사용하기 위한 캡슐, 블리스터 및 카트리지는 본원에 제공된 약제학적 조성물의 분말 믹스; 적합한 분말 기제, 이를 테면 락토오스 또는 전분; 및 성능 조절제, 이를 테면 l-류신, 만니톨 또는 스테아르산 마그네슘을 함유하도록 제형화된다. 락토오스는 무수 형태 또는 일수화물의 형태를 포함한다. 다른 적합한 부형제 또는 담체로는 덱스트란, 글루코오스, 말토스, 소르비톨, 자일리톨, 프룩토스, 수크로오스 및 트레할로오스가 포함된다. 일부 구체예에서, 흡입/비강내 투여를 위한 본원에 제공된 약제학적 조성물은 적합한 착향제, 이를 테면 멘톨 및 레보멘톨, 또는 감미제, 이를 테면 사카린 또는 사카린 나트륨을 추가로 포함한다.In some embodiments, capsules, blisters and cartridges for use in an inhaler or blower comprise a powder mix of a pharmaceutical composition provided herein; Suitable powder bases such as lactose or starch; And performance modifiers such as l-leucine, mannitol or magnesium stearate. Lactose includes anhydrous forms or monohydrate forms. Other suitable excipients or carriers include dextran, glucose, maltose, sorbitol, xylitol, fructose, sucrose and trehalose. In some embodiments, the pharmaceutical compositions provided herein for inhalation / intranasal administration further comprise suitable flavoring agents, such as menthol and levomenthol, or sweetening agents, such as saccharin or saccharin sodium.
일부 구체예에서, 국소 투여를 위한 본원에 제공된 약제학적 조성물은 지연-, 지속-, 펄스-, 제어-, 표적- 및 계획-방출을 포함하여 즉시 방출 또는 변형 방출되도록 제형화된다.In some embodiments, the pharmaceutical compositions provided herein for topical administration are formulated for immediate release or modified release, including delayed-, sustained-, pulsed-, controlled-, target- and scheduled-release.
변형 방출Strain release
본원에 제공된 약제학적 조성물은, 일부 구체예에서 변형 방출 투여형으로 제형화된다. 본원에 사용된 용어 "변형 방출"은 활성 성분(들)의 방출 속도 또는 부위가 동일한 경로에 의해 투여되는 경우 즉시 투여형의 것과 상이한 투여형을 말한다. 변형 방출 투여형으로는 지연-, 확장-, 장기-, 지속-, 펄스-, 제어-, 가속- 및 신속-, 표적-, 계획-방출, 및 위내 체류 투여형이 포함된다. 변형 방출 투여형의 약제학적 조성물은 매트릭 제어 방출 장치, 삼투성 제어 방출 장치, 복합미립자 제어 방출 장치, 이온 교환 수지, 장용 피복, 다층 코팅, 미세구, 리포솜 및 이들의 조합이 포함되나 이들에 한정되지 않는 다양한 변형 방출 장치 및 방법을 사용하여 제조된다. 일부 구체예에서, 활성 성분(들)의 방출 속도는 활성 성분(들)의 입자 크기 및 다형성을 변화시킴으로써 변형된다.The pharmaceutical compositions provided herein are formulated in a modified release dosage form in some embodiments. As used herein, the term “modified release” refers to a dosage form that is different from that of an immediate dosage form when the rate or site of release of the active ingredient (s) is administered by the same route. Modified release dosage forms include delayed-, extended-, long-term, sustained-, pulsed-, controlled-, accelerated- and rapid-, target-, planned-release, and intragastric retention dosage forms. Pharmaceutical compositions of modified release dosage forms include, but are not limited to, matrix controlled release devices, osmotic controlled release devices, multiparticulate controlled release devices, ion exchange resins, enteric coatings, multilayer coatings, microspheres, liposomes, and combinations thereof. And various modified release devices and methods. In some embodiments, the release rate of the active ingredient (s) is modified by changing the particle size and polymorphism of the active ingredient (s).
변형 방출의 예로는 미국 특허 제3,845,770호; 제3,916,899호; 제3,536,809호; 제3,598,123호; 제4,008,719호; 제5,674,533호; 제5,059,595호; 제5,591,767호; 제5,120,548호; 제5,073,543호; 제5,639,476호; 제5,354,556호; 제5,639,480호; 제5,733,566호; 제5,739,108호; 제5,891,474호; 제5,922,356호; 제5,972,891호; 제5,980,945호; 제5,993,855호; 제6,045,830호; 제6,087,324호; 제6,113,943호; 제6,197,350호; 제6,248,363호; 제6,264,970호; 제6,267,981호; 제6,376,461호; 제6,419,961호; 제6,589,548호; 제6,613,358호; 및 제6,699,500호에 개시된 것들이 포함되나 이들에 한정되지 않는다.Examples of modified releases include US Pat. No. 3,845,770; 3,916,899; 3,536,809; 3,536,809; 3,598,123; 3,598,123; 4,008,719; 4,008,719; No. 5,674,533; 5,059,595; 5,059,595; 5,591,767; 5,591,767; 5,120,548; 5,073,543; 5,639,476; 5,639,476; 5,354,556; 5,354,556; 5,639,480; 5,639,480; 5,733,566; 5,739,108; 5,739,108; 5,891,474; 5,891,474; 5,922,356; 5,922,356; 5,972,891; 5,972,891; 5,980,945; 5,980,945; 5,993,855; 5,993,855; 6,045,830; 6,045,830; 6,087,324; 6,087,324; No. 6,113,943; No. 6,197,350; 6,248,363; 6,248,363; 6,264,970; 6,264,970; 6,267,981; 6,267,981; 6,376,461; 6,376,461; 6,419,961; 6,419,961; No. 6,589,548; No. 6,613,358; And 6,699,500, including, but not limited to.
1. 매트릭스 제어 방출 장치1. Matrix controlled release device
변형 방출 투여형의 본원에 제공된 약제학적 조성물은, 일부 구체예에서 매트릭스 제어 방출 장치를 사용하여 제작된다(예를 들어, 문헌[Takada et al in "En사이클로pedia of Controlled Drug Delivery,"Vol. 2, Mathiowitz ed., Wiley, 1999]을 참조할 수 있다).Pharmaceutical compositions provided herein of modified release dosage forms are, in some embodiments, made using matrix controlled release devices (eg, Takada et al in "Encyclopedia of Controlled Drug Delivery," Vol. 2 , Mathiowitz ed., Wiley, 1999).
하나의 구체예에서, 변형 방출 투여형의 본원에 제공된 약제학적 조성물은 합성 폴리머 및 자연발생 폴리머 및 유도체, 이를 테면 폴리사카라이드 및 단백질을 비롯한 수-팽윤성, 침식성 또는 가용성 폴리머인 침식성 매트릭스 장치를 사용하여 제형화된다.In one embodiment, a pharmaceutical composition provided herein of a modified release dosage form uses an erosive matrix device that is a water-swellable, erosive or soluble polymer, including synthetic polymers and naturally occurring polymers and derivatives such as polysaccharides and proteins. Formulated.
침식성 매트릭스를 형성하는데 유용한 물질로는 키틴, 키토산, 덱스트란 및 풀루란; 검 한천, 검 아라비아, 검 카라야, 로우커스트 빈 검, 검 트라가캔스, 카라기난, 검 가티, 구아 검, 크산탄 검, 및 스클레로글루칸; 전분, 이를 테면 덱스트린 및 말토덱스트린; 친수성 콜로이드, 이를 테면 펙틴; 포스파티드, 이를 테면 레시틴; 알기네이트; 프로필렌글리콜 알기네이트; 젤라틴; 콜라겐; 및 셀룰로시스, 이를 테면 에틸 셀룰로오스(EC), 메틸에틸 셀룰로오스(MEC), 카르복시메틸 셀룰로오스(CMC), CMEC, 하이드록시에틸 셀룰로오스(HEC), 하이드록시프로필 셀룰로오스(HPC), 셀룰로오스 아세테이트(CA), 셀룰로오스 프로피오네이트(CP), 셀룰로오스 부티레이트(CB), 셀룰로오스 아세테이트 부티레이트(CAB), CAP, CAT, 하이드록시프로필 메틸 셀룰로오스(HPMC), HPMCP, HPMCAS, 하이드록시프로필 메틸 셀룰로오스 아세테이트 트리멜리테이트(HPMCAT) 및 에틸하이드록시 에틸셀룰로오스(EHEC); 폴리비닐 피롤리돈; 폴리비닐 알코올; 폴리비닐 아세테이트; 글리세롤 지방산 에스테르; 폴리acrylamide; 폴리아크릴산; 에타크릴 산 또는 메타크릴 산의 코폴리머(EUDRAGIT®, Rohm America, Inc., Piscataway, NJ); 폴리(2-하이드록시에틸-메타크릴레이트); 폴리락티드; L-글루탐산 및 에틸-L-글루타메이트의 코폴리머; 분해가능한 락트산-글리콜산 코폴리머; 폴리-D-(-)-3-하이드록시부티르산; 및 다른 아크릴산 유도체, 이를 테면 부틸메타크릴레이트, 메틸메타크릴레이트, 에틸메타크릴레이트, 에틸아크릴레이트, (2-디메틸아미노에틸)메타크릴레이트 및 (트리메틸아미노에틸)메타크릴레이트 클로라이드의 호모폴리머 및 코폴리머가 포함되나 이들에 한정되지 않는다.Materials useful for forming an erosive matrix include chitin, chitosan, dextran, and pullulan; Gum agar, gum arabian, gum karaya, locust bean gum, gum tragacanth, carrageenan, gum gatti, guar gum, xanthan gum, and scleroglucan; Starch such as dextrin and maltodextrin; Hydrophilic colloids such as pectin; Phosphatides such as lecithin; Alginate; Propylene glycol alginate; gelatin; Collagen; And cellulose, such as ethyl cellulose (EC), methylethyl cellulose (MEC), carboxymethyl cellulose (CMC), CMEC, hydroxyethyl cellulose (HEC), hydroxypropyl cellulose (HPC), cellulose acetate (CA), Cellulose propionate (CP), cellulose butyrate (CB), cellulose acetate butyrate (CAB), CAP, CAT, hydroxypropyl methyl cellulose (HPMC), HPMCP, HPMCAS, hydroxypropyl methyl cellulose acetate trimellitate (HPMCAT) And ethyl hydroxy ethyl cellulose (EHEC); Polyvinyl pyrrolidone; Polyvinyl alcohol; Polyvinyl acetate; Glycerol fatty acid esters; Polyacrylamide; Polyacrylic acid; Copolymers of etacrylic acid or methacrylic acid (EUDRAGIT ® , Rohm America, Inc., Piscataway, NJ); Poly (2-hydroxyethyl-methacrylate); Polylactide; Copolymers of L-glutamic acid and ethyl-L-glutamate; Degradable lactic acid-glycolic acid copolymers; Poly-D-(-)-3-hydroxybutyric acid; And other acrylic acid derivatives such as butyl methacrylate, methyl methacrylate, ethyl methacrylate, ethyl acrylate, (2-dimethylaminoethyl) methacrylate and (trimethylaminoethyl) methacrylate chloride and Copolymers are included, but are not limited to these.
추가의 구체예에서, 약제학적 조성물은 비-침식성 매트릭스 장치로 제형화된다. 활성 성분(들)은 불활성 매트릭스에 용해되거나 분산되고, 일단 투여되면 불활성 매트릭스를 통해 확산됨으로써 일차적으로 방출된다. 비-침식성 매트릭스 장치로서 사용하기에 적합한 물질로는 불용성 가소제, 이를 테면 폴리에틸렌, 폴리프로필렌, 폴리이소프렌 폴리가소부틸렌, 폴리부타디엔, 폴리메틸메타크릴레이트, 폴리부틸메타크릴레이트, 염소화 폴리에틸렌, 폴리비닐클로라이드, 메틸 아크릴레이트-메틸 메타크릴레이트 코폴리머, 에틸렌-비닐아세테이트 코폴리머, 에틸렌/프로필렌 코폴리머, 에틸렌/에틸 아크릴레이트 코폴리머, 비닐 아세테이트, 비닐리덴 클로라이드, 에틸렌 및 프로필렌과의 비닐클로라이드 코폴리머, 이오노머 폴리에틸렌 테레프탈레이트, 부틸 고무 에피클로로하이드린 고무, 에틸렌/비닐 알코올 코폴리머, 에틸렌/비닐 아세테이트/비닐 알코올 터폴리머, 및 에틸렌/비닐 옥시에탄올 코폴리머, 폴리비닐 클로라이드, 가소화 나일론, 가소화 폴리에틸렌테레프탈레이트, 천연 고무, 실리콘 고무, 폴리디메틸실록산, 실리콘 카보네이트 코폴리머, 및; 친수성 폴리머, 이를 테면 에틸 셀룰로오스, 셀룰로오스 아세테이트, 크로스포비돈, 및 가교결합된 부분 가수분해 폴리비닐 아세테이트; 및 지방 화합물, 이를 테면 카나우바 왁스, 미세결정성 왁스, 및 트리글리세리드가 포함되나 이들에 한정되지 않는다.In a further embodiment, the pharmaceutical composition is formulated with a non-erosive matrix device. The active ingredient (s) are dissolved or dispersed in an inert matrix and are primarily released by diffusion through the inert matrix once administered. Suitable materials for use as non-erosive matrix devices include insoluble plasticizers, such as polyethylene, polypropylene, polyisoprene polyisobutylene, polybutadiene, polymethylmethacrylate, polybutylmethacrylate, chlorinated polyethylene, polyvinyl Chloride, methyl acrylate-methyl methacrylate copolymer, ethylene-vinylacetate copolymer, ethylene / propylene copolymer, ethylene / ethyl acrylate copolymer, vinyl acetate, vinylidene chloride, vinyl chloride copolymer with ethylene and propylene , Ionomer polyethylene terephthalate, butyl rubber epichlorohydrin rubber, ethylene / vinyl alcohol copolymer, ethylene / vinyl acetate / vinyl alcohol terpolymer, and ethylene / vinyl oxyethanol copolymer, polyvinyl chloride, plasticized nylon, plasticization Polyethylene Les terephthalate, natural rubber, silicone rubbers, polydimethylsiloxanes, silicone carbonate copolymers, and; Hydrophilic polymers such as ethyl cellulose, cellulose acetate, crospovidone, and crosslinked partially hydrolyzed polyvinyl acetate; And fatty compounds such as carnauba wax, microcrystalline wax, and triglycerides.
매트릭스 제어 방출 시스템에서, 목적하는 방출 동역학은 예를 들어 사용된 폴리머 형태, 폴리머 점도, 폴리머 및/또는 활성 성분(들)의 입자 크기, 활성 성분(들) 대 폴리머의 비 및 조성물 내 기타 부형제 또는 담체를 통해 조절가능하다.In matrix controlled release systems, the desired release kinetics are, for example, the polymer form used, the polymer viscosity, the particle size of the polymer and / or active ingredient (s), the ratio of active ingredient (s) to polymer and other excipients in the composition or Controllable via a carrier.
변형 방출 투여형의 본원에 제공된 약제학적 조성물은, 일부 구체예에서 직접 압축, 건식 또는 습식 과립화후 압축, 융융 과립화후 압축을 비롯한 방법에 의해 제조된다.The pharmaceutical compositions provided herein of the modified release dosage forms are prepared in some embodiments by methods including direct compression, dry or wet granulation and then compression, and melt granulation and compression.
2. 2. 삼투성Osmotic 제어 방출 장치 Controlled release device
변형 방출 투여형의 본원에 제공된 약제학적 조성물은, 일부 구체예에서 단일 챔버 시스템, 이중 챔버 시스템, 비대칭 막 기술(asymmetric membrane technology, AMT) 및 압출 코어 시스템(extruding core system, ECS)을 비롯한 삼투성 제어 방출 장치를 사용하여 제작하였다. 일반적으로 이러한 장치는 적어도 2 개의 부품을 가진다: (a) 활성 성분(들)을 함유하는 코어; 및 (b) 이 코어를 에워싸는, 적어도 하나의 전달 포트(port)를 가진 반투과막. 반투과막은, 전달 포트(들)를 통한 분출에 의해 약물을 방출하도록, 수성의 사용 환경으로부터 코어로의 물의 유입을 조절한다.The pharmaceutical compositions provided herein of modified release dosage forms, in some embodiments, are osmotic, including single chamber systems, dual chamber systems, asymmetric membrane technology (AMT), and extruding core systems (ECS). It was made using a controlled release device. Such devices generally have at least two parts: (a) a core containing the active ingredient (s); And (b) a semipermeable membrane having at least one delivery port that surrounds this core. The semipermeable membrane regulates the ingress of water from the aqueous use environment into the core to release the drug by ejection through the delivery port (s).
활성 성분(들) 이외에, 삼투 장치의 중심은, 사용 환경으로부터 장치의 중심으로 운반하기 위한 구동력을 생성하는 삼투성 제제를 임의로 포함한다. 삼투성 제제 중 한 부류는, "오스모폴리머" 및 "하이드로겔"로도 언급되는 수-팽윤성 친수성 폴리머이며, 이들로는 친수성 비닐 및 아크릴 폴리머, 폴리사카라이드, 이를 테면 칼슘 알기네이트, 폴리에틸렌 옥사이드(PEO), 폴리에틸렌 글리콜(PEG), 폴리프로필렌글리콜(PPG), 폴리(2-하이드록시에틸 메타크릴레이트), 폴리(아크릴)산, 폴리(메타크릴)산, 폴리비닐피롤리돈(PVP), 가교결합 PVP, 폴리비닐 알코올(PVA), PVA/PVP 코폴리머, 비닐 아세테이트 및 메틸 메타크릴레이트와 같은 소수성 모노머와의 PVA/PVP 코폴리머, PEO 블록을 다량 함유하는 친수성 폴리우레탄, 나트륨 크로스카르멜로스, 카라기난, 하이드록시에틸 셀룰로오스(HEC), 하이드록시프로필 셀룰로오스(HPC), 하이드록시프로필 메틸 셀룰로오스(HPMC), 카르복시메틸 셀룰로오스(CMC) 및 카르복시에틸, 셀룰로오스(CEC), 나트륨 알기네이트, 폴리카보필, 젤라틴, 크산탄 검 및 나트륨 전분 글리콜레이트가 포함되나 이들에 한정되지 않는다.In addition to the active ingredient (s), the center of the osmotic device optionally includes an osmotic agent that generates a driving force for delivery from the environment of use to the center of the device. One class of osmotic agents are water-swellable hydrophilic polymers, also referred to as "osmopolymers" and "hydrogels", including hydrophilic vinyl and acrylic polymers, polysaccharides such as calcium alginate, polyethylene oxide ( PEO), polyethylene glycol (PEG), polypropylene glycol (PPG), poly (2-hydroxyethyl methacrylate), poly (acrylic) acid, poly (methacrylic) acid, polyvinylpyrrolidone (PVP), PVA / PVP copolymer with hydrophobic monomers such as crosslinked PVP, polyvinyl alcohol (PVA), PVA / PVP copolymer, vinyl acetate and methyl methacrylate, hydrophilic polyurethanes containing large amounts of PEO blocks, sodium croscarmellose , Carrageenan, hydroxyethyl cellulose (HEC), hydroxypropyl cellulose (HPC), hydroxypropyl methyl cellulose (HPMC), carboxymethyl cellulose (CMC) and carboxyethyl, cellulite Agarose (CEC), sodium alginate, but contains a polycarbophil, gelatin, xanthan gum, and sodium starch glycolate is not limited to these.
삼투성 제제의 다른 부류는 물을 흡수하여 주변 코팅의 장벽에 걸쳐 삽투성 압력 구배가 작용하도록 할 수 있는 오스모겐이다. 적합한 오스모겐으로는 무기염, 이를 테면 황산마그네슘, 염화마그네슘, 염화칼슘, 염화나트륨, 염화리튬, 황산칼륨, 인산칼륨, 탄산나트륨, 아황산나트륨, 황산리튬, 염화칼륨 및 황산나트륨; 당, 이를 테면 덱스트로스, 프룩토스, 글루코오스, 이노시톨, 락토오스, 말토스, 만니톨, 라피노스, 소르비톨, 수크로오스, 트레할로오스 및 자일리톨; 유기산, 이를 테면 아스코르브산, 벤조산, 푸마르산, 시트르산, 말레산, 세바신산, 소르빈산, 아디핀산, 에데트산, 글루탐산, p-톨루엔설폰산, 숙신산 및 타르타르산; 우레아; 및 이들의 혼합물이 포함되나 이들에 한정되지 않는다.Another class of osmotic agents are osmogens that can absorb water and cause an invasive pressure gradient to act across the barrier of the surrounding coating. Suitable osmogens include inorganic salts such as magnesium sulfate, magnesium chloride, calcium chloride, sodium chloride, lithium chloride, potassium sulfate, potassium phosphate, sodium carbonate, sodium sulfite, lithium sulfate, potassium chloride and sodium sulfate; Sugars such as dextrose, fructose, glucose, inositol, lactose, maltose, mannitol, raffinose, sorbitol, sucrose, trehalose and xylitol; Organic acids such as ascorbic acid, benzoic acid, fumaric acid, citric acid, maleic acid, sebacic acid, sorbic acid, adipic acid, edetic acid, glutamic acid, p-toluenesulfonic acid, succinic acid and tartaric acid; Urea; And mixtures thereof.
용출 속도가 상이한 삼투성 제제는 일부 구체예에서 얼마나 빨리 활성 성분(들)이 투여형으로부터 초기 전달되는지를 좌우하는데 사용된다. 예를 들어, 무정형 당, 이를 테면 Mannogeme EZ(SPI Pharma, Lewes, DE)을 사용하여 처음 2-3 시간동안 더 빠르게 전달되도록 함으로써, 목적하는 치료 효과를 신속하게 생산하게 하고, 남아있는 양을 서서히 그리고 연속적으로 방출하여 연장 시간에 걸쳐 치료학적 또는 예방학적 효과를 목적하는 수준으로 유지하도록 한다. 이 경우, 활성 성분(들)은 대사되고 배출되는 활성 성분(들)의 양을 대체하는 속도로 방출된다.Osmotic agents with different dissolution rates are used in some embodiments to determine how quickly the active ingredient (s) are delivered early from the dosage form. For example, using amorphous sugars, such as Mannogeme EZ (SPI Pharma, Lewes, DE), allows for faster delivery during the first 2-3 hours, resulting in faster production of the desired therapeutic effect and slowing down of the remaining amounts. And continuous release to maintain the therapeutic or prophylactic effect at the desired level over an extended period of time. In this case, the active ingredient (s) are released at a rate that replaces the amount of active ingredient (s) that is metabolized and excreted.
일부 구체예에서, 코어는 또한 투여형의 성능을 증대시키고 안정성 또는 처리능을 향상시키기 위해 본원에 기술된 다양한 다른 부형제 및 담체를 포함한다.In some embodiments, the core also includes various other excipients and carriers described herein to enhance the performance of the dosage form and enhance stability or throughput.
반투과막을 형성하는데 유용한 물질로는 다양한 등급의 아크릴, 비닐, 에테르, 폴리아미드, 폴리에스테르, 생리학적으로 적절한 pH에서 수-투과성 및 수-불용성이거나 가교결합과 같은 화학적 변경에 의해 수-불용성화하기 쉬운 셀룰로오스 유도체가 포함된다. 코팅을 형성하는데 유용한 적합한 폴리머의 예로는 가소화, 비가소화 및 강화 셀룰로오스 아세테이트(CA), 셀룰로오스 디세테이트, 셀룰로오스 트리아세테이트, CA 프로피오네이트, 셀룰로오스 니트레이트, 셀룰로오스 아세테이트 부티레이트(CAB), CA 에틸 카바메이트, CAP, CA 메틸 카바메이트, CA 숙시네이트, 셀룰로오스 아세테이트 트리멜리테이트(CAT), CA 디메틸아미노아세테이트, CA 에틸 카보네이트, CA 클로로아세테이트, CA 에틸 옥살레이트, CA 메틸 설포네이트, CA 부틸 설포네이트, CA p-톨루엔 설포네이트, 한천 아세테이트, 아밀로오스 트리아세테이트, 베타 글루칸 아세테이트, 베타 글루칸 트리아세테이트, 아세트알데히드 디메틸 아세테이트, 로우커스트 빈 검의 트리아세테이트, 하이드록시화 에틸렌 - 비닐아세테이트, EC, PEG, PPG, PEG/PPG 코폴리머, PVP, HEC, HPC, CMC, CMEC, HPMC, HPMCP, HPMCAS, HPMCAT, 폴리(아크릴)산 및 에스테르 및 폴리-(메타크릴)산 및 에스테르 및 이들의 코폴리머, 전분, 덱스트란, 덱스트린, 키토산, 콜라겐, 젤라틴, 폴리알켄, 폴리에테르, 폴리설폰, 폴리에테르설폰, 폴리스티렌, 폴리비닐 할라이드, 폴리비닐 에스테르 및 에테르, 천연 왁스 및 합성 왁스가 포함된다.Materials useful for forming semipermeable membranes include various grades of acrylic, vinyl, ethers, polyamides, polyesters, water-insoluble and water-insoluble at physiologically appropriate pH or by chemical alteration such as crosslinking. Easy cellulose derivatives are included. Examples of suitable polymers useful for forming coatings are plasticized, unplasticized and reinforced cellulose acetate (CA), cellulose discetate, cellulose triacetate, CA propionate, cellulose nitrate, cellulose acetate butyrate (CAB), CA ethyl carba Mate, CAP, CA methyl carbamate, CA succinate, cellulose acetate trimellitate (CAT), CA dimethylaminoacetate, CA ethyl carbonate, CA chloroacetate, CA ethyl oxalate, CA methyl sulfonate, CA butyl sulfonate, CA p-toluene sulfonate, agar acetate, amylose triacetate, beta glucan acetate, beta glucan triacetate, acetaldehyde dimethyl acetate, triacetate of low-cursor bean gum, hydroxylated ethylene-vinylacetate, EC, PEG, PPG, PEG / PPG copolymer, PV P, HEC, HPC, CMC, CMEC, HPMC, HPMCP, HPMCAS, HPMCAT, poly (acrylic) acids and esters and poly- (methacrylic) acids and esters and copolymers thereof, starch, dextran, dextrin, chitosan, Collagen, gelatin, polyalkenes, polyethers, polysulfones, polyethersulfones, polystyrenes, polyvinyl halides, polyvinyl esters and ethers, natural waxes and synthetic waxes.
일부 구체예에서, 반투과막은 미국 특허 제5,798,119호에 개시된 바와 같이 기공이 실질적으로 기체로 충전되며 수성 매질에 의해 습윤화되지 않지만 수증기를 투과가능한 소수성 미세다공성 막이다. 이러한 소수성이나 수증기 투과성 막은 전형적으로 소수성 폴리머, 이를 테면 폴리알켄, 폴리에틸렌, 폴리프로필렌, 폴리테트라플루오로에틸렌, 폴리아크릴산 유도체, 폴리에테르, 폴리설폰, 폴리에테르설폰, 폴리스티렌, 폴리비닐 할라이드, 폴리비닐리덴 플루오라이드, 폴리비닐 에스테르 및 에테르, 천연 왁스 및 합성 왁스로 구성된다.In some embodiments, the semipermeable membrane is a hydrophobic microporous membrane, as disclosed in US Pat. No. 5,798,119, which is substantially filled with pores and not wetted by an aqueous medium but is permeable to water vapor. Such hydrophobic or water vapor permeable membranes are typically hydrophobic polymers such as polyalkenes, polyethylene, polypropylene, polytetrafluoroethylene, polyacrylic acid derivatives, polyethers, polysulfones, polyethersulfones, polystyrenes, polyvinyl halides, polyvinylidene Fluoride, polyvinyl esters and ethers, natural waxes and synthetic waxes.
반투과막 상의 전달 포트(들)는 일부 구체예에서, 기계적 또는 레이저 드릴링(drilling)에 의한 코팅후 형성된다. 전달 포트(들)은 일부 구체예에서 수용성 물질의 플러그가 부식되거나 코어내 함입부(indentation) 위 막의 얇은 부분이 파열되어 원위치에서 형성된다. 또한, 미국 특허 제5,612,059호 및 제5,698,220호에 개시된 형태의 비대칭 막 코팅의 경우에서와 같이, 전달 포트는 코팅 과정동안 형성된다.The delivery port (s) on the semipermeable membrane is formed in some embodiments after coating by mechanical or laser drilling. The delivery port (s) is formed in some embodiments in situ due to corrosion of the plug of water soluble material or tearing of a thin portion of the membrane above the indentation in the core. In addition, as in the case of asymmetric membrane coatings of the type disclosed in US Pat. Nos. 5,612,059 and 5,698,220, delivery ports are formed during the coating process.
방출된 활성 성분(들)의 총량 및 방출 속도는 일부 구체예에서 반투고막의 두께 및 다공성, 코어의 조성, 및 전달 포트의 수, 크기 및 위치를 통해 실질적으로 조절된다.The total amount and release rate of the active ingredient (s) released are substantially controlled in some embodiments through the thickness and porosity of the semipermeable membrane, the composition of the core, and the number, size and location of the delivery ports.
삼투성 제어 방출 투여형의 약제학적 조성물은 일부 구체예에서, 제제의 성능 또는 처리능을 촉진하기 위해 본원에 기술된 바와 같은 부가적인 통상의 부형제 또는 담체를 추가로 포함한다.The pharmaceutical composition of the osmotic controlled release dosage form further comprises, in some embodiments, additional conventional excipients or carriers as described herein to promote the performance or processability of the formulation.
일부 구체예에서, 삼투성 제어 방출 투여형은 통상의 방법 및 기술에 따라 제조된다(예를 들어 문헌[Remington: The Science and Practice of Pharmacy; Santus and Baker, J. Controlled Release 1995, 35, 1-21; Verma et al., Drug Development and Industrial Pharmacy 2000, 26, 695-708; Verma et al., J. Controlled Release 2002, 79, 7-27]을 참조할 수 있다).In some embodiments, osmotic controlled release dosage forms are prepared according to conventional methods and techniques (see, eg, Remington: The Science and Practice of Pharmacy; Santus and Baker, J. Controlled Release 1995, 35, 1-). 21; Verma et al., Drug Development and
특정 구체예에서, 본원에 제공된 약제학적 조성물은, 활성 성분(들)을 포함하는 코어 및 다른 약제학적으로 허용가능한 부형제 또는 담체를 코팅하는 비대칭성 삼투막을 포함하는 AMT 제어 방출 투여형으로서 제형화된다. 미국 특허 제5,612,059호 및 WO2002/17918호를 참조할 수 있다. 일부 구체예에서, AMT 제어 방출 투여형은 집적 압축, 건식 과립, 습식 과립 및 딥-코팅 공정과 같은 방법을 사용하여 제조된다.In certain embodiments, the pharmaceutical compositions provided herein are formulated as an AMT controlled release dosage form comprising an asymmetric osmotic membrane coating a core comprising the active ingredient (s) and other pharmaceutically acceptable excipients or carriers. . See US Pat. No. 5,612,059 and WO2002 / 17918. In some embodiments, AMT controlled release dosage forms are prepared using methods such as integrated compression, dry granules, wet granules, and dip-coating processes.
특정 구체예에서, 본원에 제공된 약제학적 조성물은 활성 성분(들)을 포함하는 코어, 하이드록시에틸 셀룰로오스 및 다른 약제학적으로 허용되는 부형제 또는 담체를 코팅하는 삼투막을 포함하는 ESC 제어 방출 투여형으로 제형화된다.In certain embodiments, the pharmaceutical compositions provided herein are formulated in an ESC controlled release dosage form comprising an osmotic membrane coating a core comprising the active ingredient (s), hydroxyethyl cellulose and other pharmaceutically acceptable excipients or carriers. Become
3. 복합미립자 제어 방출 장치3. Multiparticulate Controlled Release Device
변형 방출 투여형의 본원에 제공된 약제학적 조성물은 일부 구체예에서, 직경 범위가 약 10 ㎛ 내지 약 3 ㎜, 약 50 ㎛ 내지 약 2.5 ㎜, 또는 약 100 ㎛ 내지 약 1 ㎜인 다양한 입자, 과립 또는 펠릿을 포함하는 복합미립자 제어 방출 장치로 제작된다. 이러한 복합미립자는 일부 구체예에서, 습식- 및 건식-과립화, 압출/구형화, 롤러-압밀화, 용융-응고와 같은 공정 및 스프레이-코팅 시드 코어(spray-coating seed core)에 의해 제조된다. 예를 들어, 문헌[Multiparticulate Oral Drug Delivery; Marcel Dekker: 1994; 및 Pharmaceutical Pelletization Technology; Marcel Dekker: 1989]을 참조할 수 있다.The pharmaceutical compositions provided herein of the modified release dosage forms can, in some embodiments, comprise a variety of particles, granules or particles having a diameter ranging from about 10 μm to about 3 mm, from about 50 μm to about 2.5 mm, or from about 100 μm to about 1 mm, or It is made of a multiparticulate controlled release device comprising pellets. Such multiparticulates are prepared in some embodiments by processes such as wet- and dry-granulation, extrusion / sphering, roller-consolidation, melt-coagulation, and spray-coating seed cores. . See, eg, Multiparticulate Oral Drug Delivery; Marcel Dekker: 1994; And Pharmaceutical Pelletization Technology; Marcel Dekker: 1989).
흡인에 의한 투여의 경우, 일반식 (I) 또는 (II)의 화합물은 통상적으로 적합한 분사제, 예를 들어 디클로로디플루오로메탄, 트리클로로플루오로메탄, 디클로로테트라플루오로에탄, 이산화탄소 또는 다른 적합한 기체를 사용하여 가압팩 또는 네뷸라이저로부터의 에어로졸 스프레이 제공의 형태로 전달된다. 가압 에어로졸의 경우, 투여 단위는 일부 구체예에서 계량된 양을 전달하도록 밸브를 제공함으로써 결정된다. 락토오스 또는 전분과 같은 적합한 분말 기제를 함유하는, 흡입기 또는 취입기에 사용하기 위한 캡슐 또는 카트리지, 예를 들어 젤라틴로 제형화된다.For administration by aspiration, the compounds of formula (I) or (II) are usually suitable propellants, for example dichlorodifluoromethane, trichlorofluoromethane, dichlorotetrafluoroethane, carbon dioxide or other suitable The gas is used to deliver in the form of an aerosol spray delivery from a pressurized pack or nebulizer. In the case of a pressurized aerosol, the dosage unit is determined in some embodiments by providing a valve to deliver a metered amount. Formulated into capsules or cartridges, for example gelatin, for use in an inhaler or blower containing a suitable powder base such as lactose or starch.
치료 방법, 용량 및 병용 요법Method of treatment, dosage and combination therapy
용어 "포유동물"은 인간을 비롯한 모든포 유동물을 의미한다. 포유동물로는 단지 예로서 인간, 인간을 제외한 영장류, 소, 개, 고양이, 염소, 양, 돼지, 래트, 마우스 및 토끼가 포함된다.The term "mammal" means all mammalian fluids, including humans. Mammals include, by way of example only, humans, non-human primates, cattle, dogs, cats, goats, sheep, pigs, rats, mice, and rabbits.
본원에 사용된 용어 "유효량"이란 치료되는 질환, 병상 또는 장애의 증상 중 하나 이상을 어느 정도 경감시키도록 투여되는 화합물의 양을 의미한다.As used herein, the term “effective amount” means the amount of a compound administered to alleviate to some extent one or more of the symptoms of the disease, condition or disorder being treated.
본원에 사용된 용어 "간접적으로 조절한다"란 포유동물에서 혈청 레티놀 수준을 감소시켜 포유동물의 눈에서 레티놀 수준을 감소시키는 제제를 말한다. 이러한 안내 레티놀 수준을 조절하면 시각 사이클 단백질의 활성을 조절가능하다. 이러한 형태의 조절(안내 혈청 레티놀 수준의 감소를 통해 발생함)은 간접 조절로서 본원에 언급된다.As used herein, the term “indirectly regulates” refers to an agent that reduces serum retinol levels in a mammal to reduce retinol levels in the mammal's eye. Modulating these intraocular retinol levels can modulate the activity of visual cycle proteins. This form of regulation (which occurs through the reduction of intracellular serum retinol levels) is referred to herein as indirect regulation.
일부 구체예에서, 본원에 기술된 화합물(들)을 함유하는 조성물은 예방학적 및/또는 치료학적 치료를 위해 투여될 수 있다. 용어 "치료"는 예방학적 및/또는 치료학적 치료를 언급할 목적으로 사용된다. 치료학적 적용에서, 조성물은 질환, 병상 또는 장애를 이미 앓고 있는 환자에게 질환, 장애 또는 병상의 증상을 치유하거나 적어도 부분적으로 저지하기에 충분한 양으로 투여된다. 이러한 사용에 유효한 양은 질환, 장애 또는 병상의 중증도 및 과정, 이전의 치료법, 환자의 건강 상태 및 악물에 대한 반응 및 치료 의사의 판단에 따라 달라질 것이다.In some embodiments, a composition containing a compound (s) described herein can be administered for prophylactic and / or therapeutic treatment. The term "treatment" is used for the purpose of referring to prophylactic and / or therapeutic treatments. In therapeutic applications, the composition is administered to a patient already suffering from a disease, condition or disorder in an amount sufficient to cure or at least partially arrest the condition, condition or condition. The amount effective for such use will vary depending on the severity and course of the disease, disorder or condition, previous treatment, the patient's health and adverse reactions, and the judgment of the treating physician.
예방학적 적용에서, 본원에 개시된 화합물을 함유하는 조성물은 특정 질환, 장애 또는 병상에 걸리기 쉽거나 그러한 위험이 있는 환자에게 투여된다. 이러한 양은 "예방학적 유효량 또는 용량"으로 정의된다. 그의 사용에서, 정확한 양은 또한 환자의 건강 상태, 체중 등에 따라 달라진다.In prophylactic applications, a composition containing a compound disclosed herein is administered to a patient susceptible to or at risk of a particular disease, disorder or condition. This amount is defined as "prophylactically effective amount or dose." In its use, the exact amount also depends on the patient's state of health, weight, and the like.
용어 "증대" 또는 "증대시키는"은 소정 효과의 효능 또는 기간을 증가시키거나 연장시키는 것을 의미한다. 즉, 치료제의 효과에 대한 증대에 있어서, 용어 "증대시키는"은 시스템에 대한 다른 치료제의 효과의 효능 또는 기간을 증가시키거나 연장시킬 수 있는 능력을 의미한다. 본원에 사용된 "증대시키는 유효량"은 소정의 시스템에서 다른 치료제의 효과를 증대시키기에 충분한 양을 말한다. 환자에게 사용시, 이러한 사용에 유효한 양은 질환, 장애 또는 병상의 중증도 및 과정, 이전의 치료법, 환자의 건강 상태 및 악물에 대한 반응 및 치료 의사의 판단에 따라 달라질 것이다.The term "increasing" or "increasing" means increasing or prolonging the efficacy or duration of a given effect. That is, in increasing the effectiveness of a therapeutic agent, the term “increasing” means the ability to increase or prolong the efficacy or duration of the effect of another therapeutic agent on the system. As used herein, “increasing effective amount” refers to an amount sufficient to enhance the effectiveness of other therapeutic agents in a given system. When used with a patient, the amount effective for such use will depend on the severity and course of the disease, disorder or condition, previous treatment, the patient's health and adverse reactions, and the judgment of the treating physician.
환자의 병상이 호전되지 않는 경우, 의사의 재량으로 화합물은 환자의 질환 또는 병상의 증상을 경감시키거나, 제어 또는 제한하기 위하여 장기간, 즉 환자의 생존 기간내내를 비롯한 연장된 기간 동안 투여될 수 있다.If the patient's condition does not improve, at the physician's discretion, the compound may be administered for an extended period of time, i.e., throughout the patient's survival, to alleviate, control or limit the patient's disease or condition. .
환자의 병상이 호전되는 경우, 의사의 재량으로 화합물의 투여는 연속적으로 제공될 수 있거나; 일정 기간 동안 일시적으로 중단될 수도 있다(즉, "휴약기").If the patient's condition improves, administration of the compound may be provided continuously at the discretion of the physician; It may be temporarily suspended for a period of time (ie, a "drug holiday").
환자의 병상이 호전되면, 필요에 따라 유지 용량(maintenance dose)이 투여된다. 이어, 투여량 또는 투여빈도, 또는 둘 다 호전된 질환, 장애 또는 병상이 유지되는 수준에 대한 증상의 함수로서 감소될 수 있다. 일부 구체예에서, 환자들은 임의의 증상 재발에 기초하여 장기간 간헐적인 치료를 필요로 할 수 있다.When the patient's bed improves, a maintenance dose is administered as needed. The dose or frequency of administration, or both, can then be reduced as a function of symptoms for the level at which the improved disease, disorder or condition is maintained. In some embodiments, patients may require long-term intermittent treatment based on any symptom recurrence.
이러한 양에 상응하게 될 제시된 약제의 양은 특정 화합물, 질환 상태 및 그의 중증도, 치료할 대상 또는 숙주의 고유성(예, 체중) 등의 인자에 따라 달라질 것이나, 예를 들어 특정 치료 제제, 투여 경로, 치료될 병상 및 치료될 대상 또는 숙주를 비롯하여 증례의 특정 상황에 따라 당업계에 공지된 방법에 의해 관례적으로 결정될 수도 있다. 그러나, 일반적으로 성인 치료를 위해 사용되는 용량은 전형적으로 1일 약 0.02 내지 약 5000 ㎎, 바람직하게는 1일 약 1 내지 약 1500 ㎎일 것이다. 소정 용량은 일부 구체예에서 편의상 일회량으로 또는 동시(또는 단기간에 걸쳐) 또는 적절한 간격, 예를 들어 1일 2회, 3회, 4회 또는 그 이상 회수의 미달 용량(sub-dose)으로 투여되는 분할 용량으로 주어질 수도 있다.The amount of a given agent that will correspond to this amount will vary depending on factors such as the particular compound, disease state and severity thereof, the specificity of the subject or host to be treated (eg, body weight), but for example, the specific therapeutic agent, route of administration, It may also be routinely determined by methods known in the art depending on the particular situation of the case, including the condition and the subject or host to be treated. Generally, however, the dose used for adult treatment will typically be about 0.02 to about 5000 mg per day, preferably about 1 to about 1500 mg per day. The predetermined dose is, in some embodiments, conveniently administered in a single dose or simultaneously (or over a short period of time) or in sub-dose at appropriate intervals, such as twice, three, four or more times daily. May be given in divided doses.
특정의 경우에, 본원에 개시된 화합물(또는 약제학적으로 허용가능한 염, 에스테르, 아미드, 전구약물 또는 용매화물) 중 적어도 하나를 다른 치료제와 병용하여 투여하는 것이 적절할 수 있다. 또한, 단지 예로서, 본원에 개시된 화합물 중 하나를 투여받았을 때 환자가 경험하게 되는 부작용 중 하나가 염증이라면, 항염증제를 초기 치료제와 병용하여 투여하는 것이 적절할 수 있다. 또한, 단지 예로서, 본원에 개시된 화합물 중 하나의 치료 효과는 보조제를 투여하여 증대시킬 수 있다(즉, 보조제 자체로는 최소의 치료 이점만을 얻게 되나 다른 치료제와 병용한 경우 환자에 대한 총 치료 이점이 향상된다). 또한, 단지 예로서, 본원에 개시된 화합물 중 하나를 역시 치료 효과를 가진 다른 치료제(또한 다른 치료 요법도 포함)와 함께 투여함으로써 환자가 경험하게 되는 이점을 증가시킬 수 있다. 단지 예로서, 본원에 개시된 화합물 중 하나를 투여하는 단계를 포함하는 황반 변성의 치료법에서, 환자에게 다른 황반 변성 치료제 또는 요법을 제공함으로써 치료 이점을 증가시킬 수 있다. 임의의 경우에, 치료할 질환, 장애 또는 병상과 상관없이, 환자가 경험하는 총 이점은 두 치료제의 단순 합일 수 있거나 환자는 상승적인 이점을 경험할 수 있을 것이다.In certain cases, it may be appropriate to administer at least one of the compounds (or pharmaceutically acceptable salts, esters, amides, prodrugs or solvates) disclosed herein in combination with other therapeutic agents. Also, by way of example only, if one of the side effects a patient experiences when receiving one of the compounds disclosed herein is inflammation, it may be appropriate to administer the anti-inflammatory agent in combination with the initial therapeutic agent. Also, by way of example only, the therapeutic effect of one of the compounds disclosed herein can be augmented by administering an adjuvant (ie, the adjuvant alone will yield minimal therapeutic benefit, but in combination with other therapeutic agents, the total therapeutic benefit for the patient). Is improved). In addition, by way of example only, one of the compounds disclosed herein may be administered with other therapeutic agents (also including other therapeutic regimens) that also have a therapeutic effect to increase the benefit experienced by the patient. By way of example only, in the treatment of macular degeneration comprising administering one of the compounds disclosed herein, the therapeutic benefit can be increased by providing the patient with another macular degeneration treatment or therapy. In any case, regardless of the disease, disorder or condition to be treated, the total benefit experienced by the patient may be a simple sum of the two therapeutic agents or the patient may experience a synergistic benefit.
혈청 레티놀 수준 또는 활성의 조절자와 함께 일반식 (I) 또는 (II)의 화합물의 사용을 포함하는 병용 요법이 또한 본원에 개시되어 있다. 하나의 구체예에서, 병용제는 상기 일반식 (I) 또는 (II)의 화합물 및 하기 일반식 (III)의 화합물 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구 약물 또는 용매화물을 포함한다:Also disclosed herein are combination therapies comprising the use of a compound of formula (I) or (II) with modulators of serum retinol levels or activity. In one embodiment, the combination comprises a compound of formula (I) or (II) above and a compound of formula (III) or an active metabolite or pharmaceutically acceptable prodrug or solvate thereof:
상기 식에서, X1은 NR2, O, S, CHR2로 이루어진 그룹 중에서 선택되고; R1은 (CHR2)x-L1-R3이며, 여기서 x는 0, 1, 2 또는 3이고; L1은 단일 결합 또는 -C(O)-이며; R2는 H, (C1-C4)알킬, F, (C1-C4)플루오로알킬, (C1-C4)알콕시, -C(O)OH, -C(O)-NH2, -(C1-C4)알킬아민, -C(O)-(C1-C4)알킬, -C(O)-(C1-C4)플루오로알킬, -C(O)-(C1-C4)알킬아민 및 -C(O)-(C1-C4)알콕시로 이루어진 그룹 중에서 선택된 부분이이고; R3는 H이거나 (C2-C7)알케닐, (C2-C7)알키닐, 아릴, (C3-C7)사이클로알킬, (C5-C7)사이클로알케닐 및 헤테로사이클로 이루어진 그룹 중에서 독립적으로 선택된 1-3 개의 치환기로 임의로 치환된 부분이다. 또 다른 구체예에서, 병용제는 일반식 (I) 또는 (II)의 화합물 및 일반식 (III)의 화합물을 포함하며, 여기서 병용제는 혈청 레티놀 수준 또는 활성을 조절한다. 추가의 구체예로는, 일반식 (I) 또는 (II)의 화합물 및 X1이 NR2이고 R2가 H 또는 (C1-C4)알킬인 일반식 (III) 의 화합물을 포함하는 병용제이다. 또 다른 추가의 구체예로는, 일반식 (I) 또는 (II)의 화합물 및 x가 O인 일반식 (III)의 화합물을 포함하는 병용제이다. 또 다른 구체예로는, 일반식 (I) 또는 (II)의 화합물 및 x가 1이고 L1인 -C(O)-인 일반식 (III)의 화합물을 포함하는 병용제이다. 또 다른 구체예에서, 일반식 (I) 또는 (II)의 화합물 및 R3가 임의로 치환된 헤테로아릴인 일반식 (III)의 화합물을 포함하는 병용제이다. 추가의 구체예로는, 일반식 (I) 또는 (II)의 화합물 및 일반식 (III)의 화합물을 포함하는 병용제이며, 여기서 상기 일반식 (III)의 화합물은 또는 그의 활성 대사산물 또는 약제학적으로 허용가능한 전구약물 또는 용매화물이다. 하나의 구체예로는, 일반식 (I) 또는 (II)의 화합물 및 일반식 (III)의 화합물을 포함하는 병용제이며, 여기서 일반식 (III)의 화합물은 4-하이드록시페닐레틴아미드이다.Wherein X 1 is selected from the group consisting of NR 2 , O, S, CHR 2 ; R 1 is (CHR 2 ) x -L 1 -R 3 , where x is 0, 1, 2 or 3; L 1 is a single bond or -C (O)-; R 2 is H, (C 1 -C 4 ) alkyl, F, (C 1 -C 4 ) fluoroalkyl, (C 1 -C 4 ) alkoxy, -C (O) OH, -C (O) -NH 2 ,-(C 1 -C 4 ) alkylamine, -C (O)-(C 1 -C 4 ) alkyl, -C (O)-(C 1 -C 4 ) fluoroalkyl, -C (O) - (C 1 -C 4) alkylamine, and -C (O) - (C 1 -C 4) is a moiety selected from the group consisting of alkoxy; R 3 is H or (C 2 -C 7 ) alkenyl, (C 2 -C 7 ) alkynyl, aryl, (C 3 -C 7 ) cycloalkyl, (C 5 -C 7 ) cycloalkenyl and heterocyclo Optionally substituted with 1-3 substituents independently selected from the group consisting of: In another embodiment, the combination comprises a compound of Formula (I) or (II) and a compound of Formula (III), wherein the combination modulates serum retinol levels or activity. In a further embodiment, a combination comprising a compound of formula (I) or (II) and a compound of formula (III) wherein X 1 is NR 2 and R 2 is H or (C 1 -C 4 ) alkyl Jay. Another further embodiment is a combination comprising a compound of formula (I) or (II) and a compound of formula (III) wherein x is O. In another embodiment, there is a combination comprising a compound of formula (I) or (II) and a compound of formula (III) wherein x is 1 and -C (O)-which is L 1 . In another embodiment is a combination comprising a compound of formula (I) or (II) and a compound of formula (III) wherein R 3 is optionally substituted heteroaryl. In a further embodiment, there is a combination comprising a compound of formula (I) or (II) and a compound of formula (III), wherein the compound of formula (III) Or an active metabolite or pharmaceutically acceptable prodrug or solvate thereof. In one embodiment, there is a combination comprising a compound of formula (I) or (II) and a compound of formula (III), wherein the compound of formula (III) is 4-hydroxyphenylretinamide .
병용 용법의 비한정적인 특정의 예는 일반식 (I) 또는 (II)의 화합물 중 적어도 하나를 산화질소(NO) 생산 유도제, 스타틴, 음하전 인지질, 항산화제, 미네랄, 항염증제, 혈관신생 억제제, 매트릭스 금속단백분해효소 억제제 및 카로티노이드와 함께 사용하는 것을 포함한다. 일부의 경우, 적합한 병용 제제는 여러 범주내에 속할 수 있다(단지 예로서, 루테인은 항산화제이면서 카로티노이드이다). 또한, 일반식 (I) 또는 (II)의 화합물은 일부 구체예에서 환자에 이점을 제공할 수 있는 첨가제와 함께 투여될 수 있으며, 단지 예로서 사이클로스포린 A가 예시될 수 있다.Specific non-limiting examples of combination regimens include at least one of the compounds of formula (I) or (II): nitric oxide (NO) production inducers, statins, negatively charged phospholipids, antioxidants, minerals, anti-inflammatory agents, angiogenesis inhibitors, matrices Use with metalloproteinase inhibitors and carotenoids. In some cases, suitable combination agents may fall within several categories (for example, lutein is an antioxidant and a carotenoid). In addition, the compounds of formula (I) or (II) may be administered with additives that may provide an advantage to the patient in some embodiments, by way of example only cyclosporin A may be exemplified.
또한, 일부 구체예에서, 일반식 (I) 및 (II)의 화합물은 환자에게 추가적이거나 상승적인 이점을 제공할 수 있는 방법과 병용하여 사용되며, 이로는 단지 예로서 체외 레오페레시스(또한 막 분별 여과(membrane differential filtration)로도 공지되었음)의 사용, 이식용 소형 망원경(implantable miniature telescope)의 사용, 드루젠의 레이저광 응고술 및 미세자극(microstimulation) 요법이 포함된다.In addition, in some embodiments, compounds of Formulas (I) and (II) are used in combination with methods that may provide additional or synergistic benefits to a patient, which is merely an example of in vitro leoparesis (also called membrane). The use of known differential filtration), the use of an implantable miniature telescope, the laser light coagulation of drusen and the microstimulation regimen.
항산화제의 사용은 황반 변성 및 이영양에 걸린 환자에게 유익한 것으로 밝혀졌다. 예를 들면, 문헌[Arch. Ophthalmol, 119: 1417-36(2001); Sparrow, et al., J. Biol. Chem., 278: 18207-13(2003)]을 참조할 수 있다. 일반식 (I) 또는 (II)의 구조를 가진 적어도 하나의 화합물과 병용하여 사용될 수 있는 적합한 항산화제의 예로는 비타민 C, 비타민 E, 베타-카로틴 및 다른 카로티노이드, 코엔자임 Q, 4-하이드록시-2,2,6,6-테트라메틸피페리딘-N-옥실(템폴(Tempol)로도 공지됨), 루테인, 부틸화 하이드록시톨루엔, 레스베라트롤, 트롤록스(trolox) 유사체(PNU-83836-E) 및 빌베리(bilberry) 추출물이 포함된다.The use of antioxidants has been found to be beneficial for patients with macular degeneration and dystrophy. For example, Arch. Ophthalmol, 119: 1417-36 (2001); Sparrow, et al., J. Biol. Chem., 278: 18207-13 (2003). Examples of suitable antioxidants that can be used in combination with at least one compound having the structure of Formula (I) or (II) include vitamin C, vitamin E, beta-carotene and other carotenoids, coenzyme Q, 4-hydroxy- 2,2,6,6-tetramethylpiperidine-N-oxyl (also known as Tempol), lutein, butylated hydroxytoluene, resveratrol, trolox analogs (PNU-83836-E) And bilberry extracts.
특정의 미네랄의 사용이 또한 황반 변성 및 이영양에 걸린 환자에 유익한 것으로 밝혀졌다. 예를 들어, 문헌[Arch. Ophthalmol, 119: 1417-36(2001)]을 참조할 수 있다. 일반식 (I) 또는 (II)의 구조를 가진 적어도 하나의 화합물과 병용하여 사용될 수 있는 적합한 미네랄의 예로는 구리-함유 미네랄, 이를 테면 산화 제2구리(단지 예로서); 아연-함유 미네랄, 이를 테면 산화아연(단지 예로서); 및 셀레늄-함유 화합물이 포함된다.The use of certain minerals has also been found to be beneficial for patients with macular degeneration and dystrophy. See, eg, Arch. Ophthalmol, 119: 1417-36 (2001). Examples of suitable minerals that can be used in combination with at least one compound having the structure of formula (I) or (II) include copper-containing minerals such as cupric oxide (as an example only); Zinc-containing minerals such as zinc oxide (only by way of example); And selenium-containing compounds.
특정 음하전 인지질의 사용이 또한 황반 변성 및 이영양에 걸린 환자에게 유익한 것으로 밝혀졌다. 예를 들어, 문헌[Shaban & Richter,Biol. Chem., 383:537-45(2002); Shaban, et al., Exp. Eye Res., 75:99108 (2002)]을 참조할 수 있다. 일반식 (I) 또는 (II)의 구조를 가진 적어도 하나의 화합물과 병용하여 사용될 수 있는 적합한 음하전 인지질의 예로는 카디오리핀 및 포스파티딜글리세롤이 포함된다. 양으로 하전되고/되거나 중성 인지질이 또한 일반식 (I) 또는 (II)의 구조를 가진 화합물과 병용하여 사용하는 경우, 황반 변성 및 이영양에 걸린 환자에게 유익할 수 있다.The use of certain negatively charged phospholipids has also been found to be beneficial for patients with macular degeneration and dystrophy. See, eg, Shaban & Richter, Biol. Chem., 383: 537-45 (2002); Shaban, et al., Exp. Eye Res., 75: 99108 (2002). Examples of suitable negatively charged phospholipids that can be used in combination with at least one compound having the structure of Formula (I) or (II) include cardiolipin and phosphatidylglycerol. When positively charged and / or neutral phospholipids are also used in combination with a compound having the structure of Formula (I) or (II), it may be beneficial to patients with macular degeneration and dystrophicity.
특정 카로티노이드의 사용이 광수용체 세포에 필요한 광보호 유지와 상호 관련된다. 카로티노이드는 식물, 조류, 박테리아 및 특정 동물, 이를 테면 조류 및 조개에 존재하는 테르페노이드기의 자연발생 황색-적색 안료이다. 카로티노이드는 거대 분류 분자로서 600개 이상의 자연발생 카로티노이드가 알려져 있다. 카로티노이드는 탄화수소(카로틴) 및 그의 함산소물, 알콜 유도체(크산토필)를 포함한다. 이들은 악티니오에리스롤, 아스타크산틴, 칸타크산틴, 캡산틴, 캡소루빈, β-8'-apo-카로테날(apo-카로테날), β-12'-apo-카로테날, α-카로틴, β-카로틴, "카로틴"(α-및 β-카로틴의혼합물), γ-카로틴, β-크립토크산틴, 루테인, 리코펜, 비올에리스린, 제아크산틴 및 이들의 하이드록실- 또는 카르복시-함유 구성원의 에스테르를 포함한다. 다수의 카로티노이드는 실제로 시스- 및 트랜스-이성질체 형태로 존재하는 반면, 합성 화합물은 라세미 혼합물인 경우가 빈번하다.The use of certain carotenoids is correlated with the maintenance of photoprotection required for photoreceptor cells. Carotenoids are naturally occurring yellow-red pigments of terpenoid groups present in plants, algae, bacteria and certain animals such as algae and shellfish. Carotenoids are known as large class molecules of more than 600 naturally occurring carotenoids. Carotenoids include hydrocarbons (carotene) and their oxygenates, alcohol derivatives (xanthophylls). These include actinioerysrol, astaxanthin, canthaxanthin, capxanthine, capsorubine, β-8'-apo-carotenal, β-12'-apo-carotenal, α-carotene. , β-carotene, “carotene” (mixture of α- and β-carotene), γ-carotene, β-kryptoxanthin, lutein, lycopene, violeryline, zeaxanthin and their hydroxyl- or carboxy-containing Esters of members. Many carotenoids are actually present in cis- and trans-isomer forms, while synthetic compounds are often racemic mixtures.
인간에서, 망막은 주로 두 개의 카로티노이드, 즉 제아크산틴 및 루테인을 선택적으로 축적한다. 이 두 개의 카로티노이드는 강력한 항산화제이면서 청색광을 흡수하기 때문에 망막을 보호하는데 도움이 될 것으로 생각된다. 메추라기를 대상으로 한 연구에서 카로티노이드가 결핍된 식이를 제공한 기는 제아크산틴의 농도가 낮은 망막을 가졌으며 매우 많은 수의 세포자멸 광수용체 세포에 의해 입증된 바와 같이 빛에 의해 상당한 손상을 입은 반면, 제아크산틴 농도가 높은 군은 최소의 손상을 나타낸 것으로 조사되었다. 일반식 (I)의 구조를 가진 적어도 하나의 화합물과 병용하기에 적합한 카로티노이드의 예로는 상기 언급된 임의의 카로티노이드 뿐만 아니라 루테인 및 제아크산틴이 포함된다.In humans, the retina primarily accumulates two carotenoids, namely zeaxanthin and lutein. These two carotenoids are powerful antioxidants and absorb blue light, which may help protect the retina. The group that provided the carotenoid-deficient diet in a study of quails had a low concentration of zeaxanthin and was significantly damaged by light, as evidenced by a very large number of apoptotic photoreceptor cells. The highest levels of zeaxanthin were found to show minimal damage. Examples of carotenoids suitable for use with at least one compound having the structure of Formula (I) include lutein and zeaxanthin as well as any of the carotenoids mentioned above.
적합한 산화질소 생산 유도제는 내부 NO를 자극하거나 생체내에서 내인 내피세포-유도 이완 인자(EDRF, endothelium-derived relaxation factor)의 수준을 상승시키거나, 산화질소 합성 효소에 대한 기질인 화합물을 포함한다. 이러한 화합물로는 예를 들어, L-아르기닌, L-호모아르기닌 및 N-하이드록시-L-아르기닌, 이들의 니트로화 및 니트로화 유사체(예, 니트로화 L-아르기닌, 니트로화 L-아르기닌, 니트로화 N-하이드록시-L-아르기닌, 니트로화 N-하이드록시-L-아르기닌, 니트로화 L-호모아르기닌 및 니트로화 L-호모아르기닌), L-아르기닌의 전구체 및/또는 이들의 생리학적으로 허용가능한 염, 예를 들어 시트룰린, 오르니틴, 글루타민, 리신, 적어도하나의 이들 아미노산을 포함하는 폴리펩티드, 아르기나제 효소 억제제(예, N-하이드록시-L-아르기닌 및 2(S)-아미노-6-보로노헥산산) 및 산화질소 합성효소 기질, 시토킨, 아데노신, 브래디키닌, 칼레티큘린, 비사코딜 및 페놀프탈레인이 포함된다. EDRF는 내피세포에 의해 분비되는 혈관 이완 인자이며, 산화질소 또는 그와 밀접한 관련 유도체로서 확인되었다[Palmer et al., Nature, 327:524-526(1987); Ignarro et al., Proc. Natl. Acad. Sci.USA, 84:9265-9269 (1987)].Suitable nitric oxide production inducers include compounds that stimulate internal NO, raise levels of endothelial cell-induced relaxation factors (EDRF) in vivo, or which are substrates for nitric oxide synthase. Such compounds include, for example, L-arginine, L-homoarginine and N-hydroxy-L-arginine, nitration and nitration analogs thereof (e.g., nitrated L-arginine, nitrated L-arginine, nitro) N-hydroxy-L-arginine, nitrated N-hydroxy-L-arginine, nitrated L-homoarginine and nitrated L-homoarginine), precursors of L-arginine and / or physiologically acceptable thereof Possible salts such as citrulline, ornithine, glutamine, lysine, polypeptides comprising at least one of these amino acids, arginase enzyme inhibitors (eg N-hydroxy-L-arginine and 2 (S) -amino-6 -Boronohexanoic acid) and nitric oxide synthase substrates, cytokines, adenosine, bradykinin, caleticulin, bisaccordyl and phenolphthalein. EDRF is a vascular relaxation factor secreted by endothelial cells and has been identified as nitric oxide or a closely related derivative thereof (Palmer et al., Nature, 327: 524-526 (1987); Ignarro et al., Proc. Natl. Acad. Sci. USA, 84: 9265-9269 (1987).
스타틴은 지질 저하제 및/또는 적합한 산화질소 생산 유도제로 제공된다. 또한, 스타틴 사용과 황반 변성의 발병 또는 발생 지연의 관계가 입증되었다. 문헌[G. McGwin, et al.,British Journal of Ophthalmology, 87:112125(2003)]을 참조할 수 있다. 따라서, 스타틴은 일반식 (I) 또는 (II)의 화합물과 병용하여 투여되는 경우 안과적 병상(이를 테면 황반 변성, 황반 이영양 및 망막 이영양)로 고통받는 환자에게 이점을 제공할 수 있다. 적합한 스타틴으로는 단지 예로서 로수바스타틴, 피티바스타틴, 심바스타틴, 프라바스타틴, 세리바스타틴, 메바스타틴, 벨로스타틴, 플루바스타틴, 콤팩틴, 로바스타틴, 달바스타틴, 플루인도스타틴, 아토르바스타틴, 아토르바스타틴칼슘(아토르바스타틴의 반칼슘염) 및 디하이드로콤팩틴이 포함된다.Statins serve as lipid lowering agents and / or suitable nitric oxide production inducers. In addition, the relationship between statin use and delayed onset or development of macular degeneration has been demonstrated. G. McGwin, et al., British Journal of Ophthalmology, 87: 112125 (2003). Thus, statins can provide benefits to patients suffering from ocular conditions (such as macular degeneration, macular dystrophies and retinal dystrophies) when administered in combination with a compound of formula (I) or (II). Suitable statins include, by way of example only rosuvastatin, pitavastatin, simvastatin, pravastatin, cerivastatin, mevastatin, belosstatin, fluvastatin, compactin, lovastatin, dalvastatin, fluindostatin, atorvastatin, atorvastatin calcium ( Semicalcium salts of atorvastatin) and dihydrocompactin.
일반식 (I) 또는 (II)의 화합물과 함께 사용될 수 있는 적합한 항염증제로는 단지 예로서 아스피린 및 다른 살리실레이트, 크로몰린, 네도크로밀, 테오필린, 질레우톤, 자피르루카스트, 몬텔루카스트, 프라늘루카스트, 인도메타신 및 리폭시게나제 억제제; 비스테로이드성 항염증 약물(NSAID)(이를 테면 이부프로펜 및 나프록신); 프레드니손, 덱사메타손, 사이클로옥시게나제억제제(즉, COX-1 및/또는 COX-2 억제제, 이를 테면 NaproxenTM 또는 CelebrexTM); 스타틴(단지 예로서, 로수바스타틴, 피티바스타틴, 심바스타틴, 프라바스타틴, 세리바스타틴, 메바스타틴, 벨로스타틴, 플루바스타틴, 콤팩틴, 로바스타틴, 달바스타틴, 플루인도스타틴, 아토르바스타틴, 아토르바스타틴칼슘(아토르바스타틴의 반칼슘염) 및 디하이드로콤팩틴); 및 해리된 스테로이드가 포함된다.Suitable anti-inflammatory agents that can be used with the compounds of general formula (I) or (II) include, by way of example only, aspirin and other salicylates, chromolines, nedocromil, theophylline, zileuton, zafirlukast, montelukast , Pralulucaste, indomethacin and lipoxygenase inhibitors; Nonsteroidal anti-inflammatory drugs (NSAIDs) such as ibuprofen and naproxine; Prednisone, dexamethasone, cyclooxygenase inhibitors (ie, COX-1 and / or COX-2 inhibitors such as Naproxen ™ or Celebrex ™ ); Statins (for example, rosuvastatin, pitavastatin, simvastatin, pravastatin, cerivastatin, mevastatin, belostatin, fluvastatin, compactin, lovastatin, dalvastatin, fludodostatin, atorvastatin, atorvastatin calcium (atorvastatin Semicalcium salts) and dihydrocompactin); And dissociated steroids.
일부 구체예에서, 적합한 기질 금속단백질분해효소(MMP) 억제제가 황반 또는 망막 변성과 관련한 안과적 병상 또는 증상을 치료하기 위해 일반식 (I) 또는 (II)의 화합물과 병용하여 투여될 수 있다. MMP는 대부분의 세포외기질 성분을 가수분해하는 것으로 알려져 있다. 이들 단백질분해효소는 정상 조직 재형성, 배아 형성, 상처 치유 및 혈관형성과 같은 많은 생물학적 과정에 중요한 역할을 한다. 그러나, 황반 변성을 비롯한 많은 질환 상태에서 MMP의 과발현이 관찰되었다. MMP는 대부분 다중 도메인 아연 엔도펩티다제로 확인되었다. 다수의 금속단백질분해효소 억제제가 공지되었다(예를 들어, MMP 억제제를 평가한 문헌[Whittaker M. et al., Chemical Reviews 99(9):27352776 (1999)]을 참조할 수 있다). MMP 억제제의 대표적인 예로 금속단백질분해효소의 조직 억제제(TIMP)(예, TIMP-1, TIMP-2, TIMP-3 또는 TIMP-4), α2-마크로글로불린, 테트라사이클린(예, 테트라사이클린, 미노사이클린 및 독시사이클린), 하이드록사메이트(예, BATIMASTAT, MARIMISTAT 및 TROCADE), 킬레이트제(예, EDTA, 시스테인, 아세틸시스테인, D-페니실아민 및 금염), 합성 MMP 단편, 숙시닐머캅토퓨린, 포스폰아미데이트 및 하이드록사민산이 포함된다. 일반식 (I) 또는 (II)의 화합물과 병용하여 사용될 수 있는 MMP 억제제로는 단지 예로서 상기 언급된 임의의 억제제가 포함된다.In some embodiments, a suitable matrix metalloproteinase (MMP) inhibitor may be administered in combination with a compound of formula (I) or (II) to treat an ocular condition or condition associated with macular or retinal degeneration. MMPs are known to hydrolyze most extracellular matrix components. These proteases play important roles in many biological processes such as normal tissue remodeling, embryonic formation, wound healing and angiogenesis. However, overexpression of MMP has been observed in many disease states, including macular degeneration. MMP was mostly identified as multidomain zinc endopeptidase. Many metalloproteinase inhibitors are known (see, for example, Whittaker M. et al., Chemical Reviews 99 (9): 27352776 (1999)), which evaluated MMP inhibitors. Representative examples of MMP inhibitors are tissue inhibitors of metalloproteinases (TIMPs) (eg TIMP-1, TIMP-2, TIMP-3 or TIMP-4), α 2 -macroglobulin, tetracycline (eg tetracycline, minocycline And doxycycline), hydroxamate (eg BATIMASTAT, MARIMISTAT and TROCADE), chelating agents (eg EDTA, cysteine, acetylcysteine, D-phenicylamine and gold salt), synthetic MMP fragments, succinylmercaptopurine, phosphonami Date and hydroxamic acid. MMP inhibitors that may be used in combination with a compound of formula (I) or (II) include, by way of example only, any of the inhibitors mentioned above.
혈관형성 억제 또는 VEGF 억제 약물의 사용이 또한 황반 변성 및 이영양으로 고통받는 환자에게 이점을 제공할 수 있다. 일반식 (I) 또는 (II)의 구조를 가진 적어도 하나의 화합물과 병용하여 사용될 수 있는 적합한 혈관형성 억제 또는 VEGF 억제 약물을 예로는 루파브(Rhufab) V2(LucentisTM), 트립토파닐-tRNA 합성효소(TrpRS), EyeOO1(항-VEGF 페길화 압타머), 스쿠알라민, RetaaneTM 15 ㎎(데포 현탁액용 아네코타브 아세테이트; 알콘 인코포레이션(Alcon, Inc.)), 콤브레타스타틴 A4 전구약물(CA4P), 마쿠겐(MacugenTM), 미페프렉스(MifeprexTM)(미페프렉스톤 - ru486), 서브테논 트리암시놀론 아세토나이드, 유리체내 결정성 트리암시놀론 아세토나이드, 프리노마스타트(AG3340 - 합성기질 금속단백질분해효소 억제제, Pfizer), 플루오시놀론 아세토나이드(플루오시놀론 안내 이식 포함, Bausch & Lomb/Control Delivery System)), VEGFR 억제제(Sugen) 및 VEGF-Trap(Regeneron/Aventis)가 포함된다. 호두 또는 적포도 껍질에서 추출될 수 있는 레스베라트롤이 혈관형성 억제 활성을 가진 것으로 입증되어, 일부 구체예에서 본원에 개시된 병용 요법을 위한 제2제제 또는 부가 제제로서 사용될 수 있다. 또한, 다른 트랜스-스틸벤 화합물이 유사한 활성을 나타낼 것으로 기대된다.The use of angiogenesis inhibitors or VEGF inhibitory drugs may also provide benefits for patients suffering from macular degeneration and dystrophies. Suitable angiogenesis inhibiting or VEGF inhibitory drugs that can be used in combination with at least one compound having the structure of Formula (I) or (II) include, for example, Rhufab V2 (Lucentis ™ ), tryptophanyl-tRNA Synthetase (TrpRS), EyeOO1 (anti-VEGF PEGylated aptamer), squalane,
일부 구체예에서, 시력 장애를 완화하는데 사용되었던 다른 약제학적 치료법이 적어도 하나의 일반식 (I) 또는 (II)의 화합물과 병용하여 사용될 수 있다. 이러한 치료법으로는 제제 예를 들어, 비주다인(VisudyneTM), 비열 레이저, PKC 412, 엔도비온(Endovion; NeuroSearch A/S), 신경영양 인자, 예를 들어, 신경교세포 유래 신경영양 인자 및 모양체 신경영양 인자, 디아타젬, 도르졸아미드, 포토트롭(Phototrop), 9-cis-레티날, 안약(에코요법(Echo Therapy) 포함), 예를 들어, 포스폴린 요오다이드 또는 에코티오페이트 또는 탄산탈수효소 억제제, AE941(AEterna Laboratories, Inc.), Sirna-027(Sirna Therapeutics, Inc.), 페갑타닙(pegaptanib) (NeXstarPharmaceuticals/Gilead Sciences), 뉴로트로핀(예를 들어, NT-4/5, Genentech), Cand5(Acuity Pharmaceuticals), 라니비주맵(Genentech), INS-37217(Inspire Pharmaceuticals), 인테그린 길항제(예를 들어, Jerini AG and Abbott Laboratories 제품), EG-3306(Ark Therapeutics Ltd.), BDM-E(BioDiem Ltd.), 탈리도미드(예를 들어, EntreMed, Inc.에 의해 사용), 카디오트로핀-1(Genentech), 2-메톡시에스트라디올(Allergan/Oculex), DL-8234(Toray Industries), NTC-200(Neurotech), 테트라티오몰리브데이트(Universityof Michigan), LYN-002(Lynkeus Biotech), 마이크로조류 화합물(microalgal compound)(Aquasearch/Albany, Mera Pharmaceuticals), D-9120(Celltech Group plc), ATX-S1O(Hamamatsu Photonics), TGF-베타2(Genzyme/Celtrix), 티로신키나제 억제제(Allergan, SUGEN, Pfizer), NX-278-L(NeXstar Pharmaceuticals/Gilead Sciences), Opt-24(OPTIS France SA), 망막 세포 신경절 신경보호제(CogentNeurosciences), N-니트로피라졸유도체(Texas A&M University System), KP-102(Krenitsky Pharmaceuticals) 및 사이클로스포린 A를 함께 사용하는 방법이 포함되나 이들에 한정되지 않는다. 문헌[미국 특허출원 공보20040092435호]을 참조할 수 있다.In some embodiments, other pharmaceutical therapies that have been used to alleviate vision disorders can be used in combination with at least one compound of Formula (I) or (II). Such therapies include agents such as Visudyne ™ , specific heat lasers, PKC 412, Endovion (NeuroSearch A / S), neurotrophic factors such as glial cell derived neurotrophic factors and ciliary nerves. Nutritional Factors, Diatagem, Dorzolamide, Phototrop, 9-cis-Retinal, Eye Drops (including Echo Therapy), eg, phospholine iodide or ecothioate or carbonic anhydride Enzyme inhibitors, AE941 from AEterna Laboratories, Inc., Sirna-027 from Sirna Therapeutics, Inc., pegaptanib (NeXstar Pharmaceuticals / Gilead Sciences), neurotropins (eg NT-4 / 5, Genentech ), Cand 5 (Acuity Pharmaceuticals), ranibizumab (Genentech), INS-37217 (Inspire Pharmaceuticals), integrin antagonists (e.g. from Jerini AG and Abbott Laboratories), EG-3306 from Ark Therapeutics Ltd., BDM- E (BioDiem Ltd.), thalidomide (eg, used by EntreMed, Inc.), cardiotropin-1 (Genen tech), 2-methoxyestradiol (Allergan / Oculex), DL-8234 (Toray Industries), NTC-200 (Neurotech), tetrathiomolybdate (University of Michigan), LYN-002 (Lynkeus Biotech), microalgae Microalgal compound (Aquasearch / Albany, Mera Pharmaceuticals), D-9120 (Celltech Group plc), ATX-S1O (Hamamatsu Photonics), TGF-beta2 (Genzyme / Celtrix), tyrosine kinase inhibitors (Allergan, SUGEN, Pfizer ), NX-278-L (NeXstar Pharmaceuticals / Gilead Sciences), Opt-24 (OPTIS France SA), Retinal Cell Ganglion Neuroprotectors (CogentNeurosciences), N-Nitropyrazole Derivatives (Texas A & M University System), KP-102 ( Krenitsky Pharmaceuticals) and cyclosporin A are used together, but are not limited to these. See US Patent Application Publication No. 20040092435.
임의의 경우에, 일부 구체예에서 다중 치료학적 제제(그 하나가 본원에 기술된 화 합물 중 하나임)는 임의의 순서 또는 심지어 동시에 투여된다. 동시 투여되는 경우, 다중 치료학적 제제는 일부 구체예에서 단일, 임의의 경우에 있어서, 다수의 치료학적 제제(그 하나가 본원에 기술된 화합물 중 하나임)는 일부 구체예에서 임의의 순서로 또는 동시에 투여될 수 있다. 동시 투여할 경우, 상기 복수 개의 치료학적 제제는 단일의 통합된 형태로 제공될 수 있거나, 다수의 형태(예를 들어, 단일의 환약 또는 2 개의 별도 환약)로 제공될 수 있다. 치료학적 제제 중 하나가 복수 투여될 수 있거나, 치료제 둘 다 복수투여될 수 있다. 동시에 투여하지 않을 경우, 복수 투여간 시간 간격은 0 주 이상에서 4주 미만과 같이 다양할 수 있다. 또한, 병용 방법, 조성물 및 제형은 단지 2 개의 제제만을 사용할 경우로 한정되지 않으며; 즉, 다수의 치료학적 제제를 병용 투여할 수 있다. 단지 예로서, 일반식 (I) 또는 (II)의 구조를 가진 화합물은 적어도 하나의 황산화제 및 적어도 하나의 산화질소 생산 유도제와 함께 제공될 수 있거나; 일반식 (I) 또는 (II)의 구조를 가진 화합물은 적어도 하나의 산화질소 생산 유도제 및 적어도 하나의 음하전 인지질과 함게 제공될 수 있다.In any case, in some embodiments multiple therapeutic agents, one of which is one of the compounds described herein, are administered in any order or even simultaneously. When administered concurrently, the multiple therapeutic agents are in some embodiments single, in some cases, multiple therapeutic agents, one of which is one of the compounds described herein, in some embodiments in any order or simultaneously. May be administered. When administered concurrently, the plurality of therapeutic agents may be provided in a single integrated form or may be provided in multiple forms (eg, a single pill or two separate pills). One of the therapeutic agents may be administered in multiple doses, or both therapeutic agents may be administered in multiple doses. If not administered at the same time, the time interval between multiple administrations may vary from more than zero weeks to less than four weeks. In addition, the combination methods, compositions and formulations are not limited to the use of only two agents; That is, multiple therapeutic agents can be administered in combination. By way of example only, a compound having a structure of Formula (I) or (II) may be provided with at least one sulfate agent and at least one nitric oxide production inducing agent; Compounds having the structure of formula (I) or (II) may be provided with at least one nitric oxide production inducer and at least one negatively charged phospholipid.
또한, 일반식 (I) 또는 (II)의 화합물은 일부 구체예에서 환자에게 부가적 또는 상승적 이점을 제공할 수 있는 방법과 함께 사용될 수 있다. 시력 장애를 완화시키는 것으로 알려져 있거나, 제시되어 있거나 간주되고 있는 방법으로는 제한 망막 전위법, 광역학 치료법(예를 들어, 수용체-표적화 PDT, Bristol-Myers Squibb, Co.; PDT 주사용 포르피머 나트륨; 베르테포르핀, QLT Inc.; PDT와 로스타포르핀, Miravent Medical Technologies; PDT와 탈라포르핀 나트륨, Nippon Petroleum; 모텍사핀루테튬, Pharmacyclics,, Inc.), 안티센스 올리고뉴클레오티드법[예를 들어, 노바갈리 파마에스아(Novagali PharmaSA)에 의해 검정된 제품 및 ISIS-13650(Isis Pharmaceuticals) 사용], 레이저 광응고 요법, 드루젠 레이저법, 황반 원공 수술법, 황반 전위 수술법, 이식가능한 미니어쳐 텔레스코프를 사용하는 방법, 파이-운동 심혈관 촬영술[미세-레이저요법(Micro-Laser Therapy) 및 영양 혈관 치료법(Feeder Vessel Treatment)이라고도 알려짐], 양성자 빔 치료법, 미세 자극 요법, 망막 박리 및 유리체 수술법, 공막 압편법, 황반하 수술법, 경동공 온열 치료법, 제 I 광계 요법, RNA 간섭 이용법(RNAi), 체외 혈액 여과 기법[막 감별 여과법 및 유동치료법(Rheotherapy)이라고도 알려짐], 마이크로칩 이식법, 줄기 세포 요법, 유전자 대체 요법, 리보자임 유전자 요법[예를 들어, 저산소증 반응 요소(Oxford Biomedica); 렌티팩(Lentipak; Genetix); PDEF 유전자요법(GenVec)], 광수용체/망막세포 이식법[예를 들어, 이식가능한 망막 상피세포(Diacrin, Inc.); 망막세포 이식(CellGenesys, Inc.)] 및 침술법이 포함되나 이에 한정되는 것은 아니다.In addition, the compounds of formula (I) or (II) may be used in some embodiments with methods that may provide additional or synergistic benefits to the patient. Methods known, suggested or considered to alleviate visual impairment include, but are not limited to, limiting retinal translocation, photodynamic therapy (e.g., receptor-targeting PDT, Bristol-Myers Squibb, Co .; Porformer sodium for PDT injections). Berteporphine, QLT Inc., PDT and Lostaporphine, Miravent Medical Technologies; PDT and Talaphorpine Sodium, Nippon Petroleum; Motexapine Lutetium, Pharmacyclics, Inc.), antisense oligonucleotide methods [e.g., Nova Products validated by Novagali PharmaSA and using ISIS-13650 (Isis Pharmaceuticals), laser photocoagulation therapy, drusen laser method, macular hole surgery, macular displacement surgery, implantable miniature telescopes Method, pi-kinetic cardiovascular imaging (also known as Micro-Laser Therapy and Feeder Vessel Treatment), proton beam therapy, micro ruler Extreme therapy, retinal detachment and vitreous surgery, scleral swelling, submacular surgery, carotid hyperthermia, I phototherapy, RNA interference, in vitro blood filtration [also known as membrane differential filtration and rheotherapy ], Microchip transplantation, stem cell therapy, gene replacement therapy, ribozyme gene therapy [eg, hypoxia response element (Oxford Biomedica); Lentipak (Genetix); PDEF Gene Therapy (GenVec)], photoreceptor / retinal cell transplantation (eg, transplantable retinal epithelial cells (Diacrin, Inc.); Retinal cell transplantation (CellGenesys, Inc.) and acupuncture.
개체에 이점을 주기 위해 사용될 수 있는 추가의 병용법으로는 개체가 특정의 안과적 병상과 관련이 있는 것으로 알려진 돌연변이 유전자의 보균자인지를 결정하는 유전자 테스트를 이용하는 것을 포함한다. 단지 예로서, 인간 ABCA4 유전자 결손은 스타르가르트 질환, 추상체-간상체 이영양, 연령 관련 황반 변성 및 색소성 망막염을 비롯한 5 개의 상이한 망막 표현형과 관련이 있는 것으로 판단된다. 예를 들어, 문헌[Allikmets et al., Science, 277:1805-07(1997); Lewis et al., Am. J. Hum. Genet, 64:422-34(1999); Stone et al., Nature Genetics, 20:328-29(1998); Allikmets, Am. J. Hum. Gen., 67:793-799 (2000); Klevering, et al., Ophthalmology, 111:546-553 (2004)]을 참조할 수 있다. 또한, 스타르가르트 질환의 상염색체 우성 형태는 ELOV4 유전자의 돌연변이에 의해 야기된다. 예를 들어, 문헌[Karan, et al., Proc. Natl. Acad. Sci.(2005)]을 참조할 수 있다. 이들 돌연변이중 임의의 것을 지니는 환자는 본원에 개시된 방법으로 치료학적 및/또는 예방학적 이점을 얻을 것으로 예상된다.Additional combinations that can be used to benefit an individual include using genetic tests to determine whether the individual is a carrier of a mutant gene known to be associated with a particular ophthalmic condition. By way of example only, the human ABCA4 gene deficiency is believed to be associated with five different retinal phenotypes, including Stargardt's disease, abstract-antibody dystrophies, age-related macular degeneration and retinitis pigmentosa. See, eg, Allikmets et al., Science, 277: 1805-07 (1997); Lewis et al., Am. J. Hum. Genet, 64: 422-34 (1999); Stone et al., Nature Genetics, 20: 328-29 (1998); Allikmets, Am. J. Hum. Gen., 67: 793-799 (2000); Klevering, et al., Ophthalmology, 111: 546-553 (2004). In addition, an autosomal dominant form of Stargardt disease is caused by mutations in the ELOV4 gene. See, eg, Karan, et al., Proc. Natl. Acad. Sci. (2005). Patients with any of these mutations are expected to benefit therapeutically and / or prophylactically with the methods disclosed herein.
또한, 일부 구체예에서, 혈청 레티놀 수준을 감소시키는 일반식 (I) 또는 (II)의 화합물 또는 다른 제제가 혈청 레티놀 감소로 인해 생기는 부작용을 치료하거나 완화하는 제제와 함께(투여전, 투여중 또는 투여후를 의미함) 투여될 수 있다. 이러한 부작용으로는 피부 건조 및 눈 건조가 포함된다. 따라서, 피부 건조 또는 눈 건조를 완화하거나 치료하는 제제가 일부 구체예에서 혈청 레티놀 수준을 감소시키는 일반식 (I) 또는 (II)의 화합물 또는 다른 제제와 함께 투여될 수 있다.In addition, in some embodiments, a compound of Formula (I) or (II) or another agent that reduces serum retinol levels is combined with an agent that treats or alleviates the side effects resulting from serum retinol reduction (prior to, during or After administration). These side effects include dry skin and dry eyes. Thus, agents that alleviate or treat skin dryness or eye dry may be administered in some embodiments with a compound of Formula (I) or (II) or another agent that reduces serum retinol levels.
실시예Example
다음의 실시예는 일반식 (I) 또는 (II)의 화합물을 합성하기 위한 예시적인 방법을 제공한다. 이들 실시예는 단지 예시적인 목적을 위해 제공된 것으로 본원에 제공된 청구범위를 제한하는 것은 아니다.The following examples provide exemplary methods for synthesizing compounds of formula (I) or (II). These examples are provided for illustrative purposes only and do not limit the claims provided herein.
분석적인 Analytic LCLC /Of MSMS 방법: Way:
방법 A:Method A:
기구: UV 검출기(220 nM) 및 MS 검출기(ESI)가 장착된 워터스(Waters) UPLC/MS.Instrument: Waters UPLC / MS with UV detector (220 nM) and MS detector (ESI).
HPLC 컬럼: 워터스 액퀴티(Waters Acquity) BEH C18 1.7㎛ 2.1 ㎜ x 50 ㎜.HPLC column: Waters Acquity BEH C18 1.7 μm 2.1 mm × 50 mm.
HPLC 구배: 0.6 ㎖/분, 95:5 20 mM 암모늄 포르메이트 완충액(암모늄 하이드록시드를 사용하여 pH 7.4가 되도록 함):아세토니트릴로부터 20:80 암모늄 포르메이트 완충액:아세토니트릴로 1.5 분, 1.3 분 동안 유지.HPLC gradient: 0.6 mL / min, 95: 5 20 mM ammonium formate buffer (to pH 7.4 using ammonium hydroxide): From acetonitrile 20:80 ammonium formate buffer: 1.5 min with acetonitrile, 1.3 Keep for a minute.
방법 B:Method B:
기구: DAD 검출기(220 및 254 nM) 및 MS 검출기(ESI)가 장착된 워터스(Waters) LC/MS.Instrument: Waters LC / MS with DAD detectors 220 and 254 nM and MS detector (ESI).
HPLC 컬럼: 머크(Merck) LiChroCART 30-4 Purospher STAR RP-18, 엔드캡(endcapped), 3㎛, 4.6 ㎜ x 50 ㎜.HPLC column: Merck LiChroCART 30-4 Purospher STAR RP-18, endcapped, 3 μm, 4.6 mm × 50 mm.
HPLC 구배: 1.5 ㎖/분, 95:5 20 mM 암모늄 포르메이트 완충액(암모늄 하이드록시드를 사용하여 pH 7.4가 되도록 함):아세토니트릴로부터 5:95 암모늄 포르메이트 완충액:아세토니트릴로 2.5 분, 1.8 분동안 유지HPLC gradient: 1.5 mL / min, 95: 5 20 mM ammonium formate buffer (to pH 7.4 using ammonium hydroxide): 5:95 ammonium formate buffer from acetonitrile: 2.5 min with acetonitrile, 1.8 Keep for minutes
방법 C:Method C:
기구: UV 검출기(220 nM) 및 MS 검출기(ESI)가 장착된 워터스 얼라이언스(Waters Alliance).Instrument: Waters Alliance with UV detector 220 nM and MS detector (ESI).
HPLC 컬럼: 워터스 엑스테라(Waters XTerra) MS C18, 5 ㎛, 4.6 ㎜ x 50 ㎜.HPLC column: Waters XTerra MS C18, 5 μm, 4.6 mm × 50 mm.
HPLC 구배: 2 ㎖/분, 95:5 물+5% 포름산:아세토니트릴+5% 포름산 0.5 분동안, 이어 5:95 수성:유기물로 5 분, 0.5 분동안 유지HPLC gradient: 2 ml / min, 95: 5 water + 5% formic acid: acetonitrile + 5% formic acid for 0.5 minutes, followed by 5:95 aqueous: organic for 5 minutes, 0.5 minutes
실시예Example 1: 5-(2- 1: 5- (2- terttert -부틸-4--Butyl-4- 클로로페녹시Chlorophenoxy )) 펜탄산의Pentanic 합성 synthesis
메틸 5-브로모발레레이트(1.52 ㎖, 2.09 g, 10.7 밀리몰), 2-tert-부틸-4-클로로-페놀(2.4 g, 13 밀리몰) 및 탄산칼슘(1.4 g, 10.1 밀리몰)을 무수 DMF(10 ㎖)에 현탁시키고 120℃에서 2 시간동안 교반하였다. 생성된 혼합물에 물을 첨가하고(80 ㎖), 에틸 아세테이트(3 x 20 ㎖)로 추출하였다. 유기층을 10% 수산화나트륨(2 x 20 ㎖), 물(1 x 20 ㎖)로 2 회 세척하고 황산나트륨 상에서 건조시키고 진공에서 증발시켰다. 3.46 g(정량)의 조 1a를 수득하고 이를 추가의 정제없이 다음 단계에 사용하였다.Methyl 5-bromovalerate (1.52 mL, 2.09 g, 10.7 mmol), 2-tert-butyl-4-chloro-phenol (2.4 g, 13 mmol) and calcium carbonate (1.4 g, 10.1 mmol) were added to anhydrous DMF ( 10 mL) and stirred at 120 ° C. for 2 hours. Water was added to the resulting mixture (80 mL) and extracted with ethyl acetate (3 x 20 mL). The organic layer was washed twice with 10% sodium hydroxide (2 x 20 mL), water (1 x 20 mL), dried over sodium sulphate and evaporated in vacuo. 3.46 g (quant) of crude 1a were obtained and used in the next step without further purification.
디옥산(50 ㎖) 중 10% 수산화나트륨(10 ㎖) 및 1a(3.46 g)의 혼합물을 실온에서 밤새 교반하였다. 디옥산을 진공에서 제거하고, 남아있는 혼합물을 물로 희석한 다음 에틸 아세테이트(2 x 20 ㎖)로 추출하였다. 진한 염산을 사용하여 수성층의 pH를 4로 조정하고 클로로포름(1 x 20 ㎖)으로 추출하였다. 유기층을 모아 황산나트륨 상에서 건조시키고 진공에서 증발시켰다. 생성물을 헥산으로 분쇄하여 1.87 g(61%, 메틸 5-브로모발레레이트로부터 산출됨)의 백색 결정 1-1을 수득하였다. mp. 95.4-96.4℃A mixture of 10% sodium hydroxide (10 mL) and 1a (3.46 g) in dioxane (50 mL) was stirred overnight at room temperature. Dioxane was removed in vacuo and the remaining mixture was diluted with water and then extracted with ethyl acetate (2 x 20 mL). The pH of the aqueous layer was adjusted to 4 with concentrated hydrochloric acid and extracted with chloroform (1 × 20 mL). The organic layers were combined, dried over sodium sulfate and evaporated in vacuo. The product was triturated with hexane to give 1.87 g (61%, calculated from methyl 5-bromovaleric) white crystals 1-1. mp. 95.4-96.4 ℃
2-tert-부틸-4-클로로페놀 및 적절한 메탄설포닐 에스테르를 사용하여 상기 절차에 의해 다음 화합물을 제조하였다.The following compounds were prepared by the above procedure using 2-tert-butyl-4-chlorophenol and the appropriate methanesulfonyl esters.
2-tert-부틸-4-클로로페놀, 적절한 브로모에스테르 및 제1단계의 염기로서 탄산세슘 및 제2단계의 염기로서 수산화리튬을 사용하여 상기 절차에 의해 다음 화합물을 제조하였다. The following compounds were prepared by the above procedure using 2-tert-butyl-4-chlorophenol, appropriate bromoester and cesium carbonate as the base of the first stage and lithium hydroxide as the base of the second stage.
실시예Example 2: 5-(2- 2: 5- (2- terttert -부틸-4--Butyl-4- 클로로페녹시Chlorophenoxy )-N-(4-) -N- (4- 하이드록시페닐Hydroxyphenyl )) 펜탄아미드Pentanamide 의 합성Synthesis of
카보닐 디이미다졸(0.18 g, 1.11 밀리몰) 및 1-1(0.3 g, 1.05 밀리몰)의 혼합물을 디클로로에탄(2.5 ㎖)에서 30 분동안 교반한 다음, 4-아미노페놀(0.136 g, 1.25 밀리몰) 및 N,N-디이소프로필에틸아민(220 ㎕, 1.25 밀리몰)을 첨가하였다. 생성된 용액을 추가로 4 시간동안 교반하였다. 용매를 증발시키고, 남아있는 혼합물을 20 ㎖ 에테르로 희석한 다음 1M 염화수소산(1 x 2O ㎖)으로 세척하고, 유기층을 황산나트륨 상에서 건조시킨 다음 용매를 증발시켰다. 생성물을 디이소프로필 에테르로 분쇄하여 2-1(6 ㎎, 25%)을 제공하였다.A mixture of carbonyl diimidazole (0.18 g, 1.11 mmol) and 1-1 (0.3 g, 1.05 mmol) was stirred in dichloroethane (2.5 mL) for 30 minutes, then 4-aminophenol (0.136 g, 1.25 mmol) ) And N, N-diisopropylethylamine (220 μl, 1.25 mmol) were added. The resulting solution was stirred for a further 4 hours. The solvent was evaporated and the remaining mixture was diluted with 20 mL ether and then washed with 1M hydrochloric acid (1 × 20 mL), the organic layer was dried over sodium sulphate and the solvent was evaporated. The product was triturated with diisopropyl ether to give 2-1 (6 mg, 25%).
실시예Example 3: 3: 메틸methyl 4-(5-(2- 4- (5- (2- terttert -부틸-4--Butyl-4- 클로로페녹시Chlorophenoxy )) 펜탄아미도Pentanamido )) 벤조에이트의Benzoate 합성 synthesis
디클로로에탄(5 ㎖) 중 염화옥살릴(0.12 g, 0.95 밀리몰) 및 1-1(0.25 g, 0.88 밀리몰)의 혼합물을 실온에서 48 시간동안 교반하였다. 용매를 진공에서 증발시키고, 잔류물을 디클로로에탄에 용해시켰다. 이 용액에 메틸 4-아미노벤조에이트(0.146 g, 0.96 밀리몰) 및 N,N-디이소프로필에틸아민(350 ㎕, 2.0 밀리몰)을 첨가하고 실온에서 밤새 교반하였다. 이 혼합물을 20 ㎖ 10% 염화수소산으로 세척하고, 유기층을 황산나트륨 상에서 건조시킨 다음 용매를 진공에서 제거하여 0.25 g(69%)의 3-1을 제공하였다. LCMS: 방법 A, Rt: 1.85 분, M+H=418.A mixture of oxalyl chloride (0.12 g, 0.95 mmol) and 1-1 (0.25 g, 0.88 mmol) in dichloroethane (5 mL) was stirred for 48 h at room temperature. The solvent was evaporated in vacuo and the residue was dissolved in dichloroethane. To this solution was added methyl 4-aminobenzoate (0.146 g, 0.96 mmol) and N, N-diisopropylethylamine (350 μL, 2.0 mmol) and stirred overnight at room temperature. The mixture was washed with 20
염화옥살릴 또는 염화티오닐을 사용하여 상기 절차에 의해 다음 화합물을 제조하였다.The following compounds were prepared by the above procedure using oxalyl chloride or thionyl chloride.
실시예Example 4: 4: 메틸methyl 3-(3-((2- 3- (3-((2- terttert -부틸-4--Butyl-4- 클로로페녹시Chlorophenoxy )) 메틸methyl )) 사이클로펜탄Cyclopentane -- 카르Carr 복사미도)Copying) 사이클로헥산카르복실레이트의Of cyclohexanecarboxylate 합성 synthesis
무수 DMF 중 EDC HCl(0.067 g, 0.35 밀리몰), N-하이드록시벤조트리아졸(0.053 g, 0.35 밀리몰) 및 1-2(0.109 g, 0.354 밀리몰)의 용액을 실온에서 40 분동안 교반한 다음 메틸 3-아미노사이클로헥산카르복실레이트 하이드로클로라이드(0.075 g, 0.385 밀리몰) 및 트리에틸아민(54 ㎕, 0.385 밀리몰)을 첨가하고, 4 시간동안 계속 교반하였다. 반응 혼합물을 5% 중탄산나트륨(20 ㎖)로 희석하고 디클로로메탄(3 x 20 ㎖)으로 추출하였다. 유기층을 모아 10% 염화수소산(1 x 20 ㎖), 염수(2 x 20 ㎖)로 세척한 다음 황산나트륨 상에서 건조시켰다. 용매를 진공에서 제거하고, 오일 잔류물을 용출액으로서 클로로포름을 사용하여 Kieselgel 6OH 상에서 플래쉬 크로마토그래피에 의해 정제하여 담황색 오일로서 0.1 g(63%)의 4-1을 수득하였다. LCMS: 방법 A, Rt: 1.98 분, M+H=450).A solution of EDC HCl (0.067 g, 0.35 mmol), N-hydroxybenzotriazole (0.053 g, 0.35 mmol) and 1-2 (0.109 g, 0.354 mmol) in anhydrous DMF was stirred at room temperature for 40 minutes and then methyl 3-aminocyclohexanecarboxylate hydrochloride (0.075 g, 0.385 mmol) and triethylamine (54 μL, 0.385 mmol) were added and stirring continued for 4 hours. The reaction mixture was diluted with 5% sodium bicarbonate (20 mL) and extracted with dichloromethane (3 x 20 mL). The combined organic layers were washed with 10% hydrochloric acid (1 x 20 mL), brine (2 x 20 mL) and dried over sodium sulfate. The solvent was removed in vacuo and the oil residue was purified by flash chromatography on Kieselgel 6OH using chloroform as eluent to yield 0.1 g (63%) of 4-1 as a pale yellow oil. LCMS: Method A, Rt: 1.98 min, M + H = 450).
적절한 아민을 사용하여 상기 절차에 의해 다음 화합물을 제조하였다.The following compounds were prepared by the above procedure using the appropriate amine.
실시예Example 5: 4-(5-(2- 5: 4- (5- (2- terttert -부틸-4--Butyl-4- 클로로페녹시Chlorophenoxy )) 펜탄아미도Pentanamido )벤조산의 합성Synthesis of benzoic acid
디옥산(4 ㎖) 중 수산화나트륨(1M, 3 ㎖) 및 3-1(0.25 g, 0.59 밀리몰)의 혼합물을 실온에서 밤새 교반하였다. 1M 염화수소산을 사용하여 pH 4가 되도록 조정하고 용액을 20 ㎖ 디클로로메탄으로 추출하였다. 유기층을 황산나트륨 상에서 건조시키고 용매를 진공에서 제거하여 5-1(0.2 g, 83%)을 수득하였다. LCMS: 방법 B, Rt: 2.08 분, M+H2O=421.A mixture of sodium hydroxide (1M, 3 mL) and 3-1 (0.25 g, 0.59 mmol) in dioxane (4 mL) was stirred at rt overnight. Adjust to
적절한 에스테르로부터 상기 절차에 의해 다음 화합물을 제조하였다.The following compounds were prepared by the above procedure from the appropriate esters.
가수분해 단계 동안 50℃로 가열하고 적절한 에스테르로부터 상기 절차에 의해 다음 화합물을 제조하였다.The following compounds were prepared by the above procedure from a suitable ester and heated to 50 ° C. during the hydrolysis step.
실시예Example 6: N-(4-(2- 6: N- (4- (2- terttert -부틸-4--Butyl-4- 클로로페녹시Chlorophenoxy )부틸)-4-) Butyl) -4- 하이드록시Hydroxy -3-(-3- ( 모르폴Morphol 리노메틸)-Linomethyl)- 벤자미드의Benjamid 합성 synthesis
디클로로에탄(60 ㎖) 중 트리에틸아민(7.5 ㎖, 53.6 몰) 및 Boc-4-아미노부탄올(5.07 g, 26.8 밀리몰)의 용액에 메탄설포닐 클로라이드(2.3 ㎖, 29.5 밀리몰)를 0℃에서 첨가하였다. 첨가 종료후, 혼합물을 추가로 10 분동안 교반하였다. 반응 혼합물을 30 ㎖의 차가운 포화 중탄산나트륨으로 세척하고, 유기층을 황산마그네슘 상에서 건조시켰다. 용매를 증발시켜 9.9 g의 조 6a를 황색 오일로서 제공하였다. 이 조 생성물을 다음 단계에 사용하였다.To a solution of triethylamine (7.5 mL, 53.6 mol) and Boc-4-aminobutanol (5.07 g, 26.8 mmol) in dichloroethane (60 mL) was added methanesulfonyl chloride (2.3 mL, 29.5 mmol) at 0 ° C. It was. After the addition was completed, the mixture was stirred for a further 10 minutes. The reaction mixture was washed with 30 ml of cold saturated sodium bicarbonate and the organic layer was dried over magnesium sulfate. The solvent was evaporated to give 9.9 g of crude 6a as a yellow oil. This crude product was used in the next step.
무수 DMF(40 ㎖) 중 탄산칼륨(6.0 g, 43.4 몰) 및 2-tert-부틸-4-클로로페놀 (4.0 g, 21.7 밀리몰)의 혼합물에 무수 DMF(40 ㎖) 중 24a(9.9 g, 밀리몰)의 용액을 60℃에서 적가하였다. 생성된 혼합물을 60℃에서 밤새 교반하였다. 혼합물을 물에 부은 다음 20 ㎖ 에틸 아세테이트로 추출하고 유기층을 황산나트륨 상에서 건조시킨 다음 용매를 진공에서 제거하였다. 조 생성물(8.3 g)을 헥산/디클로로메탄(1:1) 이어 디클로로메탄을 가지고 구배 용출을 사용하여 컬럼 크로마토그래피에 의해 정제하여 2.41 g(31%) 6b를 제공하였다.24a (9.9 g, mmol) in anhydrous DMF (40 mL) in a mixture of potassium carbonate (6.0 g, 43.4 mol) and 2-tert-butyl-4-chlorophenol (4.0 g, 21.7 mmol) in anhydrous DMF (40 mL) ) Was added dropwise at 60 ° C. The resulting mixture was stirred at 60 ° C. overnight. The mixture was poured into water and extracted with 20 mL ethyl acetate and the organic layer was dried over sodium sulfate and the solvent removed in vacuo. The crude product (8.3 g) was purified by column chromatography using hexane / dichloromethane (1: 1) followed by dichloromethane using a gradient elution to give 2.41 g (31%) 6b.
디옥산 중 HCl(15 ㎖, 6.5M) 및 6b(2.41 g, 6.8 밀리몰)의 혼합물을 에틸 아세테이트에서 밤새 교반하였다. 혼합물을 증발시키고 잔류물을 디에틸 에테르와 에틸 아세테이트의 혼합물로부터 재결정화시켜 1.41 g(81%)의 6c를 수득하였다.A mixture of HCl (15 mL, 6.5 M) and 6b (2.41 g, 6.8 mmol) in dioxane was stirred overnight in ethyl acetate. The mixture was evaporated and the residue was recrystallized from a mixture of diethyl ether and ethyl acetate to give 1.41 g (81%) of 6c.
무수 DMF 중 EDC HCl(0.074 g, 0.385 밀리몰), N-하이드록시벤조트리아졸(0.059 g, 0.385 밀리몰), 트리에틸아민(54 ㎕, 0.385 밀리몰), 4-하이드록시-3-모르폴린-4-일메틸-벤조산(0.091 g, 0.385 밀리몰) 및 4-(2-tert-부틸-4-클로로-페녹시)-부틸아민 하이드로클로라이드(0.102 g, 0.35 밀리몰)의 혼합물을 실온에서 3 시간동안 교반하였다. 20 ㎖의 5% 중탄산나트륨 용액을 첨가하고, 반응물을 디클로로메탄(3 x 20 ㎖)으로 추출하였다. 유기층을 모아 10% 염화수소산(1 x 20 ㎖), 염수(2 x 20 ㎖)로 세척하고 황산나트륨 상에서 건조시켰다. 용매를 진공에서 제거하고, 잔류물을 디에틸 에테르와 에틸 아세테이트의 혼합물로 분쇄하였다. 조 생성물을 용출액으로서 클로로포름:메탄올(10:3)을 사용하여 플래쉬 크로마토그래피(Kieselgel 60H)에 의해 정제하였다. 수율: 0.070 g (42%) 6-1. LCMS: 방법 A, Rt: 1.80 분, M+H=475).EDC HCl (0.074 g, 0.385 mmol), N-hydroxybenzotriazole (0.059 g, 0.385 mmol) in anhydrous DMF, triethylamine (54 μL, 0.385 mmol), 4-hydroxy-3-morpholine-4 A mixture of -ylmethyl-benzoic acid (0.091 g, 0.385 mmol) and 4- (2-tert-butyl-4-chloro-phenoxy) -butylamine hydrochloride (0.102 g, 0.35 mmol) was stirred at room temperature for 3 hours. It was. 20 mL of 5% sodium bicarbonate solution was added and the reaction was extracted with dichloromethane (3 × 20 mL). The combined organic layers were washed with 10% hydrochloric acid (1 x 20 mL), brine (2 x 20 mL) and dried over sodium sulfate. The solvent was removed in vacuo and the residue was triturated with a mixture of diethyl ether and ethyl acetate. The crude product was purified by flash chromatography (Kieselgel 60H) using chloroform: methanol (10: 3) as eluent. Yield: 0.070 g (42%) 6-1. LCMS: Method A, Rt: 1.80 min, M + H = 475).
적절한 산을 사용하여 상기 절차에 의해 다음 화합물을 제조하였다.The following compounds were prepared by the above procedure using the appropriate acid.
실시예Example 7: 4-(4-(2- 7: 4- (4- (2- terttert -부틸-4--Butyl-4- 클로로페녹시Chlorophenoxy )) 부틸카바모일Butyl Carbamoyl )벤조산의 합성Synthesis of benzoic acid
무수 DMF(5 ㎖) 중 EDC HCl(0.084 g, 0.44 밀리몰), N-하이드록시벤조트리아졸 (0.067 g, 0.44 밀리몰), 트리에틸아민(62 ㎕, 0.44 밀리몰), 테레프탈산 모노-tert-부틸 에스테르(0.098 g, 0.44 밀리몰) 및 6c(0.117 g, 0.40 밀리몰)의 혼합물을 실온에서 1 시간동안 교반하였다. 5% 중탄산나트륨 용액을 첨가하고(20 ㎖), 혼합물을 디클로로메탄(3 x 20 ㎖)으로 추출하였다. 유기층을 모아 10% 염화수소산(1 x 20 ㎖), 염수(2 x 20 ㎖)로 세척하고 황산나트륨 상에서 건조시켰다. 용매를 진공에서 제거하여 0.246 g의 조 7a를 제공하였다.EDC HCl (0.084 g, 0.44 mmol), N-hydroxybenzotriazole (0.067 g, 0.44 mmol) in anhydrous DMF (5 mL), triethylamine (62 μL, 0.44 mmol), terephthalic acid mono-tert-butyl ester (0.098 g, 0.44 mmol) and 6c (0.117 g, 0.40 mmol) were stirred at room temperature for 1 hour. 5% sodium bicarbonate solution was added (20 mL) and the mixture was extracted with dichloromethane (3 x 20 mL). The combined organic layers were washed with 10% hydrochloric acid (1 x 20 mL), brine (2 x 20 mL) and dried over sodium sulfate. The solvent was removed in vacuo to give 0.246 g of crude 7a.
에스테르 7a를 5 ㎖의 디옥산에 용해시키고, 디옥산 중 6.5 M 염화수소 4 ㎖를 첨가한 다음 혼합물을 실온에서 24 시간동안 교반하였다. 반응 혼합물을 물에 붓고 디클로로메탄(2 x 2O ㎖)으로 추출하였다. 유기층을 모아 물(1 x 20 ㎖)로 세척하고, 황산나트륨 상에서 건조시킨 다음 용매를 증발시켰다. 생성물 7-1을 에테르/헥산으로부터 결정화시키고 여과한 다음 에테르/헥산으로 수 회 세척하여 0.127(59%)의 백색 결정 25-1을 제공하였다. LCMS: 방법 A, Rt: 1.36 분, M+H=404.Ester 7a was dissolved in 5 mL of dioxane, 4 mL of 6.5 M hydrogen chloride in dioxane was added and the mixture was stirred at rt for 24 h. The reaction mixture was poured into water and extracted with dichloromethane (2 x 20 mL). The combined organic layers were washed with water (1 x 20 mL), dried over sodium sulphate and the solvent was evaporated. Product 7-1 was crystallized from ether / hexanes, filtered and washed several times with ether / hexanes to give 0.127 (59%) of white crystals 25-1. LCMS: Method A, Rt: 1.36 min, M + H = 404.
상기 절차에 의해 다음 화합물을 제조하였다.The following compound was prepared by the above procedure.
실시예Example 8 8
본원에 기술된 절차에 의해 다음 화합물을 제조하였다.The following compounds were prepared by the procedures described herein.
다음 실시예는 일반식 (I) 또는 (II)의 화합물의 효능 및 안정성을 시험하기 위한 예시적인 방법을 제공한다. 이들 실시예는 단지 예시적인 목적을 위해 제공된 것이지 본원에 제공된 청구범위를 제한하기 위해 제공된 것이 아니다.The following examples provide exemplary methods for testing the efficacy and stability of the compounds of formula (I) or (II). These examples are provided for illustrative purposes only and are not intended to limit the claims provided herein.
마우스 및 Mouse and 래트Rat 연구 Research
abca4-/- 마우스에서 A2E의 형성을 차단하기 위한 일반식 (I) 또는 (II)의 화합물의 최적 용량은 표준 용량 단계적 확대 연구를 이용하여 결정될 수 있다. 사용될 용량 범위를 결정하기 위해, RBP-TTR 상호작용을 억제하는 조절자를 검출하는 고생산성 시험관내 분석을 전개시킨다. RBP-TTR 상호작용을 50% 억제하는 약물 농도(IC5O 값)를 데이터로부터 산출한다. 이들 실험에서, RBP-TTR 상호작용의 강력한 억제제로 알려진 펜레티나이드를 양성 대조군으로서 사용한다. 전형적인 용량-반응 실험의 대표적인 데이터가 도 1에 도시되어 있다. 일반식 (I) 또는 (II)의 구조를 가진 화합물을 사용하는 생체내 접근법의 예가 아래 개시되어 있다.The optimal dose of a compound of formula (I) or (II) to block the formation of A2E in abca4-/-mice can be determined using standard dose escalation studies. To determine the dose range to be used, a high productivity in vitro assay is developed that detects modulators that inhibit RBP-TTR interaction. Drug concentrations (IC 50 values) that inhibit 50% of RBP-TTR interactions are calculated from the data. In these experiments, fenretinide, known as a potent inhibitor of RBP-TTR interaction, is used as a positive control. Representative data of a typical dose-response experiment is shown in FIG. 1. Examples of in vivo approaches using compounds having the structure of Formula (I) or (II) are disclosed below.
명순응 마우스로부터 망막내 올-트랜스-레티날에 대한 일반식 (I) 또는 (II)의 화합물의 효과는 인간의 치료학적 용량을 다룬 용량으로 결정된다. 방법으로는 마우스를 아침에 단일 복강내 용량으로 처리하는 단계를 포함한다. 일부 구체예에서, 온종일 망막내 올-트랜스-레티날을 감소된 수준으로 유지하기 위해 주사 횟수의 증가가 필요할 수 있다.The effect of the compound of formula (I) or (II) on intraretinal all-trans-retinal from bright mice is determined by the dose dealing with the therapeutic dose in humans. The method includes treating mice with a single intraperitoneal dose in the morning. In some embodiments, an increase in the number of injections may be necessary to keep all-trans-retinal in the retina at reduced levels throughout the day.
ABCA4 녹아웃 마우스. ABCA4는 간상체 및 추상체 광수용체의 외절 원반에서 ATP-결합카세트(ABC) 수송체인 림 단백질(RmP)을 코딩한다. RmP에 대한 수송 기질은 알려져 있지 않다. abca4 유전자에 녹아웃 돌연변이를 가지도록 생산된 마우스{문헌[Weng et al., Cell, 98:13-23 (1999)]을 참조할 수 있다}는 RmP 기능을 연구하는데 유용할 뿐만 아니라 후보 물질의 효능을 생체내에서 스크리닝하는데 유용하다. 이들 동물은 복잡한 안구 표현형(ocular phenotype)을 가진다: (i) 느린 광수용체 변성, (ii) 광노출에 따른 간상체 감도의 회복 지연, (iii) 광표백후 광수용체 외절에서의 atRAL 증가 및 atROL 감소, (iv) 외절에서의 구조적으로 증가된 포스파티딜에탄올아민(PE) 및 (v) RPE 세포에서의 리포푸신 축적. 문헌[Weng et al., Cell, 98:13-23 (1999)]을 참조할 수 있다. ABCA4 knockout mouse. ABCA4 encodes a rim protein (RmP), an ATP-binding cassette (ABC) transporter in the extremity discs of rods and abstract photoreceptors. The transport substrate for RmP is unknown. Mice produced with knockout mutations in the abca4 gene (see Weng et al., Cell, 98: 13-23 (1999)) are useful for studying RmP function as well as the efficacy of candidates. It is useful for screening in vivo. These animals have complex ocular phenotypes: (i) slow photoreceptor degeneration, (ii) delayed recovery of rod sensitivity following photoexposure, (iii) increased atRAL and decreased atROL at photoreceptor disruption after photobleaching, (iv) structurally increased phosphatidylethanolamine (PE) and (v) lipofucin accumulation in RPE cells at the extremities. See Weng et al., Cell, 98: 13-23 (1999).
광수용체의 변성 속도는 두 가지 기술을 이용하여 처리 및 미처리 야생형 및 abca4-/- 마우스에서 감시된다. 하나는 다른 시간에 ERG 분석에 의해 마우스를 연구하는 것으로 임상 진단 과정에 채용된다. 문헌[Weng etal., Cell, 98:13-23 (1999)]을 참조할 수 있다. 마취한 마우스의 각막 표면에 전극을 설치하고, 광섬광에 대한 전기적 반응을 망막으로부터 기록했다. 광수용체의 광유도 과다분극으로부터 야기된 α-파 진폭은 광수용체 변성의 감수성 지표(sensitive indicator)이다. 문헌[Kedzierskiet al., Invest. Ophthalmol. Vis. Sci., 38:498-509 (1997)]을 참조할 수 있다. ERG는 살아있는 동물에서 수행된다. 일부 구체예에서, 동일한 마우스를 경시적 연구 동안 반복적으로 분석한다. 광수용체 변성을 정량하는 명확한 기술은 망막 절편의 조직학적 분석이다. 각 시점에서, 망막에 잔존하는 광수용체의 수는 외핵층내 광수용체 핵의 열(row)을 계수함으로써 결정될 것이다.The denaturation rate of photoreceptors is monitored in treated and untreated wild-type and abca4-/-mice using two techniques. One is to study mice by ERG analysis at another time and is employed in the clinical diagnostic process. See Weng et al., Cell, 98: 13-23 (1999). An electrode was placed on the corneal surface of the anesthetized mouse, and the electrical response to light flash was recorded from the retina. The α-wave amplitude resulting from photoinduced hyperpolarization of the photoreceptor is a sensitive indicator of photoreceptor degeneration. Kezierski et al., Invest. Ophthalmol. Vis. Sci., 38: 498-509 (1997). ERG is performed in live animals. In some embodiments, the same mouse is analyzed repeatedly during the study. A clear technique for quantifying photoreceptor degeneration is histological analysis of retinal sections. At each time point, the number of photoreceptors remaining in the retina will be determined by counting the rows of photoreceptor nuclei in the outer nuclear layer.
조직 추출. 안구 시료를 pH 7.2의 1 ㎖ PBS 중 얼음상에서 해동시키고, 이중의 유리-유리 균질화기를 이용하여 손으로 균질화시켰다. 1 ㎖ 클로로포름/메탄올(2:1, v/v)을 첨가한 뒤 시료를 추가로 균질화시켰다. 시료를 보로실리케이트 튜브로 옮기고, 지질을 4 ㎖의 클로로포름으로 추출하였다. 유기 추출물을 3 ㎖의 물로 세척한 뒤, 시료를 3,000×g으로 10 분간 원심분리하였다. 클로로포름상을 따라내고, 수성상을 추가의 4 ㎖ 클로로포름으로 재추출하였다. 원심 분리후, 클로로포름상을 모으고, 시료를 질소 기체하에서 건조시켰다. 시료 잔류물을 200 ㎕ 2-프로판올에 재현탁시키고, 아래 기술된 바와 같이 HPLC로 분석하였다. Tissue extraction. Eye samples were thawed on ice in 1 ml PBS at pH 7.2 and homogenized by hand using a double glass-glass homogenizer. The sample was further homogenized after addition of 1 ml chloroform / methanol (2: 1, v / v). The sample was transferred to a borosilicate tube and the lipid was extracted with 4 ml of chloroform. The organic extract was washed with 3 ml of water and then the sample was centrifuged at 3,000 x g for 10 minutes. The chloroform phase was decanted and the aqueous phase was reextracted with an additional 4 mL chloroform. After centrifugation, the chloroform phases were combined and the sample was dried under nitrogen gas. Sample residue was resuspended in 200 μl 2-propanol and analyzed by HPLC as described below.
HPLC 분석. 형광 및 다이오드 어레이 검출기가 구비된 아길런트(Agilent) 1100 시리즈 액체 크로마토그래피를 이용하여 아길런트 조르박스(Agilent Zorbax) Rx-Sil 컬럼(5㎛, 4.6×250 ㎜) 상에서 크로마토그래피 분리를 수행하였다. 이동상을 분당 소정 부피의 목적하는 속도로 이동시켰다. 시료 피크를 인증 표준(authentic standard)의 체류 시간 및 흡수 스펙트럼과 비교하여 동정하였다. 데이터를 형광 검출기로부터 얻은 피크 형광(L.U.)으로 기록하였다. HPLC analysis. Chromatographic separations were performed on an Agilent Zorbax Rx-Sil column (5 μm, 4.6 × 250 mm) using Agilent 1100 series liquid chromatography with fluorescence and diode array detectors. The mobile phase was moved at a desired volume of volume per minute. Sample peaks were identified by comparison with retention time and absorption spectra of an authentic standard. Data was recorded as peak fluorescence (LU) obtained from the fluorescence detector.
실험군 마우스에게는 일반식 (I) 또는 (II)의 화합물을 투여하고, 대조군 마우스에게는 DMSO 만을 투여한 뒤 A2E 축적에 대해 분석하였다. 실험군에게는 일일 약 10 내지 약 25 ㎕의 DMSO 중 약 2.5 내지 약 20 ㎎/㎏의 일반식 (I) 또는 (II)의 화합물을 투여하였다. 약 50㎎/㎏의 최고 투여량에서도 효과가 관찰되지 않은 경우에는 더 많은 투여량으로 시험하였다. 대조군에게는 DMSO 만을 10 내지 25 ㎕ 주사하였다. 장기 투여 동안 복강내(i.p.) 주사에 의해 실험 또는 대조 물질을 마우스에게 투여하였다.Experimental mice received a compound of formula (I) or (II), and control mice received DMSO only and were then analyzed for A2E accumulation. The experimental group received from about 2.5 to about 20 mg / kg of the compound of formula (I) or (II) in about 10 to about 25 μl of DMSO per day. If no effect was observed even at the highest dose of about 50 mg / kg, the higher dose was tested. The control group was injected with 10-25 μl DMSO alone. Experimental or control substances were administered to mice by intraperitoneal (i.p.) injections during long term administration.
abca4-/- 마우스 RPE에서 A2E의 축적을 평가하기 위하여, 일일 약 2.5 내지 약 20 ㎎/㎏의 일반식 (I) 또는 (II)의 화합물을 복강내 주사에 의해 2 개월령 abca4-/- 마우스에 제공하였다. 예정된 기간후, 실험군 마우스 및 대조군 마우스를 모두 희생시키고 RPE내 A2E 수준을 HPLC로 측정하였다.abca4-/-To assess the accumulation of A2E in mouse RPE, a compound of formula (I) or (II) of about 2.5 to about 20 mg / kg per day intraperitoneally injected into two-month-old abca4-/-mice Provided. After a predetermined period, both experimental and control mice were sacrificed and A2E levels in RPE were measured by HPLC.
실시예Example 9: 9: 간상체Rod 세포사Cell death 또는 or 간상체Rod 기능 손상에 대한 시험 화합물의 효과 Effect of Test Compounds on Functional Impairment
실험군 마우스에게는 일반식 (I) 또는 (II)의 화합물을 투여하고, 대조군 마우스에게는 DMSO 만을 투여한 뒤 간상체 세포사 또는 간상체 기능 손상에 대한 시험 화합물의 효과를 분석하였다. 실험군에게는 일일 약 10 내지 약 25 ㎕의 DMSO 중의 약 2.5 내지 약 20 ㎎/㎏의 일반식 (I) 또는 (II)의 화합물을 투여하였다. 약 50 ㎎/㎏의 최고 투여량에서도 효과가 관찰되지 않은 경우에는 더 많은 투여량으로 시험하였다. 대조군에게는 DMSO 만을 약 10 내지 약 25 ㎕ 주사하였다. 다양한 실험기간 동안 복강내 주사에 의해 실험 또는 대조 물질을 마우스에게 투여하였다. 다르게는, 다양한 실험기간 동안 약 0.25 ㎕/시의 속도로 실험 물질 또는 대조 물질을 전달하는 펌프를 마우스에 이식하였다.Experimental mice were administered a compound of formula (I) or (II), and control mice were administered DMSO alone, and the effects of test compounds on rod cell death or impaired rod function were analyzed. The experimental group received from about 2.5 to about 20 mg / kg of the compound of formula (I) or (II) in about 10 to about 25 μl of DMSO daily. If no effect was observed even at the highest dose of about 50 mg / kg, the higher dose was tested. The control group was injected with about 10 to about 25 μl of DMSO alone. Mice were administered to the experiment or control material by intraperitoneal injection for various durations of the experiment. Alternatively, mice were implanted with a pump that delivered the test or control material at a rate of about 0.25 μl / hr for various durations of the experiment.
약 8 주간 일일 약 2.5 내지 약 20 ㎎/㎏의 일반식 (I) 또는 (II)의 화합물로 처리한 마우스에 대해 ERG 기록을 감시하고 망막 조직학을 수행함으로써 간상체 세포사 또는 간상체 기능 손상에 대한 일반식 (I) 또는 (II)의 화합물의 효과를 분석하였다.Formulas for rod cell death or rod function impairment by monitoring ERG recordings and performing retinal histology for mice treated with compounds of Formula (I) or (II) at about 2.5 to about 20 mg / kg daily for about 8 weeks The effect of the compound of (I) or (II) was analyzed.
실시예Example 10: 광 손상으로부터의 보호에 대한 시험 10: Test for protection from light damage
다음의 연구는 문헌[Sieving, P.A., et al, Proc. Natl. Acad. Sci, 98:1835-40 (2001)]으로부터 이루어진 것이다. 만성 광-노출 연구를 위하여, 스프래그-돌리(Sprague-Dawley) 수컷 7주령 알비노 래트를 5 룩스 형광 백색광의 12:12 시간 명/암 사이클에 순응시켰다. 복강내 주사에 의해 0.18 ㎖ DMSO 중의 약 20 내지 약 50 ㎎/㎏ 일반식 (I) 또는 (II)의 화합물을 8 주 동안 1일 3회로 만성 래트에 투여하였다. 대조군에게는 0.18 ㎖ DMSO를 복강내 주사하였다. 마지막 주사하고 이틀 후에 래트를 희생시켰다. 약 50 ㎎/㎏의 최고 투여량에서도 효과가 관찰되지 않은 경우에는 더 많은 투여량으로 시험하였다.The following study is described in Sieving, P.A., et al, Proc. Natl. Acad. Sci, 98: 1835-40 (2001). For chronic light-exposure studies, Sprague-Dawley male 7-week-old albino rats were acclimated to a 12:12 hour light / dark cycle of 5 lux fluorescent white light. About 20 to about 50 mg / kg compound of formula (I) or (II) in 0.18 ml DMSO was administered to chronic rats three times a day for 8 weeks by intraperitoneal injection. The control group was injected intraperitoneally with 0.18 ml DMSO. Rats were sacrificed two days after the last injection. If no effect was observed even at the highest dose of about 50 mg / kg, the higher dose was tested.
급성 광-노출 연구를 위하여, 래트를 밤새 암-순응시킨 뒤, 암적색광하에서 0.18 ㎖ DMSO 중의 약 20 내지 약 50 ㎎/㎏ 일반식 (I) 또는 (II)의 화합물을 단일 복강내 주사하고 ERG 측정에 앞서 표백광에 노출시키기 전 1 시간동안 어두운 상태로 유지하였다. 래트를 2,000 룩스의 백색 형광 빛에 48 시간 동안 노출시켰다. 7 일후 ERG를 기록하고, 즉시 조직구조를 조사하였다.For acute light-exposure studies, rats were cancer-adjusted overnight, followed by a single intraperitoneal injection of a compound of formula (I) or (II) with about 20 to about 50 mg / kg in 0.18 ml DMSO under dark red light and ERG It remained dark for 1 hour prior to exposure to bleached light prior to measurement. Rats were exposed to 2,000 lux white fluorescent light for 48 hours. ERGs were recorded after 7 days and tissue structures examined immediately.
래트를 안락사시키고 안구를 적출하였다. 양반구(hemisphere)에 걸쳐 200 ㎛마다 외핵층 두께 및 간상체 외절(ROS) 길이의 원주 세포수를 측정하고, 수치를 평균내어 전체 망막에 대한 세포 변화의 척도(measure)를 얻었다. 치료 4 주 및 8 주에 만성 래트로부터 ERG를 기록하였다. 급성 설치류에서는, 표백광으로부터의 간상체 회복은 추상체 기여를 유발하지 않는 자극을 이용함으로써 암-순응 ERG에 의해 추적되었다. 추상체 회복은 광순응 EGG에 의해 추적되었다. ERG에앞서, 동물을 암적색광하에서 준비하고 안락사시켰다. 동공을 확장시키고, 골드와이어 각막 루프(gold-wire corneal loop)를 이용하여 양안구로부터 ERG를 동시에 기록하였다.Rats were euthanized and eyeballs were extracted. The circumferential cell number of the outer nuclear layer thickness and rod rupture length (ROS) length was measured every 200 μm over the hemisphere, and the values were averaged to obtain a measure of cellular change over the entire retina. ERGs were recorded from chronic rats at 4 and 8 weeks of treatment. In acute rodents, rod recovery from bleaching light was tracked by cancer-compliant ERG by using stimuli that did not cause abstract contribution. Abstraction recovery was tracked by photocompliant EGG. Prior to ERG, animals were prepared and euthanized under dark red light. The pupils were expanded and ERGs were simultaneously recorded from both eyes using a gold-wire corneal loop.
실시예Example 11: 11: 펜레티나이드를Fenretinide 포함하는 병용 요법 Combination Therapies Included
추가의 두 처리군을 제외하고, 실시예 8 및 9에 개시된 방법으로 마우스 및/또는 래트를 시험하였다. 추가 처리군 중 하나에서, 마우스 및/또는 래트군에 펜레티나이드를 일일 약 5 ㎎/㎏에서 일일 약 50 ㎎/㎏로 증가시키면서 처리하였다. 두 번째 추가 처리군에서, 마우스 및/또는 래트군은 일일 약 20 ㎎/㎏의 시험 화합물 및 일일 약 5 ㎎/㎏에서 약 50 ㎎/㎏로 증가하는 용량의 펜레티나이드를 병용하여 처리하였다. 병용 요법에 대한 이점을 실시예 8 및 9에 개시된 바와 같이 분석하였다.Except for two additional treatment groups, mice and / or rats were tested by the methods described in Examples 8 and 9. In one of the additional treatment groups, mice and / or rats were treated with fenretinide increasing from about 5 mg / kg per day to about 50 mg / kg per day. In the second additional treatment group, mice and / or rat groups were treated with a combination of about 20 mg / kg of test compound per day and fenretinide increasing from about 5 mg / kg to about 50 mg / kg per day. The benefits for the combination therapy were analyzed as disclosed in Examples 8 and 9.
실시예Example 12: 12: abca4abca4 널 돌연변이 마우스에서 In null mutant mice 리포푸신(및/또는 A2E)의Of lipofucin (and / or A2E) 축적에 대한 시험 화합물의 효과: 단계( Effect of test compound on accumulation: step ( PhasePhase ) I - 용량 반응 및 혈청 레티놀에 대한 효과) I-dose response and effect on serum retinol
동물 및 인간 대상에서 혈청 레티놀 감소에 대한 일반식 (I) 또는 (II)의 화합물의 효과는 본 발명자들로 하여금 리포푸신 및 독성 비스-레티노이드 공역체 A2E의 감소가 또한 실현될 수 있는지에 관한 가능성을 탐색하게 하였다. 이러한 접근법에 관한 이론적 근거는 두 개의 독립적인 과학적 증거에 기초한다: 1) 공지의 시각 사이클 효소(11-시스 레티놀 탈수소효소)의 억제를 통한 안내 비타민 A 농도의 감소가 리포푸신 및 A2E를 상당히 감소시킨다는 것; 및 2) 비타민 A 결핍 식이로 유지된 동물이 리포푸신 축적에 현저한 감소를 나타낸다는 것. 따라서, 본 실시예의 목적은 안조직에 리포푸신 및 A2E가 다량 축적되는 동물 모델인 abca4 널 돌연변이 마우스에서 일반식 (I) 또는 (II)의 화합물의 효과를 조사하는 것이었다.The effect of the compounds of formula (I) or (II) on serum retinol reduction in animal and human subjects has made it possible for the inventors to see if reduction of lipofucin and toxic bis-retinoid conjugate A2E can also be realized. To search. The rationale for this approach is based on two independent scientific evidences: 1) Reduction of intraocular vitamin A concentrations through inhibition of known visual cycle enzymes (11-cis retinol dehydrogenase) significantly reduces lipofucin and A2E. To make; And 2) animals maintained on a vitamin A deficient diet show a significant decrease in lipofuscin accumulation. Therefore, the purpose of this example was to investigate the effect of compounds of formula (I) or (II) in abca4 null mutant mice, an animal model in which large amounts of lipofucin and A2E accumulate in ocular tissues.
초기 연구는 혈청 레티놀에 대한 일반식 (I) 또는 (II)의 화합물의 효과를 시험함으로써 개시되었다. 동물을 그룹으로 나누고, 각각 DMSO, 약 20 ㎎/㎏의 일반식 (I) 또는 (II)의 화합물을 14 일간 투여하였다. 연구 기간의 종료 시점에, 동물로부터 혈액을 채취하여 혈청을 준비하고, 혈청의 아세토니트릴 추출물을 역상 LC/MS로 분석하였다. UV-가시광선 스펙트럼 및 질량/전하 분석을 수행하여 용출된 피크를 동정하였다. DMSO 또는 일반식 (I)의 구조를 가진 화합물로 처리한 마우스에서 혈청 레티놀 수준을 나타내는 대표적인 크로마토그래피 데이터를 도 9에 도시되어 있다. 시험 화합물(일반식 (I)와 일치하는 구조)의 항정 상태 혈청 농도를 또한 HPLC에 의해 결정하였다(도 3 참조). 추가적으로, 혈청내 RBP 수준은 면역탁본법에 의해 정량하였다(도 4 참조).Initial studies were initiated by testing the effect of compounds of formula (I) or (II) on serum retinol. The animals were divided into groups, and DMSO, about 20 mg / kg of the compound of general formula (I) or (II), respectively, was administered for 14 days. At the end of the study period, blood was taken from the animals to prepare serum and the acetonitrile extract of the serum was analyzed by reverse phase LC / MS. UV-visible spectra and mass / charge analysis were performed to identify eluted peaks. Representative chromatographic data showing serum retinol levels in mice treated with DMSO or a compound having formula (I) are shown in FIG. 9. Steady state serum concentrations of test compounds (structures consistent with formula (I)) were also determined by HPLC (see FIG. 3). In addition, serum RBP levels were quantified by immunoassay (see FIG. 4).
시각 사이클에서 적어도 하나의 효소를 조절하지 않으면서 환자의 혈청 레티놀 수준을 저하시키는 제제 또는 제제들을 투여하면 황반 및/또는 망막 이영양 및 변성 또는 그와 관련된 증상이 치료될 것으로 기대된다. 본원에 개시된 것들과 같은 분석법은 일부 구체예에서 일반식 (I) 또는 (II)의 구조를 가진 화합물 중에서 선택된 제제를 비롯하여 이러한 활성을 가진 추가의 제제를 선택하는데 사용될 수 있다.Administration of an agent or agents that lower serum retinol levels in a patient without modulating at least one enzyme in the visual cycle is expected to treat macular and / or retinal dystrophy and degeneration or symptoms associated therewith. Assays, such as those disclosed herein, may be used in some embodiments to select additional agents having this activity, including agents selected from compounds having the structure of Formula (I) or (II).
실시예Example 13: 13: abca4abca4 널 돌연변이 마우스에서 In null mutant mice 리포푸신Lipofucin (및/또는 A2E)의 축적에 대한 시험 화합물의 효과: 단계 Effect of test compound on accumulation of (and / or A2E): step IIII - - abca4abca4 널 돌연변이 마우스의 만성 치료 Chronic Treatment of Null Mutant Mice
abca4 널 돌연변이 마우스에서 A2E 및 A2E 전구체 감소에 대한 일반식 (I) 또는 (II)의 화합물의 효과를 평가하기 위해 연구하였다. DMSO(약 20 ㎎/㎏, 복강내) 중에서 일반식 (I) 또는 (II)의 화합물을 적어도 28 일동안 매일 abca4 널 돌연변이 마우스(BL6/129, 2개월령)에 투여하였다. 연령/세포주-일치 대조군 마우스에는 DMSO 비히클만을 투여하였다. 0, 14 및 28 일에 마우스 시료를 취하여(n=그룹 당 3 마리), 안구를 적출하고 클로로포름-가용성 성분(지질, 레티노이드 및 지질-레티노이드 공역체)을 추출하였다. 마우스를 경추 탈골에 의해 희생시키고, 안구를 적출하고 각각을 냉동 바이알에 스냅 냉동(snap frozen)하였다. 이어서, 시료 추출물을 온라인 형광 검출과 함께 HPLC로 분석하였다. abca4 널 돌연변이 마우스의 아이컵(eyecup) 추출로부터 수득한 대표적인 크로마토그래피 추적이 도 5에 도시되어 있다. 유사한 연구를 실시하여 망막전위도 및 형태학적 표현형에 대한 일반식 (I) 또는 (II)의 화합물 처리의 효과를 확인하였다.Abca4 null mutant mice were studied to evaluate the effect of compounds of formula (I) or (II) on A2E and A2E precursor reduction. Compounds of Formula (I) or (II) in DMSO (about 20 mg / kg, intraperitoneal) were administered to abca4 null mutant mice (BL6 / 129, 2 months old) daily for at least 28 days. Age / cell line-matched control mice received DMSO vehicle only. Mouse samples were taken on
실시예Example 14: 시험 화합물 및 스타틴을 포함하는 병용 요법 14: Combination Therapies Including Test Compounds and Statins
추가의 두 처리군을 제외하고, 실시예 8 및 9에 기술된 방식으로 마우스 및/또는 래트를 시험하였다. 추가 처리군 중 하나에서, 마우스 및/또는 래트군을 체중에 기초한 최적의 투여량으로 Lipitor®(아토르바스타틴), Mevacor®(로바스타틴), Pravachol®(프라바스타틴나트륨), ZocorTM(심바스타틴), Leschol(플루바스타틴 나트륨) 등과 같은 적절한 스타틴으로 처리하였다. 두 번째 추가의 처리군에서, 마우스 및/또는 래트군을 일일 약 20 ㎎/㎏의 일반식 (I) 또는 (II)의 화합물 및 전 단계에서 사용된 스타틴의 증가 용량으로 병용 처리하였다. 이러한 스타틴에 대해 제안된 인간 투여량은 예를 들어 다음과 같다: Lipitor®(아토르바스타틴) 약 10 내지 약 80 ㎎/일, Mevacor®(로바스타틴) 약 10 내지 약 80 ㎎/일, Pravachol®(프라바스타틴 나트륨) 약 10 내지 약 40 ㎎/일, ZocorTM(심바스타틴) 약 5 내지 약 80 ㎎/일, Leschol(플루바스타틴 나트륨) 약 20 내지 약 80 ㎎/일. 마우스 및/또는 래트 대상에 대한 스타틴의 투여량은 체중에 기초하여 계산하여야 한다. 병용 요법의 이점을 실시예 8 및 9에 기술된 바에 따라 분석하였다.Except for two additional treatment groups, mice and / or rats were tested in the manner described in Examples 8 and 9. In one of the additional treatment groups, mice and / or rats were treated at the optimal dose based on body weight: Lipitor ® (atorvastatin), Mevacor ® (lovastatin), Pravachol ® (sodium pravastatin), Zocor TM (simvastatin), Leschol (flu) Treatment with appropriate statins). In the second additional treatment group, mice and / or rat groups were co-treated with about 20 mg / kg of compound of formula (I) or (II) per day and increasing doses of statin used in the previous step. Suggested human dosages for such statins are, for example: Lipitor ® (atorvastatin) about 10 to about 80 mg / day, Mevacor ® (lovastatin) about 10 to about 80 mg / day, Pravachol ® (pravastatin sodium ) About 10 to about 40 mg / day, Zocor ™ (simvastatin) about 5 to about 80 mg / day, Leschol (fluvastatin sodium) about 20 to about 80 mg / day. Dosages of statins for mice and / or rat subjects should be calculated based on body weight. The benefits of the combination therapy were analyzed as described in Examples 8 and 9.
실시예Example 15: 시험 화합물, 비타민 및 미네랄을 포함하는 병용 요법 15: Combination Therapies Including Test Compounds, Vitamins, and Minerals
선택된 비타민 및 미네랄을 사용한 점을 제외하고는 실시예 13에 기술된 방식에 따라 마우스 및/또는 래트를 시험하였다. 황반 변성의 발달 및 재발을 억제하는데 유효한 양으로 일반식 (I) 또는 (II)의 화합물을 비타민 및 미네랄과 병용하여 경구 또는 비경구 투여하였다. 시험 투여는 초기에 약 20 ㎎/㎏/일의 일반식 (I) 또는 (II)의 화합물과 약 100 내지 약 1000 ㎎의 비타민 C, 약 100 내지 약 600 ㎎의 비타민 E, 약 10,000 내지 약 40,000 IU의 비타민 A, 약 50 내지 약 200 ㎎의 아연 및 약 1 내지 약 5 ㎎의 구리로 15 내지 20 주동안이었다. 병용 요법의 이점을 실시예 8 및 9에 기재된 바에 따라 분석하였다.Mice and / or rats were tested according to the manner described in Example 13 except that selected vitamins and minerals were used. Compounds of formula (I) or (II) were administered orally or parenterally in combination with vitamins and minerals in an amount effective to inhibit the development and recurrence of macular degeneration. The test administration initially comprises about 20 mg / kg / day of a compound of formula (I) or (II) with about 100 to about 1000 mg of vitamin C, about 100 to about 600 mg of vitamin E, about 10,000 to about 40,000 With vitamin A of IU, about 50 to about 200 mg zinc and about 1 to about 5 mg copper for 15-20 weeks. The benefits of the combination therapy were analyzed as described in Examples 8 and 9.
실시예Example 16: 시험 화합물 농도의 함수로서 혈청 레티놀의 분석 16: Analysis of Serum Retinol as a Function of Test Compound Concentration
ABCA4 널 돌연변이 마우스에 DMSO 중 일반식 (I) 또는 (II)의 화합물의 지시된 용량(복강내)으로 28 일동안 매일 제공하였다(n = 투여 그룹당 4 마리). 연구 기간의 종료 시점에, 혈액을 채취하여 혈청을 준비하였다. 혈청 단백질의 아세토니트릴 침전 이후, LC/MS에 의해 가용성 상으로부터 레티놀의 농도 및 일반식 (I) 또는 (II)의 화합물의 농도를 결정하였다. 용출된 화합물의 동정을 UV-가시광선 흡수 스펙트럼 및 인증 표준과의 동일 피크의 공용출에 의해 확인하였다(도 2 참조).ABCA4 null mutant mice were given daily for 28 days at the indicated dose (intraperitoneal) of the compound of formula (I) or (II) in DMSO (n = 4 per dose group). At the end of the study period, blood was drawn to prepare serum. After acetonitrile precipitation of serum proteins, the concentration of retinol and the compound of formula (I) or (II) were determined from the soluble phase by LC / MS. Identification of the eluted compound was confirmed by co-extraction of the same peak with UV-visible absorption spectrum and certification standard (see FIG. 2).
실시예Example 17: 17: TTRTTR 에 결합하고/결합하거나 To / and to TTRTTR 의 유전자 발현을 억제하는 화합물의 동정Of compounds that inhibit gene expression in humans
글루타티온-S-전이효소 단백질을 포함하고 96-웰 마이크로티터 플레이트의 글루타티온-유도 웰에 흡착된 순수한 TTR 폴리펩티드를 생리학적 pH 7.0의 완충 용액에서 소분자 라이브러리로부터의 시험 화합물과 접촉시켰다. 순수한 TTR 폴리펩티드는 당업계에 개시되어 있다. 본원에 참고로 포함되는 미국 특허출원 제20020160394호를 참조할 수 있다. 시험 화합물은, 일부 구체예에서 형광 태그를 포함하였다. 시료를 5 분 내지 1 시간동안 인큐베이션시켰다. 대조군 시료를 시험 화합물의 부재하에 인큐베이션시켰다.Pure TTR polypeptides containing glutathione-S-transferase proteins and adsorbed to glutathione-induced wells in 96-well microtiter plates were contacted with test compounds from small molecule libraries in a buffer solution at physiological pH 7.0. Pure TTR polypeptides are disclosed in the art. See US Patent Application No. 20020160394, which is incorporated herein by reference. Test compounds included fluorescent tags in some embodiments. Samples were incubated for 5 minutes to 1 hour. Control samples were incubated in the absence of test compounds.
시험 화합물을 함유하는 완충 용액을 웰로부터 세척하였다. TTR 폴리펩티드에 대한 시험 화합물의 결합은 웰 함량의 형광 측정에 의해 검출하였다. 시험 화합물이 인큐베이션되지 않은 웰의 형광에 비해 최소 15%까지 웰의 형광을 증가시키는 시험 화합물은 TTR 폴리펩티드에 결합하는 화합물로서 동정되었다.Buffer solutions containing test compounds were washed from the wells. Binding of test compounds to TTR polypeptide was detected by fluorescence measurement of well content. Test compounds that increase the fluorescence of the wells by at least 15% relative to the fluorescence of the wells where the test compounds were not incubated were identified as compounds that bind to the TTR polypeptide.
동정된 시험 화합물은 일부 구체예에서 TTR 발현 작제물로 형질감염시킨 인간 세포 배양액에 투여하고, 37℃에서 10 내지 45 분동안 인큐베이션시켰다. 형질감염되지 않은 동일한 형태의 세포 배양액을 시험 화합물을 첨가하지 않고 동일한 시간동안 인큐베이션하여 음성 대조군으로서 제공하였다.The identified test compounds were administered to human cell cultures transfected with TTR expression constructs in some embodiments and incubated at 37 ° C. for 10-45 minutes. Cell cultures of the same type that were not transfected were incubated for the same time without the addition of test compounds to serve as negative controls.
이어, 문헌[Chirgwin et al., Biochem. 18, 5294-99, 1979]에 기술된 두 배양액으로부터 RNA를 분리하였다. 20 내지 30 ㎍의 총 RNA를 사용하여 노던 블롯을 준비하고, 32P-표지된 TTR-특이 프로브와 혼성화시켰다. TTR mRNA 전사 검출용 프로브는 이미 개시되어 있다. 시험 화합물의 부재하에 수득된 시그널과 비교하여 TTR-특이 시그널을 감소시키는 시험 화합물은 TTR 유전자 발현의 억제제로서 동정되었다.Then, Chirgwin et al., Biochem. 18, 5294-99, 1979 RNA was isolated from the two cultures described. Northern blots were prepared using 20-30 μg total RNA and hybridized with 32 P-labeled TTR-specific probes. Probes for detecting TTR mRNA transcription have already been disclosed. Test compounds that reduce TTR-specific signals compared to the signals obtained in the absence of test compounds have been identified as inhibitors of TTR gene expression.
실시예Example 18: 18: RBPRBP 에 결합하고/결합하거나 To / and to RBPRBP 의 유전자 발현을 억제하는 화합물의 동정Of compounds that inhibit gene expression in humans
순수한 apoRBP를 pH 7.0의 생리학적 완충 용액에서 소분자 라이브러리로부터의 시험 화합물과 접촉시켰다. 순수한 apoRBP는 당업계에 개시되어 있다. 본원에 참고로 포함되는 미국 특허출원 공개 제20030119715호를 참조할 수 있다. 시험 화합물은 일부 구체예에서 형광 태그를 포함하였다. 시료를 5 분 내지 1 시간동안 인큐베이션시켰다. 대조군 시료를 시험 화합물의 부재하에 인큐베이션시켰다. holoRBP(레티놀과 복합체화된 RBP)의 존재하에 경합 분석을 또한 수행하였다.Pure apoRBP was contacted with test compound from small molecule library in physiological buffer solution at pH 7.0. Pure apoRBPs are disclosed in the art. See US Patent Application Publication No. 20030119715, which is incorporated herein by reference. Test compounds included fluorescent tags in some embodiments. Samples were incubated for 5 minutes to 1 hour. Control samples were incubated in the absence of test compounds. A competitive assay was also performed in the presence of holoRBP (RBP complexed with retinol).
시험 화합물을 함유하는 완충 용액을 웰로부터 세척하였다. apoRBP에 대한 시험 화합물의 결합은 웰 함량의 형광 측정에 의해 검출하였다. 시험 화합물이 인큐베이션되지 않은 웰의 형광에 비해 최소 15%까지 웰의 형광을 증가시키는 시험 화합물은 apoRBP와 결합하는 화합물로서 동정되었다.Buffer solutions containing test compounds were washed from the wells. Binding of test compounds to apoRBP was detected by fluorescence measurement of well content. Test compounds that increase the fluorescence of the wells by at least 15% relative to the fluorescence of the wells where the test compounds were not incubated were identified as compounds that bind apoRBP.
동정된 시험 화합물을 RBP 발현 작제물로 형질감염시킨 인간 세포 배양액에 투여하고, 37℃에서 10 내지 45 분동안 인큐베이션시켰다. 형질감염시키지 않은 동일한 형태의 세포 배양액을 시험 화합물을 첨가하지 않고 동일한 시간동안 인큐베이션하여 음성 대조군으로서 제공하였다.Identified test compounds were administered to human cell cultures transfected with RBP expression constructs and incubated at 37 ° C. for 10-45 minutes. Cell cultures of the same type that were not transfected were incubated for the same time without the addition of test compounds to serve as negative controls.
이어, 문헌[Chirgwin et al., Biochem. 18, 5294-99, 1979]에 기술된 두 배양액으로부터 RNA를 분리하였다. 약 20 내지 약 30 ㎍의 총 RNA를 사용하여 노던 블롯을 준비하고, 32P-표지된 RBP-특이 프로브와 혼성화시켰다. 시험 화합물의 부재하에 수득된 시그널에 비해 RBP-특이 시그널을 감소시키는 시험 화합물은 RBP 유전자 발현의 억제제로서 동정되었다.Then, Chirgwin et al., Biochem. 18, 5294-99, 1979 RNA was isolated from the two cultures described. Northern blots were prepared using about 20 to about 30 μg total RNA and hybridized with 32 P-labeled RBP-specific probes. Test compounds that reduce RBP-specific signals relative to signals obtained in the absence of test compounds have been identified as inhibitors of RBP gene expression.
실시예Example 19: 혈청 레티놀, 19: serum retinol, 아이컵Eye Cup 레티노이드Retinoid 및 A2E 수준에 대한 시험 화합물 효과의 추가 분석 Analysis of test compound effects on A2E and A2E levels
일반식 (I) 또는 ( II )의 화합물 처리. ABCA4-/- 마우스에 28 일동안 매일 일반식 (I) 또는 (II)의 화합물을 투여하였다(25 ㎕ DMSO 중 약 1.5 내지 약 15 ㎍/㎕, 복강내). 연구 개시에 마우스는 1-2 개월령이었고, 색소(129/SV) 또는 알비노(BALB/c) 세포주였다. 마우스를 처리 기간동안 12 시간 사이클의 명/암(30-50 룩스)하에 사육하였고, 케타민(200 ㎎/㎏)과 자일라진(약 10 ㎎/㎏)의 복강내 주사에 의해 마취시킨 후 경추 탈골시켜 희생시켰다. Compound Treatment of Formula (I) or ( II ). ABCA4-/-mice were given a compound of Formula (I) or (II) daily for 28 days (about 1.5 to about 15 μg / μl in 25 μl DMSO, intraperitoneally). At the start of the study mice were 1-2 months old and were either pigment (129 / SV) or albino (BALB / c) cell lines. Mice were bred under a 12 hour cycle of light / dark (30-50 lux) during the treatment period, and were anesthetized by intraperitoneal injection of ketamine (200 mg / kg) and xylazine (about 10 mg / kg), followed by cervical dislocation. To sacrifice.
혈청 레티놀의 분석. 최종 시험 화합물 투여후(즉, 28 일째에) 18 시간 시험 화합물-처리 마우스의 꼬리 정맥으로부터 전혈을 수집하였다. 1,500×g으로 10 분동안 원심분리한 후 전혈로부터 혈청을 수득하였다. 얼음같이 차가운 평형 부피의 아세토니트릴을 첨가하고 원심분리(10,000×g, 10분)하여 혈청 단백질을 침전시켰다. 가용성 상으로부터 모액을 제거하고, 다이오드-어레이 검출기가 구비된 아길런트(Agilent) 1100 시리즈 모세관 액체 크로마토그래피를 이용하여 HPLC에 의해 분석하였다. 크로마토그래피는 상술된 바와 같이 수행하였다. Analysis of Serum Retinol. Whole blood was collected from the tail vein of the test compound-treated mice 18 hours after the last test compound administration (ie, on day 28). Serum was obtained from whole blood after centrifugation at 1,500 × g for 10 minutes. Serum protein was precipitated by addition of ice cold equilibrium volume of acetonitrile and centrifugation (10,000 × g, 10 minutes). The mother liquor was removed from the soluble phase and analyzed by HPLC using Agilent 1100 series capillary liquid chromatography with a diode-array detector. Chromatography was performed as described above.
레티노이드 및 A2E의 추출 및 분석. 일반식 (I) 또는 (II)의 화합물을 매일 투여한 후(28 일간), ABCA4-/- 마우스의 아이컵내 레티노이드 및 A2E의 항정 상태 수준을 측정하였다. 마우스를 희생시키고 안구를 적출한 다음, 각 눈의 후방 부분을 사용하여 레티노이드 또는 A2E를 추출하였다. 안조직으로부터 레티노이드 및 A2E를 추출하는데 사용되는 방법 및 HPLC 분석 기술은 개시되어 있다. 예를 들어, 문헌[Mata NL, Weng J, Travis GH. Biosynthesis of a major lipofuscin fluorophore in mice and humans with ABCR-mediated retinal and macular degeneration. Proc Natl Acad Sci USA. 2000;97:7154-7159; Weng J, et al.; Cell. 1999;98:13-23; Mata NL, et al.; Invest. Ophthalmol. Visual Sci. 2001; 42:1685-1690]을 참조할 수 있다. 모든 시료를 흡광도 및 형광 검출을 사용하여 HPLC에 의해 분석하였다. 이들 분석에서, 컬럼 항온유지장치를 사용하여 용매 및 컬럼의 온도를 40℃로 유지하였다. 지시된 화합물의 동정을 온라인 스펙트럼 분석 및 인증 표준과의 공용출에 의해 확인하였다. Extraction and Analysis of Retinoids and A2E. After daily administration of a compound of Formula (I) or (II) (28 days), steady state levels of retinoids and A2E in the eyecups of ABCA4-/-mice were measured. Mice were sacrificed and eyeballs were extracted, then the retinoid or A2E was extracted using the posterior part of each eye. Methods and HPLC analysis techniques used to extract retinoids and A2E from eye tissue are disclosed. See, eg, Mata NL, Weng J, Travis GH. Biosynthesis of a major lipofuscin fluorophore in mice and humans with ABCR-mediated retinal and macular degeneration. Proc Natl Acad Sci USA. 2000; 97: 7154-7159; Weng J, et al .; Cell. 1999; 98: 13-23; Mata NL, et al .; Invest. Ophthalmol. Visual Sci. 2001; 42: 1685-1690. All samples were analyzed by HPLC using absorbance and fluorescence detection. In these analyses, column incubators were used to maintain the solvent and column temperatures at 40 ° C. Identification of the indicated compounds was confirmed by online spectrum analysis and co-extraction with certification standards.
혈청 레티놀, 안내 레티노이드 및 A2E 사이의 상관관계. 수집한 데이터로부터 혈청 레티놀의 감소와 포유동물의 아이컵내 레티노이드 수준 및 A2E 수준의 감소 사이에는 직접적인 상관관계가 입증되었다. 특히, 혈청 레티놀 감소는 안내 레티노이드 수준 및 안내 A2E 수준 모두 용량-의존 방식으로 진행하였다. 예를 들어, 일반식 (I) 또는 (II)의 화합물은 포유동물의 혈청 레티놀 수준을 저하시켰는데, 이는 혈청 레티놀의 감소가 망막병증 및 황반 변성/이영양과 관련이 있는 물질(예를 들어 A2E)의 수준에 영향을 미친다는 것을 나타낸다. 따라서, 혈청 레티놀 감소를 야기하는 본원에 기술된 것들과 같은 제제는 또한 일부 구체예에서 안내 A2E 및 레티노이드 수준을 감소시키는데 사용되며, 더 나아가 포유동물에서 리포푸신에 기초한 망막 질환, 예를 들어 망막병증 및 황반 변성/이영양을 치료하는데 사용된다. Correlation between Serum Retinol, Intraocular Retinoid and A2E. From the collected data there was a direct correlation between the reduction of serum retinol and the reduction of retinoid levels and A2E levels in the eye cups of mammals. In particular, serum retinol reduction proceeded in a dose-dependent manner for both intraocular retinoid levels and intraocular A2E levels. For example, compounds of formula (I) or (II) have lowered serum retinol levels in mammals, which are substances in which reduction in serum retinol is associated with retinopathy and macular degeneration / ditrophy (eg A2E Affects the level of). Thus, agents such as those described herein that cause serum retinol reduction are also used in some embodiments to reduce intraocular A2E and retinoid levels, and furthermore, retinal diseases, such as retinopathy, based on lipofuscin in mammals. And macular degeneration / ditrophy.
실시예Example 20: A2E의 축적을 저지하기 위한 치료 표적으로서 20: As a therapeutic target to arrest the accumulation of A2E RBPRBP 의 타당성 확인Validation of
리포푸신 형광단을 감소시키는 비약물학적 방법이, 환자의 RBP 수준 감소에 기초한 치료학적 접근법에 대한 타당성 확인을 위해 조사될 것이다. 이러한 연구에서, RBP 단백질 수준은 유전자 조작을 통해 감소될 것이다. 레티놀 결합 단백질(RBP4)에서 이형접합 돌연변이(heterozygous mutant)를 발현하는 2 계통의 마우스를 생성하였다. 첫 번째 계통은 RBP 유전자좌에서만 이형접합 돌연변이를 가지며(RBP+/-); 두 번째 계통은 ABC4와 RBP4 유전자좌 모두에서 이형접합 돌연변이를 가진다(RBP4+/-, ABC4+/-). RBP+/- 마우스는 ABC4 유전자좌에서 야생형일 것이고, 따라서 과량의 A2E 형광단을 축적시키지 않을 것이다. 그러나, ABC4+/- 마우스는 ABC4-/-(널 동형접합) 마우스에서 관찰된 수준의 대략 50%인 수준으로 A2E 형광단을 축적할 것이다. 문제가 되는 것은 RBP4+/-, ABC4+/- 마우스에서 감소된 RBP 발현이 독성 망막 형광단(예, A2E)의 축적에 영향을 미칠 것인지의 여부이다. 도 6(패널 A)은 RBP4+/+, ABCA4-/- 마우스에 비해 RBP4+/-, ABCA4+/- 마우스에서 혈청 레티놀이 극적으로 감소(>50%)되었음을 나타낸다. RBP4+/-, ABCA4+/- 마우스에서 레티놀 감소의 정도를 28-일 기간동안 HPR을 투여한 RBP4+/+, ABCA4-/- 마우스에서 관찰된 것과 비교하였다. 이들 마우스의 혈청에서 RBP4 수준의 면역탁본법 분석은 레티놀 데이터와 일치하였다(도 6, 패널 B).Non-pharmacologic methods of reducing the lipofuscin fluorophore will be investigated to validate the therapeutic approach based on reducing RBP levels in patients. In this study, RBP protein levels will be reduced through genetic engineering. Two strains of mice expressing a heterozygous mutant in the retinol binding protein (RBP4) were generated. The first line has heterozygous mutations only at the RBP locus (RBP +/-); The second line carries heterozygous mutations at both the ABC4 and RBP4 loci (RBP4 +/-, ABC4 +/-). RBP +/− mice will be wild type at the ABC4 locus and therefore will not accumulate excess A2E fluorophores. However, ABC4 +/− mice will accumulate A2E fluorophores at levels that are approximately 50% of the levels observed in ABC4-/-(null homozygous) mice. The question is whether reduced RBP expression in RBP4 +/-, ABC4 +/- mice will affect the accumulation of toxic retinal fluorophores (eg A2E). FIG. 6 (Panel A) shows that serum retinol was dramatically reduced (> 50%) in RBP4 +/−, ABCA4 +/− mice compared to RBP4 + / +, ABCA4-/ − mice. The extent of retinol reduction in RBP4 +/-, ABCA4 +/- mice was compared to that observed in RBP4 + / +, ABCA4-/-mice receiving HPR over a 28-day period. Immunoassay analysis of RBP4 levels in the serum of these mice was consistent with retinol data (FIG. 6, Panel B).
RBP4(RBP4+/-, ABCA4+/-)의 발현이 유전적으로 감소된 상기 마우스에서의 A2E 및 전구체 형광단(A2PE 및 A2PE-H2) 수준을 3 개월의 기간에 걸쳐 매달 감시하였으며, 이를 RBP4+/-, ABCA4+/- 마우스에서의 형광단 수준과 비교하였다. 전체적으로, RBP+/-, ABCA4+/- 마우스의 총 형광단 수준은, ABCA4+/- 마우스에서 나타나는 총 형광단 수준에 비하여 약 70% 감소하였다는 것을 입증하였다(각각 패널 D및 C). 실제로, RBP4+/-, ABCA4+/- 마우스에서 측정된 형광단 수준은 야생형 마우스에서 관찰된 수준에 접근하였다(패널 D 및 E 비교). 이들 데이터를 통해, RBP가 눈에서 형광단 수준을 감소시키는 치료학적 표적임이 입증된다. 더 나아가, 상기 데이터를 통해, 환자에서 RBP 전사 또는 번역을 억제하는 제제 또는 방법이 또한 (a) 그 환자에서 혈청 레티놀 수준을 감소시키고, (b) 본원에 기술된 레티놀 관련 질환에 치료학적 이점을 제공할 것임이 입증되었다. 또한, 환자에서 RBP 제거율을 증대시키는 제제 또는 방법이 또한 이러한 효과와 이점을 생성할 것이다.A2E and precursor fluorophores (A2PE and A2PE-H 2 ) levels in these mice with genetically reduced expression of RBP4 (RBP4 +/-, ABCA4 +/-) were monitored monthly over a period of 3 months, which was RBP4 +/- , Compared with fluorophore levels in ABCA4 +/− mice. Overall, it was demonstrated that the total fluorophore levels of RBP +/-, ABCA4 +/- mice were reduced by about 70% relative to the total fluorophore levels seen in ABCA4 +/- mice (Panels D and C, respectively). Indeed, fluorophore levels measured in RBP4 +/−, ABCA4 +/− mice approached the levels observed in wild type mice (compare Panels D and E). These data demonstrate that RBP is a therapeutic target for reducing fluorophore levels in the eye. Furthermore, through the data, an agent or method for inhibiting RBP transcription or translation in a patient can also (a) reduce serum retinol levels in that patient, and (b) provide therapeutic benefit to the retinol related diseases described herein. Proven to provide. In addition, agents or methods that increase RBP clearance in patients will also produce these effects and benefits.
실시예Example 21: 안내 21: Guide 레티노이드의Retinoid 정량 dose
ABCA4-/- 마우스에게 20 일동안 매일 ATRP(대조군) 또는 ATRP+시험 화합물을 투여하였다(n = 그룹당 3 마리 마우스). 마지막 투여일에, 100 ㎕ 옥수수유 중 미량의 [3H]ATROL(0.32 pmol, 8 μCi)을 모든 동물에게 투여하였다. 5 시간후에 안구를 적출하였다. 본원에 개시된 바와 같이, 각 동물의 한쪽 눈은 레티노이드 분석을 위해 사용하였고, 다른 쪽 눈은 A2E 및 관련 형광단의 분석을 위해 사용하였다. 데이터를 통해 시험 화합물로 처리한 동물에서 [3H]ATROL 흡수의 현저한 감소를 알 수 있었다[도 9]. 각각의 레티노이드 종의 분석을 통해 시각 발색단 생합성에 대한 전구체 기질(ATRE) 및 A2E 생합성에 대한 즉각적인 전구체(AT-Ox)가 유의적으로 감소되었음을 알 수 있다.ABCA4-/-mice received ATRP (control) or ATRP + test compounds daily for 20 days (n = 3 mice per group). On the last day of administration, traces of [ 3 H] ATROL (0.32 pmol, 8 μCi) in 100 μl corn oil were administered to all animals. After 5 hours, the eye was taken out. As disclosed herein, one eye of each animal was used for retinoid analysis and the other eye was used for analysis of A2E and related fluorophores. The data showed a significant reduction in [ 3 H] ATROL uptake in animals treated with the test compound [FIG. 9]. Analysis of each retinoid species reveals a significant reduction in precursor substrate (ATRE) for visual chromophore biosynthesis and immediate precursor (AT-Ox) for A2E biosynthesis.
실시예Example 22: 총 22: gun 형광단Fluorophores 수준 감소에 있어서의 시험 화합물의 효과 Effect of Test Compounds on Reduced Levels
ABCA4-/- 마우스에서 총 형광단 수준 감소에 대한 시험 화합물의 효과. 상기 실시예 13에 기술된 바와 같이 마우스를 처리하였다. 연구의 종료 시점에, 각 동물로부터 수득한 한쪽 안구는 총 형광단 수준을 측정하기 위해 사용하였다. 요약하면, 하나의 전체 안구를 1 ㎖ 인산염 완충 염수(50 mM Na2HPO4, 150 mM NaCl, pH 7.8)에 균질화시켰다. 균질화 이후, 1 ㎖ 메탄올을 첨가하고 시료를 철저히 혼합하였다. 혼합물을 실온에서 5 분동안 인큐베이션하고 2 ㎖ 헥산으로 두 번 추출하였다. 형광 측정을 위해 추출액을 약 400 ㎕로 농축하였다. 수집된 형광 스펙트럼은 비율 모드로 조작한 Spex Fluorolog-3 분광형광계(뉴저지 에디슨 소재, 조빈 아이본 호리바(Jobin Yvon Horiba))를 사용하여 수득하였다. 시료를 488 nm로 여기시키고 500-700 m에서의 방출을 감시하였다. 데이터를 통해, 시험 화합물로 처리한 마우스에서 총 형광단 수준이 크게 감소하였음을 알 수 있다[도 10].Effect of test compound on decreasing total fluorophore levels in ABCA4-/-mice. Mice were treated as described in Example 13 above. At the end of the study, one eye from each animal was used to measure total fluorophore levels. In summary, one whole eye was homogenized in 1 ml phosphate buffered saline (50 mM Na 2 HPO 4 , 150 mM NaCl, pH 7.8). After homogenization, 1 ml methanol was added and the samples mixed thoroughly. The mixture was incubated at room temperature for 5 minutes and extracted twice with 2 mL hexanes. The extract was concentrated to about 400 μl for fluorescence measurements. The collected fluorescence spectra were obtained using a Spex Fluorolog-3 spectrofluorometer (Jobin Yvon Horiba, Edison, NJ) operated in ratio mode. Samples were excited at 488 nm and monitored at 500-700 m. The data show that the total fluorophore levels were significantly reduced in mice treated with the test compound [FIG. 10].
실시에 23: A2E 및 A2E 전구체 감소에 대한 시험 화합물의 효과Example 23: Effect of Test Compounds on A2E and A2E Precursor Reduction
상기 실시예 13에 기술된 바와 같이 마우스를 처리하였다. 연구의 종료 시점에, 각 동물로부터 수득한 한쪽 안구는 A2E 및 A2PE-H2를 측정하는데 사용되었다. 요약하면, 하나의 전체 안구를 1 ㎖ 인산염 완충 염수(50 mM Na2HPO4, 150 mM NaCl, pH 7.8)에 균질화시켰다. 균질화 이후, 1 ㎖ 메탄올을 첨가하고 시료를 철저히 혼합하였다. 혼합물을 실온에서 5 분동안 인큐베이션하고 2 ㎖ 헥산으로 두 번 추출하였다. 용매를 질소 기류하에 증발시키고, 시료 잔류물을 HPLC로 분석하기 위해 200 ㎕ 이소프로판올(IPA)에 재구성시켰다. 형광단을 1 ㎖/분의 유속으로 인지질 이동상(헥산:IPA:에탄올:25 mM 인산염 완충액:아세트산 485:376:100:37.5:0.275 v:v)을 사용하여 평형화시킨 Zorbax RX-Sil 5-㎛ 컬럼(250 x 4.6-㎜) 상에서 분리하였다. 데이터를 통해 비히클-처리 마우스에 비해 시험 화합물로 처리한 마우스에서 A2E 및 그의 전구체 둘 다를 극적으로 감소되었음을 알 수 있다[도 11].Mice were treated as described in Example 13 above. At the end of the study, one eye from each animal was used to measure A2E and A2PE-H2. In summary, one whole eye was homogenized in 1 ml phosphate buffered saline (50 mM Na 2 HPO 4 , 150 mM NaCl, pH 7.8). After homogenization, 1 ml methanol was added and the samples mixed thoroughly. The mixture was incubated at room temperature for 5 minutes and extracted twice with 2 mL hexanes. The solvent was evaporated under a stream of nitrogen and the sample residue was reconstituted in 200 μl isopropanol (IPA) for analysis by HPLC. Zorbax RX-Sil 5-μm equilibrated with phospholipid mobile phase (hexane: IPA: ethanol: 25 mM phosphate buffer: acetic acid 485: 376: 100: 37.5: 0.275 v: v) at a flow rate of 1 ml / min. Separate on column (250 x 4.6-mm). The data show that both A2E and its precursors were dramatically reduced in mice treated with the test compound compared to vehicle-treated mice (FIG. 11).
인간 대상 연구Human subject research
황반 또는 망막 변성의 검출. 눈에서 비정상적인 혈관의 동정은 예를 들어 혈관조영상으로 수행하였다. 이러한 동정은 환자가 후보 물질을 사용할 후보인지, 추가적인 시력 손상을 예방하거나 차단하기 위해 환자에게 다른 치료 방법을 사용할 것인지를 결정하는데 도움이 된다. 혈관조영상은 치료의 추적 조사 및 임의의 새로운 혈관 성장을 추가로 평가하는데 사용될 수 있다. Detection of macular or retinal degeneration. The identification of abnormal blood vessels in the eye was performed, for example, by angiography. This identification helps to determine whether the patient is a candidate to use the candidate substance and whether to use other treatment methods for the patient to prevent or block further visual impairment. Angiography can be used to follow up treatment and further assess any new blood vessel growth.
형광 혈관조영상(형광 혈관조영술, 형광 혈관내시경)은 눈 쪽의 맥락막 및 망막 순환을 가시화하는 기술이다. 형광 염료를 정맥내 주입한 후, 멀티프레임 사진촬영(혈관조영술), 검안경 평가(혈관내시경)를 하거나, 하이델베르그(Heidelberg) 망막 혈관조영술(공초점 주사 레이저 시스템)을 수행하였다. 추가적으로, 망막을 OCT 비침습성 방식으로 검사하여 망막의 단면 이미지를 고해상도로 얻을 수 있다. 형광 혈관조영상은 망막으로 공급되는 혈관에 대한 누출 또는 가능한 손상을 분석함으로써 광범위한 망막 및 맥락막 질환을 평가하는데 사용된다. 또한, 문헌[Berkow et al., Am. J. Ophthalmol. 97:143-7(1984)]에서는 시각 신경 및 홍채의 이상 여부를 판단하는데 사용하였다.Fluorescence angiography (fluorescence angiography, fluorescence angiography) is a technique for visualizing the choroid and retinal circulation on the eye side. After intravenous infusion of fluorescent dyes, multiframe photography (angiography), ophthalmoscope evaluation (vascular endoscopy), or Heidelberg retinal angiography (confocal injection laser system) were performed. Additionally, the retina can be examined in an OCT non-invasive manner to obtain cross-sectional images of the retina in high resolution. Fluorescent angiography is used to assess a wide range of retinal and choroidal diseases by analyzing leakage or possible damage to blood vessels feeding the retina. See also Berkow et al., Am. J. Ophthalmol. 97: 143-7 (1984)] was used to determine the abnormalities of the visual nerve and iris.
유사하게, 인도시아닌 그린을 이용한 혈관조영상이 안구의 뒷부분의 혈류 순환을 가시화하는데 사용된다. 형광은 망막 순환의 연구에 더욱 효과적이며, 인도시아닌은 더 깊이 있는 맥락막 혈관층을 관찰하는데 보다 효과적이다. 인도시아닌 혈관조영술의 사용은 형광염료만으로 혈관신생이 관찰되지 않는 경우에 도움이 된다.Similarly, angiography with indocyanine green is used to visualize the blood flow circulation in the posterior part of the eye. Fluorescence is more effective in the study of retinal circulation, and indocyanine is more effective in viewing deeper choroidal vascular layers. The use of indocyanine angiography is helpful when angiogenesis is not observed with fluorescein dye alone.
일반식 (I)의 구조를 가진 화합물에 대한 적절한 인간 용량은 표준 용량 단계적 확대 연구를 이용하여 결정될 것이다.Appropriate human doses for compounds having the structure of formula (I) will be determined using standard dose escalation studies.
실시예Example 24: 황반 변성을 치료하는 시험 화합물의 효능을 시험하기 위한 임상 시험 24: Clinical trial to test the efficacy of test compounds for treating macular degeneration
예비 시험으로서, 모든 인간 환자에 대해 형광 혈관조영술, 시력 측정, 전기생리학적 파라미터 및 생화학적 및 유동학적 파라미터를 비롯한 통상의 안과적 시험을 수행하였다. 시험 대상 환자 기준(inclusion criteria)은 다음과 같다: 적어도 한쪽 눈의 시력이 20/160 및 20/32 사이, 및 드루젠, 윤문상 위축(areolar atrophy), 색소 응집, 색소 상피 박리 또는 망막하 혈관신생과 같은 AMD 증상. 임신중이거나 수유를 하고 있는 환자는 연구에서 제외하였다. 다른 배제 기준으로는 이전의 유리체절제술 또는 다른 AMD 외과적 시술, 중증의 반흔형성 또는 중증의 동시 안질환(비조절성 녹내장)이 포함된다.As a preliminary test, all ophthalmic examinations, including fluorescence angiography, visual acuity, electrophysiological parameters, and biochemical and rheological parameters, were performed on all human patients. Inclusion criteria include: At least one eye has a visual acuity between 20/160 and 20/32, and drusen, areolar atrophy, pigment aggregation, pigment epithelial detachment or subretinal angiogenesis. AMD symptoms such as. Pregnant or lactating patients were excluded from the study. Other exclusion criteria include previous vitrectomy or other AMD surgical procedures, severe scarring or severe concurrent ocular disease (uncontrolled glaucoma).
황반 변성으로 진단되었거나 눈에서 A2E, 리포푸신 또는 드루젠이 형성 진행중인 환자의 그룹을 대조군 및 실험군으로 분류하였다. 일반식 (I) 또는 (II)의 화합물을 매일 실험군에 투여하였다. 시험 화합물을 실험군에 투여한 것과 동일한 요법으로 위약을 대조군에게 투여하였다.Groups of patients diagnosed with macular degeneration or undergoing A2E, lipofucin or drusen formation in the eye were divided into control and experimental groups. Compounds of formula (I) or (II) were administered to the experimental group daily. Placebo was administered to the control group in the same regime as the test compound was administered to the experimental group.
환자에 대한 일반식 (I) 또는 (II)의 화합물 또는 위약의 투여는 황반 변성의 진행 또는 재발을 억제하는데 유효한 양으로 경구적이거나 비경구적으로 투여될 수 있다. 유효 용량 범위는 1 일 3 회 이하로 약 1 내지 약 4000 ㎎/ ㎡이다.Administration of a compound of formula (I) or (II) or placebo to a patient may be administered orally or parenterally in an amount effective to inhibit the progression or recurrence of macular degeneration. The effective dose ranges from about 1 to about 4000 mg /
대조군 및 실험군 모두에서 황반 변성의 진행을 측정하는 방법 중 하나는 라인 평가(line assessment) 및 강제 선택 방법(forced choice method)(Ferris et al. Am J Ophthalmol, 94:97-98 (1982))을 이용하여 초기 치료 당뇨 망막병증 연구(Early Treatment Diabetic Retinopathy Study; ETDRS) 챠트(뉴욕 롱아일랜드 라이트하우스)에 의해 측정된 최고 교정 시력이다. 시력은 logMAR로 기록된다. ETDRS 챠트상에서 라인 하나의 변화는 0.1 logMAR에 해당한다. 대조군 및 실험군에서 황반 변성의 진행을 측정하는 통상의 추가적 방법은, 험프리 시야 검사, 미세시야계(예를 들어 NIDEK로부터의 Micro Perimeter MP-1 사용) 및 환자 눈에 특정 화합물의 자가형광을 측정/감시하는 단계를 포함하나 이에 한정되지 않는 시야계 검사의 사용을 포함한다.One method of measuring progression of macular degeneration in both the control and experimental groups is the line assessment and forced choice method (Ferris et al. Am J Ophthalmol, 94: 97-98 (1982)). The highest corrected visual acuity as measured by the Early Treatment Diabetic Retinopathy Study (ETDRS) chart (Long Island Lighthouse, NY). Visual acuity is recorded in logMAR. One line change on the ETDRS chart corresponds to 0.1 logMAR. Common additional methods for measuring the progression of macular degeneration in control and experimental groups include Humphrey visual field examination, microfield of view (eg using Micro Perimeter MP-1 from NIDEK) and measuring the autofluorescence of certain compounds in the patient's eyes. The use of visual field inspection, including but not limited to monitoring.
대조군 및 실험군 모두에서 황반 변성의 진행을 측정하는 추가적 방법은 안저 사진촬영, 하이델베르그 망막 혈관조영술{또는 문헌[M. Hammer, et al., Ophthalmologe 2004 Apr. 7(Epub ahead of patent)] 에 기재된 기술}을 이용한 시간에 따른 자가형광 변화의 관찰, 및 기저선, 3 개월, 6 개월, 9 개월 및 12 개월째 방문하여 추적조사한 형광 혈관조영상 촬영을 포함한다. 형태학적 변화의 조사는 (a) 드루젠의 크기, 특징 및 분포; (b) 맥락막 혈관신생의 발달 및 진행; (c) 다른 구간 안저 변화 또는 이상; (d) 판독 속도 및/또는 판독 정확성; (e) 암점 크기; 또는 (f) 지도형 위축 병변의 크기 및 수에 있어서의 변화를 포함한다. 또한, 암슬러 그리드 테스트(Amsler Grid Test) 및 색각 시험(color testing)이 임의로 실시된다.Additional methods for measuring the progression of macular degeneration in both control and experimental groups include fundus photography, Heidelberg retinal angiography (or M. Hammer, et al., Ophthalmologe 2004 Apr. Observation of autofluorescence changes over time using the technique described in [Epub ahead of patent]], and fluorescence angiography taken at baseline, 3 months, 6 months, 9 months and 12 months. Investigations of morphological changes include (a) the size, characteristics and distribution of drusen; (b) development and progression of choroidal neovascularization; (c) other interval fundus changes or abnormalities; (d) read speed and / or read accuracy; (e) dark spot size; Or (f) changes in the size and number of the mapped atrophic lesions. In addition, Amsler Grid Test and color testing are optionally performed.
약물 투여 중 시력 개선을 통계적으로 평가하기 위해서, 검사자는 ETDRS (LogMAR) 챠트 및 표준화된 굴절 및 시력 프로토콜을 사용한다. 입수한 처리후 방문 간격에 의해 기저선으로부터 평균 ETDRS(LogMAR) 최고 교정 시력(BCVA)을 평가하는 것은 통계적으로 시력 개선을 결정하는데 도움이 될 수 있다.To statistically evaluate visual improvement during drug administration, the examiner uses an ETDRS (LogMAR) chart and standardized refractive and visual acuity protocols. Evaluating the mean ETDRS (LogMAR) best corrected visual acuity (BCVA) from baseline by the post-treatment visit interval obtained can help statistically determine vision improvement.
대조군과 실험군 사이의 ANOVA(그룹 간의 차이 분석)를 평가하기 위해, 두 그룹의 ANOVA를 이용하여, SAS/STAT 소프트웨어(노스캐롤라이나주 캐리 소재 사스 인스티튜츠 인코포레이션(SAS Institutes Inc.))를 사용하는 비구조화된 공분산에 의한 반복 측정 분석 결과와 입수가능한 처리후 간격 방문을 통한 기저선으로부터 ETDRS(LogMAR) 시력의 평균 변화를 비교하였다.To assess ANOVA (group difference analysis) between control and experimental groups, using two groups of ANOVA, SAS / STAT software (SAS Institutes Inc., Cary, NC) The results of repeated measures analysis by unstructured covariance were compared with the average change in ETDRS (LogMAR) visual acuity from baseline through available post treatment interval visits.
혈청 레티놀 수준은 다음과 같이 평가하였다: 혈청 단백질의 아세토니트릴 침전 이후, LC/MS에 의해 가용성 상으로부터 레티놀의 농도를 측정하였다. 다르게는, 혈청 레티놀 수준을 문헌[Driskell et al., J Chromatogr, 1982, 231, 439-444 or Futterman et al., Invest. Ophthalmol Vis Sci, 1975, 14, 125]에 기술된 바와 같이 평가하였다.Serum retinol levels were evaluated as follows: After acetonitrile precipitation of serum proteins, the concentration of retinol was determined from the soluble phase by LC / MS. Alternatively, serum retinol levels are reported in Drrikell et al., J Chromatogr, 1982, 231, 439-444 or Futterman et al., Invest. Ophthalmol Vis Sci, 1975, 14, 125, were evaluated as described.
연구 개시후의 독성 평가는 다음해에는 3 개월마다, 그 다음해에는 4 개월 마다, 그 다음해는 6 개월마다 평가하였다. 시험 화합물 및 그의 대사산물, 혈청 레티놀 및/또는 RBP의 혈장 수준이 또한 이러한 방문 중에 평가되었다. 독성 평가는 일반식 (I) 또는 (II)의 화합물을 사용한 환자 및 대조군 환자를 포함한다.Toxicity assessments after the start of the study were evaluated every three months in the following year, every four months in the following year, and every six months in the following year. Plasma levels of test compounds and their metabolites, serum retinol and / or RBP were also assessed during this visit. Toxicity assessments include patients using the compounds of formula (I) or (II) and control patients.
실시예Example 25: 25: RBPRBP -- TTRTTR 및 And CYPCYP 450450 에 대한 For 비레티노이드Non-retinoid 조절자의 활성 Adjuster's Activity
IC50 surface
IC 50
억제율CYP
Suppression rate
표 1은 일반식 (I) 및 (II)의 구조를 가진 대표 화합물의 IC5O 값 및 시토크롬 P450 억제율을 보여준다.Table 1 shows the IC 50 values and cytochrome P 450 inhibition of representative compounds having the structures of formulas (I) and (II).
실시예Example 26: A2E 생산을 감소시키는 일반식 (I) 또는 ( 26: general formula (I) or (2) to reduce A2E production IIII )의 화합물의 효능에 대한 시험Test for the efficacy of the compound of
또한, 실시예 24에 기술된 예비-시험, 투여, 용량 및 독성 평가 프로토콜을 비롯한 동일한 프로토콜 디자인을 사용하여 환자 눈에서 A2E 생산을 감소시키거나 제한하는데 있어서 일반식 (I) 또는 (II)의 화합물을 효능을 시험하였다.In addition, compounds of formula (I) or (II) in reducing or limiting A2E production in the patient eye using the same protocol design, including the pre-test, administration, dose and toxicity assessment protocols described in Example 24. Was tested for efficacy.
A2E의 형성을 측정하거나 감시하는 방법은 실시예 23에 개시된 바와 같이 환자 눈에서 특정 화합물의 자가형광의 측정/감시, 시력 및 시야 시험의 사용(예를 들어 미세시야계 포함), 판독 속도 및/또는 판독 정확성 검사, 암점 및/또는 지도형 위축 병변의 크기 및 수에 대한 측정을 포함한다. 실시예 23에 기술된 통계학적인 분석을 사용하였다.Methods for measuring or monitoring the formation of A2E include the measurement / monitoring of autofluorescence of certain compounds in the patient's eye, the use of visual acuity and visual field tests (e.g. including microscopic fields), reading speed and / or as described in Example 23. Or read accuracy tests, measurements of the size and number of dark spots and / or superficial atrophic lesions. The statistical analysis described in Example 23 was used.
실시예Example 27: 27: 리포푸신Lipofucin 생산을 감소시키는 일반식 (I) 또는 ( General formula (I) or ( IIII )의 화합물의 효능에 대한 시험Test for the efficacy of the compound of
또한, 실시예 24에 기술된 예비-시험, 투여, 용량 및 독성 평가 프로토콜을 비롯한 동일한 프로토콜 디자인을 사용하여 환자 눈에서 리포푸신 생산을 감소시키거나 제한하는데 있어서 일반식 (I) 또는 (II)의 화합물을 효능을 시험하였다. 실시예 24에 기술된 통계학적인 분석을 사용하였다.In addition, using the same protocol design, including the pre-test, dosing, dose and toxicity assessment protocols described in Example 24, the formula (I) or (II) of formula (I) or (II) in reducing or limiting Compounds were tested for efficacy. The statistical analysis described in Example 24 was used.
특정 치료 효능에 대한 대리 마커로 사용되는 시험은 실시예 24에 개시된 바와 같이 환자 눈에서의 시력 및 시야 검사(예를 들어 미세시야계 포함), 판독 속도 및/또는 판독 정확성 검사, 암점 및/또는 지도형 위축 병변의 크기 및 수 측정, 및 특정 화합물의 자가형광 측정/감시의 사용을 포함한다.Tests used as surrogate markers for specific therapeutic efficacy include visual and visual field tests (eg, microscopic field), reading speed and / or reading accuracy tests, dark spots and / or in the patient's eye as disclosed in Example 24. Measurement of the size and number of geographic atrophy lesions, and the use of autofluorescence measurements / monitoring of certain compounds.
실시예Example 28: 28: 드루젠Drusen 생산을 감소시키는 일반식 (I) 또는 ( General formula (I) or ( IIII )의 화합물의 효능에 대한 시험Test for the efficacy of the compound of
또한, 실시예 24에 기술된 예비-시험, 투여, 용량 및 독성 평가 프로토콜을 비롯한 동일한 프로토콜 디자인을 사용하여 환자 눈에서 드루젠 생산 및 형성을 감소시키거나 제한하는데 있어서 일반식 (I) 또는 (II)의 화합물을 효능을 시험하였다. 실시예 24에 기술된 통계학적인 분석을 사용하였다.In addition, general formula (I) or (II) in reducing or limiting drusen production and formation in the patient eye using the same protocol design, including the pre-test, administration, dose and toxicity assessment protocols described in Example 24. ) Compounds were tested for efficacy. The statistical analysis described in Example 24 was used.
대조군 및 실험군 모두에서 드루젠 형성의 진행을 측정하는 방법은 안저 사진촬영 및 기저선, 3 개월, 6 개월, 9 개월 및 12 개월째 방문하여 추적조사한 형광 혈관조영상 촬영을 포함한다. 형태학적 변화의 조사는 (a) 드루젠 크기, 특성 및 분포; (b) 맥락막 혈관신생의 발달 및 진행; (c) 다른 구간 안저 변화 또는 이상에 있어서의 변화를 포함할 수 있다. 특정 치료 효능에 대한 대리 마커로 사용될 수 있는 다른 시험은 실시예 23에 기술된 바와 같이 환자 눈에서의 시력 및 시야 검사(예로서 미세시야계 포함); 판독 속도 및/또는 판독 정확성 검사; 암점 및/또는 지도형 위축 병변의 크기 및 수 측정; 및 특정 화합물의 자가형광 측정/감시의 사용을 포함한다.Methods for measuring the progression of drusen formation in both the control and experimental groups include fundus photography and baseline, followed by fluorescein angiography visited at 3, 6, 9, and 12 months. Investigation of morphological changes includes (a) drusen size, properties and distribution; (b) development and progression of choroidal neovascularization; (c) may include changes in fundus changes or abnormalities in other sections. Other tests that can be used as surrogate markers for specific therapeutic efficacy include visual and visual field examinations (including microscopic field) in the patient's eye as described in Example 23; Read speed and / or read accuracy checks; Measuring size and number of dark spots and / or geographic atrophy lesions; And the use of autofluorescence measurement / monitoring of certain compounds.
실시예Example 29: 황반 29: macula 이영양에In this nutrition 대한 유전적 시험 Genetic testing
인간 ABCA4 유전자의 결손은 스타르가르트 질환, 추상체-간상체 이영양, 연령 관련 황반 변성(건성 형태 및 습성 형태 모두) 및 색소성 망막염을 포함하는 5 개의 독특한 망막 표현형과 관련이 있는 것으로 생각된다. 예를 들어, 문헌[Allikmets et al., Science, 277:1805-07 (1997); Lewis et al., Am. J. Hum. Genet, 64:422-34(1999); Stone et al., Nature Genetics, 20:328-29 (1998); Allikmets, Am. J. Hum. Gen., 67:793-799(2000); Klevering, et al., Ophthalmology, 111:546-553(2004)]을 참조할 수 있다. 또한, 스타르가르트 질환의 상염색체 우성형태는 ELOV4 유전자의 돌연변이에 의해 유발된다. 문헌[Karan, et al., Proc. Natl. Acad. Sci.(2005)]을 참조할 수 있다. 환자는 다음과 같은 임의분석에 의해 스타르가르트 질환을 지니는 것으로 진단될 수 있다:Deletion of the human ABCA4 gene is thought to be associated with five unique retinal phenotypes, including Stargardt's disease, abstractor-antibody dystrophies, age-related macular degeneration (both dry and wet form) and pigmented retinitis. . See, eg, Allikmets et al., Science, 277: 1805-07 (1997); Lewis et al., Am. J. Hum. Genet, 64: 422-34 (1999); Stone et al., Nature Genetics, 20: 328-29 (1998); Allikmets, Am. J. Hum. Gen., 67: 793-799 (2000); Klevering, et al., Ophthalmology, 111: 546-553 (2004). In addition, an autosomal dominant form of Stargardt disease is caused by mutations in the ELOV4 gene. Karan, et al., Proc. Natl. Acad. Sci. (2005). Patients can be diagnosed with Stargardt's disease by any of the following analyzes:
-서열 돌연변이(들)에 대하여, ABCA4 또는 ELOV4의 모든 엑손 및 인접한 인트론 영역을 서열화하는 단계를 포함할 수 있는 직접 서열화 돌연변이 검출 방법(direct-sequencing mutation detection strategy);For sequence mutation (s), a direct-sequencing mutation detection strategy that may comprise sequencing all exons and adjacent intron regions of ABCA4 or ELOV4;
-게놈 서던 분석;-Genomic southern analysis;
-공지된 모든 ABCA4 또는 ELOV4 변이체를 포함하는 마이크로어레이 분석; 및Microarray analysis including all known ABCA4 or ELOV4 variants; And
- 항체 및 웨스턴 분석을 이용한 면역세포화학적 분석과 결합된 액체 크로마토그래피 탠덤 질량분광계에 의한 분석.Analysis by liquid chromatography tandem mass spectrometry combined with immunocytochemical analysis using antibodies and Western assay.
환자 및 그의 가족력과 함께 안저촬영, 형광 혈관조영상 및 주사 레이저 검안경 영상에 의해 진단을 예측 및/또는 확신할 수 있다.Diagnosis can be predicted and / or ascertained by fundus imaging, fluorescein angiography, and scanning laser ophthalmoscope images along with the patient and his family history.
실시예Example 30: 제형 30: Formulation
실시예Example 30a: 경구용 조성물 30a: oral composition
경구 전달용 약제학적 조성물을 제조하기 위해, 일반식 (I) 또는 일반식 (II) 중 임의의 화합물 100 ㎎을 750 ㎎의 전분과 혼합하였다. 혼합물을 경질 젤라틴 캡슐과 같이 경구 투여에 적합한 경구 투여형으로 혼입하였다.To prepare a pharmaceutical composition for oral delivery, 100 mg of any compound of Formula (I) or Formula (II) was mixed with 750 mg of starch. The mixture was incorporated into an oral dosage form suitable for oral administration such as hard gelatin capsules.
실시예Example 30b: 30b: 비경구용Parenteral 조성물 Composition
주사에 의한 투여에 적합한 비경구용 약제학적 조성물을 제조하기 위해, 일반식 (I) 또는 일반식 (II) 중 임의의 화합물의 수용성 염 100 ㎎을 DMSO에 용해시킨 다음 10 ㎖의 0.9% 멸균 염수와 혼합하였다. 혼합물을 주사에 의한 투여에 적합한 투여 단위 형태로 혼입하였다.To prepare a parenteral pharmaceutical composition suitable for administration by injection, 100 mg of a water-soluble salt of any compound of formula (I) or formula (II) are dissolved in DMSO and then 10 ml of 0.9% sterile saline and Mixed. The mixture was incorporated into a dosage unit form suitable for administration by injection.
실시예Example 30c: 30c: 설하용Sublingual (경질 (reshuffle 로젠지Lozenge ) 조성물Composition
경질 로젠지와 같은 구강 전달용 약제학적 조성물을 제조하기 위해, 일반식 (I) 또는 일반식 (II) 중 임의의 화합물 믹스 100 ㎎을 420 ㎎의 분말성 당, 1.6 ㎖의 백색 옥수수 시럽, 2.4 ㎖의 증류수 및 0.42 ㎖의 박하 추출물을 혼합하였다. 혼합물을 부드럽게 혼련하고 틀에 부어 구강 투여에 적합한 로젠지를 형성하였다.To prepare pharmaceutical compositions for oral delivery, such as hard lozenges, 100 mg of any compound mix of Formula (I) or Formula (II) is added to 420 mg of powdered sugar, 1.6 ml of white corn syrup, 2.4 Ml of distilled water and 0.42 ml of peppermint extract were mixed. The mixture was kneaded gently and poured into a mold to form a lozenge suitable for oral administration.
실시예Example 30d: 흡입용 조성물 30d: composition for inhalation
흡입 전달용 약제학적 조성물을 제조하기 위해, 일반식 (I) 또는 일반식 (II) 중 임의의 화합물 20 ㎎을 50 ㎎의 무수 시트르산 및 100 ㎖의 0.9% 염화나트륨 용액과 혼합하였다. 혼합물을 흡입 투여에 적합한 네뷸라이저와 같은 흡입 전달 단위로 혼입하였다.To prepare a pharmaceutical composition for inhalation delivery, 20 mg of any compound of Formula (I) or Formula (II) was mixed with 50 mg of citric anhydride and 100 ml of 0.9% sodium chloride solution. The mixture was incorporated into an inhalation delivery unit such as a nebulizer suitable for inhalation administration.
실시예Example 30e: 직장용 겔 조성물 30e: rectal gel composition
직장 전달용 약제학적 조성물을 제조하기 위해, 일반식 (I) 또는 일반식 (II) 중 임의의 화합물 100 ㎎을 2.5 g의 메틸셀루오스(1500 mPa), 100 ㎎의 메틸파라벤, 5 g의 글리세린 및 100 ㎖의 정제수와 혼합하였다. 이어, 생성된 겔 혼합물을 직장 투여에 적합한 시린지와 같은 직장 전달 단위로 혼입하였다.To prepare a pharmaceutical composition for rectal delivery, 100 mg of any compound of Formula (I) or Formula (II) was added 2.5 g of methylcellulose (1500 mPa), 100 mg of methylparaben, 5 g of glycerin And 100 ml of purified water. The resulting gel mixture was then incorporated into a rectal delivery unit such as a syringe suitable for rectal administration.
실시예Example 30f: 국소용 겔 조성물 30f: topical gel composition
약제학적 국소 겔 조성물을 제조하기 위해, 일반식 (I) 또는 일반식 (II) 중 임의의 화합물 100 ㎎을 1.75 g의 하이드록시프로필 셀루오스, 10 ㎖의 프로필렌글리콜, 10 ㎖의 이소프로필 미리스테이트 및 100 ㎖의 정제 알코올 USP과 혼합하였다. 이어, 생성된 겔 혼합물을 국소 투여에 적합한 튜브와 같은 용기로 혼입하였다.To prepare a pharmaceutical topical gel composition, 100 mg of any compound of formula (I) or formula (II) were added with 1.75 g of hydroxypropyl cellulose, 10 ml of propylene glycol, 10 ml of isopropyl myristate. And 100 ml of purified alcohol USP. The resulting gel mixture was then incorporated into a container such as a tube suitable for topical administration.
실시예Example 30g: 점안용 30g: for eye drops 액제Liquid 조성물 Composition
약제학적 점안용 액제 조성물을 제조하기 위해, 일반식 (I) 또는 일반식 (II) 중 임의의 화합물 100 ㎎을 정제수 100 ㎖ 중 NaCl 0.9 g과 혼합한 다음, 0.2 미크론 필터를 사용하여 여과하였다. 이어, 생성된 등장 용액을 점안 투여에 적합한 아이컵 용기와 같은 점안용 전달 단위로 혼입하였다.To prepare a pharmaceutical eye drop formulation, 100 mg of any compound of Formula (I) or Formula (II) was mixed with 0.9 g of NaCl in 100 ml of purified water and then filtered using a 0.2 micron filter. The resulting isotonic solution was then incorporated into an eye drop delivery unit such as an eyecup container suitable for eye drop administration.
본원에 기술된 실시예 및 구체예는 단지 예시적 목적을 위한 것이며, 제시된 다양한 변형 또는 변화는 본 출원의 정신 및 영역 및 첨부된 청구 범위 내에 포함되는 것이다.The examples and embodiments described herein are for illustrative purposes only, and various modifications or changes shown are intended to be included within the spirit and scope of the present application and the appended claims.
Claims (74)
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체(bioisostere), -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H 또는 이고;
G는 -OR1, -(C1-C6)알킬, -(C1-C6)알킬-OR1, 할로겐, -CO2R1, -(C1-C6)알킬-CO2R1, NHR1, -(C1-C6)알킬-NHR1, -(C=O)NHR1, -(C1-C6)알킬-(C=O)NHR1, -NHR1(C=O)R1 또는 -(C1-C6)알킬-NHR1(C=O)R1이며;
R1은 H 또는 (C1-C6)알킬이고;
X는 할로겐이다.A compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisostere,-(C = O) -NR 1 R, NR 1- (C═O) —R, — (C 1 -C 7 ) alkyl- (C═O) -OR or-(C 1 -C 7 ) alkyl- (C═O) -NR 1 R Is;
R is H or ego;
G is -OR 1 ,-(C 1 -C 6 ) alkyl,-(C 1 -C 6 ) alkyl-OR 1 , halogen, -CO 2 R 1 ,-(C 1 -C 6 ) alkyl-CO 2 R 1 , NHR 1 ,-(C 1 -C 6 ) alkyl-NHR 1 ,-(C = O) NHR 1 ,-(C 1 -C 6 ) alkyl- (C = O) NHR 1 , -NHR 1 (C ═O) R 1 or — (C 1 -C 6 ) alkyl-NHR 1 (C═O) R 1 ;
R 1 is H or (C 1 -C 6 ) alkyl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H 또는 이며;
G는 -OR1, -(C1-C6)알킬, -(C1-C6)알킬-OR1, 할로겐, -CO2R1, -(C1-C6)알킬-CO2R1, NHR1, -(C1-C6)알킬-NHR1, -(C=O)NHR1, -(C1-C6)알킬-(C=O)NHR1, -NHR1(C=O)R1 또는 -(C1-C6)알킬-NHR1(C=O)R1이고;
R1은 H 또는 (C1-C6)알킬이다.The pharmaceutical composition according to claim 1, wherein the compound has a structure of formula (II) or an active metabolite or a pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H or Is;
G is -OR 1 ,-(C 1 -C 6 ) alkyl,-(C 1 -C 6 ) alkyl-OR 1 , halogen, -CO 2 R 1 ,-(C 1 -C 6 ) alkyl-CO 2 R 1 , NHR 1 ,-(C 1 -C 6 ) alkyl-NHR 1 ,-(C = O) NHR 1 ,-(C 1 -C 6 ) alkyl- (C = O) NHR 1 , -NHR 1 (C ═O) R 1 or — (C 1 -C 6 ) alkyl-NHR 1 (C═O) R 1 ;
R 1 is H or (C 1 -C 6 ) alkyl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.A compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutically acceptable excipients or carriers:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, (C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이다.The compound of claim 16, further comprising a compound having the structure of formula (II): or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof; And pharmaceutical compositions with pharmaceutically acceptable excipients or carriers:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl, (C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.A method of treating vitreoretinal disease, comprising administering to a mammal a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, (C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.The method of claim 19, comprising administering to the mammal a therapeutically effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl, (C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.Mammalians have therapeutically effective amounts of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof that modulates serum retinol binding protein or transthyretin level or activity in a mammal. A method of lowering serum retinol binding protein or transthyretin level or activity in a mammal, the method comprising administering to:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, (C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.The method of claim 23, wherein the therapeutically effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt thereof, that modulates serum retinol binding protein or transthyretin level or activity in a mammal Or administering a solvate:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl, (C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.Treating a retinol related disease in a mammal, comprising administering to the mammal a therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof: Way:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.32. The method of claim 31 comprising administering a therapeutically effective amount of a compound of formula (II): or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.Administering to the mammal a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof that does not directly modulate the activity of the enzyme or protein in the visual cycle: To reduce serum retinol levels in mammals with dry form of age-related macular degeneration:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.35. The therapeutically effective amount of a compound of formula (II) below or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof according to claim 34, which does not directly modulate the activity of the enzyme or protein in the visual cycle. A method comprising administering:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.A method of treating hyperretinolemia comprising administering to a mammal a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.The method of claim 40 comprising administering a therapeutically effective amount of a compound of formula (II): or an active metabolite or pharmaceutically acceptable prodrug or solvate thereof:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.Administering to a mammal an effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof, wherein the compound of formula (I) is a retinol- Methods of treating retinol related diseases in mammals that inhibit retinol binding protein-transtyretin complex formation and IC 50 inhibition is less than about 5 μM:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.45. The method of claim 44, comprising administering to the mammal an effective amount of a compound of formula (II) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof: ) Compound inhibits retinol-retinol binding protein-transtyretin complex formation, and IC 5O inhibition is less than about 5 μM:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.A therapeutically effective amount of a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof, which modulates retinol binding protein or transthyretin level or activity in a mammal, A method of treating type I or type II diabetes in a mammal, comprising administering:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.50. An effective amount of a compound of formula (II) below or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof according to claim 49 which modulates retinol binding protein or transthyretin level or activity in a mammal. A method comprising administering to a mammal:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸, 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이며;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이고;
X는 할로겐이다.Serum retinol or ocular tissue in a mammal, comprising administering to the mammal a therapeutically effective amount of a compound of formula (I) and / or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof: How to reduce retinol levels:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl, methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl or optionally substituted heteroaryl;
X is halogen.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, 또는 -(C3-C8)헤테로사이클로알케닐이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R, -(C1-C7)알킬-(C=O)-OR 또는 -(C1-C7)알킬-(C=O)-NR1R이고;
R은 H, 임의로 치환된 아릴, 임의로 치환된 헤테로사이클로알킬 또는 임의로 치환된 헤테로아릴이다.The method of claim 51, comprising administering to the mammal an effective amount of a compound of formula (II): and / or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof.
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl, or-(C 3 -C 8 ) heterocycloalkenyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1 - (C = O) -R , - (C 1 -C 7) alkyl, - (C = O) -OR, or - (C 1 -C 7) alkyl, - (C = O) -NR 1 R a;
R is H, optionally substituted aryl, optionally substituted heterocycloalkyl, or optionally substituted heteroaryl.
상기 식에서,
A는 O, NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐, 또는 -(C3-C8)헤테로사이클로알케닐이며; 단, -(C2-C7)헤테로알킬은 질소 원자, -C(=O)-, -S-, -S(=O)-, -S(=O)2-, -NR1(C=O)-, -(C=O)NR1-, S(=O)2NR1-, -NR1S(=O)2, -0(C=O)NR1-, -NR1(C=O)O-, -0(C=O)O-, -NR1(C=O)NR1-, -(C=O)O- 또는 -0(C=O)-를 함유할 수 없고;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -0-C(O)NR2R3, -NR2R3(C=O)OR1 또는 -SO2NR2R3이고;
R2 및 R3는 각각 독립적으로 H, C1-C6알킬 및 C3-C6 사이클로알킬 중에서 선택되며;
R은 H, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이고, 단 B가 -S-인 경우 R은 피리미딘일 수 없으며; B가 -(C2-C7)알킬인 경우 R은 이미다졸일 수 없고;
R1은 H 또는 (C1-C6)알킬이며;
X는 할로겐이고;
단, 상기 일반식 (I)의 화합물은 다이머일 수 없다.A composition comprising a compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is O, NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl, or-(C 3 -C 8 ) heterocycloalkenyl; Provided that-(C 2 -C 7 ) heteroalkyl is a nitrogen atom, -C (= O)-, -S-, -S (= O)-, -S (= O) 2- , -NR 1 (C = O)-,-(C = O) NR 1- , S (= O) 2 NR 1- , -NR 1 S (= O) 2 , -0 (C = O) NR 1- , -NR 1 ( May contain C═O) O—, —0 (C═O) O—, —NR 1 (C═O) NR 1 —, — (C═O) O— or —0 (C═O) — No;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -C 4 Alkyl, C 2 -C 4 alkynyl, C 3 -C 6 Cycloalkyl, C 1 -C 4 Alkyl- (C 3 -C 6 Cycloalkyl), aryl, substituted aryl, arylalkyl, -C (O) R 2 , hydroxy- (C 1 -C 6 Alkyl), aryloxy, halo, C 1 -C 6 -haloalkyl, cyano, hydroxy, nitro, -0-C (O) NR 2 R 3 , -NR 2 R 3 (C = O) OR 1 or -SO 2 NR 2 R 3 ;
R 2 and R 3 are each independently H, C 1 -C 6 alkyl and C 3 -C 6 Selected from cycloalkyl;
R is H, optionally substituted aryl or optionally substituted heteroaryl, provided that when B is -S-, R cannot be pyrimidine; When B is-(C 2 -C 7 ) alkyl R cannot be imidazole;
R 1 is H or (C 1 -C 6 ) alkyl;
X is halogen;
Provided that the compound of Formula (I) cannot be a dimer.
상기 식에서,
A는 O이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며; 단, -(C2-C7)헤테로알킬은 질소 원자, -C(=O)-, -S-, -S(=O)-, -S(=O)2-, -NR1(C=O)-, -(C=O)NR1-, S(=O)2NR1-, -NR1S(=O)2, -0(C=O)NR1-, -NR1(C=O)O-, -0(C=O)O-, -NR1(C=O)NR1-, -(C=O)O- 또는 -0(C=O)-를 함유할 수 없고;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이며;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -0-C(O)NR2R3, -NR2(C=O)OR1 또는 -SO2NR2R3이고;
R2 및 R3는 각각 독립적으로 H, C1-C6알킬 및 C3-C6 사이클로알킬 중에서 선택되고;
R은 H, -(C2-C7)알킬, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이며, 단 B가 -S-인 경우 R은 피리미딘일 수 없고; B가 -(C2-C7)알킬인 경우 R은 이미다졸일 수 없으며;
R1은 H 또는 (C1-C6)알킬이고;
X는 할로겐이다.A compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is O;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl; Provided that-(C 2 -C 7 ) heteroalkyl is a nitrogen atom, -C (= O)-, -S-, -S (= O)-, -S (= O) 2- , -NR 1 (C = O)-,-(C = O) NR 1- , S (= O) 2 NR 1- , -NR 1 S (= O) 2 , -0 (C = O) NR 1- , -NR 1 ( May contain C═O) O—, —0 (C═O) O—, —NR 1 (C═O) NR 1 —, — (C═O) O— or —0 (C═O) — No;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -C 4 Alkyl, C 2 -C 4 alkynyl, C 3 -C 6 Cycloalkyl, C 1 -C 4 Alkyl- (C 3 -C 6 Cycloalkyl), aryl, substituted aryl, arylalkyl, -C (O) R 2 , hydroxy- (C 1 -C 6 Alkyl), aryloxy, halo, C 1 -C 6 -haloalkyl, cyano, hydroxy, nitro, -0-C (O) NR 2 R 3 , -NR 2 (C = O) OR 1 or -SO 2 NR 2 R 3 ;
R 2 and R 3 are each independently H, C 1 -C 6 alkyl and C 3 -C 6 Selected from cycloalkyl;
R is H,-(C 2 -C 7 ) alkyl, optionally substituted aryl or optionally substituted heteroaryl, provided that when B is -S-, R cannot be pyrimidine; When B is-(C 2 -C 7 ) alkyl R cannot be imidazole;
R 1 is H or (C 1 -C 6 ) alkyl;
X is halogen.
상기 식에서,
A는 NH 또는 S이고;
B는 결합, -(C2-C7)알킬, -(C2-C7)알케닐, -(C3-C8)사이클로알킬, -(C2-C7)헤테로알킬, -(C3-C8)헤테로사이클로알킬, -(C3-C8)사이클로알케닐 또는 -(C3-C8)헤테로사이클로알케닐이며;
D는 이소프로필, 이소부틸, sec-부틸, tert-부틸, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 메틸렌사이클로프로필, 메틸렌사이클로부틸 또는 메틸렌사이클로펜틸이고;
E는 (C=O)-OR, -0-(C=O)-R, -(C=O)-R, -OR, 카르복시산 생물동배체, -(C=O)-NR1R, NR1-(C=O)-R; -(C1-C7)알킬-(C=O)-OR, -(C1-C7)알킬-(C=O)-NR1R, C1-C4 알킬, C2-C4 알키닐, C3-C6 사이클로알킬, C1-C4 알킬-(C3-C6 사이클로알킬), 아릴, 치환된 아릴, 아릴알킬, -C(O)R2, 하이드록시-(C1-C6 알킬), 아릴옥시, 할로, C1-C6-할로알킬, 시아노, 하이드록시, 니트로, -O-C(O)NR2R3, -NR2(C=O)OR1 또는 -SO2NR2R3이며;
R2 및 R3는 각각 독립적으로 H, C1-C6 알킬 및 C3-C6 사이클로알킬 중에서 선택되고;
R은 H, -(C2-C7)알킬, 임의로 치환된 아릴 또는 임의로 치환된 헤테로아릴이며;
R1은 H 또는 (C1-C6)알킬이고;
X는 할로겐이다.A compound of formula (I) or an active metabolite or pharmaceutically acceptable prodrug, salt or solvate thereof:
Where
A is NH or S;
B is a bond,-(C 2 -C 7 ) alkyl,-(C 2 -C 7 ) alkenyl,-(C 3 -C 8 ) cycloalkyl,-(C 2 -C 7 ) heteroalkyl,-(C 3 -C 8 ) heterocycloalkyl,-(C 3 -C 8 ) cycloalkenyl or-(C 3 -C 8 ) heterocycloalkenyl;
D is isopropyl, isobutyl, sec-butyl, tert-butyl, cyclopropyl, cyclobutyl, cyclopentyl, methylenecyclopropyl, methylenecyclobutyl or methylenecyclopentyl;
E is (C = O) -OR, -0- (C = O) -R,-(C = O) -R, -OR, carboxylic acid bioisotope,-(C = O) -NR 1 R, NR 1- (C = 0) -R; - (C 1 -C 7) alkyl, - (C = O) -OR, - (C 1 -C 7) alkyl, - (C = O) -NR 1 R, C 1 -C 4 Alkyl, C 2 -C 4 alkynyl, C 3 -C 6 cycloalkyl, C 1 -C 4 Alkyl- (C 3 -C 6 Cycloalkyl), aryl, substituted aryl, arylalkyl, -C (O) R 2 , hydroxy- (C 1 -C 6 Alkyl), aryloxy, halo, C 1 -C 6 -haloalkyl, cyano, hydroxy, nitro, -OC (O) NR 2 R 3 , -NR 2 (C = O) OR 1 or -SO 2 NR 2 R 3 ;
R 2 and R 3 are each independently H, C 1 -C 6 Alkyl and C 3 -C 6 cycloalkyl;
R is H,-(C 2 -C 7 ) alkyl, optionally substituted aryl or optionally substituted heteroaryl;
R 1 is H or (C 1 -C 6 ) alkyl;
X is halogen.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US97576507P | 2007-09-27 | 2007-09-27 | |
| US60/975,765 | 2007-09-27 | ||
| US98132207P | 2007-10-19 | 2007-10-19 | |
| US60/981,322 | 2007-10-19 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20100097098A true KR20100097098A (en) | 2010-09-02 |
Family
ID=40512081
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107009129A KR20100097098A (en) | 2007-09-27 | 2008-09-16 | Methods and compounds for treating retinol-related diseases |
Country Status (8)
| Country | Link |
|---|---|
| EP (1) | EP2205234A4 (en) |
| JP (1) | JP2010540541A (en) |
| KR (1) | KR20100097098A (en) |
| CN (1) | CN101873852A (en) |
| AU (1) | AU2008305303A1 (en) |
| CA (1) | CA2699773A1 (en) |
| IL (1) | IL204728A0 (en) |
| WO (1) | WO2009042444A2 (en) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009051244A1 (en) * | 2007-10-18 | 2009-04-23 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| JP5706337B2 (en) * | 2009-04-16 | 2015-04-22 | 武田薬品工業株式会社 | Derivatives of N-acyl-N'-phenylpiperazine useful for the prevention or treatment of diabetes (among others) |
| EP2642998B1 (en) | 2010-11-24 | 2020-09-16 | The Trustees of Columbia University in the City of New York | A non-retinoid rbp4 antagonist for treatment of age-related macular degeneration and stargardt disease |
| RU2013129999A (en) * | 2010-12-02 | 2015-01-10 | Дайити Санкио Компани, Лимитед | MODIFIED SINGLE-CHAIN POLYNUCLEOTIDE |
| US9333202B2 (en) | 2012-05-01 | 2016-05-10 | The Trustees Of Columbia University In The City Of New York | Non-retinoid antagonists for treatment of age-related macular degeneration and stargardt disease |
| WO2014151936A1 (en) | 2013-03-14 | 2014-09-25 | The Trustees Of Columbia University In The City Of New York | Octahydropyrrolopyrroles, their preparation and use |
| EP2968304B1 (en) | 2013-03-14 | 2018-10-10 | The Trustees of Columbia University in the City of New York | 4-phenylpiperidines, their preparation and use |
| WO2014152018A1 (en) | 2013-03-14 | 2014-09-25 | The Trustees Of Columbia University In The City Of New York | Octahydrocyclopentapyrroles, their preparation and use |
| US9938291B2 (en) | 2013-03-14 | 2018-04-10 | The Trustess Of Columbia University In The City Of New York | N-alkyl-2-phenoxyethanamines, their preparation and use |
| CN106794364B (en) | 2014-04-30 | 2019-12-24 | 哥伦比亚大学董事会 | Substituted 4-phenylpiperidines, their preparation and use |
| LT3210973T (en) | 2014-10-24 | 2021-03-25 | Takeda Pharmaceutical Company Limited | Heteroaryl compounds for the treatment of ophthalmic diseases |
| US9944596B2 (en) * | 2014-10-24 | 2018-04-17 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2526534A (en) * | 1948-07-03 | 1950-10-17 | Dow Chemical Co | Di-(aryloxy)-methanes |
| US4255152A (en) * | 1978-09-05 | 1981-03-10 | Ciba-Geigy Corporation | Process for the dyeing of hydrophobic fibres |
| JPS577480A (en) * | 1980-06-16 | 1982-01-14 | Sankyo Co Ltd | 4-alkoxy-6-phenoxymethyl-2-pyrone derivative |
| US7510710B2 (en) * | 2004-01-08 | 2009-03-31 | The Regents Of The University Of Colorado | Compositions of UCP inhibitors, Fas antibody, a fatty acid metabolism inhibitor and/or a glucose metabolism inhibitor |
| WO2005092062A2 (en) * | 2004-03-19 | 2005-10-06 | Myriad Genetics, Inc. | Compounds for neurodegenerative disorders |
| WO2005116010A1 (en) * | 2004-05-26 | 2005-12-08 | Merck Frosst Canada Ltd. | Ep4 receptor agonist, compositions and methods thereof |
-
2008
- 2008-09-16 CA CA2699773A patent/CA2699773A1/en not_active Abandoned
- 2008-09-16 KR KR1020107009129A patent/KR20100097098A/en not_active Application Discontinuation
- 2008-09-16 EP EP08834564A patent/EP2205234A4/en not_active Withdrawn
- 2008-09-16 AU AU2008305303A patent/AU2008305303A1/en not_active Abandoned
- 2008-09-16 CN CN200880107835A patent/CN101873852A/en active Pending
- 2008-09-16 JP JP2010527024A patent/JP2010540541A/en active Pending
- 2008-09-16 WO PCT/US2008/076499 patent/WO2009042444A2/en active Application Filing
-
2010
- 2010-03-25 IL IL204728A patent/IL204728A0/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP2205234A4 (en) | 2010-12-22 |
| EP2205234A2 (en) | 2010-07-14 |
| WO2009042444A3 (en) | 2009-05-14 |
| CN101873852A (en) | 2010-10-27 |
| IL204728A0 (en) | 2010-11-30 |
| CA2699773A1 (en) | 2009-04-02 |
| WO2009042444A2 (en) | 2009-04-02 |
| AU2008305303A1 (en) | 2009-04-02 |
| JP2010540541A (en) | 2010-12-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7973079B2 (en) | Methods and compounds for treating retinol-related diseases | |
| KR20100097098A (en) | Methods and compounds for treating retinol-related diseases | |
| EP1768657B1 (en) | Methods and compositions for treating ophthalmic conditions with retinyl derivates | |
| US20120288568A1 (en) | Methods and compositions for treating ophthalmic conditions via serum retinol, serum retinol binding protein (rbp), and/or serum retinol-rbp modulation | |
| JP2008515778A (en) | Combination methods, compositions and therapies for treating ocular conditions with 13-cis-retinyl derivatives | |
| EP2427052B1 (en) | Compositions for use in the treatment of glaucoma or ocular hypertension |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| N231 | Notification of change of applicant | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |