KR102054675B1 - flame-retardant ester polyol, the manufacturing method thereof and polyisocyanurates including the anti-flame ester polyol - Google Patents
flame-retardant ester polyol, the manufacturing method thereof and polyisocyanurates including the anti-flame ester polyol Download PDFInfo
- Publication number
- KR102054675B1 KR102054675B1 KR1020170077877A KR20170077877A KR102054675B1 KR 102054675 B1 KR102054675 B1 KR 102054675B1 KR 1020170077877 A KR1020170077877 A KR 1020170077877A KR 20170077877 A KR20170077877 A KR 20170077877A KR 102054675 B1 KR102054675 B1 KR 102054675B1
- Authority
- KR
- South Korea
- Prior art keywords
- alkyl
- ester polyol
- unsubstituted
- substituted
- alkylene
- Prior art date
Links
- BHZQNPSGIHNDGM-UHFFFAOYSA-N CC(COC(CCCCCCCCC(OCCN(C)CNc1nc(NCN(C)CCO)nc(NCP(OC)(OC)=O)n1)=O)=O)O Chemical compound CC(COC(CCCCCCCCC(OCCN(C)CNc1nc(NCN(C)CCO)nc(NCP(OC)(OC)=O)n1)=O)=O)O BHZQNPSGIHNDGM-UHFFFAOYSA-N 0.000 description 1
- QFTSKDMOVWRERF-UHFFFAOYSA-N COP(C)(CNc1nc(NCN(CCO)CCOC(c(cccc2)c2C(OCCOCCO)=O)=O)nc(NCN(CCO)CCO)n1)=O Chemical compound COP(C)(CNc1nc(NCN(CCO)CCOC(c(cccc2)c2C(OCCOCCO)=O)=O)nc(NCN(CCO)CCO)n1)=O QFTSKDMOVWRERF-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K21/00—Fireproofing materials
- C09K21/06—Organic materials
- C09K21/12—Organic materials containing phosphorus
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C215/00—Compounds containing amino and hydroxy groups bound to the same carbon skeleton
- C07C215/02—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton
- C07C215/04—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being saturated
- C07C215/06—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups and amino groups bound to acyclic carbon atoms of the same carbon skeleton the carbon skeleton being saturated and acyclic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/42—Polycondensates having carboxylic or carbonic ester groups in the main chain
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Polyurethanes Or Polyureas (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Fireproofing Substances (AREA)
Abstract
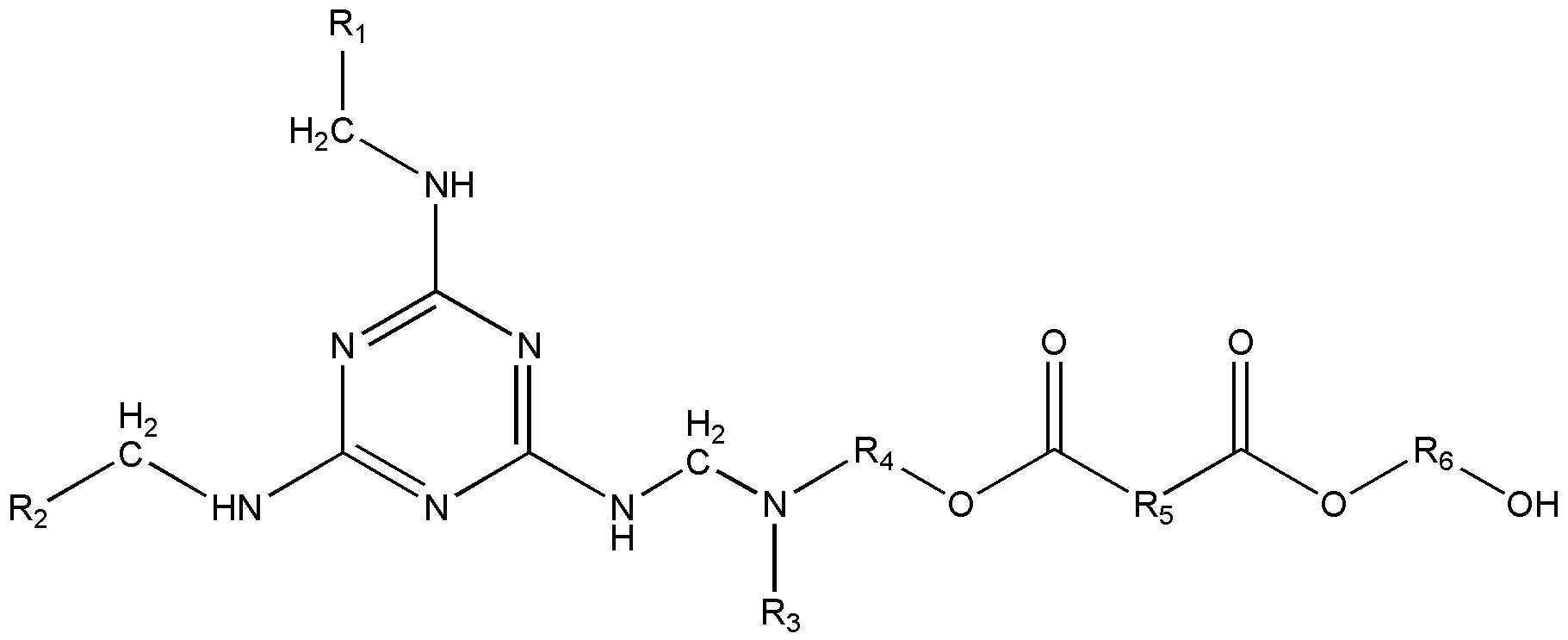
본 발명은 화학적으로 결합된 멜라민 및 인 성분을 포함하여 난연성이 향상된 하기 화학식 1로 표시되는 에스테르 폴리올과, 상기 에스테르 폴리올을 포함하여 난연성을 갖는 폴리이소시아누레이트에 관한 것이다.
[화학식 1]
The present invention relates to an ester polyol represented by the following Chemical Formula 1 including chemically bonded melamine and phosphorus components and improved flame retardancy, and a polyisocyanurate having flame retardancy including the ester polyol.
[Formula 1]
Description
본 발명은 화학적으로 결합된 멜라민 및 인 성분을 포함하여 난연성이 향상된 에스테르 폴리올과, 상기 에스테르 폴리올을 포함하여 난연성을 갖는 폴리이소시아누레이트에 관한 것이다.The present invention relates to an ester polyol having improved flame retardancy, including chemically bonded melamine and phosphorus components, and a polyisocyanurate having flame retardancy, including the ester polyol.
열경화성 수지로서 광범위하게 사용되고 있는 폴리우레탄 수지 중 경질 폴리우레탄 폼은 사용되는 폴리올이 연질에 비해 작용기가 많고, 분자량이 적어 많은 가교를 통해 단열성 및 치수 안정성을 가지므로 단열재나 건축자재로 널리 사용되고 있다. 또한 폴리올과 반응하는 이소시아네이트의 함량 및 반응을 조절할 경우 폴리이소시아누레이트 구조를 제조하여, 난연성이 보다 향상된 폴리이소시아누레이트를 제조할 수 있다.Among the polyurethane resins widely used as thermosetting resins, the rigid polyurethane foam is widely used as a heat insulating material or a building material because the polyol used has many functional groups and a low molecular weight, and thus has insulation and dimensional stability through many crosslinking. In addition, by adjusting the content and reaction of the isocyanate reacting with the polyol to prepare a polyisocyanurate structure, it is possible to produce a polyisocyanurate with improved flame retardancy.
폴리이소시아누레이트의 제조에 사용되는 폴리올은 에스터 폴리올에 비해 열적인 성질이 우수한 프탈산 계열의 에스테르 폴리올이 주로 활용되어지고 있으나, 점도로 인한 작업성의 문제로 에스터 폴리올과 섞어 사용하거나, 용제로 희석하여 사용하고 있는 실정이다.The polyols used in the production of polyisocyanurate are mainly used ester polyols of phthalic acid series which have better thermal properties than ester polyols, but due to the problem of workability due to viscosity, they can be mixed with ester polyols or diluted with solvents. I'm using it.
또한 최근 친환경적인 소재에 대한 규제가 강화되면서, 우레탄 소재에도 보다 우수한 난연성과 친환경성이 요구되어지고 있다. In addition, as regulations on environmentally friendly materials are recently strengthened, urethane materials are required to have better flame retardancy and eco-friendliness.
이에, 한국 등록특허 제10-1290529호와 한국 공개특허 제10-2014-0020819호에서는 점도, 상용성 및 물리적인 성질을 개선하기 위해 에테르 폴리올을 원료로 사용하여 축합반응에 의해 에스테르 폴리올을 제조하는 방법을 기술한다. 그러나 이러한 방법에 의해 형성된 폴리우레탄이나 폴리이소시아누레이트는 에테르 성분 함량이 증가되는 반면, 프탈산과 같은 난연성을 띄는 성분 함량은 감소됨에 따라 열적인 성질은 오히려 감소할 우려가 있다. Thus, in Korean Patent Registration No. 10-1290529 and Korean Patent Publication No. 10-2014-0020819, in order to improve viscosity, compatibility and physical properties, ester polyol is prepared by condensation reaction using ether polyol as a raw material. Describe the method. However, the polyurethane or polyisocyanurate formed by such a method has an increased ether component content, but there is a concern that the thermal properties are rather reduced as the content of flame retardant components such as phthalic acid is decreased.
또한, 한국 등록특허 제10-0910258호에서는 난연성 폴리에스테르 폴리올에 대해 기술하고 있으나, 구성 성분으로 난연제로의 사용이 규제된 할로겐 원소를 포함한 알코올을 사용하고 있어, 최근 친환경적인 소재에 대한 요구에 부합되지 않음을 알 수 있다. In addition, Korean Patent No. 10-0910258 describes a flame retardant polyester polyol, but uses alcohol containing a halogen element whose use as a flame retardant is regulated as a constituent, thus meeting the demand for environmentally friendly materials. It can be seen that.
또한 한국공개특허 제10-2009-0039473호에서는 이소시아누레이트기를 포함하는 에스테르 폴리올을 제조하는 방법을 기술하였다. 그러나 이소시아누레이트기를 포함하기 위해 결합되는 부분이 에폭시나 각종 관능기로 치환된 이소시아누레이트를 사용하므로 그 비용이 상당히 고가이며, 에스테르 폴리올 제조를 위해 고온 고압장치를 운영하므로 시설 및 생산비용이 증가하는 문제가 있을 수 있다. 또한 인과 같은 난연성분이 폴리올 내에 포함되어 있지 않아 난연 성능의 향상을 위해 난연제를 추가로 필요로 하는 번거로움이 있을 수 있다. In addition, Korean Patent Publication No. 10-2009-0039473 describes a method for preparing an ester polyol including an isocyanurate group. However, since the portion bonded to include the isocyanurate group uses isocyanurate substituted with epoxy or various functional groups, the cost is quite expensive, and since the high temperature and high pressure device is operated to manufacture the ester polyol, the facility and production cost are high. There may be an increasing problem. In addition, since a flame retardant component such as phosphorus is not included in the polyol, there may be a need for additional flame retardant to improve flame retardant performance.
이에 본 발명에서는 상기의 문제점을 해결하기 위하여, 난연성이 우수한 멜라민 및 인 성분을 화학적으로 결합시켜 난연성을 향상시킨, 멜라민 및 인 성분을 포함하는 난연성 에스테르 폴리올을 제공하는 것을 그 해결과제로 한다.In the present invention, to solve the above problems, to provide a flame-retardant ester polyol containing a melamine and phosphorus component, which is improved by flame-retardant by chemically combining the melamine and phosphorus component excellent in flame retardancy to the problem.
또한 본 발명은 상기 난연성 에스테르 폴리올의 제조방법을 제공하는 것을 또 다른 해결과제로 한다.It is another object of the present invention to provide a method for preparing the flame retardant ester polyol.
또한, 본 발명은 상기 난연성 에스테르 폴리올을 포함한 폴리이소시아누레이트를 제공하는 것을 또 다른 해결과제로 한다.It is another object of the present invention to provide a polyisocyanurate comprising the flame retardant ester polyol.
상기 과제를 해결하기 위한 본 발명의 일 측면에 따르면,According to an aspect of the present invention for solving the above problems,
하기 화학식 1로 표시되는 것을 특징으로 하는, 난연성 에스테르 폴리올을 제공한다.It provides a flame retardant ester polyol, characterized in that represented by the formula (1).
[화학식 1][Formula 1]
또한, 본 발명의 다른 과제를 해결하기 위하여, 난연성 에스테르 폴리올의 제조방법을 제공한다.Furthermore, in order to solve the another subject of this invention, it provides the manufacturing method of a flame-retardant ester polyol.
또한, 본 발명의 또 다른 과제를 해결하기 위하여, 상기 난연성 에스테르 폴리올을 포함한 폴리이소시아누레이트를 제공한다.In addition, to solve another problem of the present invention, there is provided a polyisocyanurate comprising the flame-retardant ester polyol.
본 발명에 따른 에스테르 폴리올은 화학적으로 결합된 멜라민과 인 성분을 포함함에 따라 난연성이 우수함은 물론, 관능기를 증가시킴에 따라 이를 포함하여 제조된 폴리이소시아누레이트는 물리적 성질이 향상됨은 물론이고, 별도의 난연제 성분 없이도 난연성을 나타낸다.The ester polyol according to the present invention has excellent flame retardancy according to the chemically bonded melamine and phosphorus component, as well as polyisocyanurate prepared by increasing the functional group, as well as improving physical properties, Flame retardant is shown even without the flame retardant component.
또한, 본 발명에 따라 제조된 에스테르 폴리올은 액상으로 상압 하에서 제조됨에 따라 장치 및 생산비용을 낮출 수 있는 이점이 있다.In addition, the ester polyol prepared according to the present invention has the advantage that can be lowered in the apparatus and production cost as it is prepared under normal pressure in the liquid phase.
본 발명은 멜라민 및 인 성분을 화학적으로 결합시켜 난연성을 갖도록 하는, 난연성 에스테르 폴리올에 관한 것이다.The present invention relates to a flame retardant ester polyol which chemically combines the melamine and phosphorus components to be flame retardant.
이하, 본 발명을 자세히 설명하기로 한다.Hereinafter, the present invention will be described in detail.
본 발명의 일 측면에 따르면,According to one aspect of the invention,
본 발명의 난연성 에스테르 폴리올은 하기 화학식 1로 표시되는 것을 특징으로 한다.The flame retardant ester polyol of the present invention is characterized by represented by the following formula (1).
[화학식 1][Formula 1]
상기 화학식 1에 있어서, R1은 포스파이트(phosphate)기이고, R2는 아미노기이며, R3는 수소, -CH2OH, -CH2CH2OH, C1-C10 알킬, C2-C10 알케닐, 치환 또는 비치환된 C1-C10 히드록시알킬, C1-C10 아미노알킬, C1-C10 알콕시, (C1-C10)알콕시(C1-C10)알킬, 히드록시(C1-C10)알킬옥시(C1-C10)알킬, C1-C10 알킬아미노, 아미노(C1-C10)알킬옥시(C1-C10)알킬 또는 히드록시(C1-C10)알킬아미노(C1-C10)알킬인 것을 특징으로 한다.In Formula 1, R 1 is a phosphite group, R 2 is an amino group, R 3 is hydrogen, -CH 2 OH, -CH 2 CH 2 OH, C 1 -C 10 alkyl, C 2- C 10 alkenyl, substituted or unsubstituted C 1 -C 10 hydroxyalkyl, C 1 -C 10 aminoalkyl, C 1 -C 10 alkoxy, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkyl , Hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl, C 1 -C 10 alkylamino, amino (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl or hydroxy (C 1 -C 10 ) alkylamino (C 1 -C 10 ) alkyl.
또한, 상기 화학식 1에 있어서, R4는 C1-C10 알킬렌, 치환 또는 비치환된 C1-C10 히드록시알킬렌, (C1-C10)알콕시(C1-C10)알킬렌 또는 히드록시(C1-C10)알킬옥시(C1-C10)알킬렌이며, R5는 C6~C18 아릴렌, C1-C10 알킬렌, 페닐(C1-C10)알킬렌, (C1-C10 알킬)페닐렌이고, R6는 C1-C10 알킬렌, (C1~C20)알콕시(C1~C20)알킬렌, 히드록시(C1-C10)알킬옥시(C1-C10)알킬렌 또는 C1-C20 히드록시알킬렌인 것을 특징으로 한다.In addition, in Chemical Formula 1, R 4 is C 1 -C 10 alkylene, substituted or unsubstituted C 1 -C 10 hydroxyalkylene, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkyl Ylene or hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkylene, R 5 is C 6 -C 18 arylene, C 1 -C 10 alkylene, phenyl (C 1 -C 10 ) Alkylene, (C 1 -C 10 alkyl) phenylene, R 6 is C 1 -C 10 alkylene, (C 1 -C 20 ) alkoxy (C 1 -C 20 ) alkylene, hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkylene or C 1 -C 20 hydroxyalkylene.
이때, 상기 포스파이트기는, 하기 화학식 2로 표시되는 것을 특징으로 한다.In this case, the phosphite group is represented by the following formula (2).
[화학식 2]
[Formula 2]
삭제delete
상세하게는, 상기 화학식 2에서 R7은 치환 또는 무치환의 C1-C20 알킬, 치환 또는 무치환의 C1-C20 헤테로 알킬, 치환 또는 무치환의 C3-C20 사이클로알킬, 및 치환 또는 무치환의 C7-C30 아릴알킬 중에서 선택되는 어느 하나인 것을 특징으로 한다.Specifically, in Formula 2, R 7 is substituted or unsubstituted C 1 -C 20 alkyl, substituted or unsubstituted C 1 -C 20 heteroalkyl, substituted or unsubstituted C 3 -C 20 cycloalkyl, and It is characterized in that any one selected from substituted or unsubstituted C 7 -C 30 arylalkyl.
바람직하게는 상기 포스파이트기는 디알킬포스파이트기로, R7은 치환 또는 무치환의 C1-C20 알킬, 치환 또는 무치환의 C3-C20 사이클로알킬 또는 치환 또는 무치환의 C7-C30 아릴알킬 중에서 선택되는 어느 하나인 것을 특징으로 한다.Preferably, the phosphite group is a dialkyl phosphite group, R 7 is substituted or unsubstituted C 1 -C 20 alkyl, substituted or unsubstituted C 3 -C 20 cycloalkyl or substituted or unsubstituted C 7 -C It is characterized in that any one selected from 30 arylalkyl.
보다 바람직하게는 상기 R7은 메틸, 에틸, 프로필, 부틸, 사이클로헥실인 것을 특징으로 한다. More preferably, R 7 is characterized in that methyl, ethyl, propyl, butyl, cyclohexyl.
또한, 본 발명, 화학식 1에 있어서, 아미노기는, 하기 화학식 3으로 표시되는 것을 특징으로 한다.In the present invention and formula (1), the amino group is represented by the following formula (3).
[화학식 3][Formula 3]
상기 화학식 3에서 R8 및 R9는 각각 독립적으로 수소, CH2OH, -CH2CH2OH, C1-C10 알킬, C2-C10 알케닐, 아미노, 치환 또는 비치환된 C1-C10 히드록시알킬, C1-C10 아미노알킬, C1-C10 알콕시, (C1-C10)알콕시(C1-C10)알킬, 히드록시(C1-C10)알킬옥시(C1-C10)알킬, C1-C10 알킬아미노, 아미노(C1-C10)알킬옥시(C1-C10)알킬 또는 히드록시(C1-C10)알킬아미노(C1-C10)알킬이고, 상기 R8 및 R9 중 적어도 어느 하나는 치환 또는 비치환된 C1-C10 히드록시알킬인 것을 특징으로 한다.R 8 and R 9 in Formula 3 are each independently hydrogen, CH 2 OH, —CH 2 CH 2 OH, C 1 -C 10 alkyl, C 2 -C 10 alkenyl, amino, substituted or unsubstituted C 1 -C 10 hydroxyalkyl, C 1 -C 10 aminoalkyl, C 1 -C 10 alkoxy, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkyl, hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl, C 1 -C 10 alkylamino, amino (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl or hydroxy (C 1 -C 10 ) alkylamino (C 1 -C 10 ) alkyl, wherein at least one of R 8 and R 9 is a substituted or unsubstituted C 1 -C 10 hydroxyalkyl.
삭제delete
상기 본 발명, 난연성 에스테르 폴리올은 하기 화학식 4와 같이 나타낼 수 있다.The present invention, the flame retardant ester polyol may be represented by the following formula (4).
[화학식 4][Formula 4]
상기 화학식 4에서 R' 및 R4는 각각 독립적으로 C1-C10 알킬렌, 치환 또는 비치환된 C1-C10 히드록시알킬렌, 페닐(C1-C10)알킬렌, (C1-C10)알콕시(C1-C10)알킬렌 또는 히드록시(C1-C10)알킬옥시(C1-C10)알킬렌인 것을 특징으로 한다.In the general formula R 4 'and R 4 are each independently C 1 -C 10 alkylene, substituted or unsubstituted C 1 -C 10 hydroxy-alkylene, phenyl (C 1 -C 10) alkylene, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkylene or hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkylene.
또한, 상기 화학식 4에서 R" 및 R3은 각각 독립적으로 수소, -CH2OH, -CH2CH2OH, C1-C10 알킬, C2-C10 알케닐, 치환 또는 비치환의 C1-C10 히드록시알킬, C1-C10 아미노알킬, (C1-C10 알킬)페닐, 페닐(C1-C10)알킬, C1-C10 알콕시, (C1-C10)알콕시(C1-C10)알킬, 히드록시(C1-C10)알킬옥시(C1-C10)알킬, C1-C10 알킬아미노, 아미노(C1-C10)알킬옥시(C1-C10)알킬 또는 히드록시(C1-C10)알킬아미노(C1-C10)알킬인 것을 특징으로 한다.In addition, in Formula 4, R ″ and R 3 are each independently hydrogen, —CH 2 OH, —CH 2 CH 2 OH, C 1 -C 10 alkyl, C 2 -C 10 alkenyl, substituted or unsubstituted C 1 -C 10 hydroxyalkyl, C 1 -C 10 aminoalkyl, (C 1 -C 10 alkyl) phenyl, phenyl (C 1 -C 10 ) alkyl, C 1 -C 10 alkoxy, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkyl, hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl, C 1 -C 10 alkylamino, amino (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl or hydroxy (C 1 -C 10 ) alkylamino (C 1 -C 10 ) alkyl.
또한, 상기 화학식 4에서 R5는 C6~C18 아릴렌, C1-C10 알킬렌, 페닐(C1-C10)알킬렌, (C1-C10 알킬)페닐렌이고, R6는 C1-C10 알킬렌, (C1~C20)알콕시(C1~C20)알킬렌, (C1~C10)알콕시(C6-C18)아릴렌, C3~C20 사이클로알킬렌, C6~C18 아릴렌, C7~C30 아릴알킬렌, C7~C30알킬아릴렌, 히드록시(C1-C10)알킬옥시(C1-C10)알킬렌 또는 C1-C20 히드록시 알킬렌이며, R7은 치환 또는 무치환의 C1-C20 알킬, 치환 또는 무치환의 C1-C20 헤테로 알킬, 치환 또는 무치환의 C3-C20 사이클로알킬, 치환 또는 무치환의 C5-C30의 헤테로 사이클로알킬, 치환 또는 무치환의 C7-C30알킬아릴, 치환 또는 무치환의 C6-C20 아릴 및 치환 또는 무치환의 C7-C30 아릴알킬 중에서 선택되는 어느 하나인 것을 특징으로 한다.In addition, in Formula 4, R 5 is C 6 ~ C 18 arylene, C 1 -C 10 alkylene, phenyl (C 1 -C 10 ) alkylene, (C 1 -C 10 alkyl) phenylene, R 6 Is C 1 -C 10 alkylene, (C 1 ~ C 20 ) alkoxy (C 1 ~ C 20 ) alkylene, (C 1 ~ C 10 ) alkoxy (C 6 -C 18 ) arylene, C 3 ~ C 20 Cycloalkylene, C 6 -C 18 arylene, C 7 -C 30 arylalkylene, C 7 -C 30 alkylarylene, hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkylene Or C 1 -C 20 hydroxy alkylene, R 7 is substituted or unsubstituted C 1 -C 20 alkyl, substituted or unsubstituted C 1 -C 20 heteroalkyl, substituted or unsubstituted C 3 -C 20 Cycloalkyl, substituted or unsubstituted C 5 -C 30 heterocycloalkyl, substituted or unsubstituted C 7 -C 30 alkylaryl, substituted or unsubstituted C 6 -C 20 aryl and substituted or unsubstituted C 7 It is characterized in that any one selected from -C 30 arylalkyl.
상세하게는 본 발명의 난연성 에스테르 폴리올은 하기 화학식들로 나타낼 수 있으나, 이에 한정되는 것은 아니다.Specifically, the flame retardant ester polyol of the present invention may be represented by the following chemical formula, but is not limited thereto.
본 발명의 다른 일 측면에 따르면,According to another aspect of the present invention,
상기 난연성 에스테르 폴리올의 제조방법이 제공된다.Provided are methods for preparing the flame retardant ester polyols.
상세하게는, 멜라민과 포름알데히드를 반응시켜 트리메틸올멜라민을 합성하는 제 1 단계; 상기 합성된 트리메틸올멜라민에 알칸올 아민 및 디알킬포스파이트를 첨가하여 중합시킨 다음, 물을 제거하는 제 2 단계; 및 상기 제 2 단계 완료 후, 다가산 및 다가 알코올을 첨가하여 혼합 및 반응시킴으로써 에스테르 폴리올을 합성하는 제 3 단계;를 포함하여 난연성 에스테르 폴리올을 제조하는 것을 특징으로 하는, 난연성 에스테르 폴리올의 제조방법이 제공된다.Specifically, the first step of synthesizing trimethylolmelamine by reacting melamine and formaldehyde; A second step of polymerization by adding alkanol amine and dialkyl phosphite to the synthesized trimethylolmelamine and then removing water; And a third step of synthesizing the ester polyol by mixing and reacting by adding a polyacid and a polyhydric alcohol after the completion of the second step, wherein the method for producing a flame retardant ester polyol comprises Is provided.
본 발명에 있어서, 상기 제 1 단계는 멜라민과 포름알데히드 수용액을 반응시켜 트리메틸올멜라민을 합성하는 단계로, 상세하게는 멜리민과 포름알데히드 수용액을 40 ~ 60℃에서 1 ~ 3시간 교반함으로써, 하기 화학식 5로 표시되는 트리메틸올멜라민을 합성하는 것을 특징으로 한다.In the present invention, the first step is a step of synthesizing trimethylolmelamine by reacting the melamine and formaldehyde aqueous solution, in detail by stirring the melamine and aqueous formaldehyde aqueous solution at 40 ~ 60 ℃ for 1 to 3 hours, It is characterized by synthesizing trimethylolmelamine represented by the formula (5).
이때, 반응온도를 40 ~ 60℃로 하는 것은, 반응 온도가 40℃보다 낮을 경우 트리메틸올멜라민의 합성이 이루어지지 않을 수 있고, 온도가 60℃ 보다 높을 경우 멜라민이 수지화되어 경화될 수 있기 때문이다. At this time, the reaction temperature is 40 ~ 60 ℃, when the reaction temperature is lower than 40 ℃ can not be synthesized trimethylol melamine, because when the temperature is higher than 60 ℃ melamine can be resinized and cured to be.
[화학식 5][Formula 5]
또한, 상기 제 1 단계에 의해 트리메틸올멜라민이 합성 된 후에는 이를 냉각하여 20 ~ 30℃로 조정하는 것을 특징으로 한다.In addition, after the trimethylolmelamine is synthesized by the first step it is characterized in that the cooling to adjust to 20 ~ 30 ℃.
다음으로, 제 2 단계는 상기 합성된 트리메틸올멜라민에 알칸올 아민 및 디알킬포스파이트를 첨가하여 중합시킨 다음, 물을 제거하는 단계이다.Next, the second step is to add the alkanol amine and dialkyl phosphite to the synthesized trimethylol melamine, and then to remove the water.
상세하게는 상기 제 2 단계는 트리메틸올멜라민에 알칸올 아민 및 디알킬포스파이트를 첨가하여 50 ~ 80℃에서 1~3시간 동안 반응시킴으로써 중합하고, 이 후 감압하여 물을 제거하는 것을 특징으로 한다.Specifically, the second step is the polymerization by adding an alkanol amine and dialkyl phosphite to trimethylol melamine and reacting at 50 ~ 80 ℃ for 1 to 3 hours, after which the pressure is removed to remove water .
이때 상기 반응온도가 50 ~ 80℃인 것은 50℃미만에서 상기 중합반응이 이루어질 경우 합성이 용이하게 이루어지지 않을 수 있고, 80℃를 초과할 경우는 열화되어 멜라민이 자체 축합으로 결정화되는 문제가 발생할 수 있기 때문이다.In this case, the reaction temperature of 50 ~ 80 ℃ may not be easily synthesized when the polymerization reaction is performed at less than 50 ℃, if it exceeds 80 ℃ deterioration occurs a problem that melamine crystallized by self-condensation Because it can.
또한, 상기 제 2 단계에서 상기 트리메틸올멜라민에 알칸올 아민 및 디알킬포스파이트를 첨가함에 있어서, 상기 트리메틸올멜라민 1 몰에 대해 알칸올 아민은 2 ~ 2.5몰, 디알킬포스파이트는 0.5 ~ 1몰을 첨가하는 것을 특징으로 한다.In addition, in adding the alkanol amine and dialkyl phosphite to the trimethylol melamine in the second step, 2 to 2.5 moles of alkanol amines and 0.5 to 1 dialkyl phosphites per 1 mole of the trimethylol melamine. It is characterized by adding a mole.
이는 상기 트리메틸올멜라민 1몰에 대해 상기 알칸올 아민이 2몰 미만으로 포함될 경우에는 디알킬포스파이트의 함량이 상기 트리메틸올멜라민 대비 1몰을 초과하여 함유됨에 따라 필요이상의 인의 함량으로 인해 제조 가격 상승을 야기함은 물론이고, 망상구조를 형성하기 어려워 난연성이 저하되고, 이에 따라 제조된 폴리올로 폴리우레탄 폼을 제조할 시 발포가 용이하게 이루어지지 않는 문제가 발생하게 되기 때문이다.This is because when the alkanol amine is included in less than 2 moles per 1 mole of the trimethylolmelamine, the production price is increased due to the amount of phosphorus more than necessary as the content of dialkyl phosphite is more than 1 mole compared to the trimethylolmelamine. Of course, since it is difficult to form a network structure, the flame retardancy is lowered, and when the polyurethane foam is produced with the polyol produced according to this problem is not easily made foaming occurs.
또한 상기 트리메틸올멜라민 1몰에 대해 상기 알칸올 아민이 2.5몰을 초과하여 포함될 경우에는, 점도가 지나치게 높아지고 인의 함량이 저하되어 난연성이 저하되는 문제가 발생되기 때문이다. In addition, when the alkanol amine is contained in an amount of more than 2.5 moles per 1 mole of the trimethylol melamine, the viscosity is excessively high, the content of phosphorus is lowered, and the problem of flame retardancy is generated.
또한 상기 제 2 단계에서는 상기 중합반응 후, 물을 제거할 시 50 ~ 80℃에서 감압하는 것을 특징으로 한다. 이는, 50℃ 미만에서는 물이 원활하게 탈수되지 않아 탈수 시간이 길어지는 문제가 발생할 수 있고, 온도가 80℃ 보다 높을 경우에는 자가 축합 반응이 발생하여 점도가 증가하는 문제가 발생할 수 있기 때문이다.In the second step, after the polymerization reaction, it is characterized in that the pressure at 50 ~ 80 ℃ when removing the water. This is because when the water is less than 50 ℃ dehydrated smoothly may cause a problem that the dehydration time is long, when the temperature is higher than 80 ℃ may cause a problem that the self-condensation reaction occurs to increase the viscosity.
이에 따라 상기 제 2 단계에서 제조되는 물질은 하기 화학식들로 나타낼 수 있다.Accordingly, the material prepared in the second step may be represented by the following formula.
마지막으로 제 3 단계는, 상기 제 2 단계 완료 후, 다가산과 다가 알코올을 혼합하여 반응시킴으로써 에스테르 폴리올을 합성하는 단계이다.Finally, in the third step, after the completion of the second step, a polyhydric acid and a polyhydric alcohol are mixed and reacted to synthesize an ester polyol.
상세하게는 제 3 단계는, 상기 2 단계 반응 완료된 인과 멜라민을 함유한 폴리올 10~30 wt%와, 다가산 20~60 wt% 및 다가 알코올 30~70wt%를 혼합하여 130 ~ 230℃의 온도에서, 산촉매 존재 하에서 5~20% 의 톨루엔을 물의 공비제로 사용하여 반응수를 제거하며 유수분리관을 장착하여 물만을 분리하며 합성하는 단계이다.Specifically, in the third step, 10-30 wt% of the polyol containing phosphorus and melamine, which have been completed in the two-step reaction, 20-60 wt% of polyhydric acid and 30-70wt% of polyhydric alcohol are mixed at a temperature of 130-230 ° C In the presence of acid catalyst, 5 ~ 20% of toluene is used as an azeotropic agent of water to remove the reaction water, and the oil and water separation tube is installed to separate and synthesize only water.
산촉매는 에스테르 반응에 유리하나 강한 무기산의 경우 부식의 위험이 있으므로 유기성분을 함유하고 Toluene 에 잘 섞이는 sulfonate 계열의 유기촉매가 바람직하다. Acid catalysts are preferred for ester reactions, but strong inorganic acids are susceptible to corrosion. Therefore, sulfonate-based organic catalysts containing organic components and well mixed with toluene are preferred.
이때, 상기 제 3 단계에서 반응 온도를 130 ~ 230℃로 하는 것은 130℃ 미만에서는 반응시간이 길어지는 문제가 발생하고 230℃를 초과할 경우에는 제조된 폴리올의 변색 및 점도 상승의 문제가 발생할 수 있기 때문이다.At this time, the reaction temperature in the third step to 130 ~ 230 ℃ may cause a problem that the reaction time is longer than 130 ℃ and above 230 ℃ may cause problems of discoloration and viscosity increase of the prepared polyol Because there is.
또한, 이때, 상기 다가산은 프탈산무수물, 테레프탈산, 아디프산, 나프탈렌산, 디메틸프탈레이트, 세바식산 또는 이들의 혼합물인 것을 특징으로 하며, 바람직하게는 상기 다가산은 프탈산인 것을 특징으로 한다.In this case, the polyacid is characterized in that phthalic anhydride, terephthalic acid, adipic acid, naphthalic acid, dimethyl phthalate, sebacic acid or a mixture thereof, preferably the polyacid is phthalic acid.
또한, 상기 다가 알코올은 에틸렌글라이콜, 디에틸렌글라이콜, 트리에틸렌글라이콜, 프로필렌글라이콜, 부탄디올, 네오펜틸렌글리콜, 사이클로헥산디올, 글리세롤 펜타에리트리톨, 솔비톨 또는 이들의 혼합물인 것을 특징으로 한다.In addition, the polyhydric alcohol is ethylene glycol, diethylene glycol, triethylene glycol, propylene glycol, butanediol, neopentylene glycol, cyclohexanediol, glycerol pentaerythritol, sorbitol or a mixture thereof It is characterized by.
또한, 상기 에스테르 폴리올 제조 시 사용되는 촉매로는 마그네슘 또는 칼슘아세테이트, 알칼리토금속의 알콕사이드, 파라톨루엔술폰산, 도데실벤젠술폰산, 디옥틸주석산 및 이들의 혼합물인 것을 특징으로 하며, 바람직하게는 파라톨루엔술폰산인 것을 특징으로 한다.In addition, the catalyst used in the preparation of the ester polyol is characterized in that magnesium or calcium acetate, alkoxide of alkaline earth metal, paratoluenesulfonic acid, dodecylbenzenesulfonic acid, dioctyltinic acid and mixtures thereof, preferably paratoluenesulfonic acid It is characterized by that.
이에, 상기 제 3 단계에서 합성된 난연성 에스테르 폴리올은 하기 화학식들로 나타낼 수 있으나, 이에 한정되는 것은 아니다.Thus, the flame retardant ester polyol synthesized in the third step may be represented by the following formula, but is not limited thereto.
본 발명의 또 다른 일 측면에 따르면, 상기 난연성 에스테르 폴리올을 포함하여 제조되는 것을 특징으로 하는, 난연성 폴리이소시아누레이트(polyisocyanurate)를 제공한다.According to yet another aspect of the present invention, a flame retardant polyisocyanurate is provided, comprising the flame retardant ester polyol.
상기 본 발명에 의해 제조되어지는 에스테르 폴리올을 포함하여 제조되는 폴리이소시아누레이트는 폴리올 내에 멜라민 및 인이 화학적으로 결합되어 포함됨에 따라, 별도의 난연제 추가 없이도 우수한 난연성을 가짐은 물론이고, 관능기 조절이 용이하여 적절한 물성의 폼을 형성할 수 있는 것을 특징으로 한다.The polyisocyanurate prepared by using the ester polyol prepared by the present invention is because the melamine and phosphorus are chemically bonded in the polyol, as well as having excellent flame retardancy without the addition of a flame retardant, functional group control is It is easy to form a foam of suitable physical properties.
또한, 상기 본 발명의 난연성 에스테르 폴리올을 포함하여 난연성 폴리이소시아누레이트를 제조할 시, 제조되는 제품에 요구되는 물리적 특성에 따라 다른 상용의 폴리올과 혼합될 수 있으며, 바이오 및 재생 폴리올과도 혼합될 수 있는 것을 특징으로 한다.In addition, when preparing a flame retardant polyisocyanurate including the flame retardant ester polyol of the present invention, it may be mixed with other commercially available polyols according to the physical properties required for the manufactured product, and may also be mixed with bio and recycled polyols. Characterized in that it can.
상세하게는 본 발명의 난연성 에스테르 폴리올을 포함하여 제조되는 난연성 폴리이소시아누레이트는, 상기 본 발명의 난연성 에스테르 폴리올 100중량부에 대해, 반응촉매 0.5 ~ 3.0중량부, 삼량화 촉매 0.5 ~ 3.0중량부, 실리콘 정포제 0.5 ~ 3.0중량부, 물 0 ~ 3중량부 및 발포제 1 ~ 20중량부를 상기 난연성 폴리올 100중량부에 첨가하여 폴리올 혼합물을 제조한 후, 이를 다가 이소시아네이트 100~200 중량부와 반응시킴으로써 제조되는 것을 특징으로 한다.Specifically, the flame retardant polyisocyanurate prepared by using the flame retardant ester polyol of the present invention is 0.5 to 3.0 parts by weight of the reaction catalyst and 0.5 to 3.0 parts by weight of the trimerization catalyst with respect to 100 parts by weight of the flame retardant ester polyol of the present invention. 0.5 to 3.0 parts by weight of a silicone foam stabilizer, 0 to 3 parts by weight of water and 1 to 20 parts by weight of a blowing agent were added to 100 parts by weight of the flame retardant polyol to prepare a polyol mixture, and then reacted with 100 to 200 parts by weight of polyvalent isocyanate. It is characterized by being manufactured.
이소시아누레이트는 열적으로 매우 안정한 상태로 280℃ 이상에서 분해가 일어나는 화학적 구조이다. 이 구조는 과량의 다가 이소시아네이트를 사용할 경우, 다가 이소시아네이트가 삼량화 되어 이루어지는 구조로써 삼량화 촉매하에서 생성된다. 이렇게 만들어진 이소시아누레이트는 폴리올과 반응하여 폴리이소시아누레이트 구조를 이루게 된다.Isocyanurate is a chemical structure that degrades above 280 ° C in a thermally stable state. When the excess polyisocyanate is used, this structure is a structure in which the polyvalent isocyanate is trimerized and is produced under the trimerization catalyst. The isocyanurate thus produced reacts with the polyol to form a polyisocyanurate structure.
이때 상기 다가 이소시아네이트는 1.5 ~ 3의 관능기를 갖는 모노머 또는 폴리머 이소시아네이트이고, 인덱스(INDEX)는 100 ~ 300 사이에서 조절되는 것이 바람직하다.At this time, the polyisocyanate is a monomer or a polymer isocyanate having a functional group of 1.5 to 3, the index (INDEX) is preferably adjusted between 100 to 300.
또한, 상기 발포촉매는 통상의 것으로써 유기금속계열이나 아민 계열의 물질이 사용될 수 있다. 유기금속계열은 주로 유기주석촉매가 사용될 수 있고, 아민계열 촉매로는 TEDA, Polycat 8, DMEA, Polycat 5 등이 사용될 수 있으며 이에 한정되는 것은 아니다.In addition, the foaming catalyst may be a conventional organometallic or amine-based material. The organometallic series may be mainly an organic tin catalyst, and as the amine catalyst, TEDA, Polycat 8, DMEA, or Polycat 5 may be used, but is not limited thereto.
또한, 상기 발포제로는 물이나 용제 발포제가 사용되며, 용제 발포제는 141b, cyclo-pentane, methylene chloride 등이 있으나 이에 한정되지 않는다.In addition, water or a solvent blowing agent is used as the blowing agent, and solvent blowing agents include, but are not limited to, 141b, cyclo-pentane, methylene chloride, and the like.
또한, 상기 정포제는 실리콘 성분으로 제조되는 폴리이소시아누레이트의 적용분야에 따라 분자량 300~80000까지 다양한 농도로 적용할 수 있다.In addition, the foam stabilizer can be applied in various concentrations up to molecular weight 300 ~ 80000 depending on the application of the polyisocyanurate prepared from the silicone component.
이하, 본 발명을 실시예에 의하여 더욱 상세히 설명하나, 본 발명의 범위가 실시예에 의해 제한되는 것은 아니다.Hereinafter, the present invention will be described in more detail with reference to Examples, but the scope of the present invention is not limited by Examples.
<실시예><Example>
1. 에스테르 폴리올 제조1. Ester Polyol Manufacturing
<제조예 1> 2-메틸아미노에탄올과 디메틸 포스파이트가 화학결합된 멜라민 및 인을 포함하는 에스테르 폴리올 제조Preparation Example 1 Preparation of Ester Polyols Containing Melamine and Phosphorus Chemically Bonded with 2-Methylaminoethanol and Dimethyl Phosphite
멜라민 1몰인 126g과 포름알데히드 35% 수용액 3몰인 257g을 히팅 및 냉각이 가능한 반응기에 투입한 후 천천히 50℃로 승온한 후, 온도를 유지하며 추가로 1시간 동안 반응시켜 투명한 트리메틸올멜라민을 합성하였다.1 mol of melamine and 257 g of 3 mol of formaldehyde 35% aqueous solution were added to a reactor capable of heating and cooling, and then slowly heated up to 50 ° C., and then reacted for 1 hour while maintaining the temperature to synthesize transparent trimethylolmelamine. .
이 후 히팅 장치를 끄고 20℃로 냉각한 후 교반하면서 메틸모노알칸올아민(methyl monoalkanolamine)의 한 종류인 2-메틸아미노에탄올 2.5몰인 187.78g 투입하였다. 이때의 반응은 발열반응이므로, 냉각 장치를 가동하며 천천히 5회로 나눠 상기 2-메틸아미노에탄올을 투입하였다. Thereafter, the heating device was turned off and cooled to 20 ° C., followed by stirring, and 187.78 g of 2.5 mol of 2-methylaminoethanol, which is a type of methyl monoalkanolamine, was added thereto. At this time, since the reaction was exothermic, the 2-methylaminoethanol was added slowly by dividing five times while operating the cooling device.
다음으로 디메틸 포스파이트(dimethyl phosphite) 0.5몰인 55g을 천천히 3회 나누어 투입하였다. 이때의 반응도 발열반응이므로, 냉각 장치를 가동하였다. 이후, 50℃에서 추가로 2시간 반응시킨 다음, 이어서 온도를 70℃로 천천히 승온한 후 감압장치로 압력을 낮추어 물을 제거하였다. 이에 따라 회수된 폴리올의 구조는 화학식 6과 같다.Next, 55 g, which is 0.5 mol of dimethyl phosphite, was slowly divided into three portions. Since the reaction at this time was also an exothermic reaction, the cooling device was operated. Thereafter, the mixture was further reacted at 50 ° C. for 2 hours, and then the temperature was slowly increased to 70 ° C., followed by lowering the pressure with a pressure reducing device to remove water. Accordingly, the structure of the recovered polyol is represented by the formula (6).
[화학식 6][Formula 6]
이어서 상기 합성된 인과 멜라민이 함유된 폴리올 60g과, 무수프탈산 150g 및 디에틸렌글라이콜 200g을 혼합한 후 p-톨루엔 설폰산(para toluene sulfonic acid) 0.2g 와 톨루엔 50g을 투입하여 딘스탁이 설치된 1리터 반응기에서 150℃로 승온시켜 26시간 동안 탈수 반응 진행하였다. Subsequently, 60 g of the synthesized phosphorus and melamine-containing polyol, 150 g of phthalic anhydride and 200 g of diethylene glycol were mixed, and 0.2 g of p-toluene sulfonic acid and 50 g of toluene were added thereto, and Deanstock was installed. In a 1 liter reactor, the temperature was raised to 150 ° C., followed by dehydration for 26 hours.
최종적으로 합성된 난연성 에스테르 폴리올은의 산가는 1.5 이었으며, 측정된 수산기 값은 305 이었으며, 점도는 14,000 cps이었다. 또한, 상기 합성된 에스테르 폴리올은 하기 화학식 7로 표시된다.Finally, the synthesized flame retardant ester polyol had an acid value of 1.5, a measured hydroxyl value of 305, and a viscosity of 14,000 cps. In addition, the synthesized ester polyol is represented by the following formula (7).
[화학식 7][Formula 7]
<제조예 2> 디에탄올아민과 디메틸 포스파이트가 화학결합된 멜라민 및 인을 포함하는 에스테르 폴리올 제조Preparation Example 2 Preparation of Ester Polyols Containing Melamine and Phosphorus Chemically Bonded to Ethanolamine and Dimethyl Phosphite
멜라민 1몰인 126g과 포름알데히드 35% 수용액 3몰인 257g을 히팅 및 냉각이 가능한 반응기에 투입한 후 천천히 50℃ 로 승온한 후 온도를 유지하며 추가로 1시간 동안 반응시켜 투명한 트리메틸올멜라민을 합성하였다. 126 g of melamine and 257 g of 3 mol of formaldehyde 35% aqueous solution were added to a reactor capable of heating and cooling, and then slowly heated up to 50 ° C. and maintained at a temperature for 1 hour to synthesize transparent trimethylolmelamine.
이 후 히팅장치를 끄고 20℃로 냉각한 후 교반하면서 디알칸올아민(dialkanolamine)의 한 종류인 디에탄올아민 2몰인 210g 을 투입하였다. 이때의 반응은 발열반응이므로, 냉각 장치를 가동하며 상기 디에탄올아민을 천천히 5회로 나누어 투입하였다. 이어서 디메틸 포스파이트(dimethyl phosphite) 1몰인 110g을 천천히 5회로 나누어 투입하였다. 이때의 반응도 발열반응이므로, 냉각 장치를 가동하였다. 이후 50℃에서 추가로 2시간 반응시킨 후 이어서 온도를 70℃ 로 천천히 승온한 다음 감압장치로 압력을 낮추어 물을 제거하였다. 이에 따라 회수된 폴리올의 구조는 화학식 8과 같다.Thereafter, the heating device was turned off and cooled to 20 ° C., followed by stirring, and 210 g of 2 mol of diethanolamine, which is a type of dialkanolamine, was added thereto. Since the reaction at this time was an exothermic reaction, the diethanolamine was slowly divided into five portions while the cooling device was operated. Subsequently, 110 g of 1 mole of dimethyl phosphite was slowly divided into 5 portions. Since the reaction at this time was also an exothermic reaction, the cooling device was operated. After further reacting at 50 ° C. for 2 hours, the temperature was then slowly increased to 70 ° C., and then the pressure was reduced by a pressure reducing device to remove water. Accordingly, the structure of the recovered polyol is represented by the formula (8).
[화학식 8][Formula 8]
이어서 상기 합성된 인과 멜라민이 함유된 폴리올 55g과, 무수프탈산 150g 및 디에틸렌글라이콜 205g을 혼합한 후 p-톨루엔 설폰산(para toluene sulfonic acid) 0.2g 와 톨루엔 50g을 투입하여 딘스탁이 설치된 1리터 반응기에서 150℃로 승온시켜 30시간 동안 탈수 반응 진행하였다. Subsequently, 55 g of the synthesized polyol containing phosphorus and melamine, 150 g of phthalic anhydride and 205 g of diethylene glycol were mixed, and 0.2 g of p-toluene sulfonic acid and 50 g of toluene were added thereto, and Deanstock was installed. In a 1 liter reactor, the temperature was raised to 150 ° C. and the dehydration reaction proceeded for 30 hours.
최종적으로 합성된 난연성 에스테르 폴리올은의 산가는 1.3 이었으며, 측정된 수산기값은 300 이었으며, 점도는 16,000 cps이었다. 또한, 상기 합성된 에스테르 폴리올은 하기 화학식 9로 표시된다.Finally, the synthesized flame retardant ester polyol had an acid value of 1.3, a measured hydroxyl value of 300, and a viscosity of 16,000 cps. In addition, the synthesized ester polyol is represented by the following formula (9).
[화학식 9][Formula 9]
2. 폴리이소시아누레이트 폼 제조 및 난연성 시험2. Polyisocyanurate foam manufacturing and flame retardancy test
상기 제조예 1 또는 제조예 2에서 합성한 멜라민 및 인을 포함하는 에스테르 폴리올로 폴리이소시아누레이트 폼을 제조하여, 상기 폴리이소시아누레이트 폼의 난연성을 시험하였다. A polyisocyanurate foam was prepared from an ester polyol comprising melamine and phosphorus synthesized in Preparation Example 1 or Preparation Example 2, and the flame retardancy of the polyisocyanurate foam was tested.
이때 비교예로서, 시판되는 AKPOL-7001 폴리올 및 난연제를 포함한 AKPOL-7001 폴리올로 각각 폴리이소시아누레이트 폼을 제조하여 난연성을 시험하였다.At this time, as a comparative example, polyisocyanurate foams were prepared from commercially available AKPOL-7001 polyols and flame retardants to test flame retardancy.
<실시예 1> 제조예 1의 에스테르 폴리올에 의한 폴리이소시아누레이트 폼 생성 및 난연성 시험<Example 1> Polyisocyanurate foam production and flame retardancy test by ester polyol of Preparation Example 1
상기 제조예 1에서 합성한 멜라민 및 인을 포함하는 에스테르 폴리올 100 중량부에 촉매(K15) 1.5 중량부, 실리콘계 정포제 3 중량부 및 발포제(cyclopentane) 20 중량부를 혼합하여, 추가되는 난연제 성분 없이 혼합된 폴리올을 생성하였다. 상기 혼합된 폴리올에 INDEX 250으로 조정된 이소시아네이트를 반응시킴으로써, 폴리이소시아누레이트 폼을 제조하였다.1.5 parts by weight of catalyst (K15), 3 parts by weight of a silicon foam stabilizer and 20 parts by weight of a blowing agent (cyclopentane) were mixed with 100 parts by weight of the ester polyol including melamine and phosphorus synthesized in Preparation Example 1, and mixed without an additional flame retardant component. Resulting polyols. A polyisocyanurate foam was prepared by reacting the mixed polyol with an isocyanate adjusted to INDEX 250.
이후, 22cmㅧ22cmㅧ5cm 몰드에 0.5㎜ 두께의 철판을 놓고 상기 제조된 폴리이소시아누레이트 폼을 발포하고, 상기 폴리이소시아누레이트 폼이 발포된 상부에 철판을 덮어 난연성 시험을 위한 시험샘플을 제작하였으며, 상기 제작된 시험샘플은 KSF-2271에 의해 난연성 테스트를 실시하였다.Thereafter, a 0.5 mm thick iron plate was placed in a 22 cm x 22 cm x 5 cm mold, and the polyisocyanurate foam was foamed, and the test plate for flame retardancy test was prepared by covering the iron plate on the foamed polyisocyanurate foam. The prepared test sample was subjected to a flame retardancy test by KSF-2271.
<실시예 2> 제조예 2의 에스테르 폴리올에 의한 폴리이소시아누레이트 폼 생성 및 난연성 시험Example 2 Polyisocyanurate Foam Formation and Flame Retardancy Test by Ester Polyol of Preparation Example 2
폴리올로서, 상기 제조예 2의 에스테르 폴리올을 사용한 것을 제외하고는 상기 실시예 1과 동일한 방법으로 폴리이소시아누레이트 폼을 제조 및 난연성 테스트를 실시하였다.As a polyol, except that the ester polyol of Preparation Example 2 was used, a polyisocyanurate foam was prepared in the same manner as in Example 1 and subjected to a flame retardancy test.
<비교예 1> AKPOL-7001(폴리에스테르 폴리올)에 의한 폴리이소시아누레이트 폼 생성 및 난연성 시험Comparative Example 1 Polyisocyanurate Foam Formation and Flame Retardancy Test by AKPOL-7001 (Polyester Polyol)
폴리올로서, 시중에 판매되고 있는 폴리에스테르 폴리올 AKPOL-7001 제품을 사용한 것을 제외하고는 상기 실시예 1과 동일한 방법으로 폴리이소시아누레이트 폼을 제조 및 난연성 테스트를 실시하였다.As a polyol, a polyisocyanurate foam was prepared and flame-retardantly tested in the same manner as in Example 1 except that a commercially available polyester polyol AKPOL-7001 was used.
<비교예 2> 난연제가 포함된 AKPOL-7001(폴리에스테르 폴리올)에 의한 폴리이소시아누레이트 폼 생성 및 난연성 시험Comparative Example 2 Polyisocyanurate Foam Formation and Flame Retardancy Test by AKPOL-7001 (Polyester Polyol) with Flame Retardant
폴리올로서, 시중에 판매되고 있는 폴리에스테르 폴리올 AKPOL-7001 제품을 사용하고, 난연제로서 TCPP 20 중량부를 첨가한 것을 제외하고는 상기 실시예 1과 동일한 방법으로 폴리이소시아누레이트 폼을 제조 및 난연성 테스트를 실시하였다.As a polyol, a polyisocyanurate foam was prepared and flame-retardant test was carried out in the same manner as in Example 1 except that a commercially available polyester polyol AKPOL-7001 was used and 20 parts by weight of TCPP was added as a flame retardant. Was carried out.
하기 표 1은 상기 실시예 1, 실시예 2, 비교예 1 및 비교예 2에 의해 실시한 난연성 시험 결과를 나타낸 것이다.Table 1 below shows the results of flame retardancy test performed by Example 1, Example 2, Comparative Example 1 and Comparative Example 2.
상기 표 1을 참고하면, 별도의 난연제를 첨가하지 않은 실시예 1 및 실시예 2의 폴리이소시아누레이트 폼은 화학결합된 멜라민 및 인을 포함하는 에스테르 폴리올에 의해 제조됨에 따라 난연성을 갖는 것을 확인할 수 있다.Referring to Table 1, it is confirmed that the polyisocyanurate foam of Examples 1 and 2 without the addition of a separate flame retardant is flame-retardant as it is prepared by the ester polyol containing chemically bonded melamine and phosphorus have.
반면에, 비교예 1 및 비교예 2의 경우는 난연제를 첨가한 비교예 2에서만 난연성이 나타남에 따라, 비교예 1 및 2의 경우는 난연성을 갖기 위해서는 폴리에스테르 폴리올에 별도로 난연제를 첨가하여야 함을 알 수 있다.On the other hand, in Comparative Examples 1 and 2, since the flame retardancy is shown only in Comparative Example 2 to which the flame retardant is added, in the case of Comparative Examples 1 and 2, the flame retardant must be added to the polyester polyol separately in order to have flame retardancy. Able to know.
상기 결과로부터, 화학적으로 결합된 난연성을 갖는 멜라민 및 인을 포함하는 에스테르 폴리올의 경우, 별도의 난연제 첨가 없이도 난연성을 가짐은 물론이고, 이를 포함하여 제조되는 폴리이소시아누레이트 폼 역시 난연성을 갖게 됨을 확인하였다.From the above results, in the case of the ester polyol containing melamine and phosphorus having chemically bonded flame retardancy, it is confirmed that the polyisocyanurate foam prepared as well as having flame retardancy without the addition of a separate flame retardant also has flame retardancy. It was.
이상과 같이, 본 발명은 비록 한정된 실시예에 의해 설명되었으나, 본 발명은 이것에 의해 한정되지 않으며 본 발명이 속하는 기술분야에서 통상의 지식을 가진 자에 의해 본 발명의 기술사상과 아래에 기재될 특허범위의 균등 범위에서 다양한 수정 및 변형이 가능함은 물론이다.As described above, although the present invention has been described by means of a limited embodiment, the present invention is not limited thereto and will be described below by the person skilled in the art and the technical spirit of the present invention. Various modifications and variations are possible within the scope of the patent.
Claims (8)
[화학식 1]
상기 화학식 1에 있어서, R1은 하기 화학식 2이고,
R2는 하기 화학식 3이며,
R3는 수소, -CH2OH, -CH2CH2OH, C1-C10 알킬, C2-C10 알케닐, 치환 또는 비치환된 C1-C10 히드록시알킬, C1-C10 아미노알킬, C1-C10 알콕시, (C1-C10)알콕시(C1-C10)알킬, 히드록시(C1-C10)알킬옥시(C1-C10)알킬, C1-C10 알킬아미노, 아미노(C1-C10)알킬옥시(C1-C10)알킬 또는 히드록시(C1-C10)알킬아미노(C1-C10)알킬이고,
R4는 C1-C10 알킬렌, 치환 또는 비치환된 C1-C10 히드록시알킬렌, (C1-C10)알콕시(C1-C10)알킬렌 또는 히드록시(C1-C10)알킬옥시(C1-C10)알킬렌이며,
R5는 C6~C18 아릴렌, C1-C10 알킬렌, 페닐(C1-C10)알킬렌, (C1-C10 알킬)페닐렌이고,
R6는 C1-C10 알킬렌, (C1~C20)알콕시(C1~C20)알킬렌, 히드록시(C1-C10)알킬옥시(C1-C10)알킬렌 또는 C1-C20 히드록시알킬렌인 것을 특징으로 한다.
[화학식 2]
(상기 R7은 치환 또는 무치환의 C1-C 20 알킬, 치환 또는 무치환의 C1-C20 헤테로 알킬, 치환 또는 무치환의 C3-C20 사이클로알킬, 및 치환 또는 무치환의 C7-C30 아릴알킬 중에서 선택되는 어느 하나이다.)
[화학식 3]
(상기 R8 및 R9는 각각 독립적으로 수소, CH2OH, -CH2CH2OH, C1-C10 알킬, C2-C10 알케닐, 아미노, 치환 또는 비치환된 C1-C10 히드록시알킬, C1-C10 아미노알킬, C1-C10 알콕시, (C1-C10)알콕시(C1-C10)알킬, 히드록시(C1-C10)알킬옥시(C1-C10)알킬, C1-C10 알킬아미노, 아미노(C1-C10)알킬옥시(C1-C10)알킬 또는 히드록시(C1-C10)알킬아미노(C1-C10)알킬이고, 상기 R8 및 R9 중 적어도 어느 하나는 치환 또는 비치환된 C1-C10 히드록시알킬이다.)Flame retardant ester polyol, characterized in that represented by the following formula (1):
[Formula 1]
In Chemical Formula 1, R 1 is the following Chemical Formula 2,
R 2 is the following Chemical Formula 3,
R 3 is hydrogen, —CH 2 OH, —CH 2 CH 2 OH, C 1 -C 10 alkyl, C 2 -C 10 alkenyl, substituted or unsubstituted C 1 -C 10 hydroxyalkyl, C 1 -C 10 aminoalkyl, C 1 -C 10 alkoxy, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkyl, hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl, C 1 -C 10 alkylamino, amino (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl or hydroxy (C 1 -C 10 ) alkylamino (C 1 -C 10 ) alkyl,
R 4 is C 1 -C 10 alkylene, substituted or unsubstituted C 1 -C 10 hydroxyalkylene, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkylene or hydroxy (C 1- C 10 ) alkyloxy (C 1 -C 10 ) alkylene,
R 5 is C 6 -C 18 arylene, C 1 -C 10 alkylene, phenyl (C 1 -C 10 ) alkylene, (C 1 -C 10 alkyl) phenylene,
R 6 is C 1 -C 10 alkylene, (C 1 -C 20 ) alkoxy (C 1 -C 20 ) alkylene, hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkylene or C 1 -C 20 hydroxyalkylene.
[Formula 2]
(Wherein R 7 is substituted or unsubstituted C 1 -C 20 alkyl, substituted or unsubstituted C 1 -C 20 heteroalkyl, substituted or unsubstituted C 3 -C 20 cycloalkyl, and substituted or unsubstituted C 7 -C 30 arylalkyl.)
[Formula 3]
R 8 and R 9 are each independently hydrogen, CH 2 OH, —CH 2 CH 2 OH, C 1 -C 10 alkyl, C 2 -C 10 alkenyl, amino, substituted or unsubstituted C 1 -C 10 hydroxyalkyl, C 1 -C 10 aminoalkyl, C 1 -C 10 alkoxy, (C 1 -C 10 ) alkoxy (C 1 -C 10 ) alkyl, hydroxy (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl, C 1 -C 10 alkylamino, amino (C 1 -C 10 ) alkyloxy (C 1 -C 10 ) alkyl or hydroxy (C 1 -C 10 ) alkylamino (C 1 -C and 10) alkyl, wherein R 8 and R 9 at least one of a substituted or unsubstituted C 1 -C 10 hydroxyalkyl.)
상기 합성된 트리메틸올멜라민에 알칸올 아민 및 디알킬포스파이트를 첨가하여 중합시킨 다음, 물을 제거하는 제 2 단계; 및
상기 제 2 단계 완료 후, 다가산 및 다가 알코올을 첨가하여 혼합 및 반응시킴으로써 에스테르 폴리올을 합성하는 제 3 단계;를 포함하여 난연성 에스테르 폴리올을 제조하는 것을 특징으로 하는, 난연성 에스테르 폴리올의 제조방법.A first step of synthesizing trimethylolmelamine by reacting melamine and formaldehyde at 40 to 60 ° C;
A second step of polymerization by adding alkanol amine and dialkyl phosphite to the synthesized trimethylolmelamine and then removing water; And
After the completion of the second step, a third step of synthesizing the ester polyol by mixing and reacting by adding a polyacid and a polyhydric alcohol; comprising a flame-retardant ester polyol, characterized in that for producing a flame retardant ester polyol.
상기 제 2 단계에서, 트리메틸올멜라민 1 몰에 대해 알칸올 아민은 2 ~ 2.5몰 첨가되고, 트리메틸올멜라민 1몰에 대해 디알킬포스파이트는 0.5 ~ 1몰이 첨가되는 것을 특징으로 하는, 난연성 에스테르 폴리올의 제조방법.The method of claim 4, wherein
In the second step, 2 to 2.5 moles of alkanol amine is added to 1 mole of trimethylolmelamine, and 0.5 to 1 mole of dialkyl phosphite is added to 1 mole of trimethylolmelamine, flame retardant ester polyol Manufacturing method.
상기 다가산은 프탈산무수물, 테레프탈산, 아디프산, 나프탈렌산, 디메틸프탈레이트, 세바식산 또는 이들의 혼합물인 것을 특징으로 하는, 난연성 에스테르 폴리올의 제조방법.The method of claim 4, wherein
The polyacid is phthalic anhydride, terephthalic acid, adipic acid, naphthalic acid, dimethyl phthalate, sebacic acid or a mixture thereof, characterized in that the method for producing a flame retardant ester polyol.
상기 합성된 에스테르 폴리올은 제 1 항에 따른 폴리올인 것을 특징으로 하는, 난연성 에스테르 폴리올의 제조방법.The method of claim 4, wherein
The synthesized ester polyol is characterized in that the polyol according to claim 1, the method for producing a flame retardant ester polyol.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020170077877A KR102054675B1 (en) | 2017-06-20 | 2017-06-20 | flame-retardant ester polyol, the manufacturing method thereof and polyisocyanurates including the anti-flame ester polyol |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020170077877A KR102054675B1 (en) | 2017-06-20 | 2017-06-20 | flame-retardant ester polyol, the manufacturing method thereof and polyisocyanurates including the anti-flame ester polyol |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20180137938A KR20180137938A (en) | 2018-12-28 |
| KR102054675B1 true KR102054675B1 (en) | 2019-12-11 |
Family
ID=65008433
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020170077877A KR102054675B1 (en) | 2017-06-20 | 2017-06-20 | flame-retardant ester polyol, the manufacturing method thereof and polyisocyanurates including the anti-flame ester polyol |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102054675B1 (en) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115677963A (en) * | 2021-07-23 | 2023-02-03 | 江苏长顺高分子材料研究院有限公司 | High flame-retardant rigid polyurethane foam and preparation method thereof |
| CN114409606A (en) * | 2022-01-29 | 2022-04-29 | 浙江恒丰新材料有限公司 | Synthesis method of melamine-diethanolamine-phthalic anhydride copolymer polyether polyol |
| CN116874715A (en) * | 2022-09-23 | 2023-10-13 | 江苏长顺高分子材料研究院有限公司 | Flame-retardant melamine hard foam and preparation method thereof |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3498969A (en) | 1967-10-11 | 1970-03-03 | Swift & Co | Phosphonate amine polyol compounds and a process for preparing same |
| US20140011715A1 (en) | 2012-07-03 | 2014-01-09 | Basf Se | Corrosion inhibitors |
| CN104311876A (en) | 2014-11-07 | 2015-01-28 | 东北林业大学 | Polymerization type phosphorus-containing flame retardant as well as preparation method and application thereof as epoxy resin flame retardant |
| CN104975497A (en) | 2015-06-30 | 2015-10-14 | 西南大学 | Flame retardant, preparation method and applications thereof |
| CN105199096A (en) | 2015-11-11 | 2015-12-30 | 江苏钟山化工有限公司 | Preparation and application of nitrogen and phosphorus structured flame-retardant polyether polyol |
| CN104693770B (en) | 2015-02-27 | 2016-05-11 | 鲁西化工集团股份有限公司 | A kind of halogen-free expansion type flame-proof polycarbonate composite material and preparation method thereof |
| CN106220682B (en) | 2016-07-20 | 2017-06-16 | 中国科学技术大学 | A kind of phosphorous nitrogenous flame-proof polyol and preparation method thereof |
| CN105293661B (en) | 2015-11-09 | 2017-11-10 | 淄博鲁瑞精细化工有限公司 | Without chlorion organic phosphine chelating agent and preparation method thereof |
| CN105712649B (en) | 2015-12-31 | 2018-06-26 | 江苏苏博特新材料股份有限公司 | A kind of phosphoric acid polycondensates high efficiency water reducing agent and preparation method thereof |
| KR101859184B1 (en) | 2016-08-31 | 2018-06-28 | (주)엔나노텍 | flame-retardant polyol, the manufacturing mothod thereof and polyurethan including the anti-flame property polyol |
| CN105949509B (en) | 2016-06-28 | 2018-07-17 | 武汉工程大学 | A kind of six methylenephosphonic acid magnesium fire retardant of hybrid inorganic-organic and preparation method thereof |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB919267A (en) * | 1958-07-15 | 1963-02-20 | Albright & Wilson Mfg Ltd | Improvements in or relating to the manufacture of substituted organic phosphine derivatives |
| DE3041731A1 (en) * | 1980-11-05 | 1982-06-09 | Bayer Ag, 5090 Leverkusen | If necessary, foamed intumescent materials and their use |
| DE3933549A1 (en) * | 1989-10-07 | 1991-04-11 | Bayer Ag | NEW AMINOMETHANPHOSPHONIC ACID ALTERES, METHOD FOR THE PRODUCTION THEREOF AND THEIR USE |
| DE3933546A1 (en) * | 1989-10-07 | 1991-04-11 | Bayer Ag | NEW AMINOMETHANPHOSPHONIC ACID ALTERES, METHOD FOR THE PRODUCTION THEREOF AND THEIR USE |
| KR100537135B1 (en) * | 2002-12-14 | 2005-12-16 | 금호미쓰이화학 주식회사 | Manufacturing method of the non -flammable polyurethane foam |
| KR100910258B1 (en) * | 2007-03-02 | 2009-07-31 | 에스케이씨 주식회사 | Reactive Flame Retardant Polyester polyol and its preparing method, and usage in Polyurethane |
| KR20080113741A (en) * | 2007-06-25 | 2008-12-31 | 김도균 | Polyol included phosphorus and nitrogen |
| DE102007035417A1 (en) * | 2007-07-28 | 2009-01-29 | Chemische Fabrik Budenheim Kg | Halogen-free flame retardant |
| AT513327B1 (en) * | 2012-08-29 | 2014-06-15 | Krems Chemie Chemical Services Ag | Process for the preparation of phosphorus-containing compounds |
| CN103665776A (en) * | 2012-09-06 | 2014-03-26 | 杜邦公司 | Flame-retardant copolymerized ether ester composition and article comprising same |
| JP6514769B2 (en) * | 2014-09-15 | 2019-05-15 | ケムチュア コーポレイション | Phosphorus-containing flame retardant |
-
2017
- 2017-06-20 KR KR1020170077877A patent/KR102054675B1/en active IP Right Grant
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3498969A (en) | 1967-10-11 | 1970-03-03 | Swift & Co | Phosphonate amine polyol compounds and a process for preparing same |
| US20140011715A1 (en) | 2012-07-03 | 2014-01-09 | Basf Se | Corrosion inhibitors |
| CN104311876A (en) | 2014-11-07 | 2015-01-28 | 东北林业大学 | Polymerization type phosphorus-containing flame retardant as well as preparation method and application thereof as epoxy resin flame retardant |
| CN104693770B (en) | 2015-02-27 | 2016-05-11 | 鲁西化工集团股份有限公司 | A kind of halogen-free expansion type flame-proof polycarbonate composite material and preparation method thereof |
| CN104975497A (en) | 2015-06-30 | 2015-10-14 | 西南大学 | Flame retardant, preparation method and applications thereof |
| CN105293661B (en) | 2015-11-09 | 2017-11-10 | 淄博鲁瑞精细化工有限公司 | Without chlorion organic phosphine chelating agent and preparation method thereof |
| CN105199096A (en) | 2015-11-11 | 2015-12-30 | 江苏钟山化工有限公司 | Preparation and application of nitrogen and phosphorus structured flame-retardant polyether polyol |
| CN105712649B (en) | 2015-12-31 | 2018-06-26 | 江苏苏博特新材料股份有限公司 | A kind of phosphoric acid polycondensates high efficiency water reducing agent and preparation method thereof |
| CN105949509B (en) | 2016-06-28 | 2018-07-17 | 武汉工程大学 | A kind of six methylenephosphonic acid magnesium fire retardant of hybrid inorganic-organic and preparation method thereof |
| CN106220682B (en) | 2016-07-20 | 2017-06-16 | 中国科学技术大学 | A kind of phosphorous nitrogenous flame-proof polyol and preparation method thereof |
| KR101859184B1 (en) | 2016-08-31 | 2018-06-28 | (주)엔나노텍 | flame-retardant polyol, the manufacturing mothod thereof and polyurethan including the anti-flame property polyol |
Non-Patent Citations (1)
| Title |
|---|
| CHEMIK 2013, 67, 4, 289_300 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20180137938A (en) | 2018-12-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101859184B1 (en) | flame-retardant polyol, the manufacturing mothod thereof and polyurethan including the anti-flame property polyol | |
| KR102054675B1 (en) | flame-retardant ester polyol, the manufacturing method thereof and polyisocyanurates including the anti-flame ester polyol | |
| CA2651377C (en) | Flame retardant composition | |
| CA2821152C (en) | Halogen-free poly(alkylene phosphates) | |
| JP7182601B2 (en) | Rigid polyurethane foam with reactive flame retardant | |
| DK167972B1 (en) | PROCEDURE FOR THE MANUFACTURE OF OIL EASTERS WITH HYDROXYL GROUPS, AND THE USE OF THESE FOR THE MANUFACTURING OF SUBSTANCES | |
| EP3303446B1 (en) | Flame retardant and auto-catalytic polyesters for polyurethanes | |
| CN104592470A (en) | Flame-retardant polyisocyanurate rigid foam and preparation method thereof | |
| US4094869A (en) | Thermally stable, rigid, cellular isocyanurate polyurethane foams | |
| KR20090039473A (en) | Polyesterpolyol and flame-retradant polyurethane using thereof | |
| RU2222550C2 (en) | Jointly initiated polyether-polyol and a method for preparation thereof | |
| KR100764968B1 (en) | Method of Preparing Polyurethane-Modified Polyisocyanurate Foam | |
| JP2007297627A (en) | Novel trimer catalyst having improved processability and surface hardening | |
| KR101797579B1 (en) | Method of producing Polyurethane Foam Board and Polyurethane Foam Pannel with Isocyanuric Polyol and Polyester Polyol | |
| KR101729205B1 (en) | Method of producing Polyester Polyol and Polyurethane Foam Board with the Same | |
| US3513113A (en) | Production of self-extinguishing polyurethanes | |
| JP4171999B2 (en) | Rigid polyurethane foam stock solution and rigid polyurethane foam | |
| EP2686373B1 (en) | Reactive flame retardants blends for flexible polyurethane foams | |
| KR20170104108A (en) | Method of producing Isocyanuric Polyol and Polyurethane Foam Board with the Same | |
| JP2003048943A (en) | Polyol composition for rigid polyurethane foam, rigid polyurethane foam and method for producing the same | |
| JP2020526613A (en) | Flame-retardant soundproofing heat material for internal combustion engines | |
| KR101900490B1 (en) | Method of polyester polyol excellent in mixing property with hydrocarbon blowing agent and flame retardancy | |
| JPH10168154A (en) | Production of flame retardant flexible polyurethane foam | |
| JPH1143526A (en) | Flame retardant composition for rigid polyurethane foam and its production, and flame retardant rigid polyurethane compounded therewith and its production | |
| KR100627221B1 (en) | Polyester polyol with Naphthalene Structure and the Manufacturing Process thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E90F | Notification of reason for final refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |