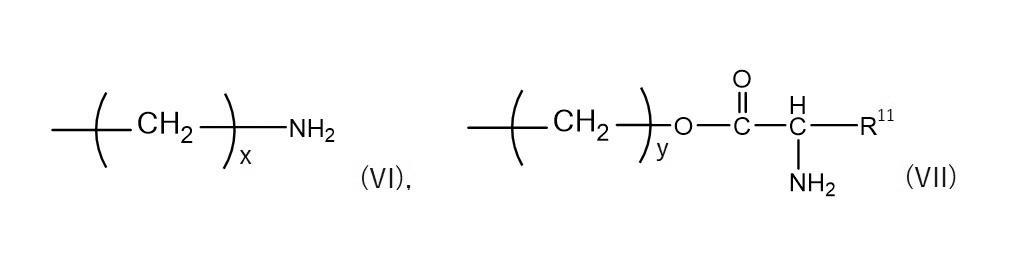JPWO2020116640A1 - 薬物複合体、ポリマー複合体及び薬物送達用組成物 - Google Patents
薬物複合体、ポリマー複合体及び薬物送達用組成物 Download PDFInfo
- Publication number
- JPWO2020116640A1 JPWO2020116640A1 JP2020560070A JP2020560070A JPWO2020116640A1 JP WO2020116640 A1 JPWO2020116640 A1 JP WO2020116640A1 JP 2020560070 A JP2020560070 A JP 2020560070A JP 2020560070 A JP2020560070 A JP 2020560070A JP WO2020116640 A1 JPWO2020116640 A1 JP WO2020116640A1
- Authority
- JP
- Japan
- Prior art keywords
- drug
- polymer
- group
- target
- complex
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 229940079593 drug Drugs 0.000 title claims abstract description 114
- 239000003814 drug Substances 0.000 title claims abstract description 114
- 229920000642 polymer Polymers 0.000 title claims description 131
- 238000012377 drug delivery Methods 0.000 title claims description 36
- 239000000203 mixture Substances 0.000 title claims description 25
- 210000004027 cell Anatomy 0.000 claims abstract description 58
- 238000000034 method Methods 0.000 claims abstract description 46
- 125000002525 phosphocholine group Chemical group OP(=O)(OCC[N+](C)(C)C)O* 0.000 claims abstract description 41
- 210000003470 mitochondria Anatomy 0.000 claims abstract description 31
- 239000000126 substance Substances 0.000 claims abstract description 13
- 239000000693 micelle Substances 0.000 claims description 63
- 150000001875 compounds Chemical class 0.000 claims description 45
- 239000002131 composite material Substances 0.000 claims description 17
- 229920001600 hydrophobic polymer Polymers 0.000 claims description 16
- 238000004519 manufacturing process Methods 0.000 claims description 16
- 239000002105 nanoparticle Substances 0.000 claims description 14
- 229920001477 hydrophilic polymer Polymers 0.000 claims description 12
- 239000003153 chemical reaction reagent Substances 0.000 claims description 10
- 239000002502 liposome Substances 0.000 claims description 10
- 238000001514 detection method Methods 0.000 claims description 9
- 238000002372 labelling Methods 0.000 claims description 9
- 229920000831 ionic polymer Polymers 0.000 claims description 6
- 230000002438 mitochondrial effect Effects 0.000 claims description 6
- 239000000499 gel Substances 0.000 claims description 4
- 150000002632 lipids Chemical class 0.000 claims description 4
- 239000002923 metal particle Substances 0.000 claims description 4
- 230000008685 targeting Effects 0.000 claims description 4
- 125000000524 functional group Chemical group 0.000 description 38
- 229920001400 block copolymer Polymers 0.000 description 30
- 235000001014 amino acid Nutrition 0.000 description 27
- 229940024606 amino acid Drugs 0.000 description 27
- 150000001413 amino acids Chemical class 0.000 description 26
- 239000000243 solution Substances 0.000 description 20
- 125000004432 carbon atom Chemical group C* 0.000 description 19
- 108010088751 Albumins Proteins 0.000 description 18
- 102000009027 Albumins Human genes 0.000 description 18
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 17
- 125000003277 amino group Chemical group 0.000 description 17
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 15
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 15
- 238000006243 chemical reaction Methods 0.000 description 15
- 229960002855 simvastatin Drugs 0.000 description 15
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 12
- -1 mRNA Chemical class 0.000 description 12
- 108020004999 messenger RNA Proteins 0.000 description 12
- 229920001223 polyethylene glycol Polymers 0.000 description 12
- 238000012360 testing method Methods 0.000 description 12
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 11
- 239000002253 acid Substances 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- 239000005090 green fluorescent protein Substances 0.000 description 11
- 239000000178 monomer Substances 0.000 description 11
- 238000005160 1H NMR spectroscopy Methods 0.000 description 10
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 10
- 238000002296 dynamic light scattering Methods 0.000 description 10
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 10
- 239000010931 gold Substances 0.000 description 10
- 229910052737 gold Inorganic materials 0.000 description 10
- 125000001165 hydrophobic group Chemical group 0.000 description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 10
- 239000002202 Polyethylene glycol Substances 0.000 description 9
- 125000000217 alkyl group Chemical group 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 230000002209 hydrophobic effect Effects 0.000 description 9
- 206010052747 Adenocarcinoma pancreas Diseases 0.000 description 8
- XLYOFNOQVPJJNP-ZSJDYOACSA-N Heavy water Chemical compound [2H]O[2H] XLYOFNOQVPJJNP-ZSJDYOACSA-N 0.000 description 8
- RYMZZMVNJRMUDD-UHFFFAOYSA-N SJ000286063 Natural products C12C(OC(=O)C(C)(C)CC)CC(C)C=C2C=CC(C)C1CCC1CC(O)CC(=O)O1 RYMZZMVNJRMUDD-UHFFFAOYSA-N 0.000 description 8
- 201000002094 pancreatic adenocarcinoma Diseases 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- 238000006116 polymerization reaction Methods 0.000 description 8
- RYMZZMVNJRMUDD-HGQWONQESA-N simvastatin Chemical compound C([C@H]1[C@@H](C)C=CC2=C[C@H](C)C[C@@H]([C@H]12)OC(=O)C(C)(C)CC)C[C@@H]1C[C@@H](O)CC(=O)O1 RYMZZMVNJRMUDD-HGQWONQESA-N 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- 229920003169 water-soluble polymer Polymers 0.000 description 8
- 125000002947 alkylene group Chemical group 0.000 description 7
- 125000000129 anionic group Chemical group 0.000 description 7
- 229920006318 anionic polymer Polymers 0.000 description 7
- 125000002091 cationic group Chemical group 0.000 description 7
- 229920006317 cationic polymer Polymers 0.000 description 7
- 125000005647 linker group Chemical group 0.000 description 7
- 125000003396 thiol group Chemical group [H]S* 0.000 description 7
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-Ethyl-3-(3-dimethylaminopropyl)carbodiimide Substances CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 6
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- 239000000969 carrier Substances 0.000 description 5
- 238000001218 confocal laser scanning microscopy Methods 0.000 description 5
- 230000009881 electrostatic interaction Effects 0.000 description 5
- 239000007850 fluorescent dye Substances 0.000 description 5
- DPBLXKKOBLCELK-UHFFFAOYSA-N n-pentylamine Natural products CCCCCN DPBLXKKOBLCELK-UHFFFAOYSA-N 0.000 description 5
- 238000012758 nuclear staining Methods 0.000 description 5
- 229920000223 polyglycerol Polymers 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 150000003141 primary amines Chemical class 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 4
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 4
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 4
- 239000004472 Lysine Substances 0.000 description 4
- 229920000954 Polyglycolide Polymers 0.000 description 4
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 4
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 4
- 235000003704 aspartic acid Nutrition 0.000 description 4
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 4
- 229920000249 biocompatible polymer Polymers 0.000 description 4
- HQABUPZFAYXKJW-UHFFFAOYSA-N butan-1-amine Chemical compound CCCCN HQABUPZFAYXKJW-UHFFFAOYSA-N 0.000 description 4
- 230000008045 co-localization Effects 0.000 description 4
- 238000000502 dialysis Methods 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 238000004108 freeze drying Methods 0.000 description 4
- 230000014509 gene expression Effects 0.000 description 4
- 235000013922 glutamic acid Nutrition 0.000 description 4
- 239000004220 glutamic acid Substances 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 230000003834 intracellular effect Effects 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 150000003904 phospholipids Chemical class 0.000 description 4
- 229920001308 poly(aminoacid) Polymers 0.000 description 4
- 239000004633 polyglycolic acid Substances 0.000 description 4
- 235000018102 proteins Nutrition 0.000 description 4
- 108090000623 proteins and genes Proteins 0.000 description 4
- 102000004169 proteins and genes Human genes 0.000 description 4
- 125000001424 substituent group Chemical group 0.000 description 4
- 229960002663 thioctic acid Drugs 0.000 description 4
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- WXWWYSORYNMCTE-UHFFFAOYSA-N C[N](C)(C)CCOP(OC)(OC)=O Chemical compound C[N](C)(C)CCOP(OC)(OC)=O WXWWYSORYNMCTE-UHFFFAOYSA-N 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 3
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 3
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 3
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 3
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 3
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 3
- 102000003867 Phospholipid Transfer Proteins Human genes 0.000 description 3
- 108090000216 Phospholipid Transfer Proteins Proteins 0.000 description 3
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 230000002860 competitive effect Effects 0.000 description 3
- 230000003013 cytotoxicity Effects 0.000 description 3
- 231100000135 cytotoxicity Toxicity 0.000 description 3
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 3
- 238000002338 electrophoretic light scattering Methods 0.000 description 3
- 150000004676 glycans Chemical class 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 239000003999 initiator Substances 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 108020004707 nucleic acids Proteins 0.000 description 3
- 102000039446 nucleic acids Human genes 0.000 description 3
- 150000007523 nucleic acids Chemical class 0.000 description 3
- 229960003104 ornithine Drugs 0.000 description 3
- 230000001766 physiological effect Effects 0.000 description 3
- 229920000570 polyether Polymers 0.000 description 3
- 229920001282 polysaccharide Polymers 0.000 description 3
- 239000005017 polysaccharide Substances 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- AGBQKNBQESQNJD-SSDOTTSWSA-N (R)-lipoic acid Chemical compound OC(=O)CCCC[C@@H]1CCSS1 AGBQKNBQESQNJD-SSDOTTSWSA-N 0.000 description 2
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 2
- 239000004475 Arginine Substances 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- 102100032373 Coiled-coil domain-containing protein 85B Human genes 0.000 description 2
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 2
- CYCGRDQQIOGCKX-UHFFFAOYSA-N Dehydro-luciferin Natural products OC(=O)C1=CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 CYCGRDQQIOGCKX-UHFFFAOYSA-N 0.000 description 2
- 239000004593 Epoxy Substances 0.000 description 2
- BJGNCJDXODQBOB-UHFFFAOYSA-N Fivefly Luciferin Natural products OC(=O)C1CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 BJGNCJDXODQBOB-UHFFFAOYSA-N 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000868814 Homo sapiens Coiled-coil domain-containing protein 85B Proteins 0.000 description 2
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 2
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 2
- 108060001084 Luciferase Proteins 0.000 description 2
- 239000005089 Luciferase Substances 0.000 description 2
- DDWFXDSYGUXRAY-UHFFFAOYSA-N Luciferin Natural products CCc1c(C)c(CC2NC(=O)C(=C2C=C)C)[nH]c1Cc3[nH]c4C(=C5/NC(CC(=O)O)C(C)C5CC(=O)O)CC(=O)c4c3C DDWFXDSYGUXRAY-UHFFFAOYSA-N 0.000 description 2
- NQTADLQHYWFPDB-UHFFFAOYSA-N N-Hydroxysuccinimide Chemical compound ON1C(=O)CCC1=O NQTADLQHYWFPDB-UHFFFAOYSA-N 0.000 description 2
- 108010053210 Phycocyanin Proteins 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 229920000805 Polyaspartic acid Polymers 0.000 description 2
- 108010020346 Polyglutamic Acid Proteins 0.000 description 2
- 229930182558 Sterol Natural products 0.000 description 2
- PZBFGYYEXUXCOF-UHFFFAOYSA-N TCEP Chemical compound OC(=O)CCP(CCC(O)=O)CCC(O)=O PZBFGYYEXUXCOF-UHFFFAOYSA-N 0.000 description 2
- DBPBBEWGTZWSRJ-UHFFFAOYSA-N [4-(2-methylprop-2-enoyloxy)-1-(trimethylazaniumyl)butan-2-yl] hydrogen phosphate Chemical compound CC(=C)C(=O)OCCC(C[N+](C)(C)C)OP(O)([O-])=O DBPBBEWGTZWSRJ-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 2
- AGBQKNBQESQNJD-UHFFFAOYSA-N alpha-Lipoic acid Natural products OC(=O)CCCCC1CCSS1 AGBQKNBQESQNJD-UHFFFAOYSA-N 0.000 description 2
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 2
- 229960003121 arginine Drugs 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- VHRGRCVQAFMJIZ-UHFFFAOYSA-N cadaverine Chemical compound NCCCCCN VHRGRCVQAFMJIZ-UHFFFAOYSA-N 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 238000010609 cell counting kit-8 assay Methods 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 230000003833 cell viability Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical group C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- LVTYICIALWPMFW-UHFFFAOYSA-N diisopropanolamine Chemical compound CC(O)CNCC(C)O LVTYICIALWPMFW-UHFFFAOYSA-N 0.000 description 2
- 239000003640 drug residue Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000002060 fluorescence correlation spectroscopy Methods 0.000 description 2
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 229960002885 histidine Drugs 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 235000019136 lipoic acid Nutrition 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 125000005439 maleimidyl group Chemical group C1(C=CC(N1*)=O)=O 0.000 description 2
- 239000012046 mixed solvent Substances 0.000 description 2
- 125000000962 organic group Chemical group 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- YHHSONZFOIEMCP-UHFFFAOYSA-O phosphocholine Chemical compound C[N+](C)(C)CCOP(O)(O)=O YHHSONZFOIEMCP-UHFFFAOYSA-O 0.000 description 2
- 229920001606 poly(lactic acid-co-glycolic acid) Polymers 0.000 description 2
- 108010064470 polyaspartate Proteins 0.000 description 2
- 229920002643 polyglutamic acid Polymers 0.000 description 2
- 239000004626 polylactic acid Substances 0.000 description 2
- 229920006254 polymer film Polymers 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 239000012192 staining solution Substances 0.000 description 2
- 150000003432 sterols Chemical class 0.000 description 2
- 235000003702 sterols Nutrition 0.000 description 2
- 239000010409 thin film Substances 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-O triphenylphosphanium Chemical compound C1=CC=CC=C1[PH+](C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-O 0.000 description 2
- 238000000108 ultra-filtration Methods 0.000 description 2
- 238000001291 vacuum drying Methods 0.000 description 2
- BGGHCRNCRWQABU-JTQLQIEISA-N (2s)-2-amino-5-oxo-5-phenylmethoxypentanoic acid Chemical compound OC(=O)[C@@H](N)CCC(=O)OCC1=CC=CC=C1 BGGHCRNCRWQABU-JTQLQIEISA-N 0.000 description 1
- PSLCKQYQNVNTQI-BHFSHLQUSA-N (2s)-2-aminobutanedioic acid;(2s)-2-aminopentanedioic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O.OC(=O)[C@@H](N)CCC(O)=O PSLCKQYQNVNTQI-BHFSHLQUSA-N 0.000 description 1
- PJRSUKFWFKUDTH-JWDJOUOUSA-N (2s)-6-amino-2-[[2-[[(2s)-2-[[(2s,3s)-2-[[(2s)-2-[[2-[[(2s)-2-[[(2s)-6-amino-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[(2-aminoacetyl)amino]-4-methylsulfanylbutanoyl]amino]propanoyl]amino]-3-hydroxypropanoyl]amino]hexanoyl]amino]propanoyl]amino]acetyl]amino]propanoyl Chemical group CSCC[C@H](NC(=O)CN)C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(N)=O PJRSUKFWFKUDTH-JWDJOUOUSA-N 0.000 description 1
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 1
- 125000004454 (C1-C6) alkoxycarbonyl group Chemical group 0.000 description 1
- SYFZCLMMUNCHNH-UHFFFAOYSA-N 2-(prop-2-ynoxymethyl)oxirane Chemical compound C#CCOCC1CO1 SYFZCLMMUNCHNH-UHFFFAOYSA-N 0.000 description 1
- IMSODMZESSGVBE-UHFFFAOYSA-N 2-Oxazoline Chemical compound C1CN=CO1 IMSODMZESSGVBE-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- MUUOUUYKIVSIAR-UHFFFAOYSA-N 2-but-3-enyloxirane Chemical compound C=CCCC1CO1 MUUOUUYKIVSIAR-UHFFFAOYSA-N 0.000 description 1
- FCZHJHKCOZGQJZ-UHFFFAOYSA-N 2-oct-7-enyloxirane Chemical compound C=CCCCCCCC1CO1 FCZHJHKCOZGQJZ-UHFFFAOYSA-N 0.000 description 1
- KIUMMUBSPKGMOY-UHFFFAOYSA-N 3,3'-Dithiobis(6-nitrobenzoic acid) Chemical compound C1=C([N+]([O-])=O)C(C(=O)O)=CC(SSC=2C=C(C(=CC=2)[N+]([O-])=O)C(O)=O)=C1 KIUMMUBSPKGMOY-UHFFFAOYSA-N 0.000 description 1
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical group N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 1
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 108091023037 Aptamer Proteins 0.000 description 1
- 244000056139 Brassica cretica Species 0.000 description 1
- 235000003351 Brassica cretica Nutrition 0.000 description 1
- 235000003343 Brassica rupestris Nutrition 0.000 description 1
- HDPKCAFRQVRNQU-UHFFFAOYSA-O C(C=C)(=O)OCCCCCCCCCCP(=O)=C(O)C[N+](C)(C)C Chemical compound C(C=C)(=O)OCCCCCCCCCCP(=O)=C(O)C[N+](C)(C)C HDPKCAFRQVRNQU-UHFFFAOYSA-O 0.000 description 1
- HELFLDITOJIBLI-UHFFFAOYSA-O C(C=C)(=O)OCCCCCCP(=O)=C(O)C[N+](C)(C)C Chemical compound C(C=C)(=O)OCCCCCCP(=O)=C(O)C[N+](C)(C)C HELFLDITOJIBLI-UHFFFAOYSA-O 0.000 description 1
- OLACVDASGOFJBM-UHFFFAOYSA-O C(C=C)(=O)OCCCCP(=O)=C(O)C[N+](C)(C)C Chemical compound C(C=C)(=O)OCCCCP(=O)=C(O)C[N+](C)(C)C OLACVDASGOFJBM-UHFFFAOYSA-O 0.000 description 1
- KOTOGMHTRKJSTM-UHFFFAOYSA-O C(C=C)(=O)OCCCP(=O)=C(O)C[N+](C)(C)C Chemical compound C(C=C)(=O)OCCCP(=O)=C(O)C[N+](C)(C)C KOTOGMHTRKJSTM-UHFFFAOYSA-O 0.000 description 1
- LWLHCZLCSDUDEL-UHFFFAOYSA-O C[N+](C)(C)CC(O)=P(=O)CCOC(=O)C=C Chemical compound C[N+](C)(C)CC(O)=P(=O)CCOC(=O)C=C LWLHCZLCSDUDEL-UHFFFAOYSA-O 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- 108090000204 Dipeptidase 1 Proteins 0.000 description 1
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 1
- 101000933461 Escherichia coli (strain K12) Beta-glucuronidase Proteins 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical group C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 241000963438 Gaussia <copepod> Species 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- CTKINSOISVBQLD-UHFFFAOYSA-N Glycidol Chemical compound OCC1CO1 CTKINSOISVBQLD-UHFFFAOYSA-N 0.000 description 1
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 1
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 1
- 101001120470 Haemophilus influenzae (strain ATCC 51907 / DSM 11121 / KW20 / Rd) Peptidoglycan-associated lipoprotein Proteins 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- QUOGESRFPZDMMT-UHFFFAOYSA-N L-Homoarginine Natural products OC(=O)C(N)CCCCNC(N)=N QUOGESRFPZDMMT-UHFFFAOYSA-N 0.000 description 1
- VGALFAWDSNRXJK-VIFPVBQESA-N L-aspartic acid beta-benzyl ester Chemical compound OC(=O)[C@@H](N)CC(=O)OCC1=CC=CC=C1 VGALFAWDSNRXJK-VIFPVBQESA-N 0.000 description 1
- QUOGESRFPZDMMT-YFKPBYRVSA-N L-homoarginine Chemical compound OC(=O)[C@@H](N)CCCCNC(N)=N QUOGESRFPZDMMT-YFKPBYRVSA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical group C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- 108091006006 PEGylated Proteins Proteins 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical group OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 1
- 229920002845 Poly(methacrylic acid) Polymers 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 108010039918 Polylysine Proteins 0.000 description 1
- 239000004721 Polyphenylene oxide Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 208000036758 Postinfectious cerebellitis Diseases 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 1
- 108010087230 Sincalide Proteins 0.000 description 1
- 108020004459 Small interfering RNA Proteins 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 229910052770 Uranium Inorganic materials 0.000 description 1
- ABUBSBSOTTXVPV-UHFFFAOYSA-H [U+6].CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O Chemical compound [U+6].CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O ABUBSBSOTTXVPV-UHFFFAOYSA-H 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 238000007259 addition reaction Methods 0.000 description 1
- 125000003172 aldehyde group Chemical group 0.000 description 1
- 108010004469 allophycocyanin Proteins 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000003862 amino acid derivatives Chemical class 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 238000007098 aminolysis reaction Methods 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000000692 anti-sense effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 1
- 125000003710 aryl alkyl group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 102000005936 beta-Galactosidase Human genes 0.000 description 1
- 102000006635 beta-lactamase Human genes 0.000 description 1
- 239000003012 bilayer membrane Substances 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- QKSKPIVNLNLAAV-UHFFFAOYSA-N bis(2-chloroethyl) sulfide Chemical compound ClCCSCCCl QKSKPIVNLNLAAV-UHFFFAOYSA-N 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 230000004700 cellular uptake Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000006482 condensation reaction Methods 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 229910003460 diamond Inorganic materials 0.000 description 1
- 239000010432 diamond Substances 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 229940043279 diisopropylamine Drugs 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 230000012202 endocytosis Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- GKIPXFAANLTWBM-UHFFFAOYSA-N epibromohydrin Chemical compound BrCC1CO1 GKIPXFAANLTWBM-UHFFFAOYSA-N 0.000 description 1
- 125000003700 epoxy group Chemical group 0.000 description 1
- 230000031857 establishment of mitochondrion localization Effects 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 239000010419 fine particle Substances 0.000 description 1
- 239000000834 fixative Substances 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- 108091006047 fluorescent proteins Proteins 0.000 description 1
- 102000034287 fluorescent proteins Human genes 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 230000005661 hydrophobic surface Effects 0.000 description 1
- 125000005462 imide group Chemical group 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000002602 lanthanoids Chemical class 0.000 description 1
- RLJMLMKIBZAXJO-UHFFFAOYSA-N lead nitrate Chemical compound [O-][N+](=O)O[Pb]O[N+]([O-])=O RLJMLMKIBZAXJO-UHFFFAOYSA-N 0.000 description 1
- 125000002463 lignoceryl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000002479 lipoplex Substances 0.000 description 1
- 150000004668 long chain fatty acids Chemical class 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- HWYHZTIRURJOHG-UHFFFAOYSA-N luminol Chemical compound O=C1NNC(=O)C2=C1C(N)=CC=C2 HWYHZTIRURJOHG-UHFFFAOYSA-N 0.000 description 1
- 229960003646 lysine Drugs 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 235000010460 mustard Nutrition 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 230000000269 nucleophilic effect Effects 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 229910052762 osmium Inorganic materials 0.000 description 1
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 1
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 125000002958 pentadecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- GPCKFIWBUTWTDH-UHFFFAOYSA-N pentane-3,3-diamine Chemical compound CCC(N)(N)CC GPCKFIWBUTWTDH-UHFFFAOYSA-N 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 1
- 101150086837 pic gene Proteins 0.000 description 1
- 229920000724 poly(L-arginine) polymer Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920000768 polyamine Polymers 0.000 description 1
- 108010011110 polyarginine Proteins 0.000 description 1
- 229920001610 polycaprolactone Polymers 0.000 description 1
- 229920002704 polyhistidine Polymers 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 229920005606 polypropylene copolymer Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical group O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229940043267 rhodamine b Drugs 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 208000015891 sexual disease Diseases 0.000 description 1
- 125000004469 siloxy group Chemical group [SiH3]O* 0.000 description 1
- IZTQOLKUZKXIRV-YRVFCXMDSA-N sincalide Chemical compound C([C@@H](C(=O)N[C@@H](CCSC)C(=O)NCC(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(N)=O)NC(=O)[C@@H](N)CC(O)=O)C1=CC=C(OS(O)(=O)=O)C=C1 IZTQOLKUZKXIRV-YRVFCXMDSA-N 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 230000007928 solubilization Effects 0.000 description 1
- 238000005063 solubilization Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000000935 solvent evaporation Methods 0.000 description 1
- 238000007440 spherical crystallization Methods 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L sulfate group Chemical group S(=O)(=O)([O-])[O-] QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 231100000820 toxicity test Toxicity 0.000 description 1
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- JFALSRSLKYAFGM-UHFFFAOYSA-N uranium(0) Chemical compound [U] JFALSRSLKYAFGM-UHFFFAOYSA-N 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
Abstract
【化1】
Description
1つの実施形態において、上記薬物送達用ポリマーが、親水性ポリマーセグメントと疎水性ポリマーセグメントとを含む。
1つの実施形態において、上記ポリマー複合体には、さらに薬物が結合されている。
本発明のさらに別の局面によれば、上記ポリマー複合体を含む、薬物送達用組成物が提供される。
1つの実施形態において、上記薬物送達用組成物は、薬物をさらに含む。
本発明のさらに別の局面によれば、送達対象化合物と、上記式(I)で表されるホスホコリン基を有する化合物と、を結合させる工程を含む、標的指向性を有する化合物の製造方法が提供される。
本発明のさらに別の局面によれば、送達対象物を上記式(I)で表されるホスホコリン基を含む標的指向性部位で修飾することを含む、送達対象物に細胞又はミトコンドリアへの指向性を付与する方法が提供される。
1つの実施形態において、上記送達対象物が、リポソーム、高分子ミセル、ポリイオンコンプレックス、ポリプレックス、リポプレックス、リポポリプレックス、無機金属粒子、脂質ナノ粒子及びゲルから選択される。
本発明はまた、細胞又はミトコンドリアへの指向性を有する化合物の製造のための、上記式(I)で表されるホスホコリン基又は上記式(I)で表されるホスホコリン基を有する化合物の使用に関する。
本発明のさらに別の局面によれば、標的指向性部位を含み、標識物質によって標識化された検出試薬であって、該標的指向性部位が、上記式(I)で表されるホスホコリン基を含む、検出試薬が提供される。
本発明の別の局面によれば、薬物送達用ポリマーと該薬物送達用ポリマーに結合された標的指向性部位とを含み、該標的指向性部位が上記式(I)で表されるホスホコリン基を含む、ポリマー複合体(コンジュゲート)が提供される。
上記静電相互作用によって電荷を有する薬物と会合してPICを形成し得る荷電性ポリマーとしては、ポリマーとしての荷電の種類により、カチオン性ポリマーと、アニオン性ポリマーとに分けられる。
上記薬物を内包可能な高分子ミセルを形成し得るブロックコポリマーは、代表的には、親水性ポリマーセグメントと疎水性ポリマーセグメントとを含むブロックコポリマーであり、好ましくはこれらのセグメントが直列に結合されたブロックコポリマーである。
Zは、式(I)で表されるホスホコリン基を表し;
L1、L2、L3、及びL4はそれぞれ独立して、二価の連結基を表し;
R1は、水素原子、未置換又は置換された直鎖もしくは分枝の炭素数1〜12のアルキル基あるいは未置換又は置換された直鎖もしくは分枝の炭素数1〜24のアルキルカルボニル基を表し;
R2は、水酸基、オキシベンジル基、−O−R2a又はNH−R2b基を表し、ここでR2a又はR2bはそれぞれ独立して、未置換又は置換された直鎖もしくは分枝の炭素数1〜12アルキル基を表し;
R3a、R3b、R4a及びR4bは、相互に独立して、メチレン基又はエチレン基を表し;
R5a及びR5bは、相互に独立して、−O−又はNH−を表し;
R6a及びR6bは、相互に独立して、水素原子又は疎水性有機基を表し;
R7a及びR7bは、相互に独立して、下記の基:
−NH−(CH2)p1−〔NH−(CH2)q1−〕r1NH2 (i);
−NH−(CH2)p2−N〔−(CH2)q2−NH2〕2 (ii);
−NH−(CH2)p3−N{〔−(CH2)q3−NH2〕〔−(CH2)q4−NH−〕r2H} (iii);
−NH−(CH2)p4−N{−(CH2)q5−N〔−(CH2)q6−NH2〕2}2 (iv);及び
−NH−(CH2)p5−NH2 (v)
からなる群の同一もしくは異なる基から選ばれ、
ここで、p1〜p5、q1〜6、及びr1〜r2は、それぞれ相互に独立して、1〜5の整数であり;
R8は、リシン、オルニチン、アルギニン、ホモアルギニン、及びヒスチジンからなる群より選択されるアミノ酸の側鎖を表し;
kは、20〜20,000の整数を表し;
a、b、c、d、及びeは、それぞれ独立して、0〜400の整数であり;
ただし、5≦a+b+c+d+e≦400の関係を満たし;
上記各アミノ酸繰り返し単位の結合順は任意であり;
R6a、R6b、R7a、R7b及びR8は、ポリマー分子内のアミノ酸繰り返し単位毎に任意に選択可能である。)
Zは、式(I)で表されるホスホコリン基を表し;
L5及びL6はそれぞれ独立して、単結合又は二価の連結基を表し;
R9は、水素原子、未置換又は置換された直鎖もしくは分枝の炭素数1〜12のアルキル基あるいは未置換又は置換された直鎖もしくは分枝の炭素数1〜24のアルキルカルボニル基を表し;
R10は、アルキレン基又はエステル結合を介した1級アミンを表し;
mは、5〜20,000の整数を表し;
nは、2〜5,000の整数を表す。)
上記薬物を担持可能な微粒子を形成し得る生体適合性ポリマーとしては、例えば、ポリグリコール酸(PGA)、ポリ乳酸(PLA)及びそれらの共重合体(PLGA)、ポリε−カプロラクトン、キトサン等が挙げられる。これらのポリマーに対して、標的指向性部位は、任意の適切な部位に結合される。例えば、ポリマーの一方又は両方の末端に結合されてもよく、側鎖に導入されてもよい。ポリマーに結合される標的指向性部位の数は、本発明の効果が得られる範囲で制限はなく、1又は2以上であり得る。ポリマーと標的指向性部位との結合は、ポリマーが有する官能基と結合可能な官能基と、標的指向性部位と、を有する化合物を用いて、A項に記載の薬物と標的指向性部位との結合と同様の方法で行うことができる。
上記水溶性ポリマーは、可溶化、徐放化、血中滞留性の向上、酵素分解の回避等を目的とした送達対象物の修飾に用いられる。このような水溶性ポリマーとしては、例えば、ポリエチレングリコール、ポリプロピレングリコール及びこれらの共重合体、アルブミン等の可溶性タンパク質、多糖等が挙げられ、なかでもポリエチレングリコールが好ましく用いられ得る。
本発明のさらに別の局面によれば、B項に記載のポリマー複合体を含む薬物送達用組成物が提供される。1つの実施形態において、薬物送達用組成物は、上記ポリマー複合体によって形成される粒子を含む。粒子の平均粒径は、用いるポリマー複合体によって変動し得るが、例えば1000nm以下、好ましくは400nm以下、200nm以下、150nm以下、100nm以下又は80nm以下であり、例えば20nm以上又は30nm以上である。当該粒子の平均粒子径は、市販の動的光散乱(DLS)測定装置を用いて測定することができる。
上記薬物複合体又は薬物送達用組成物は、薬物の投与を必要とする個体に対して投与される。1つの実施形態において、薬物は、細胞内に取り込まれることが所望される薬物であり、好ましくはミトコンドリアに送達されること所望される薬物である。
本発明の別の局面によれば、送達対象化合物と、式(I)で表されるホスホコリン基を有する化合物と、を結合させる工程を含む、標的指向性を有する化合物の製造方法が提供される。送達対象化合物に付与される標的指向性は、細胞内への指向性であり、より具体的にはミトコンドリア内への指向性である。
本発明の別の局面によれば、送達対象物を上記式(I)で表されるホスホコリン基を含む標的指向性部位で修飾することを含む、送達対象物に細胞又はミトコンドリアへの指向性を付与する方法が提供される。
本発明のさらに別の局面によれば、標的指向性部位を含み、標識物質によって標識化された検出試薬であって、該標的指向性部位が、上記式(I)で表されるホスホコリン基を含む、検出試薬が提供される。上記式(I)で表されるホスホコリン基は、ミトコンドリアへの指向性を発揮することから、上記検出試薬を用いることにより、細胞又は個体におけるミトコンドリアの観察を好適に行うことができる。
N−ブチルアミンを開始剤とするNCA重合法によりHomo−PBLAを合成した。具体的には、N−ブチルアミンに、DCMとDMFの混合溶媒(DCM:DMF=10:1、67mg/mL)に溶解したBLA−NCA(100当量)を加え、35度で3日間反応した。反応溶液を過剰量のジエチルエーテルに加え、減圧乾燥することによりHomo−PBLAを得た。重DMSO中での1H−NMRから、PBLA鎖の重合度が65であることが確認された。
PC−PEG−PAspとHomo−P(Asp−AP)をそれぞれ、10mMリン酸緩衝液(pH7.4)に溶解し、PAsp鎖のカルボキシル基とP(Asp−AP)鎖の1級アミンのモル比が1になるように混合してPC搭載PICミセルを調製した。また、コントロールのPICミセルとして、PC−PEG−PAspの代わりにコントロールのポリマー(MeO−PEG−PAsp)を用いたこと以外は上記と同様にして、非PC搭載PICミセルを調製した。次に、PICミセルにPAspのカルボキシル基に対して10当量の1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(EDC)を添加し、室温で1晩反応した。限外ろ過法(MWCO:100,000)により精製し、EDC架橋後のPICミセルのサイズ及び多分散度(PDI)を動的光散乱(DLS)法により測定した。また、PICミセルのゼータ電位を電気泳動光散乱(ELS)法により測定した。結果を表1に示す。
ヒトすい腺がん細胞(BxPC3)を96ウェルプレートに播種(5,000cells/well、培地:100μL)した。24時間後に培地を交換し、Cy5で蛍光標識したPC搭載PICミセルとCy3で蛍光標識したコントロールの非PC搭載PICミセルを添加(Cy3及びCy5の蛍光強度:1,000)した。1、6、24時間後にPBSにより洗浄し、ヘキストによる核染色を行った。Cy5、Cy3及びヘキスト由来の蛍光を共焦点レーザー顕微鏡法により測定し、蛍光強度をImageJにより定量した。
2−メタクリロイルオキシエチルホスホコリン(MPC)を用いてPC搭載PICミセルの細胞取り込みの競合試験を行った。具体的には、ヒトすい腺がん細胞(BxPC3)を96ウェルプレートに播種(5,000 cells/well、培地:100μL)した。24時間後に培地を交換し、Cy5で蛍光標識したPC搭載PICミセルとCy3で蛍光標識したコントロールのPICミセルとを添加(Cy3及びCy5の蛍光強度:1,000)し、競合実験群についてはMPC溶液(PBS、10mM)を添加した。1、6、24時間後にPBSにより洗浄し、ヘキストによる核染色を行った。Cy5、Cy3及びヘキスト由来の蛍光を共焦点レーザー顕微鏡法により測定し、蛍光強度をImageJにより定量した。
MPC溶液(PBS、10mM)の代わりにリン脂質転送タンパク質(phospholipid transfer protein (PLTP))の阻害剤であるチメロサール溶液(PBS、10nM)を添加したこと以外は上記競合試験と同様にして、PC搭載PICミセルの細胞取り込みの阻害実験を行った。
ヒトすい腺がん細胞(BxPC3)を96ウェルプレートに播種(5,000cells/well、培地:100μL)した。24時間後に培地を交換し、製品名「CellLight Mitochondria−GFP」(2μL/well)によりミトコンドリアを染色した。24時間後にCy5で蛍光標識したPC搭載PICミセルとCy3で蛍光標識した非PC搭載PICミセルとを添加(Cy3及びCy5の蛍光強度:1,000)し、製品名「CellLight Mitochondria−GFP」(2μL/well)をさらに添加した。1、6、24時間後にPBSにより洗浄し、ヘキストによる核染色を行った。Cy5、Cy3、GFP及びヘキスト由来の蛍光を共焦点レーザー顕微鏡法により測定し、Cy5とGFP又はCy3とGFPの共局在比(ミトコンドリア全量に対するミセルと共局在しているミトコンドリアの比率)をそれぞれImageJにより定量した。結果を図2に示す。
また、PC−PEG−PAspの代わりにMeO−PEG−PAspを用いたこと以外は上記と同様にして、PCのついていないシンバスタチン結合ポリマー(MeO−PEG−P(Asp−simvastatin)−Ac)を得た。
PC−PEG−P(Asp−simvastatin)−Acをメタノール(10mg/mL)に溶解し、メタノールを減圧乾燥により取り除いてポリマー薄膜を得た。得られたポリマー薄膜に純水(1mg/mL)を添加し、室温で30分間超音波処理によりミセル化してPC搭載シンバスタチン内包ミセルを調製した。また、PC−PEG−P(Asp−simvastatin)−Acの代わりにMeO−PEG−P(Asp−simvastatin)−Acを用いたこと以外は上記と同様にして、非PC搭載シンバスタチン内包ミセルを調製した。フィルターによる精製後にミセルのサイズ及びPDIをDLS法により測定し、ミセルのゼータ電位をELS法により測定した。結果を表2に示す。
ヒトすい腺がん細胞(BxPC3)を96ウェルプレートに播種(5,000cells/well、培地:100μL)した。24時間後に培地を交換し、PC搭載シンバスタチン内包ミセル溶液、非PC搭載シンバスタチン内包ミセル溶液又はシンバスタチン溶液を添加した。48時間後にPBSにより洗浄し、Cell Counting Kit−8(CCK−8、10μL/well)を添加した。30分後にプレートリーダーにより吸光度を測定し、細胞生存率及びIC50を算出した。結果を図3に示す。
以下に示すPC−PEG−PGTrpを合成した。具体的な手順は以下のとおりである。
PC−PEG−PGTrpとmRNA(Gaussia luciferase (GLuc))を10mM Hepes緩衝液(pH7.3)に溶解し、PGTrp鎖の1級アミン(N)とmRNA中のリン酸基(P)のモル比(N/P)が3になるように混合し、PC搭載mRNAミセルを調製した。また、PC−PEG−PGTrpの代わりにMeO−PEG−PGTrpを用いたこと以外は上記と同様にして、非PC搭載mRNAミセルを調製した。mRNAミセルのサイズ及びPDIをDLS法により測定した。また、ミセル1つあたりのmRNA分子の会合数を蛍光相関分光(FCS)法により測定した。結果を表3に示す。
ヒトすい腺がん細胞(BxPC3)を96ウェルプレートに播種(5,000 cells/well)した。24時間後に培地を交換し、GLuc mRNAミセル溶液(50μg/well)を添加した。24時間後に上清をプレートに添加し、ルシフェリン添加後に発光強度をルミノメーターにより測定した。結果を図4に示す。
Alexa647修飾アルブミンを10mMリン酸緩衝液(pH7.4、5mg/mL)に溶解し、100mM トリス(2−カルボキシエチル)ホスフィン(TCEP、1mL)を添加した。室温で30分の反応後にMPC(350当量)とDIPA(350当量)を添加し、室温で48時間反応した。反応後に限外ろ過法(MWCO:3,000)により精製し、アルブミンへのPCの導入を行った。イールマン試薬によるチオール基の定量から、アルブミン1分子あたりに導入されたPCは10分子であった。
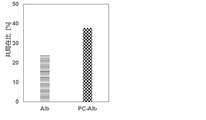
ヒトすい腺がん細胞(BxPC3)を96ウェルプレートに播種(5,000 cells/well)した。24時間後に培地を交換し、Alexa647修飾アルブミンPCコンジュゲート溶液を添加した。また、コントロール群には、Alexa647修飾アルブミンを添加した。6、24時間後にPBSにより洗浄し、ヘキストによる核染色を行った。Alexa647及びヘキスト由来の蛍光を共焦点レーザー顕微鏡法により測定し、蛍光強度をImageJにより定量した。結果を図5に示す。
ヒトすい腺がん細胞(BxPC3)を96ウェルプレートに播種(5,000cells/well、培地:100μL)した。24時間後に培地を交換し、製品名「CellLight Mitochondria−GFP」(2μL/well)によりミトコンドリアを染色した。24時間後にAlexa647修飾アルブミンPCコンジュゲート溶液又はAlexa647修飾アルブミン(コントロール)を添加(蛍光強度:1,000)し、製品名「CellLight Mitochondria−GFP」(2μL/well)をさらに添加した。6、24時間後にPBSにより洗浄し、ヘキストによる核染色を行った。Alexa647、GFP及びヘキスト由来の蛍光を共焦点レーザー顕微鏡法により測定し、Alexa647とGFPの共局在比をそれぞれImageJにより定量した。結果を図6に示す。
≪PC−PEG−lipoic acidの合成≫
製造例1と同様の方法で調製したPC−PEG−NH2(10kDa,30mg)をDMSO(4mL)に溶解し、α−リポ酸(20当量,12mg)、1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド(20当量,12mg)、N−ヒドロキシスクシンイミド(20当量,7mg)を添加し、35度で1晩撹拌した。その後、反応溶液を透析用バック(MWCO:3,500Da)に入れて純水に対して1晩透析を行った。凍結乾燥後に得られたポリマーを重クロロホルム中の1H−NMRにより、ポリマーへのα−リポ酸の導入率が77%であることが確認された。
金ナノ粒子(4.0×1011particles/mL、溶液:50μL)にPC−PEG−lipoic acid溶液(0.01mg/mL,PBS,17μL)を添加し、常温で1晩反応した。その後、フィルター(ポアサイズ:220nm)により不純物を除き、動的光散乱法(DLS)によりサイズおよび多分散度を測定したところ、86nm(PDI=0.17)であった。
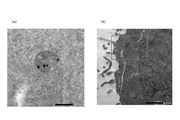
BxPC3細胞(ヒトすい臓腺がん細胞)を6ウェルプレートに播種した(1×106cells/well、培地:2mL)。24時間後に上記の手順で作製したPC搭載金ナノ粒子を各ウェルに1×1010個ずつ(2mL)添加し、24時間インキュベートした(PC搭載金ナノ粒子数は、動的光散乱法(DLS)により測定した)。細胞をトリプシン処理して、遠心にて回収し、前固定液(4%パラホルムアルデヒド、0.1MPBS、25%グルタールアルデヒドの5:4:1の混合溶液)を用いた前固定および後固定液(2%オスミウム酸、0.1PBSの1:1混合液)を用いた後固定を行った。次いで、上昇エタノール脱水を行い、エポン樹脂で包埋した後、ダイアモンドカッターで1μmの厚さに切断することにより、超薄切片を作製した。得られた超薄切片に対して、ウラン染色液(酢酸ウラン,50%アルコール溶液)を用いた染色、次いで、レイノルズ鉛染色液(硝酸鉛2.66g、クエン酸ナトリウム3.52g、1M NaOH16mL)を用いた染色を各10分行い、透過型電子顕微鏡(TEM)観察に供した。TEM観察画像を図7に示す。
Claims (11)
- 前記薬物送達用ポリマーが、親水性ポリマーセグメントと疎水性ポリマーセグメントとを含む、請求項2に記載のポリマー複合体。
- さらに薬物が結合されている、請求項2又は3に記載のポリマー複合体。
- 請求項2から4のいずれかに記載のポリマー複合体を含む、薬物送達用組成物。
- 薬物をさらに含む、請求項5に記載の薬物送達用組成物。
- 前記送達対象物が、リポソーム、高分子ミセル、ポリイオンコンプレックス、ポリプレックス、リポプレックス、リポポリプレックス、無機金属粒子、脂質ナノ粒子及びゲルから選択される、請求項8に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018229599 | 2018-12-07 | ||
| JP2018229599 | 2018-12-07 | ||
| PCT/JP2019/047917 WO2020116640A1 (ja) | 2018-12-07 | 2019-12-06 | 薬物複合体、ポリマー複合体及び薬物送達用組成物 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JPWO2020116640A1 true JPWO2020116640A1 (ja) | 2021-10-21 |
Family
ID=70974200
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020560070A Pending JPWO2020116640A1 (ja) | 2018-12-07 | 2019-12-06 | 薬物複合体、ポリマー複合体及び薬物送達用組成物 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JPWO2020116640A1 (ja) |
| WO (1) | WO2020116640A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115554272B (zh) * | 2022-09-28 | 2024-03-22 | 昆明理工大学 | 一种纳米颗粒的制备方法及其应用 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR9509938A (pt) * | 1994-11-30 | 1998-01-27 | Amur Research Corp | Processo para aumentar a biodisponibilidade de um agente farmacéutico formulação farmacéutica para tratar um mamifero sofrendo de hipoesteroidismo osteoporose asma composição de substáncia |
-
2019
- 2019-12-06 WO PCT/JP2019/047917 patent/WO2020116640A1/ja active Application Filing
- 2019-12-06 JP JP2020560070A patent/JPWO2020116640A1/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| WO2020116640A1 (ja) | 2020-06-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ofek et al. | In vivo delivery of small interfering RNA to tumors and their vasculature by novel dendritic nanocarriers | |
| Deng et al. | Functional polypeptide and hybrid materials: Precision synthesis via α-amino acid N-carboxyanhydride polymerization and emerging biomedical applications | |
| Nishiyama et al. | Nanostructured devices based on block copolymer assemblies for drug delivery: designing structures for enhanced drug function | |
| Sun et al. | Self-assembled biodegradable micellar nanoparticles of amphiphilic and cationic block copolymer for siRNA delivery | |
| US7229973B2 (en) | pH-sensitive polymeric micelles for drug delivery | |
| Gheybi et al. | Supramolecular anticancer drug delivery systems based on linear–dendritic copolymers | |
| US9114177B2 (en) | Block copolymer having phenylboronic acid group introduced therein, and use thereof | |
| KR20100138910A (ko) | 비하전성 친수성 블록 및 측사슬의 일부에 소수성 기가 도입된 카티온성 폴리아미노산 블록을 포함하여 이루어지는 공중합체, 그 사용 | |
| JP4582821B2 (ja) | カチオン性のポリ(アミノ酸)およびその使用 | |
| JP2010529214A (ja) | カチオン性基及び疎水性基により官能基化したポリグルタミン酸及びその応用、特にはその治療への応用 | |
| US20180185281A1 (en) | Drug delivery carrier, and composition containing same | |
| Tang et al. | Synergistic targeted delivery of payload into tumor cells by dual-ligand liposomes co-modified with cholesterol anchored transferrin and TAT | |
| Gao et al. | Recent advances of dendrimers in delivery of genes and drugs | |
| Xu et al. | Co-delivery of doxorubicin and P-glycoprotein siRNA by multifunctional triblock copolymers for enhanced anticancer efficacy in breast cancer cells | |
| JPWO2009133968A1 (ja) | 電荷変換型三元系ポリプレックス | |
| JP6566936B2 (ja) | 医薬組成物 | |
| Sun et al. | Cancer nanomedicines based on synthetic polypeptides | |
| Mostoufi et al. | Reversing multi-drug tumor resistance to Paclitaxel by well-defined pH-sensitive amphiphilic polypeptide block copolymers via induction of lysosomal membrane permeabilization | |
| Li et al. | Reversibly cross-linked poly (ethylene glycol)–poly (amino acid) s copolymer micelles: a promising approach to overcome the extracellular stability versus intracellular drug release challenge | |
| Li et al. | Self-assembled PEG-b-PDPA-b-PGEM copolymer nanoparticles as protein antigen delivery vehicles to dendritic cells: preparation, characterization and cellular uptake | |
| Luo et al. | Artificial peptides for antitumoral siRNA delivery | |
| Yang et al. | Folate-modified poly (malic acid) graft polymeric nanoparticles for targeted delivery of doxorubicin: synthesis, characterization and folate receptor expressed cell specificity | |
| JPWO2020116640A1 (ja) | 薬物複合体、ポリマー複合体及び薬物送達用組成物 | |
| Martin et al. | Cholesteryl to improve the cellular uptake of polymersomes within HeLa cells | |
| Guo et al. | Optimal design of novel functionalized nanoconjugates based on polymalic acid for efficient tumor endocytosis with enhanced anticancer activity |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20210518 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210531 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20221109 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230912 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231106 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240206 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240402 |