JP7665652B2 - 3次元生体サンプルのzスタック画像のセットの画像処理およびセグメント化 - Google Patents
3次元生体サンプルのzスタック画像のセットの画像処理およびセグメント化 Download PDFInfo
- Publication number
- JP7665652B2 JP7665652B2 JP2022564422A JP2022564422A JP7665652B2 JP 7665652 B2 JP7665652 B2 JP 7665652B2 JP 2022564422 A JP2022564422 A JP 2022564422A JP 2022564422 A JP2022564422 A JP 2022564422A JP 7665652 B2 JP7665652 B2 JP 7665652B2
- Authority
- JP
- Japan
- Prior art keywords
- image
- sample
- depth
- pixel
- images
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T5/00—Image enhancement or restoration
- G06T5/50—Image enhancement or restoration using two or more images, e.g. averaging or subtraction
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T5/00—Image enhancement or restoration
- G06T5/73—Deblurring; Sharpening
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/10—Segmentation; Edge detection
- G06T7/11—Region-based segmentation
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/10—Segmentation; Edge detection
- G06T7/174—Segmentation; Edge detection involving the use of two or more images
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/50—Depth or shape recovery
- G06T7/529—Depth or shape recovery from texture
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T7/00—Image analysis
- G06T7/50—Depth or shape recovery
- G06T7/55—Depth or shape recovery from multiple images
- G06T7/571—Depth or shape recovery from multiple images from focus
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/10—Image acquisition modality
- G06T2207/10056—Microscopic image
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/10—Image acquisition modality
- G06T2207/10064—Fluorescence image
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/20—Special algorithmic details
- G06T2207/20021—Dividing image into blocks, subimages or windows
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/20—Special algorithmic details
- G06T2207/20212—Image combination
- G06T2207/20221—Image fusion; Image merging
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/30—Subject of image; Context of image processing
- G06T2207/30004—Biomedical image processing
- G06T2207/30024—Cell structures in vitro; Tissue sections in vitro
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/30—Subject of image; Context of image processing
- G06T2207/30004—Biomedical image processing
- G06T2207/30072—Microarray; Biochip, DNA array; Well plate
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06T—IMAGE DATA PROCESSING OR GENERATION, IN GENERAL
- G06T2207/00—Indexing scheme for image analysis or image enhancement
- G06T2207/30—Subject of image; Context of image processing
- G06T2207/30004—Biomedical image processing
- G06T2207/30096—Tumor; Lesion
Landscapes
- Engineering & Computer Science (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Theoretical Computer Science (AREA)
- Computer Vision & Pattern Recognition (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Image Processing (AREA)
- Microscoopes, Condenser (AREA)
- Image Analysis (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Description
サンプルを微視的に撮像することは、様々なアプリケーションにおいて有益であり得る。たとえば、サンプルは、培養されたヒト細胞(たとえば、がん細胞、正常細胞)を含むことができ、サンプルを撮像することは、サンプル内で除去する細胞における薬品の有効性(たとえば、除去するがん細胞における化学療法薬の有効性)を決定すること、物質の毒性(たとえば、非がん細胞に対する化学療法薬の毒性)を決定すること、またはサンプルの内容物についてのおよび/またはサンプルの内容物に及ぼす物質の影響についてのいくつかの他の情報を決定することを容易にすることができる。サンプルを撮像することは、明視野顕微鏡、蛍光顕微鏡、構造化照明、共焦点顕微鏡、またはサンプルの内容物についての画像データを生成するためのいくつかの他の撮像技法を使用すること含むことができる。
サンプル内の深さの範囲に及ぶそれぞれの異なる深さに対応する、サンプルの狭い被写界深度画像(たとえば、明視野画像)のセットは、サンプルの内容物の深さについての情報を決定するのに十分な情報を含有し得る。そのような「スタックされた」画像のセットはまた、深さの範囲にわたって焦点が合ったサンプルの内容物を(たとえば、一種のシミュレーションされたサンプルの広い被写界深度画像として)表すサンプルの投影画像を生成するために深度情報と組み合わされ得る、十分な画像情報を含有し得る。本明細書で説明する方法は、狭い視野画像(たとえば、明視野画像、蛍光画像)のセットからそのような深度情報を(たとえば、深度マップとして)およびそのような投影画像を生成することを容易にする。
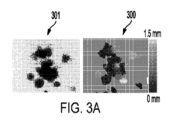
サンプルに対する深度情報(たとえば、深度マップ、個々の深度値)が、(たとえば、例示的な投影画像250および301におけるように)サンプルの画像のセットからのピクセルもしくは他の画像情報をサンプルの単一の投影画像に投影するために使用され得る。深度情報は、投影画像の各ピクセルに対する強度、色、または他の画像情報を設定するとき、画像のセットのうちのどの画像から引き出すかを決定するために使用され得る。上記のように、入力画像のセットがサンプル内の焦点面に対して変動する場合、投影画像が完全に焦点が合ったようにまたは場合によっては入力画像のセットに対して改善されたように見えるように投影画像のピクセルを生成するとき、深度情報は、画像のうちのどの画像から投影するかを選択するために使用され得る。
生体サンプルの画像または興味のある他の環境内のオルガノイド、腫瘍スフェロイド、細胞、粒子、もしくは他の3次元多細胞の個別内容物についての程度、ロケーション、サイズ、アイデンティティ、および/または他の情報を、自動的に識別することは、様々な文脈において有益であり得る。そのようなプロセスは、「画像セグメント化」と呼ばれることがある。画像セグメント化は、画像の内容物に対して様々な分析を自動的に実行するために、たとえば、サンプル内の細胞、オルガノイド、または腫瘍スフェロイドの数、タイプ、体積/サイズ、空間分布、形状、成長率、または他の特性を決定するために使用され得る。
本明細書で説明するシステムおよび方法は、サンプル撮像において様々な生物学的アプリケーションを容易にするために使用され得る。これは、数時間、数日、数週間、もしくは何らかの他の持続時間にわたって複数の時点において撮像すること、またはインキュベータからサンプルを取り除くことによってサンプルに摂動を与える必要を避けるために、自動撮像システムを使用してインキュベータ内に設置されている複数のサンプル(たとえば、96ウェルサンプルプレートのうちのそれぞれのウェル内に含有される96個のサンプル)を撮像することを含むことができる。撮像されたサンプルは、ヒト細胞もしくは腫瘍細胞、オルガノイド、腫瘍スフェロイド、または他の細胞の3D培養物を含有することができる。細胞は、自然であり得るか、または何らかの実験プロセスの結果(たとえば、がん細胞を生成するために発がん物質に暴露した結果)であり得る。さらに、細胞は、蛍光色素で標識されてよく、または蛍光タンパク質、他のレポータ物質を発現するためまたは何らかの他の生物学的洞察を提供するため(たとえば、細胞に対する遺伝子組換えの効果を評価するため)に遺伝子を組み換えられてもよい。
様々なシステムが、本明細書で説明する様々な実施形態を実行するために使用(たとえば、プログラム)され得る。そのようなシステムは、デスクトップコンピュータ、ラップトップコンピュータ、タブレット、または他のシングルユーザワークステーションを含むことができる。追加または代替として、本明細書で説明する実施形態は、サーバ、クラウドコンピューティング環境、または他のマルチユーザシステムによって実行され得る。
図8は、3次元サンプルの投影画像を生成するための方法800のフローチャートである。方法800は、サンプルの画像のセットを取得するステップを含み、画像のセットの各画像は、サンプル内のそれぞれの焦点面に対応する(810)。方法800は、サンプルの出力画像の各ピクセルに対するそれぞれの深度値を決定するために画像のセットの各画像にフィルタを適用するステップを付加的に含み、所与の深度値はサンプル内の深さを表し、その深さにおいて、サンプルの内容物が焦点を合わせて撮像され得る(820)。方法800は、出力画像のピクセルの深度値に基づいて出力画像の各ピクセルに対する画像値を決定するステップを付加的に含み、出力画像の特定のピクセルに対する画像値を決定するステップは、(i)特定のピクセルの深度値に対応する画像のセットのうちの1つの画像を識別するステップと、(ii)特定のピクセルに対応する識別された画像内にロケーションを有する識別された画像のピクセルに基づいて特定のピクセルに対する画像値を決定するステップとを含む(830)。方法800は、追加の要素または特徴を含むことができる。
上記の発明を実施するための形態は、開示するシステム、デバイス、および方法の様々な特徴および機能を、添付の図面を参照しながら説明する。図において、一般的に、文脈が別段に示さない限り、同様の記号は同様の構成要素を識別する。発明を実施するための形態、図、および特許請求の範囲の中で説明する例示的な実施形態は、制限することを意味するものではない。本明細書で提示する主題の範囲を逸脱することなく、他の実施形態が利用されてもよく、他の変更がなされてもよい。本明細書で一般的に説明され、図で示される本開示の態様は、広範な異なる構成において配列され、置換され、組み合わされ、分離され、設計されてもよく、それらのすべが明確に本明細書で考慮されることは、容易に理解されよう。
105 物体
110 撮像装置、カメラ
120 光源
130 サンプル容器
135 サンプル培地
140a 領域、第1の体積
140b 領域、第2の体積
200 画像のセット(スタック)
210a 頂部画像
210b 第2の画像
250 投影画像
300 深度マップ
301 画像、投影画像
305 特定のピクセル
310a 狭い被写界深度画像
310b 狭い被写界深度画像
310c 狭い被写界深度画像
310d 狭い被写界深度画像
315a ピクセル
315b ピクセル
315c ピクセル
315d ピクセル
320 テクスチャ値のセット
325 ピーク
400 投影画像
405 特定のピクセル
410a 狭い被写界深度画像、第1の画像
410b 狭い被写界深度画像、第2の画像
410c 狭い被写界深度画像、第3の画像
410d 狭い被写界深度画像
415a ピクセル
415b ピクセル
415c ピクセル
500 画像、入力画像
510 第1のセグメント化マップ
515a 第1の領域
515b 第2の領域
515c 第3の領域
520 深度マップ
525a エリア、第1のパッチ
525b エリア
530 第2のセグメント化マップ
535a 領域
535b 領域
535c 領域
535d 領域
535e 領域
535f 単一の領域
600 自動撮像システム
610 フレーム
620 サンプル容器
625 ウェル
630 サンプル容器トレー
640 撮像装置
650 作動ガントリー
700 コンピューティングシステム、コンピューティングデバイス
702 通信インターフェース
704 ユーザインターフェース
706 プロセッサ
707 センサ
708 データ記憶装置
710 システムバス
712 データ
718 プログラム命令
720 アプリケーションプログラム
722 オペレーティングシステム
Claims (38)
- 3次元サンプルの投影画像を生成するための方法であって、
前記サンプルの画像のセットを取得するステップであって、前記画像のセットの各画像が、前記サンプル内のそれぞれの焦点面に対応する、ステップと、
前記サンプルの出力画像の各ピクセルに対するそれぞれの深度値を決定するために前記画像のセットの各画像にフィルタを適用するステップであって、所与の深度値が前記サンプル内の深さを表し、その深さにおいて、前記サンプルの内容物が焦点を合わせて撮像され得る、ステップと、
前記出力画像の前記ピクセルの前記深度値に基づいて前記出力画像の各ピクセルに対する画像値を決定するステップとを含み、前記出力画像の特定のピクセルに対する画像値を決定するステップが、(i)前記特定のピクセルの前記深度値に対応する前記画像のセットのうちの1つの画像を識別するステップと、(ii)前記特定のピクセルに対応する前記識別された画像内にロケーションを有する、前記識別された画像のピクセルに基づいて前記特定のピクセルに対する前記画像値を決定するステップとを含み、前記方法は、
前記出力画像に基づいて前記サンプルの第1のセグメント化マップを生成するステップと、
前記決定された深度値に基づいて、前記第1のセグメント化マップの少なくとも1つのセグメントをさらに分割することによって前記サンプルの第2のセグメント化マップを生成するステップとをさらに含み、
前記第1のセグメント化マップの少なくとも1つのセグメントをさらに分割するステップが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記決定された深度値から選択するステップと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別するステップと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割するステップとを含む、方法。 - 前記フィルタはテクスチャフィルタであり、前記画像のセットのうちの特定の画像に前記フィルタを適用するステップが、前記特定の画像の特定のピクセルに対して、前記特定のピクセルの近傍にある前記特定の画像のピクセルの標準偏差、エントロピー、または数値範囲のうちの少なくとも1つを決定するステップを含む、請求項1に記載の方法。
- 前記深度値に基づいて前記サンプルに対する深度マップを生成するステップをさらに含む、請求項1または2に記載の方法。
- 前記決定された深度値を空間的に前処理するステップをさらに含み、前記出力画像の前記ピクセルの前記深度値に基づいて前記出力画像の各ピクセルに対する前記画像値を決定するステップが、前記出力画像の前記ピクセルの前記空間的に前処理された深度値に基づいて前記出力画像の各ピクセルに対する前記画像値を決定するステップを含む、請求項1から3のいずれか一項に記載の方法。
- 前記画像のセットは、前記サンプルの明視野画像のセットである、請求項1から4のいずれか一項に記載の方法。
- 前記画像のセットは、前記サンプルの蛍光画像のセットである、請求項1から5のいずれか一項に記載の方法。
- 前記サンプルは、少なくとも1つの3次元培養多細胞構造を含有する、請求項1から6のいずれか一項に記載の方法。
- 前記少なくとも1つの3次元培養多細胞構造は、細胞外基質内に埋め込まれたオルガノイドまたは腫瘍スフェロイドのうちの少なくとも1つを含む、請求項7に記載の方法。
- 前記少なくとも1つの3次元培養多細胞構造は、細胞外基質内に埋め込まれたオルガノイドを含み、前記細胞外基質は、細胞外基質のドームの形状を有する、請求項8に記載の方法。
- 前記少なくとも1つの3次元培養多細胞構造は、肝細胞オルガノイド、膵臓細胞オルガノイド、または腸細胞オルガノイドのうちの少なくとも1つを含む、請求項8に記載の方法。
- 前記出力画像の前記特定のピクセルに対する前記画像値を決定するステップが、(iii)前記特定のピクセルの前記深度値の近傍の中の深度値に対応する前記画像のセットのうちの2つ以上の追加の画像を識別するステップを付加的に含み、前記特定のピクセルに対応する前記識別された画像内にロケーションを有する、前記識別された画像の前記ピクセルに基づいて前記特定のピクセルに対する前記画像値を決定するステップが、前記識別された画像と、前記特定のピクセルに対応するそれらのそれぞれの識別された画像内にロケーションを有する前記2つ以上の追加の画像とのピクセルに対してピクセルごとの動作を実行するステップを含む、請求項1から10のいずれか一項に記載の方法。
- 3次元サンプルの投影画像を生成するための方法であって、
前記サンプルの画像のセットを取得するステップであって、前記画像のセットの各画像が、前記サンプル内のそれぞれの焦点面に対応する、ステップと、
深度マップの各ピクセルに対するそれぞれの深度値を決定するために前記画像のセットの各画像にフィルタを適用するステップであって、前記深度値は前記サンプル内の深さを表し、その深さにおいて、前記サンプルの内容物が焦点を合わせて撮像され得、前記画像のセットの各画像に前記フィルタを適用することは、前記画像の特定のピクセルについて、前記画像のセットのうちのどのピクセルが焦点が合っているかを決定するために、前記特定のピクセルの近傍におけるピクセルのセットのテクスチャの重み付けられた尺度を決定することにより、前記3次元サンプルの前記投影画像を生成することを含む、ステップと、
前記深度マップの対応するピクセルの前記深度値に基づいて、出力画像の各ピクセルに対する画像値を決定するステップとを含む、方法。 - 3次元サンプルの投影画像を生成するための方法であって、
前記サンプルの画像のセットを取得するステップであって、前記画像のセットの各画像が、前記サンプル内のそれぞれの焦点面に対応する、ステップと、
深度マップの各ピクセルに対するそれぞれの深度値を決定するために前記画像のセットの各画像にフィルタを適用するステップであって、前記深度値は前記サンプル内の深さを表し、その深さにおいて、前記サンプルの内容物が焦点を合わせて撮像され得る、ステップと、
前記深度マップの対応するピクセルの前記深度値に基づいて、出力画像の各ピクセルに対する画像値を決定するステップと、
第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記決定された深度値から選択するステップと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別するステップと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割するステップとを含む、方法。 - 前記フィルタはテクスチャフィルタであり、前記画像のセットのうちの特定の画像に前記フィルタを適用するステップが、前記特定の画像の特定のピクセルに対して、前記特定のピクセルの近傍にある前記特定の画像のピクセルの標準偏差、エントロピー、または数値範囲のうちの少なくとも1つを決定するステップを含む、請求項12または13に記載の方法。
- 前記出力画像に基づいて前記サンプルの第1のセグメント化マップを生成するステップと、
前記決定された深度値に基づいて、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することによって前記サンプルの第2のセグメント化マップを生成するステップとをさらに含む、請求項12~14のいずれか一項に記載の方法。 - 前記第1のセグメント化マップの少なくとも1つの領域をさらに分割するステップが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記決定された深度値から選択するステップと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別するステップと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割するステップとを含む、請求項15に記載の方法。 - 前記画像のセットは、前記サンプルの明視野画像のセットである、請求項12から16のいずれか一項に記載の方法。
- 前記画像のセットは、前記サンプルの蛍光画像のセットである、請求項12から16のいずれか一項に記載の方法。
- 前記サンプルが少なくとも1つのオルガノイドを含有する、請求項12から18のいずれか一項に記載の方法。
- サンプルの画像をセグメント化するための方法であって、
前記サンプルの画像を取得するステップと、
前記サンプルの内容物の深度マップを取得するステップと、
前記画像に基づいて前記サンプルの第1のセグメント化マップを生成するステップと、
前記深度マップに基づいて、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することによって前記サンプルの第2のセグメント化マップを生成するステップとを含み、
前記深度マップは複数の深度値を含み、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割するステップが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記深度値から選択するステップと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別するステップと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割するステップとを含む、方法。 - 前記サンプルが少なくとも1つのオルガノイドを含有する、請求項20に記載の方法。
- 動作を実行するために少なくとも1つのプロセッサによって実行可能な命令を記憶した非一時的コンピュータ可読媒体であって、
サンプルの画像のセットを取得することであって、前記画像のセットの各画像が、前記サンプル内のそれぞれの焦点面に対応する、ことと、
前記サンプルの出力画像の各ピクセルに対するそれぞれの深度値を決定するために前記画像のセットの各画像にフィルタを適用することであって、所与の深度値が前記サンプル内の深さを表し、その深さにおいて、前記サンプルの内容物が焦点を合わせて撮像され得る、ことと、
前記出力画像の前記ピクセルの前記深度値に基づいて前記出力画像の各ピクセルに対する画像値を決定することとを含み、前記出力画像の特定のピクセルに対する画像値を決定することが、(i)前記特定のピクセルの前記深度値に対応する前記画像のセットのうちの1つの画像を識別することと、(ii)前記特定のピクセルに対応する前記識別された画像内にロケーションを有する、前記識別された画像のピクセルに基づいて前記特定のピクセルに対する前記画像値を決定することとを含み、
前記動作が、
前記出力画像に基づいて前記サンプルの第1のセグメント化マップを生成するステップと、
前記決定された深度値に基づいて、前記第1のセグメント化マップの少なくとも1つのセグメントをさらに分割することによって前記サンプルの第2のセグメント化マップを生成するステップとをさらに含み、
前記第1のセグメント化マップの少なくとも1つのセグメントをさらに分割することが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記決定された深度値から選択することと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別することと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割することとを含む、非一時的コンピュータ可読媒体。 - 前記フィルタはテクスチャフィルタであり、前記画像のセットのうちの特定の画像に前記フィルタを適用するステップが、前記特定の画像の特定のピクセルに対して、前記特定のピクセルの近傍にある前記特定の画像のピクセルの標準偏差、エントロピー、または数値範囲のうちの少なくとも1つを決定するステップを含む、請求項22に記載の非一時的コンピュータ可読媒体。
- 前記動作は、前記深度値に基づいて前記サンプルに対する深度マップを生成することをさらに含む、請求項22または23に記載の非一時的コンピュータ可読媒体。
- 前記動作が、
前記決定された深度値を空間的に前処理することをさらに含み、前記出力画像の前記ピクセルの前記深度値に基づいて前記出力画像の各ピクセルに対する前記画像値を決定することが、前記出力画像の前記ピクセルの前記空間的に前処理された深度値に基づいて前記出力画像の各ピクセルに対する前記画像値を決定することをさらに含む、請求項22から24のいずれか一項に記載の非一時的コンピュータ可読媒体。 - 前記出力画像の前記特定のピクセルに対する前記画像値を決定することが、(iii)前記特定のピクセルの前記深度値の近傍の中の深度値に対応する前記画像のセットのうちの2つ以上の追加の画像を識別することを付加的に含み、前記特定のピクセルに対応する前記識別された画像内にロケーションを有する、前記識別された画像の前記ピクセルに基づいて前記特定のピクセルに対する前記画像値を決定することが、前記識別された画像と、前記特定のピクセルに対応するそれらのそれぞれの識別された画像内にロケーションを有する前記2つ以上の追加の画像とのピクセル上でピクセルごとの動作を実行することを含む、請求項22から25のいずれか一項に記載の非一時的コンピュータ可読媒体。
- 動作を実行するために少なくとも1つのプロセッサによって実行可能な命令を記憶した非一時的コンピュータ可読媒体であって、
サンプルの画像のセットを取得することであって、前記画像のセットの各画像が、前記サンプル内のそれぞれの焦点面に対応する、ことと、
深度マップの各ピクセルに対するそれぞれの深度値を決定するために前記画像のセットの各画像にフィルタを適用することであって、所与の深度値が、前記サンプル内の深さを表し、その深さにおいて、前記サンプルの内容物が焦点を合わせて撮像され得る、ことと、
前記深度マップの対応するピクセルの前記深度値に基づいて、出力画像の各ピクセルに対する画像値を決定することとを含み、
前記動作が、
前記出力画像に基づいて前記サンプルの第1のセグメント化マップを生成することと、
前記決定された深度値に基づいて、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することによって前記サンプルの第2のセグメント化マップを生成することとをさらに含み、
前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記決定された深度値から選択することと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別することと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割することとをさらに含む、非一時的コンピュータ可読媒体。 - 前記フィルタはテクスチャフィルタであり、前記画像のセットのうちの特定の画像に前記フィルタを適用することが、前記特定の画像の特定のピクセルに対して、前記特定のピクセルの近傍にある前記特定の画像のピクセルの標準偏差、エントロピー、または数値範囲のうちの少なくとも1つを決定することを含む、請求項27に記載の非一時的コンピュータ可読媒体。
- 動作を実行するために少なくとも1つのプロセッサによって実行可能な命令を記憶した非一時的コンピュータ可読媒体であって、
サンプルの画像を取得することと、
前記サンプルの内容物の深度マップを取得することと、
前記画像に基づいて前記サンプルの第1のセグメント化マップを生成することと、
前記深度マップに基づいて、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することによって前記サンプルの第2のセグメント化マップを生成することとを含み、
前記深度マップは複数の深度値を含み、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記深度値から選択することと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別することと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割することとを含む、非一時的コンピュータ可読媒体。 - 1つまたは複数のプロセッサと、
動作を実行するために前記1つまたは複数のプロセッサのうちの少なくとも1つのプロセッサによって実行可能な命令を記憶した非一時的コンピュータ可読媒体とを含み、前記非一時的コンピュータ可読媒体は、
サンプルの画像のセットを取得することであって、前記画像のセットの各画像が、前記サンプル内のそれぞれの焦点面に対応する、ことと、
前記サンプルの出力画像の各ピクセルに対するそれぞれの深度値を決定するために前記画像のセットの各画像にフィルタを適用することであって、所与の深度値が前記サンプル内の深さを表し、その深さにおいて、前記サンプルの内容物が焦点を合わせて撮像され得る、ことと、
前記出力画像の前記ピクセルの前記深度値に基づいて前記出力画像の各ピクセルに対する画像値を決定することとを含み、前記出力画像の特定のピクセルに対する画像値を決定することが、(i)前記特定のピクセルの前記深度値に対応する前記画像のセットのうちの1つの画像を識別することと、(ii)前記特定のピクセルに対応する前記識別された画像内にロケーションを有する、前記識別された画像のピクセルに基づいて前記特定のピクセルに対する前記画像値を決定することとを含み、
前記動作は、
前記出力画像に基づいて前記サンプルの第1のセグメント化マップを生成することと、
前記決定された深度値に基づいて、前記第1のセグメント化マップの少なくとも1つのセグメントをさらに分割することによって前記サンプルの第2のセグメント化マップを生成することとをさらに含み、
前記第1のセグメント化マップの少なくとも1つのセグメントをさらに分割することが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記決定された深度値から選択することと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別することと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割することとを含む、システム。 - 前記フィルタはテクスチャフィルタであり、前記画像のセットのうちの特定の画像に前記フィルタを適用することが、前記特定の画像の特定のピクセルに対して、前記特定のピクセルの近傍にある前記特定の画像のピクセルの標準偏差、エントロピー、または数値範囲のうちの少なくとも1つを決定することを含む、請求項30に記載のシステム。
- 前記動作は、前記深度値に基づいて前記サンプルに対する深度マップを生成することをさらに含む、請求項30または31に記載のシステム。
- 前記動作は、
前記決定された深度値を空間的に前処理することをさらに含み、前記出力画像の前記ピクセルの前記深度値に基づいて前記出力画像の各ピクセルに対する前記画像値を決定することが、前記出力画像の前記ピクセルの前記空間的に前処理された深度値に基づいて前記出力画像の各ピクセルに対する前記画像値を決定することを含む、請求項30から32のいずれか一項に記載のシステム。 - 前記出力画像の前記特定のピクセルに対する前記画像値を決定することが、(iii)前記特定のピクセルの前記深度値の近傍の中の深度値に対応する前記画像のセットのうちの2つ以上の追加の画像を識別することを付加的に含み、前記特定のピクセルに対応する前記識別された画像内にロケーションを有する、前記識別された画像の前記ピクセルに基づいて前記特定のピクセルに対する前記画像値を決定することが、前記識別された画像と、前記特定のピクセルに対応するそれらのそれぞれの識別された画像内にロケーションを有する前記2つ以上の追加の画像とのピクセル上でピクセルごとの動作を実行することを含む、請求項30から33のいずれか一項に記載のシステム。
- 1つまたは複数のプロセッサと、
動作を実行するために前記1つまたは複数のプロセッサのうちの少なくとも1つのプロセッサによって実行可能な命令を記憶した非一時的コンピュータ可読媒体とを含み、前記非一時的コンピュータ可読媒体は、
サンプルの画像のセットを取得することであって、前記画像のセットの各画像が、前記サンプル内のそれぞれの焦点面に対応する、ことと、
深度マップの各ピクセルに対するそれぞれの深度値を決定するために前記画像のセットの各画像にフィルタを適用することであって、所与の深度値が、前記サンプル内の深さを表し、その深さにおいて、前記サンプルの内容物が焦点を合わせて撮像され得る、ことと、
前記深度マップの対応するピクセルの前記深度値に基づいて、出力画像の各ピクセルに対する画像値を決定することと、
第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記決定された深度値から選択することと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別することと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割することとを含む、システム。 - 前記フィルタはテクスチャフィルタであり、前記画像のセットのうちの特定の画像に前記フィルタを適用することが、前記特定の画像の特定のピクセルに対して、前記特定のピクセルの近傍にある前記特定の画像のピクセルの標準偏差、エントロピー、または数値範囲のうちの少なくとも1つを決定することを含む、請求項35に記載のシステム。
- 前記動作は、
前記出力画像に基づいて前記サンプルの第1のセグメント化マップを生成することと、
前記決定された深度値に基づいて、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することによって前記サンプルの第2のセグメント化マップを生成することとをさらに含む、請求項35または36に記載のシステム。 - 1つまたは複数のプロセッサと、
動作を実行するために前記1つまたは複数のプロセッサのうちの少なくとも1つのプロセッサによって実行可能な命令を記憶した非一時的コンピュータ可読媒体とを含み、前記非一時的コンピュータ可読媒体は、
サンプルの画像を取得することと、
前記サンプルの内容物の深度マップを取得することと、
前記画像に基づいて前記サンプルの第1のセグメント化マップを生成することと、
前記深度マップに基づいて、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することによって前記サンプルの第2のセグメント化マップを生成することとを含み、
前記深度マップは複数の深度値を含み、前記第1のセグメント化マップの少なくとも1つの領域をさらに分割することが、
前記第1のセグメント化マップの特定の領域に対応する深度値のセットを、前記深度値から選択することと、
前記選択された深度値のセット内の少なくとも2つのクラスタを識別することと、
前記識別された少なくとも2つのクラスタに基づいて前記特定の領域をさらに分割することとを含む、システム。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US16/854,710 | 2020-04-21 | ||
| US16/854,710 US11727586B2 (en) | 2020-04-21 | 2020-04-21 | Image processing and segmentation of sets of Z-stacked images of three-dimensional biological samples |
| PCT/US2021/015308 WO2021216158A1 (en) | 2020-04-21 | 2021-01-27 | Image processing and segmentation of sets of z-stacked images of three-dimensional biological samples |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023523003A JP2023523003A (ja) | 2023-06-01 |
| JP7665652B2 true JP7665652B2 (ja) | 2025-04-21 |
Family
ID=74672449
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022564422A Active JP7665652B2 (ja) | 2020-04-21 | 2021-01-27 | 3次元生体サンプルのzスタック画像のセットの画像処理およびセグメント化 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US11727586B2 (ja) |
| EP (1) | EP4139882A1 (ja) |
| JP (1) | JP7665652B2 (ja) |
| KR (1) | KR20230004610A (ja) |
| CN (1) | CN115485714A (ja) |
| WO (1) | WO2021216158A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11501420B2 (en) * | 2019-09-26 | 2022-11-15 | Perkinelmer Cellular Technologies Germany Gmbh | Reconstructing phase images with deep learning |
| EP4361944A1 (en) | 2022-10-31 | 2024-05-01 | Sartorius Stedim Data Analytics AB | Monitoring of biofabrication processes |
| CN116012838B (zh) * | 2022-12-30 | 2023-11-07 | 创芯国际生物科技(广州)有限公司 | 基于人工智能的类器官活性识别方法及系统 |
| CN116602712A (zh) * | 2023-05-25 | 2023-08-18 | 广州斐博生物科技有限公司 | 基于女性阴道分泌物样本评估系统 |
| CN116664642B (zh) * | 2023-05-30 | 2025-02-07 | 易普森生物科技(深圳)有限公司 | 基于相对非均匀高斯模糊的z-stack图像快速配准方法 |
| JP2025024401A (ja) * | 2023-08-07 | 2025-02-20 | 国立大学法人広島大学 | 画像解析装置、画像解析方法およびプログラム、ならびにライトフィールド量子計測システムおよびライトフィールド量子計測方法 |
| KR20250111605A (ko) * | 2024-01-15 | 2025-07-22 | 삼성전자주식회사 | 이미지 분할을 지원하기 위한 전자 장치 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014071207A (ja) | 2012-09-28 | 2014-04-21 | Canon Inc | 画像処理装置、撮像システム、画像処理システム |
| US20150286044A1 (en) | 2012-11-30 | 2015-10-08 | L&T Technology Services Limited | Method and system for extended depth of field calculation for microscopic images |
| JP2017174416A (ja) | 2016-02-29 | 2017-09-28 | トムソン ライセンシングThomson Licensing | 適応的デプスガイドノンフォトリアリスティックレンダリング方法、対応するコンピュータプログラム製品、コンピュータ読取可能搬送媒体及びデバイス |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5878152A (en) | 1997-05-21 | 1999-03-02 | Cognex Corporation | Depth from focal gradient analysis using object texture removal by albedo normalization |
| US7769219B2 (en) * | 2006-12-11 | 2010-08-03 | Cytyc Corporation | Method for assessing image focus quality |
| US8907973B2 (en) * | 2012-10-22 | 2014-12-09 | Stmicroelectronics International N.V. | Content adaptive image restoration, scaling and enhancement for high definition display |
| EP2926558B1 (en) | 2012-11-30 | 2018-01-31 | L & T Technology Services Limited | A method and system for extended depth of field calculation for microscopic images |
| CA3007292A1 (en) * | 2015-12-02 | 2017-06-08 | Clearlight Diagnostics Llc | Methods for preparing and analyzing tumor tissue samples for detection and monitoring of cancers |
| JP6563517B2 (ja) * | 2015-12-08 | 2019-08-21 | オリンパス株式会社 | 顕微鏡観察システム、顕微鏡観察方法、及び顕微鏡観察プログラム |
| EP3296018A1 (en) | 2016-09-19 | 2018-03-21 | Ecole Polytechnique Fédérale de Lausanne (EPFL) | Organoid arrays |
-
2020
- 2020-04-21 US US16/854,710 patent/US11727586B2/en active Active
-
2021
- 2021-01-27 WO PCT/US2021/015308 patent/WO2021216158A1/en not_active Ceased
- 2021-01-27 EP EP21707099.4A patent/EP4139882A1/en active Pending
- 2021-01-27 KR KR1020227039606A patent/KR20230004610A/ko active Pending
- 2021-01-27 JP JP2022564422A patent/JP7665652B2/ja active Active
- 2021-01-27 CN CN202180030161.3A patent/CN115485714A/zh active Pending
-
2023
- 2023-06-20 US US18/211,948 patent/US20230334683A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014071207A (ja) | 2012-09-28 | 2014-04-21 | Canon Inc | 画像処理装置、撮像システム、画像処理システム |
| US20150286044A1 (en) | 2012-11-30 | 2015-10-08 | L&T Technology Services Limited | Method and system for extended depth of field calculation for microscopic images |
| JP2017174416A (ja) | 2016-02-29 | 2017-09-28 | トムソン ライセンシングThomson Licensing | 適応的デプスガイドノンフォトリアリスティックレンダリング方法、対応するコンピュータプログラム製品、コンピュータ読取可能搬送媒体及びデバイス |
Also Published As
| Publication number | Publication date |
|---|---|
| CN115485714A (zh) | 2022-12-16 |
| US11727586B2 (en) | 2023-08-15 |
| US20230334683A1 (en) | 2023-10-19 |
| WO2021216158A1 (en) | 2021-10-28 |
| EP4139882A1 (en) | 2023-03-01 |
| JP2023523003A (ja) | 2023-06-01 |
| US20210327080A1 (en) | 2021-10-21 |
| KR20230004610A (ko) | 2023-01-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7665652B2 (ja) | 3次元生体サンプルのzスタック画像のセットの画像処理およびセグメント化 | |
| US11482320B2 (en) | Transformation of digital pathology images | |
| Hof et al. | Long-term live imaging and multiscale analysis identify heterogeneity and core principles of epithelial organoid morphogenesis | |
| Piccinini | AnaSP: a software suite for automatic image analysis of multicellular spheroids | |
| Li et al. | High-throughput imaging: Focusing in on drug discovery in 3D | |
| Charwat et al. | Potential and limitations of microscopy and Raman spectroscopy for live-cell analysis of 3D cell cultures | |
| US11620751B2 (en) | Image analysis algorithms using control slides | |
| US20130194410A1 (en) | Cell occupancy measurement | |
| Kriston‐Vizi et al. | Getting the whole picture: High content screening using three‐dimensional cellular model systems and whole animal assays | |
| Blasse et al. | PreMosa: extracting 2D surfaces from 3D microscopy mosaics | |
| Taïeb et al. | FUCCItrack: An all-in-one software for single cell tracking and cell cycle analysis | |
| Robinson et al. | Segmentation of image data from complex organotypic 3D models of cancer tissues with Markov random fields | |
| US8693743B1 (en) | Analysis and display of multiple biomarker co-expression in cells and tissues | |
| US11068695B2 (en) | Image processing device, observation device, and program | |
| Krenacs et al. | Digital microscopy: the upcoming revolution in histopathology teaching, diagnostics, research and quality assurance | |
| Debeir et al. | Models of cancer cell migration and cellular imaging and analysis | |
| Shimoni et al. | Normalized polarization ratios for the analysis of cell polarity | |
| CN117831634A (zh) | 一种组织培养分析方法、系统和装置 | |
| Tippani et al. | VistoSeg: processing utilities for high-resolution Visium/Visium-IF images for spatial transcriptomics data | |
| Hoffman et al. | SBI2 HCS/HCA 3D imaging: best practices and unmet needs colloquium | |
| Tóth | Single-cell image analysis and machine learning methods using the cellular microenvironment | |
| Shimoni | TACTICS for bioimaging informatics and analysis of T Cells | |
| Kriston-Vizia et al. | Getting the whole picture: High Content Screening using 3-dimensional cellular model systems and whole animal assays. | |
| Åkerfelt et al. | Segmentation of Image Data from Complex Organotypic 3D Models of Cancer Tissues with Markov Random Fields | |
| HK40035030A (en) | Transformation of digital pathology images |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20240109 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20241111 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241118 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250207 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250311 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250409 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7665652 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |