JP7635582B2 - Acrylic resin, and adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same - Google Patents
Acrylic resin, and adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same Download PDFInfo
- Publication number
- JP7635582B2 JP7635582B2 JP2021035503A JP2021035503A JP7635582B2 JP 7635582 B2 JP7635582 B2 JP 7635582B2 JP 2021035503 A JP2021035503 A JP 2021035503A JP 2021035503 A JP2021035503 A JP 2021035503A JP 7635582 B2 JP7635582 B2 JP 7635582B2
- Authority
- JP
- Japan
- Prior art keywords
- adhesive
- meth
- monomer
- acrylic resin
- acrylic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000001070 adhesive effect Effects 0.000 title claims description 119
- 239000000853 adhesive Substances 0.000 title claims description 116
- 239000004925 Acrylic resin Substances 0.000 title claims description 67
- 229920000178 Acrylic resin Polymers 0.000 title claims description 67
- 239000000203 mixture Substances 0.000 title claims description 64
- 230000000873 masking effect Effects 0.000 title claims description 33
- 239000002313 adhesive film Substances 0.000 title claims description 32
- 239000003522 acrylic cement Substances 0.000 title 1
- 239000000178 monomer Substances 0.000 claims description 123
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 claims description 46
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 claims description 43
- 239000003431 cross linking reagent Substances 0.000 claims description 41
- 239000004820 Pressure-sensitive adhesive Substances 0.000 claims description 34
- 239000012790 adhesive layer Substances 0.000 claims description 15
- 238000007334 copolymerization reaction Methods 0.000 claims description 15
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 15
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 11
- 125000004432 carbon atom Chemical group C* 0.000 claims description 10
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 claims description 9
- 238000004132 cross linking Methods 0.000 claims description 9
- 125000000217 alkyl group Chemical group 0.000 claims description 8
- 239000000126 substance Substances 0.000 claims description 5
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 72
- 239000000243 solution Substances 0.000 description 49
- -1 methacryloyl Chemical group 0.000 description 38
- 239000010408 film Substances 0.000 description 34
- 239000002904 solvent Substances 0.000 description 33
- 238000006243 chemical reaction Methods 0.000 description 29
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 27
- 239000007787 solid Substances 0.000 description 27
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 22
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 21
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 21
- 238000005160 1H NMR spectroscopy Methods 0.000 description 18
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 18
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 18
- 238000005481 NMR spectroscopy Methods 0.000 description 18
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 18
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 18
- IBGBGRVKPALMCQ-UHFFFAOYSA-N 3,4-dihydroxybenzaldehyde Chemical compound OC1=CC=C(C=O)C=C1O IBGBGRVKPALMCQ-UHFFFAOYSA-N 0.000 description 16
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 16
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 16
- WVDDGKGOMKODPV-UHFFFAOYSA-N hydroxymethyl benzene Natural products OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 16
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 14
- 239000007788 liquid Substances 0.000 description 14
- 238000006116 polymerization reaction Methods 0.000 description 14
- KUJZPFLUSFIWHF-UHFFFAOYSA-N S(C)(=O)(=O)O.C(C(=C)C)(=O)OCC Chemical compound S(C)(=O)(=O)O.C(C(=C)C)(=O)OCC KUJZPFLUSFIWHF-UHFFFAOYSA-N 0.000 description 13
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 12
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 12
- 238000000034 method Methods 0.000 description 12
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 12
- 239000000047 product Substances 0.000 description 11
- YQUVCSBJEUQKSH-UHFFFAOYSA-N 3,4-dihydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C(O)=C1 YQUVCSBJEUQKSH-UHFFFAOYSA-N 0.000 description 10
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 10
- 230000007423 decrease Effects 0.000 description 10
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical compound OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 description 10
- 239000010410 layer Substances 0.000 description 10
- 238000002156 mixing Methods 0.000 description 10
- 238000002360 preparation method Methods 0.000 description 10
- 238000012360 testing method Methods 0.000 description 9
- PCYGLFXKCBFGPC-UHFFFAOYSA-N 3,4-Dihydroxy hydroxymethyl benzene Natural products OCC1=CC=C(O)C(O)=C1 PCYGLFXKCBFGPC-UHFFFAOYSA-N 0.000 description 8
- PGNKNFJJYDJGBG-UHFFFAOYSA-N 3,4-bis(1-ethoxyethoxy)benzaldehyde Chemical compound CCOC(C)OC1=CC=C(C=O)C=C1OC(C)OCC PGNKNFJJYDJGBG-UHFFFAOYSA-N 0.000 description 8
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- 235000019445 benzyl alcohol Nutrition 0.000 description 8
- 238000004440 column chromatography Methods 0.000 description 8
- 238000011109 contamination Methods 0.000 description 8
- FJKIXWOMBXYWOQ-UHFFFAOYSA-N ethenoxyethane Chemical compound CCOC=C FJKIXWOMBXYWOQ-UHFFFAOYSA-N 0.000 description 8
- 239000012948 isocyanate Substances 0.000 description 8
- DCUFMVPCXCSVNP-UHFFFAOYSA-N methacrylic anhydride Chemical compound CC(=C)C(=O)OC(=O)C(C)=C DCUFMVPCXCSVNP-UHFFFAOYSA-N 0.000 description 8
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 8
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 7
- 230000032683 aging Effects 0.000 description 7
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 7
- OZAIFHULBGXAKX-VAWYXSNFSA-N AIBN Substances N#CC(C)(C)\N=N\C(C)(C)C#N OZAIFHULBGXAKX-VAWYXSNFSA-N 0.000 description 6
- 239000004593 Epoxy Substances 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 6
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 239000011259 mixed solution Substances 0.000 description 6
- 239000012044 organic layer Substances 0.000 description 6
- 239000003960 organic solvent Substances 0.000 description 6
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 6
- 235000017557 sodium bicarbonate Nutrition 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- 238000003786 synthesis reaction Methods 0.000 description 6
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 5
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 5
- 239000012298 atmosphere Substances 0.000 description 5
- 239000012267 brine Substances 0.000 description 5
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 5
- 229920001971 elastomer Polymers 0.000 description 5
- 229940074391 gallic acid Drugs 0.000 description 5
- 235000004515 gallic acid Nutrition 0.000 description 5
- 239000000499 gel Substances 0.000 description 5
- 150000002513 isocyanates Chemical class 0.000 description 5
- 239000003505 polymerization initiator Substances 0.000 description 5
- 239000005060 rubber Substances 0.000 description 5
- 239000012279 sodium borohydride Substances 0.000 description 5
- 229910000033 sodium borohydride Inorganic materials 0.000 description 5
- 229920002554 vinyl polymer Polymers 0.000 description 5
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- CTENFNNZBMHDDG-UHFFFAOYSA-N Dopamine hydrochloride Chemical compound Cl.NCCC1=CC=C(O)C(O)=C1 CTENFNNZBMHDDG-UHFFFAOYSA-N 0.000 description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 4
- 229960001149 dopamine hydrochloride Drugs 0.000 description 4
- 238000001035 drying Methods 0.000 description 4
- 150000002148 esters Chemical group 0.000 description 4
- 150000002576 ketones Chemical group 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 238000012856 packing Methods 0.000 description 4
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 4
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 4
- ZDYVRSLAEXCVBX-UHFFFAOYSA-N pyridinium p-toluenesulfonate Chemical compound C1=CC=[NH+]C=C1.CC1=CC=C(S([O-])(=O)=O)C=C1 ZDYVRSLAEXCVBX-UHFFFAOYSA-N 0.000 description 4
- 238000010526 radical polymerization reaction Methods 0.000 description 4
- 238000001953 recrystallisation Methods 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 239000000741 silica gel Substances 0.000 description 4
- 229910002027 silica gel Inorganic materials 0.000 description 4
- 229910001220 stainless steel Inorganic materials 0.000 description 4
- 239000010935 stainless steel Substances 0.000 description 4
- DVKJHBMWWAPEIU-UHFFFAOYSA-N toluene 2,4-diisocyanate Chemical compound CC1=CC=C(N=C=O)C=C1N=C=O DVKJHBMWWAPEIU-UHFFFAOYSA-N 0.000 description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 4
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 4
- FKTHNVSLHLHISI-UHFFFAOYSA-N 1,2-bis(isocyanatomethyl)benzene Chemical compound O=C=NCC1=CC=CC=C1CN=C=O FKTHNVSLHLHISI-UHFFFAOYSA-N 0.000 description 3
- LWTJEJCZJFZKEL-UHFFFAOYSA-N 2-chloro-3',4'-dihydroxyacetophenone Chemical compound OC1=CC=C(C(=O)CCl)C=C1O LWTJEJCZJFZKEL-UHFFFAOYSA-N 0.000 description 3
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- 229920000877 Melamine resin Polymers 0.000 description 3
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 3
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 3
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 238000010790 dilution Methods 0.000 description 3
- 239000012895 dilution Substances 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 239000003822 epoxy resin Substances 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 230000009477 glass transition Effects 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 3
- 239000011976 maleic acid Substances 0.000 description 3
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 3
- 229920000647 polyepoxide Polymers 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 239000008213 purified water Substances 0.000 description 3
- 239000003643 water by type Substances 0.000 description 3
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 2
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 2
- SXIFAEWFOJETOA-UHFFFAOYSA-N 4-hydroxy-butyl Chemical group [CH2]CCCO SXIFAEWFOJETOA-UHFFFAOYSA-N 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical compound C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 description 2
- 229920002799 BoPET Polymers 0.000 description 2
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 2
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 239000005057 Hexamethylene diisocyanate Substances 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 2
- YRKCREAYFQTBPV-UHFFFAOYSA-N acetylacetone Chemical compound CC(=O)CC(C)=O YRKCREAYFQTBPV-UHFFFAOYSA-N 0.000 description 2
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 150000001299 aldehydes Chemical class 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 230000005587 bubbling Effects 0.000 description 2
- 238000012662 bulk polymerization Methods 0.000 description 2
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 2
- 239000013522 chelant Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- QSAWQNUELGIYBC-UHFFFAOYSA-N cyclohexane-1,2-dicarboxylic acid Chemical compound OC(=O)C1CCCCC1C(O)=O QSAWQNUELGIYBC-UHFFFAOYSA-N 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- 229910001873 dinitrogen Inorganic materials 0.000 description 2
- CDMADVZSLOHIFP-UHFFFAOYSA-N disodium;3,7-dioxido-2,4,6,8,9-pentaoxa-1,3,5,7-tetraborabicyclo[3.3.1]nonane;decahydrate Chemical compound O.O.O.O.O.O.O.O.O.O.[Na+].[Na+].O1B([O-])OB2OB([O-])OB1O2 CDMADVZSLOHIFP-UHFFFAOYSA-N 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- LEQAOMBKQFMDFZ-UHFFFAOYSA-N glyoxal Chemical compound O=CC=O LEQAOMBKQFMDFZ-UHFFFAOYSA-N 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- RRAMGCGOFNQTLD-UHFFFAOYSA-N hexamethylene diisocyanate Chemical compound O=C=NCCCCCCN=C=O RRAMGCGOFNQTLD-UHFFFAOYSA-N 0.000 description 2
- VKYKSIONXSXAKP-UHFFFAOYSA-N hexamethylenetetramine Chemical compound C1N(C2)CN3CN1CN2C3 VKYKSIONXSXAKP-UHFFFAOYSA-N 0.000 description 2
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 2
- FUZZWVXGSFPDMH-UHFFFAOYSA-M hexanoate Chemical compound CCCCCC([O-])=O FUZZWVXGSFPDMH-UHFFFAOYSA-M 0.000 description 2
- 150000002430 hydrocarbons Chemical group 0.000 description 2
- 238000007654 immersion Methods 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- JDSHMPZPIAZGSV-UHFFFAOYSA-N melamine Chemical compound NC1=NC(N)=NC(N)=N1 JDSHMPZPIAZGSV-UHFFFAOYSA-N 0.000 description 2
- 238000003328 mesylation reaction Methods 0.000 description 2
- SJPFBRJHYRBAGV-UHFFFAOYSA-N n-[[3-[[bis(oxiran-2-ylmethyl)amino]methyl]phenyl]methyl]-1-(oxiran-2-yl)-n-(oxiran-2-ylmethyl)methanamine Chemical compound C1OC1CN(CC=1C=C(CN(CC2OC2)CC2OC2)C=CC=1)CC1CO1 SJPFBRJHYRBAGV-UHFFFAOYSA-N 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 230000000379 polymerizing effect Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 238000006722 reduction reaction Methods 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 235000010339 sodium tetraborate Nutrition 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- FYCFRLZSMPWEPP-ODZAUARKSA-N (z)-but-2-enedioic acid;prop-2-enamide Chemical compound NC(=O)C=C.OC(=O)\C=C/C(O)=O FYCFRLZSMPWEPP-ODZAUARKSA-N 0.000 description 1
- ZXHZWRZAWJVPIC-UHFFFAOYSA-N 1,2-diisocyanatonaphthalene Chemical compound C1=CC=CC2=C(N=C=O)C(N=C=O)=CC=C21 ZXHZWRZAWJVPIC-UHFFFAOYSA-N 0.000 description 1
- 229940058015 1,3-butylene glycol Drugs 0.000 description 1
- CDMDQYCEEKCBGR-UHFFFAOYSA-N 1,4-diisocyanatocyclohexane Chemical compound O=C=NC1CCC(N=C=O)CC1 CDMDQYCEEKCBGR-UHFFFAOYSA-N 0.000 description 1
- SBJCUZQNHOLYMD-UHFFFAOYSA-N 1,5-Naphthalene diisocyanate Chemical compound C1=CC=C2C(N=C=O)=CC=CC2=C1N=C=O SBJCUZQNHOLYMD-UHFFFAOYSA-N 0.000 description 1
- FWWWRCRHNMOYQY-UHFFFAOYSA-N 1,5-diisocyanato-2,4-dimethylbenzene Chemical compound CC1=CC(C)=C(N=C=O)C=C1N=C=O FWWWRCRHNMOYQY-UHFFFAOYSA-N 0.000 description 1
- VZXPHDGHQXLXJC-UHFFFAOYSA-N 1,6-diisocyanato-5,6-dimethylheptane Chemical compound O=C=NC(C)(C)C(C)CCCCN=C=O VZXPHDGHQXLXJC-UHFFFAOYSA-N 0.000 description 1
- UWFRVQVNYNPBEF-UHFFFAOYSA-N 1-(2,4-dimethylphenyl)propan-1-one Chemical compound CCC(=O)C1=CC=C(C)C=C1C UWFRVQVNYNPBEF-UHFFFAOYSA-N 0.000 description 1
- OEURXIFGOPBMJF-UHFFFAOYSA-N 1-o-(2-hydroxyethyl) 2-o-(2-prop-2-enoyloxyethyl) benzene-1,2-dicarboxylate Chemical compound OCCOC(=O)C1=CC=CC=C1C(=O)OCCOC(=O)C=C OEURXIFGOPBMJF-UHFFFAOYSA-N 0.000 description 1
- IVIDDMGBRCPGLJ-UHFFFAOYSA-N 2,3-bis(oxiran-2-ylmethoxy)propan-1-ol Chemical compound C1OC1COC(CO)COCC1CO1 IVIDDMGBRCPGLJ-UHFFFAOYSA-N 0.000 description 1
- VBZBISQOWJYWCC-UHFFFAOYSA-N 2-(2-carboxypropan-2-yldiazenyl)-2-methylpropanoic acid Chemical compound OC(=O)C(C)(C)N=NC(C)(C)C(O)=O VBZBISQOWJYWCC-UHFFFAOYSA-N 0.000 description 1
- JAHNSTQSQJOJLO-UHFFFAOYSA-N 2-(3-fluorophenyl)-1h-imidazole Chemical compound FC1=CC=CC(C=2NC=CN=2)=C1 JAHNSTQSQJOJLO-UHFFFAOYSA-N 0.000 description 1
- KUBDPQJOLOUJRM-UHFFFAOYSA-N 2-(chloromethyl)oxirane;4-[2-(4-hydroxyphenyl)propan-2-yl]phenol Chemical compound ClCC1CO1.C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 KUBDPQJOLOUJRM-UHFFFAOYSA-N 0.000 description 1
- SYEWHONLFGZGLK-UHFFFAOYSA-N 2-[1,3-bis(oxiran-2-ylmethoxy)propan-2-yloxymethyl]oxirane Chemical compound C1OC1COCC(OCC1OC1)COCC1CO1 SYEWHONLFGZGLK-UHFFFAOYSA-N 0.000 description 1
- LCZVSXRMYJUNFX-UHFFFAOYSA-N 2-[2-(2-hydroxypropoxy)propoxy]propan-1-ol Chemical compound CC(O)COC(C)COC(C)CO LCZVSXRMYJUNFX-UHFFFAOYSA-N 0.000 description 1
- AOBIOSPNXBMOAT-UHFFFAOYSA-N 2-[2-(oxiran-2-ylmethoxy)ethoxymethyl]oxirane Chemical compound C1OC1COCCOCC1CO1 AOBIOSPNXBMOAT-UHFFFAOYSA-N 0.000 description 1
- WTYYGFLRBWMFRY-UHFFFAOYSA-N 2-[6-(oxiran-2-ylmethoxy)hexoxymethyl]oxirane Chemical compound C1OC1COCCCCCCOCC1CO1 WTYYGFLRBWMFRY-UHFFFAOYSA-N 0.000 description 1
- BNCADMBVWNPPIZ-UHFFFAOYSA-N 2-n,2-n,4-n,4-n,6-n,6-n-hexakis(methoxymethyl)-1,3,5-triazine-2,4,6-triamine Chemical compound COCN(COC)C1=NC(N(COC)COC)=NC(N(COC)COC)=N1 BNCADMBVWNPPIZ-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- FRIBMENBGGCKPD-UHFFFAOYSA-N 3-(2,3-dimethoxyphenyl)prop-2-enal Chemical compound COC1=CC=CC(C=CC=O)=C1OC FRIBMENBGGCKPD-UHFFFAOYSA-N 0.000 description 1
- RNLHGQLZWXBQNY-UHFFFAOYSA-N 3-(aminomethyl)-3,5,5-trimethylcyclohexan-1-amine Chemical compound CC1(C)CC(N)CC(C)(CN)C1 RNLHGQLZWXBQNY-UHFFFAOYSA-N 0.000 description 1
- OFNISBHGPNMTMS-UHFFFAOYSA-N 3-methylideneoxolane-2,5-dione Chemical compound C=C1CC(=O)OC1=O OFNISBHGPNMTMS-UHFFFAOYSA-N 0.000 description 1
- MECNWXGGNCJFQJ-UHFFFAOYSA-N 3-piperidin-1-ylpropane-1,2-diol Chemical compound OCC(O)CN1CCCCC1 MECNWXGGNCJFQJ-UHFFFAOYSA-N 0.000 description 1
- UPMLOUAZCHDJJD-UHFFFAOYSA-N 4,4'-Diphenylmethane Diisocyanate Chemical compound C1=CC(N=C=O)=CC=C1CC1=CC=C(N=C=O)C=C1 UPMLOUAZCHDJJD-UHFFFAOYSA-N 0.000 description 1
- VFXXTYGQYWRHJP-UHFFFAOYSA-N 4,4'-azobis(4-cyanopentanoic acid) Chemical compound OC(=O)CCC(C)(C#N)N=NC(C)(CCC(O)=O)C#N VFXXTYGQYWRHJP-UHFFFAOYSA-N 0.000 description 1
- OIYTYGOUZOARSH-UHFFFAOYSA-N 4-methoxy-2-methylidene-4-oxobutanoic acid Chemical compound COC(=O)CC(=C)C(O)=O OIYTYGOUZOARSH-UHFFFAOYSA-N 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- 239000004342 Benzoyl peroxide Substances 0.000 description 1
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- RPNUMPOLZDHAAY-UHFFFAOYSA-N Diethylenetriamine Chemical compound NCCNCCN RPNUMPOLZDHAAY-UHFFFAOYSA-N 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 239000005058 Isophorone diisocyanate Substances 0.000 description 1
- YIVJZNGAASQVEM-UHFFFAOYSA-N Lauroyl peroxide Chemical compound CCCCCCCCCCCC(=O)OOC(=O)CCCCCCCCCCC YIVJZNGAASQVEM-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 1
- WSMYVTOQOOLQHP-UHFFFAOYSA-N Malondialdehyde Chemical compound O=CCC=O WSMYVTOQOOLQHP-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 1
- WRQNANDWMGAFTP-UHFFFAOYSA-N Methylacetoacetic acid Chemical compound COC(=O)CC(C)=O WRQNANDWMGAFTP-UHFFFAOYSA-N 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 239000004721 Polyphenylene oxide Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- PCSMJKASWLYICJ-UHFFFAOYSA-N Succinic aldehyde Chemical compound O=CCCC=O PCSMJKASWLYICJ-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 description 1
- MZVQCMJNVPIDEA-UHFFFAOYSA-N [CH2]CN(CC)CC Chemical group [CH2]CN(CC)CC MZVQCMJNVPIDEA-UHFFFAOYSA-N 0.000 description 1
- 239000006096 absorbing agent Substances 0.000 description 1
- IKHGUXGNUITLKF-XPULMUKRSA-N acetaldehyde Chemical compound [14CH]([14CH3])=O IKHGUXGNUITLKF-XPULMUKRSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 125000004018 acid anhydride group Chemical group 0.000 description 1
- 239000002390 adhesive tape Substances 0.000 description 1
- 239000005456 alcohol based solvent Substances 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 229920003180 amino resin Polymers 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 230000003712 anti-aging effect Effects 0.000 description 1
- 229910052787 antimony Inorganic materials 0.000 description 1
- WATWJIUSRGPENY-UHFFFAOYSA-N antimony atom Chemical compound [Sb] WATWJIUSRGPENY-UHFFFAOYSA-N 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 239000003849 aromatic solvent Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- FFBZKUHRIXKOSY-UHFFFAOYSA-N aziridine-1-carboxamide Chemical compound NC(=O)N1CC1 FFBZKUHRIXKOSY-UHFFFAOYSA-N 0.000 description 1
- 235000019400 benzoyl peroxide Nutrition 0.000 description 1
- OHJMTUPIZMNBFR-UHFFFAOYSA-N biuret Chemical group NC(=O)NC(N)=O OHJMTUPIZMNBFR-UHFFFAOYSA-N 0.000 description 1
- 235000019437 butane-1,3-diol Nutrition 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical group OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 1
- 238000010382 chemical cross-linking Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- LDHQCZJRKDOVOX-NSCUHMNNSA-N crotonic acid Chemical compound C\C=C\C(O)=O LDHQCZJRKDOVOX-NSCUHMNNSA-N 0.000 description 1
- LSXWFXONGKSEMY-UHFFFAOYSA-N di-tert-butyl peroxide Chemical compound CC(C)(C)OOC(C)(C)C LSXWFXONGKSEMY-UHFFFAOYSA-N 0.000 description 1
- 238000007607 die coating method Methods 0.000 description 1
- GPLRAVKSCUXZTP-UHFFFAOYSA-N diglycerol Chemical compound OCC(O)COCC(O)CO GPLRAVKSCUXZTP-UHFFFAOYSA-N 0.000 description 1
- CZZYITDELCSZES-UHFFFAOYSA-N diphenylmethane Chemical compound C=1C=CC=CC=1CC1=CC=CC=C1 CZZYITDELCSZES-UHFFFAOYSA-N 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 238000007720 emulsion polymerization reaction Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 125000003700 epoxy group Chemical group 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- 239000003759 ester based solvent Substances 0.000 description 1
- UIWXSTHGICQLQT-UHFFFAOYSA-N ethenyl propanoate Chemical compound CCC(=O)OC=C UIWXSTHGICQLQT-UHFFFAOYSA-N 0.000 description 1
- XYIBRDXRRQCHLP-UHFFFAOYSA-N ethyl acetoacetate Chemical compound CCOC(=O)CC(C)=O XYIBRDXRRQCHLP-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- JGEMYUOFGVHXKV-OWOJBTEDSA-N fumaraldehyde Chemical compound O=C\C=C\C=O JGEMYUOFGVHXKV-OWOJBTEDSA-N 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- NKHAVTQWNUWKEO-UHFFFAOYSA-N fumaric acid monomethyl ester Natural products COC(=O)C=CC(O)=O NKHAVTQWNUWKEO-UHFFFAOYSA-N 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000003292 glue Substances 0.000 description 1
- 229960000587 glutaral Drugs 0.000 description 1
- 125000003055 glycidyl group Chemical group C(C1CO1)* 0.000 description 1
- 229940015043 glyoxal Drugs 0.000 description 1
- 238000007756 gravure coating Methods 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 239000011256 inorganic filler Substances 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- ZFSLODLOARCGLH-UHFFFAOYSA-N isocyanuric acid Chemical group OC1=NC(O)=NC(O)=N1 ZFSLODLOARCGLH-UHFFFAOYSA-N 0.000 description 1
- NIMLQBUJDJZYEJ-UHFFFAOYSA-N isophorone diisocyanate Chemical compound CC1(C)CC(N=C=O)CC(C)(CN=C=O)C1 NIMLQBUJDJZYEJ-UHFFFAOYSA-N 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 239000005453 ketone based solvent Substances 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- 239000004611 light stabiliser Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 1
- 229940118019 malondialdehyde Drugs 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 125000005395 methacrylic acid group Chemical group 0.000 description 1
- WSFSSNUMVMOOMR-NJFSPNSNSA-N methanone Chemical compound O=[14CH2] WSFSSNUMVMOOMR-NJFSPNSNSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- NKHAVTQWNUWKEO-IHWYPQMZSA-N methyl hydrogen fumarate Chemical compound COC(=O)\C=C/C(O)=O NKHAVTQWNUWKEO-IHWYPQMZSA-N 0.000 description 1
- LVHBHZANLOWSRM-UHFFFAOYSA-N methylenebutanedioic acid Natural products OC(=O)CC(=C)C(O)=O LVHBHZANLOWSRM-UHFFFAOYSA-N 0.000 description 1
- OMNKZBIFPJNNIO-UHFFFAOYSA-N n-(2-methyl-4-oxopentan-2-yl)prop-2-enamide Chemical compound CC(=O)CC(C)(C)NC(=O)C=C OMNKZBIFPJNNIO-UHFFFAOYSA-N 0.000 description 1
- YVOQADGLLJCMOE-UHFFFAOYSA-N n-[6-(aziridine-1-carbonylamino)hexyl]aziridine-1-carboxamide Chemical compound C1CN1C(=O)NCCCCCCNC(=O)N1CC1 YVOQADGLLJCMOE-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 239000012788 optical film Substances 0.000 description 1
- 239000012766 organic filler Substances 0.000 description 1
- 150000001451 organic peroxides Chemical class 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000011236 particulate material Substances 0.000 description 1
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 239000002985 plastic film Substances 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920001225 polyester resin Polymers 0.000 description 1
- 239000004645 polyester resin Substances 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 229920000223 polyglycerol Polymers 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- HJWLCRVIBGQPNF-UHFFFAOYSA-N prop-2-enylbenzene Chemical compound C=CCC1=CC=CC=C1 HJWLCRVIBGQPNF-UHFFFAOYSA-N 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 239000007870 radical polymerization initiator Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 239000013557 residual solvent Substances 0.000 description 1
- 238000005096 rolling process Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000010557 suspension polymerization reaction Methods 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- UWHCKJMYHZGTIT-UHFFFAOYSA-N tetraethylene glycol Chemical compound OCCOCCOCCOCCO UWHCKJMYHZGTIT-UHFFFAOYSA-N 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 239000011135 tin Substances 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- RUELTTOHQODFPA-UHFFFAOYSA-N toluene 2,6-diisocyanate Chemical compound CC1=C(N=C=O)C=CC=C1N=C=O RUELTTOHQODFPA-UHFFFAOYSA-N 0.000 description 1
- LDHQCZJRKDOVOX-UHFFFAOYSA-N trans-crotonic acid Natural products CC=CC(O)=O LDHQCZJRKDOVOX-UHFFFAOYSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- GPPXJZIENCGNKB-UHFFFAOYSA-N vanadium Chemical compound [V]#[V] GPPXJZIENCGNKB-UHFFFAOYSA-N 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 238000004383 yellowing Methods 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 229910052726 zirconium Inorganic materials 0.000 description 1
Landscapes
- Compositions Of Macromolecular Compounds (AREA)
- Adhesive Tapes (AREA)
- Adhesives Or Adhesive Processes (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
本発明は、アクリル系樹脂、および、これを用いてなる粘着剤組成物、粘着剤、粘着フィルム、マスキング用粘着剤、マスキング用粘着フィルムに関するものである。詳しくは、湿潤面に貼った場合においても充分な粘着力を有し、さらにマスキング用粘着剤として用いた場合にも、被着体表面に、糊残りのない被着体耐汚染性に優れる粘着剤を得ることができるアクリル系樹脂、および、これを用いてなる粘着剤組成物、上記粘着剤組成物が架橋されてなるマスキング用粘着剤等の粘着剤、上記粘着剤からなる粘着剤層を有するマスキング用粘着フィルム等の粘着フィルムに関するものである。 The present invention relates to an acrylic resin, and an adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same. More specifically, the present invention relates to an acrylic resin that can provide an adhesive that has sufficient adhesive strength even when applied to a wet surface, and that has excellent resistance to contamination of the adherend without leaving any adhesive residue on the adherend surface when used as a masking adhesive, and to an adhesive composition made using the same, an adhesive such as a masking adhesive formed by crosslinking the adhesive composition, and an adhesive film such as a masking adhesive film having an adhesive layer made of the adhesive.
近年、粘着テープは、作業性が良好で接着の信頼性が高い接合手段として、家電製品や自動車、OA機器、建築などの各種産業分野で利用されている。また近年、水中や湿潤条件下でも、充分な粘着性能を発揮できる粘着剤が求められている。しかし、一般に接着対象の表面が濡れていると、充分な粘着性能を得ることが困難である。 In recent years, adhesive tapes have been used in a variety of industrial fields, including home appliances, automobiles, office equipment, and construction, as a joining method with good workability and highly reliable adhesion. In addition, there has been a demand in recent years for adhesives that can demonstrate sufficient adhesive performance even under water or wet conditions. However, it is generally difficult to achieve sufficient adhesive performance when the surface of the object to be bonded is wet.
このような状況のもと、例えば、特許文献1では、結露面や湿潤面に対する良好な初期粘着力を発現でき、また定荷重剥離性に優れた水分散型粘着剤組成物及び粘着製品として、アクリル系又はゴム系の水分散型粘着剤組成物中の固形分100重量部に対して、特定の親水性ポリマーを0.5~15重量部含有することを特徴とする水分散型粘着剤組成物が開示されている。 Under these circumstances, for example, Patent Document 1 discloses a water-dispersible pressure-sensitive adhesive composition and adhesive product that can exhibit good initial adhesive strength on condensation-covered or wet surfaces and has excellent constant-load peelability, the water-dispersible pressure-sensitive adhesive composition being characterized by containing 0.5 to 15 parts by weight of a specific hydrophilic polymer per 100 parts by weight of the solid content of the acrylic or rubber-based water-dispersible pressure-sensitive adhesive composition.
しかし、特許文献1に開示の粘着剤組成物は、分散剤に水溶性樹脂を用いた水分散型の粘着剤組成物であることから、水中や湿潤条件下で長期的に使用した場合、粘着剤が水中に溶けてしまい、粘着性能を維持できないおそれがある。 However, the adhesive composition disclosed in Patent Document 1 is a water-dispersed adhesive composition that uses a water-soluble resin as a dispersant, and therefore there is a risk that the adhesive will dissolve in water and will not be able to maintain its adhesive performance if used for a long period of time in water or under humid conditions.
特許文献2では、湿潤面に被着対象物を確実にかつ簡便に配置することができる湿潤面貼着用粘着シートとして、粘着剤層の片面に吸水層があり、粘着剤層に隙間を作ることで、湿潤面の水分は吸水層に吸収され、良好な粘着力を発現できる、湿潤面貼着用粘着シートが開示されている。しかしながら、上記粘着剤層に隙間があるため、粘着力が低下する場合がある。 Patent Document 2 discloses an adhesive sheet for application to wet surfaces that allows an object to be placed reliably and easily on a wet surface, and has a water-absorbing layer on one side of the adhesive layer, and by creating gaps in the adhesive layer, moisture on the wet surface is absorbed by the water-absorbing layer, thereby achieving good adhesive strength. However, because there are gaps in the adhesive layer, the adhesive strength may decrease.
また、上記特許文献1および2に開示の技術においては、一時保護用(マスキング用)の粘着剤として使用して被着体に粘着させた後に剥離した際に、被着体表面に、糊残り、および貼り跡が生じるのを防ぐという、被着体耐汚染性については、全く考慮されてなかった。 Furthermore, the technologies disclosed in Patent Documents 1 and 2 above do not take into consideration the contamination resistance of the adherend, which would prevent adhesive residue and marks from being left on the adherend surface when the adhesive is used as a temporary protective (masking) adhesive and adhered to the adherend and then peeled off.
そこで、本発明は、このような背景下において、湿潤面に貼った場合においても充分な粘着力を有し、さらにマスキング用粘着剤として用いた場合に、被着体表面に、糊残りのない被着体耐汚染性に優れる粘着剤を得ることを可能とするアクリル系樹脂の提供を目的とするものである。さらにかかるアクリル系樹脂を用いてなる粘着剤組成物、粘着剤、粘着フィルム、マスキング用粘着剤、マスキング用粘着フィルムの提供を目的とするものである。 In light of this background, the present invention aims to provide an acrylic resin that has sufficient adhesive strength even when applied to a wet surface, and that, when used as a masking adhesive, makes it possible to obtain an adhesive that leaves no adhesive residue on the surface of the adherend and has excellent resistance to contamination of the adherend. It also aims to provide an adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film that use such an acrylic resin.
本発明者らは、前記課題を解決するため鋭意研究を重ねた。その研究の過程で、粘着剤組成物の材料であるアクリル系樹脂(A)を構成する共重合成分(a)において、炭素数1~20のアルキル基を有する(メタ)アクリル酸アルキルエステルモノマー(a3)を主体とし、それに対し少量の、水酸基および/またはカルボキシ基を有する共重合性モノマー(a2)と、一般式(1)で表される特定のアクリル系モノマー(a1)とを併用することにより、水中や湿潤条件下での粘着性能が改善されることを突き止め、本発明に到達した。 The present inventors have conducted extensive research to solve the above problems. In the course of their research, they discovered that the adhesive performance in water or under wet conditions can be improved by using a copolymerization component (a) constituting the acrylic resin (A), which is a material for the adhesive composition, that is mainly composed of (meth)acrylic acid alkyl ester monomer (a3) having an alkyl group with 1 to 20 carbon atoms, in combination with a small amount of a copolymerizable monomer (a2) having a hydroxyl group and/or a carboxyl group, and a specific acrylic monomer (a1) represented by general formula (1), and thus arrived at the present invention.
しかるに、本発明は、以下の[1]~[8]を、その要旨とする。
[1] 下記の一般式(1)に示すアクリル系モノマー(a1)0.01~50重量%と、上記(a1)を除いた水酸基および/またはカルボキシ基を有する共重合性モノマー(a2)0.1~30重量%と、炭素数1~20のアルキル基を有する(メタ)アクリル酸アルキルエステルモノマー(a3)40~99重量%とを含む共重合成分(a)を共重合してなることを特徴とするアクリル系樹脂(A)。
[3] 上記水酸基および/またはカルボキシ基を有する共重合性モノマー(a2)が、(メタ)アクリル酸および/または(メタ)アクリレート系モノマーであることを特徴とする、[1]または[2]に記載のアクリル系樹脂(A)。
[4] [1]~[3]のいずれかに記載のアクリル系樹脂(A)と、架橋剤(B)とを含有することを特徴とする粘着剤組成物。
[5] [4]に記載の粘着剤組成物が架橋されてなることを特徴とする粘着剤。
[6] [5]に記載の粘着剤からなる粘着剤層を有することを特徴とする粘着フィルム。
[7] [5]に記載の粘着剤を用いてなることを特徴とするマスキング用粘着剤。
[8] [5]に記載の粘着剤からなる粘着剤層を有することを特徴とするマスキング用粘着フィルム。
Therefore, the present invention relates to the following [1] to [8].
[1] An acrylic resin (A) obtained by copolymerizing a copolymerization component (a) containing 0.01 to 50% by weight of an acrylic monomer (a1) represented by the following general formula (1), 0.1 to 30% by weight of a copolymerizable monomer (a2) having a hydroxyl group and/or a carboxyl group excluding the above (a1), and 40 to 99% by weight of a (meth)acrylic acid alkyl ester monomer (a3) having an alkyl group having 1 to 20 carbon atoms:
[3] The acrylic resin (A) according to [1] or [2], characterized in that the copolymerizable monomer (a2) having a hydroxyl group and/or a carboxyl group is (meth)acrylic acid and/or a (meth)acrylate monomer.
[4] A pressure-sensitive adhesive composition comprising the acrylic resin (A) according to any one of [1] to [3] and a crosslinking agent (B).
[5] A pressure-sensitive adhesive obtained by crosslinking the pressure-sensitive adhesive composition according to [4].
[6] An adhesive film having an adhesive layer made of the adhesive according to [5].
[7] A masking adhesive comprising the adhesive according to [5].
[8] A masking adhesive film having an adhesive layer made of the adhesive according to [5].
本発明のアクリル系樹脂(A)は、湿潤面に貼った場合においても充分な粘着力を有し、さらにマスキング用粘着剤として用いた場合に、被着体表面に、糊残りのない被着体耐汚染性に優れる粘着剤を得ることができる。そのため、上記アクリル系樹脂を用いてなる粘着剤組成物、粘着剤、粘着フィルム、マスキング用粘着剤、およびマスキング用粘着フィルムは、水中や湿潤条件下での使用において優れた粘着性能を発揮することができる。 The acrylic resin (A) of the present invention has sufficient adhesive strength even when applied to a wet surface, and when used as a masking adhesive, it is possible to obtain an adhesive that has excellent resistance to contamination of the adherend and leaves no adhesive residue on the adherend surface. Therefore, the adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the above acrylic resin can exhibit excellent adhesive performance when used under water or under wet conditions.
以下に、本発明を詳細に説明するが、これらは望ましい実施態様の一例を示すものである。
なお、「(メタ)アクリル」とはアクリルあるいはメタクリルを、「(メタ)アクリロイル」とはアクリロイルあるいはメタクリロイルを、「(メタ)アクリレート」とはアクリレートあるいはメタクリレートをそれぞれ意味するものである。また、「アクリル系樹脂」とは、少なくとも1種の(メタ)アクリレート系モノマーを含む重合成分を重合して得られる樹脂である。
また、本発明でいう「粘着剤」とは25℃(室温)でタックを有し、手で押しつける程度の軽い圧力で被着体と接着するものであり、「フィルム」とは、シート、フィルム、テープを概念的に包含するものである。
The present invention will be described in detail below, but these are merely examples of preferred embodiments.
In addition, "(meth)acrylic" means acrylic or methacrylic, "(meth)acryloyl" means acryloyl or methacryloyl, and "(meth)acrylate" means acrylate or methacrylate, respectively. In addition, "acrylic resin" is a resin obtained by polymerizing a polymerization component containing at least one (meth)acrylate monomer.
In addition, the "adhesive" in the present invention is one that has tack at 25°C (room temperature) and adheres to an adherend with light pressure, such as that applied by hand, and the "film" conceptually encompasses sheets, films, and tapes.
<アクリル系樹脂(A)>
本発明のアクリル系樹脂(A)は、先に述べたように、下記の一般式(1)に示すアクリル系モノマー(a1)0.01~50重量%と、上記(a1)を除いた水酸基および/またはカルボキシ基を有する共重合性モノマー(a2)0.1~30重量%と、炭素数1~20のアルキル基を有する(メタ)アクリル酸アルキルエステルモノマー(a3)40~99重量%とを含む共重合成分(a)を共重合してなるものである。
<Acrylic resin (A)>
As described above, the acrylic resin (A) of the present invention is obtained by copolymerizing a copolymerization component (a) containing 0.01 to 50% by weight of an acrylic monomer (a1) represented by the following general formula (1), 0.1 to 30% by weight of a copolymerizable monomer (a2) having a hydroxyl group and/or a carboxyl group excluding the above (a1), and 40 to 99% by weight of a (meth)acrylic acid alkyl ester monomer (a3) having an alkyl group having 1 to 20 carbon atoms.
以下に、上記アクリル系樹脂(A)の共重合成分(a)である、上記の一般式(1)に示すアクリル系モノマー(a1)(以下、単にモノマー(a1)ということがある。)、上記(a1)を除いた水酸基および/またはカルボキシ基を有する共重合性モノマー(a2)(以下、単にモノマー(a2)ということがある。)、炭素数1~20のアルキル基を有する(メタ)アクリル酸アルキルエステルモノマー(a3)(以下、単にモノマー(a3)ということがある。)、任意成分であるその他のモノマー(a4)(以下、単にモノマー(a4)ということがある。)について、順に説明する。 The copolymerization components (a) of the acrylic resin (A) are the acrylic monomer (a1) shown in the above general formula (1) (hereinafter, sometimes simply referred to as monomer (a1)), the copolymerizable monomer (a2) having a hydroxyl group and/or a carboxyl group excluding the above (a1) (hereinafter, sometimes simply referred to as monomer (a2)), the (meth)acrylic acid alkyl ester monomer (a3) having an alkyl group having 1 to 20 carbon atoms (hereinafter, sometimes simply referred to as monomer (a3)), and the optional other monomer (a4) (hereinafter, sometimes simply referred to as monomer (a4)).
〔モノマー(a1)〕
上記モノマー(a1)は、下記の一般式(1)に示すアクリル系モノマーである。
[Monomer (a1)]
The monomer (a1) is an acrylic monomer represented by the following general formula (1).
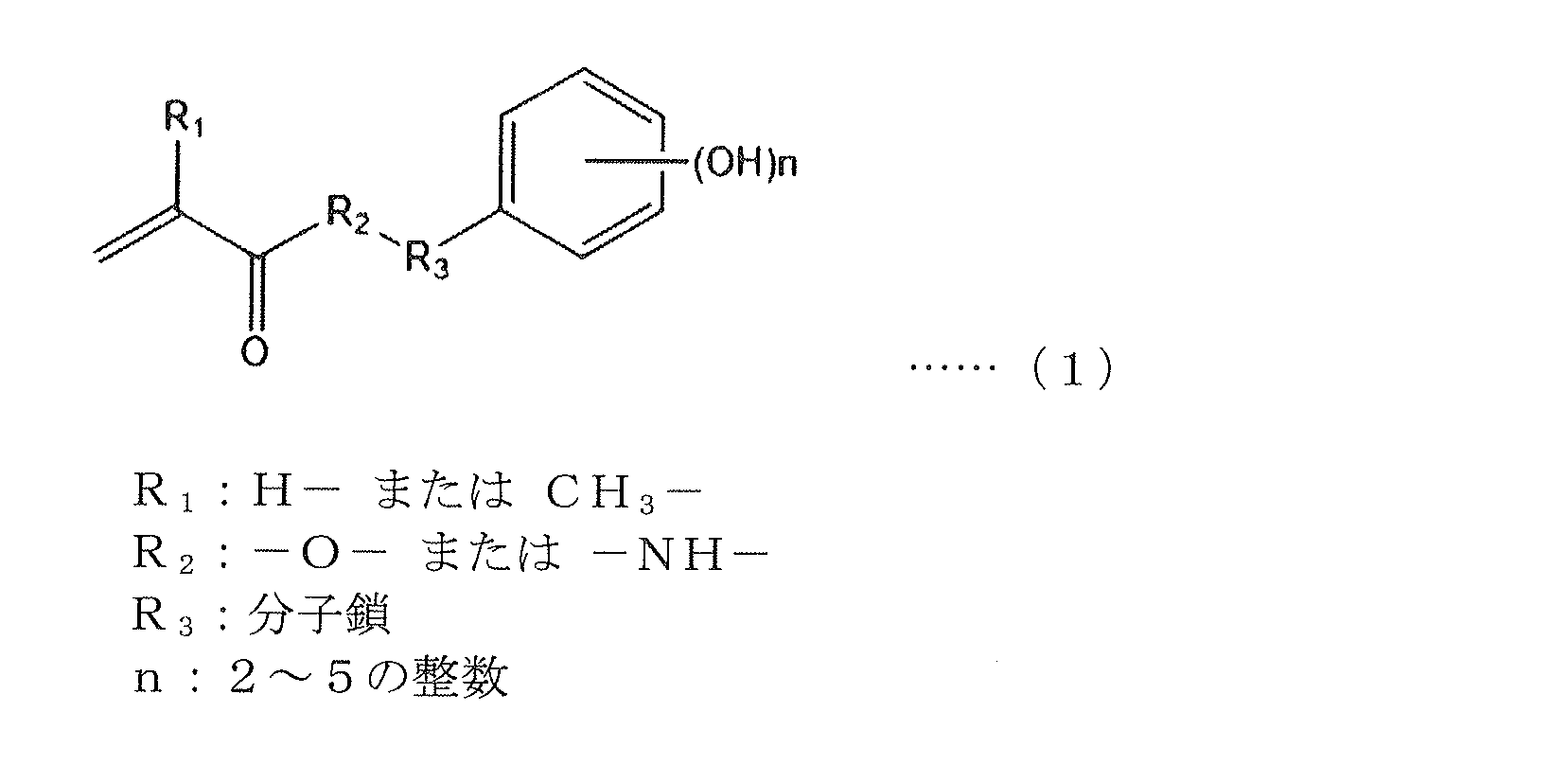
上記一般式(1)において、R1は、H- または CH3-であり、好ましくはCH3―である。R2は、-O- または -NH-であり、好ましくは、-O-である。R3は、分子鎖であり、好ましくは、ケトン構造(―C(=O)―)、エステル構造(―O―C(=O)―、―C(=O)―O―)、および炭化水素構造からなる群から選ばれた少なくとも一つを有する分子鎖である。なかでも、ケトン構造(―C(=O)―)およびエステル構造(―O―C(=O)―、―C(=O)―O―)を有する分子鎖であることが、より好ましい。なお、R3は、通常、炭素数1~5の分子鎖であり、好ましくは炭素数1~3の分子鎖である。nは、2~5の整数であり、好ましくは2または3である。
上記モノマー(a1)は、カテコール基、またはガロール基を有することが好ましい。
すなわち、上記のようにR1~R3やnが規定されていると、湿潤面に貼った場合の粘着力が、より良好なものとなる。
In the above general formula (1), R 1 is H- or CH 3 -, preferably CH 3 -. R 2 is -O- or -NH-, preferably -O-. R 3 is a molecular chain, preferably a molecular chain having at least one selected from the group consisting of a ketone structure (-C(=O)-), an ester structure (-O-C(=O)-, -C(=O)-O-), and a hydrocarbon structure. In particular, a molecular chain having a ketone structure (-C(=O)-) or an ester structure (-O-C(=O)-, -C(=O)-O-) is more preferable. R 3 is usually a molecular chain having 1 to 5 carbon atoms, preferably a molecular chain having 1 to 3 carbon atoms. n is an integer of 2 to 5, preferably 2 or 3.
The monomer (a1) preferably has a catechol group or a gallol group.
That is, when R 1 to R 3 and n are specified as above, the adhesive strength when applied to a wet surface is improved.
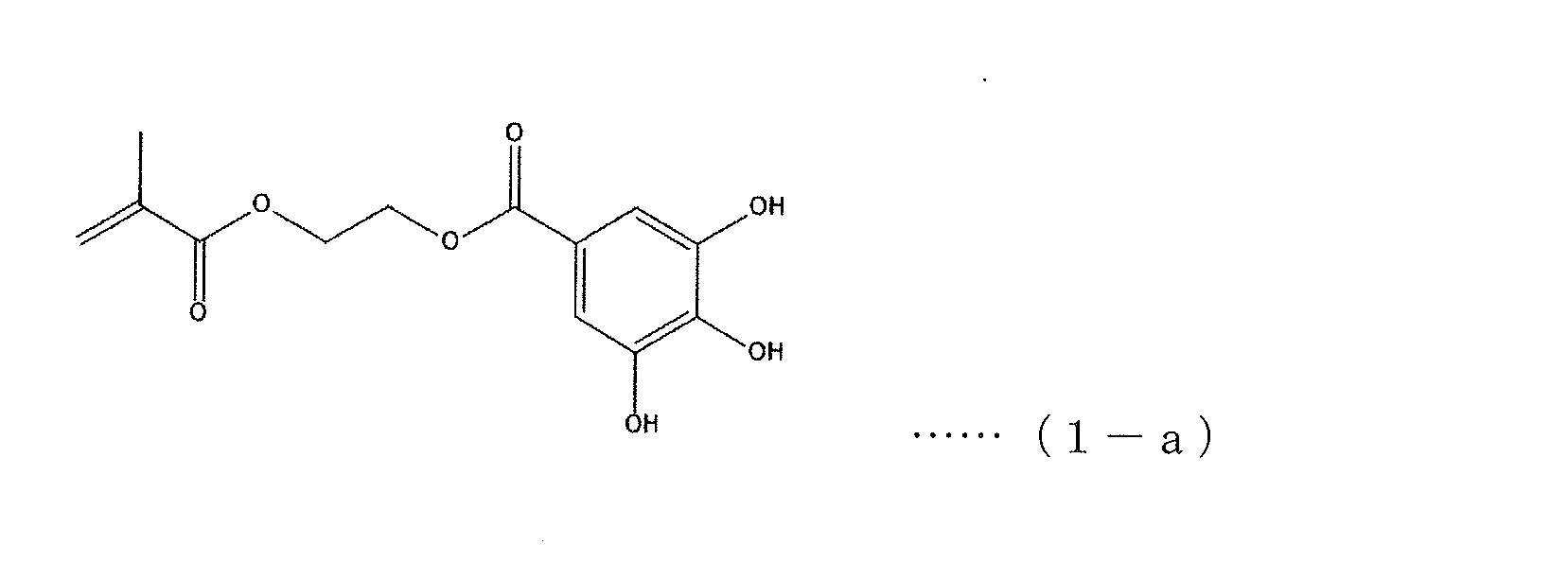
そして、上記一般式(1)に示すモノマーは、具体的には、下記に列記した化学式(1-a)~(1-e)に示されるモノマー(アクリル系モノマー(1-a)~(1-e))が、単独でもしくは二種以上併せて用いられる。なかでも、化学式(1-a),(1-b)に示されるモノマー(アクリル系モノマー(1-a)、アクリル系モノマー(1-b)が、本発明に要求される水中や湿潤条件下での粘着性能がより良好なものとなるため、好ましい。 The monomers shown in the above general formula (1) are specifically the monomers shown in the chemical formulas (1-a) to (1-e) listed below (acrylic monomers (1-a) to (1-e)), which are used alone or in combination of two or more. Among them, the monomers shown in the chemical formulas (1-a) and (1-b) (acrylic monomer (1-a) and acrylic monomer (1-b) are preferred because they provide better adhesive performance in water or under wet conditions, which is required in the present invention.
上記アクリル系樹脂(A)を構成するモノマー(a1)において、上記アクリル系モノマー(1-a)~(1-e)は、それぞれ単独で用いてもよく、併用してもよい。
また、本発明に要求される水中や湿潤条件下での粘着性能を良好なものにする観点から、上記共重合成分(a)全体に対する、上記アクリル系モノマー(1-a)~(1-e)の合計割合は、0.01~50重量%であることが好ましく、0.1~40重量%であることがより好ましく、0.5~30重量%であることが更に好ましく、0.9~20重量%であることが特に好ましい。
In the monomer (a1) constituting the acrylic resin (A), the acrylic monomers (1-a) to (1-e) may be used alone or in combination.
From the viewpoint of improving the adhesive performance in water or under wet conditions required in the present invention, the total proportion of the acrylic monomers (1-a) to (1-e) relative to the entire copolymerization component (a) is preferably 0.01 to 50% by weight, more preferably 0.1 to 40% by weight, even more preferably 0.5 to 30% by weight, and particularly preferably 0.9 to 20% by weight.
また、本発明に要求される水中や湿潤条件下での粘着性能を良好なものにする観点から、アクリル系樹脂(A)中で、上記アクリル系モノマー(1-a)~(1-e)の合計割合は、0.01~50モル%であることが好ましく、0.05~20モル%であることがより好ましく、0.1~10モル%であることが更に好ましく、0.5~3モル%であることが特に好ましい。 In addition, from the viewpoint of improving the adhesive performance under water or wet conditions required by the present invention, the total proportion of the acrylic monomers (1-a) to (1-e) in the acrylic resin (A) is preferably 0.01 to 50 mol%, more preferably 0.05 to 20 mol%, even more preferably 0.1 to 10 mol%, and particularly preferably 0.5 to 3 mol%.
ここで、上記アクリル系モノマー(1-a)~(1-e)は、例えば、以下ように製造することができる。 Here, the acrylic monomers (1-a) to (1-e) can be produced, for example, as follows:
[アクリル系モノマー(1-a)の製造]
上記アクリル系モノマー(1-a)は、例えば、下記の反応式の通り、2-ヒドロキシエチルメタクリレートのメシル化により、メタンスルホン酸-2-エチルメタクリレートを得た後、上記メタンスルホン酸-2-エチルメタクリレートと没食子酸とを反応させることにより、合成することができる。
[Production of acrylic monomer (1-a)]
The acrylic monomer (1-a) can be synthesized, for example, by obtaining methanesulfonate-2-ethyl methacrylate by mesylation of 2-hydroxyethyl methacrylate, and then reacting the methanesulfonate-2-ethyl methacrylate with gallic acid, as shown in the following reaction formula.
2-ヒドロキシエチルメタクリレートのメシル化は、2-ヒドロキシエチルメタクリレートをテトラヒドロフラン等の溶媒に溶解させ、トリエチルアミンとの混合液を得る。かかる混合液に対し、メタンスルホニルクロリドを加え、反応させる。
かかる2-ヒドロキシエチルメタクリレートとメタンスルホニルクロリドの配合モル比は、2-ヒドロキシエチルメタクリレート:メタンスルホニルクロリド=1:1.1~1:1.3程度である。
The mesylation of 2-hydroxyethyl methacrylate is carried out by dissolving 2-hydroxyethyl methacrylate in a solvent such as tetrahydrofuran to obtain a mixture with triethylamine, and then adding methanesulfonyl chloride to the mixture to cause a reaction.
The molar ratio of 2-hydroxyethyl methacrylate to methanesulfonyl chloride is about 1:1.1 to 1:1.3.
上記反応後の混合液の溶媒を除去することにより、メタンスルホン酸-2-エチルメタクリレート(黄色液体物)を得ることができる。 By removing the solvent from the mixture after the above reaction, methanesulfonic acid-2-ethyl methacrylate (yellow liquid) can be obtained.
なお、上述の黄色液体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,CDCl3): δ=6.08(s、1H)、5.57-5.54(m、1H)、4.41-4.37(m、2H)、4.35-4.31(m、2H)、2.98(s、3H)、1.88(s、3H)
The results of 1 H NMR analysis of the above yellow liquid are as follows:
1H NMR (400MHz, CDCl3): δ = 6.08 (s, 1H), 5.57-5.54 (m, 1H), 4.41-4.37 (m, 2H), 4.35-4.31 (m, 2H), 2.98 (s, 3H), 1.88 (s, 3H)
つぎに没食子酸と炭酸水素ナトリウムとジメチルスルホキシド(DMSO)の溶液を作製し、メタンスルホン酸-2-エチルメタクリレートを加え、反応させる。
かかるメタンスルホン酸-2-エチルメタクリレートと没食子酸の配合モル比は、メタンスルホン酸-2-エチルメタクリレート:没食子酸=1:1.1~1:1.3程度である。
その後、溶媒を除去し、カラムクロマトグラフィで精製し、さらに酢酸エチル/n-ヘプタンの溶液で再結晶化を行う事で、上記アクリル系モノマー(1-a)(白色固体物)を得ることができる。
Next, a solution of gallic acid, sodium hydrogen carbonate, and dimethyl sulfoxide (DMSO) is prepared, and methanesulfonate-2-ethyl methacrylate is added and reacted.
The molar ratio of methanesulfonate-2-ethyl methacrylate to gallic acid is methanesulfonate-2-ethyl methacrylate:gallic acid=about 1:1.1 to 1:1.3.
Thereafter, the solvent is removed, the residue is purified by column chromatography, and then recrystallized from a solution of ethyl acetate/n-heptane to obtain the acrylic monomer (1-a) (white solid).
なお、上記白色固体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,DMSO-d6): δ=9.22(s、3H)、6.94(s、2H)、6.05-6.02(m、1H)、5.71-5.67(m、1H)、4.46-4.36(m、4H)、1.87(t、3H)
The results of 1 H NMR analysis of the above white solid are as follows:
1H NMR (400MHz, DMSO-d6): δ = 9.22 (s, 3H), 6.94 (s, 2H), 6.05-6.02 (m, 1H), 5.71-5.67 (m, 1H), 4.46-4.36 (m, 4H), 1.87 (t, 3H)
[アクリル系モノマー(1-b)の製造]
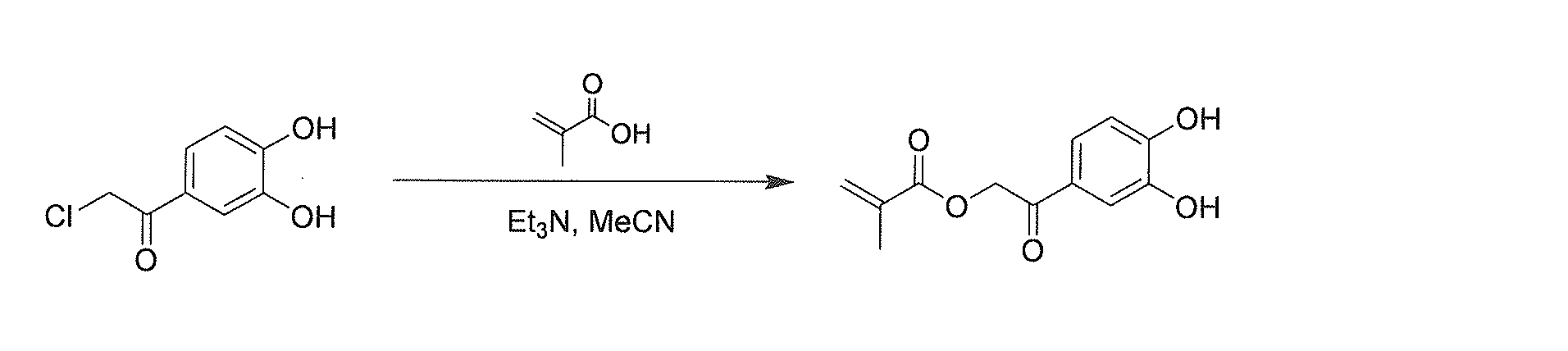
上記アクリル系モノマー(1-b)は、例えば、下記の式の通り、4-(クロロアセチル)カテコールとメタクリル酸とを反応させることにより、合成することができる。
[Production of acrylic monomer (1-b)]
The acrylic monomer (1-b) can be synthesized, for example, by reacting 4-(chloroacetyl)catechol with methacrylic acid as shown in the following formula.
4-(クロロアセチル)カテコールメタクリル酸とメタクリル酸を、アセトニトリル等の溶媒に溶解させ、混合液を得る。得られた混合液に、トリエチルアミンを加え、反応させる。
かかるメタクリル酸と4-(クロロアセチル)カテコールの配合モル比は、メタクリル酸:4-(クロロアセチル)カテコール=1:0.4~1:0.6程度である。
上記反応後の混合液の溶媒を除去し、カラムクロマトグラフィで精製する事で、上記アクリル系モノマー(1-b)(白色固体物)を得ることができる。
4-(Chloroacetyl)catechol methacrylic acid and methacrylic acid are dissolved in a solvent such as acetonitrile to obtain a mixed solution, and triethylamine is added to the resulting mixed solution to cause a reaction.
The molar ratio of methacrylic acid to 4-(chloroacetyl)catechol is about 1:0.4 to 1:0.6.
The solvent is removed from the mixed solution after the reaction, and the resulting solution is purified by column chromatography to obtain the acrylic monomer (1-b) (white solid).
なお、上記白色固体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,DMSO-d6): δ=10.45-9.27(m、2H)、7.43-7.28(m、2H)、6.84(d、1H)、6.12(s、1H)、5.77(t、1H)、5.42(s、2H)、1.93(s、3H)
The results of 1 H NMR analysis of the above white solid are as follows:
1H NMR (400MHz, DMSO-d6): δ = 10.45-9.27 (m, 2H), 7.43-7.28 (m, 2H), 6.84 (d, 1H), 6.12 (s, 1H), 5.77 (t, 1H), 5.42 (s, 2H), 1.93 (s, 3H)
[アクリル系モノマー(1-c)の製造]
上記アクリル系モノマー(1-c)は、例えば、下記の式の通り、ドーパミン塩酸塩とメタクリル酸無水物とを反応させることにより、合成することができる。
[Production of acrylic monomer (1-c)]
The acrylic monomer (1-c) can be synthesized, for example, by reacting dopamine hydrochloride with methacrylic anhydride as shown in the following formula.
炭酸水素ナトリウムと四ホウ酸ナトリウム十水和物を水(1000mL)等の溶媒に溶解させ、溶解液を作成する。その後、ドーパミン塩酸塩を加え、メタクリル酸無水物とテトラヒドロフラン(250mL)等の溶媒との混合液を上記の溶解液に滴下し、反応させる。
かかるメタクリル酸無水物とドーパミン塩酸塩の配合モル比は、メタクリル酸無水物:ドーパミン塩酸塩=1:0.8~1:1程度である。
つぎに、上記反応液を濾過し、溶媒置換により、酢酸エチル溶液とする。かかる酢酸エチル溶液を再結晶化により析出させることで、上記アクリル系モノマー(1-c)(白色固体物)を得ることができる。
Sodium bicarbonate and sodium tetraborate decahydrate are dissolved in a solvent such as water (1000 mL) to prepare a solution, after which dopamine hydrochloride is added, and a mixture of methacrylic anhydride and a solvent such as tetrahydrofuran (250 mL) is added dropwise to the solution to cause a reaction.
The molar ratio of methacrylic anhydride to dopamine hydrochloride is about 1:0.8 to 1:1.
Next, the reaction solution is filtered and the solvent is replaced to give an ethyl acetate solution, which is then precipitated by recrystallization to give the acrylic monomer (1-c) (white solid).
なお、上記白色固体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,DMSO-d6): δ=8.78-8.73(m、1H)、8.66-8.61(m、1H)、7.94(t、1H)、6.62(d、1H)、6.57(d、1H)、6.42(dd、1H)、5.61(s、1H)、5.29(t、1H)、3.25-3.18(m、2H)、2.58-2.53(m、2H)、1.83(s、3H)
The results of 1 H NMR analysis of the above white solid are as follows:
1H NMR (400MHz, DMSO-d6): δ = 8.78-8.73 (m, 1H), 8.66-8.61 (m, 1H), 7.94 (t, 1H), 6.62 (d, 1H), 6.57 (d, 1H), 6.42 (dd, 1H), 5.61 (s, 1H), 5.29 (t, 1H), 3.25-3.18 (m, 2H), 2.58-2.53 (m, 2H), 1.83 (s, 3H)
[アクリル系モノマー(1-d)の製造]
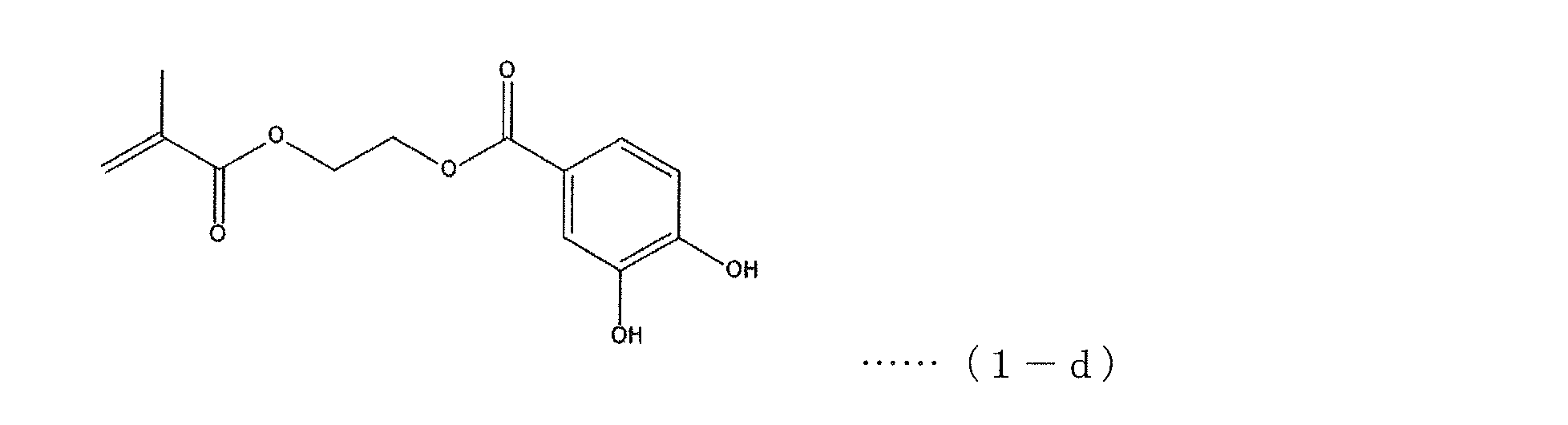
上記アクリル系モノマー(1-d)は、例えば、下記の式の通り、メタンスルホン酸-2-エチルメタクリレートと3,4-ジヒドロキシ安息香酸とを反応させることにより、合成することができる。
[Production of acrylic monomer (1-d)]
The acrylic monomer (1-d) can be synthesized, for example, by reacting methanesulfonate-2-ethyl methacrylate with 3,4-dihydroxybenzoic acid as shown in the following formula.
3,4-ジヒドロキシ安息香酸とDMSO等の溶媒に溶解し、アクリル系モノマー(1-a)と同様の手法で得られたメタンスルホン酸-2-エチルメタクリレートと、炭酸水素ナトリウムを加え、反応させる。
かかるメタンスルホン酸-2-エチルメタクリレートと3,4-ジヒドロキシ安息香酸との配合モル比は、メタンスルホン酸-2-エチルメタクリレート:3,4-ジヒドロキシ安息香酸=1:1.1~1:1.3程度である。
その後、重合禁止剤とを加え、溶媒を除去し、アセトニトリル/n-ヘプタン=10/1の溶液で再結晶化し、上記アクリル系モノマー(1-d)(白色固体物)を得ることができる。
3,4-Dihydroxybenzoic acid is dissolved in a solvent such as DMSO, and methanesulfonate-2-ethyl methacrylate obtained in the same manner as in the acrylic monomer (1-a) and sodium hydrogen carbonate are added to react with each other.
The molar ratio of methanesulfonate-2-ethyl methacrylate to 3,4-dihydroxybenzoic acid is methanesulfonate-2-ethyl methacrylate:3,4-dihydroxybenzoic acid=about 1:1.1 to 1:1.3.
Thereafter, a polymerization inhibitor is added, the solvent is removed, and the mixture is recrystallized from a solution of acetonitrile/n-heptane=10/1, to obtain the above acrylic monomer (1-d) (white solid).
上述の白色固体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,DMSO-d6): δ=9.59(s、2H)、7.38-7.24(m、2H)、6.82-6.80(d、1H)、6.03(s、1H)、5.68(s、1H)、4.48-4.36(m、4H)、1.86(s、3H)
The results of the 1 H NMR analysis of the above white solid are as follows:
1H NMR (400MHz, DMSO-d6): δ = 9.59 (s, 2H), 7.38-7.24 (m, 2H), 6.82-6.80 (d, 1H), 6.03 (s, 1H), 5.68 (s, 1H), 4.48-4.36 (m, 4H), 1.86 (s, 3H)
[アクリル系モノマー(1-e)の製造]
上記アクリル系モノマー(1-e)は、例えば、下記の式の通り、3,4-ジヒドロキシベンズアルデヒドを、下記の式に従い反応させることにより、合成することができる。
[Production of acrylic monomer (1-e)]
The acrylic monomer (1-e) can be synthesized, for example, by reacting 3,4-dihydroxybenzaldehyde according to the following formula:
上記の、3,4-ジヒドロキシベンズアルデヒドを用いたアクリル系モノマー(1-e)は、「3,4-ジヒドロキシベンズアルデヒドの水酸基保護」、「3,4-ビス(1-エトキシエトキシ)ベンズアルデヒドの還元反応」、「3,4-ビス(1-エトキシエトキシ)ベンジルアルコールのメタクリル化」、「1-エトキシエトキシ基の脱保護」を行うことにより得られる。 The above acrylic monomer (1-e) using 3,4-dihydroxybenzaldehyde can be obtained by carrying out "protection of the hydroxyl group of 3,4-dihydroxybenzaldehyde", "reduction reaction of 3,4-bis(1-ethoxyethoxy)benzaldehyde", "methacrylation of 3,4-bis(1-ethoxyethoxy)benzyl alcohol", and "deprotection of the 1-ethoxyethoxy group".
「3,4-ジヒドロキシベンズアルデヒドの水酸基保護」
3,4-ジヒドロキシベンズアルデヒドとp-トルエンスルホン酸ピリジニウムを、ジクロロメタンに溶解させ、エチルビニルエーテルを配合し、反応させる。
かかる3,4-ジヒドロキシベンズアルデヒドとエチルビニルエーテルとの配合モル比は、3,4-ジヒドロキシベンズアルデヒド:エチルビニルエーテル=1:1.8~1:2.5程度である。
その後、上記反応液の溶媒を除去し、3,4-ビス(1-エトキシエトキシ)ベンズアルデヒド(茶色油状液体物)を得る。
"Hydroxyl group protection of 3,4-dihydroxybenzaldehyde"
3,4-Dihydroxybenzaldehyde and pyridinium p-toluenesulfonate are dissolved in dichloromethane, and ethyl vinyl ether is added to the solution to cause a reaction.
The molar ratio of 3,4-dihydroxybenzaldehyde to ethyl vinyl ether is 3,4-dihydroxybenzaldehyde:ethyl vinyl ether=about 1:1.8 to 1:2.5.
Thereafter, the solvent is removed from the reaction solution to obtain 3,4-bis(1-ethoxyethoxy)benzaldehyde (a brown oily liquid).
なお、上述の茶色油状液体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,CDCl3): δ=9.84(s、1H)、7.56(t、1H)、7.48(dt、1H)、7.21(dd、1H)、5.50(qd、1H)、5.42-5.35(m、1H)、3.90-3.74(m、2H)、3.63-3.50(m、2H)、1.56-1.48(m、6H)、1.23-1.15(m、6H)
The results of 1 H NMR analysis of the above brown oily liquid are as follows:
1H NMR (400MHz, CDCl3 ): δ = 9.84 (s, 1H), 7.56 (t, 1H), 7.48 (dt, 1H), 7.21 (dd, 1H), 5.50 (qd, 1H), 5.42-5.35 (m, 1H), 3.90-3.74 (m, 2H), 3.63-3.50 (m, 2H), 1.56-1.48 (m, 6H), 1.23-1.15 (m, 6H)
「3,4-ビス(1-エトキシエトキシ)ベンズアルデヒドの還元反応」
上記の3,4-ビス(1-エトキシエトキシ)ベンズアルデヒドを、テトラヒドロフラン(900mL)等の溶媒に溶解させ、溶解液を得る。かかる溶解液に、水素化ホウ素ナトリウムを反応させる。
かかる3,4-ビス(1-エトキシエトキシ)ベンズアルデヒドと水素化ホウ素ナトリウムとの配合モル比は、3,4-ビス(1-エトキシエトキシ)ベンズアルデヒド:水素化ホウ素ナトリウム=1:0.9~1:1.1程度である。
その後、上記のようにして得られた反応液の溶媒を除去し、3,4-ビス(1-エトキシエトキシ)ベンジルアルコール(黄色油状液体物)を得る。
"Reduction of 3,4-bis(1-ethoxyethoxy)benzaldehyde"
The above 3,4-bis(1-ethoxyethoxy)benzaldehyde is dissolved in a solvent such as tetrahydrofuran (900 mL) to obtain a solution, which is then reacted with sodium borohydride.
The molar ratio of 3,4-bis(1-ethoxyethoxy)benzaldehyde to sodium borohydride is 3,4-bis(1-ethoxyethoxy)benzaldehyde:sodium borohydride=about 1:0.9 to 1:1.1.
Thereafter, the solvent is removed from the reaction solution obtained as described above to obtain 3,4-bis(1-ethoxyethoxy)benzyl alcohol (yellow oily liquid).
なお、上述の黄色油状液体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,CDCl3): δ=7.10-7.03(m、2H)、6.93(dt、1H)、5.38-5.30(m、2H)、4.58(s、2H)、3.89-3.79(m、2H)、3.62-3.51(m、2H)、1.50-1.47(m、6H)、1.23-1.16(m、6H)
The results of 1 H NMR analysis of the above yellow oily liquid are as follows:
1H NMR (400MHz, CDCl3 ): δ = 7.10-7.03 (m, 2H), 6.93 (dt, 1H), 5.38-5.30 (m, 2H), 4.58 (s, 2H), 3.8 9-3.79 (m, 2H), 3.62-3.51 (m, 2H), 1.50-1.47 (m, 6H), 1.23-1.16 (m, 6H)
「3,4-ビス(1-エトキシエトキシ)ベンジルアルコールのメタクリル化」
上記の3,4-ビス(1-エトキシエトキシ)ベンジルアルコール、トリエチルアミンと4-ジメチルアミノピリジンを入れ、テトラヒドロフラン等に溶解させ、メタクリル酸無水物(55.3g、0.36mol)を反応させる。
かかる3,4-ビス(1-エトキシエトキシ)ベンジルアルコールとメタクリル酸無水物との配合モル比は、3,4-ビス(1-エトキシエトキシ)ベンジルアルコール:メタクリル酸無水物=1:0.9~1:1.1程度である。
上記反応後、溶媒をエバポレーターで除去し、カラムクロマトグラフィで精製する事で、上記アクリル系モノマー(1-e)の1-エトキシエトキシ保護体(白色固体物)を得る。
"Methacrylation of 3,4-bis(1-ethoxyethoxy)benzyl alcohol"
The above 3,4-bis(1-ethoxyethoxy)benzyl alcohol, triethylamine and 4-dimethylaminopyridine are dissolved in tetrahydrofuran or the like, and then reacted with methacrylic anhydride (55.3 g, 0.36 mol).
The molar ratio of 3,4-bis(1-ethoxyethoxy)benzyl alcohol to methacrylic anhydride is 3,4-bis(1-ethoxyethoxy)benzyl alcohol:methacrylic anhydride=about 1:0.9 to 1:1.1.
After the reaction, the solvent is removed by an evaporator, and the resulting product is purified by column chromatography to obtain the 1-ethoxyethoxy protected acrylic monomer (1-e) (white solid).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,CDCl3): δ=7.12(d、1H)、7.06(d、1H)、6.99-6.95(m、1H)、6.14(s、1H)、5.60-5.56(m、1H)、5.40-5.30(m、2H)、5.11(s、2H)、3.91-3.77(m、2H)、3.64-3.53(m、2H)、1.96(s、3H)、1.54-1.46(m、6H)、1.24-1.17(m、6H)
The results of 1 H NMR analysis of the above white solid are as follows:
1H NMR (400MHz, CDCl3 ): δ = 7.12 (d, 1H), 7.06 (d, 1H), 6.99-6.95 (m, 1H), 6.14 (s, 1H), 5.60-5.56 (m, 1H), 5.40-5.30 (m, 2H), 5 .11 (s, 2H), 3.91-3.77 (m, 2H), 3.64-3.53 (m, 2H), 1.96 (s, 3H), 1.54-1.46 (m, 6H), 1.24-1.17 (m, 6H)
「1-エトキシエトキシ基の脱保護」
上記アクリル系モノマー(1-e)の1-エトキシエトキシ保護体を、メタノール等の溶媒に溶解させ、p-トルエンスルホン酸ピリジニウムを反応させる。
反応後、溶媒を除去し、カラムクロマトグラフィで精製し、アクリル系モノマー(1-e)(白色固体)を得ることができる。
"Deprotection of 1-ethoxyethoxy group"
The 1-ethoxyethoxy protected acrylic monomer (1-e) is dissolved in a solvent such as methanol and reacted with pyridinium p-toluenesulfonate.
After the reaction, the solvent is removed and the product is purified by column chromatography to obtain an acrylic monomer (1-e) (white solid).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りである。
1H NMR(400MHz,CDCl3): δ=6.92(d、1H)、6.88-6.81(m、2H)、6.16(s、1H)、6.04-5.75(m、3H)、5.09(s、2H)、1.96(s、3H)
The results of 1 H NMR analysis of the above white solid are as follows:
1H NMR (400MHz, CDCl3 ): δ = 6.92 (d, 1H), 6.88-6.81 (m, 2H), 6.16 (s, 1H), 6.04-5.75 (m, 3H), 5.09 (s, 2H), 1.96 (s, 3H)
〔モノマー(a2)〕
上記の、水酸基および/またはカルボキシ基を有する共重合性モノマー(a2)は、単独でもしくは二種以上併せて用いられる。そして、上記モノマー(a2)は、被着体密着性の観点から、カルボキシ基を有する共重合性モノマーが好ましく、(メタ)アクリル酸やカルボキシ基を有する(メタ)アクリレート系モノマーであることがより好ましい。特に、(メタ)アクリル酸が好ましい。
[Monomer (a2)]
The copolymerizable monomer (a2) having a hydroxyl group and/or a carboxyl group may be used alone or in combination of two or more kinds. From the viewpoint of adhesion to the adherend, the monomer (a2) is preferably a copolymerizable monomer having a carboxyl group, more preferably (meth)acrylic acid or a (meth)acrylate monomer having a carboxyl group. In particular, (meth)acrylic acid is preferred.
水酸基を有する共重合性モノマーとしては、例えば、2-ヒドロキシエチル(メタ)アクリレート、4-ヒドロキシブチル(メタ)アクリレート、5-ヒドロキシペンチル(メタ)アクリレート、6-ヒドロキシヘキシル(メタ)アクリレート、8-ヒドロキシオクチル(メタ)アクリレート等の(メタ)アクリル酸ヒドロキシアルキルエステル、カプロラクトン変性2-ヒドロキシエチル(メタ)アクリレート等のカプロラクトン変性モノマー、ジエチレングリコール(メタ)アクリレート、ポリエチレングリコール(メタ)アクリレート等のオキシアルキレン変性モノマー、2-アクリロイロキシエチル-2-ヒドロキシエチルフタル酸等の1級水酸基含有モノマー;2-ヒドロキシプロピル(メタ)アクリレート、2-ヒドロキシブチル(メタ)アクリレート、3-クロロ2-ヒドロキシプロピル(メタ)アクリレート等の2級水酸基含有モノマー;2,2-ジメチル2-ヒドロキシエチル(メタ)アクリレート等の3級水酸基含有モノマー等が挙げられる。
これらの中でも、架橋剤との反応性に優れる点で1級水酸基含有モノマーが好ましく、特には2-ヒドロキシエチル(メタ)アクリレート、4-ヒドロキシブチル(メタ)アクリレート好ましい。
Examples of copolymerizable monomers having a hydroxyl group include (meth)acrylic acid hydroxyalkyl esters such as 2-hydroxyethyl (meth)acrylate, 4-hydroxybutyl (meth)acrylate, 5-hydroxypentyl (meth)acrylate, 6-hydroxyhexyl (meth)acrylate, and 8-hydroxyoctyl (meth)acrylate; caprolactone-modified monomers such as caprolactone-modified 2-hydroxyethyl (meth)acrylate; oxyalkylene-modified monomers such as diethylene glycol (meth)acrylate and polyethylene glycol (meth)acrylate; primary hydroxyl group-containing monomers such as 2-acryloyloxyethyl-2-hydroxyethyl phthalate; secondary hydroxyl group-containing monomers such as 2-hydroxypropyl (meth)acrylate, 2-hydroxybutyl (meth)acrylate, and 3-chloro 2-hydroxypropyl (meth)acrylate; and tertiary hydroxyl group-containing monomers such as 2,2-dimethyl 2-hydroxyethyl (meth)acrylate.
Among these, primary hydroxyl group-containing monomers are preferred because of their excellent reactivity with crosslinking agents, and 2-hydroxyethyl (meth)acrylate and 4-hydroxybutyl (meth)acrylate are particularly preferred.
また、カルボキシ基を有する共重合性モノマーとしては、例えば、(メタ)アクリル酸、2-(メタ)アクリロイルオキシエチルヘキサヒドロフタル酸、2-(メタ)アクリロイルオキシプロピルヘキサヒドロフタル酸、2-(メタ)アクリロイルオキシエチルフタル酸、2-(メタ)アクリロイルオキシプロピルフタル酸、2-(メタ)アクリロイルオキシエチルマレイン酸、2-(メタ)アクリロイルオキシプロピルマレイン酸、2-(メタ)アクリロイルオキシエチルコハク酸、2-(メタ)アクリロイルオキシプロピルコハク酸、クロトン酸、フマル酸、マレイン酸、イタコン酸、マレイン酸モノメチル、イタコン酸モノメチル等が挙げられる。
なかでも粘着性の点、重合時の安定性の点で、アクリル酸が好ましい。
Examples of copolymerizable monomers having a carboxy group include (meth)acrylic acid, 2-(meth)acryloyloxyethyl hexahydrophthalic acid, 2-(meth)acryloyloxypropyl hexahydrophthalic acid, 2-(meth)acryloyloxyethyl phthalic acid, 2-(meth)acryloyloxypropyl phthalic acid, 2-(meth)acryloyloxyethyl maleic acid, 2-(meth)acryloyloxypropyl maleic acid, 2-(meth)acryloyloxyethyl succinic acid, 2-(meth)acryloyloxypropyl succinic acid, crotonic acid, fumaric acid, maleic acid, itaconic acid, monomethyl maleate, and monomethyl itaconate.
Among these, acrylic acid is preferred from the standpoint of adhesion and stability during polymerization.
前記アクリル系樹脂(A)を構成する共重合成分(a)全体に対し、上記モノマー(a2)の割合は、好ましくは0.1~30重量%であり、より好ましくは0.5~25重量%、更に好ましくは1~20重量%、特に好ましくは3~15重量%である。 The proportion of the monomer (a2) relative to the total copolymerization component (a) constituting the acrylic resin (A) is preferably 0.1 to 30% by weight, more preferably 0.5 to 25% by weight, even more preferably 1 to 20% by weight, and particularly preferably 3 to 15% by weight.
〔モノマー(a3)〕
前記の、(メタ)アクリル酸アルキルエステルモノマー(a3)は、通常、炭素数1~20のアルキル基を有する(メタ)アクリル酸アルキルエステルモノマーが用いられるが、好ましくは炭素数2~10のアルキル基を有する(メタ)アクリル酸アルキルエステルモノマー、より好ましくは炭素数4~8のアルキル基を有する(メタ)アクリル酸アルキルエステルモノマーが用いられる。
上記モノマー(a3)の具体例としては、例えば、メチル(メタ)アクリレート、エチル(メタ)アクリレート、n-プロピル(メタ)アクリレート、n-ブチル(メタ)アクリレート、i-ブチル(メタ)アクリレート、t-ブチル(メタ)アクリレート、n-へキシル(メタ)アクリレート、2-エチルヘキシル(メタ)アクリレート、n-オクチル(メタ)アクリレート、イソデシル(メタ)アクリレート、トリデシル(メタ)アクリレート、n-ラウリル(メタ)アクリレート等が挙げられる。なかでも粘着物性に優れる点、重合時の安定性に優れる点でn-ブチル(メタ)アクリレート、2-エチルヘキシル(メタ)アクリレートが好ましく、より好ましくはn-ブチルアクリレートである。
これらのモノマーは、単独でもしくは2種以上併せて用いることができる。
[Monomer (a3)]
As the (meth)acrylic acid alkyl ester monomer (a3), a (meth)acrylic acid alkyl ester monomer having an alkyl group having 1 to 20 carbon atoms is usually used, preferably a (meth)acrylic acid alkyl ester monomer having an alkyl group having 2 to 10 carbon atoms, and more preferably a (meth)acrylic acid alkyl ester monomer having an alkyl group having 4 to 8 carbon atoms.
Specific examples of the monomer (a3) include methyl (meth)acrylate, ethyl (meth)acrylate, n-propyl (meth)acrylate, n-butyl (meth)acrylate, i-butyl (meth)acrylate, t-butyl (meth)acrylate, n-hexyl (meth)acrylate, 2-ethylhexyl (meth)acrylate, n-octyl (meth)acrylate, isodecyl (meth)acrylate, tridecyl (meth)acrylate, n-lauryl (meth)acrylate, etc. Among these, n-butyl (meth)acrylate and 2-ethylhexyl (meth)acrylate are preferred from the viewpoints of excellent adhesive properties and excellent stability during polymerization, and n-butyl acrylate is more preferred.
These monomers can be used alone or in combination of two or more kinds.
前記アクリル系樹脂(A)を構成する共重合成分(a)全体に対し、上記モノマー(a3)の割合は、40~99重量%であり、好ましくは50~98重量%、より好ましくは70~97重量%、更に好ましくは80~95重量%である。 The proportion of the monomer (a3) in the total copolymerization component (a) constituting the acrylic resin (A) is 40 to 99% by weight, preferably 50 to 98% by weight, more preferably 70 to 97% by weight, and even more preferably 80 to 95% by weight.
〔モノマー(a4)〕
また、(a1)~(a3)以外のモノマー(a4)としては、本発明の効果を阻害しない範囲で、任意で含まれていてもよい。
例えば、無水マレイン酸、無水イタコン酸等の酸無水物基含有ビニル系単量体;グリジシル(メタ)アクリレート、グリジシルα-エチルアクリレート、3,4-エポキシブチル(メタ)アクリレート等のエポキシ基含有ビニル系単量体;ジメチルアミノエチル(メタ)アクリレート、ジエチルアミノエチル(メタ)アクリレート等のアミノ基含有(メタ)アクリレート系のビニル系単量体;(メタ)アクリルアミド、N-t-ブチル(メタ)アクリルアミド、N-メチロール(メタ)アクリルアミド、N-メトキシメチル(メタ)アクリルアミド、N-ブトキシメチル(メタ)アクリルアミド、ダイアセトンアクリルアミド、マレイン酸アミド、マレイミド等のアミド基を含有するビニル系単量体;スチレン、α-メチルスチレン、ビニルトルエン、(メタ)アクリロニトリル、塩化ビニル、酢酸ビニル、プロピオン酸ビニル等のビニル系単量体;ジビニルベンゼン、エチレングリコールジ(メタ)アクリレート、1,3-ブチレングリコールジ(メタ)アクリレート、1,6-ヘキサンジオールジ(メタ)アクリレート、トリエチレングリコールジ(メタ)アクリレート、テトラエチレングリコールジ(メタ)アクリレート、トリプロピレングリコールジ(メタ)アクリレート、トリメチロールプロパントリ(メタ)アクリレート、アリル(メタ)アクリレート等が挙げられる。
上記その他のモノマー(a4)は、単独でもしくは2種以上併せて用いることができる。
[Monomer (a4)]
Furthermore, a monomer (a4) other than (a1) to (a3) may be optionally contained within a range that does not impair the effects of the present invention.
For example, acid anhydride group-containing vinyl monomers such as maleic anhydride and itaconic anhydride; epoxy group-containing vinyl monomers such as glycidyl (meth)acrylate, glycidyl α-ethyl acrylate, and 3,4-epoxybutyl (meth)acrylate; amino group-containing (meth)acrylate vinyl monomers such as dimethylaminoethyl (meth)acrylate and diethylaminoethyl (meth)acrylate; (meth)acrylamide, N-t-butyl (meth)acrylamide, N-methylol (meth)acrylamide, N-methoxymethyl (meth)acrylamide, N-butoxymethyl (meth)acrylamide, diacetone acrylamide, and maleic acid acrylamide. vinyl monomers containing an amide group, such as amide and maleimide; vinyl monomers such as styrene, α-methylstyrene, vinyl toluene, (meth)acrylonitrile, vinyl chloride, vinyl acetate, and vinyl propionate; divinylbenzene, ethylene glycol di(meth)acrylate, 1,3-butylene glycol di(meth)acrylate, 1,6-hexanediol di(meth)acrylate, triethylene glycol di(meth)acrylate, tetraethylene glycol di(meth)acrylate, tripropylene glycol di(meth)acrylate, trimethylolpropane tri(meth)acrylate, and allyl (meth)acrylate.
The other monomers (a4) may be used alone or in combination of two or more kinds.
前記アクリル系樹脂(A)を構成する共重合成分(a)全体に対し、上記モノマー(a4)の含有量は、10重量%以下であることが好ましく、より好ましくは5重量%以下、更に好ましくは1重量%以下である。 The content of the monomer (a4) in the total copolymerization component (a) constituting the acrylic resin (A) is preferably 10% by weight or less, more preferably 5% by weight or less, and even more preferably 1% by weight or less.
〔アクリル系樹脂(A)の製造〕
本発明で用いられるアクリル系樹脂(A)は、前記特定のアクリル系モノマー(1-a)~(1-e)や、その他のモノマーを含む共重合成分(a)を用いて、例えば、有機溶媒中に、重合開始剤を混合あるいは滴下して、重合することにより製造することができる。
[Production of acrylic resin (A)]
The acrylic resin (A) used in the present invention can be produced by polymerizing the copolymerization component (a) containing the specific acrylic monomers (1-a) to (1-e) or other monomers by, for example, mixing or dropping a polymerization initiator into an organic solvent.
上記重合反応は、溶液ラジカル重合、懸濁重合、塊状重合、乳化重合等の従来公知の重合方法により行うことができるが、これらのなかでも、溶液ラジカル重合、塊状重合が好ましく、より好ましくは溶液ラジカル重合である。 The above polymerization reaction can be carried out by a conventionally known polymerization method such as solution radical polymerization, suspension polymerization, bulk polymerization, or emulsion polymerization. Among these, solution radical polymerization and bulk polymerization are preferred, and solution radical polymerization is more preferred.
上記重合反応に用いられる有機溶媒としては、例えば、トルエン、キシレン等の芳香族炭化水素類、ヘキサン等の脂肪族炭化水素類、酢酸エチル、酢酸ブチル等のエステル類、n-プロピルアルコール、イソプロピルアルコール等の脂肪族アルコール類、アセトン、メチルエチルケトン、メチルイソブチルケトン、シクロヘキサノン等のケトン類等が挙げられる。 Examples of organic solvents used in the above polymerization reaction include aromatic hydrocarbons such as toluene and xylene, aliphatic hydrocarbons such as hexane, esters such as ethyl acetate and butyl acetate, aliphatic alcohols such as n-propyl alcohol and isopropyl alcohol, and ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone, and cyclohexanone.
これらの有機溶媒のなかでも、重合反応のしやすさや連鎖移動の効果や粘着剤塗工時の乾燥のしやすさ、安全性の高さから、酢酸エチル、アセトン、メチルエチルケトン、酢酸ブチル、トルエン、メチルイソブチルケトンが好ましく用いられ、より好ましくは、酢酸エチル、アセトン、メチルエチルケトンである。これら有機溶媒は、単独で用いてもよいし2種以上を併用してもよい。
そして、これらの有機溶媒の使用量は、通常、アクリル系樹脂(A)を構成する共重合成分(a)100重量部に対して10~900重量部である。
Among these organic solvents, ethyl acetate, acetone, methyl ethyl ketone, butyl acetate, toluene, and methyl isobutyl ketone are preferably used, and more preferably ethyl acetate, acetone, and methyl ethyl ketone, in view of the ease of polymerization reaction, the effect of chain transfer, the ease of drying during application of the adhesive, and high safety. These organic solvents may be used alone or in combination of two or more kinds.
The amount of these organic solvents used is usually 10 to 900 parts by weight per 100 parts by weight of the copolymer component (a) constituting the acrylic resin (A).
また、かかる溶液ラジカル重合に用いられる重合開始剤としては、例えば、通常のラジカル重合開始剤である2,2’-アゾビスイソブチロニトリル、2,2’-アゾビス-2-メチルブチロニトリル、4,4’-アゾビス(4-シアノ吉草酸)、2,2’-アゾビス(メチルプロピオン酸)等のアゾ系開始剤、ベンゾイルパーオキサイド、ラウロイルパーオキサイド、ジ-t-ブチルパーオキサイド、クメンハイドロパーオキサイド等の有機過酸化物等が挙げられ、使用するモノマーに合わせて適宜選択して用いることができる。なかでも、2,2’-アゾビスイソブチロニトリルが、本発明において好ましい。そして、これらの重合開始剤は、単独で用いてもよいし2種以上を併用してもよい。
そして、これらの重合開始剤の使用量は、通常、共重合成分(a)に対して0.01~5重量%である。
Examples of the polymerization initiator used in the solution radical polymerization include azo initiators such as 2,2'-azobisisobutyronitrile, 2,2'-azobis-2-methylbutyronitrile, 4,4'-azobis(4-cyanovaleric acid), and 2,2'-azobis(methylpropionic acid), which are normal radical polymerization initiators, and organic peroxides such as benzoyl peroxide, lauroyl peroxide, di-t-butyl peroxide, and cumene hydroperoxide, which can be appropriately selected and used according to the monomer to be used. Among them, 2,2'-azobisisobutyronitrile is preferred in the present invention. These polymerization initiators may be used alone or in combination of two or more.
The amount of the polymerization initiator used is usually 0.01 to 5% by weight based on the copolymerization component (a).
〔アクリル系樹脂(A)の物性〕
かくして得られる上記アクリル系樹脂(A)の重量平均分子量(Mw)は、10万~300万であることが好ましく、より好ましくは20万~200万、更に好ましくは30万~180万、特に好ましくは35万~160万である。かかる重量平均分子量が小さすぎると耐久性が低下する傾向があり、大きすぎると調製時に希釈溶媒が大量に必要となり、乾燥性が低下し、粘着剤層中に残溶媒が多くなり耐久性が低下する傾向がある。
[Physical Properties of Acrylic Resin (A)]
The weight average molecular weight (Mw) of the acrylic resin (A) thus obtained is preferably 100,000 to 3,000,000, more preferably 200,000 to 2,000,000, even more preferably 300,000 to 1,800,000, and particularly preferably 350,000 to 1,600,000. If the weight average molecular weight is too small, durability tends to decrease, whereas if it is too large, a large amount of dilution solvent is required during preparation, drying properties decrease, and residual solvent increases in the pressure-sensitive adhesive layer, tending to decrease durability.
上記アクリル系樹脂(A)の分散度(重量平均分子量/数平均分子量)は、30以下であることが好ましく、より好ましくは20以下、更に好ましくは15以下である。
かかる分散度が高すぎるとリワーク性や耐久性が低下する傾向がある。なお、かかる分散度の下限は通常1である。
The polydispersity (weight average molecular weight/number average molecular weight) of the acrylic resin (A) is preferably 30 or less, more preferably 20 or less, and further preferably 15 or less.
If the degree of dispersion is too high, reworkability and durability tend to decrease.
上記重量平均分子量(Mw)は、標準ポリスチレン分子量換算による重量平均分子量であり、高速液体クロマトグラフ(Waters社製、「Waters 2695(本体)」と「Waters 2414(検出器)」)に、カラム:Shodex GPC KF-806L(排除限界分子量:2×107、分離範囲:100~2×107、理論段数:10000段/本、充填剤材質:スチレン-ジビニルベンゼン共重合体、充填剤粒径:10μm)の3本を直列にして用いることにより測定される。また、数平均分子量も同様の方法で測定され、数平均分子量と重量平均分子量より分散度(重量平均分子量/数平均分子量)が求められる。 The weight average molecular weight (Mw) is a weight average molecular weight calculated based on the molecular weight of standard polystyrene, and is measured using a high performance liquid chromatograph (manufactured by Waters, "Waters 2695 (main body)" and "Waters 2414 (detector)") and three columns: Shodex GPC KF-806L (exclusion limit molecular weight: 2×10 7 , separation range: 100 to 2×10 7 , theoretical plate number: 10,000 plates/column, packing material: styrene-divinylbenzene copolymer, packing particle size: 10 μm) in series. The number average molecular weight is also measured in the same manner, and the dispersity (weight average molecular weight/number average molecular weight) is determined from the number average molecular weight and the weight average molecular weight.
上記アクリル系樹脂(A)のガラス転移温度(Tg)は、粘着性能および被着体耐汚染性等の点から、-70℃以上であることが好ましく、より好ましくは-60~10℃、更に好ましくは-55~0℃、特に好ましくは-52~-10℃である。 From the viewpoints of adhesive performance and resistance to contamination of the adherend, the glass transition temperature (Tg) of the acrylic resin (A) is preferably -70°C or higher, more preferably -60 to 10°C, even more preferably -55 to 0°C, and particularly preferably -52 to -10°C.
なお、アクリル系樹脂(A)のガラス転移温度(Tg)は、TAインスツルメント社製の示差走査熱量計「DSC Q2000」を用いて測定される値である。測定温度範囲は-80~40℃で、温度上昇速度は、5℃/分である。 The glass transition temperature (Tg) of the acrylic resin (A) is a value measured using a differential scanning calorimeter "DSC Q2000" manufactured by TA Instruments. The measurement temperature range is -80 to 40°C, and the temperature rise rate is 5°C/min.
〔アクリル系樹脂(A)溶液〕
上記アクリル系樹脂(A)は、通常、溶媒等により粘度調整され、アクリル系樹脂(A)溶液として、本発明の粘着剤組成物に用いられる。希釈濃度としては、樹脂分濃度が、好ましくは5~60重量%、より好ましくは10~50重量%、更に好ましくは30~45重量%である。かかる濃度が高すぎると流動性が低下して取り扱いにくくなる傾向があり、低すぎると粘着剤としたときに塗工が困難となる傾向がある。
[Acrylic resin (A) solution]
The acrylic resin (A) is usually adjusted in viscosity with a solvent or the like, and used in the pressure-sensitive adhesive composition of the present invention as a solution of the acrylic resin (A). The dilution concentration is preferably 5 to 60% by weight, more preferably 10 to 50% by weight, and even more preferably 30 to 45% by weight in terms of resin content. If the concentration is too high, the fluidity tends to decrease, making it difficult to handle, and if the concentration is too low, it tends to be difficult to apply the pressure-sensitive adhesive.
かかるアクリル系樹脂(A)溶液の粘度としては、取扱い易さの点から100~30000mPa・sであることが好ましく、より好ましくは500~20000mPa・s、更に好ましくは1000~15000mPa・s、特に好ましくは1300~10000mPa・sである。
かかる粘度が高すぎると流動性が低下して取り扱いにくくなる傾向にあり、低すぎると粘着剤としたときに塗工が困難となる傾向がある。
上記アクリル系樹脂(A)溶液の粘度は、25℃に調温した樹脂溶液を、B型粘度計を用いた回転粘度系法により測定する。
The viscosity of the acrylic resin (A) solution is preferably 100 to 30,000 mPa·s, more preferably 500 to 20,000 mPa·s, further preferably 1,000 to 15,000 mPa·s, and particularly preferably 1,300 to 10,000 mPa·s, from the viewpoint of ease of handling.
If the viscosity is too high, the fluidity decreases and handling tends to become difficult, whereas if the viscosity is too low, application of the resulting adhesive tends to become difficult.
The viscosity of the acrylic resin (A) solution is measured by subjecting the resin solution, the temperature of which has been adjusted to 25° C., to a rotational viscosimetry using a B-type viscometer.
<粘着剤組成物>
本発明の粘着剤組成物には、糊残り性を向上させたり、粘着剤の耐久性を向上させたりする点で上記アクリル系樹脂(A)に加えて、更に架橋剤(B)を含有することが好ましい。
<Adhesive Composition>
In order to improve adhesive residual properties and the durability of the adhesive, it is preferable that the pressure-sensitive adhesive composition of the present invention further contains a crosslinking agent (B) in addition to the acrylic resin (A).
〔架橋剤(B)〕
本発明の粘着剤組成物で用いられる架橋剤(B)とは、アクリル系樹脂(A)中の官能基と反応し、架橋構造を形成させるものであり、例えば、エポキシ系架橋剤、イソシアネート系架橋剤、アジリジン系架橋剤、メラミン系架橋剤、アルデヒド系架橋剤、アミン系架橋剤、金属キレート系架橋剤等が挙げられる。なかでも粘着性能やポットライフに優れる点で、エポキシ系架橋剤を用いることが好ましい。
上記架橋剤(B)は、単独で使用してもよいし、2種以上を併用してもよい。
[Crosslinking agent (B)]
The crosslinking agent (B) used in the pressure-sensitive adhesive composition of the present invention reacts with the functional groups in the acrylic resin (A) to form a crosslinked structure, and examples thereof include epoxy-based crosslinking agents, isocyanate-based crosslinking agents, aziridine-based crosslinking agents, melamine-based crosslinking agents, aldehyde-based crosslinking agents, amine-based crosslinking agents, metal chelate-based crosslinking agents, etc. Among these, it is preferable to use an epoxy-based crosslinking agent because of its excellent adhesive performance and pot life.
The crosslinking agent (B) may be used alone or in combination of two or more kinds.
上記エポキシ系架橋剤としては、例えば、ビスフェノールA・エピクロルヒドリン型のエポキシ樹脂、エチレングリコールジグリシジルエーテル、ポリエチレングリコールジグリシジルエーテル、グリセリンジグリシジルエーテル、グリセリントリグリシジルエーテル、1,6-ヘキサンジオールジグリシジルエーテル、トリメチロールプロパントリグリシジルエーテル、ソルビトールポリグリシジルエーテル、ポリグリセロールポリグリシジルエーテル、ペンタエリスリトールポリグリシジルエリスリトール、ジグリセロールポリグリシジルエーテル、1,3'-ビス(N,N-ジグリシジルアミノメチル)シクロヘキサン、N,N,N',N'-テトラグリシジル-m-キシレンジアミン等が挙げられる。
これらエポキシ系架橋剤のなかでも、1,3'-ビス(N,N-ジグリシジルアミノメチル)シクロヘキサン、N,N,N',N'-テトラグリシジル-m-キシレンジアミン等の多官能エポキシ樹脂が反応性の高さの点で好ましい。
Examples of the epoxy crosslinking agent include bisphenol A-epichlorohydrin type epoxy resins, ethylene glycol diglycidyl ether, polyethylene glycol diglycidyl ether, glycerin diglycidyl ether, glycerin triglycidyl ether, 1,6-hexanediol diglycidyl ether, trimethylolpropane triglycidyl ether, sorbitol polyglycidyl ether, polyglycerol polyglycidyl ether, pentaerythritol polyglycidyl erythritol, diglycerol polyglycidyl ether, 1,3'-bis(N,N-diglycidylaminomethyl)cyclohexane, and N,N,N',N'-tetraglycidyl-m-xylylenediamine.
Among these epoxy crosslinking agents, polyfunctional epoxy resins such as 1,3'-bis(N,N-diglycidylaminomethyl)cyclohexane and N,N,N',N'-tetraglycidyl-m-xylylenediamine are preferred in terms of high reactivity.
上記イソシアネート系架橋剤としては、例えば、2,4-トリレンジイソシアネート、2,6-トリレンジイソシアネート等のトリレンジイソシアネート系架橋剤、1,3-キシリレンジイソシアネート等のキシリレンジイソシアネート系架橋剤、ジフェニルメタン-4,4-ジイソシアネート等のジフェニルメタン系架橋剤、1,5-ナフタレンジイソシアネート等のナフタレンジイソシアネート系架橋剤等の芳香族系イソシアネート系架橋剤;イソホロンジイソシアネート、1,4-シクロヘキサンジイソシアネート、4,4'-ジシクロヘキシルメタンジイソシアネート、メチルシクロヘキサンジイソシアネート、イソプロピリデンジシクロヘキシル-4,4'-ジイソシアネート、1,3-ジイソシアナトメチルシクロヘキサン、ノルボルナンジイソシアネート等の脂環族系イソシアネート系架橋剤;ヘキサメチレンジイソシアネート、トリメチルヘキサメチレンジイソシアネート等の脂肪族系イソシアネート系架橋剤;および上記イソシアネート系化合物のアダクト体、ビュレット体、イソシアヌレート体等が挙げられる。
これらイソシアネート系架橋剤のなかでも、トリレンジイソシアネート系架橋剤がポットライフと耐久性の点で好ましく、キシリレンジイソシアネート系架橋剤またはイソシアヌレート骨格含有イソシアネート系架橋剤がエージング時間短縮の点で好ましく、芳香環非含有イソシアネート系架橋剤が耐黄変性の点で好ましい。これらの中で具体的には、トリレンジイソシアネート、キシリレンジイソシアネート、ヘキサメチレンジイソシアネートとトリメチロールプロパンのアダクト体、およびヌレート体が、耐久性、ポットライフ、架橋速度のバランスに優れている点で好ましい。
Examples of the isocyanate-based crosslinking agent include aromatic isocyanate-based crosslinking agents such as tolylene diisocyanate-based crosslinking agents such as 2,4-tolylene diisocyanate and 2,6-tolylene diisocyanate, xylylene diisocyanate-based crosslinking agents such as 1,3-xylylene diisocyanate, diphenylmethane-4,4-diisocyanate and other diphenylmethane-based crosslinking agents, and naphthalene diisocyanate-based crosslinking agents such as 1,5-naphthalene diisocyanate; isophorone diisocyanate, 1,4-cyclohexane diisocyanate, etc. alicyclic isocyanate crosslinking agents such as hexamethylene diisocyanate, trimethylhexamethylene diisocyanate, and the like; and adducts, biuret forms, and isocyanurates of the above-mentioned isocyanate compounds.
Among these isocyanate-based crosslinking agents, tolylene diisocyanate-based crosslinking agents are preferred in terms of pot life and durability, xylylene diisocyanate-based crosslinking agents or isocyanurate skeleton-containing isocyanate-based crosslinking agents are preferred in terms of shortening the aging time, and aromatic ring-free isocyanate-based crosslinking agents are preferred in terms of yellowing resistance. Specifically, among these, tolylene diisocyanate, xylylene diisocyanate, an adduct of hexamethylene diisocyanate and trimethylolpropane, and a nurate are preferred in terms of excellent balance between durability, pot life, and crosslinking speed.
上記アジリジン系架橋剤としては、例えば、テトラメチロールメタン-トリ-β-アジリジニルプロピオネート、トリメチロールプロパン-トリ-β-アジリジニルプロピオネート、N,N'-ジフェニルメタン-4,4'-ビス(1-アジリジンカルボキシアミド)、N,N'-ヘキサメチレン-1,6-ビス(1-アジリジンカルボキシアミド)等が挙げられる。 Examples of the aziridine-based crosslinking agent include tetramethylolmethane-tri-β-aziridinyl propionate, trimethylolpropane-tri-β-aziridinyl propionate, N,N'-diphenylmethane-4,4'-bis(1-aziridinecarboxamide), and N,N'-hexamethylene-1,6-bis(1-aziridinecarboxamide).
上記メラミン系架橋剤としては、例えば、へキサメトキシメチルメラミン、ヘキサエトキシメチルメラミン、ヘキサプロポキシメチルメラミン、ヘキサプトキシメチルメラミン、ヘキサペンチルオキシメチルメラミン、ヘキサヘキシルオキシメチルメラミン、メラミン樹脂等が挙げられる。 Examples of the melamine-based crosslinking agent include hexamethoxymethylmelamine, hexaethoxymethylmelamine, hexapropoxymethylmelamine, hexaptoxymethylmelamine, hexapentyloxymethylmelamine, hexahexyloxymethylmelamine, melamine resins, etc.
上記アルデヒド系架橋剤としては、例えば、グリオキザール、マロンジアルデヒド、スクシンジアルデヒド、マレインジアルデヒド、グルタルジアルデヒド、ホルムアルデヒド、アセトアルデヒド、ベンズアルデヒド等が挙げられる。 Examples of the aldehyde crosslinking agents include glyoxal, malondialdehyde, succindialdehyde, maleic dialdehyde, glutaric dialdehyde, formaldehyde, acetaldehyde, and benzaldehyde.
上記アミン系架橋剤としては、例えば、ヘキサメチレンジアミン、トリエチルジアミン、ポリエチレンイミン、ヘキサメチレンテトラアミン、ジエチレントリアミン、トリエチルテトラアミン、イソホロンジアミン、アミノ樹脂、ポリアミド等が挙げられる。 Examples of the amine-based crosslinking agent include hexamethylenediamine, triethyldiamine, polyethyleneimine, hexamethylenetetraamine, diethylenetriamine, triethyltetraamine, isophoronediamine, amino resins, polyamides, etc.
上記金属キレート系架橋剤としては、例えば、アルミニウム、鉄、銅、亜鉛、スズ、チタン、ニッケル、アンチモン、マグネシウム、パナジウム、クロム、ジルコニウム等の多価金属とアセチルアセトンやアセトアセチルエステルとの配位化合物等が挙げられる。 Examples of the metal chelate crosslinking agent include coordination compounds of polyvalent metals such as aluminum, iron, copper, zinc, tin, titanium, nickel, antimony, magnesium, vanadium, chromium, and zirconium with acetylacetone or acetoacetyl ester.
このような上記架橋剤(B)を用いる場合、その含有量は、アクリル系樹脂(A)100重量部に対して、0.001~20重量部であることが好ましく、より好ましくは0.01~15重量部、更に好ましくは0.05~10重量部、特に好ましくは0.09~5重量部である。かかる含有量が少なすぎると、再剥離性が低下しやすい傾向があり、多すぎると被着体密着性が低くなったり、長時間のエージングが必要となったりする傾向がある。 When such a crosslinking agent (B) is used, its content is preferably 0.001 to 20 parts by weight, more preferably 0.01 to 15 parts by weight, even more preferably 0.05 to 10 parts by weight, and particularly preferably 0.09 to 5 parts by weight, per 100 parts by weight of the acrylic resin (A). If the content is too low, removability tends to decrease, while if it is too high, adhesion to the adherend tends to decrease or long-term aging is required.
<その他の成分>
本発明の粘着剤組成物には、その他の公知の添加剤を含有していてもよく、たとえば、ポリプロピレングリコール等のポリアルキレングリコールといったポリエーテル化合物、着色剤、顔料等の粉体、染料、界面活性剤、可塑剤、粘着性付与剤、表面潤滑剤、レベリング剤、軟化剤、酸化防止剤、老化防止剤、光安定剤、紫外線吸収剤、重合禁止剤、無機または有機の充填剤、金属粉、粒子状物、箔状物等を使用する用途に応じて適宜添加することができる。また、制御できる範囲内で、還元剤を加えてのレドックス系を採用してもよい。これらは、単独でもしくは2種以上併せて用いることができる。
これら添加剤は、アクリル系樹脂(A)100重量部に対して5重量部以下であることが好ましく、より好ましくは3重量部以下、更に好ましくは1重量部以下の範囲である。
<Other ingredients>
The pressure-sensitive adhesive composition of the present invention may contain other known additives, such as polyether compounds such as polyalkylene glycols such as polypropylene glycol, colorants, powders such as pigments, dyes, surfactants, plasticizers, tackifiers, surface lubricants, leveling agents, softeners, antioxidants, antiaging agents, light stabilizers, ultraviolet absorbers, polymerization inhibitors, inorganic or organic fillers, metal powders, particulate materials, foil-like materials, etc., which can be appropriately added depending on the application.In addition, a redox system in which a reducing agent is added may be adopted within a controllable range.These can be used alone or in combination of two or more.
The amount of these additives is preferably 5 parts by weight or less, more preferably 3 parts by weight or less, and further preferably 1 part by weight or less, based on 100 parts by weight of the acrylic resin (A).
かくしてアクリル系樹脂(A)、好ましくは更に、架橋剤(B)、更に必要に応じてその他の任意成分を混合することにより、本発明の粘着剤組成物を得ることができる。 Thus, the pressure-sensitive adhesive composition of the present invention can be obtained by mixing the acrylic resin (A), preferably further the crosslinking agent (B), and, if necessary, other optional components.
ここで、粘着性、再剥離性等の観点から、本発明の粘着剤組成物全体に対する上記アクリル系樹脂(A)の割合は、50重量%以上であることが好ましく、より好ましくは60重量%以上、更に好ましくは70重量%以上、特に好ましくは80~99.9重量%の範囲である。 From the viewpoints of adhesion, removability, etc., the proportion of the acrylic resin (A) in the entire pressure-sensitive adhesive composition of the present invention is preferably 50% by weight or more, more preferably 60% by weight or more, even more preferably 70% by weight or more, and particularly preferably in the range of 80 to 99.9% by weight.
なお、上記混合方法については、特に限定されるものではなく、各成分を一括で混合する方法や、任意の成分を混合した後、残りの成分を一括または順次混合する方法等、種々の方法を採用することができる。 The above mixing method is not particularly limited, and various methods can be used, such as mixing each component at once, or mixing any components and then mixing the remaining components at once or sequentially.
<粘着剤>
本発明の粘着剤組成物を乾燥および/または架橋させることにより粘着剤となる。かかる粘着剤は、湿潤面に貼った場合においても充分な粘着力を有し、さらにマスキング用粘着剤として用いた場合にも、被着体表面に、糊残りのない被着体耐汚染性に優れる粘着剤である。従って、例えば、マスキングフィルム用粘着剤、表面保護フィルム用粘着剤、表示ラベル用粘着剤、養生テープ用粘着剤等の各種部材用の粘着剤として好適に用いることができるが、なかでもマスキングフィルム用粘着剤として、特に建築用のマスキングフィルム用粘着剤として好適に用いられる。
かかる粘着剤層の形成にあたっては、架橋剤(B)を用いる場合、架橋剤(B)全体の添加量を調整することとともに、架橋処理温度や架橋処理時間の影響を充分に考慮することが好ましい。
<Adhesive>
The adhesive composition of the present invention is dried and/or crosslinked to become an adhesive. Such an adhesive has sufficient adhesive strength even when applied to a wet surface, and when used as an adhesive for masking, it is an adhesive that has excellent resistance to contamination of the adherend without leaving any adhesive residue on the adherend surface. Therefore, it can be suitably used as an adhesive for various members such as an adhesive for masking films, an adhesive for surface protection films, an adhesive for display labels, and an adhesive for masking tapes, and is particularly suitable for use as an adhesive for masking films, particularly as an adhesive for architectural masking films.
In forming such a pressure-sensitive adhesive layer, when the crosslinking agent (B) is used, it is preferable to adjust the total amount of the crosslinking agent (B) added and to fully consider the effects of the crosslinking treatment temperature and crosslinking treatment time.
使用する架橋剤(B)によって架橋処理温度や架橋処理時間は、調整が可能である。架橋処理温度は170℃以下であることが好ましい。 The crosslinking temperature and time can be adjusted depending on the crosslinking agent (B) used. The crosslinking temperature is preferably 170°C or less.
<粘着剤層>
粘着剤は、種々の基材上に粘着剤層として積層させることができる。かかる粘着剤層の厚みは、5~300μmが好ましく、より好ましくは10~200μm、更に好ましくは20~150μmである。かかる粘着剤層が薄すぎると、厚み精度が低下したり粘着力が低くなる傾向があり、厚すぎると粘着フィルムをロール状にした際に端からはみ出したりする傾向がある。
<Adhesive Layer>
The adhesive can be laminated as an adhesive layer on various substrates. The thickness of the adhesive layer is preferably 5 to 300 μm, more preferably 10 to 200 μm, and even more preferably 20 to 150 μm. If the adhesive layer is too thin, the thickness precision and adhesive strength tend to decrease, and if it is too thick, the adhesive film tends to protrude from the edge when rolled.
上記粘着剤層のゲル分率については基材との密着性、リワーク性、保持力の点から0.1~99重量%であることが好ましく、より好ましくは1~90重量%であり、更に好ましくは10~80重量%である。ゲル分率が低すぎると凝集力が低くなりリワークする際に糊残りしたり、保持力が低くなる傾向にあり、高すぎると粘着力が低くなりすぎるため剥がれやすくなる傾向がある。 The gel fraction of the pressure-sensitive adhesive layer is preferably 0.1 to 99% by weight, more preferably 1 to 90% by weight, and even more preferably 10 to 80% by weight, from the viewpoints of adhesion to the substrate, reworkability, and holding power. If the gel fraction is too low, the cohesive strength will be low, and there will be a tendency for glue to remain during rework and for holding power to be low, whereas if the gel fraction is too high, there will be a tendency for the adhesive strength to be too low and for the adhesive to peel off easily.
上記ゲル分率は、架橋度(硬化度合い)の目安となるもので、例えば、以下の方法にて算出される。すなわち、基材に粘着剤層が形成されてなる粘着フィルムから粘着剤をピッキングにより採取し、粘着剤を200メッシュのSUS製金網で包みトルエン中に23℃×24時間浸漬し、トルエン浸漬前の粘着剤の重量に対する、金網中に残存した不溶解の粘着剤成分の重量百分率をゲル分率とする。 The gel fraction is an indication of the degree of crosslinking (degree of hardening) and is calculated, for example, by the following method. That is, the adhesive is picked from an adhesive film consisting of a substrate and an adhesive layer formed thereon, and the adhesive is wrapped in a 200-mesh SUS wire mesh and immersed in toluene at 23°C for 24 hours. The gel fraction is the weight percentage of the insoluble adhesive components remaining in the wire mesh relative to the weight of the adhesive before immersion in toluene.
上記粘着剤層は、指で触れたときに程好いタック感がある方が、実際に被着体に貼る際に濡れ性が良いため、作業性が上がる傾向があり好ましい。タックはJIS Z0237(2009年)に規定された傾斜角30°の時のボールタックにより測定される。ボールタックは1以上が好ましく、3以上がより好ましい。かかるボールタックが低すぎると、粘着フィルムを被着体に貼り合わせる際に密着しにくくなる傾向にある。 The adhesive layer preferably has a moderate tackiness when touched with the fingers, which tends to improve workability due to good wettability when actually applied to an adherend. Tackiness is measured by ball tack at an inclination angle of 30° as specified in JIS Z0237 (2009). Ball tackiness is preferably 1 or more, and more preferably 3 or more. If the ball tackiness is too low, the adhesive film tends to adhere poorly when applied to an adherend.
<粘着フィルム>
本発明の粘着フィルムは、上記粘着剤層をプラスチックフィルム等の基材フィルムに積層したものである。
上記粘着フィルムには、粘着剤層に基材フィルムが積層されている面の逆の面に、更に離型フィルムを設けることが好ましい。
<Adhesive film>
The pressure-sensitive adhesive film of the present invention is obtained by laminating the above-mentioned pressure-sensitive adhesive layer on a substrate film such as a plastic film.
It is preferable that the pressure-sensitive adhesive film further has a release film provided on the surface opposite to the surface on which the base film is laminated to the pressure-sensitive adhesive layer.
上記基材フィルムとしては、ポリエチレンテレフタレートなどのポリエステル系樹脂、ポリエチレンなどのポリオレフィン、ポリウレタンなどが挙げられる。 Examples of the above-mentioned base film include polyester resins such as polyethylene terephthalate, polyolefins such as polyethylene, and polyurethane.
上記粘着フィルムの製造方法としては、〔1〕基材フィルム上に、粘着剤組成物を塗工、乾燥した後、離型フィルムを貼合し、常温または加温状態でのエージングの少なくとも一方による処理を行う方法、〔2〕離型フィルム上に、粘着剤組成物を塗布、乾燥した後、基材フィルムを貼合し、常温または加温状態でのエージングの少なくとも一方による処理を行う方法等が挙げられる。 Examples of methods for producing the above-mentioned adhesive film include (1) a method in which an adhesive composition is applied to a base film, dried, and then a release film is attached, and then a treatment is performed by at least one of aging at room temperature or at an elevated temperature, and (2) a method in which an adhesive composition is applied to a release film, dried, and then a base film is attached, and then a treatment is performed by at least one of aging at room temperature or at an elevated temperature.
かかるエージング処理は、粘着剤の化学架橋の反応時間として、粘着物性のバランスをとるために行うものであり、エージングの条件としては、温度は通常20~70℃、時間は通常1~30日間であり、具体的には、例えば23℃で3~10日間、40℃で1~7日間等の条件で行えばよい。 Such aging treatment is carried out to balance the adhesive properties as the reaction time of the adhesive's chemical crosslinking. The aging conditions are usually a temperature of 20 to 70°C and a time of 1 to 30 days. Specifically, the aging can be carried out under conditions such as 23°C for 3 to 10 days or 40°C for 1 to 7 days.
上記粘着剤組成物の塗工に際しては、この粘着剤組成物を溶媒で希釈して塗工することが好ましい。希釈濃度としては、加熱残分(固形分濃度)が5~60重量%であることが好ましく、特には10~30重量%であることが好ましい。 When applying the adhesive composition, it is preferable to dilute the adhesive composition with a solvent before application. The dilution concentration is preferably such that the heating residue (solid content concentration) is 5 to 60% by weight, and more preferably 10 to 30% by weight.
また、上記溶媒としては、粘着剤組成物を溶解させるものであれば特に限定されることなく、例えば、酢酸メチル、酢酸エチル、アセト酢酸メチル、アセト酢酸エチル等のエステル系溶媒、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン系溶媒、トルエン、キシレン等の芳香族系溶媒、メタノール、エタノール、プロピルアルコール等のアルコール系溶媒を用いることができる。なかでも、溶解性、乾燥性、価格等の点から酢酸エチル、メチルエチルケトンが好適に用いられる。これらは単独でもしくは2種以上併せて用いてもよい。 The solvent is not particularly limited as long as it dissolves the adhesive composition. For example, ester-based solvents such as methyl acetate, ethyl acetate, methyl acetoacetate, and ethyl acetoacetate, ketone-based solvents such as acetone, methyl ethyl ketone, and methyl isobutyl ketone, aromatic solvents such as toluene and xylene, and alcohol-based solvents such as methanol, ethanol, and propyl alcohol can be used. Among these, ethyl acetate and methyl ethyl ketone are preferably used in terms of solubility, drying property, cost, and the like. These may be used alone or in combination of two or more kinds.
また、上記粘着剤組成物の塗工に関しては、例えば、ロールコーティング、ダイコーティング、グラビアコーティング、コンマコーティング、スクリーン印刷等の慣用の方法により行われる。 The adhesive composition is applied by a conventional method such as roll coating, die coating, gravure coating, comma coating, screen printing, etc.
また、上記粘着フィルムは、40℃で3日間エージング処理した後、25mm×100mmの試験片となるよう作製し、表面を精製水で濡らしたステンレス板(SUS304BA板)に、23℃、相対湿度50%の雰囲気下にて2kgゴムローラー2往復で加圧貼付し、同雰囲気下で30分間静置した後、引き剥がし角度180°、剥離速度300mm/minで引き剥がした時の粘着力が、5.0N/25mm以上であることが好ましく、7.0N/25mm以上であることがより好ましい。 The adhesive film is aged at 40°C for 3 days, and then prepared into a 25 mm x 100 mm test piece. The test piece is pressed and attached to a stainless steel plate (SUS304BA plate) whose surface has been wetted with purified water using a 2 kg rubber roller in two passes at 23°C and a relative humidity of 50%. The film is then left to stand in the same atmosphere for 30 minutes, and the adhesive strength when peeled off at a peel angle of 180° and a peel speed of 300 mm/min is preferably 5.0 N/25 mm or more, and more preferably 7.0 N/25 mm or more.
本発明の粘着フィルムは、直接あるいは離型フィルムを有するものは離型フィルムを剥がした後、粘着剤層面を被着体表面に貼合して使用される。 The adhesive film of the present invention is used by attaching the adhesive layer surface to the surface of the substrate directly, or after peeling off the release film if the film has one.
本発明の粘着フィルムは、水中や湿潤条件下であっても充分な粘着性能を示し、さらに、被着体に粘着させた後に剥離した際に、被着体表面に、糊残り、および貼り跡が生じるのを防げることから、被着体耐汚染性においても優れている。そのため、例えば、表面保護フィルム、表示ラベル、養生テープ、タッチパネル用粘着フィルム、ITO等のセンサー用粘着フィルム、車載用粘着フィルム、光学フィルム、偏光板等の、各種部材の粘着フィルムとして好適に用いることができるが、なかでもマスキング用粘着フィルムとして、特に建築用のマスキングテープ(養生テープ)として好適に用いられる。 The adhesive film of the present invention exhibits sufficient adhesive performance even under water or wet conditions, and furthermore, when peeled off after adhering to an adherend, it is possible to prevent adhesive residue and the occurrence of adhesive marks on the surface of the adherend, and therefore has excellent resistance to contamination of the adherend. Therefore, it can be suitably used as an adhesive film for various members such as surface protection films, display labels, masking tapes, adhesive films for touch panels, adhesive films for sensors such as ITO, adhesive films for vehicles, optical films, and polarizing plates, but is particularly suitable for use as an adhesive film for masking, and in particular as a masking tape (masking tape) for construction.
以下、実施例を挙げて本発明を更に具体的に説明するが、本発明はその要旨を超えない限り以下の実施例に限定されるものではない。なお、例中、「部」、「%」とあるのは、重量基準を意味する。 The present invention will be explained in more detail below with reference to examples, but the present invention is not limited to the following examples as long as it does not exceed the gist of the invention. In the examples, "parts" and "%" are by weight.
まず、実施に先立ち下記の材料成分を準備した。 First, the following ingredients were prepared prior to the experiment:
<アクリル系樹脂>
下記に示される調製方法に従い、アクリル系樹脂(A-1)~(A-13),(A'-1)を調製した。なお、各アクリル系樹脂の組成および物性等を後記の表1に示す。
表1に示す、上記アクリル系樹脂の、重量平均分子量(分子量Mw)、分散度、ガラス転移温度(Tg)に関しては、前述の方法に従って測定した。
表1に示す粘度の測定に関しては、JIS K7117-1(1999)のブルックフィールド形回転粘度計を用いた粘度計法に準じて測定した。
また、各アクリル系樹脂の材料として準備したモノマー(1-a)~(1-e)は、下記の化学式で示したモノマーである。
<Acrylic resin>
Acrylic resins (A-1) to (A-13) and (A'-1) were prepared according to the preparation methods described below. The composition and physical properties of each acrylic resin are shown in Table 1 below.
The weight average molecular weight (molecular weight Mw), dispersity, and glass transition temperature (Tg) of the above acrylic resin shown in Table 1 were measured according to the above-mentioned methods.
The viscosity shown in Table 1 was measured according to the viscometer method using a Brookfield type rotational viscometer as specified in JIS K7117-1 (1999).
The monomers (1-a) to (1-e) prepared as materials for each acrylic resin are represented by the following chemical formula.
上記モノマー(1-a)~(1-e)は、以下のようにして合成した。 The above monomers (1-a) to (1-e) were synthesized as follows.
[モノマー(1-a)の合成]
回転子を入れた三つ口フラスコに滴下漏斗を取り付けた後、フラスコ内に2-ヒドロキシエチルメタクリレート(95.0g、0.73mol)を入れ、テトラヒドロフラン(1000mL)に溶解させたうえで、トリエチルアミン(89.2g、0.88mol)を加えた。このようにして得られた混合液を、0℃に冷却した後、上記混合液に対し、メタンスルホニルクロリド(101.5g、0.89mol)を滴下ロートに入れてゆっくりと滴下した。滴下後、上記混合液を25℃で16時間反応させた。
つぎに、上記反応後の混合液に水(800mL)を加え、生成物を酢酸エチル(800mL×3回)で有機層に抽出した。酢酸エチル溶液は水(800mL)、ブライン(800mL)の順で洗浄し、無水硫酸ナトリウムで脱水させた。その後、溶媒をエバポレーターで除去し、メタンスルホン酸-2-エチルメタクリレート(黄色液体物、151.0g)を得た。
[Synthesis of Monomer (1-a)]
A dropping funnel was attached to a three-necked flask containing a rotor, and 2-hydroxyethyl methacrylate (95.0 g, 0.73 mol) was placed in the flask and dissolved in tetrahydrofuran (1000 mL), and triethylamine (89.2 g, 0.88 mol) was added. The mixture thus obtained was cooled to 0°C, and then methanesulfonyl chloride (101.5 g, 0.89 mol) was placed in a dropping funnel and slowly dropped into the mixture. After the dropwise addition, the mixture was reacted at 25°C for 16 hours.
Next, water (800 mL) was added to the mixture after the reaction, and the product was extracted into an organic layer with ethyl acetate (800 mL x 3 times). The ethyl acetate solution was washed with water (800 mL) and brine (800 mL) in that order, and dehydrated with anhydrous sodium sulfate. Thereafter, the solvent was removed with an evaporator to obtain methanesulfonate-2-ethyl methacrylate (yellow liquid, 151.0 g).
なお、上述の黄色液体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,CDCl3): δ=6.08(s、1H)、5.57-5.54(m、1H)、4.41-4.37(m、2H)、4.35-4.31(m、2H)、2.98(s、3H)、1.88(s、3H)
The results of analysis of the above yellow liquid by 1 H NMR were as follows:
1H NMR (400MHz, CDCl 3 ): δ = 6.08 (s, 1H), 5.57-5.54 (m, 1H), 4.41-4.37 (m, 2H), 4.35-4.31 (m, 2H), 2.98 (s, 3H), 1.88 (s, 3H)
また、回転子を入れた三つ口フラスコに没食子酸(36.0g、0.21mol)と炭酸水素ナトリウム(43.0g、0.51mol)を入れ、DMSO(300mL)を加えたものを用意した。そこに、室温下で、上記のようにして得られたメタンスルホン酸-2-エチルメタクリレート(36.7g、0.18mol)を加えた後、80℃で16時間反応させた。
反応液を室温に戻し、水(300mL)と1N塩酸水溶液(70mL)を加え、生成物を酢酸エチル(400mL×3回)で有機層に抽出した。酢酸エチル溶液は水(400mL)、ブライン(500mL)の順で洗浄し、無水硫酸ナトリウムで脱水させた。その後、溶媒をエバポレーターで除去し、カラムクロマトグラフィ(充填剤:シリカゲル、溶剤:ヘキサン/酢酸エチル混合液)で精製し、さらに酢酸エチル/n-ヘプタン=1/8(270mL)の溶液で再結晶化を行う事で、モノマー(1-a)(白色固体、26.0g)を得た。
Also, a three-neck flask equipped with a rotor was charged with gallic acid (36.0 g, 0.21 mol) and sodium hydrogen carbonate (43.0 g, 0.51 mol), and DMSO (300 mL) was added to prepare a flask. The methanesulfonate-2-ethyl methacrylate (36.7 g, 0.18 mol) obtained as above was added thereto at room temperature, and the mixture was reacted at 80° C. for 16 hours.
The reaction solution was returned to room temperature, water (300 mL) and 1N hydrochloric acid aqueous solution (70 mL) were added, and the product was extracted into the organic layer with ethyl acetate (400 mL x 3 times). The ethyl acetate solution was washed with water (400 mL) and brine (500 mL) in that order, and dehydrated with anhydrous sodium sulfate. The solvent was then removed with an evaporator, and the product was purified by column chromatography (packing material: silica gel, solvent: hexane/ethyl acetate mixture), and further recrystallized with a solution of ethyl acetate/n-heptane = 1/8 (270 mL) to obtain monomer (1-a) (white solid, 26.0 g).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,DMSO-d6): δ=9.22(s、3H)、6.94(s、2H)、6.05-6.02(m、1H)、5.71-5.67(m、1H)、4.46-4.36(m、4H)、1.87(t、3H)
The results of 1 H NMR analysis of the above white solid were as follows:
1H NMR (400MHz, DMSO-d6): δ = 9.22 (s, 3H), 6.94 (s, 2H), 6.05-6.02 (m, 1H), 5.71-5.67 (m, 1H), 4.46-4.36 (m, 4H), 1.87 (t, 3H)
[モノマー(1-b)の合成]
回転子を入れた三つ口フラスコに滴下漏斗を取り付けた後、フラスコ内に4-(クロロアセチル)カテコール(75.0g、0.40mol)とメタクリル酸(76.1g、0.88mol)を入れ、アセトニトリル(1200mL)に溶解させた。このようにして得られた混合液を、0℃に冷却した後、上記混合液に対し、トリエチルアミン(85.4g、0.84mol)を滴下ロートに入れ、窒素気流化でゆっくりと滴下した。滴下後、その混合液を80℃で20時間反応させた。
そして、上記反応後の混合液を室温に戻し、pHが4になるまで2N塩酸水溶液を添加し、水(1000mL)を加えたうえで、生成物をジクロロメタン(1100mL×2回)で有機層に抽出した。ジクロロメタン溶液は無水硫酸ナトリウムで脱水した後、溶媒をエバポレーターで除去し、カラムクロマトグラフィ(充填剤:シリカゲル、溶剤:ヘキサン/酢酸エチル混合液)で精製する事で、モノマー(1-b)(白色固体物、46.7g)を得た。
[Synthesis of Monomer (1-b)]
After attaching a dropping funnel to a three-necked flask containing a rotor, 4-(chloroacetyl)catechol (75.0 g, 0.40 mol) and methacrylic acid (76.1 g, 0.88 mol) were placed in the flask and dissolved in acetonitrile (1200 mL). The mixture thus obtained was cooled to 0°C, and then triethylamine (85.4 g, 0.84 mol) was placed in the dropping funnel and slowly dropped into the mixture under nitrogen gas flow. After dropping, the mixture was reacted at 80°C for 20 hours.
The mixture after the reaction was returned to room temperature, a 2N aqueous hydrochloric acid solution was added until the pH reached 4, water (1000 mL) was added, and the product was extracted into an organic layer with dichloromethane (1100 mL x 2). The dichloromethane solution was dehydrated with anhydrous sodium sulfate, the solvent was removed with an evaporator, and the product was purified by column chromatography (packing material: silica gel, solvent: hexane/ethyl acetate mixture) to obtain monomer (1-b) (white solid, 46.7 g).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,DMSO-d6): δ=10.45-9.27(m、2H)、7.43-7.28(m、2H)、6.84(d、1H)、6.12(s、1H)、5.77(t、1H)、5.42(s、2H)、1.93(s、3H)
The results of 1 H NMR analysis of the above white solid were as follows:
1H NMR (400MHz, DMSO-d6): δ = 10.45-9.27 (m, 2H), 7.43-7.28 (m, 2H), 6.84 (d, 1H), 6.12 (s, 1H), 5.77 (t, 1H), 5.42 (s, 2H), 1.93 (s, 3H)
[モノマー(1-c)の合成]
回転子を入れた三つ口フラスコに滴下漏斗を取り付けた後、フラスコ内に炭酸水素ナトリウム(40.0g、0.48mol)と四ホウ酸ナトリウム十水和物(100.6g、0.26mol)を入れ、水(1000mL)に溶解させたうえで1時間窒素バブリングを行った。その後、ドーパミン塩酸塩(50.0g、0.26mol)を加えたうえで、メタクリル酸無水物(52.8g、0.34mol)とテトラヒドロフラン(250mL)の混合液を滴下ロートに入れ、室温下でゆっくりと滴下した。滴下後、その反応液に1N水酸化ナトリウム水溶液を加えてpHを8に調整し、窒素バブリングをしながら20℃で34時間反応させた。
つぎに、上記反応液を室温で減圧濾過し、濾液を酢酸エチル(150mL×2回)で洗浄した。洗浄後の水溶液はpHが2になるまで1N塩酸水溶液を加え、生成物を酢酸エチル(500mL×3回)で有機層に抽出した。酢酸エチル溶液は無水硫酸ナトリウムで脱水した後、200mL程度になるまで溶媒を減圧留去させた。その後、ヘキサン(500mL)を加え、再結晶化による析出(0℃、4時間)を行った。析出物を濾別し、酢酸エチル/n-ヘプタン=1/10の混合液で洗浄(20℃、10時間浸漬)を2回行った。さらにイソプロパノール/n-ヘプタン=5/1(2000mL)の溶液で2回再結晶化を行う事で、モノマー(1-c)(白色固体、42.3g)を得た。
[Synthesis of Monomer (1-c)]
After attaching a dropping funnel to a three-necked flask containing a rotor, sodium bicarbonate (40.0 g, 0.48 mol) and sodium tetraborate decahydrate (100.6 g, 0.26 mol) were placed in the flask, dissolved in water (1000 mL), and nitrogen bubbling was performed for 1 hour. Then, dopamine hydrochloride (50.0 g, 0.26 mol) was added, and a mixture of methacrylic anhydride (52.8 g, 0.34 mol) and tetrahydrofuran (250 mL) was placed in a dropping funnel and slowly dropped at room temperature. After dropping, 1N aqueous sodium hydroxide was added to the reaction solution to adjust the pH to 8, and the reaction was performed at 20 ° C. for 34 hours while bubbling with nitrogen.
Next, the reaction solution was filtered under reduced pressure at room temperature, and the filtrate was washed with ethyl acetate (150 mL x 2 times). After washing, a 1N aqueous hydrochloric acid solution was added to the aqueous solution until the pH became 2, and the product was extracted into the organic layer with ethyl acetate (500 mL x 3 times). The ethyl acetate solution was dehydrated with anhydrous sodium sulfate, and the solvent was distilled off under reduced pressure until the volume was about 200 mL. Then, hexane (500 mL) was added, and precipitation by recrystallization (0 ° C, 4 hours) was performed. The precipitate was filtered and washed twice with a mixed solution of ethyl acetate / n-heptane = 1 / 10 (20 ° C, immersion for 10 hours). Furthermore, recrystallization was performed twice with a solution of isopropanol / n-heptane = 5 / 1 (2000 mL) to obtain monomer (1-c) (white solid, 42.3 g).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,DMSO-d6): δ=8.78-8.73(m、1H)、8.66-8.61(m、1H)、7.94(t、1H)、6.62(d、1H)、6.57(d、1H)、6.42(dd、1H)、5.61(s、1H)、5.29(t、1H)、3.25-3.18(m、2H)、2.58-2.53(m、2H)、1.83(s、3H)
The results of 1 H NMR analysis of the above white solid were as follows:
1H NMR (400MHz, DMSO-d6): δ = 8.78-8.73 (m, 1H), 8.66-8.61 (m, 1H), 7.94 (t, 1H), 6.62 (d, 1H), 6.57 (d, 1H), 6.42 (dd, 1H), 5.61 (s, 1H), 5.29 (t, 1H), 3.25-3.18 (m, 2H), 2.58-2.53 (m, 2H), 1.83 (s, 3H)
[モノマー(1-d)の合成]
回転子を入れた三つ口フラスコに3,4-ジヒドロキシ安息香酸(71.1g、0.46mol)とDMSO(550mL)を入れ、さらに室温下で、先のアクリル系モノマー(1-a)の合成過程と同様の手法で得られたメタンスルホン酸-2-エチルメタクリレート(80.0g、0.38mol)、炭酸水素ナトリウム(93.6g、1.11mol)を順に加えた後、80℃で16時間反応させた。
上記反応液を室温に戻し、水(500mL)を加え3分間撹拌させた。その後、生成物を酢酸エチル(300mL×4回)で有機層に抽出した。酢酸エチル溶液はブライン(200mL×2回)で洗浄し、無水硫酸ナトリウムで脱水させた。その後、重合禁止剤として2,6-ジ-tert-ブチル-4-メチルフェノール(10mg)を加え、溶媒をエバポレーターで除去し、アセトニトリル/n-ヘプタン=10/1(88mL)の溶液で再結晶化(85℃から0℃へとゆっくりと冷却)を行う事で、モノマー(1-d)(白色固体物、64.3g)を得た。
[Synthesis of Monomer (1-d)]
3,4-Dihydroxybenzoic acid (71.1 g, 0.46 mol) and DMSO (550 mL) were placed in a three-neck flask equipped with a rotor, and methanesulfonate-2-ethyl methacrylate (80.0 g, 0.38 mol) obtained by the same method as in the synthesis process of the acrylic monomer (1-a) above and sodium hydrogen carbonate (93.6 g, 1.11 mol) were added in that order at room temperature, and the mixture was allowed to react at 80° C. for 16 hours.
The reaction solution was returned to room temperature, water (500 mL) was added, and the mixture was stirred for 3 minutes. The product was then extracted into an organic layer with ethyl acetate (300 mL x 4 times). The ethyl acetate solution was washed with brine (200 mL x 2 times) and dehydrated with anhydrous sodium sulfate. Then, 2,6-di-tert-butyl-4-methylphenol (10 mg) was added as a polymerization inhibitor, the solvent was removed with an evaporator, and recrystallization was performed (slowly cooled from 85 ° C. to 0 ° C.) with a solution of acetonitrile / n-heptane = 10 / 1 (88 mL) to obtain monomer (1-d) (white solid, 64.3 g).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,DMSO-d6): δ=9.59(s、2H)、7.38-7.24(m、2H)、6.82-6.80(d、1H)、6.03(s、1H)、5.68(s、1H)、4.48-4.36(m、4H)、1.86(s、3H)
The results of 1 H NMR analysis of the above white solid were as follows:
1H NMR (400MHz, DMSO-d6): δ = 9.59 (s, 2H), 7.38-7.24 (m, 2H), 6.82-6.80 (d, 1H), 6.03 (s, 1H), 5.68 (s, 1H), 4.48-4.36 (m, 4H), 1.86 (s, 3H)
[モノマー(1-e)の合成]
回転子を入れた三つ口フラスコに滴下漏斗を取り付けたフラスコ内に、3,4-ジヒドロキシベンズアルデヒド(100.0g、0.72mol)とp-トルエンスルホン酸ピリジニウム(181.9g、0.72mol)を入れ、ジクロロメタン(1000mL)に溶解させた。反応液を0℃に冷却した後、エチルビニルエーテル(114.9g、1.59mol)を滴下ロートに入れてゆっくりと滴下した。滴下後、反応液を25℃で16時間反応させた。
反応液にtert-ブチルメチルエーテル(1000mL)を加え、ブライン(800mL)で洗浄した。水層はtert-ブチルメチルエーテル(500mL×2回)で洗浄し、得られた有機層をまとめ、1N水酸化ナトリウム水溶液(1000mL)で洗浄し、無水硫酸ナトリウムで脱水させた。その後、溶媒をエバポレーターで除去し、3,4-ビス(1-エトキシエトキシ)ベンズアルデヒド(茶色油状液体物、172.0g)を得た。
[Synthesis of Monomer (1-e)]
In a three-necked flask equipped with a rotor and a dropping funnel, 3,4-dihydroxybenzaldehyde (100.0 g, 0.72 mol) and pyridinium p-toluenesulfonate (181.9 g, 0.72 mol) were placed and dissolved in dichloromethane (1000 mL). After the reaction solution was cooled to 0°C, ethyl vinyl ether (114.9 g, 1.59 mol) was placed in the dropping funnel and slowly dropped. After the dropwise addition, the reaction solution was reacted at 25°C for 16 hours.
To the reaction solution, tert-butyl methyl ether (1000 mL) was added, and the mixture was washed with brine (800 mL). The aqueous layer was washed with tert-butyl methyl ether (500 mL x 2 times), and the obtained organic layers were combined, washed with 1N aqueous sodium hydroxide solution (1000 mL), and dehydrated with anhydrous sodium sulfate. The solvent was then removed with an evaporator to obtain 3,4-bis(1-ethoxyethoxy)benzaldehyde (brown oily liquid, 172.0 g).
なお、上述の茶色油状液体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,CDCl3): δ=9.84(s、1H)、7.56(t、1H)、7.48(dt、1H)、7.21(dd、1H)、5.50(qd、1H)、5.42-5.35(m、1H)、3.90-3.74(m、2H)、3.63-3.50(m、2H)、1.56-1.48(m、6H)、1.23-1.15(m、6H)
The results of 1 H NMR analysis of the above brown oily liquid were as follows:
1H NMR (400MHz, CDCl3 ): δ = 9.84 (s, 1H), 7.56 (t, 1H), 7.48 (dt, 1H), 7.21 (dd, 1H), 5.50 (qd, 1H), 5.42-5.35 (m, 1H), 3.90-3.74 (m, 2H), 3.63-3.50 (m, 2H), 1.56-1.48 (m, 6H), 1.23-1.15 (m, 6H)
つぎに、回転子を入れた三つ口フラスコに、上記の3,4-ビス(1-エトキシエトキシ)ベンズアルデヒド(86.0g、0.30mol)を入れ、テトラヒドロフラン(900mL)に溶解させた。反応液を0℃に冷却した後、水素化ホウ素ナトリウム(12.7g、0.34mol)を徐々に加えた。水素化ホウ素ナトリウムをすべて加えた後、反応液を25℃で16時間反応させた。
室温下、反応液に塩化アンモニウム飽和水(420mL)を少しずつ加え、析出物を濾別した。濾液中の有機溶媒をエバポレーターで除去したうえで、生成物をジクロロメタン(800mL×2回)で抽出した。ジクロロメタン溶液はブライン(1000mL)で洗浄し、無水硫酸ナトリウムで脱水させた。その後、溶媒をエバポレーターで除去し、3,4-ビス(1-エトキシエトキシ)ベンジルアルコール(黄色油状液体物、85.3g)を得た。
Next, the above 3,4-bis(1-ethoxyethoxy)benzaldehyde (86.0 g, 0.30 mol) was placed in a three-neck flask equipped with a rotor and dissolved in tetrahydrofuran (900 mL). After the reaction solution was cooled to 0°C, sodium borohydride (12.7 g, 0.34 mol) was gradually added. After all the sodium borohydride was added, the reaction solution was reacted at 25°C for 16 hours.
At room temperature, saturated aqueous ammonium chloride (420 mL) was added little by little to the reaction solution, and the precipitate was filtered off. The organic solvent in the filtrate was removed using an evaporator, and the product was extracted with dichloromethane (800 mL x 2). The dichloromethane solution was washed with brine (1000 mL) and dehydrated over anhydrous sodium sulfate. The solvent was then removed using an evaporator to obtain 3,4-bis(1-ethoxyethoxy)benzyl alcohol (yellow oily liquid, 85.3 g).
なお、上述の黄色油状液体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,CDCl3): δ=7.10-7.03(m、2H)、6.93(dt、1H)、5.38-5.30(m、2H)、4.58(s、2H)、3.89-3.79(m、2H)、3.62-3.51(m、2H)、1.50-1.47(m、6H)、1.23-1.16(m、6H)
The results of analysis of the above yellow oily liquid by 1 H NMR were as follows:
1H NMR (400MHz, CDCl3 ): δ = 7.10-7.03 (m, 2H), 6.93 (dt, 1H), 5.38-5.30 (m, 2H), 4.58 (s, 2H), 3.8 9-3.79 (m, 2H), 3.62-3.51 (m, 2H), 1.50-1.47 (m, 6H), 1.23-1.16 (m, 6H)
回転子を入れた三つ口フラスコに滴下漏斗を取り付け、そのフラスコ内に、上記の3,4-ビス(1-エトキシエトキシ)ベンジルアルコール(85.0g、0.30mol)、トリエチルアミン(60.5g、0.60mol)と4-ジメチルアミノピリジン(3.7g、0.03mol)を入れ、テトラヒドロフラン(800mL)に溶解させた。その後、メタクリル酸無水物(55.3g、0.36mol)を滴下ロートに入れ、窒素気流下でゆっくりと滴下した。滴下後、反応液を25℃で16時間反応させた。
反応後、溶媒をエバポレーターで除去し、カラムクロマトグラフィ(充填剤:シリカゲル、溶剤:石油エーテル/酢酸エチル混合液)で精製する事で、モノマー(1-e)の1-エトキシエトキシ保護体(白色固体、58.5g)を得た。
A dropping funnel was attached to a three-necked flask containing a rotor, and the above 3,4-bis(1-ethoxyethoxy)benzyl alcohol (85.0 g, 0.30 mol), triethylamine (60.5 g, 0.60 mol), and 4-dimethylaminopyridine (3.7 g, 0.03 mol) were placed in the flask and dissolved in tetrahydrofuran (800 mL). Then, methacrylic anhydride (55.3 g, 0.36 mol) was placed in the dropping funnel and slowly dropped under a nitrogen stream. After dropping, the reaction solution was reacted at 25°C for 16 hours.
After the reaction, the solvent was removed using an evaporator, and the residue was purified by column chromatography (filler: silica gel, solvent: petroleum ether/ethyl acetate mixture) to obtain a 1-ethoxyethoxy protected monomer (1-e) (white solid, 58.5 g).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,CDCl3): δ=7.12(d、1H)、7.06(d、1H)、6.99-6.95(m、1H)、6.14(s、1H)、5.60-5.56(m、1H)、5.40-5.30(m、2H)、5.11(s、2H)、3.91-3.77(m、2H)、3.64-3.53(m、2H)、1.96(s、3H)、1.54-1.46(m、6H)、1.24-1.17(m、6H)
The results of 1 H NMR analysis of the above white solid were as follows:
1H NMR (400MHz, CDCl3 ): δ = 7.12 (d, 1H), 7.06 (d, 1H), 6.99-6.95 (m, 1H), 6.14 (s, 1H), 5.60-5.56 (m, 1H), 5.40-5.30 (m, 2H), 5 .11 (s, 2H), 3.91-3.77 (m, 2H), 3.64-3.53 (m, 2H), 1.96 (s, 3H), 1.54-1.46 (m, 6H), 1.24-1.17 (m, 6H)
回転子を入れた三つ口フラスコに、上記の、モノマー(1-e)の1-エトキシエトキシ保護体(100.0g、0.28mol)を入れ、、メタノール(600mL)に溶解させた。その後、p-トルエンスルホン酸ピリジニウム(14.3g、0.06mol)を加え、25℃で40分間反応させた。
反応後、溶媒をエバポレーター(水浴温度35℃)で除去し、カラムクロマトグラフィ(充填剤:シリカゲル、溶剤:n-ヘプタン/酢酸エチル混合液)で精製する事で、モノマー(1-e)(白色固体、33.5g)を得た。
The 1-ethoxyethoxy protected monomer (1-e) (100.0 g, 0.28 mol) was placed in a three-neck flask equipped with a rotor and dissolved in methanol (600 mL). Pyridinium p-toluenesulfonate (14.3 g, 0.06 mol) was then added and reacted at 25° C. for 40 minutes.
After the reaction, the solvent was removed using an evaporator (water bath temperature 35° C.), and the residue was purified by column chromatography (filler: silica gel, solvent: n-heptane/ethyl acetate mixture) to obtain monomer (1-e) (white solid, 33.5 g).
なお、上述の白色固体物の1H NMRによる分析結果は以下の通りであった。
1H NMR(400MHz,CDCl3): δ=6.92(d、1H)、6.88-6.81(m、2H)、6.16(s、1H)、6.04-5.75(m、3H)、5.09(s、2H)、1.96(s、3H)
The results of 1 H NMR analysis of the above white solid were as follows:
1H NMR (400MHz, CDCl3 ): δ = 6.92 (d, 1H), 6.88-6.81 (m, 2H), 6.16 (s, 1H), 6.04-5.75 (m, 3H), 5.09 (s, 2H), 1.96 (s, 3H)
〔アクリル系樹脂(A-1)の調製〕
還流冷却器、撹拌器、窒素ガスの吹き込み口及び温度計を備えた4ツ口丸底フラスコに、アクリル系樹脂(A-1)の共重合成分(モノマー)である、モノマー(1-a)(アクリル系モノマー(a1))1部と、アクリル酸(AAc)(共重合性モノマー(a2))8部と、n-ブチルアクリレート(BA)((メタ)アクリル酸アルキルエステルモノマー(a3))91部を仕込み、さらに、メチルエチルケトン45部、アセトン45部、重合開始剤として2,2’-アゾビスイソブチロニトリル(AIBN)0.038部を仕込み、撹拌しながら昇温し、内温を沸点まで上昇させて反応を開始させた。次いでAIBNを0.023%含むメチルエチルケトン溶液33.8部を2時間にわたって滴下した。更に、重合途中に、メチルエチルケトン33.8部にAIBN0.023部を混合させた混合溶液、メチルエチルケトン25部にAIBN0.015部を混合させた混合溶液を逐次追加しながら還流下7.5時間反応させることにより、アクリル系樹脂(A-1)の溶液を得た。
[Preparation of acrylic resin (A-1)]
In a four-necked round-bottom flask equipped with a reflux condenser, a stirrer, a nitrogen gas inlet and a thermometer, 1 part of monomer (1-a) (acrylic monomer (a1)), 8 parts of acrylic acid (AAc) (copolymerizable monomer (a2)), and 91 parts of n-butyl acrylate (BA) ((meth)acrylic acid alkyl ester monomer (a3)) were charged as copolymerization components (monomers) of the acrylic resin (A-1), and further, 45 parts of methyl ethyl ketone, 45 parts of acetone, and 0.038 parts of 2,2'-azobisisobutyronitrile (AIBN) as a polymerization initiator were charged, and the temperature was raised with stirring, and the internal temperature was raised to the boiling point to start the reaction. Then, 33.8 parts of a methyl ethyl ketone solution containing 0.023% AIBN was added dropwise over 2 hours. Further, during the polymerization, a mixed solution obtained by mixing 0.023 parts of AIBN in 33.8 parts of methyl ethyl ketone and a mixed solution obtained by mixing 0.015 parts of AIBN in 25 parts of methyl ethyl ketone were successively added and reacted under reflux for 7.5 hours to obtain a solution of acrylic resin (A-1).
〔アクリル系樹脂(A-2)~(A-6),(A-10)~(A-13)の調製〕
上記(a1)~(a3)に示すモノマーの種類および割合を、後記の表1に示す通りのモノマー組成を示すアクリル系樹脂が得られるように変更した。それ以外は、上記アクリル系樹脂(A-1)の調製方法に準じて重合を行い、目的とするアクリル系樹脂の溶液を得た。
[Preparation of acrylic resins (A-2) to (A-6), (A-10) to (A-13)]
The types and ratios of the monomers (a1) to (a3) were changed so as to obtain an acrylic resin having a monomer composition as shown in Table 1. Except for the above, polymerization was carried out in accordance with the preparation method for the acrylic resin (A-1) to obtain a solution of the desired acrylic resin.
〔アクリル系樹脂(A-7)~(A-9)の調製〕
上記(a1)~(a3)に示すモノマーの種類および割合を、後記の表1に示す通りのモノマー組成を示すアクリル系樹脂が得られるように変更し、さらに、アセトンをメタノールに変更した。それ以外は、上記アクリル系樹脂(A-1)の調製方法に準じて重合を行い、目的とするアクリル系樹脂の溶液を得た。
[Preparation of acrylic resins (A-7) to (A-9)]
The types and ratios of the monomers (a1) to (a3) were changed so as to obtain an acrylic resin having a monomer composition as shown in Table 1 below, and further, acetone was changed to methanol. Except for this, polymerization was carried out in accordance with the preparation method of the acrylic resin (A-1) above, to obtain a solution of the target acrylic resin.
〔アクリル系樹脂(A’-1)の調製〕
温度計、撹拌機、滴下ロート及び還流冷却器を備えた反応器内に、酢酸エチル61.3部、2,2’-アゾビスイソブチロニトリル(AIBN)0.037部を仕込み、撹拌しながら内温を沸点まで昇温させた後、アクリル系樹脂(A’-1)の共重合成分(モノマー)である、アクリル酸(AAc)(共重合性モノマー(a2))8部と、2-ヒドロキシエチルメタクリレート(HEMA)(共重合性モノマー(a2))0.1部とn-ブチルアクリレート(BA)((メタ)アクリル酸アルキルエステルモノマー(a3))91.9部とを混合溶解させた混合液を2時間にわたって滴下した。更に、重合途中に、トルエン13.3部に、AIBN0.08部を追加し、還流下6.0時間反応させた後、酢酸エチル90.68部、トルエン2.03部で希釈してアクリル系樹脂(A’-1)の溶液を得た。
[Preparation of Acrylic Resin (A'-1)]
In a reactor equipped with a thermometer, a stirrer, a dropping funnel and a reflux condenser, 61.3 parts of ethyl acetate and 0.037 parts of 2,2'-azobisisobutyronitrile (AIBN) were charged, and the internal temperature was raised to the boiling point while stirring, and then a mixed liquid obtained by mixing and dissolving 8 parts of acrylic acid (AAc) (copolymerizable monomer (a2)), 0.1 parts of 2-hydroxyethyl methacrylate (HEMA) (copolymerizable monomer (a2)) and 91.9 parts of n-butyl acrylate (BA) ((meth)acrylic acid alkyl ester monomer (a3)) which are copolymerization components (monomers) of the acrylic resin (A'-1) was dropped over 2 hours. Furthermore, during the polymerization, 0.08 parts of AIBN was added to 13.3 parts of toluene, and the mixture was reacted under reflux for 6.0 hours, and then diluted with 90.68 parts of ethyl acetate and 2.03 parts of toluene to obtain a solution of the acrylic resin (A'-1).
<エポキシ系架橋剤(B)>
多官能エポキシ樹脂(B-1):TETRAD-C(三菱ガス化学社製)
<Epoxy-based crosslinking agent (B)>
Multifunctional epoxy resin (B-1): TETRAD-C (manufactured by Mitsubishi Gas Chemical Company, Inc.)
[実施例1]
〔粘着剤組成物の調製〕
上記で得られたアクリル系樹脂(A-1)の固形分100部に対して、エポキシ系架橋剤(B-1)0.1部を配合し、粘着剤組成物を調製した。
[Example 1]
[Preparation of Pressure-Sensitive Adhesive Composition]
A pressure-sensitive adhesive composition was prepared by blending 0.1 part of an epoxy-based crosslinking agent (B-1) with 100 parts of the solid content of the acrylic resin (A-1) obtained above.
〔粘着フィルムの作製〕
上記で調製した粘着剤組成物を乾燥後の粘着剤層の厚みが約25μmになるように、基材のPETフィルム(厚み38μm)に塗布した後、100℃で2分間乾燥させた。その後、塗工面に、離型処理されたPETフィルム(離型フィルム:厚み38μm)を貼着して粘着剤層を保護し、粘着フィルムを作製した。
得られた粘着フィルムを用いて下記の各特性の評価を行った。結果を、後記の表2に示す。
[Preparation of adhesive film]
The pressure-sensitive adhesive composition prepared above was applied to a PET film (thickness: 38 μm) as a substrate so that the thickness of the pressure-sensitive adhesive layer after drying would be about 25 μm, and then dried for 2 minutes at 100° C. Thereafter, a release-treated PET film (release film: thickness: 38 μm) was attached to the coated surface to protect the pressure-sensitive adhesive layer, thereby producing a pressure-sensitive adhesive film.
The obtained pressure-sensitive adhesive film was evaluated for the following properties, and the results are shown in Table 2 below.
<粘着力>
(乾燥面への粘着力)
上記で得られた粘着フィルムを40℃で3日間エージング処理した後、25mm×100mmの試験片となるよう作製し、離型フィルムを剥がしたうえで、ステンレス板(SUS304BA板)に、23℃、相対湿度50%の雰囲気下にて2kgゴムローラー2往復で加圧貼付した。そして、同雰囲気下で30分間静置した後、剥離速度300mm/minで180度剥離強度(N/25mm)を測定した。
<Adhesive strength>
(Adhesion to dry surfaces)
The adhesive film obtained above was aged at 40° C. for 3 days, and then prepared into a test piece of 25 mm×100 mm. The release film was peeled off, and the test piece was pressed and attached to a stainless steel plate (SUS304BA plate) with a 2 kg rubber roller in two passes at 23° C. and 50% relative humidity. The test piece was then left to stand for 30 minutes in the same atmosphere, and the 180° peel strength (N/25 mm) was measured at a peel speed of 300 mm/min.
(湿潤面への粘着力)
上記で得られた粘着フィルムを40℃で3日間エージング処理した後、25mm×100mmの試験片となるよう作製し、離型フィルムを剥がしたうえで、表面を精製水で濡らしたステンレス板(SUS304BA板)に、23℃、相対湿度50%の雰囲気下にて2kgゴムローラー2往復で加圧貼付した。そして、同雰囲気下で30分間静置した後、剥離速度300mm/minで180度剥離強度(N/25mm)を測定し、以下の基準で評価した。
(評価基準)
○・・・7.0N/25mm以上
△・・・5.0N/25mm以上、7.0N/25mm未満
×・・・5.0N/25mm未満
(Adhesion to wet surfaces)
The adhesive film obtained above was aged at 40° C. for 3 days, and then prepared into a test piece of 25 mm×100 mm. The release film was peeled off, and the surface was wetted with purified water and the test piece was pressed and attached to a stainless steel plate (SUS304BA plate) by rolling it back and forth twice with a 2 kg rubber roller under an atmosphere of 23° C. and 50% relative humidity. After leaving the test piece for 30 minutes under the same atmosphere, the 180° peel strength (N/25 mm) was measured at a peel speed of 300 mm/min, and evaluated according to the following criteria.
(Evaluation Criteria)
○: 7.0N/25mm or more △: 5.0N/25mm or more, less than 7.0N/25mm ×: less than 5.0N/25mm
<耐汚染性>
(湿潤面への耐汚染性)
上記で得られた粘着フィルムを40℃で3日間エージング処理した後、25mm×100mmの試験片となるよう作製し、離型フィルムを剥がしたうえで、表面を精製水で濡らしたステンレス板(SUS304BA板)に、23℃、相対湿度50%の雰囲気下にて2kgゴムローラー2往復で加圧貼付した。そして、同雰囲気下で30分間静置した後、剥離速度300mm/minで180度剥離後の被着体表面の様子を観察し、以下の基準で評価した。
(評価基準)
○:糊残りは確認されなかった
×:糊残りが確認された
<Stain resistance>
(Resistance to stains on wet surfaces)
The adhesive film obtained above was aged at 40° C. for 3 days, and then prepared into a test piece of 25 mm×100 mm. The release film was peeled off, and the surface was pressed and attached to a stainless steel plate (SUS304BA plate) whose surface had been wetted with purified water, using a 2 kg rubber roller in two passes back and forth at 23° C. and a relative humidity of 50%. After leaving the film to stand for 30 minutes in the same atmosphere, the state of the adherend surface after 180° peeling at a peeling speed of 300 mm/min was observed, and the surface was evaluated according to the following criteria.
(Evaluation Criteria)
○: No adhesive residue was observed ×: Adhesive residue was observed
[実施例2~13、比較例1]
下記の表2に示すアクリル系樹脂を使用した以外は実施例1と同様にして粘着剤組成物を調製し、粘着フィルムを作製した。得られた粘着剤組成物および粘着フィルムを用いて、実施例1と同様の評価を行った。結果を、下記の表2に併せて示す。
[Examples 2 to 13, Comparative Example 1]
Pressure-sensitive adhesive compositions were prepared and pressure-sensitive adhesive films were produced in the same manner as in Example 1, except that the acrylic resins shown in Table 2 below were used. Using the obtained pressure-sensitive adhesive compositions and pressure-sensitive adhesive films, evaluations were carried out in the same manner as in Example 1. The results are also shown in Table 2 below.
上記表2の結果より、実施例においては、湿潤面に対する粘着力に優れるものであるのに対して、特定構造のモノマーを共重合成分として含まないアクリル系樹脂を用いた比較例では、湿潤面に対する粘着力が劣るものであった。
このことからも、アクリル系樹脂が特定構造のモノマーを共重合成分として含むことが重要であることが分かる。
The results in Table 2 above show that the examples have excellent adhesion to wet surfaces, whereas the comparative examples, which used acrylic resins that did not contain monomers of a specific structure as copolymerization components, had poor adhesion to wet surfaces.
This also shows that it is important that the acrylic resin contains a monomer having a specific structure as a copolymerization component.
また、実施例の粘着剤組成物は、湿潤面に対する耐汚染性も良好であることから、マスキングフィルム用粘着剤およびマスキング用粘着フィルムに好適に用いられることが分かる。 The adhesive composition of the examples also has good resistance to contamination on wet surfaces, and is therefore suitable for use as an adhesive for masking films and as an adhesive film for masking.
本発明のアクリル系樹脂を用いてなる粘着剤組成物から得られる粘着剤は、水中や湿潤条件下でも、充分な粘着性能を発揮できる粘着剤組成物を得ることができる。従って、マスキングフィルム用粘着剤、表面保護フィルム用粘着剤、表示ラベル用粘着剤、養生テープ用粘着剤等の各種部材用の粘着剤として好適に用いることができるが、なかでもマスキングフィルム用粘着剤として、特に建築用のマスキングフィルム用粘着剤として好適に用いられる。 The adhesive obtained from the adhesive composition using the acrylic resin of the present invention can provide an adhesive composition that can exhibit sufficient adhesive performance even in water or under wet conditions. Therefore, it can be suitably used as an adhesive for various components such as an adhesive for masking films, an adhesive for surface protection films, an adhesive for display labels, and an adhesive for masking tapes, but is particularly suitable for use as an adhesive for masking films, and particularly as an adhesive for masking films for construction.
Claims (7)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021035503A JP7635582B2 (en) | 2021-03-05 | 2021-03-05 | Acrylic resin, and adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021035503A JP7635582B2 (en) | 2021-03-05 | 2021-03-05 | Acrylic resin, and adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022135585A JP2022135585A (en) | 2022-09-15 |
| JP7635582B2 true JP7635582B2 (en) | 2025-02-26 |
Family
ID=83231479
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021035503A Active JP7635582B2 (en) | 2021-03-05 | 2021-03-05 | Acrylic resin, and adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7635582B2 (en) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102552695B1 (en) * | 2022-10-27 | 2023-07-06 | 제이엘켐 주식회사 | Binder resin for electrode of secondary battery, anode for secondary battery and secondary battery |
| CN117965112B (en) * | 2024-04-01 | 2024-06-11 | 广东粤港澳大湾区黄埔材料研究院 | High temperature resistant anaerobic adhesive and its use method |
| CN120365808B (en) * | 2025-06-04 | 2025-10-24 | 佛山锐涂新能源材料技术有限公司 | A water-based coating of polydopamine-modified acrylic resin and its preparation process |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003255532A (en) | 2002-02-28 | 2003-09-10 | Mitsubishi Chemicals Corp | Photopolymerizable composition, photopolymerizable lithographic printing plate, and image forming method using the same |
| JP2012233059A (en) | 2011-04-28 | 2012-11-29 | Japan Science & Technology Agency | New polymer |
| CN107805434A (en) | 2017-10-13 | 2018-03-16 | 浙江大学 | A kind of fluorescent type electronic protection coating and preparation method thereof |
| JP2019019239A (en) | 2017-07-18 | 2019-02-07 | 日本カーバイド工業株式会社 | Adhesive composition for protection films and protection film |
| WO2019131351A1 (en) | 2017-12-27 | 2019-07-04 | 富士フイルム株式会社 | Resist composition, resist film, pattern forming method and method for producing electronic device |
| WO2019194047A1 (en) | 2018-04-04 | 2019-10-10 | 株式会社ポラテクノ | Copolymerization polymer, adhesive agent composition, and optical member containing same |
| JP2020029530A (en) | 2018-08-24 | 2020-02-27 | 宇部興産株式会社 | Acrylic copolymer and adhesive composition containing the same |
| JP2022086979A (en) | 2020-11-30 | 2022-06-09 | 大阪有機化学工業株式会社 | Curable resin composition |
| JP2022133971A (en) | 2021-03-02 | 2022-09-14 | 三井化学株式会社 | Antimicrobial material |
-
2021
- 2021-03-05 JP JP2021035503A patent/JP7635582B2/en active Active
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003255532A (en) | 2002-02-28 | 2003-09-10 | Mitsubishi Chemicals Corp | Photopolymerizable composition, photopolymerizable lithographic printing plate, and image forming method using the same |
| JP2012233059A (en) | 2011-04-28 | 2012-11-29 | Japan Science & Technology Agency | New polymer |
| JP2019019239A (en) | 2017-07-18 | 2019-02-07 | 日本カーバイド工業株式会社 | Adhesive composition for protection films and protection film |
| CN107805434A (en) | 2017-10-13 | 2018-03-16 | 浙江大学 | A kind of fluorescent type electronic protection coating and preparation method thereof |
| WO2019131351A1 (en) | 2017-12-27 | 2019-07-04 | 富士フイルム株式会社 | Resist composition, resist film, pattern forming method and method for producing electronic device |
| WO2019194047A1 (en) | 2018-04-04 | 2019-10-10 | 株式会社ポラテクノ | Copolymerization polymer, adhesive agent composition, and optical member containing same |
| JP2020029530A (en) | 2018-08-24 | 2020-02-27 | 宇部興産株式会社 | Acrylic copolymer and adhesive composition containing the same |
| JP2022086979A (en) | 2020-11-30 | 2022-06-09 | 大阪有機化学工業株式会社 | Curable resin composition |
| JP2022133971A (en) | 2021-03-02 | 2022-09-14 | 三井化学株式会社 | Antimicrobial material |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022135585A (en) | 2022-09-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6782071B2 (en) | Polarizing film with double-sided adhesive layer, its manufacturing method and image display device | |
| JP7635582B2 (en) | Acrylic resin, and adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same | |
| CN103168083B (en) | The optical component of Adhesive composition for optical component, optical component tackiness agent, band binder layer and image display device | |
| JP5611883B2 (en) | Water-dispersible acrylic pressure-sensitive adhesive composition for re-peeling and pressure-sensitive adhesive sheet | |
| JP5719194B2 (en) | Water-dispersible acrylic pressure-sensitive adhesive composition for re-peeling and pressure-sensitive adhesive sheet | |
| JP6996834B2 (en) | Adhesive for masking film, heat-resistant adhesive film for masking, and how to use it | |
| US20160185083A1 (en) | Pressure-sensitive-adhesive-layer-attached polarizing film, and image display device | |
| JP4776272B2 (en) | Polymer composition for pressure-sensitive adhesive, pressure-sensitive adhesive composition for surface protective film, and surface protective film | |
| WO2011132565A1 (en) | Water-dispersible acrylic adhesive agent composition and adhesive sheet | |
| KR101206591B1 (en) | Aqueous pressure-sensitive adhesive composition, preparation method thereof and pressure-sensitive adhesive film | |
| JP6977562B2 (en) | Acrylic pressure-sensitive adhesive composition, a pressure-sensitive adhesive using the same, a pressure-sensitive adhesive for a polarizing plate, and an image display device. | |
| TW200813180A (en) | Pressure sensitive adhesive agent and pressure sensitive adhesive film | |
| EP1546280A1 (en) | Removable, water-whitening resistant pressure sensitive adhesives | |
| JP6893124B2 (en) | Resin composition, resin layer, and laminated sheet | |
| TW201831632A (en) | Adhesive composition and use of same | |
| US20160209566A1 (en) | Double-sided pressure-sensitive-adhesive-layer-attached polarizing film, method for producing thereof, and image display device | |
| JP5518370B2 (en) | Method for producing water-dispersible acrylic pressure-sensitive adhesive composition for re-peeling, water-dispersed acrylic pressure-sensitive adhesive composition for re-peeling, pressure-sensitive adhesive layer and pressure-sensitive adhesive sheet | |
| JP7496260B2 (en) | Adhesive composition and adhesive sheet | |
| JP7635583B2 (en) | Acrylic resin, and adhesive composition, adhesive, adhesive film, masking adhesive, and masking adhesive film made using the same | |
| JP4174974B2 (en) | Adhesive composition and adhesive label or tape | |
| JP2011241386A (en) | Water-dispersible acrylic self-adhesive composition and self-adhesive sheet | |
| JP6091990B2 (en) | Composition for transparent adhesive sheet | |
| JP5991833B2 (en) | Acrylic pressure-sensitive adhesive, pressure-sensitive adhesive for optical members, optical member with a pressure-sensitive adhesive layer using the same, image display device, method for producing acrylic pressure-sensitive adhesive, and acrylic pressure-sensitive adhesive composition | |
| JP5877099B2 (en) | Composition for transparent adhesive sheet | |
| JP5623967B2 (en) | Water-dispersed acrylic pressure-sensitive adhesive composition and pressure-sensitive adhesive sheet |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231101 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240919 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241001 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241128 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250114 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250127 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7635582 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |