JP7537726B2 - Extracellular matrix, method for producing mature cardiomyocytes, and cardiomyocyte maturation kit - Google Patents
Extracellular matrix, method for producing mature cardiomyocytes, and cardiomyocyte maturation kit Download PDFInfo
- Publication number
- JP7537726B2 JP7537726B2 JP2020017809A JP2020017809A JP7537726B2 JP 7537726 B2 JP7537726 B2 JP 7537726B2 JP 2020017809 A JP2020017809 A JP 2020017809A JP 2020017809 A JP2020017809 A JP 2020017809A JP 7537726 B2 JP7537726 B2 JP 7537726B2
- Authority
- JP
- Japan
- Prior art keywords
- cardiomyocytes
- cells
- laminin
- psc
- cms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 210000004413 cardiac myocyte Anatomy 0.000 title claims description 178
- 210000002744 extracellular matrix Anatomy 0.000 title claims description 69
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 title claims description 68
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 title claims description 68
- 230000035800 maturation Effects 0.000 title claims description 59
- 238000004519 manufacturing process Methods 0.000 title claims description 17
- 108010038862 laminin 10 Proteins 0.000 claims description 45
- 108010085895 Laminin Proteins 0.000 claims description 44
- 239000012634 fragment Substances 0.000 claims description 43
- 210000004027 cell Anatomy 0.000 description 125
- 108090000623 proteins and genes Proteins 0.000 description 53
- 230000004069 differentiation Effects 0.000 description 44
- 238000011282 treatment Methods 0.000 description 43
- 102000007547 Laminin Human genes 0.000 description 38
- 239000003814 drug Substances 0.000 description 34
- 210000001778 pluripotent stem cell Anatomy 0.000 description 33
- 238000000034 method Methods 0.000 description 29
- 229940079593 drug Drugs 0.000 description 25
- 230000014509 gene expression Effects 0.000 description 24
- 208000019622 heart disease Diseases 0.000 description 21
- 241000699666 Mus <mouse, genus> Species 0.000 description 20
- 108010010803 Gelatin Proteins 0.000 description 19
- 229920000159 gelatin Polymers 0.000 description 19
- 239000008273 gelatin Substances 0.000 description 19
- 235000019322 gelatine Nutrition 0.000 description 19
- 235000011852 gelatine desserts Nutrition 0.000 description 19
- 210000002235 sarcomere Anatomy 0.000 description 19
- 108091028043 Nucleic acid sequence Proteins 0.000 description 17
- 201000010099 disease Diseases 0.000 description 17
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 17
- 241000282414 Homo sapiens Species 0.000 description 15
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 14
- 239000011575 calcium Substances 0.000 description 14
- 229910052791 calcium Inorganic materials 0.000 description 14
- 230000006698 induction Effects 0.000 description 13
- 238000011156 evaluation Methods 0.000 description 11
- 241000699670 Mus sp. Species 0.000 description 10
- 238000004458 analytical method Methods 0.000 description 10
- 238000007876 drug discovery Methods 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 10
- -1 Hrc Proteins 0.000 description 9
- 102000001045 Connexin 43 Human genes 0.000 description 8
- 108010069241 Connexin 43 Proteins 0.000 description 8
- 241000282412 Homo Species 0.000 description 8
- 241001465754 Metazoa Species 0.000 description 8
- 230000029058 respiratory gaseous exchange Effects 0.000 description 8
- 238000004904 shortening Methods 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 7
- 108700008625 Reporter Genes Proteins 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 7
- 210000002064 heart cell Anatomy 0.000 description 7
- 230000001939 inductive effect Effects 0.000 description 7
- 239000003550 marker Substances 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 102000008186 Collagen Human genes 0.000 description 6
- 108010035532 Collagen Proteins 0.000 description 6
- 238000001061 Dunnett's test Methods 0.000 description 6
- 230000000747 cardiac effect Effects 0.000 description 6
- 229920001436 collagen Polymers 0.000 description 6
- 230000001605 fetal effect Effects 0.000 description 6
- 230000003834 intracellular effect Effects 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 239000002609 medium Substances 0.000 description 6
- 230000002438 mitochondrial effect Effects 0.000 description 6
- 108090000765 processed proteins & peptides Proteins 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 239000013598 vector Substances 0.000 description 6
- MNULEGDCPYONBU-WMBHJXFZSA-N (1r,4s,5e,5'r,6'r,7e,10s,11r,12s,14r,15s,16s,18r,19s,20r,21e,25s,26r,27s,29s)-4-ethyl-11,12,15,19-tetrahydroxy-6'-[(2s)-2-hydroxypropyl]-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trio Polymers O([C@@H]1CC[C@@H](/C=C/C=C/C[C@H](C)[C@@H](O)[C@](C)(O)C(=O)[C@H](C)[C@@H](O)[C@H](C)C(=O)[C@H](C)[C@@H](O)[C@H](C)/C=C/C(=O)O[C@H]([C@H]2C)[C@H]1C)CC)[C@]12CC[C@@H](C)[C@@H](C[C@H](C)O)O1 MNULEGDCPYONBU-WMBHJXFZSA-N 0.000 description 5
- MNULEGDCPYONBU-DJRUDOHVSA-N (1s,4r,5z,5'r,6'r,7e,10s,11r,12s,14r,15s,18r,19r,20s,21e,26r,27s)-4-ethyl-11,12,15,19-tetrahydroxy-6'-(2-hydroxypropyl)-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trione Polymers O([C@H]1CC[C@H](\C=C/C=C/C[C@H](C)[C@@H](O)[C@](C)(O)C(=O)[C@H](C)[C@@H](O)C(C)C(=O)[C@H](C)[C@H](O)[C@@H](C)/C=C/C(=O)OC([C@H]2C)C1C)CC)[C@]12CC[C@@H](C)[C@@H](CC(C)O)O1 MNULEGDCPYONBU-DJRUDOHVSA-N 0.000 description 5
- MNULEGDCPYONBU-YNZHUHFTSA-N (4Z,18Z,20Z)-22-ethyl-7,11,14,15-tetrahydroxy-6'-(2-hydroxypropyl)-5',6,8,10,12,14,16,28,29-nonamethylspiro[2,26-dioxabicyclo[23.3.1]nonacosa-4,18,20-triene-27,2'-oxane]-3,9,13-trione Polymers CC1C(C2C)OC(=O)\C=C/C(C)C(O)C(C)C(=O)C(C)C(O)C(C)C(=O)C(C)(O)C(O)C(C)C\C=C/C=C\C(CC)CCC2OC21CCC(C)C(CC(C)O)O2 MNULEGDCPYONBU-YNZHUHFTSA-N 0.000 description 5
- MNULEGDCPYONBU-VVXVDZGXSA-N (5e,5'r,7e,10s,11r,12s,14s,15r,16r,18r,19s,20r,21e,26r,29s)-4-ethyl-11,12,15,19-tetrahydroxy-6'-[(2s)-2-hydroxypropyl]-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trione Polymers C([C@H](C)[C@@H](O)[C@](C)(O)C(=O)[C@@H](C)[C@H](O)[C@@H](C)C(=O)[C@H](C)[C@@H](O)[C@H](C)/C=C/C(=O)OC([C@H]1C)[C@H]2C)\C=C\C=C\C(CC)CCC2OC21CC[C@@H](C)C(C[C@H](C)O)O2 MNULEGDCPYONBU-VVXVDZGXSA-N 0.000 description 5
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 5
- MNULEGDCPYONBU-UHFFFAOYSA-N 4-ethyl-11,12,15,19-tetrahydroxy-6'-(2-hydroxypropyl)-5',10,12,14,16,18,20,26,29-nonamethylspiro[24,28-dioxabicyclo[23.3.1]nonacosa-5,7,21-triene-27,2'-oxane]-13,17,23-trione Polymers CC1C(C2C)OC(=O)C=CC(C)C(O)C(C)C(=O)C(C)C(O)C(C)C(=O)C(C)(O)C(O)C(C)CC=CC=CC(CC)CCC2OC21CCC(C)C(CC(C)O)O2 MNULEGDCPYONBU-UHFFFAOYSA-N 0.000 description 5
- 208000031229 Cardiomyopathies Diseases 0.000 description 5
- 239000013614 RNA sample Substances 0.000 description 5
- 238000007792 addition Methods 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 238000011161 development Methods 0.000 description 5
- 230000018109 developmental process Effects 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 230000000877 morphologic effect Effects 0.000 description 5
- 230000002107 myocardial effect Effects 0.000 description 5
- 208000031225 myocardial ischemia Diseases 0.000 description 5
- 229930191479 oligomycin Natural products 0.000 description 5
- MNULEGDCPYONBU-AWJDAWNUSA-N oligomycin A Polymers O([C@H]1CC[C@H](/C=C/C=C/C[C@@H](C)[C@H](O)[C@@](C)(O)C(=O)[C@@H](C)[C@H](O)[C@@H](C)C(=O)[C@@H](C)[C@H](O)[C@@H](C)/C=C/C(=O)O[C@@H]([C@@H]2C)[C@@H]1C)CC)[C@@]12CC[C@H](C)[C@H](C[C@@H](C)O)O1 MNULEGDCPYONBU-AWJDAWNUSA-N 0.000 description 5
- 229950010131 puromycin Drugs 0.000 description 5
- 230000001172 regenerating effect Effects 0.000 description 5
- 210000000130 stem cell Anatomy 0.000 description 5
- 238000011222 transcriptome analysis Methods 0.000 description 5
- 101150112561 CD36 gene Proteins 0.000 description 4
- BMZRVOVNUMQTIN-UHFFFAOYSA-N Carbonyl Cyanide para-Trifluoromethoxyphenylhydrazone Chemical compound FC(F)(F)OC1=CC=C(NN=C(C#N)C#N)C=C1 BMZRVOVNUMQTIN-UHFFFAOYSA-N 0.000 description 4
- 206010048610 Cardiotoxicity Diseases 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 108010067306 Fibronectins Proteins 0.000 description 4
- 102000016359 Fibronectins Human genes 0.000 description 4
- 108020005004 Guide RNA Proteins 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 4
- 239000000556 agonist Substances 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 231100000259 cardiotoxicity Toxicity 0.000 description 4
- 230000011748 cell maturation Effects 0.000 description 4
- 238000012258 culturing Methods 0.000 description 4
- 238000000684 flow cytometry Methods 0.000 description 4
- 108091006047 fluorescent proteins Proteins 0.000 description 4
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 4
- 210000004165 myocardium Anatomy 0.000 description 4
- 210000004940 nucleus Anatomy 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 239000000523 sample Substances 0.000 description 4
- 238000012216 screening Methods 0.000 description 4
- 231100000419 toxicity Toxicity 0.000 description 4
- 230000001988 toxicity Effects 0.000 description 4
- UIFFUZWRFRDZJC-UHFFFAOYSA-N Antimycin A1 Natural products CC1OC(=O)C(CCCCCC)C(OC(=O)CC(C)C)C(C)OC(=O)C1NC(=O)C1=CC=CC(NC=O)=C1O UIFFUZWRFRDZJC-UHFFFAOYSA-N 0.000 description 3
- NQWZLRAORXLWDN-UHFFFAOYSA-N Antimycin-A Natural products CCCCCCC(=O)OC1C(C)OC(=O)C(NC(=O)c2ccc(NC=O)cc2O)C(C)OC(=O)C1CCCC NQWZLRAORXLWDN-UHFFFAOYSA-N 0.000 description 3
- 108091033409 CRISPR Proteins 0.000 description 3
- 206010059866 Drug resistance Diseases 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 241001559542 Hippocampus hippocampus Species 0.000 description 3
- 241000288906 Primates Species 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- 230000036982 action potential Effects 0.000 description 3
- 239000000427 antigen Substances 0.000 description 3
- 108091007433 antigens Proteins 0.000 description 3
- 102000036639 antigens Human genes 0.000 description 3
- UIFFUZWRFRDZJC-SBOOETFBSA-N antimycin A Chemical compound C[C@H]1OC(=O)[C@H](CCCCCC)[C@@H](OC(=O)CC(C)C)[C@H](C)OC(=O)[C@H]1NC(=O)C1=CC=CC(NC=O)=C1O UIFFUZWRFRDZJC-SBOOETFBSA-N 0.000 description 3
- PVEVXUMVNWSNIG-UHFFFAOYSA-N antimycin A3 Natural products CC1OC(=O)C(CCCC)C(OC(=O)CC(C)C)C(C)OC(=O)C1NC(=O)C1=CC=CC(NC=O)=C1O PVEVXUMVNWSNIG-UHFFFAOYSA-N 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000007877 drug screening Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 210000002458 fetal heart Anatomy 0.000 description 3
- 210000003754 fetus Anatomy 0.000 description 3
- 102000034287 fluorescent proteins Human genes 0.000 description 3
- 210000003976 gap junction Anatomy 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 239000005556 hormone Substances 0.000 description 3
- 229940088597 hormone Drugs 0.000 description 3
- 238000012744 immunostaining Methods 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 208000010125 myocardial infarction Diseases 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 239000013612 plasmid Substances 0.000 description 3
- 238000000513 principal component analysis Methods 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- JUVIOZPCNVVQFO-UHFFFAOYSA-N rotenone Natural products O1C2=C3CC(C(C)=C)OC3=CC=C2C(=O)C2C1COC1=C2C=C(OC)C(OC)=C1 JUVIOZPCNVVQFO-UHFFFAOYSA-N 0.000 description 3
- 229940080817 rotenone Drugs 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 150000003384 small molecules Chemical class 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 238000007619 statistical method Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 238000013518 transcription Methods 0.000 description 3
- 230000035897 transcription Effects 0.000 description 3
- 241000251468 Actinopterygii Species 0.000 description 2
- 241000271566 Aves Species 0.000 description 2
- 101150063956 CASQ2 gene Proteins 0.000 description 2
- 101150091725 CKMT2 gene Proteins 0.000 description 2
- 241000938605 Crocodylia Species 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 101100323278 Mus musculus Ankrd23 gene Proteins 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- 102000040945 Transcription factor Human genes 0.000 description 2
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 2
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 2
- 206010003119 arrhythmia Diseases 0.000 description 2
- 230000006793 arrhythmia Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 238000004364 calculation method Methods 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000008602 contraction Effects 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 231100000517 death Toxicity 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 210000002242 embryoid body Anatomy 0.000 description 2
- 210000002253 embryonic cardiomyocyte Anatomy 0.000 description 2
- 210000001671 embryonic stem cell Anatomy 0.000 description 2
- 230000001973 epigenetic effect Effects 0.000 description 2
- 102000034240 fibrous proteins Human genes 0.000 description 2
- 108091005899 fibrous proteins Proteins 0.000 description 2
- 238000012239 gene modification Methods 0.000 description 2
- 230000005017 genetic modification Effects 0.000 description 2
- 235000013617 genetically modified food Nutrition 0.000 description 2
- 238000010362 genome editing Methods 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 239000005090 green fluorescent protein Substances 0.000 description 2
- 229960000890 hydrocortisone Drugs 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 210000004263 induced pluripotent stem cell Anatomy 0.000 description 2
- 230000000366 juvenile effect Effects 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 238000001638 lipofection Methods 0.000 description 2
- 208000004731 long QT syndrome Diseases 0.000 description 2
- 210000001161 mammalian embryo Anatomy 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 230000036284 oxygen consumption Effects 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 230000001766 physiological effect Effects 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 239000002096 quantum dot Substances 0.000 description 2
- 230000036390 resting membrane potential Effects 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 230000001052 transient effect Effects 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- 241000701161 unidentified adenovirus Species 0.000 description 2
- 241001430294 unidentified retrovirus Species 0.000 description 2
- 239000013603 viral vector Substances 0.000 description 2
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- 101150111620 AQP1 gene Proteins 0.000 description 1
- 230000002407 ATP formation Effects 0.000 description 1
- 101150083996 ATP1A2 gene Proteins 0.000 description 1
- 108091006112 ATPases Proteins 0.000 description 1
- 101150048150 Acsl1 gene Proteins 0.000 description 1
- 102000010825 Actinin Human genes 0.000 description 1
- 108010063503 Actinin Proteins 0.000 description 1
- 102000057290 Adenosine Triphosphatases Human genes 0.000 description 1
- 239000012103 Alexa Fluor 488 Substances 0.000 description 1
- IGAZHQIYONOHQN-UHFFFAOYSA-N Alexa Fluor 555 Substances C=12C=CC(=N)C(S(O)(=O)=O)=C2OC2=C(S(O)(=O)=O)C(N)=CC=C2C=1C1=CC=C(C(O)=O)C=C1C(O)=O IGAZHQIYONOHQN-UHFFFAOYSA-N 0.000 description 1
- 239000012099 Alexa Fluor family Substances 0.000 description 1
- 241000243818 Annelida Species 0.000 description 1
- 241000238421 Arthropoda Species 0.000 description 1
- 239000012583 B-27 Supplement Substances 0.000 description 1
- 102100024505 Bone morphogenetic protein 4 Human genes 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 101150008656 COL1A1 gene Proteins 0.000 description 1
- 101150072801 COL1A2 gene Proteins 0.000 description 1
- 101150082216 COL2A1 gene Proteins 0.000 description 1
- 101150110807 COX8B gene Proteins 0.000 description 1
- 238000010354 CRISPR gene editing Methods 0.000 description 1
- 101150063057 CRYAB gene Proteins 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 241000251556 Chordata Species 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 101150008975 Col3a1 gene Proteins 0.000 description 1
- 102000004266 Collagen Type IV Human genes 0.000 description 1
- 108010042086 Collagen Type IV Proteins 0.000 description 1
- 102000010970 Connexin Human genes 0.000 description 1
- 108050001175 Connexin Proteins 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 1
- 101150030537 DCN gene Proteins 0.000 description 1
- 238000000018 DNA microarray Methods 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 101150070317 Ech1 gene Proteins 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 102000016942 Elastin Human genes 0.000 description 1
- 102000015782 Electron Transport Complex III Human genes 0.000 description 1
- 108010024882 Electron Transport Complex III Proteins 0.000 description 1
- 101150052568 Ephx2 gene Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 102100028412 Fibroblast growth factor 10 Human genes 0.000 description 1
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 1
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 1
- 101150109596 Fndc5 gene Proteins 0.000 description 1
- 101150045574 GSN gene Proteins 0.000 description 1
- 101150053089 GSTM1 gene Proteins 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 1
- 102000004144 Green Fluorescent Proteins Human genes 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 101150085568 HSPB6 gene Proteins 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 101150024039 Hjv gene Proteins 0.000 description 1
- 101000762379 Homo sapiens Bone morphogenetic protein 4 Proteins 0.000 description 1
- 101000917237 Homo sapiens Fibroblast growth factor 10 Proteins 0.000 description 1
- 101150064744 Hspb8 gene Proteins 0.000 description 1
- 102000004310 Ion Channels Human genes 0.000 description 1
- 101150023743 KLF9 gene Proteins 0.000 description 1
- 101150001241 Kcnip2 gene Proteins 0.000 description 1
- 241000713666 Lentivirus Species 0.000 description 1
- 101150034357 MYBPC3 gene Proteins 0.000 description 1
- 101150043413 MYH7 gene Proteins 0.000 description 1
- 101150074995 MYL2 gene Proteins 0.000 description 1
- 101150072768 MYZAP gene Proteins 0.000 description 1
- 241000282560 Macaca mulatta Species 0.000 description 1
- 241000237852 Mollusca Species 0.000 description 1
- 101100009090 Mus musculus Dcx gene Proteins 0.000 description 1
- 241000282339 Mustela Species 0.000 description 1
- 208000009525 Myocarditis Diseases 0.000 description 1
- 239000012580 N-2 Supplement Substances 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 101150020237 PTGDS gene Proteins 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 101150077058 Pdk2 gene Proteins 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 101150066884 Pink1 gene Proteins 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 241000282405 Pongo abelii Species 0.000 description 1
- 108010029485 Protein Isoforms Proteins 0.000 description 1
- 102000001708 Protein Isoforms Human genes 0.000 description 1
- 102000016611 Proteoglycans Human genes 0.000 description 1
- 108010067787 Proteoglycans Proteins 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 238000003559 RNA-seq method Methods 0.000 description 1
- 239000012979 RPMI medium Substances 0.000 description 1
- 238000011529 RT qPCR Methods 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 101150001016 Rgs5 gene Proteins 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 101150110386 SLC2A4 gene Proteins 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- 238000000692 Student's t-test Methods 0.000 description 1
- 206010042434 Sudden death Diseases 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 101150013356 TNNT2 gene Proteins 0.000 description 1
- 101150096321 TUBA4A gene Proteins 0.000 description 1
- AUYYCJSJGJYCDS-LBPRGKRZSA-N Thyrolar Chemical class IC1=CC(C[C@H](N)C(O)=O)=CC(I)=C1OC1=CC=C(O)C(I)=C1 AUYYCJSJGJYCDS-LBPRGKRZSA-N 0.000 description 1
- 208000018452 Torsade de pointes Diseases 0.000 description 1
- 208000002363 Torsades de Pointes Diseases 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 102000004987 Troponin T Human genes 0.000 description 1
- 108090001108 Troponin T Proteins 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- FPIPGXGPPPQFEQ-BOOMUCAASA-N Vitamin A Natural products OC/C=C(/C)\C=C\C=C(\C)/C=C/C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-BOOMUCAASA-N 0.000 description 1
- 101150056741 Xirp2 gene Proteins 0.000 description 1
- 101150092805 actc1 gene Proteins 0.000 description 1
- 108010023082 activin A Proteins 0.000 description 1
- 206010000891 acute myocardial infarction Diseases 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 description 1
- 210000004507 artificial chromosome Anatomy 0.000 description 1
- 210000002469 basement membrane Anatomy 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000000560 biocompatible material Substances 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 235000011148 calcium chloride Nutrition 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 238000000546 chi-square test Methods 0.000 description 1
- 235000013330 chicken meat Nutrition 0.000 description 1
- 210000000349 chromosome Anatomy 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 229920002549 elastin Polymers 0.000 description 1
- 230000005684 electric field Effects 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 210000002308 embryonic cell Anatomy 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 239000002158 endotoxin Substances 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 238000000855 fermentation Methods 0.000 description 1
- 230000004151 fermentation Effects 0.000 description 1
- 230000004720 fertilization Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 210000002837 heart atrium Anatomy 0.000 description 1
- 230000009067 heart development Effects 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 238000010166 immunofluorescence Methods 0.000 description 1
- 238000010874 in vitro model Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 230000002687 intercalation Effects 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 239000000644 isotonic solution Substances 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 229920006008 lipopolysaccharide Polymers 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 238000010859 live-cell imaging Methods 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000013507 mapping Methods 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000028161 membrane depolarization Effects 0.000 description 1
- 230000005787 mitochondrial ATP synthesis coupled electron transport Effects 0.000 description 1
- 230000004898 mitochondrial function Effects 0.000 description 1
- 230000006705 mitochondrial oxidative phosphorylation Effects 0.000 description 1
- 230000006540 mitochondrial respiration Effects 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 210000005087 mononuclear cell Anatomy 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 230000004660 morphological change Effects 0.000 description 1
- 239000012120 mounting media Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 210000001087 myotubule Anatomy 0.000 description 1
- 229930014626 natural product Natural products 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 238000012758 nuclear staining Methods 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 108010007425 oligomycin sensitivity conferring protein Proteins 0.000 description 1
- 238000001543 one-way ANOVA Methods 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000010827 pathological analysis Methods 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000008823 permeabilization Effects 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 238000002205 phenol-chloroform extraction Methods 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 208000014321 polymorphic ventricular tachycardia Diseases 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229940068968 polysorbate 80 Drugs 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 244000144977 poultry Species 0.000 description 1
- 235000013594 poultry meat Nutrition 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 108010054624 red fluorescent protein Proteins 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000002336 repolarization Effects 0.000 description 1
- 230000008672 reprogramming Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 210000002363 skeletal muscle cell Anatomy 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 108010067207 sodium-calcium exchanger 1 Proteins 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 238000004114 suspension culture Methods 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 206010042772 syncope Diseases 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 239000005495 thyroid hormone Substances 0.000 description 1
- 229940036555 thyroid hormone Drugs 0.000 description 1
- 230000025934 tissue morphogenesis Effects 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 1
- 230000002861 ventricular Effects 0.000 description 1
- 208000003663 ventricular fibrillation Diseases 0.000 description 1
- 206010047302 ventricular tachycardia Diseases 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 235000019155 vitamin A Nutrition 0.000 description 1
- 239000011719 vitamin A Substances 0.000 description 1
- 229940045997 vitamin a Drugs 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Landscapes
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
本発明は、特に、多能性幹細胞等から分化誘導された未成熟の心筋細胞を成熟化させる細胞外マトリックス、成熟心筋細胞製造方法、創薬支援方法、治療方法、成熟心筋細胞、及び心筋細胞成熟キットに関する。 The present invention particularly relates to an extracellular matrix that matures immature cardiomyocytes induced to differentiate from pluripotent stem cells, a method for producing mature cardiomyocytes, a drug discovery support method, a treatment method, mature cardiomyocytes, and a cardiomyocyte maturation kit.
日本生活習慣病予防協会(JPALD)の統計調査によると、特に成人以降に発症する心筋症等である心疾患の総患者数は172万9000人(2016年4月19日)、虚血性心疾患の年間死亡数、「急性心筋梗塞」3万7222人、「その他虚血性心疾患」3万4451人、心疾患による死亡数は年間19万6113人(2016年10月13日)と報告されている。また、心筋梗塞が含まれる虚血性心疾患の医療費は7,503億円、このうち65歳以上で5630億円を占める(2015年11月10日)。高齢化が進むことにより、これらが更に増加することが予想されている。 According to a statistical survey by the Japan Association for the Prevention of Lifestyle-Related Diseases (JPALD), the total number of patients with heart disease, particularly cardiomyopathy that develops after adulthood, is reported to be 1,729,000 (April 19, 2016), with the annual number of deaths from ischemic heart disease being 37,222 from "acute myocardial infarction" and 34,451 from "other ischemic heart disease," and the number of deaths due to heart disease being 196,113 per year (October 13, 2016). In addition, medical expenses for ischemic heart disease, which includes myocardial infarction, amount to 750.3 billion yen, of which 563 billion yen is for those aged 65 or older (November 10, 2015). As the aging population progresses, these figures are expected to increase further.
このような心疾患の治療のために、再生医療を用いることが検討されている。たとえば、ES細胞(Embryonic Stem Cell)やiPS細胞(induced Pluripotent Stem cells)等の多能性幹細胞を分化誘導して心筋細胞を作成し、これを移植することで、十度の心疾患を治療可能になると考えられる。さらに、このような分化誘導して作成した心筋細胞を用いることで、心疾患の解析や薬剤の毒性評価を行う技術も期待されている。 The use of regenerative medicine to treat such heart diseases is being considered. For example, it is believed that it may be possible to treat various heart diseases by inducing differentiation of pluripotent stem cells such as ES cells (embryonic stem cells) and iPS cells (induced pluripotent stem cells) to create cardiomyocytes and then transplanting these. Furthermore, it is expected that technology will be developed to analyze heart diseases and evaluate the toxicity of drugs by using cardiomyocytes created by such differentiation induction.
ここで、特許文献1を参照すると、心筋細胞前駆細胞及び成熟心筋細胞を多能性幹細胞から分化させる方法が記載されている。この方法では、(i)ラミニン511又は521及び(ii)ラミニン221の混合物を含む基材上で多能性幹細胞を分化させる。
Now, referring to
しかしながら、特許文献1に記載された技術等を用いて、多能性幹細胞等から分化誘導して作成された心筋細胞は、胎児(胎仔)型~新生児型となり、完全に成熟した大人(成人、成体)の心臓の心筋細胞と同様にはならなかった。
However, cardiomyocytes created by inducing differentiation from pluripotent stem cells using the technology described in
本発明は、このような状況に鑑みてなされたものであり、上述の課題を解消することを課題とする。 The present invention was made in light of these circumstances, and aims to resolve the above-mentioned issues.
本発明の細胞外マトリックスは、未成熟の心筋細胞を成熟させるための細胞外マトリックスであって、ラミニン断片を含み、前記ラミニン断片は、ラミニン511 E8断片及び/又はラミニン521 E8断片であることを特徴とする。
本発明の成熟心筋細胞製造方法は、未成熟の心筋細胞を、前記細胞外マトリックスを含む培地で培養し、成熟した心筋細胞を取得することを特徴とする。
本発明の心筋細胞成熟キットは、未成熟の心筋細胞を成熟させるための細胞外マトリックスを含み、前記細胞外マトリックスは、ラミニン断片を含み、前記ラミニン断片は、ラミニン511 E8断片及び/又はラミニン521 E8断片であることを特徴とする。
The extracellular matrix of the present invention is an extracellular matrix for maturing immature cardiomyocytes, and is characterized in that it contains a laminin fragment, and the laminin fragment is a laminin 511 E8 fragment and/or a laminin 521 E8 fragment.
The method for producing mature cardiomyocytes of the present invention is characterized in that immature cardiomyocytes are cultured in a medium containing the extracellular matrix to obtain mature cardiomyocytes .
The cardiomyocyte maturation kit of the present invention comprises an extracellular matrix for maturing immature cardiomyocytes, the extracellular matrix comprises a laminin fragment, and the laminin fragment is a laminin 511 E8 fragment and/or a laminin 521 E8 fragment.
本発明によれば、多能性幹細胞等に由来する未成熟の心筋細胞から、従来より成熟した成熟心筋細胞を得ることが可能な、ラミニン断片を含む細胞外マトリックスを提供することができる。 According to the present invention, it is possible to provide an extracellular matrix containing laminin fragments that can obtain more mature cardiomyocytes than conventional methods from immature cardiomyocytes derived from pluripotent stem cells, etc.
<実施の形態>
図1に、多能性幹細胞から分化誘導して得られる心筋細胞(以下、「PSC-CMs」という。)の例を示す。PSC-CMsは、胎児(胎仔)型~新生児型となり、完全に成熟した心臓の心筋細胞と同様にはならないことが分かっている。たとえば、図1(a)は、マウスのES細胞のような多能性幹細胞から分化誘導したPSC-CMsの例を示す。図2(b)は、実際のマウスの胎仔の心筋細胞の例を示す。図2(a)は、マウスのES細胞から分化誘導したPSC-CMsについて、それぞれ分化10日目、図2(b)は分化20日目、図2(c)は、分化30日目の様子を示す。このように、PSC-CMsは培養することで、多少、成熟するものの、マウス新生仔から単離した細胞と同程度にしかならない。このような状態では、マウス成体の細胞とは形態的にも大きな差がある。さらに、細胞内のカルシウム量の変化を見るカルシウムトランジェントでも、その未成熟パターンであることは明らかであった。
このため、PSC-CMsをより成熟させる成熟方法が求められていた。
<Embodiment>
FIG. 1 shows an example of cardiomyocytes (hereinafter referred to as "PSC-CMs") obtained by inducing differentiation from pluripotent stem cells. It is known that PSC-CMs become fetal (embryo) type to neonatal type, and do not become the same as cardiomyocytes of a fully mature heart. For example, FIG. 1(a) shows an example of PSC-CMs induced to differentiate from pluripotent stem cells such as mouse ES cells. FIG. 2(b) shows an example of actual mouse fetal cardiomyocytes. FIG. 2(a) shows PSC-CMs induced to differentiate from mouse ES cells on the 10th day of differentiation, FIG. 2(b) shows PSC-CMs on the 20th day of differentiation, and FIG. 2(c) shows PSC-CMs on the 30th day of differentiation. Thus, although PSC-CMs mature somewhat by culturing, they only reach the same level as cells isolated from newborn mice. In this state, there is a large morphological difference between them and adult mouse cells. Furthermore, the calcium transient, which shows the change in the amount of calcium in the cells, clearly shows that they are immature.
For this reason, a maturation method for further maturing PSC-CMs has been sought.
ここで、本発明者らは、発達の各段階(ステージ)にある細胞外マトリックスが、時期特異的に発現していることを見いだした。
このため、鋭意実験を繰り返し、この時期特異的に発現している細胞外マトリックスのうち、どの細胞外マトリックスが、心筋細胞の成熟に特異的な効果を持つかどうかを、網羅的に調べた。この際に、心筋細胞が成熟するのに合わせて発現が増加する遺伝子座に対し、蛍光タンパク質を挿入した多能性幹細胞株(レポーター細胞)を用いた。
そして、ラミニンE8フラグメント(E8断片)に効果があり、更に、ラミニン511 cE8断片及び/又はラミニン521 E8断片により、レポーター細胞の蛍光強度が増加し、形態や生理的な活性等が成熟することを確認して、本発明を完成させるに至った。
Here, the present inventors discovered that the extracellular matrix at each stage of development is expressed in a time-specific manner.
For this reason, we conducted repeated experiments to comprehensively investigate which extracellular matrices expressed specifically at this stage have a specific effect on the maturation of cardiomyocytes. In this study, we used a pluripotent stem cell line (reporter cell) in which a fluorescent protein was inserted into a gene locus whose expression increases as cardiomyocytes mature.
The present inventors then confirmed that laminin E8 fragment (E8 fragment) is effective, and further confirmed that laminin 511 cE8 fragment and/or
〔細胞外マトリックス〕
細胞外マトリックス(Extracellular Matrix、細胞外基質、細胞間マトリックス)は、生物において、細胞の外に存在する不溶性物質である。細胞外マトリックスは、細胞にとって、物理的な足場となり、更に、組織の形態の形成、分化、ホメオスタシス等についての、生化学的、生物力学的なシグナルカスケードに関連する。動物において、細胞外マトリックスは、繊維状のタンパク質、プロテオグリカン、グリコサミノグリカン等から構成される。このうち、繊維状のタンパク質は、コラーゲン、エラスチン、フィブロネクチン、ラミニン(Laminin)を含む。このうち、ラミニンは、細胞外マトリックスである基底膜を構成する巨大なタンパク質である。
[Extracellular matrix]
Extracellular matrix (ECM) is an insoluble substance present outside cells in living organisms. The ECM serves as a physical scaffold for cells, and is also involved in biochemical and biomechanical signal cascades for tissue morphogenesis, differentiation, homeostasis, and the like. In animals, the ECM is composed of fibrous proteins, proteoglycans, glycosaminoglycans, and the like. Among these, fibrous proteins include collagen, elastin, fibronectin, and laminin. Among these, laminin is a giant protein that constitutes the basement membrane, which is the extracellular matrix.
本実施形態の細胞外マトリックスは、心筋細胞の成熟を促進させるための特異的な細胞外マトリックスであり、ラミニン断片を含むことを特徴とする。
ここで、ラミニンは、3つの鎖(α鎖、β鎖、γ鎖)から構成される非常に大きなタンパク質である。本発明者らは、ラミニン全体を用いると、心筋細胞の成熟を逆に抑制して、前駆細胞の段階で安定的に止めてしまうことを見いだした。実際に、従来の組み換えラミニン521は、ヒト初期胚細胞で発現するラミニンとして、ヒト多能性幹細胞のような未分化の細胞を分化させずに維持させるのに用いられている(例えば、<URL=”https://www.veritastk.co.jp/sciencelibrary/pickup/laminin-521.html”>等参照)。
The extracellular matrix of the present embodiment is a specific extracellular matrix for promoting the maturation of cardiomyocytes, and is characterized by containing laminin fragments.
Here, laminin is a very large protein composed of three chains (α, β, and γ chains). The inventors have found that using the entire laminin inhibits the maturation of cardiomyocytes and stably stops them at the stage of precursor cells. In fact, conventional
しかしながら、本発明者らは、上述の細胞外マトリックスの網羅的な解析により、従来のラミニン全体とは逆に、ラミニンタンパクの断片(ラミニン断片)を用いることで、心筋細胞の成熟を促進させることを見いだした。すなわち、本実施形態の細胞外マトリックスは、細胞の成熟を促すシグナル伝達分子として機能し、それ以外の、細胞の成熟を抑えるシグナル伝達分子の箇所を含まないものと考えられる。また、本実施形態のラミニン断片は、心筋細胞が成熟するのに必要である、構造的な足場を提供するため、心臓の発達に役立つと考えられる。
ここで、本実施形態のラミニン断片としては、E8断片を用いることが好適である。ラミニンのE8断片は、細胞表面のインテグリンと結合する最小構成部位のタンパク片(ペプチド鎖)である。このうち、ラミニン511及び/又はラミニン522のE8断片を用いることが、特に、ヒトやマウスを含む脊椎動物の心筋細胞の成熟化に好適である。このラミニン511及び/又はラミニン522 E8断片は、それぞれの種の配列のものを用いることが好適である。また、化学的に修飾されていても、ペプチドの配列が一部異なっていても、他のペプチドと合成されたものであっても、その他の化学的な修飾を受けたものであってもよい。
However, the present inventors have found through the above-mentioned comprehensive analysis of the extracellular matrix that, contrary to the conventional use of the entire laminin, the use of a fragment of laminin protein (laminin fragment) promotes the maturation of cardiomyocytes. In other words, the extracellular matrix of this embodiment is considered to function as a signaling molecule that promotes cell maturation and does not contain any other signaling molecule that suppresses cell maturation. In addition, the laminin fragment of this embodiment is considered to be useful for cardiac development because it provides a structural scaffolding necessary for cardiomyocyte maturation.
Here, as the laminin fragment of this embodiment, it is preferable to use the E8 fragment. The E8 fragment of laminin is a protein fragment (peptide chain) of the minimum constituent portion that binds to integrin on the cell surface. Among these, the use of the E8 fragment of
本実施形態の動物は、特に限定されるものではなく、心臓がありラミニンを備える脊椎動物及び無脊椎動物を広く含む。脊椎動物としては、魚類、両生類、は虫類、鳥類、及び哺乳類を含む。具体的には、例えば、哺乳類は、例えば、マウス、ラット、フェレット、ハムスター、モルモット、又はウサギ等のげっ歯類、イヌ、ネコ、ヒツジ、ブタ、ウシ、ウマ、又は、アカゲザル、チンパンジー、オランウータン、ヒト等を含む霊長類等であってもよい。また、哺乳類の他にも、魚類、家禽を含む鳥類、爬虫類等を含む。また、無脊椎動物等であっても、脊索動物、軟体動物、環形動物、節足動物等、心臓を備える動物も広く含む。 The animals in this embodiment are not particularly limited, and broadly include vertebrates and invertebrates that have a heart and laminin. Vertebrates include fish, amphibians, reptiles, birds, and mammals. Specifically, for example, mammals may be rodents such as mice, rats, ferrets, hamsters, guinea pigs, and rabbits, dogs, cats, sheep, pigs, cows, horses, or primates including rhesus monkeys, chimpanzees, orangutans, and humans. In addition to mammals, they also include fish, birds including poultry, and reptiles. In addition, invertebrates also broadly include animals with a heart, such as chordates, mollusks, annelids, and arthropods.
本実施形態の心筋細胞は、各種の中胚葉系への分化誘導因子等を用いた手法により多能性幹細胞から分化されたPSC-CMsであってもよい。加えて、本実施形態の心筋細胞は、患者等の線維芽細胞や血液細胞に転写因子を導入して誘導されるinduced cardiomyocyte(iCM)であってもよい。さらに加えて、本実施形態の心筋細胞は、患者等の心臓から得られた初代培養(Primary Cell Culture)心筋細胞であってもよい。
さらに、本実施形態の心筋細胞は、心筋細胞に分化誘導された細胞を、各種マーカーや目視等によりコロニー等の形式で選択したものであってもよい。また、本実施形態の心筋細胞は、各種細胞の混合細胞集団、組織、臓器等(以下、「組織等」という。)であってもよい。これらの心筋細胞は、後述する成熟度スコアで示されるような様々な状態のものを混合して含んでいてもよい。すなわち、各細胞は、十分分化していなかったり、未成熟であったり、成体の細胞程、成熟していなかったりしてもよい。さらに加えて、本実施形態の心筋細胞は、後述するレポーター細胞を分化誘導したものを含んでいてもよい。
また、以下、これらの心筋細胞のうち、成熟した心筋細胞を、単に「成熟心筋細胞」という。
The cardiomyocytes of this embodiment may be PSC-CMs differentiated from pluripotent stem cells by a method using various mesodermal differentiation inducers. In addition, the cardiomyocytes of this embodiment may be induced cardiomyocytes (iCMs) induced by introducing a transcription factor into fibroblasts or blood cells of a patient or the like. Furthermore, the cardiomyocytes of this embodiment may be primary cell culture cardiomyocytes obtained from the heart of a patient or the like.
Furthermore, the cardiomyocytes of this embodiment may be cells that have been induced to differentiate into cardiomyocytes and selected in the form of colonies or the like using various markers or visual inspection. Furthermore, the cardiomyocytes of this embodiment may be a mixed cell population of various cells, tissues, organs, etc. (hereinafter referred to as "tissues, etc."). These cardiomyocytes may be mixed and contain cells in various states as indicated by the maturity score described below. That is, each cell may not be fully differentiated, may be immature, or may not be as mature as an adult cell. Furthermore, the cardiomyocytes of this embodiment may contain cells that have been induced to differentiate into reporter cells described below.
Furthermore, hereinafter, among these cardiomyocytes, mature cardiomyocytes will be simply referred to as "mature cardiomyocytes".
ここで、本実施形態の多能性幹細胞は、例えば、ヒトを含む霊長類、霊長類以外のほ乳類、その他の脊椎動物等の生物で各種細胞に分化可能な、多分化能を備える幹細胞(Stem Cell)を含む。ここで、本実施形態の多能性幹細胞は、継代可能であり、継代しても分化が進まない状態を保ち、核型等が変化しにくく、又はエピジェネティックな表現型が変化しにくい性質を有することが好適である。また、本実施形態の多能性幹細胞は、これに関連して、生体外(in vitro)又は生体内(in vivo)で十分な増殖能力を備えていることが好適である。このような本実施形態の多能性幹細胞の具体例としては、胚性幹細胞(Embryonic Stem Cell、以下、「ES細胞」という。)、人工多能性幹細胞(Induced Pluripotent Stem Cell、以下、「iPS細胞」という。)、その他の人工的に生成され若しくは選択された多能性を備える幹細胞等が挙げられる。これら本実施形態の多能性幹細胞は、特定の遺伝子を含むレトロウイルスやアデノウイルスやプラスミド等の各種ベクター、RNA、低分子化合物等により、体細胞を再プログラミングして作成された幹細胞であってもよい。
なお、本実施形態の多能性幹細胞としては、必ずしも全能性に近い多分化能を備えている細胞である必要はないものの、通常より多分化能が高いナイーブ(Naive)な細胞を用いることも可能である。また、本実施形態の多能性幹細胞は、疾患の患者から得られた細胞から作成された細胞、その他の疾患のモデルとなる細胞、レポーター遺伝子が組み込まれた細胞(レポーター細胞)、コンディショナルノックアウトが可能な細胞、その他の遺伝子組み換えされた細胞等であってもよい。この遺伝子組み換えは、染色体内の遺伝子の追加や修飾や削除、各種ベクターや人工染色体による遺伝子等の付加、エピジェネティック制御の変更、PNA等の人工遺伝物質の付加、その他の遺伝子組み換えを含む。
Here, the pluripotent stem cells of this embodiment include stem cells (stem cells) with pluripotency that can differentiate into various cells in organisms such as primates including humans, mammals other than primates, and other vertebrates. Here, the pluripotent stem cells of this embodiment are preferably passageable, maintain a state in which differentiation does not progress even when passaged, and have properties that the karyotype, etc., is unlikely to change, or the epigenetic phenotype is unlikely to change. In this regard, it is preferable that the pluripotent stem cells of this embodiment have sufficient proliferation ability in vitro or in vivo. Specific examples of such pluripotent stem cells of this embodiment include embryonic stem cells (hereinafter referred to as "ES cells"), induced pluripotent stem cells (hereinafter referred to as "iPS cells"), and other artificially generated or selected stem cells with pluripotency. These pluripotent stem cells of the present embodiment may be stem cells created by reprogramming somatic cells using various vectors such as retroviruses, adenoviruses, and plasmids containing specific genes, RNA, low molecular weight compounds, etc.
In addition, the pluripotent stem cells of this embodiment do not necessarily have to be cells with pluripotency close to totipotency, but it is also possible to use naive cells with higher pluripotency than normal. In addition, the pluripotent stem cells of this embodiment may be cells created from cells obtained from patients with a disease, cells that serve as models for other diseases, cells with reporter genes incorporated (reporter cells), cells that can be conditionally knocked out, other genetically modified cells, etc. This genetic modification includes the addition, modification, or deletion of genes in chromosomes, the addition of genes, etc. using various vectors or artificial chromosomes, changes in epigenetic control, the addition of artificial genetic materials such as PNA, and other genetic modifications.
〔成熟心筋細胞製造方法、成熟心筋細胞〕
本実施形態の成熟心筋細胞製造方法は、未成熟の心筋細胞を、本実施形態の細胞外マトリックスを含む培地で培養し、成熟した心筋細胞(成熟心筋細胞)を取得することを特徴とする。
本実施形態の成熟心筋細胞は、本実施形態の成熟心筋細胞製造方法により製造された成熟心筋細胞であって、心筋細胞の成熟に伴い発現が増加する成熟心筋細胞マーカーを指標として、未成熟の心筋細胞から、成熟した心筋細胞(成熟心筋細胞)を取得することを特徴とする。
[Method for producing mature cardiomyocytes, mature cardiomyocytes]
The method for producing mature cardiomyocytes of this embodiment is characterized in that immature cardiomyocytes are cultured in a medium containing the extracellular matrix of this embodiment to obtain mature cardiomyocytes (mature cardiomyocytes).
The mature cardiomyocytes of this embodiment are mature cardiomyocytes produced by the mature cardiomyocyte production method of this embodiment, and are characterized in that mature cardiomyocytes (mature cardiomyocytes) are obtained from immature cardiomyocytes using a mature cardiomyocyte marker whose expression increases with maturation of cardiomyocytes as an indicator.
ここで、本実施形態の成熟心筋細胞マーカーは、心筋細胞の成熟に伴い発現が増加するAcadvl、Acsl1、Acss1、Ankrd23、Aqp1、Atp1a2、Casq2、Cd36、Cep85l、Ckmt2、Clu、Cmya5、Coq10a、Cox7a1、Cox8b、Cryab、Dcn、Ech1、Ephx2、Fndc5、Gsn、Gstm1、Hfe2、Hrc、Hspb6、Hspb8、Kcnip2、Klf9、Lpi1、Lrrc2、Lrtm1、Mb、Mgp、Myom2、Myoz2、Myzap、Nfix、Pdk2、Perm1、Pink1、Ptgds、Rgs5、Rpl3l、S100a1、Sgcg、Slc2a4、Sparcl1、Tcap、Tmem182、Tuba4a、Txlnb、Xirp2、及びYipf7からなる群の一種又は任意の組み合わせを含む。
このうち、Myom2は、成人の心筋で発現し、Mバンド構造を含むタンパク質の3次元配列を安定化するタンパクの遺伝子である。
Here, the mature cardiomyocyte markers of this embodiment are Acadvl, Acsl1, Acss1, Ankrd23, Aqp1, Atp1a2, Casq2, Cd36, Cep85l, Ckmt2, Clu, Cmya5, Coq10a, Cox7a1, Cox8b, Cryab, Dcn, Ech1, Ephx2, Fndc5, Gsn, Gstm1, Hfe2, Hrc, Hspb6, H spb8, Kcnip2, Klf9, Lpi1, Lrrc2, Lrtm1, Mb, Mgp, Myom2, Myoz2, Myzap, Nfix, Pdk2, Perm1, Pink1, Ptgds, Rgs5, Rpl3l, S100a1, Sgcg, Slc2a4, Sparcll, Tcap, Tmem182, Tuba4a, Txlnb, Xirp2, and Yipf7, or any combination thereof.
Of these, Myom2 is a gene encoding a protein that is expressed in adult cardiac muscle and stabilizes the three-dimensional arrangement of proteins including the M-band structure.
具体的には、本実施形態の成熟心筋細胞は、上述の成熟心筋細胞マーカーの遺伝子座にレポーター遺伝子をノックインした多能性幹細胞を作成し、これをレポーター細胞として用いて、このレポーター細胞を成熟させることで製造可能である。
すなわち、まず、レポーター遺伝子をノックインした多能性幹細胞としてレポーター細胞を用意することが可能である。この上で、このレポーター細胞を分化誘導してPSC-CMsを作成し、レポーター遺伝子が活性化(発現)したものを指標としてフローサイトメトリーを用いた蛍光活性化セルソーティング(Fluorescence Activated Cell Sorting、以下、「FACS」という。)等で選択して取得することで、成熟心筋細胞を純化して取得することが可能である。
Specifically, the mature cardiomyocytes of this embodiment can be produced by creating pluripotent stem cells in which a reporter gene has been knocked into the gene locus of the above-mentioned mature cardiomyocyte marker, using this as a reporter cell, and maturing this reporter cell.
That is, it is possible to first prepare reporter cells as pluripotent stem cells with a reporter gene knocked in. Then, the reporter cells are induced to differentiate to produce PSC-CMs, and cells with an activated (expressed) reporter gene are selected and obtained by fluorescence activated cell sorting (hereinafter referred to as "FACS") using flow cytometry as an indicator, thereby making it possible to obtain purified mature cardiomyocytes.
より具体的に、本実施形態のレポーター細胞は、例えば、赤色蛍光タンパク質(Red Fluorescent Protein、以下「RFP」という。)やGFP緑色蛍光タンパク質(Green Fluorescent Protein、以下「GFP」という。)等の蛍光タンパク質の遺伝子を成熟心筋細胞マーカーの遺伝子座にノックインして作成可能である。 More specifically, the reporter cells of this embodiment can be created by knocking in a gene for a fluorescent protein, such as red fluorescent protein (hereinafter referred to as "RFP") or green fluorescent protein (hereinafter referred to as "GFP"), into the gene locus of a mature cardiomyocyte marker.
さらに、本実施形態のレポーター細胞は、例えば、マウスES細胞を用いる場合、キメラマウスを作成することが可能であってもよい。これにより、レポーター細胞を、動物の心臓の発達段階に対する実験等に広く用いることが可能となる。具体的には、本実施形態のレポーター細胞は、心筋細胞の成熟をより進めるための、細胞外マトリックス(Extracellular Matrix、以下、「ECM」とも省略する。)、ホルモン等の心筋細胞の成熟に関連する外部刺激のスクリーニング、成熟の最適化等に関するツールとして使用可能である。より具体的には、本実施形態のレポーター細胞は心臓病のモデリングや、後述する本実施形態の創薬支援方法において、治療薬の候補(候補薬物)、心疾患を治療するための候補薬物等のスクリーニングに用いることが可能である。 Furthermore, when using mouse ES cells, the reporter cells of this embodiment may be capable of producing chimeric mice. This allows the reporter cells to be widely used in experiments on the developmental stages of the animal's heart. Specifically, the reporter cells of this embodiment can be used as a tool for screening external stimuli related to the maturation of cardiomyocytes, such as extracellular matrix (ECM) and hormones, and optimizing maturation, in order to further promote the maturation of cardiomyocytes. More specifically, the reporter cells of this embodiment can be used for modeling heart disease and for screening candidate therapeutic drugs (candidate drugs) and candidate drugs for treating heart disease in the drug discovery support method of this embodiment described below.
本実施形態の成熟心筋細胞は、上述のレポーター細胞を成熟させた蛍光を発する成熟心筋細胞をFACSで取得して、純化することが可能である。この際、Cd36については、表面抗原に対応する、蛍光色素結合した抗体を指標として、成熟度を評価して取得することが可能である。この表面抗原は、Cd36の転写産物の細胞膜外の部分である。
以下の実施例では、Myom2に、レポーター遺伝子としてRFP遺伝子をノックインしたレポーター細胞を用いる例を示している。
なお、蛍光タンパク以外にも、薬剤耐性遺伝子を導入した細胞を用意し、これを分化誘導してPSC-CMsを作成し、成熟することで薬剤耐性を獲得した心筋細胞を純化することも可能である。すなわち、薬剤耐性遺伝子を、広義の「レポーター」細胞として用いることが可能である。
The mature cardiomyocytes of this embodiment can be purified by obtaining the mature cardiomyocytes emitting fluorescence by maturing the reporter cells described above using FACS. In this case, the maturation of Cd36 can be evaluated using a fluorescent dye-bound antibody corresponding to the surface antigen as an indicator. This surface antigen is the extracellular portion of the transcription product of Cd36.
In the following Example, an example is shown in which a reporter cell in which the RFP gene is knocked in as a reporter gene into Myom2 is used.
In addition to fluorescent proteins, it is also possible to prepare cells transfected with drug resistance genes, induce their differentiation to produce PSC-CMs, and purify cardiomyocytes that have acquired drug resistance through maturation. In other words, drug resistance genes can be used as "reporter" cells in a broad sense.
上述のように、本実施形態の成熟心臓細胞は、レポーター細胞を成熟させたPSC-CMsであってもよい。または、レポーター遺伝子をノックインしていないPSC-CMsであってもよい。すなわち、本実施形態の成熟心筋細胞製造方法により製造された成熟心筋細胞は、上述のレポーター細胞を含む、多能性幹細胞を分化誘導した任意の心筋細胞を用いることが可能である。つまり、本実施形態の成熟心筋細胞は、レポーター細胞及びレポーター細胞以外のPSC-CMsを用いることも可能である。さらに、多能性幹細胞の分化誘導を行う際に、心筋細胞成熟剤を同時に用いることも可能である。または、心筋細胞成熟剤を多能性幹細胞の分化誘導のために用いてもよい。これらは、例えば、適当な核内移行するウイルスベクター、各種プラスミド、PNA等を用いることが可能である。このウイルスベクターは、例えば、レンチウイルス、アデノウイルス、アデノ随伴ウイルス、レトロウイルス等の当業者に一般的なウイルスを用いて構成されてもよい。加えて、心筋細胞成熟剤を、適切なDDS(Drug Delivery System)、エレクトロポーション、その他の当業者に用いられる手法で細胞内、核内に導入することが可能である。 As described above, the mature cardiac cells of this embodiment may be PSC-CMs obtained by maturing reporter cells. Alternatively, the mature cardiac cells of this embodiment may be PSC-CMs in which a reporter gene is not knocked in. That is, the mature cardiac cells produced by the mature cardiac cell production method of this embodiment may be any cardiac cells obtained by inducing differentiation of pluripotent stem cells, including the reporter cells described above. That is, the mature cardiac cells of this embodiment may be reporter cells and PSC-CMs other than reporter cells. Furthermore, when inducing differentiation of pluripotent stem cells, it is also possible to use a cardiac muscle cell maturation agent at the same time. Alternatively, the cardiac muscle cell maturation agent may be used to induce differentiation of pluripotent stem cells. For example, suitable viral vectors that transfer into the nucleus, various plasmids, PNA, etc. may be used. This viral vector may be constructed using viruses that are common to those skilled in the art, such as lentivirus, adenovirus, adeno-associated virus, and retrovirus. In addition, the cardiomyocyte maturation agent can be introduced into cells or nuclei using an appropriate DDS (Drug Delivery System), electroporation, or other methods used by those skilled in the art.
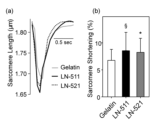
本実施形態の成熟心筋細胞製造方法にて製造されたPSC-CMs(成熟心筋細胞)は、集合し線維状のサルコメア構造を形成することが可能である。本実施形態の成熟方法にて成熟させたPSC-CMsが培養された細胞塊中にサルコメア構造が認められる場合、心筋細胞が機能性の心筋を構成していると判定することが可能である。または、本実施形態の成熟方法にて成熟させたPSC-CMsの細胞塊の一部を取得し、本実施形態の成熟度評価方法にて成熟度スコアを評価することも可能である。 PSC-CMs (mature cardiomyocytes) produced by the mature cardiomyocyte production method of this embodiment are capable of forming a fibrous sarcomere structure by aggregation. When a sarcomere structure is observed in a cell mass in which PSC-CMs matured by the maturation method of this embodiment are cultured, it is possible to determine that the cardiomyocytes constitute functional myocardium. Alternatively, it is also possible to obtain a portion of the cell mass of PSC-CMs matured by the maturation method of this embodiment and evaluate the maturity score by the maturity evaluation method of this embodiment.
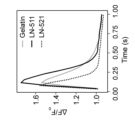
ここで、本実施形態の成熟心筋細胞製造方法にて製造された成熟心筋細胞は、生体内に存在する成人の心筋細胞と機能的及び形態的に近似した心筋細胞となる。すなわち、本実施形態の成熟心筋細胞は、細胞内カルシウムのトランジェント現象及びサルコメア短縮が観察され、ミトコンドリア活性が高くなる。さらに、イオンチャネル機能が発達し、例えば、静止膜電位、ピーク電圧、振幅等も、より生体内の成人の心筋細胞に類似した細胞となる。さらに、下記で説明するように、本実施形態の心筋細胞の成熟度評価方法で評価した場合、本実施形態のマウスの成熟心筋細胞は、高スコアになる。このため、従来の分化誘導方法において分化誘導した心筋細胞と、製造物として区別することが可能である。 Here, the mature cardiomyocytes produced by the mature cardiomyocyte production method of this embodiment are cardiomyocytes that are functionally and morphologically similar to adult cardiomyocytes present in the living body. That is, in the mature cardiomyocytes of this embodiment, intracellular calcium transients and sarcomere shortening are observed, and mitochondrial activity is high. Furthermore, the ion channel function is developed, and, for example, the resting membrane potential, peak voltage, amplitude, etc. become more similar to adult cardiomyocytes in the living body. Furthermore, as described below, when evaluated by the cardiomyocyte maturity evaluation method of this embodiment, the mouse mature cardiomyocytes of this embodiment have a high score. Therefore, it is possible to distinguish the product from cardiomyocytes induced to differentiate by conventional differentiation induction methods.
本実施形態の成熟心筋細胞は、トランスクリプトームデータのうち、共通の遺伝子についての参照により、他の種の心筋細胞の成熟度を定量的に評価することで、実際の成熟度を評価することも可能である。すなわち、心筋細胞の成熟度評価方法により成熟度を評価して、この結果に対応して、成熟心筋細胞を取得することも可能である。これは、例えば、生体組織やPSC-CMsのコロニーの一部等を取得して、成熟度を評価し、残りの心筋細胞を取得するにして対応可能である。 The actual maturity of the mature cardiomyocytes of this embodiment can be evaluated by quantitatively evaluating the maturity of other types of cardiomyocytes by referring to common genes in the transcriptome data. In other words, it is also possible to evaluate the maturity using a cardiomyocyte maturity evaluation method and obtain mature cardiomyocytes based on this result. This can be done, for example, by obtaining a portion of a living tissue or a colony of PSC-CMs, evaluating the maturity, and obtaining the remaining cardiomyocytes.
ここで、本実施形態の発達段階にある動物の心臓のトランスクリプトームのデータは、例えば、次世代シーケンサーによる大規模RNAシークエンス(以下、「RNA-seq」という。)、複数の遺伝子を設定した評価パネル(Targeted RNA-seq、又はqPCR)、DNAチップ、その他の複数の遺伝子発現を測定したものを解析したデータを用いることが可能である。このデータは、例えば、受精からの日数に対応した胎児又は胎仔~出生後の新生児~成熟の各段階(ステージ)において、各遺伝子の発現量のデータを含んでいる。RNA-seqの場合、発現量は、転写産物の量であるTranscript per million(以下、「TPM」という。)のデータとなる。 Here, in this embodiment, the transcriptome data of the heart of an animal in the developmental stage can be, for example, data obtained by analyzing large-scale RNA sequencing (hereinafter referred to as "RNA-seq") using a next-generation sequencer, an evaluation panel with multiple genes set (Targeted RNA-seq, or qPCR), a DNA chip, or other data obtained by measuring the expression of multiple genes. This data includes, for example, data on the expression level of each gene at each stage (stage) from fetus or embryo corresponding to the number of days since fertilization to newborn baby after birth to maturity. In the case of RNA-seq, the expression level is data on transcripts per million (hereinafter referred to as "TPM"), which is the amount of transcription product.
本実施形態においては、例えば、後述する実施例で示すように、発達の各段階にあるマウスの心臓のRNA-seqによるトランスクリプトームデータのうち、マウスとヒトで共通の遺伝子を参照として、ヒトのiPS細胞から分化誘導されたPSC-CMsのRNA-seqの結果データ120から、成熟度を評価することが可能である。すなわち、特にヒトPSC-CMsについて、どの程度成熟しているかを定量的に評価することが可能である。 In this embodiment, for example, as shown in the examples described below, it is possible to evaluate the maturity from the RNA-seq result data 120 of PSC-CMs differentiated from human iPS cells by using genes common to mice and humans as references from transcriptome data obtained by RNA-seq of mouse hearts at each stage of development. In other words, it is possible to quantitatively evaluate the degree of maturity of human PSC-CMs in particular.
本実施形態の成熟心筋細胞製造方法にて製造された成熟心筋細胞は、後述するように、本実施形態の創薬支援方法や治療方法に用いることが可能である。
なお、生物基礎医学分野において、特定の時点において、数万の遺伝子の発現と、生体細胞内において実際に進行している物質的、化学的変化、動作の関係とを完全に知ることは不可能である。よって、本実施形態のように遺伝子の発現レベル(トランスクリプトーム)を用いた成熟度スコア以上に、定量的に心筋細胞の成熟度を測定することは、当業者にとって非常に難しいため、本実施形態の成熟心筋細胞をその構造又は特性により直接特定することは困難であるという特段の事情が存在する。
The mature cardiomyocytes produced by the method for producing mature cardiomyocytes of this embodiment can be used in the drug discovery support method and treatment method of this embodiment, as described below.
In addition, in the field of basic biological medicine, it is impossible to completely know the relationship between the expression of tens of thousands of genes and the material, chemical changes, and operations that are actually proceeding in living cells at a specific time. Therefore, it is very difficult for those skilled in the art to quantitatively measure the maturity of cardiomyocytes beyond the maturity score using gene expression levels (transcriptome) as in this embodiment, so there is a special circumstance that it is difficult to directly identify the mature cardiomyocytes of this embodiment by their structure or characteristics.
〔心筋細胞成熟キット〕
本実施形態の心筋細胞成熟キットは、未成熟の心筋細胞を成熟させるための細胞外マトリックスを含み、細胞外マトリックスは、ラミニン断片を含むことを特徴とする。
本実施形態の心筋細胞成熟キットは、本実施形態の成熟心臓細胞の製造方法に必要な各種試薬を含む。これらの試薬には、例えば、培養用の培地、細胞外マトリックス、培地、FACS用の試薬、抗体、容器等を含む。この細胞外マトリックスは、例えば、ラミニン511 E8断片及び/又はラミニン521 E8断片のペプチドを含んでいてもよい。さらに、細胞外マトリックスは、発現ベクター等として、心筋細胞自体やフィーダー細胞等で発現されるように提供されてもよい。加えて、上述のレポーター細胞自体、更に、各種ホルモンやアゴニスト、転写因子を含む心筋細胞成熟剤、その他が含まれる特別の培地や薬剤についても、本実施形態の心筋細胞成熟キットに加えられていてもよい。さらに、レポーター細胞を保存したり維持したりするための特別の培地、分化誘導や成熟に必要な薬剤等も含んでいてもよい。
[Cardiomyocyte Maturation Kit]
The cardiomyocyte maturation kit of this embodiment includes an extracellular matrix for maturing immature cardiomyocytes, and the extracellular matrix is characterized by including laminin fragments.
The cardiomyocyte maturation kit of this embodiment includes various reagents necessary for the method for producing mature cardiac cells of this embodiment. These reagents include, for example, a culture medium, an extracellular matrix, a medium, a reagent for FACS, an antibody, a container, and the like. The extracellular matrix may include, for example, a peptide of
〔創薬支援方法〕
本実施形態の創薬支援方法は、上述の成熟心筋細胞製造方法により成熟させた成熟心筋細胞を培養し、培養された成熟心筋細胞に対して、創薬のための毒性及び/又は疾患に関する薬物を投与し、成熟心筋細胞の状態を評価することを特徴とする。
[Drug discovery support method]
The drug discovery support method of this embodiment is characterized in that mature cardiomyocytes matured by the above-mentioned mature cardiomyocyte manufacturing method are cultured, a toxic and/or disease-related drug for drug discovery is administered to the cultured mature cardiomyocytes, and the state of the mature cardiomyocytes is evaluated.
本実施形態の創薬のための毒性及び/又は疾患に関する薬物としては、心毒性を調べる必要のある薬剤スクリーニングの候補薬物、心疾患を治療するための候補薬物等を用いることが可能である。本実施形態の候補薬物は、例えば、低分子化合物、ペプチド、タンパク質、細胞の抽出物や上清や発酵産物、その他の合成化合物や天然化合物等が挙げられる。これらの候補薬物は、純度や精製度等が任意であってもよい。また、本実施形態の薬剤スクリーニングが対象とする疾患は、心疾患以外の任意の疾患を含む。 Drugs related to toxicity and/or disease for drug discovery in this embodiment can be candidate drugs for drug screening that require investigation of cardiotoxicity, candidate drugs for treating heart disease, etc. Candidate drugs in this embodiment can be, for example, low molecular weight compounds, peptides, proteins, cell extracts, supernatants, fermentation products, other synthetic compounds, natural compounds, etc. These candidate drugs may have any purity or degree of purification. In addition, diseases targeted by drug screening in this embodiment include any disease other than heart disease.
本実施形態の心毒性としては、患者に重篤な不整脈を引き起こす疾患である、薬物誘発性(後天性)QT延長症候群を、下記で説明する生理学的特性の解析により評価してもよい。薬物誘発性QT延長症候群は、薬物の投与後に心電図上のQT間隔の延長が起こり、TdP(Torsades de pointes、トルサード・ド・ポアンツ、非持続性多形性心室頻拍)から、しばしば心室細動が起こり、失神や突然死をきたす、重篤な疾患である。 As the cardiotoxicity of this embodiment, drug-induced (acquired) long QT syndrome, which is a disease that causes serious arrhythmia in patients, may be evaluated by analyzing physiological characteristics described below. Drug-induced long QT syndrome is a serious disease in which the QT interval on the electrocardiogram is prolonged after administration of a drug, and TdP (torsades de pointes, nonsustained polymorphic ventricular tachycardia) often leads to ventricular fibrillation, resulting in fainting or sudden death.
本実施形態の成熟心筋細胞の状態の評価としては、生理学的特性の解析、毒性マーカー遺伝子の発現解析等を行うことで評価が可能である。このうち、生理学的特性の解析は、例えば、得られたPSC-CMsを1個の細胞又は細胞塊として、電気生理学的特性をパッチクランプ試験、又はフィールドポテンシャル(細胞外活動電位)等を測定して解析することが可能である。この細胞外活動電位は、例えば、多数の電極を有するディッシュ上に、サンプルを載せて測定する。細胞外活動電位の測定により、QTインターバル、拍動(BPM)解析、Naピーク解析等を行うことが可能である。QTインターバルは、心室筋の収縮から拡張期に入るまでの時間であり、Naチャネルによる脱分極からKチャネルによる再分極が起こり、静止膜電位となるまでの時間をいう。このQTインターバルが長くなるQT延長が認められる場合、Kチャンネルの阻害による薬物誘導性の不整脈の原因となり得るので、スクリーニングにて不適なものとして候補薬物から除くような評価をすることが可能である。 The state of the mature cardiomyocytes of this embodiment can be evaluated by performing an analysis of physiological characteristics, an analysis of the expression of toxic marker genes, and the like. Among these, the analysis of physiological characteristics can be performed, for example, by treating the obtained PSC-CMs as a single cell or cell mass, and analyzing the electrophysiological characteristics by a patch clamp test, or measuring the field potential (extracellular action potential), etc. This extracellular action potential can be measured, for example, by placing a sample on a dish having a large number of electrodes. By measuring the extracellular action potential, it is possible to perform QT interval, beat (BPM) analysis, Na peak analysis, and the like. The QT interval is the time from the contraction of the ventricular muscle to the beginning of the diastole, and refers to the time from depolarization by the Na channel to repolarization by the K channel to the resting membrane potential. If QT prolongation, which is a lengthening of this QT interval, is observed, it may cause drug-induced arrhythmia due to inhibition of the K channel, so it is possible to perform an evaluation such that it is excluded from candidate drugs as being unsuitable in screening.
この他にも、各種、毒性マーカー遺伝子の発現解析を行うことで、心毒性の評価が可能である。さらに、臨床試験のプロトコルに合わせたり、当業者に任意の方法を用いたりして、スクリーニングを行ってもよい。
これらの解析において、候補薬物を投与した成熟心筋細胞において、正常な機能が維持された場合に、当該候補薬物が心毒性の少ないものと推定可能である。
In addition, cardiotoxicity can be evaluated by analyzing the expression of various toxicity marker genes. Furthermore, screening may be performed according to a clinical trial protocol or by any method known to those skilled in the art.
In these analyses, if normal function is maintained in mature cardiomyocytes to which a candidate drug has been administered, it can be assumed that the candidate drug has little cardiotoxicity.
〔心疾患の治療方法〕
本実施形態の心疾患の治療方法は、本実施形態の成熟心筋細胞製造方法により製造された成熟心筋細胞を培養し、培養された前記成熟心筋細胞を移植することを特徴とする。
[Method of treating heart disease]
The method for treating a heart disease of this embodiment is characterized by culturing mature cardiomyocytes produced by the method for producing mature cardiomyocytes of this embodiment, and transplanting the cultured mature cardiomyocytes.
具体的には、本実施形態の治療方法においては、心臓の再生医療として、ヒトを含む動物の心臓疾患(心臓病、心疾患)を治療するために、本実施形態の成熟心筋細胞を用いることが可能である。この心疾患としては、心筋梗塞、虚血性心疾患、心筋炎、その他の心不全等が挙げられる。
たとえば、本実施形態の成熟心筋細胞は、当該患者から取得して作成又は生成された多能性幹細胞、又は、HLA等の型が近い多能性幹細胞のライブラリーから取得され、分化誘導され、その後、心筋細胞成熟剤を加えて特定期間培養されて成熟させる。そして、成熟させた成熟心筋細胞は、分離された細胞又は細胞塊の状態で心疾患等の患者の疾病の心臓に注入、心筋シートや心筋組織や心臓臓器(以下、「心筋シート等」という。)を形成しての移植等の治療に用いることができる。この心筋シート等は、当業者に用いられる培養器材を用いて単層又は多層のシートを作成し、心疾患患者の心臓に移植してもよい。さらに、本実施形態の成熟心筋細胞を、サルコメア構造をもつ心臓の筋繊維や組織の状態にして、心疾患患者の心臓に移植してもよい。さらに、適切な担体を用いて培養したり、3Dプリンター等を用いて積層したりして、より組織化された培養物を心疾患患者の心臓に移植することも可能である。これらの担体や培養基材、及び/又は培地に、本実施形態の細胞外マトリックスを含ませることが可能である。
なお、本実施形態の成熟心筋細胞は、再生医療以外の治療用途、例えば、バイオリアクター、人工臓器の製造、クローン個体の作成等、各種用途に使用可能である。
また、本発明を日本で実施する場合、培養物の提供より後の治療は医師により行われるため、本発明の治療方法の「動物」は、ヒト(Homo sapiens)を含まないものとする。一方、それ以外の国においては、「動物」「治療法」の定義は、限定されない。
Specifically, in the treatment method of the present embodiment, the mature cardiomyocytes of the present embodiment can be used as cardiac regenerative medicine to treat cardiac diseases (heart disease, heart disease) in animals, including humans, including myocardial infarction, ischemic heart disease, myocarditis, and other heart failures.
For example, the mature cardiomyocytes of this embodiment are obtained from a library of pluripotent stem cells obtained and created or generated from the patient, or pluripotent stem cells with similar types such as HLA, induced to differentiate, and then cultured for a specific period of time with the addition of a cardiomyocyte maturation agent to mature. The matured cardiomyocytes can be injected into the heart of a patient suffering from a disease such as heart disease in the form of isolated cells or cell masses, and can be used for treatment such as transplantation by forming a myocardial sheet, myocardial tissue, or cardiac organ (hereinafter referred to as "myocardial sheet, etc."). This myocardial sheet, etc. may be prepared as a single-layer or multi-layer sheet using culture equipment used by those skilled in the art and transplanted into the heart of a patient with heart disease. Furthermore, the mature cardiomyocytes of this embodiment may be transplanted into the heart of a patient with heart disease in the state of cardiac muscle fibers or tissues having a sarcomere structure. Furthermore, it is also possible to culture the cells using an appropriate carrier or layer them using a 3D printer or the like to transplant a more organized culture into the heart of a patient with heart disease. The extracellular matrix of this embodiment can be included in these carriers, culture substrates, and/or culture media.
The mature cardiomyocytes of this embodiment can be used for various purposes other than regenerative medicine, such as the manufacture of bioreactors and artificial organs, and the creation of cloned individuals.
Furthermore, when the present invention is practiced in Japan, since treatment after provision of the culture is performed by a doctor, the "animal" in the treatment method of the present invention does not include humans (Homo sapiens). On the other hand, in other countries, the definitions of "animal" and "treatment method" are not limited.
本発明の実施の形態に係る成熟心筋細胞を上述の治療に用いる際に、投与(導入)間隔及び投与量は、疾患の状況、さらに対象の状態等の種々の条件に応じて適宜選択及び変更することが可能である。
本発明の実施の形態に係る成熟心筋細胞の1回の投与量及び投与回数は、投与の目的により、更に、患者の年齢及び体重、症状及び疾患の重篤度等の種々の条件に応じて適宜選択及び変更することが可能である。
投与回数及び期間は、1回のみでもよいし、1日1回~数回、数週間程度投与し、疾患の状態をモニターし、その状態により再度又は繰り返し投与を行ってもよい。
When using mature cardiomyocytes according to an embodiment of the present invention for the above-mentioned treatment, the administration (introduction) interval and dosage can be appropriately selected and changed depending on various conditions such as the state of the disease and the condition of the subject.
The single dose and frequency of administration of mature cardiomyocytes according to an embodiment of the present invention can be appropriately selected and changed depending on the purpose of administration, as well as various conditions such as the patient's age and weight, symptoms, and severity of the disease.
The number of administrations and the duration of administration may be just once, or administration may be once to several times a day for several weeks, and the condition of the disease may be monitored, and administration may be repeated or repeated depending on the condition.
加えて、本発明の成熟心筋細胞は、本実施形態の細胞外マトリックスに加えて、他の組成物や薬剤等と併用することも可能である。また、他の組成物と同時に本発明の組成物を投与してもよく、また間隔を空けて投与してもよいが、その投与順序は特に問わない。
また、本発明の実施の形態において、疾患が改善または軽減される期間は特に限定されないが、一時的な改善または軽減であってもよいし、一定期間の改善または軽減であってもよい。
Additionally, the mature cardiomyocytes of the present invention can be used in combination with other compositions, drugs, etc. in addition to the extracellular matrix of this embodiment. The composition of the present invention may be administered simultaneously with the other compositions, or may be administered at intervals, with no particular restriction on the order of administration.
In addition, in an embodiment of the present invention, the period during which the disease is improved or alleviated is not particularly limited, but may be temporary improvement or alleviation, or improvement or alleviation for a certain period of time.
さらに、本実施形態の細胞外マトリックスを、そのまま心筋細胞成熟用医薬として用いることも可能である。この医薬としては、例えば、未成熟の心筋細胞が存在することが原因となっている疾病、心筋シート等を移植された際の最終的な成熟等に用いることが可能である。具体的には、ゲル状物質等の各種担体に本実施形態の細胞外マトリックスを含ませたものを移植時に付加することが可能である。 Furthermore, the extracellular matrix of this embodiment can be used as it is as a medicine for cardiomyocyte maturation. This medicine can be used, for example, for diseases caused by the presence of immature cardiomyocytes, for final maturation when a myocardial sheet or the like is transplanted, etc. Specifically, it is possible to add the extracellular matrix of this embodiment to various carriers such as gel-like substances at the time of transplantation.
また、本発明の実施の形態に係る心筋細胞成熟用医薬は、任意の製剤上許容しうる担体を含んでいてもよい。この担体は、例えば、リポソーム担体、コロイド金粒子、ポリペプチド、リポ多糖類、多糖類、脂質膜等であってもよい。これらの中で、機能活性調整剤の発現調整効果を向上させる担体を用いることが好適である。 The pharmaceutical for cardiomyocyte maturation according to the embodiment of the present invention may also contain any pharma- ceutical acceptable carrier. This carrier may be, for example, a liposome carrier, colloidal gold particles, a polypeptide, a lipopolysaccharide, a polysaccharide, a lipid membrane, etc. Among these, it is preferable to use a carrier that improves the expression regulating effect of the functional activity regulator.
さらに、製薬上許容される担体としては、例えば生理食塩水、ブドウ糖やその他の補助薬を含む等張液、例えばD-ソルビトール、D-マンノース、D-マンニトール、塩化ナトリウム等を含んでいてもよい。さらに、適当な溶解補助剤、例えばアルコール、具体的にはエタノール、ポリアルコール、例えばプロピレングリコール、ポリエチレングリコール、非イオン性界面活性剤、例えばポリソルベート80(TM)、HCO-50等と共に投与することが可能である。また、適切な賦形剤等を更に含んでもよい。 Furthermore, the pharma- ceutically acceptable carrier may include, for example, physiological saline, an isotonic solution containing glucose or other auxiliary drugs, such as D-sorbitol, D-mannose, D-mannitol, sodium chloride, etc. Furthermore, it is possible to administer the drug together with a suitable solubilizing agent, such as alcohol, specifically ethanol, polyalcohol, such as propylene glycol, polyethylene glycol, non-ionic surfactant, such as polysorbate 80(TM), HCO-50, etc. Furthermore, it may further include a suitable excipient, etc.
また、本実施形態の心筋細胞成熟用医薬は、製剤上許容しうる担体を調製するために、適切な薬学的に許容可能なキャリアを含んでいてもよい。このキャリアは、シリコーン、コラーゲン、ゼラチン等の生体親和性材料を含んでもよい。また、キャリアは、乳濁液として提供されてもよい。さらには、例えば、希釈剤、香料、防腐剤、賦形剤、崩壊剤、滑沢剤、結合剤、乳化剤、可塑剤等の製剤用添加物のいずれか又は任意の組み合わせを含有させてもよい。 The pharmaceutical for cardiomyocyte maturation of this embodiment may also contain a suitable pharma- ceutical acceptable carrier to prepare a pharma-ceutical acceptable carrier. The carrier may contain a biocompatible material such as silicone, collagen, gelatin, etc. The carrier may also be provided as an emulsion. Furthermore, it may contain any one or any combination of formulation additives such as diluents, flavorings, preservatives, excipients, disintegrants, lubricants, binders, emulsifiers, plasticizers, etc.
本実施形態の心筋細胞成熟用の投与経路は、特に限定されず、非経口的又は経口的に投与を行うことが可能である。非経口投与としては、例えば、静脈内、動脈内、皮下、真皮内、筋肉内、腹腔内の投与、又は、腎臓等への直接投与が可能である。
本発明の実施の形態に係る心筋細胞成熟用医薬は、非経口的又は経口的の投与に適した投与形態において、当該分野で周知の製剤上許容しうる担体を用いて処方され得る。
The administration route for cardiomyocyte maturation in this embodiment is not particularly limited, and administration can be parenteral or oral. Parenteral administration can be, for example, intravenous, intraarterial, subcutaneous, intradermal, intramuscular, or intraperitoneal administration, or direct administration to the kidney or the like.
The pharmaceutical agent for cardiomyocyte maturation according to an embodiment of the present invention can be formulated using pharma- ceutically acceptable carriers well known in the art in an administration form suitable for parenteral or oral administration.
以上のように構成することで、以下のような効果を得ることができる。
従来、患者から得られた初代培養の心筋細胞は、ディッシュで維持することが困難であった。このため、多能性幹細胞に成長因子又は小分子を順次添加することにより、心臓分化誘導させるプロトコルが開発された。これにより生成された多能性幹細胞由来の心筋細胞(PSC-CMs)は、疾患モデリング及び薬物スクリーニングのために用いられることが期待されている。
With the above configuration, the following effects can be obtained.
Traditionally, primary cultures of cardiomyocytes obtained from patients have been difficult to maintain in a dish. For this reason, a protocol has been developed to induce cardiac differentiation of pluripotent stem cells by sequentially adding growth factors or small molecules. The pluripotent stem cell-derived cardiomyocytes (PSC-CMs) generated in this way are expected to be used for disease modeling and drug screening.
ここで、従来のPSC-CMsは、その構造と機能に関して、胎児又は新生児の心筋細胞に近い未成熟の状態であり、典型的なin vivoの出生後の成熟した心筋細胞とは異なっていた。そのため、特に成人以降に発症する心筋症等の心疾患の病態の再現や解析、薬剤の毒性評価を行う用途では不十分であった。この制限により、特にin vitroモデル及び創薬のための医療目的でのPSC-CMsの有用性が毀損されていた。したがって、PSC-CMsを、成体の細胞に近いレベルまで成熟させるための方法が求められていた。 Here, conventional PSC-CMs are in an immature state with respect to their structure and function, similar to fetal or neonatal cardiomyocytes, and are different from typical in vivo mature cardiomyocytes after birth. Therefore, they are insufficient for purposes such as reproducing and analyzing the pathology of cardiac diseases such as cardiomyopathy that develop in adulthood, and evaluating the toxicity of drugs. This limitation has diminished the usefulness of PSC-CMs, particularly for in vitro models and medical purposes for drug discovery. Therefore, a method for maturing PSC-CMs to a level close to that of adult cells has been demanded.
これに対して、本実施形態のラミニン断片を用いてPSC-CMsを成熟させることで、従来の手法で得られるよりも明らかに成熟した成熟心筋細胞が得られた。
この本実施形態の成熟心筋細胞を疾患のモデルとなるiPS細胞等に応用することで、これまで病態が再現できなかったものであっても、再現できるようになる可能性がある。具体的には、心筋梗塞等、虚血性心疾患を原因とする特発性心疾患等についても候補薬物を選択可能になる。また、QT延長について、子供では症状がないものの大人では症状が出るといった状態に対応して、候補薬物をふるい分けることが可能となる。このため、心筋症治療に向けた再生医療への応用に資することができる。
In contrast, by maturing PSC-CMs using the laminin fragment of this embodiment, mature cardiomyocytes that were clearly more mature than those obtained by conventional techniques were obtained.
By applying the mature cardiomyocytes of this embodiment to iPS cells as a disease model, it may be possible to reproduce pathological conditions that could not be reproduced until now. Specifically, it becomes possible to select candidate drugs for idiopathic heart disease caused by ischemic heart disease such as myocardial infarction. In addition, it becomes possible to screen candidate drugs in response to a condition in which QT prolongation is asymptomatic in children but symptomatic in adults. This can contribute to the application of regenerative medicine to the treatment of cardiomyopathy.
一方、従来、特許文献1の段落[0057]に記載されているように、全長のラミニン511及びラミニン521は、多能性幹細胞が接着可能な足場となり得るため、自発的な分化や遺伝的変化のリスクなしに、長期的に維持するのに用いられていた。一方、ラミニン211及びラミニン221は、心筋及び骨格筋線維(細胞)に非常に特異的であり、特許文献1の段落[0060]に記載されているように、このラミニン221を含む基材で培養することで、多能性幹細胞をPSC-CMsに分化させていた。
すなわち、従来、ラミニン511及びラミニン521が多能性幹細胞から心筋細胞への成熟に有効であるという知見は存在しなかった。
これに対して、本実施形態のラミニン511 E8断片及び/又はラミニン521 E8断片は、従来の常識と異なり、それだけで未成熟の心筋細胞を成熟させ、成熟心筋細胞を作製させることが可能な細胞外マトリックスとなる。
Meanwhile, as described in paragraph [0057] of
That is, there has been no prior knowledge that laminin-511 and laminin-521 are effective in maturing pluripotent stem cells into cardiomyocytes.
In contrast, the
さらに、本実施形態では、成熟に伴い発現が増加する成熟心筋細胞マーカーの遺伝子座に、レポーター遺伝子として蛍光タンパク質の遺伝子をノックインした多能性幹細胞であるレポーター細胞を用いた。そして、成熟心筋細胞(群)から、レポーター細胞におけるレポーター、又は、Cd36の表面抗原を指標として、FACS等で分離することにより、高純度な成熟心筋細胞を得ることができる。
本実施形態のレポーター細胞から作成した成熟心筋細胞は、病態モデルの作成が可能となり、心筋症の治療に向けた再生医療への応用に近づく可能性がある。たとえば、大人になって発症する心筋症の治療法開発に役立つ可能性がある。
Furthermore, in this embodiment, reporter cells, which are pluripotent stem cells in which a fluorescent protein gene is knocked in as a reporter gene at the gene locus of a mature cardiomyocyte marker whose expression increases with maturation, are used. Then, by separating the mature cardiomyocyte (group) by FACS or the like using the reporter in the reporter cells or the Cd36 surface antigen as an indicator, highly pure mature cardiomyocytes can be obtained.
The mature cardiomyocytes produced from the reporter cells of this embodiment will enable the creation of pathological models, and may be useful for the application of regenerative medicine to the treatment of cardiomyopathy. For example, this may be useful for the development of a treatment for cardiomyopathy that develops in adults.
より具体的には、本実施形態においては、実施例に示すように、Myom2遺伝子座にRFPをノックインした多能性幹細胞株をラミニン511 E8断片及び/又はラミニン 521 E8断片を用いて処理し、RFP強度を測定することで、成熟心筋細胞を取得した。Myom2はニワトリ、マウス、ヒトの間で、強く保存されていることが知られている。このため、心筋細胞の成熟のレポーター細胞として、病態解析等に、より適切に使用可能となる。
More specifically, in this embodiment, as shown in the examples, a pluripotent stem cell line in which RFP was knocked into the Myom2 locus was treated with
なお、本発明者らは、Myom2以外にも、Ckmt2、Hspb8、Tcapについてノックイン細胞を作成済みであり、予備実験にて同様の結果を示した。これらでは、キメラマウスの作成も可能であり、胎仔~成熟したマウスの心臓を取得して、成熟した細胞を取得することが可能である。また、それ以外の成熟心筋細胞マーカーの遺伝子についても、各遺伝子座にノックインを行うと同様の結果を示すものと考えられる。 In addition to Myom2, the inventors have already created knock-in cells for Ckmt2, Hspb8, and Tcap, and have shown similar results in preliminary experiments. These also make it possible to create chimeric mice, and obtain the hearts of fetal and mature mice to obtain mature cells. It is also believed that similar results will be seen when other genes for mature cardiomyocyte markers are knocked in at each gene locus.
また、上述の実施形態においては、セルソーティングにFACSを用いる例について記載したものの、FACS以外のセルソーティングも使用可能である。 In addition, although the above embodiment describes an example in which FACS is used for cell sorting, cell sorting other than FACS can also be used.
以下で、本発明の実施の形態に係る細胞外マトリックス、成熟心筋細胞製造方法、創薬支援方法、心疾患の治療方法、成熟心筋細胞、及び心筋細胞成熟キットについて、具体的な実験を基にして、実施例としてさらに具体的に説明する。しかしながら、この実施例は一例にすぎず、これに限定されるものではない。 The extracellular matrix, the method for producing mature cardiomyocytes, the drug discovery support method, the method for treating heart disease, the mature cardiomyocytes, and the cardiomyocyte maturation kit according to the embodiments of the present invention will be described in more detail below as examples based on specific experiments. However, this example is merely an example and is not intended to be limiting.
〔材料と方法〕
(ノックインES細胞株(レポーター細胞)の樹立)
心筋細胞の成熟度レポーター細胞は、マウスES細胞であるsyNP4細胞に対し、ゲノム編集を行うことで樹立した。Myom2は骨格筋細胞でも発現しているため、sodium-calcium exchanger 1 promoterによって駆動されるピューロマイシン耐性カセットを含んでいるsyNP4株の細胞を用いることで、in vitroで心筋細胞を、確実に純化することが可能となる。また、ゲノム編集はCRISPR/Cas9によりゲノムを切断し、ノックインベクターを目的部位に挿入することで行った。Cas9タンパク及びsingle guide RNAを一つのベクターから発現するpx330のguide RNA cloning位置に、Myom2のストップコドン直上となるguide RNAを設計し、挿入したpx330-Myom2を作成した。ノックインベクターはgRNA標的部位より約1000bpのホモロジーアームを持ち、Myom2遺伝子と同一フレームでTagRFPが挿入されている。また、TagRFPより下流にFRT-Blastcidin耐性遺伝子-FRTというカセットを持つ(Myom2-TagRFP-Blast)。Px330-Myom2、及びMyom2-TagRFP-BlastをSynp4にリポフェクションで導入し、blastcitidin処置を行うことで、ノックイン細胞を得た。ノックイン細胞はクロナール密度から培養することで、単一細胞由来のコロニーを得た。それぞれのコロニーについて、ノックインが正しく行われていることをPCR及びシーケンスで確認し、心筋細胞分化能が維持されていることを合わせて確認した。このようにして得られたMyom2-RFPノックインマウスES細胞を、SMM18と名付けた。さらに、pCAG-Flpe-IRES-puroプラスミドをリポフェクションにより導入し、短期間のpuromycynセレクションを行うことで、FRT-Blast-FRTカセットを喪失した、別のMyom2-RFP株を樹立し、SMM-B2と名付けた。カセットの喪失は薬剤の感受性試験及びPCRにより確認した。本研究では、SMM18又はSMM-B2(以下、これらを単に「Myom2-RFP株」という。)を用いて実験を行った。
Materials and Methods
(Establishment of knock-in ES cell line (reporter cell))
Cardiomyocyte maturity reporter cells were established by performing genome editing on mouse ES cells, syNP4 cells. Since Myom2 is also expressed in skeletal muscle cells, it is possible to reliably purify cardiomyocytes in vitro by using cells of the syNP4 strain containing a puromycin resistance cassette driven by the sodium-
(マウスES細胞の培養と分化誘導、ECMでの成熟処理)
Ncxプロモーター下にPuromycin耐性遺伝子を発現するトランスジェニックマウスES細胞(syNP4)を、LIF、CHIR00021、PD0325901、及び血清存在下で未分化維持培養を行い、週3回継代を行った。
分化誘導は、血清の代わりにB27サプリメント(Vitamin A不含),N2サプリメント存在下で浮遊培養にて胚様体を形成させた。分化2日目からはActivin A,BMP4,VEGFを加え、分化を継続した。分化4日目に胚様体をTrypleにより単離し、高密度平面培養(250k cells/cm2程度)をbFGF,FGF10,VEGF存在下で行った。分化7日目頃より拍動する心筋細胞が観察される。Puromycinを加えることにより、心筋細胞へと分化しなかった細胞を死滅させ、純度の高い心筋細胞を得た。また、この手法は以下で記載するノックイン細胞でも同様であった。
分化10日目にはTrypleを用いて細胞を単離し、50k/cm2で播種し直した。播種する際には培養プレートを0.1%ゼラチンでコートしたものを用い、上記分化培地に10%の血清を加えた(分化11日目まで)。ウイルス感染は分化11日目~12日目にかけて行った。分化12日目~14日目はPuromycinによる心筋細胞の純化を継続した。アゴニスト等を加えるアゴニスト処理については、分化11日目~14日目までPuromycin処理を行った後、分化14日目から最大4週間アゴニスト等を添加する処理を行った。
ECMを加えて培養するECMでの成熟処理は、濃度0.125、0.5、1μg/cm2、培養期間は1、2、4週で、それぞれ行った。
(Culture of mouse ES cells, differentiation induction, and maturation treatment with ECM)
Transgenic mouse ES cells (syNP4) expressing a Puromycin resistance gene under the control of an Ncx promoter were cultured in the presence of LIF, CHIR00021, PD0325901, and serum to maintain the undifferentiated state, and were passaged three times a week.
For differentiation induction, embryoid bodies were formed in suspension culture in the presence of B27 supplement (without Vitamin A) and N2 supplement instead of serum. From the second day of differentiation, Activin A, BMP4, and VEGF were added to continue differentiation. On the fourth day of differentiation, embryoid bodies were isolated by Tryple, and high-density flat culture (about 250k cells/ cm2 ) was performed in the presence of bFGF, FGF10, and VEGF. From about the seventh day of differentiation, pulsating cardiomyocytes were observed. By adding Puromycin, cells that did not differentiate into cardiomyocytes were killed, and highly pure cardiomyocytes were obtained. This method was also similar to the knock-in cells described below.
On the 10th day of differentiation, cells were isolated using Tryple and reseeded at 50k/ cm2 . When seeding, a culture plate coated with 0.1% gelatin was used, and 10% serum was added to the above differentiation medium (until the 11th day of differentiation). Viral infection was performed from the 11th day to the 12th day of differentiation. Purification of cardiomyocytes with Puromycin was continued from the 12th day to the 14th day of differentiation. For agonist treatment, Puromycin treatment was performed from the 11th day to the 14th day of differentiation, and then agonist treatment was performed from the 14th day of differentiation for up to 4 weeks.
Maturation treatment with ECM, in which culture was performed with ECM, was performed at concentrations of 0.125, 0.5, and 1 μg/cm 2 for culture periods of 1, 2, and 4 weeks, respectively.
(RNAサンプルの調製とRNA-sequence(RNA-seq))
マウスの心臓を胎生11日~生後10ヶ月から摘出し、心房及び心室に分離、TRIzolを用いて溶解した。また、PSC-CMsは、分化10日目のものを0.1% Gelatin上に播種し、分化14日目からアゴニスト処理を行い、2週後にTRIzolにて溶解した。RNAの抽出は、マウス心臓についてはフェノールクロロホルム抽出、又はDirect-zol RNA kit(ザイモリサーチ社製)、PSC-CMsについてはDirect-zol RNA kitにより抽出した。RNAは、Nanodrop(サーモフィッシャーサイエンティフィック社製)又はQubit Fluorometer(Invitrogen社製)を用いて定量した。また、Bioanalyzerを用いて、RNAが分解されていないことを確認した。それぞれ500ngのRNAを100ng/uLに調製し、QUANT-seq 3’mRNA-Seq Library Prep Kit(Lexogen社製)を用いて、RNA-seq用のライブラリーを作成した。得られたライブラリーサイズはBioanalyzer(アジレント・テクノロジー株式会社製)を用いて確認し、その濃度はBioanalyzerの結果ないしQubit Fluorometerを用いて定量した。それぞれのサンプルについて同量ずつになるよう混合し、Next-seq high output 75SE(イルミナ株式会社製)を用いて、超並列シーケンスを行った。なお、心臓サンプルは48サンプルずつ、PSC-CMsは96サンプルずつ混合した。追加で行った心臓サンプルは、生後10日目、30週、10ヶ月のものを、96サンプルずつシーケンスした。
(RNA sample preparation and RNA-sequence (RNA-seq))
Mouse hearts were removed from embryonic day 11 to 10 months of age, separated into atria and ventricles, and dissolved using TRIzol. PSC-CMs were seeded on 0.1% gelatin on the 10th day of differentiation, agonist treatment was performed from the 14th day of differentiation, and dissolved in TRIzol two weeks later. RNA was extracted from mouse hearts by phenol-chloroform extraction or Direct-zol RNA kit (Zymo Research), and from PSC-CMs by Direct-zol RNA kit. RNA was quantified using Nanodrop (Thermo Fisher Scientific) or Qubit Fluorometer (Invitrogen). It was also confirmed that RNA was not decomposed using a Bioanalyzer. 500ng of RNA was prepared at 100ng/uL, and a library for RNA-seq was created using QUANT-seq 3'mRNA-Seq Library Prep Kit (Lexogen). The resulting library size was confirmed using Bioanalyzer (Agilent Technologies), and the concentration was quantified using Bioanalyzer results or Qubit Fluorometer. The samples were mixed in equal amounts, and massively parallel sequencing was performed using Next-seq high output 75SE (Illumina). 48 samples of heart samples and 96 samples of PSC-CMs were mixed. Additional heart samples were sequenced at 10 days, 30 weeks, and 10 months of age, with 96 samples each.
RNA-seqで得られたサンプルごとのFastqファイルは、BBtoolsのBBDukを用いてpoly A配列及びシーケンス末端の配列、アダプター配列、シーケンスクオリティの低い配列などをトリミングした。続いて、STAR RNA-seq alignerを用いて、マウスゲノム(GRC mm10)へとマッピングを行った。最後にSubread packageに含まれるfeature Countsを用いてそれぞれの遺伝子ごとのカウントデータを得た。カウントデータは更に、独自に開発した心筋細胞成熟度評価プログラムと、統計解析用のプログラム「R」とを用いて解析を行った。まず、100万カウント以下のサンプルを除外し、遺伝子ごとのカウントを総カウント数で除した、Transcript per million(TPM)を各サンプル、各遺伝子について算出した。2019年8月末時点で実験済みの全ての実験データ(マウス)を用いて、平均して、1TPM以上ある遺伝子を発現遺伝子と定義し、以下の解析では発現遺伝子のみを用いて解析を行った。 The Fastq files for each sample obtained by RNA-seq were trimmed using BBDuk from BBtools to remove poly A sequences, sequences at the sequence ends, adapter sequences, sequences with low sequence quality, etc. Then, mapping was performed to the mouse genome (GRC mm10) using STAR RNA-seq aligner. Finally, count data for each gene was obtained using feature counts included in the Subread package. The count data was further analyzed using a proprietary cardiomyocyte maturity evaluation program and the statistical analysis program "R". First, samples with counts of 1 million or less were excluded, and the transcript per million (TPM) was calculated for each sample and each gene by dividing the count for each gene by the total count. Using all experimental data (mice) that had been tested as of the end of August 2019, genes with an average of 1 TPM or more were defined as expressed genes, and the following analysis was performed using only expressed genes.
(定量的成熟度評価法(マウス))
マウスの胎仔(E)11~生後(P)56まで、さらに10ヶ月までの各段階(Stages)の心臓サンプルについてRNA-seqを行った結果のデータについて、主成分分析を行い、成熟度スコア(Maturation Score)を算出する基準(以下、「参照」という。)となる各遺伝子の固有ベクトル(係数)を算出した。この際、TPMに1を加えた数字に、10を底とする対数に変換した上で、主成分分析を行った。成熟度スコアは、各遺伝子発現に第一主成分に対応する係数を掛けたものの総和を用い、一定のオフセット値(32)を加え、係数(1.5)を掛けることで得た。この計算により、成熟度スコアは、概ね0~100の幅となった。
(Quantitative maturation assessment method (mouse))
Principal component analysis was performed on the data obtained by performing RNA-seq on mouse heart samples from each stage (Stages) from fetal (E) 11 to postnatal (P) 56 up to 10 months, and the eigenvector (coefficient) of each gene, which serves as the standard (hereinafter referred to as "reference") for calculating the maturation score, was calculated. In this case, the number obtained by adding 1 to TPM was converted to a logarithm with a base of 10, and then principal component analysis was performed. The maturity score was obtained by using the sum of the expression of each gene multiplied by the coefficient corresponding to the first principal component, adding a certain offset value (32), and multiplying by a coefficient (1.5). This calculation resulted in a maturity score ranging from approximately 0 to 100.
(定量的成熟度評価法(ヒト))
biomaRt(RからBioMartを利用するパッケージ)を用いて、ヒトとマウスで対応する遺伝子リストを得た。この際、hsapiens_gene_ensemblと、mmusculus_gene_ensemblの2つのデータセットを用いた。同一遺伝子名を持つものに加えて、orthologueとして単一の遺伝子が登録されている遺伝子を、対応リストとして設定した。
ヒト心筋細胞の定量的成熟度評価は、これらの遺伝子のRNA-seqのデータをマウスのデータへと投写することで行った。ヒト胎児心臓RNAサンプル、ヒト成人心臓RNAサンプル、及び、in houseで分化誘導を行ったヒトPSC-CMsを用いて分化誘導後18日目、32日目、46日目のサンプルについてRNA-seqを行い、マウスのデータへ投写した。また、ヒトPSC-CMsについては、成熟を促進するホルモン処理として、Hydrocortisone(HC)と甲状腺ホルモンT3の処理を行ったものも作成した。
具体的には、対応リストに含まれる遺伝子のみを用いて、上述の各サンプルについてのRNA-seqのデータの主成分分析を行い、成熟度スコアを算出する基準となる各遺伝子の固有ベクトル(係数)を算出した。同様に、概ね0~100の幅となるように、第一主成分得点に対し、オフセット値(30)、係数(1.5)を算出した。
(Quantitative Maturity Assessment Method (Human))
Using biomaRt (a package that uses BioMart from R), we obtained a list of genes that correspond between humans and mice. In this case, two datasets, hsapiens_gene_ensembl and mmusculus_gene_ensembl, were used. In addition to those with the same gene name, genes with a single gene registered as an orthologue were set as the correspondence list.
Quantitative maturity evaluation of human cardiomyocytes was performed by projecting the RNA-seq data of these genes onto mouse data. RNA-seq was performed on samples 18, 32, and 46 days after differentiation induction using human fetal heart RNA samples, human adult heart RNA samples, and human PSC-CMs that had been induced to differentiate in house, and the results were projected onto mouse data. In addition, human PSC-CMs were also treated with Hydrocortisone (HC) and the thyroid hormone T3 as hormone treatments to promote maturation.
Specifically, using only the genes included in the correspondence list, a principal component analysis was performed on the RNA-seq data for each sample described above, and the eigenvector (coefficient) of each gene was calculated as a basis for calculating the maturity score. Similarly, an offset value (30) and a coefficient (1.5) were calculated for the first principal component score so that the range would be approximately 0 to 100.
ヒト胎児心臓RNAサンプル、ヒト成人心臓RNAサンプルを用いてRNA-seqを行い、マウスデータへ投写すると、胎児は胎仔相当に、成人は成体相当の成熟度スコアが得られた。また、ヒトPSC-CMs分化誘導後18日目、32日目、46日目のサンプルは、培養期間に伴い成熟度スコアが増加した。 When RNA-seq was performed using human fetal heart RNA samples and human adult heart RNA samples and projected onto mouse data, the fetuses obtained maturity scores equivalent to fetuses and the adults obtained maturity scores equivalent to adults. Furthermore, the maturity scores of samples taken 18, 32, and 46 days after induction of human PSC-CMs differentiation increased with the culture period.
(免疫染色)
心臓の場合、組織を埋め込み、最適切断温度(OCT)コンパウンドで(Tissue-Tek、Sakura製)直接凍結し、Leica Cryostat(4μm)で切断した。切片は、PBSで洗浄してから4%パラホルムアルデヒド(PFA、Wako製)を用いて4°Cで30分間処理し、固定した。その後、PBSで0.1%トリトンX-100(アマーシャム バイオサイエンス社製)を用いて、室温で15分間、切片を洗浄し、透明化した。透明化後、細胞を3%ウシ血清アルブミンでブロックし、続いて抗Myom2ポリクローナル抗体(LS-B9842、1:100、LifeSpan バイオサイエンス社製)、及び抗α-アクチニンモノクローナル抗体(EA-53、1:100、シグマアルドリッチ社製)を4°Cで一晩、反応させた。次いで、0.2%Tween-20(ナカライテスク社製)を含むPBSで洗浄し、二次抗体、抗ウサギIgG(1:500、サーモフィッシャーサイエンティフィック社製)、及び抗マウスIgG(1:500、サーモフィッシャーサイエンティフィック社製)で染色し、Alexa Fluor Plus 555及び488でそれぞれ重合させた。DAPI(Dojindo Laboratories製)は、核染色に用いた。スライドは、VECTASHIELDアンチフェード取り付け媒体(Vector Laboratories製)に取り付けられまた。
(Immunostaining)
For hearts, tissues were embedded and directly frozen in optimal cutting temperature (OCT) compound (Tissue-Tek, Sakura) and cut on a Leica Cryostat (4 μm). Sections were washed with PBS and fixed in 4% paraformaldehyde (PFA, Wako) for 30 min at 4°C. Sections were then washed and cleared in 0.1% Triton X-100 (Amersham Biosciences) in PBS for 15 min at room temperature. After clearing, the cells were blocked with 3% bovine serum albumin, and then reacted with anti-MyoM2 polyclonal antibody (LS-B9842, 1:100, LifeSpan Biosciences) and anti-α-actinin monoclonal antibody (EA-53, 1:100, Sigma-Aldrich) at 4°C overnight. The cells were then washed with PBS containing 0.2% Tween-20 (Nacalai Tesque), and stained with secondary antibodies, anti-rabbit IgG (1:500, Thermo Fisher Scientific), and anti-mouse IgG (1:500, Thermo Fisher Scientific), and polymerized with Alexa Fluor Plus 555 and 488, respectively. DAPI (Dojindo Laboratories) was used for nuclear staining. Slides were mounted in VECTASHIELD antifade mounting medium (Vector Laboratories).
PSC-CMsの場合、CellCarrier 96ウェルブラックポリスチレンマイクロプレート(PerkinElmer社製)で培養したPSC-CMを4%パラホルムアルデヒドで一晩固定した。次に、細胞をPBSで洗浄し、0.2%Triton X-10を含むPBS中を使用して、室温で15分間透過処理した。透過処理後、細胞をPBS中の2%FBSでブロックした後、抗α-アクチニン抗体(1:500、Sigma-Aldrich社製)又は抗カーディアックトロポニンT抗体(13-11、1:500、Thermo Fisher Scientific社製)、及び抗tRFP抗体(AAB233、1:500、Evrogen社製)で一晩処理した。細胞を洗浄し、二次抗体、抗マウスIgG(1:500、Thermo Fisher Scientific社製)及び抗ウサギIgG(1:500、Thermo Fisher Scientific社製)で染色し、それぞれAlexa Fluor 488及び555と重合させた。核は、DAPI溶液で染色された。共焦点レーザー走査顕微鏡(オリンパス社製、FluoView FV1200)又は倒立蛍光顕微鏡(オリンパス社製、IX83)により免疫蛍光画像を収集した。サルコメアの長さ、細胞の大きさ、真円度、周囲、及び細胞の形状は、ImageJソフトウェアによって分析された。 For PSC-CMs, PSC-CMs cultured in CellCarrier 96-well black polystyrene microplates (PerkinElmer) were fixed overnight with 4% paraformaldehyde. Cells were then washed with PBS and permeabilized for 15 min at room temperature using 0.2% Triton X-10 in PBS. After permeabilization, cells were blocked with 2% FBS in PBS and then treated overnight with anti-α-actinin antibody (1:500, Sigma-Aldrich) or anti-cardiac troponin T antibody (13-11, 1:500, Thermo Fisher Scientific), and anti-tRFP antibody (AAB233, 1:500, Evrogen). Cells were washed and stained with secondary antibodies, anti-mouse IgG (1:500, Thermo Fisher Scientific) and anti-rabbit IgG (1:500, Thermo Fisher Scientific), polymerized with Alexa Fluor 488 and 555, respectively. Nuclei were stained with DAPI solution. Immunofluorescence images were collected by confocal laser scanning microscope (Olympus, FluoView FV1200) or inverted fluorescence microscope (Olympus, IX83). Sarcomere length, cell size, circularity, circumference, and cell shape were analyzed by ImageJ software.
(カルシウムトランジェントとサルコメア短縮)
細胞内カルシウムトランジェントを測定するために、PSC-CMsを、ガラス底の24ウェルプレート(MatTek Corporation社製)で28日間培養した。次に、細胞をPBSで洗浄し、カルシウム指示薬Calbryte 520-AM(AAT Bioquest社製)を含むタイロード液(140mM NaCl、5.4mM KCl、0.5mM MgCl2、0.33mM NaH2PO4、2 mMCaCl2、5mM HEPES、及び11mM D-グルコース、NaOHでpHを7.4に調整)で30分間、処理された。細胞は、1Hzの電界刺激された(C-Pace、IonOptics社製)。倒立蛍光顕微鏡(オリンパス社製IX83、ORCA-Flash 4.0 V3搭載)により、40倍の対物レンズ、露出10ミリ秒、20ミリ秒の間隔で細胞内カルシウムのトランジェント現象を記録した。ImageJを使用して、細胞内カルシウムトランジェントを定量化した。サルコメア短縮については、生細胞イメージング用のタイムラプス記録で細胞収縮を継続的に記録した。タイムラプス記録は、ImageJに対してSarcOptiMによって分析された。
(Calcium Transients and Sarcomere Shortening)
To measure intracellular calcium transients, PSC-CMs were cultured in glass-bottom 24-well plates (MatTek Corporation) for 28 days. Cells were then washed with PBS and treated with Tyrode's solution (140 mM NaCl, 5.4 mM KCl, 0.5 mM MgCl2, 0.33 mM NaH2PO4 , 2 mM CaCl2, 5 mM HEPES , and 11 mM D-glucose, pH adjusted to 7.4 with NaOH) containing calcium indicator Calbryte 520-AM (AAT Bioquest) for 30 min. Cells were stimulated with a 1 Hz electric field (C-Pace, IonOptics). Intracellular calcium transients were recorded with an inverted fluorescence microscope (Olympus IX83, equipped with ORCA-Flash 4.0 V3) using a 40x objective lens, 10 ms exposure, and 20 ms intervals. Intracellular calcium transients were quantified using ImageJ. For sarcomere shortening, cell contraction was continuously recorded in time-lapse recordings for live cell imaging. Time-lapse recordings were analyzed by SarcOptiM on ImageJ.
(ミトコンドリア活性アッセイ)
ミトコンドリア機能をSeahorse XF96 extracellular flux analyzerで解析した。Seahorse XF96マイクロプレートを、0.1%ゼラチン(コントロール)又は各ECMでコーティングした。分化誘導後、10日目に、PSC-CMsを50000細胞/ウェルの密度で、プレート上に播種した。アッセイを開始する前に、38日目まで細胞を培養した。アッセイを実行する1時間前及び測定中に、培養培地をベース培地(1mM ピルビン酸、2mM グルタミン、25mM グルコースを添加したSeahorse XF RPMI培地)に交換した。選択的阻害剤は、最終濃度3μMのオリゴマイシン(ミトコンドリア電子輸送チェーン[METC]の複合体V[ATPアーゼ]のための阻害剤)、0.5μMのCarbonyl cyanide-p-trifluoromethoxyphenylhydrazone(FCCP、ミトコンドリア酸化リン酸化アンカプラー)、3μMロテノン(METCの複合体Iの阻害剤)、及びアンチマイシンA(METCの複合体IIIの阻害剤)が、測定中に、逐次的に注入された。ミトコンドリア呼吸における主要な指標である基礎呼吸(Basal respiration)は、オリゴマイシンを適用する前に、酸素消費量率(Oxygen Consumption Rate、OCR)で表された。ATP産生関連呼吸(ATP-linked respiration)は、オリゴマイシン感受性呼吸数で表された。プロトンリークは、オリゴマイシンとロテノン/アンチマイシンAの割合との差分によって算出された。最大呼吸(Maximal respiration、最大ミトコンドリア呼吸)はFCCPに対応して算出した。
Mitochondrial Activity Assay
Mitochondrial function was analyzed using a Seahorse XF96 extracellular flux analyzer. Seahorse XF96 microplates were coated with 0.1% gelatin (control) or each ECM. On
(フローサイトメトリー)
Myom2-RFP株から生成されたPSC-CMsを、TrypLE(Thermo Fisher Scientific社製)にて10分、37℃で処理して、単一細胞に解離した。PBSで洗浄した後、細胞を、DAPI(1:2000)を含むPBS中の2%FBSで懸濁した。RFP陽性(以下「RFP+」と称する。)、及びRFP強度の割合の測定と細胞選別は、SH800(SONY社製)を使用して実行された。
(Flow Cytometry)
PSC-CMs generated from the Myom2-RFP line were treated with TrypLE (Thermo Fisher Scientific) for 10 min at 37°C to dissociate into single cells. After washing with PBS, the cells were suspended in 2% FBS in PBS containing DAPI (1:2000). Measurement of the percentage of RFP positive (hereafter referred to as "RFP+") and RFP intensity and cell sorting were performed using SH800 (Sony).
(統計分析)
データは、少なくとも3つの繰り返しサンプルの平均±標準偏差(SD)として表示された。トランスクリプトームデータ等、それ以下のサンプル数の実験については、すべてのデータ点を示した。スチューデントのt検定、デネット(Dunnett)検定、カイ2乗検定、又は一元配置分散分析は、適切な場所で使用された。統計分析はすべて、統計プログラム「R」を使用して行った。0.05未満のp値(p<0.05)は有意と見なされた。
(Statistical Analysis)
Data were presented as the mean ± standard deviation (SD) of at least three replicate samples. For experiments with fewer samples, such as transcriptomic data, all data points were shown. Student's t-test, Dunnett's test, chi-square test, or one-way ANOVA were used where appropriate. All statistical analyses were performed using the statistical program "R". A p-value of less than 0.05 (p<0.05) was considered significant.
〔結果〕
Myom2-RFP株を心筋細胞の成熟のスクリーニングに使用できるかどうかをテストするために、PSC-CMsの成熟に対する細胞外マトリックス(ECM)の影響を調べた。心筋細胞の成熟を促進するECMの候補を特定するために、E11からP56までの各ステージの野生型マウス心室のRNA-seqを実行した。
〔result〕
To test whether the Myom2-RFP line could be used to screen for cardiomyocyte maturation, we investigated the effect of extracellular matrix (ECM) on the maturation of PSC-CMs. To identify candidate ECMs that promote cardiomyocyte maturation, we performed RNA-seq of wild-type mouse ventricles at stages E11 to P56.
図3は、RNA-seqを行った際の各ECMの発現の階層的クラスタリングの結果を示す。濃度は正規化されたトランスクリプト(TPM)を最も高い発現量で割り、発現量が低いもの又は高いものを濃色とした。
この階層的クラスタリングでは、初期胚、新生児、及び成熟したものの心室の遺伝子発現パターンがグループ化を示した。これらから、代表的なものを選択した。
Figure 3 shows the results of hierarchical clustering of the expression of each ECM when RNA-seq was performed. The concentration was calculated by dividing the normalized transcript (TPM) by the highest expression level, and low or high expression levels were indicated by darker colors.
This hierarchical clustering showed groupings of gene expression patterns in early embryonic, neonatal, and adult ventricles, from which representatives were selected.
図4は、発生時の心臓のラミニン、コラーゲン、フィブロネクチンを含むECMの発現プロファイル(E11~P56)を示す。フィブロネクチン(Fn1)、及びコラーゲンタイプII(Col2a1)及びタイプIV(Col4a6)は、胎仔の心臓で豊富に発現した。また、コラーゲンタイプI(Col1a1及びCol1a2)及びIII(Col3a1)は、新生児の心臓で高度に発現上昇していた。一方、ラミニン(α2、α5、及びβ2)及びコラーゲンIV型メンバーの1つ(Col4a4)は、成熟したマウスの心臓で発現した。これにより、心筋細胞の発達、成熟時期に合わせたECM発現があるという予測がなされた。 Figure 4 shows the expression profile of ECM including laminin, collagen, and fibronectin in the developing heart (E11-P56). Fibronectin (Fn1), and collagen types II (Col2a1) and IV (Col4a6) were abundantly expressed in fetal hearts. Collagen types I (Col1a1 and Col1a2) and III (Col3a1) were also highly upregulated in neonatal hearts. On the other hand, laminin (α2, α5, and β2) and one member of collagen type IV (Col4a4) were expressed in mature mouse hearts. This led to the prediction that ECM expression is timed to coincide with the development and maturation of cardiomyocytes.
次に、図5により、ECMによる心筋細胞の成熟に対する影響の評価試験について説明する。具体的には、分化誘導10日後に、各ECMとして、さまざまな濃度(0.125~1μg/cm2の範囲)のラミニンE8断片(アイソフォーム111、121、211、221、311、321、332、411、421、511、及び521)、コラーゲン(I、III、及びIV型)、フィブロネクチン、及びコントロールの0.1%ゼラチン(Gelatin)を、それぞれプレーティングした。その後、RFP+のPSC-CMsのRFP強度を定量的に測定するために、PSC-CMsを7日間(1週間、1w)、14日間(2週間、2w)、及び28日間(4週間、4w)、すなわち分化誘導後、計17日~38日間、培養した(以下、分化誘導後のPSC-CMsにECMを加えて、所定期間、培養することを「ECM処理」という。後述する「ラミニン511/521処理」も同様である。)。その後、フローサイトメトリーを行った。
Next, an evaluation test of the effect of ECM on cardiomyocyte maturation will be described with reference to Figure 5. Specifically, 10 days after differentiation induction, various concentrations (range of 0.125 to 1 μg/ cm2 ) of laminin E8 fragments (
図6は、この各ECMの影響の評価の試験の結果を示す。具体的には、各ECM処理として、分化誘導から17日(d17、1w)、24日(d24、2w)、38日(d38、4w)後に、RFP+のPSC-CMsの割合と、RFP強度とを測定した。データは平均値±SD(n=3)、RFPの蛍光強度(RFP強度)は任意単位(a.u.)として示す。
結果として、RFP+のPSC-CMsの割合及びRFP強度の両方が17~38日まで増加したことが分かった。一部のECMのPSC-CMsでは、RFP強度の増加が用量依存的に観察された。
Figure 6 shows the results of the test evaluating the effect of each ECM. Specifically, for each ECM treatment, the proportion of RFP+ PSC-CMs and RFP intensity were measured 17 days (d17, 1w), 24 days (d24, 2w), and 38 days (d38, 4w) after differentiation induction. Data are shown as mean ± SD (n = 3), and RFP fluorescence intensity (RFP intensity) is shown as arbitrary units (a.u.).
As a result, it was found that both the proportion of RFP+ PSC-CMs and RFP intensity increased from days 17 to 38. In some ECM PSC-CMs, an increase in RFP intensity was observed in a dose-dependent manner.
図7は、上述の図6における、分化の38日目のECMの1μg/cm2の結果をまとめたグラフである。Dunnett検定を使用して、各ECMの分画をコントロール(ゼラチン)と比較した。「*」はP<0.05、「§」はP<0.01、「#」はP<0.001、「†」はP<0.0001を、それぞれ示す。
これらのECMの中で、RFP+のPSC-CMsの割合は同じままであった。すなわち、成熟を惹起する効果はないと考えられた。これに対して、RFP強度は、複数のECMで増加した。特に、ラミニン511 E8断片、及びラミニン522 E8断片(以下、「ラミニン511/521」と省略する。)は、他と比較して、最も高いRFP強度を示した。この結果は、ECM、特にラミニン511/521が、成熟を惹起するのではなく、in vitroで心筋細胞の成熟を促進したことを示唆している。
Figure 7 is a graph summarizing the results of 1 μg/ cm2 ECM at
Among these ECMs, the proportion of RFP+ PSC-CMs remained the same; that is, it was considered that there was no effect of inducing maturation. In contrast, RFP intensity increased in several ECMs. In particular,
図8は、ラミニン511が心筋細胞の成熟を促進するかどうかを検証するために、PSC-CMs上のECMの構造と形態を調べた写真である。図8(a)はTagRFP、図8(b)はα-アクチニン抗体、図8(c)は核のDAPIで、それぞれ染色したものを示す。スケールバーは、20μmである。
各ECMで処理すると、特に、細胞サイズ及びサルコメア長が増加していた。
Figure 8 shows the structure and morphology of the ECM on PSC-CMs to examine whether laminin-511 promotes cardiomyocyte maturation. Figure 8(a) shows staining with TagRFP, Figure 8(b) shows staining with α-actinin antibody, and Figure 8(c) shows staining with DAPI for nuclei. Scale bar is 20 μm.
Treatment with each ECM notably increased cell size and sarcomere length.
図9は、構造的及び形態学的特徴についての測定結果を統計計算した結果を示す。図9(a)はサルコメア長(μm)、図9(b)は細胞長(μm)、図9(c)は細胞面積(μm2)、図9(d)は細胞幅(μm)について、それぞれ、測定結果をバイオリンプロットにより表現した。このバイオリンプロットにおいて、白いボックスの黒い線は中央値を示し、ボックスの制限は25パーセンタイルと75パーセンタイルを示し、ウィスカーは25パーセンタイルと75パーセンタイルの四分位範囲の1.5倍を示し、多角形はデータの密度推定値を示し、極値まで描画した。 Figure 9 shows the results of statistical calculations of the measurements of structural and morphological features. The measurements are represented by violin plots: (a) sarcomere length (μm), (b) cell length (μm), (c) cell area ( μm2 ), and (d) cell width (μm). In the violin plots, the black line in the white box indicates the median, the box limits indicate the 25th and 75th percentiles, the whiskers indicate 1.5 times the interquartile range of the 25th and 75th percentiles, and the polygon indicates the density estimate of the data, drawn to the extremes.
結果として、ECM処理した心筋細胞は、特にラミニン(LN)511/521による処理で、コントロール(ゼラチン)と比較して、サルコメア長、細胞面積、細胞長、及び細胞幅の有意な増加を示した。
また、Dunnett検定を使用して、各ECM治療をコントロール(ゼラチン)と比較した。「*」はP<0.05、「§」はP<0.01、「#」はP<0.001、「†」はP<0.0001であることを示す。すると、ラミニン511/521で培養されたPSC-CMsは、細胞サイズ、細胞長、及び細胞幅の有意な増加を示した。さらに、PSC-CMsのサルコメア長は、コントロールと比較してラミニン-511/521で長かった。
これらの結果は、ラミニン511/521が、心筋細胞の構造的成熟を強く促進することを示した。
As a result, ECM-treated cardiomyocytes showed significant increases in sarcomere length, cell area, cell length, and cell width compared to the control (gelatin), especially with treatment with laminin (LN) 511/521.
Each ECM treatment was also compared to the control (gelatin) using Dunnett's test. "*" indicates P<0.05, "§" indicates P<0.01, "#" indicates P<0.001, and "†" indicates P<0.0001. PSC-CMs cultured with laminin-511/521 showed a significant increase in cell size, cell length, and cell width. Furthermore, sarcomere length of PSC-CMs was longer in laminin-511/521 compared to the control.
These results demonstrated that laminin-511/521 potently promotes the structural maturation of cardiomyocytes.
次に、ラミニン511/521がPSC-CMの機能的および転写成熟を増強したかどうかの詳細解析として、まず細胞の2核化について調べた。 Next, to further analyze whether laminin-511/521 enhanced the functional and transcriptional maturation of PSC-CMs, we first examined binucleation of the cells.
図10は、ラミニン511/521処理して培養したPSC-CMsにおける単核細胞と2核細胞の割合を、ゼラチンと比較したものである(n>100)。薄色が単核細胞(Mononuclear Cells)、濃色が2角細胞(Binuclear Cells)の割合を示す。「†」は、P<0.0001有意であることを示す。
結果として、ラミニン511/521処理したPSC-CMsは、コントロールのゼラチン(7.77%)よりも、2核細胞の集団が多くなった。具体的には、ラミニン511 E8断片では38.68%、ラミニン521 E8短辺では54.72%であった。
Figure 10 shows the percentage of mononuclear and binuclear cells in PSC-CMs cultured with
As a result, laminin-511/521-treated PSC-CMs had a higher population of binucleated cells than control gelatin (7.77%), specifically, 38.68% for laminin-511 E8 fragment and 54.72% for laminin-521 E8 short side.
次に、心筋細胞成熟を反映したギャップ接合タンパク質であるコネキシン-43(Cx43)の局在化により、ラミニン511/521処理で、ギャップジャンクションが形成されるかどうか調べた。
ここで、胚性心筋細胞では、Cx43は細胞質中で拡散発現される。その後、新生児から若年期には、心筋細胞の側面に局在する。心筋細胞が完全に成熟すると、Cx43は主に心筋細胞のインターカレーションディスクに局在化する。このような形態変化が見られるかどうか観察した。
Next, we examined whether
Here, in embryonic cardiomyocytes, Cx43 is diffusely expressed in the cytoplasm. Then, in neonatal and juvenile stages, it is localized to the lateral surface of cardiomyocytes. When cardiomyocytes are fully mature, Cx43 is mainly localized to the intercalation disks of cardiomyocytes. We observed whether such morphological changes were observed.
図11は、分化後38日目に、Cx43用に染色されたPSC-CMsの代表的な写真を示す。スケールバーは、20μmである。
コントロールのゼラチン上のPSC-CMsは、Cx43を弱く発現した。これに対して、ラミニン511/521処理したPSC-CMsは、細胞の側面にCx43を強く発現した。すなわち、ラミニン511/521処理での培養により、ギャップジャンクション(Cx43)が形成されていた。
これらの結果は、ラミニン511/521処理により、PSC-CMsがより成熟し、少なくとも、新生児又は若年期の段階に達したことを示唆した。
Figure 11 shows representative photographs of PSC-CMs stained for Cx43 at
Control PSC-CMs on gelatin expressed weak Cx43, whereas
These results suggested that
次に、酸素消費量率(OCR)を用いたPSC-CMsのミトコンドリア活性について測定した。心筋細胞は、出生後、エネルギー産生のために糖質を脂肪酸酸化させるためである。 Next, we measured the mitochondrial activity of PSC-CMs using oxygen consumption rate (OCR). After birth, cardiomyocytes oxidize carbohydrates to fatty acids to produce energy.
図12は、ラミニン511/521処理したPSC-CMs及びゼラチンについて、オリゴマイシン、FCCP、及び、ロテノン/アンチマイシンAに対応する代表的なトレースを示す。
図13(a)は基礎呼吸、図13(b)はATP産生関連呼吸、図13(c)はプロトンリーク、図14(d)は最大呼吸についてのOCRの統計分析結果を示す。データは平均値±SD(n=3)として示される。ラミニン上のPSC-CMsとゼラチン上のPSC-CMsを対照として比較するために、Dunnett検定を行った。「*」はP<0.05、「§」はP<0.01、「#」はP<0.001、「†」はP<0.0001であることを示す。
結果として、ラミニン511/521処理したPSC-CMsは、基礎呼吸及び最大呼吸レベルがより高く、コントロールのゼラチン上のPSC-CMsよりも高いミトコンドリア活性を示唆した。
FIG. 12 shows representative traces corresponding to oligomycin, FCCP, and rotenone/antimycin A for
Statistical analysis of OCR for basal respiration (a), ATP production-related respiration (b), proton leak (c), and maximum respiration (d) are shown in Fig. 13(a), 13(b), 13(c), and 14(d), respectively. Data are shown as mean ± SD (n = 3). Dunnett's test was performed to compare PSC-CMs on laminin and gelatin as controls. * indicates P < 0.05, § indicates P < 0.01, # indicates P < 0.001, and † indicates P < 0.0001.
As a result,
次に、生理学的変化をさらに調べるために、ラミニン511/521処理したPSC-CMsのカルシウムトランジェントについて調べた。
Next, to further investigate physiological changes, we examined calcium transients in
図14は、38日目に1Hzで刺激されたカルシウムトランジェントの代表的なトレースを示す。ラミニン-511/521で培養したPSC-CMsと、ゼラチンのコントロールとを比較した。
図15(a)は、カルシウムトランジェントのピークまでの時間の平均値、図15(b)はピーク振幅、図15(c)は減衰時間(n>80)を示す。Dunnett検定にて、「*」はP<0.05、「†」はP<0.0001であることを示す。
結果として、ラミニン521処理したPSC-CMsは、ピークまでの時間が大幅に短縮され、減衰までの時間も有意に減少し、ピーク振幅も高かった。
Figure 14 shows representative traces of calcium transients stimulated at 1 Hz on
Fig. 15(a) shows the average time to peak of calcium transients, Fig. 15(b) shows the peak amplitude, and Fig. 15(c) shows the decay time (n>80). In Dunnett's test, "*" indicates P<0.05, and "†" indicates P<0.0001.
As a result, laminin-521-treated PSC-CMs exhibited a significantly reduced time to peak, a significantly reduced time to decay, and a higher peak amplitude.
次に、ラミニン511/521処理したPSC-CMsのサルコメア短縮についても調べた。
Next, we investigated sarcomere shortening in PSC-CMs treated with
図16(a)は、電気パルス(1Hz)刺激中のサルコメア長の代表的なトレースを示す。図16(b)は、サルコメア短縮の平均データを示す。データは平均±SD(n>40)として示される。Dunnett検定にて、「*」はP<0.05、「§」はP<0.01であることを示す。
結果として、ラミニン511/521処理を行うと、サルコメア短縮の割合を有意に増加させることが分かった。
これらの結果は、ラミニン511/521処理にて、PSC-CMの生理特性を改善することを示した。
Figure 16(a) shows a representative trace of sarcomere length during electrical pulse (1 Hz) stimulation. Figure 16(b) shows average data of sarcomere shortening. Data are shown as mean ± SD (n>40). "*" indicates P<0.05 and "§" indicates P<0.01 by Dunnett's test.
As a result, it was found that
These results demonstrated that
次に、ラミニン511/521処理したPSC-CMsのトランスクリプトーム解析を行った。
Next, we performed transcriptome analysis of
図17は、トランスクトリーム解析として、生物学的プロセスに対して選択された8つのGOタームの遺伝子の合計発現を示す。観察された形態学的又は生理学的変化と比較して、特定のGOタームの発現は、大まかには変化しなかった。
図18は、トランスクトリームの詳細な分析を行った結果を示す。上述の合計発現と異なり、ゼラチンと比較すると、心筋細胞の発達に関連する既知の遺伝子は、ラミニン511/521処理されたPSC-CMsでアップレギュレートされた。たとえば、心臓マーカー遺伝子(Tnnt2及びActc1)、心臓遺伝子発現に関する転写因子の遺伝子(Ankrd23)、カルシウム関連遺伝子(Casq2)、及びサルコメア遺伝子(Mybpc2、Mybpc3、Myh7、及びMyl2)等である。
これらの結果によれば、サルコメア遺伝子と成熟関連遺伝子とは、ラミニン511/521処理されたPSC-CMsでアップレギュレートされる傾向があり、ECMの効果は、転写量の変化ではなく、翻訳量の変化であることが示唆された。
Figure 17 shows the total expression of genes of eight GO terms selected for biological processes as a transcriptome analysis. Compared to the observed morphological or physiological changes, the expression of certain GO terms did not change significantly.
Detailed transcriptome analysis is shown in Figure 18. In contrast to the total expression shown above, genes known to be associated with cardiomyocyte development were upregulated in
These results suggest that sarcomere genes and maturation-related genes tended to be upregulated in
次に、ラミニン511/521処理したPSC-CMsについて、どの程度成熟しているのかを定量的に測定するため、トランスクリプトームに基づく心筋細胞成熟度評価を行った。
Next, we performed transcriptome-based cardiomyocyte maturity assessment on
図19は、成熟度スコアを解析した結果を示すグラフである。Myom2-RFP株を分化誘導後10日後から2週間(2w)及び4週間(4w)、ラミニン511/521処理したPSC-CMsと、ゼラチンのみのコントロールのPSC-CMsとをフローサイトメトリーでセルソーティングして取得した後、成熟度スコアを測定した。
結果として、ラミニン511/521処理したPSC-CMsは、2wであっても、ゼラチンで4w培養したものよりも成熟していた。
19 is a graph showing the results of maturation score analysis. PSC-CMs treated with
As a result,
以上をまとめると、Myom2-RFP株を分化したRFP+のPSC-CMsは、ラミニン511/521処理により、サルコメア短縮が観察され、RFP-のPSC-CMsよりも形態的、構造的、機能的に成熟していた。よって、ラミニン511/521処理したPSC-CMsを取得することで、成熟心筋細胞を取得可能となる。
In summary, RFP+ PSC-CMs differentiated from the Myom2-RFP line showed sarcomere shortening upon treatment with
なお、上述の結果では示していないものの、予備的な実験において、ヒトのPSC-CMsについても、ラミニン511/521処理を行って、成熟度スコアを評価している。これにより、実際に、ゼラチン等のコントロールと比べて、成熟度が増加していることを確認している。
Although not shown in the results above, in preliminary experiments, human PSC-CMs were also treated with
なお、上記実施の形態の構成及び動作は例であって、本発明の趣旨を逸脱しない範囲で適宜変更して実行することができることは言うまでもない。 It goes without saying that the configurations and operations of the above-described embodiments are merely examples and can be modified as appropriate without departing from the spirit and scope of the present invention.
本発明によれば、成熟心筋細胞製造方法により実際に成熟した心筋細胞を提供し、これを移植医療や創薬支援等に用いることができ、産業上利用可能である。 According to the present invention, the method for producing mature cardiomyocytes can provide mature cardiomyocytes that can be used in transplant medicine, drug discovery support, etc., and can be used industrially.
Claims (3)
ラミニン断片を含み、
前記ラミニン断片は、ラミニン511 E8断片及び/又はラミニン521 E8断片である
ことを特徴とする細胞外マトリックス。 An extracellular matrix for maturing immature cardiomyocytes, comprising:
Contains laminin fragments,
The laminin fragment is a laminin 511 E8 fragment and/or a laminin 521 E8 fragment.
成熟した心筋細胞を取得する
ことを特徴とする成熟心筋細胞製造方法。 Cultivating immature cardiomyocytes in a medium containing the extracellular matrix of claim 1;
A method for producing mature cardiomyocytes, comprising obtaining mature cardiomyocytes.
前記細胞外マトリックスは、ラミニン断片を含み、
前記ラミニン断片は、ラミニン511 E8断片及び/又はラミニン521 E8断片である
ことを特徴とする心筋細胞成熟キット。 containing an extracellular matrix for maturing immature cardiomyocytes;
the extracellular matrix comprises laminin fragments;
The cardiomyocyte maturation kit, wherein the laminin fragment is a laminin 511 E8 fragment and/or a laminin 521 E8 fragment.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020017809A JP7537726B2 (en) | 2020-02-05 | 2020-02-05 | Extracellular matrix, method for producing mature cardiomyocytes, and cardiomyocyte maturation kit |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020017809A JP7537726B2 (en) | 2020-02-05 | 2020-02-05 | Extracellular matrix, method for producing mature cardiomyocytes, and cardiomyocyte maturation kit |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021122233A JP2021122233A (en) | 2021-08-30 |
| JP7537726B2 true JP7537726B2 (en) | 2024-08-22 |
Family
ID=77457734
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020017809A Active JP7537726B2 (en) | 2020-02-05 | 2020-02-05 | Extracellular matrix, method for producing mature cardiomyocytes, and cardiomyocyte maturation kit |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7537726B2 (en) |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130330825A1 (en) | 2012-06-07 | 2013-12-12 | City Of Hope | Attachment substrates for directed differentiation of human embryonic stem cells in culture |
| US20150164958A1 (en) | 2012-07-12 | 2015-06-18 | Isletone Ab | Derivation and self-renewal of isi1+ cells and uses thereof |
| WO2016043168A1 (en) | 2014-09-16 | 2016-03-24 | 国立大学法人大阪大学 | Method for producing cardiomyocyte population from pluripotent stem cells |
| US20160122717A1 (en) | 2013-07-02 | 2016-05-05 | National University Of Singapore | Differentiation of pluripotent stem cells and cardiac progenitor cells into striated cardiomyocyte fibers using laminins ln-511, ln-521 and ln-221 |
| WO2016104614A1 (en) | 2014-12-25 | 2016-06-30 | 国立大学法人京都大学 | Novel mature cardiac muscle cell marker |
| WO2018038242A1 (en) | 2016-08-25 | 2018-03-01 | 国立大学法人京都大学 | Method for culturing pluripotent stem cell on specific laminin |
| WO2018143312A1 (en) | 2017-01-31 | 2018-08-09 | 国立大学法人大阪大学 | Differentiation control method for pluripotent stem cells |
-
2020
- 2020-02-05 JP JP2020017809A patent/JP7537726B2/en active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130330825A1 (en) | 2012-06-07 | 2013-12-12 | City Of Hope | Attachment substrates for directed differentiation of human embryonic stem cells in culture |
| US20150164958A1 (en) | 2012-07-12 | 2015-06-18 | Isletone Ab | Derivation and self-renewal of isi1+ cells and uses thereof |
| US20160122717A1 (en) | 2013-07-02 | 2016-05-05 | National University Of Singapore | Differentiation of pluripotent stem cells and cardiac progenitor cells into striated cardiomyocyte fibers using laminins ln-511, ln-521 and ln-221 |
| WO2016043168A1 (en) | 2014-09-16 | 2016-03-24 | 国立大学法人大阪大学 | Method for producing cardiomyocyte population from pluripotent stem cells |
| WO2016104614A1 (en) | 2014-12-25 | 2016-06-30 | 国立大学法人京都大学 | Novel mature cardiac muscle cell marker |
| WO2018038242A1 (en) | 2016-08-25 | 2018-03-01 | 国立大学法人京都大学 | Method for culturing pluripotent stem cell on specific laminin |
| WO2018143312A1 (en) | 2017-01-31 | 2018-08-09 | 国立大学法人大阪大学 | Differentiation control method for pluripotent stem cells |
Non-Patent Citations (1)
| Title |
|---|
| 心筋細胞と電気現象|心臓とはなんだろう(2),看護roo!,2015年,retrieved from the Internet on 2023.11.22, https://www.kango-roo.com/learning/1657/ |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021122233A (en) | 2021-08-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ratnayake et al. | Macrophages provide a transient muscle stem cell niche via NAMPT secretion | |
| Ribatti | The chick embryo chorioallantoic membrane (CAM). A multifaceted experimental model | |
| JP6388537B2 (en) | Patient-derived induced pluripotent stem cell-derived cardiomyocytes and methods of use | |
| Jafree et al. | Mechanisms and cell lineages in lymphatic vascular development | |
| Priori et al. | Induced pluripotent stem cell–derived cardiomyocytes in studies of inherited arrhythmias | |
| Liu et al. | Borg5 is required for angiogenesis by regulating persistent directional migration of the cardiac microvascular endothelial cells | |
| CN1671742A (en) | Use of HMGB1 in treating tissue damage and/or promoting tissue repair | |
| Kowalski et al. | Sympathetic neurons regulate cardiomyocyte maturation in culture | |
| Boezio et al. | The developing epicardium regulates cardiac chamber morphogenesis by promoting cardiomyocyte growth | |
| Hashimoto et al. | Time-lapse imaging of cell cycle dynamics during development in living cardiomyocyte | |
| Masyuk et al. | Retrograde migration of pectoral girdle muscle precursors depends on CXCR4/SDF-1 signaling | |
| JP7537726B2 (en) | Extracellular matrix, method for producing mature cardiomyocytes, and cardiomyocyte maturation kit | |
| JP7514546B2 (en) | Method for maturing cardiomyocytes, method for evaluating maturity of cardiomyocytes, method for purifying mature cardiomyocytes, device for evaluating maturity of cardiomyocytes, program for evaluating maturity of cardiomyocytes, and cardiomyocyte maturation kit | |
| Gourdie | A map of the heart: gap junctions, connexin diversity and retroviral studies of conduction myocyte lineage | |
| US12268704B2 (en) | Hippo regulation of cardiac vascularity, fibrosis, and inflammation | |
| Lohbihler et al. | Human pluripotent stem cell-derived atrioventricular node-like pacemaker cells exhibit biological conduction bridge properties in vitro and in vivo | |
| Munz et al. | Embryonic cortical layer 5 pyramidal neurons form an active, transient circuit motif perturbed by autism-associated mutations | |
| JP4536233B2 (en) | Method for producing transgenic animals | |
| Jiang | A Small Internal Deletion in Titin Yields Ion Channel-Dependent Cardiomyopathy and Atrial Fibrillation | |
| Fernández-Medarde et al. | Ras GEF mouse models for the analysis of ras biology and signaling | |
| JP2008148693A (en) | Stem cell isolation method | |
| EP4499810A1 (en) | Heart tissue models, method of producing heart tissue models and uses of heart tissue models | |
| Paquette et al. | Loss of developmentally derived Irf8+ macrophages promotes hyperinnervation and arrhythmia in the adult zebrafish heart | |
| Wang et al. | Electrophysiological profiling of exocytosis during early-stage development of the zebrafish lateral line | |
| Schiavo | The Role of VEGFC in Developmental Hematopoiesis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20221208 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20231128 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240123 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20240206 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240430 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20240430 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240507 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20240524 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240723 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240801 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7537726 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |