JP7353187B2 - 抗l1-cam抗体およびその使用 - Google Patents
抗l1-cam抗体およびその使用 Download PDFInfo
- Publication number
- JP7353187B2 JP7353187B2 JP2019569397A JP2019569397A JP7353187B2 JP 7353187 B2 JP7353187 B2 JP 7353187B2 JP 2019569397 A JP2019569397 A JP 2019569397A JP 2019569397 A JP2019569397 A JP 2019569397A JP 7353187 B2 JP7353187 B2 JP 7353187B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- cam
- antibody
- antibodies
- hue71
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/531—Production of immunochemical test materials
- G01N33/532—Production of labelled immunochemicals
- G01N33/534—Production of labelled immunochemicals with radioactive label
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/40—Immunoglobulins specific features characterized by post-translational modification
- C07K2317/41—Glycosylation, sialylation, or fucosylation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/54—F(ab')2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/20—Fusion polypeptide containing a tag with affinity for a non-protein ligand
- C07K2319/21—Fusion polypeptide containing a tag with affinity for a non-protein ligand containing a His-tag
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
Landscapes
- Health & Medical Sciences (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Engineering & Computer Science (AREA)
- Cell Biology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Animal Behavior & Ethology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Zoology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Nuclear Medicine (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicinal Preparation (AREA)
Description
(配列表)本出願は配列表を含み、前記配列表はASCII形式で電子提出され、それにより前記は参照によってその全体が本明細書に含まれる。
(技術分野)
本技術は、概して、L1-CAMタンパク質に特異的に結合する、免疫グロブリン関係組成物(例えば抗体またはその抗原結合フラグメント)および前記の使用に関する。特に、本技術は、L1-CAM中和抗体の調製、並びにL1-CAM関連癌の検出および治療における前記の使用に関する。
キメラ抗原受容体(CAR)技術(Sadelain M et al., Cancer Discov 3:388-98, 2013)の出現は、抗L1-CAM再指向遺伝子改変T細胞の治療薬研究を急速に拡大し、L1-CAM-CAR改変T細胞を用いるいくつかの臨床試験(NCT00889954(いずれもL1-CAM(+)癌)、NCT01935843(L1-CAM(+)固形腫瘍))が存在する。以下を参照されたい:Hong H et al., J Immunother 37:93-104, 2014。T細胞は低レベルのL1-CAMを有する腫瘍を効果的に標的とすることができるが、低レベルL1-CAM発現を有する正常組織内にたまたま存在するものへの潜在的毒性に関する懸念も存在する。
毒性の他に、リンパ球療法のための細胞採集、加工、貯蔵、輸送および製品出荷規制は、特に細胞が遺伝子改変を必要とするときはチャレンジングであり得る。T細胞の消耗、生存および帰巣は、莫大な数のこれら細胞の輸液にもかかわらず最適を下回る。さらにまた、CAR改変T細胞は免疫抑制腫瘍ミクロ環境にとって例外ではなく、当該環境では、腫瘍関連マクロファージおよび骨髄系抑制細胞は、CAR改変T細胞の抗腫瘍特性を回避するために協調して働く。さらにまた、CAR改変T細胞は、古典的T細胞が直面する同じ免疫抑制的制約を受ける(前記制約には腫瘍細胞上のB7によるCTLA4の嵌合またはPD-L1(B7-H1)によるPD-1の嵌合後のアネルギーが含まれる)。癌治療のためにCAR改変T細胞療法に代わる臨床的に有効な選択肢が必要とされる。
別の特徴では、本開示は以下を含む抗体を提供する:(a)配列番号:13、14、21、22、25、29、41、45、50または52のいずれか1つに存在するLC配列と少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%同一であるLC配列、および/または(b)配列番号: 9、10、17、18、26、30、42、46、49および51のいずれか1つに存在するHC配列と少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%同一であるHC配列。
ある特徴では、本開示は、本明細書に記載する抗体のいずれかをコードする組換え核酸配列を提供する。いくつかの実施態様では、組換え核酸配列は、配列番号:11、12、15、16、19、20、23、24、27、28、31、32、43、44、47および48から成る群から選択される。
別の特徴では、本開示は、本明細書に開示する組換え核酸配列のいずれかを含む宿主細胞またはベクターを提供する。
ある特徴では、本開示は、本技術の抗体または抗原結合フラグメントおよび医薬的に許容できる担体を含む組成物を提供し、ここで、抗体または抗原結合フラグメントは、場合によって以下から成る群から選択される薬剤と複合体化される:同位体、色素、色原体、造影剤、薬物、毒素、サイトカイン、酵素、酵素阻害剤、ホルモン、ホルモンアンタゴニスト、成長因子、放射性核種、金属、リポソーム、ナノ粒子、RAN、DNAまたは前記の任意の組合せ。
加えて或いはまた別に、本方法のいくつかの実施態様では、抗体は、追加の治療薬剤と別々に、逐次的に、または同時に対象動物に投与される。追加の治療薬剤の例には、以下の1つ以上が含まれる:アルキル化剤、白金剤、タキサン、ビンカ剤、抗エストロゲン薬、アロマターゼ阻害剤、卵巣抑制剤、VEGF/VEGFR阻害剤、EGF/EGFR阻害剤、PARP阻害剤、細胞増殖抑制アルカロイド、細胞傷害性抗生物質、抗代謝剤、内分泌/ホルモン剤、ビスホスホネート療法剤。
加えて或いはまた別に、いくつかの実施態様では、当該方法はさらにまた、放射性核種と複合物化させた本技術の抗体を含む免疫複合体の有効量を対象動物に投与する工程を含む。いくつかの実施態様では、放射性核種は、アルファ粒子放射同位体、ベータ粒子放射同位体、オージェ-エミッター、または前記の任意の組合せである。ベータ粒子放射同位体の例には、86Y、90Y、89Sr、165Dy、186Re、188Re、177Lu、および67Cuが含まれる。当該方法のいくつかの実施態様では、正常組織における非特異的FcR依存性結合は、(例えばFc領域におけるN297A変異(非グリコシル化をもたらす)により)排除されるかまたは軽減される。
L1-CAM関連癌の検出および/または治療キットもまた開示され、前記キットは、少なくとも1つの本技術の免疫グロブリン関係組成物(例えば本明細書に記載する任意の抗体または抗原結合フラグメント)、またはその機能性変種(例えば置換変種)を含む。ある種の実施態様では、免疫グロブリン関係組成物は、1つ以上の検出可能な標識と連結される。ある実施態様では、1つ以上の検出可能な標識は、放射能標識、蛍光標識、または色原体標識を含む。
加えて或いはまた別に、いくつかの実施態様では、キットはさらにまた、本明細書に記載の抗L1-CAM免疫グロブリン関係組成物と特異的に結合する二次抗体を含む。いくつかの実施態様では、二次抗体は、放射能標識、蛍光標識、または色原体標識から成る群から選択される少なくとも1つの検出可能標識に連結される。
本開示は概して免疫グロブリン関係組成物(例えば抗体またはその抗原結合フラグメント)を提供し、前記は、L1-CAMポリペプチドと特異的に結合し、その生物学的活性を中和することができる。本技術の免疫グロブリン関係組成物は、L1-CAM関連癌をその必要がある対象動物で検出または治療する方法で有用である。したがって、本方法の多様な特徴は、抗L1-CAM抗体の調製、特徴付けおよび操作と関係を有する。本技術の免疫グロブリン関係組成物は、単独でまたは癌治療のための追加の治療薬剤との併用で有用である。いくつかの実施態様では、免疫グロブリン関係組成物はヒト化抗体、キメラ抗体または二重特異性抗体である。
本方法の実施では、分子生物学、タンパク質化学、細胞生物学、免疫学、微生物学および組換えDNAにおける多くの通常的な技術が用いられる。例えば以下を参照されたい:Sambrook and Russell eds. (2001) Molecular Cloning: A Laboratory Manual, 3rd edition;シリーズ、Ausubel et al. eds. (2007) Current Protocols in Molecular Biology);シリーズ、Methods in Enzymology (Academic Press, Inc., N.Y.);MacPherson et al. (1991) PCR 1: A Practical Approach (IRL Press at Oxford University Press);MacPherson et al. (1995) PCR 2: A Practical Approach;Harlow and Lane eds. (1999) Antibodies, A Laboratory Manual;Freshney (2005) Culture of Animal Cells: A Manual of Basic Technique, 5th edition;Gait ed. (1984) Oligonucleotide Synthesis;米国特許4,683,195号;Hames and Higgins eds. (1984) Nucleic Acid Hybridization;Anderson (1999) Nucleic Acid Hybridization;Hames and Higgins eds. (1984) Transcription and Translation;Immobilized Cells and Enzymes (IRL Press (1986));Perbal (1984) A Practical Guide to Molecular Cloning;Miller and Calos eds. (1987) Gene Transfer Vectors for Mammalian Cells (Cold Spring Harbor Laboratory);Makrides ed. (2003) Gene Transfer and Expression in Mammalian Cells;Mayer and Walker eds. (1987) Immunochemical Methods in Cell and Molecular Biology (Academic Press, London);およびHerzenberg et al. eds (1996) Weir’s Handbook of Experimental Immunology。ポリペプチド遺伝子発現生成物レベル(すなわち遺伝子翻訳レベル)を検出および測定する方法は当業界では周知であり、前記にはポリペプチド検出方法(例えば抗体検出および定量の技術)の使用が含まれる(例えば以下を参照されたい:Strachan & Read, Human Molecular Genetics, Second Edition. (John Wiley and Sons, Inc., NY, 1999))。
特段の規定がなければ、本明細書で用いられる技術用語および学術用語はいずれも、本技術が属する分野の業者の誰もが一般的に理解する意味と同じ意味を有する。本明細書および添付の特許請求の範囲で用いられるように、単数形“a”、“an”および“the”は、文脈が明らかにそうではないことを示していないかぎり複数の対応語を含む。例えば、“a cell(細胞)”と言えば2つ以上の細胞の組合せなどを含む。概して、本明細書で用いられる用語体系、並びに下記に記載する細胞培養、分子遺伝学、有機化学、分析化学および核酸化学、およびハイブリダイゼーションにおける研究室手順は、周知であり当業界で通常的に用いられるものである。
本明細書で用いられるように、数に関して“約”という用語は、そうでないことが記載されていないかまたは文脈からそうでないことが明白でないかぎり、どちらの方向(多い方または少ない方)でも当該数の1%、5%または10%の範囲内に含まれる数を含むと考えられる(ただしそのような数があり得る値の0%未満または100%を超える場合を除く)。
“アジュバント”は、免疫系の刺激を引起す1つ以上の物質を指す。本文脈では、アジュバントは、1つ以上のワクチン抗原または抗体への応答を強化するために用いられる。アジュバントは、ワクチンの投与前、ワクチンと一緒に、または投与後に対象動物に投与できる。アジュバントとして用いられる化学的化合物の例には、アルミニウム化合物、油、ブロックポリマー、免疫刺激複合体、ビタミンおよび鉱物(例えばビタミンE、ビタミンA、セレニウムおよびビタミンB12)、Quil A(サポニン)、細菌および真菌細胞壁成分(例えばリポ多糖類、脂質タンパク質および糖タンパク質)、ホルモン、サイトカイン、および行動刺激因子が含まれる。
本明細書で用いられるように、“抗体”という用語は包括的に免疫グロブリンまたは免疫グロブリン様分子を指す。例示すれば、前記にはIgA、IgD、IgE、IgGおよびIgM、前記の組合せ、並びに任意の脊椎動物、例えば哺乳動物(例えばヒト、ヤギ、ウサギおよびマウス)とともに非哺乳動物種(例えばサメの免疫グロブリン)で免疫応答時に生成される同様な分子が含まれるが、ただしそれらに限定されない。本明細書で用いられるように、“抗体”(無傷の免疫グロブリンを含む)および“抗原結合フラグメント”は、対象の分子(または高度に類似する対象分子のグループ)と特異的に結合し、他の分子との結合を実質的に排除する。例えば、抗体および抗体フラグメントは、生物学的サンプル中の他の分子に対する結合定数よりも高い、少なくとも103 M-1、少なくとも104 M-1または少なくとも105 M-1の結合定数を対象分子に対して有する。“抗体”という用語はまた、遺伝的に操作された形態、例えばキメラ抗体(例えばヒト化マウス抗体)、ヘテロ複合体抗体(例えば二重特異性抗体)を含む。以下の文献もまた参照されたい:Pierce Catalog and Handbook, 1994-1995(Pierce Chemical Co., Rockford, Ill.);Kuby, J., Immunology, 3rd Ed., W.H. Freeman & Co., New York, 1997。
本明細書で用いられるように、“複合体化される”という用語は、当業者に公知の任意の方法による2つの分子の連合を指す。適切なタイプの連合は化学的結合および物理的結合を含む。化学的結合には、例えば共有結合および配位結合が含まれる。物理的結合には、例えば水素結合、二極性相互作用、ファンデルワールス力、静電気的相互作用、疎水性相互作用、および芳香環スタッキング相互作用が含まれる。
本明細書で用いられるように、“単鎖抗体”または“単鎖Fv(scFv)”は、Fvフラグメントの2つのドメイン(VLおよびVH)の抗体融合分子を指す。単鎖抗体分子は、多数の個々の分子を含むポリマー、例えばダイマー、トリマーまたは他のポリマーを含むことができる。さらにまた、Fvフラグメントの2つのドメイン(VLおよびVH)は別々の遺伝子によってコードされるが、それらは組換え方法を用いるか、合成リンカーによって結合させることができる。合成リンカーは、それら2つのドメインを単一タンパク質鎖として生成することを可能にし、単一タンパク質鎖ではVLおよびVH領域対は一価分子(単鎖Fv(scFv)として知られている)を形成する(Bird et al. (1988) Science 242:423-426;およびHuston et al. (1988) Proc. Natl. Acad Sci. USA 85:5879-5883)。そのような単鎖抗体は、組換え技術または無傷の抗体の酵素的もしくは化学的切断によって調製できる。
上記に記載のいずれの抗体フラグメントも、当業者に公知の通常的な技術を用いて入手でき、フラグメントは、無傷の抗体と同じ態様で、結合特異性および中和活性についてスクリーニングされる。
“抗原結合フラグメント”という用語は、抗原に結合するために必要なポリペプチドの部分を保有する、全免疫グロブリン構造物のフラグメントを指す。本技術で有用な抗原結合フラグメントの例にはscFv、(scFv)2、scFvFc、Fab、Fab′およびF(ab′)2が含まれるが、ただし前記に限定されない。
“結合親和性”とは、分子(例えば抗体)の単一結合部位とその結合パートナー(例えば抗原または抗原性ペプチド)との間の合計された非共有結合性相互作用力を意味する。分子XのそのパートナーYに対する親和性は一般的に解離定数(Kd)によって表すことができる。親和性は当業界で公知の標準的な方法(本明細書に記載する方法を含む)によって測定できる。低親和性複合体は、概して抗原から容易に解離する傾向がある抗体を含み、一方、高親和性複合体は、概してより長い期間抗原との結合を維持する傾向がある抗体を含む。
本明細書で用いられるように、“キメラ抗体”という用語は、1つの種のモノクローナル抗体のFc定常領域(例えばマウスFc定常領域)が、組換えDNA技術を用いて別の種の抗体のFc定常領域(例えばヒトFc定常領域)で取替えられる抗体を意味する。全般的には以下を参照されたい:Robinson et al., PCT/US86/02269;Akira et al., 欧州特許公開184,187;Taniguchi, 欧州特許公開171,496;Morrison et al., 欧州特許公開173,494;Neuberger et al., WO 86/01533;Cabilly et al. 米国特許4,816,567号;Cabilly et al., 欧州特許公開0125,023;Better et al., Science 240: 1041-1043, 1988;Liu et al., Proc. Natl. Acad. Sci. USA 84: 3439-3443, 1987;Liu et al., J. Immunol 139: 3521-3526, 1987;Sun et al., Proc. Natl. Acad. Sci. USA 84: 214-218, 1987;Nishimura et al., Cancer Res 47: 999-1005, 1987;Wood et al., Nature 314: 446-449, 1885;およびShaw et al., J. Natl. Cancer Inst. 80: 1553-1559, 1988。
本明細書で用いられるように、“コンセンサスFR”という用語は、コンセンサス免疫グロブリン配列のフレームワーク(FR)抗体領域を意味する。抗体のFR領域は抗原と接触しない。
本明細書で用いられるように、“有効量”という用語は、所望の治療効果および/または予防効果を達成するために十分な量を指す。前記は、例えば、本明細書に記載する疾患もしくは症状、または本明細書に記載する疾患もしくは症状に関連する1つ以上の徴候もしくは症候の予防もしくは軽減をもたらす量である。治療的または予防的適用の関係では、対象動物に投与される組成物の量は、組成物、疾患の範囲、タイプおよび重篤度、並びに個体の特徴(例えば一般的な健康状態、年齢、性別、体重および薬物に対する耐性)に応じて変動するであろう。当業者は、これらの要件および他の要件に応じて適切な投薬量を決定できるであろう。組成物はまた1つ以上の追加の治療化合物と組合わせて投与され得る。本明細書に記載する方法では、治療組成物は、本明細書に記載する疾患または症状の1つ以上の徴候または症候を有する対象動物に投与できる。本明細書で用いられるように、組成物の“治療的に有効な量”は、疾患または症状の生理学的影響を緩和または除去する組成物レベルを指す。治療的に有効な量は1回以上の投与でもたらされ得る。
本明細書で用いられるように、“発現”は以下の1つ以上を含む:遺伝子の前駆体mRNAへの転写;前駆体mRNAのスプライシングおよび他のプロセッシングによる成熟mRNAの生成;mRNAの安定性;成熟mRNAのタンパク質への翻訳(コドン利用およびtRNA利用可能性を含む);および翻訳生成物のグリコシル化および/または他の改変(適切な発現および機能が要求される場合)。
本明細書で用いられるように、“遺伝子”という用語は、RNA生成物の規制された生合成のための全情報を含むDNAのセグメントを意味し、プロモーター、エクソン、イントロン、および発現を制御する他の非翻訳領域を含む。
本明細書で用いられるように、“同一である”またはパーセント“同一性”という用語は、2つ以上の核酸またはポリペプチド配列という文脈で用いられるときは、2つ以上の配列または部分配列が同じであるか、或いは同じであるアミノ酸残基またはヌクレオチドの指定のパーセンテージを有する(すなわち、約60%、65%、70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、または前記より高い同一性を指定の領域(例えば本明細書に記載する抗体をコードする核酸配列または本明細書に記載する抗体のアミノ酸配列)にわたって有する)2つ以上の配列または部分配列を指し、このとき、2つ以上の配列は、BLASTまたはBLAST 2.0配列比較アルゴリズムを用い下記に記載の既定値パラメーターで測定されるか、または手動アラインメントおよび目視精査(例えばNCBIウェブサイト)によって、比較ウインドウまたは指定領域における最大一致のために比較およびアラインメントを実施される。そのような配列は、したがって“実質的に同一”と呼ばれる。この用語はまた、被検配列の相補配列を指し、または被検配列の相補配列に適用できる。この用語はまた、欠失および/または付加を有する配列とともに、置換を有する配列を含む。いくつかの実施態様では、同一性は、長さが少なくとも25アミノ酸またはヌクレオチド、または長さが50-100アミノ酸またはヌクレオチドである領域にわたって存在する。
本明細書で用いられるように、“個体”、“患者”または“対象動物”は、個々の器官、脊椎動物、哺乳動物、または人間であり得る。いくつかの実施態様では、個体、患者または対象動物は人間である。
本明細書で用いられるように、“ポリクローナル抗体”という用語は、少なくとも2つの異なる抗体産生細胞株に由来する抗体調製物を意味する。この用語の使用は、異なるエピトープまたは抗原領域と特異的に結合する抗体を含む、少なくとも2つの抗体の調製物を含む。
本明細書で用いられるように、“ポリペプチド”、“ペプチド”および“タンパク質”という用語は本明細書では互換的に用いられ、前記は、ペプチド結合または改変ペプチド結合(すなわちペプチド同配体)によって互いに結合された2つ以上のアミノ酸を含むポリマーを意味する。ポリペプチドは、短い鎖(通常ペプチド、糖ペプチドまたはオリゴマーと称される)およびより長い鎖(一般的にタンパク質と称される)の両方を指す。ポリペプチドは、20遺伝子によってコードされるアミノ酸以外のアミノ酸を含むことができる。ポリペプチドには、天然のプロセス(例えば翻訳後プロセッシング)によって、または化学的改変技術(当業界で周知である)によって改変されたアミノ酸配列が含まれる。そのような改変は、基礎的な教本およびより詳細にはモノグラフとともに膨大な研究論文に良く記載されている。
本明細書で用いられるように、“別々”の治療的使用という用語は、少なくとも2つの活性な成分を異なるルートで同じ時にまたは実質的に同じ時に投与することを指す。
本明細書で用いられるように、“逐次的な”治療的使用という用語は、少なくとも2つの活性成分を異なる時に投与することを指し、投与ルートは同一または相違する。より具体的には、逐次的使用は、当該複数の活性成分の1つの完全な投与が、1つまたは複数の他方の投与の開始前であることを指す。したがって、当該複数の活性成分の1つを、他方の1つまたは複数の活性成分を投与する前に、数分、数時間または数日にわたって投与することが可能である。この事例では、同時治療は存在しない。
本明細書で用いられるように、“特異的に結合する”とは、もう1つの分子(例えば抗原)を認識および結合するが、他の分子を実質的に認識および結合しない分子(例えば抗体またはその抗原結合フラグメント)を指す。本明細書で用いられるように、“特異的結合”、“~と特異的に結合する”または個々の分子(例えばポリペプチドまたはポリペプチド上のエピトープ)に対して“特異的”であるという用語は、例えば、それが結合する分子に対して約10-4 M、10-5 M、10-6 M、10-7 M、10-8 M、10-9 M、10-10 M、10-11 M、または10-12 MのKdを有する分子によって提示され得る。“特異的に結合する”という用語はまた、分子(例えば抗体またはその抗原結合フラグメント)が、個々のポリペプチド(例えばL1-CAMポリペプチド)または個々のポリペプチド上のエピトープと結合し、任意の他のポリペプチドまたはポリペプチドエピトープとは実質的に結合しない結合を指すことができる。
本明細書で用いられるように、“治療薬剤”という用語は、有効量で存在するとき、所望の治療効果をその必要がある対象動物で生じる化合物を意味することが意図される。
本明細書で用いられる“治療する”または“治療”は、本明細書に記載する疾患または異常の対象動物(例えば人間)における治療をカバーし、治療は以下を含む:(i)疾患または異常の防止、すなわちその発生の停止;(ii)疾患または異常の緩和、すなわち当該異常の沈静を引起す;(iii)異常の進行の速度低下;および/または(iv)疾患または異常の1つ以上の症候の防止、緩和、または進行の速度低下。いくつかの実施態様では、治療は、当該疾患に関連する症候が、例えば緩和され、軽減され、治癒され、または緩解状態に置かれることを意味する。
本明細書に記載する異常の多様な治療態様が“実質的”を意味することを意図することは理解されよう。前記は完全な治療を含むが完全に満たない治療もまた含み、その場合には、いくつかの生物学的にまたは医学的に関連する成果が達成される。治療は、慢性的疾患に対する持続的な長期治療であっても、または急性症状の治療のための1回または数回の実施であってもよい。
L1-CAMは、粘着分子、免疫グロブリンスーパーファミリー(IgSF CAM)の一部分のL1ファミリーのメンバーであり、軸索誘導、神経細胞遊走および分化に必要とされる。L1ファミリーには、L1-CAM(CD171)、L1-CAM(CHL1)の近縁ホモログ、ニューロファシンおよびNgCAM関係細胞粘着分子(NR-CAM)が含まれる。これらのタンパク質は、ニューロン(特にそれらの軸索上で)および神経膠細胞(例えばシュワン細胞)で発現される。L1-CAMは神経細胞粘着分子であり、中枢神経系の発達に必要とされる。L1-CAMは28個のエクソンおよび27個のイントロンから構成されており、その遺伝子生成物の分子量は200から220kDaの範囲である(Coutelle O et al., Gene 208:7-15, 1998)。細胞外ドメイン(ECM、エクソン1からエクソン24)は6つのIg様ドメイン(図1)および5つのフィブロネクチン様ドメインを有し、第一のフィブロネクチンドメインにN-グリコシル化を有する。RGDモチーフが6番目のIg様ドメインに存在する。ECMは同種親和性結合に関与し(図2)、FGFRと相同領域を共有する。細胞質ドメインは、5つの潜在的なホスホセリン残基を含み、細胞骨格、第二のメッセンジャー経路およびキナーゼと相互作用することができる。2つのエクソン(2および27)はまた別にスプライシングされる(Coutelle O et al., Gene 208:7-15, 1998)。
L1-CAMは通常は神経組織で見出され(図3)、一方、癌細胞を含む非神経細胞はもっぱらエクソン2および27を欠く変種を発現する。エクソン2(YEGHHV、N-末端Ig1ドメインをコードする)は、in vitroでの同種親和性L1-L1結合のために重要であり、異種親和性リガンドとの最適な結合に要求される。エクソン27(細胞質テール)によってコードされるRSLE含有L1-CAMは、L1Δ(RSLE)よりも2-3倍速く内在化される。RSLE依存エンドサイトーシスは、L1-CAMの表面密度調節のためのメカニズムであり、前記は順に神経突起および細胞接着を制御する。卵巣癌腫細胞株はもっぱらL1-CAMΔをin vitroで発現する。L1-CAMによるERK活性化は、エクソン27によって媒介されるL1-CAMのエンドサイトーシスを要求する。これらの異なるスプライス変種は、癌の細胞学において異なるまたは対立的ですらある機能を有するかもしれない。
卵巣癌腫上のL1-CAMは、腹膜の内壁を形成する中皮細胞上のニューロピリン-1と結合し、中皮細胞と腫瘍との間の相互シグナリングによって腫瘍増殖を誘発する。L1-CAMの非神経アイソフォームの発現は、異なる腫瘍タイプを起原とする17腫瘍細胞株のうち16で見出される(Shtutman M et al., Cancer Res 66:11370-80, 2006)。非神経L1-CAMのノックダウンは、乳癌細胞株MCF-7で接着結合を破壊し、β-カテニン転写活性を増加させる。完全長L1-CAMは、ADAM10およびプレセニリン/γ-セクレターゼによる連続切断を受け、前記事象はL1-CAMのC-末端フラグメントが遺伝子調節のために核へ移動する前に生じる。L1-CAMの6番目のIgドメインに位置するRGD結合部位は核内シグナリングのために重要であるように思われる。
L1-CAMのその可溶形(sL1-CAM)へのメタロプロテイナーゼ媒介エクトドメイン切離しは生理学的な結果を有する。sL1-CAMは血管形成を媒介し、これはおそらくRGDモチーフを介してインテグリンを繋ぐことによる。sL1-CAMは、分裂増殖、マトリゲル侵襲、ウシ大動脈内皮細胞の管形成、および血管形成促進活性を誘発する。sL1-CAMはいくつかのインテグリンのためのリガンドであり、細胞外マトリックスに沈積され得る。L1-CAMの細胞質ドメインは、基部切離しおよびアンキリン結合部位を介する細胞骨格との連合を調節する。卵巣癌腫細胞株のL1-CAMのエキソソーム保持構成的切断生成物が、卵巣癌患者の腹水および血清で見出され得る。L1-CAMはまた血管の吸収および転移性成長を脳転移モデルで媒介することができる。組織プラスミンはL1-CAMを破壊し、それによって転移プロセスを停止させる。腫瘍由来抗プラスミノーゲン、ニューロセルピンは、L1-CAMのプラスミン媒介破壊または膜結合星状細胞性FasL(癌細胞のためのパラクリン死シグナル)の放出を防ぐことができる。
L1-CAMはまた化学物質耐性に必要とされる。例えば、L1-CAMを発現する卵巣癌腫細胞は、アポトーシスに対しより耐性であり、前記は部分的には抗アポトーシス分子Bcl-2を介する。L1-CAM(+) HEK-293細胞では、L1-CAMはERK、FAKおよびPAKリン酸化を媒介する。シスプラチン耐性のために選別された細胞株はL1-CAM発現をアップレギュレートし、そのノックダウンは感受性を回復させる。
L1-CAMを指向する既存抗体:chCE7は、腎臓の癌腫細胞上のヒトL1-CAMの6番目のIg様ドメイン(RGDモチーフを有する)と結合し(図1)、ヒト神経芽細胞腫の細胞によって内在化される(Meli ML et al., Int J Cancer 83:401-8, 1999;Novak-Hofer I et al., Int J Cancer 57:427-432, 1994)。他のモノクローナル抗体もまた報告されている:5G3、A10-A3、UJ127、L1-14.10、MAB777(R&D systems Inc., Minneapolis, MN)、および0.N.378 (U.S Biological Life Sciences, Salem, MA)、前記は多様なエピトープ域および親和性を示す(図5)。しかしながら、種々のエピトープを指向するこれらのL1-CAM抗体の各々のin vitroおよびin vivo特性の系統的な評価は未だ実施されず、それらの臨床的影響は不明のままである。多くの抗L1-CAM抗体(例えばchCE7)が、抗体依存細胞媒介細胞傷害(ADCC)の惹起に関して有効ではない。いくつかの抗L1-CAM抗体は、患者の内部で望ましくない免疫原性応答を潜在的に誘発し得る。
本技術は、抗L1-CAM免疫グロブリン関係組成物(例えば抗L1-CAM抗体またはその抗原結合フラグメント)の作出および使用のための方法および組成物を記載する。本開示の抗L1-CAM免疫グロブリン関係組成物は、L1-CAM陽性癌の診断または治療で有用であり得る。本技術の範囲内の抗L1-CAM免疫グロブリン関係組成物には、モノクローナル抗体、キメラ抗体、ヒト化抗体、およびジアボディ(ただしそれらに限定されない)が含まれ、前記は、標的ポリペプチド、ホモローグ、誘導体またはそのフラグメントに特異的に結合する。本開示はまた、本明細書に開示する抗L1-CAM抗体のいずれかの抗原結合フラグメントを提供し、ここで当該抗原結合フラグメントは、Fab、F(ab)'2、Fab’、scFvおよびFvから成る群から選択される。
ある特徴では、本技術は抗体またはその抗原結合フラグメントを提供し、前記は重鎖免疫グロブリン可変ドメイン(VH)および軽鎖免疫グロブリン可変ドメイン(VL)を含み、ここで、(a)VHは、GYTFTSYWMQのVH-CDR1配列(配列番号:53)、EINPSNGRTNYNEMFKSのVH-CDR2配列(配列番号:54)、およびYDGYYAMDYのVH-CDR3配列(配列番号:55)を含み、および/または(b)VLは、KSSQSLLYSSNQKNYLAのVL-CDR1配列(配列番号:56)、WASTRESのVL-CDR2配列(配列番号:57)、およびQQYHSYPFTのVL-CDR3配列(配列番号:58)を含む。抗体または抗原結合フラグメントのいくつかの実施態様では、VHは配列番号:1のアミノ酸配列を含み、VLは配列番号:3のアミノ酸配列を含む。加えて或いはまた別に、いくつかの実施態様では、抗体はさらにまた任意のアイソタイプのFcドメインを含み、前記アイソタイプは、例えばIgG(IgG1、IgG2、IgG3、およびIgG4を含む)、IgA(IgA1およびIgA2を含む)、IgD、IgEまたはIgMおよびIgYである(ただしこれらに限定されない)。定常領域配列の非限定的な例に以下が含まれる:
APTKAPDVFPIISGCRHPKDNSPVVLACLITGYHPTSVTVTWYMGTQSQPQRTFPEIQRRDSYYMTSSQLSTPLQQWRQGEYKCVVQHTASKSKKEIFRWPESPKAQASSVPTAQPQAEGSLAKATTAPATTRNTGRGGEEKKKEKEKEEQEERETKTPECPSHTQPLGVYLLTPAVQDLWLRDKATFTCFVVGSDLKDAHLTWEVAGKVPTGGVEEGLLERHSNGSQSQHSRLTLPRSLWNAGTSVTCTLNHPSLPPQRLMALREPAAQAPVKLSLNLLASSDPPEAASWLLCEVSGFSPPNILLMWLEDQREVNTSGFAPARPPPQPGSTTFWAWSVLRVPAPPSPQPATYTCVVSHEDSRTLLNASRSLEVSYVTDHGPMK
ヒトIgG1定常領域、Uniprot:P01857(配列番号:60)
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
ヒトIgG2定常領域、Uniprot:P01859(配列番号:61)
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSNFGTQTYTCNVDHKPSNTKVDKTVERKCCVECPPCPAPPVAGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTFRVVSVLTVVHQDWLNGKEYKCKVSNKGLPAPIEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDISVEWESNGQPENNYKTTPPMLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
ヒトIgG3定常領域、Uniprot:P01860(配列番号:62)
ASTKGPSVFPLAPCSRSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYTCNVNHKPSNTKVDKRVELKTPLGDTTHTCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCPRCPEPKSCDTPPPCPRCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVQFKWYVDGVEVHNAKTKPREEQYNSTFRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKTKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESSGQPENNYNTTPPMLDSDGSFFLYSKLTVDKSRWQQGNIFSCSVMHEALHNRFTQKSLSLSPGK
ヒトIgM定常領域、Uniprot:P01871(配列番号:63)
GSASAPTLFPLVSCENSPSDTSSVAVGCLAQDFLPDSITLSWKYKNNSDISSTRGFPSVLRGGKYAATSQVLLPSKDVMQGTDEHVVCKVQHPNGNKEKNVPLPVIAELPPKVSVFVPPRDGFFGNPRKSKLICQATGFSPRQIQVSWLREGKQVGSGVTTDQVQAEAKESGPTTYKVTSTLTIKESDWLGQSMFTCRVDHRGLTFQQNASSMCVPDQDTAIRVFAIPPSFASIFLTKSTKLTCLVTDLTTYDSVTISWTRQNGEAVKTHTNISESHPNATFSAVGEASICEDDWNSGERFTCTVTHTDLPSPLKQTISRPKGVALHRPDVYLLPPAREQLNLRESATITCLVTGFSPADVFVQWMQRGQPLSPEKYVTSAPMPEPQAPGRYFAHSILTVSEEEWNTGETYTCVAHEALPNRVTERTVDKSTGKPTLYNVSLVMSDTAGTCY
ヒトIgG4定常領域、Uniprot:P01861(配列番号:64)
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPSCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK
ヒトIgA1定常領域、Uniprot:P01876(配列番号:65)
ASPTSPKVFPLSLCSTQPDGNVVIACLVQGFFPQEPLSVTWSESGQGVTARNFPPSQDASGDLYTTSSQLTLPATQCLAGKSVTCHVKHYTNPSQDVTVPCPVPSTPPTPSPSTPPTPSPSCCHPRLSLHRPALEDLLLGSEANLTCTLTGLRDASGVTFTWTPSSGKSAVQGPPERDLCGCYSVSSVLPGCAEPWNHGKTFTCTAAYPESKTPLTATLSKSGNTFRPEVHLLPPPSEELALNELVTLTCLARGFSPKDVLVRWLQGSQELPREKYLTWASRQEPSQGTTTFAVTSILRVAAEDWKKGDTFSCMVGHEALPLAFTQKTIDRLAGKPTHVNVSVVMAEVDGTCY
ひとIgA2定常領域、Uniprot:P01877(配列番号:66)
ASPTSPKVFPLSLDSTPQDGNVVVACLVQGFFPQEPLSVTWSESGQNVTARNFPPSQDASGDLYTTSSQLTLPATQCPDGKSVTCHVKHYTNPSQDVTVPCPVPPPPPCCHPRLSLHRPALEDLLLGSEANLTCTLTGLRDASGATFTWTPSSGKSAVQGPPERDLCGCYSVSSVLPGCAQPWNHGETFTCTAAHPELKTPLTANITKSGNTFRPEVHLLPPPSEELALNELVTLTCLARGFSPKDVLVRWLQGSQELPREKYLTWASRQEPSQGTTTFAVTSILRVAAEDWKKGDTFSCMVGHEALPLAFTQKTIDRMAGKPTHVNVSVVMAEVDGTCY
ヒトIgカッパ定常領域、Uniprot:P01834(配列番号:67)
TVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
別の特徴では、本開示は、単離された免疫グロブリン関係組成物(例えば抗体またはその抗原結合フラグメント)を提供し、前記は、以下の重鎖(HC)アミノ酸配列またはその変種(1つ以上の保存的アミノ酸置換を有する)を含む:
QVQLVQPGDELVKPGASVKLSCKASGYTFTSYWMQWVKQRPGQGLEWIGEINPSNGRTNYNEMFKSKAVLSVDKSVSTAYMQLSSLTAEDTAVYYCALYDGYYAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:9)(huE71-H1);
QVQLVQSGSELKKPGASVKLSCKASGYTFTSYWMQWVRQAPGQGLEWIGEINPSNGRTNYNEMFKSRAVLSVDTSVSTAYMQLCSLKAEDTAVYYCALYDGYYAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:10)(huE71-H2);
QVQLVQPGAEVVKPGASVKLSCKASGYTFTGYWMHWVKQAPGQGLEWIGEINPSNGRTNYNERFKSKATLTVDKSITTAFMELSRLRSDDTAVYFCARDYYGTSYNFDYWGQGTLLTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:17)(huE72-H1);
QVQLVQPGAEVKKPGASVKLSCKASGYTFTGYWMHWVRQAPGQGLEWIGEINPSNGRTNYNERFKSRATLTVDKSISTAYMELSRLRSDDTAVYFCARDYYGTSYNFDYWGQGTLLTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:18)(huE72-H2);
QVQLQQPGDELVKPGASVKLSCKASGYTFTSYWMQWVKQRPGQGLEWIGEINPSNGRTNYNEMFKSKATLTVDKSSSTAYMQLSSLTSEDSAVYYCALYDGYYAMDYWGQGTSVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:26)(chE71-IgG1);
QVQLQQPGDELVKPGASVKLSCKASGYTFTSYWMQWVKQRPGQGLEWIGEINPSNGRTNYNEMFKSKATLTVDKSSSTAYMQLSSLTSEDSAVYYCALYDGYYAMDYWGQGTSVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:30)(chE72-IgG1);
QVQLQQPGDELVKPGASVKLSCKASGYTFTSYWMQWVKQRPGQGLEWIGEINPSNGRTNYNEMFKSKATLTVDKSSSTAYMQLSSLTSEDSAVYYCALYDGYYAMDYWGQGTSVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPSCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK(配列番号:42)(chE71-IgG4);
QVQLVQPGDELVKPGASVKLSCKASGYTFTSYWMQWVKQRPGQGLEWIGEINPSNGRTNYNEMFKSKAVLSVDKSVSTAYMQLSSLTAEDTAVYYCALYDGYYAMDYWGQGTLVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPSCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK(配列番号:46)(huE71-IgG4);
QVQLVQPGDELVKPGASVKLSCKASGYTFTSYWMQWVKQRPGQGLEWIGEINPSNGRTNYNEMFKSKAVLSVDKSVSTAYMQLSSLTAEDTAVYYCALYDGYYAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCAVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:49)(huE71-BsAb);
QVQLVQPGAEVVKPGASVKLSCKASGYTFTGYWMHWVKQAPGQGLEWIGEINPSNGRTNYNERFKSKATLTVDKSITTAFMELSRLRSDDTAVYFCARDYYGTSYNFDYWGQGTLLTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKRVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYASTYRVVSVLTVLHQDWLNGKEYKCAVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(配列番号:51)(huE72-BsAb)。
DIVMTQSPSSLAVSVGERVTMSCKSSQSLLYSSNQKNYLAWYQQKPGQSPKLLIYWASTRESGVPDRFSGSGSGTDFTLTISSVKAEDVALYYCQQYHSYPFTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:13)(huE71-L1)、
DIVMTQSPDSLAVSLGERVTMNCKSSQSLLYSSNQKNYLAWYQQKPGQPPKLLIYWASTRESGVPDRFSGSGSGTDFTLTISSLQAEDVALYYCQQYHSYPFTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:14)(huE71-L2)、
DIQMTQSSSSFSVSVGDRVTITCKANEDINNRLAWYQQKPGKSPRLLISGATNLVTGVPSRFSGSGSGTDYTLTISSLQAEDFATYYCQQYWSTPFTFGQGTELEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:21)(huE72-L1)、
DIQMTQSPSSLSVSVGDRVTITCKANEDINNRLAWYQQKPGKAPKLLISGATNLVTGVPSRFSGSGSGTDYTLTISSLQPEDFATYYCQQYWSTPFTFGQGTELEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:22)(huE72-L2)、
DIVMSQSPSSLAVSVGEKVTMSCKSSQSLLYSSNQKNYLAWYQQKPGQSPKLLIYWASTRESGVPDRFTGSGSGTDFTLTISSVKAEDLALYYCQQYHSYPFTFGSGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:25)(chE71-IgG1軽鎖)、
DIQMTQSSSSFSVSLGDRVTITCKANEDINNRLAWYQQTPGNSPRLLISGATNLVTGVPSRFSGSGSGKDYTLTITSLQAEDFATYYCQQYWSTPFTFGSGTELEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:29)(chE72 IgG1-軽鎖)、
DIVMSQSPSSLAVSVGEKVTMSCKSSQSLLYSSNQKNYLAWYQQKPGQSPKLLIYWASTRESGVPDRFTGSGSGTDFTLTISSVKAEDLALYYCQQYHSYPFTFGSGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:41)(chE71-IgG4軽鎖)、
DIVMTQSPSSLAVSVGERVTMSCKSSQSLLYSSNQKNYLAWYQQKPGQSPKLLIYWASTRESGVPDRFSGSGSGTDFTLTISSVKAEDVALYYCQQYHSYPFTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(配列番号:45)(huE71-IgG4軽鎖)
DIVMTQSPSSLAVSVGERVTMSCKSSQSLLYSSNQKNYLAWYQQKPGQSPKLLIYWASTRESGVPDRFSGSGSGTDFTLTISSVKAEDVALYYCQQYHSYPFTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGECTSGGGGSGGGGSGGGGSQVQLVQSGGGVVQPGRSLRLSCKASGYTFTRYTMHWVRQAPGKCLEWIGYINPSRGYTNYNQKFKDRFTISRDNSKNTAFLQMDSLRPEDTGVYFCARYYDDHYSLDYWGQGTPVTVSSGGGGSGGGGSGGGGSGGGGSGGGGSGGGGSDIQMTQSPSSLSASVGDRVTITCSASSSVSYMNWYQQTPGKAPKRWIYDTSKLASGVPSRFSGSGSGTDYTFTISSLQPEDIATYYCQQWSSNPFTFGCGTKLQITR(配列番号:50)(huE71-BsAb軽鎖-huOKT3scFv)、
DIQMTQSPSSLSVSVGDRVTITCKANEDINNRLAWYQQKPGKAPKLLISGATNLVTGVPSRFSGSGSGTDYTLTISSLQPEDFATYYCQQYWSTPFTFGQGTELEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGECTSGGGGSGGGGSGGGGSQVQLVQSGGGVVQPGRSLRLSCKASGYTFTRYTMHWVRQAPGKCLEWIGYINPSRGYTNYNQKFKDRFTISRDNSKNTAFLQMDSLRPEDTGVYFCARYYDDHYSLDYWGQGTPVTVSSGGGGSGGGGSGGGGSGGGGSGGGGSGGGGSDIQMTQSPSSLSASVGDRVTITCSASSSVSYMNWYQQTPGKAPKRWIYDTSKLASGVPSRFSGSGSGTDYTFTISSLQPEDIATYYCQQWSSNPFTFGCGTKLQITR(配列番号:52)(huE72-BsAb軽鎖-huOKT3scFv)、
免疫グロブリン関係組成物の上記実施態様のいずれでも、HCおよびLC免疫グロブリン可変ドメイン配列は、L1-CAMポリペプチドのエピトープと結合する抗原結合部位を形成し、前記エピトープは、L1-CAMの2番目のIg様ドメイン(配列番号:74)またはL1-CAMの6番目のIg様ドメイン(配列番号:75)の連続する少なくとも5から8アミノ酸残基を含む。いくつかの実施態様では、エピトープは立体構造エピトープである。
いくつかの実施態様では、HCおよびLC免疫グロブリン可変ドメイン配列は、同じポリペプチド鎖の成分である。他の実施態様では、HCおよびLC免疫グロブリン可変ドメイン配列は、異なるポリペプチド鎖の成分である。ある種の実施態様では、抗体は完全長抗体である。
ある種の実施態様では、免疫グロブリン関係組成物は以下の特徴の1つ以上を含む:(a)軽鎖免疫グロブリン可変ドメイン配列は、配列番号:13、14、21、22、25、29、41、45、50または52のいずれか1つに存在する軽鎖免疫グロブリン可変ドメイン配列と少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%同一である;および/または(b)重鎖免疫グロブリン可変ドメイン配列は、配列番号: 9、10、17、18、26、30、42、46、49および51のいずれか1つに存在する重鎖免疫グロブリン可変ドメイン配列と少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%同一である。別の特徴では、本明細書で提供する免疫グロブリン関係組成物の1つ以上のアミノ酸残基は、別のアミノ酸で置換される。置換は、本明細書で定義する“保存的置換”であり得る。
いくつかの実施態様では、免疫グロブリン関係組成物は以下を含む:(a)配列番号:13、14、21、22、25、29、41、45、50または52のいずれか1つに存在するLC配列と少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%同一であるLC配列、および/または(b)配列番号: 9、10、17、18、26、30、42、46、49および51のいずれか1つに存在するHC配列と少なくとも80%、少なくとも85%、少なくとも90%、少なくとも95%、または少なくとも99%同一であるHC配列。
ある種の実施態様では、免疫グロブリン関係組成物はIgG1定常領域を含み、前記領域は、N297AおよびK322Aから成る群から選択される1つ以上のアミノ酸置換を含む。加えて或いはまた別に、いくつかの実施態様では、免疫グロブリン関係組成物は、S228P変異を含むIgG4定常領域を含む。
ある特徴では、本技術は、本明細書に記載する免疫グロブリン関係組成物の重鎖または軽鎖をコードする核酸配列を提供する。本明細書に記載する抗体のいずれかをコードする組換え核酸配列もまた開示される。いくつかの実施態様では、核酸配列は、配列番号:11、12、15、16、19、20、23、24、27、28、31、32、43、44、47および48から成る群から選択される。別の特徴では、本技術は、本明細書に記載する免疫グロブリン関係組成物の重鎖または軽鎖をコードする任意の核酸配列を発現する宿主細胞を提供する。
本技術の免疫グロブリン関係組成物はさらにまた、異種ポリペプチドとN-またはC-末端で組換えにより融合されるか、或いは化学的にポリペプチドまたは他の組成物と複合体化される(共有結合および非共有結合による複合体化を含む)。例えば、本技術の免疫グロブリン関係組成物は、検出アッセイの標識として有用な分子、およびエフェクター分子(例えば異種ポリペプチド、薬物、または毒素)と組換えにより融合または複合体化され得る。例えば以下を参照されたい:WO92/08495;WO91/14438;WO89/12624;U.S. Pat. No. 5,314,995;およびEP0 396 387。
薬剤および免疫グロブリン関係組成物上の官能基は直接的に結合させることができる。例えば、薬剤上の官能基(例えばスルフヒドリル基)を免疫グロブリン関係組成物上の官能基(例えばスルフヒドリル基)と結び付けて、ジスルフィドを形成することができる。また別に、官能基は架橋(すなわちリンカー)を介して結合させることができる。架橋剤のいくつかの例は下記に記載される。架橋を薬剤または免疫グロブリン関係組成物のどちらかに結合させることができる。複合体中の薬剤または免疫グロブリン関係組成物の数はまた、他方に存在する官能基の数によって制限される。例えば、複合体に結び付けられる薬剤の最大数は、免疫グロブリン関係組成物に存在する官能基の数に左右される。また別に、薬剤に結び付けられる免疫グロブリン関係組成物の最大数は、薬剤に存在する官能基数に左右される。
さらに別の実施態様では、複合体は、1つの薬剤に結び付けられた1つの免疫グロブリン関係組成物を含む。ある実施態様では、複合体は、少なくとも1つの免疫グロブリン関係組成物に化学的に結合された(例えば複合体化された)少なくとも1つの薬剤を含む。薬剤は、当業者に公知の任意の方法によって免疫グロブリン関係組成物に化学的に結合され得る。例えば、薬剤上の官能基を免疫グロブリン関係組成物上の官能基に直接的に結合させることができる。適切な官能基のいくつかの例には、例えばアミノ、カルボキシル、スルフヒドリル、マレイミド、イソシアネート、イソチオシアネートおよびヒドロキシルが含まれる。
また別には、薬剤および免疫グロブリン関係組成物上の官能基は同じものであり得る。同種二官能性架橋剤は、典型的には同一官能基を架橋するために用いられる。同種二官能性架橋剤の例には以下が含まれる:EGS(すなわちエチレングリコビス[スクシンイミジルスクシネート])、DSS(すなわちジスクシンイミジルスベレート)、DMA(すなわちアジプイミド酸ジメチル2HCl)、DTSSP(すなわち3,3'-ジチオビス[スルホスクシンイミジルプロピオネート])、DPDPB(すなわち1,4-ジ-[3'-(2'-ピリジルジチオ)-プロピオンアミド]ブタン)およびBMH(すなわちビス-マレイミドヘキサン)。そのような同種二官能性架橋剤もまたピアースバイオテクノロジー社から入手できる。
別の実施態様では、複合体は、少なくとも1つの免疫グロブリン関係組成物に物理的に結合された少なくとも1つの薬剤を含む。当業者に公知の任意の方法を利用して、免疫グロブリン関係組成物に薬剤を物理的に結合させることができる。例えば、当業者に公知の任意の方法によって、免疫グロブリン関係組成物および薬剤を一緒に混合することができる。混合の順番は重要ではない。例えば、当業者に公知の任意の方法によって、薬剤を免疫グロブリン関係組成物と物理的に混合することができる。例えば、免疫グロブリン関係組成物および薬剤を容器に入れ、例えば容器を振盪することによって攪拌し、免疫グロブリン関係組成物および薬剤を混合することができる。
免疫グロブリン関係組成物は、当業者に公知の任意の方法によって改変され得る。例えば、上記に記載の架橋剤または官能基の手段によって免疫グロブリン関係組成物を改変することができる。
概論:先ず初めに、本技術の抗体を惹起する標的ポリペプチドが選択される。例えば、抗体は、完全長のL1-CAMに対して、または6つのIg様ドメインおよび5つのフィブロネクチンドメインを含むL1-CAMタンパク質の細胞外ドメイン(図1参照)の部分に対して惹起することができる。そのような標的ポリペプチドに対する抗体を作出する技術は当業者には周知である。そのような技術の例には、例えば、ディスプレーライブラリー(異種またはヒト)、マウスハイブリドーマなどを必要とするものが含まれるが、ただし前記に限定されない。本技術の範囲内の標的ポリペプチドには、免疫応答を誘発することができる、細胞外ドメインを含むL1-CAMタンパク質に由来する任意のポリペプチドが含まれる。L1-CAMタンパク質に特異的な抗体の調製は実施例1、2および5に例示される。
組換え操作された抗体および抗体フラグメント、例えば抗体関係ポリペプチド(前記はL1-CAMタンパク質およびそのフラグメントを指向する)が、本開示にしたがって使用されるために適切であることは理解されよう。
本明細書に示す技術に付すことができる抗L1-CAM抗体には、モノクローナル抗体およびポリクローナル抗体、並びに抗体フラグメント、例えばFab、Fab′、F(ab′)2、Fd、scFv、ジアボディ、抗体軽鎖、抗体重鎖、および/または抗体フラグメントが含まれる。抗体Fv含有ポリペプチド(例えばFab′ and F(ab′)2抗体フラグメント)の高収量生成に有用な方法が報告されている。米国特許5,648,237号を参照されたい。
一般的には、抗体を元の種から入手する。より具体的には、標的ポリペプチドに対して特異性を有する、元の種の抗体の軽鎖、重鎖または両鎖の可変部分の核酸またはアミノ酸配列を入手する。元の種は、本技術の抗体または抗体ライブラリーを作出するために有用な任意の種(例えばラット、マウス、ウサギ、ニワトリ、サル、ヒトなど)である。
ファージまたはファージミドディスプレー技術が、本技術の抗体の誘導のために有用な技術である。モノクローナル抗体の作出およびクローニングのための技術は当業者には周知である。本技術の抗体をコードする配列の発現は大腸菌(E. coli)で実施できる。
完全長L1-CAMタンパク質またはそのフラグメントは、フラグメントとして免疫原として有用である。いくつかの実施態様では、L1-CAMフラグメントは、アミノ酸配列
PKETVKPVEVEEGESVVLPCNPPPSAEPLRIYWMNSKILHIKQDERVTMGQNGNLYFANVLTSDNHSDYICHAHFPGTRTIIQKEPID(配列番号:74)(L1-CAMのIg様C2型2ドメイン)、または
TQITQGPRSTIEKKGSRVTFTCQASFDPSLQPSITWRGDGRDLQELGDSDKYFIEDGRLVIHSLDYSDQGNYSCVASTELDVVESRAQLL(配列番号:75)(L1-CAMのIg様C2型6ドメイン)の連続する5から8つのアミノ酸残基を含み、さらに、当該ペプチドに対して生じる抗体が、L1-CAMとの特異的な免疫複合体を形成するようにL1-CAMタンパク質のエピトープを包含する。
いくつかの実施態様では、2番目または6番目のIg様ドメインとオーバーラップする抗原性L1-CAMペプチドは、少なくとも5、8、10、15、20、または30アミノ酸残基を含む。より長い抗原性ペプチドが、短い抗原性ペプチドよりも時には所望され、用途および当業界で周知の方法次第である。時には与えられるエピトープのマルチマーがモノマーよりも有効である。
必要な場合には、L1-CAMタンパク質(またはそのフラグメント)の免疫原性が、ハプテン(例えばキーホールリンペットヘモシアニン(KLH)または卵白アルブミン(OVA))との融合または複合体化によって増強される。多くのそのようなハプテンが当業界で公知である。さらにまた、L1-CAMタンパク質を通常のアジュバント(例えばフロイントの完全または不完全アジュバント)と組合わせて、当該ポリペプチドに対する対象動物の免疫反応を増強することができる。免疫学的応答を増強するために用いられる多様なアジュバントには、フロイントのアジュバント(完全および不完全)、鉱物ゲル(例えば水酸化アルミニウム)、表面活性物質(例えばリゾレシチン、プルロニックポリオール、多価陰イオン、ペプチド、油乳剤、ジニトロフェノールなど)、ヒトアジュバント(例えばカルメット-ゲラン桿菌およびコリネバクテリウム・パルブム(Corynebacterium parvum))、または類似の免疫刺激化合物が含まれるが、ただし前記に限定されない。
したがって、二次免疫応答は、例えば弱体化または減弱した既存の免疫応答を強化するために、或いは消失してしまったかまたはもはや検出できない以前の免疫応答を再現するために惹起され得る。二次またはメモリー免疫応答は、液性(抗体)応答または細胞性応答であり得る。二次またはメモリー液性応答は、抗原の最初の提示で生じたメモリーB細胞の刺激に際して発生する。遅延型過敏(DTH)反応は、細胞性二次またはメモリー免疫応答であり、CD4+ T細胞によって媒介される。抗原への最初の暴露は免疫系を始動させ、更なる暴露はDTHをもたらす。
適切な免疫に続いて、抗L1-CAM抗体を対象動物の血清から調製できる。所望される場合には、L1-CAMタンパク質に対する抗体分子を哺乳動物から(例えば血液から)単離し、IgG分画を得るために周知の技術(例えばポリペプチドAクロマトグラフィー)によってさらに精製できる。
一般的に、ディスプレーベクターでクローニングされるハイブリッド抗体またはハイブリッド抗体フラグメントは、良好な結合活性を維持する変種を識別するために適切な抗原に対して選別できる。なぜならば、抗体または抗体フラグメントは、ファージまたはファージ粒子の表面に存在するからである(例えば以下を参照されたい:Barbas III et al., Phage Display, A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 2001)。しかしながら、他のベクターフォーマットもこのプロセスに用いることができよう。例えば、選別および/またはスクリーニングのための溶解ファージベクター(改変T7またはラムダZap系)での抗体フラグメントライブラリーのクローニングである。
原核細胞におけるポリペプチドの発現はもっともしばしば大腸菌で実施され、融合または非融合ポリペプチドの発現を指令する構成的または誘導性プロモーターを含むベクターが用いられる。融合ベクターは、その中でコードされるポリペプチドに多数のアミノ酸を通常は当該組換えポリペプチドのアミノ末端に付加する。そのような融合ベクターは典型的には3つの目的のために働く:(i)組換えポリペプチドの発現を高める;(ii)組換えポリペプチドの溶解性を高める;および(iii)親和性精製のリガンドとして作用することによって、組換えポリペプチドの精製を助ける。融合発現ベクターでは、しばしばタンパク分解性切断部位が融合部分と組換えポリペプチドとの接点に導入されて、融合ポリペプチドの精製後に当該融合部分から組換えポリペプチドの分離を可能にする。そのような酵素およびそれらの同族認識配列には、第Xa因子、トロンビンおよびエンテロキナーゼが含まれる。典型的な融合発現ベクターには、pGEX(Pharmacia Biotech Inc; Smith and Johnson, 1988. Gene 67: 31-40)、pMAL(New England Biolabs, Beverly, Mass.)、およびpRIT5(Pharmacia, Piscataway, N.J.)が含まれ、前記では、それぞれ、グルタチオンS-トランスフェラーゼ(GST)、マルトースE結合ポリペプチド、またはポリペプチドAが標的組換えポリペプチドと融合する。
別の実施態様では、抗L1-CAM抗体発現ベクターは酵母発現ベクターである。酵母サッカロミセス・セレビシアエ(Saccharomyces cerevisiae)での発現用ベクターの例には、pYepSec1(Baldari, et al., 1987. EMBO J. 6: 229-234)、pMFa(Kurjan and Herskowitz, Cell 30: 933-943, 1982)、pJRY88(Schultz et al., Gene 54: 113-123, 1987)、pYES2(Invitrogen Corporation, San Diego, Calif.)、およびpicZ(Invitrogen Corp, San Diego, Calif.)が含まれる。また別には、抗L1-CAM抗体は、バキュロウイルス発現ベクターを用いて昆虫細胞で発現できる。昆虫細胞(例えばSF9細胞)でのポリペプチド(例えば抗L1-CAM抗体)の発現に利用できるバキュロウイルスベクターには、pAcシリーズ(Smith, et al., Mol. Cell. Biol. 3: 2156-2165, 1983)およびpVLシリーズ(Lucklow and Summers, 1989. Virology 170: 31-39)が含まれる。
別の実施態様では、組換え哺乳動物発現ベクターは、特定の細胞タイプで核酸の発現を指令する能力を有する(例えば組織特異的調節エレメント)。組織特異的調節エレメントは当業界で公知である。適切な組織特異的プロモーターの非限定的な例には、アルブミンプロモーター(肝臓特異的;Pinkert, et al., Genes Dev. 1: 268-277, 1987)、リンパ系特異的プロモーター(Calame and Eaton, Adv. Immunol. 43: 235-275, 1988)、T細胞受容体(Winoto and Baltimore, EMBO J. 8: 729-733, 1989)および免疫グロブリン(Banerji, et al., 1983. Cell 33: 729-740;Queen and Baltimore, Cell 33: 741-748, 1983)のプロモーター、ニューロン特異的プロモーター(例えば神経フィラメントプロモーター;Byrne and Ruddle, Proc. Natl. Acad. Sci. USA 86: 5473-5477, 1989)、膵臓特異的プロモーター(Edlund, et al., 1985. Science 230: 912-916)、並びに乳腺特異的プロモーター(例えば乳清プロモーター;米国特許4,873,316号および欧州特許公開No.264,166)が含まれる。発生に関して調節されるプロモーター、例えば、マウスHoxプロモーター(Kessel and Gruss, Science 249: 374-379, 1990)およびα-フェトプロテインプロモーター(Campes and Tilghman, Genes Dev. 3: 537-546, 1989)もまた包含される。
宿主細胞は任意の原核細胞または真核細胞であり得る。例えば、抗L1-CAM抗体は、細菌細胞(例えば大腸菌)、昆虫細胞、酵母または哺乳動物細胞で発現され得る。哺乳動物細胞は、免疫グロブリンまたはそのフラグメントをコードするヌクレオチドセグメントを発現するために適切な宿主である。以下を参照されたい:Winnacker, From Genes To Clones(VCH Publishers, NY, 1987)。無傷の異種タンパク質を分泌する能力を有する適切な多数の宿主細胞株が当業界で開発されてきた。前記には、チャイニーズハムスター卵巣(CHO)細胞株、多様なCOS細胞株、HeLa細胞、L細胞およびミエローマ細胞株が含まれる。いくつかの実施態様では、細胞は非ヒト細胞である。これらの細胞のための発現ベクターは、発現制御配列、例えば複製起点、プロモーター、エンハンサー、必要なプロセッシング情報部位、例えばリボソーム結合部位、RNAスプライス部位、ポリアデニル化部位、および転写終了配列を含むことができる(Queen et al., Immunol. Rev. 89: 49, 1986)。例示的な発現制御配列は、内因性遺伝子、サイトメガロウイルス、SV40、アデノウイルス、ウシパピローマウイルスなどに由来するプロモーターである(Co et al., J Immunol. 148: 1149, 1992)。他の適切な宿主細胞は当業者には公知である。
哺乳動物細胞の安定的トランスフェクションの場合、用いられる発現ベクターおよびトランスフェクション技術に応じて、小部分の細胞のみが外来DNAをそれらのゲノムに組み込むことができる。これら組込み体を識別および選別するために、一般的には選別可能なマーカー(例えば抗生物質耐性)をコードする遺伝子が、対象の遺伝子とともに宿主細胞に導入される。多様な選別可能マーカーには、薬物(例えばG418、ヒグロマイシンおよびメトトレキサート)に対する耐性を付与するものが含まれる。選別可能マーカーをコードする核酸は、抗L1-CAM抗体をコードするベクターと同じベクターで宿主細胞に導入されるか、または別々のベクターで導入され得る。導入核酸で安定的にトランスフェクトされた細胞は、薬物選別によって識別できる(例えば、選別可能マーカー遺伝子を取り込んだ細胞は生存し、一方、他の細胞は死滅する)。
抗L1-CAM抗体をコードするポリヌクレオチド(例えば抗L1-CAM抗体コード配列)をトランスジーンに取り込み、トランスジェニック動物のゲノムへ導入し、続いてトランスジェニック動物の乳中で発現させることができる。例えば、米国特許5,741,957号、5,304,489号、および5,849,992号を参照されたい。適切なトランスジーンには、軽および/または重鎖のためのコード配列が含まれ、前記コード配列は、乳腺特異的遺伝子(例えばカゼインまたはβ-ラクトグロビン)由来のプロモーターおよびエンハンサーに作動できるように連結される。トランスジェニック動物の作製のためには、トランスジーンを受精卵母細胞にマイクロインジェクトするか、または胚性幹細胞のゲノムにトランスジーンを取り込ませ、そのような細胞の核を脱核卵母細胞に移すことができる。
組換え抗L1-CAM抗体(例えばキメラおよびヒト化モノクローナル抗体)は、ヒトおよび非ヒトの両方の部分を含み、前記は標準的な組換えDNA技術を用いて作製でき、本技術の範囲内である。いくつかの使用のために(本技術の抗L1-CAM抗体の人間でのin vitro使用とともにin vitro検出アッセイでのこれら薬剤の使用を含む)、キメラまたはヒト化抗L1-CAM抗体を使用することができる。そのようなキメラおよびヒト化モノクローナル抗体は、当業界で公知の組換えDNA技術によって生成することができる。そのような有用な方法には例えば以下に記載される方法が含まれる(ただしそれらに限定されない):国際出願No. PCT/US86/02269;米国特許5,225,539号;欧州特許184187号;欧州特許171496号;欧州特許173494号;PCT国際公開WO86/01533;米国特許4,816,567号、5,225,539号;欧州特許125023号;Better, et al., 1988. Science 240: 1041-1043;Liu, et al., 1987. Proc. Natl. Acad. Sci. USA 84: 3439-3443;Liu, et al., 1987. J. Immunol. 139: 3521-3526;Sun, et al., 1987. Proc. Natl. Acad. Sci. USA 84: 214-218;Nishimura, et al., 1987. Cancer Res. 47: 999-1005;Wood, et al., 1985. Nature 314: 446-449;Shaw, et al., 1988. J. Natl. Cancer Inst. 80: 1553-1559;Morrison (1985) Science 229: 1202-1207;Oi, et al. (1986) BioTechniques 4: 214;Jones, et al., 1986. Nature 321: 552-525;Verhoeyan, et al., 1988. Science 239: 1534;Morrison, Science 229: 1202, 1985;Oi et al., BioTechniques 4: 214, 1986;Gillies et al., J. Immunol. Methods, 125: 191-202, 1989;米国特許5,807,715号;およびBeidler, et al., 1988. J. Immunol. 141: 4053-4060。例えば、抗体は以下を含む多様な技術を用いてヒト化され得る:CDR移植(EP0 239 400;WO91/09967;米国特許5,530,101号、5,585,089号、5,859,205号、6,248,516号;EP460167)、上張りまたは表面付け替え(EP0 592 106;EP0 519 596;Padlan E. A., Molecular Immunology, 28: 489-498, 1991;Studnicka et al., Protein Engineering 7: 805-814, 1994;Roguska et al., PNAS 91: 969-973, 1994)、および鎖のシャッフリング(米国特許5,565,332号)。ある実施態様では、Fc定常領域をコードする配列を特異的に除去するために選択した制限酵素を用いて、マウス抗L1-CAMモノクローナル抗体をコードするcDNAを消化し、ヒトFcをコードするcDNAの等価部分で置換する(以下を参照されたい:Robinson et al., PCT/US86/02269;Akira et al.,欧州特許出願184,187;Taniguchi, 欧州特許出願171,496;Morrison et al., 欧州特許出願173,494;Neuberger et al., WO86/01533;Cabilly et al.米国特許4,816,567号;Cabilly et al., 欧州特許出願125,023;Better et al. (1988) Science 240: 1041-1043;Liu et al. (1987) Proc. Natl. Acad. Sci. USA 84: 3439-3443;Liu et al. (1987) J Immunol 139: 3521-3526;Sun et al. (1987) Proc. Natl. Acad. Sci. USA 84: 214-218;Nishimura et al. (1987) Cancer Res 47: 999-1005;Wood et al. (1985) Nature 314: 446-449;およびShaw et al. (1988) J. Natl. Cancer Inst. 80: 1553-1559;米国特許6,180,370号;米国特許6,300,064号、6,696,248号、6,706,484号、6,828,422号。
ある実施態様では、本技術は、ヒト抗マウス抗体(本明細書では“HAMA”と称する)応答を誘発する可能性が低いがなお効率的な抗体エフェクター機能を有するヒト化抗L1-CAM抗体の構築を提供する。本明細書で用いられるように、抗体に関連して“ヒト”および“ヒト化”という用語は、治療的に耐え得る弱い免疫原性応答をヒト対象動物で誘発すると予想される任意の抗体に関する。ある実施態様では、本技術は、ヒト化された抗L1-CAM抗体、重軽鎖免疫グロブリンを提供する。
ハイブリッドは各フレームワーク領域に対応する複数の候補から選択して構築されるので多くの配列組合せが存在し、それら配列を本明細書に記載する原則にしたがって構築することは容易である。したがって、個々のフレームワーク領域の種々の組合せを有するメンバーを含むハイブリッドライブラリーを組み立てることができる。そのようなライブラリーは、配列コレクションの電子データベースであってもハイブリッドの物理的コレクションであってもよい。
本技術の二重特異性抗体(BsAb)および二重特異性抗体フラグメント(BsFab)は、例えばL1-CAMと特異的に結合する少なくとも1つのアーム、および第二の標的抗原と特異的に結合する少なくとも1つの他のアームを有する。いくつかの実施態様では、第二の標的抗原は、B細胞、T細胞、骨髄系細胞、形質細胞もしくは肥満細胞の抗原またはエピトープである。加えて或いはまた別に、ある種の実施態様では、第二の標的抗原は、CD3、CD4、CD8、CD20、CD19、CD21、CD23、CD46、CD80、HLA-DR、CD74、CD22、CD14、CD15、CD16、CD123、TCRガンマ/デルタ、NKp46およびKIRから成る群から選択される。ある種の実施態様では、BsAbは、細胞表面でL1-CAM抗原を発現する腫瘍細胞と結合する能力を有する。いくつかの実施態様では、BsAbは操作されて、細胞傷害性T細胞を腫瘍部位に向かわせる(動員する)ことによって腫瘍細胞の殺滅を促進する。他の例示的なBsAbには、L1-CAMに特異的な第一の抗原結合部位および小分子ハプテンに特異的な第二の抗原結合部位を有するものが含まれ、前記ハプテンは、例えばDTP A、IMP288、DOTA、DOTA-Bn、DOTA-デスフェリオキサミン、本明細書に記載する他のDOTA-キレート、ビオチン、フルオレセイン、または文献に記載されたもの(Goodwin, D A. et al, 1994, Cancer Res. 54(22):5937-5946)である。
BsAbを作製する最近の方法は追加のシステイン残基を含む操作された組換えモノクローナル抗体を含み、したがってそれらはより通常的な免疫グロブリンアイソタイプよりも強力に架橋する。例えば以下を参照されたい:FitzGerald et al., Protein Eng. 10(10):1221-1225, 1997。別のアプローチは、要求される二重特異性を有する2つ以上の異なる単鎖抗体または抗体フラグメントが連結された組換え融合タンパク質を操作することである。例えば以下を参照されたい:Coloma et al., Nature Biotech. 15:159-163, 1997。分子操作を用い、多様な二重特異性融合タンパク質を作製することができる。
いくつかの実施態様では、リンカーは、長さが少なくとも2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100または100を超えるアミノ酸である。いくつかの実施態様では、リンカーは、剛性の三次元構造を選択せず、むしろポリペプチド(例えば第一および/または第二の抗原結合部位)に可撓性を提供する傾向があるという特徴を有する。いくつかの実施態様では、リンカーは、BsAbに付与される特定の特性(例えば安定性の増強)を基準にして本明細書に記載するBsAbで用いられる。いくつかの実施態様では、本技術のBsAbはG4Sリンカー(配列番号:76)を含む。ある種のいくつかの実施態様では、本技術のBsAbは(G4S)nリンカーを含み、ここでnは1、2、3、4、5、6、7、8、9、10、11、12、13、14、15または15を超える(配列番号:78)。
いくつかの実施態様では、本技術の抗L1-CAM抗体は、活性化および/または阻害性受容体に対して改変された親和性を有し、1つ以上のアミノ酸改変を含むFc領域を有する。この場合、前記1つ以上のアミノ酸改変は、アラニンによるN297の置換またはアラニンによるK322の置換である。
いくつかの実施態様では、本技術の抗体は、対象の抗原(例えばL1-CAM)と結合する適切な参照抗体と対比して改変されたグリコシル化部位を有することができ、ただし抗体の機能性(例えば抗原との結合活性)に変化はない。本明細書で用いられるように、“グリコシル化部位”には、オリゴ糖(一緒に結合した1つ以上の単糖類を含む炭水化物)が特異的にかつ共有結合により結合する、抗体の任意の特異的なアミノ酸配列が含まれる。
オリゴ糖側鎖は、典型的には、N-またはO-結合を介して抗体の基本骨格に連結される。N-結合グリコシル化は、オリゴ糖部分とアスパラギン残基の側鎖との結合を指す。O-結合グリコシル化は、オリゴ糖部分とヒドロキシアミノ酸(例えばセリン、スレオニン)との結合を指す。例えば、ある種のオリゴ糖(フコースを含む)および末端のN-アセチルグルコサミンを欠くFc-糖型(huL1-CAM-IgGln)は特定のCHO細胞で生成され、強化されたADCCエフェクター機能を示すことができる。
いくつかの実施態様では、本明細書で開示する免疫グロブリン関係組成物の炭水化物含有量は、グリコシル化部位を付加または欠失させることによって改変される。抗体の炭水化物含有量を改変する方法は当業界で周知であり、本技術内に含まれる。例えば以下を参照されたい:米国特許6,218,149号;EP 0359096B1;米国特許公開US 2002/0028486;国際特許出願公開WO 03/035835;米国特許公開2003/0115614;米国特許6,218,149号;米国特許6,472,511号(前記のいずれも参照によってその全体が本明細書に含まれる)。いくつかの実施態様では、抗体(またはその該当部分もしくは成分)の炭水化物含有量は、抗体の1つ以上の内因性炭水化物部分を欠失させることによって改変される。ある種のいくつかの実施態様では、本技術は、297位をアスパラギンからアラニンに改変することによって、抗体のFc領域のグリコシル化部位を欠失させる工程を含む。
(IgGに起因する)ジスルフィド結合のダイマー構造を有する融合タンパク質は、モノマー型の分泌タンパク質またはタンパク質フラグメント単独と比較して、他の分子との結合および中和でより効率的であり得る(Fountoulakis et al., J. Biochem. 270: 3958-3964, 1995)。
同様に、EP-A-O 464 533(カナダの対応する特許公開2045869)は、免疫グロブリン分子定常領域の多様な部分を別のヒトタンパク質またはそのフラグメントとともに含む融合タンパク質を開示する。多くの事例で、融合タンパク質のFc部分は治療および診断で有益であり、したがって、例えば薬物動態学特性の改善をもたらすことができる(EP-A 0232 262参照)。また別に、融合タンパク質を発現、検出および精製した後で、Fc部分の欠失または改変を所望することが可能である。例えば、Fc部分は、融合タンパク質を免疫用抗原として用いる場合は治療および診断を妨害し得る。薬物発見では、高処理スクリーニングアッセイの目的で、ヒトタンパク質(例えばhIL-5)がFc部分と融合されて、hIL-5のアンタゴニストが識別された(Bennett et al., J. Molecular Recognition 8: 52-58, 1995;Johanson et al., J. Biol. Chem., 270: 9459-9471, 1995)。
標識は、当業界で公知の方法にしたがい所望のアッセイ成分に直接的または間接的に合体させることができる。上記に示したように、多種多様な標識を用いることができ、標識の選択は、複数の要因(例えば要求される感受性、化合物との複合体化の容易さ、安定性要求、利用可能な装置、および処分規定)に左右される。
非放射性標識はしばしば間接的手段によって付加される。一般的には、リガンド分子(例えばビオチン)は分子に共有結合される。続いてリガンドはアンチリガンド(例えばストレプトアビジン)分子と結合し、前記は、本来的に検出可能であるか、またはシグナル系(例えば検出可能酵素、蛍光化合物または化学発光化合物)と共有結合される。多数のリガンドおよびアンチリガンドを用いることができる。リガンドが天然のアンチリガンド(例えばビオチン、チロキシンおよびコルチゾール)を有する場合、前記リガンドを標識された天然に存在するアンチリガンドと一緒に用いることができる。また別には、任意のハプテン系または抗原性化合物を抗体(例えば抗L1-CAM抗体)と組合わせて用いることができる。
標識を検出する手段は当業者には周知である。したがって、例えば標識が放射性標識である場合、検出手段には、オートラジオグラフィーの場合のようなシンチレーション計数装置または写真撮影フィルムが含まれる。標識が蛍光標識の場合は、蛍光色素を適切な波長の光で励起し生じた蛍光を検出することによって標識を検出できる。蛍光は、写真撮影フィルムによって、電子的検出装置(電荷結合素子(CCD)または光電子増倍管など)によって視覚的に検出できる。同様に、酵素標識は、酵素に適切な基質を提供し生じた反応生成物を検出することによって検出できる。最後に、簡単な比色標識は、標識に付随する色を観察することによって簡単に検出できる。したがって、多様なディップスティックアッセイで、複合体化された金はしばしば桃色に見え、一方、多様な複合体化されたビーズはビーズの色に見える。
いくつかのアッセイフォーマットは標識成分の使用を必要としない。例えば、凝集アッセイを用いて標的抗体(例えば抗L1-CAM抗体)の存在を検出できる。この事例では、抗原被覆粒子が標的抗体を含むサンプルによって凝集される。このフォーマットでは、成分のいずれも標識する必要が無く、標識抗体の存在は簡単な目視精査によって検出される。
本技術の抗L1-CAM抗体を識別およびスクリーニングする方法:L1-CAMポリペプチドに対する抗体を、L1-CAMタンパク質に対する所望の特異性を保有するものについて識別およびスクリーニングするために有用な方法には、当業界で公知の任意の免疫学的媒介技術が含まれる。免疫応答成分は、当業者に周知の多様な方法によってin vitroで検出できる。例えば、(1)細胞傷害性Tリンパ球を放射能標識標的細胞とともにインキュベートし、これら標的細胞の溶解を放射能の放出によって検出することができる;(2)ヘルパーT細胞を抗原および抗原提示細胞とともにインキュベートし、サイトカインの合成および分泌を標準的な方法によって測定することができる(Windhagen A et al., Immunity, 2: 373-80, 1995);(3)抗原提示細胞をタンパク質抗原全体とともにインキュベートし、MHCでの当該抗原の提示をTリンパ球活性化アッセイまたは生物物理的方法によって検出することができる(Harding et al., Proc. Natl. Acad. Sci., 86: 4230-4, 1989);(4)肥満細胞をそれらのFc-イプシロン受容体と架橋する試薬とともにインキュベートし、ヒスタミン放出を酵素免疫アッセイによって測定することができる(Siraganian et al., TIPS, 4: 432-437, 1983);および(5)酵素結合免疫吸着アッセイ(ELISA)。
いくつかの実施態様では、本技術の抗L1-CAM抗体は、酵母宿主細胞表面のL1-CAMペプチドディスプレーを用いて選別される。酵母表面ディスプレーによるscFvポリペプチドの単離に有用な方法はKiekeらによって記載されている(Kieke et al., Protein Eng. 1997 Nov; 10(11): 1303-10)。
いくつかの実施態様では、本技術の抗L1-CAM抗体はリボソームディスプレーを用いて選別される。リボソームディスプレーを用いるペプチドライブラリーでリガンドを識別するために有用な方法は文献に記載されている(Mattheakis et al., Proc. Natl. Acad. Sci. USA 91: 9022-26, 1994;およびHanes et al., Proc. Natl. Acad. Sci. USA 94: 4937-42, 1997)。
ある種の実施態様では、本技術の抗L1-CAM抗体は、L1-CAMペプチドのtRNAディスプレーを用いて選別される。tRNAディスプレーを用いるリガンドのin vitro選別に有用な方法は、Merrymanらによって記載されている(Merryman et al., Chem. Biol., 9: 741-46, 2002)。
いくつかの実施態様では、本技術の抗L1-CAM抗体は、グラム陰性細菌のペリプラズムで発現され、標識L1-CAMタンパク質と混合される(WO02/34886を参照されたい)。L1-CAMタンパク質に親和性を有する組換えポリペプチドを発現するクローンで、抗L1-CAM抗体と結合する標識L1-CAMタンパク質の濃度は増加し、Harveyら(Proc. Natl. Acad. Sci. 22: 9193-98 2004)および米国特許公開No. 2004/0058403に記載されるように当該細胞がライブラリーの残りの細胞から単離されるのを可能にする。
所望の抗L1-CAM抗体の選別後、当業者に公知の任意の技術(例えば原核または真核細胞発現など)によって前記抗体を大量に生成することができる。抗L1-CAM抗体(例えば抗L1-CAMハイブリッド抗体またはフラグメントであるがそれらに限定されない)は、抗体重鎖をコードする発現ベクターを構築する通常的な技術を用いることによって生成することができる。前記抗体重鎖では、CDRおよび必要な場合には可変領域フレームワークの最小限部分(前記最小限部分は元の種の抗体結合特異性の維持に必要であり、本明細書に記載の技術にしたがって操作される)は元の種の抗体に由来し、抗体の残余部は標的種の免疫グロブリンに由来し、前記は本明細書に記載するように操作することができ、それによってハイブリッド抗体重鎖発現のためのベクターを作製することができる。
L1-CAM中和の測定:本明細書で用いられるように、“L1-CAM中和”は、抗L1-CAM抗体の結合によるL1-CAMタンパク質の活性および/または発現の減少を指す。L1-CAM活性/発現を中和する本技術の抗L1-CAM抗体の能力は、当業界で公知の方法を用いてin vitroまたはin vivoで評価され得る。
概説:本技術の抗L1-CAM抗体は、L1-CAMタンパク質の局在および/または定量に関して当業界で公知の方法で有用である(例えば適切な生理学的サンプル中のL1-CAMタンパク質のレベルの測定における使用、診断方法における使用、当該ポリペプチドの画像化における使用など)。本技術の抗体は、標準的技術(例えば親和性クロマトグラフィーまたは免疫沈澱)によってL1-CAMタンパク質を単離するために有用である。本技術の抗L1-CAM抗体は、宿主系で発現された組換え生成免疫反応性L1-CAMタンパク質と同様に、天然の免疫反応性L1-CAMタンパク質の生物学的サンプル(例えば哺乳動物の血清または細胞)からの精製を促進する。さらにまた、抗L1-CAM抗体を(例えば血漿、細胞溶解物または細胞懸濁物で)免疫反応性L1-CAMタンパク質を検出するために用いて、免疫反応性ポリペプチドの豊富さおよび発現パターンを評価することができる。本技術の抗L1-CAM抗体を診断に用いて、臨床検査手順の部分として組織の免疫反応性L1-CAMタンパク質レベルをモニターし、例えば施された治療レジメンの有効性を決定することができる。上記に特筆したように、検出は、本技術の抗L1-CAM抗体を検出可能な物質と合体させる(すなわち物理的に連結する)ことによって促進できる。
抗L1-CAM抗体に関して“標識される”という用語は、検出可能物質を抗体と合体させる(物理的に連結する)ことによる抗体の直接標識とともに、直接標識されるもう1つの化合物(例えば二次抗体)との反応性による抗体の間接標識を包含することが意図される。間接標識の例には、蛍光標識二次抗体を用いる一次抗体の検出、DNAプローブが蛍光標識ストレプトアビジンで検出できるようにビオチンによるDNAプローブの末端標識が含まれる。
いくつかの実施態様では、本明細書で開示される抗L1-CAM抗体は1つ以上の検出可能標識と複合体化される。そのような使用のために、抗L1-CAM抗体は、発色性、酵素性、放射性同位体、同位体性、蛍光性、毒性、化学発光性薬剤、核磁気共鳴造影剤または他の標識の共有結合または非共有結合によって検出できるように標識される。
適切な発色性標識の例には、ジアミノベンジジンおよび4-ヒドロキシアゾ-ベンゼン-2-カルボン酸が含まれる。適切な酵素標識の例には、リンゴ酸デヒドロゲナーゼ、ブドウ球菌ヌクレアーゼ、Δ-5-ステロイドイソメラーゼ、酵母アルコールデヒドロゲナーゼ、α-グリセロールリン酸デヒドロゲナーゼ、トリオースリン酸イソメラーゼ、ペルオキシダーゼ、アルカリホスファターゼ、アスパラギナーゼ、グルコースオキシダーゼ、β-ガラクトシダーゼ、リボヌクレアーゼ、ウレアーゼ、カタラーゼ、グルコース-6-リン酸デヒドロゲナーゼ、グルコアミラーゼ、およびアセチルコリンエステラーゼが含まれる。
適切な蛍光標識の例には、152Eu標識、フルオレセイン標識、イソチオシアネート標識、ローダミン標識、フィコエリスリン標識、フィコシアニン標識、アロフィコシアニン標識、緑色蛍光タンパク質(GFP)標識、o-フタルアルデヒド標識、およびフルオレサミン標識が含まれる。適切な毒素標識にはジフテリア毒素、リシン、およびコレラ毒素が含まれる。
化学発光標識の例には、ルミノール標識、イソルミノール標識、芳香族アクリジニウムエステル標識、イミダゾール標識、アクリジニウム塩標識、シュウ酸エステル標識、ルシフェリン標識、ルシフェラーゼ標識、およびイクオリン標識が含まれる。核磁気共鳴造影剤の例には重金属核、例えばGd、Mnおよび鉄が含まれる。
本技術の検出方法を用いて、免疫反応性L1-CAMタンパク質をin vivoと同様に生物学的サンプルでin vitroで検出することができる。免疫反応性L1-CAMタンパク質のin vitro検出技術には、酵素結合免疫吸着アッセイ(ELISA)、ウェスタンブロット、免疫沈澱、放射性免疫アッセイ、および免疫蛍光が含まれる。さらにまた、免疫反応性L1-CAMタンパク質のin vivo検出技術には、標識抗L1-CAM抗体の対象動物への導入が含まれる。例えば、抗L1-CAM抗体を放射能マーカーで標識し、対象動物におけるその存在および場所を標準的技術によって検出することができる。ある実施態様では、生物学的サンプルは試験対象動物由来のL1-CAMタンパク質を含む。
生物学的サンプルにおける免疫反応性L1-CAMタンパク質レベルのアッセイに加えて、本技術の抗L1-CAM抗体は、L1-CAMのin vivo画像診断のために用いることができる。この方法に有用な抗体には、X線撮影法、NMRまたはESRによって検出できるものが含まれる。X線撮影法の場合、適切な標識には放射性同位体、例えばバリウムまたはセシウムが含まれ、前記は検出可能な放射線を放射するが、対象動物に対して明白には有害ではない。NMRおよびESRのための適切なマーカーには、検出可能な特徴的スピンを有するもの(例えばデューテリウム)が含まれ、前記は対応するscFvクローンのための栄養素の標識によって抗L1-CAM抗体に取り込まれ得る。
適切な検出可能画像化部分で標識した抗L1-CAM抗体を、対象動物に(例えば経口的、皮下または腹腔内に)導入する。前記画像化部分は、例えば放射性同位体(例えば131I、112In、99mTc)、放射性不透明物質、または核磁気共鳴によって検出できる材料である。対象動物のサイズおよび用いられる画像化系が、診断画像の作製に必要とされる画像化部分の量を決定することは当業者には理解されるであろう。放射性同位体の事例では、ヒト対象動物の場合、注入される放射能の量は通常5から20ミリキューリーの範囲の99mTcである。続いて標識抗L1-CAM抗体が、特異的な標的ポリペプチドを含む細胞の場所に蓄積されるであろう。例えば、本技術の標識抗L1-CAM抗体は、対象動物内でL1-CAMタンパク質が限局している細胞および組織に蓄積されるであろう。
したがって、本技術は症状の診断方法を提供し、前記方法は以下の工程を必要とする:(a)個体の細胞または体液において本技術の抗L1-CAM抗体の結合を測定することによって、免疫反応性L1-CAMタンパク質の発現をアッセイする工程;(b)サンプルに存在する免疫反応性L1-CAMタンパク質の量を標準参照と比較する工程、ここで、標準物と比較して免疫反応性L1-CAMタンパク質レベルの増減が症状の指標である。
抗原を抗体支持マトリックスに結合させるもっとも簡単な方法は、カラムにビーズを収集し抗原溶液をカラムに通すことである。この方法の有効性は、固定された抗体と抗原との間の接触時間に左右され、前記時間は低流速を用いることによって延長することができる。固定された抗体は、抗原が通過するときに抗原を捕捉する。また別には、抗原溶液を支持体(例えばビーズ)と混合し当該スラリーを回転させるかまたは揺らして抗原と固定抗体間の最大接触を可能にすることによって、抗原を抗体-支持体マトリックスと接触させることができる。結合反応が完了した後、ビーズの収集のためにスラリーをカラムに通す。適切な洗浄緩衝液を用いてビーズを洗浄し、続いて純粋なまたは実質的に純粋な抗原を溶出させる。
対象の抗体またはポリペプチドは固体支持体(例えばビーズ)と複合体化させることができる。加えて、第一の固体支持体(例えばビーズ)はまた、所望の場合には第二の固体支持体(第二のビーズまたは他の支持体であり得る)と複合体化させることができる。前記複合体化は、任意の適切な手段(ポリペプチドと支持体との複合体化について本明細書で開示する手段を含む)によって実施される。したがって、ポリペプチドと固体支持体の複合体化に関して本明細書で開示する複合体化の方法および手段のいずれも、第一および第二の固体支持体が同じであれ異なるものであれ、第一の支持体と第二の支持体との複合体化のためにも適用できる。
抗体またはポリペプチドは固体支持体(例えばビーズ)上に固定され得る。前記固定は、カルボキシル基官能化ビーズとポリペプチドのアミノ末端との間で形成される共有アミド結合を介するか、または反対にアミノ基官能化ビーズとポリペプチドのカルボキシル末端との間で形成される共有アミド結合を介する。加えて、二官能性トリチルリンカーが、支持体に、例えば樹脂(例えば(Wang樹脂))上の4-ニトロフェニル活性エステルに当該樹脂上のアミノ基またはカルボキシル基によりアミノ樹脂を介して結合され得る。二官能性トリチルによるアプローチを用いるとき、固体支持体は揮発酸(例えばギ酸またはトリフルオロ酢酸)による処理を要求し、ポリペプチドが切断され除去され得ることを担保することができる。そのような事例では、ポリペプチドは、固体支持体のウェルの底にまたは固体支持体の平らな表面に無ビーズパッチとして沈積され得る。マトリックス溶液の添加後、ポリペプチドはMS中に放出され得る。
直交切断可能なリンカーもまた、第一の固体支持体(例えばビーズ)を第二の固体支持体に結合するために、または対象のポリペプチドを固体支持体に結合するために有用であり得る。そのようなリンカーを用いて、ポリペプチドを支持体から切断することなく、第一の固体支持体(例えばビーズ)を選択的に第二の固体支持体から切断できる。その後でポリペプチドを続いてビーズから切断することができる。例えば、ジスルフィドリンカー(還元剤(例えばDTT)を用いて切断できる)を利用して、ビーズを第二の固体支持体に結合することができ、さらに酸切断可能な二官能性トリチル基を用いポリペプチドを支持体に固定できよう。所望の場合、例えば第一の支持体と第二の支持体との間の結合を無傷にしたままで、ポリペプチドと固体支持体との結合を最初に切断することができる。トリチルリンカーは、複合体化の性質にかかわりなく、共有結合性または疎水性複合体化を提供することができ、トリチル基は酸性条件下で容易に切断される。
例えば、ビーズは連結基を介して第二の支持体と結合させることができ、前記連結基は、固体支持体とビーズの高密度結合またはビーズとポリペプチドの高密度結合が促進される長さおよび化学的性質を有するように選択できる。そのような連結基は、例えば“樹木様”構造を有し、それによって固体支持体上の一結合部位につき複数の官能基を提供することができる。そのような連結基の例には、ポリリジン、ポリグルタミン酸、ペンタエリスロールおよびtris-ヒドロキシ-アミノメタンが含まれる。
固体支持体にはまた特異的結合対のメンバーを提供することができ、したがって、相補的結合部分を含むポリペプチドまたは第二の固体支持体と複合体化することができる。例えば、アビジンまたはストレプトアビジンで被覆したビーズは、その中にビオチン部分を取り込ませたポリペプチドまたはビオチンもしくはビオチン誘導体(例えばイミノビオチン)で被覆した第二の固体支持体と結合することができる。
本明細書に開示のまたは当業界で公知の結合メンバーのいずれも逆にできることは理解されるべきである。したがって、例えばビオチンをポリペプチドまたは固体支持体に取り込むことができ、反対にアビジンまたは他のビオチン結合部分を支持体またはポリペプチドにそれぞれ取り込むことができよう。本明細書での使用に意図される他の特異的結合対には、ホルモンおよびそれらの受容体、酵素およびそれらの基質、ヌクレオチド配列およびその相補配列、抗体およびそれが特異的に相互作用する抗原、並びに当業者に公知の他の対が含まれるが、ただし前記に限定されない。
概説:本技術の抗L1-CAM抗体は診断方法で有用である。したがって、本技術は、対象動物のL1-CAM活性の診断で当該抗体を用いる方法を提供する。本技術の抗L1-CAM抗体は、L1-CAMタンパク質に対して任意のレベルのエピトープ結合特異性および非常に高い結合親和性をもつものを選択することができる。一般的には、抗体の結合親和性が高ければ高いほど、より厳しい洗浄条件を免疫アッセイで実施して、標的ポリペプチドを除去することなく非特異的に結合した物質を除去することができる。したがって、診断アッセイで有用な本技術の抗L1-CAM抗体は、通常約108 M-1、109 M-1、1010 M-1、1011 M-1または1012 M-1の結合親和性を有する。さらにまた、診断試薬として使用される抗L1-CAM抗体は、標準的条件下で少なくとも12時間、少なくとも5時間、または少なくとも1時間で平衡に達する十分なカイネティック-オン速度を有する。
抗L1-CAM抗体を用い、多様な標準的アッセイフォーマットで免疫反応性L1-CAMタンパク質を検出することができる。そのようなフォーマットには、免疫沈澱、ウェスタンブロット形成、ELISA、放射性免疫アッセイ、および免疫測定アッセイが含まれる。以下を参照されたい:Harlow & Lane, Antibodies, A Laboratory Manual (Cold Spring Harbor Publications, New York, 1988);米国特許3,791,932号、3,839,153号、3,850,752号、3,879,262号、4,034,074号、3,791,932号、3,817,837号、3,839,153号、3,850,752号、3,850,578号、3,853,987号、3,867,517号、3,879,262号、3,901,654号、3,935,074号、3,984,533号、3,996,345号、4,034,074号、および4,098,876号。生物学的サンプルは、対象動物の任意の組織または体液から入手できる。ある種の実施態様では、対象動物は癌病期の初期である。ある実施態様では、癌病期の初期は、対象動物から得られるサンプルのL1-CAMタンパク質のレベルまたは発現パターンによって決定される。ある種の実施態様では、サンプルは、尿、血液、血清、血漿、唾液、羊水、脳脊髄液(CSF)、および生検体組織から成る群から選択される。
いくつかの実施態様では、本開示は、診断用薬剤と複合体化された本技術の抗L1-CAM抗体を提供する。診断用薬剤は、放射性または非放射性標識、造影剤(例えば磁性共鳴画像診断、コンピュータ支援断層撮影または超音波用)を含むことができ、放射性標識は、ガンマ-、ベータ-、アルファ-、オージェ電子-、または陽電子-放射同位体であり得る。診断用薬剤は、抗体部分(すなわち抗体または抗体フラグメントまたは準フラグメント)と複合体化されて投与される分子であり、前記は、抗原を含む細胞に局在することによって疾患の診断または検出で有用である。
他の環型キレート、例えば大環状ポリエーテルもまた意図され、前記は核種(例えばRAITのための223Ra)を安定的に結合させるために有益である。
本技術の免疫グロブリン関係組成物(例えば抗体またはその抗原結合フラグメント)は、L1-CAM関連癌の治療に有用である。そのような治療は、病理学的に高レベルのL1-CAMを有すると識別された患者(例えば本明細書に記載の方法によって診断された患者)またはそのような病理学的的レベルと関連することが知られている疾患を有すると診断された患者で用いることができる。ある特徴では、本開示は、L1-CAM関連癌をその必要がある対象動物で治療する方法を提供し、前記方法は、本技術の抗体(またはその抗原結合フラグメント)の有効量を対象動物に投与する工程を含む。本技術の抗体によって治療できる癌の例には以下が含まれる(ただしそれらに限定されない):白血病、ユーイング肉腫、神経芽細胞腫、骨肉腫、多形性神経膠芽腫、卵巣癌、子宮内膜癌、子宮癌、三陰性乳癌、メラノーマ、明細胞腎細胞癌、褐色細胞腫および傍神経節腫、中皮腫、小細胞肺癌(SCLC)、非小細胞肺癌(NSCLC)、膵管癌、結腸癌、膵臓癌、肝細胞癌腫、胃癌、胆管癌腫、カルチノイド、神経内分泌腫瘍、胃腸管間質腫(GIST)、褐色細胞腫、神経膠腫、膵臓の神経外胚葉癌、膵臓の腺癌腫、結腸直腸癌、腎細胞癌腫、血管腫、軟骨肉腫、食道の腺癌腫、乏突起神経膠腫、星状細胞腫、上衣腫、膵臓の神経内分泌癌腫、副腎腺腫、平滑筋肉腫、脂肪肉腫、卵巣の顆粒細胞腫瘍、シュワン細胞腫、原始神経外胚葉腫瘍(PNET)、類上皮肉腫、鼻腔神経芽細胞腫、髄芽腫、毛細血管腫、カポジ肉腫、横紋筋肉腫、顎下腺の癌、および頭頸部の扁平上皮癌。
投与は任意の適切なルートによって実施でき、前記ルートには、経口、鼻内、非経口(静脈内、筋肉内、腹腔内、または皮下)、直腸、頭蓋内、髄腔内、または局所投与が含まれる。投与には自己投与および別人による投与が含まれる。さらに理解されるべきことは、記載の症状の治療における多様な態様は“実質的”を意味することが意図されることである。“実質的”は完全治療を含むが、完全治療未満を含み、その場合にはいくらかの生物学的または臨床的に対応する成果が達成される。
いくつかの実施態様では、本技術の抗体は、その必要がある対象動物に1用量以上で投与することができる医薬処方物を含む。投薬レジメンは、所望の応答(例えば治療的応答)を提供するために調整することができる。
いくつかの実施態様では、対象動物は、癌を有すると診断されるか。または癌を有すると疑われる。抗体によって放射される放射能レベルは、陽電子放射断層撮影法または単光子放射コンピュータ断層撮影法を用いて検出できる。
加えて或いはまた別に、いくつかの実施態様では、当該方法はさらにまた、放射性核種と複合体化された本技術の抗体を含む免疫複合体の有効量を対象動物に投与する工程を含む。いくつかの実施態様では、放射性核種は、アルファ粒子放射同位体、ベータ粒子放射同位体、オージェ-エミッター、またはそれらの任意の組合せである。ベータ粒子放射同位体の例には、86Y、90Y、89Sr、165Dy、186Re、188Re、177Lu、および67Cuが含まれる。アルファ粒子放射同位体の例には、213Bi、211At、225Ac、152Dy、212Bi、223Ra、219Rn、215Po、211Bi、221Fr、217At、および255Fmが含まれる。オージェ-エミッターの例には、111In、67Ga、51Cr、58Co、99mTc、103mRh、195mPt、119Sb、161Ho、189mOs、192Ir、201Tl、および203Pbが含まれる。当該方法のいくつかの実施態様では、正常組織の非特異的FcR依存結合は排除または軽減される(例えばFc領域のN297A変異を介する(前記変異は非グリコシル化をもたらす))。そのような免疫複合体の治療有効性は、腫瘍曲線下面積(AUC):正常組織AUC比をコンピュータで計算することによって決定できる。いくつかの実施態様では、免疫複合体は、約2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1、10:1、15:1、20:1、25:1、30:1、35:1、40:1、45:1、50:1、55:1、60:1、65:1、70:1、75:1、80:1、85:1、90:1、95:1、または100:1の腫瘍AUC:正常組織AUC比を有する。
“医薬的に許容できる”、“生理学的に耐え得る”、およびその文法的変形である用語は、それらが組成物、担体、希釈剤および試薬に関するときには互換的に用いられ、望ましくない生理学的作用を当該組成物の投与を禁止するほどに生じることなく、対象動物に投与できる物質を表す。例えば、“医薬的に許容できる賦形剤”は、医薬組成物の調製で有用であり、一般的には安全で非毒性で望ましい賦形剤を意味し、人間用医薬の使用と同様に獣医の使用にも許容し得る賦形剤を含む。そのような賦形剤は固体、液体、半固体で、エーロゾル組成物の事例では気体であり得る。“医薬的に許容できる塩およびエステル”は、医薬的に許容でき、かつ望ましい薬理学特性を有する塩およびエステルを意味する。そのような塩には、組成物に存在する酸性陽子が無機または有機塩基と反応する能力を有する場合に形成される塩が含まれる。適切な無機塩には、アルカリ金属(例えばナトリウムおよびカリウム)、マグネシウム、カルシウムおよびアルミニウムとともに形成されるものが含まれる。適切な有機塩には、有機塩基、例えばアミン塩基(例えばエタノールアミン、ジエタノールアミン、トリエタノールアミン、N-メチルグルカミンなど)とともに形成されるものが含まれる。そのような塩にはまた、無機酸(例えば塩酸および臭化水素酸)および有機酸(例えば酢酸、クエン酸、マレイン酸、並びにアルカン-およびアレーン-スルホン酸(例えばメタンスルホン酸およびベンゼンスルホン酸))とともに形成される酸付加塩が含まれる。医薬的に許容できるエステルには、抗L1-CAM抗体に存在するカルボキシ、スルホニルオキシ、およびホスホノキシ基から形成されるエステル、例えばC1-6アルキルエステルが含まれる。2つの酸性基が存在する場合、医薬的に許容できる塩またはエステルは一酸-一塩もしくはエステルまたは二塩もしくはエステルであることができ、同様に3つ以上の酸性基が存在する場合には、そのような基のいくつかまたは全てが塩化またはエステル化され得る。本技術で示す抗L1-CAM抗体は、非塩化もしくは非エステル化形で、または塩化および/またはエステル化形で存在することができ、抗L1-CAM抗体の呼称は、本来の(非塩化および非エステル化)の化合物およびその医薬的に許容できる塩およびエステルを含むことが意図される。さらにまた、本技術のある種の実施態様は、2つ以上の立体異性体形で存在することができ、抗L1-CAM抗体の呼称は、全ての単独立体異性体およびそのような立体異性体の全ての混合物(ラセミであれそれ以外であれ)を含むことが意図される。本技術の具体的な薬物および組成物の投与のための適切なタイミング、順序および投薬量の決定に、当業者は何ら困難を有しないであろう。
本技術の医薬組成物は、その意図される投与ルートに適合するように処方される。本技術の抗L1-CAM抗体組成物は、非経口、外用、静脈内、経口、皮下、動脈内、皮内、経皮、直腸、頭蓋内、髄腔内、腹腔内、鼻内、もしくは筋肉内ルートによって投与されるか、または吸入薬である。抗L1-CAM抗体は、場合によって、多様なL1-CAM関連癌の治療で少なくとも部分的に有効な他の薬剤と併用して投与することができる。
経口、皮内または皮下適用に用いられる溶液または懸濁物は、以下の成分を含むことができる:無菌的希釈剤、例えば注射水、食塩水、不揮発油、ポリエチレングリコール、グリセリン、プロピレングリコール、または他の合成溶媒;抗菌化合物、例えばベンジルアルコールまたはメチルパラベン;抗酸化剤、例えばアスコルビン酸または亜硫酸水素ナトリウム;キレート化合物、例えばエチレンジアミン四酢酸(EDTA);緩衝剤、例えば酢酸、クエン酸、またはリン酸;および張度を調整する化合物、例えば塩化ナトリウムまたはデキストロース。pHは、酸または塩基(例えば塩酸または水酸化ナトリウム)で調整することができる。非経口調製物は、アンプル、使い捨て注射器またはガラス製もしくはプラスチック製マルチ用量バイアルに封入できる。
無菌的な注射可能溶液は、本技術の抗L1-CAM抗体を必要な場合には上記に列挙した成分の1つとともに適切な溶媒に必要とされる量で取り込み、続いてろ過滅菌することによって調製できる。一般的には、分散液は無菌的ビヒクルに抗L1-CAM抗体を取り込むことによって調製され、前記ビヒクルは、基本的分散媒体および上記に列挙したもののうち必要とされる他の成分を含む。無菌的注射可能溶液を調製するための無菌的粉末の事例では、調製方法は真空乾燥および凍結乾燥であり、前記によって、活性成分プラス以前にろ過滅菌された当該溶液に由来する任意の所望される追加成分が得られる。本技術の抗体は、デポー注射または移植調製物(活性成分の持続性または拍動性放出を可能にする態様で処方され得る)の形態で投与することができる。
吸入による投与の場合、抗L1-CAM抗体は、加圧容器もしくはディスペンサー(推進剤、例えば気体(例えば二酸化炭素)を含む)またはネブライザーからエーロゾルスプレーの形態でデリバリーされる。
抗L1-CAM抗体はまた、座薬(例えば通常的な座薬基剤(例えばカカオ脂および他のグリセリド)を用いる)または直腸デリバリーのための保持浣腸剤の形態で医薬組成物として調製できる。
ある実施態様では、抗L1-CAM抗体は、身体からの急速な排除に対して抗L1-CAM抗体を保護する担体を用いて調製され、前記は例えば制御放出処方物であり、埋込み物およびマイクロカプセル化デリバリー系が含まれる。生物分解性、生体適合性ポリマーを用いることができ、前記は、例えば、酢酸エチレンビニル、ポリ無水物、ポリグリコール酸、コラーゲン、ポリオルトエステル、およびポリ乳酸である。そのような処方物の調製方法は当業者には明白であろう。当該材料はまた市場でアルザ社およびノバ社(Alza Corporation;およびNova Pharmaceuticals, Inc)から入手できる。リポソーム懸濁物(ウイルス抗原に対するモノクローナル抗体を用いて感染細胞に標的誘導されるリポソームを含む)もまた、医薬的に許容できる担体として用いることができる。これらは、当業者に公知の方法にしたがって調製でき、当該方法は米国特許4,522,811号に記載されている。
本技術はL1-CAM関連癌を検出および/または治療するキットを提供し、前記は、本技術の少なくとも1つの免疫グロブリン関係組成物(本明細書に記載する任意の抗体または抗原結合フラグメント)、またはその機能的変種(例えば置換変種)を含む。場合によって、本技術のキットの上記記載成分は適切な容器に詰められ、L1-CAM関連癌の診断および/または治療のためのラベルが付される。上述の成分は、一ユニット容器またはマルチ用量容器(例えば封入アンプル、バイアル、ボトル、注射器、および試験管)に、水性(好ましくは無菌的)溶液として、または再構成のための凍結乾燥(好ましくは無菌的)処方物として保存され得る。キットはさらにまた第二の容器を含むことができ、前記容器は、医薬組成物をより大きな体積に希釈するために適切な希釈剤を保持する。適切な希釈剤には、当該医薬組成物の医薬的に許容できる賦形剤および食塩水溶液が含まれるが、ただし前記に限定されない。さらにまた、キットは、医薬組成物の希釈の指示および/または医薬組成物の投与の指示(希釈するか否かにかかわらず)を含むことができる。容器は、多様な材料(例えばガラスまたはプラスチック)から形成でき、無菌的なアクセス口を有することができる(例えば、容器は静脈内溶液用バッグまたはストッパー付きバイアル(ストッパーは皮下注射針によって穿刺できる)であり得る。キットはさらにまたより多くの容器を含むことができ、それらは、医薬的に許容できる緩衝液(例えばリン酸緩衝食塩水)、リンゲル液およびデキストロース溶液を含む。キットは、さらにまた市場および使用者の見地から所望される他の物質を含むことができ、それらには、他の緩衝液、希釈剤、フィルター、針、注射器、1つ以上の適切な宿主のための培養液が含まれる。キットは、場合によって、治療用または診断用製品の市販パッケージに慣例的に含まれる指示を含むことができ、前記指示は、例えば適応症、用法、投薬量、製造、投与、禁忌についての情報および/またはそのような治療用または診断用製品の使用に関する警告を含む。
抗体系キットの場合、キットは例えば以下を含む:1)固体支持体に結合されている第一の抗体、例えば本技術のヒト化、キメラまたは二重特異性L1-CAM抗体(またはその抗原結合フラグメント)、前記はL1-CAMタンパク質と結合する;2)L1-CAMタンパク質または第一の抗体と結合する第二の異なる抗体、前記は検出可能標識と複合体化される。
キットはまた、例えば緩衝剤、保存料またはタンパク質安定化剤を含む。キットはさらにまた、検出可能標識を検出するために必要な成分(例えば酵素または基質)を含むことができる。キットはまた、コントロールサンプルまたはコントロールサンプルシリーズを含むことができ、それらをアッセイして試験サンプルと比較することができる。キットの各成分は個々の容器に封入され、多様な容器のいずれも単一のパッケージ内に、キットを用いて実施されるアッセイの結果を解釈するための指示と一緒に存在する。前記記述物は、例えばL1-CAMタンパク質のin vitroまたはin vivoの検出のために、またはその必要がある対象動物でのL1-CAM関連癌の治療のために、キットに収められた試薬をどのように使用するかを説明する。ある種の実施態様では、試薬の使用は本技術の方法にしたがうことができる。
実施例
本技術をさらにまた以下の実施例によって例証するが、これらの実施例は、如何なる態様においても制限と解されるべきではない。以下の実施例は、本技術の例示的L1-CAM抗体の調製、特徴付けおよび使用を示す。実施例1-11は本技術のキメラ抗体、ヒト化抗体および二重特異性抗体の生成、並びにそれらの結合特異性およびin vivoの生物学的活性の特徴付けを示す。
免疫組織化学(IHC):IHCのためのヒト腫瘍および正常組織の使用は、スローンケタリング癌センター研究所内監査委員会(Memorial Sloan-Kettering Cancer Center institutional review board)によって承認された。瞬間凍結組織の5から7ミクロンメートル切片をアセトンで30分間-20℃で固定した。内因性ビオチン結合活性を、アビジンおよびビオチン(ベクターアビジン-ビオチン封鎖キット(Invitrogen, Carlsbad, CA))の連続処理(各々20分間)とそれに続く室温で1時間の10%ウマ血清ブロッキングによってブロッキングした。続いて、切片を逐次的に一次抗体、ビオチン化ウマ抗マウスIgG(H+L)(Vector Laboratories, Inc., Burlingame, CA)およびアビジン-ビオチン複合体(ベクタスタチンABCキット(Vector Laboratories, Inc., Burlingame, CA))でそれぞれ60分間室温で反応させ、各反応の間で洗浄した。その後、切片を色素(DABペルオキシダーゼ基質キット(Vector Laboratories, Burlingame, CA))で2分間染色して洗浄し、マイヤーのヘマトキシリンで対比染色して洗浄し、95%エチルアルコールで脱水した。
E71およびE72のキメラおよびヒト化フォーマットの構築:ヒトホモログを基にして、E71およびE72の重鎖および軽鎖の両方のCDR配列をヒトIgG1フレームワークに移植し最適化した。huE71およびhuE72遺伝子を合成し(Blue Heron Biotechnology, Bothhell, WA or Genscript, Piscataway, NY)、哺乳動物発現ベクター(Eureka, CA)に取り込み、安定的生成のためにDG44細胞またはCHO-S細胞にトランスフェクトした。同様に、ヒトVHおよびVL配列をヒトIgG4フレームワークに移植してIgG4組換え抗体を作製した。最後に、GnT1酵素を欠くDG44細胞にこれらの遺伝子をトランスフェクトして、固有のIgG1糖型を作製した。
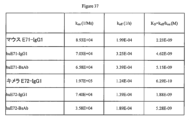
Biacore T-100バイオセンサー(GE Healthcare, Uppsala, Sweden)によるin vitro結合カイネティクス:CM5センサーチップ(研究グレード)および関連試薬はBiacore USA(Piscataway, NJ)から購入した。抗原L1-CAM-FcまたはL1-CAM-Hisは、製造業者の指示にしたがってCM5センサーチップに直接固定した。精製モノクローナル抗体(MoAb)(マウス、キメラIgG1およびIgG4、並びにE71およびE72のヒト化OgG1およびIgG4バージョン、並びにそれらのIgG1n糖型)を変動濃度(41.7~666.7nM)でHBS-EP緩衝液で分析前に希釈した。サンプルはセンサー表面に30μL/分の流速で1分かけて注いだ。結合時間は1分に設定し、解離時間は5分から15分に設定した。各サイクルの終了時に、表面を50mMのNaOHを50μL/分の流速で用い1分かけて再生した。データを二価アナライトモデルおよびBiacore T-100評価ソフトウェアによる規定パラメータ設定を用いて分析し、速度一定での見かけの結合(kon)、速度一定での解離(koff)および平衡解離定数(Kd=koff/kon)を計算した。
(実験cpm-バックグラウンドcpm)/(全cpm-バックグラウンドcpm)x100%
式中、cpmは51Cr放出の毎分の計数である。全放出は10%SDS(Sigma(St Louis, Mo))による溶解によって評価し、バックグラウンド放出はエフェクター細胞の非存在下で測定した。EC50は、シグマプロット(Sigmaplot)またはグラフパッドプリズム(Graphpad Prism)ソフトウェアを用いて計算した。
異種移植マウスのMoAb生体分布:雌無胸腺ヌードマウスを業者から購入した(Harlan Sprague Dawley, Inc(Indianapolis, IN))。全ての手順は、当研究所(スローンケタリング記念癌センター)の動物管理使用委員会が承認したプロトコルおよび当研究所の実験動物の適切な人道的使用のためのガイドラインにしたがって実施された。腫瘍細胞を採集し、マトリゲル(Matrigel(BD Biosciences, Bedford, MA))に再懸濁した。細胞(2-10x106)をマウスの脇腹の皮下に22ゲージ針を用い0.1mLの体積で移植した。処置を開始する前に腫瘍を~200mm3のサイズに増殖させた。樹立腫瘍を有するマウスをランダムに複数の治療グループに分けた。マウス当たり100μCiの放射性ヨウ素化抗体を静脈内に注射し、通常48時間で動物を犠牲にし、それらの器官を取り出し、ガンマカウンター(Packard Instruments, Perkin Elmer, Waltham, MA)で計数した。これらの器官には皮膚、肝臓、脾臓、腎臓、副腎、胃、小腸、大腸、膀胱、大腿骨、筋肉、腫瘍、心臓、肺臓、脊椎および脳が含まれていた。器官に蓄積されたμCiおよび器官重量を基準にして、マウス1グラム当たりの%注射線量(%ID)を計算した。%ID/gの腫瘍対非腫瘍比もまた計算した。
定量のために、クォンタムシンプリーセルラー(Quantum Simply Cellular)抗マウスIgGキット(Bangs Laboratories, Fishers, IN)を用いた。簡単に記せば、当該キットは、5つの微小球集団を含む(1つはブランクであり、4つは量が増していく抗マウスIgGで標識されている)。続いてビーズおよび腫瘍細胞(37℃で5分間)を同じ蛍光複合体化マウスE71で30分間氷上にて標識した。続いて、細胞をPBSで洗浄し、BD FACSカリバー(BD Biosciences, Bedford, MA)で標識ビーズと一緒に分析した。各キットとともに提供されたエクセルベースのQuickCal分析テンプレートは、蛍光強度を腫瘍細胞上の抗原と相関させるために役立つ。各データ点は二つ組の平均である。
in vivo抗腫瘍アッセイ:in vivo試験のために、BALB-Rag2-KO-IL-2R-γc-KO(DKO)マウス(Dr. Mamoru Ito(CIEA, Kawasaki)のコロニーに由来する)を用いた(以下を参照されたい:Koo GC et al., Expert Rev Vaccines 8:113-20, 2009)。新鮮培地/BDマトリゲル(BD Biosciences, Bedford, MA)の1:1混合物の腫瘍細胞を皮下に移植した。腫瘍体積の測定のために、携帯用TM900スキャナー(Peira, Brussels, BE)を用いて全腫瘍を測定した。
細胞培養:細胞を含むT-75フラスコ(Corning, Corning NY)は、37℃にて5%CO2濃度で維持した細胞インキュベーターで保存した。SKOV3(ヒト上皮卵巣癌種細胞株(ATCC, Manassas, VA))は、RPMIマッコイ5A培地(RPMI McCoy's 5A Medium(Thermo Fisher Scientific, Waltham, MA))(改変されて1.5mM L-グルタミンを含む)で培養し、いずれも100ユニット/mLペニシリンGおよび100μg/mLストレプトマイシン並びに10%ウシ胎児血清とともに増殖させた。SKOV3細胞株は1週間に1回、ハンクス緩衝食塩水溶液中の0.25%トリプシン/53mM EDTA(カルシウムおよびマグネシウムを含まない)を用いてサブ培養し、標準的細胞株継代のために1:5で継代した。
抗体のバイオコンジュゲーション:抗体は、4-5mg/mLの平均濃度で酢酸緩衝液(25mM酢酸ナトリウム、150mM塩化ナトリウム)中で得られた。50,000分子量カットオフを有する遠心分離用フィルターユニット(Amicon Ultra 4 Centrifugal Filtration Units, Millipore Corp., Billerica, MA)を用いて、抗体を最終濃度12-15mg/mLに濃縮した。濃縮した後、DMSOに溶解した10当量のp-SCN-Bn-DFOまたはp-SCN-Bn-DOTA(Macrocyclics, Inc. Dallas, TX)を添加する前に、0.1 M Na2CO3を用いて抗体のpHを8.5-9.0に調整した。反応物を37℃で1時間、定常的に500rpmで振盪させながらインキュベートした。50,000分子量カットオフを有する遠心分離用フィルターユニット(Amicon Ultra 4 Centrifugal Filtration Units, Millipore Corp., Billerica, MA)を用いて、リガンド-抗体複合体を精製した。この最終的バイオ複合体をアリコットに分け、PBS(pH7.4)中で-80℃で保存した。
放射性標識:89Zrは、1.0Mシュウ酸中のシュウ酸-89Zrとしてターゲットプロセッシング後に受けとった。溶液を1.0M炭酸ナトリウムで中和してpH~7にした。DFO-抗体を中和89Zrとともにインキュベートし、37℃で60分間PBS(pH7.4)中で標識した。177LuCl(比活性170MBq/mg(Perkin Elmer, Waltham, MA))を入手し、アンモニア酢酸緩衝液(200 mmol/L, pH 5.4)で希釈し、DOTA-抗体と42℃で1時間インキュベートした。反応の進行は、シリカゲル含浸ミクロガラス繊維紙片の放射性-ITLC(ITLC-SG, Varian, Lake Forest, CA)により、移動相として50mM EDTA(pH5)を用いてモニターした(AR-2000(Bioscan Inc., Washington, DC)によって分析)。抗体複合体は起点に留まり、一方、遊離放射性核種は移動相中のEDTAによって捕捉され、溶媒前端と一緒に泳動した。粗雑な放射性化学物質収量は放射-ITLCデータを用いて計算した。続いて放射性標識抗体をサイズ排除クロマトグラフィー(PD10)を用いて精製し、続いて、処方のために遠心分離ろかにより最終体積に濃縮した。最終精製放射性標識抗体の放射性化学物質純度は、使用前放射-ITLCによって99%を超えることが確認された。
免疫反応性:89Zr-DFO-抗体の免疫反応部分をLindmo細胞結合アッセイを用いて決定した(Ben QW et al., Ann Surg Oncol 17:2213-21, 2010)。この目的のために、500μLのPBS、1% BSA(pH7.4)中に5.0x105-5.0x106細胞/mLの範囲の濃度でSKOV3細胞をマイクロ遠心管に懸濁した。89Zr-DFO-抗体のアリコット(1μCi/mLストックの50μL)を各遠心管に500μL最終体積で加えた。サンプルをサーモミキサー上で37℃にて60分間インキュベートした。続いて処理細胞を遠心分離によりペレットにし(1400RPMで4分間)、上清を吸引し、細胞結合放射能活性を計数する前に冷PBSで3回洗浄した。活性データをバックグラウンド修正し、適切なコントロールサンプルの計数総数と比較した。免疫反応部分は、(1/[正規化細胞濃度])に対する(全体/結合)活性のプロットの線形回帰分析によって決定した。
生体分布:89Zr-抗体SKOV3腫瘍を有する雌無胸腺ヌードマウスを用いて生体分布試験を実施した。動物に150μLのPBS中の89Zr-抗体の各々を尾静脈内注射により投与した(192-214μCi)。注射後96時間でCO2窒息によって動物(n=4/グループ)を安楽死させた。安楽死に続いて、17の器官(血液、腫瘍、心臓、肝臓、脾臓、胃、大腸、小腸、膵臓、卵巣、腎臓、骨、筋肉、リンパ、皮膚、尾)を収集し、重量を測定し、ガンマカウンター(89Zrについて較正)で放射能をアッセイした。既知標準物から作製した較正曲線を用いて計数を活性に変換した。計数データはバックグラウンドおよび注射時間に対する崩壊について修正し、注射総活性に対して正規化することによって、各組織サンプルについて1グラム当たりのパーセント注射線量(%ID/g)を計算した。この試験で示されるデータは平均±標準偏差として表される。統計的相違は、グラフパッドプリズム7ソフトウェア(GraphPad Prism 7 software)を用い独立両側スチューデントのt検定によって分析した。0.05より小さいP値を統計的に有意とみなし、星印によって示した。
ヒト化E71およびE72抗L1-CAM抗体を作製した。配列設計は、重要なマウスアミノ酸残基を保存しながら、ヒトIgG相同性計算を基準にした。図6および7は、それぞれ、マウスE71のVHおよびVL(配列番号:1および3として表される)およびマウスE72のVHおよびVL(配列番号:5および7として表される)を示す。マウスE71(図6参照)およびE72(図7参照)の軽重鎖のCDRを、ヒトIgG1フレームワークにヒトフレームワークとのそれらの相同性に基づいて移植した。E71では、用いた相同なヒト配列は、重鎖についてはIGHV7-4-1(配列番号:2)および軽鎖についてはIGKV-58(配列番号:4)であった(図6)。E72では、それらは、それぞれ、重鎖についてはIGHV1-2*02|66.3|IGHJ4*01|85.7(配列番号:6)および軽鎖についてはIGKV1-NL1*01|73.7|IGKJ2*02|81.8(配列番号:8)であった(図7)。
2つの異なる重鎖配列(huE71ではH1およびH2(対応するアミノ酸配列については図8、およびcDNA配列については図9参照))および2つの異なる軽鎖配列(L1およびL2(対応するアミノ酸については図10、およびcDNA配列については図11参照))をhuE71のために完全なIgGとして発現させ、構築および安定性について試験した。2つの異なる重鎖配列(huE72ではH1およびH2(対応するアミノ酸配列については図12、およびcDNA配列については図13参照))および2つの異なる軽鎖配列(L1およびL2(対応するアミノ酸配列については図14、およびcDNA配列については図15を参照))をhuE72のために完全なIgGとして発現させ、構築および安定性について試験した。
E71(対応するアミノ酸配列については図16、cDNA配列については図17)およびE72(対応するアミノ酸配列については図18、cDNA配列については図19)のキメラ型もまた比較のために作製した。もっとも安定な、E71のためのH1およびL1組合せ(それぞれ図20および図21)並びにE72のためのH1およびL2組合せ(それぞれ図22および図23)を、huE71およびhuE72の最終型について実験の残りのために選択した。追加の構築物は、chE71の重鎖配列をヒトIgG4フレームワークで取り替え(図24にアミノ酸配列および図25にcDNA配列)、さらにhuE71のそれをヒトIgG4フレームワークで取り替えて(それぞれ図26にアミノ酸および図27にcDNA)作製した。huE71を単一ベクターにパッケージングし(バランスのとれた重鎖および軽鎖分泌のため)、DG44細胞に形質導入した。huE71-IgG1nは別のhuE71-IgG1糖型であり、前記は、GnT1欠損由来変種グリコシル化を有するCHO細胞において発現される(Jefferis R, Nat Rev Drug Discov 8:226-34, 2009)。標準的なプロテインA親和性クロマトグラフィーを用いて、HuE71-IgG1、huE71-IgG4およびhuE71-IgG1nを精製した。糖分析は、huE71-IgG1nが71.1%(Mol%)マンノース、26.3%(Mol%)N-アセチルグルコサミン、および2.6%(Mol%)グルコースを有することを確認した。SDSゲルでは、huE71およびhuE72は適切なサイズの重軽鎖を有するIgGとして泳動し、HPLCでは、それらはいずれも完全なIgGとして溶出し、5%未満の凝集を形成した。
抗原(L1-CAM-FcおよびL1-CAM-His)をCM5チップに固定し、抗体結合カイネティクス(kon、koffおよびKd)を、Biacore T-100を用いて表面プラズモン共鳴(SPR)によって比較した(L1-CAM-Fcについては図28)。キメラおよびヒト化抗体のL1-CAM-Fcにおける結合カイネティクスは図29および図30で要約し、他のL1-CAMマウス抗体と比較した。キメラおよびヒト化抗体のL1-CAM-Hisにおける結合カイネティクスは図31で要約されている。
抗原結合はまた、L1-CAM(+)腫瘍細胞を用いてFACS分析によって分析された。データは、フローサイトメトリーによって決定し、使用抗体の最高濃度の結合パーセンテージとして正規化した平均蛍光強度として表した(1μg/106細胞):中皮腫(図32)、白血病、乳癌およびユーイング腫瘍ファミリー(図33)、並びにメラノーマ、神経芽細胞腫、骨肉腫、横紋筋肉腫、小細胞肺癌(図34)。
HuE71-IgG1は安定であり、5回の凍結融解プロセスに付した後でもその抗原結合のEC50は0.03μg/百万細胞に留まった。抗原としてプラスチックプレート被覆腫瘍細胞を用いたELISA方法もまたhuマウス-IgG1およびhuE71-IgG1n結合アッセイに用いられ、huE71-IgG1およびhuE72-IgG1の両方が腫瘍細胞に対し相応の結合を示した。huE71-IgG1nの腫瘍細胞に対する結合は5回繰返した凍結融解の後でも変化がなかった。
これらの結果は、本技術の抗体またはその抗原結合フラグメントは、高い結合親和性でL1-CAMと特異的に結合することを示している。したがって、本明細書に開示する免疫グロブリン関係組成物は、サンプル中のL1-CAMタンパク質の検出に有用である。
ADCC(抗体依存細胞媒介細胞傷害)をエフェクターとして正常ボランティア由来PBMCを用いて評価した。特定の糖型とは対照的に、chE71、huE71、chE72およびhuE72の全ての野生型ヒトIgG1型はADCCを媒介できない。2つの標的細胞株LAN-1およびNB1691を試験した。huE71-IgG1nのみがADCCを媒介できた(LAN-1細胞に対するEC50は0.06μg/mL、NB1691細胞に対するEC50は0.1μg/mLであった)。図61および62参照。
これらの結果は、本技術の抗体またはその抗原結合フラグメントはしたがってADCCを引き出すことができることを示している。したがって、本明細書に開示する免疫グロブリン関係組成物は、L1-CAM陽性癌の治療に有用である。
IgG-scFvフォーマット(図35)を用いて、図36に示すアミノ酸配列を有するBsAbを設計した。huE71-huOKT3フォーマットの場合、重鎖はhuE71 IgG1のそれと同一であり、軽鎖は、huE71軽鎖をC-末端(G4S)3リンカー(配列番号:77)で延長することによって構築され、その後にhuOKT3 scFVが続いた。huE72-huOKT3は同様に設計された。両抗体のために、N297AおよびK322A変異がhIgG1 Fc領域に導入され、グリコシル化および補体活性化が除去された。BsAbの重鎖および軽鎖の両方をコードするDNAを哺乳動物発現ベクターに挿入してCHO-S細胞にトランスフェクトし、高発現を示す安定的なクローンを選別した。上清を振盪フラスコから収集し、プロテインA親和性クロマトグラフィーで精製した。サイズ排除クロマトグラフィーによって、90%を超えるモノマーまでタンパク質をさらに精製した。
還元SDS-PAGE条件下では、両BsAbは50KDa辺りに2本のバンドを生じた。なぜならば、軽鎖とのhuOKT3 scFv融合はMWを~50KDaに増加させたからでである。SEC-HPLCは、両抗体について約210KDaのMWを有する主要ピーク(UV分析で97%)を、マルチマーの小さなピーク(ゲルろ過で除去できる)とともに示した。SPRによってL1-CAMでアッセイしたとき、BsAbのL1-CAMに対する親和性は、親のIgGのそれに匹敵した(図37)。
これらの結果は、本技術の抗体またはその抗原結合フラグメントは、高い結合親和性でL1-CAMと特異的に結合することを示している。したがって、本明細書に開示する免疫グロブリン関係組成物はサンプルのL1-CAMタンパク質の検出に有用である。
両BsAbのL1-CAM-FcにおけるSPRによる結合カイネティクスが図28および37に示される。huE71-BsAbおよびhuE72-BsAbの標的細胞およびエフェクター細胞の双方との結合をFACS免疫染色によって試験した。huE71-BsAbは、L1-CAM(+)神経芽細胞腫BE(2)Cとの結合で親のhuE71と等しく有効であったが、huE72-BsAbとBE(2)Cとの結合はhuE71-BsAbで観察されたものの半分であった(図38(A))。CD3(+)T細胞との結合については、huE71-BsAbおよびhuE72-BsAbの両方がhuOKT3 IgG1と比較して有効性は低く、huOKT3よりおよそ20倍低かった(図38(B))。BsAbの軽鎖に係留したscFvのT細胞に対するアビディティーの低下は、部分的にはこのフォーマットの空間的拘束に起因するが、特に標的細胞が存在しないときにはサイトカイン放出を最小限するために有益である。
これらのデータは、CD3との結合は機能的に一価であったことを示唆し、これは腫瘍標的の非存在下ではT細胞の自発的活性化を阻む。
huE71-BsAbおよびhuE72-BsAbの両方が、細胞株IMR32-ルシフェラーゼを用いた活性化の24時間後に、PBMCからTh1サイトカイン(例えばTNFα)の遊離を誘発した。IFNγおよびIL2レベルは比較的低かった。huE71-BsAbおよびhuE72-BsAbの両方はまた、Th2サイトカイン(IL6およびIL10)遊離を誘発した。しかしながら、これらのサイトカインレベルはコントロールhu3F8-BsAbによって誘発されたレベルよりも低かった(図39(A)-(E))。
huE71-BsAbまたはhuE72-BsAbは、L1-CAM陽性癌細胞においてT細胞による細胞傷害を媒介した(前記癌細胞株は、活性化T細胞を用いて(E:T比=10:1)標準的な4時間51Cr放出アッセイで試験された)。両BsAbが腫瘍細胞に対してT細胞細胞傷害を誘発し、huE72-BsAbはhuE71-BsAbよりも強力であった(IMR32-ルシフェラーゼ細胞株を用いたEC50はそれぞれ50.0pMおよび62.9pM)(図40)。ヒト腫瘍細胞株の拡大パネル(神経芽細胞腫、メラノーマ、卵巣癌、乳癌、子宮頸腺癌腫を含む)を試験したとき、huE71-BsAbまたはhuE72-BsAb媒介T細胞細胞傷害は、FACSで評価した場合、L1-CAM発現腫瘍と相関性を有した(図41および図42(A)-42(B))。
in vivo治療試験のために、BALB-Rag2-KO-IL-2R-γc-KO(DKO)マウス(Koo GC et al., Expert Rev Vaccines 8:113-20, 2009;Andrade D et al., Arthritis Rheum 63:2764-73, 2011)を用いた。別々のヒト化マウス異種移植モデルで(皮下腫瘍+皮下エフェクター細胞、皮下腫瘍+静注エフェクター細胞)、静注L1-CAM-BsAbは、健常ドナーのPBMCの存在下で樹立腫瘍に対して高い活性を示した。
in vivo試験のために、L1-CAM(+)神経芽細胞腫患者由来異種移植片(PDX)(図3)をDKOマウスの皮下に移植した。HuE71-BsAbまたはhuE72-BsAb治療は、15日目(腫瘍が測定可能な時)に、5週間の間毎週2回注射の投与スケジュールを用いて開始した。PBMC(7.5x106)は、16日目に開始してその後3週間毎週静脈内に投与された。毎週腫瘍サイズを測定した。huE72-BsAbおよびPBMCで処置されたマウスはコントロールと等価の腫瘍増殖を有した。したがって、huE72-BsAbのin vivo抗腫瘍応答は、その高い結合親和性および優れたin vitro腫瘍殺滅能力にもかかわらず目覚ましいものではなかった。対照的に、huE71-BsAbはPBMCとともに腫瘍増殖を顕著に抑制した。
図44では、PDXの代わりに、IMR32神経芽細胞腫細胞株を用い、等しい数のPBMCと混合して皮下に植え付けた。huE71-BsAbまたはhuE71-IgGnは腫瘍増殖を顕著に抑制したが、一方、huE72-BsAbは腫瘍体積に影響を与えなかった。
SKOV3ヒト卵巣異種移植片を植え付けたヌードマウスを89Zr-huE71-IgG1nおよび89Zr-huE72-IgG1nを用いて画像化した(それぞれ図45および46)。huE72と比較してhuE71は親和性が低いにもかかわらず、89Zr-huE71-IgG1nのin vivo標的への誘導有効性は優れていた。
以下の試験は、ヒト化抗体Fc領域内の改変のin vivo生体分布における影響を評価する。ヒトでは4つのIgG抗体サブクラス(IgG1、IgG2、IgG3およびIgG4)が存在し、それらはさらにサブタイプに分けられる。加えて、IgG抗体と結合する数タイプのFc受容体が存在する(すなわちFcガンマ受容体)。
Fcガンマ受容体はさらにまた複数のクラスに細分割され、それらは免疫細胞上で弁別的に発現され、Fcガンマ受容体IはIgG抗体に対して最高の親和性を有する(Nimmerjahn F, Ravetch JV. Nat Rev Immunol 8:34-47, 2008)。IgG1抗体はヒトでもっとも豊富であり、活性化Fcガンマ受容体に対して最高の親和性を有する(Bruhns P et al., Blood 113:3716-25, 2009)。加えて、IgGの糖部分またはグリコシル化状態は、Fcガンマ受容体との結合で大きな役割を果たす。具体的には、IgG1抗体の場合、定常領域のN297残基に付着している糖部分は抗体と相互作用し、そのFc結合特徴を変化させる(Sazinsky SL et al., Proc Natl Acad Sci U S A 105:20167-72, 2008)。この残基に付着する複合糖部分は、マンノースおよびN-アセチルグルコサミン(GlcNAc)を他の分枝糖(フコース、ガラクトースおよびシアル酸を含む)とともに含み、このグリコシル化部位の変更は結合に劇的な影響を与えることができる(Maverakis E et al., J Autoimmun 57:1-13, 2015;Arnold JN et al., Annu Rev Immunol 25:21-50, 2007)。これらの糖が完全に欠失したIgG抗体は、それらのFcR(n)親和性に影響を与えることなく顕著に低下したFcガンマ受容体結合を示す。他方、当該グリコシル部位からフコース残基を除去することは、Fcガンマ受容体に対するIgGの親和性を大いに増加させる(Maverakis E et al., J Autoimmun 57:1-13, 2015)。IgG1抗体はFcガンマ受容体に対して最高の親和性を有するが、IgG4抗体(ヒトではもっとも少ないIgGである)は、Fcガンマ受容体に対する親和性が顕著に低く、一般的には、調節性メカニズムとして免疫応答を弱める抗炎症性IgGと考えられている。理論に拘束されないが、この現象は、部分的には、ダイナミックなFabアーム交換として知られているIg4抗体の固有の特性によるものである(Van der Neut Kolfschoten M et al., Science 317:1554-7, 2007)。
放射性化学物質収量および比活性は、インスタント薄層クロマトグラフィー(ITLC)を用いEDTA(pH5.0、50mM)移動相で計算した。ここで、遊離89Zrは溶媒前端とともに泳動し、キレート化89Zrは基準線に留まった。抗体の全てについて放射性化学物質収量は95%より高く、抗体の全てについて放射性化学物質純度は、サイズ排除クロマトグラフィー(PD-10カラム)精製後に99%より高かった。全ての抗体について(89Zr-HuE71-4 変異型を除く)比活性は、放射能標識後6.18-6.89μCi/μgであった。89Zr-HuE71-4 変異型の最適な放射能標識の多くの試みにかかわらず、2.14μCi/μgを超える比活性は達成できず、これはMALDI-ToF MSデータと一致した(MALDI-ToF MSデータは89Zr-HuE71-4 変異型は最低の平均キレート数(0.63)を有することを示した)。
放射能標識後にこれらの抗体が標的と結合する能力の程度を決定するために、免疫反応性アッセイを実施した。簡単に記せば、89Zr-標識抗体を標的陽性卵巣癌細胞(SKOV3)と濃度を増加させながらインキュベートし続いて洗浄し、細胞結合活性を計数して免疫反応性画分の計算に用いた。これらの実験で、全ての抗体について85%を超える免疫反応性が得られ、具体的には以下のとおりであった:89Zr-HuE71-1 MAGEについては89.5±1.5%、89Zr-HuE71-1 WTについては93.1±2.2%、89Zr-HuE71-1 Aglycoについては85.8±2.9%、89Zr-HuE71-4 WTについては86.7±1.9%、89Zr-HuE71-4 変異型については88.6±2.8%(図48(A)-48(E))。トレーサーの全ての免疫反応性が互いの範囲内にあるので、放射性免疫複合体の画像化パターンおよび分布で観察され得るいずれの相違も、標的抗原(L1-CAM)とのそれらの結合能力における相違によるものではないと推定することができる。
89Zr-HuE71-1 MAGEについては(図45)、腫瘍組織におけるトレーサーの高い放射能濃度が、非標的器官における最小限の放射能とともに注射後24時間に観察された。心臓または大血管は観察できないので、トレーサーは迅速に血液プールから消失した。興味深いことに、動物の上方部分の4つの両側性構造物(灰色の矢印)が同様に高い放射能濃度を有するように見える。これらのPET陽性組織を採集し、それらは顎下および腋窩リンパ節と分かった。さらにまた、リンパ節の89Zr-HuE71-1 MAGE取込みは放射性トレーサーの注射後96時間まで持続した。89Zr-HuE71-1 WTを注射したSKOV-3異種移植片のPET画像は、24時間で腫瘍組織内の高いトレーサー取込みを示し、これは96時間まで蓄積し続けた(図49)。24時間で非常に強い高放射能濃度が肝臓に存在し、前記はその後96時間を通してわずかながら徐々に消失した。もう一度言えば、マウスの上方部分の4つのリンパ節は24時間にPETで明るく照らされ、下方リンパ節も同様であったが、それらは96時間を通してわずかに薄れたように見えた。
89Zr-HuE71-1 Aglyco画像では(図50)、24時間の腫瘍組織内にトレーサーの高い放射能濃度が観察され、それは96時間まで蓄積し続けた。血液プールのこのトレーサーによる活性は極めて高く、24時間では心臓、下降大動脈、および左右の総頸動脈で明瞭に可視化され得るが、この活性は注射後72時間までに迅速に消失した。IgG1放射能標識抗体のPET画像化データを基にして、89Zr-HuE71-1 Aglycoは、注射後24時間から96時間まで腫瘍組織が最高の放射能濃度を有し非標的組織は最小量の活性を有するという点でもっともすっきりした生体分布プロフィールを有する。
89Zr-HuE71-4 Mutant(変異型)の画像では(図52)、24時間でわずかな腫瘍の取り込みが観察され、前記は96時間にわたって徐々に蓄積され続けた。血液プールの活性が存在し、この事例では、前記は96時間を通して部分的に減少するように見えた。しかしながら、きわめて注目すべきことに、89Zr-HuE71-4 WTでは明瞭に観察された腎臓取込みが、89Zr-HuE71-4 変異型では存在しなかった。
この試験で画像化された最後のトレーサーは、非特異的コントロール抗体89Zr-HuCtrl-4 WTであった(図53)。全ての時点で、腫瘍組織内の活性は非常に小さく、抗体の標的(GD2)はSKOV-3細胞株で高度には発現されないという事実と一致する。肝臓の活性は、全ての時点を通して強い腎臓の活性と同様に観察できた。
IgG4トレーサーに関しては、高い腎臓取込みが野生型変種で観察された。このトレーサーのS228P変異は、いずれの時点でもそれがPETで可視化されない点まで腎臓取込みを減少させることができた。IgG4抗体は、以前に記載したように、ダイナミックなFab交換を受けてヒンジ領域で自発的に分解され(~75kDa構築物を形成する)、続いて他の半分分子と再結合され得る。理論に拘束されないが、野生型IgG4 L1-CAM抗体で観察される腎臓取込みはダイナミックFabアーム交換特性の二次作用であるかもしれない。なぜならば、S228P変異はこの腎臓蓄積が生じるのを妨害するからである。さらにまた、75kDaの半抗体は、25と50kDaフラグメントへの更なる縮小を受けて、腎臓内の糸球体の通過を可能にするかもしれない。非特異的89Zr-HuCtrl-4 WT IgG4抗体は腎組織内での高い蓄積を示し、このことは、IgG4腎取込み理論と一致する。
IgG4抗体については、89Zr-HuE71-4 WTは3.98±0.969%ID/グラムのリンパ節取込みを示し、一方、89Zr-HuE71-4 変異型は3.70±0.975%ID/グラムのリンパ節取込みを示した(図56および57)。リンパ節内のこれら2つの抗体に関して有意な相違は認められなかった。89Zr-HuE71-4 WTは12.06±1.23%ID/グラムという値で腎臓に蓄積し、一方、89Zr-HuE71-4 変異型は5.83±0.537%ID/グラムで有意に低かった。これらのデータはPET画像診断データで観察されたものを概括し、さらにまたIgG4のダイナミックなFabアーム交換特性はトレーサーの腎臓取込みで役割を果たすと提唱している。
標的に対するこれらトレーサーの特異性を評価するために、ex vivo生体分布試験で封鎖群を用いた。50倍過剰のコールドトレーサーを放射能標識トレーサーとともに尾静脈から共同注射した。理論では、コールドトレーサーの添加はホットトレーサーの特異性を劇的に低下させ、ホットトレーサーの取り込みに有意な減少が観察されよう。これは、5つのL1-CAM標的抗体の全てについて観察された。腫瘍組織の取込み値は、89Zr-HuE71-1 MAGEについては16.15±0.85%ID/グラムから5.87±0.76%ID/グラムに、89Zr-HuE71-1 WTについては19.67±1.23%ID/グラムから6.82±0.809%ID/グラムに、89Zr-HuE71-1 Aglycoについては32.02±2.99%ID/グラムから10.58±1.52%ID/グラムに、89Zr-HuE71-4 WTについては27.29±1.55%ID/グラムから10.65±0.472%ID/グラムに、89Zr-HuE71-4 変異型については16.90±1.21%ID/グラムから9.04±1.42%ID/グラムに減少した。89Zr-HuCtrl-4 WT(このモデルの非特異的抗体)の場合、腫瘍取込みは6.02±0.90%ID/グラムで極めて低かった。腫瘍組織におけるこの取込みは、透過性亢進および保持(EPR)効果に起因し得る。以下を参照されたい:Heneweer C et al., J Nucl Med 52:625-33, 2011。
177 Lu放射性免疫療法試験:上記で提示したように、89Zr-HuE71-1 Aglycoは、低いバックグラウンド組織(特に腎臓および血液)取り込みとともに、注射後96時間で32.02±2.99%ID/グラムという高い腫瘍活性濃度を示した。89Zr-HuE71-1 Aglycoを金属性核種177Luで標識した(理由は、その放射性化学特性(半減期、6.7日;平均飛程、0.2mm;%β=100)、並びに画像診断および放射性免疫療法応用における177Luの広範囲使用である)。HuE71-1 Aglyco抗体をDOTAと複合体化し、3.94 mCi/mgの比活性の177Lu(放射性化学純度>99%)で標識し、SKOV3皮下腫瘍を有する雌無胸腺ヌードマウスでの画像診断試験およびex vivo生体分布試験に付した(図59(A)-59(C))。これらの試験は、89Zr-HuE71-1 Aglycoで観察された生体分布プロフィールと類似のプロフィールを確認し(活性の大半は、SPECT/CT画像およびチェレンコフ画像で観察されるように腫瘍組織に局在する)、注射後168時間のex vivo生体分布を確認した。
放射性免疫療法剤としての177Lu-HuE71-1 Aglycoの有効性を、3用量(800μCi、800μCi分割(14日ずらして2用量)、および400μCi)で評価し、同じ動物モデル(n=8-9/グループ)でコールド抗体(800μCiの非特異性抗体コントロール)および食塩水と比較した(図60)。80日間(最初の処置後60日間)を通して平均腫瘍体積を追跡して、有意な弁別的応答がコントロールグループと放射性標識治療グループとの間で観察された。とりわけ、コントロールグループのいずれも出発体積を超える腫瘍退縮の形跡を示さなかった。177Lu-HuE71-1 Aglycoの3グループは、接種後80日間を通して有意な増殖遅延効果を示した。しかしながら、試験の後期時点の間の腫瘍体積に関しては、177Lu-HuE71-1 Aglycoグループ内で有意な相違は存在せず、3つのグループの平均腫瘍体積は80日目で誤差範囲内で等価であった。加えて、毒性徴候(80%を超える体重低下および点状出血)が、最高処置グループ(800μCi、177Lu-HuE71-1 Aglyco)のマウスで処置から最初の2週間以内に4/8で観察された。毒性は、800μCiの非特異的コントロール抗体を注射したマウスでは全く観察されず、これはおそらくトレーサーの除去/排除における相違のためであろう。これらのデータは、400μCi 177Lu-HuE71-1 Aglycoの単一線量が、毒性の問題を回避しながらこのモデルでは腫瘍増殖を遅延させるために十分であることを提唱している。
総合すれば、これらの結果は、本技術の抗体または抗原結合フラグメントは、腫瘍を検出できること、および腫瘍増殖の進行および/または転移を阻害できることを示す。したがって、本明細書で開示する免疫グロブリン関係組成物は、その必要がある対象動物でL1-CAM陽性癌を検出および治療するために有用である。
本技術は、本明細書で記載した特定の実施態様の言葉に限定されるべきではなく、それら実施態様は、本技術の個々の特徴の単一の例示として意図される。当業者には明白であるように、本技術の趣旨および範囲を外れることなく、本技術の多くの改変および変型が実施され得る。本明細書に列挙したものの他に、本技術の範囲内の機能的に等価の方法および装置は前述の記載から当業者には明白であろう。そのような改変および変型は本技術の範囲内であることが意図される。本技術は、特定の方法、試薬、化合物、組成物、または生物学的な系に制限されず、当然それらは変動し得ることは理解されるべきである。本明細書で用いられる用語は特定の実施態様を説明する目的のためであり、制限することを意図しないこともまた理解されるべきである。
加えて、本開示の特色または特徴がマーカッシュグループに関して記載されている場合、当該開示はまた、それによってマーカッシュグループのメンバーの個々のメンバーまたはサブグループに関して記載されていることは当業者には理解されよう。
当業者には理解されるように、任意の目的および全ての目的のために、特に書面による説明を提供する場合には、本明細書に開示される全ての範囲はまた、任意のおよび全ての可能な部分範囲およびその部分範囲の組合せを包含する。列挙されたいずれの範囲も、十分に記載され、同じ範囲を少なくとも同じ半分、1/3、1/4、1/5、1/10などに分解することが可能であることは容易に理解されよう。非限定的な例として、本明細書で考察される各範囲は、下方の3/1、真ん中の1/3、上方の1/3などに容易に分解することができる。当業者にはまた理解されるように、例えば、“まで”、“少なくとも”、“を超える”、“未満”などの言葉はいずれも列挙された数を含み、さらに上記で考察したように続いて部分範囲に分解することができる範囲を指す。最後に、当業者には理解されるように、範囲は個々のメンバーの各々を含む。したがって、例えば1-3つの細胞を含むグループは、1、2または3つの細胞を含むグループを指す。同様に、1-5つの細胞を含むグループは、1、2、3、4または5つの細胞を含むグループを指し、以下同様である。
本明細書で参照または引用した全ての特許、特許出願、仮特許出願、および公開物は、参照によってその全体(全ての図および表を含む)が本明細書に、本出願の明快な教示と一致する範囲まで含まれる。
Claims (25)
- 重鎖免疫グロブリン可変ドメイン(VH)および軽鎖免疫グロブリン可変ドメイン(VL)を含む、抗L1-CAM抗体またはその抗原結合フラグメントであって、
(a)前記VHが、GYTFTSYWMQ(配列番号:53)のVH-CDR1配列、EINPSNGRTNYNEMFKS(配列番号:54)のVH-CDR2配列、およびYDGYYAMDY(配列番号:55)のVH-CDR3配列を含み;および
(b)前記VLが、KSSQSLLYSSNQKNYLA(配列番号:56)のVL-CDR1配列、WASTRES(配列番号:57)のVL-CDR2配列、およびQQYHSYPFT(配列番号:58)のVL-CDR3配列を含む、
前記抗体またはその抗原結合フラグメント。 - さらにまた、IgG1、IgG2、IgG3、IgG4、IgA1、IgA2、IgM、IgD、およびIgEから成る群から選択されるアイソタイプのFcドメインを含む、請求項1に記載の抗L1-CAM抗体またはその抗原結合フラグメント。
- Fab、F(ab’)2、Fab’、scFv、およびFvから成る群から選択される、請求項1に記載の抗原結合フラグメント。
- 以下から成る群から選択されるHCアミノ酸配列およびLCアミノ酸配列を含む抗L1-CAM抗体:
配列番号:9および配列番号:13(huE71 H1/L1);
配列番号:9および配列番号:14(huE71 H1/L2);
配列番号:10および配列番号:13(huE71 H2/L1);
配列番号:10および配列番号:14(huE71 H2/L2);
配列番号:17および配列番号:21(huE72 H1/L1);
配列番号:17および配列番号:22(huE72 H1/L2);
配列番号:18および配列番号:21(huE72 H2/L1);
配列番号:18および配列番号:22(huE72 H2/L2);
配列番号:26および配列番号:25(chE71 IgG1);
配列番号:30および配列番号:29(chE72 IgG1);
配列番号:42および配列番号:41(chE71 IgG4);
配列番号:46および配列番号:45(huE71 IgG4);
配列番号:49および配列番号:50(huE71 BsAb);並びに
配列番号:51および配列番号:52(huE72 BsAb)。 - 配列番号:9および配列番号:13 (huE71 H1/L1);
配列番号:9および配列番号:14 (huE71 H1/L2);
配列番号:10および配列番号:13 (huE71 H2/L1);
配列番号:10および配列番号:14 (huE71 H2/L2);
配列番号:17および配列番号:21 (huE72 H1/L1);
配列番号:17および配列番号:22 (huE72 H1/L2);
配列番号:18および配列番号:21 (huE72 H2/L1);または
配列番号:18および配列番号:22 (huE72 H2/L2)
に存在する重鎖免疫グロブリン可変ドメイン配列および軽鎖免疫グロブリン可変ドメイン配列のそれぞれと同一である重鎖免疫グロブリン可変ドメイン配列および軽鎖免疫グロブリン可変ドメイン配列、を含む抗L1-CAM抗体またはその抗原結合フラグメント。 - 以下を含む、請求項1記載の抗L1-CAM抗体またはその抗原結合フラグメント:
(a)配列番号:13、14、25、41、45または50のいずれか1つに存在するLC配列と少なくとも95%同一であるLC配列、および
(b)配列番号: 9、10、26、42、46または49のいずれか1つに存在するHC配列と少なくとも95%同一であるHC配列。 - キメラ抗体、ヒト化抗体、または二重特異性抗体である、請求項1-6のいずれか1項に記載の抗L1-CAM抗体またはその抗原結合フラグメント。
- 配列番号:74または配列番号:75の連続する少なくとも5つから8つのアミノ酸残基を含むL1-CAMタンパク質のエピトープと結合し、および/またはα-1,6-フコース改変を欠く、請求項1-7のいずれか1項に記載の抗L1-CAM抗体またはその抗原結合フラグメント。
- N297AおよびK322Aから成る群から選択される1つ以上のアミノ酸置換を含むIgG1定常領域を含む、または、S228P変異を含むIgG4定常領域を含む、請求項1-8のいずれか1項に記載の抗L1-CAM抗体またはその抗原結合フラグメント。
- 請求項1-9のいずれか1項に記載の抗L1-CAM抗体またはその抗原結合フラグメントをコードする組換え核酸。
- 配列番号:11および配列番号:15 (huE71 H1/L1);
配列番号:11および配列番号:16 (huE71 H1/L2);
配列番号:12および配列番号:15 (huE71 H2/L1);
配列番号:12および配列番号:16 (huE71 H2/L2);
配列番号:19および配列番号:23 (huE72 H1/L1);
配列番号:19および配列番号:24 (huE72 H1/L2);
配列番号:20および配列番号:23 (huE72 H2/L1);
配列番号:20および配列番号:24 (huE72 H2/L2);
配列番号:28および配列番号:27 (chE71 IgG1);
配列番号:32および 配列番号:31 (chE72 IgG1);
配列番号:44および配列番号:43 (chE71 IgG4);および
配列番号:48および配列番号:47 (huE71 IgG4)、
から成る群から選択される、請求項10記載の組換え核酸。 - 請求項10または11に記載の組換え核酸を含む宿主細胞またはベクター。
- 請求項1-9のいずれか1項に記載の抗L1-CAM抗体またはその抗原結合フラグメント、および医薬的に許容できる担体を含む組成物。
- 抗L1-CAM抗体またはその抗原結合フラグメントが同位体、色素、色原体、造影剤、薬物、毒素、サイトカイン、酵素、酵素阻害剤、ホルモン、ホルモンアンタゴニスト、成長因子、放射性核種、金属、リポソーム、ナノ粒子、RNA、DNAまたは前記の任意の組合せから成る群から選択される薬剤と複合体化される、請求項13記載の組成物。
- T細胞、B細胞、骨髄性細胞、形質細胞または肥満細胞と結合する、または、CD3、CD4、CD8、CD20、CD19、CD21、CD23、CD46、CD80、HLA-DR、CD74、CD22、CD14、CD15、CD16、CD123、TCRガンマ/デルタ、NKp46、KIR、または小分子DOTAハプテンと結合する、請求項7に記載の二重特異性抗体。
- 対象動物においてL1-CAM関連癌を治療するための組成物であって、以下から成る群から選択されるHCアミノ酸配列およびLCアミノ酸配列を含む抗L1-CAM抗体の有効量を含み、ここで、当該抗L1-CAM抗体が、L1-CAMと特異的に結合し、L1-CAM活性を中和する、前記組成物:
配列番号:9および配列番号:13(huE71 H1/L1);
配列番号:9および配列番号:14(huE71 H1/L2);
配列番号:10および配列番号:13(huE71 H2/L1);
配列番号:10および配列番号:14(huE71 H2/L2);
配列番号:17および配列番号:21(huE72 H1/L1);
配列番号:17および配列番号:22(huE72 H1/L2);
配列番号:18および配列番号:21(huE72 H2/L1);
配列番号:18および配列番号:22(huE72 H2/L2);
配列番号:26および配列番号:25(chE71 IgG1);
配列番号:30および配列番号:29(chE72 IgG1);
配列番号:42および配列番号:41(chE71 IgG4);
配列番号:46および配列番号:45(huE71 IgG4);
配列番号:49および配列番号:50(huE71 BsAb);並びに
配列番号:51および配列番号:52(huE72 BsAb)。 - L1-CAM関連癌が、白血病、ユーイング肉腫、神経芽細胞腫、骨肉腫、多形性神経膠芽腫、卵巣癌、子宮内膜癌、子宮癌、三陰性乳癌、メラノーマ、明細胞腎細胞癌、褐色細胞腫および傍神経節腫、中皮腫、小細胞肺癌(SCLC)、非小細胞肺癌(NSCLC)、膵管癌、結腸癌、膵臓癌、肝細胞癌腫、胃癌、胆管癌腫、カルチノイド、神経内分泌腫瘍、胃腸管間質腫(GIST)、褐色細胞腫、神経膠腫、膵臓の神経外胚葉癌、膵臓の腺癌腫、結腸直腸癌、腎細胞癌腫、血管腫、軟骨肉腫、食道の腺癌腫、乏突起神経膠腫、星状細胞腫、上衣腫、膵臓の神経内分泌癌腫、副腎腺腫、平滑筋肉腫、脂肪肉腫、卵巣の顆粒細胞腫瘍、シュワン細胞腫、原始神経外胚葉腫瘍(PNET)、類上皮肉腫、鼻腔神経芽細胞腫、髄芽腫、毛細血管腫、カポジ肉腫、横紋筋肉腫、顎下腺の癌、または頭頸部の扁平上皮癌腫である、請求項16に記載の組成物。
- 抗L1-CAM抗体が、追加の治療薬剤と別々に、逐次的に、または同時に対象動物に投与されるように処方されている、請求項16または17に記載の組成物。
- 追加の治療薬剤が、アルキル化剤、白金剤、タキサン、ビンカ剤、抗エストロゲン薬、アロマターゼ阻害剤、卵巣抑制剤、VEGF/VEGFR阻害剤、EGF/EGFR阻害剤、PARP阻害剤、細胞増殖抑制アルカロイド、細胞傷害性抗生物質、抗代謝剤、内分泌/ホルモン剤、ビスホスホネート療法剤の1つ以上である、請求項18に記載の組成物。
- 請求項1-9のいずれか1項に記載の抗L1-CAM抗体を含む、対象動物の腫瘍をin vivoで検出するための組成物であって、前記検出が、
(a)請求項1-9のいずれか1項に記載の抗L1-CAM抗体の有効量を対象動物に投与する工程(ここで当該抗L1-CAM抗体はL1-CAMを発現する腫瘍に局在するように構成され、かつ放射性同位体で標識される)、および
(b)抗L1-CAM抗体によって放射される、参照値よりも高い放射能レベルを検出することによって対象動物で腫瘍の存在を検出する工程、
を含む、前記組成物。 - 対象動物が癌と診断されるか、癌を有すると疑われる、請求項20に記載の組成物。
- 抗L1-CAM抗体によって放射される放射能レベルが、陽電子放射断層撮影法または単光子放射コンピュータ断層撮影法を用いて検出される、請求項20または21に記載の組成物。
- さらにまた、放射性核種と複合体化させた請求項1-9のいずれか1項に記載の抗L1-CAMkout抗体を含む免疫複合体を含む、請求項20に記載の組成物。
- 放射性核種が、アルファ粒子放射同位体、ベータ粒子放射同位体、オージェ-エミッター、または前記の任意の組合せである、請求項23に記載の組成物。
- ベータ粒子放射同位体が、86Y、90Y、89Sr、165Dy、186Re、188Re、177Lu、および67Cuから成る群から選択される、請求項24に記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762520382P | 2017-06-15 | 2017-06-15 | |
| US62/520,382 | 2017-06-15 | ||
| PCT/US2018/037645 WO2018232188A1 (en) | 2017-06-15 | 2018-06-14 | Anti-l1-cam antibodies and uses thereof |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020523029A JP2020523029A (ja) | 2020-08-06 |
| JP2020523029A5 JP2020523029A5 (ja) | 2021-07-26 |
| JP7353187B2 true JP7353187B2 (ja) | 2023-10-05 |
Family
ID=64660699
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019569397A Active JP7353187B2 (ja) | 2017-06-15 | 2018-06-14 | 抗l1-cam抗体およびその使用 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US11597764B2 (ja) |
| EP (1) | EP3638299A4 (ja) |
| JP (1) | JP7353187B2 (ja) |
| CN (1) | CN111093693B (ja) |
| CA (1) | CA3067351A1 (ja) |
| IL (1) | IL271398A (ja) |
| WO (1) | WO2018232188A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2994951A1 (en) | 2015-08-07 | 2017-02-16 | Imaginab, Inc. | Antigen binding constructs to target molecules |
| MX2020013923A (es) | 2018-06-29 | 2021-03-29 | Apitbio Inc | Anticuerpos anti molécula de adhesión celular l1 (l1cam) y usos de estos. |
| US20220177581A1 (en) * | 2019-03-11 | 2022-06-09 | Memorial Sloan Kettering Cancer Center | Cd22 antibodies and methods of using the same |
| CN114558122B (zh) * | 2022-04-27 | 2023-02-21 | 北京肿瘤医院(北京大学肿瘤医院) | 放射核素标记的过氧化氢酶及其应用 |
| TW202421652A (zh) * | 2022-09-21 | 2024-06-01 | 瑞士商艾爾瑟拉股份有限公司 | 結合至l1cam之新穎結合分子 |
| WO2024100200A1 (en) | 2022-11-09 | 2024-05-16 | Cis Pharma Ag | Anti-l1-cam antibodies and their uses for diagnostic and therapeutic applications |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130189287A1 (en) | 2011-12-23 | 2013-07-25 | Paul Scherrer Institut | Enzymatic conjugation of polypeptides |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6972323B1 (en) | 1997-04-01 | 2005-12-06 | Sankyo Company, Limited | Anti-Fas antibodies |
| EP2380908A1 (en) | 2006-06-02 | 2011-10-26 | Aveo Pharmaceuticals, Inc. | Hepatocyte growth factor (hgf) binding proteins |
| BRPI0715844A2 (pt) | 2006-08-23 | 2013-11-26 | Korea Res Inst Of Bioscience | Composição farmacêutica para tratamento do colangiocarcinoma, método de inibição do crescimento ou invasão do colangiocarcinoma e método de tratamento do colangiocarcinoma |
| AU2008201871A1 (en) | 2008-04-16 | 2009-11-26 | Deutsches Krebsforschungszentrum Stiftung Des Oeffentlichen Rechts | Inhibition of angiogenesis and tumor metastasis |
| KR101501736B1 (ko) * | 2008-12-05 | 2015-03-12 | 한국생명공학연구원 | 인간 및 마우스에서 발현하는 l1cam에 특이적으로 결합하는 재조합 단일클론항체 및 그 이용 |
| RU2627163C2 (ru) | 2009-11-24 | 2017-08-03 | Алетиа Байотерапьютикс Инк. | Антикластериновые антитела и антигенсвязывающие фрагменты и их использование для уменьшения объема новообразований |
| SG190362A1 (en) | 2010-11-24 | 2013-06-28 | Glaxo Group Ltd | Multispecific antigen binding proteins targeting hgf |
| CA2828289C (en) * | 2011-03-29 | 2020-07-21 | Roche Glycart Ag | Antibody fc variants |
| KR101504039B1 (ko) | 2012-11-16 | 2015-03-19 | 강원대학교산학협력단 | 인간 및 마우스 l1cam 단백질에 특이적으로 결합하는 항체 및 이의 용도 |
| CN105849120A (zh) | 2013-10-06 | 2016-08-10 | 美国卫生和人力服务部 | 修饰的假单胞菌外毒素a |
-
2018
- 2018-06-14 EP EP18818419.6A patent/EP3638299A4/en active Pending
- 2018-06-14 US US16/622,274 patent/US11597764B2/en active Active
- 2018-06-14 CA CA3067351A patent/CA3067351A1/en active Pending
- 2018-06-14 WO PCT/US2018/037645 patent/WO2018232188A1/en unknown
- 2018-06-14 JP JP2019569397A patent/JP7353187B2/ja active Active
- 2018-06-14 CN CN201880052266.7A patent/CN111093693B/zh active Active
-
2019
- 2019-12-12 IL IL271398A patent/IL271398A/en unknown
-
2023
- 2023-03-06 US US18/179,159 patent/US20240002501A1/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130189287A1 (en) | 2011-12-23 | 2013-07-25 | Paul Scherrer Institut | Enzymatic conjugation of polypeptides |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2020523029A (ja) | 2020-08-06 |
| EP3638299A1 (en) | 2020-04-22 |
| CA3067351A1 (en) | 2018-12-20 |
| US20200199224A1 (en) | 2020-06-25 |
| EP3638299A4 (en) | 2021-03-31 |
| WO2018232188A1 (en) | 2018-12-20 |
| US11597764B2 (en) | 2023-03-07 |
| CN111093693A (zh) | 2020-05-01 |
| IL271398A (en) | 2020-01-30 |
| CN111093693B (zh) | 2024-08-09 |
| US20240002501A1 (en) | 2024-01-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7353187B2 (ja) | 抗l1-cam抗体およびその使用 | |
| JP7303802B2 (ja) | A33抗体組成物および放射性免疫療法におけるその使用方法 | |
| US20230212289A1 (en) | Anti-cd3 antibodies and uses thereof | |
| US20220177581A1 (en) | Cd22 antibodies and methods of using the same | |
| US20220251192A1 (en) | Anti-cd33 antibodies for treating cancer | |
| CN114502584A (zh) | Cd33抗体和使用所述抗体治疗癌症的方法 | |
| JP2022546572A (ja) | 抗steap1抗体およびその使用 | |
| CN114341176A (zh) | Cd19抗体及其使用方法 | |
| KR20230070203A (ko) | 항-클라우딘 18.2 다중 특이적 항체 및 이의 용도 | |
| JP7386800B2 (ja) | 抗ポリシアル酸抗体およびその使用 | |
| US20240026037A1 (en) | Anti-gpa33 multi-specific antibodies and uses thereof | |
| CA3141614A1 (en) | Anti-glypican-3 antibodies and uses thereof | |
| US20230374150A1 (en) | Anti-psma antibodies and uses thereof | |
| EA046795B1 (ru) | Композиции на основе антител против a33 и способы их применения в радиоиммунотерапии | |
| EA045226B1 (ru) | Меченные радиоактивной меткой антитела против pd-l1 для иммуно-пэт визуализации |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210609 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210609 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220713 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220819 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20221003 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230113 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230406 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230703 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230821 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230919 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7353187 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |