JP7335877B2 - 共結晶、その医薬組成物、およびそれを伴う治療方法 - Google Patents
共結晶、その医薬組成物、およびそれを伴う治療方法 Download PDFInfo
- Publication number
- JP7335877B2 JP7335877B2 JP2020524501A JP2020524501A JP7335877B2 JP 7335877 B2 JP7335877 B2 JP 7335877B2 JP 2020524501 A JP2020524501 A JP 2020524501A JP 2020524501 A JP2020524501 A JP 2020524501A JP 7335877 B2 JP7335877 B2 JP 7335877B2
- Authority
- JP
- Japan
- Prior art keywords
- compound
- pharmaceutical composition
- crystal
- formula
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/145—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C57/00—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms
- C07C57/02—Unsaturated compounds having carboxyl groups bound to acyclic carbon atoms with only carbon-to-carbon double bonds as unsaturation
- C07C57/13—Dicarboxylic acids
- C07C57/145—Maleic acid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C59/00—Compounds having carboxyl groups bound to acyclic carbon atoms and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C59/235—Saturated compounds containing more than one carboxyl group
- C07C59/245—Saturated compounds containing more than one carboxyl group containing hydroxy or O-metal groups
- C07C59/265—Citric acid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
ある特定の癌細胞内に存在するIDH2の変異が結果として酵素の新たな能力をもたらし、α-ケトグルタル酸からR(-)-2-ヒドロキシグルタル酸(2HG)へのNADPH依存的還元を触媒することが発見された。2HGは、野生型IDH2によって形成されない。2HGの産生は、癌の形成および進行に寄与すると考えられる(Dang,L et al,Nature 2009,462:739-44)。
米国公開第2015/0018328 A1号は、化学名6-(6-クロロピリジン-2-イル)-N2,N4-ビス((R)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンによって記載される化合物を開示しており、該化合物は、生化学的アッセイおよび細胞アッセイにおいて、変異体IDH1およびIDH2タンパク質の阻害剤として作用することが示されている。
特定の実施形態では、例えば、以下が提供される:
(項目1)
式(I)の化合物と、
クエン酸と、を含む、共結晶。
(項目2)
前記共結晶が、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる、項目1に記載の共結晶。
(項目3)
前記X線粉末回折パターンが、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも2つのピーク位置を含む、項目1または2に記載の共結晶。
(項目4)
前記X線粉末回折パターンが、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、項目1~3のいずれか一項に記載の共結晶。
(項目5)
前記X線粉末回折パターンが、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも4つのピーク位置を含む、項目1~4のいずれか一項に記載の共結晶。
(項目6)
前記X線粉末回折パターンが、5.7および8.4の度2シータ(±0.2度2シータ)におけるピーク位置、ならびに11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、少なくとも3つのピーク位置を含む、項目1~5のいずれか一項に記載の共結晶。
(項目7)
前記共結晶が、170.6℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、項目1~6のいずれか一項に記載の共結晶。
(項目8)
水をさらに含む、項目1~7のいずれか一項に記載の共結晶。
(項目9)
式(I)の前記化合物、クエン酸、および水が、2:1:1のモル比で存在する、項目1~8のいずれか一項に記載の共結晶。
(項目10)
前記共結晶が、単位セル当たり、式(I)の前記化合物の4つの分子、2つのクエン酸分子、および2つの水分子を含む、項目1~9のいずれか一項に記載の共結晶。
(項目11)
項目1~10のいずれか一項に記載の共結晶を含む、原薬。
(項目12)
前記原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N 2 -(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、(R)-6-(6-クロロピリジン-2-イル)-N 2 -エチル-N 4 -(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、(R)-6-(6-クロロピリジン-2-イル)-N 2 -イソプロピル-N 4 -(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、6-(6-クロロピリジン-2-イル)-N 2 ,N 4 -ビス((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、6-(6-クロロピリジン-2-イル)-N 2 -((R)-1,1,1-トリフルオロプロパン-2-イル)-N4-((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、(R)-4-(6-クロロピリジン-2-イル)-6-((1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-オール、(R)-4-クロロ-6-(6-クロロピリジン-2-イル)-N-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2-アミン、および6-(4,6-ビス(((R)-1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-イル)ピリジン-2-オールのうちのいずれかを含有する、項目11に記載の原薬。
(項目13)
治療有効量の項目1~10のいずれか一項に記載の共結晶、または項目11もしくは12に記載の原薬、および1つ以上の医薬賦形剤を含む、医薬組成物。
(項目14)
前記医薬組成物が、1~10%w/wの式(I)の前記化合物を含む、項目13に記載の医薬組成物。
(項目15)
前記医薬組成物が、20~30%w/wの式(I)の前記化合物を含む、項目13に記載の医薬組成物。
(項目16)
前記医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の前記化合物を含む、項目13~15のいずれか一項に記載の医薬組成物。
(項目17)
前記医薬組成物が、約10mgまたは約50mgの式(I)の前記化合物を含む、項目16に記載の医薬組成物。
(項目18)
式(I)の化合物と、
クエン酸と、を含む共結晶を調製する方法であって、
式(I)の前記化合物およびクエン酸を溶媒中に溶解して、溶液を得ることと、
前記共結晶を沈殿させることと、を含む、方法。
(項目19)
前記溶媒が、アセトニトリルまたはアセトンを含む、項目18に記載の方法。
(項目20)
前記沈殿が、前記溶液を冷却することを含む、項目18または19に記載の方法。
(項目21)
前記沈殿が、前記溶液から前記溶媒の一部分を蒸発させることを含む、項目18~20のいずれか一項に記載の方法。
(項目22)
前記沈殿が、抗溶媒を前記溶液に添加することを含む、項目18~21のいずれか一項に記載の方法。
(項目23)
前記抗溶媒が、C 5~ C 12 アルカンまたはシクロアルカンを含む、項目22に記載の方法。
(項目24)
前記抗溶媒が、トルエンまたはMTBEを含む、項目22に記載の方法。
(項目25)
前記沈殿が、前記溶液に前記共結晶の結晶を播種することを含む、項目18~24のいずれか一項に記載の方法。
(項目26)
前記共結晶を単離することをさらに含む、項目18~25のいずれか一項に記載の方法。
(項目27)
IDH1またはIDH2変異の存在によって特徴付けられる癌を治療することを必要としている患者において、それを行う方法であって、治療有効量の項目1~10のいずれか一項に記載の共結晶、項目11もしくは12のいずれか一項に記載の原薬、または項目13~17のいずれか一項に記載の医薬組成物を前記患者に投与することを含む、方法。
(項目28)
前記癌が、IDH1変異の存在によって特徴付けられる、項目27に記載の方法。
(項目29)
前記IDH1変異が、R132X変異である、項目28に記載の方法。
(項目30)
前記IDH1変異が、R132HまたはR132C変異である、項目28に記載の方法。
(項目31)
前記IDH1変異が、前記患者におけるR(-)-2-ヒドロキシグルタル酸の蓄積をもたらす、項目28~30のいずれか一項に記載の方法。
(項目32)
前記癌が、IDH2変異の存在によって特徴付けられる、項目27に記載の方法。
(項目33)
前記IDH2変異が、R140X変異である、項目32に記載の方法。
(項目34)
前記IDH2変異が、R140Q、R140W、またはR140L変異である、項目32に記載の方法。
(項目35)
前記IDH2変異が、R172X変異である、項目32に記載の方法。
(項目36)
前記IDH2変異が、R172KまたはR172G変異である、項目32に記載の方法。
(項目37)
前記IDH2変異が、前記患者におけるR(-)-2-ヒドロキシグルタル酸の蓄積をもたらす、項目32~36のいずれか一項に記載の方法。
(項目38)
IDH1変異およびIDH2変異の存在によって特徴付けられる癌を治療することを必要としている患者において、それを行う方法であって、治療有効量の項目1~10のいずれか一項に記載の共結晶、項目11もしくは12のいずれか一項に記載の原薬、または項目13~17のいずれか一項に記載の医薬組成物を前記患者に投与することを含む、方法。
(項目39)
前記癌が、神経膠腫、急性骨髄性白血病、肉腫、黒色腫、非小細胞肺癌(NSCLC)、胆管癌、軟骨肉腫、骨髄異形成症候群(MDS)、骨髄増殖性腫瘍(MPN)、結腸癌、および血管免疫芽球性非ホジキンリンパ腫(NHL)から選択される、項目27~38のいずれか一項に記載の方法。
(項目40)
前記癌が、神経膠腫である、項目27~39のいずれか一項に記載の方法。
(項目41)
前記神経膠腫が、低悪性度神経膠腫または二次性の高悪性度神経膠腫である、項目40に記載の方法。
(項目42)
前記神経膠腫が、二次性の高悪性度神経膠腫であり、前記二次性の高悪性度神経膠腫が、膠芽腫である、項目40または41に記載の方法。
(項目43)
前記癌が、難治性または再発性である、項目27~42のいずれか一項に記載の方法。
(項目44)
前記癌が、新たに診断されたか、または以前に治療されていない、項目27~42のいずれか一項に記載の方法。
(項目45)
追加的療法を前記患者に併用投与することをさらに含む、項目27~44のいずれか一項に記載の方法。
(項目46)
前記患者が、前記癌のための癌治療を以前に投与されている、項目27~45のいずれか一項に記載の方法。
(項目47)
前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、1日当たり約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの量で投与される、項目27~46のいずれか一項に記載の方法。
(項目48)
前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、1日当たり約10mgまたは約25mgの量で投与される、項目27~46のいずれか一項に記載の方法。
(項目49)
前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの量で1日2回投与される、項目27~46のいずれか一項に記載の方法。
(項目50)
前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、約10mgまたは約25mgの量で1日2回投与される、項目27~46のいずれか一項に記載の方法。
本開示はまた、本明細書に記載の式(I)の化合物の固体形態を含む原薬に関する。
本開示はまた、本明細書に記載される固体形態の不純物として存在し得る化合物に関する。そのような化合物は、本明細書に記載される固体形態(例えば、共結晶、原薬、結晶形態、および非晶質固体分散体)の純度を決定するための基準として有用である。
(R)-6-(6-クロロピリジン-2-イル)-N2-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、
(R)-6-(6-クロロピリジン-2-イル)-N2-エチル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、
(R)-6-(6-クロロピリジン-2-イル)-N2-イソプロピル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、
(R)-4-(6-クロロピリジン-2-イル)-6-((1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-オール、
(R)-4-クロロ-6-(6-クロロピリジン-2-イル)-N-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2-アミン、および
6-(4,6-ビス(((R)-1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-イル)ピリジン-2-オール、からなる群から選択される、化合物。
本開示はまた、式(I)の化合物として識別される化学構造の互変異性体に関する。そのような互変異性体には、以下が含まれる。
またはその薬学的に許容可能な塩である、化合物に関する。
またはその薬学的に許容可能な塩である、化合物。
またはその薬学的に許容可能な塩である、化合物。
またはその薬学的に許容可能な塩である、化合物。
式(I)の化合物の固体形態を調製する方法
式(I)の化合物およびクエン酸を溶媒中に溶解して、溶液を得ることと、
共結晶を沈殿させることと、を含む。
式(I)の化合物およびマレイン酸を溶媒中に溶解して、溶液を得ることと、
共結晶を沈殿させることと、を含む。
式(I)の化合物を酢酸エチル中に溶解して、溶液を得ることと、
結晶形態を沈殿させることと、を含む。
式(I)の化合物をメチルイソブチルケトン中に溶解して、溶液を得ることと、
結晶形態を沈殿させることと、を含む、方法。
式(I)の化合物をジオキサン中に溶解して、溶液を得ることと、
結晶形態を沈殿させることと、を含む、方法。
別の態様では、本開示は、本明細書の実施形態のいずれかに記載される固体形態、原薬、または化合物もしくは薬学的に許容可能な塩と、1つ以上の医薬賦形剤とを含む、医薬組成物に関する。
別の態様では、本発明は、IDH1またはIDH2変異の存在によって特徴付けられる癌を治療することを、それを必要としている患者において行う方法に関し、治療有効量の、本明細書の実施形態のいずれかに記載される固体形態、原薬、または化合物もしくは薬学的に許容可能な塩、あるいはその医薬組成物を患者に投与することを含む。
いくつかの実施形態では、IDH1またはIDH2変異の存在によって特徴付けられる癌の治療を必要としている患者は、癌療法を以前に投与されている。いくつかの実施形態では、患者は、癌のための癌治療を以前に投与されている。以前に投与された癌療法は、癌の治療に有効であったか、もしくは効果的でなかった可能性があり、または癌の治療における一部の期間にわたって有効であった可能性がある。
いくつかの実施形態では、本明細書に記載される方法は、追加的療法を、それを必要としている患者に併用投与する追加的ステップを含む。
いくつかの実施形態では、本開示は、以下に関する。
1.式(I)の化合物と、
2.共結晶が、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる、実施形態1に記載の共結晶。
3.X線粉末回折パターンが、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも2つのピーク位置を含む、実施形態1または2に記載の共結晶。
4.X線粉末回折パターンが、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、実施形態1~3のいずれか1つに記載の共結晶。
5.X線粉末回折パターンが、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも4つのピーク位置を含む、実施形態1~4のいずれか1つに記載の共結晶。
6.X線粉末回折パターンが、5.7および8.4の度2シータ(±0.2度2シータ)におけるピーク位置、ならびに11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、少なくとも3つのピーク位置を含む、実施形態1~5のいずれか1つに記載の共結晶。
7.共結晶が、170.6℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、実施形態1~6のいずれか1つに記載の共結晶。
8.水をさらに含む、実施形態1~7のいずれか1つに記載の共結晶。
9.式(I)の化合物、クエン酸、および水が、2:1:1のモル比で存在する、実施形態1~8のいずれか1つに記載の共結晶。
10.共結晶が、単位セル当たり、式(I)の化合物の4つの分子、2つのクエン酸分子、および2つの水分子を含む、実施形態1~9のいずれか1つに記載の共結晶。
11.実施形態1~10のいずれか1つに記載の共結晶を含む、原薬。
12.原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N2-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態11に記載の原薬。
13.原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N2-エチル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態11または12に記載の原薬。
14.原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N2-イソプロピル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態11~13のいずれか1つに記載の原薬。
15.原薬が、1.0%以下(HPLCによる面積%)の6-(6-クロロピリジン-2-イル)-N2,N4-ビス((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態11~14のいずれか1つに記載の原薬。
16.原薬が、1.0%以下(HPLCによる面積%)の6-(6-クロロピリジン-2-イル)-N2-((R)-1,1,1-トリフルオロプロパン-2-イル)-N4-((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態11~15のいずれか1つに記載の原薬。
17.原薬が、1.0%以下(HPLCによる面積%)の(R)-4-(6-クロロピリジン-2-イル)-6-((1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-オールを含有する、実施形態11~16のいずれか1つに記載の原薬。
18.原薬が、1.0%以下(HPLCによる面積%)の(R)-4-クロロ-6-(6-クロロピリジン-2-イル)-N-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2-アミンを有する、実施形態11~17のいずれか1つに記載の原薬。
19.原薬が、1.0%以下(HPLCによる面積%)の6-(4,6-ビス(((R)-1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-イル)ピリジン-2-オールを含有する、実施形態11~18のいずれか1つに記載の原薬。
20.治療有効量の実施形態1~10のいずれか1つに記載の共結晶、または実施形態11~19のいずれか1つに記載の原薬と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
21.医薬組成物が、1~10%w/wの式(I)の化合物を含む、実施形態20に記載の医薬組成物。
22.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態20または21に記載の医薬組成物。
23.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態22に記載の医薬組成物。
24.医薬組成物が、20~30%w/wの式(I)の化合物を含む、実施形態20に記載の医薬組成物。
25.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態24に記載の医薬組成物。
26.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態25に記載の医薬組成物。
27.治療有効量の実施形態1~10のいずれか1つに記載の共結晶、または実施形態11~19のいずれか1つに記載の原薬を、1つ以上の医薬品賦形剤と混合して、医薬組成物を得ることを含む、プロセスによって調製された医薬組成物。
28.式(I)の化合物と、
式(I)の化合物およびクエン酸を溶媒中に溶解して、溶液を得ることと、
共結晶を沈殿させることと、を含む、方法。
29.溶媒が、アセトニトリルまたはアセトンを含む、実施形態28に記載の方法。
30.前述の沈殿が、溶液を冷却することを含む、実施形態28または29に記載の方法。
31.前述の沈殿が、溶液から溶媒の一部分を蒸発させることを含む、実施形態28~30のいずれか1つに記載の方法。
32.前述の沈殿が、抗溶媒を溶液に添加することを含む、実施形態28~31のいずれか1つに記載の方法。
33.抗溶媒が、C5~C12アルカンまたはシクロアルカンを含む、実施形態32に記載の方法。
34.抗溶媒が、トルエンまたはMTBEを含む、実施形態32に記載の方法。
35.前述の沈殿が、溶液に共結晶の結晶を播種することを含む、実施形態28~34のいずれか1つに記載の方法。
36.共結晶を単離することをさらに含む、実施形態28~35のいずれか1つに記載の方法。
37.式(I)の化合物と、
38.共結晶が、5.9、8.1、15.0、15.2、16.9、17.8、18.5、21.1、23.4、26.9、および28.2からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる、実施形態37に記載の共結晶。
39.X線粉末回折パターンが、5.9、8.1、15.0、15.2、16.9、17.8、18.5、21.1、23.4、26.9、および28.2からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも2つのピーク位置を含む、実施形態37または38に記載の共結晶。
40.X線粉末回折パターンが、5.9、8.1、15.0、15.2、16.9、17.8、18.5、21.1、23.4、26.9、および28.2からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、実施形態37~39のいずれか1つに記載の共結晶。
41.X線粉末回折パターンが、5.9、8.1、15.0、15.2、16.9、17.8、18.5、21.1、23.4、26.9、および28.2からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、実施形態37~39のいずれか1つに記載の共結晶。
42.X線粉末回折パターンが、8.1、17.8、および18.5の度2シータ(±0.2度2シータ)におけるピーク位置、ならびに5.9、15.0、15.2、16.9、21.1、23.4、26.9、および28.2からなる群から選択される、少なくとも3つのピーク位置を含む、実施形態37~41のいずれか1つに記載の共結晶。
43.共結晶が、91.2℃および128.4℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、実施形態37~42のいずれか1つに記載の共結晶。
44.式(I)の化合物およびクエン酸水が、1:1のモル比で存在する、実施形態37~43のいずれか1つに記載の共結晶。
45.治療有効量の実施形態37~44のいずれか1つに記載の共結晶と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
46.医薬組成物が、1~10%w/wの式(I)の化合物を含む、実施形態45に記載の医薬組成物。
47.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態45または46に記載の医薬組成物。
48.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態47に記載の医薬組成物。
49.医薬組成物が、20~30%w/wの式(I)の化合物を含む、実施形態45に記載の医薬組成物。
50.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態49に記載の医薬組成物。
51.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態50に記載の医薬組成物。
52.治療有効量の実施形態37~44のいずれか1つに記載の共結晶を、1つ以上の医薬品賦形剤と混合して、医薬組成物を得ることを含む、プロセスによって調製された医薬組成物。
53.式(I)の化合物と、
式(I)の化合物およびマレイン酸を溶媒中に溶解して、溶液を得ることと、
共結晶を沈殿させることと、を含む、方法。
54.溶媒が、アセトニトリルまたはアセトンを含む、実施形態53に記載の方法。
55.前述の沈殿が、溶液に共結晶の結晶を播種することを含む、実施形態53または54に記載の方法。
56.共結晶を単離することをさらに含む、実施形態53~55のいずれか1つに記載の方法。
57.式(I)の化合物の結晶形態であって、
58.X線粉末回折パターンが、11.7、12.8、14.2、17.8、19.8、20.7、21.8、22.2、および25.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも2つのピーク位置を含む、実施形態57に記載の結晶形態。
59.X線粉末回折パターンが、11.7、12.8、14.2、17.8、19.8、20.7、21.8、22.2、および25.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、実施形態57または58に記載の結晶形態。
60.X線粉末回折パターンが、11.7、12.8、14.2、17.8、19.8、20.7、21.8、22.2、および25.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも4つのピーク位置を含む、実施形態57~59のいずれか1つに記載の結晶形態。
61.X線粉末回折パターンが、11.7、17.8、および21.8の度2シータ(±0.2度2シータ)におけるピーク位置、ならびに12.8、14.2、19.8、20.7、22.2、および25.0からなる群から選択される、少なくとも3つのピーク位置を含む、実施形態57~60のいずれか1つに記載の結晶形態。
62.結晶形態が、221.9℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、実施形態57~61のいずれか1つに記載の結晶形態。
63.実施形態57~62のいずれか1つに記載の結晶形態を含む、原薬。
64.原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N2-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態63に記載の原薬。
65.原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N2-エチル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態63または64に記載の原薬。
66.原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N2-イソプロピル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態63~65のいずれか1つに記載の原薬。
67.原薬が、1.0%以下(HPLCによる面積%)の6-(6-クロロピリジン-2-イル)-N2,N4-ビス((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態63~66のいずれか1つに記載の原薬。
68.原薬が、1.0%以下(HPLCによる面積%)の6-(6-クロロピリジン-2-イル)-N2-((R)-1,1,1-トリフルオロプロパン-2-イル)-N4-((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミンを含有する、実施形態63~67のいずれか1つに記載の原薬。
69.原薬が、1.0%以下(HPLCによる面積%)の(R)-4-(6-クロロピリジン-2-イル)-6-((1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-オールを含有する、実施形態63~68のいずれか1つに記載の原薬。
70.原薬が、1.0%以下(HPLCによる面積%)の(R)-4-クロロ-6-(6-クロロピリジン-2-イル)-N-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2-アミンを有する、実施形態63~69のいずれか1つに記載の原薬。
71.原薬が、1.0%以下(HPLCによる面積%)の6-(4,6-ビス(((R)-1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-イル)ピリジン-2-オールを含有する、実施形態63~70のいずれか1つに記載の原薬。
72.治療有効量の実施形態57~62のいずれか1つに記載の結晶形態、または実施形態63~71のいずれか1つに記載の原薬と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
73.医薬組成物が、1~10%w/wの式(I)の化合物を含む、実施形態72に記載の医薬組成物。
74.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態72または73に記載の医薬組成物。
75.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態74に記載の医薬組成物。
76.医薬組成物が、20~30%w/wの式(I)の化合物を含む、実施形態72に記載の医薬組成物。
77.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態76に記載の医薬組成物。
78.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態77に記載の医薬組成物。
79.
治療有効量の実施形態57~62のいずれか1つに記載の結晶形態、または実施形態63~71のいずれか1つに記載の原薬を、1つ以上の医薬品賦形剤と混合して、医薬組成物を得ることを含む、プロセスによって調製された医薬組成物。
80.式(I)の化合物の結晶形態を調製する方法であって、
結晶形態を沈殿させることと、を含む、方法。
81.結晶形態を沈殿させることが、溶液にヘプタンを添加することを含む、実施形態80に記載の方法。
82.前述の沈殿が、溶液に結晶形態の結晶を播種することを含む、実施形態80または81に記載の方法。
83.結晶形態を単離することをさらに含む、実施形態80~82のいずれか1つに記載の方法。
84.式(I)の化合物の結晶形態であって、
85.X線粉末回折パターンが、11.9、13.2、15.5、17.8、18.6、20.8、23.2、23.9、および26.5からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも2つのピーク位置を含む、実施形態84に記載の結晶形態。
86.X線粉末回折パターンが、11.9、13.2、15.5、17.8、18.6、20.8、23.2、23.9、および26.5からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、実施形態84または85に記載の結晶形態。
87.X線粉末回折パターンが、11.9、13.2、15.5、17.8、18.6、20.8、23.2、23.9、および26.5からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも4つのピーク位置を含む、実施形態84~86のいずれか1つに記載の結晶形態。
88.X線粉末回折パターンが、11.9、17.8、および23.9の度2シータ(±0.2度2シータ)におけるピーク位置、ならびに13.2、15.5、18.6、20.8、23.2、および26.5からなる群から選択される、少なくとも3つのピーク位置を含む、実施形態84~87のいずれか1つに記載の結晶形態。
89.結晶形態が、221.5℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、実施形態84~88のいずれか1つに記載の結晶形態。
90.結晶形態が、無水である、実施形態84~89のいずれか1つに記載の結晶形態。
91.治療有効量の実施形態84~90のいずれか1つに記載の結晶形態と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
92.医薬組成物が、1~10%w/wの式(I)の化合物を含む、実施形態91に記載の医薬組成物。
93.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態91または92に記載の医薬組成物。
94.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態93に記載の医薬組成物。
95.医薬組成物が、20~30%w/wの式(I)の化合物を含む、実施形態91に記載の医薬組成物。
96.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態95に記載の医薬組成物。
97.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態96に記載の医薬組成物。
98.治療有効量の実施形態84~90のいずれか1つに記載の結晶形態を、1つ以上の医薬品賦形剤と混合して、医薬組成物を得ることを含む、プロセスによって調製された医薬組成物。
99.式(I)の化合物の結晶形態を調製する方法であって、
結晶形態を沈殿させることと、を含む、方法。
100.結晶形態を沈殿させることが、溶液にヘプタンを添加することを含む、実施形態99に記載の方法。
101.前述の沈殿が、溶液に結晶形態の結晶を播種することを含む、実施形態99または100に記載の方法。
102.結晶形態を単離することをさらに含む、実施形態99~101のいずれか1つに記載の方法。
103.式(I)の化合物の結晶形態であって、
104.X線粉末回折パターンが、8.6、10.5、18.2、20.2、21.1、および25.9からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも2つのピーク位置を含む、実施形態103に記載の結晶形態。
105.X線粉末回折パターンが、8.6、10.5、18.2、20.2、21.1、および25.9からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、実施形態103または104に記載の結晶形態。
106.X線粉末回折パターンが、8.6、10.5、18.2、20.2、21.1、および25.9からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも4つのピーク位置を含む、実施形態103~105のいずれか1つに記載の結晶形態。
107.X線粉末回折パターンが、8.6および21.1の度2シータ(±0.2度2シータ)におけるピーク位置、ならびに8.6、10.5、18.2、20.2、21.1、および25.9からなる群から選択される、少なくとも3つのピーク位置を含む、実施形態103~106のいずれか1つに記載の結晶形態。
108.結晶形態が、221.3℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、実施形態103~107のいずれか1つに記載の結晶形態。
109.結晶形態が、三水和物である、実施形態103~108のいずれか1つに記載の結晶形態。
110.治療有効量の実施形態103~109のいずれか1つに記載の結晶形態と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
111.医薬組成物が、1~10%w/wの式(I)の化合物を含む、実施形態110に記載の医薬組成物。
112.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態110または111に記載の医薬組成物。
113.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態112に記載の医薬組成物。
114.医薬組成物が、20~30%w/wの式(I)の化合物を含む、実施形態110に記載の医薬組成物。
115.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態114に記載の医薬組成物。
116.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態115に記載の医薬組成物。
117.治療有効量の実施形態103~109のいずれか1つに記載の結晶形態を、1つ以上の医薬品賦形剤と混合して、医薬組成物を得ることを含む、プロセスによって調製された医薬組成物。
118.式(I)の化合物の結晶形態を調製する方法であって、
結晶形態を沈殿させることと、を含む、方法。
119.結晶形態を沈殿させることが、溶液に水を添加することを含む、実施形態118に記載の方法。
120.前述の沈殿が、溶液に結晶形態の結晶を播種することを含む、実施形態118または119に記載の方法。
121.結晶形態を単離することをさらに含む、実施形態118~120のいずれか1つに記載の方法。
122.式(I)の化合物の結晶形態であって、
123.X線粉末回折パターンが、8.6、9.7、10.5、15.6、15.9、16.7、17.9、20.3、21.2、24.9、26.6、および27.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも2つのピーク位置を含む、実施形態122に記載の結晶形態。
124.X線粉末回折パターンが、8.6、9.7、10.5、15.6、15.9、16.7、17.9、20.3、21.2、24.9、26.6、および27.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも3つのピーク位置を含む、実施形態122または123に記載の結晶形態。
125.X線粉末回折パターンが、8.6、9.7、10.5、15.6、15.9、16.7、17.9、20.3、21.2、24.9、26.6、および27.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも4つのピーク位置を含む、実施形態122~124のいずれか1つに記載の結晶形態。
126.X線粉末回折パターンが、15.9、16.7、および21.2の度2シータ(±0.2度2シータ)におけるピーク位置、ならびに8.6、9.7、10.5、15.6、17.9、20.3、24.9、26.6、および27.0からなる群から選択される、少なくとも3つのピーク位置を含む、実施形態122~125のいずれか1つに記載の結晶形態。
127.結晶形態が、221.3℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、実施形態122~126のいずれか1つに記載の結晶形態。
128.結晶形態が、ジオキサン溶媒和物である、実施形態122~127のいずれか1つに記載の結晶形態。
129.治療有効量の実施形態122~128のいずれか1つに記載の結晶形態と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
130.医薬組成物が、1~10%w/wの式(I)の化合物を含む、実施形態129に記載の医薬組成物。
131.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態129または130に記載の医薬組成物。
132.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態131に記載の医薬組成物。
133.医薬組成物が、20~30%w/wの式(I)の化合物を含む、実施形態29に記載の医薬組成物。
134.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態133に記載の医薬組成物。
135.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態134に記載の医薬組成物。
136.治療有効量の実施形態122~128のいずれか1つに記載の結晶形態を、1つ以上の医薬品賦形剤と混合して、医薬組成物を得ることを含む、プロセスによって調製された医薬組成物。
137.式(I)の化合物と、
138.ポリマーが、HPMCASである、実施形態137に記載の非晶質固体分散体。
139.式(I)の化合物およびHPMCASが、約1:1の重量比で存在する、実施形態138に記載の非晶質固体分散体。
140.式(I)の化合物の非晶質固体分散体を調製する方法であって、
混合物を噴霧乾燥させて、非晶質固体分散体を得ることと、を含む、方法。
141.前述の混合で使用される式(I)の化合物が、5.7、8.4、11.4、15.8、18.1、19.2、21.1、22.5、および23.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる共結晶の形態である、実施形態140に記載の方法。
142.前述の混合で使用される式(I)の化合物が、5.9、8.1、15.0、15.2、16.9、17.8、18.5、21.1、23.4、26.9、および28.2からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる共結晶の形態である、実施形態140に記載の方法。
143.前述の混合で使用される式(I)の化合物が、11.7、12.8、14.2、17.8、19.8、20.7、21.8、22.2、および25.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる結晶形態である、実施形態140に記載の方法。
144.前述の混合で使用される式(I)の化合物が、11.9、13.2、15.5、17.8、18.6、20.8、23.2、23.9、および26.5からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる結晶形態である、実施形態140に記載の方法。
145.前述の混合で使用される式(I)の化合物が、8.6、10.5、18.2、20.2、21.1、および25.9からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる結晶形態である、実施形態140に記載の方法。
146.前述の混合で使用される式(I)の化合物が、8.6、9.7、10.5、15.6、15.9、16.7、17.9、20.3、21.2、24.9、26.6、および27.0からなる群から選択される、度2シータ(±0.2度2シータ)における少なくとも1つのピーク位置を含む、反射モードで取得されたX線粉末回折パターンによって特徴付けられる結晶形態である、実施形態140に記載の方法。
147.治療有効量の実施形態137~139のいずれか1つに記載の非晶質固体分散体と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
148.医薬組成物が、1~10%w/wの式(I)の化合物を含む、実施形態147に記載の医薬組成物。
149.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態147または148に記載の医薬組成物。
150.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態149に記載の医薬組成物。
151.医薬組成物が、20~30%w/wの式(I)の化合物を含む、実施形態147に記載の医薬組成物。
152.医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の化合物を含む、実施形態151に記載の医薬組成物。
153.医薬組成物が、約10mgまたは約50mgの式(I)の化合物を含む、実施形態152に記載の医薬組成物。
154.治療有効量の実施形態137~139のいずれか1つに記載の噴霧乾燥分散体を、1つ以上の医薬品賦形剤と混合して、医薬組成物を得ることを含む、プロセスによって調製された医薬組成物。
155.
またはその薬学的に許容可能な塩である、化合物。
156.
またはその薬学的に許容可能な塩である、化合物。
157.
またはその薬学的に許容可能な塩である、化合物。
158.
またはその薬学的に許容可能な塩である、化合物。
159.治療有効量の実施形態114~117のいずれか1つに記載の化合物またはその薬学的に許容可能な塩と、1つ以上の医薬品賦形剤と、を含む、医薬組成物。
160.治療有効量の実施形態1~10および37~44のいずれか1つに記載の共結晶、実施形態57~62、84~90、103~109、および122~128のいずれか1つに記載の結晶形態、実施形態137~139のいずれか1つに記載の非晶質固体分散体、実施形態11~19および63~71のいずれか1つに記載の原薬、実施形態155~158のいずれか1つに記載の化合物もしくは薬学的に許容可能な塩、または実施形態20~27、45~52、72~79、91~98、110~117、129~136、147~154、および159のいずれか1つに記載の医薬組成物を患者に投与することを含む、IDH1またはIDH2変異の存在によって特徴付けられる癌を治療することを、それを必要としている患者において行う方法。
161.癌が、IDH1変異の存在によって特徴付けられる、実施形態160に記載の方法。
162.IDH1変異が、R132X変異である、実施形態161に記載の方法。
163.IDH1変異が、R132HまたはR132C変異である、実施形態161に記載の方法。
164.IDH1変異が、患者におけるR(-)-2-ヒドロキシグルタル酸の蓄積をもたらす、実施形態161~163のいずれか1つに記載の方法。
165.癌が、IDH2変異の存在によって特徴付けられる、実施形態160に記載の方法。
166.IDH2変異が、R140X変異である、実施形態165に記載の方法。
167.IDH2変異が、R140Q、R140W、またはR140L変異である、実施形態165に記載の方法。
168.IDH2変異が、R172X変異である、実施形態165に記載の方法。
169.IDH2変異が、R172KまたはR172G変異である、実施形態165に記載の方法。
170.IDH2変異が、患者におけるR(-)-2-ヒドロキシグルタル酸の蓄積をもたらす、実施形態165~169のいずれか1つに記載の方法。
171.治療有効量の実施形態1~10および37~44のいずれか1つに記載の共結晶、実施形態57~62、84~90、103~109、および122~128のいずれか1つに記載の結晶形態、実施形態137~139のいずれか1つに記載の非晶質固体分散体、実施形態11~19および63~71のいずれか1つに記載の原薬、実施形態155~158のいずれか1つに記載の化合物もしくは薬学的に許容可能な塩、または実施形態20~27、45~52、72~79、91~98、110~117、129~136、147~154、および159のいずれか1つに記載の医薬組成物を患者に投与することを含む、IDH変異およびIDH2変異の存在によって特徴付けられる癌を治療することを、それを必要としている患者において行う方法。
172.癌が、神経膠腫、急性骨髄性白血病、肉腫、黒色腫、非小細胞肺ガン(NSCLC)、胆管癌、軟骨肉腫、骨髄異形成症候群(MDS)、骨髄増殖性腫瘍(MPN)、結腸癌、および血管免疫芽球性非ホジキンリンパ腫(NHL)から選択される、実施形態160~171のいずれか1つに記載の方法。
173.癌が、神経膠腫である、実施形態160~172のいずれか1つに記載の方法。
174.神経膠腫が、低悪性度神経膠腫または二次性の高悪性度神経膠腫である、実施形態173に記載の方法。
175.神経膠腫が、二次性の高悪性度神経膠腫であり、二次性の高悪性度神経膠腫が、膠芽腫である、実施形態173または174に記載の方法。
176.癌が、難治性または再発性である、実施形態160~175のいずれか1つに記載の方法。
177.癌が、新たに診断されたか、または以前に治療されていない、実施形態160~175のいずれか1つに記載の方法。
178.追加的療法を患者に併用投与することをさらに含む、実施形態160~177のいずれか1つに記載の方法。
179.患者が、癌のための癌治療を以前に投与されている、実施形態160~178のいずれか1つに記載の方法。
180.共結晶、結晶形態、非晶質固体分散体、原薬、化合物もしくは薬学的に許容可能な塩、または医薬組成物が、式(I)の化合物の量に基づいて、1日当たり約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの量で投与される、実施形態160~179のいずれか1つに記載の方法。
181.共結晶、結晶形態、非晶質固体分散体、原薬、化合物もしくは薬学的に許容可能な塩、または医薬組成物が、式(I)の化合物の量に基づいて、1日当たり約10mgまたは約50mgの量で投与される、実施形態160~179のいずれか1つに記載の方法。
182.共結晶、結晶形態、非晶質固体分散体、原薬、化合物もしくは薬学的に許容可能な塩、または医薬組成物が、式(I)の化合物の量に基づいて、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの量で1日2回投与される、実施形態160~179のいずれか1つに記載の方法。
183.共結晶、結晶形態、非晶質固体分散体、原薬、化合物もしくは薬学的に許容可能な塩、または医薬組成物が、式(I)の化合物の量に基づいて、約10mgまたは約50mgの量で1日2回投与される、実施形態160~179のいずれか1つに記載の方法。
184.(R)-6-(6-クロロピリジン-2-イル)-N2-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、
(R)-6-(6-クロロピリジン-2-イル)-N2-エチル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、
(R)-6-(6-クロロピリジン-2-イル)-N2-イソプロピル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、
(R)-4-(6-クロロピリジン-2-イル)-6-((1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-オール、
(R)-4-クロロ-6-(6-クロロピリジン-2-イル)-N-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2-アミン、および
6-(4,6-ビス(((R)-1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-イル)ピリジン-2-オール、からなる群から選択される、化合物。
以下の実施例では、特に断りのない限り、試薬(化学物質)を、商業的供給源(Alfa、Acros、Sigma Aldrich、TCI、およびShanghai Chemical Reagent Companyなど)から購入し、さらに精製することなく使用した。
X線粉末回折(XRPD)分析. XRPD分析を、12自動試料ステージを備えたPANalytical Empyrean X線回折計またはBruker D8 Advance X線回折計をのいずれかで実施した。
6-(6-クロロピリジン-2-イル)-N2,N4-ビス((R)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン(化合物1)の調製
(R)-4-クロロ-6-(6-クロロピリジン-2-イル)-N-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2-アミン(化合物2)の調製
(R)-6-(6-クロロピリジン-2-イル)-N2-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン(化合物3)の調製
(R)-4-(6-クロロピリジン-2-イル)-6-(1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-オール(化合物4)の調製
(R)-6-(6-クロロピリジン-2-イル)-N2-イソプロピル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン(化合物5)の調製
(R)-6-(6-クロロピリジン-2-イル)-N2-エチル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン(化合物6)の調製
6-(4,6-ビス(((R)-1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-イル)ピリジン-2-オール(化合物7)の調製
6-(6-クロロピリジン-2-イル)-N2-((R)-1,1,1-トリフルオロプロパン-2-イル)-N4-((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン(化合物8)の調製
6-(6-クロロピリジン-2-イル)-N2,N4-ビス((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン(化合物9)の調製
6-(6-クロロピリジン-2-イル)-N2,N4-ビス((R)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン(化合物1)の代替的な調製
2000L反応器をエタノール(344kg)、6-クロロピコリン酸メチル(20.1kg、117.1mol)、およびビウレット(2-イミドジカルボンジアミド)(14.85kg、140.5mol)で満たした。得られた混合物を30~35℃まで温め、この温度で30~60分間撹拌し、この時点で、オルトギ酸トリメチル(15.4kg、140.5mol)およびトリフルオロ酢酸(1.4kg、12.3mol)を添加した。得られた混合物を50~55℃まで温め、この温度で2時間撹拌し、次いで25~30℃まで冷却した。水(200kg)を添加し、HCl(35%水性)の添加によってpHを1以下に調節した。混合物を30~35℃で2~4時間撹拌し、次いで濾過した。湿潤ケーキを60%水性エタノール(185kg)で洗浄し、反応器に戻した。ジクロロメタン(213kg)を添加し、得られた混合物を25~30℃で2~3時間撹拌し、次いで濾過した。湿潤ケーキをジクロロメタン(40kg)で洗浄し、45~50℃において真空下で40~80時間乾燥させて、粗化合物A(11.7kg)を得た。
250L反応器を化合物A(8.9kg、39.7mol)、塩化ベンジルトリエチルアンモニウム(19.0kg、79.4mol)、およびPOCl3(37.0kg、238.2mol)で満たした。得られた混合物を95~105℃で18~24時間撹拌し、30~40℃まで冷却し、減圧下で18~36Lまで濃縮した。酢酸エチル(3×53.0kg)を添加し、得られた溶液を減圧下で18~36Lまで濃縮した。追加の酢酸エチル(112.0kg)を添加し、得られた混合物を10~20℃まで冷却した。
300L反応器を化合物B(7.3kg、27.9mol)、(R)-1,1,1-トリフルオロプロパン-2-アミン塩酸塩(9.7kg、64.2mol)、およびN-メチル-2-ピロリドン(44.4kg)で満たした。反応混合物を10~25℃まで冷却し、ジイソプロピルエチルアミン(17.0kg、128.4mol)を約1時間にわたって添加した。混合物を10~20℃で約10分間、45~55℃で約1~2時間、および95~105℃で約20時間撹拌し、次いで45~55℃まで冷却した。プロセス水(4kg)を約1時間にわたって滴下し、得られた溶液を500L反応器に移し、N-メチル-2-ピロリドン(2kg)で洗浄した。追加のプロセス水(34.0kg)を45~55℃で約3時間にわたって滴下し、得られた混合物を20~30℃で約3.5時間撹拌した。追加のプロセス水(7.4kg)を添加し、得られた混合物を遠心分離し、プロセス水(9kg)で洗浄した。湿潤ケーキをプロセス水(89kg)でスラリー化し、得られたスラリーを遠心分離し、プロセス水(21kg)で洗浄した。湿潤ケーキを500L反応器に戻し、アセトニトリル(2×133kg)を添加した。得られた溶液を減圧下で3~5体積まで濃縮し、炭素(1.1kg)および珪藻土(6.0kg)を添加した。混合物を濾過し、アセトニトリル(37kg)で洗浄し、濾液を100L反応器にカートリッジフィルタを通して移した。溶液を減圧下で5~5.5体積まで濃縮し、精製水(55kg)をカートリッジフィルタを介して2~3時間にわたって滴下した。混合物を20~30℃で2~5時間で撹拌し、追加の精製水(4kg)を、カートリッジフィルタを介して1時間にわたって滴下した。混合物を濾過し、アセトニトリル/水(15kg、1:1)で洗浄し、湿潤ケーキを50~60℃で20~80時間乾燥させて、化合物1(8.38kg)を得た。
化合物1のクエン酸共結晶タイプAの調製および特徴付け
20mLバイアルを1.02gの化合物1および508.0mgのクエン酸一水和物で満たし、アセトニトリル(20mL)を添加した。得られた溶液を室温(20~25℃)で24時間撹拌し、その間に沈殿物が形成された。沈殿物をブフナー漏斗を通して濾過することによって収集し、固体を室温で15.5時間乾燥させて、化合物1のクエン酸共結晶タイプAを得た。共結晶をXRPD、1H NMR、DSC、TGA、およびDVS分析によって分析した。
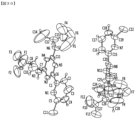
化合物1のクエン酸共結晶タイプAの単結晶X線回折分析
構造決定に適したクエン酸共結晶タイプAの単結晶を、n-ブタノール/ヘプタン(1/3、v/v)中の化合物1および無水クエン酸の溶液をゆっくり冷却することによって得た。実験の詳細は、以下のとおりであった。12.5mgの化合物1および6.1mgの無水クエン酸を3mLバイアルに計量して入れた。1.2mLの溶媒(n-ブタノール/ヘプタン、1/3v/v)をバイアルに添加し、混合物を45℃で平衡化して、懸濁液を形成し、これを2つの3mLバイアルに濾過した(0.45μm PTFE膜)。クエン酸共結晶タイプAの種晶を飽和溶液に添加し、次いで、これを0.01℃/分の速度で(4000分間)45℃から5℃まで冷却した。5日後、クエン酸共結晶タイプAの針様結晶を得た。
化合物1のマレイン酸共結晶タイプAの調製および特徴付け
化合物1(100.4mg)およびマレイン酸(28.3mg)をアセトン(2.0mL)中に溶解し、得られた溶液を室温で1日撹拌し、その間に沈殿物が形成された。沈殿物を単離し、室温で空気乾燥させて、化合物1のマレイン酸共結晶タイプAを得た。共結晶をXRPD、1H NMR、DSC、TGA、およびDVS分析によって分析した。
化合物1のクエン酸共結晶タイプAの調製および特徴付け
100L反応器を、1.5kg(7.9mol)の無水クエン酸および31.0kgのアセトンで満たした。クエン酸が完全に溶解するまで、混合物を20~30℃で撹拌し、得られた溶液を500L反応器に移した。100L反応器を追加の5.0kgのアセトンで洗浄し、次いで500L反応器に添加した。化合物1(6.73kg、16.2mol)を実施例10に記載されるように調製し、反応器に添加し、化合物1が完全に溶解するまで(約1時間)、混合物を20~30℃で撹拌した。20~30℃でさらに1~2時間撹拌した後、75.0gの精製水を反応器に添加した。N-ヘプタン(13.0kg)を1時間にわたって反応器に添加し、次いでクエン酸共結晶タイプAの種晶(46g)を添加した。混合物を20~30℃で1~2時間撹拌し、次いで追加のn-ヘプタン(104.0kg)を2~4時間にわたって添加した。
化合物1のクエン酸共結晶タイプAの調製
30L反応器(反応器1)を1.2kgの化合物1(2.9mol)および1.87kgのアセトンで満たし、得られた混合物を25~28℃で0.5時間撹拌した。第2の反応器(反応器2)を297.9gのクエン酸一水和物(1.42mol)および674gのアセトンで満たし、得られた混合物を25~28℃で0.5時間撹拌した。反応器2の内容物の半分を37~43℃で反応器1に移し、次いでクエン酸共結晶タイプAの種晶(6g)を反応器1に添加した。反応器1内の得られた混合物を37~43℃で1.5時間撹拌した。反応器2の残りの内容物を37~43℃で0.5~1.5時間にわたって反応器1に移し、次いでn-へプタン(6690g)を37~43℃で2.5時間にわたって反応器1に添加した。反応器1を2.5時間にわたって8~12℃まで冷却し、8~12℃で1~3時間撹拌を継続した。
化合物1の遊離形態タイプAの調製および特徴付け
実施例10に記載されるように調製された化合物1(450.0g)を、70~80℃で1.0Lの酢酸エチル中に溶解した。4.0Lのn-ヘプタンを70~80℃で溶液中に2時間にわたって滴下した。混合物を3時間にわたって0~10℃まで冷却し、次いで0~10℃で16時間撹拌した。得られた懸濁液を濾過し、湿潤ケーキを40~45℃で16時間乾燥させて、結晶遊離形態タイプAの400gの乾燥ケーキを得た。単離した結晶材料を元素分析XRPD分析、DSC分析、TGA分析、およびHPLC分析によって特徴付けた。
化合物1の遊離形態タイプAの単結晶X線回折分析
化合物1の単一無色針状結晶を、低速蒸発によってジクロロメタンとトルエンの混合物から再結晶化した。
Olex2(O.V.Dolomanov,L.J.Bourhis,R.J.Gildea,J.A.K.Howard and H.Puschmann.“OLEX2:a complete structure solution,refinement and analysis program”.J.Appl.Cryst.2009,42,339-341)に組み込まれたF2、ShelXL-97上での最小二乗法によって構造を精密化した。全てのH原子を計算された位置に置き、ライディングモデルを使用して精密化した。
化合物1の遊離形態タイプBの調製および特徴付け
20mLバイアルを100mgの化合物1(遊離形態タイプA)および1mLのメチルイソブチルケトンで満たして、溶液を形成した。ヘプタン(15mL)を滴下し、混合物を室温で90分間撹拌し、その間に沈殿物が形成された。沈殿物を単離し、乾燥させて、化合物1の遊離形態タイプBを得た。遊離形態タイプBを、XRPD、DSC、およびTGA分析によって分析した。
化合物1の遊離形態タイプBの単結晶X線回折分析
構造決定に適した単結晶を、THF/ヘプタン(1/3、v/v)共溶媒系における蒸気拡散によって得た。化合物1の遊離形態タイプA(21.0mg)を、0.5mLのTHF/ヘプタン(1/3、v/v)共溶媒を添加しながら3mLバイアルに計量して入れた。溶液をナイロンフィルタ(0.45μm)で濾過し、3つの4mLバイアルに収集した。遊離形態タイプBの種晶をバイアルに添加した。バイアルを20mLバイアル(抗溶媒として4mLのヘプタンを有する)に入れ、20mLバイアルに蓋をした。バイアルを室温で保持し、ヘプタンをTHF/ヘプタン溶液中に拡散させた。3日後、遊離形態タイプBのプレート様結晶を得た。
化合物1の遊離形態タイプCの調製および特徴付け
20mLバイアルを150mgの化合物1(遊離形態タイプA)および1.5mLの1,4-ジオキサンで満たして、溶液を形成した。水(2.25mL)を滴下し、得られた懸濁液を室温で3日間撹拌した。固体材料を単離し、乾燥させて、化合物1の遊離形態タイプCを得た。遊離形態タイプCを、XRPD、DSC、およびTGA分析によって分析した。
化合物1の遊離形態タイプCの単結晶X線回折分析
構造決定に適した単結晶を、ACN/H2O(4/1、v/v)中の低速蒸発によって得た。化合物1の遊離形態タイプA(4.2mg)およびクエン酸(2.1mg)を、3mLバイアルに計量して入れ、0.5mLのACN/H2O(4/1、v/v)を添加した。溶液を単結晶バイアルに濾過し、溶媒を蒸発させた。7日後、遊離形態タイプCのラス結晶を得た。
化合物1の遊離形態タイプDの調製および特徴付け
化合物1の遊離形態タイプA(135.0mg)を、2.0mLの1,4-ジオキサン/ヘプタン(4:1、v/v)中に懸濁した。懸濁液を室温で17日間撹拌し、固体材料を分離し、空気乾燥させて、化合物1の遊離形態タイプDを得た。遊離形態タイプDを、XRPD、1H NMR、DSC、およびTGA分析によって分析した。
化合物1の非晶質固体分散体
化合物1およびHPMCAS(ヒドロキシプロピルメチルセルロースアセテートスクシネート)の50:50の噴霧乾燥分散体を調製した。アセトン中の化合物1およびHPMCASの溶液をBuchi B-290上で噴霧乾燥させた。噴霧乾燥後、固体分散体を40℃で一晩乾燥させて、残留溶媒を除去した。得られた材料のXRPD分析は、非晶質形態と一致する回折パターンを明らかにした。材料が単一のガラス転移温度(Tg=84.6℃)を有する単相固体分散体であることを、DSC分析によって決定した。人工腸液における溶解試験は、材料がインビボでの曝露を達成するのに十分な過飽和を維持することができることを実証した。
雄のSprague Dawleyラットにおける単一PO投与後の血漿中の化合物1固形形態の薬物動態
研究設計.12匹の雄のSprague Dawleyラット(SLAC Laboratory Animal Co.LTDから購入)を4つの群(1群当たり3匹の動物)に無作為化した。動物を一晩絶食させ、表24に示される化合物1の形態を強制経口投与し、動物に投与後4時間餌を与えた。化合物1の各形態を、0.5%微結晶セルロースと0.1%Tween 80とを含有する水中の懸濁液として投与した。表24に示される用量レベルおよび用量濃度は、遊離化合物1の対応する量に基づく。
Claims (46)
- 前記共結晶が、170.6℃(±2.0℃)の開始温度を有する吸熱ピークを含む示差走査熱量測定サーモグラムによって特徴付けられる、請求項1に記載の共結晶。
- 水をさらに含む、請求項1または2に記載の共結晶。
- 式(I)の前記化合物、クエン酸、および水が、2:1:1のモル比で存在する、請求項1~3のいずれか一項に記載の共結晶。
- 前記共結晶が、単位セル当たり、式(I)の前記化合物の4つの分子、2つのクエン酸分子、および2つの水分子を含む、請求項1~4のいずれか一項に記載の共結晶。
- 請求項1~5のいずれか一項に記載の共結晶を含む、原薬。
- 前記原薬が、1.0%以下(HPLCによる面積%)の(R)-6-(6-クロロピリジン-2-イル)-N2-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、(R)-6-(6-クロロピリジン-2-イル)-N2-エチル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、(R)-6-(6-クロロピリジン-2-イル)-N2-イソプロピル-N4-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、6-(6-クロロピリジン-2-イル)-N2,N4-ビス((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、6-(6-クロロピリジン-2-イル)-N2-((R)-1,1,1-トリフルオロプロパン-2-イル)-N 4 -((S)-1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2,4-ジアミン、(R)-4-(6-クロロピリジン-2-イル)-6-((1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-オール、(R)-4-クロロ-6-(6-クロロピリジン-2-イル)-N-(1,1,1-トリフルオロプロパン-2-イル)-1,3,5-トリアジン-2-アミン、および6-(4,6-ビス(((R)-1,1,1-トリフルオロプロパン-2-イル)アミノ)-1,3,5-トリアジン-2-イル)ピリジン-2-オールのうちのいずれかを含有する、請求項6に記載の原薬。
- 治療有効量の請求項1~5のいずれか一項に記載の共結晶、または請求項6もしくは7に記載の原薬、および1つ以上の医薬賦形剤を含む、医薬組成物。
- 前記医薬組成物が、1~10%w/wの式(I)の前記化合物を含む、請求項8に記載の医薬組成物。
- 前記医薬組成物が、20~30%w/wの式(I)の前記化合物を含む、請求項8に記載の医薬組成物。
- 前記医薬組成物が、経口的に許容可能な剤形の形態であり、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの式(I)の前記化合物を含む、請求項8~10のいずれか一項に記載の医薬組成物。
- 前記医薬組成物が、約10mgまたは約50mgの式(I)の前記化合物を含む、請求項11に記載の医薬組成物。
- 前記溶媒が、アセトニトリルまたはアセトンを含む、請求項13に記載の方法。
- 前記沈殿が、前記溶液を冷却することを含む、請求項13または14に記載の方法。
- 前記沈殿が、前記溶液から前記溶媒の一部分を蒸発させることを含む、請求項13~15のいずれか一項に記載の方法。
- 前記沈殿が、抗溶媒を前記溶液に添加することを含む、請求項13~16のいずれか一項に記載の方法。
- 前記抗溶媒が、C5~C12アルカンまたはシクロアルカンを含む、請求項17に記載の方法。
- 前記抗溶媒が、トルエンまたはMTBEを含む、請求項17に記載の方法。
- 前記沈殿が、前記溶液に前記共結晶の結晶を播種することを含む、請求項13~19のいずれか一項に記載の方法。
- 前記共結晶を単離することをさらに含む、請求項13~20のいずれか一項に記載の方法。
- IDH1またはIDH2変異の存在によって特徴付けられる癌を治療することを必要としている患者において、それを行うための、請求項1~5のいずれか一項に記載の共結晶を含む組成物、請求項6もしくは7に記載の原薬を含む組成物、または請求項8~12のいずれか一項に記載の医薬組成物。
- 前記癌が、IDH1変異の存在によって特徴付けられる、請求項22に記載の組成物または医薬組成物。
- 前記IDH1変異が、R132X変異である、請求項23に記載の組成物または医薬組成物。
- 前記IDH1変異が、R132HまたはR132C変異である、請求項23に記載の組成物または医薬組成物。
- 前記IDH1変異が、前記患者におけるR(-)-2-ヒドロキシグルタル酸の蓄積をもたらす、請求項23~25のいずれか一項に記載の組成物または医薬組成物。
- 前記癌が、IDH2変異の存在によって特徴付けられる、請求項22に記載の組成物または医薬組成物。
- 前記IDH2変異が、R140X変異である、請求項27に記載の組成物または医薬組成物。
- 前記IDH2変異が、R140Q、R140W、またはR140L変異である、請求項27に記載の組成物または医薬組成物。
- 前記IDH2変異がR172X変異である、請求項27に記載の組成物または医薬組成物。
- 前記IDH2変異が、R172KまたはR172G変異である、請求項27に記載の組成物または医薬組成物。
- 前記IDH2変異が、前記患者におけるR(-)-2-ヒドロキシグルタル酸の蓄積をもたらす、請求項27~31のいずれか一項に記載の組成物または医薬組成物。
- IDH1変異およびIDH2変異の存在によって特徴付けられる癌を治療することを必要としている患者において、それを行うための、請求項1~5のいずれか一項に記載の共結晶を含む組成物、請求項6もしくは7のいずれか一項に記載の原薬を含む組成物、または請求項8~12のいずれか一項に記載の医薬組成物。
- 前記癌が、神経膠腫、急性骨髄性白血病、肉腫、黒色腫、非小細胞肺癌(NSCLC)、胆管癌、軟骨肉腫、骨髄異形成症候群(MDS)、骨髄増殖性腫瘍(MPN)、結腸癌、および血管免疫芽球性非ホジキンリンパ腫(NHL)から選択される、請求項22~33のいずれか一項に記載の組成物または医薬組成物。
- 前記癌が、神経膠腫である、請求項22~34のいずれか一項に記載の組成物または医薬組成物。
- 前記神経膠腫が、低悪性度神経膠腫または二次性の高悪性度神経膠腫である、請求項35に記載の組成物または医薬組成物。
- 前記神経膠腫が、二次性の高悪性度神経膠腫であり、前記二次性の高悪性度神経膠腫が、膠芽腫である、請求項36に記載の組成物または医薬組成物。
- 前記神経膠腫が、低悪性度神経膠腫である、請求項36に記載の組成物または医薬組成物。
- 前記癌が、難治性または再発性である、請求項22~38のいずれか一項に記載の組成物または医薬組成物。
- 前記癌が、新たに診断されたか、または以前に治療されていない、請求項22~38のいずれか一項に記載の組成物または医薬組成物。
- 前記組成物または医薬組成物が、追加的療法と組み合わせて前記患者に投与されることを特徴とする、請求項22~40のいずれか一項に記載の組成物または医薬組成物。
- 前記患者が、前記癌のための癌治療を以前に投与されている、請求項22~41のいずれか一項に記載の組成物または医薬組成物。
- 前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、1日当たり約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの量で投与される、請求項22~42のいずれか一項に記載の組成物または医薬組成物。
- 前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、1日当たり約10mgまたは約50mgの量で投与される、請求項22~42のいずれか一項に記載の組成物または医薬組成物。
- 前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、約10mg、約25mg、約50mg、約100mg、約200mg、または約300mgの量で1日2回投与される、請求項22~42のいずれか一項に記載の組成物または医薬組成物。
- 前記共結晶、原薬、または医薬組成物が、式(I)の前記化合物の量に基づいて、約10mgまたは約50mgの量で1日2回投与される、請求項22~42のいずれか一項に記載の組成物または医薬組成物。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023070786A JP7499377B2 (ja) | 2017-11-02 | 2023-04-24 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
| JP2024090124A JP7780576B2 (ja) | 2017-11-02 | 2024-06-03 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762580501P | 2017-11-02 | 2017-11-02 | |
| US62/580,501 | 2017-11-02 | ||
| PCT/US2018/058930 WO2019090059A1 (en) | 2017-11-02 | 2018-11-02 | Cocrystals, pharmaceutical compositions thereof, and methods of treatment involving same |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023070786A Division JP7499377B2 (ja) | 2017-11-02 | 2023-04-24 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2021501766A JP2021501766A (ja) | 2021-01-21 |
| JP2021501766A5 JP2021501766A5 (ja) | 2021-12-16 |
| JP7335877B2 true JP7335877B2 (ja) | 2023-08-30 |
Family
ID=64572453
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020524501A Active JP7335877B2 (ja) | 2017-11-02 | 2018-11-02 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
| JP2023070786A Active JP7499377B2 (ja) | 2017-11-02 | 2023-04-24 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
| JP2024090124A Active JP7780576B2 (ja) | 2017-11-02 | 2024-06-03 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023070786A Active JP7499377B2 (ja) | 2017-11-02 | 2023-04-24 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
| JP2024090124A Active JP7780576B2 (ja) | 2017-11-02 | 2024-06-03 | 共結晶、その医薬組成物、およびそれを伴う治療方法 |
Country Status (16)
| Country | Link |
|---|---|
| US (3) | US11345677B2 (ja) |
| EP (1) | EP3704101A1 (ja) |
| JP (3) | JP7335877B2 (ja) |
| KR (2) | KR102731624B1 (ja) |
| CN (2) | CN118359585A (ja) |
| AU (2) | AU2018360827B2 (ja) |
| CA (1) | CA3081535A1 (ja) |
| EA (1) | EA202091112A1 (ja) |
| IL (2) | IL274123B2 (ja) |
| MA (1) | MA50526A (ja) |
| MX (2) | MX2020004513A (ja) |
| PH (1) | PH12020550462A1 (ja) |
| SG (1) | SG11202003612VA (ja) |
| TW (2) | TWI839131B (ja) |
| UA (1) | UA127380C2 (ja) |
| WO (1) | WO2019090059A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20200085832A1 (en) * | 2019-11-22 | 2020-03-19 | Agios Pharmaceuticals, Inc. | Deuterated analogs of an organic compound |
| AR123228A1 (es) | 2020-08-12 | 2022-11-09 | Servier Pharmaceuticals Llc | Formas en estado sólido de un compuesto orgánico |
| US20230346789A1 (en) * | 2022-03-31 | 2023-11-02 | Msd International Gmbh | Methods of treating enhancing brain tumors using combination therapy |
| AR133332A1 (es) | 2023-07-25 | 2025-09-17 | Servier Lab | Sales, cocristales, composiciones farmacéuticas de los mismos, y métodos de tratamiento que implican los mismos |
| WO2025060940A1 (zh) * | 2023-09-18 | 2025-03-27 | 贝达药业股份有限公司 | 突变型idh抑制剂化合物及其盐的固体形式 |
| EP4538262A1 (en) | 2023-10-12 | 2025-04-16 | Sandoz Ag | Cocrystals of vorasidenib |
| WO2025168757A1 (en) | 2024-02-09 | 2025-08-14 | Les Laboratoires Servier | Process for the preparation of vorasidenib |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016526561A (ja) | 2013-07-11 | 2016-09-05 | アジオス ファーマシューティカルズ, インコーポレイテッド | 治療活性化合物およびそれらの使用方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NZ710636A (en) * | 2010-11-01 | 2017-02-24 | Celgene Avilomics Res Inc | Heterocyclic compounds and uses thereof |
| US9579324B2 (en) | 2013-07-11 | 2017-02-28 | Agios Pharmaceuticals, Inc | Therapeutically active compounds and their methods of use |
-
2018
- 2018-11-02 SG SG11202003612VA patent/SG11202003612VA/en unknown
- 2018-11-02 KR KR1020207015661A patent/KR102731624B1/ko active Active
- 2018-11-02 EA EA202091112A patent/EA202091112A1/ru unknown
- 2018-11-02 IL IL274123A patent/IL274123B2/en unknown
- 2018-11-02 IL IL305426A patent/IL305426B2/en unknown
- 2018-11-02 TW TW112106677A patent/TWI839131B/zh active
- 2018-11-02 JP JP2020524501A patent/JP7335877B2/ja active Active
- 2018-11-02 EP EP18812419.2A patent/EP3704101A1/en active Pending
- 2018-11-02 WO PCT/US2018/058930 patent/WO2019090059A1/en not_active Ceased
- 2018-11-02 CA CA3081535A patent/CA3081535A1/en active Pending
- 2018-11-02 TW TW107139079A patent/TWI796377B/zh active
- 2018-11-02 KR KR1020247037879A patent/KR20240166601A/ko active Pending
- 2018-11-02 US US16/760,520 patent/US11345677B2/en active Active
- 2018-11-02 CN CN202410230044.7A patent/CN118359585A/zh active Pending
- 2018-11-02 MX MX2020004513A patent/MX2020004513A/es unknown
- 2018-11-02 AU AU2018360827A patent/AU2018360827B2/en active Active
- 2018-11-02 MA MA050526A patent/MA50526A/fr unknown
- 2018-11-02 CN CN201880079771.0A patent/CN111527076B/zh active Active
- 2018-11-02 UA UAA202003279A patent/UA127380C2/uk unknown
-
2020
- 2020-04-22 PH PH12020550462A patent/PH12020550462A1/en unknown
- 2020-07-13 MX MX2022014792A patent/MX2022014792A/es unknown
-
2022
- 2022-04-19 US US17/723,666 patent/US11851417B2/en active Active
-
2023
- 2023-04-24 JP JP2023070786A patent/JP7499377B2/ja active Active
- 2023-11-08 US US18/504,859 patent/US20240343705A1/en active Pending
-
2024
- 2024-05-14 AU AU2024203186A patent/AU2024203186A1/en active Pending
- 2024-06-03 JP JP2024090124A patent/JP7780576B2/ja active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016526561A (ja) | 2013-07-11 | 2016-09-05 | アジオス ファーマシューティカルズ, インコーポレイテッド | 治療活性化合物およびそれらの使用方法 |
Non-Patent Citations (2)
| Title |
|---|
| Pharm Tech Japan,2009年,Vol. 25, No.12,p.155-166 |
| 日本薬理学雑誌,2017年,Vol. 150,pp. 36-40 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7499377B2 (ja) | 共結晶、その医薬組成物、およびそれを伴う治療方法 | |
| US11865079B2 (en) | Therapeutically active compounds and their methods of use | |
| US20250034109A1 (en) | Salts, cocrystals, pharmaceutical compositions thereof, and methods of treatment involving the same | |
| US20250041283A1 (en) | Cocrystal of an idh1 inhibitor, process of preparation thereof, pharmaceutical compositions thereof, and methods of treatment involving the same | |
| EA048730B1 (ru) | Сокристаллы, фармацевтические композиции на их основе и способы лечения, предусматривающие их применение | |
| BR112020008598B1 (pt) | Cocristal, composição farmacêutica e usos de um cocristal ou de uma composição farmacêutica | |
| EA042081B1 (ru) | Сокристаллы, фармацевтические композиции на их основе и способы лечения, предусматривающие их применение | |
| AU2022219973A1 (en) | Therapeutically active compounds and their methods of use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200703 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211102 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20211102 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20221007 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20221129 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230227 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20230320 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230424 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20230424 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230724 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230818 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7335877 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |