JP6830094B2 - 染色体異常を検出するための核酸及び方法 - Google Patents
染色体異常を検出するための核酸及び方法 Download PDFInfo
- Publication number
- JP6830094B2 JP6830094B2 JP2018503647A JP2018503647A JP6830094B2 JP 6830094 B2 JP6830094 B2 JP 6830094B2 JP 2018503647 A JP2018503647 A JP 2018503647A JP 2018503647 A JP2018503647 A JP 2018503647A JP 6830094 B2 JP6830094 B2 JP 6830094B2
- Authority
- JP
- Japan
- Prior art keywords
- mip
- target
- sequence
- sequencing
- sample
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6811—Selection methods for production or design of target specific oligonucleotides or binding molecules
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6827—Hybridisation assays for detection of mutation or polymorphism
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B25/00—ICT specially adapted for hybridisation; ICT specially adapted for gene or protein expression
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B25/00—ICT specially adapted for hybridisation; ICT specially adapted for gene or protein expression
- G16B25/20—Polymerase chain reaction [PCR]; Primer or probe design; Probe optimisation
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B30/00—ICT specially adapted for sequence analysis involving nucleotides or amino acids
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B30/00—ICT specially adapted for sequence analysis involving nucleotides or amino acids
- G16B30/10—Sequence alignment; Homology search
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H50/00—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics
- G16H50/20—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics for computer-aided diagnosis, e.g. based on medical expert systems
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/156—Polymorphic or mutational markers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
Description
本出願は、2015年7月29日に出願された米国特許仮出願第62/198,654号の利益を主張するものであり、その全体は本明細書に参照として組み込まれる。
本発明は、検出を必要とする対象における、とりわけ、異数性及び染色体異常を検出するためのシステム及び方法に関する。
主な染色体異常は、生産数のほぼ140分の1で検出されており、満期に達しない胎児、または、死産になる胎児において、はるかに高い比率で検出されている。Hsu(1998)「Prenatal diagnosis of chromosomal abnormalities through amniocentesis.」(In:Milunsky A,editor.Genetic Disorders and the Fetus.4 ed.Baltimore:The Johns Hopkins University Press.179−180;Staebler et al.(2005))、「Should determination of the karyotype be systematic for all malformations detected by obstetrical ultrasound?」(Prenat Diagn 25:567−573.)。最も一般的な異数性は21トリソミー(ダウン症候群)であり、現時点における生産数の730分の1で発生している(Hsu;Staebler et al.)。21トリソミーより一般的ではないが、18トリソミー(エドワーズ症候群)及び13トリソミー(パトー症候群)はそれぞれ、生産数の5,500分の1、生産数の17,200分の1で発生している(Hsu.)。多種多様な先天性欠損症、発育不全症、及び、知的障害は、染色体の異数性を有する小児に見られるが、これらは、家族及び社会に、生涯にわたる課題を提示している(Jones(2006)「Smith’s recognizable patterns of human malformation.」(Philadelphia:Elsevier Saunders.))。胎児異数性リスクの大きさを示すことが可能である様々な出生前検査法があり、例えば、羊水穿刺または絨毛採取などの侵襲的な診断検査法が挙げられる。これらは現時点におけるゴールドスタンダードとなっているが、無視できないほどの胎児の死亡リスクを伴う(American College of Obstetricians and Gynecologists(2007) ACOG Practice Bulletin No.88,December 2007.「Invasive prenatal testing for aneuploidy.」Obstet Gynecol 110:1459−1467.)。それゆえ、胎児異数性に関する、より信頼性が高く非侵襲的な検査法が長きにわたり求められている。これらのうち最も有望な検査法は、母体血漿中に存在する胎児DNAを検出することに基づいている。母体血漿から作製したライブラリに対して超並列シークエンシングを行うことにより、21番染色体の異常を確実に検出可能であることが示されてきた(Chiu et al.,(2008)「Noninvasive prenatal diagnosis of fetal chromosomal aneuploidy by massively parallel genomic sequencing of DNA in maternal plasma.」(Proc Natl Acad Sci USA 105:20458−20463;Fan et al.,(2008))、及び、「Noninvasive diagnosis of fetal aneuploidy by shotgun sequencing DNA from maternal blood.」 (Proc Natl Acad Sci USA 105:16266−16271.) )。
[発明の概要]
1.胎児における異数性を検出するための方法であって、
a)母体血液試料から単離した核酸試料を得ることと、
b)分子反転プローブ(MIP)の1つまたは複数の集団を用いることにより、工程a)で得た前記核酸試料中における複数の目的の標的配列を捕捉して、複数のレプリコンを作製することと、
前記MIP集団内の前記MIPのそれぞれは、以下の構成要素、
第1の標的ポリヌクレオチドアーム−第1の固有分子タグ−ポリヌクレオチドリンカー−第2の固有分子タグ−第2の標的ポリヌクレオチドアームを配列内に含み、
前記MIPのそれぞれにおける前記一対の第1及び第2の標的ポリヌクレオチドアームは、同一であり、前記複数の目的の標的配列内におけるそれぞれの配列に隣接する、前記核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的であり、
前記MIPのそれぞれにおける前記第1及び第2の固有標的分子タグの組み合わせは、前記MIPのそれぞれにおいて異なっており、
c)工程b)で得た前記レプリコンから増幅した複数のMIPアンプリコンをシークエンスすることと、
d)レプリコンを増幅したそれぞれのMIPにおける前記固有分子タグの数に基づいて、工程c)で得た前記複数のアンプリコンにおける第1のアンプリコン集団のそれぞれの捕捉現象の数を測定することと、前記第1のアンプリコン集団は、前記目的の標的配列の前記シークエンスにより同定され、
e)レプリコンを増幅したそれぞれのMIPにおける前記固有分子タグの数に基づいて、工程c)で得た前記複数のアンプリコンにおける第2のアンプリコン集団のそれぞれの捕捉現象の数を測定することと、前記第2のアンプリコン集団は、前記目的の標的配列の前記シークエンスにより同定され、
f)工程d)で測定した捕捉現象の数の少なくとも一部に基づいて、そこから前記第1のアンプリコン集団を作製した、それぞれの目的の標的配列の部位捕捉基準を決定することと、
g)少なくとも1つの判定基準を満たす、工程f)で決定した前記部位捕捉基準の第1のサブセットを同定することと、
h)工程e)で測定した捕捉現象の数の少なくとも一部に基づいて、そこから前記第2のアンプリコン集団を作製した、それぞれの目的の標的配列の部位捕捉基準を決定することと、
i)前記少なくとも1つの判定基準を満たす、工程h)で決定した前記部位捕捉基準の第2のサブセットを同定することと、
j)工程g)で同定した部位捕捉基準の前記第1のサブセットから求めた第1の指標を、工程i)で同定した部位捕捉基準の前記第2のサブセットから求めた第2の指標で正規化して、検査比率を得ることと、
k)前記検査比率を、正倍数性または異数性を示すことが既知である参照対象から単離した参照核酸試料に基づいて計算した、複数の参照比率と比較することと、
l)工程k)の前記比較に基づいて、異数性が前記胎児において検出されるかどうかを判定することと、
を含む、前記方法。
i)前記第1及び第2の標的ポリヌクレオチドアームをそれぞれ、前記核酸試料中の対応する前記第1及び第2の領域にハイブリダイズすることと、前記第1及び第2の領域は目的の標的配列に隣接し、
ii)前記ハイブリダイゼーション後、ライゲーション/伸長用混合液を用いて、前記2つの標的ポリヌクレオチドアーム間に存在するギャップ領域を伸長及びライゲートし、一本鎖環状核酸分子を作製することと、
により作製される、実施形態1から実施形態30のいずれか1つに記載の方法。
a)母体血液試料由来のゲノムDNA試料を得ることと、
b)前記ゲノムDNA試料を、マルチウェルプレートのそれぞれのウェルへと加えることと、前記マルチウェルプレートのそれぞれのウェルはプローブ混合液を含み、前記プローブ混合液は分子反転プローブ(MIP)集団及び緩衝液を含み、
前記MIP集団内のそれぞれのMIPは、以下の構成要素、
第1の標的ポリヌクレオチドアーム−第1の固有分子タグ−ポリヌクレオチドリンカー−第2の固有分子タグ−第2の標的ポリヌクレオチドアームを配列内に含み、
前記MIPのそれぞれにおける前記一対の第1及び第2の標的ポリヌクレオチドアームは、同一であり、複数の目的の標的配列内におけるそれぞれの配列に隣接する、前記核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的であり、
前記MIPのそれぞれにおける前記第1及び第2の固有標的分子タグの組み合わせは、前記MIPのそれぞれにおいて異なっており、
c)前記MIPの前記プローブ混合液を含む前記ゲノムDNA試料をインキュベートして、前記複数の目的の標的配列を捕捉することと、
d)伸長/ライゲーション用混合液を、前記MIP及び前記複数の目的の標的配列を含むc)の前記試料へと加えて、複数のMIPアンプリコンを作製することと、前記伸長/ライゲーション用混合液は、ポリメラーゼ、複数のdNTP、リガーゼ、及び、緩衝液を含み、
e)エキソヌクレアーゼ混合液を、前記標的及び対照MIPアンプリコンへと加えて、過剰プローブまたは過剰ゲノムDNAを除去することと、
f)インデックスPCR用混合液をe)の前記試料へと加えて、一対のインデックスプライマー、固有試料バーコード、及び、一対のシークエンシングアダプターを、前記複数のアンプリコンへと加えることと、
g)超並列シークエンシング法を用いて、前記固有標的分子タグの数に基づいて、工程f)で提供したバーコード化アンプリコンの第1の集団におけるシークエンシングリードの数を測定することと、バーコード化アンプリコンの前記第1の集団は、前記目的の標的配列の前記シークエンスにより同定され、
h)超並列シークエンシング法を用いて、前記固有標的分子タグの数に基づいて、工程f)で提供したバーコード化アンプリコンの第2の集団におけるシークエンシングリードの数を測定することと、バーコード化アンプリコンの前記第2の集団は、前記目的の標的配列の前記シークエンスにより同定され、
i)工程g)で測定した第1のシークエンシングリードの数の少なくとも一部に基づいて、部位捕捉基準を計算し、工程h)で測定した第2のシークエンシングリードの数の少なくとも一部に基づいて、複数の対照プローブ捕捉基準を計算することと、
j)少なくとも1つの判定基準を満たす対照プローブ捕捉基準を有する前記MIPアンプリコンの前記集団における部位捕捉基準のサブセットを同定することと、
k)前記部位捕捉基準を、前記少なくとも1つの判定基準を満たす対照プローブ捕捉基準の前記サブセットから計算した係数で正規化して、検査正規化部位捕捉基準を得ることと、
l)工程b)〜工程h)における同一の標的部位及び対照部位、標的集団、対照集団のサブセットを用いて、前記検査正規化部位捕捉基準を、既知の遺伝子型を示す参照対象から得た参照ゲノムDNA試料に基づいて計算した複数の参照正規化部位捕捉基準と比較することと、
m)工程l)の前記比較、及び、参照対象の前記既知の遺伝子型に基づいて、異数性が前記胎児において検出されるかどうかを判定することと、
を含む、前記方法。
a)前記複数の候補MIPの核酸配列を受信することと、
b)前記複数の候補MIP中のそれぞれの対応するMIPについて、
i)前記対応するMIPにより捕捉されると予測される、目的の染色体上におけるミスマッチのない固有部位の第1の数(A)を計算することと、
ii)前記対応するMIPにより捕捉されると予測される、前記目的の染色体上におけるミスマッチが1つある固有部位の第2の数(C)を計算することと、
iii)前記対応するMIPにより捕捉されると予測される、ゲノムの全体にわたるミスマッチのない固有部位の第3の数(E)を計算することと、
iv)前記対応するMIPにより捕捉されると予測される、前記ゲノムの全体にわたるミスマッチが1つある固有部位の第4の数(G)を計算することと、
v)前記対応するMIPにより捕捉されると予測される、前記ゲノムの全体にわたるミスマッチのない非固有部位の第5の数(F)を計算することと、
vi)前記対応するMIPにより捕捉されると予測される、前記ゲノムの全体にわたるミスマッチが1つある非固有部位の第6の数(H)を計算することと、
vii)前記第1の、第2の、第3の、第4の、第5の、及び、第6の数の少なくとも一部に基づいて、前記対応するMIPの性能測定基準を計算することと、
c)工程b)vii)で前記複数の候補MIP中のそれぞれのMIPについて計算した前記性能測定基準の少なくとも一部に基づいて、MIPを選択することと、
を含む、前記方法。
a)前記複数の候補MIPの核酸配列を受信することと、
b)前記複数の候補MIP中のそれぞれの対応するMIPについて、
i)前記対応するMIPにより捕捉されると予測される、目的の染色体上におけるミスマッチのない固有部位の第1の数(A)を計算することと、
ii)前記対応するMIPにより捕捉されると予測される、前記目的の染色体上におけるミスマッチが1つある固有部位の第2の数(C)を計算することと、
iii)前記第1及び第2の数の少なくとも一部に基づいて、前記対応するMIPの性能測定基準を計算することと、
c)工程b)iii)で前記複数の候補MIP中のそれぞれのMIPについて計算した前記性能測定基準の少なくとも一部に基づいて、MIPを選択することと、
を含む、前記方法。
a)前記複数の候補MIPの核酸配列を受信することと、
b)前記複数の候補MIP中のそれぞれの対応するMIPについて、
i)前記対応するMIPにより捕捉されると予測される、目的の染色体上におけるミスマッチのない固有部位の第1の数(A)を計算することと、
ii)前記対応するMIPにより捕捉されると予測される、前記ゲノムの全体にわたるミスマッチのない非固有部位の第2の数(F)を計算することと、
iii)前記第1及び第2の数の少なくとも一部に基づいて、前記対応するMIPの性能測定基準を計算することと、
c)工程b)iii)で前記複数の候補MIP中のそれぞれのMIPについて計算した前記性能測定基準の少なくとも一部に基づいて、MIPを選択することと、
を含む、前記方法。
a)前記複数の候補MIPの核酸配列を受信することと、
b)前記複数の候補MIP中のそれぞれの対応するMIPについて、
i)前記対応するMIPにより捕捉されると予測される、目的の染色体上におけるミスマッチのない固有部位の第1の数(A)を計算することと、
ii)前記対応するMIPにより捕捉されると予測される、ゲノムの全体にわたるミスマッチのない固有部位の第2の数(E)を計算することと、
iii)前記第1及び第2の数の少なくとも一部に基づいて、前記対応するMIPの性能測定基準を計算することと、
c)工程b)iii)で前記複数の候補MIP中のそれぞれのMIPについて計算した前記性能測定基準の少なくとも一部に基づいて、MIPを選択することと、
を含む、前記方法。
式中、(N)xは第1の固有分子タグを表し、(N)yは第2の固有分子タグを表し、式中、X及びYは4〜15塩基対であり、
式中、Aは、i)5´−TGCACTCCAGCCTG−3´(配列番号:15)の配列、または、5´−TGCACTCCAGCCTG−3´(配列番号:15)の配列に少なくとも85%類似した配列を含み、ii)30塩基対以下の長さを有し、
式中、Cは、i)5´−GAGGCTGAGGCAGGA−3´(配列番号:16)の配列、または、5´−GAGGCTGAGGCAGGA−3´(配列番号:16)の配列に少なくとも85%類似した配列を含み、ii)30塩基対以下の長さを有する、
前記核酸分子。
式中、(N)xは第1の固有分子タグを表し、(N)yは第2の固有分子タグを表し、式中、X及びYは4〜15塩基対であり、
式中、Aは、i)5´−TCCTGCCTCAGCCTC−3´(配列番号:17)の配列、または、5´−TCCTGCCTCAGCCTC−3´(配列番号:17)の配列に少なくとも85%類似した配列を含み、ii)30塩基対以下の長さを有し、
式中、Cは、i)5´−AGGCTGGAGTGC−3´(配列番号:18)の配列、または、5´−AGGCTGGAGTGC−3´(配列番号:18)の配列に少なくとも85%類似した配列を含み、ii)30塩基対以下の長さを有する、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
式中、(N1−6)は第1の固有分子タグを表し、(N7−12)は第2の固有分子タグを表す、
前記核酸分子。
[図面の簡単な説明]
[図2]本開示における一部の方法に従い、プローブを設計及び選択するための例示的なプロセスを示すフローチャートである。
[図3]本開示における一部の方法に従い、検査対象の異数性状態を予測するための例示的なプロセスを示すフローチャートである。
[図4]本開示における一部の方法に従い、検査対象の異数性状態を予測するための、より詳細な別の例示的なプロセスを示すフローチャートである。
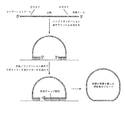
[図5]本開示における一部の方法に用いる、例示的な分子反転プローブ(MIP)の配列を示す図である。MIPは、以下の構成要素、第1の標的ポリヌクレオチドアーム(「ライゲーションアーム」と記載)、ポリヌクレオチドリンカー(「主鎖」と記載)、及び、第2の標的ポリヌクレオチドアーム(「伸長アーム」と記載)を配列内に含み、またそのリンカーは、第1の固有標的分子タグ(「6N」と記載)、PCR用フォワードプライマー、PCR用リバースプライマー、及び、第2の固有標的分子タグ(こちらも「6N」と記載)を含む。MIPのそれぞれにおける第1及び第2の標的ポリヌクレオチドアームは、目的の部位に隣接する、核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的である。固有分子タグは、ランダムなポリヌクレオチド配列である。一部の実施形態では、「実質的に相補的」とは、両方のアームにおいてミスマッチが0であること、または、一方のアームのみにおいてミスマッチがせいぜい1であることを意味する(例えば、標的ポリヌクレオチドアームが、目的の部位に隣接する、核酸内の第1及び第2の領域にそれぞれハイブリダイズする場合)。一部の実施形態では、「実質的に相補的」とは、両方のアームにおいてミスマッチの数が少ないこと、例えば、せいぜい1、2、3、3、5、6、7、または、8であることを意味する。
[図6]本開示の方法における、プローブによるハイブリダイゼーション及び伸長/ライゲーションを示す図である。第1の標的ポリヌクレオチドアーム(「ライゲーションアーム」と記載)及び第2の標的ポリヌクレオチドアーム(「伸長アーム」と記載)を、DNA鋳型にハイブリダイズするのに好適な条件下で、DNAにMIPを添加する。ハイブリダイゼーション後、伸長/ライゲーション条件下で、ポリメラーゼ及びリガーゼを添加してから、ライゲーションアームと伸長アームとの間に固有ギャップ配列を含む目的の標的配列全体にわたりDNA合成を行うことにより、環状オリゴヌクレオチド(「捕捉済みプローブ」)を作製する。アンプリコン及びcsDNAが融解すると、捕捉済みプローブを増幅する準備が整う。
[図7]捕捉済みプローブの増幅及びシークエンシングを示す図である。シークエンシングアダプター及びPCR用フォワードプライマーまたはPCR用リバースプライマーを含む核酸分子を環状アンプリコンの主鎖に結合させてから、MIPにより作製された全ての環状オリゴヌクレオチドをPCRを用いて増幅する。その後、例えば、次世代シークエンシング(NGS)を用いてアンプリコンのシークエンスを行ってから、それぞれのアンプリコン内に存在する固有分子タグの数をカウントすることにより、得られたアンプリコンのリード数を測定する。
[図8]21番染色体トリソミー(ダウン症候群)検査の結果を示す図である。検査した48点の試料のうち46点がダウン症候群に対して陰性であった一方、2点の試料がダウン症候群に対して陽性であった。2点の陽性試料を、Z値が6超の上部右側に示す。
[図9]本開示の実施形態における、Alu因子へのプローブのハイブリダイゼーションを示す図である。
[図10]トリソミー13を検出するためのMIP実施例において評価した、検査性能を示す図である。
[図11]トリソミー18を検出するためのMIP実施例において評価した、検査性能を示す図である。
[図12]トリソミー21を検出するためのMIP実施例において評価した、検査性能を示す図である。
本開示を更に明示するために、本明細書において、以下の用語及び定義を提供する。
現行のシークエンシング法は、有効な変動係数を得るのに数千万ものリードを必要とする面倒なシークエンシングライブラリ調製工程を採用しており、試料中における胎児由来の比率が4%未満に下がる場合、その有効性が失われることがある。非標的「ショットガン」法は、ヒト異数性に関連する染色体における適切な領域のカバレッジを得るのに、本質的に多数のリードを必要とする。標的法は、多数のPCR用プライマー操作、及び多重化を必要とする。ライブラリ調製において、反復領域のPCR増幅に1種類のプライマーペアを用いる方法では、生成配列に不明瞭さ(干渉)を生じさせるPCRアーティファクトの悪影響を受ける場合があり、特徴的なマッピングリードの比率、及び、全体効率が低下してしまう。
a)母体血液試料から単離した核酸試料を得ることと、
b)分子反転プローブ(MIP)の1つまたは複数の集団を用いることにより、工程a)で得た核酸試料中における複数の目的の標的配列を捕捉して、複数のレプリコンを作製することと、
MIP集団内のMIPのそれぞれは、以下の構成要素、
第1の標的ポリヌクレオチドアーム、及び、第2の標的ポリヌクレオチドアームを、配列内に含み、
MIPのそれぞれにおける一対の第1及び第2の標的ポリヌクレオチドアームは、同一であり、第1の複数の目的の標的配列内におけるそれぞれの配列に隣接する、核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的であり、
c)目的の標的配列を増幅することと、
d)目的の標的配列をシークエンスすることと、
e)遺伝子座において、目的の標的配列をインシリコでゲノム配列にマッチさせることと、
f)個々の遺伝子座においてマッチするアンプリコンの数をカウントし、検査染色体上の遺伝子座にマッチするアンプリコンの数を、参照染色体上の遺伝子座にマッチするアンプリコンの数と比較すること。
a)母体血液試料から単離した核酸試料を得ることと、
b)分子反転プローブ(MIP)の1つまたは複数の集団を用いることにより、工程a)で得た核酸試料中における複数の目的の標的配列を捕捉して、複数のレプリコンを作製することと、
MIP集団内のMIPのそれぞれは、以下の構成要素、
第1の標的ポリヌクレオチドアーム−第1の固有分子タグ−ポリヌクレオチドリンカー−第2の固有分子タグ−第2の標的ポリヌクレオチドアームを配列内に含み、
MIPのそれぞれにおける一対の第1及び第2の標的ポリヌクレオチドアームは、同一であり、複数の目的の標的配列内におけるそれぞれの配列に隣接する、核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的であり、
MIPのそれぞれにおける第1及び第2の固有標的分子タグの組み合わせは、MIPのそれぞれにおいて異なっており、
c)工程b)で得たレプリコンから増幅した複数のMIPアンプリコンをシークエンスすることと、
d)レプリコンを増幅したそれぞれのMIPにおける固有分子タグの数に基づいて、工程c)で得た複数のアンプリコンにおける第1のアンプリコン集団のそれぞれの捕捉現象の数を測定することと、第1のアンプリコン集団は、目的の標的配列のシークエンスにより同定され、
e)レプリコンを増幅したそれぞれのMIPにおける固有分子タグの数に基づいて、工程c)で得た複数のアンプリコンにおける第2のアンプリコン集団のそれぞれの捕捉現象の数を測定することと、第2のアンプリコン集団は、目的の標的配列のシークエンスにより同定され、
f)工程d)で測定したシークエンシングリードの数の少なくとも一部に基づいて、そこから第1のアンプリコン集団を作製した、それぞれの目的の標的配列の部位捕捉基準を決定することと、
g)少なくとも1つの判定基準を満たす、工程f)で決定した部位捕捉基準の第1のサブセットを同定することと、
h)工程e)で測定した捕捉現象の数の少なくとも一部に基づいて、そこから第2のアンプリコン集団を作製した、それぞれの目的の標的配列の部位捕捉基準を決定することと、
i)少なくとも1つの判定基準を満たす、工程h)で決定した部位捕捉基準の第2のサブセットを同定することと、
j)工程g)で同定した部位捕捉基準の第1のサブセットから求めた第1の指標を、工程i)で同定した部位捕捉基準の第2のサブセットから求めた第2の指標で正規化して、検査比率を得ることと、
k)検査比率を、正倍数性または異数性を示すことが既知である参照対象から単離した参照核酸試料に基づいて計算した、複数の参照比率と比較することと、
l)工程k)の比較に基づいて、異数性が胎児において検出されるかどうかを判定すること。あるいは、この方法を用いて、胎児ではない対象内における異数性を検出することも可能である。特定の実施形態では、異数性の検出に代えて、本開示の方法を用いて、染色体のアーム内における遺伝的機能の欠失及び重複に加えて、微細欠失及び微細重複、極微細欠失及び極微細欠失、及び、一塩基多型、一塩基欠失、及び、一塩基挿入を含む一ヌクレオチド機能を検出及び定量することができる。
a)母体血液試料由来のゲノムDNA試料を得ることと、
b)ゲノムDNA試料を、マルチウェルプレートのそれぞれのウェルへと加えることと、マルチウェルプレートのそれぞれのウェルはプローブ混合液を含み、プローブ混合液は分子反転プローブ(MIP)集団及び緩衝液を含み、
MIP集団内のそれぞれのMIPは、以下の構成要素、
第1の標的ポリヌクレオチドアーム−第1の固有分子タグ−ポリヌクレオチドリンカー−第2の固有分子タグ−第2の標的ポリヌクレオチドアームを配列内に含み、
MIPのそれぞれにおける一対の第1及び第2の標的ポリヌクレオチドアームは、同一であり、複数の目的の標的配列内におけるそれぞれの配列に隣接する、核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的であり、
MIPのそれぞれにおける第1及び第2の固有標的分子タグの組み合わせは、MIPのそれぞれにおいて異なっており、
c)MIPのプローブ混合液を含むゲノムDNA試料をインキュベートして、複数の目的の標的配列を捕捉することと、
d)伸長/ライゲーション用混合液を、MIP及び複数の目的の標的配列を含むc)の試料へと加えて、複数のMIPアンプリコンを作製することと、伸長/ライゲーション用混合液は、ポリメラーゼ、複数のdNTP、リガーゼ、及び、緩衝液を含み、
e)エキソヌクレアーゼ混合液を、標的及び対照MIPアンプリコンへと加えて、過剰プローブまたは過剰ゲノムDNAを除去することと、
f)インデックスPCR用混合液をe)の試料へと加えて、一対のインデックスプライマー、固有試料バーコード、及び、一対のシークエンシングアダプターを、複数のアンプリコンへと加えることと、
g)超並列シークエンシング法を用いて、固有標的分子タグの数に基づいて、工程f)で提供したバーコード化アンプリコンの第1の集団におけるシークエンシングリードの数を測定することと、バーコード化アンプリコンの第1の集団は、目的の標的配列のシークエンスにより同定され、
h)超並列シークエンシング法を用いて、固有標的分子タグの数に基づいて、工程f)で提供したバーコード化アンプリコンの第2の集団におけるシークエンシングリードの数を測定することと、バーコード化アンプリコンの第2の集団は、目的の標的配列のシークエンスにより同定され、
i)工程g)で測定した第1のシークエンシングリードの数の少なくとも一部に基づいて、部位捕捉基準を計算し、工程h)で測定した第2のシークエンシングリードの数の少なくとも一部に基づいて、複数の対照プローブ捕捉基準を計算することと、
j)少なくとも1つの判定基準を満たす対照プローブ捕捉基準を有するMIPアンプリコンの集団における部位捕捉基準のサブセットを同定することと、
k)部位捕捉基準を、少なくとも1つの判定基準を満たす対照プローブ捕捉基準のサブセットから計算した係数で正規化して、検査正規化部位捕捉基準を得ることと、
l)工程b)〜工程h)における同一の標的部位及び対照部位、標的集団、対照集団のサブセットを用いて、検査正規化部位捕捉基準を、既知の遺伝子型を示す参照対象から得た参照ゲノムDNA試料に基づいて計算した複数の参照正規化部位捕捉基準と比較することと、
m)工程l)の比較、及び、参照対象の既知の遺伝子型に基づいて、異数性が胎児において検出されるかどうかを判定すること。
a)複数の候補MIPの核酸配列を受信することと、
b)複数の候補MIP中のそれぞれの対応するMIPについて、
i)対応するMIPにより捕捉されると予測される、目的の染色体上におけるミスマッチのない固有部位の第1の数(A)を計算することと、
ii)対応するMIPにより捕捉されると予測される、目的の染色体上におけるミスマッチが1つある固有部位の第2の数(C)を計算することと、
iii)対応するMIPにより捕捉されると予測される、ゲノムの全体にわたるミスマッチのない固有部位の第3の数(E)を計算することと、
iv)対応するMIPにより捕捉されると予測される、ゲノムの全体にわたるミスマッチが1つある固有部位の第4の数(G)を計算することと、
v)対応するMIPにより捕捉されると予測される、ゲノムの全体にわたるミスマッチのない非固有部位の第5の数(F)を計算することと、
vi)対応するMIPにより捕捉されると予測される、ゲノムの全体にわたるミスマッチが1つある非固有部位の第6の数(H)を計算することと、
vii)第1の、第2の、第3の、第4の、第5の、及び、第6の数の少なくとも一部に基づいて、対応するMIPの性能測定基準を計算することと、
c)工程b)vii)で複数の候補MIP中のそれぞれのMIPについて計算した性能測定基準の少なくとも一部に基づいて、MIPを選択すること。
図1は、本明細書に記載するプロセス(プロセス200、プロセス300、及び、プロセス500を含む)のいずれかを実行するためのコンピュータデバイス100のブロック図である。本発明で使用する場合、用語「プロセッサ」または「コンピュータデバイス」とは、本明細書に記載のコンピュータ技術の1つまたは複数を実行するように構成された、1つまたは複数のコンピュータ、マイクロプロセッサ、論理回路、サーバ、または、ハードウェア、ファームウェア、及び、ソフトウェアを備えたその他のデバイスのことを意味する。プロセッサ及び処理デバイスは更に、入力、出力、及び、処理中データを格納するための、1つまたは複数のメモリデバイスを含んでいてもよい。コンピュータデバイス100としては、1つまたは複数の入力デバイス(例えば、キーパッド、タッチスクリーン、トラックボール、音声認識システムなど)、及び/または、1つまたは複数の出力デバイス(例えば、表示装置、スピーカー、触感ディスプレイ、印刷装置など)の任意の適切な組み合わせが挙げられるがこれらに限定されない、「ユーザインターフェース」を挙げてもよい。コンピュータデバイス100としては、本明細書に記載のコンピュータ技術の1つまたは複数を実行するように構成された、1つまたは複数のハードウェア、ファームウェア、及び、ソフトウェアの任意の適切な組み合わせを挙げてもよいが、これらに限定されない。本明細書に記載する構成部材のそれぞれは、1つまたは複数のコンピュータデバイス100上に実装されてもよい。特定の態様では、これらシステムにおける複数の構成部材は、1つのコンピュータデバイス100内に含まれていてもよい。特定の実施形態では、構成部材及び格納デバイスは、いくつかのコンピュータデバイス100にわたり実装されていてもよい。
・レフトプライマーの長さ:18、19、20、21塩基対(bp)
・プライマーペアの頻度:100、250、500、2500、5000、10000
・アンプリコンの長さ:50〜150bp、例えば、85bp未満
・プライマーあたりの最低GC含有量:40%
・アンプリコンの固有性(目的の標的配列が固有であるパーセント):80%超
・ゲノム内におけるプライマーの分布:反復ラン、それぞれのバケットサイズ(bs)が1〜50%の範囲、バケットフィル(bf)が1〜bs−1(バケットサイズ(bs)とは、ゲノム長のbs%のことを意味し、それぞれのバケットは全ヒットのbf%を含む必要がある)
レフトアーム内に1つのミスマッチがあり、ライトアーム内に0のミスマッチがある
レフトアーム内に0のミスマッチがあり、ライトアーム内に1つのミスマッチがある
レフトアーム内に1つのミスマッチがあり、ライトアーム内に1つのミスマッチがある
レフトアーム内に2つのミスマッチがあり、ライトアーム内に0のミスマッチがある、または、
レフトアーム内に0のミスマッチがあり、ライトアーム内に2つのミスマッチがある
それぞれの候補プライマーまたは候補プローブ用の例示的な目的関数を、目的の染色体(例えば、21番染色体)由来の有効リード総数として定義してもよい。
それぞれの候補プライマーまたは候補プローブ用の別の例示的な目的関数を、目的の染色体(例えば、21番染色体)上の有効部位総数として定義してもよい。
それぞれの候補プライマーまたは候補プローブ用の目的関数を求めるための包括的な手法においては、以下の式を用いる。
[実施例]
実施例1:
MIP設計、及び、目的の標的配列を捕捉するための方法
図5に示すように、80〜105bpのサイズ範囲の単一オリゴヌクレオチド(第1及び第2の標的ポリヌクレオチドアームの長さによる)を合成する。6Nボックスとは、それぞれの目的の標的配列における捕捉現象を定量するために用いる分子タグ配列のことを意味する。この特定の実施形態では、リードをカウントする代わりに、捕捉部位あたりの固有配列の数をカウントする。
第1及び第2の標的ポリヌクレオチドアーム(実験で決めた濃度の)を、20uL緩衝反応液中の1〜2mL血漿から抽出したcsDNAと混合した。混合液を、サーモサイクラー内で、プローブを鋳型へとアニールするのに最適化した温度でインキュベートした(98℃で3分間→85℃で30分間→66℃で15分間)。このインキュベーションの間に、プローブ分子は、プローブ配列に対して相補的な特定の染色体位置において、csDNA鋳型にアニールする(図6の中央)。最も容易に予測される部位は、第1及び第2の標的ポリヌクレオチドアームに対して正確に相補的な配列を有する部位(不変部位)であるが、一方のアームに1つまたは複数の変異を有する部位もまた、やや効率は低くなるが標的となる。それぞれの反応液中における最適量のMIPは、以下の3つの変動要因によって決まる。1)鋳型として用いるゲノム数(個体により幅広く変動し得る)、2)特定のプローブが標的とする総部位数、及び、3)不変部位と変異部位の比率。
捕捉済みMIPの混合液(20uL)を、反応用混合液(耐熱性ポリメラーゼ、dNTPS、PCR緩衝液、及び、プローブ主鎖に対して相補的なユニバーサルプライマーを含有)(50uL)へと加えた(図Fの上部)。プールした試料ライブラリのマルチプレックスシークエンシングを可能とする、異なる「バーコード」配列を有するプライマーを用いて、それぞれの試料を増幅させた。電気泳動できれいなアンプリコンバンドが観察されるまで、反応液を実験で決めた数のPCRサイクルに供した。Ampureビーズを用いてPCR産物を精製してから、Qubitフルオロメーターを用いて定量した。
全ての試料が等しい濃度となり、リードの割り当てが試料全体にわたり確実に均一となるように、精製したPCR産物をライブラリにプールした。部位特異的なギャップの完全配列を決定するために、シングルエンドシークエンシングまたはペアエンドシークエンシングのいずれかを用いて、75〜100サイクルでライブラリをシークエンスした。シングルエンドシークエンシングを用いる場合、リードは、ライゲーションアームに続き、分子タグ、及び、伸長/ライゲーション工程中に埋められた固有ギャップ配列からなる。伸長アームのシークエンシングは、プローブから配列が判明しているため不要である。
シークエンスデータ解析、及び、対象内の異数性検出
異数性検出に有用とするために、シークエンシングの生データを処理する必要がある。まず最初に、シークエンシングリードをフィルタリングし、既知のアーティファクト(プローブ−プローブ間の相互作用、主鎖配列、または、アダプター配列など)を除去する。それから、MIPのライゲーションアーム及び伸長アーム(すなわち、第1及び第2の標的ポリヌクレオチドアーム)を、それぞれのアーム内に最大1塩基対のミスマッチを許容として、シークエンスリードにマッチさせる。この基準に適合しないリードを無効として扱い棄却する。有効リードのアーム配列をトリミングし、続く処理工程で使用するリードファイルからシークエンスを削除することにより、シークエンスデータから非ゲノム部分を除去する。同時に、ライゲーション末端及び伸長末端の両方にある分子タグは、後の工程にて捕捉現象をカウントするために別々に残す。bowtie2ソフトウェアプログラムを用いて、トリミングしたリードをヒトゲノム(hg19)にアラインする。それから、samtoolsソフトウェアプログラムを用いて、アラインしたリードに対してフィルタリングを行い、有効ペアとしてアラインしないリード、または、非固有にアラインするリードを除去する。固有にアラインしたリードのみを残すように、アライメントパラメータ及びフィルタリングパラメータを慎重に選択する。アラインしフィルタリングしたリード(bam形式ファイル)を調査し、固有MIPギャップ配列を有するそれぞれの標的部位(すなわち、固有な目的の標的配列)の固有分子タグをカウントする。これらのカウントは、次世代シークエンシングプラットフォーム(例えば、Illumina HiSeq 2500フローセル)を用いてシークエンスしたMIP−標的ハイブリダイゼーション現象における、初期の数である。個々のそれぞれの部位における部位捕捉性能指標(SCE)を計算する。個々のそれぞれの部位における部位捕捉密度指標(SCC)を、SCEの変動係数として計算する。実験データから得た部位捕捉性能の変動指標に基づいて、これら部位の一部を棄却する。この工程には、染色体比率における試料−試料間のばらつきを抑え、後の工程で計算する陽性試料のZ値を上昇させる働きがある。任意の試料について、目的の染色体(例えば、21番染色体)上における残りの部位由来の固有分子タグカウントの合計(S1)を計算し保存する。残りの参照部位における合計(S2)を計算し保存する。2つの合計間の比率(染色体比率 = S1/(S1+S2))を、任意の試料における目的の染色体の比率指標として計算する。それぞれの検査試料について、正常な胎児染色体カウント(すなわち、正常核型の胎児)を有する参照試料集合と対照させて、染色体比率指標を用いて目的の染色体(例えば、21番染色体)のZ値を計算する。任意の試料におけるZ値の絶対値が所定の閾値を超えた場合に、異数性(例えば、トリソミー及びモノソミー)または正倍数性の同定を行う。
妊娠している対象内における13トリソミー、18トリソミー、及び、21トリソミーの検出
本実施例では、本明細書に記載の方法を用いて、13トリソミー、トリソミー18、及び、トリソミー21を有する妊娠女性と、健康な妊娠女性とを識別(または分類)することについて説明する。
妊娠女性由来の血漿試料(48点)の訓練事例集合(治験審査委員会承認済みの研究)を用いて、13トリソミー、18トリソミー、及び、21トリソミーを検出するためのZ値カットオフを決定した。血漿試料のそれぞれは、異なる妊娠女性から採取した。48点の血漿試料には、40点の健康な試料、4点の21トリソミー試料、3点の18トリソミー試料、及び、1点の13トリソミー試料が含まれていた。CVS(絨毛採取)または羊水穿刺で採取した胎盤細胞または胎児細胞の核型解析により、トリソミー症例を確認した。
48人の妊娠女性のそれぞれから抽出した血漿DNAに対して、以下の部位捕捉反応を実施した。抽出した血漿DNAを、実験で決めたプローブ濃度で、水、Ampligase緩衝液(1x)、及び、RO−MIPと混合した。部位捕捉反応用混合液を、サーマルサイクラー内で、98℃で3分間、85℃で30分間、そして66℃で15分間インキュベートした。インキュベート後、dNTP(0.6mM)、NAD(0.4x)、ベタイン(0.3M)、Ampligase緩衝液(1x)、水、Ampligase(5ユニット)、及び、Phusion HFポリメラーゼ(0.4ユニット)を含有するマスターミックスを、部位捕捉反応用混合液に加えた。それから、混ぜ合わせた混合液を、サーマルサイクラー内で、66℃で60分間、そして、72℃で30分間インキュベートしてから、4℃で保持した。
インキュベート後、混ぜ合わせた混合液(20μL)を、フォワードインデックスプライマー(500nM)及びリバースインデックスプライマー(500nM)、Phusion HF緩衝液(1x)、dNTP(0.2mM)、水、ならびに、Phusion HSポリメラーゼ(0.4ユニット)を含有するPCRマスターミックスに加えた。固有のリバースプライマーインデックスを用いて、それぞれの試料にバーコードを付加した。PCR反応用混合液を、サーマルサイクラー内で、98℃で3分間、98℃で10秒間を20サイクル、65℃で20秒間、そして72℃で30秒間インキュベートした。それから、PCR反応用混合液を72℃で5分間保持後、4℃で保持した。
PCR増幅したライブラリをAmpureXPビーズで精製し、試料を等しい濃度で共にプールした(プールあたり試料48点)。マルチプレックスライブラリのそれぞれを、シングルSRフローセルにロードし、HiSeq 2500のRapid Runモードで106サイクル、シークエンスした。
シークエンシングデータをフィルタリングしアラインした。それぞれの染色体(すなわち、13番染色体、18番染色体、または、21番染色体)に固有にアラインしたリード由来の固有分子タグ/識別子の数(この分子は「A」と「C」との合計に類似)を、1番染色体〜22番染色体に固有にアラインしたリード由来の固有分子タグ/識別子の総数(この分母は「A」、「C」、「E」及び「G」の合計に類似)で割ることにより、13番染色体、18番染色体、及び、21番染色体の染色体比率(Pi)を計算した。しかしながら、表2の値(E〜H)がゲノム全体(1番染色体〜22番染色体、X染色体、及び、Y染色体を含む)にわたる全ての染色体を含む一方で、ここでの分母は、X染色体またはY染色体にアラインするリードを含まない場合がある。詳細には、X染色体またはY染色体にアラインするリードの数は、その他の染色体(目的の染色体を含む)にアラインするリードの数よりも著しく多い場合がある。この場合、分母内に、X染色体またはY染色体にアラインするリードを含むことは、結果として得られる比率を著しく下げる場合があり、Z統計値の計算にノイズ及びひずみが生じる恐れがある。それゆえ、目的の染色体がX染色体でもY染色体でもない場合(例えば、常染色体異数性を検出する場合)、X染色体またはY染色体にアラインするリードは、分子及び分母の両方から除外され得る。あるいは、目的の染色体が性染色体である場合(例えば、性染色体異数性を検出する場合)、X染色体及び/またはY染色体にアラインするリードは、分子及び分母に含まれ得る。
妊娠女性由来の試料(422点)のテスト事例集合(治験審査委員会承認済みの研究)を用いて、テストの感度及び特異度を測定した。それぞれの試料は、異なる妊娠女性から採取した。これら422点の試料には、387点の健康な試料、21点のT21試料、9点のT18試料、及び、5点のT13試料が含まれていた。CVSまたは羊水穿刺で採取した胎盤細胞または胎児細胞の核型解析により、トリソミー症例を確認した。
422人の妊娠女性のそれぞれから抽出した血漿DNAに対して、以下の部位捕捉反応を実施した。抽出した血漿DNAを、実験で決めたプローブ濃度で、水、Ampligase緩衝液(1x)、及び、RO−MIPと混合した。捕捉反応用混合液を、サーマルサイクラー内で、98℃で3分間、85℃で30分間、そして66℃で15分間インキュベートした。インキュベート後、dNTP(0.6mM)、NAD(0.4x)、ベタイン(0.3M)、Ampligase緩衝液(1x)、水、Ampligase(5ユニット)、及び、Phusion HFポリメラーゼ(0.4ユニット)を含有するマスターミックスを、部位捕捉反応用混合液に加えた。それから、混ぜ合わせた反応用混合液を、サーマルサイクラー内で、66℃で60分間、そして、72℃で30分間インキュベートしてから、4℃で保持した。
インキュベート後、混ぜ合わせた混合液(20μL)を、フォワードインデックスプライマー(500nM)及びリバースインデックスプライマー(500nM)、Phusion HF緩衝液(1x)、dNTP(0.2mM)、水、ならびに、Phusion HSポリメラーゼ(0.4ユニット)を含有するPCRマスターミックスに加えた。固有のリバースプライマーインデックスを用いて、それぞれの試料にバーコードを付加した。PCR反応用混合液を、サーマルサイクラー内で、98℃で3分間、98℃で10秒間を20サイクル、65℃で20秒間、そして72℃で30秒間インキュベートした。それから、PCR反応用混合液を72℃で5分間保持後、4℃で保持した。
増幅ライブラリをAmpureXPビーズで精製し、試料を等しい濃度で共にプールした(プールあたり試料48点)。全体で9つのプールがあり、最初の8つのプールは、プールあたり47点の検査試料及び1点の対照試料を含み、9つ目のプールは、46点の検査試料及び1点の対照試料を含んでいた。マルチプレックスライブラリのそれぞれを、シングルSRフローセルにロードし、HiSeq 2500のRapid Runモードで106サイクル、シークエンスした。
訓練事例集合と同様に、422人の妊娠女性それぞれに由来するDNAに対して、部位捕捉反応、捕捉部位の増幅、及び、106サイクルのシングルエンドシークエンシングを実施した。それぞれの試料から得たシークエンスデータを用いて、13番染色体、18番染色体、及び、21番染色体のZ値を計算した(図10〜図12)。訓練事例集合により決定したカットオフを用いると、特異度(例えば、真陰性率、または、真陰性数を真陰性と偽陽性との合計で割ったもの)は、13トリソミーで5/5、18トリソミーで9/9、及び、21トリソミーで21/21となり、>99.9%となった。感度(例えば、真陽性率、または、真陽性数を真陽性と偽陰性との合計で割ったもの)は、13番染色体で>99.2%となり、18番染色体で>99.9%となり、また、21番染色体で>99.5%となった。
Claims (22)
- 胎児における異数性をスクリーニングするための方法であって、
a)母体血液試料から単離した核酸試料を得ることと、
b)分子反転プローブ(MIP)の1つまたは複数の集団を用いることにより、工程a)で得た前記核酸試料中における複数の目的の標的配列を捕捉して、複数のレプリコンを作製することと、
前記MIP集団内の前記MIPのそれぞれは、
i)一対の第1及び第2の標的ポリヌクレオチドアームであって、前記MIPのそれぞれにおける前記第1及び第2の標的ポリヌクレオチドアームの対は、同一であり、且つ、前記複数の目的の標的配列におけるそれぞれの配列に隣接する、前記核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的である、前記一対の第1及び第2の標的ポリヌクレオチドアーム;
ii)1つまたは複数の固有分子タグ;及び
iii)ポリヌクレオチドリンカー;
を含み、
c)工程b)で得た前記レプリコンから増幅した複数のMIPアンプリコンをシークエンスすることと、
d)レプリコンを増幅したそれぞれのMIPにおける前記固有分子タグの数に基づいて、工程c)で得た前記複数のアンプリコンにおける第1のアンプリコン集団のそれぞれの捕捉現象の数を測定することと、前記第1のアンプリコン集団は、前記目的の標的配列の前記シークエンスにより同定され、
e)レプリコンを増幅したそれぞれのMIPにおける前記固有分子タグの数に基づいて、工程c)で得た前記複数のアンプリコンにおける第2のアンプリコン集団のそれぞれの捕捉現象の数を測定することと、前記第2のアンプリコン集団は、前記目的の標的配列の前記シークエンスにより同定され、
f)工程d)で測定した捕捉現象の数の少なくとも一部に基づいて、そこから前記第1のアンプリコン集団を作製した、それぞれの目的の標的配列の部位捕捉基準を決定することと、
g)少なくとも1つの判定基準を満たす、工程f)で決定した前記部位捕捉基準の第1のサブセットを同定することと、
h)工程e)で測定した捕捉現象の数の少なくとも一部に基づいて、そこから前記第2のアンプリコン集団を作製した、それぞれの目的の標的配列の部位捕捉基準を決定することと、
i)前記少なくとも1つの判定基準を満たす、工程h)で決定した前記部位捕捉基準の第2のサブセットを同定することと、
j)工程g)で同定した部位捕捉基準の前記第1のサブセットから求めた第1の指標を、工程i)で同定した部位捕捉基準の前記第2のサブセットから求めた第2の指標で正規化して、検査比率を得ることと、
k)前記検査比率を、正倍数性または異数性を示すことが既知である参照対象から単離した参照核酸試料に基づいて計算した、複数の参照比率と比較し、前記胎児における異数性を示す検査比率の有無を判定することと、
を含む、前記方法。 - 前記1つまたは複数の固有分子タグが、前記配列内の少なくとも2つの固有分子タグ:
第1の標的ポリヌクレオチドアーム−第1の固有分子タグ−ポリヌクレオチドリンカー−第2の固有分子タグ−第2の標的ポリヌクレオチドアーム;
であり、
前記MIPのそれぞれにおける前記第1及び第2の固有分子タグの組み合わせは、前記MIPのそれぞれにおいて異なっている、請求項1に記載の方法。 - 前記核酸試料はDNAまたはRNAである、請求項1または請求項2に記載の方法。
- 前記部位捕捉基準は、部位捕捉性能指標(SCE)または部位捕捉密度指標(SCC)である、請求項1から請求項3のいずれか1項に記載の方法。
- 工程b)で提供した前記MIPレプリコンのそれぞれは、
iii)前記第1及び第2の標的ポリヌクレオチドアームをそれぞれ、前記核酸試料中の対応する前記第1及び第2の領域にそれぞれハイブリダイズすることと、前記第1及び第2の領域は目的の標的配列に隣接し、
iv)前記ハイブリダイゼーション後、ライゲーション/伸長用混合液を用いて、前記2つの標的ポリヌクレオチドアーム間に存在するギャップ領域を伸長及びライゲートし、一本鎖環状核酸分子を作製することと、
により作製される、請求項1から請求項4のいずれか1項に記載の方法。 - 請求項1から請求項5のいずれか1項に記載の方法であって、前記方法は、c)の前記シークエンシング工程の前に、インデックスPCR反応を含み、前記インデックスPCR反応は、以下の構成要素、一対のインデックスプライマー、固有試料バーコード、及び、一対のシークエンシングアダプターを、前記MIPアンプリコンのそれぞれに導入する、前記方法。
- 前記バーコード化MIPアンプリコンは、以下の構成要素、第1のシークエンシングアダプター−第1のシークエンシングプライマー−前記第1の固有分子タグ−前記第1の標的ポリヌクレオチドアーム−捕捉核酸−前記第2の標的ポリヌクレオチドアーム−前記第2の固有分子タグ−固有試料バーコード−第2のシークエンシングプライマー−第2のシークエンシングアダプター、を配列内に含む、請求項6に記載の方法。
- 前記検査比率及び前記参照比率は、染色体比率である、請求項1から請求項7のいずれか1項に記載の方法。
- 前記染色体比率は、目的の染色体由来の全固有捕捉現象の合計(S1)と、全ての染色体由来の全固有捕捉現象の合計(S1+S2)との比率により定義される、請求項8に記載の方法。
- 胎児における異数性をスクリーニングするための方法であって、
a)母体血液試料由来のゲノムDNA試料を得ることと、
b)前記ゲノムDNA試料を、マルチウェルプレートのそれぞれのウェルへと加えることと、前記マルチウェルプレートのそれぞれのウェルはプローブ混合液を含み、前記プローブ混合液は分子反転プローブ(MIP)集団及び緩衝液を含み、
前記MIP集団内のそれぞれのMIPは、
i)一対の第1及び第2の標的ポリヌクレオチドアームであって、前記MIPのそれぞれにおける前記第1及び第2の標的ポリヌクレオチドアームの対は、同一であり、且つ、前記複数の目的の標的配列におけるそれぞれの配列に隣接する、前記核酸内の第1及び第2の領域に対して、それぞれ実質的に相補的である、前記一対の第1及び第2の標的ポリヌクレオチドアーム;
ii)1つまたは複数の固有分子タグ;及び
iii)ポリヌクレオチドリンカー;
を含み、
前記MIPのそれぞれにおける前記第1及び第2の固有分子タグの組み合わせは、前記MIPのそれぞれにおいて異なっており、
c)前記MIPの前記プローブ混合液を含む前記ゲノムDNA試料をインキュベートして、前記複数の目的の標的配列を捕捉することと、
d)伸長/ライゲーション用混合液を、前記MIP及び前記複数の目的の標的配列を含むc)の前記試料へと加えて、複数のMIPアンプリコンを作製することと、前記伸長/ライゲーション用混合液は、ポリメラーゼ、複数のdNTP、リガーゼ、及び、緩衝液を含み、
e)エキソヌクレアーゼ混合液を、前記標的及び対照MIPアンプリコンへと加えて、過剰プローブまたは過剰ゲノムDNAを除去することと、
f)インデックスPCR用混合液をe)の前記試料へと加えて、一対のインデックスプライマー、固有試料バーコード、及び、一対のシークエンシングアダプターを、前記複数のアンプリコンへと加えることと、
g)超並列シークエンシング法を用いて、前記固有分子タグの数に基づいて、工程f)で提供したバーコード化アンプリコンの第1の集団におけるシークエンシングリードの数を測定することと、バーコード化アンプリコンの前記第1の集団は、前記目的の標的配列の前記シークエンスにより同定され、
h)超並列シークエンシング法を用いて、前記固有分子タグの数に基づいて、工程f)で提供したバーコード化アンプリコンの第2の集団におけるシークエンシングリードの数を測定することと、バーコード化アンプリコンの前記第2の集団は、前記目的の標的配列の前記シークエンスにより同定され、
i)工程g)で測定した第1のシークエンシングリードの数の少なくとも一部に基づいて、部位捕捉基準を計算し、工程h)で測定した第2のシークエンシングリードの数の少なくとも一部に基づいて、複数の対照プローブ捕捉基準を計算することと、
j)少なくとも1つの判定基準を満たす対照プローブ捕捉基準を有する前記MIPアンプリコンの前記集団における部位捕捉基準のサブセットを同定することと、
k)前記部位捕捉基準を、前記少なくとも1つの判定基準を満たす対照プローブ捕捉基準の前記サブセットから計算した係数で正規化して、検査正規化部位捕捉基準を得ることと、
l)工程b)〜工程h)における同一の標的部位及び対照部位、標的集団、対照集団のサブセットを用いて、前記検査正規化部位捕捉基準を、既知の遺伝子型を示す参照対象から得た参照ゲノムDNA試料に基づいて計算した複数の参照正規化部位捕捉基準と比較し、前記胎児における異数性を示す検査正規化部位捕捉基準の有無を判定することと、
を含む、前記方法。 - 前記1つまたは複数の固有分子タグが、前記配列内の少なくとも2つの固有分子タグ:
第1の標的ポリヌクレオチドアーム−第1の固有分子タグ−ポリヌクレオチドリンカー−第2の固有分子タグ−第2の標的ポリヌクレオチドアーム;
であり、
前記MIPのそれぞれにおける前記第1及び第2の固有分子タグの組み合わせは、前記MIPのそれぞれにおいて異なっている、請求項10に記載の方法。 - 前記血液試料は、全血試料、血漿試料、または、血清試料である、請求項1から請求項11のいずれか1項に記載の方法。
- 前記血液試料は、血漿試料である、請求項12に記載の方法。
- a)前記第1及び/または第2の標的ポリヌクレオチドアームの長さは、14〜30塩基対であり、及び/または、前記標的ポリヌクレオチドアームのそれぞれは、45℃〜80℃の融解温度を有し、及び/または、前記標的ポリヌクレオチドアームのそれぞれは、30%〜80%のGC含有量を有する;及び/または
b)前記第1及び/または第2の固有分子タグの長さは、4〜15塩基対であり、及び/または、前記固有分子タグのそれぞれは、45℃〜80℃の融解温度を有する;及び/または
c)前記ポリヌクレオチドリンカーは、20〜1,000塩基対の長さを有し、及び/または、前記ポリヌクレオチドリンカーは、45℃〜80℃の融解温度を有し、及び/または、前記ポリヌクレオチドリンカーは、30%〜80%のGC含有量を有する、請求項1から請求項13のいずれか1項に記載の方法。 - 前記標的ポリヌクレオチドアームのそれぞれは、30%〜70%のGC含有量を有する;及び/または、前記ポリヌクレオチドリンカーは、30%〜70%のGC含有量を有する、請求項14に記載の方法。
- 前記ポリヌクレオチドリンカーは、少なくとも1種の増幅用プライマーを含む、請求項1から請求項15のいずれか1項に記載の方法。
- 前記ポリヌクレオチドリンカーは、増幅用フォワードプライマー及び増幅用リバースプライマーを含む、請求項16に記載の方法。
- 前記増幅用フォワードプライマーの前記配列は、5´−CTTCAGCTTCCCGATTACGG−3´(配列番号:1)のヌクレオチド配列を含む;及び/または、
前記増幅用リバースプライマーの前記配列は、5´−GCACGATCCGACGGTAGTGT−3´(配列番号:2)のヌクレオチド配列を含む、請求項17に記載の方法。 - 前記ポリヌクレオチドリンカーは、5´−CTTCAGCTTCCCGATTACGGGCACGATCCGACGGTAGTGT−3´(配列番号:3)のヌクレオチド配列を含む、請求項1から請求項18のいずれか1項に記載の方法。
- 前記第1の標的ポリヌクレオチドアームは、5´−CACTGCACTCCAGCCTGG−3´(配列番号:4)のヌクレオチド配列を含む;及び/または、
前記第2の標的ポリヌクレオチドアームは、5´−GAGGCTGAGGCAGGAGAA−3´(配列番号:5)のヌクレオチド配列を含む、請求項1から請求項19のいずれか1項に記載の方法。 - 前記MIPは、5´−CACTGCACTCCAGCCTGG(N1−6)CTTCAGCTTCCCGATTACGGGCACGATCCGACGGTAGTGT(N7−12)GAGGCTGAGGCAGGAGAA−3´(配列番号:6)のヌクレオチド配列を含み、(N1−6)は前記第1の固有分子タグを表し、(N7−12)は前記第2の固有分子タグを表す、請求項1から請求項20のいずれか1項に記載の方法。
- 前記シークエンシング工程は、6〜8百万リードの読み取り深度を有する、請求項1から請求項21のいずれか1項に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562198654P | 2015-07-29 | 2015-07-29 | |
| US62/198,654 | 2015-07-29 | ||
| PCT/US2016/044914 WO2017020023A2 (en) | 2015-07-29 | 2016-07-29 | Nucleic acids and methods for detecting chromosomal abnormalities |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018524993A JP2018524993A (ja) | 2018-09-06 |
| JP2018524993A5 JP2018524993A5 (ja) | 2019-09-05 |
| JP6830094B2 true JP6830094B2 (ja) | 2021-02-17 |
Family
ID=56610036
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018503647A Active JP6830094B2 (ja) | 2015-07-29 | 2016-07-29 | 染色体異常を検出するための核酸及び方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US10465245B2 (ja) |
| EP (2) | EP3608420B1 (ja) |
| JP (1) | JP6830094B2 (ja) |
| CN (1) | CN108350500A (ja) |
| CA (1) | CA2993347A1 (ja) |
| ES (1) | ES2745556T3 (ja) |
| HK (1) | HK1256543A1 (ja) |
| WO (1) | WO2017020023A2 (ja) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2760439A1 (en) | 2009-04-30 | 2010-11-04 | Good Start Genetics, Inc. | Methods and compositions for evaluating genetic markers |
| US9163281B2 (en) | 2010-12-23 | 2015-10-20 | Good Start Genetics, Inc. | Methods for maintaining the integrity and identification of a nucleic acid template in a multiplex sequencing reaction |
| US8209130B1 (en) | 2012-04-04 | 2012-06-26 | Good Start Genetics, Inc. | Sequence assembly |
| WO2016040446A1 (en) | 2014-09-10 | 2016-03-17 | Good Start Genetics, Inc. | Methods for selectively suppressing non-target sequences |
| WO2016112073A1 (en) * | 2015-01-06 | 2016-07-14 | Good Start Genetics, Inc. | Screening for structural variants |
| ES2745556T3 (es) * | 2015-07-29 | 2020-03-02 | Progenity Inc | Acidos nucleicos y métodos para detectar anomalías cromosómicas |
| CA3005101A1 (en) * | 2015-11-16 | 2017-05-26 | Progenity, Inc. | Nucleic acids and methods for detecting methylation status |
| US10787699B2 (en) * | 2017-02-08 | 2020-09-29 | Microsoft Technology Licensing, Llc | Generating pluralities of primer and payload designs for retrieval of stored nucleotides |
| US11535886B2 (en) | 2017-06-02 | 2022-12-27 | Affymetrix, Inc. | Array-based methods for analysing mixed samples using different allele-specific labels, in particular for detection of fetal aneuploidies |
| WO2018223053A1 (en) * | 2017-06-02 | 2018-12-06 | Affymetrix, Inc. | Array-based methods for analysing mixed samples using differently labelled allele-specific probes |
| WO2018223055A1 (en) * | 2017-06-02 | 2018-12-06 | Affymetrix, Inc. | Array-based methods for analysing mixed samples using differently labelled allele-specific probes |
| AU2019247652A1 (en) | 2018-04-02 | 2020-10-15 | Enumera Molecular, Inc. | Methods, systems, and compositions for counting nucleic acid molecules |
| CN112739828B (zh) * | 2018-06-11 | 2024-04-09 | 深圳华大生命科学研究院 | 确定待测样本类型的方法及系统 |
| WO2020206170A1 (en) | 2019-04-02 | 2020-10-08 | Progenity, Inc. | Methods, systems, and compositions for counting nucleic acid molecules |
| CN112063690A (zh) * | 2020-09-18 | 2020-12-11 | 北京求臻医学检验实验室有限公司 | 单分子探针多重靶向捕获文库的构建方法及应用 |
| EP4214243A1 (en) | 2020-09-21 | 2023-07-26 | Progenity, Inc. | Compositions and methods for isolation of cell-free dna |
| CN112266948A (zh) * | 2020-11-06 | 2021-01-26 | 中山大学孙逸仙纪念医院 | 一种高通量靶向建库的方法和应用 |
| CN112458085A (zh) * | 2020-12-10 | 2021-03-09 | 北京求臻医学检验实验室有限公司 | 一种新型分子捕获优化探针及其文库构建方法 |
| WO2022140579A1 (en) * | 2020-12-24 | 2022-06-30 | Progenity, Inc. | Methods of preparing assays, systems, and compositions for determining fetal fraction |
Family Cites Families (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5866337A (en) | 1995-03-24 | 1999-02-02 | The Trustees Of Columbia University In The City Of New York | Method to detect mutations in a nucleic acid using a hybridization-ligation procedure |
| US5750341A (en) | 1995-04-17 | 1998-05-12 | Lynx Therapeutics, Inc. | DNA sequencing by parallel oligonucleotide extensions |
| US6852487B1 (en) | 1996-02-09 | 2005-02-08 | Cornell Research Foundation, Inc. | Detection of nucleic acid sequence differences using the ligase detection reaction with addressable arrays |
| SE9601676D0 (sv) | 1996-04-30 | 1996-04-30 | Ulf Landegren | Improved probing of specific mucleic acids |
| WO1997045559A1 (en) | 1996-05-29 | 1997-12-04 | Cornell Research Foundation, Inc. | Detection of nucleic acid sequence differences using coupled ligase detection and polymerase chain reactions |
| US5817921A (en) | 1996-07-12 | 1998-10-06 | Advanced Technology Materials, Inc. | Piezoelectric enviromental fluid monitoring assembly and method |
| GB9620209D0 (en) | 1996-09-27 | 1996-11-13 | Cemu Bioteknik Ab | Method of sequencing DNA |
| US6054276A (en) | 1998-02-23 | 2000-04-25 | Macevicz; Stephen C. | DNA restriction site mapping |
| WO1999049079A1 (en) | 1998-03-25 | 1999-09-30 | Ulf Landegren | Rolling circle replication of padlock probes |
| US6787308B2 (en) | 1998-07-30 | 2004-09-07 | Solexa Ltd. | Arrayed biomolecules and their use in sequencing |
| FR2784683B1 (fr) * | 1998-10-15 | 2002-12-13 | Genset Sa | Sondes fluorescentes de peinture chromosomique |
| GB9901475D0 (en) | 1999-01-22 | 1999-03-17 | Pyrosequencing Ab | A method of DNA sequencing |
| US6818395B1 (en) | 1999-06-28 | 2004-11-16 | California Institute Of Technology | Methods and apparatus for analyzing polynucleotide sequences |
| WO2001023610A2 (en) | 1999-09-29 | 2001-04-05 | Solexa Ltd. | Polynucleotide sequencing |
| EP1366192B8 (en) | 2000-10-24 | 2008-10-29 | The Board of Trustees of the Leland Stanford Junior University | Direct multiplex characterization of genomic dna |
| GB2378245A (en) | 2001-08-03 | 2003-02-05 | Mats Nilsson | Nucleic acid amplification method |
| WO2005014846A2 (en) * | 2003-07-24 | 2005-02-17 | Sequenom, Inc. | Methods for identifying risk of breast cancer and treatments thereof |
| ATE510024T1 (de) | 2003-10-31 | 2011-06-15 | Advanced Genetic Analysis Corp Ab | Verfahren zur herstellung eines gepaarten tag aus einer nukleinsäuresequenz sowie verfahren zur verwendung davon |
| WO2007145612A1 (en) | 2005-06-06 | 2007-12-21 | 454 Life Sciences Corporation | Paired end sequencing |
| US10081839B2 (en) | 2005-07-29 | 2018-09-25 | Natera, Inc | System and method for cleaning noisy genetic data and determining chromosome copy number |
| US9424392B2 (en) | 2005-11-26 | 2016-08-23 | Natera, Inc. | System and method for cleaning noisy genetic data from target individuals using genetic data from genetically related individuals |
| US7329860B2 (en) | 2005-11-23 | 2008-02-12 | Illumina, Inc. | Confocal imaging methods and apparatus |
| US8828661B2 (en) | 2006-04-24 | 2014-09-09 | Fluidigm Corporation | Methods for detection and quantification of nucleic acid or protein targets in a sample |
| WO2007147076A2 (en) * | 2006-06-14 | 2007-12-21 | Living Microsystems, Inc. | Methods for the diagnosis of fetal abnormalities |
| EP4108780A1 (en) * | 2006-06-14 | 2022-12-28 | Verinata Health, Inc. | Rare cell analysis using sample splitting and dna tags |
| US7754429B2 (en) | 2006-10-06 | 2010-07-13 | Illumina Cambridge Limited | Method for pair-wise sequencing a plurity of target polynucleotides |
| CN101652780B (zh) | 2007-01-26 | 2012-10-03 | 伊鲁米那股份有限公司 | 核酸测序系统以及方法 |
| US20080269068A1 (en) | 2007-02-06 | 2008-10-30 | President And Fellows Of Harvard College | Multiplex decoding of sequence tags in barcodes |
| CA2760439A1 (en) * | 2009-04-30 | 2010-11-04 | Good Start Genetics, Inc. | Methods and compositions for evaluating genetic markers |
| EP2473638B1 (en) | 2009-09-30 | 2017-08-09 | Natera, Inc. | Methods for non-invasive prenatal ploidy calling |
| EP2504448B1 (en) * | 2009-11-25 | 2016-10-19 | Bio-Rad Laboratories, Inc. | Methods and compositions for detecting genetic material |
| CA2767028A1 (en) * | 2009-11-25 | 2011-06-03 | Quantalife, Inc. | Methods and compositions for detecting genetic material |
| WO2011085491A1 (en) * | 2010-01-15 | 2011-07-21 | The University Of British Columbia | Multiplex amplification for the detection of nucleic acid variations |
| US8759036B2 (en) * | 2011-03-21 | 2014-06-24 | Affymetrix, Inc. | Methods for synthesizing pools of probes |
| US10227635B2 (en) * | 2012-04-16 | 2019-03-12 | Molecular Loop Biosolutions, Llc | Capture reactions |
| US10497461B2 (en) * | 2012-06-22 | 2019-12-03 | Sequenom, Inc. | Methods and processes for non-invasive assessment of genetic variations |
| KR102393608B1 (ko) | 2012-09-04 | 2022-05-03 | 가던트 헬쓰, 인크. | 희귀 돌연변이 및 카피수 변이를 검출하기 위한 시스템 및 방법 |
| CN105074007A (zh) * | 2013-03-12 | 2015-11-18 | 考希尔股份有限公司 | 用于产前遗传分析的系统和方法 |
| MX2015012733A (es) * | 2013-03-15 | 2016-06-21 | Immucor Gti Diagnostics Inc | Metodos y composiciones para evaluar el estado renal usando adn libre de celulas de la orina. |
| US20150141257A1 (en) | 2013-08-02 | 2015-05-21 | Roche Nimblegen, Inc. | Sequence capture method using specialized capture probes (heatseq) |
| WO2017020024A2 (en) | 2015-07-29 | 2017-02-02 | Progenity, Inc. | Systems and methods for genetic analysis |
| ES2745556T3 (es) | 2015-07-29 | 2020-03-02 | Progenity Inc | Acidos nucleicos y métodos para detectar anomalías cromosómicas |
-
2016
- 2016-07-29 ES ES16748036T patent/ES2745556T3/es active Active
- 2016-07-29 CA CA2993347A patent/CA2993347A1/en not_active Abandoned
- 2016-07-29 WO PCT/US2016/044914 patent/WO2017020023A2/en unknown
- 2016-07-29 EP EP19185115.3A patent/EP3608420B1/en active Active
- 2016-07-29 US US15/224,463 patent/US10465245B2/en active Active
- 2016-07-29 JP JP2018503647A patent/JP6830094B2/ja active Active
- 2016-07-29 CN CN201680054740.0A patent/CN108350500A/zh active Pending
- 2016-07-29 EP EP16748036.7A patent/EP3329010B1/en not_active Not-in-force
-
2018
- 2018-12-06 HK HK18115613.5A patent/HK1256543A1/zh unknown
-
2019
- 2019-10-08 US US16/596,118 patent/US20200032344A1/en not_active Abandoned
-
2020
- 2020-07-30 US US16/943,870 patent/US10947595B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3329010A2 (en) | 2018-06-06 |
| EP3329010B1 (en) | 2019-07-10 |
| EP3608420A1 (en) | 2020-02-12 |
| ES2745556T3 (es) | 2020-03-02 |
| US20170183731A1 (en) | 2017-06-29 |
| CA2993347A1 (en) | 2017-02-02 |
| WO2017020023A2 (en) | 2017-02-02 |
| US10947595B2 (en) | 2021-03-16 |
| CN108350500A (zh) | 2018-07-31 |
| US20200032344A1 (en) | 2020-01-30 |
| JP2018524993A (ja) | 2018-09-06 |
| EP3608420B1 (en) | 2021-05-19 |
| US10465245B2 (en) | 2019-11-05 |
| US20200354792A1 (en) | 2020-11-12 |
| WO2017020023A3 (en) | 2017-03-09 |
| HK1256543A1 (zh) | 2019-09-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6830094B2 (ja) | 染色体異常を検出するための核酸及び方法 | |
| US20220127683A1 (en) | Detecting mutations for cancer screening | |
| TWI661049B (zh) | 使用不含細胞之dna片段大小以測定複製數變異之方法 | |
| JP6328934B2 (ja) | 非侵襲性出生前親子鑑定法 | |
| EP3117011B1 (en) | Methods and processes for non-invasive assessment of genetic variations | |
| JP6161607B2 (ja) | サンプルにおける異なる異数性の有無を決定する方法 | |
| EP3377647B1 (en) | Nucleic acids and methods for detecting methylation status | |
| US20190309352A1 (en) | Multimodal assay for detecting nucleic acid aberrations | |
| US20210130900A1 (en) | Multiplexed parallel analysis of targeted genomic regions for non-invasive prenatal testing | |
| EP3827095A1 (en) | Cell-free dna damage analysis and its clinical applications | |
| Ishida et al. | Molecular genetics testing | |
| AU2018298437A1 (en) | Target-enriched multiplexed parallel analysis for assessment of fetal DNA samples | |
| US20220145368A1 (en) | Methods for noninvasive prenatal testing of fetal abnormalities |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190729 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190729 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200520 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200602 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200831 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210106 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210125 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6830094 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D02 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D04 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |