JP6469767B2 - Use of PEDF-derived polypeptides for preventing and / or improving skin aging - Google Patents
Use of PEDF-derived polypeptides for preventing and / or improving skin aging Download PDFInfo
- Publication number
- JP6469767B2 JP6469767B2 JP2017131741A JP2017131741A JP6469767B2 JP 6469767 B2 JP6469767 B2 JP 6469767B2 JP 2017131741 A JP2017131741 A JP 2017131741A JP 2017131741 A JP2017131741 A JP 2017131741A JP 6469767 B2 JP6469767 B2 JP 6469767B2
- Authority
- JP
- Japan
- Prior art keywords
- mer
- pharmaceutical composition
- skin
- amino acid
- uvb
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims description 112
- 230000009759 skin aging Effects 0.000 title claims description 45
- 108090000102 pigment epithelium-derived factor Proteins 0.000 title description 63
- 102000004196 processed proteins & peptides Human genes 0.000 title description 26
- 102100035846 Pigment epithelium-derived factor Human genes 0.000 title description 23
- 229920001184 polypeptide Polymers 0.000 title description 6
- 239000008194 pharmaceutical composition Substances 0.000 claims description 65
- 210000003491 skin Anatomy 0.000 claims description 58
- 210000004207 dermis Anatomy 0.000 claims description 27
- 230000037317 transdermal delivery Effects 0.000 claims description 25
- 125000000539 amino acid group Chemical group 0.000 claims description 22
- 239000002674 ointment Substances 0.000 claims description 21
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 12
- 206010051246 Photodermatosis Diseases 0.000 claims description 10
- 230000008845 photoaging Effects 0.000 claims description 9
- 239000007788 liquid Substances 0.000 claims description 7
- 239000003961 penetration enhancing agent Substances 0.000 claims description 7
- 239000006071 cream Substances 0.000 claims description 6
- 239000000443 aerosol Substances 0.000 claims description 5
- 239000006260 foam Substances 0.000 claims description 5
- 239000006210 lotion Substances 0.000 claims description 5
- 239000007921 spray Substances 0.000 claims description 5
- 125000003275 alpha amino acid group Chemical group 0.000 claims 4
- 102000008186 Collagen Human genes 0.000 description 41
- 108010035532 Collagen Proteins 0.000 description 41
- 229920001436 collagen Polymers 0.000 description 41
- 210000002950 fibroblast Anatomy 0.000 description 38
- 239000003981 vehicle Substances 0.000 description 38
- 150000001413 amino acids Chemical group 0.000 description 36
- 210000004027 cell Anatomy 0.000 description 29
- 238000000034 method Methods 0.000 description 28
- 230000002500 effect on skin Effects 0.000 description 27
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 20
- 238000011282 treatment Methods 0.000 description 20
- 241001465754 Metazoa Species 0.000 description 18
- 241000699670 Mus sp. Species 0.000 description 18
- 108010016113 Matrix Metalloproteinase 1 Proteins 0.000 description 15
- 230000035755 proliferation Effects 0.000 description 15
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 14
- 102000000380 Matrix Metalloproteinase 1 Human genes 0.000 description 14
- 230000015572 biosynthetic process Effects 0.000 description 14
- 210000001519 tissue Anatomy 0.000 description 14
- 102000013127 Vimentin Human genes 0.000 description 12
- 108010065472 Vimentin Proteins 0.000 description 12
- 238000012360 testing method Methods 0.000 description 12
- 210000005048 vimentin Anatomy 0.000 description 12
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 11
- 238000002474 experimental method Methods 0.000 description 11
- 230000037303 wrinkles Effects 0.000 description 11
- 241000699666 Mus <mouse, genus> Species 0.000 description 10
- 108090000623 proteins and genes Proteins 0.000 description 10
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 9
- 230000032683 aging Effects 0.000 description 9
- 235000018102 proteins Nutrition 0.000 description 9
- 102000004169 proteins and genes Human genes 0.000 description 9
- 238000003786 synthesis reaction Methods 0.000 description 9
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 8
- 102000012422 Collagen Type I Human genes 0.000 description 8
- 108010022452 Collagen Type I Proteins 0.000 description 8
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 8
- 230000000694 effects Effects 0.000 description 8
- 239000000203 mixture Substances 0.000 description 8
- 239000002953 phosphate buffered saline Substances 0.000 description 8
- 241000124008 Mammalia Species 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 239000012091 fetal bovine serum Substances 0.000 description 6
- 238000003119 immunoblot Methods 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 235000001014 amino acid Nutrition 0.000 description 5
- 229940024606 amino acid Drugs 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 239000003814 drug Substances 0.000 description 5
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 230000001965 increasing effect Effects 0.000 description 5
- 239000004615 ingredient Substances 0.000 description 5
- DHRLEVQXOMLTIM-UHFFFAOYSA-N phosphoric acid;trioxomolybdenum Chemical compound O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.O=[Mo](=O)=O.OP(O)(O)=O DHRLEVQXOMLTIM-UHFFFAOYSA-N 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 230000002062 proliferating effect Effects 0.000 description 5
- 238000009281 ultraviolet germicidal irradiation Methods 0.000 description 5
- 102000001187 Collagen Type III Human genes 0.000 description 4
- 108010069502 Collagen Type III Proteins 0.000 description 4
- 102000029816 Collagenase Human genes 0.000 description 4
- 108060005980 Collagenase Proteins 0.000 description 4
- 108050005238 Collagenase 3 Proteins 0.000 description 4
- 102100027995 Collagenase 3 Human genes 0.000 description 4
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 229960002424 collagenase Drugs 0.000 description 4
- 230000006378 damage Effects 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 239000000975 dye Substances 0.000 description 4
- 239000003623 enhancer Substances 0.000 description 4
- 210000002615 epidermis Anatomy 0.000 description 4
- 235000019441 ethanol Nutrition 0.000 description 4
- 239000000499 gel Substances 0.000 description 4
- 238000002372 labelling Methods 0.000 description 4
- YBYRMVIVWMBXKQ-UHFFFAOYSA-N phenylmethanesulfonyl fluoride Chemical compound FS(=O)(=O)CC1=CC=CC=C1 YBYRMVIVWMBXKQ-UHFFFAOYSA-N 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 239000011550 stock solution Substances 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 3
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 102000004142 Trypsin Human genes 0.000 description 3
- 108090000631 Trypsin Proteins 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 230000003833 cell viability Effects 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 238000010790 dilution Methods 0.000 description 3
- 239000012895 dilution Substances 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 210000002744 extracellular matrix Anatomy 0.000 description 3
- 239000000835 fiber Substances 0.000 description 3
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 3
- 239000001963 growth medium Substances 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 230000035515 penetration Effects 0.000 description 3
- INAAIJLSXJJHOZ-UHFFFAOYSA-N pibenzimol Chemical compound C1CN(C)CCN1C1=CC=C(N=C(N2)C=3C=C4NC(=NC4=CC=3)C=3C=CC(O)=CC=3)C2=C1 INAAIJLSXJJHOZ-UHFFFAOYSA-N 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 239000003381 stabilizer Substances 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 210000000434 stratum corneum Anatomy 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 239000012588 trypsin Substances 0.000 description 3
- BQCIDUSAKPWEOX-UHFFFAOYSA-N 1,1-Difluoroethene Chemical compound FC(F)=C BQCIDUSAKPWEOX-UHFFFAOYSA-N 0.000 description 2
- AXTGDCSMTYGJND-UHFFFAOYSA-N 1-dodecylazepan-2-one Chemical compound CCCCCCCCCCCCN1CCCCCC1=O AXTGDCSMTYGJND-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 229930182816 L-glutamine Natural products 0.000 description 2
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 229930040373 Paraformaldehyde Natural products 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 230000003321 amplification Effects 0.000 description 2
- 230000001772 anti-angiogenic effect Effects 0.000 description 2
- 230000000692 anti-sense effect Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 230000003366 colagenolytic effect Effects 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- GHVNFZFCNZKVNT-UHFFFAOYSA-N decanoic acid Chemical compound CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 108010007093 dispase Proteins 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 2
- 238000002073 fluorescence micrograph Methods 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 238000013467 fragmentation Methods 0.000 description 2
- 238000006062 fragmentation reaction Methods 0.000 description 2
- 125000001165 hydrophobic group Chemical group 0.000 description 2
- 238000010166 immunofluorescence Methods 0.000 description 2
- 230000001976 improved effect Effects 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 229940059904 light mineral oil Drugs 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 239000012139 lysis buffer Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000000508 neurotrophic effect Effects 0.000 description 2
- 238000003199 nucleic acid amplification method Methods 0.000 description 2
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 2
- 229920002866 paraformaldehyde Polymers 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 230000008263 repair mechanism Effects 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- 230000003827 upregulation Effects 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- NOOLISFMXDJSKH-KXUCPTDWSA-N (-)-Menthol Chemical compound CC(C)[C@@H]1CC[C@@H](C)C[C@H]1O NOOLISFMXDJSKH-KXUCPTDWSA-N 0.000 description 1
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 1
- PRDFBSVERLRRMY-UHFFFAOYSA-N 2'-(4-ethoxyphenyl)-5-(4-methylpiperazin-1-yl)-2,5'-bibenzimidazole Chemical compound C1=CC(OCC)=CC=C1C1=NC2=CC=C(C=3NC4=CC(=CC=C4N=3)N3CCN(C)CC3)C=C2N1 PRDFBSVERLRRMY-UHFFFAOYSA-N 0.000 description 1
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- IZXIZTKNFFYFOF-UHFFFAOYSA-N 2-Oxazolidone Chemical class O=C1NCCO1 IZXIZTKNFFYFOF-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- TWJNQYPJQDRXPH-UHFFFAOYSA-N 2-cyanobenzohydrazide Chemical compound NNC(=O)C1=CC=CC=C1C#N TWJNQYPJQDRXPH-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- IUWVYVOQTFVXKL-UHFFFAOYSA-N 4-decyl-1,3-oxazolidin-2-one Chemical compound CCCCCCCCCCC1COC(=O)N1 IUWVYVOQTFVXKL-UHFFFAOYSA-N 0.000 description 1
- RSWGJHLUYNHPMX-UHFFFAOYSA-N Abietic-Saeure Natural products C12CCC(C(C)C)=CC2=CCC2C1(C)CCCC2(C)C(O)=O RSWGJHLUYNHPMX-UHFFFAOYSA-N 0.000 description 1
- 241000486679 Antitype Species 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 238000009010 Bradford assay Methods 0.000 description 1
- 238000012756 BrdU staining Methods 0.000 description 1
- 239000005632 Capric acid (CAS 334-48-5) Substances 0.000 description 1
- 102000000503 Collagen Type II Human genes 0.000 description 1
- 108010041390 Collagen Type II Proteins 0.000 description 1
- 102100040995 Collagen alpha-1(XXI) chain Human genes 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- 102000007260 Deoxyribonuclease I Human genes 0.000 description 1
- 108010008532 Deoxyribonuclease I Proteins 0.000 description 1
- 241000283074 Equus asinus Species 0.000 description 1
- 206010015150 Erythema Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 102000013382 Gelatinases Human genes 0.000 description 1
- 108010026132 Gelatinases Proteins 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 101100114371 Homo sapiens COL21A1 gene Proteins 0.000 description 1
- 101000878605 Homo sapiens Low affinity immunoglobulin epsilon Fc receptor Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 102100034343 Integrase Human genes 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 102100038007 Low affinity immunoglobulin epsilon Fc receptor Human genes 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 108060003100 Magainin Proteins 0.000 description 1
- 102000002274 Matrix Metalloproteinases Human genes 0.000 description 1
- 108010000684 Matrix Metalloproteinases Proteins 0.000 description 1
- 102000005741 Metalloproteases Human genes 0.000 description 1
- 108010006035 Metalloproteases Proteins 0.000 description 1
- 101000577888 Mus musculus Collagenase 3 Proteins 0.000 description 1
- 101000819572 Mus musculus Glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 1
- 235000021360 Myristic acid Nutrition 0.000 description 1
- TUNFSRHWOTWDNC-UHFFFAOYSA-N Myristic acid Natural products CCCCCCCCCCCCCC(O)=O TUNFSRHWOTWDNC-UHFFFAOYSA-N 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 108010050808 Procollagen Proteins 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 101000933967 Pseudomonas phage KPP25 Major capsid protein Proteins 0.000 description 1
- 238000002123 RNA extraction Methods 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- 238000010240 RT-PCR analysis Methods 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- KHPCPRHQVVSZAH-HUOMCSJISA-N Rosin Natural products O(C/C=C/c1ccccc1)[C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 KHPCPRHQVVSZAH-HUOMCSJISA-N 0.000 description 1
- 206010040829 Skin discolouration Diseases 0.000 description 1
- 206010040865 Skin hyperpigmentation Diseases 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 230000021736 acetylation Effects 0.000 description 1
- 238000006640 acetylation reaction Methods 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 1
- 230000009435 amidation Effects 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- 230000003367 anti-collagen effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 230000001153 anti-wrinkle effect Effects 0.000 description 1
- 239000002518 antifoaming agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 239000003908 antipruritic agent Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000008827 biological function Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 230000025084 cell cycle arrest Effects 0.000 description 1
- 230000032823 cell division Effects 0.000 description 1
- 230000012292 cell migration Effects 0.000 description 1
- 108091092328 cellular RNA Proteins 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 231100000321 erythema Toxicity 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 230000001815 facial effect Effects 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 239000008394 flocculating agent Substances 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 230000002431 foraging effect Effects 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000002695 general anesthesia Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- -1 glidants Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 210000004209 hair Anatomy 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- 230000003810 hyperpigmentation Effects 0.000 description 1
- 238000005286 illumination Methods 0.000 description 1
- 238000003125 immunofluorescent labeling Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 108091005601 modified peptides Proteins 0.000 description 1
- 125000000896 monocarboxylic acid group Chemical group 0.000 description 1
- 238000004264 monolayer culture Methods 0.000 description 1
- GOQYKNQRPGWPLP-UHFFFAOYSA-N n-heptadecyl alcohol Natural products CCCCCCCCCCCCCCCCCO GOQYKNQRPGWPLP-UHFFFAOYSA-N 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 230000037311 normal skin Effects 0.000 description 1
- 238000011580 nude mouse model Methods 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 239000003002 pH adjusting agent Substances 0.000 description 1
- 206010033675 panniculitis Diseases 0.000 description 1
- 230000037368 penetrate the skin Effects 0.000 description 1
- 108010043655 penetratin Proteins 0.000 description 1
- MCYTYTUNNNZWOK-LCLOTLQISA-N penetratin Chemical compound C([C@H](NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CCCNC(N)=N)[C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(N)=O)C1=CC=CC=C1 MCYTYTUNNNZWOK-LCLOTLQISA-N 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 229920000131 polyvinylidene Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 239000011535 reaction buffer Substances 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 238000012827 research and development Methods 0.000 description 1
- 230000025600 response to UV Effects 0.000 description 1
- 229930002330 retinoic acid Natural products 0.000 description 1
- 238000003757 reverse transcription PCR Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000012764 semi-quantitative analysis Methods 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 230000037370 skin discoloration Effects 0.000 description 1
- 210000001626 skin fibroblast Anatomy 0.000 description 1
- 231100000245 skin permeability Toxicity 0.000 description 1
- 230000036560 skin regeneration Effects 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 210000004304 subcutaneous tissue Anatomy 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- 150000003505 terpenes Chemical class 0.000 description 1
- 235000007586 terpenes Nutrition 0.000 description 1
- UWHCKJMYHZGTIT-UHFFFAOYSA-N tetraethylene glycol Chemical compound OCCOCCOCCOCCO UWHCKJMYHZGTIT-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- KHPCPRHQVVSZAH-UHFFFAOYSA-N trans-cinnamyl beta-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OCC=CC1=CC=CC=C1 KHPCPRHQVVSZAH-UHFFFAOYSA-N 0.000 description 1
- PBKWZFANFUTEPS-CWUSWOHSSA-N transportan Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(N)=O)[C@@H](C)CC)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)CN)[C@@H](C)O)C1=CC=C(O)C=C1 PBKWZFANFUTEPS-CWUSWOHSSA-N 0.000 description 1
- 108010062760 transportan Proteins 0.000 description 1
- 229960001727 tretinoin Drugs 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 239000013598 vector Substances 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 210000001835 viscera Anatomy 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 238000001262 western blot Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 239000003871 white petrolatum Substances 0.000 description 1
- 239000012130 whole-cell lysate Substances 0.000 description 1
- 230000037373 wrinkle formation Effects 0.000 description 1
Images
Description
(発明の背景)
(1.発明の分野)
(Background of the Invention)
(1. Field of Invention)
本発明の開示は、皮膚老化の予防及び/又は改善に関する。特に、開示された発明は、
皮膚老化を予防及び/又は改善するためのPEDF-由来のポリペプチドの使用に関する。
The present disclosure relates to the prevention and / or improvement of skin aging. In particular, the disclosed invention
It relates to the use of PEDF-derived polypeptides for preventing and / or improving skin aging.
(2.関連技術の説明) (2. Explanation of related technology)
ヒトの皮膚は、他の生存組織のように、時と共に老化する。皮膚老化は、皺及び小皺の
形成、皮膚の菲薄化、皮膚変色又は色素沈着過剰、並びに堅さ及び弾性の喪失につながる
。原因に応じて、皮膚老化は、内因性老化及び外因性老化に分類することができる。内因
性老化、又は実年齢老化は、ほぼ全ての内臓器官に影響を及ぼし、対象の遺伝子構造によ
り主として調節される。外因性老化は、様々な環境因子、主として紫外線(UV)照射への曝
露の結果であり、従ってこれは光老化と称されることが多い。顔面、首、及び手の甲など
の、太陽へ曝された領域において、内因性老化と光老化の損傷の組合せは、より顕著な変
化を生じることがある。
Human skin ages with time like other living tissues. Skin aging leads to the formation of wrinkles and wrinkles, thinning of the skin, skin discoloration or hyperpigmentation, and loss of firmness and elasticity. Depending on the cause, skin aging can be divided into intrinsic aging and extrinsic aging. Endogenous aging, or real age aging, affects almost all internal organs and is primarily regulated by the genetic structure of the subject. Exogenous aging is the result of exposure to various environmental factors, primarily ultraviolet (UV) radiation, and is therefore often referred to as photoaging. In areas exposed to the sun, such as the face, neck, and back of the hand, the combination of endogenous aging and photoaging damage can produce more significant changes.
コラーゲンは、結合組織の主成分を構成する、線維性の細胞外不溶性タンパク質である
。様々な型のコラーゲンの中で、I型及びIII型が、主に関連している。I型コラーゲンは
、皮膚の乾燥重量の90%より多くを成す、ヒト皮膚における主要な構造タンパク質である
のに対し、III型コラーゲンはまた、体全体に広範に分布し、胎児組織において支配的で
ある。皮膚が老化するにつれて、総コラーゲン含量及びI型コラーゲンのIII型コラーゲン
に対する比は、漸減し、且つ細胞外マトリックス(ECM)は、脱組織化され始める。例えば
、内因性老化及び紫外線B波(UVB)曝露の両方は、コラーゲン線維(特にI型コラーゲン)の
再生を衰えさせる。またUVB曝露は、マトリックスメタロプロテアーゼ(MMP)として知られ
ているいくつかのコラーゲン分解酵素の生成をアップレギュレートする。ヒトにおけるMM
P、具体的にはコラゲナーゼ及びゼラチナーゼは、UVB曝露の数時間以内に誘導される。そ
のような事象は全て、真皮の細胞外マトリックス組成の変更をおそらく生じるであろう。
Collagen is a fibrous extracellular insoluble protein that constitutes the main component of connective tissue. Among the various types of collagen, type I and type III are mainly related. Type I collagen is the major structural protein in human skin, making up more than 90% of the dry weight of the skin, whereas type III collagen is also widely distributed throughout the body and is dominant in fetal tissue is there. As the skin ages, the total collagen content and the ratio of type I collagen to type III collagen gradually decreases and the extracellular matrix (ECM) begins to be disorganized. For example, both endogenous aging and ultraviolet B wave (UVB) exposure attenuate the regeneration of collagen fibers (especially type I collagen). UVB exposure also upregulates the production of several collagenolytic enzymes known as matrix metalloproteases (MMPs). MM in humans
P, specifically collagenase and gelatinase, are induced within hours of UVB exposure. All such events will likely result in a change in the extracellular matrix composition of the dermis.
老化した皮膚に関して利用可能な多くの治療が存在する。例えば、老化過程におけるコ
ラーゲンの重要性は、多くのコラーゲン-含有局所性製品の開発に繋がっている。その他
の成分、例えばレチノイン酸、ビタミンC及びヒアルロン酸などは、コラーゲン合成を刺
激することができるという主張により、これらは化粧品において使用される。一部の化粧
的手法(例えば、レーザー皮膚蘇生(laser skin resurfacing))も、顔面の皺及び皮膚の凹
凸を減少するのに有効である。
There are many treatments available for aging skin. For example, the importance of collagen in the aging process has led to the development of many collagen-containing topical products. Other ingredients, such as retinoic acid, vitamin C and hyaluronic acid, are used in cosmetics by claiming that they can stimulate collagen synthesis. Some cosmetic techniques (eg, laser skin resurfacing) are also effective in reducing facial wrinkles and skin irregularities.
老化の徴候を減少するか、又は皮膚再生を刺激することが提唱されている解決法が多数
であるにもかかわらず、それらはいずれも、皮膚の内因性修復機構(すなわち、コラーゲ
ン合成)を喚起することは不可能である。前述の観点から、皮膚老化、特に皮膚の光老化
を効果的に治療する手段の必要性が、当該技術分野において依然存在している。
Despite the numerous solutions proposed to reduce signs of aging or stimulate skin regeneration, they all evoke an intrinsic repair mechanism of the skin (i.e., collagen synthesis) It is impossible to do. In view of the foregoing, there remains a need in the art for a means of effectively treating skin aging, particularly skin photoaging.
(概要)
以下は、読者に基本的理解を提供するために、本開示の簡単な概要を提供する。この概
要は、本開示の広範な全体像ではなく、本発明の鍵となる/重要な要素を確定せず、本発
明の範囲の線引きもしない。その唯一の目的は、後に提供する、より詳細な説明への前置
きとしての簡単な形で、本明細書に開示されるある種の概念を提供することである。
(Overview)
The following provides a brief overview of the present disclosure to provide a basic understanding to the reader. This summary is not an extensive overview of the disclosure and it does not identify key / critical elements of the invention or delineate the scope of the invention. Its sole purpose is to provide certain concepts disclosed herein in a simplified form as a prelude to the more detailed description that is presented later.
本開示は、色素上皮由来因子(PEDF)に由来する合成ペプチドが、コラーゲン合成を刺激
し、真皮線維芽細胞増殖を促進し、且つUVB-誘導したMMP-1発現をダウンレギュレーショ
ンし、その結果これらは対象における皮膚老化の予防及び/又は改善に有効であるという
発見に少なくとも基づいている。従って、本発明のPEDF由来の合成ペプチドは、皮膚老化
に対する薬剤又は医薬品として有用である。
The present disclosure shows that synthetic peptides derived from pigment epithelium-derived factor (PEDF) stimulate collagen synthesis, promote dermal fibroblast proliferation, and down-regulate UVB-induced MMP-1 expression, resulting in these Is based at least on the discovery that it is effective in preventing and / or improving skin aging in a subject. Therefore, the PEDF-derived synthetic peptide of the present invention is useful as a drug or pharmaceutical for skin aging.
従って、一態様では、本開示は、対象における皮膚老化を予防及び/又は改善するため
の合成ペプチドに関する。
Accordingly, in one aspect, the present disclosure relates to a synthetic peptide for preventing and / or ameliorating skin aging in a subject.
本開示の実施態様によれば、この合成ペプチドは、20〜39アミノ酸残基の長さであり、
且つ、配列番号:1と少なくとも80%同一であるアミノ酸配列を有する。また、該アミノ酸
配列は、配列番号:1の残基11〜30と少なくとも90%同一である少なくとも20個の連続的な
残基を含み、その結果、該合成ペプチドが、対象における皮膚老化を予防及び/又は改善
するのに有用となる。
According to an embodiment of the present disclosure, the synthetic peptide is 20-39 amino acid residues long,
And having an amino acid sequence that is at least 80% identical to SEQ ID NO: 1. The amino acid sequence also comprises at least 20 consecutive residues that are at least 90% identical to residues 11-30 of SEQ ID NO: 1, so that the synthetic peptide prevents skin aging in a subject And / or useful to improve.
本開示の任意の実施態様によれば、この合成ペプチドの少なくとも4個の連続的な残基
は、配列番号:1の残基11〜14と同一である。こうした合成ペプチドの非制限的な例として
は、それぞれ、配列番号:1(39-mer)、配列番号:2(34-mer)、配列番号:3(29-mer)、配列番
号:5(24-mer)、配列番号:6(20-mer)、配列番号:8(MO 29-mer)、及び配列番号:9(MO 20-me
r)のアミノ酸配列を有するものが挙げられる。本開示のいくつかの実施態様では、合成ペ
プチドのアミノ酸配列は、配列番号:3(29-mer)、配列番号:5(24-mer)、又は配列番号:6(2
0-mer)のいずれかである。
According to any embodiment of the present disclosure, at least 4 consecutive residues of the synthetic peptide are identical to residues 11-14 of SEQ ID NO: 1. Non-limiting examples of such synthetic peptides include SEQ ID NO: 1 (39-mer), SEQ ID NO: 2 (34-mer), SEQ ID NO: 3 (29-mer), SEQ ID NO: 5 (24 -mer), SEQ ID NO: 6 (20-mer), SEQ ID NO: 8 (MO 29-mer), and SEQ ID NO: 9 (MO 20-me)
Those having the amino acid sequence of r). In some embodiments of the disclosure, the amino acid sequence of the synthetic peptide is SEQ ID NO: 3 (29-mer), SEQ ID NO: 5 (24-mer), or SEQ ID NO: 6 (2
0-mer).
本開示の様々な実施態様により、皮膚老化は、UV照射により引き起こされる。 According to various embodiments of the present disclosure, skin aging is caused by UV irradiation.
本開示の様々な実施態様により、対象は、ヒトを含めた哺乳類に分類されるあらゆる動
物であり得る。
According to various embodiments of the present disclosure, the subject can be any animal classified as a mammal, including a human.
別の態様では、本開示は、対象における皮膚老化を予防及び/又は改善するための医薬
組成物に関する。対象は、ヒトを含めた哺乳類に分類されるあらゆる動物であり得る。
In another aspect, the present disclosure relates to a pharmaceutical composition for preventing and / or ameliorating skin aging in a subject. The subject can be any animal classified as a mammal, including a human.
本開示の一実施態様によれば、この医薬組成物は、前述の態様/実施態様のいずれかに
よる合成ペプチドを含み、且つ、該合成ペプチドは、対象における皮膚老化を治療するの
に十分な有効量で存在する。医薬組成物はまた、合成ペプチドのための医薬として許容し
得る賦形剤も含む。
According to one embodiment of the present disclosure, the pharmaceutical composition comprises a synthetic peptide according to any of the foregoing aspects / embodiments, and the synthetic peptide is effective enough to treat skin aging in a subject. Present in quantity. The pharmaceutical composition also includes a pharmaceutically acceptable excipient for the synthetic peptide.
特定の任意の実施態様において、医薬組成物は、本合成ペプチド又は医薬組成物の流れ
を促進する少なくとも1種(on)の浸透促進剤を更に含む。
In certain optional embodiments, the pharmaceutical composition further comprises at least one penetration enhancer that facilitates the flow of the synthetic peptide or pharmaceutical composition.
本開示の様々な実施態様において、医薬組成物は、液剤、噴霧剤、エアゾール剤、泡剤
、クリーム剤、ローション剤、軟膏、ゲル、又は貼付剤に製剤化されることができる。
In various embodiments of the present disclosure, the pharmaceutical composition can be formulated into solutions, sprays, aerosols, foams, creams, lotions, ointments, gels, or patches.
更に別の態様において、本発明は、対象における皮膚老化を予防及び/又は改善する方
法に関する。この対象は、ヒトを含めた哺乳類に分類されるあらゆる動物であり得る。
In yet another aspect, the present invention relates to a method for preventing and / or ameliorating skin aging in a subject. The subject can be any animal classified as a mammal, including a human.
一実施態様では、該方法は、合成ペプチドを対象の真皮へ経真皮送達するために、該対
象に、前述の態様/実施態様のいずれかによる合成ペプチドの有効量を投与することを含
む。
In one embodiment, the method comprises administering to the subject an effective amount of a synthetic peptide according to any of the foregoing aspects / embodiments for transdermal delivery of the synthetic peptide to the subject's dermis.
任意の実施態様によれば、この合成ペプチドは、本開示の前述の態様/実施態様による
医薬組成物に製剤化される。一例において、本医薬組成物は、対象の皮膚へ局所的に投与
されてよい。任意の実施態様において、本方法は、合成ペプチド又は医薬組成物の経真皮
送達を促進するために、医薬組成物の局所的投与の前、それと同時に、又はその後、対象
の皮膚へ外部刺激(例えば、機械的、電気的、熱的、超音波的、又は高周波的刺激)を適用
する工程を更に含む。更に任意に、医薬組成物は、本合成ペプチド又は医薬組成物の流れ
を促進するために、少なくとも1種の(on)浸透促進剤を更に含むことができる。
According to any embodiment, the synthetic peptide is formulated into a pharmaceutical composition according to the previous aspect / embodiment of the present disclosure. In one example, the pharmaceutical composition may be administered topically to the subject's skin. In any embodiment, the method comprises external stimulation (e.g., to the subject's skin) prior to, concurrently with, or after topical administration of the pharmaceutical composition to facilitate transdermal delivery of the synthetic peptide or pharmaceutical composition. Mechanical, electrical, thermal, ultrasonic, or high frequency stimulation). Further optionally, the pharmaceutical composition can further comprise at least one on-permeation enhancer to facilitate the flow of the synthetic peptide or pharmaceutical composition.
本開示の特定の実施態様により、皮膚老化は、UV照射により引き起こされる。 According to certain embodiments of the present disclosure, skin aging is caused by UV irradiation.
本開示の付随的な特徴及び利点の多くは、添付の図面と関連付けて考慮される以下の詳
細な説明を参照して、いっそう良く理解されるようになるであろう。
Many of the attendant features and advantages of the present disclosure will become better understood with reference to the following detailed description considered in conjunction with the accompanying drawings.
(図面の簡単な説明)
本特許及び出願のファイルは、カラーで製作された少なくとも1つの図面を含む。カラ
ーの図面を伴うこの特許又は特許出願公開の複写は、請求及び必要な料金の支払い後に、
事務局によって提供されることとなる。
(Brief description of the drawings)
The file of this patent and application contains at least one drawing made in color. Copies of this patent or patent application publication with color drawings will be accepted after request and payment of the necessary fee:
It will be provided by the secretariat.
本発明の説明は、添付の図面に照らして読む以下の詳細な説明から、いっそう良く理解
されるであろう:
The description of the present invention will be better understood from the following detailed description read in light of the accompanying drawings:
(説明)
添付の図面に関連して以下に提供する詳細な説明は、本発明の実施例の説明を目的とし
、本発明の実施例が構成又は利用され得る唯一の形態を表すことを意図しない。この説明
は、実施例の機能、及び実施例を構成及び操作するための工程の順序を述べる。しかし、
異なる例によって、同一又は同等の機能及び順序を実現することもできる。
(Description)
The detailed description provided below in connection with the accompanying drawings is intended as a description of embodiments of the invention and is not intended to represent the only forms in which embodiments of the invention may be constructed or utilized. This description describes the function of the example and the sequence of steps for configuring and operating the example. But,
Different examples may implement the same or equivalent functions and sequences.
便宜上、(明細書、実施例、及び添付の特許請求の範囲を含めて)出願全体において用い
られるある種の用語を、ここにまとめる。本明細書で別段に定義されない限り、本開示で
用いられる科学技術用語は、当分野の技術者によって普通に理解及び使用される意味を有
するものとする。文脈によって他に必要とされない限り、単数形の用語には、複数形の同
一のものが含まれるものとし、複数形の用語には、単数形が含まれるものとすることを理
解されたい。具体的には、本明細書及び特許請求の範囲では、文脈によってそうではない
と明らかに示されない限り、単数形「a」及び「an」には、複数の指示物が含まれる。
For convenience, certain terms used throughout the application (including the description, examples, and appended claims) are collected here. Unless otherwise defined herein, scientific and technical terms used in this disclosure shall have the meanings that are commonly understood and used by those skilled in the art. Unless otherwise required by context, singular terms shall include the same plural form and plural terms shall include the singular form. Specifically, in the present specification and claims, the singular forms “a” and “an” include plural referents unless the context clearly indicates otherwise.
本発明の広い範囲を説明する数値範囲及びパラメータは、おおよその値であるものの、
具体例において説明する数値は、可能な限り正確に報告する。しかし、いかなる数値も、
それぞれの試験測定において判明する標準偏差から必然的に生じるある種の誤差を本質的
に含んでいる。また、本明細書で使用する場合、用語「約」は一般に、所与の値又は範囲
の10%、5%、1%、又は0.5%以内を意味する。或いは、用語「約」は、当分野の技術者
によって判断される場合には、平均の許容し得る標準誤差以内を意味する。具体例/試験
実施例以外では、又は他に指定がない限り、本明細書に開示される、材料の量、時間、温
度、操作条件、量の割合、及びこれらと同類のものに対するものなどの、数値範囲、量、
値、及び割合は全て、全ての場合において、用語「約」によって修飾されるものと理解さ
れるべきである。従って、そうではないと示されない限り、本開示及び添付の特許請求の
範囲に示される数値パラメータは、所望される場合に変動し得るおおよその値である。最
低限でも、各数値パラメータは、少なくとも、報告される有効数字の数を考慮して、且つ
、通常の丸め技術を適用することによって解釈されるべきである。
The numerical ranges and parameters describing the broad scope of the invention are approximate values,
The numerical values described in the examples are reported as accurately as possible. But any number
It inherently contains certain errors that necessarily arise from the standard deviation found in each test measurement. Also, as used herein, the term “about” generally means within 10%, 5%, 1%, or 0.5% of a given value or range. Alternatively, the term “about” means within an acceptable standard error of the mean, as judged by those skilled in the art. Except for specific examples / test examples, or unless otherwise specified, such as those disclosed herein for material amounts, times, temperatures, operating conditions, proportions of amounts, and the like. , Numerical range, quantity,
All values and percentages are to be understood as being modified in all cases by the term “about”. Accordingly, unless indicated to the contrary, the numerical parameters set forth in the present disclosure and appended claims are approximate values that may vary if desired. At a minimum, each numeric parameter should be interpreted at least by considering the number of significant digits reported and applying normal rounding techniques.
本明細書で使用する場合、用語「ペプチド」は、アミノ酸残基のポリマーを指す。用語
「合成ペプチド」は、本明細書で使用する場合、天然に存在する全長タンパク質分子を含
まないペプチドを意味する。ペプチドは、化学合成、組換え遺伝子技術、又は全長タンパ
ク質の断片化などの技術を使用する、人の介入によって製造することができる点で、「合
成」である。本開示全体を通して、あるペプチド内の任意の特定のアミノ酸残基の位置は
、ペプチドのN末端を始点に番号付けされる。
As used herein, the term “peptide” refers to a polymer of amino acid residues. The term “synthetic peptide” as used herein means a peptide that does not contain a naturally occurring full-length protein molecule. Peptides are “synthetic” in that they can be produced by human intervention using techniques such as chemical synthesis, recombinant gene technology, or full-length protein fragmentation. Throughout this disclosure, the position of any particular amino acid residue within a peptide is numbered starting from the N-terminus of the peptide.
本明細書で使用する場合、「増殖すること」及び「増殖」とは、細胞分裂による、集団
中の細胞数の増加をいう。
As used herein, “proliferating” and “proliferation” refer to an increase in the number of cells in a population due to cell division.
本明細書で特定される合成ポリペプチド配列に関する「アミノ酸配列同一性の割合(%)
」は、配列を整列させ、且つ、最大の割合の配列同一性を得るために必要であればギャッ
プを導入した後の、配列同一性の一部としてのいかなる保存的置換も考慮しない、特定の
ポリペプチド配列内のアミノ酸残基と同一である候補配列内のアミノ酸残基の割合と定義
される。配列同一性の割合を決定する目的のアラインメントは、当分野の技術の範囲内の
様々な方式で、例えば、BLAST、BLAST-2、ALIGN、又はMegalign(DNASTAR)ソフトウェアな
どの公的に利用可能なコンピュータソフトウェアを使用して、実現することができる。当
分野の技術者は、比較される配列の完全長にわたる最大アラインメントを実現するために
必要とされるあらゆるアルゴリズムを含めた、アラインメントを測定するための適切なパ
ラメータを決定することができる。本明細書の目的では、2つのアミノ酸配列間の配列比
較は、米国立生物工学情報センター(NCBI)によってオンラインで提供されているコンピュ
ータプログラムBlastp(タンパク質-タンパク質BLAST)によって実施した。所与のアミノ酸
配列Bに対する所与のアミノ酸配列Aのアミノ酸配列同一性の割合(或いは、これは、所与
のアミノ酸配列Bに対するアミノ酸配列同一性が、いくらかの%である、所与のアミノ酸
配列Aと表現することができる)は、以下の通りの式によって算出する:
プログラムによって同一のマッチとしてスコア化されるアミノ酸残基の数であり、Yは、A
又はB内のいずれか短い方のアミノ酸残基の総数である。
“Percentage of amino acid sequence identity (%) with respect to the synthetic polypeptide sequences identified herein.
Is a specific alignment that does not consider any conservative substitutions as part of sequence identity after aligning the sequences and introducing gaps if necessary to obtain the greatest percentage of sequence identity. Defined as the percentage of amino acid residues in a candidate sequence that are identical to amino acid residues in a polypeptide sequence. Alignments for the purpose of determining percent sequence identity are available in various ways within the skill of the art and are publicly available, for example, BLAST, BLAST-2, ALIGN, or Megalign (DNASTAR) software Can be implemented using computer software. One skilled in the art can determine appropriate parameters for measuring alignment, including any algorithms needed to achieve maximal alignment over the full length of the sequences being compared. For purposes herein, sequence comparison between two amino acid sequences was performed by the computer program Blastp (protein-protein BLAST) provided online by the National Center for Biotechnology Information (NCBI). The percentage of amino acid sequence identity of a given amino acid sequence A to a given amino acid sequence B (or a given amino acid sequence in which the amino acid sequence identity to a given amino acid sequence B is some percent (Which can be expressed as A) is calculated by the following formula:
Or the total number of amino acid residues in B, whichever is shorter.
用語「治療すること」とは、本明細書で使用する場合、皮膚老化に関連した1種以上の
徴候又は特徴を部分的又は完全に、緩和する、改善させる、軽減する、発症を遅らせる、
進行を妨げる、重篤度を軽減する、及び/又は発生率を低下させる目的での、皮膚老化の
徴候を有するか又は皮膚老化の素因を有する対象への、本開示の合成ペプチド又は医薬組
成物の適用又は投与をいう。治療は、一般に、この用語が本明細書で定義される通り、1
以上の症状又は臨床マーカーが低下した場合に「有効」である。
The term `` treating '' as used herein partially or completely alleviates, ameliorates, reduces, delays the onset of one or more signs or features associated with skin aging,
Synthetic peptides or pharmaceutical compositions of the present disclosure to subjects with signs of skin aging or predisposition to skin aging for the purpose of preventing progression, reducing severity and / or reducing incidence Application or administration. Treatment generally includes 1 as the term is defined herein.
“Effective” when the above symptoms or clinical markers are reduced.
用語「有効量」とは、本明細書で使用する場合、所望の反応をもたらすのに十分な成分
の量をいう。具体的な有効量は、治療される特定の状態、患者の身体的状態(例えば、患
者の体重、年齢、又は性別)、治療される哺乳類又は動物の種類、治療の期間、(もしあれ
ば)併用療法の特性、及び用いられる具体的な製剤などの要因によって変動することとな
る。有効量はまた、化合物又は組成物の治療的に有益な効果が、いかなる有毒又は有害な
作用も上回る量でもある。
The term “effective amount” as used herein refers to the amount of an ingredient sufficient to effect the desired reaction. The specific effective amount is the particular condition being treated, the physical condition of the patient (e.g., the patient's weight, age, or gender), the type of mammal or animal being treated, the duration of the treatment, if any It will vary depending on factors such as the characteristics of the combination therapy and the specific formulation used. An effective amount is also an amount by which the therapeutically beneficial effect of the compound or composition exceeds any toxic or deleterious effects.
用語「塗布」又は「投与」は、本明細書において互換的に使用され、皮膚老化を予防及
び/又は改善するために、本発明の合成ペプチド又は医薬組成物を対象へ提供する手段を
指す。本開示の様々な実施態様により、経真皮送達は、好ましい送達経路である。例えば
、本発明の合成ペプチド又は医薬組成物は、対象の皮膚へ、局所的に塗布され、その結果
合成ペプチド又は本医薬組成物は、皮膚老化を予防及び/又は改善するために、標的部位(
例えば真皮)へ到達する。
The terms “application” or “administration” are used interchangeably herein and refer to a means of providing a subject with a synthetic peptide or pharmaceutical composition of the present invention to prevent and / or ameliorate skin aging. According to various embodiments of the present disclosure, transdermal delivery is a preferred delivery route. For example, the synthetic peptide or pharmaceutical composition of the present invention is topically applied to the subject's skin, so that the synthetic peptide or pharmaceutical composition can be used to prevent and / or ameliorate skin aging.
For example, the dermis is reached.
用語「賦形剤」は、本明細書で使用する場合、本開示の合成PEDFペプチドのためのビヒ
クル/担体を形成する任意の不活性物質(粉末又は液体など)を意味する。賦形剤は一般に
、安全で、無毒であり、且つまた広い意味で、充填剤、希釈剤、凝集剤、結合剤、滑沢剤
、流動促進剤、安定剤、着色剤、湿潤剤、崩壊剤など、医薬組成物の調製に有用な製薬産
業において任意の公知の物質を含むことができる。
The term “excipient” as used herein means any inert material (such as a powder or liquid) that forms a vehicle / carrier for the synthetic PEDF peptides of the present disclosure. Excipients are generally safe, non-toxic and, in a broad sense, fillers, diluents, flocculants, binders, lubricants, glidants, stabilizers, colorants, wetting agents, disintegrants. Any known substance in the pharmaceutical industry useful for preparing pharmaceutical compositions can be included.
本明細書で使用する場合、「医薬として許容し得る」成分は、妥当なベネフィット/リ
スク比と釣り合いのとれた過度の有害な副作用(毒性、刺激、及びアレルギー反応など)を
伴わないヒト及び/又は動物での使用に適している成分である。また、各賦形剤は、医薬
製剤の他の成分と適合性があるという意味で、「許容し得る」ものでなければならない。
担体は、固体の、半固体の、又は液体の希釈剤、クリーム、又はカプセルの形態であり得
る。
As used herein, a “pharmaceutically acceptable” ingredient is a human and / or without excessive adverse side effects (such as toxicity, irritation, and allergic reactions) that are balanced with a reasonable benefit / risk ratio. Or an ingredient suitable for use in animals. Each excipient must also be “acceptable” in the sense of being compatible with the other ingredients of the pharmaceutical formulation.
The carrier can be in the form of a solid, semi-solid, or liquid diluent, cream, or capsule.
用語「対象」とは、本発明の合成ペプチド、組成物、及び/又は方法で治療可能である
、ヒト種を含めた哺乳類をいう。用語「対象」は、一方の性別が具体的に示されない限り
、男性と女性の両方を指すものとする。
The term “subject” refers to a mammal, including a human species, that is treatable with the synthetic peptides, compositions, and / or methods of the present invention. The term “subject” is intended to refer to both men and women unless one gender is specifically indicated.
本明細書で使用する場合、用語「経真皮」は、表皮を通る真皮への活性物質(例えば、
本合成ペプチド又は医薬組成物)の経路を意味する。
As used herein, the term `` transdermal '' refers to an active substance (e.g.
This synthetic peptide or pharmaceutical composition).
色素上皮由来因子(PEDF)は、抗血管新生機能、抗腫瘍形成機能、及び神経栄養機能を有
する、多機能の分泌タンパク質である。ヒトPEDFタンパク質(配列番号:11)は、サイズが
およそ50kDa、長さが418アミノ酸の分泌タンパク質である。PEDFの34-mer断片(残基44〜7
7)及び44-mer断片(残基78〜121:配列番号:10)は、それぞれ、抗血管新生特性及び神経栄
養特性を有することが確定されている。
Pigment epithelium-derived factor (PEDF) is a multifunctional secreted protein having an anti-angiogenic function, an anti-tumor forming function, and a neurotrophic function. Human PEDF protein (SEQ ID NO: 11) is a secreted protein having a size of approximately 50 kDa and a length of 418 amino acids. 34-mer fragment of PEDF (residues 44-7
The 7) and 44-mer fragments (residues 78-121: SEQ ID NO: 10) have been determined to have anti-angiogenic and neurotrophic properties, respectively.
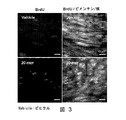
本開示は、44-mer PEDFに由来する合成ペプチドが、様々な機序を介し皮膚老化の損傷
から皮膚を保護することができるという発見に、少なくとも基づいている。本開示の実施
例は、合成ペプチドは、真皮中のコラーゲンレベルを増大し、真皮線維芽細胞の増殖を誘
導し、且つMMP-1(UVB-誘導性コラゲナーゼ)の発現を減少し得ることを明らかにしている
。本発明の別の独創的特徴は、この合成ペプチドが、完全長PEDFよりもかなり短い(最大
でも39アミノ酸残基)ので、高い製造コスト、低い生物学的利用能、及び不十分な薬物動
態を含めた従来のタンパク質薬物の臨床使用に伴う制限を克服することにある。従って、
本合成ペプチドは、皮膚老化を予防及び/又は改善するために有用である。
The present disclosure is based at least on the discovery that synthetic peptides derived from 44-mer PEDF can protect the skin from damage of skin aging through various mechanisms. Examples of this disclosure demonstrate that synthetic peptides can increase collagen levels in the dermis, induce proliferation of dermal fibroblasts, and reduce the expression of MMP-1 (UVB-induced collagenase) I have to. Another inventive feature of the present invention is that this synthetic peptide is much shorter than full-length PEDF (up to 39 amino acid residues), which results in high manufacturing costs, low bioavailability, and poor pharmacokinetics. It is to overcome the limitations associated with the clinical use of conventional protein drugs including. Therefore,
This synthetic peptide is useful for preventing and / or improving skin aging.
従って、一態様において、本開示は、対象における皮膚老化を予防及び/又は改善する
合成ペプチドに関する。
Accordingly, in one aspect, the present disclosure relates to a synthetic peptide that prevents and / or ameliorates skin aging in a subject.
本開示の実施態様によれば、この合成ペプチドは、長さが20〜39アミノ酸残基であり、
且つ
ドは、配列番号:1とのアミノ酸配列同一性が、約80、81、82、83、84、85、86、87、88、
89、90、91、92、93、94、95、96、97、98、99、又は100%であり得る。また、合成ペプ
チドは、配列番号:1の残基11〜30と少なくとも90%同一である少なくとも20個の連続的な
残基を含む。具体的には、この20個の連続的なアミノ酸残基は、配列番号:1の残基11〜30
とのアミノ酸配列同一性が、約90、91、92、93、94、95、96、97、98、99、又は100%で
あり得る。
According to an embodiment of the present disclosure, the synthetic peptide is 20-39 amino acid residues in length,
and
It can be 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, or 100%. The synthetic peptide also comprises at least 20 consecutive residues that are at least 90% identical to residues 11-30 of SEQ ID NO: 1. Specifically, the 20 consecutive amino acid residues are residues 11-30 of SEQ ID NO: 1.
The amino acid sequence identity to can be about 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, or 100%.
一実施態様では、合成ペプチドは、長さが39アミノ酸である配列番号:1の配列を有する
。この合成ペプチドは、以下の説明では、39-merと呼ばれる。この39-merペプチドは、ヒ
トPEDFの残基83〜121に相当し、従って、これは、公知のPEDF 44-mer(PEDFの残基78〜121
に相当する)に由来する短いバリアントである。
In one embodiment, the synthetic peptide has the sequence of SEQ ID NO: 1 which is 39 amino acids in length. This synthetic peptide is referred to as 39-mer in the following description. This 39-mer peptide corresponds to residues 83-121 of human PEDF, and thus this is known to be the known PEDF 44-mer (residues 78-121 of PEDF).
Is a short variant derived from
同時係属出願US 13/428,996(その全体を参照により本明細書に組み込む)に開示されて
いるものなどの、本発明者らによって実施された以前の実験、及び、以下に提供される実
験は、この39-merに由来するいくつかの短い合成のPEDFペプチドが、対象における皮膚老
化を予防及び/又は改善することが可能であることを明らかにしている。
Previous experiments performed by the inventors, such as those disclosed in co-pending application US 13 / 428,996 (incorporated herein by reference in its entirety) and the experiments provided below, Several short synthetic PEDF peptides derived from this 39-mer have been shown to be able to prevent and / or ameliorate skin aging in subjects.
例えば、先願と本出願との両方において開示されている実験に基づくと、
のに有効である。この34-merペプチドは、ヒトPEDFの残基88〜121に相当する。上で提供
された2つの所与の配列間の配列同一性の割合を推定するためのプロセスによれば、この3
4-merは、39-merとのアミノ酸配列同一性が100%であり、34-merの第6〜第25アミノ酸残
基は、39-merのアミノ酸残基11〜30とのアミノ酸配列同一性が100%である。
For example, based on experiments disclosed in both the prior application and the present application,
4-mer has 100% amino acid sequence identity with 39-mer, and the 6-th to 25th amino acid residues of 34-mer have amino acid sequence identity with amino acid residues 11-30 of 39-mer Is 100%.
さらに、以下の様々な実施例によれば、
のに有効であることが確認されている。この29-merペプチドは、39-merに対する100%ア
ミノ酸配列同一性を有するヒトPEDFの残基93〜121に相当する。また、29-merの第1〜第20
アミノ酸残基は、39-merのアミノ酸残基11〜30とのアミノ酸配列同一性が100%である。
Furthermore, according to the various examples below,
The amino acid residues have 100% amino acid sequence identity with the 39-mer amino acid residues 11-30.
いくつかの実施例では、24-merが、対象における皮膚老化を予防及び/又は改善するの
に有効であることが確認されている。この24-merは、ヒトPEDFの残基93〜116に相当する
、
、その最初の20個のアミノ酸残基は、39-merのアミノ酸残基11〜30とのアミノ酸配列同一
性が100%である。
In some examples, a 24-mer has been found to be effective in preventing and / or ameliorating skin aging in a subject. This 24-mer corresponds to residues 93 to 116 of human PEDF,
他の実施例では、20-merが、対象における皮膚老化を予防及び/又は改善することがで
きることが確立されている。この20-merは、ヒトPEDFの残基93〜112に相当する、
%アミノ酸配列同一性)であり、且つ39-merとのアミノ酸配列同一性が100%である。
In other examples, it has been established that a 20-mer can prevent and / or ameliorate skin aging in a subject. This 20-mer corresponds to residues 93 to 112 of human PEDF,
% Amino acid sequence identity) and 100% amino acid sequence identity with the 39-mer.
先願と本出願との両方において開示されている実験に基づくと、マウスPEDFに由来する
2種の合成ペプチドもまた、対象における皮膚老化を予防及び/又は改善することができる
。最初のマウス由来ペプチドは、本開示では、「Mo 29-mer」と呼ばれる。Mo 29-merは、
アミノ酸残基の、39-merの11〜30アミノ酸残基とのアミノ酸配列同一性が90%である。別
のマウス由来のペプチド、Mo 20-merは、
アミノ酸配列同一性が90%である。
Based on mouse PEDF, based on experiments disclosed in both prior application and this application
Two synthetic peptides can also prevent and / or ameliorate skin aging in a subject. The first mouse-derived peptide is referred to in this disclosure as “Mo 29-mer”. Mo 29-mer
Amino acid sequence identity with the 39-mer 11-30 amino acid residues is 90%. Another mouse-derived peptide, Mo 20-mer,
任意に、この合成ペプチドは、配列番号:1の残基11〜14と同一である4つの連続する残
基を含む。配列番号:1の残基11〜14(すなわちSLGA)は、短いPEDFペプチドの生物学的機能
の維持において重要な役割を果たすと考えられている。例えば、以下で提供する様々な実
施例によれば、SLGA残基を有しない18-merペプチド
願と本出願との両方において開示されている実験に基づくと、SLGA残基を有しない25-mer
ペプチド
peptide
本発明の合成ペプチドは、α-アミノ基のt-BOC又はFMOC保護などの一般に使用される方
法によって合成することができる。どちらの方法も、ペプチドのC末端から開始する、各
ステップで単独のアミノ酸が付加される段階的合成に関与している。本発明のペプチドは
、周知の固相ペプチド合成方法によって合成することもできる。
The synthetic peptides of the present invention can be synthesized by commonly used methods such as t-BOC or FMOC protection of the α-amino group. Both methods involve a step-wise synthesis where a single amino acid is added at each step, starting from the C-terminus of the peptide. The peptide of the present invention can also be synthesized by a well-known solid phase peptide synthesis method.
39-merに関する保存的変形を伴う他の合成ペプチドも考えられる。用語「保存的変形」
は、本明細書で使用する場合、アミノ酸残基の、別の生物学的に類似の残基による置き換
えを示す。保存的変形の例としては、イソロイシン、バリン、ロイシン、若しくはメチオ
ニンなどの、ある疎水性残基への、別の疎水性残基からの置換、又は、ある極性残基への
、別の極性残基からの置換、例えば、リジンからアルギニンへの、アスパラギン酸からグ
ルタミン酸への、アスパラギンからグルタミンへの置換などが挙げられる。用語「保存的
変形」はまた、置換されたポリペプチドに対して産生される抗体が、置換されていないポ
リペプチドとも免疫反応するという条件で、置換されていない親アミノ酸の代わりの置換
されたアミノ酸の使用も含む。
Other synthetic peptides with conservative variations on the 39-mer are also contemplated. The term "conservative deformation"
As used herein indicates the replacement of an amino acid residue by another biologically similar residue. Examples of conservative variations include substitution from one hydrophobic residue to another hydrophobic residue, such as isoleucine, valine, leucine, or methionine, or another polar residue to one polar residue. Substituent substitution, for example, lysine to arginine, aspartic acid to glutamic acid, asparagine to glutamine, and the like. The term “conservative variation” also refers to a substituted amino acid in place of the parent amino acid that is not substituted, provided that the antibody produced against the substituted polypeptide also immunoreacts with the unsubstituted polypeptide. Including the use of
本開示の様々な実施態様により、皮膚老化は、UV(特にUVB)照射により引き起こされ得
る。
According to various embodiments of the present disclosure, skin aging can be caused by UV (particularly UVB) irradiation.
本開示の様々な実施態様により、対象は、ヒトを含む、哺乳類に分類される任意の動物
であってよい。
According to various embodiments of the present disclosure, the subject may be any animal classified as a mammal, including humans.
前述の実施態様による合成ペプチドは、対象における皮膚老化を予防及び/又は改善す
るための医薬組成物に製剤化することができ、これは、本開示の他の態様に含まれる。
Synthetic peptides according to the foregoing embodiments can be formulated into a pharmaceutical composition for preventing and / or ameliorating skin aging in a subject, which is included in other aspects of the present disclosure.
本開示の一実施態様によれば、医薬組成物は、前述の態様/実施態様のいずれかによる
合成ペプチドを含み、且つ、該合成ペプチドは、対象における皮膚老化を予防及び/又は
改善するのに十分に有効な量で存在する。該医薬組成物はまた、合成ペプチドのための、
医薬として許容し得る賦形剤も含む。
According to one embodiment of the present disclosure, the pharmaceutical composition comprises a synthetic peptide according to any of the foregoing aspects / embodiments, and the synthetic peptide is used to prevent and / or improve skin aging in a subject. Present in a sufficiently effective amount. The pharmaceutical composition is also for synthetic peptides,
Also included are pharmaceutically acceptable excipients.
医薬組成物は、「レミントン薬科学(Remington’s Pharmaceutical Sciences)」、第17
版、Alfonoso R. Gennaro編集、Mack Publishing社、ペンシルバニア州、Easton (1985)
に記載されたような、許容し得る製薬手法に従い、調製される。
Pharmaceutical compositions are described in “Remington's Pharmaceutical Sciences”, 17th.
Edition, edited by Alfonoso R. Gennaro, Mack Publishing, Pennsylvania, Easton (1985)
Prepared according to acceptable pharmaceutical practice, as described in
合成ペプチドと共に使用されることとなる医薬として許容し得る賦形剤の選択は、基本
的には、医薬組成物が投与されることとなる方式によって決定される。本開示の一つの任
意の実施態様により、医薬組成物又はそれに含まれる合成ペプチドは、対象の真皮へ経真
皮的に送達され、結果的にその手段に適した賦形剤が使用される。当該技術分野において
周知の多種多様な皮膚科用の許容し得る不活性賦形剤を利用することができる。典型的不
活性賦形剤は、例えば、水、エチルアルコール、ポリビニルピロリドン、プロピレングリ
コール、鉱油、ステアリルアルコール、及びゲル-生成物質であることができる。
The selection of a pharmaceutically acceptable excipient to be used with a synthetic peptide is basically determined by the manner in which the pharmaceutical composition will be administered. According to one optional embodiment of the present disclosure, the pharmaceutical composition or the synthetic peptide contained therein is delivered transdermally to the subject's dermis and consequently excipients suitable for the means are used. A wide variety of dermatological acceptable inert excipients well known in the art can be utilized. Typical inert excipients can be, for example, water, ethyl alcohol, polyvinyl pyrrolidone, propylene glycol, mineral oil, stearyl alcohol, and gel-generating materials.
別のアプローチにおいて、この合成ペプチドは、最初に小胞-形成ビヒクル(リポソーム
、ミクロスフェア、又はナノソームなど)により封入され、その後所望の剤形へ製剤化す
ることができる。これらの小胞-形成ビヒクルは、本合成ペプチドの経真皮送達速度を促
進することができる。加えてこれらは、治療のより延長された治療的作用を確実にするた
めに、持続放出剤形を提供することができる。
In another approach, the synthetic peptide can be initially encapsulated by a vesicle-forming vehicle (such as a liposome, microsphere, or nanosome) and then formulated into the desired dosage form. These vesicle-forming vehicles can facilitate the transdermal delivery rate of the synthetic peptides. In addition, they can provide sustained release dosage forms to ensure a more prolonged therapeutic effect of the treatment.
あるいは又は加えて、医薬組成物は、合成ペプチド又は医薬組成物の経真皮送達速度を
促進することが可能である任意の浸透促進剤を更に含有することができる。例えば、浸透
促進剤は、角質層脂質の高度に秩序だった構造を破壊するか、細胞間タンパク質と相互作
用するか、又は角質層への薬物、共-促進剤(co-enhancer)又はビヒクルの分配を改善する
よう、作用することができる。浸透促進剤の例は、スルホキシド(例えば、ジメチルスル
ホキシド(DMSO)及びジメチルホルムアミド(DMF))、アゾン(例えば、1-ドデシルアザシク
ロヘプタン-2-オン)、ピロリドン(例えば、N-メチル-2-ピロリドン)、油類(例えば、テル
ペン及びL-メントール)、オキサゾリジノン(例えば、4-デシルオキサゾリジン-2-オン)、
脂肪酸(例えば、ラウリン酸、ミリスチン酸及びカプリン酸)、グリコール(例えば、ジエ
チレングリコール及びテトラエチレングリコール)、界面活性剤(例えば、ポリオキシエチ
レン-2-オレイルエーテル及びポリオキシエチレン-2-ステアリル(stearly)エーテル)、細
孔-形成ペプチド(例えば、マゲイニン)、及び細胞-浸透性ペプチド(例えば、トランスポ
ータン及びペネトラチン)が挙げられるが、これらに限定されるものではない。
Alternatively or in addition, the pharmaceutical composition can further contain any penetration enhancer that can enhance the transdermal delivery rate of the synthetic peptide or pharmaceutical composition. For example, penetration enhancers can disrupt the highly ordered structure of stratum corneum lipids, interact with intercellular proteins, or have drugs, co-enhancers or vehicles in the stratum corneum. Can act to improve distribution. Examples of penetration enhancers include sulfoxides (e.g. dimethyl sulfoxide (DMSO) and dimethylformamide (DMF)), azone (e.g. 1-dodecylazacycloheptan-2-one), pyrrolidone (e.g. N-methyl-2- Pyrrolidone), oils (e.g. terpenes and L-menthol), oxazolidinones (e.g. 4-decyloxazolidine-2-one),
Fatty acids (e.g. lauric acid, myristic acid and capric acid), glycols (e.g. diethylene glycol and tetraethylene glycol), surfactants (e.g. polyoxyethylene-2-oleyl ether and polyoxyethylene-2-stearyl) Ethers), pore-forming peptides (eg, magainin), and cell-permeable peptides (eg, transportan and penetratin), but are not limited to these.
更に任意に、本発明の医薬組成物はまた、当該技術分野において周知の様々な医薬用-(
特に皮膚科用-)の許容し得る添加剤も含有することができる。該添加剤としては、乾燥剤
、抗掻痒剤、消泡剤、緩衝剤、中和剤、pH調整剤、着色剤、脱色剤、緩和剤、乳化剤、エ
マルション安定剤、粘度上昇剤、保湿剤、着香剤、保存剤、抗酸化剤、化学安定剤、増粘
剤、硬化剤、又は懸濁化剤が挙げられるが、これらに限定されるものではない。
Further optionally, the pharmaceutical composition of the present invention may also be prepared by various pharmaceutical-
It may also contain acceptable additives, especially for dermatology-). Examples of the additive include a drying agent, an anti-pruritic agent, an antifoaming agent, a buffering agent, a neutralizing agent, a pH adjusting agent, a coloring agent, a decoloring agent, a relaxation agent, an emulsifying agent, an emulsion stabilizer, a viscosity increasing agent, Examples include, but are not limited to, flavoring agents, preservatives, antioxidants, chemical stabilizers, thickeners, curing agents, or suspending agents.
本開示の様々な実施態様において、医薬組成物は、液剤、噴霧剤、エアゾール剤、泡剤
、クリーム剤、ローション剤、軟膏、ゲル剤、又は貼付剤など、経真皮送達に適した様々
な剤形に製剤化することができる。
In various embodiments of the present disclosure, the pharmaceutical composition comprises various agents suitable for transdermal delivery, such as solutions, sprays, aerosols, foams, creams, lotions, ointments, gels, or patches. It can be formulated into a form.
本開示の任意の実施態様により、この合成ペプチドは、医薬組成物中に、約0.1〜100μ
M、及び好ましくは約1〜25μMの量で存在する。例えば、合成ペプチドの濃度は、約0.1、
0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4、5、6、7、8、9、10、15、20、2
5、30、35、40、45、50、55、60、65、70、75、80、85、90、95、又は100μMであること
ができる。具体的には、下記試験実施例においてマウス(体重約20g)について使用される
濃度は、約25μMである。当分野の技術者は、本合成ペプチド又は医薬組成物に関するヒ
ト相当量(HEQ)を、本明細書に提供された動物投与量を基に、算出することができる。例
えば、米国食品医薬品局(FDA)は、「健常成人志願者の治療に関する初期臨床試験におけ
る安全な最大開始用量の算出(Estimating the Maximum Safe Starting Dose in Initial
Clinical Trials for Therapeutics in Adult Healthy Volunteers)」と題する産業用指
針を公表している。
According to any embodiment of the present disclosure, the synthetic peptide is about 0.1-100 μm in a pharmaceutical composition.
M, and preferably present in an amount of about 1-25 μM. For example, the concentration of the synthetic peptide is about 0.1,
0.2, 0.3, 0.4, 0.5, 0.6, 0.7, 0.8, 0.9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 2
It can be 5, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, or 100 μM. Specifically, the concentration used for mice (body weight about 20 g) in the following test examples is about 25 μM. One skilled in the art can calculate the human equivalent (HEQ) for the synthetic peptide or pharmaceutical composition based on the animal dosage provided herein. For example, the U.S. Food and Drug Administration (FDA) stated, `` Estimating the Maximum Safe Starting Dose in Initial Clinical Trial for the Treatment of Healthy Adult Volunteers.
"Clinical Trials for Therapeutics in Adult Healthy Volunteers").
更に別の態様において、本発明は、対象における皮膚老化を予防及び/又は改善する方
法に関する。対象は、ヒトを含む、哺乳類に分類される任意の動物であってよい。本開示
の原理及び精神に従い、皮膚老化は、UV照射により引き起こされる。
In yet another aspect, the present invention relates to a method for preventing and / or ameliorating skin aging in a subject. The subject may be any animal classified as a mammal, including humans. In accordance with the principles and spirit of the present disclosure, skin aging is caused by UV irradiation.
一実施態様において、この方法は、合成ペプチドが、対象の真皮へ経真皮的に送達され
るように、前述の態様/実施態様のいずれかに従い、有効量の合成ペプチドを対象へ投与
することを含む。
In one embodiment, the method comprises administering to the subject an effective amount of the synthetic peptide according to any of the foregoing aspects / embodiments, such that the synthetic peptide is delivered transdermally to the dermis of the subject. Including.
任意の実施態様により、合成ペプチドは、本開示の前述の態様/実施態様に従う医薬組
成物へ製剤化される。
According to any embodiment, the synthetic peptide is formulated into a pharmaceutical composition according to the foregoing aspect / embodiment of the present disclosure.
一例において、本医薬組成物は、対象の皮膚へ局所的に投与されてよく、且つ合成ペプ
チド又は医薬組成物は、外部刺激の助けを借りて又は借りずに、対象の真皮へ経真皮的に
送達される。
In one example, the pharmaceutical composition may be administered topically to the subject's skin, and the synthetic peptide or pharmaceutical composition transdermally into the subject's dermis with or without the aid of an external stimulus. Delivered.
外部刺激が適用されない事象において、医薬組成物は、対象の皮膚上に、局所的に塗り
広げられるか、塗沫されるか、マッサージされるか、噴霧されるか、又はそうでなければ
塗布されることができる。この場合、医薬組成物は、先に考察したような少なくとも1種
の任意の浸透促進剤を含有することが好ましい。或いは又は加えて、合成ペプチドは、合
成ペプチドの経真皮送達速度を改善するために、先に教示したように、封入され、製剤化
されてよい。
In the event that no external stimulus is applied, the pharmaceutical composition is applied topically, smeared, massaged, sprayed or otherwise applied onto the subject's skin. Can. In this case, the pharmaceutical composition preferably contains at least one optional penetration enhancer as discussed above. Alternatively or in addition, the synthetic peptide may be encapsulated and formulated as taught above to improve the transdermal delivery rate of the synthetic peptide.
多くの外部刺激は、化合物(例えば、本合成ペプチド)に対する皮膚透過性を増大するこ
とがわかっている。そのような外部刺激としては、機械的、電気的、熱的、超音波的、又
は高周波的刺激が挙げられるが、これらに限定されるものではない。実践において、外部
刺激は、医薬適用の適用の前、それと同時に、又はその後に皮膚に適用されてよい。同様
に、そのような外部刺激の助けを借りて送達される医薬組成物又は合成ペプチドは、前述
の浸透促進剤及び/又は小胞-形成ビヒクルを任意に含有することができる。
Many external stimuli have been found to increase skin permeability to compounds (eg, the present synthetic peptides). Such external stimuli include, but are not limited to, mechanical, electrical, thermal, ultrasonic, or high frequency stimuli. In practice, external stimuli may be applied to the skin before, simultaneously with, or after application of the pharmaceutical application. Similarly, pharmaceutical compositions or synthetic peptides delivered with the aid of such external stimuli can optionally contain the aforementioned penetration enhancers and / or vesicle-forming vehicles.
一実施態様において、皮膚に機械的刺激を供するために、微小構造のアプリケーター(
極微針システム又はマイクロチャネルシステムなど)が、利用される。極微針システムは
、長さが約100〜1000μMである複数の中実又は中空の極微針を備えることができる。中実
の極微針システムに関して、本合成ペプチド又は医薬組成物は、各極微針の先端上にコー
ティングされ、且つ適用時に、極微針は角質層を貫通し、皮膚内に留まり、これにより本
合成ペプチド又は医薬組成物は真皮へ送達される。中空の極微針システムについては、液
体形状に製剤化された医薬組成物が、各極微針の内部空洞へ装填され、且つ適用時に、極
微針は皮膚を貫通し、この装置から皮膚の真皮への液体流れを可能にする。或いは、本医
薬組成物は、皮膚へ局所的に適用され、その後多数の極微針を有するマイクロチャネルシ
ステムが、皮膚に対し押しつけられ、その結果極微針は、皮膚へと100ミクロン未満貫通
し、これにより医薬組成物の経真皮送達を可能にする多数のマイクロチャネルが皮膚上に
形成される。更に或いは、本医薬組成物は、マイクロチャネルが形成された後に、局所的
に適用される。
In one embodiment, a microstructured applicator (to provide mechanical stimulation to the skin)
A microneedle system or a microchannel system) is utilized. The microneedle system can comprise a plurality of solid or hollow microneedles that are approximately 100-1000 μM in length. For solid microneedle systems, the synthetic peptide or pharmaceutical composition is coated on the tip of each microneedle, and upon application, the microneedle penetrates the stratum corneum and remains in the skin, thereby causing the synthetic peptide Alternatively, the pharmaceutical composition is delivered to the dermis. For hollow microneedle systems, a pharmaceutical composition formulated in liquid form is loaded into the internal cavity of each microneedle, and upon application, the microneedle penetrates the skin and from this device to the dermis of the skin Allows liquid flow. Alternatively, the pharmaceutical composition is applied topically to the skin, after which a microchannel system having a large number of microneedles is pressed against the skin so that the microneedles penetrate less than 100 microns into the skin. Thus, a number of microchannels are formed on the skin that allow transdermal delivery of the pharmaceutical composition. Additionally or alternatively, the pharmaceutical composition is applied topically after the microchannel is formed.
加えて、本開示の任意の実施態様による合成ペプチド又は局所性医薬組成物は、特定の
条件(例えば特定の湿度又は温度)下で、投与することができる。例えば、より湿った暖か
い環境下での投与は、合成ペプチドの経真皮送達速度を促進することができる。
In addition, a synthetic peptide or topical pharmaceutical composition according to any embodiment of the present disclosure can be administered under certain conditions (eg, certain humidity or temperature). For example, administration in a moist and warm environment can facilitate the rate of transdermal delivery of synthetic peptides.
本発明のある種の態様を明らかにするために、また、当分野の技術者が本発明を実施す
るのを助けるために、以下の実施例を提供する。これらの実施例は、決して、本発明の範
囲をいかなる方法によっても制限するものとみなされるべきではない。さらなる詳説がな
くとも、当分野の技術者は、本明細書の説明に基づいて、本発明を最大限に利用すること
ができると考えられる。本明細書に引用した全ての刊行物の全体を、参照により本明細書
に組み込む。
In order to clarify certain aspects of the present invention and to assist one of ordinary skill in practicing the present invention, the following examples are provided. These examples should in no way be construed as limiting the scope of the invention in any way. Without further details, one skilled in the art will be able to make the most of the invention based on the description herein. All publications cited herein are hereby incorporated by reference in their entirety.
(実施例)
(材料及び方法)
(Example)
(Materials and methods)
(材料) (material)
ダルベッコ改変イーグル培地(DMEM)、ウシ胎仔血清(FBS)、0.25%トリプシンは、Invit
rogen社(カリフォルニア州、Carlsbad)から購入した。軽質鉱油、グリセロール、ジメチ
ルスルホキシド(DMSO)、ウシ血清アルブミン(BSA)、5-ブロモ-2'-デオキシウリジン(BrdU
)、Hoechst 33258色素、Hoechst 33342色素、抗-β-アクチン抗体及び他の化学物質は全
て、Sigma-Aldrich社(ミズリー州、St.Louis)から得た。ディスパーゼII及びI型コラゲナ
ーゼは、Roche社(インディアナ州、Indianapolis)から入手した。抗-BrdU抗体(GTX42641)
、抗-MMP-1抗体、及び抗-ビメンチン抗体(GTX100619)は、GeneTex社(台湾、台北)から購
入した。抗コラーゲン1A1抗体は、Santa Cruz Biotechnology社(カリフォルニア州、Sant
a Cruz)から入手した。蛍光色素結合型の全ての二次抗体は、BioLegend社(カリフォルニ
ア州、San Diego)から購入した。ヘマトキシリン及びエオシン(H&E)色素は、Merck社(米
国、ニュージャージー州、Rayway)から購入した。
Dulbecco's Modified Eagle Medium (DMEM), Fetal Bovine Serum (FBS), 0.25% Trypsin, Invit
Purchased from rogen (Carlsbad, CA). Light mineral oil, glycerol, dimethyl sulfoxide (DMSO), bovine serum albumin (BSA), 5-bromo-2'-deoxyuridine (BrdU
), Hoechst 33258 dye, Hoechst 33342 dye, anti-β-actin antibody and other chemicals were all obtained from Sigma-Aldrich (St. Louis, MO). Dispase II and type I collagenase were obtained from Roche (Indianapolis, IN). Anti-BrdU antibody (GTX42641)
Anti-MMP-1 antibody and anti-vimentin antibody (GTX100619) were purchased from GeneTex (Taipei, Taiwan). Anti-collagen 1A1 antibody is available from Santa Cruz Biotechnology (Sant, CA).
a Cruz). All fluorescent dye-conjugated secondary antibodies were purchased from BioLegend (San Diego, Calif.). Hematoxylin and eosin (H & E) dyes were purchased from Merck (Rayway, NJ, USA).
FITC-結合型29-mer、並びに29-mer(配列番号:3)、24-mer(配列番号:5)、20-mer(配列番
号:6)、及び18-mer(配列番号:7)を含む他の短い合成PEDFペプチドを合成し、且つNH2末端
でのアセチル化、及びCOOH末端でのアミド化により修飾した。修飾されたペプチドは引き
続き、質量分析(>95%純度)によって特徴付けを行った(GenScript社、ニュージャージー
州、Piscataway)。各PEDF-由来の短い合成ペプチド(29-mer、24-mer、又は20-mer;本明
細書において以下では、PEDFペプチド)は、DMSO中に、ストック液(5mM)として再構成し、
且つ更なる使用まで-20℃で貯蔵した。
FITC-conjugated 29-mer, and 29-mer (SEQ ID NO: 3), 24-mer (SEQ ID NO: 5), 20-mer (SEQ ID NO: 6), and 18-mer (SEQ ID NO: 7). Other short synthetic PEDF peptides, including, were synthesized and modified by acetylation at the NH 2 terminus and amidation at the COOH terminus. The modified peptide was subsequently characterized by mass spectrometry (> 95% purity) (GenScript, Piscataway, NJ). Each PEDF-derived short synthetic peptide (29-mer, 24-mer, or 20-mer; hereinafter PEDF peptide) is reconstituted in DMSO as a stock solution (5 mM),
And stored at -20 ° C until further use.
皮膚軟膏は、蒸留水中、白色ワセリン(10%w/w)、グリセロール(10%w/w)、及び軽質鉱
油(1%w/w)を混合することにより、調製した。PEDFペプチドを含有する軟膏の調製に関し
て、PEDFペプチドストック液5μlを、軟膏1g中に溶解した。ビヒクル対照として使用する
ための軟膏については、DMSO 5μlを、軟膏1g中に溶解した。
The skin ointment was prepared by mixing white petrolatum (10% w / w), glycerol (10% w / w), and light mineral oil (1% w / w) in distilled water. For the preparation of an ointment containing PEDF peptide, 5 μl of PEDF peptide stock solution was dissolved in 1 g of ointment. For an ointment for use as a vehicle control, 5 μl of DMSO was dissolved in 1 g of ointment.
(動物) (animal)
本開示の実施態様において使用される全ての動物は、温度コントロール(24〜25℃)及び
12:12明暗周期下で、動物飼育室で飼育した。標準の実験用飼料及び水道水は、自由に摂
取可能であった。実験手順は、Mackay Memorial Hospital Review Board(台湾(R.O.C.)、
New Taipei City)によって承認され、国内の動物福祉規定に従って実施した。
All animals used in the embodiments of the present disclosure are temperature controlled (24-25 ° C.) and
12:12 Breeding in an animal room under a light-dark cycle. Standard laboratory feed and tap water were freely available. The experimental procedure is Mackay Memorial Hospital Review Board (Taiwan (ROC),
Approved by New Taipei City) and implemented according to domestic animal welfare regulations.
(マウス真皮由来の真皮線維芽細胞の単離及び培養) (Isolation and culture of mouse dermis-derived dermal fibroblasts)
完全な厚さの皮膚組織を、C57BL/6マウスの背中から入手した。皮下組織を、この皮膚
から慎重に切り出し、滅菌リン酸-緩衝食塩水(PBS)中で3回洗浄した。次に組織を、小片(
1〜2mm3)に切断した。0.1%ディスパーゼにより4℃で一晩消化させた後、表皮層を除去し
、残存する真皮部分を更に、0.1%I型コラゲナーゼにより37℃で更に4時間消化した。次
に消化した細胞を、遠心分離(400gで5分間)により収集し、10%FBS、2mM L-グルタミン、
及び1%ペニシリン-ストレプトマイシン抗生物質混合物を補充した高-グルコースDMEM中
に再懸濁させた。細胞を、組織培養プレート(Falcon Labware社;米国、ニュージャージ
ー州)上に、1×103個細胞/cm2で播種し、5%CO2により37℃で維持した。24時間後、培地
を廃棄し、残存する非-接着細胞を除去し、且つ細胞培養物を、新たな培地で満たした。
継代のために、0.25%トリプシン/EDTAを用いてほぼコンフルエントの細胞を収集した。
Full thickness skin tissue was obtained from the back of C57BL / 6 mice. The subcutaneous tissue was carefully excised from the skin and washed three times in sterile phosphate-buffered saline (PBS). Next, the tissue
Cut to 1-2 mm 3 ). After digestion with 0.1% dispase overnight at 4 ° C., the epidermal layer was removed, and the remaining dermis was further digested with 0.1% type I collagenase at 37 ° C. for an additional 4 hours. The digested cells are then collected by centrifugation (400 g for 5 minutes), 10% FBS, 2 mM L-glutamine,
And resuspended in high-glucose DMEM supplemented with 1% penicillin-streptomycin antibiotic mixture. Cells were seeded at 1 × 10 3 cells / cm 2 on tissue culture plates (Falcon Labware, NJ, USA) and maintained at 37 ° C. with 5% CO 2 . After 24 hours, the medium was discarded, the remaining non-adherent cells were removed, and the cell culture was filled with fresh medium.
For passage, nearly confluent cells were collected using 0.25% trypsin / EDTA.
(WS-1の細胞培養) (WS-1 cell culture)
ヒト皮膚線維芽細胞WS-1細胞株を、食品産業研究開発機構(Food Industry Reserch and
Development Institute)(台湾、Hsin-Chu)から入手した。WS-1細胞を、培養フラスコ中
、単層として、37℃で5%CO2の加湿したインキュベーター内で維持した。これらは、2mM
L-グルタミン、0.1mM非必須アミノ酸、1%ペニシリン/ストレプトマイシンを補充した10
%FBS-DMEM中で成長させた。継代のために、0.25%トリプシン/EDTAによりほぼコンフル
エントの細胞を継代培養した。
Human skin fibroblast WS-1 cell line was purchased from Food Industry Research and Development Organization
Development Institute) (Hsin-Chu, Taiwan). WS-1 cells were maintained as a monolayer in culture flasks at 37 ° C. in a humidified incubator with 5% CO 2 . These are 2mM
10 supplemented with L-glutamine, 0.1 mM non-essential amino acid, 1% penicillin / streptomycin
Grown in% FBS-DMEM. For passage, nearly confluent cells were subcultured with 0.25% trypsin / EDTA.
(組織診断) (Tissue diagnosis)
皮膚試料を、4%パラホルムアルデヒドで固定し、段階的な一連のエタノールで脱水し
、パラフィン処理した。組織を、5μm切片にスライスした。使用前に、固定された試料を
、キシレン中で脱パラフィン処理し、段階的な一連のエタノール中で再水和した。
Skin samples were fixed with 4% paraformaldehyde, dehydrated with a graded series of ethanol and paraffinized. The tissue was sliced into 5 μm sections. Prior to use, the fixed samples were deparaffinized in xylene and rehydrated in a graded series of ethanol.
ヘマトキシリン及びエオシン(H&E)色素を使用して、一般的な組織診断を実施した。脱
パラフィン処理した皮膚組織切片を、マッソントリクローム(Sigma-Aldrich社、ミズーリ
州、St. Louis)を製造業者の指示に従い使用し、染色し;切片を、試験し、且つNikon Ec
lipse 80i光学顕微鏡により撮影した(元の倍率、×400)。コラーゲン領域の半定量的分析
のために、各スライドから10視野を、光学顕微鏡下で無作為に選択し、断面の全領域当た
りの青色に染まった領域(mm2/mm2)を、Image-Pro Plus 4.5.1システム(Media Cybernetic
s社)を用いて測定した。
General histology was performed using hematoxylin and eosin (H & E) dye. Deparaffinized skin tissue sections were stained using Masson Trichrome (Sigma-Aldrich, St. Louis, MO) according to the manufacturer's instructions; the sections were examined and Nikon Ec
Photographed with a lipse 80i optical microscope (original magnification, x400). For semi-quantitative analysis of the collagen area, 10 fields from each slide were randomly selected under a light microscope, and the blue-stained area (mm 2 / mm 2 ) per total area of the cross section was image- Pro Plus 4.5.1 system (Media Cybernetic
s).
(免疫蛍光測定及びBrdU染色) (Immunofluorescence measurement and BrdU staining)
4%パラホルムアルデヒドによる固定後、細胞を、冷メタノールに2分間曝し、その後1N
HClにより室温で1時間処理し、その後免疫蛍光染色を行った。
After fixation with 4% paraformaldehyde, the cells were exposed to cold methanol for 2 minutes and then 1N
Treatment with HCl for 1 hour at room temperature followed by immunofluorescence staining.
動物実験のために、BrdUを、DMSO中にストック液(80mM)として再構成した。PBS 90μl
と混合したBrdUストック液10μlを、マウスへ、腹腔内注射し、16時間後に安楽死させた
。ホルマリン固定し、パラフィン-包埋した皮膚標本を、キシレン中で脱パラフィン処理
し、段階的な一連のエタノール中で再水和した。その後標本を、1N HClに、室温で1時間
曝し、引き続き免疫蛍光測定試験を行った。
For animal experiments, BrdU was reconstituted as a stock solution (80 mM) in DMSO. PBS 90μl
Mice were injected with 10 μl of BrdU stock solution intraperitoneally and euthanized 16 hours later. Formalin-fixed, paraffin-embedded skin specimens were deparaffinized in xylene and rehydrated in a graded series of ethanol. Thereafter, the specimens were exposed to 1N HCl for 1 hour at room temperature, and subsequently subjected to an immunofluorescence measurement test.
BrdU-標識されたDNAを、ポリクローナル抗-BrdU抗体及びローダミン-結合型ロバ抗-ウ
サギIgGにより検出した。核は、Hoechst 33258により対比染色した(青色)。
BrdU-labeled DNA was detected with polyclonal anti-BrdU antibody and rhodamine-conjugated donkey anti-rabbit IgG. Nuclei were counterstained with Hoechst 33258 (blue).
(免疫ブロット分析) (Immunoblot analysis)
皮膚組織を、20mM HEPES(pH7.4)、150mM NaCl、1%SDS、1mMエチレンジアミン四酢酸(E
DTA)、5mMフェニルメタンスルホニルフルオリド(PMSF)、及び1mMジチオスレイトール(DTT
)、1%Triton X-100を含有する氷冷した溶解緩衝液中で、プロテアーゼインヒビターカク
テル(Roche社、インディアナ州、Indianapolis)を新たに添加し、ホモジナイズした。次
にホモジネートを、12,000gで、4℃、30分間遠心分離し、その後上清を収集し、-70℃で
貯蔵した。溶解液中のタンパク質含量を、Bradfordアッセイを用いて決定した。全細胞溶
解液を、前述の溶解緩衝液を用いて調製した。次に溶解液のアリコートを、SDS-PAGE上で
分解し、ポリ2フッ化ビニリデン(PVDF)メンブレン(Millipore社、米国、マサチューセッ
ツ州、Bedford)上に電気転写し、免疫ブロット分析に進めた。
Skin tissue was treated with 20 mM HEPES (pH 7.4), 150 mM NaCl, 1% SDS, 1 mM ethylenediaminetetraacetic acid (E
DTA), 5 mM phenylmethanesulfonyl fluoride (PMSF), and 1 mM dithiothreitol (DTT)
), Freshly added protease inhibitor cocktail (Roche, Indianapolis, Ind.) In ice-cold lysis buffer containing 1% Triton X-100 and homogenized. The homogenate was then centrifuged at 12,000g for 30 minutes at 4 ° C, after which the supernatant was collected and stored at -70 ° C. The protein content in the lysate was determined using the Bradford assay. A whole cell lysate was prepared using the lysis buffer described above. An aliquot of the lysate was then resolved on SDS-PAGE, electrotransferred onto a poly (vinylidene difluoride) (PVDF) membrane (Millipore, Bedford, Mass., USA) and proceeded to immunoblot analysis.
免疫ブロット試験に使用した抗体は、抗-I型コラーゲン1A1抗体(1:1000希釈)、抗-MMP-
1抗体(1:500希釈)及び抗-β-アクチン抗体(1:10000希釈)を含んだ。関心対象のタンパク
質は、好適なIgG-HRP二次抗体及びECL試薬(Amersham社、米国、イリノイ州、Arlington H
eights)を用いて、検出した。X線フィルムを、モデルGS-700 Image Densitometer(Bio-Ra
d Laboratories社、カリフォルニア州、Hercules)上で走査し、且つLabworks 4.0ソフト
ウェアを用い解析した。定量のためには、少なくとも3回の独立した実験からのブロット
を使用した。
The antibodies used in the immunoblot test were anti-type I collagen 1A1 antibody (1: 1000 dilution), anti-MMP-
1 antibody (1: 500 dilution) and anti-β-actin antibody (1: 10000 dilution) were included. Proteins of interest include suitable IgG-HRP secondary antibodies and ECL reagents (Amersham, Illinois, USA, Arlington H
eights). X-ray film is modeled on model GS-700 Image Densitometer (Bio-Ra
d Laboratories, Inc., Hercules, Calif.) and analyzed using Labworks 4.0 software. For quantification, blots from at least 3 independent experiments were used.
(RNA抽出及び逆転写-ポリメラーゼ連鎖反応) (RNA extraction and reverse transcription-polymerase chain reaction)
TRIzol(Invitrogen社)を使用して、細胞から全RNAを抽出し、RNase-非含有DNase I(Qia
gen社、カリフォルニア州、Santa Clarita)で処理してゲノムDNAを除去し、次いで、RNA
精製キット(Dynabeads;Invitrogen社)で精製した。初代真皮線維芽細胞から回収した1μ
gの全RNAを、0.25μgのランダムプライマー及び0.8mM dNTPを含有する20μlの反応緩衝液
中で、200単位のエキスパンド逆転写酵素(Roche社、独国、Mannheim)によって、42℃で1
時間、cDNAに逆転写させた。2μlのcDNAを、PCR反応における鋳型として使用した。PCRは
、15μlのEconoTaq(登録商標)PLUS GREEN 2×マスターミックス(Lucigen(登録商標)社)、
1μMの各プライマー、及び2μlの鋳型DNAを含有する30μlの反応体積中で実施した。18〜
22サイクルの増幅反応(変性、20秒、94℃;アニーリング、30秒、57℃;及び重合、40秒、7
2℃)で、cDNAを合成した。プライマーセットに対するサイクル数は、増幅の線形範囲内で
あるように選択した。具体的PCRプライマーの配列は、マウスMMP-13(寄託番号:NM_00860
7)のセンス、
;寄託番号;M32599)のセンス、
スゲル中で電気泳動させ、UV照明によって視覚化した。FUJI LAS-3000システム及びMulti
Gauge Ver. 1.01ソフトウェア(富士フイルム社、日本、東京)を使用して、PCR産物の強
度を濃度測定的に定量化した。
Total RNA was extracted from cells using TRIzol (Invitrogen) and RNase-free DNase I (Qia
Gen, Santa Clarita, CA) to remove genomic DNA and then RNA
Purification was performed using a purification kit (Dynabeads; Invitrogen). 1μ recovered from primary dermal fibroblasts
g total RNA was added at 42 ° C. with 200 units of expanded reverse transcriptase (Roche, Mannheim, Germany) in 20 μl reaction buffer containing 0.25 μg random primer and 0.8 mM dNTP.
Time was reverse transcribed into cDNA. 2 μl of cDNA was used as a template in the PCR reaction. PCR was performed using 15 μl EconoTaq® PLUS GREEN 2 × Master Mix (Lucigen®),
Performed in a 30 μl reaction volume containing 1 μM of each primer and 2 μl of template DNA. 18 ~
22 cycles of amplification reaction (denaturation, 20 seconds, 94 ° C; annealing, 30 seconds, 57 ° C; and polymerization, 40 seconds, 7 ° C
CDNA was synthesized at 2 ° C. The number of cycles for the primer set was chosen to be within the linear range of amplification. The specific PCR primer sequence is mouse MMP-13 (deposit number: NM_00860).
7) sense,
Sense of deposit number; M32599)
The intensity of PCR products was quantified densitometrically using Gauge Ver. 1.01 software (Fujifilm, Tokyo, Japan).
(統計) (statistics)
結果は、平均±平均値の標準誤差(SEM)として表した。統計比較のために、一元配置ANO
VAを使用した。別段の指定がない限り、P<0.05を、有意であるとみなした。
The results were expressed as mean ± standard error of the mean (SEM). One-way ANO for statistical comparison
VA was used. P <0.05 was considered significant unless specified otherwise.
(実施例1) (Example 1)
(PEDFペプチドの経真皮送達) (Transdermal delivery of PEDF peptide)
フルオレセイン(FITC)-結合型29-merペプチドを、インビボにおける本PEDFペプチドの
経真皮送達を調べるために使用した。
Fluorescein (FITC) -conjugated 29-mer peptide was used to study transdermal delivery of the PEDF peptide in vivo.
最初に、8週齢の雄C57BL/6マウスの背側の毛を、全身麻酔下で、溶融したワックス/ロ
ジン混合物(1:1)を使用し、除去した。翌日、FITC-結合型29-merペプチド(25μM)を含有
する軟膏を、マウスの背側皮膚に塗布し、その後極微針パッチ(3M(商標)マイクロチャネ
ルスキンシステム;3M社(シンガポール)から提供)を、背側皮膚に対し穏やかに押しつけ
、極微針を皮膚へ100ミクロン未満貫通させた(FITC-29mer/MN群)。対照群(FITC-29mer/CT
)に関しては、マウスは、軟膏を受け取り、引き続きの極微針処置は受けなかった。24時
間後、皮膚を収集し、固定し、凍結切片とし、蛍光顕微鏡により試験した。3回の独立し
た実験の代表的画像(元の倍率、×400)を、図1に提供している。
Initially, dorsal hairs of 8 week old male C57BL / 6 mice were removed using a melted wax / rosin mixture (1: 1) under general anesthesia. The next day, an ointment containing FITC-conjugated 29-mer peptide (25 μM) was applied to the dorsal skin of the mice, followed by a microneedle patch (3M ™ microchannel skin system; provided by 3M Company (Singapore)) Was gently pressed against the dorsal skin, and a microneedle was allowed to penetrate the skin less than 100 microns (FITC-29mer / MN group). Control group (FITC-29mer / CT
), The mice received ointment and did not receive subsequent microneedle treatment. After 24 hours, skin was collected, fixed, frozen, and examined with a fluorescence microscope. A representative image of three independent experiments (original magnification, x400) is provided in FIG.
図1の左側パネルのH&E染色した切片は、標本の表皮及び真皮を強調している。図1の中
央パネル及び右側パネルの蛍光画像は、皮膚を横切るFITC-結合型29-merの分布を図示し
ている。特に、FITC-29mer/MN群における表皮及び真皮を超えるフルオレセインからの高
度に認識可能な緑色シグナルは、FITC-結合型29-merペプチドは、真皮までうまく送達さ
れたことを指摘している。対照的に、FITC-29mer/CT群において、緑色シグナルは、真皮
においてかろうじて検出可能であるが、ほとんどのフルオレセインシグナルは、表皮に残
存した。
The H & E stained section in the left panel of FIG. 1 highlights the epidermis and dermis of the specimen. The fluorescence images in the center panel and right panel of FIG. 1 illustrate the distribution of FITC-conjugated 29-mer across the skin. In particular, the highly recognizable green signal from fluorescein beyond the epidermis and dermis in the FITC-29mer / MN group indicates that the FITC-conjugated 29-mer peptide was successfully delivered to the dermis. In contrast, in the FITC-29mer / CT group, a green signal was barely detectable in the dermis, but most of the fluorescein signal remained in the epidermis.
(実施例2) (Example 2)
(PEDFペプチドは真皮のコラーゲン含量を増加する) (PEDF peptide increases the collagen content of the dermis)
コラーゲンは、真皮の主要なマトリックス成分であり、且つ皮膚の弾性特性を提供する
強靱な線維構造を形成する。この試験実施例は、本PEDFペプチドは、真皮のコラーゲン含
量を増加するかどうかを調べた。実施例1に説明したように脱毛したマウスを、いくつか
の実験群に無作為に割り当て、且つ下記のように処置した。各マウスについて、背側正中
線の片側(約2cm2)には、軟膏50μl(29-mer、20-mer、又はDMSO-含有軟膏)を塗り、引き続
き極微針処置し;他方で、背側正中線の他の側(約2cm2)には、同じ軟膏50μlを塗り、極
微針処置は行わなかった。この処置を2週間にわたり週2回施し、皮膚を、覆わないまま放
置し、最初の処置から14日後に収集した。皮膚標本を、真皮コラーゲンについて、マッソ
ントリクローム染色(青色)により染色し;代表的画像を図2に提供した。皮膚の染色され
たコラーゲン領域は、「材料及び方法」の項において先に記したように定量し、結果を、
ビヒクル/MNの領域について規準化した。I型コラーゲン(COL1A1)のレベルを、先に説明し
た免疫ブロット分析により調べ、結果を、ビヒクル/CT群のレベルについて規準化した。
定量的結果を、表1にまとめている。
The vehicle / MN area was normalized. The level of type I collagen (COL1A1) was examined by immunoblot analysis as described above, and the results were normalized to the level of the vehicle / CT group.
Quantitative results are summarized in Table 1.
図2の画像は、ビヒクル/MN切片と比べた場合に、29-mer/MN及び20-mer/MN切片における
より顕著な青色染色により証明されるように、極微針処置と組合せた29-mer又は20-merの
処置は、真皮におけるコラーゲンレベルを増加することを指摘している。更に、ビヒクル
/CT切片とビヒクル/MN切片を比較することにより、本発明者らは、極微針処置のみでは、
コラーゲンレベルに対し効果を有さないことがわかった。また、ビヒクル/CT、20-mer/CT
、及び29-mer/CTの切片間ではコラーゲンレベルにおける有意な差異は存在せず、このこ
とは、コラーゲンレベルは、被験対象間では有意には変動しないことを指摘している。
The image in FIG. 2 shows the 29-mer combined with the microneedle treatment as evidenced by the more prominent blue staining in the 29-mer / MN and 20-mer / MN sections when compared to the vehicle / MN sections. Alternatively, 20-mer treatments indicate that collagen levels in the dermis are increased. In addition, the vehicle
By comparing the / CT section and the vehicle / MN section, we can
It has been found that it has no effect on collagen levels. Vehicle / CT, 20-mer / CT
, And there is no significant difference in collagen levels between sections of 29-mer / CT, indicating that collagen levels do not vary significantly between subjects.
I型コラーゲン(COL1A1)は、真皮コラーゲンの主要成分であり、その免疫ブロット分析
は、29-mer/MN及び20-mer/MN処置は、対照処置(ビヒクル/CT)のそれと比べ、COL1A1レベ
ルの有意な増加を生じることを指摘している。
Type I collagen (COL1A1) is a major component of dermal collagen, and its immunoblot analysis shows that 29-mer / MN and 20-mer / MN treatments have COL1A1 levels compared to that of control treatments (vehicle / CT). It points out that it produces a significant increase.
(実施例3) (Example 3)
(PEDFペプチドは真皮線維芽細胞増殖を促進する) (PEDF peptide promotes dermal fibroblast proliferation)
線維芽細胞は、ヒト皮膚における主要なコラーゲン-産生細胞であり、従って本PEDFペ
プチドの、真皮線維芽細胞の増殖に対する効果を評価するために、インビトロ及びインビ
ボ分析を行った。
Fibroblasts are the primary collagen-producing cells in human skin, and thus in vitro and in vivo analyzes were performed to evaluate the effect of the PEDF peptide on dermal fibroblast proliferation.
(実施例3.1) (Example 3.1)
(PEDFペプチドはインビトロにおいて真皮線維芽細胞増殖を促進する) (PEDF peptide promotes dermal fibroblast proliferation in vitro)
初代マウス真皮線維芽細胞を、「材料及び方法」の項に説明したように、単離し且つ培
養した。2回継代した真皮線維芽細胞を、6-ウェルプレート中のゼラチン-コートされたス
ライドに、1ウェル当たり2×105個細胞の密度で播種し、成長培地(DMEM+10%FBS)におい
て24時間培養し、その後1%FBSのみ(対照群)又は1%FBSと追加の50nMのPEDF-由来のペプ
チド(すなわち、29-mer、24-mer、20-mer、18-mer、Mo 29-mer、又はMo 20-mer)を含有す
る基本成長培地と置き換え、24時間培養した。BrdU標識アッセイに関して、BrdU(最終濃
度10μM)を、この培養物に2時間添加した。線維芽細胞はまた、線維芽細胞マーカーであ
るビメンチンにより染色し;代表的画像を、図3に提供した。BrdU-及びビメンチン-二重
陽性細胞のレベルを、総ビメンチン-陽性細胞当たりのBrdU-及びビメンチン-二重陽性細
胞の割合として表し(BrdU/ビメンチン標識指標)、結果を表2にまとめた。
まとめると、本開示の実施態様によるPEDF-由来のペプチド(例えば、29-mer、24-mer、
20-mer及び2種のマウスホモログペプチド)を含有する培地において培養した真皮線維芽細
胞は、対照培地において培養したものよりも、より多く増殖した(約5倍)(表2)。対照的に
、「SLGA」残基を持たない18-merの処置は、そのような効果を誘発することに失敗した。
In summary, PEDF-derived peptides according to embodiments of the present disclosure (e.g., 29-mer, 24-mer,
Dermal fibroblasts cultured in medium containing 20-mer and two mouse homolog peptides) proliferated more (about 5 times) than those cultured in control medium (Table 2). In contrast, treatment of 18-mer without the “SLGA” residue failed to induce such effects.
(実施例3.2) (Example 3.2)
(PEDFペプチドはインビボにおいて真皮線維芽細胞の増殖を促進する) (PEDF peptide promotes dermal fibroblast proliferation in vivo)
先の実施例2からの標本を同じく、線維芽細胞マーカーのビメンチンについて染色し、
ビメンチン-陽性細胞を、顕微鏡下でカウントした。
Vimentin-positive cells were counted under a microscope.
表3のデータは、29-mer/MN及び20-mer/MNで処置した試料は、ビヒクル/MN及びビヒクル
単独(すなわち、ビヒクル/CT)で処置したものと比べ、真皮領域中に有意に多い数の線維
芽細胞を有することを指摘している。この観察は、本PEDFペプチドの経真皮送達は、真皮
中の線維芽細胞密度と正の関係にあることを示唆している。
The data in Table 3 shows that samples treated with 29-mer / MN and 20-mer / MN are significantly more in the dermis region than those treated with vehicle / MN and vehicle alone (ie, vehicle / CT). It is pointed out that it has a number of fibroblasts. This observation suggests that transdermal delivery of the PEDF peptide is positively related to fibroblast density in the dermis.
本PEDFペプチドの経真皮送達が、インビボにおいて、真皮線維芽細胞の増殖を促進する
かどうかを調べるために、マウスに、BrdUを腹腔内注射し、PEDFペプチド/MN処置又はビ
ヒクル/MN処置の16時間後に安楽死させた。皮膚切片を、ビメンチン(緑色)及びBrdU(赤色
)について染色した。BrdU-及びビメンチン-二重陽性細胞のレベルを、総ビメンチン-陽性
細胞当たりのBrdU-及びビメンチン-二重陽性細胞の割合として表し(BrdU/ビメンチン標識
指標)、結果を表4にまとめた。
). The level of BrdU- and vimentin-double positive cells was expressed as the ratio of BrdU- and vimentin-double positive cells per total vimentin-positive cells (BrdU / vimentin labeling index) and the results are summarized in Table 4.
表4に認めることができるように、29-mer/MN群及び20-mer/MN群からの皮膚切片におい
て、DMSO-含有軟膏で処置した切片(ビヒクル/MN)と比べ、線維芽細胞がより増殖している
。この観察は、本合成ペプチドの経真皮送達は、真皮線維芽細胞の増殖活性を促進する上
で有効であることを指摘している。この真皮線維芽細胞の増殖の増加は、コラーゲン含量
は、本PEDFペプチドの経真皮送達により改善される(表1、上記)という知見と合致する。
As can be seen in Table 4, the fibroblasts in the skin sections from the 29-mer / MN group and the 20-mer / MN group had more fibroblasts than the sections treated with DMSO-containing ointment (vehicle / MN). Proliferating. This observation points out that transdermal delivery of the synthetic peptide is effective in promoting the proliferation activity of dermal fibroblasts. This increased proliferation of dermal fibroblasts is consistent with the finding that collagen content is improved by transdermal delivery of the PEDF peptide (Table 1, above).
(実施例3.3) (Example 3.3)
(PEDFペプチドはインビボにおいて光損傷された皮膚の真皮線維芽細胞増殖を促進する) (PEDF peptide promotes dermal fibroblast proliferation in photodamaged skin in vivo)
UVB照射は、真皮のコラーゲンマトリックスの断片化を引き起こし、これは線維芽細胞
の細胞周期の停止を誘導することが知られている。この試験実施例において、本発明者ら
は、本PEDFペプチドの経真皮送達が、UVB照射により損傷を受けた線維芽細胞の増殖活性
を回復するのに有効であるかどうかを調べた。
UVB irradiation causes fragmentation of the dermal collagen matrix, which is known to induce cell cycle arrest of fibroblasts. In this test example, we examined whether transdermal delivery of the PEDF peptide was effective in restoring the proliferative activity of fibroblasts damaged by UVB irradiation.
6週齢の雌のヌードマウス(BALB/cAnN.Cg-Foxn1nu/CrlNarl)の背中に、紫外線B波(UVB)
を、1週間に5回、8週間にわたり、動物の背中の上方約20cmに配置した5個のUVBランプ(モ
デルXL-1000B、Spectrolinker(商標)装置;発光ピーク:312nm)の列(bank)を用い、照射
した。UVB曝露の間、マウスは、ケージ内を自由に移動させた。最小紅斑形成照射量(MED)
として表した照射強度は、最初の2週間は1MEDに設定し(60mJ/cm2)、実験の第3週から第4
週にかけて2MED(120mJ/cm2)まで、第5週から第6週にかけて3MED(180mJ/cm2)まで、第7週
から第8週にかけて4MED(240mJ/cm2)まで、次第に増大させた。8週目のUVB曝露後に、動物
は、注目される皺を呈し、且つ引き続き、各群マウス3匹で、下記の4群に無作為に分けた
。UVB/ビヒクル、UVB/29-mer、UVB/20-mer、及びUVB/18-mer群において、軟膏(DMSO、29-
mer、20-mer又は18-mer PEDFを含有)350μlを、背側皮膚へ塗布し、その後経真皮送達を
、軟膏処置した皮膚を、極微針パッチで押し抜くことにより達成した。同じく、UVB照射
に供しなかったマウスを、対照(正常)として使用した。軟膏/極微針処置は、2週間にわた
り週2回与えた。マウスには、BrdUを腹腔内投与し、最後の処置の16時間後に安楽死させ
た。皮膚切片を、ビメンチン及びBrdUについて染色した。BrdU-及びビメンチン-二重陽性
細胞のレベルを、総ビメンチン-陽性細胞当たりのBrdU-及びビメンチン-二重陽性細胞の
割合として表した(BrdU/ビメンチン標識指標)。定量結果を、表5にまとめた。
A bank of 5 UVB lamps (model XL-1000B, Spectrolinker ™ instrument; emission peak: 312 nm) placed approximately 20 cm above the animal's back 5 times a week for 8 weeks. Used and irradiated. During UVB exposure, the mice moved freely within the cage. Minimum erythema formation dose (MED)
The irradiation intensity expressed as is set to 1 MED for the first two weeks (60 mJ / cm 2 ), and from the third week to the fourth of the experiment
Subjected week until 2MED (120mJ / cm 2), from week 5 until 3MED (180mJ / cm 2) over the first 6 weeks, from week 7 toward Week 8 to 4MED (240mJ / cm 2), was gradually increased. After 8 weeks of UVB exposure, the animals exhibited noticeable wrinkles and were subsequently randomly divided into the following 4 groups with 3 mice in each group. In the UVB / vehicle, UVB / 29-mer, UVB / 20-mer, and UVB / 18-mer groups, ointment (DMSO, 29-
350 μl) (containing mer, 20-mer or 18-mer PEDF) was applied to the dorsal skin, after which transdermal delivery was achieved by pressing the ointment-treated skin with a microneedle patch. Similarly, mice that were not subjected to UVB irradiation were used as controls (normal). Ointment / microneedle treatment was given twice a week for 2 weeks. Mice received BrdU intraperitoneally and were euthanized 16 hours after the last treatment. Skin sections were stained for vimentin and BrdU. The level of BrdU- and vimentin-double positive cells was expressed as the ratio of BrdU- and vimentin-double positive cells per total vimentin-positive cells (BrdU / vimentin labeling index). The quantitative results are summarized in Table 5.
表5に認めることができるように、UVB曝露は、UVB照射に曝露されていない皮膚と比べ
、真皮線維芽細胞の増殖活性を、約50%低下した(UVB/ビヒクル:2.1±1.1%、対、正常
:4.1±0.8%)。他方で、UVB曝露後の29-mer及び20-merの経真皮送達は、真皮線維芽細胞
の増殖活性を、UVB/ビヒクル群のそれと比べ、約2.5倍増強した。29-mer又は20-mer処置
した動物における増殖活性は、UVBにより照射されない動物のものよりも更により高いが
、その差は有意性が小さいことは注記される。対照的に、重要な「SLGA残基」を欠いてい
る18-merは、真皮線維芽細胞増殖を促進することに失敗した。
As can be seen in Table 5, UVB exposure reduced dermal fibroblast proliferative activity by approximately 50% compared to skin not exposed to UVB irradiation (UVB / vehicle: 2.1 ± 1.1% vs. Normal: 4.1 ± 0.8%). On the other hand, transdermal delivery of 29-mer and 20-mer after UVB exposure enhanced the proliferation activity of dermal fibroblasts by about 2.5 times compared to that of UVB / vehicle group. It is noted that the proliferative activity in 29-mer or 20-mer treated animals is even higher than that of animals not irradiated with UVB, but the difference is less significant. In contrast, an 18-mer lacking an important “SLGA residue” failed to promote dermal fibroblast proliferation.
結論として、実施例3(実施例3.1から3.3を含む)に示されたデータは、本PEDFペプチド
は、正常皮膚組織(すなわち、UVB照射による処置を受けていない組織)に加え、光損傷を
受けた皮膚組織(すなわち、UVB照射による処置を受け、曝露の結果として注目される皺を
伴う組織)における、真皮線維芽細胞の増殖を促進する点で有効であることを明らかにし
ている。線維芽細胞は、コラーゲン合成に係わっているので、改善された線維芽細胞の増
殖活性及び結果としてのより高い線維芽細胞密度は、次にコラーゲン合成を促進すること
ができる。従って、本PEDFペプチドは、コラーゲン合成のための皮膚の内因性修復機構を
惹起することが可能である。
In conclusion, the data presented in Example 3 (including Examples 3.1 to 3.3) show that the PEDF peptide is not only damaged by normal skin tissue (i.e., tissue that has not been treated with UVB irradiation), but also photodamaged. Have been shown to be effective in promoting the proliferation of dermal fibroblasts in fresh skin tissue (ie, tissues with wrinkles that have been treated with UVB irradiation and noted as a result of exposure). Since fibroblasts are involved in collagen synthesis, improved fibroblast proliferation activity and the resulting higher fibroblast density can then promote collagen synthesis. Thus, the present PEDF peptide is capable of inducing an endogenous repair mechanism of the skin for collagen synthesis.
(実施例4) (Example 4)
(PEDFペプチドはUVB-誘導したMMP-1発現を減少する) (PEDF peptide reduces UVB-induced MMP-1 expression)
MMP-1(間質コラゲナーゼ)は、I型及びIII型コラーゲンのコラーゲントリプルヘリック
スの切断を触媒することが可能な唯一の酵素である。更に、MMP-1は、ヒト皮膚に存在す
る主要なコラーゲン分解酵素であり、且つUV照射に反応してアップレギュレートされる。
齧歯類は、MMP-1遺伝子を欠いており、これらの動物においてはMMP-1は、MMP-13により機
能的に代替される。従って、本試験実施例は、本合成ペプチドは、UVB曝露により誘導さ
れるMMP-1及びMMP-13の発現を減少するかどうかを解明することを目的としている。
MMP-1 (interstitial collagenase) is the only enzyme capable of catalyzing the cleavage of collagen triple helices of type I and type III collagen. Furthermore, MMP-1 is a major collagenolytic enzyme present in human skin and is upregulated in response to UV irradiation.
Rodents lack the MMP-1 gene, and MMP-1 is functionally replaced by MMP-13 in these animals. Therefore, this test example aims to elucidate whether this synthetic peptide reduces the expression of MMP-1 and MMP-13 induced by UVB exposure.
本発明者らの先の研究により、細胞生存度は、UVB照射15mJ/cm2への曝露後は、対照の
生存度に対し、95%より大きかった(データは示さず)。100nM 29-merで24時間前処理され
たヒト真皮線維芽細胞(WS-1細胞)及び初代マウス真皮線維芽細胞は、細胞生存度において
有意な変化を引き起こさず(データは示さず)、且つトランスウェルアッセイによりアッセ
イされた細胞遊走において有意な変化を引き起こさなかった(データは示さず)。本発明者
らは、この照射量でのUV照射は、MMP発現レベルの増加に繋がることを認めた。従って、
曝露量は、以下の実験において15mJ/cm2に設定した。
According to our previous studies, cell viability was greater than 95% relative to control viability after exposure to 15 mJ / cm 2 of UVB irradiation (data not shown). Human dermal fibroblasts (WS-1 cells) and primary mouse dermal fibroblasts pretreated with 100 nM 29-mer for 24 hours did not cause significant changes in cell viability (data not shown) and trans It did not cause a significant change in cell migration assayed by the well assay (data not shown). The present inventors have found that UV irradiation at this dose leads to an increase in MMP expression level. Therefore,
The amount of exposure was set to 15 mJ / cm 2 in the following experiment.
WS-1を、6-ウェルプレートに、1ウェル当たり1×105個細胞の密度で播種し、10%FBS-D
MEM成長培地において24時間成長させ、その後100nM PEDFペプチドを補充した又は補充し
ていない1%FBS-DMEMと共に、更に24時間インキュベーションした。細胞を、リン酸緩衝
食塩水(PBS)により2回洗浄し、PBSで被覆しUVB照射に曝露した。UVB処置は、細胞培養フ
ード内で、UVBランプ(モデルXL-1000B、Spectrolinker(商標)社)を用い、最終照射量15mJ
/cm2で約100秒間実施した。細胞生存度は、トリパンブルー排除アッセイを用いて、アッ
セイした(>95%)。UVB照射後、PBSを、PEDFペプチドを含む又は含まない1%FBS-DMEMと
交換し、更に48時間培養し、次にタンパク質抽出物を、MMP-1タンパク質の発現に関して
ウェスタンブロットによりアッセイした。UVB照射に供さなかった細胞を、対照(正常)と
して使用した。MMP-1の発現レベルは、ビヒクル/UVB群における発現レベル(100%に設定)
に対し規準化し、定量結果を表6にまとめている。
Growth was performed in MEM growth medium for 24 hours, followed by an additional 24 hours incubation with 1% FBS-DMEM supplemented or not supplemented with 100 nM PEDF peptide. Cells were washed twice with phosphate buffered saline (PBS), coated with PBS and exposed to UVB irradiation. UVB treatment is performed in a cell culture hood using a UVB lamp (Model XL-1000B, Spectrolinker (trademark)), with a final irradiation dose of 15 mJ
Performed at / cm 2 for about 100 seconds. Cell viability was assayed using the trypan blue exclusion assay (> 95%). After UVB irradiation, PBS was replaced with 1% FBS-DMEM with or without PEDF peptide and incubated for a further 48 hours, then protein extracts were assayed by Western blot for expression of MMP-1 protein. Cells that were not subjected to UVB irradiation were used as controls (normal). The expression level of MMP-1 is the expression level in the vehicle / UVB group (set to 100%)
Table 6 summarizes the quantitative results.
ビヒクル/UVB群と正常群を比較することにより、本発明者らは、UVB照射は、MMP-1タン
パク質発現の有意な増加を生じたことに注目した(100%、対、正常群における約5%)。し
かし、線維芽細胞の29-mer、24-mer又は20-merとの予備インキュベーションは、MMP-1タ
ンパク質レベルを、ビヒクル/UVB群の約半分まで、有意に低下した。
By comparing the vehicle / UVB group with the normal group, we noted that UVB irradiation resulted in a significant increase in MMP-1 protein expression (100% vs. about 5 in the normal group). %). However, preincubation of fibroblasts with 29-mer, 24-mer or 20-mer significantly reduced MMP-1 protein levels to about half of the vehicle / UVB group.
単層培養において2回継代した初代マウス真皮線維芽細胞を、100nM PEDFペプチドを補
充した又は補充していない1%FBS-DMEMと共に、24時間インキュベーションし、その後先
に説明したようにUVB照射に供した。UVB照射後、PBSを、PEDFペプチドを含む又は含まな
い1%FBS-DMEMと交換し、更に24時間培養し、その後後続のRT-PCR分析のために、細胞の
全RNAを抽出した。MMP-13 mRNAの発現レベルを、ビヒクル/UVB群における発現レベル(100
%に設定)に対し規準化し、定量結果を表7にまとめている。
Table 7 summarizes the quantitative results.
表6における先の知見同様、MMP-13の発現レベルも、UVB曝露によりアップレギュレート
された(ビヒクル/UVB群、対、正常群)。同じくそのようなアップレギュレーションは、本
PEDFペプチドにより予備処理された細胞において、実質的に低下された(29-mer/UVB、24-
mer/UVB、及び20-mer/UVB、対、ビヒクル/UVB)。対照的に、「SLGA残基」を伴わない18-m
erは、UVB-誘導したアップレギュレーションを低下することはできなかった。
Similar to previous findings in Table 6, MMP-13 expression levels were also up-regulated by UVB exposure (vehicle / UVB group vs. normal group). Such up-regulation is also
In cells pretreated with PEDF peptide, it was substantially reduced (29-mer / UVB, 24-
mer / UVB, and 20-mer / UVB vs. vehicle / UVB). In contrast, 18-m without the “SLGA residue”
er was unable to reduce UVB-induced upregulation.
これらの結果は、本PEDFペプチドは、UVB-誘導したMMP-1誘導に対し、ヒト真皮線維芽
細胞を保護することができることを示唆している。MMP-1によるI型コラーゲンの破壊は、
光老化の重要な寄与因子である。従って本PEDFペプチドは、光老化防止剤として使用する
ことができる。
These results suggest that the PEDF peptide can protect human dermal fibroblasts against UVB-induced MMP-1 induction. The destruction of type I collagen by MMP-1
It is an important contributor to photoaging. Therefore, the present PEDF peptide can be used as a photoaging inhibitor.
(実施例5) (Example 5)
(PEDFペプチドはUV-誘導した皺を減少する) (PEDF peptide reduces UV-induced wrinkles)
皺の形成は、UVB照射への反復曝露に密接に関連している。詳細には、UVB照射は、コラ
ーゲン破壊を誘導し、且つ真皮におけるプロコラーゲン生合成を阻害し;このことは、コ
ラーゲン喪失を生じ、結果的に皺形成を生じる。この試験実施例において、本発明者らは
、本PEDFペプチドの抗-皺効果を、ヌード(すなわち無毛)マウスにおいて調べた。皺は、
先の実施例3.3に示した手順に従う8週間のUVB照射により誘導した。マウスの外観を、UVB
照射前(正常)、UVB照射後(UVB/UT)、並びに各軟膏により2週間処置後(UVB/ビヒクル、UVB
/29-mer、UVB/20-mer及びUVB/18-mer)に撮影し;代表的写真を、図4に提供した。
The formation of wrinkles is closely related to repeated exposure to UVB radiation. Specifically, UVB irradiation induces collagen destruction and inhibits procollagen biosynthesis in the dermis; this results in collagen loss and results in wrinkle formation. In this test example, we examined the anti-wrinkle effect of the PEDF peptide in nude (ie hairless) mice.皺
Induced by 8 weeks of UVB irradiation following the procedure shown in Example 3.3 above. Mouse appearance, UVB
Before irradiation (normal), after UVB irradiation (UVB / UT), and after treatment with each ointment for 2 weeks (UVB / vehicle, UVB
/ 29-mer, UVB / 20-mer and UVB / 18-mer); representative photographs are provided in FIG.
図4に図示したように、マウスは、UVB照射後に、注目し得る量の深くて長い皺を呈した
(正常群、対、UVB/UT群)。ビヒクル-又は18-mer-含有軟膏で処置したマウスも、深くて長
い皺を有し、このことは、18-merは、UVB照射の結果として形成された皺を減らすことは
不可能であることを示唆している。対照的に、本PEDFペプチド(例えば、29-mer及び20-me
r)で処置したマウスは、UVB/UT群、UVB/ビヒクル群、及びUVB/18-mer群において認められ
たものよりも、皺の線が少なくより細い。
As illustrated in FIG. 4, mice exhibited a noticeable amount of deep and long wrinkles after UVB irradiation.
(Normal group, vs. UVB / UT group). Mice treated with vehicle- or 18-mer-containing ointments also have deep and long wrinkles, indicating that 18-mer cannot reduce wrinkles formed as a result of UVB irradiation It suggests. In contrast, the PEDF peptides (e.g. 29-mer and 20-me
Mice treated with r) have fewer wrinkle lines and are thinner than those observed in the UVB / UT, UVB / vehicle, and UVB / 18-mer groups.
皮膚標本を、マッソントリクローム染色に供し、それらのコラーゲン含量を概算し、且
つ代表的写真を図5に提供した(元の倍率、×200)。I型コラーゲン(COL1A1)のレベルも、
免疫ブロット分析により調べ、結果を、未処置の正常群のレベル(100%に設定)に対して
規準化した。定量結果を表8にまとめている。
** UVB/ビヒクル群に対し、P<0.001。
Skin specimens were subjected to Masson trichrome staining to approximate their collagen content and a representative photograph was provided in FIG. 5 (original magnification, × 200). The level of type I collagen (COL1A1)
Examined by immunoblot analysis, the results were normalized to the level of the untreated normal group (set to 100%). The quantitative results are summarized in Table 8.
** P <0.001 for UVB / vehicle group.
図5及び表8の両方を参照し、反復UVB照射(UVB/UT)は、未処置の正常群の正常マウスの
それと比べ、真皮におけるコラーゲンシグナル及びCOL1A1レベルを有意に減少したことが
わかる。対照的に、本PEDFペプチドの経真皮送達(例えば、UVB/29-mer群及びUVB/20-mer
群において)は、UVB/ビヒクル群のそれと比べ、真皮におけるコラーゲン及びCOL1ALの両
方のレベルを有意に増強した。これらの知見は、本PEDFペプチドの経真皮送達は、UVB-損
傷された真皮において、コラーゲン合成を誘導することができ、これは、本PEDFペプチド
により処置されたマウスにおける減少した皺形成により正当化され得ることを示唆してい
る。
With reference to both FIG. 5 and Table 8, it can be seen that repeated UVB irradiation (UVB / UT) significantly reduced collagen signal and COL1A1 levels in the dermis as compared to that of normal mice in the untreated normal group. In contrast, transdermal delivery of the PEDF peptide (e.g. UVB / 29-mer group and UVB / 20-mer
Group) significantly enhanced both collagen and COL1AL levels in the dermis compared to that of the UVB / vehicle group. These findings indicate that transdermal delivery of the PEDF peptide can induce collagen synthesis in UVB-damaged dermis, which is justified by reduced wing formation in mice treated with the PEDF peptide. Suggest that it can be.
本開示は、最初に、短い合成PEDFペプチドの経真皮送達は、皮膚老化に対する保護作用
を有することを明らかにしている。完全長PEDFペプチドを発現するベクターの静脈内又は
筋肉内送達と比べ、短い合成PEDFペプチドの経真皮送達は、安全で経費のかからない方策
である。
The present disclosure first reveals that transdermal delivery of short synthetic PEDF peptides has a protective effect against skin aging. Compared to intravenous or intramuscular delivery of vectors expressing full-length PEDF peptides, transdermal delivery of short synthetic PEDF peptides is a safe and inexpensive strategy.
実施態様の上記の説明は、例示目的でのみ与えられ、当分野の技術者によって様々な改変を行うことができることが理解されよう。上記の明細書、実施例、及びデータは、本発明の例示的な実施態様の構造及び使用の完全な説明を提供する。本発明の種々の実施態様を、ある程度の具体性を伴って、又は、1以上の個々の実施態様に関して先に記載してきたが、当分野の技術者は、本発明の精神及び範囲を逸脱せずに、開示した実施態様に対して多くの変更を行うことができるであろう。
本件出願は、以下の構成の発明を提供する。
(構成1)
長さ20〜39アミノ酸残基であり、且つ、配列番号:1と少なくとも80%のアミノ酸配列同一性を有するアミノ酸配列であって、配列番号:1の残基11〜30とのアミノ酸配列同一性が少なくとも90%である少なくとも20個の連続的な残基を含む前記アミノ酸配列からなる、対象における皮膚老化を予防及び/又は改善するための合成ペプチドの使用。
(構成2)
前記合成ペプチドの少なくとも4個の連続的な残基が、配列番号:1の残基11〜14と同一である、構成1記載の使用。
(構成3)
前記皮膚老化が、光老化である、構成1記載の使用。
(構成4)
前記対象が、ヒトである、構成1記載の使用。
(構成5)
構成1の合成ペプチドの有効量;及び
医薬として許容し得る賦形剤
を含む、対象における皮膚老化を予防及び/又は改善するための医薬組成物。
(構成6)
前記合成ペプチドの少なくとも4個の連続的な残基が、配列番号:1の残基11〜14と同一である、構成5記載の医薬組成物。
(構成7)
前記医薬組成物が、液剤、噴霧剤、エアゾール剤、泡剤、クリーム剤、ローション剤、軟膏、ゲル剤、又は貼付剤の形態である、構成5記載の医薬組成物。
(構成8)
浸透促進剤を更に含む、構成5記載の医薬組成物。
(構成9)
前記皮膚老化が、光老化である、構成5記載の医薬組成物。
(構成10)
前記対象が、ヒトである、構成5記載の医薬組成物。
(構成11)
対象における皮膚老化を予防及び/又は改善する方法であって、
構成1記載の合成ペプチドを対象の真皮へ経真皮送達することにより、該合成ペプチドの有効量を、該対象に投与することを含む、前記方法。
(構成12)
前記合成ペプチドの少なくとも4個の連続的な残基が、配列番号:1の残基11〜14と同一である、構成11記載の方法。
(構成13)
前記合成ペプチドが、前記合成ペプチドと医薬として許容し得る賦形剤とを含む医薬組成物に製剤化される、構成11記載の方法。
(構成14)
前記医薬組成物が、液剤、噴霧剤、エアゾール剤、泡剤、クリーム剤、ローション剤、軟膏、ゲル剤、又は貼付剤の形態である、構成13記載の方法。
(構成15)
前記医薬組成物が、対象の皮膚に局所的に投与される、構成13記載の方法。
(構成16)
前記医薬組成物の局所的投与の前、それと同時に、又はその後、対象の皮膚へ外部刺激を適用することをさらに含み、それにより前記合成ペプチドの経真皮送達が促進される、構成15記載の方法。
(構成17)
前記外部刺激が、機械的、電気的、熱的、超音波的、又は高周波的刺激である、構成16記載の方法。
(構成18)
前記医薬組成物が、浸透促進剤を更に含む、構成16記載の方法。
(構成19)
前記皮膚老化が、光老化である、構成11記載の方法。
(構成20)
前記対象が、ヒトである、構成11記載の方法。
It will be appreciated that the above description of the embodiments is given for illustrative purposes only and that various modifications can be made by those skilled in the art. The above specification, examples and data provide a complete description of the structure and use of exemplary embodiments of the invention. While various embodiments of the invention have been described above with some specificity or with respect to one or more individual embodiments, those skilled in the art will depart from the spirit and scope of the invention. Rather, many modifications may be made to the disclosed embodiments.
The present application provides an invention having the following configuration.
(Configuration 1)
Amino acid sequence that is 20-39 amino acid residues in length and has at least 80% amino acid sequence identity with SEQ ID NO: 1, and amino acid sequence identity with residues 11-30 of SEQ ID NO: 1 Use of a synthetic peptide for preventing and / or ameliorating skin aging in a subject consisting of said amino acid sequence comprising at least 20 consecutive residues, wherein is at least 90%.
(Configuration 2)
The use according to configuration 1, wherein at least 4 consecutive residues of the synthetic peptide are identical to residues 11-14 of SEQ ID NO: 1.
(Configuration 3)
The use according to configuration 1, wherein the skin aging is photoaging.
(Configuration 4)
The use according to configuration 1, wherein the subject is a human.
(Configuration 5)
An effective amount of the synthetic peptide of composition 1; and
Pharmaceutically acceptable excipient
A pharmaceutical composition for preventing and / or improving skin aging in a subject.
(Configuration 6)
The pharmaceutical composition according to configuration 5, wherein at least 4 consecutive residues of the synthetic peptide are the same as residues 11 to 14 of SEQ ID NO: 1.
(Configuration 7)
6. The pharmaceutical composition according to constitution 5, wherein the pharmaceutical composition is in the form of a liquid, a spray, an aerosol, a foam, a cream, a lotion, an ointment, a gel, or a patch.
(Configuration 8)
6. The pharmaceutical composition according to constitution 5, further comprising a penetration enhancer.
(Configuration 9)
6. The pharmaceutical composition according to constitution 5, wherein the skin aging is photoaging.
(Configuration 10)
6. The pharmaceutical composition according to constitution 5, wherein the subject is a human.
(Configuration 11)
A method for preventing and / or improving skin aging in a subject comprising:
The method comprising administering to the subject an effective amount of the synthetic peptide by transdermal delivery of the synthetic peptide of configuration 1 to the dermis of the subject.
(Configuration 12)
12. The method of configuration 11, wherein at least 4 consecutive residues of the synthetic peptide are identical to residues 11-14 of SEQ ID NO: 1.
(Configuration 13)
12. The method of configuration 11, wherein the synthetic peptide is formulated into a pharmaceutical composition comprising the synthetic peptide and a pharmaceutically acceptable excipient.
(Configuration 14)
14. The method according to configuration 13, wherein the pharmaceutical composition is in the form of a liquid, a spray, an aerosol, a foam, a cream, a lotion, an ointment, a gel, or a patch.
(Configuration 15)
14. The method of configuration 13, wherein the pharmaceutical composition is administered topically to the subject's skin.
(Configuration 16)
16. The method of configuration 15, further comprising applying an external stimulus to the skin of the subject prior to, simultaneously with, or after topical administration of the pharmaceutical composition, thereby facilitating transdermal delivery of the synthetic peptide. .
(Configuration 17)
The method of configuration 16, wherein the external stimulus is a mechanical, electrical, thermal, ultrasonic, or high frequency stimulus.
(Configuration 18)
The method of configuration 16, wherein the pharmaceutical composition further comprises a penetration enhancer.
(Configuration 19)
12. The method according to configuration 11, wherein the skin aging is photoaging.
(Configuration 20)
12. The method of configuration 11, wherein the subject is a human.
Claims (9)
該アミノ酸配列が、少なくとも配列番号: 3、配列番号: 5、配列番号: 6、 配列番号: 8 及び配列番号: 9の配列からなる群から選ばれたアミノ酸配列を含む、前記医薬組成物。 A pharmaceutical composition for preventing and / or improving skin aging in a subject comprising a synthetic peptide consisting of an amino acid sequence having a length of 20 to 29 amino acid residues,
The pharmaceutical composition, wherein the amino acid sequence comprises at least an amino acid sequence selected from the group consisting of SEQ ID NO: 3, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 8 and SEQ ID NO: 9.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017131741A JP6469767B2 (en) | 2017-07-05 | 2017-07-05 | Use of PEDF-derived polypeptides for preventing and / or improving skin aging |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017131741A JP6469767B2 (en) | 2017-07-05 | 2017-07-05 | Use of PEDF-derived polypeptides for preventing and / or improving skin aging |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015532263A Division JP6484174B2 (en) | 2012-09-19 | 2012-09-19 | Use of PEDF-derived polypeptides for preventing and / or improving skin aging |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2017222676A JP2017222676A (en) | 2017-12-21 |
| JP2017222676A5 JP2017222676A5 (en) | 2018-02-08 |
| JP6469767B2 true JP6469767B2 (en) | 2019-02-13 |
Family
ID=60687635
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017131741A Active JP6469767B2 (en) | 2017-07-05 | 2017-07-05 | Use of PEDF-derived polypeptides for preventing and / or improving skin aging |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6469767B2 (en) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2022138350A1 (en) * | 2020-12-23 | 2022-06-30 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1684692A2 (en) * | 2003-10-29 | 2006-08-02 | The Johns Hopkins University | Pigment epithelium-derived factor, novel biological activity and methods of use |
-
2017
- 2017-07-05 JP JP2017131741A patent/JP6469767B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2017222676A (en) | 2017-12-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6484174B2 (en) | Use of PEDF-derived polypeptides for preventing and / or improving skin aging | |
| Lahiji et al. | Transcutaneous implantation of valproic acid-encapsulated dissolving microneedles induces hair regrowth | |
| AU2013312120B2 (en) | Compositions and methods for treating cutaneous scarring | |
| US20200289541A1 (en) | Composition for ameliorating loss of hair and graying of hair, and use thereof | |
| Zhang et al. | Valproate promotes survival of retinal ganglion cells in a rat model of optic nerve crush | |
| JP2008530003A (en) | Use of a myostatin (GDF-8) antagonist for improving wound healing and for preventing fibrosis | |
| JP2023145532A (en) | Treatment of local skin hypotrophy conditions | |
| TWI353849B (en) | Methods and compositions for the promotion of hair | |
| Chung et al. | TGF-β-stimulated aberrant expression of class III β-tubulin via the ERK signaling pathway in cultured retinal pigment epithelial cells | |
| JP6469767B2 (en) | Use of PEDF-derived polypeptides for preventing and / or improving skin aging | |
| Werner et al. | Neural MMP‐28 expression precedes myelination during development and peripheral nerve repair | |
| US9351914B2 (en) | Methods for modulating hair growth using truncated laminin-511 | |
| CN104903345B (en) | Purposes of the polypeptide derived from PEDF in hair growth and/or hair decoloration | |
| JP5858482B2 (en) | Novel anti-aging peptides that modulate survivin and compositions containing the same | |
| WO2021241428A1 (en) | Elastin production promoter and cosmetic preparation for skin | |
| JP6522063B2 (en) | Use of PEDF-Derived Polypeptides for Treating Alopecia and / or Hair Depigmentation | |
| JP6324597B1 (en) | Melanin production inhibitor, whitening agent, gene expression inhibitor, cosmetic composition for inhibiting melanin production, and cosmetic composition for whitening | |
| Tsai et al. | Pigment epithelium‑derived factor short peptides facilitate full‑thickness cutaneous wound healing by promoting epithelial basal cell and hair follicle stem cell proliferation | |
| TWI449532B (en) | Use of pedf-derived polypeptides for preventing and/or ameliorating skin aging | |
| US11679178B2 (en) | Methods for improving mechanical properties of a tissue or for regenerating an injured or diseased tissue | |
| EP3900733A1 (en) | Src kinase activators and eng function inhibitors as enhancers of skin homeostasis/regeneration and hair growth | |
| US20230348913A1 (en) | Methods to re-engage a fetal wound healing pathway for adult skin repair | |
| No et al. | A Hair Growth-Enhancing Component of Hydrolysate of Human Placenta | |
| Zamiri | Towards a comprehensive resource for elucidating the pathogenesis of inherited keratodermas |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171222 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180717 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181015 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20181218 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190116 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6469767 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |