JP6280127B2 - 試薬材料および関連検査素子 - Google Patents
試薬材料および関連検査素子 Download PDFInfo
- Publication number
- JP6280127B2 JP6280127B2 JP2015540118A JP2015540118A JP6280127B2 JP 6280127 B2 JP6280127 B2 JP 6280127B2 JP 2015540118 A JP2015540118 A JP 2015540118A JP 2015540118 A JP2015540118 A JP 2015540118A JP 6280127 B2 JP6280127 B2 JP 6280127B2
- Authority
- JP
- Japan
- Prior art keywords
- case
- test element
- reagent material
- coenzyme
- glucose
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 *C1C(*)C(*)C(COP(*P(**[n+]2cc(*)ccc2)([U])=*)([U])=*)*1 Chemical compound *C1C(*)C(*)C(COP(*P(**[n+]2cc(*)ccc2)([U])=*)([U])=*)*1 0.000 description 7
- DGPLSUKWXXSBCU-UHFFFAOYSA-N NC(c1ccc[n+](C(CC(COP([O-])(OP(O)(OCC(C(C2O)O)OC2[n]2c3ncnc(N)c3nc2)=O)=O)C2O)C2O)c1)=O Chemical compound NC(c1ccc[n+](C(CC(COP([O-])(OP(O)(OCC(C(C2O)O)OC2[n]2c3ncnc(N)c3nc2)=O)=O)C2O)C2O)c1)=O DGPLSUKWXXSBCU-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/54—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving glucose or galactose
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/001—Enzyme electrodes
- C12Q1/005—Enzyme electrodes involving specific analytes or enzymes
- C12Q1/006—Enzyme electrodes involving specific analytes or enzymes for glucose
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- General Engineering & Computer Science (AREA)
- Immunology (AREA)
- Physics & Mathematics (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Analytical Chemistry (AREA)
- Biophysics (AREA)
- Emergency Medicine (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Biomedical Technology (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Hematology (AREA)
- Medicinal Chemistry (AREA)
- Urology & Nephrology (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Saccharide Compounds (AREA)
- Enzymes And Modification Thereof (AREA)
- Pathology (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Diabetes (AREA)
- Cell Biology (AREA)
Description
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型、からなる群から選択される補酵素を含む。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
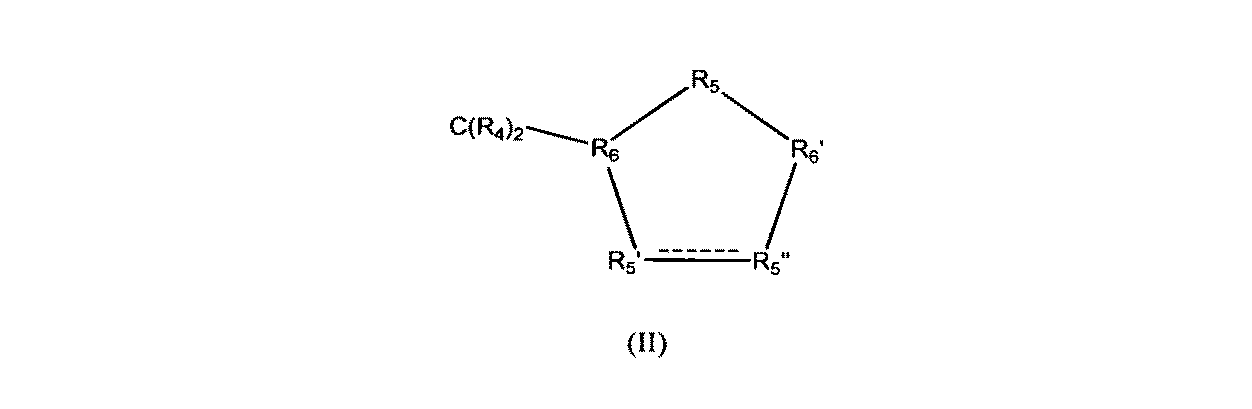
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である。
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の補酵素化合物と、
又は、その塩もしくは任意にその還元型と、を含む。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の飽和炭素環式5員環を表わす]に従う。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の飽和炭素環式5員環を表わす]に従う。
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型、とからなる群から選択される補酵素を含む。
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型、からなる群から選択される補酵素、を含む前記検査素子を設けること;
前記検査素子に試料を接触させること;第1の分析物を検出すること;及び第2の分析物を検出すること、を含む。
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型からなる群から選択される補酵素、を含む。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である。
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型を含む。
Z上の典型的な置換基は、OH、F、Cl、及びC1〜C2アルキルからなる群から選択され、これらは任意にフッ素化又は塩素化及び/又はOH置換されたO−C1〜C2アルキルである。
[式中、
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2(ここで、RはHを表わす)を表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす)]の化合物は、カルバNAD又はcNADである。
[式中、
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし、
Wは、CON(R)2(ここで、RはHを表わす)を表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす)]の化合物は、カルバNADP又はcNADPである。
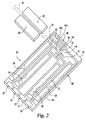
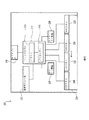
ある実施態様において、試薬材料60、120は、ヒドロキシ酪酸塩の存在及び/又は濃度の検出を促進するように動作可能である場合、試薬材料62、122は、グルコースの存在及び/又は濃度の検出を促進するように動作可能であり、グルコースに対する酵素を含む。ある具体的な形態において、この酵素は、グルコース脱水素酵素又はグルコースオキシダーゼである。この実施態様において、試薬材料62、122はさらに、FAD、NAD、NADP、及び式(I)の化合物又はその塩もしくは任意にその還元型を更に含む。従前に議論されたことはないが、試薬材料60および62は、共通の補酵素、例えば、式(I)の化合物又はその塩もしくは任意にその還元型、を有し、それらの間のスペース64が排除されるように一緒に併合されて単一試薬層を形成する形態も企図される。また、グルコースの存在および/または濃度を検出するための本明細書に記載されている試薬材料は限定的ではなく、他の形態も当分野で知られていることを理解すべきである。グルコースの存在及び/又は濃度の検出するように動作可能な試薬材料の追加的な非限定例は、米国特許第7,727,467号(上述)及び米国特許第8,008,037号に開示されており、これらの内容は、参照することによりその全体が本明細書に組み込まれる。第2の試薬素材は、メディエーターを含むこともできる。メディエーターは、検出可能な電子活性反応生成物を生成するために、第2の酵素、第2の分析物、補酵素、及びその反応生成物が関与する反応スキームに参加することができる任意の化学種(一般的に電子活性)として選択することができる。典型的には、反応中のメディエーターの関与は、第2の分析物、第2の酵素、又は補酵素、又はこれらの1つの反応生成物である分子種(例えば、異なる酸化状態に反応した補酵素)との相互作用による酸化状態の変化(例えば、還元)を伴う。種々のメディエーターが、適切な電気化学的挙動を示す。メディエーターは好ましくは、その酸化型でも非常に安定しており、任意に可逆的な酸化還元的電気化学を示し、好ましくは水溶液中で良好な溶解性を示すことができ、好ましくは急速に反応して電気活性な反応生成物を生成することができる。メディエーターの例としては、ベンゾキノン、メルドラブルー、遷移金属錯体、例えばフェリシアン化カリウム及びオスミウム誘導体(国際公開WO98/35225号パンフレットを参照)、及びフェナジン誘導体とヘキサンアミンルテニウムクロリド(米国特許第8,008,037号を参照)を含む。第2の試薬材料はまた、メディエーター前駆体として作用するニトロソアニリン系化合物を含んでよい(例えば、米国特許第5,286,362号を参照)。この点でニトロソアニリン系メディエーター前駆体は、血液などの分析物試料と接触すると、可逆的メディエーター成分に分解する。
図6の試薬材料
7.344gのMOPSナトリウム塩、0.125gのトリトン(登録商標)X−100(Sigma-Aldrich Corporation, St. Louis, MOの非イオン性界面活性剤)、2.400gのトレハロース、及び2.026gのコハク酸ナトリウム六水和物を、400mLの2回蒸留水に加え、溶液のpHを8.14に調整することにより、ストック緩衝液を調製した。この溶液を500mLのメスフラスコに加え、2回蒸留水で希釈して500mLの溶液を作成した。
9.086gのトリス塩基、0.125gのトリトン(登録商標)X−100、0.625gのタージトール(登録商標)15−S−9(The Dow Chemical Company, Midland, MIからの非イオン性界面活性剤)、2.400gのトレハロース、及び2.026gのコハク酸ナトリウム六水和物を、400mLの2回蒸留水に加え、溶液のpHを7.95に調整することにより、ストック緩衝液を調製した。この溶液を500mLのメスフラスコに加え、2回蒸留水で希釈して500mLの溶液を作成した。
図7の試薬材料に関連して上記した4.048gのトリス緩衝液/PEO/ナトロゾール(登録商標)ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ヘキサアミンルテニウム/カルバNAD試薬材料を調製した:a)0.062gの塩化ヘキサアミンルテニウムとb)0.003gの1−(3−カルボキシプロピルオキシ)−5−エチルフェナジンをカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.9に調整した;c)3mLのヘキサアミンルテニウム/フェナジン溶液を含有する10mLスピード混合カップに0.079gのカルバNAD遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.24にした。次にアルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素を容器に加え、24,000rpmで2分間スピード混合した。
9.086gのトリス塩基、0.125gのトリトン(登録商標)X−100、0.625gのタージトール(登録商標)15−S−9、2.40gのトレハロース、及び2.026gのコハク酸ナトリウム六水和物を、400mLの2回蒸留水に加え、溶液のpHを7.95に調整することにより、ストック緩衝液を調製した。この溶液を500mLのメスフラスコに加え、2回蒸留水で希釈して500mLの溶液を作成した。
図10の試薬材料に関連して上記した4.049gのトリス/コリドン(登録商標)緩衝ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ヘキサアミンルテニウム/カルバNAD試薬材料を調製した:a)0.040gの未処理ヒュームドシリカ(カボシル、Cabot Corporation, Boston, MA)、b)0.062gの塩化ヘキサアミンルテニウムとc)0.003gの1−(3−カルボキシプロピルオキシ)−5−エチルフェナジンをカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.9に調整した;d)3mLのヘキサアミンルテニウム/フェナジン溶液を含有する10mLスピード混合カップに0.079gのカルバNAD遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及びe)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
図10の試薬材料に関連して上記した6.074gのトリス/コリドン(登録商標)緩衝ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ニトロソアニリン/カルバNAD試薬材料を調製した:a)0.060gの未処理ヒュームドシリカ(カボシル(登録商標)、Cabot Corporation, Boston, MA)とb)0.050gの置換ニトロソアニリン誘導体(Roche Diagnostics, Inc.により供給されるNA1144)をこのカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.8に調整した;c)3mLのニトロソアニリン溶液を含有する10mLスピード混合カップに0.069gのカルバNAD遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及び、e)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
図10の試薬材料に関連して上記した6.074gのトリス/コリドン(登録商標)緩衝ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ヘキサアミンルテニウム/チオNAD試薬材料を調製した:a)0.060gの未処理ヒュームドシリカ(カボシル、Cabot Corporation, Boston, MA)、b)0.093gの塩化ヘキサアミンルテニウムとc)0.005gの1−(3−カルボキシプロピルオキシ)−5−エチルフェナジンをカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.9に調整した;d)3mLのヘキサアミンルテニウム/フェナジン溶液を含有する10mLスピード混合カップに0.079gのカルバNAD遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及びe)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
図10の試薬材料に関連して上記した6.074gのトリス/コリドン(登録商標)緩衝ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ニトロソアニリン/チオNAD試薬材料を調製した:a)0.060gの未処理ヒュームドシリカ(カボシル(登録商標)、Cabot Corporation, Boston, MA)とb)0.050gの置換ニトロソアニリン誘導体(Roche Diagnostics, Inc., Indianapolis, INにより供給されるNA1144)をこのカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.8に調整した;c)3mLのニトロソアニリン溶液を含有する10mLスピード混合カップに0.079gのチオNAD遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及び、d)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
図10の試薬材料に関連して上記した6.074gのトリス/コリドン(登録商標)緩衝ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ヘキサアミンルテニウム/カルバNADP試薬材料を調製した:a)0.060gの未処理ヒュームドシリカ(カボシル、Cabot Corporation, Boston, MA)、b)0.093gの塩化ヘキサアミンルテニウムとc)0.005gの1−(3−カルボキシプロピルオキシ)−5−エチルフェナジンをカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.9に調整した;c)3mLのヘキサアミンルテニウム/フェナジン溶液を含有する10mLスピード混合カップに0.076gのカルバNADP遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及びd)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
図10の試薬材料に関連して上記した6.074gのトリス/コリドン(登録商標)緩衝液/ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ニトロソアニリン/カルバNADP試薬材料を調製した:a)0.060gの未処理ヒュームドシリカ(カボシル、Cabot Corporation, Boston, MA)、b)0.050gの置換ニトロソアニリン誘導体(Roche Diagnostics, Inc., Indianapolis, INにより供給されるNA1144)をこのカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.8に調整した;c)3mLのニトロソアニリン溶液を含有する10mLスピード混合カップに0.076gのカルバNADP遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及び、d)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
図10の試薬材料に関連して上記した4.049gのトリス/コリドン(登録商標)緩衝液/ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、フェリシアニド/カルバNAD試薬材料を調製した:a)0.040gの未処理ヒュームドシリカ(カボシル、Cabot Corporation, Boston, MA)とb)0.026gのフェリシアン化カリウムをカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.8に調整した;c)3mLのフェリシアニド溶液を含有する10mLスピード混合カップに0.076gのカルバNAD遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及びd)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
図10の試薬材料に関連して上記した6.074gのトリス/コリドン(登録商標)緩衝液/ポリマーストック溶液を含有する20mLスピード混合カップに、以下の成分を連続して加えることにより、ニトロソアニリン/カルバNAD試薬材料を調製した:a)0.060gの未処理ヒュームドシリカ(カボシル(登録商標)、Cabot Corporation, Boston, MA)とb)0.050gの置換ニトロソアニリン誘導体(Roche Diagnostics, Inc.により供給されるNA1144)をこのカップに加え、このマトリックスを24,000rpmで1分間混合し、pHを7.8に調整した;c)3mLのニトロソアニリン溶液を含有する10mLスピード混合カップに0.079gのカルバNAD遊離酸を加え、マトリックスを24,000rpmで1分間混合し、pHを7.2に調整した;及び、e)アルカリゲネス・フェカリス(alcaligenes faecalis)からの0.259gのベータヒドロキシ酪酸脱水素酵素をカップに加え、24,000rpmで2分間スピード混合した。
スペーサーと毛細管デザインを有するACCU-CHECK(登録商標)Avivaブランド電極のカードを使用して、検査ストリップを作製した。上記した1.5μLの試薬材料を、PixSys(登録商標)SQシリーズ分注システム(Cartesian Technologies Irvine California)を用いて、各電極のキャピラリーチャネルに分注し、45℃で1.5分間乾燥した。乾燥したカードを乾燥雰囲気中で一晩保存し、親水性のトップホイルのストリップを、用手的に毛細血管上のスペーサ層上に積層した。次に、カードを個々のセンサーに切断し、使用するまで乾燥バイアル中で保存した。
0.1829gのリン酸カリウム一塩基性塩、0.2007gのリン酸カリウム二塩基性塩、及び2.7956gの塩化カリウムを、200mLの2回蒸留水に加え、溶液のpHを7.00に調整することにより、リン酸生理食塩水緩衝液のストック溶液を調製した。この溶液を250mLのメスフラスコに加え、2回蒸留水で希釈して250mLの溶液を作成した。
種々のレベルのヒドロキシ酪酸塩(mM)を含有する全血又は食塩水試料を、上記で調製した検査ストリップを使用して測定した。ストリップ上の試料に接触後、必要な電圧(ヘキサンアミンルテニウムストリップについては222mV、ニトロソアニリンストリップについては450mV)を印加した。総アッセイ時間は6秒であった。アッセイのためのエンドポイントは、検査ストリップに試料を接触させた後、0.5秒(図7)及び5秒(図9及び10)とした。
種々のレベルのヒドロキシ酪酸塩(0〜10mM)を含有する全血又は食塩水試料を、上記で調製した検査ストリップを使用して測定した。アッセイは、試料が検査ストリップに接触後の4.5秒の遅延と、この遅延期間後6秒間の電圧印加(ニトロソアニリンストリップについては450mV,ヘキサンアミンルテニウムストリップについては222mV)から構成されていた。アッセイのためのエンドポイントは、検査ストリップに試料を接触させた後、5秒とした。
第1の補酵素依存性酵素又は前記第1の酵素用の基質と、
第2の補酵素依存性酵素又は前記第2の酵素用の基質と、
チオNAD、チオNADP、及び式(I):
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型、からなる群から選択される補酵素と、
を含む上記検査素子。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である、上記検査素子。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である、上記検査素子。
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の補酵素化合物、
又は、その塩もしくは任意にその還元型と、を含む上記試薬材料。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の飽和炭素環式5員環を表わす]に従う、上記試薬材料。
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の飽和炭素環式5員環を表わす]に従う、上記試薬材料。
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42(CR42は前記環状基とX2に結合している)を含む、5個の炭素原子を有する環状基を含む残基を表わし、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型、とからなる群から選択される補酵素をさらに含む、上記検査素子。
実施態様1の検査素子を設ける工程と、
前記検査素子に前記試料を接触させる工程と、
前記第1の分析物を検出する工程と、
前記第2の分析物を検出する工程と、を含む上記方法。
前記検査素子に試料を接触させる工程と;
前記検査素子に試料を接触後7.5秒以内に試料中のグルコース値とケトン値とを測定する工程と、を含む方法。
Claims (30)
- 第1及び第2分析物を測定するために構成された検査素子であって、
第1の補酵素依存性酵素
(ここで、前記第1分析物がヒドロキシ酪酸塩であり、前記第1の補酵素依存性酵素がヒドロキシ酪酸脱水素酵素である)と、
第2の補酵素依存性酵素
(ここで、前記第2分析物がグルコースであり、前記第2の補酵素依存性酵素がグルコース脱水素酵素又はグルコースオキシダーゼである)と、
チオNAD、チオNADP、及び式(I):
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42を含む、5個の炭素原子を有する環状基を含む残基を表わし(ここで、CR42は前記環状基とX2に結合している)、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型、からなる群から選択される補酵素と、
を含む上記検査素子。 - 前記ヒドロキシ酪酸脱水素酵素が3−ヒドロキシ酪酸脱水素酵素である、請求項1に記載の検査素子。
- 請求項1に記載の検査素子であって、前記補酵素は式(I):
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である、上記検査素子。 - 請求項1に記載の検査素子であって、前記補酵素は式(I):
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である、上記検査素子。 - 前記補酵素がチオNADである、請求項1に記載の検査素子。
- 前記補酵素がチオNADPである、請求項1に記載の検査素子。
- 請求項1に記載の検査素子であって、前記第1の酵素と、チオNAD、チオNADP、及び式(I)の化合物又はその塩もしくは任意にその還元型からなる群から選択される前記補酵素は、第1の試薬材料に含まれる、上記検査素子。
- 請求項7に記載の検査素子であって、前記第2の酵素と、式(I)の化合物又はその塩もしくは任意にその還元型からなる群から選択される前記補酵素は、第2の試薬材料に含まれる、上記検査素子。
- 前記検査素子は、前記第1及び第2の試薬材料を担持するように構成された検査ストリップである、請求項8に記載の検査素子。
- 前記検査ストリップが、前記第1の試薬材料に関する第1の電極系と、前記第2の試薬材料に関する第2の電極系とを含む、請求項9に記載の検査素子。
- 前記第2の試薬材料は、FAD、NAD、又はNADPを更に含む、請求項8に記載の検査素子。
- 前記第1の試薬材料が、ニトロソアニリン、フェリシアン化カリウム、及びフェナジン化合物と塩化ヘキサアミンルテニウムとの組み合わせ、の1つをさらに含む、請求項7に記載の検査素子。
- ヒドロキシ酪酸塩を測定するための試薬材料であって、
3−ヒドロキシ酪酸脱水素酵素と、
式(I):
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42を含む、5個の炭素原子を有する環状基を含む残基を表わし(ここで、CR42は前記環状基とX2に結合している)、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の補酵素化合物、
又は、その塩もしくは任意にその還元型と、を含む上記試薬材料。 - 請求項13に記載の試薬材料であって、前記補酵素化合物が、式(I):
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の飽和炭素環式5員環を表わす]に従う、上記試薬材料。 - 請求項13に記載の試薬材料であって、前記補酵素化合物が、式(I):
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の飽和炭素環式5員環を表わす]に従う、上記試薬材料。 - ニトロソアニリン、フェリシアン化カリウム、及びフェナジン化合物と塩化ヘキサアミンルテニウムとの組み合わせ、の1つをさらに含む、請求項13に記載の試薬材料。
- 第1分析物を測定するための、請求項13に記載の第1の試薬材料を担持する検査ストリップを含む検査素子であって、
ここで、上記第1分析物はヒドロキシ酪酸塩である、上記検査素子。 - 前記検査ストリップが、第2分析物を測定するための第2の試薬材料をさらに担持する、請求項17に記載の検査素子であって、
ここで、上記第2分析物はグルコースである、上記検査素子。 - 前記第2の試薬材料が、グルコース脱水素酵素又はグルコースオキシダーゼを含む、請求項18に記載の検査素子。
- 請求項19に記載の検査素子であって、前記第2の試薬材料が、FAD、NAD、NADP、及び式(I):
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42を含む、5個の炭素原子を有する環状基を含む残基を表わし(ここで、CR42は前記環状基とX2に結合している)、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]の化合物、
又は、その塩もしくは任意にその還元型、とからなる群から選択される補酵素をさらに含む、上記検査素子。 - 前記検査ストリップが、前記第1及び第2分析物を電気化学的に測定するために構成されている、請求項18に記載の検査素子。
- 試料中のグルコース値及びケトン値を測定するための方法であって、
試料中のグルコース値とケトン値とを電気化学的に測定するように構成された、検査素子を設ける工程と、
前記検査素子に該試料を接触させる工程と、
ここで、前記検査素子は、
ケトン値を決定するための第1の補酵素依存型酵素と、チオNAD、チオNADP、及び式(I)の化合物からなる群から選択される少なくとも1つの第1試薬材料補酵素とを含む第1試薬材料(ここで、第1試薬材料は、前記検査素子の第1の電極システムと関連する)と、
グルコース値を決定するための第2の補酵素依存型酵素と、FAD、NAD、NADP、チオNAD、チオNADP、及び式(I)の化合物からなる群から選択される少なくとも1つの第2試薬材料補酵素とを含む第2試薬材料(ここで、第2試薬材料は、前記検査素子の第2の電極システムと関連する)とを含み、 ここで、式(I)の化合物は、以下の通りである:
Aは、アデニン又はその類似体を表わし、
Tは、各場合に独立してO又はSを表わし、
Uは、各場合に独立してOH、SH、BH3 -、又はBCNH2 -を表わし、
Vは、各場合に独立してOH又はリン酸基を表わし、
Wは、COOR、CON(R)2、COR、又はCSN(R)2を表わし、ここで、Rは各場合に独立してH又はC1〜C2アルキルを表わし、
X1、X2は、各場合に独立してO、CH2、CHCH3、C(CH3)2、NH、又はNCH3を表わし、
Yは、NH、S、O、又はCH2を表わし、
Zは、O、S及びNから選択されるヘテロ原子を任意に含み、1つ又はそれ以上の置換基を任意に含み、及び残基CR42を含む、5個の炭素原子を有する環状基を含む残基を表わし(ここで、CR42は前記環状基とX2に結合している)、
ここで、R4は、各場合に独立してH、F、Cl、又CH3を表わすが、但し、Zとピリジン残基はグリコシド結合により連結されていない]、
又は、その塩もしくは任意にその還元型;
第1および第2の電極システムに電位を与え、その電位に対する反応を測定する工程、並びに
測定した反応より、該検査素子に試料を接触後7.5秒以内に試料中のグルコース値とケトン値とを測定する工程と、を含む上記方法。 - 前記第1の補酵素依存型酵素がヒドロキシ酪酸脱水素酵素であり、前記第2の補酵素依存型酵素がグルコース脱水素酵素又はグルコースオキシダーゼである、請求項22に記載の方法。
- 前記試料中のグルコース値とケトン値とを測定する工程が、検査素子に試料を接触後5秒以内に完了する、請求項22に記載の方法。
- 前記測定工程中に、グルコース値とケトン値は、互いに2秒以内に測定される、請求項22に記載の方法。
- 前記試料が血液を含む、請求項22に記載の方法。
- 前記ヒドロキシ酪酸脱水素酵素は3−ヒドロキシ酪酸脱水素酵素である、請求項23に記載の方法。
- 前記少なくとも1つの第1試薬材料補酵素および前記少なくとも1つの第2試薬材料補酵素は、式(I):
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、各場合にOHを表わし、
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である、請求項22に記載の方法。 - 前記少なくとも1つの第1試薬材料補酵素および前記少なくとも1つの第2試薬材料補酵素は、式(I):
Aは、アデニンを表わし、
Tは、各場合にOを表わし、
Uは、各場合にOHを表わし、
Vは、第1の場合にOHを表わし、第2の場合にリン酸基を表わし
Wは、CON(R)2を表わし、ここでRはHを表わし、
X1は、Oを表わし、
X2は、Oを表わし、
Yは、Oを表わし、そして
Zは、一般式(II)
R4は、Hを表わし、
R5’は、CHOHを表わし、
R5”は、CHOHを表わし、
R5は、CR42を表わし、
R6は、CHを表わし、そして
R6’は、CHを表わす)の炭素環式5員環を表わす]の化合物である、請求項22に記載の方法。 - 前記第1試薬材料が、ニトロソアニリン、フェリシアン化カリウム、及びフェナジン化合物と塩化ヘキサアミンルテニウムとの組み合わせからなる群から選択されるメディエーターをさらに含む、請求項22に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US13/667,057 US8921061B2 (en) | 2012-11-02 | 2012-11-02 | Reagent materials and associated test elements |
| US13/667,057 | 2012-11-02 | ||
| PCT/EP2013/072754 WO2014068022A1 (en) | 2012-11-02 | 2013-10-31 | Reagent materials and associated test elements |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016232405A Division JP6313407B2 (ja) | 2012-11-02 | 2016-11-30 | 試薬材料および関連検査素子 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2015536138A JP2015536138A (ja) | 2015-12-21 |
| JP2015536138A5 JP2015536138A5 (ja) | 2017-12-14 |
| JP6280127B2 true JP6280127B2 (ja) | 2018-02-14 |
Family
ID=49518949
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015540118A Expired - Fee Related JP6280127B2 (ja) | 2012-11-02 | 2013-10-31 | 試薬材料および関連検査素子 |
| JP2016232405A Expired - Fee Related JP6313407B2 (ja) | 2012-11-02 | 2016-11-30 | 試薬材料および関連検査素子 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016232405A Expired - Fee Related JP6313407B2 (ja) | 2012-11-02 | 2016-11-30 | 試薬材料および関連検査素子 |
Country Status (18)
| Country | Link |
|---|---|
| US (2) | US8921061B2 (ja) |
| EP (1) | EP2914735B1 (ja) |
| JP (2) | JP6280127B2 (ja) |
| KR (1) | KR101730281B1 (ja) |
| CN (5) | CN108802397A (ja) |
| AU (1) | AU2013340841B2 (ja) |
| BR (1) | BR112015009901A2 (ja) |
| CA (1) | CA2886162C (ja) |
| ES (1) | ES2707872T3 (ja) |
| HK (1) | HK1211627A1 (ja) |
| IL (1) | IL238077B (ja) |
| MX (1) | MX359319B (ja) |
| NZ (2) | NZ745469A (ja) |
| PL (1) | PL2914735T3 (ja) |
| RU (1) | RU2652888C2 (ja) |
| SG (1) | SG11201503344SA (ja) |
| WO (1) | WO2014068022A1 (ja) |
| ZA (1) | ZA201502999B (ja) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10898116B2 (en) | 2013-03-15 | 2021-01-26 | Cambridge Medical Technologies LLC | Methods of manufacture to optimize performance of transdermal sampling and analysis device |
| WO2016161430A1 (en) * | 2015-04-02 | 2016-10-06 | President And Fellows Of Harvard College | Three-dimensional microfluidic devices with pop-up feature |
| CN107533028A (zh) * | 2015-05-07 | 2018-01-02 | 聚合物技术系统公司 | 用于电化学酮检测和测量的系统和方法 |
| ES2974312T3 (es) | 2016-03-04 | 2024-06-26 | Abbott Diabetes Care Inc | Enzimas sensibles dependientes de NAD(P), electrodos y sensores y procedimientos para la fabricación y utilización de los mismos |
| CA3035874C (en) * | 2016-10-05 | 2025-09-09 | F. Hoffmann-La Roche Ag | DETECTION REAGENTS AND ELECTRODE ARRANGEMENTS FOR MULTI-ANALYTICAL DIAGNOSTIC TEST ELEMENTS, AS WELL AS THEIR METHODS OF USE |
| CN110383064B (zh) | 2016-10-24 | 2021-06-29 | 豪夫迈·罗氏有限公司 | 校正生物传感器的导电元件中的无补偿电阻的方法以及装置和系统 |
| CN107505368B8 (zh) * | 2017-07-21 | 2019-08-23 | 山东朱氏药业集团有限公司 | 一种血糖试纸 |
| CN111758032A (zh) * | 2018-02-23 | 2020-10-09 | 希森美康株式会社 | 尿中酮体检测用试验片 |
| DK3917396T3 (da) * | 2019-01-28 | 2024-12-02 | Abbott Diabetes Care Inc | Analytsensorer, der er forsynet med dualdetektering af glukose og ketoner |
| EP4552565A1 (en) | 2019-01-28 | 2025-05-14 | Abbott Diabetes Care, Inc. | Analyte sensors and sensing methods for dual detection of glucose and ethanol |
| EP4663121A1 (en) | 2019-01-28 | 2025-12-17 | Abbott Diabetes Care Inc. | Analyte sensors employing multiple enzymes |
| US11633129B2 (en) | 2019-04-05 | 2023-04-25 | Cambridge Medical Technologies LLC | Non-invasive transdermal sampling and analysis device incorporating redox cofactors |
| US11375931B2 (en) | 2019-08-08 | 2022-07-05 | Cambridge Medical Technologies LLC | Non-invasive transdermal sampling and analysis device incorporating an electrochemical bioassay |
| WO2021138473A1 (en) | 2020-01-03 | 2021-07-08 | Abbott Diabetes Care Inc. | Sensor array systems and methods for detecting multiple analytes |
| US20210267501A1 (en) * | 2020-02-27 | 2021-09-02 | Cambridge Medical Technologies LLC | Non-Invasive Transdermal Sampling and Analysis Device for Detection of Multiple Analytes |
| US11808708B2 (en) | 2020-08-12 | 2023-11-07 | F.A.T. Stats LLC | Method for maintaining the health of a diabetic patient by preventing the occurrence of diabetic ketoacidosis |
| CN114858886A (zh) * | 2021-02-03 | 2022-08-05 | 南京晶捷生物科技有限公司 | 一种电化学生物传感器 |
| IN202311040216A (ja) * | 2023-06-13 | 2023-07-21 | ||
| IN202311040523A (ja) * | 2023-06-14 | 2023-07-28 | ||
| WO2025224173A1 (en) | 2024-04-23 | 2025-10-30 | Directsens Gmbh | Enzymatic assessment of glucose metabolic disorders |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4397956A (en) | 1981-12-10 | 1983-08-09 | Maggio Edward T | Means for monitoring the status of control of ketoacidosis-prone diabetics |
| US5071769A (en) | 1986-12-22 | 1991-12-10 | Abbott Laboratories | Method and device for ketone measurement |
| US5633143A (en) | 1991-12-12 | 1997-05-27 | Asahi Kasei Kogyo Kabushiki Kaisha | Method for the quantitative determination of D-3-hydroxybutyric acid and acetoacetic acid, and analytical reagent therefor |
| CO5040209A1 (es) | 1997-10-16 | 2001-05-29 | Abbott Lab | Electrodos biosensores mediadores de la regeneracion de cofactores |
| EP1801229B1 (en) | 1997-10-16 | 2010-09-01 | Abbott Laboratories | Biosensor electrode |
| US6736957B1 (en) | 1997-10-16 | 2004-05-18 | Abbott Laboratories | Biosensor electrode mediators for regeneration of cofactors and process for using |
| GB2337122B (en) | 1998-05-08 | 2002-11-13 | Medisense Inc | Test strip |
| US5902731A (en) * | 1998-09-28 | 1999-05-11 | Lifescan, Inc. | Diagnostics based on tetrazolium compounds |
| US6380380B1 (en) * | 1999-01-04 | 2002-04-30 | Specialty Assays, Inc. | Use of nicotinamide adenine dinucleotide (NAD) and nicotinamide adenine dinucliotide phosphate (NADP) analogs to measure enzyme activities metabolites and substrates |
| US6541216B1 (en) | 1999-12-22 | 2003-04-01 | Roche Diagnostics Corporation | Amperometric biosensor test strip |
| CA2404421A1 (en) | 2000-03-28 | 2001-10-04 | Tianmei Ouyang | Reagent systems for detecting the presence of a reduced cofactor in a sample and methods for using the same |
| US7758744B2 (en) | 2001-10-05 | 2010-07-20 | Stephen Eliot Zweig | Dual glucose-turbidimetric analytical sensors |
| US6984307B2 (en) | 2001-10-05 | 2006-01-10 | Stephen Eliot Zweig | Dual glucose-hydroxybutyrate analytical sensors |
| US6762035B1 (en) | 2002-02-04 | 2004-07-13 | Surendra K. Gupta | Method and test strips for the measurement of fat loss during weight loss programs |
| US7501053B2 (en) | 2002-10-23 | 2009-03-10 | Abbott Laboratories | Biosensor having improved hematocrit and oxygen biases |
| US20040118704A1 (en) | 2002-12-19 | 2004-06-24 | Yi Wang | Analyte test intrument having improved versatility |
| TR201810169T4 (tr) | 2003-06-20 | 2018-08-27 | Hoffmann La Roche | Dar, homojen belirteç şeritlerinin üretilmesi için yöntem ve belirteç. |
| US7553615B2 (en) | 2005-07-28 | 2009-06-30 | Roche Diagnostics Operations, Inc. | Compounds, methods, complexes, apparatuses and uses relating to stabile forms of NAD/NADH |
| DE102005035461A1 (de) | 2005-07-28 | 2007-02-15 | Roche Diagnostics Gmbh | Stabile NAD/NADH-Derivate |
| EP2093284A1 (de) * | 2008-02-19 | 2009-08-26 | F.Hoffmann-La Roche Ag | Stabilisierung von Dehydrogenasen mit stabilen Coenzymen |
| US8008037B2 (en) | 2008-03-27 | 2011-08-30 | Roche Diagnostics Operations, Inc. | Matrix composition with alkylphenazine quaternary salt and a nitrosoaniline |
| US8500990B2 (en) | 2009-04-22 | 2013-08-06 | Nova Biomedical Corporation | Electrochemical biosensors based on NAD(P)-dependent dehydrogenase enzymes |
| EP2287605A1 (de) * | 2009-08-20 | 2011-02-23 | Roche Diagnostics GmbH | Vereinfachte Magazinierung integrierter Systeme |
| EP2292751A1 (de) * | 2009-08-20 | 2011-03-09 | Roche Diagnostics GmbH | Stabilisierung von Enzymen mit stabilen Coenzymen |
| US20110048972A1 (en) * | 2009-08-31 | 2011-03-03 | Lifescan Scotland Limited | Multi-analyte test strip with shared counter/reference electrode and inline electrode configuration |
| US20110079522A1 (en) | 2009-10-02 | 2011-04-07 | Lifescan Scotland Limited | Multi-analyte test strip with inline working electrodes and shared opposing counter/reference electrode |
| US8323467B2 (en) | 2009-10-27 | 2012-12-04 | Lifescan Scotland Limited | Dual chamber, multi-analyte test strip with opposing electrodes |
| US8632664B2 (en) | 2009-10-27 | 2014-01-21 | Lifescan Scotland Limited | Test meter for use with a dual chamber, multi-analyte test strip with opposing electrodes |
| EP2333544A1 (de) * | 2009-12-11 | 2011-06-15 | F. Hoffmann-La Roche AG | Sterilisierbare Chemie für Testelemente |
| IL209760A (en) * | 2009-12-11 | 2015-05-31 | Lifescan Scotland Ltd | A system and method for measuring filling is satisfactory |
| EP2513648B1 (de) * | 2009-12-16 | 2015-05-27 | F.Hoffmann-La Roche Ag | Detektion der zersetzung von enzymen in einem testelement durch kontrollierte freisetzung von geschütztem analyt |
| WO2012003306A1 (en) | 2010-06-30 | 2012-01-05 | Roche Diagnostics Operations, Inc. | Methods for manufacturing a dual biosensor test strip |
-
2012
- 2012-11-02 US US13/667,057 patent/US8921061B2/en not_active Expired - Fee Related
-
2013
- 2013-10-31 CN CN201810737277.0A patent/CN108802397A/zh active Pending
- 2013-10-31 CN CN201380057254.0A patent/CN104736717A/zh active Pending
- 2013-10-31 MX MX2015004980A patent/MX359319B/es active IP Right Grant
- 2013-10-31 SG SG11201503344SA patent/SG11201503344SA/en unknown
- 2013-10-31 HK HK15112488.7A patent/HK1211627A1/xx unknown
- 2013-10-31 EP EP13786219.9A patent/EP2914735B1/en not_active Not-in-force
- 2013-10-31 CN CN201810736123.XA patent/CN108841913A/zh active Pending
- 2013-10-31 PL PL13786219T patent/PL2914735T3/pl unknown
- 2013-10-31 NZ NZ74546913A patent/NZ745469A/en not_active IP Right Cessation
- 2013-10-31 CN CN201810737279.XA patent/CN108802398A/zh active Pending
- 2013-10-31 NZ NZ706368A patent/NZ706368A/en not_active IP Right Cessation
- 2013-10-31 AU AU2013340841A patent/AU2013340841B2/en not_active Ceased
- 2013-10-31 KR KR1020157011629A patent/KR101730281B1/ko not_active Expired - Fee Related
- 2013-10-31 JP JP2015540118A patent/JP6280127B2/ja not_active Expired - Fee Related
- 2013-10-31 ES ES13786219T patent/ES2707872T3/es active Active
- 2013-10-31 WO PCT/EP2013/072754 patent/WO2014068022A1/en not_active Ceased
- 2013-10-31 RU RU2015120693A patent/RU2652888C2/ru active
- 2013-10-31 BR BR112015009901A patent/BR112015009901A2/pt not_active Application Discontinuation
- 2013-10-31 CA CA2886162A patent/CA2886162C/en not_active Expired - Fee Related
- 2013-10-31 CN CN201810736125.9A patent/CN108845132A/zh active Pending
-
2014
- 2014-11-21 US US14/549,724 patent/US9416397B2/en not_active Expired - Fee Related
-
2015
- 2015-04-01 IL IL238077A patent/IL238077B/en active IP Right Grant
- 2015-04-30 ZA ZA2015/02999A patent/ZA201502999B/en unknown
-
2016
- 2016-11-30 JP JP2016232405A patent/JP6313407B2/ja not_active Expired - Fee Related
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6313407B2 (ja) | 試薬材料および関連検査素子 | |
| JP2017104101A5 (ja) | ||
| JP2015536138A5 (ja) | ||
| JP7141433B2 (ja) | 多検体診断用試験エレメントのための検出試薬および電極配置、ならびにそれらを使用する方法 | |
| US10466196B2 (en) | Systems and methods for multiple analyte analysis | |
| HK40000347A (en) | Reagent materials and associated test elements | |
| HK40000351A (en) | Reagent materials and associated test elements | |
| HK40000484A (en) | Reagent materials and associated test elements | |
| HK40000482A (en) | Reagent materials and associated test elements | |
| HK40009082A (en) | Detection reagents and electrode arrangements for multi-analyte diagnostic test elements, as well as methods of using the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20161027 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20161027 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170815 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20171027 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20171219 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20180118 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6280127 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |