JP6231170B2 - リボ核酸及びジエチレントリアミン五酢酸の高収量の迅速な結合方法 - Google Patents
リボ核酸及びジエチレントリアミン五酢酸の高収量の迅速な結合方法 Download PDFInfo
- Publication number
- JP6231170B2 JP6231170B2 JP2016137056A JP2016137056A JP6231170B2 JP 6231170 B2 JP6231170 B2 JP 6231170B2 JP 2016137056 A JP2016137056 A JP 2016137056A JP 2016137056 A JP2016137056 A JP 2016137056A JP 6231170 B2 JP6231170 B2 JP 6231170B2
- Authority
- JP
- Japan
- Prior art keywords
- acid
- ribonucleic acid
- dtpa
- diethylenetriaminepentaacetic
- dna
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/0497—Organic compounds conjugates with a carrier being an organic compounds
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K51/00—Preparations containing radioactive substances for use in therapy or testing in vivo
- A61K51/02—Preparations containing radioactive substances for use in therapy or testing in vivo characterised by the carrier, i.e. characterised by the agent or material covalently linked or complexing the radioactive nucleus
- A61K51/04—Organic compounds
- A61K51/0491—Sugars, nucleosides, nucleotides, oligonucleotides, nucleic acids, e.g. DNA, RNA, nucleic acid aptamers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H1/00—Processes for the preparation of sugar derivatives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
- C07H21/02—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids with ribosyl as saccharide radical
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Biomedical Technology (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Optics & Photonics (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicinal Preparation (AREA)
Description
まず、16merの一本鎖DNA (5`-ATGGAATTCAGTTCTC-3`) 32.4nmolを20 μLの0.5MのNaHCO3溶液に溶かす。次に、36μLのDMSO (ジメチルスルホキシド、Dimethyl sulfoxide)を加え、DMSOは50倍のDNAモル数のp-SCN-Bn-DTPA(イソチオシアン酸p-ベンジル基-ジエチレントリアミン五酢酸、2-(4-isothiocyanatobenzyl)-diethylenetriaminepentaacetic acid)を含有する。その後、室温で夜通し振動反応を行う(overnight、12時間以上)。そして、獲得した反応物を遠心分離機で1000gの回転速度で3分間持続させる条件の下、Centri-Pure MINI SEQ Z−25 size exclusion column (emp BIOTECH社製、一種の脱塩遠沈管)で遠心分離を行う。続いて、溶離液を収集し、即ちDTPA−DNAである。それから、質量分析計を使用して分析を行い、過程は以下に簡潔に述べる:純化されたDTPA-DNAから0.5μL及び1.5μLの3-HPA (3-Hydroxypicolinic acid) を取って基質とし、均一に混合させた後に試験盤に載せ、混合液が自然に乾くまで待ち、マトリックス支援レーザー脱離イオン化飛行時間型質量分析計(MALDI-TOF) によりDTPA-DNAの分子量の鑑定を行う。16merの一本鎖DNAの分子量は質量分析計による分析では5200Daであり、p-SCN-Bn-DTPAに結合された後には、質量分析計による分析では分子量のピークが5766Daになる。但し、多量のDNAがp-SCN-Bn-DTPAに結合されない(図1参照)。
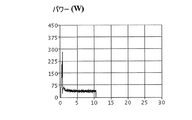
まず、16merの一本鎖DNA (5`-ATGGAATTCAGTTCTC-3`)32.4nmolを25μLの0.5MのNaHCO3溶液中に溶かす。次に、25μLのDMSOを加え、DMSOは1mgのp-SCN-Bn-DTPAを含有する。その後、Biotage Initiatorマイクロ波加熱器で75°Cの環境下で10分間反応させる(マイクロ波加熱反応温度及びパワー変化について、図7A及び図7B参照)。続いて、獲得した反応物を遠心分離機を使用して1000gの回転速度で3分間持続させる条件の下、Z-25 size exclusion columnで遠心分離を行う。そして、溶離液を収集し、即ちDTPA-Bn-SCN-DNAである。マトリックス支援レーザー脱離イオン化飛行時間型質量分析計(MALDI-TOF)により生成物の分子量の鑑定を行い、図2に示すように、p-SCN-Bn-DTPAのマイクロ波加熱を行ってDNAに結合させる試験からは、100%のDTPA-Bn-SCN-DNAが得られる。
まず、32.4nmolのDNAを37.5μLの0.5MのNaHCO3に溶かし、62.5μLのDMSOを獲得し、DMSOには濃度8mg/mLのDTPA anhydrideが含まれる。その後、均一に混合させた後にマイクロ波加熱器により75°Cの環境で10分間反応させる(マイクロ波加熱反応温度及びパワー変化について、図7A及び図7B参照)。次に、獲得した反応物を遠心分離機を用いて1000gの回転速度で3分間持続させる条件の下、Z-25 size exclusion columnで遠心分離を行う。そして、溶離液を収集し、即ち、DTPA-DNAである。質量分析計(MALDI-TOF) により生成物の分子量の鑑定を行い、図3に示すように、DTPA anhydrideにマイクロ波加熱を行ってDNAに結合させる試験からは、100%のDTPA -DNAが得られる。
まず、10 nmolのDNAを10μLの二次水に溶かし、10μLの0.5MのNaHCO3を獲得し、NaHCO3は0.333mgのp-SCN-Bn-DTPAを含む。その後、30μLの二次水を補給して総体積を50μLにする。均一に混合させた後、マイクロ波加熱器を用いて94°Cの環境で5分間反応させる(マイクロ波加熱反応温度及びパワー変化について、図6A及び図6B参照)。次に、得られた反応物を遠心分離機を用いて1000gの回転速度で3分間持続させる条件の下、Z-25 size exclusion columnで遠心分離を行い、溶離液を収集し、即ち、DTPA-Bn-NCS-DNAである。質量分析計により生成物の分子量の鑑定を行い、100%のDTPA-Bn-SCN-DNAが得られたことを確認する(図4参照)。但し、水相で75°Cで10分間マイクロ波反応を行った場合、結合反応は発生しない。
まず、16merの配列が(5`-ATGGAATTCAGTTCTC-3`)のLNA30nmolを25μLの0.25MのNaHCO3溶液に溶かす。その後、30μLのDMSOを加え、DMSOは1mgのp-SCN-Bn-DTPAを含有する。続いて、Biotage Initiatorマイクロ波加熱器により75°Cの環境で10分間反応させる(マイクロ波加熱反応温度及びパワー変化について、図7A及び図7B参照)。次に、獲得した反応物を遠心分離機を用いて1000gの回転速度で3分間持続させる条件の下、Z-25 size exclusion columnで遠心分離を行い、溶離液を収集し、即ち、DTPA-Bn-SCN-LNAである。マトリックス支援レーザー脱離イオン化飛行時間型質量分析計により生成物の分子量の鑑定を行い、図5に示すように、p-SCN-Bn-DTPAのマイクロ波加熱を行ってLNAを結合させる試験からは、100%のDTPA-Bn-SCN-LNAが得られる。
Claims (5)
- マイクロ波を用いてリボ核酸、及び、ジエチレントリアミン五酢酸二無水物或いはイソチオシアネート‐ベンジル基‐ジエチレントリアミン五酢酸の加熱を行い、水相の重炭酸ナトリウム溶液中で94℃で5分間反応させ、或いは2‐10%の有機相を含むDMSO重炭酸ナトリウム溶液中で75℃で10分間反応させることで完成することを含むことを特徴とする迅速な結合方法。
- 前記重炭酸ナトリウム溶液のpHは8.0〜8.5であることを特徴とする、請求項1に記載の迅速な結合方法。
- 前記リボ核酸はアミンを含有する鎖リボ核酸或いはDNAであることを特徴とする、請求項1に記載の迅速な結合方法。
- 反応体積が僅か50μL以下で反応が完全になることを特徴とする、請求項1に記載の迅速な結合方法。
- リボ核酸‐ジエチレントリアミン五酢酸結合物の反応収率は100%であることを特徴とする、請求項1に記載の迅速な結合方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| TW104143832A TWI574972B (zh) | 2015-12-25 | 2015-12-25 | 一種高產率核糖核酸與二乙烯三胺五乙酸之快速鍵結方法 |
| TW104143832 | 2015-12-25 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017114841A JP2017114841A (ja) | 2017-06-29 |
| JP6231170B2 true JP6231170B2 (ja) | 2017-11-15 |
Family
ID=56368880
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016137056A Active JP6231170B2 (ja) | 2015-12-25 | 2016-07-11 | リボ核酸及びジエチレントリアミン五酢酸の高収量の迅速な結合方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9873874B2 (ja) |
| EP (1) | EP3184123B1 (ja) |
| JP (1) | JP6231170B2 (ja) |
| TW (1) | TWI574972B (ja) |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4962045A (en) * | 1988-05-02 | 1990-10-09 | The Perkin-Elmer Corporation | Time-resolved fluorimetric detection of lanthanide labeled nucleotides |
| US6232295B1 (en) * | 1994-10-12 | 2001-05-15 | Jon Faiz Kayyem | Cell-specific contrast agent and gene delivery vehicles |
| WO2008126837A1 (ja) * | 2007-04-10 | 2008-10-23 | Yokohama City University | 標識可能な核酸、標識核酸及びその用途 |
| TWI478726B (zh) * | 2013-06-10 | 2015-04-01 | Inst Nuclear Energy Res Atomic Energy Council | 奈米金與二乙烯三胺五乙酸之鍵結方法 |
-
2015
- 2015-12-25 TW TW104143832A patent/TWI574972B/zh active
-
2016
- 2016-07-06 EP EP16178202.4A patent/EP3184123B1/en active Active
- 2016-07-11 JP JP2016137056A patent/JP6231170B2/ja active Active
- 2016-07-18 US US15/212,697 patent/US9873874B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| TWI574972B (zh) | 2017-03-21 |
| US9873874B2 (en) | 2018-01-23 |
| JP2017114841A (ja) | 2017-06-29 |
| EP3184123B1 (en) | 2020-10-07 |
| EP3184123A1 (en) | 2017-06-28 |
| TW201722981A (zh) | 2017-07-01 |
| US20170183651A1 (en) | 2017-06-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Yamasaki et al. | Differential excision from DNA of the C-8 and N2 guanosine adducts of N-acetyl-2-aminofluorene by single strand-specific endonucleases | |
| Farzan et al. | Automated solid-phase click synthesis of oligonucleotide conjugates: from small molecules to diverse N-acetylgalactosamine clusters | |
| CN101550175B (zh) | 一种修饰体外合成rna的试剂盒和方法 | |
| Bhadra et al. | Synthesis of phosphorodiamidate morpholino oligonucleotides by H-phosphonate method | |
| CN112779260B (zh) | 黄素单核苷酸的核酸适配体、其筛选方法及应用 | |
| O'Shea et al. | An efficient deprotection method for 5′-[O, O-bis (pivaloyloxymethyl)]-(E)-vinylphosphonate containing oligonucleotides | |
| JP2024112974A (ja) | 改変された酸化プロトコルを使用してオリゴヌクレオチドを調製するための方法 | |
| JP6231170B2 (ja) | リボ核酸及びジエチレントリアミン五酢酸の高収量の迅速な結合方法 | |
| JPH10505354A (ja) | 官能テルピリジン−金属錯体、その製法及びテルピリジン−金属錯体とのオリゴヌクレオチド複合体 | |
| CN111454288B (zh) | 含酚羟基的亚膦酰胺、制备方法及其应用 | |
| Warminski et al. | Solid‐Phase Synthesis of RNA 5′‐Azides and Their Application for Labeling, Ligation, and Cyclization Via Click Chemistry | |
| CN119285688A (zh) | 修饰的核苷酸单体及其用途 | |
| Kitoun et al. | Traceless Staudinger ligation for bioconjugation of RNA | |
| Wang et al. | One pot conjugation of small molecules to RNA using click chemistry | |
| WO2024217535A1 (zh) | 一种寡聚核酸及用于降低脱靶活性的化合物 | |
| Parr et al. | Oligonucleotide therapeutics in sports? An antidoping perspective | |
| EP3957733B1 (en) | Simple method for detecting nucleic acid sequence, etc | |
| JPH03128364A (ja) | ウラシルヌクレオシドおよびヌクレオチド誘導体およびその製法 | |
| WO2021230204A1 (ja) | 新型コロナウイルスSARS-CoV-2の検出キットおよび検出方法 | |
| Gissberg et al. | Fast and efficient synthesis of Zorro-LNA type 3′-5′-5′-3′ oligonucleotide conjugates via parallel in situ stepwise conjugation | |
| US12297225B2 (en) | Detection method for natural and modified small nucleic acids | |
| CN114957364B (zh) | 一种碘苷碱基及其制备方法和构建的两亲核酸 | |
| CN118834250A (zh) | 一类新型递送载体 | |
| WO2019081680A1 (en) | NUCLEIC ACID IMMOBILIZATION USING AN ENZYMATIC HISTIDINE LABEL MIMETIC FOR DIAGNOSTIC APPLICATIONS | |
| Xu et al. | Novel trinucleotide mRNA capping reagents: improved synthetic route and efficient cotranscriptional incorporation in mRNA |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170530 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170829 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170919 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20171018 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6231170 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |