JP6055845B2 - ペプチドおよびその使用 - Google Patents
ペプチドおよびその使用 Download PDFInfo
- Publication number
- JP6055845B2 JP6055845B2 JP2014551680A JP2014551680A JP6055845B2 JP 6055845 B2 JP6055845 B2 JP 6055845B2 JP 2014551680 A JP2014551680 A JP 2014551680A JP 2014551680 A JP2014551680 A JP 2014551680A JP 6055845 B2 JP6055845 B2 JP 6055845B2
- Authority
- JP
- Japan
- Prior art keywords
- cell
- peptide
- cells
- adiponectin
- composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims description 139
- 102000004196 processed proteins & peptides Human genes 0.000 title description 33
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 123
- 230000012292 cell migration Effects 0.000 claims description 44
- 230000005012 migration Effects 0.000 claims description 40
- 238000013508 migration Methods 0.000 claims description 40
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 claims description 35
- 108091033319 polynucleotide Proteins 0.000 claims description 23
- 102000040430 polynucleotide Human genes 0.000 claims description 23
- 239000002157 polynucleotide Substances 0.000 claims description 23
- 230000001404 mediated effect Effects 0.000 claims description 19
- 239000000203 mixture Substances 0.000 claims description 19
- 238000011282 treatment Methods 0.000 claims description 13
- 208000037976 chronic inflammation Diseases 0.000 claims description 11
- 208000037893 chronic inflammatory disorder Diseases 0.000 claims description 11
- 210000000496 pancreas Anatomy 0.000 claims description 11
- 230000002265 prevention Effects 0.000 claims description 9
- 206010012601 diabetes mellitus Diseases 0.000 claims description 8
- 208000023275 Autoimmune disease Diseases 0.000 claims description 7
- 210000004153 islets of langerhan Anatomy 0.000 claims description 7
- 201000001320 Atherosclerosis Diseases 0.000 claims description 5
- 210000003038 endothelium Anatomy 0.000 claims description 5
- 230000002757 inflammatory effect Effects 0.000 claims description 5
- 208000011231 Crohn disease Diseases 0.000 claims description 4
- 208000004930 Fatty Liver Diseases 0.000 claims description 4
- 206010016654 Fibrosis Diseases 0.000 claims description 4
- 201000004681 Psoriasis Diseases 0.000 claims description 4
- 206010046851 Uveitis Diseases 0.000 claims description 4
- 230000007882 cirrhosis Effects 0.000 claims description 4
- 208000019425 cirrhosis of liver Diseases 0.000 claims description 4
- 208000036449 fibrotic liver disease Diseases 0.000 claims description 4
- 208000027866 inflammatory disease Diseases 0.000 claims description 4
- 239000013612 plasmid Substances 0.000 claims description 4
- 208000014644 Brain disease Diseases 0.000 claims description 3
- 208000007342 Diabetic Nephropathies Diseases 0.000 claims description 3
- 206010012689 Diabetic retinopathy Diseases 0.000 claims description 3
- 208000033679 diabetic kidney disease Diseases 0.000 claims description 3
- 208000019622 heart disease Diseases 0.000 claims description 3
- 208000033808 peripheral neuropathy Diseases 0.000 claims description 3
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 3
- 239000013603 viral vector Substances 0.000 claims description 3
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 2
- 230000036770 blood supply Effects 0.000 claims description 2
- 208000017169 kidney disease Diseases 0.000 claims 1
- 102000011690 Adiponectin Human genes 0.000 description 87
- 108010076365 Adiponectin Proteins 0.000 description 87
- 210000003719 b-lymphocyte Anatomy 0.000 description 71
- 210000005105 peripheral blood lymphocyte Anatomy 0.000 description 59
- 210000002889 endothelial cell Anatomy 0.000 description 42
- 210000004698 lymphocyte Anatomy 0.000 description 39
- DUYSYHSSBDVJSM-KRWOKUGFSA-N sphingosine 1-phosphate Chemical compound CCCCCCCCCCCCC\C=C\[C@@H](O)[C@@H](N)COP(O)(O)=O DUYSYHSSBDVJSM-KRWOKUGFSA-N 0.000 description 21
- 108090000179 Adiponectin Receptors Proteins 0.000 description 20
- 102000003808 Adiponectin Receptors Human genes 0.000 description 20
- 150000001413 amino acids Chemical group 0.000 description 19
- 239000006228 supernatant Substances 0.000 description 18
- 108090000623 proteins and genes Proteins 0.000 description 17
- 238000002474 experimental method Methods 0.000 description 16
- 102000004169 proteins and genes Human genes 0.000 description 16
- 238000001543 one-way ANOVA Methods 0.000 description 14
- 230000001629 suppression Effects 0.000 description 14
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 13
- 102100037850 Interferon gamma Human genes 0.000 description 13
- 108010074328 Interferon-gamma Proteins 0.000 description 13
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 13
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- 230000005764 inhibitory process Effects 0.000 description 13
- 230000006870 function Effects 0.000 description 11
- 241000699670 Mus sp. Species 0.000 description 10
- 238000000692 Student's t-test Methods 0.000 description 10
- 230000002401 inhibitory effect Effects 0.000 description 10
- 210000000265 leukocyte Anatomy 0.000 description 10
- 238000012353 t test Methods 0.000 description 10
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 9
- 238000003556 assay Methods 0.000 description 9
- 239000003112 inhibitor Substances 0.000 description 9
- 239000002609 medium Substances 0.000 description 9
- 230000037361 pathway Effects 0.000 description 9
- 210000004303 peritoneum Anatomy 0.000 description 9
- 210000002966 serum Anatomy 0.000 description 9
- 108020004414 DNA Proteins 0.000 description 8
- 101000800583 Homo sapiens Transcription factor 20 Proteins 0.000 description 8
- 102100033142 Transcription factor 20 Human genes 0.000 description 8
- 229920000392 Zymosan Polymers 0.000 description 8
- 210000004027 cell Anatomy 0.000 description 8
- 230000001965 increasing effect Effects 0.000 description 8
- 238000000034 method Methods 0.000 description 8
- LVTJOONKWUXEFR-FZRMHRINSA-N protoneodioscin Natural products O(C[C@@H](CC[C@]1(O)[C@H](C)[C@@H]2[C@]3(C)[C@H]([C@H]4[C@@H]([C@]5(C)C(=CC4)C[C@@H](O[C@@H]4[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@@H](O)[C@H](O[C@H]6[C@@H](O)[C@@H](O)[C@@H](O)[C@H](C)O6)[C@H](CO)O4)CC5)CC3)C[C@@H]2O1)C)[C@H]1[C@H](O)[C@H](O)[C@H](O)[C@@H](CO)O1 LVTJOONKWUXEFR-FZRMHRINSA-N 0.000 description 8
- 102000005962 receptors Human genes 0.000 description 8
- 108020003175 receptors Proteins 0.000 description 8
- 230000028327 secretion Effects 0.000 description 8
- 230000032258 transport Effects 0.000 description 8
- 102000014156 AMP-Activated Protein Kinases Human genes 0.000 description 7
- 108010011376 AMP-Activated Protein Kinases Proteins 0.000 description 7
- 102100039024 Sphingosine kinase 1 Human genes 0.000 description 7
- 238000004458 analytical method Methods 0.000 description 7
- 238000000338 in vitro Methods 0.000 description 7
- 238000001727 in vivo Methods 0.000 description 7
- 238000011813 knockout mouse model Methods 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- 108010035597 sphingosine kinase Proteins 0.000 description 7
- 102100038719 Histone deacetylase 7 Human genes 0.000 description 6
- 101001032113 Homo sapiens Histone deacetylase 7 Proteins 0.000 description 6
- 206010061218 Inflammation Diseases 0.000 description 6
- 102100025390 Integrin beta-2 Human genes 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 108010076181 Proinsulin Proteins 0.000 description 6
- 231100000673 dose–response relationship Toxicity 0.000 description 6
- 230000004054 inflammatory process Effects 0.000 description 6
- 108010037801 Myosin-Light-Chain Phosphatase Proteins 0.000 description 5
- 102100037764 Serine/threonine-protein phosphatase PP1-beta catalytic subunit Human genes 0.000 description 5
- 230000009471 action Effects 0.000 description 5
- 210000004185 liver Anatomy 0.000 description 5
- 238000004949 mass spectrometry Methods 0.000 description 5
- 210000003071 memory t lymphocyte Anatomy 0.000 description 5
- 210000001616 monocyte Anatomy 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 230000011664 signaling Effects 0.000 description 5
- 230000000638 stimulation Effects 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- 108010064548 Lymphocyte Function-Associated Antigen-1 Proteins 0.000 description 4
- 102000011011 Sphingosine 1-phosphate receptors Human genes 0.000 description 4
- 108050001083 Sphingosine 1-phosphate receptors Proteins 0.000 description 4
- 102100027662 Sphingosine kinase 2 Human genes 0.000 description 4
- 101710156532 Sphingosine kinase 2 Proteins 0.000 description 4
- 230000003110 anti-inflammatory effect Effects 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- KQNZDYYTLMIZCT-KQPMLPITSA-N brefeldin A Chemical compound O[C@@H]1\C=C\C(=O)O[C@@H](C)CCC\C=C\[C@@H]2C[C@H](O)C[C@H]21 KQNZDYYTLMIZCT-KQPMLPITSA-N 0.000 description 4
- JUMGSHROWPPKFX-UHFFFAOYSA-N brefeldin-A Natural products CC1CCCC=CC2(C)CC(O)CC2(C)C(O)C=CC(=O)O1 JUMGSHROWPPKFX-UHFFFAOYSA-N 0.000 description 4
- 230000004656 cell transport Effects 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 238000012417 linear regression Methods 0.000 description 4
- 210000003289 regulatory T cell Anatomy 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 230000003068 static effect Effects 0.000 description 4
- 102100025248 C-X-C motif chemokine 10 Human genes 0.000 description 3
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 102000001708 Protein Isoforms Human genes 0.000 description 3
- 108010029485 Protein Isoforms Proteins 0.000 description 3
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000001143 conditioned effect Effects 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 238000010232 migration assay Methods 0.000 description 3
- 230000004203 pancreatic function Effects 0.000 description 3
- 230000001575 pathological effect Effects 0.000 description 3
- 230000008685 targeting Effects 0.000 description 3
- 101150076297 ywhaz gene Proteins 0.000 description 3
- 102000002281 Adenylate kinase Human genes 0.000 description 2
- 108020000543 Adenylate kinase Proteins 0.000 description 2
- 101710098275 C-X-C motif chemokine 10 Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 101000935040 Homo sapiens Integrin beta-2 Proteins 0.000 description 2
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 2
- 101000917839 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-B Proteins 0.000 description 2
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 2
- 206010039438 Salmonella Infections Diseases 0.000 description 2
- 210000001789 adipocyte Anatomy 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 230000003915 cell function Effects 0.000 description 2
- 239000013553 cell monolayer Substances 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 238000010835 comparative analysis Methods 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 230000002500 effect on skin Effects 0.000 description 2
- 238000000684 flow cytometry Methods 0.000 description 2
- 238000013467 fragmentation Methods 0.000 description 2
- 238000006062 fragmentation reaction Methods 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 230000004957 immunoregulator effect Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 229940043355 kinase inhibitor Drugs 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 210000004877 mucosa Anatomy 0.000 description 2
- 210000000822 natural killer cell Anatomy 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 238000001422 normality test Methods 0.000 description 2
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 2
- 210000003200 peritoneal cavity Anatomy 0.000 description 2
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 230000004481 post-translational protein modification Effects 0.000 description 2
- 239000002464 receptor antagonist Substances 0.000 description 2
- 229940044551 receptor antagonist Drugs 0.000 description 2
- 238000000611 regression analysis Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 206010039447 salmonellosis Diseases 0.000 description 2
- 210000003752 saphenous vein Anatomy 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 229960000814 tetanus toxoid Drugs 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 210000003954 umbilical cord Anatomy 0.000 description 2
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- 102100033497 Adiponectin receptor protein 1 Human genes 0.000 description 1
- 102100032358 Adiponectin receptor protein 2 Human genes 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 1
- 101000914947 Bungarus multicinctus Long neurotoxin homolog TA-bm16 Proteins 0.000 description 1
- 101100191768 Caenorhabditis elegans pbs-4 gene Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101001135206 Homo sapiens Adiponectin receptor protein 1 Proteins 0.000 description 1
- 101000589401 Homo sapiens Adiponectin receptor protein 2 Proteins 0.000 description 1
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 1
- 101000858088 Homo sapiens C-X-C motif chemokine 10 Proteins 0.000 description 1
- 101000946889 Homo sapiens Monocyte differentiation antigen CD14 Proteins 0.000 description 1
- 101000693265 Homo sapiens Sphingosine 1-phosphate receptor 1 Proteins 0.000 description 1
- 108090000144 Human Proteins Proteins 0.000 description 1
- 102000003839 Human Proteins Human genes 0.000 description 1
- 208000003456 Juvenile Arthritis Diseases 0.000 description 1
- 206010059176 Juvenile idiopathic arthritis Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102100035877 Monocyte differentiation antigen CD14 Human genes 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 241000233805 Phoenix Species 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 206010062237 Renal impairment Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 229940126064 S1PR antagonist Drugs 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 102100025750 Sphingosine 1-phosphate receptor 1 Human genes 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 230000008485 antagonism Effects 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 210000000234 capsid Anatomy 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 208000019069 chronic childhood arthritis Diseases 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 230000004087 circulation Effects 0.000 description 1
- 239000003636 conditioned culture medium Substances 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 230000007783 downstream signaling Effects 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 230000000482 effect on migration Effects 0.000 description 1
- 230000001210 effect on neutrophils Effects 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 230000008519 endogenous mechanism Effects 0.000 description 1
- 230000010595 endothelial cell migration Effects 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 229940124589 immunosuppressive drug Drugs 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000000126 in silico method Methods 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 201000002215 juvenile rheumatoid arthritis Diseases 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 230000023404 leukocyte cell-cell adhesion Effects 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 230000002101 lytic effect Effects 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 210000005063 microvascular endothelium Anatomy 0.000 description 1
- 210000002200 mouth mucosa Anatomy 0.000 description 1
- 210000002850 nasal mucosa Anatomy 0.000 description 1
- 230000013152 negative regulation of cell migration Effects 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 238000007427 paired t-test Methods 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000006320 pegylation Effects 0.000 description 1
- 206010034674 peritonitis Diseases 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 239000013600 plasmid vector Substances 0.000 description 1
- 238000010149 post-hoc-test Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 238000000575 proteomic method Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 239000003488 releasing hormone Substances 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 230000009962 secretion pathway Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000011277 treatment modality Methods 0.000 description 1
- 239000013598 vector Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/10—Peptides having 12 to 20 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1703—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- A61K38/1709—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Marine Sciences & Fisheries (AREA)
- Zoology (AREA)
- Heart & Thoracic Surgery (AREA)
- Rheumatology (AREA)
- Urology & Nephrology (AREA)
- Cardiology (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Transplantation (AREA)
- Hematology (AREA)
- Ophthalmology & Optometry (AREA)
- Obesity (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Dermatology (AREA)
- Pain & Pain Management (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Vascular Medicine (AREA)
Description
5’-AGU GUU ACU GAA CAA GGU GCU GAG UUA UCU AAU GAG GAG AGA-3’(配列番号2);
あるいは
5’-AGC GUC ACC GAG CAG GGC GCC GAA UUG UCC AAC GAA GAG AGG-3’(配列番号3)
である。
〔アディポネクチンは、末梢血リンパ球(PBL)の経内皮細胞移動を抑制する〕
内皮細胞を、低血清培地中で培養し、アディポネクチンの非存在下でTNF-α/IFN-γで24時間刺激した。PBLを単離して、0.0001〜15μg/mlのアディポネクチンで1時間処理した。
内皮細胞を、低血清培地中で培養し、TNF-α/IFN-γで24時間刺激した。コンパウンドCを10μg/mlにて30分間 PBLに加えた後、アディポネクチンを15μg/mlにて1時間加えた。アディポネクチン処理は、遊出の減少を誘導し、これはコンパウンドCの存在下では正常な対照レベルまで回復された。結果は図2に示されており、そこではデータは3回の実験を表すものであって、一元配置ANOVAおよびダネットの多重比較ポストテストを用いて解析された。**p≦0.001、***p≦0.0001。
内皮細胞を、低血清培地中で培養し、アディポネクチンの非存在下でTNF-α/IFN-γで24時間刺激した。結果を図3に示す。a)の部分は、T1DにおいてPBL遊出に対するアディポネクチン媒介性抑制が消失していることを示し、b)の部分は、アディポネクチン処理による遊出のパーセンテージを未処理PBLの遊出のパーセンテージで割ることによって抑制のパーセンテージが計算されたことを示す。HC(健常者対照)群についてはn= 13であり、T1D群についてはn=12である。データは、t検定および一元配置ANOVA、ならびにボンフェローニの多重比較ポストテストを用いて解析された。***p≦0.0001。
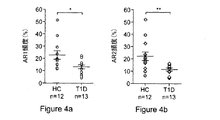
アディポネクチン受容体AR1またはAR2を発現するPBLの頻度を、健康被験者または疾患被験者の各々について決定し、それぞれ図4a)および4b)に示している。データは、平均±SEMとして表され、t検定、またはデータがコルモゴロフ・スミルノフ正規性検定を通らない場合にはマン・ホイットニーt検定を用いて解析した。
図5a)は、AR1の発現とリンパ球移動の抑制との間の相関を示し、図5b)は、AR2の発現とリンパ球移動の抑制との間の相関を示す。相関は、線形回帰分析を用いて決定された。
図6a)およびb)は、異なる細胞型上のAR1(図6a)およびAR2(図6b)の発現を示す。データは平均±SEMであり、7人の健常者対照を表す。データは、一元配置ANOVAおよびボンフェローニの多重比較ポストホックテストを用いて解析された。***p≦0.0001。
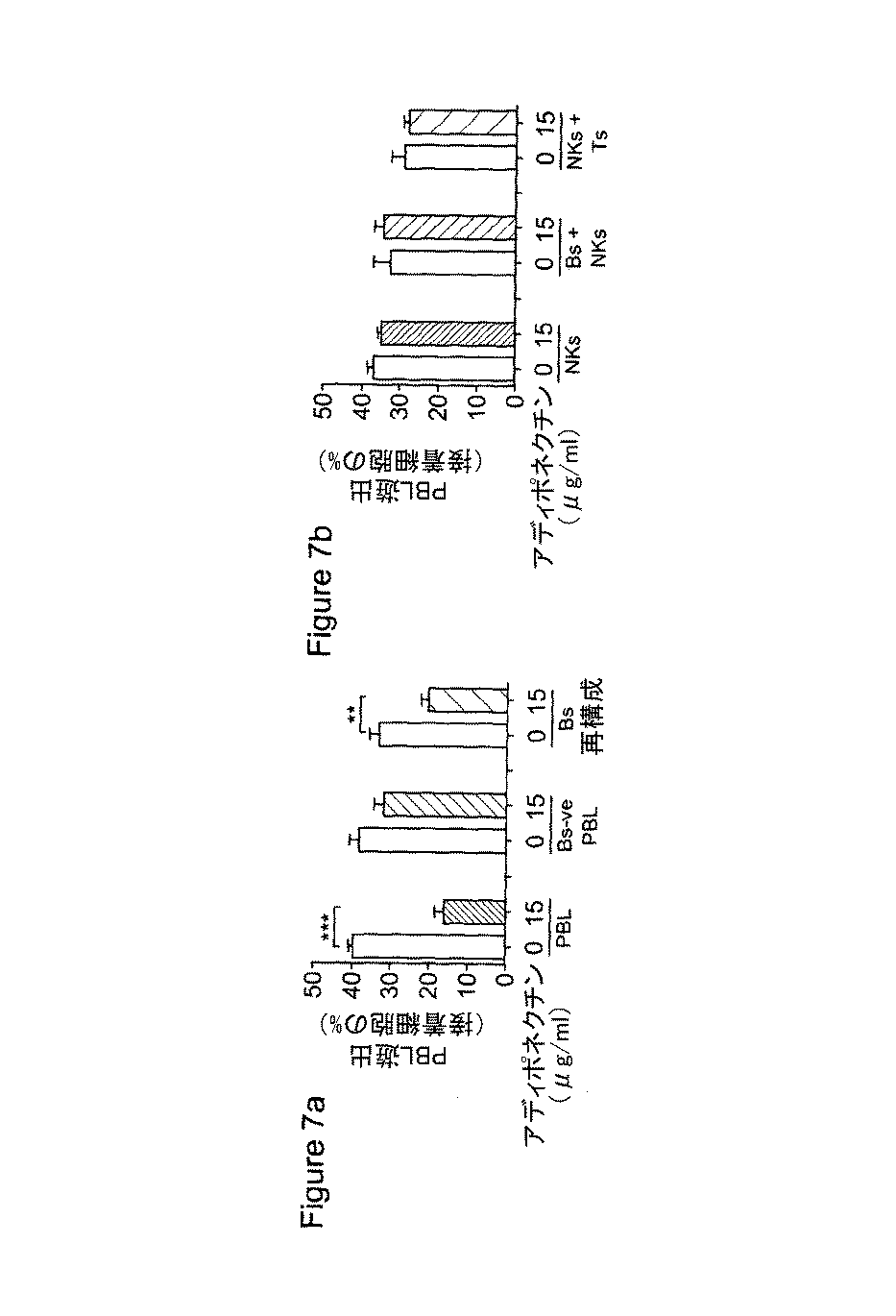
図7a)は、PBLからB細胞(Bs)を枯渇させるとPBLの移動が消失し、単離T細胞にB細胞を加え戻すと回復することを示す。図7b)は、ナチュラルキラー細胞(NKs)の移動はアディポネクチンによって影響されず、NKsをT細胞に添加してもT細胞の移動は制御されないことを示す。データは平均±SEMであり、少なくとも3回の独立した実験を表す。データは、一元配置ANOVAおよびボンフェローニの多重比較ポストテストを用いて解析された。**p≦0.001、***p≦0.0001。
B細胞を単離して、15μg/mlのアディポネクチンの存在下または非存在下でインキュベートした。1時間後に上清(Sup)を採取してBs-ve PBLに添加したところ、PBL遊出のアディポネクチン抑制が有意に回復した。いくつかの実験では、B細胞は、B細胞分泌の阻害剤であるブレフェルジンA(BrefA)で処理された。これらの上清はT細胞の移動を制御することができなかった。このことは図8に示されているが、そのデータは平均±SEMとして示され、一元配置ANOVAおよびボンフェローニの多重比較ポストテストを用いて解析された3つの独立した実験を表す。***p<0.001、ns=非有意。
m/z 774.88イオンは、解析プロトコールのフラグメンテーション産物であり、一般的にMS/MSを使用した同定のためにのみ使用されるが、比較のための重要なパラメータになり得る。
アディポネクチン(陽性対照として、15μg/ml)または0.001〜10ng/mlの濃度のペプチドでPBLを処理し、スクランブル化ペプチドを陰性対照として使用した(10ng/mlで使用)。本ペプチドの特異性を実証するために、その他の生活性ペプチドも使用した(すなわち、10ng/mlの破傷風トキソイドペプチド(TTp)および10ng/mlのプロインスリン(PI))。結果を図11に示す。図11 a)は、PBL遊出は本ペプチドの存在下では用量依存的に減少したが、スクランブル化ペプチド対照、TTp対照、またはPI対照の存在下では減少しなかったことを示している。図11b)は、非線形回帰分析を用いて本ペプチドのEC50(18.6pM)を算出したことを示す。データは3回の独立した実験を表し、一元配置ANOVAおよびボンフェローニの多重比較ポストテストを用いて解析された。*p≦0.01、**p≦0.001、***p≦0.0001。
本ペプチドもしくはスクランブル化ペプチドの有りまたは無しでザイモサン(または対照としてのPBS)を48時間注入した後に、腹膜から白血球を採取した。T細胞はCD3の発現により同定した。本ペプチドまたはスクランブル化ペプチドは、300μg/マウスの最終濃度にて注射した。結果を図12に示すが、そこでは、各群についてデータは平均であり、一元配置ANOVAおよびボンフェローニの多重比較ポストテストを用いて解析された。*p≦0.01。
この実施例は、さらなる実験を行った結果を示すものであり、従って実施例1を補足する。
図13を参照。内皮細胞を低血清培地中で培養し、アディポネクチンの非存在下で、TNF-α/IFN-γで24時間刺激した。PBLを単離して、0.0001〜15μg/mlのアディポネクチンで1時間処理した。(a)の部分は、静的接着アッセイにおいてPBL遊出がアディポネクチンにより有意にかつ用量依存的に減少したこと、および、アディポネクチンは線形回帰により決定されるEC50が約40nMであることを示している。(b)の部分は、アディポネクチンが、フローベースの接着アッセイにおいても、PBL移動を抑制することに関して同等に効果的であったことを示している。(c)の部分は、アディポネクチンが、異なる組織、例えばHUVEC(臍帯)、HSEC(肝臓類洞内皮細胞)、およびDMEC(真皮微小血管上皮)から単離された上皮細胞に対して有効であるが、HSAVEC(伏在静脈)からのものに対しては有効ではないことを示している。(d)の部分においては、AMPキナーゼ阻害剤であるコンパウンドCを10μg/mlにて30分間 PBLに添加された後、アディポネクチンを15μg/mlにて1時間添加した。AMPKは、アディポネクチン受容体シグナル伝達のために必要とされるシグナル伝達アダプターである。アディポネクチン処理は、遊出の減少を誘導したが、これはコンパウンドCの存在下では正常な対照レベルまで回復された。これらのデータは、アディポネクチンが、PBL上に発現されるその受容体に対する作用を通じて、リンパ球の遊出を制御する強い能力を有することを示している。データは、少なくとも3回の独立した実験をまとめたものであり、t検定、一元配置ANOVA、およびダネットの多重比較ポストテストを用いて解析された。**p≦0.01、***p≦0.001。
前の実験の最も単純な解釈は、T細胞がAqの直接的制御下にあるということである。しかしながら、T細胞は適切な受容体を欠いている。しかしながら、他の白血球はAdipo- R1/2を有しており、単球およびB細胞はどちらも高いレベルの発現を示す。
図14を参照。内皮細胞を低血清培地中で培養し、アディポネクチンの非存在下で、TNF-α/IFN-γで24時間刺激した。ビーズによるポジティブ選択を用いたB細胞の除去後、および、ビーズによるネガティブ選択を用いて単離したB細胞による再構成後に、アディポネクチン(15μg/ml)の存在下または非存在下でPBL遊出を測定した。アディポネクチン処理B細胞、またはタンパク質分泌を遮断するためにブレフェルジンAで処理したB細胞からの上清を、PBLに添加した。
図15を参照。B細胞は、ネガティブ選択を用いて単離し、アディポネクチンとともに1時間インキュベートした。上清を回収して、C18カラムで精製して大きなサイズのタンパク質を除去し、質量分析器によって獲得した。AQ刺激B細胞からの上清の質量分析を用いたプロテオミクス解析により、SVTEQGAELSNEERという配列を有する14アミノ酸のペプチドが明らかとなった。これを、刊行された配列および予測されている配列のインシリコライブラリーと比較したところ、このペプチドは、単一のヒトタンパク質に対する正確な配列相同性を示し、すなわち14.3.3ゼータ/デルタ(14.3.3.ζδ)タンパク質の第28〜41アミノ酸を表し、このタンパク質はYWHAZ遺伝子の245アミノ酸産物である。このペプチドは、既知の免疫調節ペプチドのファミリーのいずれの構成員でもないし、それらのいずれかと関係していたり、配列類似性を有していたりもしない。質量分析による合成ペプチドの分析は、天然ペプチドと同一の質量:電荷比を示し(m/z=774.88)、このことは、B細胞由来の産物は放出に先立っていかなる形態の翻訳後修飾も受けていなかったことを実証している。これらのデータは、同定された14アミノ酸ペプチドが、アディポネクチン刺激下におけるB細胞から放出されるメディエーターであることを示している。
図16を参照。内皮細胞を低血清培地中で培養し、アディポネクチンの非存在下で、TNF-α/IFN-γで24時間刺激した。PBLは、アディポネクチン(陽性対照として、15μg/ml)、または0.001〜10ng/mlの濃度の本ペプチドで処理し、スクランブル化ペプチドを陰性対照として使用した(10ng/ml)。本ペプチドの特異性を実証するために、その他の生活性ペプチドも使用した(すなわち、10ng/mlの破傷風トキソイドペプチド(TTp)および10ng/mlのプロインスリン(PI))。a)の部分は、PBL遊出が本ペプチドの存在下では用量依存的に減少したが、スクランブル化ペプチド対照、TTp対照、またはPI対照の存在下では減少しなかったことを示している。b)の部分は、非線形回帰分析を用いて本ペプチドのEC50(18.6pM)を算出したことを示す。これらのデータは、PEPITEMが、アディポネクチンと同様に、PBL遊出を抑制することができることを示している。データは少なくとも3回の独立した実験をまとめたものであり、一元配置ANOVAおよびボンフェローニの多重比較ポストテストを用いて解析された。*p≦0.05、**p≦0.01、***p≦0.001。
図17を参照。内皮細胞を低血清培地中で培養し、アディポネクチンの非存在下で、TNF-α/IFN-γで24時間刺激した。PBLおよび異なるサブセットならびにPEPITEMを、異なる内皮細胞に添加し、遊出を測定した。異なるサブセットは、Treg、CD4+およびCD8+メモリーT 細胞ならびにナイーブT細胞についてのネガティブ選択を用いて単離した。ポジティブ選択を用いて異なる単球サブセットを単離した。
図18を参照。内皮細胞(EC)を低血清培地中で培養し、アディポネクチンの非存在下で、TNF-α/IFN-γで24時間刺激した。PEPITEMをPBLとともに内皮細胞に加えるか、または、内皮細胞をPEPITEMで前処理して洗浄後にPBLを加えるか、または、PBLをPEPITEMで前処理して洗浄して内皮細胞に加えた。
図19を参照。IFN-γ/TNF-α処理したHUVECを通したPBLまたはB細胞枯渇化PBLの遊出を、S1PRアンタゴニスト(W146、10μM)を用いてS1Pシグナル伝達を遮断した後に、アディポネクチン(15μg/ml)(a)またはPEPITEM(b)の存在下または非存在下において測定した。B細胞枯渇化PBLは、異なる濃度(0〜100μM)のS1Pで前処理され、IFN-γ/TNF-α処理HUVECを通した遊出を測定した(c)。SPHK1およびSPHK2のmRNA発現のレベルは、B細胞およびHUVEC(dの部分、n=2)からのRNAのリアルタイムPCRにより決定した。PEPITEM(10 ng/ml)の存在下、SPHK1特異的阻害剤(5μM)で前処理したIFN-γ/TNF-α処理HUVECを通したPBL遊出を測定した(e)。
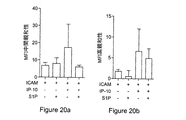
図20を参照。96ウェルプレートを50ug/mlの組換えICAMで4℃にて一晩コーティングした。PBS 4% BSAを用いて1時間室温にてプレートをブロッキングし、IP-10(10ng/ml)および/またはS1P(10uM)で処理したPBLを30分間添加した。剰余の未結合PBLを洗い流し、リンパ球インテグリンLFA-1(CD11a/CD18;αLβ2)の中間親和性部位についてはKIM127抗体(10ug/ml)を使用して、高親和性部位については抗体24(10ug/ml)を使用して、4℃にてPBLを標識した。平均蛍光強度(MFI)を使用して、メモリーT細胞について両方の親和性部位の発現を測定した。データは、IP-10刺激により増加した中間親和性部位および高親和性部位の両方の発現が、S1Pの存在下で下方調節されることを示している。このデータは、S1Pが、リンパ球遊出にとって重要であるインテグリンLFA-1の親和性を調節することにより、リンパ球遊出を制御することを示している。データは2つの独立した実験をまとめたものである。
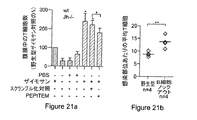
図21を参照。(a)の部分では、野生型マウスまたはB細胞ノックアウト(Jh-/-)BALB/cマウスに100ugのザイモサンを注射した。本ペプチドもしくはスクランブル化ペプチドを伴わせて、または伴わせないで、ザイモサン(または対照としてのPBS)を48時間注入した後に、腹膜から白血球を回収した。T細胞はCD3の発現により同定した。本ペプチドまたはスクランブル化ペプチドは、300μg/マウスという最終濃度にて注射された。その結果を(a)の部分に示しているが、そこでは、各群におけるデータは平均であり、一元配置ANOVAおよびボンフェローニの多重比較ポストテストを用いて解析された。*p≦0.01。(b)の部分では、野生型マウスまたはB細胞ノックアウトC56BL/6マウスにネズミチフス菌(Salmonella typhirium)を注射した。5日後、肝臓を採取して、切片をT細胞について染色した。(b)の部分のデータは、肝臓切片における感染部位あたりのT細胞の数を示す。
図22を参照。アディポネクチン受容体AR1またはAR2を発現するPBLの頻度を、フローサイトメトリーによって各々の健康被験者または疾患被験者について決定し、それぞれ(a)および(b)の部分に示している。データは平均±SEMとして表され、t検定、またはデータがコルモゴロフ・スミルノフ正規性検定を通らない場合にはマン・ホイットニーt検定を用いて解析した。内皮細胞を低血清培地中で培養し、アディポネクチンの非存在下で、TNF-α/IFN-γで24時間刺激した。健常者対照および1型糖尿病の患者からPBLを単離し、15μg/mlのアディポネクチンで1時間処理した。(c)の部分は、AdipoR2の発現とリンパ球移動の抑制との間の相関を示している。相関は線形回帰分析を用いて決定した。(d)の部分は、新たに診断された1型糖尿病患者に由来し、アディポネクチンまたはPEPITEMで前処理されたPBL(n=5)の遊出を示す。データはt検定を用いて解析した。**p<0.01。
Claims (14)
- T細胞媒介性慢性炎症疾患に関連する状態の治療および/または予防における使用のための、ペプチドを含む組成物であって、前記ペプチドは配列N’-SVTEQGAELSNEER-C’(配列番号1)からなりT細胞の移動を抑制する、組成物。
- 前記状態が、T細胞自己反応性、T細胞媒介性慢性炎症疾患、および自己免疫疾患からなる群から選択される、請求項1に記載の組成物。
- 前記状態が、糖尿病(1型)である、請求項1または2に記載の組成物。
- 前記状態が、若年発症糖尿病、関節リウマチ、クローン病、アテローム性動脈硬化症、乾癬、脂肪性肝炎および肝硬変を含む炎症性および線維性の肝疾患、ならびにブドウ膜炎からなる群から選択される、請求項1または2に記載の組成物。
- 前記状態が、腎障害、糖尿病性腎疾患、末梢神経障害、糖尿病性網膜症、および心・脳疾患からなる群から選択される、請求項1または2に記載の組成物。
- 前記T細胞の移動は、島細胞を血液供給から隔てる膵臓微小血管系の内皮を通した経内皮移動である、請求項1〜5のいずれかに記載の組成物。
- 前記T細胞は自己反応性T細胞である、請求項1〜6のいずれかに記載の組成物。
- 前記ペプチドが、膵島への自己反応性T細胞の徴集を抑制する作用をする、請求項7に記載の組成物。
- T細胞媒介性慢性炎症疾患に関連する状態の治療および/または予防における使用のための、ポリヌクレオチドを含む組成物であって、前記ポリヌクレオチドは、配列N’-SVTEQGAELSNEER-C’(配列番号1)からなるペプチドをコードする、組成物。
- 前記ポリヌクレオチドは、配列番号2、配列番号3、およびそれらのDNA形態またはDNA/RNAハイブリッド形態からなる群から選択される、請求項9に記載の組成物。
- 前記ポリヌクレオチドはプロモーターに作動可能に連結される、請求項10に記載の組成物。
- 前記プロモーターは膵臓特異的プロモーターである、請求項11に記載の組成物。
- 前記ポリヌクレオチドはプラスミドに含まれる、請求項9〜12のいずれかに記載の組成物。
- 前記プラスミドはウイルスベクターに含まれる、請求項13に記載の組成物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1200555.9 | 2012-01-13 | ||
| GB201200555A GB201200555D0 (en) | 2012-01-13 | 2012-01-13 | Peptide |
| PCT/GB2013/050068 WO2013104928A1 (en) | 2012-01-13 | 2013-01-14 | Peptide and uses thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015509095A JP2015509095A (ja) | 2015-03-26 |
| JP6055845B2 true JP6055845B2 (ja) | 2016-12-27 |
Family
ID=45813974
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014551680A Active JP6055845B2 (ja) | 2012-01-13 | 2013-01-14 | ペプチドおよびその使用 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9597368B2 (ja) |
| EP (1) | EP2802342B1 (ja) |
| JP (1) | JP6055845B2 (ja) |
| CN (1) | CN104168910B (ja) |
| GB (1) | GB201200555D0 (ja) |
| IN (1) | IN2014DN05784A (ja) |
| WO (1) | WO2013104928A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110381920A (zh) * | 2017-03-09 | 2019-10-25 | 雅利斯塔制药公司 | 用于干眼病的肽 |
| WO2020102623A1 (en) * | 2018-11-15 | 2020-05-22 | The University Of Toledo | Materials and methods for the prevention of rheumatoid arthritis |
| US20210100870A1 (en) * | 2019-10-08 | 2021-04-08 | The University Of Birmingham | Bone disease treatment |
| GB202211043D0 (en) | 2022-07-28 | 2022-09-14 | Univ Birmingham | Peptide agonist |
| CN117244043B (zh) * | 2023-11-02 | 2024-09-20 | 徐州医科大学附属医院 | 破伤风类毒素在治疗血管内皮细胞损伤中的应用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2002054081A2 (en) | 2000-12-29 | 2002-07-11 | Oxford Glycosciences (Uk) Limited | Proteins, genes and their use for diagnosis and treatment of kidney response |
| CA2679301C (en) * | 2007-02-28 | 2015-08-11 | University Of Virginia Patent Foundation | Lisofylline analogs and methods for use in protecting pancreatic .beta.-cells, treating type 1 diabetes, and treating inflammatory and autoimmune diseases |
| AU2008329529B2 (en) * | 2007-11-27 | 2015-02-19 | The University Of British Columbia | 14-3-3 eta antibodies and uses thereof for the diagnosis and treatment of arthritis |
| JP2012504650A (ja) * | 2008-10-02 | 2012-02-23 | セルタクシス,インコーポレイテッド | 免疫細胞の負の走化性の調節方法 |
| US20110130415A1 (en) * | 2009-12-01 | 2011-06-02 | Rajinder Singh | Protein kinase c inhibitors and uses thereof |
| JP5707489B2 (ja) * | 2010-06-09 | 2015-04-30 | ポクセル・エスアーエスPoxelsas | 1型糖尿病の処置 |
-
2012
- 2012-01-13 GB GB201200555A patent/GB201200555D0/en not_active Ceased
-
2013
- 2013-01-14 JP JP2014551680A patent/JP6055845B2/ja active Active
- 2013-01-14 US US14/370,881 patent/US9597368B2/en active Active
- 2013-01-14 IN IN5784DEN2014 patent/IN2014DN05784A/en unknown
- 2013-01-14 WO PCT/GB2013/050068 patent/WO2013104928A1/en active Application Filing
- 2013-01-14 EP EP13700346.3A patent/EP2802342B1/en active Active
- 2013-01-14 CN CN201380013630.6A patent/CN104168910B/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| IN2014DN05784A (ja) | 2015-05-15 |
| EP2802342B1 (en) | 2018-05-02 |
| JP2015509095A (ja) | 2015-03-26 |
| US20150051137A1 (en) | 2015-02-19 |
| CN104168910A (zh) | 2014-11-26 |
| EP2802342A1 (en) | 2014-11-19 |
| CN104168910B (zh) | 2017-07-28 |
| US9597368B2 (en) | 2017-03-21 |
| GB201200555D0 (en) | 2012-02-29 |
| WO2013104928A1 (en) | 2013-07-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6055845B2 (ja) | ペプチドおよびその使用 | |
| US11447555B2 (en) | Methods for treating type 1 diabetes using glucagon receptor antagonistic antibodies | |
| JP2008504249A (ja) | 糖尿病を治療するための方法 | |
| ES2908838T3 (es) | Antagonista del receptor de GLP-1 para usar en el tratamiento del hiperinsulinismo congénito | |
| WO2021075536A1 (ja) | 幹細胞遊走剤を使用した糖尿病治療 | |
| US20190002527A1 (en) | Methods and compositions for the inhibition of trpv4 | |
| EP4395779A1 (en) | Lou064 for treating multiple sclerosis | |
| US9839671B2 (en) | Peptide and uses therefor | |
| US20180221369A1 (en) | Compositions and methods for treating fibrosing disorders and cancer | |
| JP2016538289A (ja) | マクロファージ活性化の主要制御因子としてのparp9およびparp14 | |
| US20130196925A1 (en) | Compositions and methods useful in enhancement of memory | |
| US20190062441A1 (en) | Methods For Treating Rare Genetic Disorders Using Glucagon Receptor Antagonistic Antibodies | |
| US9909108B2 (en) | Preparations and methods for treating malignancies | |
| JP2019520341A (ja) | 代謝疾患を治療する組成物と方法 | |
| EP4424327A1 (en) | Method or agent with hdac regulator, for treatment of diabetes and complications | |
| WO2011109874A1 (en) | Inhibition of glutathione transferase zeta | |
| US20210087582A1 (en) | Method and composition for endogenous production of constitutively activated receptors, and receptors with broader binding ranges or higher affinity than native receptors | |
| Han et al. | Pulmonary Delivery of Engineered Exosomes to Suppress Postoperative Melanoma Lung Metastasis through Preventing Premetastatic Niche Formation | |
| EP2578227B1 (en) | Cancer therapy method | |
| Kexin et al. | Picroside II promotes HSC apoptosis and inhibits the cholestatic liver fibrosis in Mdr2−/− mice by polarizing M1 macrophages and balancing immune responses | |
| WO2024170480A1 (en) | Debio-0123 in combination with temozolomide and radiotherapy for use in treating glioma | |
| Ganea et al. | Vasoactive intestinal peptide: an antiinflammatory neuropeptide | |
| US20100284911A1 (en) | Preparations and methods for treating malignancies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20151216 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20160520 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160607 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160907 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20161108 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20161205 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6055845 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |