JP5388564B2 - 糖尿病診療支援システム、コンピュータプログラム、及び記録媒体 - Google Patents
糖尿病診療支援システム、コンピュータプログラム、及び記録媒体 Download PDFInfo
- Publication number
- JP5388564B2 JP5388564B2 JP2008325875A JP2008325875A JP5388564B2 JP 5388564 B2 JP5388564 B2 JP 5388564B2 JP 2008325875 A JP2008325875 A JP 2008325875A JP 2008325875 A JP2008325875 A JP 2008325875A JP 5388564 B2 JP5388564 B2 JP 5388564B2
- Authority
- JP
- Japan
- Prior art keywords
- glucose
- block
- simulated
- insulin
- liver
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B40/00—ICT specially adapted for biostatistics; ICT specially adapted for bioinformatics-related machine learning or data mining, e.g. knowledge discovery or pattern finding
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B25/00—ICT specially adapted for hybridisation; ICT specially adapted for gene or protein expression
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B5/00—ICT specially adapted for modelling or simulations in systems biology, e.g. gene-regulatory networks, protein interaction networks or metabolic networks
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B5/00—ICT specially adapted for modelling or simulations in systems biology, e.g. gene-regulatory networks, protein interaction networks or metabolic networks
- G16B5/20—Probabilistic models
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H50/00—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics
- G16H50/50—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics for simulation or modelling of medical disorders
Landscapes
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medical Informatics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Computational Biology (AREA)
- Biotechnology (AREA)
- Evolutionary Biology (AREA)
- Biophysics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Theoretical Computer Science (AREA)
- Molecular Biology (AREA)
- Public Health (AREA)
- Physiology (AREA)
- Data Mining & Analysis (AREA)
- Epidemiology (AREA)
- Databases & Information Systems (AREA)
- Artificial Intelligence (AREA)
- Biomedical Technology (AREA)
- Bioethics (AREA)
- Evolutionary Computation (AREA)
- Probability & Statistics with Applications (AREA)
- Software Systems (AREA)
- Genetics & Genomics (AREA)
- Computer Vision & Pattern Recognition (AREA)
- Pathology (AREA)
- Primary Health Care (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Management, Administration, Business Operations System, And Electronic Commerce (AREA)
- Medical Treatment And Welfare Office Work (AREA)
- Measurement Of The Respiration, Hearing Ability, Form, And Blood Characteristics Of Living Organisms (AREA)
- Instructional Devices (AREA)
Description
特許文献1記載のシステムは、生体器官の機能が数理モデルによって表現された生体モデルを備えており、この生体モデルを用いて生体器官の機能をコンピュータによってシミュレートするものである。
また、前記肝臓ブロックは、外部からのグルコース吸収、末梢組織ブロックから与えられる血糖値、及び膵臓ブロックから与えられるインスリン分泌速度に基づいて、肝臓からの正味グルコース放出及び肝臓通過後インスリンを求める。肝臓からの正味グルコース放出は、末梢組織ブロックに与えられ、肝臓通過後インスリンは、インスリン動態ブロックに与えられる。
前記末梢組織ブロックは、肝臓ブロックからの正味グルコース放出及びインスリン動態ブロックからの末梢組織インスリン濃度に基づいて、血糖値を求める。血糖値は、膵臓ブロック及び肝臓ブロックに与えられる。
また、特許文献1の末梢組織ブロックは、肝臓ブロックからのグルコース放出量に基づいて血糖値(血漿中のグルコース量)を計算しているだけで、収支を勘案した末梢組織ブロック自体のグルコースの蓄積量若しくは濃度を求めているわけではない。
本発明によれば、複数の模擬臓器ブロックにおいて、グルコースの流入出及び/又はインスリンの流入出の収支をとることができるため、各模擬臓器ブロックにおけるグルコースの蓄積量若しくは濃度、及び/又は、インスリン蓄積量若しくは濃度を算出することができる。
なお、糖負荷試験としては、経口糖負荷試験(OGTT)や食事試験(MT)のように経口から糖を摂取するものがある。また、糖負荷試験の結果とは、例えば、採血により測定されたグルコース濃度(以下、採血グルコース濃度という)及び/又は採血により測定されたインスリン濃度(以下、採血インスリン濃度という)である。
また、前記診療支援情報生成部は、前記指標に基づいて前記患者の病態を分類し、分類された病態及び前記指標を含む診療支援情報を生成することが好ましい。
さらに他の観点からみた本発明は、前記コンピュータプログラムを記録した記録媒体である。
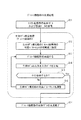
図1は、本発明の一実施の形態に係る糖尿病診療支援システム(以下、単に「システム」ともいう)のハードウェア構成を示すブロック図である。本実施の形態に係るシステム100は、本体110と、ディスプレイ120と、入力デバイス130とから主として構成されたコンピュータによって構成されている。本体110は、CPU110aと、ROM110bと、RAM110cと、ハードディスク110dと、読出装置110eと、入出力インタフェース110fと、画像出力インタフェース110hとから主として構成されており、CPU110a、ROM110b、RAM110c、ハードディスク110d、読出装置110e、入出力インタフェース110f、及び画像出力インタフェース110hは、バス110iによってデータ通信可能に接続されている。
ROM110bは、マスクROM、PROM、EPROM、EEPROM等によって構成されており、CPU110aに実行されるコンピュータプログラムおよびこれに用いるデータ等が記録されている。
ハードディスク110dは、オペレーティングシステム及びアプリケーションプログラム等、CPU110aに実行させるための種々のコンピュータプログラム及び当該コンピュータプログラムの実行に用いるデータがインストールされている。後述するアプリケーションプログラム140aも、このハードディスク110dにインストールされている。
また、ハードディスク110dには、例えば米マイクロソフト社が製造販売するWindows(登録商標)等のグラフィカルユーザインタフェース環境を提供するオペレーティングシステムがインストールされている。以下の説明においては、本実施形態に係るアプリケーションプログラム140aは当該オペレーティングシステム上で動作するものとしている。
画像出力インタフェース110hは、LCDまたはCRT等で構成されたディスプレイ120に接続されており、CPU110aから与えられた画像データに応じた映像信号をディスプレイ120に出力するようになっている。ディスプレイ120は、入力された映像信号にしたがって、画像(画面)を表示する。
本システム100は、OGTTなどの糖負荷試験の結果(採血グルコース濃度及び/又は採血インスリン濃度など)を模した疑似応答を再現する生体モデルMに基づいて、患者の糖尿病に関する病態分析に用いられる指標を生成し、糖尿病に関する診療支援情報を生成・出力するものである。
以下では、本システム100における生体モデルについて説明し、その後、システム100のその他の機能について説明する。
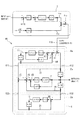
模擬臓器ブロックには、肝臓を模した模擬肝臓ブロック1(以下、「肝臓ブロック」という)、血漿を模した模擬血漿ブロック2(以下、「血漿ブロック」という)、末梢組織を模した模擬末梢ブロック3(以下、「末梢ブロック」という)、腸を模した模擬腸ブロック4(以下、「腸ブロック」という)、膵臓を模した模擬膵臓ブロック5(以下、「膵臓ブロック」という)を有している。
なお、可変パラメータは、本実施形態において例示されたものに限らず、本実施形態における固定パラメータ、設定パラメータの一部を可変パラメータとしてもよい。
後述するように、第1模擬臓器ブロック1,2,3と第2模擬臓器ブロック4,5とでは、臓器の表現の仕方が異なっている。
インスリン動態部M1には、肝臓ブロック1のインスリンに関する機能と、血漿ブロック2のインスリンに関する機能と、末梢ブロック3のインスリンに関する機能、及び膵臓ブロック5が属する。
グルコース動態部M2には、肝臓ブロック1のグルコースに関する機能と、血漿ブロック2のグルコースに関する機能と、末梢ブロック3のグルコースに関する機能、及び腸ブロック4が属する。
具体的には、第1模擬臓器ブロック1,2,3としては、ブロック間でのグルコース収支及びインスリン収支が同じ単位次元で計算され、グルコース及びインスリンの蓄積状態が、第1模擬臓器ブロック1,2,3単位で計算されるコンパートメントが採用されている。
つまり、第1模擬臓器ブロック1,2,3では、これら臓器における間質液又は血漿へのグルコース及びインスリンの流入出、臓器における取込・消失などが表現され、各臓器の間質液又は血漿でのグルコース及びインスリンの蓄積量が算出されるよう構成されている。
このように第1模擬臓器ブロック1,2,3では、血液循環に伴う間質液及び血漿におけるグルコース及びインスリンの移動が表現されているのである。
ただし、臓器としては、上記のものに限られるわけではなく、他の臓器を含んでも良い。
また、肝臓ブロック1には、膵臓ブロック5からのインスリン流入Y15及び血漿ブロック2からのインスリン流入Y12があり、血漿ブロック2へインスリン流出21がある。
図2に示すように、血漿ブロック2には、肝臓ブロック2からのグルコース流入X21及び末梢ブロック3からのグルコース流入X23があり、肝臓ブロック2へのグルコース流出X12及び末梢ブロック3へのグルコース流出X32がある。
また、血漿ブロック2には、肝臓ブロック2からのインスリン流入Y21及び末梢ブロック3からのインスリン流入Y23があり、肝臓ブロック2へのグルコース流出Y12及び末梢ブロックへのグルコース流出Y32がある。
末梢ブロック3は、末梢組織における間質液へのグルコース及びインスリンの流入出に基づくとともに、末梢の機能(末梢糖取り込みなど)によって末梢の間質液から増減する量をも考慮して、末梢(の間質液)におけるグルコース及びインスリンの蓄積量(濃度)などを表現するためのものである。
また、末梢ブロック3には、血漿ブロックからのインスリン流入Y32があり、血漿ブロックへインスリン流出Y23がある。
つまり、腸ブロック4は、腸の間質液におけるグルコース蓄積量ではなく、腸におけるグルコース吸収という腸の機能を表現したものである。
つまり、膵臓ブロック5は、膵臓の間質液におけるインスリン蓄積量ではなく、膵臓におけるインスリン分泌という膵臓の機能を表現したものである。
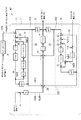
図3及び図4は、インスリン動態部M1及びグルコース動態部M2を更に詳細に示したものである。
図3に示すように、インスリン動態部M1は、膵臓ブロック5と、インスリン動態ブロック6とからなる。インスリン動態ブロック6は、肝臓ブロック1のうちインスリンに関する肝インスリン動態ブロック1a、血漿ブロック2のうちインスリンに関する血漿インスリン動態ブロック2a、及び末梢ブロック3のうちインスリンに関する末梢インスリン動態ブロック3aから構成されている。
Vi1=88
Vi2=45
Vi3=95
ki12=12.1
ki32=1.9
ki01=16.3
ki02=5.6
Rib=(ki01+ki02)*I2(0)
ki23=ki32
ki21=ki12+ki32+ki02−ki23
Sis:最小値0〜最大値500
Sid:最小値0〜6000
τis:最小値1〜240
Ris(0)=0
I1(0)=I2(0)
I3(0)=I2(0)
膵臓ブロック5において行われる演算の方程式は、下記(数1)の通りであり、採血グルコース濃度G2からインスリン分泌速度Ri10が算出される。下記式は、図3の膵臓ブロック5内のブロック線図と対応している。
上記式のRidは、グルコース濃度G2の「時間的変動に」依存したインスリン分泌速度であり、グルコース濃度の微分値(dG2/dt)と、グルコース濃度の時間的変動に依存したインスリン分泌感度Sidから算出される。
上記インスリン分泌速度Ris(t),Rid(t)を決定するパラメータであるSis,τis,Sidは、生体モデル生成時に、個々の患者に合わせて値が探索される可変パラメータであるため、個々の患者に合わせたインスリン分泌速度が得られる。
肝インスリン動態ブロック1aでは、インスリン流入として、Y15とY12があり、これらの和が、流入総量である。Y15とY12の和をとるため、演算部11が設けられている。
また、肝インスリン動態ブロック1aでは、インスリン流出として、Y21があり、肝インスリン動態ブロック1aにおけるインスリン濃度(蓄積量)を求めるには、インスリン流入総量からインスリン流出量Y21を減算する必要がある。この減算を行うため、インスリン流出Y21を流入側にフィードバックするためのループ14が設けられ、流入総量(Y15+Y12)から流出量Y21を減算するための演算部12が設けられている。
血漿インスリン動態ブロック2aでは、インスリン流入として、Y21とY23があり、これらの和が、流入総量である。Y21とY23の和をとるため、演算部15が設けられている。
また、血漿インスリン動態ブロック2aでは、インスリン流出として、Y12及びY32があり、血漿インスリン動態ブロック2aにおけるインスリン濃度(蓄積量)を求めるには、インスリン流入総量(Y21+Y23)からインスリン流出総量(Y12+Y32)を減算する必要がある。この減算を行うため、インスリン流出を流入側にフィードバックするためのループ16,17が設けられ、流入総量(Y21+Y23)から流出総量(Y12+Y32)を減算するための演算部18が設けられている。
末梢インスリン動態ブロック3aでは、インスリン流入として、Y32があり、インスリン流出として、Y23がある。したがって、末梢インスリン動態ブロック3aにおけるインスリン濃度(蓄積量)を求めるには、インスリン流入量Y32からインスリン流出量Y23を減算する必要がある。この減算を行うため、インスリン流出Y23を流入側にフィードバックするためのループ21が設けられ、流入量Y32から流出量Y23を減算するための演算部21が設けられている。
図4に示すように、グルコース動態部M2は、腸ブロック5と、グルコース動態ブロック7とからなる。グルコース動態ブロック7は、肝臓ブロック1のうちグルコースに関する肝グルコース動態ブロック1b、血漿ブロック2のうちグルコースに関する血漿グルコース動態ブロック2b、及び末梢ブロック3のうちグルコースに関する末梢グルコース動態ブロック3bから構成されている。
Vg1=0.88
Vg2=0.45
Vg3=0.95
kg12=0.464
kg32=0.131
Pup=0.008
Poff=1.9
Pexp=1.38
P50=0.2
aoff=160
b10=1.4
c01=1.5
kg23=kg32−(Rg20(0)/G2(0))
kg21=kg12
a10=aoff−a01
b01=b10
I50=p50*G2(0)
a01:最小値10〜最大値150
Spgu:最小値0〜最大値0.16
Rg20(0)=(Pup×G2(0)+poff)
G1(0)=G2(0)
G3(0)=G2(0)
腸ブロック4は、肝グルコース動態ブロック1bへの外因性グルコース流入速度Rg10(X14)を算出する。肝グルコース動態ブロック1bへの外因性グルコース流入速度Rg10は、上記(数7)に示すように、OGTTにおける経口からのグルコース負荷量Dに、Weibull関数を乗じることで算出される。
したがって、肝グルコース動態ブロック1bへの外因性グルコース流入速度Rg10(X14)は、個々の患者に合わせて調整される。つまり、腸ブロック4は、肝グルコース動態ブロック1bへの外因性グルコース流入速度をコントロールするコントロール部として機能する。
肝グルコース動態ブロック1bでは、グルコース流入として、X14とX12があり、これらの和が、流入総量である。X14とX12の和をとるため、演算部22が設けられている。
また、肝グルコース動態ブロック1bでは、グルコース流出として、X21aがあり、肝グルコース動態ブロック1bにおけるグルコース濃度(蓄積量)を求めるには、グルコース流入総量(X14+X12)からグルコース流出量X21aを減算する必要がある。この減算を行うため、グルコース流出X21aを流入側にフィードバックするためのループ25が設けられ、グルコース流入総量(X14+X12)からグルコース流出量X21aを減算する演算部23が設けられている。
ここで、肝糖取り込み率kg01を求める式は、上記(数9)に示すように、パラメータa01を含み、このパラメータa01は、生体モデル生成時に、個々の患者に合わせて値が探索される可変パラメータであるため、個々の患者に合わせた肝糖取り込み率kg01が得られ、ひいては個々の患者に合わせた肝糖取込速度Rg01が得られる。
また、パラメータa01とパラメータa10が相互依存する関係式を用いているのは、肝糖取込機能が低下するほど、肝臓からの糖放出は増加するという関係を表現するためのものである。
肝糖産生速度Rg20は、前記(数8)に基づいて算出される。肝糖産生速度Rg20を算出する(数8)には、(数6)に示す肝糖産生抑制に関わる関数fpが含まれている。
算出された肝糖産生速度Rg20は、血漿グルコース動態ブロック2bへの第2のグルコース流入速度(X21b)として、血漿グルコース動態ブロック2bへ出力される。
このように、肝グルコース動態ブロック1bから血漿グルコース動態ブロック2bへは、2つのグルコース流入速度X21a,X21bが与えられる。
血漿グルコース動態ブロック2bでは、グルコース流入として、X21aとX21bとX23とがあり、これらの和が、流入総量である。X21aとX21bとX23の和をとるため、演算部26が設けられている。
また、血漿グルコース動態ブロック2bでは、グルコース流出として、X12及びX32があり、血漿グルコース動態ブロック2bにおけるグルコース濃度(蓄積量)を求めるには、グルコース流入総量(X21a+X21b+X23)からグルコース流出総量(X12+X32)を減算する必要がある。この減算を行うため、グルコース流出を流入側にフィードバックするためのループ28,29が設けられ、流入総量(X21a+X21b+X23)から流出総量(X12+X32)を減算するための演算部27が設けられている。
末梢グルコース動態ブロック3bでは、グルコース流入として、X32があり、グルコース流出として、X23がある。したがって、末梢グルコース動態ブロック3bにおけるグルコース濃度(蓄積量)を求めるには、グルコース流入量X32からグルコース流出量X23を減算する必要がある。この減算を行うため、グルコース流出X23を流入側にフィードバックするためのループ33が設けられ、流入量X32から流出量X23を減算するための演算部30が設けられている。
基礎に対する末梢糖取り込みの速度の変化Rg03は、上記(数11)に示すように、基礎に対する末梢糖取り込み率の変化kg03(t)に、末梢グルコース濃度G3(t)を乗じることによって算出される。
この末梢糖取込感度Spguは、生体モデル生成時に、個々の患者に合わせて値が探索される可変パラメータであるため、個々の患者に合わせた末梢糖取込感度Spguが得られ、ひいては個々の患者に合わせた末梢糖取り込み速度PGU(t)が得られる。
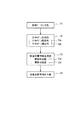
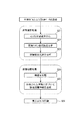
図4は、本システム100の全体構成を示している。このシステム100は、診療データ入力部31、生体モデル生成部32、診療支援情報生成部33、及び診療支援情報出力部34を有している。生体モデル生成部32は、生体モデル推定部32aと生体モデル構成部32bとを備えている。また、診療支援情報生成部33は、病態推定部32aと病態分類部32bとを備えている。
入力された情報は、生体モデル生成部32等において使用できるように、ハードディスク110dなどの不揮発性記憶装置に格納される。
入力部31によって入力される診療データとしては、採血グルコース濃度G2_ref、採血インスリン濃度I2_ref(t)のほか、経口からのグルコース負荷量Dがある。また、入力される所見情報(臨床所見)としては、肥満または痩せの状態、糖質の摂取状態などが挙げられる。
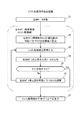
生体モデル推定部32aは、可変パラメータの候補値を、生体モデルMの可変パラメータとしてセットし、生体モデルMの演算を生体モデル構成部32bに行わせる。これにより生体モデルMから出力される血漿グルコース濃度G2(t)及び血漿インスリン濃度I2(t)は、それぞれ、採血グルコース濃度G2_ref(t)及び採血インスリン濃度I2_ref(t)と比較される。
こうして決定された可変パラメータを持つ生体モデルMは、個々の患者の糖負荷試験の結果を模した疑似応答を再現することができるため、数理モデルとしての生体モデルMが持つ各種パラメータ・変数は、個々の患者の特性を表したものとなる。
そして、生体モデル推定部32aは、インスリン動態ブロックM1の可変パラメータセット(Sis,Sid,τis)を、適当な初期値に設定する(ステップS2)。
なお、生成されたインスリン動態部M1(の変数・パラメータの各値)は、記憶装置に記憶される。
なお、生成されたグルコース動態部M2(の変数・パラメータの各値)は、記憶装置に記憶される。
なお、図8及び図9において、正常型生体モデルの可変パラメータは、Sis=21.2、Sid=122.7、τis=4.7、a01=75.6、Spgu=10.4に調整されており、糖尿病型生体モデルの可変パラメータは、Sis=3.1、Sid=24、τis=19.2、a01=84.7、Spgu=12.9に調整されている。
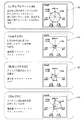
具体的には、生体モデルMの各値及び入力された診療データに基づいて、上記観点からの病態分析のための指標を演算する。指標としては、例えば、「基礎分泌」、「分泌量」、「分泌感度」、「末梢糖取込」、「末梢感受性」、「肝糖取込」、「肝糖産生」が挙げられる。
「分泌量」とは、OGTTにおけるインスリン分泌総量であり、生体モデルMの血漿インスリン濃度I2(t)の積分値から算出される。
「分泌感度」とは、血糖依存性インスリン分泌感度であり、生体モデルMの可変パラメータであるグルコース濃度に依存したインスリン分泌感度Sisから算出される。
「末梢感受性」とは、末梢インスリン感受性であり、生体モデルMの可変パラメータである末梢糖取り込み感度Spguから算出される。
「肝糖取込」とは、OGTTにおける肝糖取込総量であり、生体モデルMの変数である肝糖取込速度Rg01(t)の積分値から算出される。なお、肝糖取込速度Rg01は、肝グルコース濃度G1(t)及び可変パラメータa01に基づいて算出される値である。
「肝糖産生」とは、OGTTにおける肝糖産生総量であり、生体モデルMの変数である肝糖産生速度Rg20(t)の積分値から算出される。なお、肝糖産生速度Rg20(t)は、肝インスリン濃度I1(t)に基づいて算出される値である。
また、他の分類例としては、「スルホニル尿素薬型」、「グリニド型」、「チアゾリジン誘導体薬型」、「ビグアナイド薬型」など、各薬剤の適応グループに分類するものであってもよい。
また、病態プロファイルに含まれる各指標の値に基づく所定の分類基準を予め定めておき、当該分類基準に基づいて病態を分類してもよい。また、薬剤の作用部位に対応する生体モデルのパラメータを擬似的に改善させるなど、生体モデルを利用した薬効予測結果を用いて、病態を分類してもよい。このように、病態分類の方法は特に限定されるものではない。
M 生体モデル
M1 インスリン動態部
M2 グルコース動態部
1 模擬肝臓ブロック
1a 肝インスリン動態ブロック
1b 肝グルコース動態ブロック
2 模擬血漿ブロック
2a 血漿インスリン動態ブロック
2b 血漿グルコース動態ブロック
3 模擬末梢ブロック
3a 末梢インスリン動態ブロック
3b 末梢グルコース動態ブロック
4 模擬腸ブロック(コントロール部)
5 模擬膵臓ブロック
31 診療データ入力部
32 生体モデル生成部
33 診療支援情報生成部
34 診療支援情報出力部
Claims (10)
- 患者に対する糖負荷試験の結果を模した疑似応答を再現する生体モデルに基づいて、前記患者の診療支援情報を生成する糖尿病診療支援システムであって、
患者の採血グルコース濃度及び/又は採血インスリン濃度を含む診療データを入力するための入力部と、
糖尿病に関連する臓器の機能を複数のパラメータを有する数理モデルとして記述した生体モデルを記憶する記憶部と、
前記記憶部に記憶された前記生体モデルの出力が前記入力部によって入力された診療データと合致するまで各パラメータの値を調整し、前記診療データと合致するパラメータのセットを求め、当該パラメータのセットを持つ患者固有の生体モデルを生成する生体モデル生成部と、
前記生体モデル生成部によって生成された生体モデルに基づいて、患者の病態を分析し、診療支援情報を生成する診療支援情報生成部と、を備え、
前記記憶部に記憶された前記生体モデルは、患者の肝臓の機能と当該肝臓における間質液とを表現した模擬肝臓ブロック、患者の血漿を表現した模擬血漿ブロック、及び患者の末梢組織の機能と当該末梢組織における間質液とを表現した模擬末梢ブロックを含む複数の模擬臓器ブロックを有し、かつ前記模擬肝臓ブロック、前記模擬血漿ブロック、及び前記模擬末梢ブロックの間で、血液循環に伴う間質液、及び血漿におけるグルコースの流入出及び/又はインスリンの流入出が相互に生じるように構成され、
前記模擬肝臓ブロック、前記模擬血漿ブロック、及び前記模擬末梢ブロックのそれぞれは、各模擬臓器ブロックのグルコース流入出量及び/又はインスリン流入出量に基づいて、各模擬臓器ブロックにおけるグルコースの蓄積量若しくは濃度、及び/又は、インスリン蓄積量若しくは濃度を算出するよう構成され、
前記診療支援情報生成部は、前記模擬肝臓ブロック、前記模擬血漿ブロック、及び前記模擬末梢ブロックのそれぞれにおけるグルコースの蓄積量若しくは濃度、及び/又は、インスリン蓄積量若しくは濃度に基づいて、患者の病態を分析することを特徴とする糖尿病診療支援システム。 - 前記生体モデルは、前記糖負荷試験におけるグルコース負荷量が前記生体モデル外からの外因性グルコース量として与えられる腸ブロックを有し、
前記腸ブロックは、外因性グルコース量に基づいて、前記模擬肝臓ブロックへ与えられる外因性グルコース流入速度を算出するように構成されている請求項1記載の糖尿病診療支援システム。 - 前記生体モデルは、グルコース濃度に基づいてインスリンを分泌する膵臓に対応した模擬膵臓ブロックを更に備え、
前記模擬膵臓ブロックは、前記模擬肝臓ブロックへ流入させるためのインスリンの分泌量を、前記グルコース濃度とともに、前記グルコース濃度の時間的変動にも依存して決定するよう構成されている請求項1又は2に記載の糖尿病診療支援システム。 - 前記診療支援情報生成部は、前記模擬肝臓ブロック、前記模擬血漿ブロック、及び前記模擬末梢ブロックのそれぞれにおけるグルコースの蓄積量若しくは濃度、及び/又は、インスリン蓄積量若しくは濃度に基づいて、前記患者の病態の分析に用いられる指標を生成する手段及び/又は病態を分類する手段を更に備える請求項1〜3のいずれか1項に記載の糖尿病診療支援システム。
- 前記模擬肝臓ブロックは、当該模擬肝臓ブロックにおけるグルコースの蓄積量若しくは濃度に基づいて、当該模擬肝臓ブロックにおける肝糖取込及び/又は肝糖産生の機能を示す値を演算するよう構成されているとともに、
前記肝糖取込及び/又は前記肝糖産生の機能によるグルコースの蓄積量若しくは濃度の変動を算出しながら、当該模擬肝臓ブロックにおけるグルコースの蓄積量若しくは濃度を算出するよう構成されている請求項1〜4のいずれか1項に記載の糖尿病診療支援システム。 - 前記模擬末梢ブロックは、当該模擬末梢ブロックにおけるグルコースの蓄積量若しくは濃度に基づいて、当該模擬末梢ブロックにおける末梢糖取込機能を示す値を演算するように構成されているとともに、
前記末梢糖取込機能によるグルコースの蓄積量若しくは濃度の変動を算出しながら、当該模擬末梢ブロックにおけるグルコースの蓄積量若しくは濃度を算出するよう構成されている請求項1〜5のいずれか1項に記載の糖尿病診療支援システム。 - 前記診療支援情報生成部は、前記指標として、空腹時のインスリン分泌量、血糖依存性インスリン分泌感度、糖負荷試験における末梢糖取込総量の変化量、末梢インスリン感受性、糖負荷試験における肝糖取込総量、及び糖負荷試験における肝糖産生総量の少なくとも一つを生成する請求項4に記載の糖尿病診療支援システム。
- 前記診療支援情報生成部は、前記指標に基づいて前記患者の病態を分類し、分類された病態及び前記指標を含む診療支援情報を生成する、請求項7に記載の糖尿病診療支援システム。
- 患者に対する糖負荷試験の結果を模した疑似応答を再現する生体モデルに基づいて、前記患者の診療支援情報を生成する糖尿病診療支援システムとしてコンピュータを機能させるためのコンピュータプログラムであって、
当該コンピュータを、患者の採血グルコース濃度及び/又は採血インスリン濃度を含む診療データの入力を受け付ける入力受付手段、
糖尿病に関連する臓器の機能を複数のパラメータを有する数理モデルとして記述した生体モデルを記憶部から読み出し、読み出した生体モデルの出力が前記入力受付手段によって受け付けた診療データと合致するまで各パラメータの値を調整し、診療データと合致するパラメータのセットを求め、当該パラメータセットを持つ患者固有の生体モデルを生成する生体モデル生成手段、及び
前記生体モデル生成手段によって生成された生体モデルに基づいて、患者の病態を分析し、診療支援情報を生成する診療支援情報生成手段、として機能させ、
前記記憶部から読み出された前記生体モデルは、患者の肝臓の機能と当該肝臓における間質液とを表現した模擬肝臓ブロック、患者の血漿を表現した模擬血漿ブロック、及び患者の末梢組織の機能と当該末梢組織における間質液とを表現した模擬末梢ブロックを含む複数の模擬臓器ブロックを有し、前記模擬肝臓ブロック、前記模擬血漿ブロック、及び前記模擬末梢ブロックの間で、血液循環に伴う間質液、及び血漿におけるグルコースの流入出及び/又はインスリンの流入出が相互に生じるように構成され、
前記模擬肝臓ブロック、前記模擬血漿ブロック、及び前記模擬末梢ブロックのそれぞれは、各模擬臓器ブロックのグルコース流入出量及び/又はインスリン流入出量に基づいて、各模擬臓器ブロックにおけるグルコースの蓄積量若しくは濃度、及び/又は、インスリン蓄積量若しくは濃度を算出するよう構成され、
前記診療支援情報生成手段は、前記模擬肝臓ブロック、前記模擬血漿ブロック、及び前記模擬末梢ブロックのそれぞれにおけるグルコースの蓄積量若しくは濃度、及び/又は、インスリン蓄積量若しくは濃度に基づいて、患者の病態を分析することを特徴とするコンピュータプログラム。 - 請求項9に記載のコンピュータプログラムを記録した記録媒体。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008325875A JP5388564B2 (ja) | 2008-12-22 | 2008-12-22 | 糖尿病診療支援システム、コンピュータプログラム、及び記録媒体 |
| CN200910254160.8A CN101763464B (zh) | 2008-12-22 | 2009-12-10 | 糖尿病诊疗支援装置 |
| EP09015715.7A EP2224363A3 (en) | 2008-12-22 | 2009-12-18 | Diagnostic support apparatus for diabetes and computer program product |
| US12/644,863 US9202009B2 (en) | 2008-12-22 | 2009-12-22 | Diagnostic support apparatus for diabetes and computer program product |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008325875A JP5388564B2 (ja) | 2008-12-22 | 2008-12-22 | 糖尿病診療支援システム、コンピュータプログラム、及び記録媒体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010146491A JP2010146491A (ja) | 2010-07-01 |
| JP5388564B2 true JP5388564B2 (ja) | 2014-01-15 |
Family
ID=42267338
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008325875A Expired - Fee Related JP5388564B2 (ja) | 2008-12-22 | 2008-12-22 | 糖尿病診療支援システム、コンピュータプログラム、及び記録媒体 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9202009B2 (ja) |
| EP (1) | EP2224363A3 (ja) |
| JP (1) | JP5388564B2 (ja) |
| CN (1) | CN101763464B (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2880175A4 (en) | 2012-08-03 | 2016-04-06 | Univ Virginia Patent Found | COMPUTER SIMULATION FOR CHECKING AND MONITORING TREATMENT STRATEGIES FOR STRESS-RELATED HYPERGLYCEMIA |
| WO2016061308A1 (en) | 2014-10-17 | 2016-04-21 | Kahlbaugh Bradley E | Human metabolic condition management |
| CN109903838B (zh) * | 2019-02-22 | 2020-01-10 | 爱尔眼科医院集团股份有限公司 | 糖尿病及糖尿病视网膜病变网络防治系统 |
| CN117373681B (zh) * | 2023-10-30 | 2024-04-26 | 中国航天科工集团七三一医院 | 一种基于血糖调节系统作用的骨折愈合仿真方法及系统 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4547173B2 (ja) * | 2004-03-17 | 2010-09-22 | シスメックス株式会社 | 糖尿病診療支援システム |
| JP5102439B2 (ja) * | 2004-05-11 | 2012-12-19 | シスメックス株式会社 | シミュレーションシステム及びコンピュータプログラム |
| US20090312620A1 (en) * | 2005-04-27 | 2009-12-17 | Hou-Mei Henry Chang | Diabetes monitor |
| JP2006313481A (ja) | 2005-05-09 | 2006-11-16 | Sysmex Corp | 生体器官の機能のシミュレーションシステム及びそのプログラム |
| US8758245B2 (en) * | 2007-03-20 | 2014-06-24 | Lifescan, Inc. | Systems and methods for pattern recognition in diabetes management |
-
2008
- 2008-12-22 JP JP2008325875A patent/JP5388564B2/ja not_active Expired - Fee Related
-
2009
- 2009-12-10 CN CN200910254160.8A patent/CN101763464B/zh not_active Expired - Fee Related
- 2009-12-18 EP EP09015715.7A patent/EP2224363A3/en not_active Withdrawn
- 2009-12-22 US US12/644,863 patent/US9202009B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2010146491A (ja) | 2010-07-01 |
| US9202009B2 (en) | 2015-12-01 |
| EP2224363A3 (en) | 2013-07-31 |
| US20100161299A1 (en) | 2010-06-24 |
| CN101763464B (zh) | 2015-12-09 |
| CN101763464A (zh) | 2010-06-30 |
| EP2224363A2 (en) | 2010-09-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Romero-Brufau et al. | Using machine learning to improve the accuracy of patient deterioration predictions: Mayo Clinic Early Warning Score (MC-EWS) | |
| JP7293050B2 (ja) | 軽度認知障害判定システム | |
| Viceconti et al. | Big data, big knowledge: big data for personalized healthcare | |
| EP2911642B1 (en) | Drug monitoring and regulation systems and methods | |
| JP4781710B2 (ja) | 治療効果予測システム及びそのプログラム | |
| US20150148621A1 (en) | Methods and systems for creating a preventative care plan in mental illness treatment | |
| JP2007507814A (ja) | 患者に固有の結果のシミュレーション | |
| CN111297329B (zh) | 预测糖尿病患者心血管并发症动态发病风险的方法及系统 | |
| US20210241909A1 (en) | Method and a system for evaluating treatment strategies on a virtual model of a patient | |
| Narayanan et al. | An inverse method for mechanical characterization of heterogeneous diseased arteries using intravascular imaging | |
| EP4173006A2 (en) | System and method for peri-anaesthetic risk evaluation | |
| WO2020027213A1 (ja) | 認知症リスクの提示システムおよび方法 | |
| CN117133471A (zh) | 急性主动脉夹层疾病的输血预测方法、系统、设备及介质 | |
| JP5388564B2 (ja) | 糖尿病診療支援システム、コンピュータプログラム、及び記録媒体 | |
| JP7027359B2 (ja) | ヘルスケアデータ分析装置及びヘルスケアデータ分析方法 | |
| Herrgårdh et al. | Digital twins and hybrid modelling for simulation of physiological variables and stroke risk | |
| JP2006304833A (ja) | 診断支援システム及びコンピュータプログラム | |
| Meixide et al. | Neural interval‐censored survival regression with feature selection | |
| JP5102439B2 (ja) | シミュレーションシステム及びコンピュータプログラム | |
| CN120260941A (zh) | 一种心血管及代谢疾病的风险预测方法及系统 | |
| JP7266807B1 (ja) | 生活習慣予測装置、生活習慣予測システム、生活習慣予測方法、生活習慣予測プログラムおよび記録媒体 | |
| EP1722311A1 (en) | Simulation system for functions of biological organs and recording medium in which program therefor is recorded | |
| Cate | Quantile-Based Precision Medicine for Diabetes Management: A High-Dimensional Single-Index Regression Framework | |
| Saxena | Predicting the Prognosis of Ulcerative Colitis with Machine Learning | |
| CN120072156A (zh) | 一种溃疡性结肠炎严重程度评估方法及系统 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20111214 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130130 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130226 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130426 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130917 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20131008 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 5388564 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |