JP5060304B2 - 閉ループ神経刺激のためのシステム - Google Patents
閉ループ神経刺激のためのシステム Download PDFInfo
- Publication number
- JP5060304B2 JP5060304B2 JP2007543316A JP2007543316A JP5060304B2 JP 5060304 B2 JP5060304 B2 JP 5060304B2 JP 2007543316 A JP2007543316 A JP 2007543316A JP 2007543316 A JP2007543316 A JP 2007543316A JP 5060304 B2 JP5060304 B2 JP 5060304B2
- Authority
- JP
- Japan
- Prior art keywords
- neural
- nerve
- signal
- stimulation
- sensed
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/3605—Implantable neurostimulators for stimulating central or peripheral nerve system
- A61N1/3606—Implantable neurostimulators for stimulating central or peripheral nerve system adapted for a particular treatment
- A61N1/36114—Cardiac control, e.g. by vagal stimulation
Description
本明細書において、2004年11月18日に出願した米国特許出願第10/992319号、および米国特許法第119(e)条のもとに2005年8月29日に出願した米国仮出願第60/712302号の利点を主張する2005年11月16日に出願した米国特許出願第XX/XXXXXX号(代理人整理番号第279.957US1)、出願が参照により本明細書に組み込まれている、米国特許出願第10/992320号に対する優先権の利益が主張される。
以下の同一出願人による米国特許出願が関連し、全体として参照により本明細書に組み込まれている。第10/746846号「Automatic Baroreflex Modulation Based on Cardiac Activity」、2003年12月24日出願。
読者が本開示を理解する上で役立つように、高血圧と圧受容体に関連する生理機能について簡単に説明される。この簡単な説明では、高血圧、自律神経系、圧反射を扱う。
神経刺激装置の例は、高血圧症を治療するために使用される抗高血圧(AHT)機器またはAHTコンポーネントを含む。本主題のさまざまな実施形態は、独立の埋め込み型神経刺激装置システムを含み、組み込まれたNSと心調律管理(CRM)コンポーネントを有する埋め込み型機器を含み、無線によるか、または埋め込み型機器を接続するリード線を通じて相互に通信することができる少なくとも1つの埋め込み型NS機器および埋め込み型CRM機器を備えるシステムを含む。埋め込み型システムが示され、説明されるが、本主題のさまざまな態様および実施形態は、外部機器において実施される。
Claims (66)
- 閉ループ神経刺激治療を、反射回路を含む自律神経系(ANS)内の所望の神経ターゲットに伝達して所望の神経反応を生じさせる機器であって、
リードを接続するように適合されたポートと、
前記ポートに接続されたパルス発生器であって、所望の神経ターゲットを刺激して、ANSの反射回路を介して神経感知部位における神経作用固有レベルに影響を与える反射反応を誘引するために神経刺激信号を前記リードに供給するよう適合されたパルス発生器と、
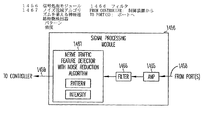
前記ポートに接続され、前記リードから、前記神経ターゲットへの刺激に対する感知された反射神経反応を示す前記神経感知部位における感知された神経作用を表す神経連絡信号を受け取り、その神経連絡信号を前記神経連絡を示す信号に処理するように適合された信号処理モジュールと、
前記パルス発生器と前記信号処理モジュールに接続された制御装置であって、前記神経刺激信号に対し所望の反射神経反応結果がでるように前記感知された反射神経反応に基づいて前記神経刺激信号による神経刺激治療を実施し、前記神経刺激信号の少なくとも1つの刺激パラメータを調整するように適合される制御装置と、
から構成され、
前記制御装置は、
前記感知された反射神経反応を示す前記信号のための、メモリに格納されたプログラム可能なターゲット値と、
前記信号処理モジュールから前記感知された反射神経反応を示す前記信号を受け取り、前記感知された反射神経反応を示す前記信号を前記プログラム可能なターゲット値と比較し、前記閉ループ神経刺激治療を制御するのに用いられるフィードバック信号を生成するように適合されたフィードバック比較器と、
前記神経ターゲットでの刺激イベントを前記神経感知部位における感知された神経作用に関連付けて、前記刺激イベントと前記感知された神経作用との間の因果関係を確認し、ANSの反射回路を介して前記感知された神経作用が前記刺激イベントと因果関係を有するときを示す関連付け結果を提供するように適合された連想器と、
前記関連付け結果を受け取り前記感知された神経作用が前記感知された反射神経反応であることを確認し、前記フィードバック信号を受け取り、前記感知された反射神経反応を前記所望の神経反応に集中させるために前記少なくとも1つの刺激パラメータを調整するように、前記フィードバック信号を用いて刺激制御信号を生成するように適合された神経制御装置と、を含むことを特徴とする機器。 - 前記神経連絡信号は神経連絡パターンを示す信号を含むことを特徴とする請求項1に記載の機器。
- 前記神経連絡信号は神経連絡強度を示す信号を含むことを特徴とする請求項1に記載の機器。
- 前記神経連絡信号は神経連絡パターンと神経連絡強度を示す信号を含むことを特徴とする請求項1に記載の機器。
- 信号処理モジュールは前記神経連絡信号の特徴を識別するためのノイズ低減アルゴリズムを実装するように適合されることを特徴とする請求項1に記載の機器。
- 前記ノイズ低減アルゴリズムはウェーブレット変換を含むことを特徴とする請求項5に記載の機器。
- 前記ノイズ低減アルゴリズムは前記神経連絡信号のパターンと強度を識別することを特徴とする請求項5に記載の機器。
- 前記信号処理モジュールは神経連絡を処理し、監視するように適合された増幅器とフィルタを含むことを特徴とする請求項1に記載の機器。
- 前記増幅器は約1,000から約99,000のゲインを備える増幅器を含むことを特徴とする請求項8に記載の機器。
- 前記フィルタは約30Hzから約3,000Hzの範囲の周波数を通過させる帯域フィルタを含むことを特徴とする請求項9に記載の機器。
- 前記制御装置は前記神経刺激信号の継続時間を調整するための神経刺激プロトコルを実施するように適合されることを特徴とする請求項1に記載の機器。
- 前記制御装置は前記神経刺激信号の周波数を調整するための神経刺激プロトコルを実施するように適合されることを特徴とする請求項1に記載の機器。
- 前記制御装置は前記神経刺激信号の振幅を調整するための神経刺激プロトコルを実施するように適合されることを特徴とする請求項1に記載の機器。
- 前記制御装置は前記神経刺激信号の2つ以上のパラメータを調整するための神経刺激プロトコルを実施するように適合され、前記2つ以上のパラメータは前記神経刺激信号の継続時間、前記神経刺激信号の周波数、前記神経刺激信号の振幅からなるパラメータグループから選択されることを特徴とする請求項1に記載の機器。
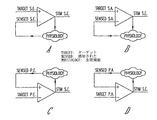
- 前記制御装置は第1の部位において前記神経連絡信号を感知し、前記第1の部位において前記神経刺激信号を適用するように適合されることを特徴とする請求項1に記載の機器。
- 前記制御装置は神経経路上の第1の部位において前記神経連絡信号を感知し、前記神経経路上の第2の部位において前記神経刺激信号を適用するように適合されることを特徴とする請求項1に記載の機器。
- 前記制御装置は同時に前記神経連絡信号を感知して前記神経刺激信号を適用するように適合されることを特徴とする請求項16に記載の機器。
- 閉ループ神経刺激治療を、反射回路を含む自律神経系(ANS)内の所望の神経ターゲットに伝達して所望の神経反応を生じさせる機器であって、
少なくとも第1のリードに接続するように適合された第1のポートと第2のリードに接続するように適合された第2のポートと、
前記ポートに接続されたパルス発生器であって、所望の神経ターゲットを刺激して、ANSの反射回路を介して神経感知部位における神経作用固有レベルに影響を与える反射反応を誘引するために第1の神経刺激信号を前記第1のリードに供給するように適合されたパルス発生器と、
少なくとも前記第2のポートに接続され、前記第2のリードから、前記神経ターゲットへの刺激に対して感知された反射神経反応を示す前記神経感知部位における感知された神経作用を表す神経連絡信号を受け取り、その神経連絡信号を、前記第2のリードの電極において神経連絡を示す第1の信号に処理するように適合された信号処理モジュールと、
前記パルス発生器と前記信号処理モジュールに接続された制御装置であって、前記神経刺激信号に対し所望の反射神経反応結果がでるように前記感知された反射神経反応に基づき、前記神経刺激信号による神経刺激治療を実施し、前記第1の神経刺激信号の少なくとも1つの刺激パラメータを調整するように適合される制御装置と、
から構成され、
前記制御装置は、
前記感知された反射神経反応を示す前記信号のための、メモリに格納されたプログラム可能なターゲット値と、
前記信号処理モジュールから前記感知された反射神経反応を示す前記信号を受け取り、前記感知された反射神経反応を示す前記信号を前記プログラム可能なターゲット値と比較し、前記閉ループ神経刺激治療を制御するのに用いられるフィードバック信号を生成するように適合されたフィードバック比較器と、
前記神経ターゲットでの刺激イベントを前記神経感知部位における感知された神経作用に関連付けて、前記刺激イベントと前記感知された神経作用との間の因果関係を確認し、ANSの反射回路を介して前記感知された神経作用が前記刺激イベントと因果関係を有するときを示す関連付け結果を提供するように適合された連想器と、
前記関連付け結果を受け取り前記感知された神経作用が前記感知された反射神経反応であることを確認し、前記フィードバック信号を受け取り、前記感知された反射神経反応を前記所望の神経反応に集中させるために前記少なくとも1つの刺激パラメータを調整するように、前記フィードバック信号を用いて刺激制御信号を生成するように適合された神経制御装置と、を含むことを特徴とする機器。 - 前記パルス発生器はさらに、前記第2のポートに接続され、第2の神経刺激信号を前記第2のリードに供給するように適合され、
前記信号処理モジュールはさらに、前記第1のポートに接続され、前記第1のリードから神経連絡信号を受け取り、この神経連絡信号を、前記第2のリードの電極において前記神経連絡を示す第2の信号に処理するように適合され、
前記制御装置によって実施される刺激プロトコルは、前記神経連絡を示す前記第2の信号に基づいて所望の神経刺激パラメータを持つ前記第2の神経刺激信号を供給するように適合されることを特徴とする請求項18に記載の機器。 - 前記神経連絡を示す前記信号は神経連絡パターンを示す信号を含むことを特徴とする請求項19に記載の機器。
- 前記神経連絡を示す前記第1と第2の信号は、神経連絡強度を示す信号を含むことを特徴とする請求項19に記載の機器。
- 前記神経連絡を示す前記第1と第2の信号は、神経連絡パターンと神経連絡強度を示す信号を含むことを特徴とする請求項19に記載の機器。
- 信号処理モジュールは前記神経連絡信号の特徴を識別するためのノイズ低減アルゴリズムを実装するように適合されることを特徴とする請求項18に記載の機器。
- 前記ノイズ低減アルゴリズムはウェーブレット変換を含むことを特徴とする請求項23に記載の機器。
- 前記信号処理モジュールは、約1,000から約99,000のゲインを備える増幅器と、約30Hzから約3,000Hzの範囲の信号を通過させる帯域フィルタとを含むことを特徴とする請求項23に記載の機器。
- 前記神経連絡は求心性神経部位において神経連絡を含み、前記制御装置は求心性神経部位において前記神経連絡を示す前記第1の信号に基づいて遠心性神経部位の所望のパラメータを有する前記第1の神経刺激信号を供給するように適合されることを特徴とする請求項18に記載の機器。
- 前記神経連絡は第1の神経経路上の神経連絡を含み、前記制御装置は前記第1の神経経路において前記神経連絡を示す前記第1の信号に基づいて第2の神経経路の所望のパラメータを有する前記第1の神経刺激信号を供給するように適合されることを特徴とする請求項18に記載の機器。
- 閉ループ神経刺激治療を、反射回路を含む自律神経系(ANS)内の所望の神経ターゲットに伝達して所望の神経反応を生じさせる機器であって、
自律神経系(ANS)内の神経刺激部位において適用される神経刺激信号を供給し、前記ANSの反射回路を介して神経感知部位における神経作用固有レベルに作用する反射反応を誘引するように適合されたパルス発生器と、
前記神経刺激部位へ与えた刺激に対し感知された反射神経反応を示す前記ANS内の前記神経感知部位において感知された神経連絡を受け取り、感知された神経連絡を処理するように適合された信号処理モジュールと、
前記パルス発生器に接続され、前記神経刺激信号を生成するために前記パルス発生器に神経刺激制御信号を供給するように適合され、前記感知された神経連絡を示すフィードバック制御信号を受け取るために前記信号処理モジュールに接続された制御装置であって、前記神経刺激信号の少なくとも1つのパラメータが前記神経感知部位において所望の反射神経反応に集中するように調整するために前記神経刺激制御信号を調整するように適合される制御装置と、
から構成され、
前記制御装置は、
前記感知された反射神経反応を示す前記信号のための、メモリに格納されたプログラム可能なターゲット値と、
前記信号処理モジュールから前記感知された反射神経反応を示す前記信号を受け取り、前記感知された反射神経反応を示す前記信号を前記プログラム可能なターゲット値と比較し、前記閉ループ神経刺激治療を制御するのに用いられるフィードバック信号を生成するように適合されたフィードバック比較器と、
前記神経ターゲットでの刺激イベントを前記神経感知部位における感知された神経作用に関連付けて、前記刺激イベントと前記感知された神経作用との間の因果関係を確認し、ANSの反射回路を介して前記感知された神経作用が前記刺激イベントと因果関係を有するときを示す関連付け結果を提供するように適合された連想器と、
前記関連付け結果を受け取り前記感知された神経作用が前記感知された反射神経反応であることを確認し、前記フィードバック信号を受け取り、前記感知された反射神経反応を前記所望の神経反応に集中させるために前記少なくとも1つの刺激パラメータを調整するように、前記フィードバック信号を用いて刺激制御信号を生成するように適合された神経制御装置と、を含むことを特徴とする機器。 - 前記ANS内の前記神経刺激部位は副交感神経刺激部位であり、前記ANS内の前記神経感知部位は副交感神経感知部位であり、前記制御装置は、前記神経刺激信号の前記少なくとも1つのパラメータが前記副交感神経感知部位において前記所望の感知された神経連絡に集中するように調整するために前記フィードバック制御信号を負のフィードバックとして受け取るように適合されることを特徴とする請求項28に記載の機器。
- 前記副交感神経刺激部位は前記副交感神経感知部位であることを特徴とする請求項29に記載の機器。
- 前記副交感神経刺激部位と前記副交感神経感知部位は圧受容器部位を含むことを特徴とする請求項30に記載の機器。
- 心臓周期を感知するために前記制御装置に接続されたセンサをさらに備え、前記制御装置は、1つの心臓周期中に前記圧受容器を神経刺激して、別の心臓周期中に神経作用を感知するように適合されることを特徴とする請求項31に記載の機器。
- 前記副交感神経刺激部位は前記副交感神経感知部位とは異なる部位であることを特徴とする請求項29に記載の機器。
- 前記副交感神経刺激部位は少なくとも1つの迷走神経と心脂肪体を含み、前記副交感神経感知部位は圧受容器部位を含むことを特徴とする請求項33に記載の機器。
- 前記副交感神経刺激部位は迷走神経上の第1の部位を含み、前記副交感神経感知部位は迷走神経上の第2の部位を含むことを特徴とする請求項29に記載の機器。
- 前記第1の部位と前記第2の部位のうちの1つは、遠心性部位であり、もう一方は求心性部位であることを特徴とする請求項35に記載の機器。
- 前記第1と第2の部位は共に、前記迷走神経上の求心性部位であることを特徴とする請求項35に記載の機器。
- 前記第1と第2の部位は共に、前記迷走神経上の遠心性部位であることを特徴とする請求項35に記載の機器。
- 前記ANS内の前記神経刺激部位は交感神経刺激部位であり、前記ANS内の前記神経感知部位は交感神経感知部位であり、前記制御装置は、前記神経刺激信号の前記少なくとも1つのパラメータが前記交感神経感知部位において前記所望の感知された神経連絡に集中するように調整するために前記フィードバック制御信号を負のフィードバックとして受け取るように適合されることを特徴とする請求項28に記載の機器。
- 前記神経刺激部位と前記神経感知部位は共に、心臓交感神経枝を含むことを特徴とする請求項39に記載の機器。
- 前記ANS内の前記神経刺激部位は副交感神経刺激部位であり、前記ANS内の前記神経感知部位は交感神経感知部位であり、前記制御装置は、前記神経刺激信号の前記少なくとも1つのパラメータが前記交感神経感知部位において前記所望の感知された神経連絡に集中するように調整するために前記フィードバック制御信号を正のフィードバックとして受け取るように適合されることを特徴とする請求項28に記載の機器。
- 前記副交感神経刺激部位は迷走神経部位を含むことを特徴とする請求項41に記載の機器。
- 前記副交感神経刺激部位は圧受容器部位を含み、前記交感神経感知部位は心臓交感神経枝を含むことを特徴とする請求項41に記載の機器。
- 前記ANS内の前記神経刺激部位は前記ANS内の交感神経刺激部位であり、前記神経感知部位は副交感神経感知部位であり、前記制御装置は、前記神経刺激信号の前記少なくとも1つのパラメータが前記副交感神経感知部位において前記所望の感知された神経連絡に集中するように調整するために前記フィードバック制御信号を正のフィードバックとして受け取るように適合されることを特徴とする請求項28に記載の機器。
- 前記交感神経刺激部位は心臓交感神経枝を含み、前記副交感神経感知部位は圧受容器部位を含むことを特徴とする請求項44に記載の機器。
- 動的入力制御信号をさらに備え、前記制御装置は前記感知された神経連絡のターゲットを調整するために前記動的入力制御信号を受け取るように適合されることを特徴とする請求項28に記載の機器。
- ゲインを調整するためにゲイン入力制御信号をさらに備え、前記制御装置は前記フィードバック制御信号に基づいて前記神経刺激の強度に対してゲインを増分と減分するために前記ゲイン入力制御信号を受け取るように適合されることを特徴とする請求項28に記載の機器。
- 動的入力制御信号をさらに備え、前記制御装置は前記ゲインを調整するために前記動的入力制御信号を受け取るように適合されることを特徴とする請求項47に記載の機器。
- 関連する入力制御信号をさらに備え、前記制御装置は前記感知された神経作用を神経刺激イベントに関連付けるために前記関連する入力制御信号を受け取るように適合されることを特徴とする請求項28に記載の機器。
- 動的入力制御信号と、ゲイン入力制御信号と、関連入力制御信号とをさらに備え、前記制御装置は、感知された神経作用と刺激された神経作用との間の因果関係を確認するために前記関連入力制御信号を使用して前記感知された神経作用を神経刺激イベントに関連付け、前記フィードバック制御信号に基づいて前記神経刺激の強度に対するゲインを増分と減分するために前記ゲイン入力制御信号を受け取り、前記感知された神経連絡のターゲットを調整して前記ゲインを調整するために前記動的入力制御信号を受け取るように適合されることを特徴とする請求項28に記載の機器。
- 前記神経刺激部位は神経経路上にあり、前記神経感知部位は前記同じ神経経路上にあることを特徴とする請求項28に記載の機器。
- 前記神経刺激部位は前記神経感知部位にあることを特徴とする請求項28に記載の機器。
- 閉ループ神経刺激治療を、反射回路を含む自律神経系(ANS)内の所望の神経ターゲットに伝達して所望の神経反応を生じさせる埋め込み型医療機器であって、
自律神経系(ANS)内の神経刺激部位において適用される神経刺激信号を供給し、前記ANS内の神経感知部位における神経作用固有レベルに作用する反射反応を誘引するように適合された神経刺激装置と、
前記神経刺激部位へ与えた刺激に対し感知された反射神経反応を示す前記ANS内の前記神経感知部位において感知された神経連絡を受け取り、感知された神経連絡を処理するように適合された神経センサと信号処理モジュールと、
前記神経刺激装置に接続され、前記神経刺激信号を生成するために前記神経刺激装置に神経刺激制御信号を供給するように適合され、前記感知された神経連絡を示すフィードバックを受け取るために前記信号処理モジュールに接続された制御装置と、
から構成され、前記制御装置は、
前記神経センサと信号処理モジュールから処理され感知された信号を受け取り、前記処理され感知された信号のターゲット信号を受け取り、前記処理され感知された信号を前記ターゲット信号と比較して対応するフィードバック信号を生成するように適合されたフィードバック比較器と、
前記フィードバック信号を受け取り、前記フィードバック信号を使用して前記刺激制御信号を生成するように適合された神経制御装置と、
を備え、
感知された生理パラメータと時間信号のうちの少なくとも1つに基づいて動的制御信号を生成するために動的入力モジュールをさらに備え、
前記制御装置はさらに、感知された神経作用と刺激された神経作用との間の因果関係を確認する関連結果制御信号を生成する連想器を備え、前記神経制御装置は、前記動的制御信号と前記関連結果信号を受け取り、前記フィードバック信号,前記動的制御信号,前記関連結果信号を使用して前記刺激制御信号を生成するように適合されていることを特徴とする埋め込み型医療機器。 - 前記制御装置は、神経連絡を感知すること、神経刺激を供給すること、前記動的制御信号を生成することに関連するプログラム可能パラメータを格納するように適合されたメモリを有することを特徴とする請求項53に記載の機器。
- 前記制御装置は、前記刺激イベントから、前記刺激された所望の神経ターゲットがANSの反射回路を介して神経感知部位における神経連絡に影響を及ぼすときまでの反射回路時間を考慮に入れるように適合されている請求項1に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激イベントに関連付けるために、平均化を使用するように適合されている請求項1に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激イベントに関連付けるために、一時的相関を使用するように適合されている請求項1に記載の機器。
- 前記制御装置は、前記刺激イベントから、前記刺激された所望の神経ターゲットがANSの反射回路を介して神経感知部位における神経連絡に影響を及ぼすときまでの反射回路時間を考慮に入れるように適合されている請求項18に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激イベントに関連付けるために、平均化を使用するように適合されている請求項18に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激イベントに関連付けるために、一時的相関を使用するように適合されている請求項18に記載の機器。
- 前記制御装置は、前記刺激イベントから、前記刺激された所望の神経ターゲットがANSの反射回路を介して神経感知部位における神経連絡に影響を及ぼすときまでの反射回路時間を考慮に入れるように適合されている請求項28に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激イベントに関連付けるために、平均化を使用するように適合されている請求項28に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激イベントに関連付けるために、一時的相関を使用するように適合されている請求項28に記載の機器。
- 前記制御装置は、前記刺激された神経作用から、前記刺激された所望の神経ターゲットがANSの反射回路を介して神経感知部位における神経連絡に影響を及ぼすときまでの反射回路時間を考慮に入れるように適合されている請求項53に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激された神経作用に関連付けるために、平均化を使用するように適合されている請求項53に記載の機器。
- 前記連想器は、前記感知された作用を前記刺激された神経作用に関連付けるために、一時的相関を使用するように適合されている請求項53に記載の機器。
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/992,320 US7769450B2 (en) | 2004-11-18 | 2004-11-18 | Cardiac rhythm management device with neural sensor |
| US10/992,320 | 2004-11-18 | ||
| US10/992,319 | 2004-11-18 | ||
| US10/992,319 US8396560B2 (en) | 2004-11-18 | 2004-11-18 | System and method for closed-loop neural stimulation |
| US71230205P | 2005-08-29 | 2005-08-29 | |
| US60/712,302 | 2005-08-29 | ||
| US11/280,940 US8332047B2 (en) | 2004-11-18 | 2005-11-16 | System and method for closed-loop neural stimulation |
| US11/280,940 | 2005-11-16 | ||
| PCT/US2005/042009 WO2006055849A1 (en) | 2004-11-18 | 2005-11-17 | System for closed-loop neural stimulation |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2008520376A JP2008520376A (ja) | 2008-06-19 |
| JP2008520376A5 JP2008520376A5 (ja) | 2009-01-15 |
| JP5060304B2 true JP5060304B2 (ja) | 2012-10-31 |
Family
ID=35985300
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007543316A Expired - Fee Related JP5060304B2 (ja) | 2004-11-18 | 2005-11-17 | 閉ループ神経刺激のためのシステム |
Country Status (6)
| Country | Link |
|---|---|
| EP (2) | EP1814627B1 (ja) |
| JP (1) | JP5060304B2 (ja) |
| AT (1) | ATE468152T1 (ja) |
| DE (1) | DE602005021392D1 (ja) |
| ES (1) | ES2345208T3 (ja) |
| WO (1) | WO2006055849A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11944579B2 (en) | 2016-08-24 | 2024-04-02 | Cyberdyne Inc. | Biological activity detection apparatus and biological activity detection system |
Families Citing this family (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7783353B2 (en) | 2003-12-24 | 2010-08-24 | Cardiac Pacemakers, Inc. | Automatic neural stimulation modulation based on activity and circadian rhythm |
| US7460906B2 (en) | 2003-12-24 | 2008-12-02 | Cardiac Pacemakers, Inc. | Baroreflex stimulation to treat acute myocardial infarction |
| US7769450B2 (en) | 2004-11-18 | 2010-08-03 | Cardiac Pacemakers, Inc. | Cardiac rhythm management device with neural sensor |
| US8396560B2 (en) | 2004-11-18 | 2013-03-12 | Cardiac Pacemakers, Inc. | System and method for closed-loop neural stimulation |
| US20050149132A1 (en) | 2003-12-24 | 2005-07-07 | Imad Libbus | Automatic baroreflex modulation based on cardiac activity |
| US7509166B2 (en) | 2003-12-24 | 2009-03-24 | Cardiac Pacemakers, Inc. | Automatic baroreflex modulation responsive to adverse event |
| US10912712B2 (en) | 2004-03-25 | 2021-02-09 | The Feinstein Institutes For Medical Research | Treatment of bleeding by non-invasive stimulation |
| US8332047B2 (en) | 2004-11-18 | 2012-12-11 | Cardiac Pacemakers, Inc. | System and method for closed-loop neural stimulation |
| EP2298410B1 (en) | 2004-12-27 | 2013-10-09 | The Feinstein Institute for Medical Research | Treating inflammatory disorders by electrical vagus nerve stimulation |
| US11207518B2 (en) | 2004-12-27 | 2021-12-28 | The Feinstein Institutes For Medical Research | Treating inflammatory disorders by stimulation of the cholinergic anti-inflammatory pathway |
| US9555252B2 (en) | 2005-04-25 | 2017-01-31 | Cardiac Pacemakers, Inc. | Systems for providing neural markers for sensed autonomic nervous system activity |
| US7640057B2 (en) | 2005-04-25 | 2009-12-29 | Cardiac Pacemakers, Inc. | Methods of providing neural markers for sensed autonomic nervous system activity |
| US7647101B2 (en) * | 2006-06-09 | 2010-01-12 | Cardiac Pacemakers, Inc. | Physical conditioning system, device and method |
| US20080091255A1 (en) * | 2006-10-11 | 2008-04-17 | Cardiac Pacemakers | Implantable neurostimulator for modulating cardiovascular function |
| US9211409B2 (en) | 2008-03-31 | 2015-12-15 | The Feinstein Institute For Medical Research | Methods and systems for reducing inflammation by neuromodulation of T-cell activity |
| US9662490B2 (en) | 2008-03-31 | 2017-05-30 | The Feinstein Institute For Medical Research | Methods and systems for reducing inflammation by neuromodulation and administration of an anti-inflammatory drug |
| US20100191304A1 (en) | 2009-01-23 | 2010-07-29 | Scott Timothy L | Implantable Medical Device for Providing Chronic Condition Therapy and Acute Condition Therapy Using Vagus Nerve Stimulation |
| US9211410B2 (en) | 2009-05-01 | 2015-12-15 | Setpoint Medical Corporation | Extremely low duty-cycle activation of the cholinergic anti-inflammatory pathway to treat chronic inflammation |
| US8996116B2 (en) | 2009-10-30 | 2015-03-31 | Setpoint Medical Corporation | Modulation of the cholinergic anti-inflammatory pathway to treat pain or addiction |
| WO2010144578A2 (en) | 2009-06-09 | 2010-12-16 | Setpoint Medical Corporation | Nerve cuff with pocket for leadless stimulator |
| JP5646157B2 (ja) * | 2009-10-30 | 2014-12-24 | オリンパス株式会社 | 心臓治療装置 |
| US8682432B2 (en) | 2009-10-30 | 2014-03-25 | Olympus Corporation | Cardiac-event processor and heart treatment device |
| US9833621B2 (en) | 2011-09-23 | 2017-12-05 | Setpoint Medical Corporation | Modulation of sirtuins by vagus nerve stimulation |
| US11051744B2 (en) | 2009-11-17 | 2021-07-06 | Setpoint Medical Corporation | Closed-loop vagus nerve stimulation |
| EP3636314B1 (en) | 2009-12-23 | 2021-09-08 | Setpoint Medical Corporation | Neural stimulation devices and systems for treatment of chronic inflammation |
| US9579504B2 (en) | 2010-06-24 | 2017-02-28 | Robert Bosch Llc | Personalized patient controlled neurostimulation system |
| EP4159273A1 (en) * | 2011-05-13 | 2023-04-05 | Saluda Medical Pty Ltd | Implantable device for controlling a neural stimulus |
| US9572983B2 (en) | 2012-03-26 | 2017-02-21 | Setpoint Medical Corporation | Devices and methods for modulation of bone erosion |
| WO2014164421A1 (en) | 2013-03-11 | 2014-10-09 | Ohio State Innovation Foundation | Systems and methods for treating autonomic instability and medical conditions associated therewith |
| US9717428B2 (en) | 2014-02-07 | 2017-08-01 | Medtronic, Inc. | Devices and methods for sensing physiological signals during stimulation therapy |
| US11311725B2 (en) | 2014-10-24 | 2022-04-26 | Setpoint Medical Corporation | Systems and methods for stimulating and/or monitoring loci in the brain to treat inflammation and to enhance vagus nerve stimulation |
| US11406833B2 (en) | 2015-02-03 | 2022-08-09 | Setpoint Medical Corporation | Apparatus and method for reminding, prompting, or alerting a patient with an implanted stimulator |
| US10596367B2 (en) | 2016-01-13 | 2020-03-24 | Setpoint Medical Corporation | Systems and methods for establishing a nerve block |
| US11471681B2 (en) | 2016-01-20 | 2022-10-18 | Setpoint Medical Corporation | Batteryless implantable microstimulators |
| WO2017127758A1 (en) | 2016-01-20 | 2017-07-27 | Setpoint Medical Corporation | Implantable microstimulators and inductive charging systems |
| CN108882885A (zh) | 2016-01-20 | 2018-11-23 | 赛博恩特医疗器械公司 | 迷走神经刺激的控制 |
| US10583304B2 (en) | 2016-01-25 | 2020-03-10 | Setpoint Medical Corporation | Implantable neurostimulator having power control and thermal regulation and methods of use |
| US11173307B2 (en) | 2017-08-14 | 2021-11-16 | Setpoint Medical Corporation | Vagus nerve stimulation pre-screening test |
| US11260229B2 (en) | 2018-09-25 | 2022-03-01 | The Feinstein Institutes For Medical Research | Methods and apparatuses for reducing bleeding via coordinated trigeminal and vagal nerve stimulation |
| US20210379383A1 (en) * | 2018-10-23 | 2021-12-09 | Saluda Medical Pty Limited | Supervisor for implantable stimulation devices |
| EP3873589A4 (en) | 2018-11-01 | 2022-07-27 | Kyushu University, National University Corporation | BLOOD PRESSURE CONTROL DEVICE, NON-TRANSITORY COMPUTER READABLE RECORDING MEDIUM HAVING STORED THEREON A CONTROL PROGRAM OF A BLOOD PRESSURE MONITOR AND METHOD FOR CONTROLLING BLOOD PRESSURE |
| US11938324B2 (en) | 2020-05-21 | 2024-03-26 | The Feinstein Institutes For Medical Research | Systems and methods for vagus nerve stimulation |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5199428A (en) * | 1991-03-22 | 1993-04-06 | Medtronic, Inc. | Implantable electrical nerve stimulator/pacemaker with ischemia for decreasing cardiac workload |
| US5522854A (en) * | 1994-05-19 | 1996-06-04 | Duke University | Method and apparatus for the prevention of arrhythmia by nerve stimulation |
| EP0688578B1 (en) * | 1994-06-24 | 1999-11-10 | Pacesetter AB | Arrhythmia detector |
| US5702429A (en) * | 1996-04-04 | 1997-12-30 | Medtronic, Inc. | Neural stimulation techniques with feedback |
| US6195585B1 (en) * | 1998-06-26 | 2001-02-27 | Advanced Bionics Corporation | Remote monitoring of implantable cochlear stimulator |
| US6748276B1 (en) * | 2000-06-05 | 2004-06-08 | Advanced Neuromodulation Systems, Inc. | Neuromodulation therapy system |
| US6622041B2 (en) * | 2001-08-21 | 2003-09-16 | Cyberonics, Inc. | Treatment of congestive heart failure and autonomic cardiovascular drive disorders |
| WO2003076008A1 (en) * | 2002-03-14 | 2003-09-18 | Brainsgate Ltd. | Technique for blood pressure regulation |
| US7277761B2 (en) * | 2002-06-12 | 2007-10-02 | Pacesetter, Inc. | Vagal stimulation for improving cardiac function in heart failure or CHF patients |
| JP4189448B2 (ja) * | 2002-08-05 | 2008-12-03 | 国立循環器病センター総長 | 生体調節機能代替を用いた治療用システム |
| US7130677B2 (en) * | 2002-12-04 | 2006-10-31 | Medtronic, Inc. | Methods and apparatus for discriminating polymorphic tachyarrhythmias from monomorphic tachyarrhythmias facilitating detection of fibrillation |
| JP4252826B2 (ja) * | 2003-03-14 | 2009-04-08 | テルモ株式会社 | 心臓治療装置 |
| US7155278B2 (en) * | 2003-04-21 | 2006-12-26 | Medtronic, Inc. | Neurostimulation to treat effects of sleep apnea |
-
2005
- 2005-11-17 WO PCT/US2005/042009 patent/WO2006055849A1/en active Application Filing
- 2005-11-17 AT AT05851890T patent/ATE468152T1/de not_active IP Right Cessation
- 2005-11-17 ES ES05851890T patent/ES2345208T3/es active Active
- 2005-11-17 EP EP05851890A patent/EP1814627B1/en not_active Not-in-force
- 2005-11-17 JP JP2007543316A patent/JP5060304B2/ja not_active Expired - Fee Related
- 2005-11-17 DE DE602005021392T patent/DE602005021392D1/de active Active
- 2005-11-17 EP EP10157396.2A patent/EP2213330A3/en not_active Withdrawn
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11944579B2 (en) | 2016-08-24 | 2024-04-02 | Cyberdyne Inc. | Biological activity detection apparatus and biological activity detection system |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2006055849A1 (en) | 2006-05-26 |
| EP2213330A2 (en) | 2010-08-04 |
| EP1814627B1 (en) | 2010-05-19 |
| EP1814627A1 (en) | 2007-08-08 |
| DE602005021392D1 (de) | 2010-07-01 |
| JP2008520376A (ja) | 2008-06-19 |
| ES2345208T3 (es) | 2010-09-17 |
| ATE468152T1 (de) | 2010-06-15 |
| EP2213330A3 (en) | 2014-08-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5060304B2 (ja) | 閉ループ神経刺激のためのシステム | |
| US11672985B2 (en) | Intermittent neural stimulation with physiologic response monitor | |
| US11724109B2 (en) | System and method for sustained baroreflex stimulation | |
| US8332047B2 (en) | System and method for closed-loop neural stimulation | |
| US10029099B2 (en) | System and method for closed-loop neural stimulation | |
| US9440078B2 (en) | Neural stimulation modulation based on monitored cardiovascular parameter | |
| JP5080262B2 (ja) | 神経刺激をフィルタリングするためのシステムおよび方法 | |
| US8447394B2 (en) | Physical conditioning system, device and method | |
| US7769450B2 (en) | Cardiac rhythm management device with neural sensor | |
| US20050149128A1 (en) | Barorflex stimulation system to reduce hypertension | |
| US20050149129A1 (en) | Baropacing and cardiac pacing to control output |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081117 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081117 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7422 Effective date: 20090309 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20090309 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20090723 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20090723 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110627 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110630 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110926 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111003 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120213 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120510 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120517 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120606 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20120717 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20120803 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20150810 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D03 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |