JP4164652B2 - Thermoelectric conversion material and method for producing the same - Google Patents
Thermoelectric conversion material and method for producing the same Download PDFInfo
- Publication number
- JP4164652B2 JP4164652B2 JP2002347322A JP2002347322A JP4164652B2 JP 4164652 B2 JP4164652 B2 JP 4164652B2 JP 2002347322 A JP2002347322 A JP 2002347322A JP 2002347322 A JP2002347322 A JP 2002347322A JP 4164652 B2 JP4164652 B2 JP 4164652B2
- Authority
- JP
- Japan
- Prior art keywords
- thermoelectric conversion
- conversion material
- coo
- alkali metal
- crystal
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000006243 chemical reaction Methods 0.000 title claims description 82
- 239000000463 material Substances 0.000 title claims description 64
- 238000004519 manufacturing process Methods 0.000 title claims description 29
- 239000013078 crystal Substances 0.000 claims description 72
- 239000011734 sodium Substances 0.000 claims description 48
- YKYOUMDCQGMQQO-UHFFFAOYSA-L cadmium dichloride Chemical compound Cl[Cd]Cl YKYOUMDCQGMQQO-UHFFFAOYSA-L 0.000 claims description 36
- 229910052783 alkali metal Inorganic materials 0.000 claims description 32
- 150000001340 alkali metals Chemical class 0.000 claims description 30
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical group [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 claims description 27
- 229910017052 cobalt Inorganic materials 0.000 claims description 15
- 239000010941 cobalt Substances 0.000 claims description 15
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 claims description 15
- 239000000203 mixture Substances 0.000 claims description 15
- 239000011229 interlayer Substances 0.000 claims description 13
- 239000011148 porous material Substances 0.000 claims description 10
- 229910052751 metal Inorganic materials 0.000 claims description 6
- 239000002184 metal Substances 0.000 claims description 6
- 229910018871 CoO 2 Inorganic materials 0.000 claims description 4
- 150000001875 compounds Chemical class 0.000 claims description 4
- 150000004820 halides Chemical class 0.000 claims description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 claims description 4
- 150000004679 hydroxides Chemical class 0.000 claims description 2
- 229910052793 cadmium Inorganic materials 0.000 claims 1
- BDOSMKKIYDKNTQ-UHFFFAOYSA-N cadmium atom Chemical compound [Cd] BDOSMKKIYDKNTQ-UHFFFAOYSA-N 0.000 claims 1
- 239000010410 layer Substances 0.000 description 34
- 239000007795 chemical reaction product Substances 0.000 description 16
- 238000010438 heat treatment Methods 0.000 description 15
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 12
- 238000002441 X-ray diffraction Methods 0.000 description 12
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 9
- 238000000034 method Methods 0.000 description 9
- 239000001301 oxygen Substances 0.000 description 9
- 229910052760 oxygen Inorganic materials 0.000 description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 8
- 229910001508 alkali metal halide Inorganic materials 0.000 description 7
- 150000008045 alkali metal halides Chemical class 0.000 description 7
- 238000007796 conventional method Methods 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 238000001816 cooling Methods 0.000 description 6
- 239000002994 raw material Substances 0.000 description 6
- 239000011780 sodium chloride Substances 0.000 description 6
- 229910019850 NaxCoO2 Inorganic materials 0.000 description 5
- 238000001035 drying Methods 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 4
- 238000003917 TEM image Methods 0.000 description 4
- 229910052744 lithium Inorganic materials 0.000 description 4
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- FGDZQCVHDSGLHJ-UHFFFAOYSA-M rubidium chloride Chemical compound [Cl-].[Rb+] FGDZQCVHDSGLHJ-UHFFFAOYSA-M 0.000 description 4
- 229910052708 sodium Inorganic materials 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- MWUXSHHQAYIFBG-UHFFFAOYSA-N nitrogen oxide Inorganic materials O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 description 3
- 229910052700 potassium Inorganic materials 0.000 description 3
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 3
- 229910001415 sodium ion Inorganic materials 0.000 description 3
- 231100000331 toxic Toxicity 0.000 description 3
- 230000002588 toxic effect Effects 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 2
- NPYPAHLBTDXSSS-UHFFFAOYSA-N Potassium ion Chemical compound [K+] NPYPAHLBTDXSSS-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- FKNQFGJONOIPTF-UHFFFAOYSA-N Sodium cation Chemical compound [Na+] FKNQFGJONOIPTF-UHFFFAOYSA-N 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 230000005540 biological transmission Effects 0.000 description 2
- 229910052792 caesium Inorganic materials 0.000 description 2
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 2
- XJHCXCQVJFPJIK-UHFFFAOYSA-M caesium fluoride Chemical compound [F-].[Cs+] XJHCXCQVJFPJIK-UHFFFAOYSA-M 0.000 description 2
- NCMHKCKGHRPLCM-UHFFFAOYSA-N caesium(1+) Chemical compound [Cs+] NCMHKCKGHRPLCM-UHFFFAOYSA-N 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- 229910000428 cobalt oxide Inorganic materials 0.000 description 2
- IVMYJDGYRUAWML-UHFFFAOYSA-N cobalt(ii) oxide Chemical compound [Co]=O IVMYJDGYRUAWML-UHFFFAOYSA-N 0.000 description 2
- 239000007772 electrode material Substances 0.000 description 2
- 238000010894 electron beam technology Methods 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 2
- HSZCZNFXUDYRKD-UHFFFAOYSA-M lithium iodide Chemical compound [Li+].[I-] HSZCZNFXUDYRKD-UHFFFAOYSA-M 0.000 description 2
- 229910001416 lithium ion Inorganic materials 0.000 description 2
- 239000007773 negative electrode material Substances 0.000 description 2
- 239000001103 potassium chloride Substances 0.000 description 2
- 235000011164 potassium chloride Nutrition 0.000 description 2
- NROKBHXJSPEDAR-UHFFFAOYSA-M potassium fluoride Chemical compound [F-].[K+] NROKBHXJSPEDAR-UHFFFAOYSA-M 0.000 description 2
- 229910001414 potassium ion Inorganic materials 0.000 description 2
- 238000010248 power generation Methods 0.000 description 2
- 229910052701 rubidium Inorganic materials 0.000 description 2
- 229940102127 rubidium chloride Drugs 0.000 description 2
- AHLATJUETSFVIM-UHFFFAOYSA-M rubidium fluoride Chemical compound [F-].[Rb+] AHLATJUETSFVIM-UHFFFAOYSA-M 0.000 description 2
- CPRMKOQKXYSDML-UHFFFAOYSA-M rubidium hydroxide Chemical compound [OH-].[Rb+] CPRMKOQKXYSDML-UHFFFAOYSA-M 0.000 description 2
- WFUBYPSJBBQSOU-UHFFFAOYSA-M rubidium iodide Chemical compound [Rb+].[I-] WFUBYPSJBBQSOU-UHFFFAOYSA-M 0.000 description 2
- 229910001419 rubidium ion Inorganic materials 0.000 description 2
- PUZPDOWCWNUUKD-UHFFFAOYSA-M sodium fluoride Chemical compound [F-].[Na+] PUZPDOWCWNUUKD-UHFFFAOYSA-M 0.000 description 2
- 230000005068 transpiration Effects 0.000 description 2
- 229910006525 α-NaFeO2 Inorganic materials 0.000 description 2
- 229910006596 α−NaFeO2 Inorganic materials 0.000 description 2
- MFGOFGRYDNHJTA-UHFFFAOYSA-N 2-amino-1-(2-fluorophenyl)ethanol Chemical compound NCC(O)C1=CC=CC=C1F MFGOFGRYDNHJTA-UHFFFAOYSA-N 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 229910020647 Co-O Inorganic materials 0.000 description 1
- 229910021503 Cobalt(II) hydroxide Inorganic materials 0.000 description 1
- 229910020704 Co—O Inorganic materials 0.000 description 1
- KRHYYFGTRYWZRS-UHFFFAOYSA-M Fluoride anion Chemical compound [F-] KRHYYFGTRYWZRS-UHFFFAOYSA-M 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 229910002665 PbTe Inorganic materials 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 229940006460 bromide ion Drugs 0.000 description 1
- HUCVOHYBFXVBRW-UHFFFAOYSA-M caesium hydroxide Inorganic materials [OH-].[Cs+] HUCVOHYBFXVBRW-UHFFFAOYSA-M 0.000 description 1
- XQPRBTXUXXVTKB-UHFFFAOYSA-M caesium iodide Chemical compound [I-].[Cs+] XQPRBTXUXXVTKB-UHFFFAOYSA-M 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- KYKAJFCTULSVSH-UHFFFAOYSA-N chloro(fluoro)methane Chemical compound F[C]Cl KYKAJFCTULSVSH-UHFFFAOYSA-N 0.000 description 1
- GFHNAMRJFCEERV-UHFFFAOYSA-L cobalt chloride hexahydrate Chemical compound O.O.O.O.O.O.[Cl-].[Cl-].[Co+2] GFHNAMRJFCEERV-UHFFFAOYSA-L 0.000 description 1
- OBWXQDHWLMJOOD-UHFFFAOYSA-H cobalt(2+);dicarbonate;dihydroxide;hydrate Chemical compound O.[OH-].[OH-].[Co+2].[Co+2].[Co+2].[O-]C([O-])=O.[O-]C([O-])=O OBWXQDHWLMJOOD-UHFFFAOYSA-H 0.000 description 1
- ASKVAEGIVYSGNY-UHFFFAOYSA-L cobalt(ii) hydroxide Chemical compound [OH-].[OH-].[Co+2] ASKVAEGIVYSGNY-UHFFFAOYSA-L 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- HEQUOWMMDQTGCX-UHFFFAOYSA-L dicesium;oxalate Chemical compound [Cs+].[Cs+].[O-]C(=O)C([O-])=O HEQUOWMMDQTGCX-UHFFFAOYSA-L 0.000 description 1
- YNQRWVCLAIUHHI-UHFFFAOYSA-L dilithium;oxalate Chemical compound [Li+].[Li+].[O-]C(=O)C([O-])=O YNQRWVCLAIUHHI-UHFFFAOYSA-L 0.000 description 1
- 238000007599 discharging Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000002524 electron diffraction data Methods 0.000 description 1
- 238000000921 elemental analysis Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 239000002803 fossil fuel Substances 0.000 description 1
- 238000005469 granulation Methods 0.000 description 1
- 230000003179 granulation Effects 0.000 description 1
- 239000012212 insulator Substances 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-M iodide Chemical compound [I-] XMBWDFGMSWQBCA-UHFFFAOYSA-M 0.000 description 1
- 229940006461 iodide ion Drugs 0.000 description 1
- 238000003475 lamination Methods 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 229940039748 oxalate Drugs 0.000 description 1
- DUXDETQJUQZYEX-UHFFFAOYSA-L oxalate;rubidium(1+) Chemical compound [Rb+].[Rb+].[O-]C(=O)C([O-])=O DUXDETQJUQZYEX-UHFFFAOYSA-L 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 150000002926 oxygen Chemical class 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000011698 potassium fluoride Substances 0.000 description 1
- 235000003270 potassium fluoride Nutrition 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000011775 sodium fluoride Substances 0.000 description 1
- 235000013024 sodium fluoride Nutrition 0.000 description 1
- 235000009518 sodium iodide Nutrition 0.000 description 1
- ZNCPFRVNHGOPAG-UHFFFAOYSA-L sodium oxalate Chemical compound [Na+].[Na+].[O-]C(=O)C([O-])=O ZNCPFRVNHGOPAG-UHFFFAOYSA-L 0.000 description 1
- 229940039790 sodium oxalate Drugs 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- OCGWQDWYSQAFTO-UHFFFAOYSA-N tellanylidenelead Chemical compound [Pb]=[Te] OCGWQDWYSQAFTO-UHFFFAOYSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Landscapes
- Inorganic Compounds Of Heavy Metals (AREA)
Description
【0001】
【発明の属する技術分野】
本発明は、新規な熱電変換材料及びその製造方法に関する。
【0002】
【従来の技術】
近年、環境問題や化石燃料の代替エネルギーの問題が社会的に大きく注目されている。そのような状況下において、例えば、イ)二酸化炭素、窒素酸化物等の有害ガスを排出せず、排熱等の未利用熱エネルギーを有効に電気エネルギーに変換する熱電変換エネルギー技術、ロ)有害なフロン系ガスを使用しない熱電冷却技術等への期待が高まっている。これらの期待に応えるためには、高性能な熱電変換材料の開発が不可欠である。
【0003】
熱電変換材料は、熱エネルギーと電気エネルギーとを相互に変換できる材料であり、その性能指数(Z)は、次式で与えられる;
Z = S2/(ρκ)
式中、Sは熱起電力(ゼーベック係数)を示し、ρは電気抵抗率を示し、κは熱伝導率を示す。熱電変換効率を高めるためには、Sの絶対値が大きく、ρ及びκがともに小さいことが必要となる。
【0004】
熱電変換材料としては、これまでに種々のものが提案されている。例えば、Bi2Te3系熱電変換材料は、室温から200℃の温度範囲において高い性能指数を示し、ペルチェ素子として熱電冷却等に用いられている。PbTe系熱電変換材料は、200℃〜500℃の温度範囲において高い性能指数を示し、発電装置として主に用いられている。
【0005】
ところが、これらは非酸化物系材料であるため、合成プロセスが複雑という問題がある。また、これらの熱電変換材料を構成するTeは、資源として乏しく、しかも毒性があるため、環境への影響及び一般家庭での使用を考慮した場合に問題がある。これらの理由より、合成プロセスが比較的簡単な酸化物系材料において、有害な元素を含まない新しい熱電変換材料の探索が進められている。
【0006】
このような状況下において、とりわけα−NaFeO2型結晶構造を有する酸化物であるNa0.5CoO2が熱電変換材料として脚光を浴びている。
【0007】
非特許文献1には、Na0.5CoO2が室温下で100μV/Kという大きな熱起電力を示し、かつ200μΩmという低い電気抵抗率を示すことが報告されている。Na0.5CoO2の出力因子(S2/ρ)は前記Bi2Te3の出力因子を上回っており、新しい熱電変換材料として期待されている。
【0008】
非特許文献2には、Na0.5CoO2が上記特性を発揮する理由として、次のように報告されている。
【0009】
Na0.5CoO2は、図1に示すようにCoO2層とNa層とが交互に積層した層状化合物であり、P6322の対称性をもつ結晶構造を有する。かかる結晶の対称性は、例えば、X線回折等により容易に確認できる。P6322の対称性を表すX線回折パターンの一例を図4に点線で示す。
【0010】
CoO2層では、CoO6八面体が稜を共有している。Na層では、Naサイトの1/2をNaがランダムに占有しており、残りの1/2のサイトには原子空孔型格子欠陥が存在する。これらの層のうち、電気伝導はCoO2層が担っていると考えられ、Na層は熱伝導を阻害していると考えられる。これにより、Na0.5CoO2は液体窒素温度から400℃以上の広い温度範囲において優れた熱電変換特性を発揮する。
【0011】
しかしながら、P6322の対称性をもつNa0.5CoO2では、CoO2層の層間距離が0.54nmと比較的大きく、単位体積あたりに含まれるCoO2層及びNa層の数が少ないため、CoO2層による電気伝導効率及びNa層による熱伝導阻害効率が十分ではない。
【0012】
そのため、Na0.5CoO2のゼーベック係数はなお不十分であり、より実用的な熱電変換材料を目指すには更なる改善が必要である。これに関して、特許文献1には、Na0.5CoO2の熱電変換性能を向上させる手段として、Naサイト又はCoサイトを部分的に他元素で置換する方法が開示されている。しかし、このような不純物を含む系のNa0.5CoO2でも熱電変換性能は未だ十分ではない。しかも、これら従来技術では、その製造方法にも改善すべき点がある。
【0013】
Na0.5CoO2で示される結晶並びに当該結晶のNa又はCoを部分的に他元素で置換した結晶では、熱電変換性能に異方性がある。例えば、Na0.5CoO2では、CoO2層の面内(即ち、c軸に垂直な方向)は良好な電気伝導を示し、CoO2層の面間(即ち、c軸方向)は導電性に乏しいため、CoO2層の面内(即ち、c軸に垂直な方向)にのみ大きな熱電変換性能が発揮される。
【0014】
このような異方性を有する結晶を集めて多結晶体を製造する場合、Na0.5CoO2で示される結晶の方位がランダムに集合した多結晶体では、熱電変換性能が大きく低下して単結晶よりも不利になるという問題がある。
【0015】
特許文献2には、このような異方性を有する結晶を集めて結晶の方位を揃えた多結晶体を製造する方法として、複数の結晶が該結晶のc軸方向が揃うように成形した積層体を形成し、この積層体に該結晶のc軸方向に加圧しながら熱処理して焼結体を製造する方法が開示されている。
【0016】
しかしながら、かかる多結晶体の製造方法では、熱処理時に結晶が熱分解して絶縁体である酸化コバルトが不純物として生成するため、熱電変換性能が低下するという問題がある。
【0017】
更に、上記Na0.5CoO2の製造方法では、アルカリ金属元素の供給源として炭酸塩及び酸化物が用いられるが、高温での熱処理が必要であるためにアルカリ金属が蒸散し易く、アルカリ金属量を制御することが困難である。またLi及びNa以外のアルカリ金属(例えば、K、Rb、Cs等)を含む大気中で安定なコバルト含有層状酸化物の製造は困難である。
【0018】
【非特許文献1】
寺崎 一郎、笹子 佳孝、内野倉 國光、「フィジカルレビューB(Physical Review B)」、米国、第56号、1997年、p.R12685
【0019】
【非特許文献2】
エム.フォン ヤンセン(M.Von Jansen)、アール.ホープ(R.Hope)、「ツァイストクラフト フューア アンオルガーニッシュ ウント アレゴーリッシュヒェミー(Zeitschrift fur Anorganisch und Allegorisch Chemie)」、ドイツ、第408号、1974年、p.104
【0020】
【特許文献1】
特開平11−266038号公報
【0021】
【特許文献2】
特開2000−269560号公報
【0022】
【発明が解決しようとする課題】
本発明は、従来品よりも熱電変換性能に優れた材料を効率的に提供することを主な目的とする。
【0023】
【課題を解決するための手段】
本発明者は、上記した目的を達成すべく鋭意研究を重ねた結果、特定の方法により製造される材料が上記目的を達成できることを見出し、本発明を完成するに至った。
【0024】
即ち、本発明は、下記の熱電変換材料及びその製造方法に係る。
1.一般式Na x CoO 2 (但し、0<x≦0.25)で示され、かつ塩化カドミウム型結晶構造を有する酸化物からなる熱電変換材料。
2.層間距離Lが0.3nm<L<0.54nmの範囲内の層間構造を有する上記項1に記載の熱電変換材料。
3.単結晶又は配向性の高い単結晶集合体から構成される上記項1又は2に記載の熱電変換材料。
4.結晶中に平均孔径5〜100nmの微細孔を有する上記項1〜3のいずれかに記載の熱電変換材料。
5.1)アルカリ金属元素を含む水酸化物の少なくとも1種と、2)コバルトを含む化合物及び金属コバルトの少なくとも1種とを含有する混合物を熱処理することを特徴とする、一般式Na x CoO 2 (但し、0<x≦0.25)で示され、かつ塩化カドミウム型結晶構造を有する酸化物からなる熱電変換材料の製造方法。
6.アルカリ金属元素を含む水酸化物の少なくとも1種が、水酸化ナトリウムである上記項5に記載の熱電変換材料の製造方法。
7.更に、アルカリ金属元素を含むハロゲン化物を配合する上記項5又は6に記載の熱電変換材料の製造方法。
【0025】
【発明の実施の形態】
熱電変換材料
本発明の熱電変換材料は、一般式AxCoO2(但し、0<x<0.5、Aはアルカリ金属元素)で示される酸化物からなることを特徴とする。
【0026】
アルカリ金属元素としては、Li、Na、K、Rb及びCsの少なくとも1種が好ましい。この中でも、本発明ではNaを用いることがより好ましい。
【0027】
上記xはアルカリ金属元素の含有量を示し、その値は0<x<0.5、好ましくは0.01≦x≦0.45、より好ましくは0.02≦x≦0.4、最も好ましくは0.02≦x≦0.3である。かかる含有量に限定することにより、従来品(Na0.5CoO2)と比較して優れた熱電変換性能を発揮できる。
【0028】
特に、アルカリ金属元素としてNaを用いる場合には、xの値は0<x≦0.25が好ましく、0.01≦x≦0.2がより好ましく、0.02≦x≦0.15が最も好ましい。アルカリ金属元素としてNaを用いて、かつxの値を0<x≦0.25の範囲内に限定した酸化物は、塩化カドミウム型結晶構造を有するため、特に優れた熱電変換性能を発揮できる。
【0029】
即ち、一般式AxCoO2(但し、0<x<0.5、Aはアルカリ金属元素)で示される酸化物からなる本発明の熱電変換材料の中でも、一般式NaxCoO2(但し、0<x≦0.25)で示され、かつ塩化カドミウム型結晶構造を有する酸化物からなる熱電変換材料が特に好ましい。
【0030】
本発明の熱電変換材料において、一般式NaxCoO2(但し、0<x≦0.25)で示され、かつ塩化カドミウム型結晶構造を有する酸化物以外では、酸化物の結晶構造は一定ではないが、一般にアルカリ金属元素の含有量が多くなるほど、塩化カドミウム型結晶構造とα−NaFeO2型結晶構造との混晶となる傾向がある。
【0031】
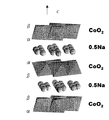
塩化カドミウム型結晶構造は、例えば、図2の模式図のように、R−3mで表される結晶の対称性を有する。図3は、塩化カドミウム型結晶構造(R−3m)を有するNaxCoO2(但し、0<x≦0.25)の積層構造を具体的に図示したものである。図3に示されるように、塩化カドミウム型結晶構造は、α−NaFeO2型結晶構造(P6322)を有するNa0.5CoO2と同様に、c軸方向に[A−O−Co−O(Aはアルカリ金属)]を最小単位とする積層構造を形成する。
【0032】
一方、塩化カドミウム型結晶構造(R−3m)は、c軸方向に対する酸素層の積層構造が、α−NaFeO2型結晶構造(P6322)と異なる。
【0033】
例えば、イ)ある酸素層の積層方法をα、ロ)αとは異なる酸素層の積層方法をβ、ハ)α及びβのどちらとも異なる酸素層の積層方法をγと定義し、これらの記号を用いて酸素層の積層構造を表すと図1及び図2のようになる。
【0034】
図1はα−NaFeO2型結晶構造の積層構造を示したものであり、酸素層の積層構造は(αββα)を最小単位とする。これに対し、図2は塩化カドミウム型結晶構造の積層構造を示したものであり、酸素層の積層態様は(αβγ)を最小単位とする。
【0035】
なお、当該2種の結晶構造は、X線回折(XRD)パターン、電子線回折(ED)パターン等により明確に区別することができる。
【0036】
このように、塩化カドミウム型結晶構造では(αβγ)を最小単位として酸素層が積層するため、(αββα)を最小単位とする従来のα−NaFeO2型結晶構造に比べて、酸素層がより密に積層できる。即ち、単位体積あたりに含まれるCoO2層とNa層の数が多くなるため、CoO2層による電気伝導効率及びNa層による熱伝導阻害効率が高まり、結果として熱伝変換性能を相乗的に高めることができる。
【0037】
層間距離Lは、図3に示すように、CoO2層とアルカリ金属層とが交互に積層した結晶構造において、一つのCoO2層(1)内に含まれるCo面(2)と当該CoO2層(1)に最も近接するCoO2層(3)内に含まれるCo面(4)との面間隔をいう。層間距離Lは、X線回折(XRD)分析及び高分解能透過型電子顕微鏡(TEM)により算出できる。
【0038】
本発明の熱電変換材料では、CoO2層の層間距離Lとしては、0.3nm<L<0.54nm程度が好ましく、0.45nm≦L≦0.47nmがより好ましい。層間距離をかかる範囲に限定することにより、熱電変換性能をより高めることができる。
【0039】
本発明の熱電変換材料は、単結晶又は多結晶(単結晶集合体を含む)のどちらで構成されてもよい。本発明では、優れた熱電変換性能がより確実に得られる点から、特に実質的に単結晶又は配向性の高い単結晶集合体から構成されることが好ましい。
【0040】
配向性の程度としては、XRDパターンにおいて、結晶構造を六方晶表示した場合のc軸(層状構造の積層方向)に垂直な結晶面、即ち(00L)(Lは整数)面以外の結晶面に由来するXRDピークが実質的に観察されないものは、本発明の熱電変換材料に全て含まれる。なお、配向性の高い多結晶体では、所定の熱電変換性能が得られる限り、他の組成からなる結晶(例えば、CoO2)等が含まれてもよい。
【0041】
本発明の熱電変換材料は多孔質であることが望ましい。具体的には、結晶中に平均孔径100nm以下、好ましくは50nm以下、特に5〜10nmの範囲の微細孔を有することが好ましい。多孔質な材料であれば、熱伝導率の低減を図ることができるため、より効果的に熱電変換性能が高められる。
【0042】
このような本発明の熱電変換材料は、300Kにおけるゼーベック係数が通常80μV/K以上、特に100μV/K以上という優れた値も達成できる。本発明の熱電変換材料の中でも、特に一般式NaxCoO2(但し、0<x≦0.25)で示され、かつ塩化カドミウム型結晶構造を有する酸化物からなるものは、300Kにおけるゼーベック係数が通常100μV以上、特に150μV/K以上という非常に優れた値も達成できる。
【0043】
本発明の熱電変換材料は、液体窒素温度から300℃という広い温度範囲において優れた熱電変換性能を発揮でき、しかも有毒なTeも含まないため、家庭での用途も含めて幅広く使用できる。例えば、熱電変換素子、排熱等の熱エネルギー等を電気エネルギーに変換する発電装置、熱電冷却装置、温度センサー等として有用である。
【0044】
また、本発明の熱電変換材料を構成する酸化物は、熱電変換材料以外にも、例えば、電極材料、特にリチウム電池の負極材料として有用である。
【0045】
熱電変換材料の製造方法
本発明の熱電変換材料の製造方法は、1)アルカリ金属元素を含む水酸化物の少なくとも1種(以下、「アルカリ金属水酸化物」とも言う)と、2)コバルトを含む化合物及び金属コバルトの少なくとも1種(以下、「コバルト成分」とも言う)とを含有する混合物を熱処理することを特徴とする。
【0046】
アルカリ金属水酸化物としては特に限定されず、陽イオンとしてリチウムイオン、ナトリウムイオン、カリウムイオン、ルビジウムイオン、セシウムイオン等を含むものが挙げられる。具体的には、水酸化ナトリウム、水酸化リチウム、水酸化カリウム、水酸化ルビジウム、水酸化セシウム等が挙げられる。これらのアルカリ金属水酸化物は単独又は2種以上を混合して使用できる。
【0047】
本発明の製造方法では、アルカリ金属水酸化物としては、特にナトリウムイオンを含むものが好ましく、上記で列挙した中でも、特に水酸化ナトリウムが好ましい。水酸化ナトリウムとしては市販品が使用でき、特に純度90%以上のものが好ましい。
【0048】
コバルト成分としては特に限定されず、金属コバルト、酸化コバルト、塩基性炭酸コバルト、水酸化コバルト、塩化コバルト(6水和物)等が挙げられる。この中でも、未反応の残余物を磁力により容易に除去でき、しかも配向性の高い多結晶体を製造し易い点から金属コバルトが好ましい。
【0049】
本発明の製造方法では、上記1)アルカリ金属水酸化物、2)コバルト成分の原料に、必要に応じて、他の成分を配合することができる。例えば、アルカリ金属元素を含むハロゲン化物(以下、「アルカリ金属ハロゲン化物」とも言う)を好適に配合できる。アルカリ金属ハロゲン化物の量を調整しながら配合することにより、得られる熱電変換材料のアルカリ金属の含有量を制御できる。アルカリ金属ハロゲン化物の配合量は限定的ではないが、アルカリ金属水酸化物100重量部に対して10〜50重量部の範囲内で調整することが好ましい。
【0050】
アルカリ金属ハロゲン化物としては特に限定されない。例えば、陰イオンとしてフッ化物イオン、塩化物イオン、臭化物イオン、ヨウ化物イオン等を含むものが挙げられる。また陽イオンとしてリチウムイオン、ナトリウムイオン、カリウムイオン、ルビジウムイオン、セシウムイオン等を含むものが挙げられる。
【0051】
具体的には、フッ化リチウム、フッ化ナトリウム、フッ化カリウム、フッ化ルビジウム、フッ化セシウム、塩化リチウム、塩化ナトリウム、塩化カリウム、塩化ルビジウム、塩化セシウム、シュウ化リチウム、シュウ化ナトリウム、シュウ化カリウム、シュウ化ルビジウム、シュウ化セシウム、ヨウ化リチウム、ヨウ化ナトリウム、ヨウ化カリウム、ヨウ化ルビジウム、ヨウ化セシウム等が挙げられる。これらは単独又は2種以上を混合して使用できる。
【0052】
本発明の製造方法では、アルカリ金属ハロゲン化物としては、陰イオンとして塩化物イオンを含むものが化学的に安定なため好ましい。具体的には、塩化リチウム、塩化ナトリウム、塩化カリウム、塩化ルビジウム及び塩化セシウムが好ましい。
【0053】
本発明の製造方法では、上記した原料の配合割合は、原料の組み合わせに応じて適宜設定できる。通常は反応生成物がAxCoO2(但し、0<x<0.5、好ましくは0.01≦x≦0.45、より好ましくは0.02≦x≦0.4、最も好ましくは0.02≦x≦0.3)となるように設定すればよい。
【0054】
但し、アルカリ金属元素としてNaを用いる場合には、反応生成物がNaxCoO2(但し、好ましくは0<x≦0.25、より好ましくは0.01≦x≦0.2、最も好ましくは0.02≦x≦0.15)となるように設定すればよい。
【0055】
通常、アルカリ金属水酸化物:アルカリ金属ハロゲン化物:金属コバルト量に換算したコバルト成分=20:(0〜20):0.1〜10(重量比)の範囲内で適宜調整することができる。但し、必ずしもこの範囲に限定されない。
【0056】
次いで、原料を混合する。混合方法は限定的ではなく、例えば、ミキサー、ボールミル、乳鉢等が使用できる。混合物は、熱処理前に、例えば、プレス成形、造粒法等の公知の方法により成形してもよい。
【0057】
次いで、上記混合物又は成形体の熱処理を行う。熱処理温度は特に限定されないが、通常400℃以上、好ましくは500℃〜900℃、より好ましくは550〜800℃、最も好ましくは550℃〜700℃である。熱処理時間は、熱処理温度等に応じて適宜調整すればよい。熱処理雰囲気は、酸化雰囲気又は大気中とすればよい。
【0058】
なお、熱処理する際に容器を用いる場合には、反応生成物を汚染しない容器を用いるのが好ましい。例えば、純度95%以上のアルミナ製容器を好適に使用できる。
【0059】
本発明の製造方法では、従来法と比べて低温域で熱処理するため、アルカリ金属の蒸散を抑制できて得られる材料のアルカリ金属量の制御が容易であり、熱電変換材料としてより高品質な酸化物が得られる。
【0060】
本発明の製造方法では、結晶の粒成長を促進するために、熱処理後の反応生成物を徐冷(30℃/hr以下)することが好ましい。徐冷することにより、大きく粒成長した結晶を含む多結晶体が得られ易くなる。例えば、5mm以上、特に10mm以上の粒径を有する薄片状の多結晶体が得られる。
【0061】
得られた反応生成物は、必要に応じて水洗・乾燥してもよい。水洗によって、反応生成物に残存する未反応原料(アルカリ金属水酸化物、アルカリ金属ハロゲン化物等)を除去できる。乾燥は自然乾燥又は加熱乾燥のいずれでもよい。加熱乾燥の場合の乾燥温度は特に限定されないが、通常300℃以下、好ましくは110〜250℃である。かかる温度範囲であれば効率的に乾燥できる。
【0062】
このような本発明の製造方法は、一般式AxCoO2(但し、0<x<0.5、Aはアルカリ金属元素)で示される酸化物からなる熱電変換材料、特に、一般式NaxCoO2(但し、0<x≦0.25)で示され、かつ塩化カドミウム型結晶構造を有する酸化物からなる熱電変換材料の製造に有用である。
【0063】
【発明の効果】
(1)本発明の熱電変換材料は、一般式AxCoO2(但し、0<x<0.5、Aはアルカリ金属元素)で示される酸化物からなり、従来品(Na0.5CoO2)よりも高いゼーベック係数、熱電変換性能等を有しており、熱電変換材料として優れた性能を発揮する。具体的には、300Kにおけるゼーベック係数が通常80μV/K以上、特に100μV/K以上という優れた値も達成できる。本発明の熱電変換材料は、液体窒素温度から300℃という広い温度範囲で優れた熱電変換特性を発揮できる点、毒性のあるTeを含まない点等において好ましく、家庭での使用を含めて幅広い用途に適用できる。
(2)本発明の熱電変換材料の中でも、一般式NaxCoO2(但し、0<x≦0.25)で示され、かつ塩化カドミウム型結晶構造を有する酸化物からなる熱電変換材料は、特に優れたゼーベック係数、熱電変換性能等を有しており、熱電変換材料として特に優れた性能を発揮できる。具体的には、300Kにおけるゼーベック係数が通常100μV以上、特に150μV/K以上という非常に優れた値も達成できる。
(3)かかる特徴を有する本発明の熱電変換材料は、例えば、熱電変換素子、排熱等の熱エネルギー等を電気エネルギーに変換する発電装置、熱電冷却装置、温度センサー等として有用である。本発明の熱電変換素子を構成する酸化物は、熱電変換材料以外にも、例えば、電極材料、特にリチウム電池の負極材料として有用である。
(4)本発明の製造方法は、上記(1)、特に(2)に記載の熱電変換材料を効率的に製造できる点で有用である。本発明の製造方法においてアルカリ金属水酸化物を用いる利点としては、ナトリウムの供給源として炭酸ナトリウムを用いる従来法と比較して、次の▲1▼〜▲5▼が挙げられる。なお、水酸化ナトリウムを用いる場合には、これらの利点が特に効果的に得られる。
【0064】
▲1▼ 比較的低い温度域で熱処理できるため、製造コストの低減化できる。低温域での熱処理が可能なため、製造過程におけるアルカリ金属の蒸散を抑制又は防止でき、これにより熱設備損耗が低減できるともに反応生成物中のコバルト:アルカリ金属元素比の精度を高めることができる。
【0065】
▲2▼ 低温域での熱処理によって、従来の1050℃に至る高温で熱処理する方法と比べて、同程度又はそれ以上の大きさの六角板状結晶が得られる。
【0066】
▲3▼ 熱処理時に、アルカリ金属元素を含む水酸化物に対して10〜50重量%のアルカリ金属を含むハロゲン化物を混合することによって、結晶体中におけるアルカリ金属元素の含有量を制御することができる。
【0067】
▲4▼ 作製される結晶中に平均孔径100nm以下程度の微細孔を形成させることにより、熱伝導率を低減できるため、従来法により作製されたNa0.5CoO2よりも優れた熱電変換性能が得られる。
【0068】
▲5▼ 特定のフラックスを用いることなく、比較的低温域での熱処理により、大きく粒成長した多結晶体を作製できる。
【0069】
【実施例】
以下に実施例を示し、本発明をより具体的に説明する。但し、本発明は実施例に限定されるものではない。
【0070】
実施例1
(1)製造方法
NaOH:20g、NaCl:5g及び金属Co:1gを秤量して混合し、アルミナルツボ中に入れた。熱処理中のNaOH、NaCl等の蒸散を防ぐため、ルツボにはアルミナ製の蓋をした。次いで、空気中650℃で12時間熱処理した後、電気炉内において冷却速度27℃/hrで徐冷した。反応生成物を蒸留水で洗浄することにより、残留物であるNaOH、NaCl等を除去し、5mm程度の大きさをもつ配向性の高い多結晶体(配向性の高い六角板状の単結晶集合体)が多数得られた。得られた多結晶体を150℃で2時間乾燥した。
(2)反応生成物(多結晶体)の評価方法
上記(1)で得られた反応生成物の物性等を調べた。
【0071】
評価方法としては、先ずX線回折(XRD)パターン及び電子線回折(ED)パターンを測定して所望の物質が得られているかを確認した。また、超高分解能透過型電子顕微鏡(TEM)に付属する元素分析(EDS)装置を用いた観察により、反応生成物の化学組成分析を行った。更に、XRDパターン及びEDパターンにより層間距離を求めた。次いで、TEM像観察により、結晶中の微細な空孔構造を観察した。最後に300Kの温度においてゼーベック係数を測定した。
(3)反応生成物の評価結果
〔XRDパターン〕
反応生成物は、塩化カドミウム型(R−3m)の結晶構造を有していることが確認された。実質的に00L(Lは整数)面に由来する回折ピークのみが観察され、高い配向性を有していることが確認された。当該XRDパターンを従来品のNa0.5CoO2(P6322)のXRDパターンとの比較において図4に示す。
〔化学組成分析〕
反応生成物の化学組成は、Na0.063CoO2であった。
〔層間距離〕
反応生成物の層間距離は0.44nmであった。
〔TEM観察像〕
TEM観察の結果、結晶中に5〜10nmの孔径を有する微細孔(白い部分)が多数存在することが確認できた。
【0072】
本発明の熱電変換材料が従来法で得られたものよりも優れた熱電変換性能を有する理由の一つとして、微細孔が結晶内の熱伝導を減少させていることが考えられる。
【0073】
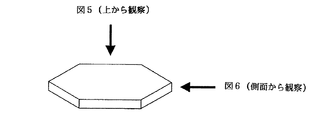
反応生成物:Na0.063CoO2のTEM像観察結果を図5及び図6に示す。図5は六角板状結晶の平面部を観察(上から観察)した結果を示す。図6は六角板状結晶の側面を観察(側面から観察)した結果を示す。六角板状結晶と観察方向との関係を図7に示す。
〔ゼーベック係数〕
300Kでのゼーベック係数は230μV/Kであった。従来法で得られた材料(約100μV/K)と比べて、2倍以上のゼーベック係数であった。
【0074】
実施例2
原料としてNaClを加えなかった他は、実施例1と同様にして多結晶体を作製した。生成物の組成はNa0.33CoO2で表され、300Kでのゼーベック係数は105μV/Kであった。層間距離は0.466nmであった。
【図面の簡単な説明】
【図1】Na0.5CoO2の層状構造(P6322)を示す図である。
【図2】塩化カドミウム型結晶構造を有する酸化物の層状構造(R−3m)を示す図である。
【図3】本発明の熱電変換材料の結晶構造(層状構造)及びその層間距離Lを示す図である。
【図4】実施例1で得られたNa0.063CoO2のX線回折パターンを示す図である。
【図5】実施例1で得られたNa0.063CoO2のTEM像(上から観察:×49万倍)である。
【図6】実施例1で得られたNa0.063CoO2のTEM像(側面から観察:×49万倍)である。
【図7】実施例1で得られたNa0.063CoO2のTEM観察における、六角板状結晶と観察方向との関係を示す図である。[0001]
BACKGROUND OF THE INVENTION
The present invention relates to a novel thermoelectric conversion material and a method for producing the same.
[0002]
[Prior art]
In recent years, environmental issues and the problem of alternative energy for fossil fuels have attracted much social attention. Under such circumstances, for example, a) thermoelectric conversion energy technology that effectively converts unused heat energy such as exhaust heat into electrical energy without discharging harmful gases such as carbon dioxide and nitrogen oxides; b) harmful Expectations are growing for thermoelectric cooling technology that does not use chlorofluorocarbon-based gases. In order to meet these expectations, development of high-performance thermoelectric conversion materials is essential.
[0003]
A thermoelectric conversion material is a material that can convert thermal energy and electrical energy to each other, and its figure of merit (Z) is given by:
Z = S2/ (Ρκ)
In the formula, S represents the thermoelectromotive force (Seebeck coefficient), ρ represents the electrical resistivity, and κ represents the thermal conductivity. In order to increase the thermoelectric conversion efficiency, it is necessary that the absolute value of S is large and both ρ and κ are small.
[0004]
Various thermoelectric conversion materials have been proposed so far. For example, Bi2TeThreeThe system thermoelectric conversion material exhibits a high performance index in a temperature range from room temperature to 200 ° C., and is used as a Peltier element for thermoelectric cooling or the like. The PbTe-based thermoelectric conversion material exhibits a high performance index in a temperature range of 200 ° C. to 500 ° C., and is mainly used as a power generator.
[0005]
However, since these are non-oxide materials, there is a problem that the synthesis process is complicated. Moreover, since Te which comprises these thermoelectric conversion materials is scarce as a resource and is toxic, there exists a problem when the influence on an environment and use in a general household are considered. For these reasons, a search for a new thermoelectric conversion material that does not contain harmful elements in an oxide material that is relatively easy to synthesize is underway.
[0006]
Under such circumstances, in particular, α-NaFeO2Na, an oxide having a type crystal structure0.5CoO2Is in the limelight as a thermoelectric conversion material.
[0007]
[0008]
[0009]
Na0.5CoO2As shown in FIG.2Layered compound in which layers and Na layers are alternately laminated, and P6ThreeIt has a crystal structure with 22 symmetry. The symmetry of the crystal can be easily confirmed by, for example, X-ray diffraction. P6ThreeAn example of an X-ray diffraction pattern representing 22 symmetry is shown by a dotted line in FIG.
[0010]
CoO2In the layer, CoO6The octahedron shares a ridge. In the Na layer, Na randomly occupies 1/2 of Na sites, and atomic vacancy type lattice defects exist in the remaining 1/2 sites. Of these layers, electrical conduction is CoO.2The Na layer is thought to be responsible for the heat conduction. As a result, Na0.5CoO2Exhibits excellent thermoelectric conversion characteristics in a wide temperature range from liquid nitrogen temperature to 400 ° C. or higher.
[0011]
However, P6ThreeNa with 22 symmetry0.5CoO2Then, CoO2The inter-layer distance of the layers is relatively large at 0.54 nm, and CoO contained per unit volume2Since the number of layers and Na layers is small, CoO2The electric conduction efficiency by the layer and the heat conduction inhibition efficiency by the Na layer are not sufficient.
[0012]
Therefore, Na0.5CoO2The Seebeck coefficient is still inadequate, and further improvement is necessary to achieve a more practical thermoelectric conversion material. In this regard,
[0013]
Na0.5CoO2And a crystal in which Na or Co in the crystal is partially substituted with another element have anisotropy in thermoelectric conversion performance. For example, Na0.5CoO2Then, CoO2The in-plane of the layer (ie, the direction perpendicular to the c-axis) shows good electrical conduction and CoO2Since the conductivity between layers (ie, c-axis direction) is poor, CoO2A large thermoelectric conversion performance is exhibited only in the plane of the layer (that is, in a direction perpendicular to the c-axis).
[0014]
When collecting crystals having such anisotropy to produce a polycrystal, Na0.5CoO2In the polycrystalline body in which the orientations of the crystals shown in FIG. 2 are randomly assembled, there is a problem that the thermoelectric conversion performance is greatly deteriorated and becomes disadvantageous as compared with the single crystal.
[0015]
In
[0016]
However, such a method for producing a polycrystalline body has a problem in that thermoelectric conversion performance is deteriorated because the crystal is thermally decomposed during heat treatment to produce cobalt oxide as an insulator as an impurity.
[0017]
Furthermore, the Na0.5CoO2In this production method, carbonates and oxides are used as the source of alkali metal elements, but since heat treatment at high temperatures is required, alkali metals are likely to evaporate and it is difficult to control the amount of alkali metals. . In addition, it is difficult to produce a cobalt-containing layered oxide that is stable in the atmosphere containing an alkali metal other than Li and Na (for example, K, Rb, Cs, etc.).
[0018]
[Non-Patent Document 1]
Ichiro Terasaki, Yoshitaka Saeko, Kunimitsu Uchinokura, “Physical Review B”, USA, No. 56, 1997, p. R12585
[0019]
[Non-Patent Document 2]
M. M.Von Jansen, Earl. Hope, "Zeitschrift fur Anorganisch und Allegorisch Chemie", Germany, No. 408, 1974, p. 104
[0020]
[Patent Document 1]
Japanese Patent Laid-Open No. 11-266038
[0021]
[Patent Document 2]
JP 2000-269560 A
[0022]
[Problems to be solved by the invention]
The main object of the present invention is to efficiently provide a material having superior thermoelectric conversion performance than conventional products.
[0023]
[Means for Solving the Problems]
As a result of intensive studies to achieve the above object, the present inventor has found that a material produced by a specific method can achieve the above object, and has completed the present invention.
[0024]
That is, this invention relates to the following thermoelectric conversion material and its manufacturing method.
1. General formula Na x CoO 2 A thermoelectric conversion material composed of an oxide represented by (where 0 <x ≦ 0.25) and having a cadmium chloride type crystal structure.
2.
3.
4).
5.1) heat-treating a mixture containing at least one hydroxide containing an alkali metal element and 2) at least one compound containing cobalt and at least one metal cobalt. x CoO 2 (However, 0 <x ≦ 0.25) and a method for producing a thermoelectric conversion material comprising an oxide having a cadmium chloride type crystal structure.
6). Item 6. The method for producing a thermoelectric conversion material according to Item 5, wherein at least one of the hydroxides containing an alkali metal element is sodium hydroxide.
7). Furthermore, the manufacturing method of the thermoelectric conversion material of said claim | item 5 or 6 which mix | blends the halide containing an alkali metal element.
[0025]
DETAILED DESCRIPTION OF THE INVENTION
Thermoelectric conversion material
The thermoelectric conversion material of the present invention has a general formula AxCoO2(Where 0 <x <0.5, A is an alkali metal element).
[0026]
As the alkali metal element, at least one of Li, Na, K, Rb and Cs is preferable. Among these, Na is more preferably used in the present invention.
[0027]
The above x represents the content of an alkali metal element, and the value is 0 <x <0.5, preferably 0.01 ≦ x ≦ 0.45, more preferably 0.02 ≦ x ≦ 0.4, and most preferably Is 0.02 ≦ x ≦ 0.3. By limiting to this content, conventional products (Na0.5CoO2) And superior thermoelectric conversion performance.
[0028]
In particular, when Na is used as the alkali metal element, the value of x is preferably 0 <x ≦ 0.25, more preferably 0.01 ≦ x ≦ 0.2, and 0.02 ≦ x ≦ 0.15. Most preferred. An oxide using Na as an alkali metal element and having the value of x limited to a range of 0 <x ≦ 0.25 has a cadmium chloride crystal structure, and thus can exhibit particularly excellent thermoelectric conversion performance.
[0029]
That is, the general formula AxCoO2(However, among the thermoelectric conversion materials of the present invention comprising an oxide represented by 0 <x <0.5, A is an alkali metal element), the general formula NaxCoO2(However, a thermoelectric conversion material composed of an oxide represented by 0 <x ≦ 0.25) and having a cadmium chloride type crystal structure is particularly preferable.
[0030]
In the thermoelectric conversion material of the present invention, the general formula NaxCoO2(However, the oxide structure is not constant except for the oxides represented by 0 <x ≦ 0.25) and having a cadmium chloride type crystal structure, but generally the more the content of alkali metal elements, Cadmium chloride type crystal structure and α-NaFeO2There is a tendency to be a mixed crystal with a type crystal structure.
[0031]
The cadmium chloride type crystal structure has crystal symmetry represented by R-3m, for example, as shown in the schematic diagram of FIG. FIG. 3 shows Na having a cadmium chloride type crystal structure (R-3m).xCoO2(However, the layered structure of 0 <x ≦ 0.25) is specifically illustrated. As shown in FIG. 3, the cadmium chloride type crystal structure is α-NaFeO.2Type crystal structure (P6Three22) Na0.5CoO2Similarly to the above, a stacked structure having [A-O-Co-O (A is an alkali metal)] as a minimum unit is formed in the c-axis direction.
[0032]
On the other hand, in the cadmium chloride type crystal structure (R-3m), the laminated structure of the oxygen layer with respect to the c-axis direction is α-NaFeO.2Type crystal structure (P6Three22).
[0033]
For example, a) an oxygen layer stacking method is defined as α, b) an oxygen layer stacking method different from α is defined as β, and c) an oxygen layer stacking method different from both α and β is defined as γ. The laminated structure of the oxygen layer is expressed as shown in FIG. 1 and FIG.
[0034]
FIG. 1 shows α-NaFeO.21 shows a stacked structure of a type crystal structure, and the stacked structure of an oxygen layer has (αββα) as a minimum unit. On the other hand, FIG. 2 shows a laminated structure of a cadmium chloride type crystal structure, and the laminated form of the oxygen layer has (αβγ) as a minimum unit.
[0035]
Note that the two crystal structures can be clearly distinguished by an X-ray diffraction (XRD) pattern, an electron beam diffraction (ED) pattern, or the like.
[0036]
Thus, in the cadmium chloride type crystal structure, since the oxygen layer is stacked with (αβγ) as the minimum unit, the conventional α-NaFeO having (αββα) as the minimum unit.2Compared to the type crystal structure, the oxygen layer can be stacked more densely. That is, CoO contained per unit volume2Since the number of layers and Na layers increases, CoO2The electric conduction efficiency by the layer and the heat conduction inhibition efficiency by the Na layer are increased, and as a result, the heat transfer performance can be increased synergistically.
[0037]
As shown in FIG. 3, the interlayer distance L is determined as CoO.2In a crystal structure in which layers and alkali metal layers are alternately stacked, one CoO2Co face (2) contained in layer (1) and the CoO2CoO closest to layer (1)2It refers to the spacing between the Co plane (4) contained in the layer (3). The interlayer distance L can be calculated by X-ray diffraction (XRD) analysis and high-resolution transmission electron microscope (TEM).
[0038]
In the thermoelectric conversion material of the present invention, CoO2The interlayer distance L between the layers is preferably about 0.3 nm <L <0.54 nm, and more preferably 0.45 nm ≦ L ≦ 0.47 nm. By limiting the interlayer distance to such a range, the thermoelectric conversion performance can be further enhanced.
[0039]
The thermoelectric conversion material of the present invention may be composed of either single crystal or polycrystal (including a single crystal aggregate). In the present invention, it is preferable that the thermoelectric conversion performance of the present invention is made of a single crystal or a single crystal aggregate having a substantially high orientation, particularly from the viewpoint of more reliably obtaining excellent thermoelectric conversion performance.
[0040]
As the degree of orientation, in the XRD pattern, a crystal plane perpendicular to the c-axis (lamination direction of the layered structure) when the crystal structure is displayed in a hexagonal crystal plane, that is, a crystal plane other than the (00L) (L is an integer) plane. All of the thermoelectric conversion materials of the present invention include those in which the derived XRD peak is not substantially observed. Note that in a highly oriented polycrystal, crystals having other compositions (for example, CoO) can be used as long as a predetermined thermoelectric conversion performance is obtained.2) Etc. may be included.
[0041]
The thermoelectric conversion material of the present invention is preferably porous. Specifically, it is preferable to have fine pores in the crystal having an average pore diameter of 100 nm or less, preferably 50 nm or less, particularly 5 to 10 nm. If it is a porous material, since thermal conductivity can be reduced, the thermoelectric conversion performance can be more effectively enhanced.
[0042]
Such a thermoelectric conversion material of the present invention can achieve an excellent value such that the Seebeck coefficient at 300K is usually 80 μV / K or more, particularly 100 μV / K or more. Among the thermoelectric conversion materials of the present invention, in particular, the general formula NaxCoO2(Provided that 0 <x ≦ 0.25) and an oxide having a cadmium chloride type crystal structure has an excellent value such that the Seebeck coefficient at 300K is usually 100 μV or more, particularly 150 μV / K or more. Can also be achieved.
[0043]
The thermoelectric conversion material of the present invention can exhibit excellent thermoelectric conversion performance in a wide temperature range from liquid nitrogen temperature to 300 ° C. and does not contain toxic Te, and can be used widely including home use. For example, it is useful as a thermoelectric conversion element, a power generation device that converts heat energy such as exhaust heat into electrical energy, a thermoelectric cooling device, a temperature sensor, and the like.
[0044]
Moreover, the oxide which comprises the thermoelectric conversion material of this invention is useful as an electrode material, especially a negative electrode material of a lithium battery other than a thermoelectric conversion material, for example.
[0045]
Method for producing thermoelectric conversion material
The method for producing a thermoelectric conversion material of the present invention comprises 1) at least one hydroxide containing an alkali metal element (hereinafter also referred to as “alkali metal hydroxide”), 2) a compound containing cobalt, and metal cobalt. A mixture containing at least one (hereinafter also referred to as “cobalt component”) is heat-treated.
[0046]
It does not specifically limit as an alkali metal hydroxide, What contains lithium ion, sodium ion, potassium ion, rubidium ion, a cesium ion etc. as a cation is mentioned. Specific examples include sodium hydroxide, lithium hydroxide, potassium hydroxide, rubidium hydroxide, cesium hydroxide and the like. These alkali metal hydroxides can be used alone or in admixture of two or more.
[0047]
In the production method of the present invention, as the alkali metal hydroxide, those containing sodium ions are particularly preferable, and sodium hydroxide is particularly preferable among those listed above. As the sodium hydroxide, a commercially available product can be used, and those having a purity of 90% or more are particularly preferred.
[0048]
It does not specifically limit as a cobalt component, Metal cobalt, cobalt oxide, basic cobalt carbonate, cobalt hydroxide, cobalt chloride (hexahydrate) etc. are mentioned. Among these, metal cobalt is preferable because unreacted residues can be easily removed by magnetic force and a highly oriented polycrystalline body can be easily produced.
[0049]
In the production method of the present invention, other components can be blended in the raw materials of 1) alkali metal hydroxide and 2) cobalt component as necessary. For example, a halide containing an alkali metal element (hereinafter also referred to as “alkali metal halide”) can be suitably blended. By blending while adjusting the amount of alkali metal halide, the content of alkali metal in the resulting thermoelectric conversion material can be controlled. The blending amount of the alkali metal halide is not limited, but is preferably adjusted within a range of 10 to 50 parts by weight with respect to 100 parts by weight of the alkali metal hydroxide.
[0050]
The alkali metal halide is not particularly limited. For example, the anion includes fluoride ion, chloride ion, bromide ion, iodide ion and the like. Moreover, what contains lithium ion, sodium ion, potassium ion, rubidium ion, cesium ion etc. as a cation is mentioned.
[0051]
Specifically, lithium fluoride, sodium fluoride, potassium fluoride, rubidium fluoride, cesium fluoride, lithium chloride, sodium chloride, potassium chloride, rubidium chloride, cesium chloride, lithium oxalate, sodium oxalate, oxalate Examples include potassium, rubidium oxalate, cesium oxalate, lithium iodide, sodium iodide, potassium iodide, rubidium iodide, cesium iodide, and the like. These can be used individually or in mixture of 2 or more types.
[0052]
In the production method of the present invention, alkali metal halides containing chloride ions as anions are preferable because they are chemically stable. Specifically, lithium chloride, sodium chloride, potassium chloride, rubidium chloride and cesium chloride are preferable.
[0053]
In the production method of the present invention, the blending ratio of the raw materials described above can be appropriately set according to the combination of the raw materials. Usually the reaction product is AxCoO2(However, 0 <x <0.5, preferably 0.01 ≦ x ≦ 0.45, more preferably 0.02 ≦ x ≦ 0.4, most preferably 0.02 ≦ x ≦ 0.3) What is necessary is just to set.
[0054]
However, when Na is used as the alkali metal element, the reaction product is NaxCoO2(However, it is preferable to set so that 0 <x ≦ 0.25, more preferably 0.01 ≦ x ≦ 0.2, and most preferably 0.02 ≦ x ≦ 0.15).
[0055]
Usually, it can adjust suitably in the range of alkali metal hydroxide: alkali metal halide: cobalt component converted into the amount of metallic cobalt = 20: (0-20): 0.1-10 (weight ratio). However, it is not necessarily limited to this range.
[0056]
Next, the raw materials are mixed. The mixing method is not limited. For example, a mixer, a ball mill, a mortar or the like can be used. You may shape | mold a mixture by well-known methods, such as press molding and a granulation method, before heat processing.
[0057]
Next, the mixture or molded body is heat-treated. Although heat processing temperature is not specifically limited, Usually, 400 degreeC or more, Preferably it is 500 to 900 degreeC, More preferably, it is 550 to 800 degreeC, Most preferably, it is 550 to 700 degreeC. The heat treatment time may be appropriately adjusted according to the heat treatment temperature and the like. The heat treatment atmosphere may be an oxidizing atmosphere or air.
[0058]
In addition, when using a container at the time of heat processing, it is preferable to use the container which does not contaminate a reaction product. For example, an alumina container having a purity of 95% or more can be suitably used.
[0059]
In the production method of the present invention, heat treatment is performed at a lower temperature than in the conventional method, so that it is easy to control the amount of alkali metal in the material obtained by suppressing transpiration of alkali metal, and higher quality oxidation as a thermoelectric conversion material. Things are obtained.
[0060]
In the production method of the present invention, the reaction product after the heat treatment is preferably gradually cooled (30 ° C./hr or less) in order to promote crystal grain growth. By slowly cooling, it becomes easy to obtain a polycrystalline body containing crystals with large grain growth. For example, a flaky polycrystalline body having a particle size of 5 mm or more, particularly 10 mm or more is obtained.
[0061]
The obtained reaction product may be washed with water and dried as necessary. By washing with water, unreacted raw materials (alkali metal hydroxide, alkali metal halide, etc.) remaining in the reaction product can be removed. Drying may be either natural drying or heat drying. Although the drying temperature in the case of heat drying is not specifically limited, Usually, it is 300 degrees C or less, Preferably it is 110-250 degreeC. If it is this temperature range, it can dry efficiently.
[0062]
Such a production method of the present invention has the general formula AxCoO2(However, 0 <x <0.5, A is an alkali metal element)xCoO2(However, it is useful for the production of a thermoelectric conversion material composed of an oxide represented by 0 <x ≦ 0.25) and having a cadmium chloride type crystal structure.
[0063]
【The invention's effect】
(1) The thermoelectric conversion material of the present invention has a general formula AxCoO2(However, 0 <x <0.5, A is an alkali metal element)0.5CoO2) Higher Seebeck coefficient, thermoelectric conversion performance, etc., and exhibits excellent performance as a thermoelectric conversion material. Specifically, an excellent value can be achieved in which the Seebeck coefficient at 300K is usually 80 μV / K or more, particularly 100 μV / K or more. The thermoelectric conversion material of the present invention is preferable in that it can exhibit excellent thermoelectric conversion characteristics in a wide temperature range from liquid nitrogen temperature to 300 ° C., does not contain toxic Te, and has a wide range of uses including use at home. Applicable to.
(2) Among the thermoelectric conversion materials of the present invention, the general formula NaxCoO2(However, 0 <x ≦ 0.25) and a thermoelectric conversion material made of an oxide having a cadmium chloride type crystal structure has a particularly excellent Seebeck coefficient, thermoelectric conversion performance, etc. Excellent performance can be exhibited as a material. Specifically, a very excellent value such that the Seebeck coefficient at 300 K is usually 100 μV or more, particularly 150 μV / K or more can be achieved.
(3) The thermoelectric conversion material of the present invention having such characteristics is useful as, for example, a thermoelectric conversion element, a power generation device that converts heat energy such as exhaust heat into electric energy, a thermoelectric cooling device, a temperature sensor, and the like. In addition to the thermoelectric conversion material, the oxide constituting the thermoelectric conversion element of the present invention is useful as, for example, an electrode material, particularly a negative electrode material for a lithium battery.
(4) The production method of the present invention is useful in that the thermoelectric conversion material according to the above (1), particularly (2) can be efficiently produced. Advantages of using an alkali metal hydroxide in the production method of the present invention include the following (1) to (5) as compared with the conventional method using sodium carbonate as a sodium supply source. When sodium hydroxide is used, these advantages can be obtained particularly effectively.
[0064]
(1) Since the heat treatment can be performed in a relatively low temperature range, the manufacturing cost can be reduced. Since heat treatment in a low temperature range is possible, it is possible to suppress or prevent transpiration of alkali metal during the production process, thereby reducing heat equipment wear and increasing the accuracy of the cobalt: alkali metal element ratio in the reaction product. .
[0065]
{Circle around (2)} By the heat treatment in the low temperature region, a hexagonal plate-like crystal having the same or larger size can be obtained as compared with the conventional method of heat treatment up to 1050 ° C.
[0066]
(3) It is possible to control the content of the alkali metal element in the crystal by mixing a halide containing 10 to 50% by weight of the alkali metal with respect to the hydroxide containing the alkali metal element during the heat treatment. it can.
[0067]
(4) Since the thermal conductivity can be reduced by forming micropores with an average pore diameter of about 100 nm or less in the produced crystal, Na produced by the conventional method is used.0.5CoO2Better thermoelectric conversion performance.
[0068]
(5) A polycrystal having large grains can be produced by heat treatment at a relatively low temperature without using a specific flux.
[0069]
【Example】
Hereinafter, the present invention will be described in more detail with reference to examples. However, the present invention is not limited to the examples.
[0070]
Example 1
(1) Manufacturing method
NaOH: 20 g, NaCl: 5 g and metal Co: 1 g were weighed and mixed, and placed in an alumina crucible. In order to prevent evaporation of NaOH, NaCl, etc. during heat treatment, the crucible was covered with an alumina lid. Next, after heat treatment in air at 650 ° C. for 12 hours, it was gradually cooled in an electric furnace at a cooling rate of 27 ° C./hr. The reaction product is washed with distilled water to remove residual NaOH, NaCl, etc., and a highly oriented polycrystal having a size of about 5 mm (a highly oriented hexagonal plate-like single crystal aggregate Many bodies were obtained. The obtained polycrystal was dried at 150 ° C. for 2 hours.
(2) Evaluation method of reaction product (polycrystal)
The physical properties of the reaction product obtained in (1) above were examined.
[0071]
As an evaluation method, first, an X-ray diffraction (XRD) pattern and an electron beam diffraction (ED) pattern were measured to confirm whether a desired substance was obtained. Moreover, the chemical composition analysis of the reaction product was performed by observation using the elemental analysis (EDS) apparatus attached to an ultra high resolution transmission electron microscope (TEM). Furthermore, the interlayer distance was determined from the XRD pattern and the ED pattern. Next, a fine pore structure in the crystal was observed by TEM image observation. Finally, the Seebeck coefficient was measured at a temperature of 300K.
(3) Evaluation results of reaction products
[XRD pattern]
It was confirmed that the reaction product had a cadmium chloride type (R-3m) crystal structure. Only a diffraction peak substantially derived from the 00L (L is an integer) plane was observed, and it was confirmed that the film had high orientation. The XRD pattern is changed to the conventional Na0.5CoO2(P6ThreeComparison with the XRD pattern of 22) is shown in FIG.
[Chemical composition analysis]
The chemical composition of the reaction product is Na0.063CoO2Met.
[Distance between layers]
The interlayer distance of the reaction product was 0.44 nm.
[TEM observation image]
As a result of TEM observation, it was confirmed that a large number of micropores (white portions) having a pore diameter of 5 to 10 nm exist in the crystal.
[0072]
One of the reasons why the thermoelectric conversion material of the present invention has a thermoelectric conversion performance superior to that obtained by the conventional method may be that the micropores reduce the heat conduction in the crystal.
[0073]
Reaction product: Na0.063CoO2TEM image observation results are shown in FIGS. FIG. 5 shows the result of observing (observing from above) the flat portion of the hexagonal plate crystal. FIG. 6 shows the result of observing the side surface of the hexagonal plate crystal (observed from the side surface). The relationship between the hexagonal plate crystal and the observation direction is shown in FIG.
[Seebeck coefficient]
The Seebeck coefficient at 300K was 230 μV / K. Compared with the material obtained by the conventional method (about 100 μV / K), the Seebeck coefficient was twice or more.
[0074]
Example 2
A polycrystal was produced in the same manner as in Example 1 except that NaCl was not added as a raw material. The composition of the product is Na0.33CoO2The Seebeck coefficient at 300K was 105 μV / K. The interlayer distance was 0.466 nm.
[Brief description of the drawings]
FIG. 1 Na0.5CoO2Layered structure (P6Three22).
FIG. 2 is a diagram showing a layered structure (R-3m) of an oxide having a cadmium chloride type crystal structure.
FIG. 3 is a diagram showing a crystal structure (layered structure) of a thermoelectric conversion material of the present invention and an interlayer distance L thereof.
4 shows Na obtained in Example 1. FIG.0.063CoO2It is a figure which shows the X-ray-diffraction pattern of.
FIG. 5 shows Na obtained in Example 1.0.063CoO2TEM image (observed from above: × 490,000 times).
6 shows Na obtained in Example 1. FIG.0.063CoO2TEM image (observed from the side: × 490,000 times).
7 shows Na obtained in Example 1. FIG.0.063CoO2It is a figure which shows the relationship between the hexagonal plate-shaped crystal | crystallization and observation direction in TEM observation of.
Claims (7)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002347322A JP4164652B2 (en) | 2001-11-29 | 2002-11-29 | Thermoelectric conversion material and method for producing the same |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2001363880 | 2001-11-29 | ||
| JP2001-363880 | 2001-11-29 | ||
| JP2002347322A JP4164652B2 (en) | 2001-11-29 | 2002-11-29 | Thermoelectric conversion material and method for producing the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2003229605A JP2003229605A (en) | 2003-08-15 |
| JP4164652B2 true JP4164652B2 (en) | 2008-10-15 |
Family
ID=27759440
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002347322A Expired - Fee Related JP4164652B2 (en) | 2001-11-29 | 2002-11-29 | Thermoelectric conversion material and method for producing the same |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4164652B2 (en) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4543127B2 (en) * | 2005-03-17 | 2010-09-15 | 独立行政法人産業技術総合研究所 | Structure of oxide thermoelectric conversion material |
| CN101032038B (en) * | 2005-08-16 | 2010-04-21 | 松下电器产业株式会社 | Thermoelectric conversion device, and cooling method and power generation method using the same |
| JP5011949B2 (en) * | 2006-10-25 | 2012-08-29 | トヨタ自動車株式会社 | Thermoelectric conversion element and manufacturing method thereof |
| JP5398050B2 (en) * | 2008-03-26 | 2014-01-29 | 株式会社Gsユアサ | Cobalt compound, alkaline battery, and method for producing positive electrode for alkaline storage battery |
| JP6411782B2 (en) * | 2013-08-07 | 2018-10-24 | 株式会社Nttファシリティーズ | Method for manufacturing thermoelectric material |
| EP3428984A4 (en) | 2016-03-09 | 2019-11-20 | Japan Science And Technology Agency | Thermoelectric conversion material, and thermoelectric conversion device, thermochemical battery and thermoelectric sensor having said material |
| TW201829572A (en) * | 2016-09-21 | 2018-08-16 | 日商日產化學工業股份有限公司 | Composition for forming thermoelectric conversion layer and production method for thermoelectric conversion layer |
| KR102445508B1 (en) | 2016-12-13 | 2022-09-20 | 린텍 가부시키가이샤 | Thermoelectric conversion material and manufacturing method thereof |
-
2002
- 2002-11-29 JP JP2002347322A patent/JP4164652B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2003229605A (en) | 2003-08-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Koumoto et al. | Thermoelectric ceramics for energy harvesting | |
| Koumoto et al. | Thermoelectric properties of single crystal CuAlO2 with a layered structureElectronic supplementary information (ESI) available: crystal structure of delafossite-type ABO2; SEM image, XRD patterns, ED and HRTEM images of a CuAlO2 single crystal. See http://www. rsc. org/suppdata/jm/b0/b006850k | |
| US10950774B2 (en) | Thermoelectric materials and devices comprising graphene | |
| Pei et al. | Enhancing the thermoelectric performance of Ce x Bi 2 S 3 by optimizing the carrier concentration combined with band engineering | |
| KR101902925B1 (en) | Thermoelectric material, thermoelectric element, and thermoelectric module | |
| KR20120106730A (en) | Gasb-filled skutterudite composite material and method of preparing the same | |
| Liu et al. | Optimising the thermoelectric properties of Bi2Sr2Co2Oy using Ag substitution and Nano-SiC doping | |
| Romo-De-La-Cruz et al. | Role of oversized dopant potassium on the nanostructure and thermoelectric performance of calcium cobaltite ceramics | |
| JP4164652B2 (en) | Thermoelectric conversion material and method for producing the same | |
| Park et al. | Thermoelectric properties of Ca 0.8 Dy 0.2 MnO 3 synthesized by solution combustion process | |
| Ashok | Realization of high thermoelectric power factor in Ta-doped ZnO by grain boundary engineering | |
| JP4168628B2 (en) | Thermoelectric conversion material and method of using the same | |
| KR102180065B1 (en) | Rare-earth metals including complex Zintl compounds and manufacturing method of the same compounds | |
| Vengust et al. | Improved environmental stability of thermoelectric ceramics based on intergrowths of Ca3Co4O9–Na0. 75CoO2 | |
| KR101948159B1 (en) | Ytterbium and Germanium Doped Quaternary Zintl Compound And Manufacturing Method Thereof | |
| Song et al. | Phase evolution and thermoelectric performance of calcium cobaltite upon high temperature aging | |
| JP4608940B2 (en) | Thermoelectric material | |
| JP4013245B2 (en) | CRYSTAL-ORIENTED CERAMIC AND PROCESS FOR PRODUCING THE SAME, PLATE POWDER FOR PRODUCTION OF CRYSTAL-ORIENTED CERAMIC, AND THERMOELECTRIC CONV | |
| JP2004087537A (en) | P type thermoelectric converting material and its manufacturing method | |
| JP3515478B2 (en) | Thermoelectric conversion material, thermoelectric conversion element, thermal battery and cooler | |
| JP2003188425A (en) | Thermoelectric transductional material and element using the same | |
| JP2004134454A (en) | Thermoelectric conversion material and its manufacturing method | |
| JP4143724B2 (en) | Method for producing complex oxide single crystal | |
| JP3472814B2 (en) | Composite oxide with excellent thermoelectric conversion performance | |
| JP4844043B2 (en) | Thermoelectric conversion material and method for producing the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20041022 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20070306 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080402 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080530 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080625 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080715 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110808 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |