JP2022511366A - 神経変性疾患の処置における神経保護剤としてのドネコプリド - Google Patents
神経変性疾患の処置における神経保護剤としてのドネコプリド Download PDFInfo
- Publication number
- JP2022511366A JP2022511366A JP2021517453A JP2021517453A JP2022511366A JP 2022511366 A JP2022511366 A JP 2022511366A JP 2021517453 A JP2021517453 A JP 2021517453A JP 2021517453 A JP2021517453 A JP 2021517453A JP 2022511366 A JP2022511366 A JP 2022511366A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- group
- mice
- neurons
- disease
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 230000004770 neurodegeneration Effects 0.000 title claims abstract description 60
- 208000015122 neurodegenerative disease Diseases 0.000 title claims abstract description 56
- 238000011282 treatment Methods 0.000 title claims abstract description 30
- 239000004090 neuroprotective agent Substances 0.000 title claims abstract description 14
- 150000001875 compounds Chemical class 0.000 claims abstract description 188
- 230000002265 prevention Effects 0.000 claims abstract description 13
- 208000024827 Alzheimer disease Diseases 0.000 claims description 32
- 208000023105 Huntington disease Diseases 0.000 claims description 17
- 208000018737 Parkinson disease Diseases 0.000 claims description 17
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 17
- 230000007850 degeneration Effects 0.000 claims description 13
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 11
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 claims description 10
- 239000000460 chlorine Substances 0.000 claims description 10
- 229910052801 chlorine Inorganic materials 0.000 claims description 10
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 claims description 10
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 9
- 125000000217 alkyl group Polymers 0.000 claims description 8
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 claims description 8
- 229910052731 fluorine Inorganic materials 0.000 claims description 8
- 239000011737 fluorine Substances 0.000 claims description 8
- 208000005264 motor neuron disease Diseases 0.000 claims description 8
- 125000004434 sulfur atom Chemical group 0.000 claims description 8
- 150000003839 salts Chemical class 0.000 claims description 7
- 229910052717 sulfur Chemical group 0.000 claims description 7
- 239000002253 acid Substances 0.000 claims description 6
- 125000001153 fluoro group Chemical group F* 0.000 claims description 6
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 5
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 5
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 5
- 125000005843 halogen group Chemical group 0.000 claims description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 5
- 201000010374 Down Syndrome Diseases 0.000 claims description 4
- 206010044688 Trisomy 21 Diseases 0.000 claims description 4
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 3
- 125000002619 bicyclic group Chemical group 0.000 claims description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 3
- 229910052794 bromium Inorganic materials 0.000 claims description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 3
- 239000012453 solvate Substances 0.000 claims description 3
- 208000001089 Multiple system atrophy Diseases 0.000 claims description 2
- 125000006527 (C1-C5) alkyl group Chemical group 0.000 claims 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 claims 1
- NPDLYUOYAGBHFB-WDSKDSINSA-N Asn-Arg Chemical group NC(=O)C[C@H](N)C(=O)N[C@H](C(O)=O)CCCN=C(N)N NPDLYUOYAGBHFB-WDSKDSINSA-N 0.000 claims 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims 1
- 239000011630 iodine Substances 0.000 claims 1
- 229910052740 iodine Inorganic materials 0.000 claims 1
- 241000699670 Mus sp. Species 0.000 description 199
- 210000002569 neuron Anatomy 0.000 description 95
- 230000000694 effects Effects 0.000 description 86
- 210000002241 neurite Anatomy 0.000 description 80
- 238000012360 testing method Methods 0.000 description 74
- 239000003981 vehicle Substances 0.000 description 69
- ADEBPBSSDYVVLD-UHFFFAOYSA-N donepezil Chemical compound O=C1C=2C=C(OC)C(OC)=CC=2CC1CC(CC1)CCN1CC1=CC=CC=C1 ADEBPBSSDYVVLD-UHFFFAOYSA-N 0.000 description 68
- 210000004027 cell Anatomy 0.000 description 59
- 239000000243 solution Substances 0.000 description 57
- 102100023174 Methionine aminopeptidase 2 Human genes 0.000 description 45
- 108090000192 Methionyl aminopeptidases Proteins 0.000 description 44
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 37
- 210000004295 hippocampal neuron Anatomy 0.000 description 36
- 238000000034 method Methods 0.000 description 35
- 239000001397 quillaja saponaria molina bark Substances 0.000 description 35
- 229930182490 saponin Natural products 0.000 description 35
- 150000007949 saponins Chemical class 0.000 description 35
- 241001465754 Metazoa Species 0.000 description 33
- 239000002609 medium Substances 0.000 description 33
- 230000000324 neuroprotective effect Effects 0.000 description 33
- 239000007924 injection Substances 0.000 description 32
- 238000002347 injection Methods 0.000 description 32
- 210000000225 synapse Anatomy 0.000 description 32
- 238000004458 analytical method Methods 0.000 description 31
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 30
- 230000006399 behavior Effects 0.000 description 30
- 229960003530 donepezil Drugs 0.000 description 30
- 238000001543 one-way ANOVA Methods 0.000 description 30
- 230000004083 survival effect Effects 0.000 description 30
- 108010064539 amyloid beta-protein (1-42) Proteins 0.000 description 28
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 27
- 229930195712 glutamate Natural products 0.000 description 27
- 241000700159 Rattus Species 0.000 description 26
- 108010026424 tau Proteins Proteins 0.000 description 26
- 102000013498 tau Proteins Human genes 0.000 description 26
- 238000010790 dilution Methods 0.000 description 25
- 239000012895 dilution Substances 0.000 description 25
- 238000011818 5xFAD mouse Methods 0.000 description 23
- 210000004556 brain Anatomy 0.000 description 22
- 239000001963 growth medium Substances 0.000 description 22
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 21
- 230000006378 damage Effects 0.000 description 20
- 239000012091 fetal bovine serum Substances 0.000 description 20
- 238000010150 least significant difference test Methods 0.000 description 20
- 210000002161 motor neuron Anatomy 0.000 description 20
- 102000004219 Brain-derived neurotrophic factor Human genes 0.000 description 19
- 108090000715 Brain-derived neurotrophic factor Proteins 0.000 description 19
- 241000283707 Capra Species 0.000 description 19
- 229940077737 brain-derived neurotrophic factor Drugs 0.000 description 19
- 230000000946 synaptic effect Effects 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 19
- 230000004064 dysfunction Effects 0.000 description 18
- 229940098773 bovine serum albumin Drugs 0.000 description 17
- 230000001149 cognitive effect Effects 0.000 description 17
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 17
- 239000000203 mixture Substances 0.000 description 17
- 238000007619 statistical method Methods 0.000 description 17
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 16
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 16
- 230000006951 hyperphosphorylation Effects 0.000 description 16
- 230000015654 memory Effects 0.000 description 16
- 238000002360 preparation method Methods 0.000 description 16
- 238000012549 training Methods 0.000 description 16
- 241000699666 Mus <mouse, genus> Species 0.000 description 15
- 208000027418 Wounds and injury Diseases 0.000 description 15
- 230000007812 deficiency Effects 0.000 description 15
- 208000014674 injury Diseases 0.000 description 15
- 230000013016 learning Effects 0.000 description 15
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 14
- 210000003618 cortical neuron Anatomy 0.000 description 14
- 230000002829 reductive effect Effects 0.000 description 14
- 238000010186 staining Methods 0.000 description 14
- 230000003442 weekly effect Effects 0.000 description 14
- 239000003814 drug Substances 0.000 description 13
- 210000001320 hippocampus Anatomy 0.000 description 13
- 235000002639 sodium chloride Nutrition 0.000 description 13
- 230000003931 cognitive performance Effects 0.000 description 12
- 239000003102 growth factor Substances 0.000 description 12
- 102000004169 proteins and genes Human genes 0.000 description 12
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 12
- 206010002091 Anaesthesia Diseases 0.000 description 11
- 102100040347 TAR DNA-binding protein 43 Human genes 0.000 description 11
- 230000037005 anaesthesia Effects 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- 229940079593 drug Drugs 0.000 description 11
- 238000002474 experimental method Methods 0.000 description 11
- 230000014511 neuron projection development Effects 0.000 description 11
- 230000006576 neuronal survival Effects 0.000 description 11
- 108090000623 proteins and genes Proteins 0.000 description 11
- 239000006228 supernatant Substances 0.000 description 11
- 239000012103 Alexa Fluor 488 Substances 0.000 description 10
- 108700019745 Disks Large Homolog 4 Proteins 0.000 description 10
- 102000047174 Disks Large Homolog 4 Human genes 0.000 description 10
- 238000000540 analysis of variance Methods 0.000 description 10
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 10
- 238000011156 evaluation Methods 0.000 description 10
- 230000007787 long-term memory Effects 0.000 description 10
- 230000032405 negative regulation of neuron apoptotic process Effects 0.000 description 10
- 230000001537 neural effect Effects 0.000 description 10
- 230000026731 phosphorylation Effects 0.000 description 10
- 238000006366 phosphorylation reaction Methods 0.000 description 10
- 230000004044 response Effects 0.000 description 10
- 239000000523 sample Substances 0.000 description 10
- 230000007596 spatial working memory Effects 0.000 description 10
- 230000009182 swimming Effects 0.000 description 10
- 230000009471 action Effects 0.000 description 9
- 230000033228 biological regulation Effects 0.000 description 9
- 230000001684 chronic effect Effects 0.000 description 9
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 9
- 201000010099 disease Diseases 0.000 description 9
- 238000011534 incubation Methods 0.000 description 9
- 239000011780 sodium chloride Substances 0.000 description 9
- 239000012109 Alexa Fluor 568 Substances 0.000 description 8
- 102000004142 Trypsin Human genes 0.000 description 8
- 108090000631 Trypsin Proteins 0.000 description 8
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 8
- 208000035475 disorder Diseases 0.000 description 8
- 101150069842 dlg4 gene Proteins 0.000 description 8
- 229960003638 dopamine Drugs 0.000 description 8
- 210000001353 entorhinal cortex Anatomy 0.000 description 8
- 210000005153 frontal cortex Anatomy 0.000 description 8
- 210000001222 gaba-ergic neuron Anatomy 0.000 description 8
- 230000005764 inhibitory process Effects 0.000 description 8
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 8
- 230000016273 neuron death Effects 0.000 description 8
- 239000008188 pellet Substances 0.000 description 8
- 230000008823 permeabilization Effects 0.000 description 8
- 239000012588 trypsin Substances 0.000 description 8
- 208000037259 Amyloid Plaque Diseases 0.000 description 7
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 7
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 7
- 241000282412 Homo Species 0.000 description 7
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 7
- 229930182816 L-glutamine Natural products 0.000 description 7
- 101710150875 TAR DNA-binding protein 43 Proteins 0.000 description 7
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 7
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 7
- 230000007717 exclusion Effects 0.000 description 7
- 239000008103 glucose Substances 0.000 description 7
- 238000012744 immunostaining Methods 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 210000001259 mesencephalon Anatomy 0.000 description 7
- 229920000729 poly(L-lysine) polymer Polymers 0.000 description 7
- 230000035935 pregnancy Effects 0.000 description 7
- 108090000765 processed proteins & peptides Proteins 0.000 description 7
- 230000009467 reduction Effects 0.000 description 7
- 229960005322 streptomycin Drugs 0.000 description 7
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- 229930182555 Penicillin Natural products 0.000 description 6
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 6
- 230000002776 aggregation Effects 0.000 description 6
- 238000004220 aggregation Methods 0.000 description 6
- 208000010877 cognitive disease Diseases 0.000 description 6
- 238000010494 dissociation reaction Methods 0.000 description 6
- 230000005593 dissociations Effects 0.000 description 6
- 231100000673 dose–response relationship Toxicity 0.000 description 6
- 230000003492 excitotoxic effect Effects 0.000 description 6
- 210000003754 fetus Anatomy 0.000 description 6
- 230000002068 genetic effect Effects 0.000 description 6
- 230000036541 health Effects 0.000 description 6
- 229940049954 penicillin Drugs 0.000 description 6
- 230000002269 spontaneous effect Effects 0.000 description 6
- 239000012583 B-27 Supplement Substances 0.000 description 5
- 206010012289 Dementia Diseases 0.000 description 5
- 238000010162 Tukey test Methods 0.000 description 5
- 230000001154 acute effect Effects 0.000 description 5
- 230000003110 anti-inflammatory effect Effects 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 239000008280 blood Substances 0.000 description 5
- 125000001309 chloro group Chemical group Cl* 0.000 description 5
- 229940000406 drug candidate Drugs 0.000 description 5
- 208000025688 early-onset autosomal dominant Alzheimer disease Diseases 0.000 description 5
- 231100000063 excitotoxicity Toxicity 0.000 description 5
- 208000015756 familial Alzheimer disease Diseases 0.000 description 5
- 230000014509 gene expression Effects 0.000 description 5
- 230000000848 glutamatergic effect Effects 0.000 description 5
- 238000010874 in vitro model Methods 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 210000001577 neostriatum Anatomy 0.000 description 5
- 231100000572 poisoning Toxicity 0.000 description 5
- 230000000607 poisoning effect Effects 0.000 description 5
- 230000001105 regulatory effect Effects 0.000 description 5
- 230000000007 visual effect Effects 0.000 description 5
- FUFZNHHSSMCXCZ-UHFFFAOYSA-N 5-piperidin-4-yl-3-[3-(trifluoromethyl)phenyl]-1,2,4-oxadiazole Chemical compound FC(F)(F)C1=CC=CC(C=2N=C(ON=2)C2CCNCC2)=C1 FUFZNHHSSMCXCZ-UHFFFAOYSA-N 0.000 description 4
- 208000000044 Amnesia Diseases 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 206010003694 Atrophy Diseases 0.000 description 4
- 238000001061 Dunnett's test Methods 0.000 description 4
- 206010018341 Gliosis Diseases 0.000 description 4
- 208000006083 Hypokinesia Diseases 0.000 description 4
- 102000004868 N-Methyl-D-Aspartate Receptors Human genes 0.000 description 4
- 108090001041 N-Methyl-D-Aspartate Receptors Proteins 0.000 description 4
- 241000283984 Rodentia Species 0.000 description 4
- 101150014554 TARDBP gene Proteins 0.000 description 4
- 230000004075 alteration Effects 0.000 description 4
- 238000010171 animal model Methods 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 208000037875 astrocytosis Diseases 0.000 description 4
- 230000007341 astrogliosis Effects 0.000 description 4
- 230000037444 atrophy Effects 0.000 description 4
- 230000002490 cerebral effect Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 4
- 238000007405 data analysis Methods 0.000 description 4
- 230000034994 death Effects 0.000 description 4
- 239000006185 dispersion Substances 0.000 description 4
- 230000012010 growth Effects 0.000 description 4
- 238000001802 infusion Methods 0.000 description 4
- 201000010901 lateral sclerosis Diseases 0.000 description 4
- 230000001404 mediated effect Effects 0.000 description 4
- 210000003205 muscle Anatomy 0.000 description 4
- 230000035772 mutation Effects 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 230000001575 pathological effect Effects 0.000 description 4
- 230000007170 pathology Effects 0.000 description 4
- 239000008194 pharmaceutical composition Substances 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 239000008223 sterile water Substances 0.000 description 4
- 230000035882 stress Effects 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 238000011830 transgenic mouse model Methods 0.000 description 4
- 210000004291 uterus Anatomy 0.000 description 4
- FTRZTHFGTILUPE-UHFFFAOYSA-N 1-(4-amino-5-chloro-2-methoxyphenyl)-3-[1-(cyclohexylmethyl)piperidin-4-yl]propan-1-one Chemical compound COC1=CC(N)=C(Cl)C=C1C(=O)CCC1CCN(CC2CCCCC2)CC1 FTRZTHFGTILUPE-UHFFFAOYSA-N 0.000 description 3
- 241000283690 Bos taurus Species 0.000 description 3
- 206010006100 Bradykinesia Diseases 0.000 description 3
- 206010052804 Drug tolerance Diseases 0.000 description 3
- 241000287828 Gallus gallus Species 0.000 description 3
- 102100035902 Glutamate decarboxylase 1 Human genes 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 238000012313 Kruskal-Wallis test Methods 0.000 description 3
- 208000026139 Memory disease Diseases 0.000 description 3
- 208000026072 Motor neurone disease Diseases 0.000 description 3
- 241000699660 Mus musculus Species 0.000 description 3
- 206010029350 Neurotoxicity Diseases 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 206010033799 Paralysis Diseases 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- FTALBRSUTCGOEG-UHFFFAOYSA-N Riluzole Chemical compound C1=C(OC(F)(F)F)C=C2SC(N)=NC2=C1 FTALBRSUTCGOEG-UHFFFAOYSA-N 0.000 description 3
- 206010044221 Toxic encephalopathy Diseases 0.000 description 3
- 208000030886 Traumatic Brain injury Diseases 0.000 description 3
- 230000035508 accumulation Effects 0.000 description 3
- 238000009825 accumulation Methods 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 238000013528 artificial neural network Methods 0.000 description 3
- 230000003542 behavioural effect Effects 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 230000037396 body weight Effects 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 210000005056 cell body Anatomy 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- 239000012228 culture supernatant Substances 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 230000008034 disappearance Effects 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 230000001605 fetal effect Effects 0.000 description 3
- 230000003371 gabaergic effect Effects 0.000 description 3
- BTCSSZJGUNDROE-UHFFFAOYSA-N gamma-aminobutyric acid Chemical compound NCCCC(O)=O BTCSSZJGUNDROE-UHFFFAOYSA-N 0.000 description 3
- 230000026781 habituation Effects 0.000 description 3
- 238000003364 immunohistochemistry Methods 0.000 description 3
- 230000006698 induction Effects 0.000 description 3
- 230000035987 intoxication Effects 0.000 description 3
- 231100000566 intoxication Toxicity 0.000 description 3
- 239000003550 marker Substances 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 208000023060 memory loss Diseases 0.000 description 3
- 230000008450 motivation Effects 0.000 description 3
- 230000003387 muscular Effects 0.000 description 3
- 210000005036 nerve Anatomy 0.000 description 3
- 230000004112 neuroprotection Effects 0.000 description 3
- 230000007135 neurotoxicity Effects 0.000 description 3
- 231100000228 neurotoxicity Toxicity 0.000 description 3
- 238000007474 nonparametric Mann- Whitney U test Methods 0.000 description 3
- 210000004940 nucleus Anatomy 0.000 description 3
- 239000013641 positive control Substances 0.000 description 3
- 230000001144 postural effect Effects 0.000 description 3
- 210000002442 prefrontal cortex Anatomy 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 230000001737 promoting effect Effects 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 210000000278 spinal cord Anatomy 0.000 description 3
- 239000008174 sterile solution Substances 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 210000003523 substantia nigra Anatomy 0.000 description 3
- 230000008719 thickening Effects 0.000 description 3
- JADVWWSKYZXRGX-UHFFFAOYSA-M thioflavine T Chemical compound [Cl-].C1=CC(N(C)C)=CC=C1C1=[N+](C)C2=CC=C(C)C=C2S1 JADVWWSKYZXRGX-UHFFFAOYSA-M 0.000 description 3
- 239000003053 toxin Substances 0.000 description 3
- 230000009529 traumatic brain injury Effects 0.000 description 3
- PLRACCBDVIHHLZ-UHFFFAOYSA-N 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine Chemical compound C1N(C)CCC(C=2C=CC=CC=2)=C1 PLRACCBDVIHHLZ-UHFFFAOYSA-N 0.000 description 2
- 101800000263 Acidic protein Proteins 0.000 description 2
- 206010001541 Akinesia Diseases 0.000 description 2
- 206010003591 Ataxia Diseases 0.000 description 2
- 208000024806 Brain atrophy Diseases 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 206010008025 Cerebellar ataxia Diseases 0.000 description 2
- 101150014889 Gad1 gene Proteins 0.000 description 2
- 208000003098 Ganglion Cysts Diseases 0.000 description 2
- 101000823051 Homo sapiens Amyloid-beta precursor protein Proteins 0.000 description 2
- 101000617536 Homo sapiens Presenilin-1 Proteins 0.000 description 2
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 101100260568 Mus musculus Thy1 gene Proteins 0.000 description 2
- 108010025020 Nerve Growth Factor Proteins 0.000 description 2
- 102000007072 Nerve Growth Factors Human genes 0.000 description 2
- 208000012902 Nervous system disease Diseases 0.000 description 2
- 208000025966 Neurological disease Diseases 0.000 description 2
- 229920005372 Plexiglas® Polymers 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- 102100022033 Presenilin-1 Human genes 0.000 description 2
- 241000288906 Primates Species 0.000 description 2
- 208000010112 Spinocerebellar Degenerations Diseases 0.000 description 2
- 241001661355 Synapsis Species 0.000 description 2
- 102000004874 Synaptophysin Human genes 0.000 description 2
- 108090001076 Synaptophysin Proteins 0.000 description 2
- 208000005400 Synovial Cyst Diseases 0.000 description 2
- 108700019146 Transgenes Proteins 0.000 description 2
- 206010044565 Tremor Diseases 0.000 description 2
- 201000004810 Vascular dementia Diseases 0.000 description 2
- 230000005856 abnormality Effects 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 2
- 230000002528 anti-freeze Effects 0.000 description 2
- 230000001946 anti-microtubular Effects 0.000 description 2
- 230000006907 apoptotic process Effects 0.000 description 2
- 239000012736 aqueous medium Substances 0.000 description 2
- 238000003149 assay kit Methods 0.000 description 2
- 230000000740 bleeding effect Effects 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 235000011089 carbon dioxide Nutrition 0.000 description 2
- 208000025434 cerebellar degeneration Diseases 0.000 description 2
- 230000019771 cognition Effects 0.000 description 2
- 230000008602 contraction Effects 0.000 description 2
- 230000001054 cortical effect Effects 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 239000002612 dispersion medium Substances 0.000 description 2
- 230000009189 diving Effects 0.000 description 2
- 230000003291 dopaminomimetic effect Effects 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- -1 etc. Substances 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 238000007667 floating Methods 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000012737 fresh medium Substances 0.000 description 2
- 229960003692 gamma aminobutyric acid Drugs 0.000 description 2
- 238000003304 gavage Methods 0.000 description 2
- 102000046783 human APP Human genes 0.000 description 2
- 238000000185 intracerebroventricular administration Methods 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 2
- 208000028867 ischemia Diseases 0.000 description 2
- 229960003299 ketamine Drugs 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 230000013011 mating Effects 0.000 description 2
- 230000002438 mitochondrial effect Effects 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 230000000626 neurodegenerative effect Effects 0.000 description 2
- 230000002232 neuromuscular Effects 0.000 description 2
- 239000003900 neurotrophic factor Substances 0.000 description 2
- 230000036542 oxidative stress Effects 0.000 description 2
- DIVDFFZHCJEHGG-UHFFFAOYSA-N oxidopamine Chemical compound NCCC1=CC(O)=C(O)C=C1O DIVDFFZHCJEHGG-UHFFFAOYSA-N 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- 230000000750 progressive effect Effects 0.000 description 2
- 239000000018 receptor agonist Substances 0.000 description 2
- 229940044601 receptor agonist Drugs 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 229960004181 riluzole Drugs 0.000 description 2
- 230000001953 sensory effect Effects 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 239000001488 sodium phosphate Substances 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 230000009897 systematic effect Effects 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 231100000765 toxin Toxicity 0.000 description 2
- 108700012359 toxins Proteins 0.000 description 2
- 238000012762 unpaired Student’s t-test Methods 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- 230000003936 working memory Effects 0.000 description 2
- BPICBUSOMSTKRF-UHFFFAOYSA-N xylazine Chemical compound CC1=CC=CC(C)=C1NC1=NCCCS1 BPICBUSOMSTKRF-UHFFFAOYSA-N 0.000 description 2
- 229960001600 xylazine Drugs 0.000 description 2
- OGNSCSPNOLGXSM-UHFFFAOYSA-N (+/-)-DABA Natural products NCCC(N)C(O)=O OGNSCSPNOLGXSM-UHFFFAOYSA-N 0.000 description 1
- RSDQBPGKMDFRHH-MJVIGCOGSA-N (3s,3as,5ar,9bs)-3,5a,9-trimethyl-3a,4,5,7,8,9b-hexahydro-3h-benzo[g][1]benzofuran-2,6-dione Chemical compound O=C([C@]1(C)CC2)CCC(C)=C1[C@@H]1[C@@H]2[C@H](C)C(=O)O1 RSDQBPGKMDFRHH-MJVIGCOGSA-N 0.000 description 1
- HAFWELDDNUXLCK-TYYBGVCCSA-N (e)-but-2-enedioic acid;hydrate Chemical compound O.OC(=O)\C=C\C(O)=O HAFWELDDNUXLCK-TYYBGVCCSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- 238000010178 5xFAD (B6SJL) Methods 0.000 description 1
- 229940100578 Acetylcholinesterase inhibitor Drugs 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 239000012110 Alexa Fluor 594 Substances 0.000 description 1
- 102100026882 Alpha-synuclein Human genes 0.000 description 1
- 108010090849 Amyloid beta-Peptides Proteins 0.000 description 1
- 102000013455 Amyloid beta-Peptides Human genes 0.000 description 1
- 241000473391 Archosargus rhomboidalis Species 0.000 description 1
- 206010003840 Autonomic nervous system imbalance Diseases 0.000 description 1
- 238000000035 BCA protein assay Methods 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 201000006474 Brain Ischemia Diseases 0.000 description 1
- QKKVJPARHUGCGO-UHFFFAOYSA-N COC(CC(C(CCC1CCN(CC2CCCCC2)CC1)=O)=C1)=CC(N)=C1Cl Chemical compound COC(CC(C(CCC1CCN(CC2CCCCC2)CC1)=O)=C1)=CC(N)=C1Cl QKKVJPARHUGCGO-UHFFFAOYSA-N 0.000 description 1
- RVKSBAURRKECBI-UHFFFAOYSA-N COc(c(C(CCC1CCN(CC2CCCC2)CC1)=O)c1)cc(N)c1Cl Chemical compound COc(c(C(CCC1CCN(CC2CCCC2)CC1)=O)c1)cc(N)c1Cl RVKSBAURRKECBI-UHFFFAOYSA-N 0.000 description 1
- RUCWXMRMXGLFKN-UHFFFAOYSA-N COc(c(C(CCC1CCN(CC2CCNCC2)CC1)=O)c1)cc(N)c1Cl Chemical compound COc(c(C(CCC1CCN(CC2CCNCC2)CC1)=O)c1)cc(N)c1Cl RUCWXMRMXGLFKN-UHFFFAOYSA-N 0.000 description 1
- 0 COc(cc(CC(CC1CC*(Cc2ccccc2)CC1)C1=O)c1c1)c1OC Chemical compound COc(cc(CC(CC1CC*(Cc2ccccc2)CC1)C1=O)c1c1)c1OC 0.000 description 1
- HKRQNSWIPOUSMA-UHFFFAOYSA-N COc(cc(c(F)c1)N)c1C(CCC1CCN(CC2CCCCCC2)CC1)=O Chemical compound COc(cc(c(F)c1)N)c1C(CCC1CCN(CC2CCCCCC2)CC1)=O HKRQNSWIPOUSMA-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 102000007590 Calpain Human genes 0.000 description 1
- 108010032088 Calpain Proteins 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 102000003952 Caspase 3 Human genes 0.000 description 1
- 108090000397 Caspase 3 Proteins 0.000 description 1
- 108010076667 Caspases Proteins 0.000 description 1
- 102000011727 Caspases Human genes 0.000 description 1
- 206010008120 Cerebral ischaemia Diseases 0.000 description 1
- 208000028698 Cognitive impairment Diseases 0.000 description 1
- 102000010831 Cytoskeletal Proteins Human genes 0.000 description 1
- 108010037414 Cytoskeletal Proteins Proteins 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 102000052510 DNA-Binding Proteins Human genes 0.000 description 1
- 101710096438 DNA-binding protein Proteins 0.000 description 1
- 208000019505 Deglutition disease Diseases 0.000 description 1
- 102000007260 Deoxyribonuclease I Human genes 0.000 description 1
- 108010008532 Deoxyribonuclease I Proteins 0.000 description 1
- 208000035859 Drug effect increased Diseases 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 206010017577 Gait disturbance Diseases 0.000 description 1
- 101000979001 Homo sapiens Methionine aminopeptidase 2 Proteins 0.000 description 1
- 101000969087 Homo sapiens Microtubule-associated protein 2 Proteins 0.000 description 1
- 101100192145 Homo sapiens PSEN1 gene Proteins 0.000 description 1
- 101000801254 Homo sapiens Tumor necrosis factor receptor superfamily member 16 Proteins 0.000 description 1
- 208000004044 Hypesthesia Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- ZRVUJXDFFKFLMG-UHFFFAOYSA-N Meloxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=NC=C(C)S1 ZRVUJXDFFKFLMG-UHFFFAOYSA-N 0.000 description 1
- 102000008109 Mixed Function Oxygenases Human genes 0.000 description 1
- 108010074633 Mixed Function Oxygenases Proteins 0.000 description 1
- 238000012347 Morris Water Maze Methods 0.000 description 1
- 208000016285 Movement disease Diseases 0.000 description 1
- 208000002740 Muscle Rigidity Diseases 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- 208000029955 Nervous System Heredodegenerative disease Diseases 0.000 description 1
- 208000001738 Nervous System Trauma Diseases 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 1
- 101710138657 Neurotoxin Proteins 0.000 description 1
- 102000043141 Nuclear RNA Human genes 0.000 description 1
- 108020003217 Nuclear RNA Proteins 0.000 description 1
- 240000007817 Olea europaea Species 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 208000027089 Parkinsonian disease Diseases 0.000 description 1
- 206010034010 Parkinsonism Diseases 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 229920000776 Poly(Adenosine diphosphate-ribose) polymerase Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 108010039918 Polylysine Proteins 0.000 description 1
- 108010036933 Presenilin-1 Proteins 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 102000004245 Proteasome Endopeptidase Complex Human genes 0.000 description 1
- 108090000708 Proteasome Endopeptidase Complex Proteins 0.000 description 1
- 108010090931 Proto-Oncogene Proteins c-bcl-2 Proteins 0.000 description 1
- 230000004570 RNA-binding Effects 0.000 description 1
- 208000010476 Respiratory Paralysis Diseases 0.000 description 1
- 108091027981 Response element Proteins 0.000 description 1
- 206010071390 Resting tremor Diseases 0.000 description 1
- 206010042674 Swelling Diseases 0.000 description 1
- RSDQBPGKMDFRHH-UHFFFAOYSA-N Taurin Natural products C1CC2(C)C(=O)CCC(C)=C2C2C1C(C)C(=O)O2 RSDQBPGKMDFRHH-UHFFFAOYSA-N 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 102100033725 Tumor necrosis factor receptor superfamily member 16 Human genes 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 108090000185 alpha-Synuclein Proteins 0.000 description 1
- 108010064397 amyloid beta-protein (1-40) Proteins 0.000 description 1
- 230000036592 analgesia Effects 0.000 description 1
- 210000003484 anatomy Anatomy 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000002424 anti-apoptotic effect Effects 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000003460 anti-nuclear Effects 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 239000003048 aphrodisiac agent Substances 0.000 description 1
- 230000002509 aphrodisiac effect Effects 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 208000030137 articulation disease Diseases 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 210000004227 basal ganglia Anatomy 0.000 description 1
- 108700041737 bcl-2 Genes Proteins 0.000 description 1
- 230000006736 behavioral deficit Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 108091008324 binding proteins Proteins 0.000 description 1
- 238000012742 biochemical analysis Methods 0.000 description 1
- 229920002988 biodegradable polymer Polymers 0.000 description 1
- 239000004621 biodegradable polymer Substances 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 239000005388 borosilicate glass Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 235000011148 calcium chloride Nutrition 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000006721 cell death pathway Effects 0.000 description 1
- 210000003855 cell nucleus Anatomy 0.000 description 1
- 210000001638 cerebellum Anatomy 0.000 description 1
- 206010008118 cerebral infarction Diseases 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000000544 cholinesterase inhibitor Substances 0.000 description 1
- 210000003703 cisterna magna Anatomy 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000003920 cognitive function Effects 0.000 description 1
- 230000007370 cognitive improvement Effects 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000006059 cover glass Substances 0.000 description 1
- 210000003792 cranial nerve Anatomy 0.000 description 1
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000001120 cytoprotective effect Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000003412 degenerative effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 238000013400 design of experiment Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 230000009429 distress Effects 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 210000001951 dura mater Anatomy 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000008482 dysregulation Effects 0.000 description 1
- 230000003503 early effect Effects 0.000 description 1
- 230000008451 emotion Effects 0.000 description 1
- 230000002996 emotional effect Effects 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 239000008393 encapsulating agent Substances 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 231100000318 excitotoxic Toxicity 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 210000003414 extremity Anatomy 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000002518 glial effect Effects 0.000 description 1
- 210000001905 globus pallidus Anatomy 0.000 description 1
- 239000003292 glue Substances 0.000 description 1
- 108010024847 glutamate decarboxylase 1 Proteins 0.000 description 1
- 239000003823 glutamate receptor agonist Substances 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 229960004198 guanidine Drugs 0.000 description 1
- PJJJBBJSCAKJQF-UHFFFAOYSA-N guanidinium chloride Chemical compound [Cl-].NC(N)=[NH2+] PJJJBBJSCAKJQF-UHFFFAOYSA-N 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- 210000000548 hind-foot Anatomy 0.000 description 1
- 102000055060 human PSEN1 Human genes 0.000 description 1
- 208000034783 hypoesthesia Diseases 0.000 description 1
- 230000003483 hypokinetic effect Effects 0.000 description 1
- 230000002055 immunohistochemical effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 239000003978 infusion fluid Substances 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 208000030309 inherited neurodegenerative disease Diseases 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 229940102223 injectable solution Drugs 0.000 description 1
- 210000001153 interneuron Anatomy 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 230000003447 ipsilateral effect Effects 0.000 description 1
- 208000037906 ischaemic injury Diseases 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 210000003140 lateral ventricle Anatomy 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 231100000863 loss of memory Toxicity 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 235000011147 magnesium chloride Nutrition 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 210000001767 medulla oblongata Anatomy 0.000 description 1
- 206010027175 memory impairment Diseases 0.000 description 1
- 230000006993 memory improvement Effects 0.000 description 1
- 230000007334 memory performance Effects 0.000 description 1
- 229940001676 metacam Drugs 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 239000003094 microcapsule Substances 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 230000006676 mitochondrial damage Effects 0.000 description 1
- 230000004065 mitochondrial dysfunction Effects 0.000 description 1
- 230000003990 molecular pathway Effects 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 229910000403 monosodium phosphate Inorganic materials 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 230000037023 motor activity Effects 0.000 description 1
- 208000022084 motor paralysis Diseases 0.000 description 1
- 208000028412 nervous system injury Diseases 0.000 description 1
- 210000004498 neuroglial cell Anatomy 0.000 description 1
- 230000003959 neuroinflammation Effects 0.000 description 1
- 230000007991 neuronal integrity Effects 0.000 description 1
- 230000002981 neuropathic effect Effects 0.000 description 1
- 239000002581 neurotoxin Substances 0.000 description 1
- 231100000618 neurotoxin Toxicity 0.000 description 1
- 230000000508 neurotrophic effect Effects 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 231100000862 numbness Toxicity 0.000 description 1
- 210000000956 olfactory bulb Anatomy 0.000 description 1
- 210000002475 olfactory pathway Anatomy 0.000 description 1
- 210000004248 oligodendroglia Anatomy 0.000 description 1
- 210000004205 output neuron Anatomy 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000004792 oxidative damage Effects 0.000 description 1
- 208000021090 palsy Diseases 0.000 description 1
- 206010033675 panniculitis Diseases 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000007331 pathological accumulation Effects 0.000 description 1
- 230000007310 pathophysiology Effects 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000011458 pharmacological treatment Methods 0.000 description 1
- 230000036314 physical performance Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 230000007505 plaque formation Effects 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920000656 polylysine Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 230000008092 positive effect Effects 0.000 description 1
- 230000029279 positive regulation of transcription, DNA-dependent Effects 0.000 description 1
- 231100000683 possible toxicity Toxicity 0.000 description 1
- 230000001242 postsynaptic effect Effects 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 230000003518 presynaptic effect Effects 0.000 description 1
- 230000000861 pro-apoptotic effect Effects 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 230000007425 progressive decline Effects 0.000 description 1
- 230000004224 protection Effects 0.000 description 1
- 230000004845 protein aggregation Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 229940072169 rilutek Drugs 0.000 description 1
- 229940080817 rotenone Drugs 0.000 description 1
- JUVIOZPCNVVQFO-UHFFFAOYSA-N rotenone Natural products O1C2=C3CC(C(C)=C)OC3=CC=C2C(=O)C2C1COC1=C2C=C(OC)C(OC)=C1 JUVIOZPCNVVQFO-UHFFFAOYSA-N 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 230000006403 short-term memory Effects 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 208000019116 sleep disease Diseases 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 210000004304 subcutaneous tissue Anatomy 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 230000008184 synaptic development Effects 0.000 description 1
- 230000003956 synaptic plasticity Effects 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 210000001103 thalamus Anatomy 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 230000002861 ventricular Effects 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/08—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms
- C07D211/18—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms
- C07D211/30—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms with hydrocarbon radicals, substituted by doubly bound oxygen or sulfur atoms or by two oxygen or sulfur atoms singly bound to the same carbon atom
- C07D211/32—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon or substituted hydrocarbon radicals directly attached to ring carbon atoms with substituted hydrocarbon radicals attached to ring carbon atoms with hydrocarbon radicals, substituted by doubly bound oxygen or sulfur atoms or by two oxygen or sulfur atoms singly bound to the same carbon atom by oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Veterinary Medicine (AREA)
- Biomedical Technology (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Hospice & Palliative Care (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Psychiatry (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
Xは、
水素原子を表し、又は
ハロゲン原子(Hal)を表し、ここで(Hal)はフッ素、塩素、臭素若しくはヨウ素であり、又は
直鎖若しくは分枝鎖のCp(Hal)2p+1ポリハロゲン化アルキル(polyhalogenoalkyl)基を表し、ここでp=1、2、3又は4であり、(Hal)は上記に示されているのと同じ意味を有し、
Yは、
酸素原子を表し、又は
硫黄原子を表し、又は
N-R"基を表し、ここでR"は、水素原子、-OH基、-O-A基(ここでAは、直鎖又は分枝鎖のC1~C6アルキル基を表し、特にAは、メチル基を表し)、又は直鎖若しくは分枝鎖のCqH2q+1アルキル基を表し、q=1、2、3又は4であり、
mは、1、2及び3から選択される整数であり、
nは、0、1、2及び3から選択される整数であり、
r及びsは、その値が、r=s=0、又はr=s=1、又はr=s=2、又はr=0及びs=1、又は最後にr=0及びs=2である整数であり、
Rは、
水素原子、又は
1個若しくは複数のF原子を有することが可能な直鎖若しくは分枝鎖のC1~C5アルキル基を表し、
R'は、
分枝鎖C1~C6アルキル基、或いは
1つ若しくは複数のR基を有すること及び酸素原子、又はRで置換されていてもよい窒素原子、又は硫黄原子、又は-SO2-基若しくは-SO-基を保有することが可能なC3~C10シクロアルキル又はC5~C13二環式基を表す)
並びにそのエナンチオマー又はジアステレオ異性体及びそのラセミ体、その酸との塩、その水和物又はその溶媒和生成物に関する。
本発明との関連で使用される化合物は、以下の式(I)の化合物:
Xは、
水素原子を表し、又は
ハロゲン原子(Hal)を表し、ここで(Hal)はフッ素、塩素、臭素若しくはヨウ素であり、又は
直鎖若しくは分枝鎖のCp(Hal)2p+1ポリハロゲン化アルキル基を表し、ここでp=1、2、3又は4であり、(Hal)は上記に示されているのと同じ意味を有し、
Yは、
酸素原子を表し、又は
硫黄原子を表し、又は
N-R"基を表し、ここでR"は、水素原子、-OH基、-O-A基(ここでAは、直鎖又は分枝鎖のC1~C6アルキル基を表し、特にAは、メチル基を表す)、又は直鎖若しくは分枝鎖のCqH2q+1アルキル基を表し、q=1、2、3又は4であり、
mは、1、2及び3から選択される整数であり、
nは、0、1、2及び3から選択される整数であり、
r及びsは、その値が、r=s=0、又はr=s=1、又はr=s=2、又はr=0及びs=1、又は最後にr=0及びs=2である整数であり、
Rは、
水素原子、又は
1個若しくは複数のF原子を有することが可能な直鎖若しくは分枝鎖のC1~C5アルキル基を表し、
R'は、
分枝鎖C1~C6アルキル基、或いは
1つ若しくは複数のR基を有すること及び酸素原子、又はRで置換されていてもよい窒素原子、又は硫黄原子、又は-SO2-基若しくは-SO-基を保有することが可能なC3~C10シクロアルキル又はC5~C13二環式基を表す)
並びにそのエナンチオマー又はジアステレオ異性体及びそのラセミ体、その酸との塩、その水和物又はその溶媒和生成物である。
酸素原子を表し、又は
硫黄原子を表し、又は
N-R”基を表し、ここでR”は、水素原子、-OH基、又は直鎖若しくは分枝鎖のCqH2q+1アルキル基を表し、q=1、2、3又は4である。
「神経変性疾患」とは、神経細胞の系統的変性及び脱落に基づく、神経回路の神経ネットワークの崩壊により誘発される疾患を本明細書で意味する。
本発明は、上記「神経変性疾患」のセクションで定義されている神経変性疾患の予防及び/又は処置における神経保護剤としての使用のための、上記「化合物」のセクションで定義されている化合物に関する。
この実施例は、Aβで損傷した(24時間曝露)ラット初代海馬ニューロンにおけるドネコプリドの作用を示すものである。
〔海馬ニューロンの初代培養物〕
ラットの海馬ニューロンをCallizotら (2013) J. Neurosci. Res. 91:706~716頁に記載されている通り培養した。妊娠第17日の妊娠した雌のラット(Rats Wistar;Janvier Labs社、France)を、CO2チャンバーでの深麻酔、これに続く頸部脱臼を使用して屠殺した。次いで、胎児を子宮から取り出し、2 %ペニシリン(10,000 U/ml)及びストレプトマイシン(10 mg/ml)溶液(PS)及び1 %ウシ血清アルブミン(BSA)を有する、氷冷したL15 Leibovitz培地内に直ちに配置した。海馬ニューロンを、37℃で20分間、0.05 %トリプシン及び0.02 %EDTAの最終濃度のトリプシン-EDTA溶液で処理した。DNAse I グレードII(最終濃度0.5 mg/ml)及び10 %ウシ胎児血清(FCS)を含有する、4.5 g/lのグルコースを有するダルベッコ改変イーグル培地(DMEM)の添加により、解離を停止した。10 mlピペットの先端を介した3回の強制的通過により細胞を機械的に解離し、次いで515×gで、4℃で10分間遠心分離した。上清を廃棄し、B27サプリメントの2 %溶液を有するNeurobasal培地、2 mmol/lのL-グルタミン、2 %PS溶液、及び10 ng/mlの脳由来の神経栄養因子(BDNF)からなる規定の培養用培地にペレットを再懸濁した。トリパンブルー排除試験を使用して、生存細胞をNeubauerサイトメーターでカウントした。ポリ-L-リジンをプレコートした96ウェルプレート内に、1ウェル当たり20,000個の密度で細胞を播種し、大気(95 %)-CO2(5 %)インキュベーター内で、37℃で培養した。培地は2日ごとに交換した。
17日間の培養後、海馬ニューロンをAβ溶液(以下を参照されたい)に曝露した。Aβ1-42調製は、Callizotら (2013) J. Neurosci. Res. 91:706~716頁に記載されている手順に従い行った。簡単に説明すると、Aβ1-42ペプチドを上述の規定の培養用培地に初濃度40μMで溶解した。この溶液を暗所で、37℃で3日間穏やかに撹拌し、培養用培地内で使用される濃度へと適切に希釈した直後使用した(2μM又は0.25μMのオリゴマー(AβO)にそれぞれ対応する20μM(プレート1)又は2.5μM(プレート2))。
1種の培養物に対して、96ウェルプレート(1条件当たり6つのウェル)内でドネコプリドフマレート(ドネコプリド)を試験した。Aβ適用の1時間前に、化合物を予備インキュベートした。以下の条件を評価した:
[プレート1:生存、神経突起ネットワーク及びホスホタウ評価]
被毒させてから24時間後、海馬ニューロンをエタノール(95 %)及び酢酸(5 %)の冷たい溶液で、-20℃で5分間固定した。0.1 %のサポニンで透過化後、細胞を以下と共に2時間インキュベートした:
a) 1 %ウシ胎児血清及び0.1 %のサポニンを含有するPBS中、1/1000希釈でのニワトリポリクローナル抗体抗微小管関連タンパク質2(MAP-2)(この抗体は、神経細胞体及び神経突起の特異的染色を可能にし、神経細胞の死及び神経突起ネットワークの研究を可能にする)。
b) 1 %ウシ胎児血清及び0.1 %のサポニンを含有するPBS中、1/400希釈でのマウスモノクローナル抗体抗ホスホタウ(AT100)。
- ニューロンの総数(ニューロン生存、MAP-2陽性ニューロンの数)
- 神経突起ネットワーク(MAP-2陽性ニューロン、単位:μm)
- ニューロン内のタウの領域(μm2、MAP-2陽性ニューロンとの重複)。
被毒させてから24時間後、海馬ニューロンをエタノール(95 %)及び酢酸(5 %)の冷たい溶液で-20℃で、5分間固定した。0.1 %のサポニンで透過化後、細胞を以下と共に2時間インキュベートした:
a) 1 %ウシ胎児血清及び0.1 %のサポニンを含有するPBS中、1/100希釈でのマウスモノクローナル抗体抗シナプス後肥厚95 kDa(PSD95)。
b) 1 %ウシ胎児血清及び0.1 %のサポニンを含有するPBS中、1/100希釈でのウサギポリクローナル抗体抗シナプトフィジン(SYN)。
- シナプスの総数(PSD95/SYNの間で重複)。
すべての値は平均値+/-SEMとして表現される。一元ANOVAにより統計分析を実施し、これに続いてフィッシャーのPLSD検定を実施した。p<0.05は有意であると考えられた。
MAP-2海馬ニューロンの生存及び神経突起ネットワーク及びタウの過剰リン酸化に対するドネコプリドの作用。
海馬ニューロンの初代培養物における、MAP-2ニューロンの生存に対するドネコプリドの作用が以下の表1に示されている。
海馬ニューロンの初代培養物における、MAP-2ニューロンの神経突起ネットワークに対するドネコプリドの作用が以下の表2に示されている。
海馬ニューロンの初代培養物におけるMAP-2ニューロンのタウ(AT100)のリン酸化に対するドネコプリドの作用が以下の表4に示されている。
シナプスの形成を評価するため、シナプス後マーカーPSD-95、及びシナプス前マーカーシナプトフィジンの分布を研究した。PSD-95とシナプトフィジン染色の両方に対して陽性の構造をシナプスと考えた。
本研究は、ドネコプリドがアルツハイマー病のin vitroモデルである、Aβ1-42ペプチドで損傷した海馬ニューロンの生存及び神経突起ネットワークに対して有益な作用を有することを示唆している。
本実施例は、本発明の化合物が、in vivoモデルのAD/sにおいてマウスの認知パフォーマンスを改善することができることを実証するものである。
簡単に説明すると、144C57Bl6/J雄のマウス(月齢3カ月)を納入してもらい、7日間又はそれよりも長く隔離して飼育した(1ケージ当たり4~5匹)。試験品目は1日1回異なる濃度で、-1日から+17日まで経口投薬した(強制経口投与を介して)。
研究は、1実験群当たり12匹のマウスを有する12の実験群に分割した合計144匹のマウスを含んだ。すべての動物にビヒクル又はAβOの単一(及び片側のみの)icv注射、総量1μLを行った。
・ 群A (ビヒクルCTRL):poビヒクル及びビヒクルのicv注射 (n=12)
・ 群B (AβO CTRL):poビヒクル及びAβOのicv注射(n=12)
・ 群C (陽性CTRL):poドネペジル亜慢性及びAβOのicv注射(n=12)
・ 群D (ドネコプリドCTRL):poドネコプリド (9 mg/kg)及びビヒクルのicv注射 (n=12)
・ 群E (フルコプリドCTRL):poフルコプリド (9 mg/kg)及びビヒクルのicv注射 (n=12)
・ 群F (ドネコプリドで処置):poドネコプリド (1 mg/kg) 及びAβOのicv注射 (n=12)
・ 群G (ドネコプリドで処置):poドネコプリド (3 mg/kg) 及びAβOのicv注射 (n=12)
・ 群H (ドネコプリドで処置):poドネコプリド (9 mg/kg) 及びAβOのicv注射 (n=12)
・ 群I (フルオコプリドで処置):poフルコプリド(1 mg/kg) 及びAβOのicv注射(n=12)
・ 群J (フルコプリドで処置):poフルコプリド (3 mg/kg) 及びAβOのicv注射 (n=12)
・ 群K (フルコプリドで処置):poフルコプリド (9 mg/kg) 及びAβOのicv注射 (n=12)
・ 群L (陽性CTRL):試験日にipドネペジル急性及びAβOのicv注射 (n=12)
〔動物住居〕
144 1C57Bl6/J雄の(Janvier社、France)マウス(月齢3カ月)の受理。納入されたら、動物を7日間、又はそれよりも長く隔離した。
0.9 %NaClに溶解することにより、経口投薬用に、ドネコプリド及びフルコプリドを製剤化した。疾患の誘導 (AβOのicv注射を介した) の1日前に化合物投薬(総量200μL)を開始し、19日連続して投薬を行った。
<マウス144匹のビヒクル又はAβOの単一脳室内注射 (1日当たり最大24匹のマウス、すべてのマウスは無作為抽出した)>:麻酔下 (ケタミン/キシラジン混合物のそれぞれ110及び15 mg/kgの用量でのip注射)、AβO(1μL)、又はビヒクル (1μL) を右の側脳室に注射した。注射は、26ゲージ針を装着した10μLのHamiltonミクロシリンジを使用して行った。手順は、5 mg/kgの用量のメタカム (鎮痛) の皮下注射で終結した。次いで、動物をこれらのホーム-ケージに個々に配置し、動物が完全に回復するまで、ケージを温めたキャビネット内に配置した。動物を慎重にモニターして、麻酔後の回復を制御した。
各24匹のマウス (すなわち各実験群からマウス2匹)、合計144匹のマウスが+4日において関与する6つの独立したトライアル - 行動試験を投薬の1時間後に実施した。
各24匹のマウス (すなわち各実験群からマウス2匹)、合計144匹のマウスが+4日において関与する6つの独立したトライアル - 投薬から1時間後に行動試験を実施した。
各24マウス(すなわち各実験群からマウス2匹)、合計144匹のマウスが+4日において関与する6つの独立したトライアル。
マウスを+17日に屠殺した。
〔空間作業記憶に対する本発明の化合物の作用〕
ビヒクル又はAβOのいずれかのicv注射の4日後、マウスの空間作業記憶に対するドネコプリド及びフルコプリドの作用を決定するため、Y迷路試験を実施した。5分間トライアルの間、動物はY迷路デバイスを探索させ、実験手順に記載されている通り、交替行動を採点した。
本発明の化合物の学習能力及び長期記憶に対する作用を決定するため、MWM試験を、ビヒクル又はAβOのいずれかのicv注射の+3~+14日後に実施した。
第1ステップにおいて (ビヒクル又はAβOのicv点滴の+3日及び+4日後に馴化トライアルを実施した)、他の視覚的手がかりの不在下で、水から可視プラットフォームへと脱出するためにマウスを訓練した。これらのトライアルの間、逃避潜時、遊泳距離及び遊泳スピードを記録した。逃避潜時において群間の有意な差異はなかった。遊泳スピード又は遊泳距離における差異は検出されなかった。
マウスの学習能力を5日間連続してモニターした (ビヒクル又はAβOのicv点滴の+7日から+11日後)。動物には、1日当たり4回のトライアルを実施し、視覚的手がかりを使用して、隠されたプラットフォームを突き止めるよう訓練した。これらの学習トライアルの間、逃避潜時、遊泳距離及び遊泳スピードを記録した。
最後のトレーニングセッションから4日後及びビヒクル又はAβOのicv注射から14日後に長期記憶パフォーマンスを決定した。プラットフォームを取り除き、各動物を60秒間遊泳させた。プローブトライアルの間、プールの様々な四分円の中で費やした時間、以前のプラットフォームの場所を横断した数及び最初の横断の時間(すなわち標的に対する反応潜時)を決定した。プローブトライアルの間、遊泳スピードの差異は群間で観察されず、正常な物理的能力及びモチベーションを示した。
認識記憶に対する試験項目の作用を決定するため、ビヒクル又はAβOのいずれかのicv注射から16日後、NOR試験を実施した。行動トライアルは、実験手順に記載されている通り実施した。
全体で、これらのデータはドネコプリド及びフルコプリドの両方がAβOを投与したマウスの認知パフォーマンスを改善させたことを強く示唆している。
本実施例は、アルツハイマー病の5XFADマウスモデルへの慢性投与において、ドネコプリド及びフルコプリドの抗記憶喪失、抗アミロイド及び抗炎症性作用を示すものである。
この研究の目的は、アルツハイマー病のマウスモデルにおける慢性投与において、ドネコプリド及びフルコプリドの潜在的な抗記憶喪失、抗アミロイド及び抗炎症性作用を評価することであった。
〔マウス〕
動物実験は、1986年11月24日の欧州共同体理事会 (the Council of the European Communities) による指令 (86/609/EEC) に従い行った。動物の苦痛を最小化し、使用するマウスの数を減少させるようあらゆる努力を払った。5XFADマウスの生成はOakleyら (2006) J. Neurosci. 26:10129~10140頁に記載されている。これらのトランスジェニックマウスは、スウェーデン (K670N、M671L)、フロリダ (I716V) 及びロンドン (V717I) の家族性AD (FAD) 突然変異を持つヒトAPP(695)と、2つのFAD突然変異M146L及びL286Vを持つヒトプレセニリン1 (PS1) の両方を過剰発現する。両方の導入遺伝子の発現は、マウスThy1プロモーターのニューロン特異的エレメントにより調節される。5XFAD系統(B6/SJL遺伝的バックグラウンド)は、半接合体トランスジェニックマウスをB6/SJL F1ブリーダーと交配することにより維持された。5XFAD系統 (C57BL/6J遺伝的バックグラウンド) は、半接合体トランスジェニックマウスをC57BL/6J F1ブリーダーと交配することにより維持された。すべての動物は、テールゲノムDNAを使用したPCRにより遺伝子型を決定した。トランスジェニック及びWTマウスを発明者らの動物施設内で飼育し、食物及び水を自由に摂取させ、12時間の明暗サイクル下、22~24℃で飼育した。雌の5XFADマウスをこの研究に使用した。各実験に対して、マウスの年齢は月で示される(2週間区切りで)。
ドネコプリド (ドネコプリドフマレート、MR31155) 及びフルコプリド (フルコプリドフマレート、MR31193) は、CERMN、Caen、Franceにおいて合成された。
5XFADマウスは、2つの異なるプロトコルに従い、薬物又はビヒクルで慢性的処置を施した。各実験では、薬物又はビヒクル溶液を週2回i.p.投与した (1 mg/kg)。「プロトコル1」では、マウス (n=1群当たり6~7匹のマウス) は、月齢2カ月から4カ月まで2カ月間化合物で処置した。「プロトコル2」では、マウス (n=7) は、月齢1カ月から4カ月まで3カ月間化合物で処置した。各プロトコルの終わりに、マウスを100 mg/kgケタミン及び10 mg/kgキシラジンの生理食塩水中混合物で麻酔下におき、PBSを経心灌流した。脳を氷上にすばやく単離し、嗅球及び小脳を取り除き、2つの脳半球を分割した。一方の脳半球をドライアイス上で凍結し、生化学的分析用に-80℃で貯蔵し、他方は免疫組織化学法(IHC)用に4 %PFA中に後固定した。
マウスを麻酔下におき、定位固定装置に載せた。頸部皮膚を切り取り、ミクロリトラクター (Fine Science Tools社、Heidelberg、Germany) の助けを受けて皮下組織及び筋肉を分離した。次いで、マウスを寝かせて、身体に対して頭部が約135°の角度を形成するように置いた (Liu及びDuff (2008) J. Vis. Exp. 10:960頁)。キャピラリーチューブ (ボロシリケートガラス、B100-75-10、Sutter Instruments社、Novato、California、USA) を使用して、大槽の硬膜に穴を開けた。キャピラリー作用によりCSFを収集し、0.5 mLミクロチューブに移し、直ちにドライアイス上で凍結し、使用時まで-80℃で貯蔵した。解凍したら、国際出願WO2008/009868号に記載されている通り、試料を60℃で5分間加熱し、さらなる冷凍-解凍サイクルなしに分析した。
5XFADマウス及び対照の脳の脳半球、前頭皮質及び海馬を解凍し、秤量し、プロテアーゼ阻害剤カクテル (Roche Applied Science社、Meylan、France) を有する4容量のトリス-生理食塩水 (50 mM トリス-HCl pH=7.4、150 mM NaCl) 中でホモジナイズした。生成したホモジネートを54,000×gで20分間遠心分離し、上清 (「可溶性画分」) を収集し、貯蔵用に-80℃でアリコートした。短い超音波処理で、50 mM トリス-HCl、pH=7.6中の10容量の6MグアニジンHClにペレットを再懸濁させ、再度26,500×gで20分間遠心分離した。上清 (「不溶性画分」) をアリコートし、-80℃で貯蔵した (Morishima-Kawashimaら (2000) Am. J. Pathol. 157:2093~2099頁)。
Aβ40 (ヒトアミロイドβ(1-40)アッセイキット、#27713) 又はAβ42 (ヒトアミロイドβ(1-42)アッセイキット、#27719) の投与のためのIBL International (Hamburg、Germany) 製ELISAキットを製造者の指示書に従い使用した。Infinite 2000ルミネセンスカウンターを使用して、反応を620 nm及び450 nmで読み取った。入手した値を各試料のタンパク質濃度に正規化し、BCAタンパク質アッセイ (Sigma-Aldrich) を使用して測定した。
ビブラトーム (Microm HM 650V、Thermo Scientific社、Saint Herblain、France)を使用して30マイクロメートルの厚さの切片を切り取り、凍結防止剤培地内で、-20℃で貯蔵した。アミロイド斑の標識のため、前頭皮質、海馬及び嗅内皮質の浮遊性組織切片 (ブレグマからの座標:前頭皮質=1.98 mm、海馬=-1.94 mm、嗅内皮質=-3.08 mm) をPBS中で十分に洗浄し、次いでブロッキング溶液 (PBS;3 %BSA;0.1 %Triton X-100)中で1時間インキュベートした。切片を、細胞核を検出するためにHoechst色素 (1:1000、Life Technologies社、Saint Aubin、France) で15分間染色して、次いで新たに調製したチオフラビンT溶液 (#T3516-5G、Sigma-Aldrich) (最終濃度:ブロッキング緩衝液中0.01 mg/ml) で15分間染色した。70 %エタノール中で5分間洗浄後、試料を、カバーガラスを有するポリ-リジンスライド上にマウントした。GFAP (グリア細胞繊維性酸性タンパク質) 染色のため、浮遊性脳切片を前の通りブロッキングし、ポリクローナルウサギ抗GFAP (1:1000、Z0334、Dako社、Les Ullis、France) と共に4℃で終夜インキュベートした。チオフラビンT染色及び70 %エタノールでの洗浄後、2次Alexafluor 594ヤギ抗ウサギ抗体 (1:1000、A11012、Life Technologies社) を2時間の間加えた。PBS洗浄及びマウンティングを前に記載された通り実施した。
AxioImager Z1顕微鏡 (Carl Zeiss S.A.S.社、Marly le Roi、France) を用いて画像を取得した。チオフラビンT染色の分析を無分別に実施した。データは、同じ脳領域/動物からの2~3枚の組織切片中の1 mm2当たりの粒子の平均数として提示される (Image Jソフトウエア)。Image Jソフトウエアを使用してGFAP発現を定量化し、結果を面積率として表現する。
新奇物体認識 (NOR) 試験を使用して、マウスの認知パフォーマンスを試験した (Bevins及びBesheer (2006) Nat. Protoc. 1:1306~1311頁)。試験開始前の薬物処置中、動物には十分に注意を払った。マウスは、毎日試験の少なくとも1時間前には試験部屋に慣らした。試験は、薄暗い明かりの部屋の中に配置されたPlexiglasボックス (幅:35 cm、長さ:20 cm、高さ:20 cm) 内で行った。第1日及び第2日には、各マウスを空のボックスに10分/日慣らした。第3日には、2つの物体 (プラスチックのおもちゃで作られたもの)をケージ内、向かいの壁から5 cm離して配置した。トレーニングセッション中、各動物を壁に向いている2つの物体の間に配置し、次いで5分間物体を探索させた。次いで、マウスをこれらのホームケージに戻し、24時間後に5分間の試験セッションを行い、このセッションでは2つの(馴染みのある)物体のうちの1つを新しい(新奇の)ものに置き換えた。全体の実験をビデオに記録し、物体探索 [マウスの鼻を物体に接触させることで費やした時間又は≦1 cmの距離でにおいを嗅ぐことにより費やした時間] を無分別に測定した。2つのパラメーターが考えられた:試験中の全探索時間 ([新奇/(馴染みのある+新奇)]×100) に対して、1) トレーニングセッション中、動物が2つの馴染みのある物体と触れ合うことに費やした探索時間(秒)、及び2) 動物が新奇の物体と触れ合うことに費やした探索時間。識別指数もまた計算した ([新奇-馴染みのある]/[馴染みのある+新奇])。
すべての値は平均±SEMとして表現される。処置の有意な作用を、複数の比較群の事例において、ANOVA分析これに続くテューキーのポストホック検定で決定した。他のすべての事例では、不対スチューデントのt検定を使用した。すべての統計試験に対して、P<0.05が有意であると考えられた。分析はGraphPad Prism 7 (GraphPad Software社、La Jolla、CA) で実施した。
〔5XFAD脳におけるアミロイド負荷に対するドネコプリド及びフルコプリドの作用〕
27匹の雌の5XFADマウス (B6/SJL遺伝的バックグラウンド) をこの研究に使用した。マウスにはビヒクル又は化合物(1 mg/kg)i.p.を週2回2カ月間、月齢2~4カ月の間与えた。
* 可溶性画分:
・ Aβ40 = 9.48±1.08μg/mgのタンパク質、
・ Aβ42 = 0.24±0.03μg/mgのタンパク質、
* 不溶性画分:
・ Aβ40 = 0.68±0.10μg/mgのタンパク質、
・ Aβ42 = 10.84±0.73μg/mgのタンパク質。
28匹の雌の5XFADマウス (C57BL/6J遺伝的バックグラウンド) を本研究に使用した。マウスには、週2回、3カ月間、月齢1カ月から4カ月までビヒクル又は化合物 (1 mg/kg) i.p.を与えた。
この研究は、アルツハイマー病のトランスジェニックマウスモデルである5XFADマウスへの慢性投与により、ドネコプリド及びフルコプリドが抗アミロイド作用 (Aβ42レベル及びアミロイド斑の減少) 及び抗炎症性作用 (アストログリオーシスの減少) を発揮したことを実証している。これらの作用は嗅内皮質及び前頭皮質において主に突出している。更に、ドネコプリド及びフルコプリドの慢性投与は、5XFADマウスにおいて、抗記憶喪失症作用を発揮し、記憶欠損の出現を予防することができる。
本実施例は、上で定義された一般式(I)の複数の化合物の、アミロイドペプチドオリゴマーで被毒した海馬ニューロンに対する神経保護作用を開示するものである。
〔海馬ニューロンの初代培養物〕
ラットの海馬ニューロンをCallizotら (2013) J. Neurosci. Res. 91:706~716頁に記載されている通り培養した。簡単に説明すると、妊娠第17日の妊娠した雌のラット (Rats Wistar;Janvier Labs社、France) を、CO2チャンバーでの深麻酔及び頸部脱臼を使用して屠殺した。次いで、胎児を子宮から取り出し、2 %ペニシリン (10,000 U/ml)及びストレプトマイシン(10 mg/ml)溶液(PS) 及び1 %ウシ血清アルブミン (BSA) を有する、氷冷したL15 Leibovitz培地内に直ちに配置した。海馬を、37℃で20分間、0.05 %トリプシン及び0.02 %EDTAの最終濃度のトリプシン-EDTA溶液で処理した。DNAse I グレードII (最終濃度0.5 mg/ml) 及び10 %ウシ胎児血清 (FCS) を含有する、4.5 g/lのグルコースを有するダルベッコ改変イーグル培地 (DMEM) の添加により、解離を停止した。10 mlピペットの先端を介した3回の強制的通過により細胞を機械的に解離した。
<試験化合物>:以下の化合物を試験した:
- MR31193
- MR31176
- MR31192、及び
- MR33583
<予備インキュベーション>:培養の第17日に、化合物を培養用培地に溶解し、Aβ1-42曝露前、初代海馬ニューロンと共に1時間予備インキュベートした。
被毒させてから24時間後、上清を取り出し、将来の解析的分析のために直ちに凍結した。これらを-20℃で6カ月まで保持した。次いで、海馬ニューロンをエタノール (95 %) 及び酢酸 (5 %) の冷たい溶液で、-20℃で5分間固定した。これらを再度PBS中で2回洗浄し、次いで透過処理し、0.1 %のサポニン及び1 %のFCSを含有するPBSの溶液を使用して、室温で15分間非特異的部位をブロッキングした。
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/1000希釈でのニワトリポリクローナル抗体抗微小管関連タンパク質2 (MAP-2) (この抗体は細胞体及び神経突起を特異的に染色し、神経細胞消滅及び神経突起ネットワークの研究を可能にする);並びに
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/100希釈でのマウスモノクローナル抗体抗ホスホタウ (AT100)。
- ニューロンの総数(ニューロン生存数、MAP-2陽性ニューロンの数)
- 神経突起ネットワーク(MAP-2陽性ニューロン、単位:μm)
- AT100の領域(μm2、MAP-2陽性ニューロンと重複)。
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/200希釈でのマウスモノクローナル抗体抗シナプス後肥厚95 kDa (PSD95);
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/100希釈でのウサギポリクローナル抗体抗シナプトフィジン (SYN)。
- シナプスの数 (PSD95/SYNの間で重複)
〔統計分析〕
すべての値は平均値+/-SEM (平均の標準誤差) として表現される。統計分析を一元ANOVA、これに続くダネットの検定又はLSDフィッシャーの検定で実施した。p<0.05は有意であると考えられた。
以下の結果を得た。
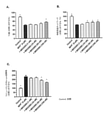
- MR31193は強い神経保護作用を示す (生存、神経突起及びシナプスのネットワーク)。図1及び図2を見て分かる通り、作用はベル型曲線に従い、生存及び神経突起ネットワークについて最大作用は100 nMの濃度で観察された (図1A~図1C)。シナプスネットワークに対する最大作用はより低い濃度で得られた (5 nM~100 nMの間、図2)。タウ過剰リン酸化に対する有意な作用もまた観察され、最大の作用は50 nMで観察された (図1Dを参照されたい)。
- 図3及び図4を見て分かる通り、MR31176は高濃度で神経保護作用を示す (生存、神経突起及びシナプスのネットワーク。タウ過剰リン酸化に対する有意な作用もまた高濃度で観察された (図3Dを参照されたい)。
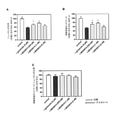
- 図5及び図6を見て分かる通り、MR31192は、非常に低用量で非常に強い神経保護作用を示す (例えば、生存に対して1~5 nM、図5Aを参照されたい)。神経突起ネットワークについても、非常に大きな作用がすべての試験した用量において観察された (図5Bを参照されたい)。図5Cを見て分かる通り、この化合物は神経栄養作用も更に示した (神経突起成長を誘発させた)。シナプスの数もまた低用量で増加した (1~5 nM、図6を参照されたい)。重要な作用はタウ過剰リン酸化でも観察された (図5Dを参照されたい)。
- ベル型曲線に従う神経保護作用はMR33583でも観察された (図7及び図8を参照されたい)。活性のある濃度は50~500 nMより上であった。神経突起ネットワークに対する強い作用はほとんどすべての試験した用量で観察された (図7Bを参照されたい)。ベル型作用はタウ過剰リン酸化でも観察され、最大作用は50~100 nMであった (図7Dを参照されたい)。
本実施例は化合物MR31192、及びMR36014の神経保護作用を示すものである。
〔海馬ニューロンの初代培養物〕
ラット海馬ニューロンを、Callizotら (2013) J. Neurosci. Res. 91:706~716頁により記載されている通り培養した。簡単に説明すると、妊娠第17日の妊娠した雌のラット (Rats Wistar;Janvier Labs社、France) を、CO2チャンバーでの深麻酔及び頸部脱臼を使用して屠殺した。次いで、胎児を子宮から取り出し、2 %ペニシリン (10,000 U/ml) 及びストレプトマイシン (10 mg/ml) 溶液(PS)及び1 %ウシ血清アルブミン (BSA) を有する、氷冷したL15 Leibovitz培地内に直ちに配置した。海馬を、37℃で20分間、0.05 %トリプシン及び0.02 %EDTAの最終濃度のトリプシン-EDTA溶液で処理した。DNAse I グレードII (最終濃度0.5 mg/ml) 及び10 %ウシ胎児血清 (FCS) を含有する、4.5 g/lのグルコースを有するダルベッコ改変イーグル培地 (DMEM) の添加により、解離を停止した。10 mlピペットの先端を介した3回の強制的通過により細胞を機械的に解離した。
<試験化合物>:以下の化合物を試験した:
- MR31192、
- MR36014、及び
- ドネペジル
<予備インキュベーション>:培養の第17日に、化合物を培養用培地に溶解し、Aβ1-42曝露前、初代海馬ニューロンと共に1時間予備インキュベートした。
被毒させてから24時間後、上清を取り出し、将来解析的分析のため直ちに凍結した。これらを-20℃で6カ月まで保持した。次いで、海馬ニューロンをエタノール (95 %) 及び酢酸 (5 %) の冷たい溶液で、-20℃で5分間固定した。これらを再度PBS中で2回洗浄し、次いで透過処理し、0.1 %のサポニン及び1 %のFCSを含有するPBSの溶液を使用して、室温で15分間非特異的部位をブロッキングした。
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/1000希釈でのニワトリポリクローナル抗体抗微小管関連タンパク質2(MAP-2) (この抗体は細胞体及び神経突起を特異的に染色し、神経細胞消滅及び神経突起ネットワークの研究を可能にする);並びに
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/100の希釈でのマウスモノクローナル抗体抗ホスホタウ (AT100)。
- ニューロンの総数 (ニューロン生存、MAP-2陽性ニューロンの数)
- 神経突起ネットワーク (MAP-2陽性ニューロン、単位:μm)
- AT100の領域 (μm2、MAP-2陽性ニューロンと重複)。
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/200希釈でのマウスモノクローナル抗体抗シナプス後肥厚95 kDa (PSD95);
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/100希釈でのウサギポリクローナル抗体抗シナプトフィジン (SYN)。
- シナプスの数 (PSD95/SYNの間で重複)
すべての値は平均値+/-SEM (平均の標準誤差) として表現される。統計分析を一元ANOVA、これに続くダネットの検定又はLSDフィッシャーの検定で実施した。p<0.05は有意であると考えられた。
図9及び図10を見て分かる通り、化合物MR31192は、濃度500 pMまで活性があり (生存及び神経突起ネットワーク、図9A、図9B、図9Cを参照されたい)、タウ過剰リン酸化の有意な減少 (図9Dを参照されたい) もまた100 pMで観察されている。シナプスに対する神経保護作用は500 pMで更に観察されている (図10を参照されたい)。
本実施例は、MPP+で損傷したドーパミン作動性TH-陽性ニューロンに対するMR36014及びMR33583の神経保護作用を示すものである。
〔中脳神経の初代培養物〕
すべての実験は、国立衛生研究所の実験動物の管理と使用に関する指針 (National Institutes of Health Guide for the Care and Use of Laboratory Animals) に従い行い、現在の欧州連合規則に従った (European Union regulations)(Directive 2010/63/EU)。契約番号:A1301310。
<予備インキュベーション>:培養の第6日において、化合物を培養用培地内で希釈し、初代ドパミンニューロンと共に1時間予備インキュベートしてから、MPP+に曝露した。
試験化合物を96-ウェルプレート内で試験した (1条件当たりn=6培養ウェル)。MR36014及びMR33583を1時間予備インキュベートしてから、MPP+により被毒させる。以下の条件を評価した:
被毒させてから48時間後、細胞培養物上清を取り出し、将来の分析用に直ちに凍結した。4 %パラホルムアルデヒドのPBS中溶液、pH=7.3で細胞を室温で20分間固定した。細胞をPBS中で2回洗浄した。0.1 %サポニン及び1 %FCSを含有する溶液を使用して、細胞膜透過化及び非特異的部位のブロッキングを室温で15分間行った。
- 1 %FCS、0.1 %サポニンを含有するPBS中、1/10,000希釈で、マウスにおいて生成されたモノクローナル抗チロシンヒドロキシラーゼ (TH) 抗体、室温で2時間。
- 1 %FCS、0.1 %サポニンを含有するPBS中、1/200希釈で、ウサギにおいて生成されたポリクローナル抗アルファシヌクレイン (α-syn) 抗体、室温で2時間。
- THニューロンの総数の分析 (TH陽性ニューロン)、
- TH陽性ニューロンの全神経突起ネットワーク (単位:μm)
- α-syn凝集 (THとα-syn染色との間で重複する領域、単位:μm2)
〔統計分析〕
すべての値は平均値+/-SEM (平均の標準誤差) として表現される。統計分析は一元ANOVA、これに続くダネットの検定又はLSDフィッシャーの検定により実施した。p<0.05は有意であると考えられた。
〔MPP+での損傷後の、THニューロンの生存、神経突起ネットワーク及びα-syn凝集に対するMR36014の作用〕。
MPP+での損傷後、MR33583は、ニューロンの生存を改善し (100 nM、図14Aを参照されたい)、神経突起ネットワークを部分的に保護した (10 nMから100 nMへ、図14Bを参照されたい)。MR33583のプラス効果はα-synの凝集でも観察された (50 nM及び100 nM、図14Cを参照されたい)。
研究の狙いは、パーキンソン病のin vitroモデルにおいて、MR36014及びMR33583の神経保護作用を調査することであった。
- 両方の化合物は、ドパミンニューロンに対して、MPP+の毒性に反対に作用する、
- MR36014は、この化合物がTHニューロンの生存を促進するためのより高い効力を示したため、MR33583よりも強力である。
-MR36014はMR33583より低い用量で活性があった。
本実施例は、グルタメートで損傷後のラットの初代皮質ニューロンに対する化合物MR36014及びMR33583の神経保護作用の評価を開示するものである。
〔皮質ニューロンの初代培養物〕
すべての実験は、国立衛生研究所の実験動物の管理と使用に関する指針 (National Institutes of Health Guide for the Care and Use of Laboratory Animals) に従い行い、現在の欧州連合規則に従った (European Union regulations) (Directive 2010/63/EU)。契約番号:A1301310。
<予備インキュベーション>:培養の第13日、化合物を培養用培地に溶解し、グルタメートへの曝露前、初代皮質ニューロンと共に1時間予備インキュベートした。
試験化合物を96-ウェルプレート内で試験した(1条件当たりn=6培養ウェル)。以下の条件を評価した:
<免疫染色:MAP-2 (生存及び神経突起ネットワーク) > - 被毒させてから48時間後、細胞培養物上清を取り出し、将来の分析のために、直ちに凍結した。細胞をエタノール (95 %) 及び酢酸 (5 %) の冷たい溶液で、-20℃で5分間固定した。細胞をPBS中で2回洗浄した。細胞を透過処理し、0.1 %サポニン及び1 %FCSを含有するPBSの溶液を用いて、室温で15分間、非特異的結合部位をブロッキングした。
- 全ニューロン生存 (MAP-2陽性、数)、(データは1ウェル当たり30枚の像のニューロンの平均数で表現)。
- 全神経突起ネットワーク (MAP-2、単位:μm)、(データは1ウェル当たり30枚の像のニューロンの平均値で表現)。
すべての値は平均値+/-SEM (平均の標準誤差) として表現される。統計分析を一元ANOVA、これに続くダネットの検定又はLSDフィッシャーの検定により実施した。p<0.05は有意であると考えられた。
〔グルタメートで損傷した皮質ニューロンに対するMR36014及びMR33583の作用〕
グルタミン酸作動性損傷は、皮質ニューロンの損失 (図15A及び図15C;32 %のニューロン死) 及び全神経突起ネットワークの収縮 (図15B及び図15D;38 %の神経突起損失) を誘発させた。
研究の狙いは、グルタミン酸作動性の興奮毒性により誘発させたニューロンストレスのin vitroモデルにおけるMR36014及びMR33583の神経保護作用を調査することであった。グルタミン酸作動性ストレスは、アルツハイマー病及び脳虚血を含む、異なる神経疾患に存在する病理学的特徴である。
- 両方の化合物は、皮質ニューロンに対するグルタメートの毒性に反対に作用する、
- MR36014及びMR33583は同様の効力を示したが、MR36014はより低い用量で活性があった(ニューロンの生存に対して)。
本実施例は、グルタメート損傷後のラット初代皮質ニューロンに対するMR36014及びMR33583の神経保護作用の評価を開示するものである。
〔脊髄運動ニューロンの初代培養物〕
すべての実験は、国立衛生研究所の実験動物の管理と使用に関する指針 (National Institutes of Health Guide for the Care and Use of Laboratory Animals) に従い行い、現在の欧州連合規則に従った (European Union regulations)(Directive 2010/63/EU)。契約番号:A1301310。
<予備インキュベーション>:培養の第13日、化合物を培養用培地に溶解し、グルタメートへの曝露前、初代皮質ニューロンと共に1時間予備インキュベートした。
試験化合物を96ウェルプレート内で試験した (1条件当たりn=6培養ウェル)。
被毒させてから24時間後、上清を取り出し、将来の分析のために直ちに凍結した。細胞をエタノール (95 %) 及び酢酸 (5 %) の冷たい溶液で、-20℃で5分間固定した。0.1 %サポニンでの透過化後、細胞を以下と共に2時間インキュベートした:
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/400希釈でのマウスモノクローナル抗体抗微小管関連タンパク質2 (MAP-2)。この抗体を、1 %FCS、0.1 %サポニンを含有するPBS中、1/400希釈でのAlexa Fluor 488ヤギ抗マウスIgGに室温で1時間曝露した。
- 1 %ウシ胎児血清及び0.1 %サポニンを含有するPBS中、1/100希釈でのウサギポリクローナル抗体抗核タールDNA-結合タンパク質43 (TDP-43)。抗体TDP-43を、1 %FCS、0.1 %サポニンを含有するPBS中、1/400希釈でのAlexa Fluor 568ヤギ抗ウサギに室温で1時間曝露した。
以下のエンドポイントを自動的に評価した:
- ニューロン生存の分析 (MAP-2染色、ニューロンの数)、
- 神経突起ネットワークの分析 (MAP-2染色、全神経突起長、単位:μm)、
- 神経突起ネットワーク/ニューロンの分析 (ニューロンネットワーク/MAP2ニューロンの数)、
- MAP-2陽性ニューロンにおける原形質TDP-43の分析 (MAP-2と原形質TDP-43との間の重複、単位:μm2)。
すべての値は平均値+/-SEM (平均の標準誤差) として表現される。統計分析は一元ANOVA、これに続くフィッシャーのLSD検定で実施した。p<0.05は有意であると考えられた。
〔グルタメートで損傷した脊髄運動ニューロンの初代培養物におけるMR36014の作用〕
<ニューロンの生存>。大きなMAP-2脊髄運動ニューロンの損失がグルタメートの適用の後に続いた (42 %のニューロン死) (図16A)。500 pM及び1 nMにおいて、MR36014は脊髄運動ニューロンの生存を有意に改善した。
<ニューロンの生存>。図17に示されているように、大きなMAP-2脊髄運動ニューロンの損失がグルタメートの適用の後に続いた (図17A)。MR33583 (グルタメートの1時間前に加え、損傷後24時間放置) は用量依存性神経保護作用を発揮した (10~100 nM)。
本研究の狙いは、グルタメートで損傷した脊髄運動ニューロンの初代培養物に基づく、筋萎縮性側索硬化症のin vitroモデルにおいて、2つの化合物、MR36014及びMR33583の神経保護作用を評価することであった。
・ MR36014は、ニューロンの生存を改善し、神経突起ネットワークを保護したことから、500 pM及び1 nMにおいて明白な神経保護作用を提供した。
・ MR33583は、すべてのパラメーターにおいて明白な神経保護作用を示した (ニューロンの生存、神経突起ネットワークの保存及び原形質TDP43の蓄積)。
本実施例は、成長因子欠乏状態でのラット初代GABA作動性ニューロンに対するMR33583の神経保護作用の評価を示すものである。
〔GABA作動性ニューロンの初代培養物〕
すべての実験は、国立衛生研究所の実験動物の管理と使用に関する指針 (National Institutes of Health Guide for the Care and Use of Laboratory Animals) に従い行い、現在の欧州連合規則に従った (European Union regulations)(Directive 2010/63/EU)。契約番号:A1301310。
<予備インキュベーション>:培養の第13日、試験化合物を培養用培地内で希釈し、成長因子 (BDNF及びGDNF) の欠乏前、GABA作動性ニューロンと共に1時間予備インキュベートした。
試験化合物を96ウェルプレート内で試験した (1条件当たりn=6培養ウェル)。以下の条件を評価した:
成長因子欠乏から96時間後、細胞培養物上清を取り出し、将来の分析のために直ちに凍結した。細胞をエタノール (95 %) 及び酢酸 (5 %) の冷たい溶液で、-20℃で5分間固定した。細胞をPBS中で2回洗浄し、次いで透過処理した。0.1 %サポニン及び1 %FCSを含有するPBSの溶液で、室温で15分間非特異的部位をブロッキングした。
すべての値は平均値+/-SEM (平均の標準誤差) として表現される。統計分析は、一元ANOVA、これに続くフィッシャーのLSD検定で実施した。p<0.05は有意であると考えられた。
〔成長因子の欠乏によりストレスがかかったGABA作動性ニューロンの初代培養物におけるMR33583の作用〕
<ニューロンの生存>。大きなGAD-67陽性GABA作動性ニューロンの損失が、成長因子の欠乏後に続いた (図18)。
全体で、これらの結果は、MR33583が、GABA作動性ニューロンにおいて神経保護作用(50 nM)を促進することができ、ハンチントン病に対する潜在的な薬物候補になり得ることを示唆している。
Claims (16)
- 神経変性疾患の予防及び/又は処置における神経保護剤としての使用のための、以下の式(I)の化合物:
Xは、
水素原子、又は
ハロゲン原子(Hal)(ここで(Hal)はフッ素、塩素、臭素、若しくはヨウ素である)、又は
直鎖若しくは分枝鎖のCp(Hal)2p+1ポリハロゲン化アルキル基(ここでp=1、2、3、又は4であり、(Hal)は上に示したものと同じ意味を有する)
を表し;
Yは、
酸素原子、又は
硫黄原子、又は
N-R”基(ここで、R”は、水素原子、-OH基、-O-A基(Aは、直鎖又は分枝鎖のC1~C6アルキル基を表し、特にAは、メチル基を表す)、又は直鎖若しくは分枝鎖のCqH2q+1アルキル基(q=1、2、3、又は4)を表す)
を表し;
mは、1、2、及び3から選択される整数であり;
nは、0、1、2、及び3から選択される整数であり;
r及びsは、その値が、r=s=0、又はr=s=1、又はr=s=2、又はr=0かつs=1、又は最後に、r=0かつs=2である整数であり;
Rは、
水素原子、又は
1個若しくは複数のF原子を有していてもよい直鎖若しくは分枝鎖のC1~C5アルキル基を表し;
R’は、
分枝鎖C1~C6アルキル基、又は
1つ若しくは複数のR基を有していてもよく、また、酸素原子、又はRで置換されていてもよい窒素原子、又は硫黄原子、又は-SO2-基若しくは-SO-基を有していてもよい、C3~C10シクロアルキル又はC5~C13二環式基
を表す)、
並びにそのエナンチオマー又はジアステレオ異性体及びそのラセミ体、その酸との塩、その水和物又はその溶媒和物。 - 式(I)においてYが、
酸素原子、又は
硫黄原子、又は
N-R”基(ここで、R”は、水素原子、-OH基、又は直鎖若しくは分枝鎖のCqH2q+1アルキル基(q=1、2、3、又は4)を表す)
を表す、請求項1に記載のその使用のための化合物。 - 式(I)においてXがハロゲン原子を表す、請求項1又は2に記載のその使用のための化合物。
- 式(I)においてYが酸素原子を表す、請求項1~3のいずれか一項に記載のその使用のための化合物。
- 式(I)においてm、n、r、及びsのすべてが値1を有する、請求項1~4のいずれか一項に記載のその使用のための化合物。
- 式(I)においてRが、H、CH3、CH2CH3、又はCH2-CH2Fを表す、請求項1~5のいずれか一項に記載のその使用のための化合物。
- 式(I)においてR’が、シクロプロピル、シクロブチル、シクロペンチル、シクロヘキシル、シクロヘプチル、及び4-ピペリジン基からなる群から選択される基を表す、請求項1~6のいずれか一項に記載のその使用のための化合物。
- 式(I)においてRがメチル基を表し、R’がC4~C7シクロアルキル基を表す、請求項3~7のいずれか一項に記載のその使用のための化合物。
- 前記の酸との塩が、フマレート又はジヒドロクロレートである、請求項1~13のいずれか一項に記載のその使用のための化合物。
- 神経変性疾患が、アルツハイマー病、パーキンソン病、ハンチントン病、多系統萎縮症、筋萎縮性側索硬化症を含む運動ニューロン疾患、ダウン症候群、及び前頭側頭変性症からなる群から選択される、請求項1~14のいずれか一項に記載のその使用のための化合物。
- 神経変性疾患が、アルツハイマー病、パーキンソン病、ハンチントン病、及び筋萎縮性側索硬化症からなる群から選択される、請求項15に記載のその使用のための化合物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18306280.1A EP3628660A1 (en) | 2018-09-28 | 2018-09-28 | Donecopride and flucopride as neuroprotective agents in the treatment of neurodegenerative diseases |
| EP18306280.1 | 2018-09-28 | ||
| PCT/EP2019/076229 WO2020065028A1 (en) | 2018-09-28 | 2019-09-27 | Donecopride as neuroprotective agent in the treatment of neurodegenerative diseases |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022511366A true JP2022511366A (ja) | 2022-01-31 |
| JPWO2020065028A5 JPWO2020065028A5 (ja) | 2022-10-05 |
Family
ID=63798921
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021517453A Pending JP2022511366A (ja) | 2018-09-28 | 2019-09-27 | 神経変性疾患の処置における神経保護剤としてのドネコプリド |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20220031680A1 (ja) |
| EP (2) | EP3628660A1 (ja) |
| JP (1) | JP2022511366A (ja) |
| KR (1) | KR20210098429A (ja) |
| CN (1) | CN113195452A (ja) |
| AU (1) | AU2019346024A1 (ja) |
| BR (1) | BR112021005952A2 (ja) |
| CA (1) | CA3115342A1 (ja) |
| SG (1) | SG11202103070VA (ja) |
| WO (1) | WO2020065028A1 (ja) |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7407966B2 (en) * | 2004-10-07 | 2008-08-05 | Epix Delaware, Inc. | Thienopyridinone compounds and methods of treatment |
| FR2904113A1 (fr) | 2006-07-21 | 2008-01-25 | Exonhit Therapeutics S A Sa | Procedes et outils pour la therapie de pathologies neurodegeneratives |
| FR3006686A1 (fr) | 2013-06-05 | 2014-12-12 | Univ Caen | Composes inhibiteurs de l'acetylcholinesterase et agonistes des recepteurs serotoninergiques 5ht4, a effet promnesiant, leurs procedes de preparation et compositions pharmaceutiques les contenant |
-
2018
- 2018-09-28 EP EP18306280.1A patent/EP3628660A1/en not_active Withdrawn
-
2019
- 2019-09-27 SG SG11202103070VA patent/SG11202103070VA/en unknown
- 2019-09-27 BR BR112021005952-0A patent/BR112021005952A2/pt unknown
- 2019-09-27 JP JP2021517453A patent/JP2022511366A/ja active Pending
- 2019-09-27 KR KR1020217009149A patent/KR20210098429A/ko unknown
- 2019-09-27 US US17/280,217 patent/US20220031680A1/en active Pending
- 2019-09-27 WO PCT/EP2019/076229 patent/WO2020065028A1/en unknown
- 2019-09-27 EP EP19783459.1A patent/EP3856716A1/en active Pending
- 2019-09-27 AU AU2019346024A patent/AU2019346024A1/en active Pending
- 2019-09-27 CN CN201980063618.3A patent/CN113195452A/zh active Pending
- 2019-09-27 CA CA3115342A patent/CA3115342A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| BR112021005952A2 (pt) | 2021-06-29 |
| CA3115342A1 (en) | 2020-04-02 |
| AU2019346024A1 (en) | 2021-04-29 |
| EP3628660A1 (en) | 2020-04-01 |
| WO2020065028A1 (en) | 2020-04-02 |
| SG11202103070VA (en) | 2021-04-29 |
| CN113195452A (zh) | 2021-07-30 |
| EP3856716A1 (en) | 2021-08-04 |
| US20220031680A1 (en) | 2022-02-03 |
| KR20210098429A (ko) | 2021-08-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Weng et al. | Roles of sigma-1 receptors on mitochondrial functions relevant to neurodegenerative diseases | |
| Hou et al. | NAD+ supplementation normalizes key Alzheimer’s features and DNA damage responses in a new AD mouse model with introduced DNA repair deficiency | |
| JP5712207B2 (ja) | 脳疾患及び状態の予防及び治療のための組成物及び方法 | |
| Leung et al. | Microglia activation mediates fibrillar amyloid-β toxicity in the aged primate cortex | |
| Bailey et al. | A novel effect of rivastigmine on pre‐synaptic proteins and neuronal viability in a neurodegeneration model of fetal rat primary cortical cultures and its implication in Alzheimer’s disease | |
| Ma et al. | MG53 protects hUC-MSCs against inflammatory damage and synergistically enhances their efficacy in neuroinflammation injured brain through inhibiting NLRP3/caspase-1/IL-1β axis | |
| JP5968878B2 (ja) | イソアクテオシドまたはその製薬上許容される塩の使用 | |
| Ren et al. | Spatial training ameliorates long-term alzheimer's disease-like pathological deficits by reducing NLRP3 inflammasomes in PR5 mice | |
| Yu et al. | Baicalin attenuates amyloid β oligomers induced memory deficits and mitochondria fragmentation through regulation of PDE-PKA-Drp1 signalling | |
| Ju et al. | 9R, the cholinesterase and amyloid beta aggregation dual inhibitor, as a multifunctional agent to improve cognitive deficit and neuropathology in the triple-transgenic Alzheimer's disease mouse model | |
| Kelliny et al. | A new approach to model sporadic Alzheimer’s disease by intracerebroventricular streptozotocin injection in APP/PS1 mice | |
| KR20210098428A (ko) | 신경퇴행성 질환의 치료에서 신경보호제로서 아세틸콜린에스테라제 억제제 및 5-ht4 수용체 작용제의 조합물 | |
| JP2022511366A (ja) | 神経変性疾患の処置における神経保護剤としてのドネコプリド | |
| RU2800802C2 (ru) | Донекоприд как нейропротекторный агент при лечении нейродегенеративных заболеваний | |
| Yaghoubi | The Effects of Aerobic Training and Omega-3 Intake on Aβ42, Neprilysin, and γ-Secretase in the Hippocampus of Male Rats Alzheimer’s model | |
| Dhinakaran et al. | Targets for Alzheimer's Disease | |
| WO2020165802A1 (en) | Compositions and methods relating to use of agonists of alpha5-containing gabaa receptors | |
| Evrard et al. | Ethanol effects on the cytoskeleton of nerve tissue cells | |
| KR102612229B1 (ko) | N-[(4'-브로모[1,1'-바이페닐]-4-일)설포닐]-l-발린 또는 이의 약제학적으로 허용 가능한 염을 포함하는 아밀로이드 베타의 올리고머화 및 피브릴화 억제용 조성물 | |
| Orciani et al. | Early treatment with an M1 and sigma-1 receptor agonist prevents cognitive decline in a transgenic rat model displaying Alzheimer-like amyloid pathology | |
| RU2676100C1 (ru) | Применение производных пиперазина для лечения болезни Альцгеймера и деменций альцгеймеровского типа с нарушенной внутриклеточной кальциевой сигнализацией | |
| Liu et al. | Blockage of IL-17 Ameliorates Aβ-Induced Neurotoxicity and Cognitive Decline | |
| Wang et al. | Mitophagy Eliminates the Accumulation of SARM1 on the Mitochondria, Alleviating Axon Degeneration in Acrylamide Neuropathy | |
| US20200306314A1 (en) | Method for treating and/or preventing alzheimer's disease | |
| Wijshake et al. | Targeting senescent cells to improve human health |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220927 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220927 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230710 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20231010 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231208 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20240311 |