JP2020510050A - がんを治療するための、腫瘍溶解性ウイルスの単独又はチェックポイント阻害剤との組み合わせでの使用 - Google Patents
がんを治療するための、腫瘍溶解性ウイルスの単独又はチェックポイント阻害剤との組み合わせでの使用 Download PDFInfo
- Publication number
- JP2020510050A JP2020510050A JP2019549569A JP2019549569A JP2020510050A JP 2020510050 A JP2020510050 A JP 2020510050A JP 2019549569 A JP2019549569 A JP 2019549569A JP 2019549569 A JP2019549569 A JP 2019549569A JP 2020510050 A JP2020510050 A JP 2020510050A
- Authority
- JP
- Japan
- Prior art keywords
- tumor
- cancer
- csf
- oncovex
- mgm
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 206010028980 Neoplasm Diseases 0.000 title claims abstract description 368
- 244000309459 oncolytic virus Species 0.000 title claims abstract description 87
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 title claims abstract description 55
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 title claims abstract description 55
- 201000011510 cancer Diseases 0.000 title abstract description 64
- 238000011282 treatment Methods 0.000 claims abstract description 119
- 229940045513 CTLA4 antagonist Drugs 0.000 claims abstract description 88
- 210000004027 cell Anatomy 0.000 claims description 75
- 201000001441 melanoma Diseases 0.000 claims description 47
- 208000003950 B-cell lymphoma Diseases 0.000 claims description 43
- 206010009944 Colon cancer Diseases 0.000 claims description 41
- 208000001333 Colorectal Neoplasms Diseases 0.000 claims description 40
- 238000000034 method Methods 0.000 claims description 39
- 241000700584 Simplexvirus Species 0.000 claims description 38
- 101710089372 Programmed cell death protein 1 Proteins 0.000 claims description 36
- 208000003721 Triple Negative Breast Neoplasms Diseases 0.000 claims description 34
- 208000022679 triple-negative breast carcinoma Diseases 0.000 claims description 34
- 208000000102 Squamous Cell Carcinoma of Head and Neck Diseases 0.000 claims description 31
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 claims description 31
- 201000000459 head and neck squamous cell carcinoma Diseases 0.000 claims description 31
- 206010006187 Breast cancer Diseases 0.000 claims description 30
- 208000026310 Breast neoplasm Diseases 0.000 claims description 30
- 201000009410 rhabdomyosarcoma Diseases 0.000 claims description 30
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 claims description 24
- 206010029260 Neuroblastoma Diseases 0.000 claims description 24
- 239000008194 pharmaceutical composition Substances 0.000 claims description 24
- 241000700605 Viruses Species 0.000 claims description 23
- 206010035226 Plasma cell myeloma Diseases 0.000 claims description 19
- 208000031673 T-Cell Cutaneous Lymphoma Diseases 0.000 claims description 19
- 201000007241 cutaneous T cell lymphoma Diseases 0.000 claims description 19
- 201000005962 mycosis fungoides Diseases 0.000 claims description 19
- 208000025638 primary cutaneous T-cell non-Hodgkin lymphoma Diseases 0.000 claims description 19
- 208000002154 non-small cell lung carcinoma Diseases 0.000 claims description 17
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 claims description 17
- 208000006168 Ewing Sarcoma Diseases 0.000 claims description 16
- 208000034578 Multiple myelomas Diseases 0.000 claims description 16
- 201000008968 osteosarcoma Diseases 0.000 claims description 16
- 208000005718 Stomach Neoplasms Diseases 0.000 claims description 13
- 206010017758 gastric cancer Diseases 0.000 claims description 13
- 206010073071 hepatocellular carcinoma Diseases 0.000 claims description 13
- 231100000844 hepatocellular carcinoma Toxicity 0.000 claims description 13
- 201000011549 stomach cancer Diseases 0.000 claims description 13
- 102000008203 CTLA-4 Antigen Human genes 0.000 claims 2
- 108010021064 CTLA-4 Antigen Proteins 0.000 claims 2
- 102100023990 60S ribosomal protein L17 Human genes 0.000 claims 1
- 108010074708 B7-H1 Antigen Proteins 0.000 claims 1
- 102000008096 B7-H1 Antigen Human genes 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 7
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 abstract description 6
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 abstract description 6
- 150000001875 compounds Chemical class 0.000 abstract description 2
- 241000699670 Mus sp. Species 0.000 description 70
- 241000700588 Human alphaherpesvirus 1 Species 0.000 description 57
- 108090000623 proteins and genes Proteins 0.000 description 56
- 230000000694 effects Effects 0.000 description 50
- 230000004083 survival effect Effects 0.000 description 49
- 241001465754 Metazoa Species 0.000 description 48
- 230000005764 inhibitory process Effects 0.000 description 45
- 239000007924 injection Substances 0.000 description 44
- 238000002347 injection Methods 0.000 description 44
- 101150076998 ICP34.5 gene Proteins 0.000 description 36
- 102100040678 Programmed cell death protein 1 Human genes 0.000 description 35
- 239000012275 CTLA-4 inhibitor Substances 0.000 description 28
- 230000004044 response Effects 0.000 description 27
- 101000801234 Homo sapiens Tumor necrosis factor receptor superfamily member 18 Proteins 0.000 description 26
- 102100033728 Tumor necrosis factor receptor superfamily member 18 Human genes 0.000 description 26
- 230000004614 tumor growth Effects 0.000 description 26
- 239000000556 agonist Substances 0.000 description 24
- 230000002601 intratumoral effect Effects 0.000 description 24
- 230000001965 increasing effect Effects 0.000 description 23
- 238000012360 testing method Methods 0.000 description 22
- 210000004881 tumor cell Anatomy 0.000 description 22
- 210000001744 T-lymphocyte Anatomy 0.000 description 21
- 229960003301 nivolumab Drugs 0.000 description 19
- 230000000259 anti-tumor effect Effects 0.000 description 18
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 description 17
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 17
- 229960002621 pembrolizumab Drugs 0.000 description 17
- 108700030875 Programmed Cell Death 1 Ligand 2 Proteins 0.000 description 16
- 101000746373 Homo sapiens Granulocyte-macrophage colony-stimulating factor Proteins 0.000 description 15
- 101100407308 Mus musculus Pdcd1lg2 gene Proteins 0.000 description 15
- 102100024213 Programmed cell death 1 ligand 2 Human genes 0.000 description 15
- 230000006870 function Effects 0.000 description 15
- 102000046157 human CSF2 Human genes 0.000 description 14
- 230000028993 immune response Effects 0.000 description 14
- 206010027476 Metastases Diseases 0.000 description 13
- 239000003112 inhibitor Substances 0.000 description 13
- 208000037819 metastatic cancer Diseases 0.000 description 13
- 208000011575 metastatic malignant neoplasm Diseases 0.000 description 13
- 241000699666 Mus <mouse, genus> Species 0.000 description 12
- 230000037396 body weight Effects 0.000 description 12
- 229960005386 ipilimumab Drugs 0.000 description 12
- 230000009885 systemic effect Effects 0.000 description 12
- 239000002246 antineoplastic agent Substances 0.000 description 11
- 229960003852 atezolizumab Drugs 0.000 description 11
- 229940127089 cytotoxic agent Drugs 0.000 description 11
- 239000003814 drug Substances 0.000 description 11
- 239000003446 ligand Substances 0.000 description 11
- 238000010172 mouse model Methods 0.000 description 11
- 102100034922 T-cell surface glycoprotein CD8 alpha chain Human genes 0.000 description 10
- DDRJAANPRJIHGJ-UHFFFAOYSA-N creatinine Chemical compound CN1CC(=O)NC1=N DDRJAANPRJIHGJ-UHFFFAOYSA-N 0.000 description 10
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 10
- 230000012010 growth Effects 0.000 description 10
- 230000003902 lesion Effects 0.000 description 10
- 230000009401 metastasis Effects 0.000 description 10
- 238000009097 single-agent therapy Methods 0.000 description 10
- 235000018102 proteins Nutrition 0.000 description 9
- 102000004169 proteins and genes Human genes 0.000 description 9
- 101100508081 Human herpesvirus 1 (strain 17) ICP34.5 gene Proteins 0.000 description 8
- 101150027249 RL1 gene Proteins 0.000 description 8
- 230000010261 cell growth Effects 0.000 description 8
- 230000008859 change Effects 0.000 description 8
- 229940079593 drug Drugs 0.000 description 8
- 238000001727 in vivo Methods 0.000 description 8
- 230000000174 oncolytic effect Effects 0.000 description 8
- 230000005855 radiation Effects 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 238000007920 subcutaneous administration Methods 0.000 description 8
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 7
- 239000000427 antigen Substances 0.000 description 7
- 108091007433 antigens Proteins 0.000 description 7
- 102000036639 antigens Human genes 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 7
- 229960004316 cisplatin Drugs 0.000 description 7
- 201000010099 disease Diseases 0.000 description 7
- 229950009791 durvalumab Drugs 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 210000000987 immune system Anatomy 0.000 description 7
- 230000003993 interaction Effects 0.000 description 7
- 230000003389 potentiating effect Effects 0.000 description 7
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 7
- 230000003612 virological effect Effects 0.000 description 7
- 238000011729 BALB/c nude mouse Methods 0.000 description 6
- 102100024263 CD160 antigen Human genes 0.000 description 6
- 101000761938 Homo sapiens CD160 antigen Proteins 0.000 description 6
- 102000037982 Immune checkpoint proteins Human genes 0.000 description 6
- 108091008036 Immune checkpoint proteins Proteins 0.000 description 6
- 208000037844 advanced solid tumor Diseases 0.000 description 6
- 238000002512 chemotherapy Methods 0.000 description 6
- 231100000371 dose-limiting toxicity Toxicity 0.000 description 6
- 208000015181 infectious disease Diseases 0.000 description 6
- 238000001990 intravenous administration Methods 0.000 description 6
- 238000011835 investigation Methods 0.000 description 6
- 238000011275 oncology therapy Methods 0.000 description 6
- 230000010076 replication Effects 0.000 description 6
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 5
- 102100038078 CD276 antigen Human genes 0.000 description 5
- 101710185679 CD276 antigen Proteins 0.000 description 5
- 241000701074 Human alphaherpesvirus 2 Species 0.000 description 5
- 241001529936 Murinae Species 0.000 description 5
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 5
- 239000012271 PD-L1 inhibitor Substances 0.000 description 5
- 102100024216 Programmed cell death 1 ligand 1 Human genes 0.000 description 5
- 108010079206 V-Set Domain-Containing T-Cell Activation Inhibitor 1 Proteins 0.000 description 5
- 102100038929 V-set domain-containing T-cell activation inhibitor 1 Human genes 0.000 description 5
- 230000002411 adverse Effects 0.000 description 5
- 208000025997 central nervous system neoplasm Diseases 0.000 description 5
- 229940109239 creatinine Drugs 0.000 description 5
- 230000006378 damage Effects 0.000 description 5
- 239000012634 fragment Substances 0.000 description 5
- 108020001507 fusion proteins Proteins 0.000 description 5
- 102000037865 fusion proteins Human genes 0.000 description 5
- 230000002401 inhibitory effect Effects 0.000 description 5
- 210000004072 lung Anatomy 0.000 description 5
- 229940121656 pd-l1 inhibitor Drugs 0.000 description 5
- 238000011002 quantification Methods 0.000 description 5
- 238000001959 radiotherapy Methods 0.000 description 5
- 102000005962 receptors Human genes 0.000 description 5
- 108020003175 receptors Proteins 0.000 description 5
- 102100029822 B- and T-lymphocyte attenuator Human genes 0.000 description 4
- 102100031351 Galectin-9 Human genes 0.000 description 4
- 101100229077 Gallus gallus GAL9 gene Proteins 0.000 description 4
- 101000864344 Homo sapiens B- and T-lymphocyte attenuator Proteins 0.000 description 4
- 101001137987 Homo sapiens Lymphocyte activation gene 3 protein Proteins 0.000 description 4
- 101000666896 Homo sapiens V-type immunoglobulin domain-containing suppressor of T-cell activation Proteins 0.000 description 4
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical class C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 4
- 102000017578 LAG3 Human genes 0.000 description 4
- 108010061593 Member 14 Tumor Necrosis Factor Receptors Proteins 0.000 description 4
- 101000597780 Mus musculus Tumor necrosis factor ligand superfamily member 18 Proteins 0.000 description 4
- 101710094000 Programmed cell death 1 ligand 1 Proteins 0.000 description 4
- 230000006044 T cell activation Effects 0.000 description 4
- 102100028785 Tumor necrosis factor receptor superfamily member 14 Human genes 0.000 description 4
- 101150085955 US11 gene Proteins 0.000 description 4
- 102100038282 V-type immunoglobulin domain-containing suppressor of T-cell activation Human genes 0.000 description 4
- 108700005077 Viral Genes Proteins 0.000 description 4
- 229960004150 aciclovir Drugs 0.000 description 4
- MKUXAQIIEYXACX-UHFFFAOYSA-N aciclovir Chemical compound N1C(N)=NC(=O)C2=C1N(COCCO)C=N2 MKUXAQIIEYXACX-UHFFFAOYSA-N 0.000 description 4
- 230000033289 adaptive immune response Effects 0.000 description 4
- 210000003719 b-lymphocyte Anatomy 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 229950007712 camrelizumab Drugs 0.000 description 4
- 208000029742 colonic neoplasm Diseases 0.000 description 4
- 230000009089 cytolysis Effects 0.000 description 4
- 238000012217 deletion Methods 0.000 description 4
- 230000037430 deletion Effects 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 239000012537 formulation buffer Substances 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 238000003780 insertion Methods 0.000 description 4
- 230000037431 insertion Effects 0.000 description 4
- 239000007928 intraperitoneal injection Substances 0.000 description 4
- 238000013207 serial dilution Methods 0.000 description 4
- 238000001356 surgical procedure Methods 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 238000002560 therapeutic procedure Methods 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- 108020004414 DNA Proteins 0.000 description 3
- 208000009889 Herpes Simplex Diseases 0.000 description 3
- 241000725303 Human immunodeficiency virus Species 0.000 description 3
- -1 TIM3 Proteins 0.000 description 3
- 102000006601 Thymidine Kinase Human genes 0.000 description 3
- 108020004440 Thymidine kinase Proteins 0.000 description 3
- 229940024606 amino acid Drugs 0.000 description 3
- 235000001014 amino acid Nutrition 0.000 description 3
- 230000005975 antitumor immune response Effects 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- 210000001072 colon Anatomy 0.000 description 3
- 238000003745 diagnosis Methods 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 239000012636 effector Substances 0.000 description 3
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 230000035876 healing Effects 0.000 description 3
- 230000008821 health effect Effects 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 238000007912 intraperitoneal administration Methods 0.000 description 3
- 210000001165 lymph node Anatomy 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 201000000050 myeloid neoplasm Diseases 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 230000001603 reducing effect Effects 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 238000009256 replacement therapy Methods 0.000 description 3
- 208000011581 secondary neoplasm Diseases 0.000 description 3
- 230000001568 sexual effect Effects 0.000 description 3
- 150000003384 small molecules Chemical class 0.000 description 3
- 210000000952 spleen Anatomy 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 150000003431 steroids Chemical class 0.000 description 3
- 230000002459 sustained effect Effects 0.000 description 3
- 229950007217 tremelimumab Drugs 0.000 description 3
- 230000004565 tumor cell growth Effects 0.000 description 3
- PGOHTUIFYSHAQG-LJSDBVFPSA-N (2S)-6-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-4-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-5-amino-2-[[(2S)-2-[[(2S)-2-[[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-5-amino-2-[[(2S)-1-[(2S,3R)-2-[[(2S)-2-[[(2S)-2-[[(2R)-2-[[(2S)-2-[[(2S)-2-[[2-[[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-1-[(2S)-2-[[(2S)-2-[[(2S)-2-[[(2S)-2-amino-4-methylsulfanylbutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]propanoyl]pyrrolidine-2-carbonyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-methylpentanoyl]amino]acetyl]amino]-3-hydroxypropanoyl]amino]-4-methylpentanoyl]amino]-3-sulfanylpropanoyl]amino]-4-methylsulfanylbutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-hydroxybutanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-3-hydroxypropanoyl]amino]-3-hydroxypropanoyl]amino]-3-(1H-imidazol-5-yl)propanoyl]amino]-4-methylpentanoyl]amino]-3-hydroxybutanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-5-carbamimidamidopentanoyl]amino]-5-oxopentanoyl]amino]-3-hydroxybutanoyl]amino]-3-hydroxypropanoyl]amino]-3-carboxypropanoyl]amino]-3-hydroxypropanoyl]amino]-5-oxopentanoyl]amino]-5-oxopentanoyl]amino]-3-phenylpropanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-methylbutanoyl]amino]-4-methylpentanoyl]amino]-4-oxobutanoyl]amino]-5-carbamimidamidopentanoyl]amino]-3-(1H-indol-3-yl)propanoyl]amino]-4-carboxybutanoyl]amino]-5-oxopentanoyl]amino]hexanoic acid Chemical compound CSCC[C@H](N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H](Cc1cnc[nH]1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](Cc1ccccc1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](Cc1c[nH]c2ccccc12)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(O)=O PGOHTUIFYSHAQG-LJSDBVFPSA-N 0.000 description 2
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 2
- 108010082126 Alanine transaminase Proteins 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- BPYKTIZUTYGOLE-IFADSCNNSA-N Bilirubin Chemical compound N1C(=O)C(C)=C(C=C)\C1=C\C1=C(C)C(CCC(O)=O)=C(CC2=C(C(C)=C(\C=C/3C(=C(C=C)C(=O)N\3)C)N2)CCC(O)=O)N1 BPYKTIZUTYGOLE-IFADSCNNSA-N 0.000 description 2
- 108091026890 Coding region Proteins 0.000 description 2
- 206010055114 Colon cancer metastatic Diseases 0.000 description 2
- 206010061818 Disease progression Diseases 0.000 description 2
- 102000003886 Glycoproteins Human genes 0.000 description 2
- 108090000288 Glycoproteins Proteins 0.000 description 2
- 102000001554 Hemoglobins Human genes 0.000 description 2
- 108010054147 Hemoglobins Proteins 0.000 description 2
- 101000777277 Homo sapiens Serine/threonine-protein kinase Chk2 Proteins 0.000 description 2
- 102000037978 Immune checkpoint receptors Human genes 0.000 description 2
- 108091008028 Immune checkpoint receptors Proteins 0.000 description 2
- 102000013462 Interleukin-12 Human genes 0.000 description 2
- 108010065805 Interleukin-12 Proteins 0.000 description 2
- 102000002698 KIR Receptors Human genes 0.000 description 2
- 108010043610 KIR Receptors Proteins 0.000 description 2
- 229940125568 MGD013 Drugs 0.000 description 2
- 108091054437 MHC class I family Proteins 0.000 description 2
- 102000043129 MHC class I family Human genes 0.000 description 2
- 102000002356 Nectin Human genes 0.000 description 2
- 108060005251 Nectin Proteins 0.000 description 2
- 239000012272 PD-L2 inhibitor Substances 0.000 description 2
- 208000006265 Renal cell carcinoma Diseases 0.000 description 2
- 241001068295 Replication defective viruses Species 0.000 description 2
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 2
- 206010039491 Sarcoma Diseases 0.000 description 2
- 102100031075 Serine/threonine-protein kinase Chk2 Human genes 0.000 description 2
- 208000021712 Soft tissue sarcoma Diseases 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 230000006052 T cell proliferation Effects 0.000 description 2
- 230000005867 T cell response Effects 0.000 description 2
- 108010000499 Thromboplastin Proteins 0.000 description 2
- 102000002262 Thromboplastin Human genes 0.000 description 2
- 230000003213 activating effect Effects 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 208000009956 adenocarcinoma Diseases 0.000 description 2
- 150000001413 amino acids Chemical class 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000003146 anticoagulant agent Substances 0.000 description 2
- 230000001363 autoimmune Effects 0.000 description 2
- 102000023732 binding proteins Human genes 0.000 description 2
- 108091008324 binding proteins Proteins 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 238000000423 cell based assay Methods 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 238000011284 combination treatment Methods 0.000 description 2
- 239000003246 corticosteroid Substances 0.000 description 2
- CVSVTCORWBXHQV-UHFFFAOYSA-N creatine Chemical compound NC(=[NH2+])N(C)CC([O-])=O CVSVTCORWBXHQV-UHFFFAOYSA-N 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 231100000517 death Toxicity 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000004069 differentiation Effects 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 230000005750 disease progression Effects 0.000 description 2
- 229940121432 dostarlimab Drugs 0.000 description 2
- 230000007717 exclusion Effects 0.000 description 2
- IJJVMEJXYNJXOJ-UHFFFAOYSA-N fluquinconazole Chemical compound C=1C=C(Cl)C=C(Cl)C=1N1C(=O)C2=CC(F)=CC=C2N=C1N1C=NC=N1 IJJVMEJXYNJXOJ-UHFFFAOYSA-N 0.000 description 2
- 238000001415 gene therapy Methods 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 2
- 230000036039 immunity Effects 0.000 description 2
- 238000009169 immunotherapy Methods 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 208000032839 leukemia Diseases 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 208000037841 lung tumor Diseases 0.000 description 2
- 208000022766 lymph node neoplasm Diseases 0.000 description 2
- 230000002101 lytic effect Effects 0.000 description 2
- 230000036210 malignancy Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000001394 metastastic effect Effects 0.000 description 2
- 206010061289 metastatic neoplasm Diseases 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 238000011375 palliative radiation therapy Methods 0.000 description 2
- 210000000496 pancreas Anatomy 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 229940121654 pd-l2 inhibitor Drugs 0.000 description 2
- 238000009597 pregnancy test Methods 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000005180 public health Effects 0.000 description 2
- 230000000306 recurrent effect Effects 0.000 description 2
- 210000003289 regulatory T cell Anatomy 0.000 description 2
- 238000012552 review Methods 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 229940121497 sintilimab Drugs 0.000 description 2
- 210000003491 skin Anatomy 0.000 description 2
- 206010040882 skin lesion Diseases 0.000 description 2
- 231100000444 skin lesion Toxicity 0.000 description 2
- 206010041823 squamous cell carcinoma Diseases 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 238000011272 standard treatment Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 229960005486 vaccine Drugs 0.000 description 2
- 230000009278 visceral effect Effects 0.000 description 2
- KUOAJOVOKFATQE-UHFFFAOYSA-N 2-[(2-amino-6-oxo-3h-purin-9-yl)methoxy]ethyl dihydrogen phosphate Chemical compound N1C(N)=NC(=O)C2=C1N(COCCOP(O)(O)=O)C=N2 KUOAJOVOKFATQE-UHFFFAOYSA-N 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 201000004384 Alopecia Diseases 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 238000012935 Averaging Methods 0.000 description 1
- 206010061728 Bone lesion Diseases 0.000 description 1
- 206010065553 Bone marrow failure Diseases 0.000 description 1
- 102100027207 CD27 antigen Human genes 0.000 description 1
- 101150091609 CD274 gene Proteins 0.000 description 1
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 1
- 108050005493 CD3 protein, epsilon/gamma/delta subunit Proteins 0.000 description 1
- 101150050673 CHK1 gene Proteins 0.000 description 1
- 238000003734 CellTiter-Glo Luminescent Cell Viability Assay Methods 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 102000000311 Cytosine Deaminase Human genes 0.000 description 1
- 108010080611 Cytosine Deaminase Proteins 0.000 description 1
- XUIIKFGFIJCVMT-GFCCVEGCSA-N D-thyroxine Chemical compound IC1=CC(C[C@@H](N)C(O)=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-GFCCVEGCSA-N 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 238000008789 Direct Bilirubin Methods 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 208000000471 Dysplastic Nevus Syndrome Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 101800001467 Envelope glycoprotein E2 Proteins 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 241000713813 Gibbon ape leukemia virus Species 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 208000002250 Hematologic Neoplasms Diseases 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 241000700721 Hepatitis B virus Species 0.000 description 1
- 208000000903 Herpes simplex encephalitis Diseases 0.000 description 1
- 206010019973 Herpes virus infection Diseases 0.000 description 1
- 208000017604 Hodgkin disease Diseases 0.000 description 1
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 1
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 1
- 101100407305 Homo sapiens CD274 gene Proteins 0.000 description 1
- 101001078133 Homo sapiens Integrin alpha-2 Proteins 0.000 description 1
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 1
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 1
- 101001117317 Homo sapiens Programmed cell death 1 ligand 1 Proteins 0.000 description 1
- 101000777293 Homo sapiens Serine/threonine-protein kinase Chk1 Proteins 0.000 description 1
- 101000716102 Homo sapiens T-cell surface glycoprotein CD4 Proteins 0.000 description 1
- 101000946843 Homo sapiens T-cell surface glycoprotein CD8 alpha chain Proteins 0.000 description 1
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 1
- 101000597779 Homo sapiens Tumor necrosis factor ligand superfamily member 18 Proteins 0.000 description 1
- 101100427508 Human cytomegalovirus (strain AD169) UL39 gene Proteins 0.000 description 1
- 101001042049 Human herpesvirus 1 (strain 17) Transcriptional regulator ICP22 Proteins 0.000 description 1
- 101000999690 Human herpesvirus 2 (strain HG52) E3 ubiquitin ligase ICP22 Proteins 0.000 description 1
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 1
- 241000282620 Hylobates sp. Species 0.000 description 1
- 101150090364 ICP0 gene Proteins 0.000 description 1
- 101150027427 ICP4 gene Proteins 0.000 description 1
- 108700002232 Immediate-Early Genes Proteins 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 206010062016 Immunosuppression Diseases 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102100025305 Integrin alpha-2 Human genes 0.000 description 1
- 102000006992 Interferon-alpha Human genes 0.000 description 1
- 108010047761 Interferon-alpha Proteins 0.000 description 1
- 102100026878 Interleukin-2 receptor subunit alpha Human genes 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 108091054438 MHC class II family Proteins 0.000 description 1
- 102000043131 MHC class II family Human genes 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 206010027145 Melanocytic naevus Diseases 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 206010027458 Metastases to lung Diseases 0.000 description 1
- 241000714177 Murine leukemia virus Species 0.000 description 1
- 101000979301 Mus musculus Nectin-1 Proteins 0.000 description 1
- 206010028813 Nausea Diseases 0.000 description 1
- 108700019961 Neoplasm Genes Proteins 0.000 description 1
- 102000048850 Neoplasm Genes Human genes 0.000 description 1
- 206010061309 Neoplasm progression Diseases 0.000 description 1
- 206010029350 Neurotoxicity Diseases 0.000 description 1
- 208000007256 Nevus Diseases 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 208000001388 Opportunistic Infections Diseases 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 239000012270 PD-1 inhibitor Substances 0.000 description 1
- 239000012668 PD-1-inhibitor Substances 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 208000031951 Primary immunodeficiency Diseases 0.000 description 1
- 102000043850 Programmed Cell Death 1 Ligand 2 Human genes 0.000 description 1
- 102100027378 Prothrombin Human genes 0.000 description 1
- 108010094028 Prothrombin Proteins 0.000 description 1
- 101150093191 RIR1 gene Proteins 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- IWUCXVSUMQZMFG-AFCXAGJDSA-N Ribavirin Chemical compound N1=C(C(=O)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 IWUCXVSUMQZMFG-AFCXAGJDSA-N 0.000 description 1
- 102000000505 Ribonucleotide Reductases Human genes 0.000 description 1
- 108010041388 Ribonucleotide Reductases Proteins 0.000 description 1
- 102100031081 Serine/threonine-protein kinase Chk1 Human genes 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 101800001271 Surface protein Proteins 0.000 description 1
- 230000024932 T cell mediated immunity Effects 0.000 description 1
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 description 1
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 1
- 238000008050 Total Bilirubin Reagent Methods 0.000 description 1
- 206010044221 Toxic encephalopathy Diseases 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 102000004357 Transferases Human genes 0.000 description 1
- 108090000992 Transferases Proteins 0.000 description 1
- 108700019146 Transgenes Proteins 0.000 description 1
- 102100035283 Tumor necrosis factor ligand superfamily member 18 Human genes 0.000 description 1
- 108091005906 Type I transmembrane proteins Proteins 0.000 description 1
- 101150054371 UL24 gene Proteins 0.000 description 1
- 101150050057 UL43 gene Proteins 0.000 description 1
- 101150041938 US5 gene Proteins 0.000 description 1
- 208000025865 Ulcer Diseases 0.000 description 1
- 108010003533 Viral Envelope Proteins Proteins 0.000 description 1
- 108010067390 Viral Proteins Proteins 0.000 description 1
- 206010047700 Vomiting Diseases 0.000 description 1
- 201000006083 Xeroderma Pigmentosum Diseases 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229960001997 adefovir Drugs 0.000 description 1
- WOZSCQDILHKSGG-UHFFFAOYSA-N adefovir depivoxil Chemical compound N1=CN=C2N(CCOCP(=O)(OCOC(=O)C(C)(C)C)OCOC(=O)C(C)(C)C)C=NC2=C1N WOZSCQDILHKSGG-UHFFFAOYSA-N 0.000 description 1
- 230000001919 adrenal effect Effects 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- 125000003275 alpha amino acid group Chemical group 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 230000003602 anti-herpes Effects 0.000 description 1
- 230000000118 anti-neoplastic effect Effects 0.000 description 1
- 230000000702 anti-platelet effect Effects 0.000 description 1
- 238000011319 anticancer therapy Methods 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 230000030741 antigen processing and presentation Effects 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 229940127218 antiplatelet drug Drugs 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 210000002798 bone marrow cell Anatomy 0.000 description 1
- 206010006007 bone sarcoma Diseases 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000007975 buffered saline Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 230000003915 cell function Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 201000007455 central nervous system cancer Diseases 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 239000013043 chemical agent Substances 0.000 description 1
- 230000007012 clinical effect Effects 0.000 description 1
- 238000009535 clinical urine test Methods 0.000 description 1
- 238000005345 coagulation Methods 0.000 description 1
- 201000010989 colorectal carcinoma Diseases 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 239000003433 contraceptive agent Substances 0.000 description 1
- 230000002254 contraceptive effect Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000000139 costimulatory effect Effects 0.000 description 1
- 229960003624 creatine Drugs 0.000 description 1
- 239000006046 creatine Substances 0.000 description 1
- 208000035250 cutaneous malignant susceptibility to 1 melanoma Diseases 0.000 description 1
- 208000035255 cutaneous malignant susceptibility to 2 melanoma Diseases 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 230000001461 cytolytic effect Effects 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 239000007933 dermal patch Substances 0.000 description 1
- 230000001066 destructive effect Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 230000009429 distress Effects 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 229940056913 eftilagimod alfa Drugs 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 229960000980 entecavir Drugs 0.000 description 1
- YXPVEXCTPGULBZ-WQYNNSOESA-N entecavir hydrate Chemical compound O.C1=NC=2C(=O)NC(N)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)C1=C YXPVEXCTPGULBZ-WQYNNSOESA-N 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 230000000799 fusogenic effect Effects 0.000 description 1
- 101150064645 gJ gene Proteins 0.000 description 1
- 238000012239 gene modification Methods 0.000 description 1
- 230000005017 genetic modification Effects 0.000 description 1
- 235000013617 genetically modified food Nutrition 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 230000009036 growth inhibition Effects 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 208000024963 hair loss Diseases 0.000 description 1
- 230000003676 hair loss Effects 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 208000010710 hepatitis C virus infection Diseases 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- 229940091204 imlygic Drugs 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 229940126546 immune checkpoint molecule Drugs 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 238000013394 immunophenotyping Methods 0.000 description 1
- 229960001438 immunostimulant agent Drugs 0.000 description 1
- 239000003022 immunostimulating agent Substances 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 230000001861 immunosuppressant effect Effects 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 238000002650 immunosuppressive therapy Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 229940117681 interleukin-12 Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 206010023332 keratitis Diseases 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 238000011005 laboratory method Methods 0.000 description 1
- 101150066555 lacZ gene Proteins 0.000 description 1
- 229960001627 lamivudine Drugs 0.000 description 1
- JTEGQNOMFQHVDC-NKWVEPMBSA-N lamivudine Chemical compound O=C1N=C(N)C=CN1[C@H]1O[C@@H](CO)SC1 JTEGQNOMFQHVDC-NKWVEPMBSA-N 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 101710130522 mRNA export factor Proteins 0.000 description 1
- 230000003211 malignant effect Effects 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 108010082117 matrigel Proteins 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 210000002752 melanocyte Anatomy 0.000 description 1
- 208000037843 metastatic solid tumor Diseases 0.000 description 1
- 238000007799 mixed lymphocyte reaction assay Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000009126 molecular therapy Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 201000003731 mucosal melanoma Diseases 0.000 description 1
- 230000008693 nausea Effects 0.000 description 1
- 230000035407 negative regulation of cell proliferation Effects 0.000 description 1
- 230000007135 neurotoxicity Effects 0.000 description 1
- 231100000228 neurotoxicity Toxicity 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 210000004882 non-tumor cell Anatomy 0.000 description 1
- 230000009279 non-visceral effect Effects 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 230000037360 nucleotide metabolism Effects 0.000 description 1
- 230000000474 nursing effect Effects 0.000 description 1
- 238000002515 oligonucleotide synthesis Methods 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 229940121655 pd-1 inhibitor Drugs 0.000 description 1
- 210000004197 pelvis Anatomy 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 238000009520 phase I clinical trial Methods 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 230000006584 pituitary dysfunction Effects 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 238000012809 post-inoculation Methods 0.000 description 1
- 230000035935 pregnancy Effects 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000037452 priming Effects 0.000 description 1
- 238000012913 prioritisation Methods 0.000 description 1
- 210000001948 pro-b lymphocyte Anatomy 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 230000004952 protein activity Effects 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 229940039716 prothrombin Drugs 0.000 description 1
- 208000020016 psychiatric disease Diseases 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 208000019465 refractory cytopenia of childhood Diseases 0.000 description 1
- 230000001177 retroviral effect Effects 0.000 description 1
- 229960000329 ribavirin Drugs 0.000 description 1
- HZCAHMRRMINHDJ-DBRKOABJSA-N ribavirin Natural products O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1N=CN=C1 HZCAHMRRMINHDJ-DBRKOABJSA-N 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 208000002491 severe combined immunodeficiency Diseases 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 210000004872 soft tissue Anatomy 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 229950007213 spartalizumab Drugs 0.000 description 1
- 210000004989 spleen cell Anatomy 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 201000009032 substance abuse Diseases 0.000 description 1
- 231100000736 substance abuse Toxicity 0.000 description 1
- 208000011117 substance-related disease Diseases 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229960004556 tenofovir Drugs 0.000 description 1
- VCMJCVGFSROFHV-WZGZYPNHSA-N tenofovir disoproxil fumarate Chemical compound OC(=O)\C=C\C(O)=O.N1=CN=C2N(C[C@@H](C)OCP(=O)(OCOC(=O)OC(C)C)OCOC(=O)OC(C)C)C=NC2=C1N VCMJCVGFSROFHV-WZGZYPNHSA-N 0.000 description 1
- 229940034208 thyroxine Drugs 0.000 description 1
- XUIIKFGFIJCVMT-UHFFFAOYSA-N thyroxine-binding globulin Natural products IC1=CC(CC([NH3+])C([O-])=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-UHFFFAOYSA-N 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 102000035160 transmembrane proteins Human genes 0.000 description 1
- 108091005703 transmembrane proteins Proteins 0.000 description 1
- 230000014599 transmission of virus Effects 0.000 description 1
- 230000005909 tumor killing Effects 0.000 description 1
- 230000005751 tumor progression Effects 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 231100000402 unacceptable toxicity Toxicity 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 230000007442 viral DNA synthesis Effects 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- 210000002845 virion Anatomy 0.000 description 1
- 230000007923 virulence factor Effects 0.000 description 1
- 239000000304 virulence factor Substances 0.000 description 1
- 230000008673 vomiting Effects 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/76—Viruses; Subviral particles; Bacteriophages
- A61K35/763—Herpes virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70596—Molecules with a "CD"-designation not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
Abstract
Description
本出願は、参照により本明細書に組み込まれる、2017年3月15日に出願された米国仮特許出願第62/471,875号明細書の利益を米国特許法第119条(e)の下で主張するものである。
本明細書で論議されるように、本発明は、腫瘍溶解性ウイルスが単独で又はチェックポイント阻害剤と組み合わせて様々な腫瘍型において抗腫瘍効果をもたらし得ることを証明している。本発明の腫瘍溶解性ウイルスの顕著な有益性は、例えば、化学療法と比べて抗腫瘍効果がそれほど重篤/マイナスではない副作用を伴うことである。例えば、一実施形態では、本発明は、がんの治療における腫瘍溶解性ウイルスの使用に関する。別の実施形態では、本発明は、ユーイング肉腫、神経芽細胞腫、横紋筋肉腫様腫瘍、骨肉腫、横紋筋肉腫、B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、非小細胞肺癌、結腸直腸癌、メラノーマ、頭頸部扁平上皮癌、肝細胞癌、胃癌、乳がん(例えば、トリプルネガティブ乳癌)、皮膚T細胞性リンパ腫又は多発性骨髄腫を治療するための腫瘍溶解性ウイルスの使用に関する。別の実施形態では、本発明は、B細胞性リンパ腫、結腸直腸癌、メラノーマ、頭頸部扁平上皮癌又は乳がん(例えば、トリプルネガティブ乳癌を治療するための、腫瘍溶解性ウイルスとチェックポイント阻害剤との組み合わせの使用に関する。
免疫チェックポイントは、T細胞(細胞媒介性免疫において中心的役割を果たす)などの何らかの種類の免疫系細胞を制御するタンパク質である。免疫チェックポイントは、免疫応答を抑制することを補助するが、これらは、T細胞ががん細胞を死滅させないようにすることもできる。免疫チェックポイント阻害剤(又は簡単に「チェックポイント阻害剤」)は、免疫チェックポイントタンパク質活性をブロックし、免疫系の「ブレーキ」を解除し、T細胞ががん細胞をより良好に死滅させることを可能にし得る。
グルココルチコイド誘導性TNFR関連遺伝子(GITR:TNFRSF 18)は、活性化誘導性TNFRファミリーメンバー(AITR)と呼ばれることもあり、TNF受容体スーパーファミリー(TNFRSF)に属する受容体である。これは、その同族リガンドのGITRリガンド(GITRL、TNFSF18)によって活性化される。GITRは、TNFRファミリーメンバーの特徴である、システインに富む細胞外ドメインを含有するI型膜貫通タンパク質である。例えば、GITRの細胞質ドメインは、4−1BB及びCD27などの特定の他のTNFRファミリーメンバーと密接な相同性を共有する(Nocentini,et al.,Proc.Natl.Acad.Sci.,94:6216−6221(1997))。GITRアゴニスト抗体は、CD8+Tエフェクターメモリー細胞集団を増殖させる手段として、一方では同時にTregの消失又は阻害の促進の手段として現在検証中である。
本発明は、がんなどの疾患又は障害を治療する方法にも関する。いくつかの実施形態では、がんは、ユーイング肉腫、神経芽細胞腫、横紋筋肉腫様腫瘍、骨肉腫、横紋筋肉腫、B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、非小細胞肺癌、結腸直腸癌、メラノーマ、頭頸部扁平上皮癌、肝細胞癌、胃癌、乳がん(例えば、トリプルネガティブ乳癌)、皮膚T細胞性リンパ腫又は多発性骨髄腫である。他の実施形態では、がんは、B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、結腸直腸がん、メラノーマ又は乳がん(例えば、トリプルネガティブ乳癌)である。いくつかの実施形態では、がんは、転移性がんである。
本発明は、腫瘍溶解性ウイルスを含むか、又は腫瘍溶解性ウイルスとチェックポイント阻害剤との組み合わせを含む医薬組成物にも関する。医薬組成物は、例えば、組成物のpH、オスモル濃度、粘度、清澄度、色、等張性、臭気、無菌性、安定性、溶解若しくは放出の速度、吸着又は浸透を変更、維持又は保存するための製剤材料を含有し得る。医薬的に活性な薬剤は、例えば、経口又は非経口、例えば静脈内、筋肉内、皮下、眼窩内、嚢内、腹腔内、大槽内、直腸内、腫瘍内、血管内、皮内を含む様々な経路により、又は例えば皮膚パッチ若しくは経皮イオントフォレーシスをそれぞれ使用して、皮膚を介した受動的若しくは促進された吸収により患者に投与することができる。一実施形態では、腫瘍溶解性ウイルス(例えば、タリモジーン・ラハーパレプベック)は、腫瘍内に注入される(すなわち腫瘍内注射を介して)。別の実施形態では、チェックポイント阻害剤(例えば、抗PD−1抗体、抗PD−L1抗体又は抗CTLA−4抗体)は、全身投与される(例えば、静脈内で)。
別の態様では、本発明は、[1]任意選択で、チェックポイント阻害剤と組み合わせた腫瘍溶解性ウイルスと、[2]患者への投与に関する指示書とを含むキットに関する。例えば、本発明のキットは、腫瘍溶解性ウイルス(例えば、タリモジーン・ラハーパレプベック)と、がんの患者を治療するための指示書(例えば、添付文書又はラベルにおいて)とを含み得る。いくつかの実施形態では、このがんは、転移性がんである。別の実施形態では、本発明のキットは、腫瘍溶解性ウイルス(例えば、タリモジーン・ラハーパレプベック)と、チェックポイント阻害剤(例えば、抗PD−1抗体、抗PD−L1抗体又は抗CTLA−4抗体)と、がんの患者を治療するための指示書(例えば、添付文書又はラベルにおいて)とを含み得る。
この実施例は、タリモジーン・ラハーパレプベックの腫瘍担持マウスへの投与が腫瘍死滅をもたらすことを証明する。
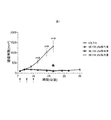
A−673ユーイング肉腫担持マウスをタリモジーン・ラハーパレプベックで5×104、5×105又は5×106PFU/投与量において治療的に処置した。タリモジーン・ラハーパレプベックは、試験8日目、11日目及び14日目に1日1回の腫瘍内注射によって投与した(図1の赤色の矢印)。腫瘍を1週間当たり2〜3回測定した。結果は、0日目が腫瘍摂取の日である日数での時間の関数として、mm3±平均値の標準誤差での群の平均腫瘍体積として表される(16日目、20日目及び23日目のビヒクル対照群について注記されている場合を除き、1群当たりn=10)。星印は、試験23日目にビヒクル対照に対して全てのタリモジーン・ラハーパレプベック群がp<0.0001であることを示す。
SK−N−AS神経芽細胞腫担持マウスをタリモジーン・ラハーパレプベックで5×104、5×105又は5×106PFU/投与量において治療的に処置した。タリモジーン・ラハーパレプベックは、試験6日目、9日目及び12日目に1日1回の腫瘍内注射によって投与した(図2の赤色の矢印)。腫瘍を1週間当たり2〜3回測定した。結果は、0日目が腫瘍摂取の日である日数での時間の関数として、mm3±平均値の標準誤差での群の平均腫瘍体積として表される(18日目、20日目及び23日目の5×104PFU/投与量の群について注記されている場合を除き、1群当たりn=10)。星印は、試験23日目に製剤緩衝液対照に対して5×106及び5×105PFU/投与量群についてp<0.0001であり、5×104PFU/投与量群についてp=0.0001であることを示す。
G−401横紋筋肉腫様腫瘍担持マウスをタリモジーン・ラハーパレプベックで5×104、5×105又は5×106PFU/投与量において治療的に処置した。タリモジーン・ラハーパレプベックは、試験14日目、17日目及び20日目に1日1回の腫瘍内注射によって投与した(図3の赤色の矢印)。腫瘍を1週間当たり2〜3回測定した。結果は、0日目が腫瘍摂取の日である日数での時間の関数として、mm3±平均値の標準誤差での群の平均腫瘍体積として表される(注記されている場合を除き、1群当たりn=10)。星印は、試験40日目にビヒクル対照に対して全てのタリモジーン・ラハーパレプベック投与群がp<0.0001であることを示す。
SJSA−1骨肉腫担持マウスをタリモジーン・ラハーパレプベックで5×104、5×105又は5×106PFU/投与量において治療的に処置した。タリモジーン・ラハーパレプベックは、試験9日目、12日目及び15日目に1日1回の腫瘍内注射によって投与した(図4の赤色の矢印)。腫瘍を1週間当たり2〜3回測定した。結果は、0日目が腫瘍摂取の日である日数での時間の関数として、mm3±平均値の標準誤差での群の平均腫瘍体積として表される(1群当たりn=10)。
SJCRH30横紋筋肉腫担持マウスをタリモジーン・ラハーパレプベックで5×104、5×105又は5×106PFU/投与量において治療的に処置した。タリモジーン・ラハーパレプベックは、試験8日目、11日目及び14日目に1日1回の腫瘍内注射によって投与した(図5の赤色の矢印)。腫瘍を1週間当たり2〜3回測定した。結果は、0日目が腫瘍摂取の日である日数での時間の関数として、mm3±平均値の標準誤差での群の平均腫瘍体積として表される(26日目、30日目及び33日目の5×104PFU/投与量の群と、30日目及び33日目の5×106PFU/投与量の群とについて注記されている場合を除き、1群当たりn=10)。星印は、試験26日目(全ての対照動物が試験中である最後の試験日)にビヒクル対照に対して全てのタリモジーン・ラハーパレプベック投与群についてp<0.0001であることを示す。
びまん性大細胞型B細胞性リンパ腫(DLBCL又はDLBL)
いくつかのDLBCL細胞株(SU−DHL−2、OCI−LY−3、TMD8、RI−1(ABCサブタイプ)及びWSU−NHL(GCBサブタイプ))を1ウェル当たり5,000個細胞で96ウェルプレートに播種し、37℃で一晩インキュベートした。各細胞株について、タリモジーン・ラハーパレプベックを、100MOIで開始して9個のウェル中で段階希釈した(1:4の段階希釈)。72時間のインキュベーション後、各ウェルに残った細胞数を、CellTiter−Glo Luminescent cell viability assay(Promega,Madison,WI)を使用して定量化した。
様々な固形腫瘍細胞株(メラノーマ、非小細胞肺癌、結腸直腸癌、頭頸部扁平上皮癌、肝細胞癌、胃癌及びトリプルネガティブ乳癌)を1ウェル当たり2,000〜10,000個細胞で96ウェルプレートに播種し、37℃で一晩インキュベートした。各細胞株について、タリモジーン・ラハーパレプベックを、100MOIで開始して9個のウェル中で段階希釈した(1:4の段階希釈)。72時間のインキュベーション後、各ウェルに残った細胞数を、ATP−Lite(Perkin Elmer,Waltham,MA)を使用して定量化した。
CTCL及びMM細胞株を1ウェル当たり2,000〜10,000個細胞で96ウェルプレートに播種し、37℃で一晩インキュベートした。各細胞株について、タリモジーン・ラハーパレプベックを、100MOIで開始して9個のウェル中で段階希釈した(1:4の段階希釈)。72時間のインキュベーション後、各ウェルに残った細胞数を、ATP−Lite(Perkin Elmer,Waltham,MA)を使用して定量化した。
メラノーマ、結腸直腸癌及びB細胞性リンパ腫のネズミ細胞株を1ウェル当たり2,000〜10,000個細胞で96ウェルプレートに播種し、37℃で一晩インキュベートした。各細胞株について、タリモジーン・ラハーパレプベックを、100MOIで開始して9個のウェル中で段階希釈した(1:4の段階希釈)。72時間のインキュベーション後、各ウェルに残った細胞数を、ATP−Lite(Perkin Elmer,Waltham,MA)を使用して定量化した。
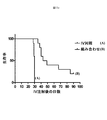
A20腫瘍細胞を0日目において雌BALB/cマウスの右及び左脇腹に皮下注射した(2×106個細胞)。腫瘍体積(mm3)を、電子ノギスを用いて週に2回(Q2W)測定した。腫瘍が平均でおよそ100mm3に達したら、マウスを、処置施行の開始時の平均腫瘍体積(両脇腹における)及び腫瘍体積のばらつきが処置群全体に均一であるように群に無作為化した(1群当たり10匹のマウス)。次いで、マウスにOncoVexmGM−CSF(3×104〜3×106PFU/投与量)又はビヒクルの3回の腫瘍内注射を10日目、13日目及び16日目に施した。臨床徴候、体重変化及び生存期間(腫瘍が800mm3に達した場合、マウスを試験から除外した)を試験が終了するまで週に2〜3回測定した。
A20腫瘍細胞を0日目において雌BALB/cマウスの右及び左脇腹に皮下注射した(2×106個細胞)。腫瘍体積(mm3)を、電子ノギスを用いて週に2回(Q2W)測定した。腫瘍が平均でおよそ100mm3に達したら、動物を、処置施行の開始時の平均腫瘍体積(両脇腹における)及び腫瘍体積のばらつきが処置群全体に均一であるように群に無作為化した(1群当たり10匹のマウス)。次いで、動物にOncoVexmGM−CSF(5×106PFU/投与量)単独又は抗PD−L1 mAb若しくは抗CTLA−4 mAbの腹腔内注射と組み合わせて3回の腫瘍内注射を施した。臨床徴候、体重変化及び生存期間(腫瘍が800mm3に達した場合、マウスを試験から除外した)を試験が終了するまで週に2〜3回測定した。
CT−26腫瘍細胞を0日目において雌BALB/cマウスの右及び左脇腹に皮下注射した(2×106個細胞)。腫瘍体積(mm3)を、電子ノギスを用いて週に2回(Q2W)測定した。腫瘍が平均でおよそ100mm3に達したら、動物を、処置施行の開始時の平均腫瘍体積(両脇腹における)及び腫瘍体積のばらつきが処置群全体に均一であるように4つの群に無作為化した(1群当たり10匹のマウス)。次いで、動物にa)PBS+IgG対照、b)OncoVexmGM−CSF+IgG対照、c)PBS+抗CTTLA−4 mAb若しくはPBS+抗PD−L1 mAb、又はd)OncoVexmGM−CSF+抗CTLA−4 mAb若しくはOncoVexmGM−CSF+抗PD−L1mAbを投与した。臨床徴候、体重変化及び生存期間(腫瘍が800mm3に達した場合、マウスを試験から除外した)を試験が終了するまで週に2〜3回測定した。
B16F10細胞(5×104−HSV−1エントリー受容体の欠如のためにOncoVexmGM−CSF溶菌に対して耐性)を0日目に静脈内注射した。2日目に、マウスネクチン1でトランスフェクトしたB16F 10メラノーマ細胞(OncoVexmGM−CSF溶菌に対して感受性)を雌BL6マウスの右脇腹に皮下注射した。腫瘍体積(mm3)を、電子ノギスを用いて週に2回(Q2W)測定した。皮下腫瘍が平均でおよそ100mm3に達したら、動物を、処置施行の開始時の平均腫瘍体積及び腫瘍体積のばらつきが処置群全体に均一であるように4つの群に無作為化した(1群当たり10匹のマウス)。次いで、動物にOncoVexmGM−CSF(5×106PFU/投与量)の3回の腫瘍内注射、抗CTLA−4 mAbの4回の腹腔内注射、OncoVexmGM−CSF(5×106PFU/投与量)の3回の腫瘍内注射と抗CTLA−4 mAbの4回の腹腔内注射との組み合わせ又はビヒクル単独を施した。臨床徴候、体重変化及び生存期間(腫瘍が800mm3に達した場合、マウスを試験から除外した)を試験が終了するまで週に2〜3回測定した。
4T1腫瘍細胞を0日目において雌BALB/cマウスの右脇腹に皮下注射した(2×106個細胞)。腫瘍体積(mm3)を、電子ノギスを用いて週に2回(Q2W)測定した。腫瘍が平均でおよそ100mm3に達したら、動物を、処置施行の開始時の平均腫瘍体積及び腫瘍体積のばらつきが処置群全体に均一であるように4つの群に無作為化した(1群当たり10匹のマウス)。次いで、動物にOncoVexmGM−CSF(5×104、5×105又は5×106PFU/投与量)又はビヒクルの3回の腫瘍内注射を施した。臨床徴候、体重変化及び生存期間(腫瘍が800mm3に達した場合、マウスを試験から除外した)を試験が終了するまで週に2〜3回測定した。
A20腫瘍細胞を0日目において雌BALB/cマウスの右及び左脇腹に皮下注射した(2×106個細胞)。腫瘍体積(mm3)を、電子ノギスを用いて週に2回(Q2W)測定した。腫瘍が平均でおよそ100mm3に達したら、動物を、処置施行の開始時の平均腫瘍体積(両脇腹における)及び腫瘍体積のばらつきが処置群全体に均一であるように4つの群に無作為化した(1群当たり10匹のマウス)。次いで、動物にOncoVexmGM−CSF又はOncoVexmGM−CSFと抗GITR mAbとの組み合わせを投与した。臨床徴候、体重変化及び生存期間(腫瘍が800mm3に達した場合、マウスを試験から除外した)を試験が終了するまで週に2〜3回測定した。
この試験は、マウスMC−38腫瘍モデルにおいて、OncoVexmuGM−CSF、抗PD−1阻害又はOncoVexmuGM−CSFと抗PD−1阻害との組み合わせの忍容性及び抗腫瘍活性を評価するように設計した。
この試験は、マウスMC−38腫瘍モデルにおいて、OncoVexmuGM−CSF、抗PD−L1阻害又はOncoVexmuGM−CSFと抗PD−L1阻害との組み合わせの忍容性及び抗腫瘍活性を評価するように設計した。
この試験は、マウスメラノーマ(B16F10)腫瘍モデルにおいて、OncoVexmuGM−CSF、抗PD−1阻害又はOncoVexmuGM−CSFと抗PD−1阻害との組み合わせの忍容性及び抗腫瘍活性を評価するように設計した。
この実施例は、直接注入しやすい進行性非中枢神経系腫瘍を有する小児対象においてタリモジーン・ラハーパレプベックの安全性及び有効性を評価するための第1相、多施設、オープンラベル、用量デエスカレーション試験の記述である。米国国立公衆衛生研究所ウェブサイト(clinicaltrials.gov)、試験識別子:NCT 02756845を参照されたい(これは、参照により本明細書に組み込まれる)。
・対象がインフォームドコンセント/アセントを提出するには法的にあまりにも若すぎる場合、対象の法的に認められる代理人がインフォームドコンセント/アセントを提出しており、対象には、いかなる試験に特定な活動/処置も開始される前に、条例及び/又はガイドラインに基づいて書かれたアセントが提供されていること。
・インフォームドコンセント/アセントの時点で男性又は女性の対象が0歳〜18歳未満であること。
・登録前28日以内に局所的HSV−1血清状態を提出する意思があるべきであること。
・標準的治療後に再発したか又は利用できる標準的治療がない、組織学的若しくは細胞学的に確認された非CNS固形腫瘍であること。
・測定可能な(irRC−RECISTにより定義された)又は修正irRC−RECISTによって定義されるような測定不能な病変が存在すること。
・以下の1つ以上として定義される病変内注射の候補である対象:
− 最長径≧10mmの少なくとも1つの注射可能な病変
− 全体として≧10mmの最長径を有する、複数の注射可能な病変
注記:内蔵病変は、注射対象外である。更に、注射が容易である軟組織成分がない限り、骨病変は、注射対象外である。
・パフォーマンスステータス:
− 12歳〜18歳未満について、カルノフスキーパフォーマンスステータスが≧70%であること
− 0歳〜12歳未満の子供について、ランスキープレースケールが≧70%であること
・平均余命が登録の日時から>4ヶ月であること
・以下のように定義される十分な臓器機能があること:
− 血液機能(造血成長因子を必要とすることなく)
好中球絶対数(ANC)が≧1.0×109/Lであること
血小板数が≧75×109/Lであること
ヘモグロビンが≧8g/dLのヘモグロビン(輸血支援なしに)であること
− 腎機能
血清クレアチニンが≦1.5×年齢の正常値上限(ULN)であるか、又は>1.5×年齢のULNのクレアチニンレベルを有する対象について、クレアチニンクリアランスが≧60mL/分/1.73m2であること(クレアチンクリアランスは、ベースライン血清クレアチニンが≦1.5×年齢のULNである場合、判定される必要がないことに留意されたい。クレアチニンクリアランスは、施設内規準に従って判定されるべきである)。
− 肝機能
血清ビリルビンが≦1.5×年齢のULNであるか、又は直接型ビリルビンが、>1.5×年齢のULNの総ビリルビンレベルを有する対象について≦年齢のULNであること
アスパラギン酸アミノトランスフェラーゼ(AST)が≦2.5×年齢のULNであるか、又は肝臓転移を有する対象について≦5×年齢のULNであること
アラニンアミノトランスフェラーゼ(ALT)が≦2.5×年齢のULNであるか、又は肝臓転移を有する対象について≦5×年齢のULNであること
− 凝固機能
国際標準比(INR)又はプロトロンビン時間(PT)が≦1.5×年齢のULNであること
部分トロンボプラスチン時間(PTT)又は活性化部分トロンボプラスチン時間(aPTT)が≦1.5×年齢のULNであること
・投与前72時間以内に尿又は血清妊娠検査が陰性でなければならない妊娠が可能な女性対象。尿検査が陽性であるか又は陰性と確認できない場合、血清妊娠検査が必要となる。
・白血病、非ホジキンリンパ腫、ホジキン病又は他の血液悪性腫瘍と診断されていること
・登録前6週間以内又は頭蓋脊髄軸若しくは骨盤の少なくとも60%への事前放射を受けている場合には登録前3ヶ月以内、局所緩和放射線療法を受けている場合には登録の2週間前以内に骨髄への放射線療法を受けていること
・CNS腫瘍又は臨床的に活動性の脳転移があること
・原発性眼内メラノーマ又は粘膜メラノーマがあること
・巨大先天性色素細胞性母斑、異形成母斑症候群又は色素性乾皮症の病歴又は証拠があること
・以下の例外を除いて、過去5年以内に他の悪性腫瘍の病歴があること:
− 治療目的で処置された悪性腫瘍であり、既知の活動性疾患を有さず、登録前>5年間化学療法を受けておらず、治療医が再発のリスクが低いと感じている悪性腫瘍
・全身治療(すなわち疾患修飾剤、コルチコステロイド又は免疫抑制薬を使用しての)を必要とする活動性自己免疫疾患の病歴又は証拠があること。補充療法(例えば、チロキシン、インスリン又は副腎若しくは下垂体機能不全のための生理学的コルチコステロイド補充療法など)は、全身治療の形態とみなされない。
・以下のような臨床的に意味がある免疫抑制があること:
− 重度複合免疫不全症などの原発性免疫不全症
− 同時日和見感染
− 経口ステロイド投与を含む全身免疫抑制療法を受けていること(登録の>2週間前)(維持的な生理学的補充療法を除外する)。吸入のためのステロイドの不連続使用又は局所ステロイド注射を必要とする対象は、本試験から除外されない。
・活動性のヘルペス性皮膚病変があること、又は以前にヘルペス感染症の合併症(例えば、ヘルペス性角膜炎若しくはヘルペス性脳炎)があること
・タリモジーン・ラハーパレプベック又は任意の他の腫瘍溶解性ウイルスによる処置を以前に受けていること
・腫瘍ワクチンによる処置を以前に受けていること
・不連続的な局所使用以外の、抗ヘルペス薬(例えば、アシクロビル)による不連続的又は慢性的処置の必要性があること
・登録前28日以内に化学療法、放射線療法若しくは生物学的がん療法を以前に受けているか、又は登録前28日を超えて施されたがん療法に起因する有害事象から有害事象共通用語規準(CTCAE)のグレード1以上まで回復していないこと
・別の治験用医療機器若しくは薬物における処置を現在受けているか、又は別の治験用医療機器若しくは薬物での処置終了から28日未満であること。本試験に参加しながら他の治験処置を受けることは除外される。
・登録前≦28日に大手術を受けていること
・本試験中、局所緩和放射線治療を除いて他のがん療法を必要とすることが予想されること
・急性若しくは慢性の活動性B型肝炎ウイルス若しくはC型肝炎ウイルス感染症を有するか、又は試験処置の開始から12週間以内において、B型肝炎ウイルスの処置で使用されるもの(例えば、ラミブジン、アデホビル、テノホビル、テルビブジン及びエンテカビル)、リバビリン若しくはインターフェロンアルファなどのヌクレオチド類似体での処置を受けていること
・ヒト免疫不全ウイルス(HIV)感染症が既知であるか又はそれが疑われること
・登録前28日以内に生ワクチンを受けていること
・静脈カテーテルの開通性を維持するために必要な低用量ヘパリンを除く、タリモジーン・ラハーパレプベックの注入前7日以内に許可された抗血小板薬又は抗凝固薬がないこと
・試験処置中及びタリモジーン・ラハーパレプベックの最後の投与後3か月間を通して、女性対象が妊娠若しくは授乳しているか又は妊娠することを計画していること
・試験処置中及びタリモジーン・ラハーパレプベックの最後の投与後3か月間を通して、有効な避妊の承諾可能な方法の使用を望んでいない妊娠可能な女性対象であること。注記:有効な避妊の承諾可能な方法は、インフォームドコンセント/アセントフォームで規定されている。条例及び規制で義務付けられている場合、追加の国で規定された避妊要件は、プロトコルの付録セクションの最後にある国で規定されたプロトコル捕足で概説されている。
・処置中及びタリモジーン・ラハーパレプベックによる処置後30日以内の性的接触時、ウイルス伝播を回避するための男性用又は女性用ラテックスコンドームの使用を望まない性的に活発な対象及びそのパートナー
・投薬中、投与される製剤又は構成成分のいずれかに感受性であることが知られている対象
・全てのプロトコルで要求される試験時の来院若しくは処置を完了することができず、且つ/又は全ての要求される試験手順を、対象及び治験医師が知っている限りで遵守することができない可能性が高い対象
・相談にあずかる場合、治験医師又はAmgenの医師の意見では、対象の安全性に危険を及ぼすか、又は試験評価、処置若しくは完了を妨害すると思われる任意の精神障害、薬物乱用又は任意の他の臨床的に意味のある障害、状態若しくは疾患(上記に概説されたものを除く)の病歴又は証拠があること
・タリモジーン・ラハーパレプベック処置中及びタリモジーン・ラハーパレプベックの最後の投与後28日間を通して、対象の血液又は体液を、HIV−1誘発性合併症のリスクがより高い個体(免疫抑制個体、HIV陽性個体、妊娠女性又は1歳以下の乳児)への暴露を最小限に抑えることを望まない対象
・骨の肉腫:ユーイング肉腫及び骨肉腫
・軟部肉腫:横紋筋肉腫及び非横紋筋肉腫軟部肉腫
・神経芽細胞腫
・メラノーマ
1.前回の注射以降に出現した任意の新たな注入可能な腫瘍
2.腫瘍サイズによって最大の腫瘍から開始する
3.現在では注入するのに十分に大きくなった、腫瘍評価時に注入するには小さすぎた以前に見られた任意の腫瘍
Claims (16)
- 治療有効量の腫瘍溶解性ウイルスを投与することにより、ユーイング肉腫、神経芽細胞腫、横紋筋肉腫様腫瘍、骨肉腫、横紋筋肉腫、B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、非小細胞肺癌、結腸直腸癌、メラノーマ、頭頸部扁平上皮癌、肝細胞癌、胃癌、乳がん(例えば、トリプルネガティブ乳癌)、皮膚T細胞性リンパ腫又は多発性骨髄腫を治療する方法。
- 前記腫瘍溶解性ウイルスは、単純ヘルペスウイルスである、請求項1に記載の方法。
- 前記腫瘍溶解性ウイルスは、タリモジーン・ラハーパレプベックである、請求項1又は2に記載の方法。
- (i)治療有効量の腫瘍溶解性ウイルスと、
(ii)治療有効量のチェックポイント阻害剤と
を投与することにより、B細胞性リンパ腫、結腸直腸がん、頭頸部扁平上皮癌又は乳がん(例えば、トリプルネガティブ乳癌)を治療する方法。 - 前記チェックポイント阻害剤は、CTLA−4、PD−L1又はPD−L1ブロッカーである、請求項4に記載の方法。
- 前記腫瘍溶解性ウイルスは、単純ヘルペスウイルスである、請求項4又は5に記載の方法。
- 前記単純ヘルペスウイルスは、タリモジーン・ラハーパレプベックである、請求項6に記載の方法。
- ユーイング肉腫、神経芽細胞腫、横紋筋肉腫様腫瘍、骨肉腫、横紋筋肉腫、B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、非小細胞肺癌、結腸直腸癌、頭頸部扁平上皮癌、肝細胞癌、胃癌、乳がん(例えば、トリプルネガティブ乳癌)、皮膚T細胞性リンパ腫又は多発性骨髄腫の治療において使用するための治療有効量の腫瘍溶解性ウイルス。
- ユーイング肉腫、神経芽細胞腫、横紋筋肉腫様腫瘍、骨肉腫、横紋筋肉腫、B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、非小細胞肺癌、結腸直腸癌、頭頸部扁平上皮癌、肝細胞癌、胃癌、乳がん(例えば、トリプルネガティブ乳癌)、皮膚T細胞性リンパ腫又は多発性骨髄腫を治療する方法で使用するための医薬組成物であって、腫瘍溶解性ウイルスを含む医薬組成物。
- 単純ヘルペスウイルスである、請求項8又は9に記載の腫瘍溶解性ウイルス。
- 前記単純ヘルペスウイルスは、タリモジーン・ラハーパレプベックである、請求項10に記載の腫瘍溶解性ウイルス。
- B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、結腸直腸がん、頭頸部扁平上皮癌又は乳がん(例えば、トリプルネガティブ乳癌)の治療で使用するための治療有効量の腫瘍溶解性ウイルス及びチェックポイント阻害剤。
- B細胞性リンパ腫(例えば、びまん性大細胞型B細胞性リンパ腫)、結腸直腸がん、頭頸部扁平上皮癌又は乳がん(例えば、トリプルネガティブ乳癌)を治療する方法において使用するための医薬組成物であって、治療有効量の腫瘍溶解性ウイルス及びチェックポイント阻害剤を含む医薬組成物。
- CTLA−4、PD−1又はPD−L1ブロッカーである、請求項12又は13に記載のチェックポイント阻害剤。
- 単純ヘルペスウイルスである、請求項13又は14に記載の腫瘍溶解性ウイルス。
- 前記単純ヘルペスウイルスは、タリモジーン・ラハーパレプベックである、請求項15に記載の腫瘍溶解性ウイルス。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023066170A JP2023089171A (ja) | 2017-03-15 | 2023-04-14 | がんを治療するための、腫瘍溶解性ウイルスの単独又はチェックポイント阻害剤との組み合わせでの使用 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762471875P | 2017-03-15 | 2017-03-15 | |
| US62/471,875 | 2017-03-15 | ||
| PCT/US2018/022442 WO2018170133A1 (en) | 2017-03-15 | 2018-03-14 | Use of oncolytic viruses, alone or in combination with a checkpoint inhibitor, for the treatment of cancer |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023066170A Division JP2023089171A (ja) | 2017-03-15 | 2023-04-14 | がんを治療するための、腫瘍溶解性ウイルスの単独又はチェックポイント阻害剤との組み合わせでの使用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2020510050A true JP2020510050A (ja) | 2020-04-02 |
| JP2020510050A5 JP2020510050A5 (ja) | 2021-04-22 |
Family
ID=61913527
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019549569A Pending JP2020510050A (ja) | 2017-03-15 | 2018-03-14 | がんを治療するための、腫瘍溶解性ウイルスの単独又はチェックポイント阻害剤との組み合わせでの使用 |
| JP2023066170A Pending JP2023089171A (ja) | 2017-03-15 | 2023-04-14 | がんを治療するための、腫瘍溶解性ウイルスの単独又はチェックポイント阻害剤との組み合わせでの使用 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023066170A Pending JP2023089171A (ja) | 2017-03-15 | 2023-04-14 | がんを治療するための、腫瘍溶解性ウイルスの単独又はチェックポイント阻害剤との組み合わせでの使用 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20200009204A1 (ja) |
| EP (1) | EP3595690A1 (ja) |
| JP (2) | JP2020510050A (ja) |
| CN (1) | CN110461346A (ja) |
| AU (2) | AU2018235944B2 (ja) |
| CA (1) | CA3056392A1 (ja) |
| MA (1) | MA51630A (ja) |
| MX (1) | MX2019010797A (ja) |
| WO (1) | WO2018170133A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN114984062A (zh) * | 2012-08-30 | 2022-09-02 | 安姆根有限公司 | 使用单纯疱疹病毒和免疫检查点抑制剂治疗黑色素瘤的方法 |
| JP2020530003A (ja) * | 2017-08-07 | 2020-10-15 | アムジェン インコーポレイテッド | 抗pd−l1抗体及び腫瘍溶解性ウイルスでの、肝転移を伴う三種陰性乳がん又は結腸直腸がんの処置 |
| CN110833622A (zh) * | 2018-08-17 | 2020-02-25 | 北京奥源和力生物技术有限公司 | 用于治疗癌症的组合及其治疗用途 |
| CN116802278A (zh) * | 2020-09-18 | 2023-09-22 | 成都美杰赛尔生物科技有限公司 | 溶瘤病毒与经改造的免疫细胞联合治疗肿瘤 |
| CA3207359A1 (en) | 2021-02-05 | 2022-08-11 | Cecile Chartier-Courtaud | Adjuvant therapy for cancer |
| EP4332218A1 (en) * | 2021-06-03 | 2024-03-06 | Shanghai Yunying Biopharmaceutical Technology Co., Ltd. | Oncolytic virus vector and use thereof |
| TW202321458A (zh) * | 2021-09-22 | 2023-06-01 | 瑞典商生物創新國際公司 | 新穎抗體組合及其用途 |
| CN115463161A (zh) * | 2022-09-15 | 2022-12-13 | 广东天普生化医药股份有限公司 | 一种溶瘤病毒在制备治疗骨肉瘤的药物组合物中的应用 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015526525A (ja) * | 2012-08-30 | 2015-09-10 | アムジエン・インコーポレーテツド | 単純ヘルペスウイルスおよび免疫チェックポイント阻害薬を使用して、メラノーマを治療するための方法 |
| WO2016009017A1 (en) * | 2014-07-16 | 2016-01-21 | Institut Gustave-Roussy | Combination of oncolytic virus with immune checkpoint modulators |
| WO2017013419A1 (en) * | 2015-07-20 | 2017-01-26 | Virttu Biologics Limited | Use of oncolytic herpes simplex virus, alone or in combination with immune checkpoint inhibitor, in the treatment of cancer |
Family Cites Families (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6770274B1 (en) | 1990-09-14 | 2004-08-03 | The General Hospital Corporation | Viral mutant HSV mediated destruction of neoplastic cells |
| US5728379A (en) | 1994-06-23 | 1998-03-17 | Georgetown University | Tumor- or cell-specific herpes simplex virus replication |
| US6699468B1 (en) | 1994-06-23 | 2004-03-02 | Georgetown University | Replication-competent herpes simplex virus mediates destruction of neoplastic cells |
| US5585096A (en) | 1994-06-23 | 1996-12-17 | Georgetown University | Replication-competent herpes simplex virus mediates destruction of neoplastic cells |
| US6051227A (en) | 1995-07-25 | 2000-04-18 | The Regents Of The University Of California, Office Of Technology Transfer | Blockade of T lymphocyte down-regulation associated with CTLA-4 signaling |
| US5855887A (en) | 1995-07-25 | 1999-01-05 | The Regents Of The University Of California | Blockade of lymphocyte down-regulation associated with CTLA-4 signaling |
| US5811097A (en) | 1995-07-25 | 1998-09-22 | The Regents Of The University Of California | Blockade of T lymphocyte down-regulation associated with CTLA-4 signaling |
| US6207157B1 (en) | 1996-04-23 | 2001-03-27 | The United States Of America As Represented By The Department Of Health And Human Services | Conjugate vaccine for nontypeable Haemophilus influenzae |
| US5824318A (en) | 1996-07-24 | 1998-10-20 | American Cyanamid Company | Avirulent herpetic viruses useful as tumoricidal agents and vaccines |
| US6379674B1 (en) | 1997-08-12 | 2002-04-30 | Georgetown University | Use of herpes vectors for tumor therapy |
| US6682736B1 (en) | 1998-12-23 | 2004-01-27 | Abgenix, Inc. | Human monoclonal antibodies to CTLA-4 |
| WO2000040734A1 (en) | 1998-12-31 | 2000-07-13 | Arch Development Corporation | Recombinant herpes simplex virus useful for treating neoplastic disease |
| AU2905199A (en) | 1999-03-15 | 2000-10-04 | Trustees Of The University Of Pennsylvania, The | Combined therapy with a chemotherapeutic agent and an oncolytic virus for killing tumor cells in a subject |
| US6764675B1 (en) | 1999-06-08 | 2004-07-20 | The Uab Research Foundation | Herpes simplex virus expressing foreign genes and method for treating cancers therewith |
| US7605238B2 (en) | 1999-08-24 | 2009-10-20 | Medarex, Inc. | Human CTLA-4 antibodies and their uses |
| WO2001014424A2 (en) | 1999-08-24 | 2001-03-01 | Medarex, Inc. | Human ctla-4 antibodies and their uses |
| ATE282708T1 (de) | 2000-01-21 | 2004-12-15 | Biovex Ltd | Herpes-virusstämme für die gentherapie |
| CN1286303A (zh) | 2000-08-17 | 2001-03-07 | 上海市农业科学院生物技术研究中心 | 抗人龋齿致病菌蛋白基因及其制备方法 |
| AU2002306919B2 (en) | 2001-03-27 | 2007-11-22 | Tomoki Todo | Viral vectors and their use in therapeutic methods |
| WO2003042402A2 (en) | 2001-11-13 | 2003-05-22 | Dana-Farber Cancer Institute, Inc. | Agents that modulate immune cell activation and methods of use thereof |
| CN1753912B (zh) | 2002-12-23 | 2011-11-02 | 惠氏公司 | 抗pd-1抗体及其用途 |
| US7731952B2 (en) | 2004-06-24 | 2010-06-08 | New York University | Avirulent oncolytic herpes simplex virus strains engineered to counter the innate host response |
| CN105315373B (zh) | 2005-05-09 | 2018-11-09 | 小野药品工业株式会社 | 程序性死亡-1(pd-1)的人单克隆抗体及使用抗pd-1抗体来治疗癌症的方法 |
| KR101607288B1 (ko) | 2005-07-01 | 2016-04-05 | 이. 알. 스퀴부 앤드 선즈, 엘.엘.씨. | 예정 사멸 리간드 1 (피디-엘1)에 대한 인간 모노클로날 항체 |
| CN101230334B (zh) | 2007-01-22 | 2011-06-01 | 北京奥源和力生物技术有限公司 | 单纯疱疹病毒和重组病毒及宿主细胞及其药物组合物 |
| CN101230335B (zh) | 2007-01-22 | 2010-08-11 | 北京奥源和力生物技术有限公司 | 单纯疱疹病毒和重组病毒及宿主细胞及其药物组合物 |
| KR101562580B1 (ko) | 2007-06-18 | 2015-10-22 | 머크 샤프 앤 도메 비.브이. | 사람 프로그램된 사멸 수용체 pd-1에 대한 항체 |
| WO2009114335A2 (en) | 2008-03-12 | 2009-09-17 | Merck & Co., Inc. | Pd-1 binding proteins |
| US8552154B2 (en) | 2008-09-26 | 2013-10-08 | Emory University | Anti-PD-L1 antibodies and uses therefor |
| SG196798A1 (en) | 2008-12-09 | 2014-02-13 | Genentech Inc | Anti-pd-l1 antibodies and their use to enhance t-cell function |
| EP3192811A1 (en) | 2009-02-09 | 2017-07-19 | Université d'Aix-Marseille | Pd-1 antibodies and pd-l1 antibodies and uses thereof |
| EP2504028A4 (en) | 2009-11-24 | 2014-04-09 | Amplimmune Inc | SIMULTANEOUS INHIBITION OF PD-L1 / PD-L2 |
| WO2011082400A2 (en) | 2010-01-04 | 2011-07-07 | President And Fellows Of Harvard College | Modulators of immunoinhibitory receptor pd-1, and methods of use thereof |
| WO2011159877A2 (en) | 2010-06-18 | 2011-12-22 | The Brigham And Women's Hospital, Inc. | Bi-specific antibodies against tim-3 and pd-1 for immunotherapy in chronic immune conditions |
| US8907053B2 (en) | 2010-06-25 | 2014-12-09 | Aurigene Discovery Technologies Limited | Immunosuppression modulating compounds |
| DK2753355T3 (en) | 2011-09-08 | 2019-01-28 | Univ New York | ONCOLYTIC HERP SIMPLEX VIRUSES AND THERAPEUTIC APPLICATIONS THEREOF |
| TW201605896A (zh) | 2013-08-30 | 2016-02-16 | 安美基股份有限公司 | Gitr抗原結合蛋白 |
| WO2017120670A1 (en) * | 2016-01-11 | 2017-07-20 | Brian Lichty | Oncolytic virus and checkpoint inhibitor combination therapy |
| WO2017156349A1 (en) * | 2016-03-10 | 2017-09-14 | Cold Genesys, Inc. | Methods of treating solid or lymphatic tumors by combination therapy |
| EP3225253A1 (en) * | 2016-04-01 | 2017-10-04 | Deutsches Krebsforschungszentrum Stiftung des Öffentlichen Rechts | Cancer therapy with an oncolytic virus combined with a checkpoint inhibitor |
-
2018
- 2018-03-14 AU AU2018235944A patent/AU2018235944B2/en active Active
- 2018-03-14 CA CA3056392A patent/CA3056392A1/en active Pending
- 2018-03-14 CN CN201880017970.9A patent/CN110461346A/zh active Pending
- 2018-03-14 WO PCT/US2018/022442 patent/WO2018170133A1/en unknown
- 2018-03-14 MX MX2019010797A patent/MX2019010797A/es unknown
- 2018-03-14 MA MA051630A patent/MA51630A/fr unknown
- 2018-03-14 JP JP2019549569A patent/JP2020510050A/ja active Pending
- 2018-03-14 US US16/493,376 patent/US20200009204A1/en active Pending
- 2018-03-14 EP EP18716700.2A patent/EP3595690A1/en active Pending
-
2023
- 2023-04-14 JP JP2023066170A patent/JP2023089171A/ja active Pending
-
2024
- 2024-04-02 AU AU2024202086A patent/AU2024202086A1/en active Pending
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015526525A (ja) * | 2012-08-30 | 2015-09-10 | アムジエン・インコーポレーテツド | 単純ヘルペスウイルスおよび免疫チェックポイント阻害薬を使用して、メラノーマを治療するための方法 |
| WO2016009017A1 (en) * | 2014-07-16 | 2016-01-21 | Institut Gustave-Roussy | Combination of oncolytic virus with immune checkpoint modulators |
| WO2017013419A1 (en) * | 2015-07-20 | 2017-01-26 | Virttu Biologics Limited | Use of oncolytic herpes simplex virus, alone or in combination with immune checkpoint inhibitor, in the treatment of cancer |
Non-Patent Citations (6)
| Title |
|---|
| ANN. SURG. ONCOL., 2010, VOL.17, PP.718-730, JPN6022011189, ISSN: 0004947414 * |
| CANCER RES., 2015, VOL.75, 15_SUPPL., ABSTRACT NO.258, JPN6022011190, ISSN: 0004737239 * |
| CANCER SCI., 2016, VOL.107, PP.1373-1379, JPN6022011188, ISSN: 0004947415 * |
| CLINICALTRIALS.GOV., "STUDY OF TALIMOGENE LAHERPAREPVEC IN CHILDREN WITH ADVANCED NON CNS TUMORS", 2, JPN6022011187, ISSN: 0004947416 * |
| GENE THERAPY, 2003, VOL.10, PP.292-303, JPN6022011185, ISSN: 0004737243 * |
| MOLECULAR THERAPY, 2013, VOL.21, NO.5, PP.1014-1023, JPN6022011193, ISSN: 0004737238 * |
Also Published As
| Publication number | Publication date |
|---|---|
| MA51630A (fr) | 2020-01-22 |
| CN110461346A (zh) | 2019-11-15 |
| US20200009204A1 (en) | 2020-01-09 |
| WO2018170133A1 (en) | 2018-09-20 |
| MX2019010797A (es) | 2019-10-24 |
| AU2018235944A1 (en) | 2019-09-26 |
| EP3595690A1 (en) | 2020-01-22 |
| AU2024202086A1 (en) | 2024-04-18 |
| AU2018235944B2 (en) | 2024-01-04 |
| JP2023089171A (ja) | 2023-06-27 |
| CA3056392A1 (en) | 2018-09-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2018235944B2 (en) | Use of oncolytic viruses, alone or in combination with a checkpoint inhibitor, for the treatment of cancer | |
| US20210169955A1 (en) | Use of Oncolytic Herpes Simplex Virus, Alone or in Combination with Immune Check-Point Inhibitor, in the Treatment of Cancer | |
| JP6656349B2 (ja) | 単純ヘルペスウイルスおよび免疫チェックポイント阻害薬を使用して、メラノーマを治療するための方法 | |
| JP6954648B2 (ja) | 併用療法による固形腫瘍又はリンパ系腫瘍の治療方法 | |
| RU2702332C2 (ru) | Антитела к в7-н1 и к ctla-4 для лечения немелкоклеточного рака легкого | |
| EP3242678B1 (en) | Combined preparations for the treatment of cancer or infection | |
| TW202102543A (zh) | 溶瘤病毒在癌症新輔助療法中之用途 | |
| US20140205609A1 (en) | Methods for inducing systemic immune responses to cancer | |
| TWI817958B (zh) | 用於治療肝癌之組合物及方法 | |
| TW202100542A (zh) | 溶瘤病毒用於治療癌症之用途 | |
| RU2802962C2 (ru) | Композиции и способы лечения рака печени | |
| WO2022048574A1 (zh) | 一种编码Kras基因突变体的核酸分子 | |
| US20230279132A1 (en) | Treatment of b cell malignancies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210312 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210312 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220329 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220623 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220926 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20221220 |