JP2017200959A - Composition for oral quickly-disintegrating tablets - Google Patents
Composition for oral quickly-disintegrating tablets Download PDFInfo
- Publication number
- JP2017200959A JP2017200959A JP2017159294A JP2017159294A JP2017200959A JP 2017200959 A JP2017200959 A JP 2017200959A JP 2017159294 A JP2017159294 A JP 2017159294A JP 2017159294 A JP2017159294 A JP 2017159294A JP 2017200959 A JP2017200959 A JP 2017200959A
- Authority
- JP
- Japan
- Prior art keywords
- composition
- tablet
- disintegrating tablet
- rapidly disintegrating
- intraoral
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 59
- TUSDEZXZIZRFGC-UHFFFAOYSA-N 1-O-galloyl-3,6-(R)-HHDP-beta-D-glucose Natural products OC1C(O2)COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC1C(O)C2OC(=O)C1=CC(O)=C(O)C(O)=C1 TUSDEZXZIZRFGC-UHFFFAOYSA-N 0.000 claims abstract description 41
- 239000001263 FEMA 3042 Substances 0.000 claims abstract description 41
- LRBQNJMCXXYXIU-PPKXGCFTSA-N Penta-digallate-beta-D-glucose Natural products OC1=C(O)C(O)=CC(C(=O)OC=2C(=C(O)C=C(C=2)C(=O)OC[C@@H]2[C@H]([C@H](OC(=O)C=3C=C(OC(=O)C=4C=C(O)C(O)=C(O)C=4)C(O)=C(O)C=3)[C@@H](OC(=O)C=3C=C(OC(=O)C=4C=C(O)C(O)=C(O)C=4)C(O)=C(O)C=3)[C@H](OC(=O)C=3C=C(OC(=O)C=4C=C(O)C(O)=C(O)C=4)C(O)=C(O)C=3)O2)OC(=O)C=2C=C(OC(=O)C=3C=C(O)C(O)=C(O)C=3)C(O)=C(O)C=2)O)=C1 LRBQNJMCXXYXIU-PPKXGCFTSA-N 0.000 claims abstract description 41
- LRBQNJMCXXYXIU-NRMVVENXSA-N tannic acid Chemical compound OC1=C(O)C(O)=CC(C(=O)OC=2C(=C(O)C=C(C=2)C(=O)OC[C@@H]2[C@H]([C@H](OC(=O)C=3C=C(OC(=O)C=4C=C(O)C(O)=C(O)C=4)C(O)=C(O)C=3)[C@@H](OC(=O)C=3C=C(OC(=O)C=4C=C(O)C(O)=C(O)C=4)C(O)=C(O)C=3)[C@@H](OC(=O)C=3C=C(OC(=O)C=4C=C(O)C(O)=C(O)C=4)C(O)=C(O)C=3)O2)OC(=O)C=2C=C(OC(=O)C=3C=C(O)C(O)=C(O)C=3)C(O)=C(O)C=2)O)=C1 LRBQNJMCXXYXIU-NRMVVENXSA-N 0.000 claims abstract description 41
- 235000015523 tannic acid Nutrition 0.000 claims abstract description 41
- 229940033123 tannic acid Drugs 0.000 claims abstract description 41
- 229920002258 tannic acid Polymers 0.000 claims abstract description 41
- 210000000214 mouth Anatomy 0.000 claims abstract description 26
- 238000000034 method Methods 0.000 claims abstract description 24
- 239000000546 pharmaceutical excipient Substances 0.000 claims abstract description 16
- 150000005846 sugar alcohols Chemical class 0.000 claims abstract description 16
- 150000001720 carbohydrates Chemical class 0.000 claims abstract description 15
- 239000011230 binding agent Substances 0.000 claims description 18
- 239000007884 disintegrant Substances 0.000 claims description 11
- 229920002134 Carboxymethyl cellulose Polymers 0.000 claims description 8
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 claims description 8
- 229930195725 Mannitol Natural products 0.000 claims description 8
- VJHCJDRQFCCTHL-UHFFFAOYSA-N acetic acid 2,3,4,5,6-pentahydroxyhexanal Chemical compound CC(O)=O.OCC(O)C(O)C(O)C(O)C=O VJHCJDRQFCCTHL-UHFFFAOYSA-N 0.000 claims description 8
- 235000010948 carboxy methyl cellulose Nutrition 0.000 claims description 8
- 229950008138 carmellose Drugs 0.000 claims description 8
- 239000000594 mannitol Substances 0.000 claims description 8
- 235000010355 mannitol Nutrition 0.000 claims description 8
- 239000001913 cellulose Substances 0.000 claims description 7
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 claims description 6
- 229920002678 cellulose Polymers 0.000 claims description 6
- 235000010980 cellulose Nutrition 0.000 claims description 6
- 239000000843 powder Substances 0.000 claims description 6
- 235000012239 silicon dioxide Nutrition 0.000 claims description 6
- WSVLPVUVIUVCRA-KPKNDVKVSA-N Alpha-lactose monohydrate Chemical group O.O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O WSVLPVUVIUVCRA-KPKNDVKVSA-N 0.000 claims description 5
- YKTSYUJCYHOUJP-UHFFFAOYSA-N [O--].[Al+3].[Al+3].[O-][Si]([O-])([O-])[O-] Chemical compound [O--].[Al+3].[Al+3].[O-][Si]([O-])([O-])[O-] YKTSYUJCYHOUJP-UHFFFAOYSA-N 0.000 claims description 5
- WMGSQTMJHBYJMQ-UHFFFAOYSA-N aluminum;magnesium;silicate Chemical compound [Mg+2].[Al+3].[O-][Si]([O-])([O-])[O-] WMGSQTMJHBYJMQ-UHFFFAOYSA-N 0.000 claims description 5
- 239000000378 calcium silicate Substances 0.000 claims description 5
- 229910052918 calcium silicate Inorganic materials 0.000 claims description 5
- OYACROKNLOSFPA-UHFFFAOYSA-N calcium;dioxido(oxo)silane Chemical compound [Ca+2].[O-][Si]([O-])=O OYACROKNLOSFPA-UHFFFAOYSA-N 0.000 claims description 5
- 229940031703 low substituted hydroxypropyl cellulose Drugs 0.000 claims description 5
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 claims description 5
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 claims description 4
- 229920002785 Croscarmellose sodium Polymers 0.000 claims description 4
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 claims description 4
- 239000011575 calcium Substances 0.000 claims description 4
- 229910052791 calcium Inorganic materials 0.000 claims description 4
- 229960005069 calcium Drugs 0.000 claims description 4
- 235000001465 calcium Nutrition 0.000 claims description 4
- 229960001681 croscarmellose sodium Drugs 0.000 claims description 4
- 229960000913 crospovidone Drugs 0.000 claims description 4
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 claims description 4
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 claims description 4
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 claims description 4
- 239000003795 chemical substances by application Substances 0.000 claims description 3
- 239000007921 spray Substances 0.000 claims 1
- 238000004519 manufacturing process Methods 0.000 abstract description 19
- 239000002994 raw material Substances 0.000 abstract description 19
- 238000001035 drying Methods 0.000 abstract description 11
- 239000000463 material Substances 0.000 abstract description 7
- 238000002156 mixing Methods 0.000 abstract description 7
- 239000008187 granular material Substances 0.000 abstract description 6
- 239000003826 tablet Substances 0.000 description 97
- 239000000047 product Substances 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 14
- 235000019589 hardness Nutrition 0.000 description 12
- 238000005507 spraying Methods 0.000 description 12
- 238000005469 granulation Methods 0.000 description 10
- 230000003179 granulation Effects 0.000 description 10
- 239000000654 additive Substances 0.000 description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- 239000007916 tablet composition Substances 0.000 description 7
- 238000000748 compression moulding Methods 0.000 description 6
- 229920002472 Starch Polymers 0.000 description 5
- 239000004480 active ingredient Substances 0.000 description 5
- 239000006189 buccal tablet Substances 0.000 description 4
- 230000000052 comparative effect Effects 0.000 description 4
- 239000003814 drug Substances 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- 239000008186 active pharmaceutical agent Substances 0.000 description 3
- 230000000996 additive effect Effects 0.000 description 3
- 239000003086 colorant Substances 0.000 description 3
- 238000007906 compression Methods 0.000 description 3
- 230000006835 compression Effects 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 235000003599 food sweetener Nutrition 0.000 description 3
- 239000000314 lubricant Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 239000003765 sweetening agent Substances 0.000 description 3
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 2
- 229920000881 Modified starch Polymers 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 239000004372 Polyvinyl alcohol Substances 0.000 description 2
- 229920001218 Pullulan Polymers 0.000 description 2
- 239000004373 Pullulan Substances 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- SESFRYSPDFLNCH-UHFFFAOYSA-N benzyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1=CC=CC=C1 SESFRYSPDFLNCH-UHFFFAOYSA-N 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 239000010628 chamomile oil Substances 0.000 description 2
- 239000007910 chewable tablet Substances 0.000 description 2
- 239000000470 constituent Substances 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 229940099112 cornstarch Drugs 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- 239000003205 fragrance Substances 0.000 description 2
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical compound OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 description 2
- 229920000578 graft copolymer Polymers 0.000 description 2
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 2
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 2
- JEIPFZHSYJVQDO-UHFFFAOYSA-N iron(III) oxide Inorganic materials O=[Fe]O[Fe]=O JEIPFZHSYJVQDO-UHFFFAOYSA-N 0.000 description 2
- YOBAEOGBNPPUQV-UHFFFAOYSA-N iron;trihydrate Chemical compound O.O.O.[Fe].[Fe] YOBAEOGBNPPUQV-UHFFFAOYSA-N 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 229920001592 potato starch Polymers 0.000 description 2
- 229940116317 potato starch Drugs 0.000 description 2
- 229940069328 povidone Drugs 0.000 description 2
- 229920003124 powdered cellulose Polymers 0.000 description 2
- 235000019814 powdered cellulose Nutrition 0.000 description 2
- 235000019423 pullulan Nutrition 0.000 description 2
- 239000012264 purified product Substances 0.000 description 2
- 229940100486 rice starch Drugs 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 238000010998 test method Methods 0.000 description 2
- 229940100445 wheat starch Drugs 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- NOOLISFMXDJSKH-UTLUCORTSA-N (+)-Neomenthol Chemical compound CC(C)[C@@H]1CC[C@@H](C)C[C@@H]1O NOOLISFMXDJSKH-UTLUCORTSA-N 0.000 description 1
- SPFMQWBKVUQXJV-BTVCFUMJSA-N (2r,3s,4r,5r)-2,3,4,5,6-pentahydroxyhexanal;hydrate Chemical compound O.OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O SPFMQWBKVUQXJV-BTVCFUMJSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- SERLAGPUMNYUCK-DCUALPFSSA-N 1-O-alpha-D-glucopyranosyl-D-mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O SERLAGPUMNYUCK-DCUALPFSSA-N 0.000 description 1
- WBZFUFAFFUEMEI-UHFFFAOYSA-M Acesulfame k Chemical compound [K+].CC1=CC(=O)[N-]S(=O)(=O)O1 WBZFUFAFFUEMEI-UHFFFAOYSA-M 0.000 description 1
- 240000007185 Albizia julibrissin Species 0.000 description 1
- 235000011468 Albizia julibrissin Nutrition 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- CAQWNKXTMBFBGI-UHFFFAOYSA-N C.[Na] Chemical compound C.[Na] CAQWNKXTMBFBGI-UHFFFAOYSA-N 0.000 description 1
- 241001070941 Castanea Species 0.000 description 1
- 235000014036 Castanea Nutrition 0.000 description 1
- 240000003538 Chamaemelum nobile Species 0.000 description 1
- 235000007866 Chamaemelum nobile Nutrition 0.000 description 1
- YASYEJJMZJALEJ-UHFFFAOYSA-N Citric acid monohydrate Chemical compound O.OC(=O)CC(O)(C(O)=O)CC(O)=O YASYEJJMZJALEJ-UHFFFAOYSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- NOOLISFMXDJSKH-UHFFFAOYSA-N DL-menthol Natural products CC(C)C1CCC(C)CC1O NOOLISFMXDJSKH-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 235000011511 Diospyros Nutrition 0.000 description 1
- 244000236655 Diospyros kaki Species 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- BIVBRWYINDPWKA-VLQRKCJKSA-L Glycyrrhizinate dipotassium Chemical compound [K+].[K+].O([C@@H]1[C@@H](O)[C@H](O)[C@H](O[C@@H]1O[C@H]1CC[C@]2(C)[C@H]3C(=O)C=C4[C@@H]5C[C@](C)(CC[C@@]5(CC[C@@]4(C)[C@]3(C)CC[C@H]2C1(C)C)C)C(O)=O)C([O-])=O)[C@@H]1O[C@H](C([O-])=O)[C@@H](O)[C@H](O)[C@H]1O BIVBRWYINDPWKA-VLQRKCJKSA-L 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- 235000019501 Lemon oil Nutrition 0.000 description 1
- 235000006679 Mentha X verticillata Nutrition 0.000 description 1
- 235000002899 Mentha suaveolens Nutrition 0.000 description 1
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 1
- 235000019502 Orange oil Nutrition 0.000 description 1
- WINXNKPZLFISPD-UHFFFAOYSA-M Saccharin sodium Chemical compound [Na+].C1=CC=C2C(=O)[N-]S(=O)(=O)C2=C1 WINXNKPZLFISPD-UHFFFAOYSA-M 0.000 description 1
- 244000228451 Stevia rebaudiana Species 0.000 description 1
- 239000004376 Sucralose Substances 0.000 description 1
- 240000004584 Tamarindus indica Species 0.000 description 1
- 235000004298 Tamarindus indica Nutrition 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- 235000010358 acesulfame potassium Nutrition 0.000 description 1
- 229960004998 acesulfame potassium Drugs 0.000 description 1
- 239000000619 acesulfame-K Substances 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229960004977 anhydrous lactose Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 229960002903 benzyl benzoate Drugs 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 235000019480 chamomile oil Nutrition 0.000 description 1
- 239000010630 cinnamon oil Substances 0.000 description 1
- 239000001926 citrus aurantium l. subsp. bergamia wright et arn. oil Substances 0.000 description 1
- 239000010634 clove oil Substances 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 229940101029 dipotassium glycyrrhizinate Drugs 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- MVPICKVDHDWCJQ-UHFFFAOYSA-N ethyl 3-pyrrolidin-1-ylpropanoate Chemical compound CCOC(=O)CCN1CCCC1 MVPICKVDHDWCJQ-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 239000010642 eucalyptus oil Substances 0.000 description 1
- 229940044949 eucalyptus oil Drugs 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000010643 fennel seed oil Substances 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 239000000989 food dye Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 229940074391 gallic acid Drugs 0.000 description 1
- 235000004515 gallic acid Nutrition 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 239000000905 isomalt Substances 0.000 description 1
- 235000010439 isomalt Nutrition 0.000 description 1
- HPIGCVXMBGOWTF-UHFFFAOYSA-N isomaltol Natural products CC(=O)C=1OC=CC=1O HPIGCVXMBGOWTF-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000011031 large-scale manufacturing process Methods 0.000 description 1
- 239000000171 lavandula angustifolia l. flower oil Substances 0.000 description 1
- 239000010501 lemon oil Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 235000010449 maltitol Nutrition 0.000 description 1
- 239000000845 maltitol Substances 0.000 description 1
- VQHSOMBJVWLPSR-WUJBLJFYSA-N maltitol Chemical compound OC[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O VQHSOMBJVWLPSR-WUJBLJFYSA-N 0.000 description 1
- 229940035436 maltitol Drugs 0.000 description 1
- 229960001855 mannitol Drugs 0.000 description 1
- 239000001683 mentha spicata herb oil Substances 0.000 description 1
- 229940041616 menthol Drugs 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 239000010502 orange oil Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- HELXLJCILKEWJH-NCGAPWICSA-N rebaudioside A Chemical compound O([C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O[C@]12C(=C)C[C@@]3(C1)CC[C@@H]1[C@@](C)(CCC[C@]1([C@@H]3CC2)C)C(=O)O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O HELXLJCILKEWJH-NCGAPWICSA-N 0.000 description 1
- 235000019719 rose oil Nutrition 0.000 description 1
- 239000010666 rose oil Substances 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 238000007873 sieving Methods 0.000 description 1
- 125000005624 silicic acid group Chemical class 0.000 description 1
- 238000004513 sizing Methods 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 229940045902 sodium stearyl fumarate Drugs 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 235000019721 spearmint oil Nutrition 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 235000019408 sucralose Nutrition 0.000 description 1
- BAQAVOSOZGMPRM-QBMZZYIRSA-N sucralose Chemical compound O[C@@H]1[C@@H](O)[C@@H](Cl)[C@@H](CO)O[C@@H]1O[C@@]1(CCl)[C@@H](O)[C@H](O)[C@@H](CCl)O1 BAQAVOSOZGMPRM-QBMZZYIRSA-N 0.000 description 1
- -1 sucrose fatty acid ester Chemical class 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000000892 thaumatin Substances 0.000 description 1
- 235000010436 thaumatin Nutrition 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 238000009423 ventilation Methods 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
Abstract
Description
本発明は、口腔内の唾液又は少量の水の存在下において速やかにかつ良好に崩壊する口腔内速崩壊性錠剤用の造粒物、この造粒物を含む口腔内速崩壊性錠剤、及び口腔内速崩壊性錠剤の製造方法に関するものである。 The present invention relates to a granulated product for a rapidly disintegrating tablet in the oral cavity that rapidly and well disintegrates in the presence of saliva or a small amount of water in the oral cavity, an intraoral rapidly disintegrating tablet containing the granulated product, and an oral cavity The present invention relates to a method for producing an internally disintegrating tablet.
経口固形製剤の剤形としては、錠剤、カプセル剤、顆粒剤、散剤等が一般的に知られている。しかしながら、これらの剤形で取り扱い性が良く、かつ服用し易いものは少ない。例えば、錠剤及びカプセル剤は、その形状が大きくなるに従い飲み込み難くなるという問題があり、また、顆粒剤及び散剤は、服用時にむせるという問題や歯の間に入り込むという問題がある。更に、これらの剤形はいずれも服用時に水を必要とし、緊急時や、重症患者が寝ながらにして服用することは困難であるという問題もある。 As dosage forms of oral solid preparations, tablets, capsules, granules, powders and the like are generally known. However, few of these dosage forms are easy to handle and easy to take. For example, tablets and capsules have a problem that it becomes difficult to swallow as the shape thereof becomes larger, and granules and powders have a problem that they are peeled off when taken and a problem that they enter between teeth. Further, all of these dosage forms require water at the time of taking, and there is a problem that it is difficult to take while sleeping in an emergency or a serious patient.
水なしで服用できる剤形としては、錠剤を噛み砕いて服用するチュアブル錠が知られているが、現在提供されているものは崩壊性が悪く、高齢者、小児及び幼児の患者、嚥下困難な患者、寝たきりの患者等が服用することは困難であるという問題がある。 Chewable tablets that can be taken without water are known as chewable tablets that can be taken without water, but what is currently offered is poorly disintegrative and is elderly, pediatric and infant patients, patients who have difficulty swallowing There is a problem that it is difficult for a bedridden patient or the like to take.
従って、水なしでも容易に服用することができ、また手軽に何時、何処でも随時服用することのできる口腔内速崩壊性錠剤の開発が要望されている。 Accordingly, there is a demand for the development of an orally rapidly disintegrating tablet that can be easily taken without water and can be taken easily at any time and anywhere.
このような口腔内速崩壊性錠剤を製造する技術としては、薬物懸濁液をPTPの鋳型に精密充填し、低温通風乾燥する方法や(特許文献1)、薬剤、糖類、結合剤の混合物を少量の水或いは水とアルコール混液で湿潤し、この湿潤混合品(粉体)を極めて低い圧力で成形し、乾燥する方法(特許文献2)が知られている。
しかし、これらの方法は、特殊な製造設備を必要とし、また、それに伴い製造工程が複雑であるという問題がある。
As a technique for producing such an orally rapidly disintegrating tablet, a method of precisely filling a drug suspension into a PTP mold and drying at low temperature by ventilation (Patent Document 1), a mixture of a drug, a saccharide, and a binder is used. There is known a method (Patent Document 2) in which a small amount of water or a water / alcohol mixture is moistened, and this wet mixture (powder) is molded at an extremely low pressure and dried.
However, these methods have a problem that a special manufacturing facility is required and the manufacturing process is complicated accordingly.
そのため、簡単な製造設備を用いて簡単な工程で製造可能であり、かつ口腔内で優れた崩壊性を示すと共に実用上問題のない成型性を有する製剤の開発が望まれている。 Therefore, it is desired to develop a preparation that can be produced by a simple process using a simple production facility, has excellent disintegration properties in the oral cavity, and has moldability that is not problematic in practice.
従って、本発明は、簡単な製造装置を用いて簡単な工程で製造でき、且つ口腔内で速やかな崩壊性を有するとともに、実用に耐えうる適度な成型性を有する口腔内速崩壊性錠剤、その製造方法、及びこの口腔内速崩壊性錠剤の構成材料となる造粒物を提供することを課題とする。 Therefore, the present invention is an intraoral rapidly disintegrating tablet that can be manufactured in a simple process using a simple manufacturing apparatus and has a rapid disintegration property in the oral cavity and an appropriate moldability that can withstand practical use, It is an object of the present invention to provide a production method and a granulated product that is a constituent material of the intraoral rapidly disintegrating tablet.
本発明者らは、上記課題を解決するために鋭意検討した結果、糖類、及び糖アルコールからなる群より選ばれる少なくとも1種を含む賦形剤、及びタンニン酸を含む口腔内速崩壊性錠剤用組成物を調製するに当たり、溶解状態のタンニン酸を用いて各原料を混合し、乾燥することにより、錠剤用組成物を調製し、得られた錠剤用組成物を、必要に応じて、結合剤、及び/又は崩壊剤などと共に圧縮成型することにより、特殊な製造装置を使用することなく簡単な工程で、従来の口腔内速崩壊性錠剤と同等又はそれ以上の崩壊性と成型性とを兼ね備えた口腔内速崩壊性錠剤が製造できることを見出した。 As a result of intensive studies to solve the above-described problems, the present inventors have found that the present invention includes an excipient containing at least one selected from the group consisting of saccharides and sugar alcohols, and an intraoral rapidly disintegrating tablet containing tannic acid. In preparing the composition, each raw material is mixed using dissolved tannic acid and dried to prepare a tablet composition, and the obtained tablet composition is combined with a binder as necessary. , And / or compression molding together with disintegrants, etc., with a disintegration and moldability equivalent to or higher than conventional intraoral quick disintegrating tablets in a simple process without using a special manufacturing device It was found that an intraoral rapidly disintegrating tablet can be produced.
本発明は、上記知見に基づき完成されたものであり、下記の口腔内速崩壊性錠剤用組成物、口腔内速崩壊性錠剤、及び口腔内速崩壊性錠剤の製造方法を提供する。
項1. 糖類、及び糖アルコール類からなる群より選ばれる少なくとも1種の賦形剤、並びにタンニン酸を含む口腔内速崩壊性錠剤用組成物であって、溶解状態のタンニン酸を用いて各原料を混合し、乾燥することにより得られる、口腔内速崩壊性錠剤用組成物。
項2. 溶解状態のタンニン酸を、口腔内速崩壊性錠剤用組成物のその他の原料に噴霧することにより混合し、乾燥することにより得られる項1に記載の口腔内速崩壊性錠剤用組成物。
項3. 糖類、及び糖アルコール類からなる群より選ばれる少なくとも1種の賦形剤を含む口腔内速崩壊性錠剤用組成物原料に、溶解状態のタンニン酸を噴霧しながら、造粒操作を行う項2に記載の口腔内速崩壊性錠剤用組成物。
項4. 糖類が乳糖水和物であり、糖アルコール類がマンニトールである項1〜3の何れかに記載の口腔内速崩壊性錠剤用組成物。
項5. 項1〜4の何れかに記載の口腔内速崩壊性錠剤用組成物を含む口腔内速崩壊性錠剤。
項6. さらに、結合剤、及び/又は崩壊剤を含有する項5に記載の口腔内速崩壊性錠剤。
項7. 結合剤が、メタケイ酸アルミン酸マグネシウム、合成ケイ酸アルミニウム、軽質無水ケイ酸、ケイ酸カルシウム、及び結晶セルロースからなる群より選ばれる少なくとも1種である項6に記載の口腔内速崩壊性錠剤。
項8. 崩壊剤が、クロスポビドン、カルメロースカルシウム、カルメロース、クロスカルメロースナトリウム、及び低置換度ヒドロキシプロピルセルロースからなる群より選ばれる少なくとも1種である項6又は7に記載の口腔内速崩壊性錠剤。
項9. 日本薬局方に規定される崩壊試験により測定される崩壊時間が30秒以内である項5〜8の何れかに記載の口腔内速崩壊性錠剤。
項10. 硬度が40N以上である項5〜9の何れかに記載の口腔内速崩壊性錠剤。
項11. 糖類、及び糖アルコール類からなる群より選ばれる少なくとも1種の賦形剤、並びにタンニン酸を含む口腔内速崩壊性錠剤用組成物の製造方法であって、溶解状態のタンニン酸を用いて各原料を混合する第1工程と、得られた混合物を乾燥する第2工程とを含む、口腔内速崩壊性錠剤用組成物の製造方法。
項12. 第1工程において、溶解状態のタンニン酸を、口腔内速崩壊性錠剤用組成物のその他の原料に噴霧することにより混合する項11に記載の、口腔内速崩壊性錠剤用組成物の製造方法。
項13. 第1工程において、溶解状態のタンニン酸を、口腔内速崩壊性錠剤用組成物のその他の原料に噴霧しながら、造粒操作を行う項12に記載の方法。
項14. 糖類が乳糖水和物であり、糖アルコール類がマンニトールである項12又は13に記載の方法。
項15. 糖類、及び糖アルコール類からなる群より選ばれる少なくとも1種の賦形剤、並びにタンニン酸を含む原料を、溶解状態のタンニン酸を用いて混合する第1工程と、得られた混合物を乾燥して口腔内速崩壊性錠剤用組成物を得る第2工程と、この口腔内速崩壊性錠剤用組成物を圧縮成型するか、又はこの口腔内速崩壊性錠剤用組成物、並びに添加剤、及び/若しくは医薬有効成分の混合物を圧縮成型する第3工程とを含む、口腔内速崩壊性錠剤の製造方法。
項16. 第1工程において、溶解状態のタンニン酸を、口腔内速崩壊性錠剤用組成物のその他の原料に噴霧することにより混合する項15に記載の口腔内速崩壊性錠剤の製造方法。
項17. 第1工程において、口腔内速崩壊性錠剤用組成物のその他の原料に、溶解状態のタンニン酸を噴霧しながら、造粒操作を行う項16に記載の方法。
項18. 添加剤が、結合剤、及び/又は崩壊剤である項15〜17の何れかに記載の方法。
This invention is completed based on the said knowledge, and provides the manufacturing method of the following intraoral quick disintegrating tablet composition, an intraoral quick disintegrating tablet, and an intraoral quick disintegrating tablet.
Item 1. A composition for an orally rapidly disintegrating tablet comprising at least one excipient selected from the group consisting of sugars and sugar alcohols, and tannic acid, wherein each raw material is mixed using dissolved tannic acid And a composition for rapidly disintegrating tablets in the oral cavity, obtained by drying.
Item 2. Item 2. The composition for rapidly disintegrating tablets in the oral cavity according to Item 1, obtained by spraying the dissolved tannic acid onto the other raw materials of the composition for rapidly disintegrating tablets in the oral cavity and drying the mixture.
Item 3. Item 2. The granulation operation is carried out while spraying dissolved tannic acid on the composition material for rapidly disintegrating tablets in the oral cavity containing at least one excipient selected from the group consisting of sugars and sugar alcohols. The composition for intraoral rapidly disintegrating tablets as described in 2. above.
Item 4. Item 4. The intraoral rapidly disintegrating tablet composition according to any one of Items 1 to 3, wherein the saccharide is lactose hydrate and the sugar alcohol is mannitol.
Item 5. Item 5. An intraoral rapidly disintegrating tablet comprising the composition for intraorally rapidly disintegrating tablet according to any one of Items 1 to 4.
Item 6. Furthermore, the intraoral quick disintegrating tablet of claim | item 5 containing a binder and / or a disintegrating agent.
Item 7. Item 7. The intraoral rapidly disintegrating tablet according to Item 6, wherein the binder is at least one selected from the group consisting of magnesium aluminate metasilicate, synthetic aluminum silicate, light anhydrous silicic acid, calcium silicate, and crystalline cellulose.
Item 8. Item 8. The intraorally rapidly disintegrating tablet according to Item 6 or 7, wherein the disintegrant is at least one selected from the group consisting of crospovidone, carmellose calcium, carmellose, croscarmellose sodium, and low-substituted hydroxypropylcellulose.
Item 9. Item 9. The intraoral rapidly disintegrating tablet according to any one of Items 5 to 8, wherein the disintegration time measured by a disintegration test specified in the Japanese Pharmacopoeia is within 30 seconds.
Item 10. Item 10. The intraoral rapidly disintegrating tablet according to any one of Items 5 to 9 having a hardness of 40 N or more.
Item 11. A method for producing a composition for an orally rapidly disintegrating tablet comprising at least one excipient selected from the group consisting of saccharides and sugar alcohols, and tannic acid, wherein each tannic acid is used in a dissolved state. The manufacturing method of the composition for intraoral quick disintegrating tablets including the 1st process of mixing a raw material and the 2nd process of drying the obtained mixture.
Item 12. Item 12. The method for producing an intraoral rapidly disintegrating tablet composition according to Item 11, wherein in the first step, dissolved tannic acid is mixed by spraying the other raw materials of the intraoral rapidly disintegrating tablet composition. .
Item 13. Item 13. The method according to Item 12, wherein in the first step, the granulated operation is performed while spraying the dissolved tannic acid to the other raw materials of the composition for rapidly disintegrating tablets in the oral cavity.
Item 14. Item 14. The method according to Item 12 or 13, wherein the saccharide is lactose hydrate and the sugar alcohol is mannitol.
Item 15. A first step of mixing at least one excipient selected from the group consisting of saccharides and sugar alcohols, and a raw material containing tannic acid using tannic acid in a dissolved state, and drying the resulting mixture; A second step of obtaining a composition for rapidly disintegrating tablets in the oral cavity, compressing the composition for rapidly disintegrating tablets in the oral cavity, or a composition for rapidly disintegrating tablets in the oral cavity, and additives, and And / or a third step of compression-molding a mixture of pharmaceutically active ingredients.
Item 16. Item 16. The method for producing an orally rapidly disintegrating tablet according to Item 15, wherein in the first step, the dissolved tannic acid is mixed by spraying the other raw materials of the composition for rapidly disintegrating tablet in the oral cavity.
Item 17. Item 17. The method according to Item 16, wherein in the first step, granulation is performed while spraying dissolved tannic acid on the other raw materials of the composition for rapidly disintegrating tablets in the oral cavity.
Item 18. Item 18. The method according to any one of Items 15 to 17, wherein the additive is a binder and / or a disintegrant.
本発明の口腔内速崩壊性錠剤は、口腔内で優れた崩壊性を示すと共に適度な成型性を有する製剤であるため、服用性に優れたものである。 The intraoral rapidly disintegrating tablet of the present invention is a formulation that exhibits excellent disintegration properties in the oral cavity and has an appropriate moldability, and therefore has excellent dosing properties.
以下、本発明を詳細に説明する。
(I)口腔内速崩壊性錠剤用組成物
本発明の口腔内速崩壊性錠剤用組成物は、糖類、及び糖アルコール類からなる群より選ばれる少なくとも1種の賦形剤、並びにタンニン酸を含む口腔内速崩壊性錠剤用組成物であって、溶解状態のタンニン酸を用いて各原料を混合し、乾燥することにより得られる組成物である。
本発明において、「口腔内速崩壊性錠剤用」とは、口腔内速崩壊性錠剤の構成材料ないしは製造材料としての用途を有するという意味である。
Hereinafter, the present invention will be described in detail.
(I) Composition for intraorally rapidly disintegrating tablets The composition for intraorally rapidly disintegrating tablets of the present invention comprises at least one excipient selected from the group consisting of saccharides and sugar alcohols, and tannic acid. It is a composition for intraoral rapidly disintegrating tablets containing, and is a composition obtained by mixing each raw material using a dissolved tannic acid and drying.
In the present invention, “for intraorally rapidly disintegrating tablets” means having use as a constituent material or a production material of intraoral rapidly disintegrating tablets.
賦形剤の糖類としては、乳糖水和物、無水乳糖、白糖、精製白糖、果糖、ブドウ糖、ブドウ糖水和物、トレハロース等が挙げられ、糖アルコール類としては、マンニトール、ソルビトール、キシリトール、エリスリトール、マルチトール、イソマルト等が挙げられる。造粒物を口腔内で素早く崩壊させ得る点で、糖類の乳糖水和物、及び糖アルコール類のマンニトールが好ましい。 Examples of the saccharide of the excipient include lactose hydrate, anhydrous lactose, sucrose, purified sucrose, fructose, glucose, glucose hydrate, trehalose and the like, and sugar alcohols include mannitol, sorbitol, xylitol, erythritol, Examples include maltitol and isomalt. Lactose hydrate of saccharides and mannitol of sugar alcohols are preferable in that the granulated product can be rapidly disintegrated in the oral cavity.
糖類、及び糖アルコール類からなる群より選ばれる少なくとも1種の使用量は、口腔内速崩壊性錠剤用組成物の全量に対して、約10重量%以上が好ましく、約20重量%以上がより好ましく、約30重量%以上がさらにより好ましい。 The amount of at least one selected from the group consisting of saccharides and sugar alcohols is preferably about 10% by weight or more, more preferably about 20% by weight or more based on the total amount of the composition for rapidly disintegrating tablets in the oral cavity. Preferably, about 30% by weight or more is even more preferred.
タンニン酸は、各種の植物材料から抽出できる。例えば、柿の実、栗の渋皮、五倍子、没食子、タラ末、マメ科のタマリンドの種子皮、又はミモザ樹皮などから水又はエタノールを用いて抽出できる。好ましくは、第16改正日本薬局方に収載されている五倍子、又は没食子から抽出したタンニン酸を用いることができる。タンニン酸は未精製品であっても、精製品であってもよいが、精製品がより好ましい。 Tannic acid can be extracted from various plant materials. For example, water or ethanol can be extracted from persimmon fruit, chestnut astringent skin, pentaploid, gallic, cod powder, leguminous tamarind seed skin, or mimosa bark. Preferably, tannic acid extracted from pentaploid or gallic acid listed in the 16th revised Japanese Pharmacopoeia can be used. Tannic acid may be an unpurified product or a purified product, but a purified product is more preferable.
タンニン酸の使用量は、乾燥後の口腔内速崩壊性錠剤用組成物の全量に対して、好ましくは約0.001重量%以上、より好ましくは約0.01重量%、さらにより好ましくは約0.1重量%以上となる量とすればよい。この範囲であれば、この口腔内速崩壊性錠剤用組成物を用いて製造した錠剤が、十分な崩壊性を有するものとなる。また、タンニン酸の使用量は、乾燥後の口腔内速崩壊性錠剤用組成物の全量に対して、好ましくは約30重量%以下、より好ましくは約20重量%以下、さらにより好ましくは約10重量%以下となる量とすればよい。この範囲であれば、この造粒物を用いて製造した錠剤が、十分な成型性を有するものとなる。
タンニン酸溶液としては、水、エタノール、イソプロピルアルコール等のアルコール類からなる群より選ばれる1種以上を含む液にタンニン酸を溶解させた溶液が挙げられる。この溶液中のタンニン酸の濃度は、タンニン酸以外の材料の種類や、口腔内速崩壊性錠剤用組成物の調製操作(例えば、造粒操作)の種類等によって適宜定めることができ、約0.001〜30重量%とすることができる。
The amount of tannic acid used is preferably about 0.001% by weight or more, more preferably about 0.01% by weight, even more preferably about about 1% by weight, based on the total amount of the composition for rapidly disintegrating buccal tablets after drying. The amount may be 0.1% by weight or more. If it is this range, the tablet manufactured using this intraoral quick disintegrating tablet composition will have sufficient disintegration. The amount of tannic acid used is preferably about 30% by weight or less, more preferably about 20% by weight or less, still more preferably about 10% by weight based on the total amount of the composition for rapidly disintegrating buccal tablets after drying. What is necessary is just to set it as the quantity used as weight% or less. If it is this range, the tablet manufactured using this granulated material will have sufficient moldability.
Examples of the tannic acid solution include a solution in which tannic acid is dissolved in a liquid containing at least one selected from the group consisting of alcohols such as water, ethanol, and isopropyl alcohol. The concentration of tannic acid in this solution can be determined as appropriate depending on the type of material other than tannic acid, the type of preparation operation (for example, granulation operation) of the composition for rapidly disintegrating tablets in the oral cavity, and the like. 0.001 to 30% by weight.
タンニン酸溶液は、特別な操作をすることなく、そのままその他の原料に混合ないしは配合してもよく、その他の原料に噴霧することにより混合ないしは配合してもよい。何れの場合も、得られる組成物中のタンニン酸濃度が均一になるようにすればよい。 The tannic acid solution may be mixed or blended with other raw materials as it is without any special operation, or may be mixed or blended by spraying on other raw materials. In any case, the tannic acid concentration in the resulting composition may be made uniform.
また、タンニン酸以外の原料を、タンニン酸と共に、又はタンニン酸とは別に溶液状態とし、噴霧等の方法で、その他の原料に配合することもできる。さらに、タンニン酸を含む全原料を溶液状態とし、板などに噴霧することで、成形することもできる。 In addition, raw materials other than tannic acid can be mixed with tannic acid or separately from tannic acid and mixed with other raw materials by a method such as spraying. Furthermore, all the raw materials containing tannic acid can be made into a solution state and sprayed onto a plate or the like for molding.
口腔内速崩壊性錠剤用組成物は、糖類及び糖アルコール以外にも賦形剤を含むことができ、このような賦形剤として、トウモロコシデンプン、バレイショデンプン、コムギデンプン、コメデンプン等のデンプン類;グリシン、アラニンなどのアミノ酸類;軽質無水ケイ酸、合成ケイ酸アルミニウム、メタケイ酸アルミン酸マグネシウム、ケイ酸カルシウム等のケイ酸類;結晶セルロース、粉末セルロース等のセルロース類;タルク;酸化チタン;ポビドン;ヒドロキシプロピルセルロース;プルラン;ポリビニルアルコール・ポリエチレングリコールグラフトコポリマー;コポリビドン等の1種以上が挙げられる。 The composition for rapidly disintegrating tablets in the oral cavity can contain excipients in addition to saccharides and sugar alcohols. Examples of such excipients include starches such as corn starch, potato starch, wheat starch, and rice starch. Amino acids such as glycine and alanine; silicic acids such as light anhydrous silicic acid, synthetic aluminum silicate, magnesium aluminate metasilicate and calcium silicate; celluloses such as crystalline cellulose and powdered cellulose; talc; titanium oxide; povidone; One or more of hydroxypropyl cellulose; pullulan; polyvinyl alcohol / polyethylene glycol graft copolymer; copolyvidone and the like.
また、口腔内速崩壊性錠剤用組成物は、滑沢剤、着色剤、矯味剤、甘味剤、香料、防腐剤等の医薬品に一般的に使用される添加剤を適量含むことができる。
滑沢剤としては、ステアリン酸マグネシウム、ステアリン酸カルシウム、タルク、ショ糖脂肪酸エステル、フマル酸ステアリルナトリウム等が挙げられる。
着色剤としては、食用色素、食用レーキ色素、三二酸化鉄、黄色三二酸化鉄等が挙げられる。
矯味剤としては、クエン酸水和物、酒石酸、リンゴ酸、アスコルビン酸等が挙げられる。
甘味剤としては、アスパルテーム、アセスルファムカリウム、サッカリン、サッカリンナトリウム、グリチルリチン酸二カリウム、ステビア、ソーマチン、スクラロース等が挙げられる。
香料としては、ウイキョウ油、オレンジ油、カミツレ油、スペアミント油、ケイヒ油、チョウジ油、ハッカ油、ベルガモット油、ユーカリ油、ラベンダー油、レモン油、ローズ油、ローマカミツレ油、メントール等が挙げられる。
防腐剤としては、安息香酸、安息香酸ナトリウム、安息香酸ベンジル、パラオキシ安息香酸イソブチル、パラオキシ安息香酸イソプロピル、パラオキシ安息香酸エチル、パラオキシ安息香酸ブチル、パラオキシ安息香酸プロピル、パラオキシ安息香酸プロピルナトリウム、パラオキシ安息香酸メチル、パラオキシ安息香酸メチルナトリウム等が挙げられる。
添加剤は、1種を単独で使用してもよく、2種以上を用いてもよい。
Moreover, the composition for intraoral quick disintegrating tablets can contain an appropriate amount of additives generally used in pharmaceutical products such as lubricants, colorants, flavoring agents, sweeteners, flavors, and preservatives.
Examples of the lubricant include magnesium stearate, calcium stearate, talc, sucrose fatty acid ester, sodium stearyl fumarate and the like.
Examples of the colorant include food dyes, food lake dyes, iron sesquioxide, and yellow iron sesquioxide.
Examples of the corrigent include citric acid hydrate, tartaric acid, malic acid, ascorbic acid and the like.
Examples of the sweetening agent include aspartame, acesulfame potassium, saccharin, sodium saccharin, dipotassium glycyrrhizinate, stevia, thaumatin, sucralose and the like.
Examples of the fragrances include fennel oil, orange oil, chamomile oil, spearmint oil, cinnamon oil, clove oil, mint oil, bergamot oil, eucalyptus oil, lavender oil, lemon oil, rose oil, roman chamomile oil, menthol and the like.
Examples of preservatives include benzoic acid, sodium benzoate, benzyl benzoate, isobutyl paraoxybenzoate, isopropyl paraoxybenzoate, ethyl paraoxybenzoate, butyl paraoxybenzoate, propyl paraoxybenzoate, sodium propyl paraoxybenzoate, paraoxybenzoic acid Examples thereof include methyl and methyl sodium paraoxybenzoate.
An additive may be used individually by 1 type and may use 2 or more types.
口腔内速崩壊性錠剤用組成物は、医薬の有効成分を適量含むことができる。医薬有効成分は、この造粒物を含む口腔内速崩壊性錠剤の崩壊性、及び成型性を損なわない種類、及び量であれば良く、特に限定されない。 The composition for orally rapidly disintegrating tablets can contain an appropriate amount of an active ingredient of a medicine. The pharmaceutical active ingredient is not particularly limited as long as it is a kind and an amount that do not impair the disintegration property and moldability of the intraoral rapidly disintegrating tablet containing the granulated product.
上記各成分を含む本発明の口腔内速崩壊性錠剤用組成物は、顆粒のような造粒物の形態であってもよく、造粒されていない粉末の形態であってもよい。造粒物を得る場合は、タンニン酸溶液、又はタンニン酸及びその他の原料を含む溶液を、その他の原料に噴霧しながら造粒操作を行えばよい。また、タンニン酸等の全原料を含む溶液を板等に噴霧することにより、板上で造粒することもできる。
造粒方法としては、噴霧乾燥造粒法、流動層乾燥造粒法等が挙げられ、簡便性に優れる点で、特に流動層乾燥造粒法が好ましく、これに用いる装置は、医薬、食品等の当業者に良く知られたものを使用することができる。
賦形剤が結合剤としても機能する成分を含む場合は、流動層造粒法が好ましい。また、賦形剤が結合剤としても機能する成分を含まない場合は、撹拌造粒法が好ましい。これにより、速崩壊性及び成型性に優れる錠剤が得られる。結合剤としても機能する賦形剤としては、デンプン類、ポビドン、ヒドロキシプロピルセルロース、プルラン、ポリビニルアルコール・ポリエチレングリコールグラフトコポリマー、コポリビドンなどが挙げられる。
The composition for intraorally rapidly disintegrating tablets of the present invention containing the above-described components may be in the form of a granulated product such as a granule, or may be in the form of an ungranulated powder. In the case of obtaining a granulated product, the granulation operation may be performed while spraying the tannic acid solution or the solution containing tannic acid and other raw materials on the other raw materials. Moreover, it can also granulate on a board | plate by spraying the solution containing all raw materials, such as a tannic acid, on a board | substrate.
Examples of the granulation method include spray drying granulation method, fluidized bed drying granulation method, etc., and fluidized bed drying granulation method is particularly preferable in terms of excellent convenience. Those well known to those skilled in the art can be used.
When the excipient contains a component that also functions as a binder, fluidized bed granulation is preferred. In addition, when the excipient does not contain a component that also functions as a binder, a stirring granulation method is preferable. Thereby, the tablet excellent in quick disintegration property and moldability is obtained. Examples of excipients that also function as binders include starches, povidone, hydroxypropylcellulose, pullulan, polyvinyl alcohol / polyethylene glycol graft copolymers, and copolyvidone.
(II)口腔内速崩壊性錠剤
打錠
上記説明した口腔内速崩壊性錠剤用組成物を用いて、本発明の口腔内速崩壊性錠剤(以下、「本発明の錠剤」と言うこともある)を製造するには、上記説明した本発明の口腔内速崩壊性錠剤用組成物を、必要に応じて、結合剤、崩壊剤などのその他の成分と混合し、圧縮成型すればよい。
圧縮成型には、ロータリー式打錠機、単発打錠機等の一般に錠剤の成型に使用される方法や装置を使用することができる。また、この圧縮成型における圧縮圧は、約1kN以上が好ましく、約2kN以上がより好ましく、約4kN以上がさらにより好ましい。また、60kN以下が好ましく、約30kN以下がより好ましく、約15kN以下がさらにより好ましい。この範囲であれば、打錠時における臼杵の負担が少なく、さらに打錠時における打錠圧の維持もし易い。
(II) Orally rapidly disintegrating tablets
Tableting In order to produce the intraorally rapidly disintegrating tablet of the present invention (hereinafter sometimes referred to as “tablet of the present invention”) using the composition for intraorally rapidly disintegrating tablet described above, The composition for rapidly disintegrating tablets in the oral cavity according to the present invention may be mixed with other components such as a binder and a disintegrant, if necessary, and compression molded.
For the compression molding, a method and an apparatus generally used for tablet formation such as a rotary tableting machine and a single tableting machine can be used. The compression pressure in this compression molding is preferably about 1 kN or more, more preferably about 2 kN or more, and even more preferably about 4 kN or more. Moreover, 60 kN or less is preferable, about 30 kN or less is more preferable, and about 15 kN or less is still more preferable. If it is this range, the burden of the mortar at the time of tableting is small, and also it is easy to maintain the tableting pressure at the time of tableting.
なお、上記圧縮成型に先立ち、スクリーンミル、ジェットミル、ハンマーミル、ピンミル等を用いた整粒;振動ふるいを用いた篩過等の錠剤の製造に必要な操作に付してもよい。 Prior to the above compression molding, it may be subjected to operations necessary for the production of tablets such as sizing using a screen mill, jet mill, hammer mill, pin mill or the like; sieving using a vibrating sieve.
錠剤は、実質的に、上記説明した本発明の口腔内速崩壊性錠剤用組成物のみで構成することもできるが、結合剤、崩壊剤などのその他の成分を含むこともできる。
その他の成分を含む場合でも、本発明の錠剤における口腔内速崩壊性錠剤用組成物の含有量は、錠剤の全量に対して、約10重量%以上が好ましく、約30重量%以上がより好ましく、約60重量%以上がさらにより好ましい。即ち、本発明の錠剤が口腔内速崩壊性錠剤用組成物以外の成分を含む場合、口腔内速崩壊性錠剤用組成物以外の含有量は、錠剤の全量に対して、約90重量%以下が好ましく、約70重量%以下がより好ましく、約40重量%以下がさらにより好ましい。上記範囲であれば、実用上十分な成型性及び崩壊性を得ることができる。
The tablet can be composed substantially only of the composition for rapidly disintegrating buccal tablets of the present invention described above, but can also contain other components such as a binder and a disintegrant.
Even when other components are contained, the content of the composition for rapidly disintegrating buccal tablets in the tablet of the present invention is preferably about 10% by weight or more, more preferably about 30% by weight or more based on the total amount of the tablet. About 60% by weight or more is even more preferred. That is, when the tablet of the present invention contains components other than the composition for rapidly disintegrating tablets in the oral cavity, the content other than the composition for rapidly disintegrating tablets in the oral cavity is about 90% by weight or less based on the total amount of the tablet. About 70% by weight or less is more preferred, and about 40% by weight or less is even more preferred. If it is the said range, practically sufficient moldability and disintegration can be obtained.
なお、本発明の錠剤は圧縮成型により製造されるため、造粒物の形状と、本発明の錠剤中の造粒物の形状とは、通常、異なる。 In addition, since the tablet of the present invention is produced by compression molding, the shape of the granulated product is usually different from the shape of the granulated product in the tablet of the present invention.
結合剤
本発明の錠剤は、結合剤を含むことができる。結合剤は、圧縮時に造粒物を相互に結合させる作用を有するものである。
結合剤としては、メタケイ酸アルミン酸マグネシウム、合成ケイ酸アルミニウム、軽質無水ケイ酸、ケイ酸カルシウム、結晶セルロース、粉末セルロース、低置換度ヒドロキシプロピルセルロース等が挙げられる。中でも、メタケイ酸アルミン酸マグネシウム、合成ケイ酸アルミニウム、軽質無水ケイ酸、ケイ酸カルシウム、及び結晶セルロースが好ましい。
結合剤の含有量は、錠剤の全量に対して、約0.01重量%以上が好ましく、約0.1重量%以上がより好ましく、約1重量%以上がさらにより好ましい。また、錠剤の全量に対して、約30重量%以下が好ましく、約20重量%以下がより好ましく、約10重量%以下がさらに好ましい。上記範囲であれば、実用上十分な成型性及び崩壊性を得ることができる。
結合剤は、1種を単独で使用してもよく、2種以上を用いてもよい。
Binder The tablet of the present invention may contain a binder. The binder has an action of binding the granulated materials to each other during compression.
Examples of the binder include magnesium aluminate metasilicate, synthetic aluminum silicate, light anhydrous silicic acid, calcium silicate, crystalline cellulose, powdered cellulose, low-substituted hydroxypropylcellulose, and the like. Among these, magnesium aluminate metasilicate, synthetic aluminum silicate, light anhydrous silicic acid, calcium silicate, and crystalline cellulose are preferable.
The content of the binder is preferably about 0.01% by weight or more, more preferably about 0.1% by weight or more, and still more preferably about 1% by weight or more based on the total amount of the tablet. Moreover, about 30 weight% or less is preferable with respect to the whole quantity of a tablet, About 20 weight% or less is more preferable, About 10 weight% or less is further more preferable. If it is the said range, practically sufficient moldability and disintegration can be obtained.
A binder may be used individually by 1 type and may use 2 or more types.
崩壊剤
本発明の錠剤は、崩壊剤を含むことができる。崩壊剤は、水を含んで膨れる成分、又は水を含んで崩れる成分である。
崩壊剤としては、クロスポビドン、カルメロースカルシウム、カルメロース、アルギン酸、クロスカルメロースナトリウム、低置換度ヒドロキシプロピルセルロース、トウモロコシデンプン、バレイショデンプン、コムギデンプン、コメデンプン、部分アルファー化デンプン、アルファー化デンプン、カルボキシメチルスターチナトリウム等が挙げられる。中でも、クロスポビドン、カルメロースカルシウム、カルメロース、クロスカルメロースナトリウム、低置換度ヒドロキシプロピルセルロースが好ましい。
崩壊剤の含有量は、錠剤の全量に対して、約0.01重量%以上が好ましく、約0.1重量%以上がより好ましく、約1重量%以上がさらにより好ましい。また、錠剤の全量に対して、約30重量%以下が好ましく、約20重量%以下がより好ましく、約10重量%以下がさらに好ましい。上記範囲であれば、実用上十分な成型性及び崩壊性を得ることができる。
崩壊剤は、1種を単独で使用してもよく、2種以上を用いてもよい。
Disintegrant The tablet of the present invention may contain a disintegrant. The disintegrant is a component that swells with water or a component that collapses with water.
Disintegrants include crospovidone, carmellose calcium, carmellose, alginic acid, croscarmellose sodium, low-substituted hydroxypropylcellulose, corn starch, potato starch, wheat starch, rice starch, partially pregelatinized starch, pregelatinized starch, carboxy Examples include methyl starch sodium. Of these, crospovidone, carmellose calcium, carmellose, croscarmellose sodium, and low-substituted hydroxypropylcellulose are preferred.
The content of the disintegrant is preferably about 0.01% by weight or more, more preferably about 0.1% by weight or more, and still more preferably about 1% by weight or more based on the total amount of the tablet. Moreover, about 30 weight% or less is preferable with respect to the whole quantity of a tablet, About 20 weight% or less is more preferable, About 10 weight% or less is further more preferable. If it is the said range, practically sufficient moldability and disintegration can be obtained.
A disintegrating agent may be used individually by 1 type, and may use 2 or more types.
その他の成分
本発明の錠剤は、賦形剤、滑沢剤、着色剤、矯味剤、甘味剤、香料、防腐剤等の医薬品に一般的に使用される添加剤を適量含むことができる。また、医薬有効成分を含むこともできる。
添加剤、及び医薬の有効成分は、それぞれ、1種を単独で使用してもよく、2種以上を用いてもよい。
Other Components The tablet of the present invention can contain an appropriate amount of additives generally used in pharmaceuticals such as excipients, lubricants, coloring agents, flavoring agents, sweeteners, fragrances, and preservatives. Moreover, a pharmaceutical active ingredient can also be included.
Each of the additive and the active pharmaceutical ingredient may be used alone or in combination of two or more.
このようにして得られる本錠剤は、実用上問題ない適度な成型性を有し、更に口腔内での優れた崩壊性を有している。 The tablet thus obtained has an appropriate moldability with no practical problem, and further has an excellent disintegration property in the oral cavity.
本発明の錠剤は、第16改正日本薬局方解説書に規定の崩壊試験法による崩壊時間(特に、崩壊試験器(富山産業製)を用いて測定した崩壊時間)が、30秒以下であることが好ましく、20秒以下であることが好ましく、10秒以下であることがさらにより好ましい。
本発明の錠剤は、硬度(特に、錠剤硬度計(富山産業製)を用いて測定した硬度)が50N以上であることが好ましく、60N以上であることがより好ましく、70N以上であることがさらにより好ましい。
The tablet of the present invention has a disintegration time (particularly, a disintegration time measured using a disintegration tester (manufactured by Toyama Sangyo)) of 30 seconds or less according to the disintegration test method prescribed in the 16th revised Japanese Pharmacopoeia Manual. Is preferably 20 seconds or shorter, and more preferably 10 seconds or shorter.
The tablet of the present invention preferably has a hardness (particularly, a hardness measured using a tablet hardness meter (manufactured by Toyama Sangyo)) of 50 N or more, more preferably 60 N or more, and even more preferably 70 N or more. More preferred.
以下、実施例及び比較例を挙げて本発明を更に詳しく説明するが、本発明はこれらに限定されない。
(1)物性試験
<崩壊試験>
試験は、第16改正日本薬局方解説書に規定の崩壊試験法に従い、但し、崩壊試験器(富山産業製)を用いて実施し、試験数は6錠とし、その崩壊時間の平均値で評価した。
<硬度試験>
試験は、錠剤硬度計(富山産業製)を用いて実施し、試験数は10錠とし、その硬度の平均値で評価した。
EXAMPLES Hereinafter, although an Example and a comparative example are given and this invention is demonstrated in more detail, this invention is not limited to these.
(1) Physical property test <Disintegration test>
The test follows the disintegration test method stipulated in the 16th revised Japanese Pharmacopoeia Manual, except that the disintegration tester (manufactured by Toyama Sangyo Co., Ltd.) is used, the number of tests is 6 tablets, and the average value of disintegration time is evaluated. did.
<Hardness test>
The test was carried out using a tablet hardness tester (manufactured by Toyama Sangyo Co., Ltd.), the number of tests was 10 tablets, and the average value of the hardness was evaluated.
(2)錠剤の製造
実施例1
後掲の表1に示す組成に基づき、流動層造粒乾燥機にマンニトールを投入した後、流動させながら、タンニン酸を適量の水に溶解した液を徐々に噴霧して造粒した。次に、この造粒品を流動層造粒機で引き続き乾燥した後、この乾燥品を整粒した。更に、この整粒品にその他の添加剤を加えて、混合した後、打錠機を用い、約8kNの打錠圧で、1錠の直径が8.5mmで、その質量が240mgの錠剤を得た。
(2) Manufacture of tablets
Example 1
Based on the composition shown in Table 1 below, mannitol was charged into a fluidized bed granulator / dryer and then granulated by gradually spraying a liquid in which tannic acid was dissolved in an appropriate amount of water while flowing. Next, the granulated product was subsequently dried with a fluidized bed granulator, and then the dried product was sized. Furthermore, after adding other additives to this sized product and mixing, a tablet with a tableting pressure of about 8 kN and a tablet diameter of 8.5 mm and a mass of 240 mg using a tableting machine. Obtained.
比較例1
後掲の表1に示す組成に基づき、流動層造粒乾燥機にマンニトールを投入した後、流動させながら、適量の水を徐々に噴霧して造粒した。更に、この造粒品を流動層造粒機で引き続き乾燥した後、この乾燥品を整粒した。更に、この整粒品にその他の添加剤を加えて、混合した後、打錠機を用い、約8kNの打錠圧で、1錠の直径が8.5mmで、その質量が240mgの錠剤を得た。
Comparative Example 1
Based on the composition shown in Table 1 below, mannitol was charged into a fluidized bed granulator / dryer, and then granulated by gradually spraying an appropriate amount of water while flowing. Further, the granulated product was subsequently dried with a fluidized bed granulator, and then the dried product was sized. Furthermore, after adding other additives to this sized product and mixing, a tablet with a tableting pressure of about 8 kN and a tablet diameter of 8.5 mm and a mass of 240 mg using a tableting machine. Obtained.
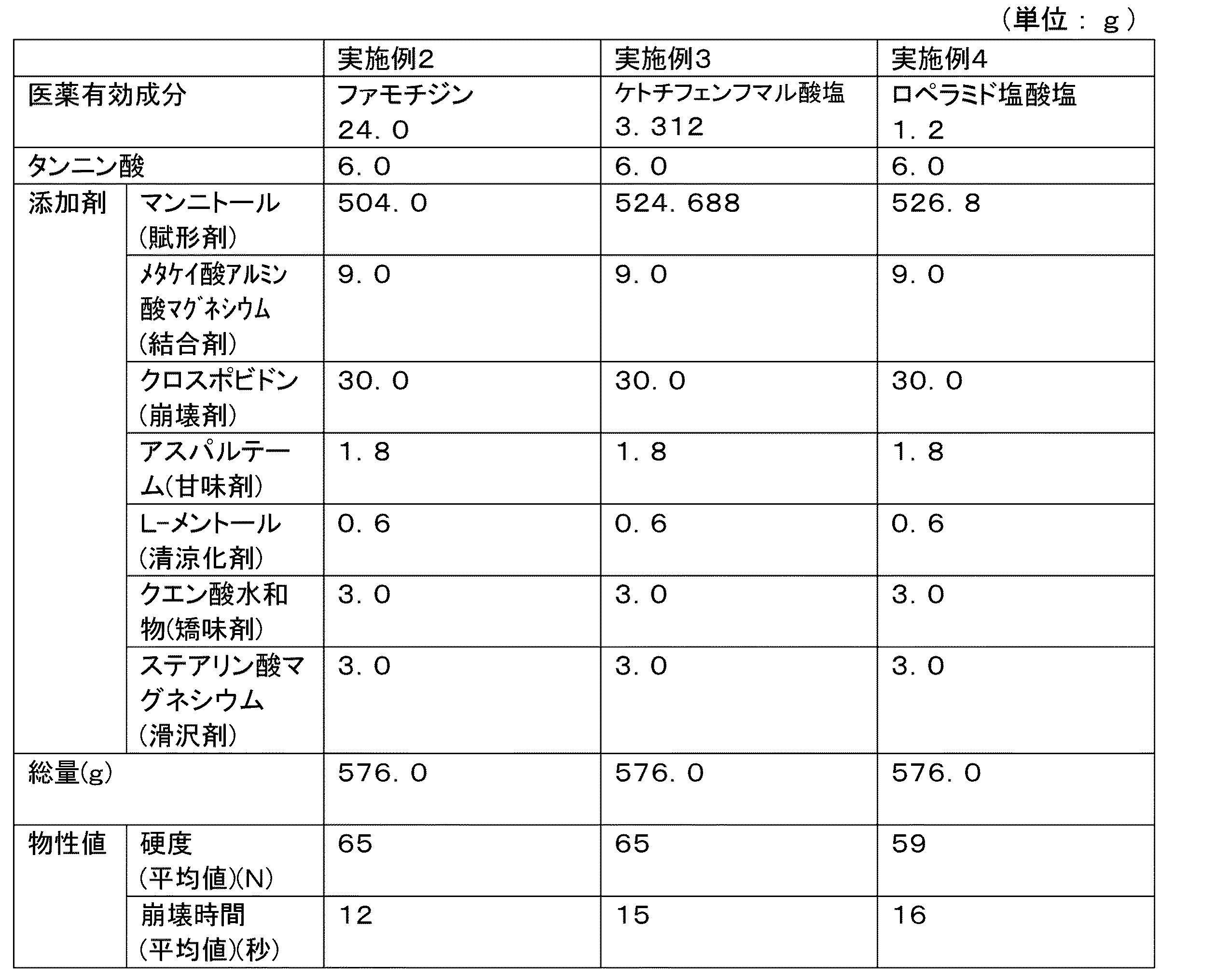
実施例2〜4
後掲の表2に示す組成に基づき、流動層造粒乾燥機に医薬有効成分とマンニトールを投入した後、流動させながら、タンニン酸を適量の水に溶解した液を徐々に噴霧して造粒した。更に、この造粒品を流動層造粒機で引き続き乾燥した後、この乾燥品を整粒した。更に、この整粒品に、その他の添加剤を加えて、混合した後、打錠機を用い、約8kNの打錠圧で、1錠の直径が8.5mmで、その質量が240mgの錠剤を得た。
Examples 2-4
Based on the composition shown in Table 2 below, the pharmaceutically active ingredient and mannitol are charged into a fluidized bed granulator / dryer, and then a solution of tannic acid dissolved in an appropriate amount of water is gradually sprayed and granulated while flowing. did. Further, the granulated product was subsequently dried with a fluidized bed granulator, and then the dried product was sized. Furthermore, after adding other additives to this sized product and mixing, using a tableting machine, a tablet having a tablet diameter of 8.5 mm and a mass of 240 mg with a tableting pressure of about 8 kN. Got.
(3)結果
実施例1及び比較例1の錠剤の組成、崩壊試験及び硬度試験の結果を下記の表1に示す。
表1から明らかなように、実施例1の錠剤は、崩壊時間が15秒で、更に硬度が62Nで、優れた崩壊性と成型性を示した。これに対し、タンニン酸を含まない比較例1の錠剤は、崩壊時間が12秒で、特に崩壊性に問題は認めなかったが、硬度が24Nで、実施例1の錠剤に比べて低く、成型性が悪かった。 As is apparent from Table 1, the tablet of Example 1 showed excellent disintegration and moldability with a disintegration time of 15 seconds and a hardness of 62N. On the other hand, the tablet of Comparative Example 1 containing no tannic acid had a disintegration time of 12 seconds and had no particular problem in disintegration, but had a hardness of 24 N and was lower than the tablet of Example 1, and was molded. The nature was bad.
実施例2〜4の錠剤の組成、崩壊試験及び硬度試験の結果を下記の表2に示す。
表2から明らかなように、実施例2〜4の錠剤は、崩壊時間がそれぞれ12秒、15秒及び16秒で、硬度がそれぞれ65N、65N及び59Nであり、優れた崩壊性と成型性を示した。 As is apparent from Table 2, the tablets of Examples 2 to 4 have a disintegration time of 12 seconds, 15 seconds, and 16 seconds, respectively, and hardnesses of 65 N, 65 N, and 59 N, respectively. Indicated.
本発明の口腔内速崩壊性錠剤は、複雑な製造工程や特殊な製造装置を使用しないで製造できるものであり、かつ、含有する医薬有効成分の種類にかかわらず優れた崩壊性と成型性を兼ね備えたものである。従って、工業的な大規模生産に適すると同時に、種々の医薬有効成分を配合することのできる口腔内速崩壊性錠剤として、広く利用可能なものである。 The intraoral rapidly disintegrating tablet of the present invention can be manufactured without using a complicated manufacturing process or a special manufacturing apparatus, and has excellent disintegration and moldability regardless of the kind of active pharmaceutical ingredient to be contained. It is a combination. Therefore, it is suitable for industrial large-scale production, and at the same time, can be widely used as an orally rapidly disintegrating tablet in which various active pharmaceutical ingredients can be blended.
Claims (13)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017159294A JP6438547B2 (en) | 2017-08-22 | 2017-08-22 | Intraoral rapidly disintegrating tablet composition |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017159294A JP6438547B2 (en) | 2017-08-22 | 2017-08-22 | Intraoral rapidly disintegrating tablet composition |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013217586A Division JP6262490B2 (en) | 2013-10-18 | 2013-10-18 | Intraoral rapidly disintegrating tablet composition |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017200959A true JP2017200959A (en) | 2017-11-09 |
| JP6438547B2 JP6438547B2 (en) | 2018-12-12 |
Family
ID=60264866
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017159294A Active JP6438547B2 (en) | 2017-08-22 | 2017-08-22 | Intraoral rapidly disintegrating tablet composition |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6438547B2 (en) |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH089897A (en) * | 1994-07-01 | 1996-01-16 | Kao Corp | Coated composition for bitter taste-having substance |
| JP2000119175A (en) * | 1998-10-13 | 2000-04-25 | Taisho Yakuhin Kogyo Kk | Intraoral rapid disintegrative solid preparation |
| JP2006008543A (en) * | 2004-06-23 | 2006-01-12 | Eisai Co Ltd | Ampiroxicam-containing pharmaceutical composition, its stabilizing method and its manufacturing method |
| JP2009235066A (en) * | 2008-03-07 | 2009-10-15 | Sawai Pharmaceutical Co Ltd | Orally disintegrable tablet containing coated microparticle |
| JP2014224086A (en) * | 2013-04-22 | 2014-12-04 | テイカ製薬株式会社 | Composition for orally quickly disintegrating composition solid formulation |
| WO2015115453A1 (en) * | 2014-01-30 | 2015-08-06 | テイカ製薬株式会社 | Composition for orally rapidly disintegrating solid preparation |
| JP5775223B2 (en) * | 2012-09-05 | 2015-09-09 | テイカ製薬株式会社 | Granules for intraoral rapidly disintegrating tablets |
| JP6262490B2 (en) * | 2013-10-18 | 2018-01-17 | テイカ製薬株式会社 | Intraoral rapidly disintegrating tablet composition |
-
2017
- 2017-08-22 JP JP2017159294A patent/JP6438547B2/en active Active
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH089897A (en) * | 1994-07-01 | 1996-01-16 | Kao Corp | Coated composition for bitter taste-having substance |
| JP2000119175A (en) * | 1998-10-13 | 2000-04-25 | Taisho Yakuhin Kogyo Kk | Intraoral rapid disintegrative solid preparation |
| JP2006008543A (en) * | 2004-06-23 | 2006-01-12 | Eisai Co Ltd | Ampiroxicam-containing pharmaceutical composition, its stabilizing method and its manufacturing method |
| JP2009235066A (en) * | 2008-03-07 | 2009-10-15 | Sawai Pharmaceutical Co Ltd | Orally disintegrable tablet containing coated microparticle |
| JP5775223B2 (en) * | 2012-09-05 | 2015-09-09 | テイカ製薬株式会社 | Granules for intraoral rapidly disintegrating tablets |
| JP2014224086A (en) * | 2013-04-22 | 2014-12-04 | テイカ製薬株式会社 | Composition for orally quickly disintegrating composition solid formulation |
| JP6262490B2 (en) * | 2013-10-18 | 2018-01-17 | テイカ製薬株式会社 | Intraoral rapidly disintegrating tablet composition |
| WO2015115453A1 (en) * | 2014-01-30 | 2015-08-06 | テイカ製薬株式会社 | Composition for orally rapidly disintegrating solid preparation |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6438547B2 (en) | 2018-12-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5775223B2 (en) | Granules for intraoral rapidly disintegrating tablets | |
| JP6325627B2 (en) | Orally disintegrating tablet and method for producing the same | |
| JP5366233B2 (en) | Orally disintegrating tablets | |
| JP6133445B2 (en) | Oral rapidly disintegrating composition for solid preparation | |
| JP6204141B2 (en) | Oral rapidly disintegrating composition for solid preparation | |
| JP2003034655A (en) | Fast degradable solid tablet | |
| JP5945191B2 (en) | Intraoral quick disintegrating tablet | |
| JP6262490B2 (en) | Intraoral rapidly disintegrating tablet composition | |
| JP2010241760A (en) | Tablet quickly disintegrable in oral cavity that has unpleasant taste reduced, and method for preparing the same | |
| TWI771287B (en) | Granules for orally rapidly disintegrating tablet | |
| JP2007224021A (en) | Fast-disintegrating tablet containing iguratimod | |
| JP6092672B2 (en) | Orally rapidly disintegrating tablets | |
| JP6438547B2 (en) | Intraoral rapidly disintegrating tablet composition | |
| KR102431738B1 (en) | Very rapidly disintegrating tablet, and method for producing same | |
| JP6341196B2 (en) | Solid preparation | |
| JP2005029557A (en) | Quickly disintegrating tablet in oral cavity and method for producing the same | |
| TW201446287A (en) | Rapidly disintegrating tablet suitable for administration to infants and simple production method therefor | |
| JP5502358B2 (en) | Oral rapidly disintegrating tablet and method for producing the same | |
| JP2016020329A (en) | Solid preparations | |
| WO2002092058A1 (en) | Rapidly disintegratable solid preparation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170823 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A132 Effective date: 20180508 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180628 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20180702 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20181113 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20181116 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6438547 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |