JP2013508411A - 癌治療の効果を高め、その副作用を軽減する方法および栄養製剤 - Google Patents
癌治療の効果を高め、その副作用を軽減する方法および栄養製剤 Download PDFInfo
- Publication number
- JP2013508411A JP2013508411A JP2012535426A JP2012535426A JP2013508411A JP 2013508411 A JP2013508411 A JP 2013508411A JP 2012535426 A JP2012535426 A JP 2012535426A JP 2012535426 A JP2012535426 A JP 2012535426A JP 2013508411 A JP2013508411 A JP 2013508411A
- Authority
- JP
- Japan
- Prior art keywords
- patient
- meal
- cancer
- chemotherapy
- predetermined period
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G06—COMPUTING; CALCULATING OR COUNTING
- G06Q—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR ADMINISTRATIVE, COMMERCIAL, FINANCIAL, MANAGERIAL OR SUPERVISORY PURPOSES; SYSTEMS OR METHODS SPECIALLY ADAPTED FOR ADMINISTRATIVE, COMMERCIAL, FINANCIAL, MANAGERIAL OR SUPERVISORY PURPOSES, NOT OTHERWISE PROVIDED FOR
- G06Q10/00—Administration; Management
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L13/00—Meat products; Meat meal; Preparation or treatment thereof
- A23L13/60—Comminuted or emulsified meat products, e.g. sausages; Reformed meat from comminuted meat product
- A23L13/65—Sausages
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23P—SHAPING OR WORKING OF FOODSTUFFS, NOT FULLY COVERED BY A SINGLE OTHER SUBCLASS
- A23P20/00—Coating of foodstuffs; Coatings therefor; Making laminated, multi-layered, stuffed or hollow foodstuffs
- A23P20/20—Making of laminated, multi-layered, stuffed or hollow foodstuffs, e.g. by wrapping in preformed edible dough sheets or in edible food containers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/07—Retinol compounds, e.g. vitamin A
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/202—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids having three or more double bonds, e.g. linolenic
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
- A61K31/375—Ascorbic acid, i.e. vitamin C; Salts thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/59—Compounds containing 9, 10- seco- cyclopenta[a]hydrophenanthrene ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/02—Nutrients, e.g. vitamins, minerals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Abstract
本発明は、化学療法および/または放射線療法を組み合わせて、患者を保護し、かつ癌細胞の感受性を高める方法に関する。より詳しくは、本発明は、患者の慢性的な体重減少を引き起こさずに癌の増殖を抑制し、正常な細胞、組織および臓器を化学療法および/または放射線療法から保護し、かつ低用量、通常用量、高用量の化学療法に対する癌細胞の感受性を高めることができる、栄養学的方法および処方を提供する。それらの方法のいくつかはまた、化学療法を行わない場合でさえも癌の成長を妨げる。
【選択図】図51
Description
本願は、2009年10月22日出願の米国仮特許出願第61/254,154号の利益を主張するものであり、その開示内容はすべて参照することによりここに組み込まれる。
多様な悪性腫瘍があると診断された患者らが、化学療法の前(48〜140時間)および/または後(24〜56時間)に自発的に絶食を行った10の症例について記載する。絶食と組み合わせて平均4サイクルの化学療法を受けた10人の患者は、空腹以外は誰も、絶食自体による重大な副作用を訴えることはなかった。毒性のグレード分け、National Cancer Institute(NCI)のCommon Toxicity Criteria(CTC)に基づいて行い、そして5人の患者が自己申告した副作用は、絶食が疲労、衰弱および消化器への副作用から保護し得ることを示している。癌の進行をモニターできた患者では、絶食が化学療法依存の腫瘍量または腫瘍マーカーの減少を阻害することはなかった。臨床転帰および患者の生活の質を高めることにおける絶食の役割を調べるには、制御した臨床試験が必要であるが、ここに示した10の症例は、化学療法と併用した絶食は、妥当であり、安全であり、かつ従来の化学療法を増強する可能性を有していることを示唆している。
ドセタキセル(DTX)およびシクロホスファミド(CP)による補助化学療法が推奨された、ステージIIAの乳癌と診断された51歳の白人女性。彼女は第1回の化学療法を実施する前に絶食を行った。絶食の方法は、化学療法前の120時間、および化学療法後の60時間(計180時間)はカロリーを完全に断ち、その間、彼女は水とビタミンのみを摂取するというものであった。患者は、この長期に亘る絶食を重大な不都合もなく終え、体重は7ポンド減少したが、これは治療が終わるまでに回復した(図IH)。絶食−化学療法のサイクル後、患者は軽い疲労、口内乾燥、吃逆を経験した(図2)が、それにもかかわらず、彼女は日々の活動(1日に12時間まで仕事)を行うことができた。対照的に、その後の化学療法サイクル(第2回および第3回)では、彼女は絶食せずに化学療法を受け、軽度から重度に至る疲労、衰弱、悪心、腹部痙攣および下痢を訴えた(図2)。今度は、副作用によって彼女はいつもの仕事のスケジュールをこなせなかった。第4回および最後のサイクルでは、化学療法前の120時間、および化学療法後の24時間の絶食からなる異なる方法であったが、再度、絶食することを選択した。注目すべきことに、前のサイクルで組織には蓄積された損傷が見込まれるにもかかわらず、彼女が自己申告した副作用は軽度なものであった。これと一致して、血液検査の結果も、絶食が血液細胞の保護に好ましい効果をもたらし得ることを支持するものであった。化学療法の前に絶食を行ったときは、総白血球数(WBC)および好中球絶対数(ANC)は、最下点で僅かではあるが一貫して増大した(図1A、C;表1)。さらに、絶食−化学療法において、第1および第4サイクルそれぞれで、血小板数は減少せず、むしろ安定を維持するか、または増加することが観察された。(図1D)。興味深いことに、144時間の絶食と併用した第4回化学療法サイクル後、ANC、WBCおよび血小板数は、80日前の化学療法の開始以来、最高値に達した(図1A、CおよびD)。研究室での数値とCTCの調査は、概ね、絶食が安全であって、化学療法による有害な副作用からこの患者を保護することができたことを示唆している。
2008年2月に食道腺癌と診断された68歳の白人男性。診断時までに、CT−PETスキャンで左副腎への転移が発見され、これはステージIVの疾患と一致する。初期の治療は、シスプラチン(CDDP)を併用した5−フルオロウラシル(5−FU)であった。この化学療法と同時に、彼はまた最初の2サイクルで局所放射線照射を受けた。この期間を通して患者は、重度の衰弱、極度の疲労、激しい嘔吐および重篤な末梢神経障害を含む多くの副作用を経験した(図3)。さらに患者は、放射線治療により最も引き起こされやすい、重篤な粘膜炎に続いて強い嚥下障害を訴えた。第3のサイクルの間、重度の悪心と難治性嘔吐のために、5−FUの投与を中断せざるを得なかった(図3)。化学療法と放射線を使用する攻撃的な治療にもかかわらず、彼の病気は進行した。2008年8月に測定した新しいCT−PETからは、右の副腎、右肺の下葉、左仙骨、および烏口突起への新たな転移の展開が示された。これらのことから、彼の化学療法の強化が促された(第4のサイクル)。カルボプラチン(CBDCA)のDTXおよび5−Fuとの併用(5−FUは96時間投与された)。患者は、第4のサイクルの間、化学療法前72時間と、化学療法後51時間の絶食を組み込んだ。化学療法後51時間絶食したのは、5−FUの継続投与から保護するためであった。患者は体重が約7ポンド減少したが、通常食を再開して最初の数日のうちに4ポンド回復した(データを示さず)。このサイクルの間、3種類の化学療法薬剤を併用したが、報告された自己申告の副作用は、アドリブ食−化学療法サイクルより一貫して軽度であった(図3)。第5の化学療法治療の前に、患者は再び絶食することを選択した。前に彼が受けたような96時間の5−FUの点滴を受ける代わりに、同用量の薬が48時間以内に投与され、絶食の方法も薬剤送達前の48時間と薬剤送達後56時間に修正された。興味深いことに、自己申告の副作用が軽度であったばかりでなく、CT−PETスキャンで記録された臨床応答も励みになるものであった。主な食道腫瘤、副腎転移、および肺の右下葉小結節の標準摂取率(SUV)が減少したことが、スキャンで示された。第6、第7、第8サイクルでは、患者は化学療法治療の前後で絶食を行った(表3)。毒性の蓄積が予想されたにもかかわらず、第7化学療法サイクルの間に軽い下痢と腹部痙攣があったことを除いて、ほとんどの副作用が絶食により軽減された。非常に攻撃的な癌であり、十分に耐えられた化学療法であったにもかかわらず、患者の病気は進行し、患者は2009年2月に死亡した。
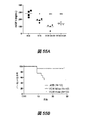
2000年7月に、グリーソンスコア7、PSA値5.8ng/mlの両側前立腺癌と診断された74歳の白人男性。2000年9月に前立腺切除を行い、2003年1月にPSA値が1.4ng/mlに上昇するまでは、検出不能のPSA値であった。ビカルタミドおよびフィナステリドと共に酢酸リュープロリドが処方された。しかしながら、テストステロンの欠乏に関係した重度の副作用のために、2004年4月にはこれらの薬の投与を中止せざるを得なかった。この病気をコントロールするために、トリプトレリンパモ酸塩、ニルタミド、サリドマイド、CPおよびケトコナゾールを含む、異なる薬剤が使用された。2007年には、患者のPSA値は9ng/mlに達し、骨スキャン中に新たな転移が認められた。1週当たり25mg/m2のDTXを投与したが、PSA値は増加を続け、40.6ng/ml(データを示さず)に達した。ベバシズマブを治療に加え、それによって初めて、PSAが顕著に低下した(データを示さず)。これに一致して、新たな骨スキャンは全体的な改善を示した。化学療法を伴うサイクルを通じて、患者は、疲労、衰弱、金属味、眩暈、失念、短期記憶障害および末梢神経障害を含む重篤な副作用を経験した(図5)。化学療法治療の停止後、彼のPSAは急激に上昇した。3週サイクルで75mg/m2のDTX投与が方法として選択され、患者は、再度、重篤な副作用を経験することになった(図5)。2008年6月、化学療法を中止した。患者は、CYP17(非性腺アンドロゲンの生合成に必要な一連の反応を触媒するミクロゾーム酵素)を選択的に遮断することができる薬剤である酢酸アビラテロンのフェーズIII臨床試験に参加した(Derek RaghavanおよびEric A.Klein著、J.C.O、2008)。試験中、患者のPSA値は20.9ng/dlまで上昇し(図4H)、化学療法治療の再開を促された。今度は、患者は化学療法前に絶食することを選択した。彼の絶食スケジュールは、ほとんどが薬剤投与前60時間および薬剤投与後24であった(表3)。PSA値は化学療法−絶食治療(DTX 75mg/m2)を再開すると直ちに低下し、そして注目すべきことに、患者の副作用の報告は、以前のアドリブ食化学療法サイクルのときよりかなり少なかった(図5)。患者の経験と一致して、血液検査の結果は、治療の期間中一貫して安定しており、正常範囲に留まっていた(図4A〜G)。最後の3サイクルの間、患者に、絶食に加えて、化学療法前の5日間、テストステロン(クリーム1%)を塗布した。その結果、PSA値はテストステロン値と共に顕著に増加した。それにもかかわらず、絶食と併用した3サイクルの化学療法により、PSAは34.2ng/mlから6.43ng/mlへと低下した(図4H)。これらの結果は、絶食が癌細胞を部分的に保護し得る可能性を支持するものではない。
2008年6月に低分化の非小細胞肺癌(NSCLC)と診断された61歳の白人女性。最初にCTスキャンで見られた腫瘤は、PETスタディ(2008年、6月)で異化亢進であることがわかり、生検の結果とも相関した。同じPETスキャンで、多数の縦隔および左の肺門周囲のリンパ節に、広範囲に及ぶ転移性の病変が認められた。骨、肝臓、脾臓および膵臓への転移も認められた。最初の治療は、21日毎にDTXを75mg/m2とCBDCAを540mg/m2投与することから始められた。彼女は通常の食を摂っていたが、最初の5サイクルの間、各化学療法治療の後で平均4ポンド体重が減少した。化学療法毒性が原因である可能性が最も高い。彼女の報告によれば、元の体重に戻るのに約3週間を要したということであった。経験した副作用の中でも、彼女は激しい筋痙攣、下肢神経障害、強い疲労、口内および舌の痛み、内出血のしやすさ、ならびに腸の不快感を訴えた(図7)。同じ薬と用量からなる第6サイクルの間、患者は、化学療法前48時間と化学療法後24時間、絶食した。この期間中に彼女の体重は約6ポンド減少したが、これは10日で回復した(データを示さず)。患者は、軽い疲労と衰弱以外は、先の5回のサイクルの間に経験した他の副作用を訴えることはなかった(図7)。なお、末梢神経障害、脱毛または短期記憶障害などの蓄積性の副作用は、一度発現すると絶食により元に戻すことはできないことに留意しなければならない。一方、急性の有毒な副作用は、絶食状態で化学療法を行うと、回避できた(図7)。第6および最後のサイクルの後で、患者から、薬剤投与の僅か3日後に3マイルを歩けるほど急速に活力が回復したとの報告があった。患者の血液検査では大きな差異は認められなかった(図6A〜G)。2009年2月に行われた最後の放射線検査(PET)は、ベースライン検査と比較して、主要腫瘤(左肺の下葉)の病変が安定しており、かつ脾臓および肝臓中のトレーサーの吸収が減少していることを示した。
2008年にステージIVの子宮体部漿液性腺癌であると診断された74歳の女性患者。外科的処置(TAH−BSO)に続いて補助化学療法を行うことが推奨された。さらに、骨盤、傍大静脈および大静脈前のリンパ節を切除した。最後に右尿管が大きく肥大していたので、右腎摘出を行った。CBDCA(480mg)およびパクリタクセル(280mg)の投与を、21日毎に、6サイクル行った。第1の治療の間、患者は通常の食を摂っており、疲労、衰弱、脱毛、頭痛を経験し、胃腸の不快感を訴えた(図8)。一方、サイクル2〜6の間は、患者は薬剤投与の前後に絶食を行い、化学療法後の副作用が軽減したことを報告した(表3;図8)。他の報告と一致して、絶食は化学療法依存の癌細胞殺滅を妨害することはなく、これは第4サイクルの後でCA−125腫瘍マーカーが87%減少したことで実証された(データを示さず)。
2007年7月に、右卵巣腫瘤(10×12cm)と診断された44歳の白人女性患者。外科的処置(TAH−BSO)が行われた。腫瘍は、卵巣被膜への浸潤がなく、切除した30+のリンパ節は全て陰性であった。彼女の病変はステージIAの卵巣癌肉腫とグレードづけられた。最初に行われた治療は、イホスファミドとCDDPによる6サイクルのコースであり、患者はこれを2007年7月から11月まで受けた。2008年1月に行われた彼女の最初のCTスキャンでは、卵巣の病変の拡大は認められなかった。7か月後、MRIによって新たな多数の肺結節が見出された。この発見はCTスキャンにより確認され、脾臓領域における数か所の異常(低密度の像=MTS?)、および脊椎の退行性変化と共に、20を超える新たな小結節が肺の内部に認められた。これらの結果に基づき、Taxol、カルボプラチンおよびアバスチンを含む薬剤による新たな投薬計画が立てられた。2008年8月に点滴が開始され、3週間のスケジュールで行われた。同時に、患者には、高用量のビタミンC(50mg/日)が追加された。2008年9月には、CTスキャンによる再評価が行われ、散在する多数の両側性肺結節のサイズと数が顕著に減少したことを示した。しかしながら、11月までに、主な結節の1つが0.5〜0.8cmまで拡大していることがCTスキャンにより判明し、病気が進行していることを示した。1日目にゲムシタビン、続いて8日目にゲムシタビンおよびドセタキセルからなる新たな治療が決められた。しかしながら、最初にゲムシタビンを総量(900mg/m2)投与した後、患者の好中球減少(図9A)および血小板減少(図9D)が長引き、そのためその後の治療を中止しなければならなくなった。第2のサイクルでは、患者へのゲムシタビンの投与量を減らした(720mg/m2)が、再び長期に亘る好中球減少および血小板減少がみられ、当初のスケジュールを完遂することは困難であった。第3サイクルの前に、患者は化学療法前62時間と化学療法後24時間の絶食を行った。患者は、絶食を行ったか否かにかかわらず、副作用を報告することはなかったが、興味深いことに、血液検査は絶食−化学療法治療の間に顕著な改善を示した(図10)。最下点はあまり明瞭でないが、最高点はANC、リンパ球およびWBC数においてはかなり高くなっていく傾向が認められた(それぞれ図9A、B、C;表2)。さらに、第1および第2の化学療法サイクルの間、ゲムシタビン単独では、血小板数が急速かつ大幅に減少し、回復にそれぞれ11および12日を要した(表2)。しかしながら、最初の絶食−化学療法併用治療(第3サイクル)の後は、血小板数は減少せず、むしろ増加した(図9D)。先の化学療法単独治療と比べて、血小板の最下点はより低い値となったが、これは、3種類の化学療法薬の相加効果で説明できよう(図9D;表2)。それにもかかわらず、化学療法単独と比較すれば、絶食−化学療法治療の間は、血小板数の最高点と正常値への回復時間は、それぞれきわめて明瞭であり、かつ短縮された(図9D;表2)。複数回の絶食/化学療法後の血小板の、この顕著な改善と急速な回復は、患者が化学療法治療を完遂させるのを可能としたばかりでなく、この戦略が、血液細胞前駆体に対する保護効果を有し得るものであり、血小板および顆粒球の急速な再増殖を可能にすることを示唆している。
1998年7月にグリーソンスコアー8の前立腺腺癌と診断された66歳の白人男性。同年に実施したProstaScint検査では、右腸骨リンパ節に放射性トレーサーの明白な吸収がみられ、ステージD1の病気と一致した。1998年に、患者は初めて、酢酸リュープロリドとビカルタミドによる治療を受けた。1999年9月には、これらの薬剤を減らして、フィナステライドが処方された。2000年12月、CTスキャンから、病気の局所進行が疑われた。彼は、酢酸リュープロリドによる第2サイクルを開始し、また高線量率(HDR)近接照射療法、および強度変調放射線療法(IMRT)による外部ビーム照射も受けた。病気をコントロールするために、ビカルタミド、トリプトレリンパモ酸塩およびナンドロロンなどの複数の薬剤を使用する相補的治療を行った。しかしながら、治療を止める度に、彼のPSA値は急激に上昇した。2008年4月、Combidexスキャンにより、3×5cmの骨盤腔内腫瘤と左の水腎症が見つかり、同年6月には、新たなPSA値の逆戻りがあり、そしてまた新たなCTスキャン測定により、さらに左腸骨領域の腫瘤を確認したため、DTXによる治療が促された。患者は、化学療法前60〜66時間と化学療法後8〜24時間の絶食を行うことを決めた(表3)。絶食中、患者は意識が朦朧とし、血圧が大きく低下する経験をしたが、化学療法後の自己申告による副作用は、7回の連続DTXサイクル後に発現した足の軽度の振動感覚以外にはほとんど何もなかった(図12)。患者の検査結果を解析すると、ANC、WBC,血小板およびリンパ球数は正常の範囲に維持されていたが、赤血球とその関連パラメータ(ヘマトクリットおよびヘモグロビン)はそうでなかった(図11A〜G)。このことは、血液細胞の中には絶食依存性の保護の利益を受け得るものがあり、その他はそうでないことを示唆している。最後に、サイクルを通してPSA値は一貫して減少傾向を示したが、これは絶食が前立腺癌細胞の殺滅を妨げなかったことを立証するものである(図11H)。
ステージIIAの乳癌(HER2+)と診断された53歳の白人女性患者。2008年に行われた乳腺腫瘤摘出手術後、患者は21日毎に予定された4サイクルの化学療法を受けた。投与計画にはDXT(75mg/m2)およびCP(600mg/m2)が含まれた。4サイクルを通して、患者は化学療法実施前64時間と化学療法実施後24時間の絶食を行った。報告された副作用には、軽度の衰弱および軽度の短期記憶障害が含まれた(図13)
乳癌と診断され、補助化学療法が推奨された乳癌と診断された48歳の白人女性患者。彼女の化学療法は、21日スケジュールの4サイクルのCP(1100mg)併用ドキソルビシン(DXR)(110mg)と、それに続く、週1回の頻度による12週のパクリタキセルおよびトラスツズマブからなるものであった。患者は、最初の化学療法治療の前に、48時間の絶食を行ったが、副作用の言及はなかった。第2のサイクルの間、患者は化学療法前60時間と、薬剤投与後5時間の絶食を組み込んだ。興味深いことに、彼女は絶食を行うことにいかなる困難も示さなかった。彼女は脱毛と軽度の衰弱を経験したが、化学療法でよく報告されている他の副作用に苦しむことはなかった(図14)。
RER2陽性乳癌と診断された78歳の白人女性。診断時および複雑な乳腺腫瘤摘出手術の後、患者は乳房全切除術を受けた。G−CSF(Neulasta)を補ったCBDCA400mg(AUC=6)、DTX(75mg/m2)による6サイクルの補助化学療法と、その後の6か月までのトラスツズマブによる化学療法が、腫瘍学者により指示された(表3)。化学療法治療の期間を通して、患者は薬剤投与の前後に絶食を行った。患者は変動がある絶食法を採用したが、重度の副作用は経験しなかった(図16;表3)。さらに血液検査の結果では、WBC、ANC、血小板およびリンパ球の数は、治療期間を通して正常な範囲であった(図15A〜D)。
メジアン年齢が61歳(44〜78歳の範囲)の、女性7人および男性3人の、化学療法を受けている10人の癌患者が、この研究に参加している。4人は乳癌を患い、2人は前立腺癌、そして4人は卵巣癌、子宮、肺の非小細胞癌または食道腺癌を患っていた。患者は全員、彼らを治療する腫瘍学者の監視の下、化学療法前に合計48〜140時間の絶食および/または化学療法後24〜56時間の絶食を自発的に行った。全ての症例で、絶食によく耐えることができた。空腹および血圧低下が、長い絶食の後に患者が言う共通の症状であった。
癌治療中に一般に推奨される食は、栄養不足を防止または高める、脂肪のない体を保護する、栄養が関係する副作用(食欲減退、悪心、味覚の変化、または腸の変化など)を最小にするという総合的な目標に基づく(Doyle、Nutrition and Physical Activity During and After Cancer Treatment、2006)。化学療法後の標準的な食とは対照的に、このシリーズの大部分の患者は、疲労、衰弱、悪心、嘔吐および腹部痙攣などの副作用が軽減されるため、絶食は実行可能であり、有益であると報告した。絶食中に、眩暈、空腹または頭痛などの軽い症状は生じたが、仕事を含む通常な活動を妨げるほどのレベルではなかった。
図18を参照すると、絶食は悪性細胞の放射線照射に対する感受性を高める。マウス乳癌(4T1−luc)細胞を96ウェルの細胞培養プレートに播種し(20,000/ウェル)、平衡化させ、48時間かけて培養密度に到達させた。その後、放射線照射前の48時間、培地を低または高グルコース培地のいずれかに切り替えた(5または10Gy;図18A、18B)。生存率をMTT試験により測定した(図18C)。統計的分析をStudentのt−検定(N=60)により行った。
絶食により引き起こされるエネルギー源、成長因子および他の細胞外因子の多くの変化が、保護を阻害するだけでなく、多様な癌細胞の化学療法薬に対する感受性の増大を促進するという仮説を試験した。
細胞培養
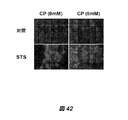
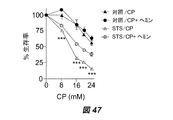
4T1−lucマウス乳癌細胞は、SibTech社(Brookfield、CT)から購入した。B16−flucマウスメラノーマ細胞は、Noah Craft(UCLA)から提供された。GL26マウスグリオーマ、U87−MGヒト神経膠芽細胞腫の細胞は、Thomas Chen(USC)から提供された。PC3および22RV1ヒト前立腺癌細胞は、Pinchas Cohen(UCLA)から提供された。MCF−7およびC42Bヒト乳癌細胞と、HeLaヒト子宮頚癌細胞は、Amy Lee(USC)から提供された。LOVOヒト結腸癌細胞は、Darryl Shibata(USC)から提供された。NXS2およびNeuro−2aマウス神経芽細胞腫、ヒトACNおよびSH−SY5Y神経芽細胞腫、OVCARヒト卵巣癌、MZ−MELヒトメラノーマ、A431類表皮癌細胞は、Gaslini InstituteのLaboratory of Oncologyで常法により培養された。4T1にはLC3−GFPが安定に移入されており、これは、USCのJae Jungからの自己貪食の研究に対する親切な贈り物であった。全ての細胞は、常法により、DMEM10%FBS中、37℃、5%CO2下で維持した。自己貪食を回避するために、インビトロでのSTS中、5μMのクロロキン(CQ)で細胞を48時間処理した。HO−1の活性を調節するために、4T1細胞を、化学療法治療前の24時間と、化学療法治療中の24時間、10μMのヘミン(Sigma)、または20μMの亜鉛プロトポルフィリン(ZnPP;Sigma)で処理した。
ドキソルビシン(DXR;Bedford Laboratories、USA)およびシクロホスファミド(CP;Baxter、USA)は、インビトロおよびインビボで使用した。
University of Southern CaliforniaのInstitutional Animal Care and Use Committeeと、Italy、GenoaのNational cancer Research Instituteのライセンスおよび倫理委員会により、そしてまたItalian Ministry of Healthにより認められている手順にしたがって、全ての動物実験を行った。皮下癌マウスモデルの作成には、12週齢のメスBALB/c、12週齢のメスおよびオスのC57BL/6マウス、ならびに7週齢のヌードマウスに、4T1乳癌細胞、B16メラノーマおよびGL26グリオーマ細胞、ならびにACNヒト神経芽細胞腫細胞をそれぞれ注射した。転移癌マウスモデルでは、12週齢のメスBALB/c、12週齢のメスおよびオスのC57BL/6マウスに、それぞれ2×105の4T1、B16、GL26細胞を、尾側部静脈から静脈注射し、6週齢のメスA/Jマウスに、2×105のNXS2および1×106のNeuro−2a細胞を、尾側部静脈から注射した。注射の前に、成長の対数期にある細胞を集め、2×106細胞/mlでPBSに懸濁させ、100μL(2×105細胞/マウス)を腰背部へ皮下注射、または尾側部静脈から静脈注射した。ACNおよびNeuro−2a細胞は、5×107および1×107細胞/mlの濃度でPBSに懸濁させ、それぞれ100μL(5×106ACN細胞/マウスおよび1×106Neuro−2a細胞/マウス)を腰背部へ皮下注射、または尾側部静脈から静脈注射した。全てのマウスは、皮下腫瘍注射の前に体毛を剃り、また静脈注射の前に穏やかに温めて静脈を膨張させた。定期的に体重を測定し、腫瘍サイズをデジタルノギスにより測定した。腫瘍体積を次式:腫瘍体積(mm3)=(長さ×幅×高さ)×π/6(長さ、幅および高さの単位はmmである)により算出した。
絶食マウスおよび通常給餌マウスの血中グルコースの測定に基づき、グルコースおよび/または血清を制限することにより、細胞を飢餓状態にした(低濃度約0.5g/Lおよび高濃度約2.0g/L)。ヒト細胞株には、通常のグルコースは1.0g/Lであるとみなした。絶食培地に変更する前に、細胞をPBSで2回洗浄した。
餌を完全に取り去ったが、水は自由に飲めるようにして、動物をトータルで48〜60時間、絶食させた。マウスは、共食い、食糞および残留飼料を減少させるために、一匹ずつ清潔な新しいケージに入れた。絶食の直前、直後に体重を測定した。
臭化メチルチアゾリルジフェニルテトラゾリウム(MTT)を還元する能力によって細胞毒性を測定した。簡単に説明すると、MTTをPBS中に5mg/mlの濃度で溶解し、測定用として0.5mg/mlの最終濃度に希釈し、37℃で3〜4時間インキュベートした。ホルマザンの結晶を、37℃で100μlの溶解緩衝液(SDS15%(w/v)、ジメチルホルムアミド50%(v/v)、pH4.7)に終夜(16時間)溶解した。生存率は、対照細胞に対する処理細胞のMTT還元レベルのパーセントで表示した。吸光度は、マイクロプレートリーダーSpectraMax250(Molecular Devices)およびSoftMax Pro 3.0ソフトウェア(Molecular Devices)を使用して570nmで読み取った。
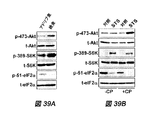
氷冷PBS中で細胞を一度洗浄し、プロテアーゼ阻害剤(Roche)およびホスファターゼ阻害剤のカクテル(Sigma)を含むRIPAlysis緩衝液中に集めた。同じプロテアーゼおよびホスファターゼ阻害剤を添加したRIPAlysis緩衝液中で腫瘍細胞を均質化した。全溶解液からのタンパク質を8〜12%のSDS−PAGEに溶解し、GAPDH、Aktおよびホスフォ−Ser473Akt、P70S6キナーゼおよびホスフォ−Thr389p70S6キナーゼ、eIF2αおよびホスフォ−Ser51 eIF2α用抗体(1:1000〜2000、Cell Signaling Technology)使用し、免疫ブロット法により分析した。
細胞を培地中(10%FBSを含むDMEM/F12)、105/mlに希釈し、50μMのDXRにより37℃で1時間処理した。その後、氷冷PBSで細胞を1回洗浄し、製造業者が推奨する手順にしたがってCometAssay(Trevigen,Inc、Gaithersburg、MD)に供した。コメット像をNikon Eclipse TE300蛍光顕微鏡により取得し、ソフトウェアComet Score(TriTek Corp.、バージョン1.5)で分析した。遺伝子型/処理グループ毎に100〜300の細胞を採点した。
マウスを2%イソフルラン吸入薬で麻酔し、左心室穿刺により血液を採取した。血液はK2−EDTAでコーティングしたチューブに採取し、血清を処理した(BD、USA)。血中グルコース値をPrecision Xtra血中グルコース値モニタリングシステム(Abbott Laboratories、USA)を使用して測定した。
Qiagen製RNeasyキット(カタログ番号74106)を使用し、製造者から示された手順にしたがって、組織からRNAを単離した。その後、IlluminaBeadchips(San Diego、CA)製のBD−202−0202チップにRNAをハイブリダイズした。先述したように、生データをZ正規化した。ANOVAフィルタリング(ANOVA p<0.05)を使用し、SAMプロトコールにしたがって、パラメータ化した有意性検定を行った。有意な遺伝子をそれぞれの対比較のために選択する。先述したPAGE法を使用して遺伝子セットの濃縮を試験した。Gene Ontology Database and Pathway Data Setにより提供される名前と説明に基づいて図面を選択した。さらに、Ingenuity Pathway Analysis System(Ingenuity Systems;Redwood City、CA)を使用し、遺伝子の系統的関係および標準経路の分析を行う。
Qiagen製RNeasyキット(カタログ番号74106)を使用し、製造業者から示された手順にしたがって組織からRNAを単離した。High Capacity cDNA Reverse Transcription Kit(AB Applied Biosystems カタログ番号4368814)を使用してcDNAを合成し、SYBR Green PCR master mix(AB Applied Biosystems カタログ番号4309159)を使用してRT−PCRを行った。キャリブレータ遺伝子としてGAPDH遺伝子を使用した。分析したそれぞれの処理は、3つの生物学的レプリカを使用して行い、少なくとも3つの反応を使用して、発現を計算した。発現比を2−ΔΔCP法にしたがって計算した。
化学療法を受けている癌患者の食計画を確認するために、様々な食組成をマウスモデルで試験した。目標点は、ホストの保護と広範な癌細胞の増感に有効であるとわかっている、血清グルコースおよび/またはIGF−1を20〜75%低下させることである。組成は、通常の体重を十分に維持することができるだけの栄養レベルが提供されるように選択される。毎日の食物摂取量、体重、および一般的健康(動作および身体的外見)がモニターされる。各給餌スケジュールの終わりには、グルコースおよびIGF−1の測定のために採血する。通常の総カロリーを有するが、特定のアミノ酸が不足している食(AA−D)では、5日間の給餌で(図52)、血清IGF−1(図52)とグルコース(図54A)は顕著に低下することがわかった。短期飢餓の後にAA−D食が続く再給餌パラダイム(図53および54B)で使用すれば、この有益な効果は増大する。
Claims (28)
- 癌の増殖または癌の症状を軽減する方法において、
a)癌患者を同定するステップと
b)前記患者に、第1の所定期間、第1の食を提供するステップであって、前記第1の食は、前記患者が通常摂取するカロリーの最大でも50%を前記患者に与え、前記キロカロリーの少なくとも50%は脂肪から得るステップと、
c)前記患者に、第2の所定期間、第2の食を提供するステップであって、前記第2の食は、前記患者に、最大500kcal/日を与えるステップと
を含むことを特徴とする方法。 - 請求項1に記載の方法において、前記第1の所定期間が約1日であり、かつ前記第2の所定期間が約3日であることを特徴とする方法。
- 請求項1に記載の方法において、前記第2の食は、前記患者に最大200kcal/日を与えることを特徴とする方法。
- 請求項1に記載の方法において、前記第1の食は、前記患者に700〜1200kcal/日を与えることを特徴とする方法。
- 請求項1に記載の方法において、
前記患者に、第3の所定期間、第3の食を提供するステップであって、前記第3の食は、前記患者が通常摂取するカロリーの50%を超えるカロリーを有する食品と補充組成物とを含み、前記補充組成物は必須アミノ酸を含むステップをさらに含むことを特徴とする方法。 - 請求項5に記載の方法において、前記第3の所定期間が少なくとも5日であることを特徴とする方法。
- 請求項5に記載の方法において、前記補充組成物が、野菜抽出物源、オメガ−3/6必須脂肪酸、タンパク質および/または必須アミノ酸と非必須アミノ酸、ビタミン、ミネラル、並びにそれらの組み合わせからなる群から選択される成分をさらに含むことを特徴とする方法。
- 請求項1に記載の方法において、前記患者の血清中のIGF−I濃度を、25〜90%減少させることを特徴とする方法。
- 請求項1に記載の方法において、前記患者の血中グルコース濃度を、25〜75%減少させることを特徴とする方法。
- 癌の化学療法薬に対する感受性を高める方法において、
a)癌患者を同定するステップ、および
b)前記患者に、第1の所定期間、第1の食を提供するステップであって、前記第1の食は、前記患者が通常摂取するカロリーの最大でも50%を前記患者に与え、前記キロカロリーの少なくとも50%は脂肪から得るステップ、
c)前記患者に、第2の所定期間、第2の食を提供するステップであって、前記第2の食は、前記患者に、最大500kcal/日を与えるステップ、および
d)前記患者が前記第2の食を少なくとも48時間摂取している間、またはその後に、化学療法薬剤を前記患者に投与するステップ
を含むことを特徴とする方法。 - 請求項10に記載の方法において、前記化学療法薬剤が、DNAアルキル化剤、オキシダントまたはトポイソメラーゼ阻害薬であることを特徴とする方法。
- 請求項10に記載の方法において、前記化学療法薬剤が、メチルメタンスルホネート、シクロホスファミド、エトポシド、ドキソルビシン、またはメナジオンシスプラチン、カルボプラチン、および他のプラチナベースの薬剤、ゲムシタビン、ドセタキセル、5−FU、またはトポイソメラーゼ阻害薬であることを特徴とする方法。
- 請求項10に記載の方法において、前記癌が、皮膚癌、結腸癌、乳癌、食道癌、前立腺癌、肺癌、子宮癌、卵巣癌、および前立腺癌、またはグリオーマ、メラノーマ、神経芽細胞腫、褐色細胞腫であることを特徴とする方法。
- 請求項10に記載の方法において、前記患者に前記第1の食および前記第2の食が与えられないとき、前記化学療法薬剤は、前記化学療法薬剤の標準の実施基準よりも長期間投与されることを特徴とする方法。
- 請求項10に記載の方法において、前記化学療法薬剤の長期投与中、前記第1および前記第2の食が投与されることを特徴とする方法。
- 請求項10に記載の方法において、前記患者に前記第1の食および前記第2の食が与えられないとき、前記化学療法薬剤は、前記化学療法薬剤の標準の実施基準よりも短期間投与されることを特徴とする方法。
- 請求項10に記載の方法において、前記化学療法薬剤が、通常与えられる量より少なくとも10%多く投与されることを特徴とする方法。
- 請求項10に記載の方法において、前記化学療法薬剤が、通常与えられる量より少なくとも10%少なく投与されることを特徴とする方法。
- 請求項10に記載の方法において、ステップb)の前に、前記患者が化学療法に関連する毒性症状を示していることを特徴とする方法。
- 請求項10に記載の方法において、ステップb)の前に、前記患者が末期と診断されていることを特徴とする方法。
- 請求項10に記載の方法において、前記第1の所定期間が約1日であり、かつ前記第2の所定期間が約3日であることを特徴とする方法。
- 請求項10に記載の方法において、前記第2の食が最大200kcal/日であることを特徴とする方法。
- 請求項10に記載の方法において、前記患者に、第3の所定期間、第3の食を提供するステップであって、前記患者の通常の食を補う前記第3の食が補充組成物を含み、前記補充組成物は必須アミノ酸および他のアミノ酸を含むステップをさらに含むことを特徴とする方法。
- 請求項23に記載の方法において、前記第3の所定期間が少なくとも5日であることを特徴とする方法。
- 請求項23に記載の方法において、前記補充組成物が、野菜抽出物源、オメガ−3/6必須脂肪酸、非必須アミノ酸、ミネラル、およびそれらの組み合わせからなる群から選択される成分をさらに含むことを特徴とする方法。
- 癌の放射線療法に対する感受性を高める方法において、
a)癌患者を同定するステップ、および
b)前記患者に、第1の所定期間、第1の食を提供するステップであって、前記第1の食は、前記患者が通常摂取するカロリーの最大でも50%を前記患者に与え、前記キロカロリーの少なくとも50%は脂肪から得るステップ、
c)前記患者に、第2の所定期間、第2の食を提供するステップであって、前記第2の食は、前記患者に、最大500kcal/日を与えるステップ、および
d)前記患者が前記第2の食を少なくとも48時間摂取している間、またはその後に、放射線療法を前記患者に実施するステップ
を含むことを特徴とする方法。 - 癌患者に食事を提供するための、癌の増殖を抑制し、化学療法薬の効果を高める治療食パッケージであって、
前記患者が通常摂取するカロリーの最大でも50%を前記癌患者に与え、前記キロカロリーの少なくとも50%を脂肪から得る食事に分割され、第1の所定期間に十分な量の食事を提供する第1の食のコンポーネントと、
前記癌患者に最大500kcal/日を与える食事に分割され、第2の所定期間に十分な量の食事を提供する第2の食事コンポーネントと、
必須アミノ酸および他の非必須アミノ酸、必須脂肪酸、ミネラル、ビタミン、並びに/または野菜抽出物を含む、第3の所定期間のための補充組成物と、
前記第1の食のコンポーネントおよび前記第2の食事コンポーネントを前記癌患者に与えるための使用説明書と
を含むことを特徴とする治療食パッケージ。 - 請求項27に記載の治療食パッケージにおいて、前記第1の食のコンポーネント、前記第2の食事コンポーネント、および前記第3食コンポーネントはそれぞれ独立して、野菜抽出物、ミネラル、オメガ−3/6必須脂肪酸、およびそれらの組み合わせからなる群から選択される成分を含んでいることを特徴とする治療食パッケージ。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US25415409P | 2009-10-22 | 2009-10-22 | |
| US61/254,154 | 2009-10-22 | ||
| PCT/US2010/053821 WO2011050302A2 (en) | 2009-10-22 | 2010-10-22 | Methods and nutritional formulations to increase the efficacy and reduce the side effects of cancer treatment |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013508411A true JP2013508411A (ja) | 2013-03-07 |
| JP2013508411A5 JP2013508411A5 (ja) | 2013-11-21 |
Family
ID=43900993
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012535426A Pending JP2013508411A (ja) | 2009-10-22 | 2010-10-22 | 癌治療の効果を高め、その副作用を軽減する方法および栄養製剤 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US20110118528A1 (ja) |
| EP (1) | EP2490684B1 (ja) |
| JP (1) | JP2013508411A (ja) |
| CN (1) | CN102753162A (ja) |
| AU (2) | AU2010310515B2 (ja) |
| BR (1) | BR112012009423A2 (ja) |
| CA (1) | CA2779282C (ja) |
| DK (1) | DK2490684T3 (ja) |
| ES (1) | ES2659353T3 (ja) |
| PL (1) | PL2490684T3 (ja) |
| PT (1) | PT2490684T (ja) |
| RU (1) | RU2549954C2 (ja) |
| WO (1) | WO2011050302A2 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017509671A (ja) * | 2014-03-28 | 2017-04-06 | ウニベルシタ デリィ ストゥディ ディ ジェノバ | カロリー摂取量減少と協同したがん治療方法で使用されるチロシンキナーゼ阻害剤 |
| JP2017513460A (ja) * | 2014-03-06 | 2017-06-01 | ユニヴァーシティ オブ サザン カリフォルニアUniversity of Southern California | 従来の化学療法剤の効力および実行可能性を増強し、かつ正常な細胞および組織におけるキナーゼの副作用を逆転させるための、キナーゼ阻害剤と併用した短期間絶食レジメンの使用 |
| JP2019504073A (ja) * | 2016-01-12 | 2019-02-14 | ユニバーシティ オブ サザン カリフォルニア | 多発性骨髄腫及び他のがんに対する食事療法としての長期断食模倣の使用 |
| JP7376718B2 (ja) | 2019-12-13 | 2023-11-08 | 株式会社ベリタスバイオセラピューティクス | 癌の予防または治療用薬学組成物 |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2822178T3 (es) * | 2012-10-22 | 2021-04-29 | Univ Southern California | Formulaciones dietéticas que promueven la regeneración de tejidos/órganos |
| AU2014216349B2 (en) * | 2013-02-12 | 2019-10-24 | University Of Southern California | Methods and diets to protect against chemotoxicity and age related illnesses |
| EP3915399A1 (en) | 2013-07-01 | 2021-12-01 | University of Southern California | Fasting condition as dietary treatment of diabetes |
| US10172839B2 (en) | 2014-03-06 | 2019-01-08 | University Of Southern California | Use of short term starvation regimen in combination with kinase inhibitors to enhance traditional chemo-drug efficacy and feasibility and reverse side effects of kinases in normal cells and tissues |
| WO2015153850A2 (en) * | 2014-04-02 | 2015-10-08 | University Of Southern California | Autoimmunity and multiple sclerosis treatment |
| WO2016168802A2 (en) | 2015-04-16 | 2016-10-20 | University Of Southern California | Fasting mimicking diet (fmd) and glucose lowering drugs protect normal cells and generate cancer sensitizing conditions in response to standard and high glucose conditions induced by rapamycin and dexamethasone |
| KR20180016380A (ko) | 2015-05-06 | 2018-02-14 | 유니버시티 오브 써던 캘리포니아 | 고혈압 및 지질 장애를 치료하기 위한 금식 모방 및 향상된 규정식 |
| CN108601838A (zh) * | 2015-09-21 | 2018-09-28 | 意大利癌症研究基金会分子肿瘤学研究所(Ifom) | 对抗血液癌症的新治疗策略 |
| US10660932B2 (en) | 2016-02-15 | 2020-05-26 | University Of Southern California | Drug combinations and methods to stimulate embryonic-like regeneration to treat diabetes and other diseases |
| BR112018073155A2 (pt) | 2016-05-11 | 2019-03-12 | University Of Southern California | método para tratar doença autoimune e/ou inflamatória, e pacote de dieta |
| IT201700008499A1 (it) | 2017-01-26 | 2018-07-26 | Univ Degli Studi Genova | Composizione dietetica per la prevenzione e/o il trattamento dell’iperplasia dell’endometrio |
| US11284640B2 (en) | 2017-02-14 | 2022-03-29 | University Of Southern California | Fasting mimicking diet |
| CN107951892A (zh) * | 2018-01-19 | 2018-04-24 | 丽水学院 | 锌原卟啉在制备增强人结直肠癌细胞对5-氟尿嘧啶化疗敏感性药物中的应用 |
| CA3092354A1 (en) | 2018-03-15 | 2019-09-19 | University Of Southern California | Fasting-mimicking diet (fmd) but not water-only fasting promotes reversal of inflammation and ibd pathology |
| WO2020015842A1 (en) * | 2018-07-18 | 2020-01-23 | Michalsen Andreas | Effects of a short-term fasting mimicking diet on quality of life and tolerance to chemotherapy in patients with cancer |
| US20200146320A1 (en) | 2018-11-09 | 2020-05-14 | L-Nutra | Nutrition bar for intermittent fasting-mimicking |
| MX2021013901A (es) | 2019-05-14 | 2022-04-12 | Tyme Inc | Composiciones y métodos para el tratamiento del cáncer. |
| IT202000007153A1 (it) | 2020-04-03 | 2021-10-03 | Ifom Fondazione St Firc Di Oncologia Molecolare | Apporto calorico ridotto e immunoterapia per il trattamento del cancro |
| US10905698B1 (en) | 2020-05-14 | 2021-02-02 | Tyme, Inc. | Methods of treating SARS-COV-2 infections |
| EP4262438A1 (en) * | 2020-12-17 | 2023-10-25 | Fondazione IRCCS Istituto Nazionale dei Tumori | Diet preparation for the nutrition of cancer patients with a restricted calorie intake |
| EP4066823A1 (en) | 2021-03-30 | 2022-10-05 | IFOM Fondazione Istituto Firc di Oncologia Molecolare | Reduced caloric intake and anticancer agents for the treatment of cancer |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001515510A (ja) * | 1997-03-17 | 2001-09-18 | ビーティージー・インターナショナル・リミテッド | 治療用組成物 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2074731C1 (ru) * | 1994-12-29 | 1997-03-10 | Игорь Александрович Бойко | Фитокомплекс, обладающий противоопухолевым действием, и способ лечения онкологических больных |
| AU5319499A (en) * | 1999-07-22 | 2001-02-13 | Ivan L. Cameron | Fatty acids to minimize cancer therapy side effects |
| US20070275934A1 (en) * | 2004-05-10 | 2007-11-29 | Curd John G | Treatment of pancreatic cancer with active vitamin d compounds in combination with other treatments |
| WO2006043966A2 (en) * | 2004-10-15 | 2006-04-27 | University Of Tennessee Research Foundation | Methods for inducing apoptosis in adipocytes |
| US20070116802A1 (en) * | 2005-11-23 | 2007-05-24 | Carl Germano | High quality caloric composition |
| US20080038367A1 (en) * | 2006-08-11 | 2008-02-14 | Sal Saloum | Nutritional supplement compositions and methods of preparing |
| RU2354369C2 (ru) * | 2007-03-16 | 2009-05-10 | Михаил Владимирович Кутушов | Применение родамина 6ж в качестве лекарственного средства для лечения злокачественных новообразований и амилоидозов |
| AU2008329988A1 (en) * | 2007-11-26 | 2009-06-04 | Nestec S.A. | Compositions and methods for inhibiting the activation of dsRNA-dependent protein kinase and tumor growth inhibition |
-
2010
- 2010-10-22 AU AU2010310515A patent/AU2010310515B2/en active Active
- 2010-10-22 US US12/910,508 patent/US20110118528A1/en not_active Abandoned
- 2010-10-22 EP EP10825771.8A patent/EP2490684B1/en active Active
- 2010-10-22 ES ES10825771.8T patent/ES2659353T3/es active Active
- 2010-10-22 WO PCT/US2010/053821 patent/WO2011050302A2/en active Application Filing
- 2010-10-22 JP JP2012535426A patent/JP2013508411A/ja active Pending
- 2010-10-22 PT PT108257718T patent/PT2490684T/pt unknown
- 2010-10-22 BR BR112012009423A patent/BR112012009423A2/pt not_active Application Discontinuation
- 2010-10-22 CN CN2010800560747A patent/CN102753162A/zh active Pending
- 2010-10-22 CA CA2779282A patent/CA2779282C/en active Active
- 2010-10-22 PL PL10825771T patent/PL2490684T3/pl unknown
- 2010-10-22 DK DK10825771.8T patent/DK2490684T3/en active
- 2010-10-22 RU RU2012118588/15A patent/RU2549954C2/ru active
-
2016
- 2016-03-11 AU AU2016201607A patent/AU2016201607B2/en active Active
-
2021
- 2021-03-17 US US17/204,419 patent/US20210209516A1/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001515510A (ja) * | 1997-03-17 | 2001-09-18 | ビーティージー・インターナショナル・リミテッド | 治療用組成物 |
Non-Patent Citations (1)
| Title |
|---|
| SERVING VEGETARIANS A GUIDE FOR THE CATERING INDUSTRY,2006,, JPN6014039547, 2006, pages 1 - 16, ISSN: 0002901105 * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017513460A (ja) * | 2014-03-06 | 2017-06-01 | ユニヴァーシティ オブ サザン カリフォルニアUniversity of Southern California | 従来の化学療法剤の効力および実行可能性を増強し、かつ正常な細胞および組織におけるキナーゼの副作用を逆転させるための、キナーゼ阻害剤と併用した短期間絶食レジメンの使用 |
| JP2021020926A (ja) * | 2014-03-06 | 2021-02-18 | ユニヴァーシティ オブ サザン カリフォルニアUniversity of Southern California | 従来の化学療法剤の効力および実行可能性を増強し、かつ正常な細胞および組織におけるキナーゼの副作用を逆転させるための、キナーゼ阻害剤と併用した短期間絶食レジメンの使用 |
| JP7038432B2 (ja) | 2014-03-06 | 2022-03-18 | ユニヴァーシティ オブ サザン カリフォルニア | 従来の化学療法剤の効力および実行可能性を増強し、かつ正常な細胞および組織におけるキナーゼの副作用を逆転させるための、キナーゼ阻害剤と併用した短期間絶食レジメンの使用 |
| JP2017509671A (ja) * | 2014-03-28 | 2017-04-06 | ウニベルシタ デリィ ストゥディ ディ ジェノバ | カロリー摂取量減少と協同したがん治療方法で使用されるチロシンキナーゼ阻害剤 |
| JP2020147598A (ja) * | 2014-03-28 | 2020-09-17 | ウニベルシタ デリィ ストゥディ ディ ジェノバ | カロリー摂取量減少と協同したがん治療方法で使用されるチロシンキナーゼ阻害剤 |
| JP2019504073A (ja) * | 2016-01-12 | 2019-02-14 | ユニバーシティ オブ サザン カリフォルニア | 多発性骨髄腫及び他のがんに対する食事療法としての長期断食模倣の使用 |
| JP2021183622A (ja) * | 2016-01-12 | 2021-12-02 | ユニバーシティ オブ サザン カリフォルニア | 多発性骨髄腫及び他のがんに対する食事療法としての長期断食模倣の使用 |
| JP7376718B2 (ja) | 2019-12-13 | 2023-11-08 | 株式会社ベリタスバイオセラピューティクス | 癌の予防または治療用薬学組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102753162A (zh) | 2012-10-24 |
| ES2659353T3 (es) | 2018-03-14 |
| AU2016201607B2 (en) | 2017-11-30 |
| BR112012009423A2 (pt) | 2017-06-13 |
| US20110118528A1 (en) | 2011-05-19 |
| AU2016201607A1 (en) | 2016-03-31 |
| US20210209516A1 (en) | 2021-07-08 |
| EP2490684A4 (en) | 2016-05-04 |
| AU2010310515A1 (en) | 2012-05-17 |
| CA2779282C (en) | 2017-12-05 |
| RU2012118588A (ru) | 2013-11-27 |
| PL2490684T3 (pl) | 2018-07-31 |
| WO2011050302A3 (en) | 2011-08-25 |
| CA2779282A1 (en) | 2011-04-28 |
| EP2490684B1 (en) | 2018-01-03 |
| EP2490684A2 (en) | 2012-08-29 |
| DK2490684T3 (en) | 2018-04-09 |
| WO2011050302A2 (en) | 2011-04-28 |
| PT2490684T (pt) | 2018-04-02 |
| AU2010310515B2 (en) | 2016-01-07 |
| RU2549954C2 (ru) | 2015-05-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210209516A1 (en) | Methods and Nutritional Formulations to Increase the Efficacy and Reduce the Side Effects of Cancer Treatment | |
| JP7038432B2 (ja) | 従来の化学療法剤の効力および実行可能性を増強し、かつ正常な細胞および組織におけるキナーゼの副作用を逆転させるための、キナーゼ阻害剤と併用した短期間絶食レジメンの使用 | |
| JP7168943B2 (ja) | 癌における食事療法の開発 | |
| Morland et al. | n-3 polyunsaturated fatty acid supplementation during cancer chemotherapy | |
| ES2822178T3 (es) | Formulaciones dietéticas que promueven la regeneración de tejidos/órganos | |
| US10172839B2 (en) | Use of short term starvation regimen in combination with kinase inhibitors to enhance traditional chemo-drug efficacy and feasibility and reverse side effects of kinases in normal cells and tissues | |
| JP2021008491A (ja) | 正常細胞を保護し、かつラパマイシンおよびデキサメタゾンにより誘導される標準および高グルコース状態に反応して癌増感状態を生じさせる絶食模倣食(fmd)およびグルコース低下薬 | |
| Brandhorst | Fasting and fasting-mimicking diets for chemotherapy augmentation | |
| Evangeliou et al. | Restricted ketogenic diet therapy for primary lung cancer with metastasis to the brain: a case report | |
| JP2021183622A (ja) | 多発性骨髄腫及び他のがんに対する食事療法としての長期断食模倣の使用 | |
| Isaac-Lam et al. | Calorie restriction and breast cancer treatment: A mini-review | |
| Cipolla et al. | Treating metastatic castration-resistant prostate cancer with novel polyamine-free oral nutritional supplementation: Phase I study | |
| Van der Meij et al. | The effects of supplementation of n-3 polyunsaturated fatty acids on clinical outcome parameters in patients with cancer: a systematic review | |
| JP2020059699A (ja) | 難治性癌の食事療法およびそれに適した治療食 | |
| Ogilvie | Nutrition and cancer: polyunsaturated fatty acids and beyond. | |
| Wright | Evidence-Based Treatment of Digestive Symptoms in Pancreatic Cancer Patients | |
| Skorupski | Nutraceuticals: a role in the management of the cancer patient? | |
| Tat | Breast Cancer Guide-Encouraging Self-Study Among Patients of Non-Medical Scientific Professionals, Do it Yourself |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131004 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20131004 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140924 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20141205 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150224 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20150226 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150630 |