JP2011527695A - 2−メチレン−19,26−ジノル−(20r,22e,25r)−ビタミンd類似物質 - Google Patents
2−メチレン−19,26−ジノル−(20r,22e,25r)−ビタミンd類似物質 Download PDFInfo
- Publication number
- JP2011527695A JP2011527695A JP2011517601A JP2011517601A JP2011527695A JP 2011527695 A JP2011527695 A JP 2011527695A JP 2011517601 A JP2011517601 A JP 2011517601A JP 2011517601 A JP2011517601 A JP 2011517601A JP 2011527695 A JP2011527695 A JP 2011527695A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- administered
- day
- methylene
- formula
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C401/00—Irradiation products of cholesterol or its derivatives; Vitamin D derivatives, 9,10-seco cyclopenta[a]phenanthrene or analogues obtained by chemical preparation without irradiation
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/14—The ring being saturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2602/00—Systems containing two condensed rings
- C07C2602/02—Systems containing two condensed rings the rings having only two atoms in common
- C07C2602/14—All rings being cycloaliphatic
- C07C2602/24—All rings being cycloaliphatic the ring system containing nine carbon atoms, e.g. perhydroindane
Abstract
Description
(R)−(−)−1,3−ブタンジオール1(1g、11.1mmol)、DMAP(30mg、0.25mmol)、Et3N(4.6mL、3.33g、33mmol)の無水塩化メチレン(20mL)溶液を撹拌し、これに、p−トルエンスルホニルクロリド(2.54g、13.3mmol)を0℃で添加した。この反応混合物を、4℃で22時間攪拌した。塩化メチレンを添加し、混合物を水で洗浄し、乾燥し(Na2SO4)、減圧下で濃縮した。残渣をシリカゲルクロマトグラフィーによってヘキサン/酢酸エチル(8:2、次いで1:1)で精製して、トシレートを無色油状物として得た(2.17g、収率80%)。
2−位にメチレン基、及び側鎖の25−位(C−25)に接続したヒドロキシル置換基を導入すること、通常は側鎖の26位(C−26)に位置しているメチル基を、側鎖の25位にある炭素原子に結合した水素原子と置き換えること、および側鎖の炭素原子22と23(C−22とC−23)の間の位置への二重結合の導入は、1α,25−ジヒドロキシビタミンD3と比較して、全長組み換えラットビタミンD受容体に対するRR−22の結合にほとんど影響を及ぼさなかった。化合物RR−22は、標準物質1,25−(OH)2D3と比較して、核内ビタミンD受容体に対してほとんど同じ親和性で結合した(図1)。これらの結果から、化合物RR−22は、同等の生体活性を有するであろうと予想され得る。しかし、驚くべきことに、化合物RR−22は、固有の生体活性を有し、極めて選択的な類似物質である。
(ビタミンD受容体の結合)
(試験物質)
(タンパク質源)
全長組み換えラット受容体が、E.coli BL21(DE3)Codon Plus RIL細胞で発現され、2種類の異なるカラムクロマトグラフィーシステムを用いて均一になるように精製した。第1の系は、このタンパク質に対し、C−末端ヒスチジンタグを利用するニッケル親和性樹脂であった。この樹脂から溶出したタンパク質を、イオン交換クロマトグラフィー(S−Sepharose Fast Flow)を用いてさらに精製した。精製したタンパク質を等分し、液体窒素で迅速に凍結し、使用するまで−80℃で保存した。結合アッセイで使用するために、このタンパク質を、0.1% Chaps洗浄剤を含むTEDK50(50mM Tris、1.5mM EDTA、pH7.4、5mM DTT、150mM KCl)で希釈した。受容体タンパク質及びリガンド濃度は、受容体に結合する添加された放射能標識されたリガンドが20%を超えないように最適化された。
標識されていないリガンドを、エタノールに溶解し、UV分光光度法を用いて濃度を決定した(1,25(OH)2D3:モル吸光係数=18,200及びλmax=265nm;類似物質:モル吸光係数=42,000及びλmax=252nm)。放射能標識されたリガンド(3H−1,25(OH)2D3、約159Ci/mmole)を、最終濃度が1nMになるようにエタノールに添加した。
放射能標識されたリガンド及び標識されていないリガンドを、最終エタノール濃度が10%以下になるように希釈したタンパク質100mclに添加し、混合され、結合を平衡状態にするため、氷上で一晩インキュベーションした。次の日に、ヒドロキシルアパタイトスラリー(50%)100mclをそれぞれの管に添加し、10分間隔で30分間混合した。ヒドロキシルアパタイトを、遠心分離によって収集し、次いで、0.5% Titron X−100を含有するTris−EDTAバッファ(50mM Tris、1.5mM EDTA、pH7.4)で3回洗浄した。最後の洗浄が終わったら、Biosafe IIシンチレーションカクテル4mlを含有するシンチレーションバイアルにペレットを移し、混合して、シンチレーションカウンターに置いた。放射能標識されたリガンドのみを含む管から、全結合を決定した。
(試験物質)
(試験薬物)
試験薬物を、エタノールに溶解し、UV分光光度法を用いて濃度を決定した。細胞培養物中の最終エタノール濃度(≦0.2)を変えずに、さまざまな薬物濃度を試験することができるように、段階希釈物を調製した。
ヒト前骨髄球性白血病(HL60)細胞を、10%胎児ウシ血清を含有するRPMI−1640培地で成長させた。この細胞を、5%CO2存在下、37℃でインキュベーションした。
HL60細胞を、1.2×105細胞/mlで播種した。播種してから18時間後、2ッ組の細胞を、薬物で処理した。4日後、細胞を採集し、ニトロブルーテトラゾリウム還元アッセイを行った(Collins et al.、1979;J.Exp.Med.149:969−974)。分化した細胞の割合は、合計200細胞を計数し、細胞内に黒〜青色のホルマザンの沈殿を含む数を記録することによって決定した。単球細胞への分化の検証を、食作用活性を測定することによって決定した(データは示されていない)。
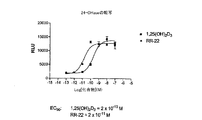
転写活性を、ルシフェラーゼレポーター遺伝子の上流の24−ヒドロキシラーゼ(24Ohase)遺伝子プロモーターで安定にトランスフェクトされたROS 17/2.8(骨)細胞で測定した(Arbour et al.、1998)。細胞に、さまざまな用量を与えた。投与の16時間後、細胞を採集し、ルシフェラーゼ活性を、照度計を用いて測定した。
雄の離乳期Sprague−Dawleyラットを、Diet 11(0.47% Ca)食餌+AEK油の状態に1週間置き、次いで、Diet 11(0.02% Ca)+AEK油の状態に3週間置いた。次いで、このラットを、0.47% Caを含む食餌に1週間変更し、次いで、0.02% Caを含有する食餌に2週間変更した。0.02% カルシウムの食餌の最後の週に、投与量の投与を開始した。約24時間の間隔をあけて、4回連続して腹腔内投与を行った。最後の投与から24時間後、切断された頸部から血液を採集し、血清カルシウム濃度を、骨のカルシウム動員の測定値として測定した。反転腸管法を用いて腸のカルシウム移動を分析するために、最初の腸10cmも採集した。
生物学的知見のまとめ。この化合物RR−22は、天然のホルモンよりもわずかに低い親和性でVDRに結合し、この活性において、1,25(OH)2D3よりも、効能が約1log低い、すなわち、約10分の1よりも低いと考えることができる。また、RR−22は、1,25(OH)2D3と比較して、約10倍以上の細胞分化活性を示し、約10倍以上のin vitroでの遺伝子転写活性を示す。この化合物は、in vitroでは1,25(OH)2D3よりも効能が強いが、天然ホルモンと比較して、in vivoでのカルシウム動員の活性が低く、腸では同様の活性又はこれより低い活性を示す。この化合物は、1,25(OH)2D3が活性を示す投与量よりも約3倍以上多い投与量で、骨においてなんら活性を示さない。RR−22は、骨の貯蔵庫からカルシウムを動員する効能は低いが、細胞分化における効能は高いため、すでに作られている化合物よりも安全性の範囲が大きい化合物をもたらすため、治療薬開発には潜在的に価値のある化合物である。この化合物は、比較的顕著な細胞分化及び転写活性を示すが、骨でのカルシウム血症活性はほとんど有していないため、種々の自己免疫疾患、癌、腎性骨ジストロフィー、乾癬又は他の皮膚疾患を患う患者を治療するのに有用であり得る。RR−22は、上に列挙した疾患の治療に有用なだけではなく、上に列挙した疾患の予防にも有用であろう。
RR−22(Ki=1x10−10M)は、全長組み換えラットビタミンD受容体に対する結合について、[3H]−1,25−(OH)2−D3と競合する能力に関し、天然ホルモンである1α,25−ジヒドロキシビタミンD3(Ki=5x10−11M)よりもほんのわずか活性が低い(図1)。RR−22は、1α,25−ジヒドロキシビタミンD3(EC50=2x10−9M)と比較した場合、HL−60の細胞分化を促進する能力(有効性又は効力)において、約1log以上、すなわち、約10倍以上の活性を示す(EC50=2x10−10M)(図2を参照)。また、化合物RR−22(EC50=2x10−11M)は、1α,25−ジヒドロキシビタミンD3(EC50=2x10−10M)よりも、骨細胞における転写活性が約10倍以上である(図3を参照)。これらの結果は、RR−22が、細胞分化、遺伝子転写を引き起こし、細胞成長を抑制するという直接的な細胞活性を有しているため、乾癬に極めて有効である可能性を示唆している。また、これらのデータは、RR−22が、抗癌剤として、特に、白血病、結腸癌、乳癌、皮膚癌、前立腺癌に対して顕著な活性を有する可能性を示しており、さらに、乾燥肌(皮膚の水分が失われること)、過度な皮膚のたるみ(不十分な皮膚の堅さ)、不十分な皮脂分泌、しわのような皮膚の状態に対して顕著な活性を有する可能性を示している。また、RR−22は、二次的な副甲状腺機能亢進症を抑制することに非常に活性があると予想されるであろう。
Claims (79)
- X3が水素である、請求項1に記載の化合物。
- X1が水素である、請求項1に記載の化合物。
- X1、X2、X3がすべてt−ブチルジメチルシリルである、請求項1に記載の化合物。
- 有効な量の請求項1に記載の少なくとも1つの化合物を、医薬的に許容される賦形剤とともに含有する、医薬組成物。
- 前記有効量が、前記組成物1gあたり約0.01μg〜約1000μgを含む、請求項5に記載の医薬組成物。
- 前記有効量が、前記組成物1gあたり約0.1μg〜約500μgを含む、請求項5に記載の医薬組成物。
- 有効な量の2−メチレン−19,26−ジノル−(20R,22E,25R)−1α,25−ジヒドロキシビタミンD3を、医薬的に許容される賦形剤とともに含有する、医薬組成物。
- 前記有効量が、前記組成物1gあたり約0.01μg〜約1000μgを含む、請求項9に記載の医薬組成物。
- 前記有効量が、前記組成物1gあたり約0.1μg〜約500μgを含む、請求項9に記載の医薬組成物。
- 前記化合物が経口投与される、請求項12に記載の方法。
- 前記化合物が非経口投与される、請求項12に記載の方法。
- 前記化合物が経皮投与される、請求項12に記載の方法。
- 前記化合物が局所投与される、請求項12に記載の方法。
- 前記化合物が直腸投与される、請求項12に記載の方法。
- 前記化合物が経鼻投与される、請求項12に記載の方法。
- 前記化合物が舌下投与される、請求項12に記載の方法。
- 前記化合物が、約0.01μg/日〜約1000μg/日の用量で投与される、請求項12に記載の方法。
- 前記化合物が経口投与される、請求項22に記載の方法。
- 前記化合物が非経口投与される、請求項22に記載の方法。
- 前記化合物が経皮投与される、請求項22に記載の方法。
- 前記化合物が直腸投与される、請求項22に記載の方法。
- 前記化合物が経鼻投与される、請求項22に記載の方法。
- 前記化合物が舌下投与される、請求項22に記載の方法。
- 前記化合物が、約0.01μg/日〜約1000μg/日の用量で投与される、請求項22に記載の方法。
- 前記化合物が経口投与される、請求項31に記載の方法。
- 前記化合物が非経口投与される、請求項31に記載の方法。
- 前記化合物が経皮投与される、請求項31に記載の方法。
- 前記化合物が直腸投与される、請求項31に記載の方法。
- 前記化合物が経鼻投与される、請求項31に記載の方法。
- 前記化合物が舌下投与される、請求項31に記載の方法。
- 前記化合物が、約0.01μg/日〜約1000μg/日の用量で投与される、請求項31に記載の方法。
- 前記化合物が経口投与される、請求項40に記載の方法。
- 前記化合物が非経口投与される、請求項40に記載の方法。
- 前記化合物が経皮投与される、請求項40に記載の方法。
- 前記化合物が直腸投与される、請求項40に記載の方法。
- 前記化合物が経鼻投与される、請求項40に記載の方法。
- 前記化合物が舌下投与される、請求項40に記載の方法。
- 前記化合物が、約0.01μg/日〜約1000μg/日の用量で投与される、請求項40に記載の方法。
- 前記化合物が経口投与される、請求項49に記載の方法。
- 前記化合物が非経口投与される、請求項49に記載の方法。
- 前記化合物が経皮投与される、請求項49に記載の方法。
- 前記化合物が局所投与される、請求項49に記載の方法。
- 前記化合物が直腸投与される、請求項49に記載の方法。
- 前記化合物が経鼻投与される、請求項49に記載の方法。
- 前記化合物が舌下投与される、請求項49に記載の方法。
- 前記化合物が、約0.01μg/日〜約1000μg/日の用量で投与される、請求項49に記載の方法。
- 前記化合物が経口投与される、請求項59に記載の方法。
- 前記化合物が非経口投与される、請求項59に記載の方法。
- 前記化合物が経皮投与される、請求項59に記載の方法。
- 前記化合物が直腸投与される、請求項59に記載の方法。
- 前記化合物が経鼻投与される、請求項59に記載の方法。
- 前記化合物が舌下投与される、請求項59に記載の方法。
- 前記化合物が、約0.01μg/日〜約1000μg/日の用量で投与される、請求項59に記載の方法。
- 前記化合物が経口投与される、請求項68に記載の方法。
- 前記化合物が非経口投与される、請求項68に記載の方法。
- 前記化合物が経皮投与される、請求項68に記載の方法。
- 前記化合物が直腸投与される、請求項68に記載の方法。
- 前記化合物が経鼻投与される、請求項68に記載の方法。
- 前記化合物が舌下投与される、請求項68に記載の方法。
- 前記化合物が、約0.01μg/日〜約1000μg/日の用量で投与される、請求項68に記載の方法。
- 前記動物がヒトである、請求項68に記載の方法。
- 前記動物が飼育されている動物である、請求項68に記載の方法。
- 前記動物が農業用動物である、請求項68に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/171,113 US8193170B2 (en) | 2008-07-10 | 2008-07-10 | 2-methylene-19,26-dinor-(20R,22E,25R)-vitamin D analogs |
| US12/171,113 | 2008-07-10 | ||
| PCT/US2009/050048 WO2010006125A2 (en) | 2008-07-10 | 2009-07-09 | 2-methylene-19,26-dinor-(20r,22e,25r)-vitamin d analogs |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2011527695A true JP2011527695A (ja) | 2011-11-04 |
| JP2011527695A5 JP2011527695A5 (ja) | 2012-08-23 |
Family
ID=41382480
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011517601A Pending JP2011527695A (ja) | 2008-07-10 | 2009-07-09 | 2−メチレン−19,26−ジノル−(20r,22e,25r)−ビタミンd類似物質 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US8193170B2 (ja) |
| EP (1) | EP2313367A2 (ja) |
| JP (1) | JP2011527695A (ja) |
| AU (1) | AU2009268557B2 (ja) |
| CA (1) | CA2730244A1 (ja) |
| WO (1) | WO2010006125A2 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008035206A2 (en) * | 2006-04-06 | 2008-03-27 | Wisconsin Alumni Research Foundation | 2-methylene-1 alpha-hydroxy-18,19,21-trinorvitamin d3 analogs and uses thereof |
| JP5931845B2 (ja) * | 2010-03-23 | 2016-06-08 | ウイスコンシン アラムニ リサーチ ファンデーション | 2−メチレン−19−ノル−22−メチル−1α,25−ジヒドロキシビタミンD3のジアステレオマー |
| US8664206B2 (en) | 2010-03-23 | 2014-03-04 | Wisconsin Alumni Research Foundation | Diastereomers of 2-methylene-19-nor-22-methyl-1α,25-dihydroxyvitamin D3 |
| CA2794006C (en) * | 2010-03-23 | 2017-11-28 | Wisconsin Alumni Research Foundation | (20s)-2-methylene-19-nor-22-dimethyl-1.alpha.,25-dihydroxyvitamin d3 and (20r)-2-methylene-19-nor-22-dimethyl-1.alpha.,25-hydroxyvitamin d3 |
| US8993547B2 (en) * | 2011-06-14 | 2015-03-31 | Wisconsin Alumni Research Foundation | 3-desoxy-2-methylene-19-nor-vitamin D analogs and their uses |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007512376A (ja) * | 2003-11-25 | 2007-05-17 | ウイスコンシン アラムニ リサーチ ファンデーション | 肥満症の予防及び治療用ビタミンd類似体 |
| WO2008039754A1 (en) * | 2006-09-28 | 2008-04-03 | Wisconsin Alumni Research Foundation | 2-methylene-(20r,25s)-19,27-dinor-(22e)-vitamin d analogs |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5063221A (en) | 1989-04-05 | 1991-11-05 | Chugai Seiyaku Kabushiki Kaisha | Treatment for hyperparathyroidism with use of vitamin d derivatives |
| US5086191A (en) | 1991-05-28 | 1992-02-04 | Wisconsin Alumni Research Foundation | Intermediates for the synthesis of 19-nor vitamin D compounds |
| GB9214202D0 (en) | 1992-07-03 | 1992-08-12 | Leo Pharm Prod Ltd | Chemical compounds |
| EP0619306B1 (en) | 1993-04-05 | 1996-09-11 | Wisconsin Alumni Research Foundation | 19-Nor-vitamin D3 compounds with substituent at 2-position |
| DK0717034T3 (da) | 1994-12-14 | 1999-10-18 | Duphar Int Res | Vitamin D-forbindelser og fremgangsmåde til fremstilling af disse forbindelser |
| US5843928A (en) * | 1997-03-17 | 1998-12-01 | Wisconsin Alumni Research Foundation | 2-alkylidene-19-nor-vitamin D compounds |
| US5945410A (en) * | 1997-03-17 | 1999-08-31 | Wisconsin Alumni Research Foundation | 2-alkyl-19-nor-vitamin D compounds |
| GB9721156D0 (en) | 1997-10-06 | 1997-12-03 | Leo Pharm Prod Ltd | Novel vitamin d analogues |
| AU7544501A (en) | 2000-09-08 | 2002-03-22 | Wisconsin Alumni Res Found | 1alpha-hydroxy-2-methylene-19-nor-homopregnacalciferol and its therapeutic applications |
| US6566352B1 (en) | 2002-02-18 | 2003-05-20 | Wisconsin Alumni Research Foudation | 1 α-hydroxy-2-methylene-19-nor-pregnacalciferol and its uses |
| US7232810B2 (en) * | 2003-08-20 | 2007-06-19 | Wisconsin Alumni Research Foundation | 2-methylene-19-nor-vitamin D2 compounds |
| MX2007006263A (es) | 2004-11-22 | 2007-07-10 | Wisconsin Alumni Res Found | Analogos 2a-metil y 2??-metil de 19,26,27-trinor-(20s)-1a- hidroxivitamina d3 y sus usos. |
| MX2007006542A (es) | 2004-11-22 | 2007-07-25 | Wisconsin Alumni Res Found | 2a-metil-19-nor-(20s)-1a-hidroxi-bishomopregnacalciferol y sus usos. |
| CA2588415C (en) | 2004-11-22 | 2012-07-10 | Wisconsin Alumni Research Foundation | 2-methylene-19,26,27-trinor-(20s)-1-alpha-hydroxyvitamin d3 and its uses |
| EP1877063A4 (en) * | 2005-05-03 | 2009-11-04 | Wisconsin Alumni Res Found | COMPOUNDS OF 19,26,27-TRINOR-1ALPHA, 25-DIHYDROXYVITAMIN D3 |
| US7803789B2 (en) | 2006-02-02 | 2010-09-28 | Wisconsin Alumni Research Foundation | Vitamin D analog—RAK, methods and uses thereof |
| US7528122B2 (en) | 2006-02-02 | 2009-05-05 | Wisconsin Alumni Research Foundation | Vitamin D analog—NEL, methods and uses thereof |
| US8404666B2 (en) | 2006-04-06 | 2013-03-26 | Wisconsin Alumni Research Foundation | 2-substituted-1α,25-dihydroxy-19,26,27-trinor vitamin D analogs and uses thereof |
-
2008
- 2008-07-10 US US12/171,113 patent/US8193170B2/en not_active Expired - Fee Related
-
2009
- 2009-07-09 EP EP09790197A patent/EP2313367A2/en not_active Withdrawn
- 2009-07-09 WO PCT/US2009/050048 patent/WO2010006125A2/en active Application Filing
- 2009-07-09 JP JP2011517601A patent/JP2011527695A/ja active Pending
- 2009-07-09 CA CA2730244A patent/CA2730244A1/en not_active Abandoned
- 2009-07-09 AU AU2009268557A patent/AU2009268557B2/en not_active Ceased
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007512376A (ja) * | 2003-11-25 | 2007-05-17 | ウイスコンシン アラムニ リサーチ ファンデーション | 肥満症の予防及び治療用ビタミンd類似体 |
| WO2008039754A1 (en) * | 2006-09-28 | 2008-04-03 | Wisconsin Alumni Research Foundation | 2-methylene-(20r,25s)-19,27-dinor-(22e)-vitamin d analogs |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2009268557A1 (en) | 2010-01-14 |
| WO2010006125A2 (en) | 2010-01-14 |
| US8193170B2 (en) | 2012-06-05 |
| CA2730244A1 (en) | 2010-01-14 |
| WO2010006125A3 (en) | 2010-04-01 |
| AU2009268557B2 (en) | 2013-12-19 |
| EP2313367A2 (en) | 2011-04-27 |
| US20100009946A1 (en) | 2010-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5161582B2 (ja) | 17,20(z)−デヒドロビタミンd類似体およびそれらの使用 | |
| JP2008520691A (ja) | 2−メチレン−19,26,27−トリノル−(20S)−1α−ヒドロキシビタミンD3およびその使用 | |
| US7741314B2 (en) | 2-Methylene-(20R,25S)-19,27-Dinor-(22E)-Vitamin D Analogs | |
| US8609643B2 (en) | 2-methylene-(20S,25R)-19,26-dinor-vitamin D analogs | |
| JP2011527695A (ja) | 2−メチレン−19,26−ジノル−(20r,22e,25r)−ビタミンd類似物質 | |
| US8399439B2 (en) | 2-methylene-19,26-dinor-(20S,22E,25R)-vitamin D analogs | |
| US8114859B2 (en) | 2-methylene-(20S,25S)-19,27-dinor-(22E)-vitamin D analogs | |
| JP2013506685A (ja) | (20S,22E)−2−メチレン−19−ノル−22−エン−1α,25−ジヒドロキシビタミンD3類似体 | |
| JP5629682B2 (ja) | 2−メチレン−(17z)−17(20)−デヒドロ−19,21−ジノル−ビタミンd類似物質 | |
| JP2011527700A (ja) | 2−メチレン−20(21)−デヒドロ−19−ノル−ビタミンd類似物質 | |
| JP2011527698A (ja) | 2−メチレン−(20e)−20(22)−デヒドロ−19−ノル−ビタミンd類似物質 | |
| US7947666B2 (en) | 2-methylene-(20S,25S)-19,26-dinor-vitamin D analogs |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120706 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120706 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140218 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140225 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140318 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140326 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140624 |