JP2010105945A - Tetrathiafulvalene derivative and nanofiber composed of the derivative - Google Patents
Tetrathiafulvalene derivative and nanofiber composed of the derivative Download PDFInfo
- Publication number
- JP2010105945A JP2010105945A JP2008278534A JP2008278534A JP2010105945A JP 2010105945 A JP2010105945 A JP 2010105945A JP 2008278534 A JP2008278534 A JP 2008278534A JP 2008278534 A JP2008278534 A JP 2008278534A JP 2010105945 A JP2010105945 A JP 2010105945A
- Authority
- JP
- Japan
- Prior art keywords
- tetrathiafulvalene
- tetrathiafulvalene derivative
- derivative
- compound
- charge transfer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Heterocyclic Compounds Containing Sulfur Atoms (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
本発明は、新規化合物であってキラル分子が導入され、相互作用によって自己組織化し形成されたテトラチアフルバレン誘導体、該テトラチアフルバレン誘導体にアクセプター分子の配位した電荷移動錯体、および電荷移動錯体からなる電気伝導性ナノファイバーに関するものである。 The present invention relates to a tetrathiafulvalene derivative that is a novel compound and is self-assembled and formed by interaction with a chiral molecule, a charge-transfer complex in which an acceptor molecule is coordinated to the tetrathiafulvalene derivative, and a charge-transfer complex. It relates to an electrically conductive nanofiber.
発達したπ共役系を有するディスク状分子は、π電子系により非局在化した電子が豊富であり、そのπ電子に由来する優れた電気的・光学的特性を有し、π−π相互作用を通じて多様な組織体に自己組織化する。 Disk-shaped molecules with developed π-conjugated systems are rich in electrons delocalized by the π-electron system, have excellent electrical and optical properties derived from the π-electrons, and π-π interaction Through self-organization into various organizations.
このπ−π相互作用は、芳香環の間に働く分散力であり、いろいろな分子の立体配座や分子構造形成に影響を与えており、例えば生体を構成するDNAの二重らせん高次構造の安定化において、核酸塩基間で作用している。同様に、左右のどちらか一方向巻きのヘリカルな構造を有する。核酸やタンパク質などの分子においても、この分子構造とそれらの物質がもつ特有で高度な機能の発現とが深く関わると知られている。 This π-π interaction is a dispersion force that acts between aromatic rings, and affects the conformation and molecular structure formation of various molecules. For example, the double-helix higher-order structure of DNA constituting the living body Acts between nucleobases in the stabilization of Similarly, it has a helical structure wound in one direction on either side. In molecules such as nucleic acids and proteins, it is known that this molecular structure and the expression of unique and advanced functions of these substances are deeply related.
そこで、π−π相互作用を通じて自己組織化をするディスク状分子は、その自己組織化過程において分子間相互作用をデザインすることで形成され、組織構造及び機能性の制御が可能であるため、分子設計に基づく自己組織化制御による高機能マテリアルとして注目されている。 Therefore, disc-like molecules that self-assemble through π-π interactions are formed by designing intermolecular interactions in the self-assembly process, and the structure and functionality of the molecules can be controlled. It is attracting attention as a highly functional material by self-organization control based on design.
特許文献1に、分子の自己組織化を利用してアミノ酸から形成したペプチドナノファイバーに導電性物質を付加した導電性ペプチドナノファイバーが開示されている。生体分子であるアミノ酸を材料とすることで生分解性が可能であり、環境に悪影響を及ぼすことがないが、導電性を機能付加する際に、導電性物質となる金属粒子を付加する必要を有する。
本発明は前記の課題を解決するためになされたもので、テトラチアフルバレンに光学活性水素結合鎖、すなわちキラル分子を導入することで、キラル化され自己組織化制御を可能とする新規化合物であるテトラチアフルバレン誘導体、およびその誘導体を電荷移動錯体とすることで組織体の安定化と機能化に優れた電気伝導性ナノファイバーを提供することを目的とする。 The present invention has been made to solve the above-described problems, and is a novel compound that is capable of controlling self-organization by being chiralized by introducing an optically active hydrogen-bonded chain, that is, a chiral molecule, into tetrathiafulvalene. It is an object of the present invention to provide a tetrathiafulvalene derivative and an electrically conductive nanofiber excellent in stabilization and functionalization of a tissue body by using the derivative as a charge transfer complex.
前記の目的を達成するためになされた、特許請求の範囲の請求項1に記載されたD体または/およびS体のテトラチアフルバレン誘導体は、
下記化学式(I)
The D-form and / or the S-form tetrathiafulvalene derivative according to
The following chemical formula (I)
請求項2に記載されたテトラチアフルバレン誘導体は、請求項1に記載のものであって、前記D体テトラチアフルバレン誘導体の分子中の少なくとも1つの−NH−基と、同じくD体テトラチアフルバレン誘導体の別な分子中の=O基とが、水素結合して自己組織化したことを特徴とする。
The tetrathiafulvalene derivative according to
請求項3に記載されたテトラチアフルバレン誘導体は、請求項1に記載のものであって、前記S体テトラチアフルバレン誘導体の分子中の少なくとも1つの−NH−基と、同じくS体テトラチアフルバレン誘導体の別な分子中の=O基とが、水素結合して自己組織化したことを特徴とする。
The tetrathiafulvalene derivative according to claim 3 is the one according to
請求項4に記載された電荷移動錯体は、請求項1に記載されたD体または/およびS体のテトラチアフルバレン誘導体にアクセプター分子が配位してなることを特徴とする。
The charge transfer complex described in
請求項5に記載された電荷移動錯体は、請求項4に記載のものであって、該アクセプター分子がフッ素化テトラシアノキノジメタンであることを特徴とする。
The charge transfer complex described in claim 5 is the one described in
請求項6に記載された電気伝導性ナノファイバーは、請求項4に記載されたD体テトラチアフルバレン誘導体にアクセプター分子の配位した電荷移動錯体が、右旋捩れで相互に絡み合ったことを特徴とする。
The electrically conductive nanofiber according to
請求項7に記載された電気伝導性ナノファイバーは、請求項4に記載されたS体テトラチアフルバレン誘導体にアクセプター分子の配位した電荷移動錯体が、左旋捩れで相互に絡み合ったことを特徴とする。
The electrically conductive nanofiber according to claim 7 is characterized in that the charge transfer complex in which an acceptor molecule is coordinated to the S-form tetrathiafulvalene derivative according to
D(Dextro:右旋性)体または/およびS(Sinistro:左旋性)体のテトラチアフルバレン誘導体は、高い導電性をもつテトラチアフルバレンに光学活性水素結合鎖、すなわちキラル分子を導入することで、自己組織化を制御可能な新規化合物である。 Tetrathiafulvalene derivatives in the D (Dextro) form and / or the S (Sinistro) form can be obtained by introducing an optically active hydrogen-bonded chain, that is, a chiral molecule, into highly conductive tetrathiafulvalene. , A novel compound capable of controlling self-assembly.
このため、前記テトラチアフルバレン誘導体とアクセプター分子とで、錯体化することにより、電荷移動体を形成することができ、前記電荷移動体中におけるキラル分子によって、D体あるいはS体の立体構造をした組織体であり高い電気伝導性を有したナノファイバーを提供することができる。 For this reason, a charge transfer body can be formed by complexing with the tetrathiafulvalene derivative and the acceptor molecule, and the three-dimensional structure of the D form or the S form is formed by the chiral molecule in the charge transfer body. A nanofiber which is a tissue body and has high electrical conductivity can be provided.
前記電気伝導性ナノファイバーは、帯電防止や電極膜等に使用することが可能である。 The electrically conductive nanofibers can be used for antistatic, electrode films and the like.
以下、本発明を実施するための好ましい形態について、詳細に説明するが、本発明の範囲はこれらの形態に限定されるものではない。 Hereinafter, although the preferable form for implementing this invention is demonstrated in detail, the scope of the present invention is not limited to these forms.
本発明の新規化合物であるテトラチアフルバレン誘導体(TTF誘導体)は、高い導電性をもつテトラチアフルバレンに光学活性水素結合鎖すなわちキラル分子を導入し、キラル化することでD体とS体をそれぞれ有する構造を形成する。 The tetrathiafulvalene derivative (TTF derivative), which is a novel compound of the present invention, introduces an optically active hydrogen-bonded chain, ie, a chiral molecule, into tetrathiafulvalene, which has high conductivity, and chiralizes it to form D and S forms respectively. Forming a structure having
S体テトラチアフルバレン誘導体の反応スキームを以下に示す。 A reaction scheme of the S-form tetrathiafulvalene derivative is shown below.
下記反応式(a)に示すように、ハロゲン置換脂肪酸ハロゲン化物とアミノ基をもつキラル分子を反応させて、テトラチアフルバレンに導入する光学活性水素結合鎖すなわちキラル分子とする。S(−)−フェニルエチルアミンを用いた際に化合物1−Sを合成することができる。 As shown in the following reaction formula (a), a halogen-substituted fatty acid halide and a chiral molecule having an amino group are reacted to form an optically active hydrogen bond chain that is introduced into tetrathiafulvalene, that is, a chiral molecule. Compound 1-S can be synthesized when S (-)-phenylethylamine is used.
アミノ基をもつキラル分子と反応させる化合物は、ハロゲン置換脂肪酸ハロゲン化物を好適とし、具体的には、6−ブロモヘキサン酸クロリド、12−ブロモラウリン酸クロリド、4−ブロモプロパン酸クロリド、1−ブロモ酢酸クロリド等が挙げられる。 The compound to be reacted with a chiral molecule having an amino group is preferably a halogen-substituted fatty acid halide, specifically, 6-bromohexanoic acid chloride, 12-bromolauric acid chloride, 4-bromopropanoic acid chloride, 1-bromo. Examples include acetic acid chloride.
この化合物の脂肪酸の長さの違いによって、得られるS体テトラチアフルバレン誘導体の大きさ、分子量は異なる。この脂肪酸は炭素数6であると好ましく、この炭素数は多過ぎるとアルキル鎖が長くなり、合成反応に時間がかかるなど合成効率の低下を招くために適切でない場合を有する。 The size and molecular weight of the obtained S-form tetrathiafulvalene derivative differ depending on the difference in the fatty acid length of this compound. This fatty acid preferably has 6 carbon atoms, and if this carbon number is too large, the alkyl chain becomes long, and there are cases where it is not suitable for causing a reduction in synthesis efficiency, such as taking a long time for the synthesis reaction.
アミノ基をもつキラル分子としては、S体を有するキラル分子であって、具体的には、S(−)−フェニルエチルアミン、S(−)−1−(p−トリル)エチルアミン等が挙げられる。 The chiral molecule having an amino group is a chiral molecule having an S form, and specifically includes S (-)-phenylethylamine, S (-)-1- (p-tolyl) ethylamine, and the like.
下記反応式(b)、(c)、(d)の順に、合成を行い、前記反応式(a)で得られた化合物1−Sと反応させる化合物3を得る。 Synthesis is performed in the order of the following reaction formulas (b), (c), and (d) to obtain compound 3 to be reacted with compound 1-S obtained in the above reaction formula (a).
下記反応式(e)、(f)、(g)の順に反応を行い、テトラチアフルバレンにキラル分子を導入した化合物6−SであるS体テトラチアフルバレン誘導体を合成することができる。 By reacting in the order of the following reaction formulas (e), (f), and (g), an S-form tetrathiafulvalene derivative that is a compound 6-S in which a chiral molecule is introduced into tetrathiafulvalene can be synthesized.
前記反応スキームで示されるように、反応(a)においてS(−)フェニルエチルアミンを用いた場合には、S体のテトラチアフルバレン誘導体を得ることができる。 As shown in the reaction scheme, when S (-) phenylethylamine is used in the reaction (a), an S-form tetrathiafulvalene derivative can be obtained.
S体テトラチアフルバレン誘導体に対して、同様な反応スキームに基づき、段落番号0026に記載のアミノ基をもつキラル分子をD体の物質とすることで、D体のテトラチアフルバレン誘導体を合成することができ、ここでは、D(+)フェニルエチルアミンを用いることで、D体のテトラチアフルバレン誘導体が合成される。 For the S-form tetrathiafulvalene derivative, a D-form tetrathiafulvalene derivative is synthesized by using a chiral molecule having an amino group described in paragraph No. 0026 as a D-form substance based on the same reaction scheme. Here, D-form tetrathiafulvalene derivative is synthesized by using D (+) phenylethylamine.
図1のテトラチアフルバレン誘導体2に図示されるように、その構造は、前記化学式(I)中の−CnH2n−においてn=3の場合、36Å×27Åのディスク状分子となる。
As illustrated in the
S体テトラチアフルバレン誘導体はキラル化されており、そのキラル分子中の−NH−基の少なくとも1つの基と、同テトラチアフルバレン誘導体であって他の分子である=O基とが水素結合を形成し、この水素結合によって自己組織化された相互作用物質となる。自己組織力が安定することで、温度変化に対し可逆的に高い秩序性をもつ組織体となる。この相互作用物質である組織体は、温度に対して高い依存性をもつ水素結合により自己組織化されているため、熱により組織体の崩壊を生じ、冷却により組織体の再構築を成す。 The S-form tetrathiafulvalene derivative is chiralized, and at least one group of —NH— group in the chiral molecule and a ═O group which is the same tetrathiafulvalene derivative and other molecule form a hydrogen bond. It forms and becomes an interactive substance self-organized by this hydrogen bond. By stabilizing the self-organizing force, it becomes an organization having reversible high order with respect to temperature change. Since the tissue body which is this interacting substance is self-organized by hydrogen bonds having a high dependence on temperature, the tissue body collapses due to heat, and the tissue body is reconstructed by cooling.
S体テトラチアフルバレン誘導体にアクセプター分子を配位させることで、電荷移動錯体とすることが可能である。 A charge transfer complex can be formed by coordinating an acceptor molecule to an S-form tetrathiafulvalene derivative.
電子供与性の分子であるテトラチアフルバレンは、電子受容体の分子と反応して電荷移動錯体や導電性の混合原子価錯体になると知られており、同様に、テトラチアフルバレン誘導体は電子供与性分子として、電子受容体であるアクセプター分子と反応して電荷移動錯体の形成を可能とする。 Tetrathiafulvalene, an electron-donating molecule, is known to react with an electron acceptor molecule to form a charge transfer complex or a conductive mixed-valence complex. Similarly, a tetrathiafulvalene derivative is an electron-donating molecule. As a molecule, it reacts with an acceptor molecule, which is an electron acceptor, to enable formation of a charge transfer complex.
形成された電荷移動錯体を図1に示す。 The formed charge transfer complex is shown in FIG.
図1に示されるように、電荷移動錯体においてS体のテトラチアフルバレン誘導体中に存在しているキラル分子はそのまま存在しており、S体のテトラチアフルバレン誘導体と同様に電荷移動錯体もキラル化されている。 As shown in FIG. 1, in the charge transfer complex, the chiral molecule existing in the S-form tetrathiafulvalene derivative remains as it is, and the charge-transfer complex is also chiralized in the same manner as the S-form tetrathiafulvalene derivative. Has been.
電荷移動錯体は、キラル分子を有することで自己組織化を制御し、組織体を構築することができ、この組織体は電荷移動相互作用によって、強度強化され、安定化したものとなる。 The charge transfer complex has a chiral molecule, and can control self-organization and build an organization. The organization is strengthened and stabilized by charge transfer interaction.
1分子のテトラチアフルバレン誘導体に対し、2分子のアクセプター分子であるフッ素化テトラシアノキノジメタン(F4TCQ)が配位されており、縦横へと結合をなしている。それぞれ重なる部位の記載については、省略している。 Fluorinated tetracyanoquinodimethane (F 4 TCQ), which is an acceptor molecule, is coordinated with one molecule of a tetrathiafulvalene derivative, and is bonded vertically and horizontally. The description of the overlapping portions is omitted.
また、この組織体は、電荷移動相互作用によって電気伝導性を有する。 In addition, this tissue body has electrical conductivity due to charge transfer interaction.
このアクセプター分子は、導電性有機化合物であることが好ましく、具体的にはフッ素化テトラシアノキノジメタン、2,3−ジヨード−5,6−ジシアノベンゾキノン、テトラニトロビフェノール、2,4,7−トリニトロフルオレノン等が挙げられる。 This acceptor molecule is preferably a conductive organic compound, specifically, fluorinated tetracyanoquinodimethane, 2,3-diiodo-5,6-dicyanobenzoquinone, tetranitrobiphenol, 2,4,7- And trinitrofluorenone.
アクセプター分子は、S体テトラチアフルバレン誘導体が1molであるのに対し1molであることが好ましい。 The acceptor molecule is preferably 1 mol compared to 1 mol of the S-form tetrathiafulvalene derivative.
さらに、この構築された組織体は、キラル分子における空間的相互作用によって規律性が与えられ、キラル化によりヘリシティーが付加されることで捩れた状態となり、互いにバンドルを形成することで、ヘリシティーに依存した捩れを有する電気伝導性ナノファイバーとして組織化される。 Furthermore, this constructed structure is given discipline by spatial interaction in the chiral molecule, becomes twisted by adding helicity by chiralization, and forms a bundle with each other. It is organized as electrically conductive nanofibers with a twist that depends on the.
この電気伝導性ナノファイバーの捩れた状態は、S体のテトラチアフルバレン誘導体にアクセプター分子を配位させた電荷移動錯体の場合に、左旋捩れで互いに絡み合った形態となる。 In the case of a charge transfer complex in which an acceptor molecule is coordinated to an S-type tetrathiafulvalene derivative, the electrically conductive nanofibers are twisted in a twisted manner.
この電気伝導性ナノファイバーの直径は長径80nm、短径20nmであることが好ましく、長さは10μm以上であることが好ましい。 The electric conductive nanofibers preferably have a major axis of 80 nm and a minor axis of 20 nm, and the length is preferably 10 μm or more.
自己組織化を制御して形成された電気伝導性ナノファイバーである組織体は、導電性を有するテトラチアフルバレン誘導体の電荷移動錯体であり、電荷移動相互作用によって、半導体的な挙動を示し高い電気伝導性を示す。この電気伝導度は1×10−3S/cm〜1×10−4S/cmであることが好ましい。 The tissue body, which is an electrically conductive nanofiber formed by controlling self-assembly, is a charge transfer complex of tetrathiafulvalene derivative with conductivity, and it exhibits a semiconductor-like behavior due to charge transfer interaction. Shows conductivity. The electrical conductivity is preferably 1 × 10 −3 S / cm to 1 × 10 −4 S / cm.
このため、強度強化され安定であり、機能性を付加された電気伝導性ナノファイバーは様々な用途で汎用性を有する。例えば、繊維担持、帯電防止、電極膜の使用、導電線などが挙げられる。 For this reason, the strength and stability of the electrically conductive nanofibers with added functionality are versatile in various applications. For example, fiber support, antistatic, use of an electrode film, conductive wire and the like can be mentioned.
D体テトラチアフルバレン誘導体についても同様な性質をもっており、これにアクセプター分子を配位することで得られる電荷移動錯体・電気伝導性ナノファイバーも同様の性質をもつ。しかし、キラル分子によって構造が異なるため、電気伝導性ナノファイバーの捩れた状態については、D体のテトラチアフルバレン誘導体にアクセプター分子を配位させた電荷移動錯体の場合、右旋捩れで互いに絡み合った形態となり、キラル分子に依存して変化する。 The D-form tetrathiafulvalene derivative has similar properties, and the charge transfer complex / electrically conductive nanofiber obtained by coordinating the acceptor molecule to this has the same properties. However, since the structure differs depending on the chiral molecule, the twisted state of the electrically conductive nanofiber was entangled with the right-handed twist in the case of the charge transfer complex in which the acceptor molecule was coordinated with the D-form tetrathiafulvalene derivative. It becomes a form and changes depending on the chiral molecule.
(実施例1):S体テトラチアフルバレン誘導体の合成
6−ブロモヘキサン酸クロリド6.7mmolに対し、S(−)フェニルエチルアミン4.47mmolを混合し、溶媒としてテトラヒドロフラン8ml、ベースとしてトリエチルアミン13.4mmolを添加して反応させ、化合物1−Sを得た。この化合物1−Sの収量は0.95g、収率は97%であった。下記にフーリエ変換型赤外分光(FT−IR)、核磁気共鳴分光法(1H−NMR、13C−NMR)の分析結果を示す。
(Example 1): Synthesis of S-form tetrathiafulvalene derivative 6.7 mmol of 6-bromohexanoic acid chloride was mixed with 4.47 mmol of S (-) phenylethylamine, 8 ml of tetrahydrofuran as a solvent, and 13.4 mmol of triethylamine as a base. To give compound 1-S. The yield of Compound 1-S was 0.95 g, and the yield was 97%. The analysis results of Fourier transform infrared spectroscopy (FT-IR) and nuclear magnetic resonance spectroscopy ( 1 H-NMR, 13 C-NMR) are shown below.
N,N−ジメチルホルムアミド200ml中に、二硫化炭素3molに対し、ナトリウム1molを加え、4,5−ビス(ソジオチオ)−1,3−ジチオール−2−4オンとトリチオ炭酸ジナトリウムの混合溶液を得た。ここに、塩化亜鉛0.15molを添加し、メタノール−水の混合溶液中で反応させ、さらにテトラエチルアンモニウムブロミド0.25molを添加して反応させ、化合物2を得た。化合物2の収量は77.0g、収率は86%であった。
In 200 ml of N, N-dimethylformamide, 1 mol of sodium is added to 3 mol of carbon disulfide, and a mixed solution of 4,5-bis (sodiothio) -1,3-dithiol-2-4one and disodium trithiocarbonate is added. Obtained. To this, 0.15 mol of zinc chloride was added and reacted in a methanol-water mixed solution, and further 0.25 mol of tetraethylammonium bromide was added and reacted to obtain
また、アセトニトリル中に化合物2を20.9mmolと3−ブロモプロピオニトリル100.8mmolを添加し、化合物3を得た。化合物3の収量は9.78g、収率は77%であった。
Further, 20.9 mmol of
続いて、乾燥アセトニトリル−メタノール混合溶液中に化合物3を0.385mmolに対し3.09mmolの化合物1−Sを混合し、水酸化セシウム水和物0.85mmolを添加し化合物4−Sを得た。化合物4−Sの収量は0.15g、収率は63%であった。下記にFT−IR、1H,13C−NMR、マトリックス支援レーザー脱離イオン化法−飛行時間型−質量分析計(MALDI−TOF−Mass)の分析結果を示す。 Subsequently, compound 3 was mixed in dry acetonitrile-methanol mixed solution with 3.085 mmol of compound 1-S with respect to 0.385 mmol, and cesium hydroxide hydrate 0.85 mmol was added to obtain compound 4-S. . The yield of compound 4-S was 0.15 g, and the yield was 63%. The analysis results of FT-IR, 1 H, 13 C-NMR, matrix-assisted laser desorption / ionization method—time of flight type—mass spectrometer (MALDI-TOF-Mass) are shown below.
さらに、酢酸−クロロホルム混合溶液中で化合物4−S0.38mmolと酢酸水銀1.95mmolを反応させ、化合物5−Sを得た。化合物5−Sの収量は0.23g、収率は99%であった。下記にMALDI−TOF−Massの分析結果を示す。 Further, compound 8-S 0.38 mmol and mercury acetate 1.95 mmol were reacted in an acetic acid-chloroform mixed solution to obtain compound 5-S. The yield of compound 5-S was 0.23 g, and the yield was 99%. The analysis results of MALDI-TOF-Mass are shown below.
最後に、化合物5−S0.376mmolに亜リン酸トリエチル3mlを添加し、120℃で一晩、加熱拡拌し反応させて化合物6−Sを得た。化合物6−Sの収量は1128mg、収率は57%であった。この化合物がS体のテトラチアフルバレン誘導体である。下記にFT−IR、1H,13C−NMR、MALDI−TOF−Massの分析結果を示す。 Finally, 3 ml of triethyl phosphite was added to 0.376 mmol of compound 5-S, and the mixture was heated and stirred overnight at 120 ° C. to obtain compound 6-S. The yield of compound 6-S was 1128 mg, and the yield was 57%. This compound is an S-form tetrathiafulvalene derivative. The analysis results of FT-IR, 1 H, 13 C-NMR, and MALDI-TOF-Mass are shown below.
S体テトラチアフルバレン誘導体の透過型電子顕微鏡での観察結果を図2に示す。 The observation result of the S-form tetrathiafulvalene derivative with a transmission electron microscope is shown in FIG.
(実施例1における化合物の各分析結果)
化合物1−S
FT−IR(ATR,cm−1):
ν=3285(−NH−),2932(−CH2−),1638(−C=O)
1H−NMR(400.13MHz Chloroform−D):
δ=7.32(m,5H,Ar−H),5.14(q,J=7,20,1H,ArCH(CH3)NH−),3.39(t,J=6.6Hz,2H,BrCH 2CH2−),2.18(t,J=8.0Hz,2H,−CH2CH 2CO−),1.64(m,3H,-CHCH 3),1.48(m,6H,−CH 2−)
(Each analysis result of the compound in Example 1)
Compound 1-S
FT-IR (ATR, cm -1 ):
ν = 3285 (—NH—), 2932 (—CH 2 —), 1638 (—C═O)
1 H-NMR (400.13 MHz Chloroform-D):
δ = 7.32 (m, 5H, Ar—H), 5.14 (q, J = 7, 20, 1H, ArC H (CH 3 ) NH—), 3.39 (t, J = 6.6 Hz) , 2H, BrC H 2 CH 2 -), 2.18 (t, J = 8.0Hz, 2H, -
化合物4−S
FT−IR(ATR,cm−1):
ν=3304(−NH−),2972(−CH2−),1643(−C=O)
1H−NMR(400.13MHz Chloroform−D):
δ=7.29(m,10H,Ar−H),5.11(q,J=7.2Hz,2H,NH(CH3)CH−Ar),2.85(t,J=7.2Hz,4H,−SCH 2CH2−),2.16(t,J=7.6Hz,4H,−CH2CH 2CO−),1.68(m,6H,−CHCH 3),1.47(m,12H,−CH2−)
13C−NMR(100.61MHz Chloroform−D):
δ=21.81,25.11,28.09,29.42,36.49,36.66,48.77,126.23,127.39,128.71,143.44,171.59,207.9
MALDI−TOF−Mass(Dithranol):
m/z=634.20[M+H]+,calc for C31H40N2O2S5:632.99
Compound 4-S
FT-IR (ATR, cm −1 ):
ν = 3304 (—NH—), 2972 (—CH 2 —), 1643 (—C═O)
1 H-NMR (400.13 MHz Chloroform-D):
δ = 7.29 (m, 10H, Ar-H), 5.11 (q, J = 7.2Hz, 2H, NH (CH 3) C H -Ar), 2.85 (t, J = 7. 2Hz, 4H, -SC H 2 CH 2 -), 2.16 (t, J = 7.6Hz, 4H, -
13 C-NMR (100.61MHz Chloroform- D):
δ = 21.81, 25.11, 28.09, 29.42, 36.49, 36.66, 48.77, 126.23, 127.39, 128.71, 143.44, 171.59, 207.9
MALDI-TOF-Mass (Dithranol):
m / z = 634.20 [M + H] + , calc for C 31 H 40 N 2 O 2 S 5 : 632.999
化合物5−S
MALDI−TOF−Mass(Dithranol):
m/z=617.5[M+H]+,calc for C31H40N2O3S4:616.92
Compound 5-S
MALDI-TOF-Mass (Dithranol):
m / z = 617.5 [M + H] + , calc for C 31 H 40 N 2 O 3 S 4 : 616.92
化合物6−S
FT−IR(ATR,cm−1):
ν=3305(−NH−),2929(−CH2−),1643(−C=O)
1H−NMR(400.13MHz Chloroform−D):
δ=7.25(m,20H,Ar−H),5.09(q,J=7.20Hz,4H,NH(CH3)CH−Ar),2.78(t,J=7.20Hz,8H,−SCH 2CH2−),2.14(t,J=7.20Hz,8H,−CH2CH 2CO−),1.64(m,12H,−CHCH 3),1.44(m,24H,−CH2−)
13C−NMR(100.61MHz Chloroform−D):
δ=21.85,25.22,28.07,29.19,29.47,36.51,48.65,126.20,127.29,127.75,128.64,143.44,171.87
MALDI−TOF−Mass(Dithranol):
m/z=1201.12[M+H]+,calc for C52H90O4:1201.85
Compound 6-S
FT-IR (ATR, cm −1 ):
ν = 3305 (-NH -), 2929 (-CH 2 -), 1643 (-C = O)
1 H-NMR (400.13 MHz Chloroform-D):
δ = 7.25 (m, 20H, Ar-H), 5.09 (q, J = 7.20Hz, 4H, NH (CH 3) C H -Ar), 2.78 (t, J = 7. 20Hz, 8H, -SC H 2 CH 2 -), 2.14 (t, J = 7.20Hz, 8H, -
13 C-NMR (100.61 MHz Chloroform-D):
δ = 21.85, 25.22, 28.07, 29.19, 29.47, 36.51, 48.65, 126.20, 127.29, 127.75, 128.64, 143.44, 171.87
MALDI-TOF-Mass (Dithranol):
m / z = 1101.12 [M + H] + , calc for C 52 H 90 O 4 : 1201.85
(実施例2):D体テトラチアフルバレン誘導体の合成
6−ブロモヘキサン酸クロリド6.7mmolに対し、D(+)フェニルエチルアミン14.3mmolを混合し、溶媒としてテトラヒドロフラン8ml、ベースとしてトリエチルアミン13.4mmolを添加して反応させ、化合物1−Dを得た。化合物1−Dの収量は0.5g、収率は7%であった。下記にFT−IRの分析結果を示す。
(Example 2): Synthesis of D-form tetrathiafulvalene derivative 6.7 mmol of 6-bromohexanoic acid chloride was mixed with 14.3 mmol of D (+) phenylethylamine, 8 ml of tetrahydrofuran as a solvent, and 13.4 mmol of triethylamine as a base. To give compound 1-D. The yield of compound 1-D was 0.5 g, and the yield was 7%. The analysis results of FT-IR are shown below.
実施例1と同様に化合物2と3を合成し、乾燥アセトニトリル−メタノール混合溶液中に化合物3を0.385mmolに対し3.09mmolの化合物1−Dを混合し、水酸化セシウム水和物0.85mmolを添加して化合物4−Dを得た。化合物4−Dの収量は50mg、収率は36%であった。下記にMALDI−TOF−Massの分析結果を示す。
In the same manner as in Example 1,
また、酢酸−クロロホルム混合溶液中で化合物4−Dを0.38mmolと酢酸水銀1.95mmolを反応させ、化合物5−Dを得た。化合物5−Dの収量は40mg、収率は82%であった。
さらに、化合物5−D0.376mmolに亜リン酸トリエチル3mlを添加し、120℃で一晩、加熱拡拌し反応させて化合物6−Dを得た。化合物6−Dの収量は6mg、収率は15%であった。この化合物がD体のテトラチアフルバレン誘導体である。下記にMALDI−TOF−Massの分析結果を示す。
Further, 0.38 mmol of compound 4-D and 1.95 mmol of mercury acetate were reacted in an acetic acid-chloroform mixed solution to obtain compound 5-D. The yield of compound 5-D was 40 mg, and the yield was 82%.
Furthermore, 3 ml of triethyl phosphite was added to 0.376 mmol of compound 5-D, and the mixture was heated and stirred overnight at 120 ° C. to obtain compound 6-D. The yield of compound 6-D was 6 mg, and the yield was 15%. This compound is a D-form tetrathiafulvalene derivative. The analysis results of MALDI-TOF-Mass are shown below.
(実施例2における化合物の各分析結果)
化合物1−D
FT−IR(ATR,cm−1):
ν=3285(−NH−),2932(−CH2−),1639(−C=O)
(Each analysis result of the compound in Example 2)
Compound 1-D
FT-IR (ATR, cm −1 ):
ν = 3285 (-NH -), 2932 (-CH 2 -), 1639 (-C = O)
化合物4−D
MALDI−TOF−Mass(Dithranol):
m/z=632.6[M+H]+,calc for C31H40N2O2S5:632.99
Compound 4-D
MALDI-TOF-Mass (Dithranol):
m / z = 632.6 [M + H] + , calc for C 31 H 40 N 2 O 2 S 5 : 632.99
化合物6−D
MALDI−TOF−Mass(Dithranol):
m/z=1202.0[M+H]+,calc for C62H80N4O4S8:1201.85
Compound 6-D
MALDI-TOF-Mass (Dithranol):
m / z = 1202.0 [M + H] + , calc for C 62 H 80 N 4 O 4 S 8 : 1201.85
(実施例3):電荷移動錯体の形成
トルエン1mlに、S体のテトラチアフルバレン誘導体0.23mMを溶解させて、その後フッ素化テトラシアノキノジメタン11.4mMを添加した。その結果、黒緑色の沈澱物が得られた。
(Example 3): Formation of charge transfer complex 0.23 mM of S-form tetrathiafulvalene derivative was dissolved in 1 ml of toluene, and then 11.4 mM of fluorinated tetracyanoquinodimethane was added. As a result, a blackish green precipitate was obtained.
この沈澱物について紫外可視分光光度(UV−Vis)スペクトル測定、FT−IR測定を行った。UV−Visスペクトルを図3に示す。700〜900nmにフッ素化テトラシアノキノジメタンの分子内遷移、396nmにテトラチアフルバレンカチオンラジカルの分子内遷移が観察された。また、FT−IRスペクトルを図4に示す。ここで、電荷移動体に特有のブロードな吸収が高波数域で観察された。 The precipitate was subjected to ultraviolet-visible spectrophotometric (UV-Vis) spectrum measurement and FT-IR measurement. The UV-Vis spectrum is shown in FIG. Intramolecular transition of fluorinated tetracyanoquinodimethane was observed at 700 to 900 nm, and intramolecular transition of tetrathiafulvalene cation radical was observed at 396 nm. The FT-IR spectrum is shown in FIG. Here, broad absorption peculiar to the charge transfer body was observed in a high wavenumber region.
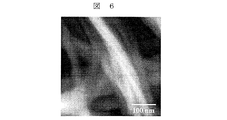
また、得られた電荷移動錯体の透過型電子顕微鏡及び走査型電子顕微鏡の観察を行った。透過型電子顕微鏡の観察結果を図5に示し、その拡大したものとして原子間力顕微鏡での観察結果を図6に示す。また、走査型電子顕微鏡の観察結果を図7に示す。 The obtained charge transfer complex was observed with a transmission electron microscope and a scanning electron microscope. The observation result with a transmission electron microscope is shown in FIG. 5, and the observation result with an atomic force microscope is shown in FIG. Moreover, the observation result of a scanning electron microscope is shown in FIG.
図5は、図2で示されたS体のテトラチアフルバレン誘導体が円状に凝集しているのに比べて、ナノファイバーを形成しており、図5の拡大図である図6をみると、左巻きに捩れたナノファイバーであることが分かる。 FIG. 5 shows that nanofibers are formed in comparison with the S-type tetrathiafulvalene derivative shown in FIG. 2 that is aggregated in a circular shape, and FIG. 6 is an enlarged view of FIG. It can be seen that the nanofiber is twisted counterclockwise.
さらに、S体テトラチアフルバレン誘導体とD体テトラチアフルバレン誘導体の円二色性スペクトル測定を行った。これより、テトラチアフルバレンの吸収領域において正と負のコットン効果が観察され、ヘリカルな組織体であることを確認した。この円二色性スペクトルを図8に示す。 Furthermore, circular dichroism spectrum measurement of S-form tetrathiafulvalene derivative and D-form tetrathiafulvalene derivative was performed. As a result, positive and negative cotton effects were observed in the tetrathiafulvalene absorption region, confirming that the tissue was a helical tissue. This circular dichroism spectrum is shown in FIG.
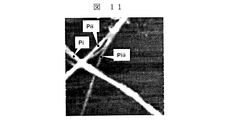
この電荷移動体の組織体において伝導度測定を行った。この結果を図9に示す。さらに、触電流像原子間力顕微鏡(PCI−AFM)測定法により、1本のナノファイバー電気伝導度を測定した。その測定値のグラフを図10、測定箇所の写真を図11に示す。 Conductivity measurement was performed on the structure of the charge transfer body. The result is shown in FIG. Furthermore, the electrical conductivity of one nanofiber was measured by a galvanostatic image atomic force microscope (PCI-AFM) measurement method. A graph of the measured values is shown in FIG. 10, and a photograph of the measurement location is shown in FIG.
キラル分子を有する新規化合物であるテトラチアフルバレン誘導体は、アクセプター分子と錯体化することで、自己組織化制御を可能とする優れた電気伝導性をもったナノファイバーを形成する。 The tetrathiafulvalene derivative, which is a novel compound having a chiral molecule, forms a nanofiber with excellent electrical conductivity that enables self-organization control by complexing with an acceptor molecule.
この電気伝導性ナノファイバーはヘリカルな構造を有しており、帯電防止材料、電極、導電線等の様々な用途で使用できるものである。 This electrically conductive nanofiber has a helical structure and can be used in various applications such as antistatic materials, electrodes, and conductive wires.
1は電荷移動錯体、2はテトラチアフルバレン誘導体、3はフッ素化テトラシアノキノジメタンである。 1 is a charge transfer complex, 2 is a tetrathiafulvalene derivative, and 3 is a fluorinated tetracyanoquinodimethane.
Claims (7)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008278534A JP2010105945A (en) | 2008-10-29 | 2008-10-29 | Tetrathiafulvalene derivative and nanofiber composed of the derivative |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008278534A JP2010105945A (en) | 2008-10-29 | 2008-10-29 | Tetrathiafulvalene derivative and nanofiber composed of the derivative |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2010105945A true JP2010105945A (en) | 2010-05-13 |
Family
ID=42295759
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008278534A Pending JP2010105945A (en) | 2008-10-29 | 2008-10-29 | Tetrathiafulvalene derivative and nanofiber composed of the derivative |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2010105945A (en) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021012809A (en) * | 2019-07-05 | 2021-02-04 | 国立大学法人東京農工大学 | Electromagnetic material, and shielding material, conductive sheet and power supply member comprising the same |
| CN115746326A (en) * | 2022-12-02 | 2023-03-07 | 桂林理工大学 | Photostimulation responsive europium-based metal organic framework for orderly packaging tetrathiafulvalene guest |
-
2008
- 2008-10-29 JP JP2008278534A patent/JP2010105945A/en active Pending
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2021012809A (en) * | 2019-07-05 | 2021-02-04 | 国立大学法人東京農工大学 | Electromagnetic material, and shielding material, conductive sheet and power supply member comprising the same |
| CN115746326A (en) * | 2022-12-02 | 2023-03-07 | 桂林理工大学 | Photostimulation responsive europium-based metal organic framework for orderly packaging tetrathiafulvalene guest |
| CN115746326B (en) * | 2022-12-02 | 2023-08-15 | 桂林理工大学 | Light stimulus response europium-based metal organic framework for orderly packaging tetrathiafulvalene object |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Dong et al. | Supramolecular interactions induced fluorescent organic nanowires with high quantum yield based on 9, 10-distyrylanthracene | |
| JP4005571B2 (en) | Amphiphilic hexaperihexabenzocoronene derivatives | |
| JPWO2007129768A1 (en) | Photoelectric conversion material containing fullerene derivative | |
| US20100019205A1 (en) | Liquid Fullerene Derivative, Method for Producing the Same, and Device Using the Same | |
| JP5062765B2 (en) | Photoelectric conversion material containing fullerene derivative | |
| JP6181317B2 (en) | Composition for photoelectric conversion element and photoelectric conversion element | |
| JP4099526B2 (en) | Separation and purification of porphyrin dimer derivatives and carbon nanotubes using them | |
| Rom et al. | Syntheses, crystal structures, topology and dual electronic behaviors of a family of amine-templated three-dimensional zinc-organophosphonate hybrid solids | |
| JP2010105945A (en) | Tetrathiafulvalene derivative and nanofiber composed of the derivative | |
| US8735594B2 (en) | Functionalized substrate and uses thereof | |
| JP5749921B2 (en) | C60-porphyrin covalent conjugate | |
| JP4884284B2 (en) | Tubular nano-sized self-assembled body in which hexaperihexabenzocoronene (HBC) derivatives substituted with fluorine-containing groups are oriented in the plane direction, and method for producing the same | |
| JP2014220286A (en) | Thermoelectric conversion element | |
| WO2010132951A1 (en) | Oligothiophenes and uses thereof in photovoltaic devices | |
| WO2009113511A1 (en) | Liquid porphyrin derivative and method for producing the same | |
| JP2012236777A (en) | Indolocarbazole-containing imide compound, and intermediate for synthesizing the same, method for producing them, organic semiconductor composition, and organic solar cell element | |
| Liang et al. | Synthesis of oligo (para-phenylenevinylene) methyl thiols for self-assembled monolayers on gold surfaces | |
| JP5211362B2 (en) | Azo compound having linker and metal ion recovery method using the azo compound | |
| JPH0631219B2 (en) | Fulvalene derivative | |
| JP2013008647A (en) | Solid conductive material | |
| JP5860313B2 (en) | Intramolecular donor-acceptor type molecules useful as dyes for organic solar cells | |
| JP2021012809A (en) | Electromagnetic material, and shielding material, conductive sheet and power supply member comprising the same | |
| JP2000344779A (en) | Photoconductive silicon complex, liquid crystalline material and its composition and element using the same | |
| JP4849410B2 (en) | Fullerene derivative and method for producing the same | |
| JP5015040B2 (en) | Field effect transistor using supramolecular nanotubes with fullerenes on the inner and outer wall surfaces |