JP2010006705A - Her2サブセット - Google Patents
Her2サブセット Download PDFInfo
- Publication number
- JP2010006705A JP2010006705A JP2008155676A JP2008155676A JP2010006705A JP 2010006705 A JP2010006705 A JP 2010006705A JP 2008155676 A JP2008155676 A JP 2008155676A JP 2008155676 A JP2008155676 A JP 2008155676A JP 2010006705 A JP2010006705 A JP 2010006705A
- Authority
- JP
- Japan
- Prior art keywords
- cancer
- affinity ligand
- her2
- seq
- subset
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
Abstract
【解決手段】ブドウ球菌プロテインAおよびそのドメイン、リポカリン、アンキリンリピートドメイン、セルロース結合ドメイン、γクリスタリン、緑色蛍光タンパク質、ヒト細胞毒性Tリンパ球関連抗原4、プロテアーゼ阻害剤、PDZドメイン、ペプチドアプタマー、ブドウ球菌ヌクレアーゼ、テンダミスタット、フィブロネクチンIII型ドメインおよびジンクフィンガーからなる群から選択される骨格に由来するタンパク質リガンド。
【選択図】なし
Description
ヒト上皮増殖因子受容体2(HER2またはerbB-2)は、膜貫通受容体チロシンキナーゼのファミリーである、上皮増殖因子受容体ファミリー(EGFR、HER2、HER3、HER4)のメンバーである。これらの受容体は、全体的に40-50%の配列同一性を有し、同様のドメインを有する。それらは全て、細胞外リガンド結合ドメイン、単一の、膜を貫通する部分、および細胞内チロシンキナーゼおよび調節ドメインを含む。
上皮増殖因子受容体ファミリーのメンバーは、様々な癌の種類、例えば、上皮性悪性腫瘍における腫瘍細胞増殖を促進することが分かっている。HER2は様々なヒト細胞腫において研究されており、多数の腫瘍において、特に乳腺、肺、膵臓および結腸直腸癌、およびウィルムス腫瘍において、さらに卵巣、膀胱、子宮内膜、腎臓、頭頸部、胃、食道および前立腺癌において、上方制御されることが見出されている(Menard et al (2001) Annals of Oncology 12 (Suppl. 1) S15-S19。
癌は、西欧諸国における疾患および死亡の最も一般的な要因のひとつである。一般に、ほとんどの型の癌において、罹患率は年齢と共に増加する。一般健康状態の向上によりヒト集団はより長い生存を続けているので、癌はより多くの個体に影響し得る。最も一般的な種類の癌の要因は依然として大部分は未知であるが、環境要因(食事、タバコの煙、UV照射など)ならびに遺伝的要因(「癌遺伝子」、例えば、p53、APC、BRCA1、XPなどにおける生殖細胞系列変異)と、癌発症の危険性との連関が認識されている個体が増加している。
乳癌は、2番目に最も一般的な形態の世界的な癌であり、圧倒的に女性において最も頻繁に起こる癌である。Parkinらが表したGLOBOCAM 2002データベースのデータにより、2002年には115万の新しい症例が、および同期間に41万の死亡例が明らかにされている(Parkin DM et al. (2005) CA Cancer J Clin 55, 74-108)。早期の段階に発見された場合、予後は、先進国で生活する患者において比較的良好であり、一般に発展途上国の57%に対して73%の5年生存率を有する。罹患率は緩やかに増加しており、先進諸国の女性の約9人に1人が寿命中に乳癌になると考えられている。外来性ホルモンへの曝露を含む、雌性ステロイドホルモンに関する生活様式の変化は、乳癌の発症の危険性に影響するが、これらの要因は病因のほんの一部分を占めるに過ぎず、予防処置の利益は低いと考えられている。死亡率の減少は、マンモブラフィー検診による早期発見および現代の全身的補助(adjuvant)療法の使用によるものである。
癌の処置には、例えば、手術、放射線治療、化学療法、標的療法、免疫治療、ホルモン療法および血管新生阻害剤が含まれる。
乳房保存手術と術後放射線治療を組み合わせた乳房保存治療は、1970年代後期に導入されてから、女性が主に選択する処置となっており、腫瘍の根本的な切除と良好な美容的仕上がりが両立できる。それでもやはり、乳房切除術は、一部の患者、すなわち小さな乳房に大きな腫瘍(>4 cm)を有する、または多巣性/多中心性疾患を有する女性において好ましい。
本発明の一局面の目的は、HER2の細胞外ドメインからのアミノ酸残基のサブセットを提供することである。本発明の他の局面の目的は、そのサブセットと相互作用することができる親和性リガンド、およびかかる親和性リガンドを含む組成物を提供することである。本発明の特定の他の局面のさらなる目的は、そのサブセットを標的、例えば治療のための標的として利用する使用および方法を提供することである。
a)第三の局面によるポリペプチドを、結合を可能にする条件において推定の親和性リガンドと接触させる工程;および
b)推定の親和性リガンドがそのポリペプチドと結合するか否かを決定する工程。
c)推定の親和性リガンドが、癌細胞、例えば乳癌細胞、例えばBT474乳癌細胞の増殖を阻害する、またはそれらのアポトーシスを誘導するか否かを決定する工程。
a)第三の局面によるポリペプチドを、1以上の推定の親和性リガンドと接触させる工程;および
b)そのポリペプチドと結合する親和性リガンドを同定する工程。
a)第一の局面によるサブセットを含む抗原により免疫化された哺乳動物から得られた、そのサブセットと選択的に相互作用することができる抗体をコードするDNAを含む細胞を提供する;および
b)それらの細胞を骨髄腫細胞と融合させ、少なくとも1つのクローンを得る。
a')哺乳動物を抗原により免疫化する工程、
ここで、工程a')は工程a)に先行する。
c)工程b)からの、本サブセットと選択的に相互作用することができる抗体を分泌するクローンを選択する工程。
d)工程b)において得られるクローン、または工程c)において選択されたクローンを提供し、そのクローンにより発現された、サブセットと選択的に相互作用する抗体の少なくとも一部をコードする、クローンからのDNAを、ヒト抗体を産生するDNAと統合する工程;および
e)工程d)からの統合したDNAを細胞に組み込み、HER2の過剰発現を特徴とする障害の処置のための治療用抗体を発現するためのクローンを得る工程。
本発明の上記の局面の様々な実施形態による親和性リガンド、例えば、第一の局面の親和性リガンドおよび第二の局面の第2の親和性リガンドは、あらゆる種類の親和性リガンドであり得る。
上記の局面(一から八の局面)の実施形態において、HER2の過剰発現を特徴とする障害は癌であり得る。
1.抗原の作製
a)材料および方法
EnsEMBL遺伝子ID ENSG00000141736によってコードされた標的タンパク質の適切なフラグメントを、生物情報学的ツールを用いて、ヒトゲノム配列を鋳型として選択した(Lindskog M et al (2005) Biotechniques 38:723-727、EnsEMBL、www.ensembl.org)。そのフラグメントを、HER2タンパク質(配列番号2;EnsEMBLエントリー番号ENSP00000269571)のアミノ酸274-400(配列番号1)に対応する127アミノ酸長フラグメントの産生のための鋳型として用いた。そのタンパク質フラグメントを、生じる親和性試薬の望まれない交差反応性を最小化し、かつ依然として、立体構造のエピトープの形成および細菌系における効果的な発現が可能である適切なサイズであるように、他のヒトタンパク質に対して低配列類似性を有する独特の配列からなるように設計した。
HER2遺伝子の長転写物(配列番号3)のヌクレオチド1058-1438に対応し、標的タンパク質HER2(配列番号2)のアミノ酸274-400からなるペプチド(配列番号1)をコードする遺伝子フラグメントを、ヒトRNAプールから、そのタンパク質フラグメントに特異的なプライマーを用いてRT-PCRにより成功裡に単離した。
a)材料および方法
上記のようにして得られた精製HER2フラグメントを抗原として用い、国の指針に従ってウサギを免疫化した(スウェーデン許認可番号A 84-02)。ウサギを一次免疫化としてフロイント完全アジュバント中の抗原200μgを筋肉内投与して免疫化し、4週間の間隔をおいてフロイント不完全アジュバント中の抗原100μgにより3回追加免役した。
下記の3b節を参照のこと。
a)材料および方法
EnsEMBL遺伝子ID ENSG00000141736(EnsEMBL、www.ensembl.org)によってコードされた標的タンパク質の3つのフラグメントを、免疫化のために用いたタンパク質フラグメント(配列番号1)との適切なオーバーラップについて選択した。HER2タンパク質(配列番号2;EnsEMBLエントリー番号ENSP00000269571)のアミノ酸236-363(配列番号4)、347-492(配列番号5)および364-530(配列番号6)に対応するこれらの3つのタンパク質フラグメントを、上記の免疫化のために用いたタンパク質フラグメント(配列番号1)と類似の方法にて産生した。
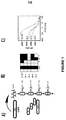
免疫化のために用いたタンパク質フラグメントのC末端、中間およびN末端部分にそれぞれ対応する特異的タンパク質配列、ならびに完全抗原フラグメント(配列番号1)を含む4つの短いアフィニティーカラムを、選択的アフィニティークロマトグラフィーが可能なように連続的に結合させた。この方法により、抗原特異的抗体を以下の4つの個別の抗体集団へと分ける分離ができた:msAb-N(集団の18%)、msAb-M(集団の35%)、msAb-C(集団の39%)、msAb-S(集団の8%)(図1a)。
a)タンパク質アレイ
親和性精製抗体画分の特異性および選択性を、タンパク質アレイ構成において、免疫化に用いたタンパク質フラグメント(配列番号1)およびそれにオーバーラップするタンパク質フラグメント(配列番号4-6)を含む抗原自体に対する結合分析、および92の他のヒトタンパク質フラグメントに対する結合分析により分析した(Nilsson P et al (2005) Proteomics 5:4327-4337)。タンパク質フラグメントを0.1 M尿素および1×PBS(pH 7.4)中40μg/mlまで希釈し、それぞれ50μlを96ウェルスポットプレートのウェルに移した。タンパク質フラグメントをpin-and-ring arrayer(Affymetrix 427)を用いてエポキシスライド(SuperEpoxy、TeleChem)上に二複製ずつスポットし、固定化した。スライドを1×PBS中にて洗浄し(5分)、次いで表面を30分間ブロックした(SuperBlock(登録商標)、Pierce)。接着性16ウェルシリコンマスク(adhesive 16-well silicone mask)(Schleicher&Schuell)をそのガラスに適用し、単一特異性抗体を加え(1×PBSTに約50 ng/mlとなるよう1:5000に希釈)、シェーカー上にて60分間インキュベートした。アフィニティータグ特異的IgY抗体を、各スポットにおけるタンパク質の量を定量化するために単一特異性抗体とともに、共インキュベーションした。スライドを1×PBSTおよび1×PBSにより2回、各10分間洗浄した。二次抗体(Alexa 647とコンジュゲートしたヤギ抗ウサギ抗体、およびAlexa 555とコンジュゲートしたヤギ抗ニワトリ抗体、Molecular Probes)を1×PBSTにおいて30 ng/mlになるよう1:60000に希釈し、60分間インキュベートした。はじめのインキュベーションと同じ洗浄手順を行った後、スライドを遠心力で脱水し、スキャンした(G2565BA array scanner、Agilent);その後、画像を画像分析ソフトウェア(GenePix 5.1、Axon Instruments)を用いて定量化した。
さらに、特異性、選択性および相対的親和性をLuminexサスペンションビーズアレイシステムを用いて分析した。結合特異性のマルチプレックスな分析を、先に報告されているように行った(Schwenk et al., 2007)。短く説明すると、免疫化に用いた抗原(配列番号1)およびサブ精製抗原に用いた3つのフラグメント(配列番号4-6)、1つのHisABPフラグメントおよび1つの抗ウサギIgG抗体を含む98のタンパク質フラグメントに対応する100のビーズIDの抗体希釈物およびビーズ混合物をPBSTにおいて調製した。msAb希釈物45μlをビーズ5μlに加え、96ウェルプレート(Corning)において混合しながら60分間インキュベートした。次に、R-フィコエリトリン標識化抗ウサギIgG抗体(0.5μg/ml、Jackson ImmunoResearch)25μlを加え、最後に60分間インキュベーションした。
競合タンパク質フラグメントの連続希釈をPBST中に調製し、msAb-866、msAb-N、msAb-MおよびmsAb-Cの溶液と1:1の割合にて混合した。インキュベーションは全体積50μlにて撹拌しながら60分間行った。次に、msAb-PrEST溶液を各ウェルにつきビーズ混合物5μlを含む第2のプレートに移した。60分後、R-フィコエリトリン標識化抗ウサギIgG抗体(0.5μg/ml、Jackson ImmunoResearch)25μl を加え、さらに60分間インキュベートした。独立して3回繰り返して行い、それらの平均値をデータ分析に用いた。4つのパラメーターのロジスティックな関数を競合曲線に適合するように選択し、EC50値を計算し、相対的な結合の質を比較する。競合についての測定として、得られた曲線をそれらの形および標準誤差よりも高い数値であるべき推定EC50値について観察した。
測定をLuminex LX200計測手段を用いてLuminex IS 2.3ソフトウェアにより行った。各実験についてビーズIDにつき100事象をカウントし、相互作用を示すために平均蛍光強度(MFI)を選択した。データ分析およびグラフ表示を、R(統計学的コンピュータ計算およびグラフィックスのための言語および環境)(a language and environment for statistical computing and graphics)(Ihaka and Gentleman、1996)により行った。
親和性精製後の抗体特異性および選択性を検証するために、タンパク質マイクロアレイ分析を平面アレイおよびLuminexサスペンションビーズアレイ技術を用いて行った。分析により、His6-tagおよびABP-tagに対する抗体が成功裡に枯渇していることを確認し(結果は示さず)ならびに、高特異性抗体が、固定された他のタンパク質フラグメントとの非特異的相互作用の可能性の低さを有することを確かめた(図1b)。
a)細胞培養物
BT474乳癌細胞をアメリカン・タイプ・カルチャー・コレクション(ATCC、Manassas、VA)から購入し、10%FCSおよび1%ウシインスリンを補足したRPMIにおいて維持し、37℃、5%CO2の湿気のある環境に保持した。
細胞をトリプシン処理により培養皿から遊離させ、遠心分離し、PBS:HSA(1%ヒト血清アルブミンを補足したPBS pH 7.2)に再懸濁し、カウントした。96ウェルプレートにおいて、150000細胞を、抗体(msAb-N、msAb-M、msAb-CおよびmsAb-866)0.35μgにより反応体積75μlにて室温において45分間標識化した。洗浄剤として2×100μl PBS:HSAを用いて非結合抗体を洗い流した。次いで、Alexa 488とコンジュゲートした二次ヤギ抗ウサギモノクローナル抗体(Invitrogen)0.35μgを用いて反応体積75μlにて45分間室温にて抗体を標識化した。細胞をPBS:HSA 2×100μlにて洗浄し、サンプルチューブ中に最終体積が150ulになるように再懸濁した。抗体のBT474細胞との結合能を、FL-1(488 nmでの励起)にて蛍光放出を測定するBD FACS Vantage SE flowcytometer(BD Biosciences)を用いて蛍光励起細胞分取により評価した。HER2の細胞内部分(HPA001383、Atlas Antibodies AB、Sweden)を標的とする等モル量のウサギ単一特異性抗体(msAb-intra)を陰性対照として用い、細胞を二次抗体のみにより標識化した。トラスツズマブ(Herceptin、Roche)を陽性細胞標識対照として用い、Alexa 488ヤギ抗ヒトモノクローナル抗体(Invitrogen)を二次試薬として用いた。
BT474細胞を24ウェル皿に5×104細胞/ウェルにて播種した。24時間後、1 ng/ml〜1000 ng/mlの範囲の濃度のmsAb-866の3複製の希釈において細胞を処理した。PBS pH 7.2により処理した細胞を対照として用いた。5日後、細胞をトリプシン処理し、それぞれ3回カウントした。増殖阻害を、非処置培養物に対する細胞の百分率として算出した。
0日目にBT474細胞を24ウェル皿に5×104細胞/ウェルにて播種した。2つの抗体の再構成ミックスを、3b)において得られた画分の比率を用いて作製した:msAb-NおよびmsAb-Cは18:39の比で混合し、msAb-NCと名付けた;msAb-N、msAb-MおよびmsAb-Cは18:35:39の比で混合し、msAb-NMCと名付けた。24時間後、細胞をmsAb-866、msAb-N、msAb-M、msAb-C、msAb-NCおよびmsAb-NMCの3複製の希釈物において最終抗体濃度500 ng/mlを用いて処理した。msAb-intraおよびPBS pH 7.2を対照として用いた。5日後、細胞をトリプシン処理し、それぞれ3回カウントした。増殖阻害を、対照抗体msAb-intraにより処理した培養物に対する細胞の百分率として算出した。
1日目に、BT474細胞を、5×104細胞/ウェルにて、msAb-866、msAb-Cおよびトラスツズマブの希釈物とともに、最終抗体濃度500 ng/mlを用いて3複製分播種した。msAb-intraおよびPBS pH 7.2を対照として用いた。4日後、細胞をトリプシン処理し、それぞれ3回カウントした。増殖阻害を、対照抗体msAb-intraにより処理した培養物に対する細胞の百分率として算出した。
msAb-866、msAb-NおよびmsAb-Cにより標識化したBT474細胞の蛍光励起細胞分取は、非標識化細胞に対して高い蛍光に富む集団を示し、これは細胞結合を示しており、一方msAb-intraまたはmsAb-Mについては有意な蛍光の豊富さは見られなかった(図2)。
a)ブドウ球菌ディスプレイベクターへのライブラリーのサブクローニング
大腸菌株RR1ΔM15(Ruther, U. pUR 250 allows rapid chemical sequencing of both DNA strands of its inserts. Nucleic. Acids Res. 10, 5765-5772 (1982))を、プラスミド構成のための宿主株として用いた。新たな制限部位(PmeI)を含有する遺伝子フラグメントを、BamHIおよびSalI(New England Biolabs、Beverly、MA)により消化された先に報告されているブドウ球菌ベクターpSCXm(Wernerus, H.&Stahl、S. Vector engineering to improve a staphylococcal surface display system. FEMS Microbiol Lett 212、47-54 (2002).)にライゲートすることにより、新たなブドウ球菌ベクター、pSCEM1を作製した。N末端FLAG配列を有するHER2-ECDの増幅のための鋳型を得た。遺伝子フラグメントをPCRにより増幅し(9.6 ml、プールした)、無作為なフラグメントを作製するために、50ml Falconチューブ中において氷上にてマイクロチップ(microtip)を用いて60分間超音波処理した(21%の振幅、一定の超音波処理)。その後サンプルをCentricon Plus 20 column(CO 10 kDa;Millipore、Billerica、MA)を用いて限外濾過により濃縮した。濃縮したフラグメントを平滑末端化し、T4 DNAポリメラーゼおよびT4ポリヌクレオチドキナーゼ(New England Biolabs)を製造者の推奨に従って加えてフラグメントをリン酸化した。その後、平滑末端化した遺伝子フラグメントを、T4 DNA Ligase(Invitrogen、Carlsbad、CA)を用いてPmeI(New England Biolabs)により消化したブドウ球菌ディスプレイベクター、pSCEM1へライゲートした。ライブラリーを、電気的形質転換受容性である(electrocompetent)スタフィロコッカス・カルノスス(S. carnosus)TM300(Gotz, F. Staphylococcus carnosus: a new host organism for gene cloning and protein production. Soc. Appl. Bacteriol. Symp. Ser. 19, 49S-53S (1990))に、先に報告されているように(Lofblom, J., Kronqvist, N., Uhlen, M., Stahl, S.&Wernerus, H. Optimization of electroporation-mediated transformation: Staphylococcus carnosus as model organism. J Appl Microbiol 102, 736-747 (2007))形質転換し、15%グリセリン中、−80℃にて保存した。
Sc:HER2-libまたはSc:Ephrin-B3-libのアリコート(少なくとも10倍のライブラリーサイズ)を、20μg/mlのクロラムフェニコールを含むTSB+Y(トリプシン大豆ブロス+酵母エキス)100 mlに播種し、37℃、150 rpmにて一晩増殖させた。16時間後、107細胞を、0.1%Pluronic(登録商標)F108 NF Sufactant(PBSP; BASF Corporation、Mount Olive、NJ)を含むリン酸緩衝生理食塩水(PBS、pH 7.4)1 mlにより洗浄した。細胞を遠心分離(3500×g、4℃、6分)によりペレット化し、抗体(すなわちエピトープマッピングに用いる抗体;典型的には約100 nMの濃度)を含有するPBSP 100μlに再懸濁し、緩やかに混合しながら平衡結合に達するまで室温にて1時間インキュベートした。その後、細胞を氷冷したPBSP 1 mlにより洗浄し、次いで4μg/mlのAlexa Fluor(登録商標)488ヤギ抗ウサギIgGまたは4μg/mlのAlexa Fluor(登録商標)488ヤギ抗マウスIgG(Invitrogen)および225 nMのAlexa Fluor(登録商標)647 HSAコンジュゲートを含有するPBSP 1 mlにおいて、暗中、氷上にて1時間インキュベーションした。氷冷したPBSP 1 mlにおける最後の洗浄工程の後、細胞を分別する前に氷冷したPBSP 300μlに再懸濁した。細胞をFACSVantage SE(BD Biosciences、San Jose、CA)フローサイトメーターを用いて分別した。細胞をB2培地(Lofblom, J., Kronqvist, N., Uhlen, M., Stahl, S.&Wernerus, H. Optimization of electroporation-mediated transformation: Staphylococcus carnosus as model organism. J Appl Microbiol 102, 736-747 (2007))0.5 mlに直接分別し、10μg/mlのクロラムフェニコールを含有する血液寒天基礎培地(blood agar base)(Merck)プレート上に広げ、37℃にて24時間インキュベートした。最後のラウンドにおいて、細胞を半固体培地を含有する96ウェルプレートの個々のウェルに分別し、コロニーを形成させた。
それぞれのコロニーの一部をPCRのために96ウェルプレートの2つの別のウェルに移した。ブドウ球菌ディスプレイベクターの挿入領域を、2つの別のプライマー対を用いてPCRにより増幅し、フォワード末端およびリバース末端のそれぞれにビオチン分子を含有する2つのPCR産物が得られた。それぞれの挿入物の両方の末端における10サイクルのピロシークエンシングを、PSQ(商標)96 HS instrument(Biotage AB、Uppsala、Sweden)を用いて製造者の指示書に従って行った。エピトープ配列をBLASTを用いて抗原配列にマッピングした(Altschul et al, Basic local alignment search tool, J.Mol.Biol. 147:195-197, (1990))。
Claims (83)
- HER2の細胞外ドメイン2および3(配列番号7)からの37以下の連続アミノ酸残基のサブセットと選択的に相互作用することができる親和性リガンドであって、該サブセットがアミノ酸配列LQVF(配列番号8)および/またはESFDGD(配列番号9)を含む、親和性リガンド。
- 前記サブセットが26アミノ酸残基以下である、請求項1に記載の親和性リガンド。
- 前記サブセットが配列番号11および15-20からなる群から選択される、請求項2に記載の親和性リガンド。
- 前記サブセットが21アミノ酸残基以下である、請求項2に記載の親和性リガンド。
- 前記サブセットがLQVF(配列番号8)および/またはLPESFDGD(配列番号11)を含む、前記請求項のいずれかに記載の親和性リガンド。
- 前記サブセットが10アミノ酸残基以上である、前記請求項のいずれかに記載の親和性リガンド。
- 前記サブセットが8アミノ酸残基以下である、請求項1〜5のいずれかに記載の親和性リガンド。
- 前記サブセットが配列番号6のアミノ酸1-37の配列である、請求項1に記載の親和性リガンド。
- 培養物中におけるヒト乳癌細胞の増殖を、HER2の細胞外ドメインと選択的に相互作用することができない親和性リガンドに比して20-100%阻害する、前記請求項のいずれかに記載の親和性リガンド。
- ヒト乳癌細胞がBT474乳癌細胞である、請求項9に記載の親和性リガンド。
- 500 ng/mlの濃度にて増殖を阻害する、請求項9〜10のいずれかに記載の親和性リガンド。
- 100 nM未満のEC50にてサブセットと結合する、前記請求項のいずれかに記載の親和性リガンド。
- 医薬として用いるための、前記請求項のいずれかに記載の親和性リガンド。
- HER2の過剰発現を特徴とする障害を有する、または有する疑いのある哺乳類対象を処置するための、前記請求項のいずれかに記載の親和性リガンド。
- 前記対象が、HER2、例えばHER2の細胞外ドメインと選択的に相互作用することができる、前記親和性リガンドとは異なる治療用抗体によって処置されている、請求項14に記載の親和性リガンド。
- HER2の過剰発現を特徴とする障害が癌であり、該癌が前記治療用抗体に対して耐性を生じたものである、請求項15に記載の親和性リガンド。
- HER2の過剰発現を特徴とする障害が癌である、前記請求項のいずれかに記載の親和性リガンド。
- 癌が、乳癌、扁平上皮癌、肺癌、例えば小細胞または非小細胞肺癌、膵臓癌、膠芽腫、子宮頸癌、卵巣癌、外陰癌、肝臓癌、肝細胞癌、結腸直腸癌、例えば結腸癌、子宮内膜細胞腫、唾液腺癌、腎臓癌、甲状腺癌、ウィルムス腫瘍、膀胱癌、子宮内膜癌、腎臓の癌、頭頸部癌、胃癌、食道癌および前立腺癌からなる群から選択される、請求項17に記載の親和性リガンド。
- 癌が、乳癌、肺癌、膵臓癌、結腸直腸癌およびウィルムス腫瘍からなる群から選択される、請求項18に記載の親和性リガンド。
- 癌が乳癌である、請求項19に記載の親和性リガンド。
- 癌が転移性乳癌である、請求項20に記載の親和性リガンド。
- 抗体またはそのフラグメントまたは誘導体である、前記請求項のいずれかに記載の親和性リガンド。
- ブドウ球菌プロテインAおよびそのドメイン、リポカリン、アンキリンリピートドメイン、セルロース結合ドメイン、γクリスタリン、緑色蛍光タンパク質、ヒト細胞毒性Tリンパ球関連抗原4、プロテアーゼ阻害剤、PDZドメイン、ペプチドアプタマー、ブドウ球菌ヌクレアーゼ、テンダミスタット、フィブロネクチンIII型ドメインおよびジンクフィンガーからなる群から選択される骨格に由来するタンパク質リガンドである、請求項1〜21のいずれかに記載の親和性リガンド。
- オリゴヌクレオチド分子である、請求項1〜21のいずれかに記載の親和性リガンド。
- 前記請求項のいずれかに記載の親和性リガンド、およびHER2の細胞外ドメイン2および3(配列番号7)からの73以下の連続アミノ酸残基の第2のサブセットと選択的に相互作用することができる第2の親和性リガンドを含む組成物であって、該第2のサブセットが配列番号12、配列番号13および/または配列番号14のアミノ酸配列を含む、組成物。
- 第2のサブセットが配列番号21-35からなる群から選択される、請求項25に記載の組成物。
- 第2のサブセットが50アミノ酸残基以下である、請求項25に記載の組成物。
- 第2のサブセットが16アミノ酸残基以下である、請求項27に記載の組成物。
- 第2のサブセットが配列番号4の配列のアミノ酸39-111である、請求項25に記載の組成物。
- 培養物中におけるヒト乳癌細胞の増殖を、HER2の細胞外ドメインと選択的に相互作用することができない親和性リガンドに比して20〜100%阻害する、請求項25〜29のいずれかに記載の組成物。
- ヒト乳癌細胞がBT474 乳癌細胞である、請求項30に記載の組成物。
- 500 ng/mlの濃度にて増殖を阻害する、請求項30〜31のいずれかに記載の組成物。
- 第2の親和性リガンドが100 nM未満のEC50にて第2のサブセットと結合する、請求項25〜32のいずれかに記載の組成物。
- 第2の親和性リガンドが、抗体またはそのフラグメントもしくは誘導体である、請求項25〜33のいずれかに記載の組成物。
- 第2の親和性リガンドが、ブドウ球菌プロテインAおよびそのドメイン、リポカリン、アンキリンリピートドメイン、セルロース結合ドメイン、γクリスタリン、緑色蛍光タンパク質、ヒト細胞毒性Tリンパ球関連抗原4、プロテアーゼ阻害剤、PDZドメイン、ペプチドアプタマー、ブドウ球菌ヌクレアーゼ、テンダミスタット、フィブロネクチンIII型ドメインおよびジンクフィンガーからなる群から選択される骨格に由来するタンパク質リガンドである、請求項25〜33のいずれかに記載の組成物。
- 第2の親和性リガンドがオリゴヌクレオチド分子である、請求項25〜33のいずれかに記載の組成物。
- 請求項1〜24のいずれかに記載の親和性リガンドまたは請求項25〜36のいずれかに記載の組成物、およびHER2に対するチロシンキナーゼ阻害剤を含む組成物。
- 医薬として使用するための、請求項25〜37のいずれかに記載の組成物。
- HER2の過剰発現を特徴とする障害を有する、または有する疑いのある哺乳類対象を処置するための、請求項25〜38のいずれかに記載の組成物。
- 前記対象が、HER2、例えばHER2の細胞外ドメインと選択的に相互作用することができる、前記親和性リガンドおよび第2の親和性リガンドとは異なる治療用抗体によって処置されている、請求項39に記載の組成物。
- HER2の過剰発現を特徴とする障害が癌であり、該癌が前記治療用抗体に耐性を生じたものである、請求項40に記載の組成物。
- HER2の細胞外ドメイン2および3(配列番号7)からの37以下の連続アミノ酸残基からなり、アミノ酸配列LQVF(配列番号8)および/またはESFDGD(配列番号9)を含む、単離ポリペプチド。
- 26アミノ酸残基以下からなる、請求項42に記載のポリペプチド。
- 配列番号11および15-20からなる群から選択されるアミノ酸配列からなる、請求項42〜43のいずれかに記載のポリペプチド。
- 21アミノ酸残基以下からなる、請求項42〜44のいずれかに記載のポリペプチド。
- アミノ酸配列LQVF(配列番号8)および/またはLPESFDGD(配列番号11)を含む、請求項42〜45のいずれかに記載のポリペプチド。
- 10アミノ酸残基以上からなる、請求項42〜46のいずれかに記載のポリペプチド。
- 8アミノ酸残基以下からなる、請求項42〜46のいずれかに記載のポリペプチド。
- 配列LQVFを含む場合に、LQVFのC末端側に隣接する2以下のアミノ酸を有する、請求項42〜48のいずれかに記載のポリペプチド。
- 配列番号6の配列のアミノ酸1-37からなる、請求項42に記載のポリペプチド。
- 抗原として使用するための、請求項42〜50のいずれかに記載のポリペプチド。
- 免疫化において抗原として使用するための、請求項42に記載のポリペプチド。
- 治療用抗体の調製において使用するための、請求項42〜52のいずれかに記載のポリペプチド。
- 抗原としての、請求項42〜53のいずれかに記載のポリペプチドの使用。
- 免疫化のための、請求項42〜53のいずれかに記載のポリペプチドの使用。
- 免疫化がヒトでない哺乳動物の免疫化である、請求項55に記載の使用。
- 治療用抗体の調製における、請求項42〜53のいずれかに記載のポリペプチドの使用。
- HER2の過剰発現を特徴とする障害を処置するための治療用親和性リガンドの選択または精製における、請求項42〜53のいずれかに記載のポリペプチドの使用。
- 治療標的としての、請求項42〜53のいずれかに記載のポリペプチドの使用。
- 医薬としての、請求項1〜24のいずれかに記載の親和性リガンドの使用。
- HER2の過剰発現を特徴とする障害を有する、または有する疑いのある哺乳類対象を処置するための医薬の製造における、請求項1〜24のいずれかに記載の親和性リガンドの使用。
- 前記対象が、HER2、例えばHER2の細胞外ドメインと選択的に相互作用することができ、前記親和性リガンドとは異なる治療用抗体によって処置されている、請求項61に記載の使用。
- HER2の過剰発現を特徴とする障害が癌であり、該癌が前記治療用抗体に耐性を生じたものである、請求項62に記載の使用。
- HER2の過剰発現を特徴とする障害の処置のための親和性リガンドを同定する方法であって、以下の工程を含む方法:
a)請求項35〜45のいずれかに記載のポリペプチドを、結合を可能とする条件において、推定の親和性リガンドと接触させる工程;および
b)推定の親和性リガンドが該ポリペプチドと結合するか否かを決定する工程。 - 障害が癌であり、さらに以下の工程を含む、請求項64に記載の方法:
c)推定の親和性リガンドが、癌細胞、例えばBT474乳癌細胞の増殖を阻害するか、または該癌細胞のアポトーシスを誘導するか否かを決定する工程。 - クローンを産生する方法であって、以下の工程を含む方法:
a)請求項1〜24のいずれかに記載のサブセットを含む抗原により免疫化された哺乳動物から得られる、該サブセットと選択的に相互作用することができる抗体をコードするDNAを含む細胞を提供する工程;および
b)該細胞を骨髄腫細胞と融合させて少なくとも1つのクローンを得る工程。 - さらに以下の工程を含む、請求項66に記載の方法:
a')哺乳動物を抗原により免疫化する工程、
ここで工程a')は工程a)に先行する。 - 以下の工程をさらに含む、請求項66〜67のいずれかに記載の方法:
c)前記サブセットと選択的に相互作用することができる抗体を発現する、工程b)からのクローンを選択する工程。 - 工程a)の抗原が、請求項42〜53のいずれかに記載のポリペプチドからなる、請求項66〜67のいずれかに記載の方法。
- さらに以下の工程を含む、請求項69に記載の方法:
c)前記抗原と選択的に相互作用することができる抗体を発現する、工程b)からのクローンを選択する工程。 - さらに以下の工程を含む、請求項66〜70のいずれかに記載の方法:
d)工程b)において得られる、または工程c)において選択されるクローンを提供し、該クローンからのDNAであって、該クローンにより発現される、前記サブセットと選択的に相互作用する抗体の少なくとも一部をコードするDNAを、ヒト抗体産生DNAと統合させる工程;および
e)工程d)からの統合されたDNAを細胞に組み込み、HER2の過剰発現を特徴とする障害を処置するための治療用抗体の発現のためのクローンを得る工程。 - HER2の過剰発現を特徴とする障害を有する、または有する疑いのある哺乳類対象を処置する方法であって、有効量の請求項1〜24のいずれかに記載の親和性リガンドまたは請求項25〜41のいずれかに記載の組成物を対象に投与することを含む方法。
- HER2に対するチロシンキナーゼ阻害剤を対象に投与することをさらに含む、請求項72に記載の方法。
- 前記処置が前外科的処置である、請求項72〜73のいずれかに記載の方法。
- 前記処置が手術後の処置である、請求項72〜73のいずれかに記載の方法。
- 前記対象が、HER2、例えばHER2の細胞外ドメインと選択的に相互作用することができる、前記親和性リガンドとは異なる治療用抗体によって処置されている、請求項72〜75のいずれかに記載の方法。
- HER2の過剰発現を特徴とする障害が癌であり、該癌が前記治療用抗体に対する耐性を生じたものである、請求項76に記載の方法。
- HER2の過剰発現を特徴とする障害が癌である、請求項72〜77のいずれかに記載の方法。
- 癌が、乳癌、扁平上皮癌、肺癌、例えば小細胞または非小細胞肺癌、膵臓癌、膠芽腫、子宮頸癌、卵巣癌、外陰癌、肝臓癌、肝細胞癌、結腸直腸癌、例えば結腸癌、子宮内膜細胞腫、唾液腺癌、腎臓癌、甲状腺癌、ウィルムス腫瘍、膀胱癌、子宮内膜癌、腎臓の癌、頭頸部癌、胃癌、食道癌および前立腺癌からなる群から選択される、請求項78に記載の方法。
- 癌が、乳癌、肺癌、膵臓癌、結腸直腸癌およびウィルムス腫瘍からなる群から選択される、請求項79に記載の方法。
- 癌が乳癌である、請求項80に記載の方法。
- 癌が転移性乳癌である、請求項81に記載の方法。
- 容器、請求項1〜24のいずれかに記載の親和性リガンドまたは請求項25〜41のいずれかに記載の組成物を含む、該容器内の組成物、および該容器上のまたは該容器に結合した標識、を含む製造品であって、該標識が、該組成物がHER2の過剰発現を特徴とする障害を処置するために用いることができることを示す、製造品。
Priority Applications (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008155676A JP2010006705A (ja) | 2008-06-13 | 2008-06-13 | Her2サブセット |
| PCT/SE2008/000694 WO2009151356A1 (en) | 2008-06-13 | 2008-12-12 | Antibodies against extracellular domains 2 and 3 or her2 |
| AU2008357729A AU2008357729A1 (en) | 2008-06-13 | 2008-12-12 | Antibodies against extracellular domain 2 and 3 of HER2 |
| KR1020127017264A KR20130026418A (ko) | 2008-06-13 | 2008-12-12 | Her2 의 세포외 도메인 2 및 3 에 대한 항체 |
| CA2727941A CA2727941A1 (en) | 2008-06-13 | 2008-12-12 | Antibodies against extracellular domains 2 and 3 or her2 |
| EP08874636A EP2294088A1 (en) | 2008-06-13 | 2008-12-12 | Antibodies against extracellular domains 2 and 3 or her2 |
| US12/997,823 US20110158988A1 (en) | 2008-06-13 | 2008-12-12 | Antibodies against extracellular domains 2 and 3 or her2 |
| CN2008801297639A CN102099376A (zh) | 2008-06-13 | 2008-12-12 | 针对her2的细胞外结构域2和3的抗体 |
| KR1020107027939A KR20110036534A (ko) | 2008-06-13 | 2008-12-12 | Her2 의 세포외 도메인 2 및 3 에 대한 항체 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008155676A JP2010006705A (ja) | 2008-06-13 | 2008-06-13 | Her2サブセット |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010006705A true JP2010006705A (ja) | 2010-01-14 |
| JP2010006705A5 JP2010006705A5 (ja) | 2011-07-21 |
Family
ID=40427661
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008155676A Pending JP2010006705A (ja) | 2008-06-13 | 2008-06-13 | Her2サブセット |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20110158988A1 (ja) |
| EP (1) | EP2294088A1 (ja) |
| JP (1) | JP2010006705A (ja) |
| KR (2) | KR20130026418A (ja) |
| CN (1) | CN102099376A (ja) |
| AU (1) | AU2008357729A1 (ja) |
| CA (1) | CA2727941A1 (ja) |
| WO (1) | WO2009151356A1 (ja) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013529904A (ja) * | 2010-05-27 | 2013-07-25 | ゲンマブ エー/エス | Her2に対するモノクローナル抗体 |
| JP2013534809A (ja) * | 2010-05-27 | 2013-09-09 | ゲンマブ エー/エス | Her2エピトープに対するモノクローナル抗体 |
| KR101759209B1 (ko) | 2010-01-22 | 2017-07-19 | 성균관대학교산학협력단 | Her-2 과발현 유방암 세포 또는 조직에 특이적으로 결합할 수 있는 핵산 압타머 및 그 용도 |
| JP2021509288A (ja) * | 2017-11-14 | 2021-03-25 | グリーン クロス ラボ セル コーポレーションGreen Cross Lab Cell Corporation | 抗−her2抗体又はその抗原結合フラグメント、及びこれを含むキメラ抗原受容体 |
| US11649294B2 (en) | 2017-11-14 | 2023-05-16 | GC Cell Corporation | Anti-HER2 antibody or antigen-binding fragment thereof, and chimeric antigen receptor comprising same |
| US11970547B2 (en) | 2017-11-14 | 2024-04-30 | GC Cell Corporation | Anti-HER2 antibody or antigen-binding fragment thereof, and chimeric antigen receptor comprising same |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8609095B2 (en) | 2010-03-04 | 2013-12-17 | Symphogen A/S | Anti-HER2 antibodies and compositions |
| AU2016201799B2 (en) * | 2010-05-27 | 2017-09-07 | Genmab A/S | Monoclonal antibodies aganst HER2 epitope |
| US20140170149A1 (en) | 2011-04-20 | 2014-06-19 | Genmab A/S | Bispecific antibodies against her2 and cd3 |
| CN105017425B (zh) * | 2014-04-30 | 2018-02-16 | 京天成生物技术(北京)有限公司 | 抗her2中和活性单克隆抗体及其应用 |
| WO2019116089A2 (en) * | 2017-12-11 | 2019-06-20 | Medizinische Universitaet Wien | A method of producing a vaccine composition and uses thereof |
| EP3842460A1 (en) * | 2019-03-01 | 2021-06-30 | RemeGen Co., Ltd. | Antibody for her2 concomitant diagnosis immunohistochemical detection and application thereof |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5726023A (en) * | 1993-03-17 | 1998-03-10 | University Of Washington | Immune reactivity to HER-2/neu protein for diagnosis and treatment of malignancies in which the HER-2/neu oncogene is associated |
| WO2001041787A1 (en) * | 1999-12-10 | 2001-06-14 | Epimmune Inc. | INDUCING CELLULAR IMMUNE RESPONSES TO HER2/neu USING PEPTIDE AND NUCLEIC ACID COMPOSITIONS |
| US20030027766A1 (en) * | 1995-03-14 | 2003-02-06 | Board Of Regents, The University Of Texas System | Methods and compositions for stimulating T-lymphocytes |
| WO2004052917A2 (en) * | 2002-12-10 | 2004-06-24 | Epimmune Inc. | Hla-a1, a2 -a3,-a24,-b7,and -b44 tumor associated antigen peptides and compositions |
| WO2006007398A1 (en) * | 2004-06-16 | 2006-01-19 | Genentech, Inc. | Therapy of platinum-resistant cancer |
| WO2007118660A2 (en) * | 2006-04-13 | 2007-10-25 | Bio Life Science Forschungs- Und Entwicklungsges M.B.H. | Her-2/neu multi-peptide vaccine |
| WO2007146959A2 (en) * | 2006-06-12 | 2007-12-21 | Receptor Biologix Inc. | Pan-cell surface receptor- specific therapeutics |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5783404A (en) * | 1995-04-13 | 1998-07-21 | Amgen Inc. | Methods and compositions for determining HER-2/neu expression using monoclonal antibodies |
| WO2002102973A2 (en) * | 2001-06-20 | 2002-12-27 | Prochon Biotech Ltd. | Antibodies that block receptor protein tyrosine kinase activation, methods of screening for and uses thereof |
| CN1136917C (zh) * | 2001-10-10 | 2004-02-04 | 北京迪威华宇生物技术有限公司 | 一种卡介苗热休克蛋白65和多表位her-2抗原融合蛋白重组蛋白疫苗 |
| US7767792B2 (en) * | 2004-02-20 | 2010-08-03 | Ludwig Institute For Cancer Research Ltd. | Antibodies to EGF receptor epitope peptides |
| ES2521140T3 (es) * | 2004-07-22 | 2014-11-12 | Genentech, Inc. | Composición de anticuerpos de HER2 |
| CN101165068B (zh) * | 2006-10-18 | 2011-09-21 | 上海复旦张江生物医药股份有限公司 | 抗HER2/ErbB2抗原的单克隆抗体及其制备方法和药物组合物 |
-
2008
- 2008-06-13 JP JP2008155676A patent/JP2010006705A/ja active Pending
- 2008-12-12 US US12/997,823 patent/US20110158988A1/en not_active Abandoned
- 2008-12-12 EP EP08874636A patent/EP2294088A1/en not_active Withdrawn
- 2008-12-12 AU AU2008357729A patent/AU2008357729A1/en not_active Abandoned
- 2008-12-12 KR KR1020127017264A patent/KR20130026418A/ko not_active Application Discontinuation
- 2008-12-12 WO PCT/SE2008/000694 patent/WO2009151356A1/en active Application Filing
- 2008-12-12 KR KR1020107027939A patent/KR20110036534A/ko active Search and Examination
- 2008-12-12 CA CA2727941A patent/CA2727941A1/en not_active Abandoned
- 2008-12-12 CN CN2008801297639A patent/CN102099376A/zh active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5726023A (en) * | 1993-03-17 | 1998-03-10 | University Of Washington | Immune reactivity to HER-2/neu protein for diagnosis and treatment of malignancies in which the HER-2/neu oncogene is associated |
| US20030027766A1 (en) * | 1995-03-14 | 2003-02-06 | Board Of Regents, The University Of Texas System | Methods and compositions for stimulating T-lymphocytes |
| WO2001041787A1 (en) * | 1999-12-10 | 2001-06-14 | Epimmune Inc. | INDUCING CELLULAR IMMUNE RESPONSES TO HER2/neu USING PEPTIDE AND NUCLEIC ACID COMPOSITIONS |
| WO2004052917A2 (en) * | 2002-12-10 | 2004-06-24 | Epimmune Inc. | Hla-a1, a2 -a3,-a24,-b7,and -b44 tumor associated antigen peptides and compositions |
| WO2006007398A1 (en) * | 2004-06-16 | 2006-01-19 | Genentech, Inc. | Therapy of platinum-resistant cancer |
| WO2007118660A2 (en) * | 2006-04-13 | 2007-10-25 | Bio Life Science Forschungs- Und Entwicklungsges M.B.H. | Her-2/neu multi-peptide vaccine |
| WO2007146959A2 (en) * | 2006-06-12 | 2007-12-21 | Receptor Biologix Inc. | Pan-cell surface receptor- specific therapeutics |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101759209B1 (ko) | 2010-01-22 | 2017-07-19 | 성균관대학교산학협력단 | Her-2 과발현 유방암 세포 또는 조직에 특이적으로 결합할 수 있는 핵산 압타머 및 그 용도 |
| JP2013529904A (ja) * | 2010-05-27 | 2013-07-25 | ゲンマブ エー/エス | Her2に対するモノクローナル抗体 |
| JP2013534809A (ja) * | 2010-05-27 | 2013-09-09 | ゲンマブ エー/エス | Her2エピトープに対するモノクローナル抗体 |
| JP2017038599A (ja) * | 2010-05-27 | 2017-02-23 | ゲンマブ エー/エス | Her2に対するモノクローナル抗体 |
| JP2017046694A (ja) * | 2010-05-27 | 2017-03-09 | ゲンマブ エー/エス | Her2エピトープに対するモノクローナル抗体 |
| JP2021509288A (ja) * | 2017-11-14 | 2021-03-25 | グリーン クロス ラボ セル コーポレーションGreen Cross Lab Cell Corporation | 抗−her2抗体又はその抗原結合フラグメント、及びこれを含むキメラ抗原受容体 |
| US11649294B2 (en) | 2017-11-14 | 2023-05-16 | GC Cell Corporation | Anti-HER2 antibody or antigen-binding fragment thereof, and chimeric antigen receptor comprising same |
| JP7386796B2 (ja) | 2017-11-14 | 2023-11-27 | グリーン クロス ラボ セル コーポレーション | 抗-her2抗体又はその抗原結合フラグメント、及びこれを含むキメラ抗原受容体 |
| US11970547B2 (en) | 2017-11-14 | 2024-04-30 | GC Cell Corporation | Anti-HER2 antibody or antigen-binding fragment thereof, and chimeric antigen receptor comprising same |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102099376A (zh) | 2011-06-15 |
| KR20130026418A (ko) | 2013-03-13 |
| CA2727941A1 (en) | 2009-12-17 |
| KR20110036534A (ko) | 2011-04-07 |
| EP2294088A1 (en) | 2011-03-16 |
| AU2008357729A1 (en) | 2009-12-17 |
| AU2008357729A8 (en) | 2011-02-03 |
| WO2009151356A1 (en) | 2009-12-17 |
| US20110158988A1 (en) | 2011-06-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2010006705A (ja) | Her2サブセット | |
| AU2016340764B2 (en) | Binding molecules that inhibit cancer growth | |
| US10793633B2 (en) | Therapeutic peptides | |
| DK2494359T3 (en) | PODXL protein in colorectal cancer | |
| TW201713684A (zh) | 用於對抗食道癌及其他癌症的新穎胜肽及胜肽的組合物 | |
| CN109069639B (zh) | Gitr抗体、方法及用途 | |
| EP2396346B1 (en) | Rbm3 protein in colorectal cancer prognostics | |
| AU2018274932A1 (en) | Cancer cell-specific antibody, anticancer drug and cancer testing method | |
| KR20140107615A (ko) | 엑소좀 검출용 모노클로날 항체 | |
| KR20180026758A (ko) | 식도암 및 기타 암에 대한 면역요법에 사용하기 위한 펩티드 및 펩티드의 조합 | |
| WO2018094282A1 (en) | Engineered antibodies and uses thereof | |
| US9416176B2 (en) | RBM3 protein in colorectal cancer prognostics | |
| WO2018115377A9 (en) | Immunocytokines with progressive activation mechanism | |
| CN112823168A (zh) | 结合her2的四聚体多肽 | |
| 성준식 | Development and Characterization of Monoclonal Antibody Specific to Oncogenic Variant AIMP2-DX2 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20110223 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20110223 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110519 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110519 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130205 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130502 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130510 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130730 |