JP2009000525A - 磁気共鳴装置による潅流の自動決定方法および装置 - Google Patents
磁気共鳴装置による潅流の自動決定方法および装置 Download PDFInfo
- Publication number
- JP2009000525A JP2009000525A JP2008160828A JP2008160828A JP2009000525A JP 2009000525 A JP2009000525 A JP 2009000525A JP 2008160828 A JP2008160828 A JP 2008160828A JP 2008160828 A JP2008160828 A JP 2008160828A JP 2009000525 A JP2009000525 A JP 2009000525A
- Authority
- JP
- Japan
- Prior art keywords
- magnetic resonance
- perfusion
- resonance data
- organism
- data
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01R—MEASURING ELECTRIC VARIABLES; MEASURING MAGNETIC VARIABLES
- G01R33/00—Arrangements or instruments for measuring magnetic variables
- G01R33/20—Arrangements or instruments for measuring magnetic variables involving magnetic resonance
- G01R33/44—Arrangements or instruments for measuring magnetic variables involving magnetic resonance using nuclear magnetic resonance [NMR]
- G01R33/48—NMR imaging systems
- G01R33/54—Signal processing systems, e.g. using pulse sequences ; Generation or control of pulse sequences; Operator console
- G01R33/56—Image enhancement or correction, e.g. subtraction or averaging techniques, e.g. improvement of signal-to-noise ratio and resolution
- G01R33/563—Image enhancement or correction, e.g. subtraction or averaging techniques, e.g. improvement of signal-to-noise ratio and resolution of moving material, e.g. flow contrast angiography
- G01R33/56341—Diffusion imaging
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/02—Detecting, measuring or recording pulse, heart rate, blood pressure or blood flow; Combined pulse/heart-rate/blood pressure determination; Evaluating a cardiovascular condition not otherwise provided for, e.g. using combinations of techniques provided for in this group with electrocardiography or electroauscultation; Heart catheters for measuring blood pressure
- A61B5/026—Measuring blood flow
- A61B5/0263—Measuring blood flow using NMR
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/05—Detecting, measuring or recording for diagnosis by means of electric currents or magnetic fields; Measuring using microwaves or radio waves
- A61B5/055—Detecting, measuring or recording for diagnosis by means of electric currents or magnetic fields; Measuring using microwaves or radio waves involving electronic [EMR] or nuclear [NMR] magnetic resonance, e.g. magnetic resonance imaging
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01R—MEASURING ELECTRIC VARIABLES; MEASURING MAGNETIC VARIABLES
- G01R33/00—Arrangements or instruments for measuring magnetic variables
- G01R33/20—Arrangements or instruments for measuring magnetic variables involving magnetic resonance
- G01R33/44—Arrangements or instruments for measuring magnetic variables involving magnetic resonance using nuclear magnetic resonance [NMR]
- G01R33/48—NMR imaging systems
- G01R33/54—Signal processing systems, e.g. using pulse sequences ; Generation or control of pulse sequences; Operator console
- G01R33/56—Image enhancement or correction, e.g. subtraction or averaging techniques, e.g. improvement of signal-to-noise ratio and resolution
- G01R33/563—Image enhancement or correction, e.g. subtraction or averaging techniques, e.g. improvement of signal-to-noise ratio and resolution of moving material, e.g. flow contrast angiography
- G01R33/56366—Perfusion imaging
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01R—MEASURING ELECTRIC VARIABLES; MEASURING MAGNETIC VARIABLES
- G01R33/00—Arrangements or instruments for measuring magnetic variables
- G01R33/20—Arrangements or instruments for measuring magnetic variables involving magnetic resonance
- G01R33/44—Arrangements or instruments for measuring magnetic variables involving magnetic resonance using nuclear magnetic resonance [NMR]
- G01R33/48—NMR imaging systems
- G01R33/4806—Functional imaging of brain activation
Landscapes
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- High Energy & Nuclear Physics (AREA)
- Radiology & Medical Imaging (AREA)
- Heart & Thoracic Surgery (AREA)
- Surgery (AREA)
- General Physics & Mathematics (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Signal Processing (AREA)
- Biophysics (AREA)
- Pathology (AREA)
- Biomedical Technology (AREA)
- Vascular Medicine (AREA)
- Medical Informatics (AREA)
- Molecular Biology (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Physiology (AREA)
- Cardiology (AREA)
- Hematology (AREA)
- Magnetic Resonance Imaging Apparatus (AREA)
Abstract
【解決手段】潅流に感応する撮像シーケンスによりボリューム要素(15)から複数の第1の磁気共鳴データ(21)が時間経過と共に検出され、制御撮像シーケンス、特に潅流に感応しない撮像シーケンスにより同一のボリューム要素(15)から複数の第2の磁気共鳴データ(22)が時間経過と共に検出される。ボリューム要素(15)における潅流(μ)を決定するために、これらの第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の統計的解析(16)が行なわれる。
【選択図】図2A
Description
潅流に感応する撮像シーケンスによりボリューム要素から検出される複数の第1の磁気共鳴データを時間経過と共に作成するステップと、
制御撮像シーケンスにより同一のボリューム要素から検出される複数の第2の磁気共鳴データを時間経過と共に作成するステップと、
ボリューム要素における潅流を決定するために第1の磁気共鳴データおよび第2の磁気共鳴データの統計的解析を行なうステップと
を有することによって解決される。
磁気共鳴装置による潅流の自動決定方法に関する本発明の実施態様は次の通りである。
・ 制御撮像シーケンスは潅流に感応しない撮像シーケンスである(請求項2)。
・ 潅流に感応する撮像シーケンスは潅流に感応する傾斜磁場設定により作成され、潅流に感応しない撮像シーケンスは潅流に感応しない傾斜磁場設定により作成される(請求項3)。
・ 第1の磁気共鳴データおよび第2の磁気共鳴データから一連の磁気共鳴画像が作成され、時間経過と共に(つまり経時的に)個々の画素の信号経過が求められる(請求項4)。前記信号経過が前記統計的解析により検査され、係数が求められ、この係数の解析により潅流に関する情報が求められる(請求項5)。
・ ボリューム要素について第1の磁気共鳴データの成分および第2の磁気共鳴データの成分が交互に検出される(請求項6)。
・ 前記統計的解析が、一般線形モデルにしたがって、またはスチューデントのt検定にしたがって、または相互相関にしたがって行なわれる(請求項7)。
・ 前記統計的解析に少なくとも1つのモデル関数が少なくとも1つのリグレッサとして付加され、該少なくとも1つのリグレッサは、磁気共鳴装置によって検出された測定結果から導き出されたリグレッサと、磁気共鳴装置に属さない装置によって検出されたリグレッサと、潅流測定が行なわれる生物の機能的変化から導き出されたリグレッサとを有するグループの中の1つ又は複数のリグレッサを含む(請求項8)。
・ 前記統計的解析に少なくとも1つのモデル関数が少なくとも1つのリグレッサとして付加され、該少なくとも1つのリグレッサは、潅流測定が行なわれる生物の運動と、磁気共鳴装置の走査安定性と、生物の呼吸と、生物の心拍動と、生物の生理学的状態と、生物の機能的活性とを有するグループの中の1つ又は複数のリグレッサを含む(請求項9)。
・ 前記統計的解析によって、方法によりボリューム要素について求められた結果の信頼性に関する情報と、ボリューム要素の画素についてのコントラスト対ノイズ比に関する情報と、アーチファクトに関する情報とを有するグループから少なくとも1つの他の結果が求められ、前記アーチファクトが、潅流測定が行なわれる生物の呼吸と、生物の心拍動と、生物の運動と、生物の機能的活性と、BOLD効果とを含む(請求項10)。前記統計的解析によって検出されたアーチファクトが予め定められた閾値を上回っている場合、既に作成された第1の磁気共鳴データおよび第2の磁気共鳴データが方法から排除されることおよび/または他の第1の磁気共鳴データおよび第2の磁気共鳴データが作成されることによって、作成された第1の磁気共鳴データおよび第2の磁気共鳴データの品質制御が前記少なくとも1つの結果により行なわれる(請求項11)。
・ ボリューム要素の磁気共鳴画像は、前記統計的解析により、該磁気共鳴画像が、ボリューム要素の組織の血中酸素含有量に関する情報と、潅流測定が行なわれる生物の機能的活性に関する情報と、BOLD効果と機能的活性との相関結果に関する情報とを有するグループの中の少なくとも1つの情報を含んでいるように作成される(請求項12)。
・ ボリューム要素の磁気共鳴画像は、絶えずリアルタイムで作成され、新しい第1の磁気共鳴データおよび第2の磁気共鳴データによって更新される(請求項13)。
・ ボリューム要素の磁気共鳴画像は、第1の磁気共鳴データおよび第2の磁気共鳴データの全体に基づいて、または第1の磁気共鳴データおよび第2の磁気共鳴データの一部分に基づいて作成される(請求項14)。
・ 前記統計的解析が一般線形モデルにより実施され、該一般線形モデルの係数は、この係数がボリューム要素における相対的または絶対的な潅流単位を生じるように基準化される(請求項15)。
潅流の自動決定装置が、磁気共鳴装置を制御する制御ユニットと、磁気共鳴装置によって撮影されたボリューム要素の複数の第1の磁気共鳴データおよび第2の磁気共鳴データを受信する受信装置と、第1の磁気共鳴データおよび第2の磁気共鳴データを評価して第1の磁気共鳴データおよび第2の磁気共鳴データに基づいてボリューム要素における潅流を可視化するボリューム要素の磁気共鳴画像を作成する評価装置とを含み、
磁気共鳴装置が第1の磁気共鳴データの受信時にボリューム要素において潅流に感応する撮像シーケンスを実行しかつ磁気共鳴装置が第2の磁気共鳴データの受信時にボリューム要素において制御撮像シーケンスを実行するように潅流の自動決定装置が制御ユニットを介して磁気共鳴装置を制御し、
評価装置がボリューム要素における潅流を決定するために第1の磁気共鳴データおよび第2の磁気共鳴データの統計的解析を実行することによって解決される。
・ 潅流の自動決定装置は、磁気共鳴装置が第2の磁気共鳴データの作成時にボリューム要素において潅流に感応しない撮像シーケンスを実行するように制御ユニットを介して磁気共鳴装置を制御する請求項(17)。
・ 制御ユニットは、受信装置が第1の磁気共鳴データの成分と第2の磁気共鳴データの成分とを交互に受信するように制御される(請求項18)。
・ 評価装置は一般線形モデルにしたがって、またはスチューデントのt検定にしたがって、または相互相関にしたがって前記統計的解析を行なう(請求項19)。
・ 評価装置は前記統計的解析時に少なくとも1つのモデル関数を少なくとも1つのリグレッサとして付加し、該少なくとも1つのリグレッサは、磁気共鳴装置によって検出された測定結果から導き出されたリグレッサと、磁気共鳴装置に属さない装置によって検出されたリグレッサと、潅流測定が行なわれる生物の機能的変化から導き出されたリグレッサとを有するグループの中の1つ又は複数のリグレッサを含む(請求項20)。
・ 評価装置は前記統計的解析時に少なくとも1つのモデル関数を少なくとも1つのリグレッサとして付加し、該少なくとも1つのリグレッサは、潅流測定が行なわれる生物の運動と、磁気共鳴装置の走査安定性と、生物の呼吸と、生物)の心拍動と、生物の運動と、生物の生理学的状態と、生物の機能的活性とを有するグループの中の1つ又は複数のリグレッサを含む(請求項21)。
・ 評価装置は、前記統計的解析によって少なくとも1つの他の結果を、方法によってボリューム要素について求められた結果の信頼性に関する情報と、ボリューム要素の画素についてのコントラスト対ノイズ比に関する情報と、アーチファクトに関する情報とを有するグループから求め、前記アーチファクトが、潅流測定が行なわれる生物の呼吸と、生物の心拍動と、生物の運動と、生物の機能的活性と、BOLD効果とを含む(請求項22)。前記統計的解析によって検出されたアーチファクトが予め定められた閾値を上回っていることを評価装置が検出した場合に、評価装置が既に作成された第1の磁気共鳴データおよび第2の磁気共鳴データを磁気共鳴画像の作成から排除することおよび/または装置が他の第1の磁気共鳴データおよび第2の磁気共鳴データを作成することによって、潅流の自動決定装置が、前記少なくとも1つの結果により、作成された第1の磁気共鳴データおよび第2の磁気共鳴データの品質制御を行なう(請求項23)。
・ 評価装置は、前記統計的解析により磁気共鳴画像を、該磁気共鳴画像が、ボリューム要素の組織の血中酸素含有量に関する情報と、潅流測定が行なわれる生物の機能的活性に関する情報と、BOLD効果と機能的活性との相関結果に関する情報とを有するグループの中の少なくとも1つの情報を含むように作成する(請求項24)。
・ 評価装置は、磁気共鳴画像を絶えずリアルタイムで作成し、新しい第1の磁気共鳴データおよび第2の磁気共鳴データによって更新する(請求項25)。
・ 評価装置は、磁気共鳴画像を、第1の磁気共鳴データおよび第2の磁気共鳴データの全体に基づいてまたは第1の磁気共鳴データおよび第2の磁気共鳴データの一部分に基づいて作成する(請求項26)。
・ 評価装置は一般線形モデルを用いて前記統計的解析を実施し、評価装置は、一般線形モデルの係数がボリューム要素における相対的または絶対的な潅流単位を生じるように一般線形モデルの係数を基準化する(請求項27)。
・ 潅流の自動決定装置が上述した本発明による方法を実施する(請求項28)。
●磁気共鳴装置によって検出された測定結果から導き出されたリグレッサ:例えば、測定結果から磁気共鳴装置の系統的な誤差が導き出される場合には、この誤差が相応のモデル関数を介して統計的解析によって考慮される。潅流決定が行なわれる生物の運動も、剛体の運動であるかぎり、つまり運動時に体の変形が生じないかぎり、測定結果を介して検出される。
●磁気共鳴装置に属さない装置によって検出されたリグレッサ:第1および第2の磁気共鳴データの検出が影響を及ぼされる障害がこれらの装置によって検出される場合には、これらの故障は相応のモデル関数を介して統計的解析によって考慮される。
●生物の機能的変化もしくは変更から導き出されたリグレッサ:機能的変化のもとで、特に生物の生理学的状態の変化または生物の機能的活性が生じる。機能的活性の例は、生物の体部分、例えば指の周期的な動きである。機能的活性は、潅流変化を介して、脳血流量の変化を介して、またはBOLD(=Blood Oxygenation Level Dependent、血中酸素レベル依存)効果によって検出可能である。
●生物の運動:これは、特に予定外の運動と理解すべきである。
●磁気共鳴装置の走査安定性:例えば、磁気共鳴装置が第1および第2の磁気共鳴データを検出する安定性が一定でない場合に、第1および第2の磁気共鳴データの検出は或る振動の影響下にある。
●生物の呼吸:呼吸に依存して生物の少なくとも一部が動く。
●生物の心拍動:心拍動に依存して少なくとも生物の心臓が動き、他方では、例えば血液の流速も心拍動に依存する。
●当該ボリューム要素についての本発明による方法によって求められた結果の信頼性に関する情報:例えばスチューデントのt検定により、例えば本発明にしたがって決定された定量的な潅流情報がどのように良好であるかの品質指定がなされる。
●ボリューム要素内部の特定の画素についてのコントラスト対ノイズ比に関する情報:それによって、好ましいことに本発明による方法によって決定された潅流情報の質に関する検証が可能である。
●次のアーチファクトに関する情報:
○生物の呼吸、
○生物の心拍動、
○生物の運動、
○生物の機能的活性、
○BOLD効果。
●観察すべきボリューム要素の組織の血中酸素含有量の変化:BOLD効果が磁気共鳴装置によって検出された結果に対して影響を有するので、血中酸素含有量の変化を第1および第2の磁気共鳴データから導き出すことができる。
●生物の機能的活性:生物の機能的活性が同様に磁気共鳴装置によって検出された結果に対して影響を有するので、機能的活性の範囲を第1および第2の磁気共鳴データから導き出すことができる。
●BOLD効果と特定の機能的活性との間の相関結果:統計的解析が既に潅流情報の検出のために使用されることから、統計的解析によりBOLD効果と特定の機能的活性との間の相関も求めるために多大な費用はかからない。
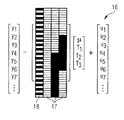
図2Aは第1および第2の磁気共鳴データもしくは磁気共鳴画像の時系列を示し、
図2Bは第1および第2の磁気共鳴データの相応の一般線形モデルを示す。
1 局所コイル
2 寝台
3 断層撮影部
4 測定空間
5 磁気共鳴装置
6 制御装置
7 端末装置
8 画面
9 キーボード
10 マウス
11 制御ユニット
12 受信装置
13 評価ユニット
14 DVD
15 ボリューム要素
16 一般線形モデル
17 関数モデル
18 潅流モデル
19 ボクセル
21 第1の磁気共鳴データ
22 第2の磁気共鳴データ
Claims (31)
- 磁気共鳴装置(5)による潅流の自動決定方法であって、
潅流に感応する撮像シーケンスによりボリューム要素(15)から検出される複数の第1の磁気共鳴データ(21)を時間経過と共に作成するステップと、
制御撮像シーケンスにより同一のボリューム要素(15)から検出される複数の第2の磁気共鳴データ(22)を時間経過と共に作成するステップと、
ボリューム要素(15)における潅流(μ)を決定するために第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の統計的解析(16)を行なうステップと
を有する磁気共鳴装置による潅流の自動決定方法。 - 制御撮像シーケンスは潅流に感応しない撮像シーケンスである請求項1記載の方法。
- 潅流に感応する撮像シーケンスは潅流に感応する傾斜磁場設定により作成され、潅流に感応しない撮像シーケンスは潅流に感応しない傾斜磁場設定により作成される請求項2記載の方法。
- 第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)から一連の磁気共鳴画像が作成され、時間経過と共に個々の画素(19)の信号経過が求められる請求項1乃至3の1つに記載の方法。
- 前記信号経過が前記統計的解析(16)により検査され、係数(μ)が求められ、この係数(μ)の解析により潅流に関する情報が求められる請求項4記載の方法。
- ボリューム要素(15)について第1の磁気共鳴データ(21)の成分および第2の磁気共鳴データ(22)の成分が交互に検出される請求項1乃至5の1つに記載の方法。
- 前記統計的解析(16)が、一般線形モデル(16)にしたがって、またはスチューデントのt検定にしたがって、または相互相関にしたがって行なわれる請求項1乃至6の1つに記載の方法。
- 前記統計的解析(16)に少なくとも1つのモデル関数(17)が少なくとも1つのリグレッサとして付加され、該少なくとも1つのリグレッサは、磁気共鳴装置(5)によって検出された測定結果から導き出されたリグレッサと、磁気共鳴装置(5)に属さない装置によって検出されたリグレッサと、潅流測定が行なわれる生物(0)の機能的変化から導き出されたリグレッサとを有するグループの中の1つ又は複数のリグレッサを含む請求項1乃至7の1つに記載の方法。
- 前記統計的解析(16)に少なくとも1つのモデル関数(17)が少なくとも1つのリグレッサとして付加され、該少なくとも1つのリグレッサは、潅流測定が行なわれる生物(0)の運動と、磁気共鳴装置(5)の走査安定性と、生物(0)の呼吸と、生物(0)の心拍動と、生物(0)の生理学的状態と、生物(0)の機能的活性とを有するグループの中の1つ又は複数のリグレッサを含む請求項1乃至8の1つに記載の方法。
- 前記統計的解析(16)によって、方法によりボリューム要素(15)について求められた結果の信頼性に関する情報と、ボリューム要素(15)の画素(19)についてのコントラスト対ノイズ比に関する情報と、アーチファクトに関する情報とを有するグループから少なくとも1つの他の結果が求められ、前記アーチファクトが、潅流測定が行なわれる生物(0)の呼吸と、生物(0)の心拍動と、生物(0)の運動と、生物(0)の機能的活性と、BOLD効果とを含む請求項1乃至9の1つに記載の方法。
- 前記統計的解析(16)によって検出されたアーチファクトが予め定められた閾値を上回っている場合、既に作成された第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)が方法から排除されることおよび/または他の第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)が作成されることによって、作成された第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の品質制御が前記少なくとも1つの結果により行なわれる請求項10記載の方法。
- ボリューム要素(15)の磁気共鳴画像は、前記統計的解析(16)により、該磁気共鳴画像が、ボリューム要素(15)の組織の血中酸素含有量に関する情報と、潅流測定が行なわれる生物(0)の機能的活性に関する情報と、BOLD効果と機能的活性との相関結果に関する情報とを有するグループの中の少なくとも1つの情報を含んでいるように作成される請求項1乃至11の1つに記載の方法。
- ボリューム要素(15)の磁気共鳴画像は、絶えずリアルタイムで作成され、新しい第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)によって更新される請求項1乃至12の1つに記載の方法。
- ボリューム要素(15)の磁気共鳴画像は、第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の全体に基づいて、または第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の一部分に基づいて作成される請求項1乃至13の1つに記載の方法。
- 前記統計的解析が一般線形モデル(16)により実施され、該一般線形モデルの係数(μ)は、この係数(μ)がボリューム要素(15)における相対的または絶対的な潅流単位を生じるように基準化される請求項1乃至14の1つに記載の方法。
- 磁気共鳴装置用の潅流の自動決定装置であって、
潅流の自動決定装置(6)が、磁気共鳴装置(5)を制御する制御ユニット(11)と、磁気共鳴装置(5)によって撮影されたボリューム要素(15)の複数の第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)を受信する受信装置(12)と、第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)を評価して第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)に基づいてボリューム要素(15)における潅流(μ)を可視化するボリューム要素(15)の磁気共鳴画像を作成する評価装置(13)とを含み、
磁気共鳴装置(5)が第1の磁気共鳴データ(21)の受信時にボリューム要素(15)において潅流に感応する撮像シーケンスを実行しかつ磁気共鳴装置(5)が第2の磁気共鳴データ(22)の受信時にボリューム要素(15)において制御撮像シーケンスを実行するように潅流の自動決定装置(6)が制御ユニット(11)を介して磁気共鳴装置(5)を制御し、
評価装置(13)がボリューム要素(15)における潅流(μ)を決定するために第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の統計的解析(16)を実行する磁気共鳴装置用の潅流の自動決定装置。 - 潅流の自動決定装置(6)は、磁気共鳴装置(5)が第2の磁気共鳴データ(22)の作成時にボリューム要素(15)において潅流に感応しない撮像シーケンスを実行するように制御ユニット(11)を介して磁気共鳴装置(5)を制御する請求項16記載の装置。
- 制御ユニット(11)は、受信装置(12)が第1の磁気共鳴データ(21)の成分と第2の磁気共鳴データ(22)の成分とを交互に受信するように制御される請求項16又は17記載の装置。
- 評価装置(13)は一般線形モデル(16)にしたがって、またはスチューデントのt検定にしたがって、または相互相関にしたがって前記統計的解析を行なう請求項16乃至18の1つに記載の装置。
- 評価装置(13)は前記統計的解析時に少なくとも1つのモデル関数(17)を少なくとも1つのリグレッサとして付加し、該少なくとも1つのリグレッサは、磁気共鳴装置(5)によって検出された測定結果から導き出されたリグレッサと、磁気共鳴装置(5)に属さない装置によって検出されたリグレッサと、潅流測定が行なわれる生物(0)の機能的変化から導き出されたリグレッサとを有するグループの中の1つ又は複数のリグレッサを含む請求項16乃至19の1つに記載の装置。
- 評価装置(13)は前記統計的解析時に少なくとも1つのモデル関数(17)を少なくとも1つのリグレッサとして付加し、該少なくとも1つのリグレッサは、潅流測定が行なわれる生物(0)の運動と、磁気共鳴装置(5)の走査安定性と、生物(0)の呼吸と、生物(0)の心拍動と、生物(0)の運動と、生物(0)の生理学的状態と、生物(0)の機能的活性とを有するグループの中の1つ又は複数のリグレッサを含む請求項16乃至20の1つに記載の装置。
- 評価装置(13)は、前記統計的解析(16)によって少なくとも1つの他の結果を、方法によってボリューム要素(15)について求められた結果の信頼性に関する情報と、ボリューム要素(15)の画素についてのコントラスト対ノイズ比に関する情報と、アーチファクトに関する情報とを有するグループから求め、前記アーチファクトが、潅流測定が行なわれる生物(0)の呼吸と、生物(0)の心拍動と、生物(0)の運動と、生物(0)の機能的活性と、BOLD効果とを含む請求項16乃至21の1つに記載の装置。
- 前記統計的解析(16)によって検出されたアーチファクトが予め定められた閾値を上回っていることを評価装置(13)が検出した場合に、評価装置(13)が既に作成された第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)を磁気共鳴画像の作成から排除することおよび/または装置(6)が他の第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)を作成することによって、潅流の自動決定装置(6)が、前記少なくとも1つの結果により、作成された第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の品質制御を行なう請求項22記載の装置。
- 評価装置(13)は、前記統計的解析(16)により磁気共鳴画像を、該磁気共鳴画像が、ボリューム要素(15)の組織の血中酸素含有量に関する情報と、潅流測定が行なわれる生物(0)の機能的活性に関する情報と、BOLD効果と機能的活性との相関結果に関する情報とを有するグループの中の少なくとも1つの情報を含むように作成する請求項16乃至23の1つに記載の装置。
- 評価装置(13)は、磁気共鳴画像を絶えずリアルタイムで作成し、新しい第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)によって更新する請求項16乃至24の1つに記載の装置。
- 評価装置(13)は、磁気共鳴画像を、第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の全体に基づいてまたは第1の磁気共鳴データ(21)および第2の磁気共鳴データ(22)の一部分に基づいて作成する請求項16乃至25の1つに記載の装置。
- 評価装置(13)は一般線形モデル(16)を用いて前記統計的解析を実施し、評価装置(13)は、一般線形モデル(16)の係数(μ)がボリューム要素(15)における相対的または絶対的な潅流単位を生じるように一般線形モデル(16)の係数(μ)を基準化する請求項16乃至26の1つに記載の装置。
- 潅流の自動決定装置(6)が請求項1乃至15の1つに記載の方法を実施する請求項16乃至27の1つに記載の装置。
- 請求項16乃至28の1つに記載の潅流の自動決定装置(6)を有する磁気共鳴装置。
- 磁気共鳴装置(5)のプログラム可能な制御装置(6)のメモリに直接に読み込み可能であるコンピュータプログラム製品であって、プログラムが磁気共鳴装置(5)の制御装置(6)において実行されるときに、請求項1乃至15の1つに記載の方法の全てのステップを実行するためのプログラム手段を有するコンピュータプログラム製品。
- データ媒体(14)の使用時に磁気共鳴装置(5)の制御装置(6)において請求項1乃至15の1つに記載の方法を実行するように構成されている電子的に読取可能な制御情報が記憶されている電子的に読取可能なデータ媒体。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102007028901A DE102007028901B4 (de) | 2007-06-22 | 2007-06-22 | Verfahren und Vorrichtung zur automatischen Bestimmung von Perfusion mittels einer Magnetresonanzanlage |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009000525A true JP2009000525A (ja) | 2009-01-08 |
| JP2009000525A5 JP2009000525A5 (ja) | 2011-06-30 |
Family
ID=40075837
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008160828A Pending JP2009000525A (ja) | 2007-06-22 | 2008-06-19 | 磁気共鳴装置による潅流の自動決定方法および装置 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8233961B2 (ja) |
| JP (1) | JP2009000525A (ja) |
| CN (1) | CN101329388B (ja) |
| DE (1) | DE102007028901B4 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102009015516A1 (de) * | 2009-04-02 | 2010-10-07 | Mediri Gmbh | Verfahren und Vorrichtung zur Ermittlung von T2 und T2* mittels Magnet- Resonanz-Tomographie |
| US8532353B2 (en) * | 2011-11-23 | 2013-09-10 | Vital Images, Inc. | Synthetic visualization and quantification of perfusion-related tissue viability |
| JP5820549B2 (ja) * | 2012-04-17 | 2015-11-24 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | 灌流イメージング |
| JP6645831B2 (ja) * | 2012-10-31 | 2020-02-14 | コーニンクレッカ フィリップス エヌ ヴェKoninklijke Philips N.V. | かん流撮像 |
| DE102013224264B4 (de) * | 2013-11-27 | 2018-12-27 | Siemens Healthcare Gmbh | Verfahren zur Verarbeitung von Magnetresonanz-Diffusionsbilddaten |
| DE102014205789A1 (de) * | 2014-03-27 | 2015-10-01 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Magnetresonanzsystem |
| DE102015109678A1 (de) * | 2015-06-17 | 2016-12-22 | Julius-Maximilians-Universität Würzburg | Dynamische Fourier-Raum-Magnetresonanz |
| US10478557B2 (en) | 2015-08-21 | 2019-11-19 | Medtronic Minimed, Inc. | Personalized parameter modeling methods and related devices and systems |
| CN109669151A (zh) | 2019-02-12 | 2019-04-23 | 泰山医学院 | 磁共振动脉自旋标记灌注成像的质量控制体模及评价方法 |
| US11295448B1 (en) * | 2021-07-28 | 2022-04-05 | Ischemaview, Inc. | Concurrent display of hemodynamic parameters and damaged brain tissue |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6278893B1 (en) * | 1998-01-05 | 2001-08-21 | Nycomed Imaging As | Method of magnetic resonance imaging of a sample with ex vivo polarization of an MR imaging agent |
| US6980845B1 (en) * | 1998-04-13 | 2005-12-27 | The Trustees Of The University Of Pennsylvania | Multi-slice cerebral blood flow imaging with continuous arterial spin labeling MRI |
| US6564080B1 (en) * | 1999-03-31 | 2003-05-13 | Kabushiki Kaisha Toshiba | MR imaging on ASL technique |
| US6717405B2 (en) * | 2002-04-12 | 2004-04-06 | Beth Israel Deaconess Medical Center, Inc. | Arterial spin labeling using time varying gradients |
| JP3920140B2 (ja) * | 2002-05-13 | 2007-05-30 | 株式会社東芝 | Mri装置及びフロー定量化装置 |
| AU2003239436A1 (en) * | 2002-05-13 | 2003-11-11 | The Regents Of The University Of California | Velocity-selective arterial spin labeling without spatial selectivity |
| US7243064B2 (en) * | 2002-11-14 | 2007-07-10 | Verizon Business Global Llc | Signal processing of multi-channel data |
| JP4342809B2 (ja) * | 2003-02-14 | 2009-10-14 | 株式会社東芝 | Mri装置 |
| US7328054B2 (en) * | 2003-04-09 | 2008-02-05 | The Mcw Research Foundation, Inc. | Perfusion magnetic resonance imaging using encoded RF tagging pulses |
| WO2004114213A2 (en) * | 2003-06-13 | 2004-12-29 | The General Hospital Corporation | Noise and cancellation for time domain reconstruction |
| DE102004043809B4 (de) * | 2004-09-08 | 2008-01-24 | Charité-Universitätsmedizin Berlin | Verfahren zum Kalibrieren einer kontrastmittelgestützten Perfusionsbildgebung |
| WO2006127687A2 (en) * | 2005-05-20 | 2006-11-30 | Advanced Mri Technologies Llc | Efficient visualization of cortical vascular territories and functional mri by cycled arterial spin labeling mri |
| EP1978868A4 (en) * | 2005-09-19 | 2011-05-11 | Advanced Mri Technologies Llc | EXTREME ACCELERATION OF PERFUSION TIME SERIES ACQUISITION BY MAGNETIC RESONANCE IMAGING OF CYCLIC ARTERIAL SPIN MARKING |
| US7545142B2 (en) * | 2005-11-01 | 2009-06-09 | Beth Israel Deaconess Medical Center, Inc. | Arterial spin labeling with pulsed radio frequency sequences |
| US20090253982A1 (en) * | 2006-04-03 | 2009-10-08 | Jiongjiong Wang | Assessing subject's reactivity to psychological stress using fmri |
| US8195274B2 (en) * | 2007-04-27 | 2012-06-05 | The Regents Of The University Of California | Mapping of vascular perfusion territories |
| EP2189112A1 (en) * | 2008-11-24 | 2010-05-26 | Bracco Research S.A. | Real-time perfusion imaging and quantification |
| WO2010108161A2 (en) * | 2009-03-19 | 2010-09-23 | The Regents Of The University Of California | Multi-phase pseudo-continuing arterial spin labeling |
-
2007
- 2007-06-22 DE DE102007028901A patent/DE102007028901B4/de not_active Expired - Fee Related
-
2008
- 2008-06-19 JP JP2008160828A patent/JP2009000525A/ja active Pending
- 2008-06-20 US US12/143,265 patent/US8233961B2/en active Active
- 2008-06-23 CN CN200810110254.3A patent/CN101329388B/zh not_active Expired - Fee Related
Non-Patent Citations (1)
| Title |
|---|
| JPN6013006414; K. Restom, et al.: '"A Filtered Subtraction Approach for the Reduction of Physiological Noise in Perfusion Based fMRI"' Proc. Intl. Soc. Mag. Reson. Med. 14 , 200605, #3301 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN101329388B (zh) | 2013-09-11 |
| DE102007028901B4 (de) | 2010-07-22 |
| US20080319302A1 (en) | 2008-12-25 |
| CN101329388A (zh) | 2008-12-24 |
| US8233961B2 (en) | 2012-07-31 |
| DE102007028901A1 (de) | 2009-01-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2009000525A (ja) | 磁気共鳴装置による潅流の自動決定方法および装置 | |
| US7821266B2 (en) | Method and device for optimization of imaging parameters | |
| US8125484B2 (en) | Method, apparatus and user interface for determining an arterial input function used for calculating hemodynamic parameters | |
| KR101652387B1 (ko) | 영상 데이터를 생성하는 방법 | |
| JP6979151B2 (ja) | 磁気共鳴イメージング装置及び磁気共鳴画像処理方法 | |
| CN103168248B (zh) | 使用生理监测的mr数据采集 | |
| JP6261871B2 (ja) | 画像処理装置及び磁気共鳴イメージング装置 | |
| JP2009000525A5 (ja) | ||
| CN102215749B (zh) | 磁共振成像装置及磁共振成像方法 | |
| US7863896B2 (en) | Systems and methods for calibrating functional magnetic resonance imaging of living tissue | |
| CN106796275A (zh) | 用于单体素波谱分析的成像系统 | |
| CN113412430A (zh) | 借助于人工神经网络的功能性磁共振成像伪影移除 | |
| US20150208930A1 (en) | Method and medical imaging facility for determining perfusion | |
| CN103371826B (zh) | 用于生成磁共振图像的方法和设备 | |
| JP5352109B2 (ja) | 磁気共鳴イメージング装置 | |
| JP2004523330A (ja) | 周期的に変化する対象物を検査するmr方法 | |
| JP7337603B2 (ja) | 磁気共鳴イメージング装置 | |
| CN117063075A (zh) | Fmri检查的监测 | |
| US7961920B2 (en) | Method for the computer-assisted visualization of diagnostic image data | |
| CN107918943B (zh) | 用于产生与解剖图像数据相关的结果图的方法 | |
| US20050010097A1 (en) | System and method for measuring fluid volumes in brain images | |
| US10402974B2 (en) | Method and apparatus for evaluation of medical data having a temporal resolution | |
| JP6423066B2 (ja) | 画像処理装置及び磁気共鳴イメージング装置 | |
| JP2024521908A (ja) | 誘導を伴う医療用撮像方法 | |
| JP2023526012A (ja) | 医用イメージングにおける品質管理 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110516 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110516 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20110516 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130219 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130516 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130820 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20131115 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140311 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140530 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140604 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140930 |