JP2007284591A - Styrene- (meth) acrylic resin and molded product thereof - Google Patents
Styrene- (meth) acrylic resin and molded product thereof Download PDFInfo
- Publication number
- JP2007284591A JP2007284591A JP2006114396A JP2006114396A JP2007284591A JP 2007284591 A JP2007284591 A JP 2007284591A JP 2006114396 A JP2006114396 A JP 2006114396A JP 2006114396 A JP2006114396 A JP 2006114396A JP 2007284591 A JP2007284591 A JP 2007284591A
- Authority
- JP
- Japan
- Prior art keywords
- meth
- styrene
- branched
- macromonomer
- monomer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Macromonomer-Based Addition Polymer (AREA)
Abstract
Description
本発明は、分岐末端に重合性二重結合を有する多分岐マクロモノマーとスチレン系単量体及び(メタ)アクリル系単量体との共重合体及びそれを用いた成形品に関する。 The present invention relates to a copolymer of a multi-branched macromonomer having a polymerizable double bond at a branched end, a styrene monomer and a (meth) acrylic monomer, and a molded article using the same.
スチレン-(メタ)アクリル系共重合体を押出加工することにより、板、シート、フィルムなどの押出成形体にすることが広く行われている。しかしながら、現在、スチレン-(メタ)アクリル系共重合体は、十分に要求を満たしたバランスの優れた成形材料ではなく、さまざまな性能向上が求められている。例えば、プロジェクションテレビなどの画面用部材では、成形品の変形(反り・たわみ)の一因である吸湿性を抑制するために、スチレンの割合が高い共重合体を使用することで対応しているが、成形品の強度低下が生じてしまうため、十分満足がいくレベルに達していないのが現状である(例えば、特許文献1)。
最近、これらの分野において成形品が薄肉化、大型化の傾向があり、従来以上に耐衝撃性や曲げエネルギーといった実用強度と成形加工性とのバランス改良が要求されている。 ところで、特定構造を有する多分岐状マクロモノマーを添加することにより重合時のゲル化を抑制しつつ分岐構造を導入したスチレン系樹脂として、20万〜35万の重量平均分子量を有する線状ポリスチレンと、100万〜1000万の重量平均分子量を有する多分岐状ポリスチレンを混合し、全体として25万〜70万の重量平均分子量を有し、かつメルトマスフローレイト(MFR)およびメルトテンション(MT)が特定の値であるスチレン樹脂が提案されている(例えば、特許文献2参照)。しかしながら、当該技術は上記の曲げエネルギーの向上について検討されたものではない。
また、線状ポリスチレンと多分岐状ポリスチレンとを含有してなるスチレン系樹脂組成物であって、(1)そのGPC−MALLS法により求められる重量平均分子量が25万〜75万であり、(2)該重量平均分子量を横軸とし、又GPC−MALLSにより求められる該樹脂組成物の慣性半径を縦軸とした対数グラフに於ける傾きが0.35〜0.45であるスチレン系樹脂が提案されている(例えば、特許文献3参照)。しかしながら、当該技術においても上記の曲げエネルギーの向上については何ら検討されていない。
It has been widely practiced to form extruded bodies such as plates, sheets, and films by extruding styrene- (meth) acrylic copolymers. However, at present, the styrene- (meth) acrylic copolymer is not a well-balanced molding material that sufficiently satisfies the requirements, and various performance improvements are required. For example, in a screen member such as a projection television, in order to suppress hygroscopicity that is a cause of deformation (warping / deflection) of a molded product, a copolymer having a high ratio of styrene is used. However, since the strength of the molded product is reduced, the level is not sufficiently satisfactory (for example, Patent Document 1).
Recently, in these fields, molded products tend to be thinner and larger, and there is a demand for improving the balance between practical strength such as impact resistance and bending energy and molding processability. By the way, linear polystyrene having a weight average molecular weight of 200,000 to 350,000 as a styrene resin introduced with a branched structure while suppressing gelation during polymerization by adding a multi-branched macromonomer having a specific structure; , Mixed with multi-branched polystyrene having a weight average molecular weight of 1 million to 10 million, has a weight average molecular weight of 250,000 to 700,000 as a whole, and has specified melt mass flow rate (MFR) and melt tension (MT) A styrene resin having a value of is proposed (see, for example, Patent Document 2). However, this technique has not been studied for improving the bending energy.
Moreover, it is a styrene resin composition containing linear polystyrene and multi-branched polystyrene, (1) The weight average molecular weight calculated | required by the GPC-MALLS method is 250,000-750,000, (2 A styrenic resin having a slope of 0.35 to 0.45 in a logarithmic graph with the weight average molecular weight as the horizontal axis and the inertial radius of the resin composition determined by GPC-MALLS as the vertical axis is proposed. (For example, see Patent Document 3). However, even in this technique, no consideration is given to the improvement of the bending energy.
したがって、本発明が解決しようとする課題は、成形品の曲げエネルギーに優れるスチレン‐(メタ)アクリル系樹脂組成物およびその成形品を提供することにある。 Therefore, the problem to be solved by the present invention is to provide a styrene- (meth) acrylic resin composition excellent in bending energy of a molded product and the molded product thereof.
本発明者らは、上記の課題を解決すべく鋭意研究を重ねた結果、多分岐状マクロモノマーとスチレン系単量体及び(メタ)アクリル系単量体を重合することにより得られる多分岐状スチレン-(メタ)アクリル系共重合体が、従来のスチレン-(メタ)アクリル系共重合体と比較して飛躍的に高い曲げエネルギーが得られる事を見出し、本発明を完成するに至った。 As a result of intensive studies to solve the above problems, the present inventors have obtained a hyperbranched form obtained by polymerizing a hyperbranched macromonomer, a styrene monomer, and a (meth) acrylic monomer. It has been found that a styrene- (meth) acrylic copolymer can provide a significantly higher bending energy than a conventional styrene- (meth) acrylic copolymer, and the present invention has been completed.
即ち、本発明は、分岐末端に重合性二重結合を有する多分岐状マクロモノマーと、スチレン系単量体と、(メタ)アクリル系単量体とを共重合した樹脂であり、
前記スチレン系単量体と前記(メタ)アクリル系単量体の重合比率(質量基準)が、スチレン系単量体/(メタ)アクリル系単量体=85/15〜70/30であり、
GPC-MALLS(多角度光散乱検出器)により求められる重量平均分子量が60万〜100万であり、
GPC-MALLS(多角度光散乱検出器)による慣性半径(R.M.S Radius)とMolar massの両対数の傾きが、0.15〜0.40の範囲(Molar massが50万から500万の範囲)であるスチレン系樹脂を提供するものである。
また、本発明は、上記のスチレン系樹脂を用いたプラスチック板を提供するものである。また、本発明は、上記のスチレン系樹脂を用いたシートを提供するものである。また、本発明は、上記のスチレン系樹脂を用いたフィルムを提供するものである。
That is, the present invention is a resin obtained by copolymerizing a multi-branched macromonomer having a polymerizable double bond at a branched end, a styrene monomer, and a (meth) acrylic monomer,
The polymerization ratio (mass basis) of the styrene monomer and the (meth) acrylic monomer is styrene monomer / (meth) acrylic monomer = 85/15 to 70/30,
The weight average molecular weight required by GPC-MALLS (multi-angle light scattering detector) is 600,000 to 1,000,000,
Styrenic resin in which the slope of the logarithm of both the radius of inertia (RMS Radius) and Molar mass by GPC-MALLS (multi-angle light scattering detector) is in the range of 0.15 to 0.40 (Molar mass is in the range of 500,000 to 5,000,000). Is to provide.
The present invention also provides a plastic plate using the above styrene resin. Moreover, this invention provides the sheet | seat using said styrenic resin. Moreover, this invention provides the film using said styrene resin.
本発明は、成形加工品として高い重量平均分子量を持ちながら、従来のスチレン-(メタ)アクリル系樹脂よりも高い曲げエネルギーを有し、割れにくいスチレン-(メタ)アクリル系樹脂およびその成形品を提供することができる。 The present invention provides a styrene- (meth) acrylic resin and a molded product thereof that have a high weight-average molecular weight as a molded product, have higher bending energy than conventional styrene- (meth) acrylic resins, and are difficult to crack. Can be provided.
以下に本発明について詳細に説明する。
本発明のスチレン-(メタ)アクリル系樹脂は、分子末端に複数の重合性二重結合を有する多分岐状マクロモノマーとスチレン系単量体、メタクリル酸エステル、アクリル酸エステルとを重合させることにより得られる多分岐状共重合体である。
The present invention is described in detail below.
The styrene- (meth) acrylic resin of the present invention is obtained by polymerizing a multi-branched macromonomer having a plurality of polymerizable double bonds at the molecular terminals and a styrene monomer, a methacrylic ester, and an acrylic ester. The resulting multi-branched copolymer.
本発明において使用することができるスチレン系単量体は、スチレンの他にα-メチルスチレン、α-メチル-p-メチルスチレンなどのα-アルキル置換スチレン、o-メチルスチレン、p-メチルスチレン、m-メチルスチレン、2,4-ジメチルスチレン、2,5-ジメチルスチレン、m-ビニルフェノール、p-メトキシスチレンなどの核置換スチレンなどが挙げられ、これらは1種類のみであっても2種類以上用いても構わない。これらの中でも、スチレンを使用することが好ましい。 In addition to styrene, styrene monomers that can be used in the present invention include α-methylstyrene, α-alkyl-substituted styrene such as α-methyl-p-methylstyrene, o-methylstyrene, p-methylstyrene, Examples include m-methylstyrene, 2,4-dimethylstyrene, 2,5-dimethylstyrene, m-vinylphenol, p-methoxystyrene, and other nuclear-substituted styrene. You may use. Among these, it is preferable to use styrene.
一方、本発明に使用することができるアクリル酸エステル系(メタクリル酸エステル系)構成単位を形成する単量体とは、アルキル基の炭素数が1〜20のものであり、これらは1種類のみであっても2種類以上用いても構わない。これらの中でも、メタクリル酸メチル、メタクリル酸エチル、メタクリル酸ブチル、アクリル酸メチル、アクリル酸エチル、アクリル酸ブチルを使用することが好ましい。 On the other hand, the monomer forming the acrylic ester (methacrylic ester) structural unit that can be used in the present invention is an alkyl group having 1 to 20 carbon atoms, and these are only one kind. However, two or more types may be used. Among these, it is preferable to use methyl methacrylate, ethyl methacrylate, butyl methacrylate, methyl acrylate, ethyl acrylate, and butyl acrylate.
本発明のスチレン-(メタ)アクリル系樹脂に含まれる多分岐状共重合体の分岐構造には、特に制限はないが、電子吸引基と、該電子吸引基に結合する結合手以外の3つの結合手すべてが炭素原子に結合している飽和炭素原子とからなる分岐構造を含有するもの、及びエーテル結合、エステル結合及びアミド結合から選ばれる繰り返し構造単位からなる分岐構造を含有するものが好ましい。 There are no particular restrictions on the branched structure of the multi-branched copolymer contained in the styrene- (meth) acrylic resin of the present invention, but there are three types other than an electron-withdrawing group and a bond bonded to the electron-withdrawing group. Those containing a branched structure consisting of a saturated carbon atom in which all the bonds are bonded to a carbon atom and those containing a branched structure consisting of a repeating structural unit selected from an ether bond, an ester bond and an amide bond are preferred.
多分岐状共重合体の分岐構造は基本的には、スチレン、メタクリル酸エステル、アクリル酸エステルと共重合させる多分岐状マクロモノマーに由来するものである。本発明のスチレン-(メタ)アクリル系樹脂に含まれる多分岐状共重合体の分岐構造の電子吸引基含有量は多分岐状ポリスチレン1g当たり2.5×10−4ミリモル〜5.0×10−1ミリモル、好ましくは5.0×10−4ミリモル〜5.0×10−2ミリモルであることが好ましい。 The branched structure of the multi-branched copolymer is basically derived from a multi-branched macromonomer that is copolymerized with styrene, methacrylic acid ester or acrylic acid ester. The electron-withdrawing group content in the branched structure of the multi-branched copolymer contained in the styrene- (meth) acrylic resin of the present invention is 2.5 × 10 −4 mmol to 5.0 × 10 10 g per multi-branched polystyrene. −1 mmol, preferably 5.0 × 10 −4 mmol to 5.0 × 10 −2 mmol.
本発明において使用する多分岐状マクロモノマーには、多分岐鎖を有するモノマーであること以外には特に限定はないが、その好ましいものの一つとして1分子中に電子吸引基と、該電子吸引基に結合する結合手以外の3つの結合手すべてが炭素原子に結合している飽和炭素原子とから成る分岐構造と、芳香環に直接結合した重合性二重結合とを含有する多分岐状マクロモノマーがある。この多分岐状マクロモノマーは、AB2型モノマーから誘導されるハイパーブランチマクロモノマーであり、図5に模式的に示すような分岐構造を有する。 The multi-branched macromonomer used in the present invention is not particularly limited except that it is a monomer having a multi-branched chain. As one of the preferred ones, an electron-withdrawing group in one molecule and the electron-withdrawing group A multi-branched macromonomer containing a branched structure consisting of a saturated carbon atom in which all three bonds other than a bond bonded to a carbon atom are bonded to a carbon atom, and a polymerizable double bond directly bonded to an aromatic ring There is. This hyperbranched macromonomer is a hyperbranched macromonomer derived from an AB type 2 monomer and has a branched structure as schematically shown in FIG.
このような分岐構造は、電子吸引基が結合した活性メチレン基の求核置換反応によって容易に得られる。電子吸引基としては、例えば、−CN、−NO2、−CONH2、−CON(R)2、−SO2CH3、−P(=O)(OR)2、などがあげられ、これらの電子吸引基が結合したメチレン基が芳香環またはカルボニル基に直接結合している場合は、メチレン基の活性はさらに高いものとなる。 Such a branched structure can be easily obtained by a nucleophilic substitution reaction of an active methylene group to which an electron withdrawing group is bonded. Examples of the electron withdrawing group include —CN, —NO 2 , —CONH 2 , —CON (R) 2 , —SO 2 CH 3 , —P (═O) (OR) 2 , and the like. When the methylene group to which the electron withdrawing group is bonded is directly bonded to the aromatic ring or the carbonyl group, the activity of the methylene group is further increased.
本発明に用いる多分岐状マクロモノマーの1つとしては、例えば、下記の一般式(1)で表される繰り返し単位を含有する分岐鎖を有する多分岐状マクロモノマーが挙げられる。
一般式(1)
As one of the multibranched macromonomers used in the present invention, for example, a multibranched macromonomer having a branched chain containing a repeating unit represented by the following general formula (1) can be mentioned.
General formula (1)
[式中、Y1は−CN、−NO2、−CONH2、−CON(R)2、−SO2CH3、−P(=O)(OR)2(ここでRはアルキル基またはアリール基を表す)から成る群から選ばれる電子吸引基であり、Y2はアリーレン基、−O−CO−または−NH−CO−であり、Zは−(CH2)nO−、−(CH2CH2O)n−、−(CH2CH2CH2O)n−から成る群から選ばれる基であり、かつY2が−O−CO−または−NH−CO−である場合はZは−(CH2)n−、−(CH2)nAr−、−(CH2)nO−Ar−、−(CH2CH2O)n−Ar−、または−(CH2CH2CH2O)n−Ar−(ここでArはアリール基である)を表す]
ここで、Y2は例えば、
[Wherein Y 1 represents —CN, —NO 2 , —CONH 2 , —CON (R) 2 , —SO 2 CH 3 , —P (═O) (OR) 2 (where R represents an alkyl group or aryl Y 2 is an arylene group, —O—CO— or —NH—CO—, and Z is — (CH 2 ) n O—, — (CH 2 CH 2 O) n —, a group selected from the group consisting of — (CH 2 CH 2 CH 2 O) n —, and when Y 2 is —O—CO— or —NH—CO—, Z is - (CH 2) n -, - (CH 2) n Ar -, - (CH 2) n O-Ar -, - (CH 2 CH 2 O) n -Ar-, or - (CH 2 CH 2 CH 2 O) n -Ar- (wherein Ar represents an aryl group)]
Here, Y 2 is, for example,
上記分岐構造を有する多分岐状マクロモノマーは、塩基性化合物の存在下で、(1)1分子中に活性メチレン基と、活性メチレン基の求核置換反応における脱離基とを有するAB2型モノマーを求核置換反応させて得られる多分岐状の自己縮合型重縮合体を前駆体として、
(2)該重縮合体中に残存する未反応の活性メチレン基またはメチン基を、1分子中に芳香環に直接結合した重合性二重結合と活性メチレン基の求核置換反応における脱離基とを有する化合物と求核置換反応させることによって得られる。
The hyperbranched macromonomer having the above branched structure is, in the presence of a basic compound, (1) AB 2 type having an active methylene group and a leaving group in a nucleophilic substitution reaction of an active methylene group in one molecule. A precursor of a multi-branched self-condensation polycondensate obtained by subjecting a monomer to a nucleophilic substitution reaction,
(2) A leaving group in a nucleophilic substitution reaction of a polymerizable double bond and an active methylene group in which an unreacted active methylene group or methine group remaining in the polycondensate is directly bonded to an aromatic ring in one molecule. And a nucleophilic substitution reaction.
ここで、活性メチレン基の求核置換反応における脱離基とは、いずれも飽和炭素原子に結合したハロゲン、−OS(=O)2R(Rはアルキル基またはアリール基を表す)などであり、具体的には、臭素、塩素、メチルスルホニルオキシ基、トシルオキシ基などが挙げられる。
塩基性化合物としては、水酸化ナトリウム、水酸化カリウムなどの強アルカリが好適であり、反応に際しては水溶液として使用する。
Here, the leaving group in the nucleophilic substitution reaction of the active methylene group is any halogen bonded to a saturated carbon atom, —OS (═O) 2 R (R represents an alkyl group or an aryl group), and the like. Specific examples include bromine, chlorine, methylsulfonyloxy group, tosyloxy group and the like.
The basic compound is preferably a strong alkali such as sodium hydroxide or potassium hydroxide, and used as an aqueous solution in the reaction.
1分子中に活性メチレン基と活性メチレン基の求核置換反応における脱離基とを有するAB2型モノマーとしては、たとえばブロモエトキシ−フェニルアセトニトリル、クロロメチルベンジルオキシ−フェニルアセトニトリルなどのハロゲン化アルコキシ−フェニルアセトニトリル類、トシルオキシ−(エチレンオキシ)−フェニルアセトニトリル、トシルオキシ−ジ(エチレンオキシ)−フェニルアセトニトリルなどのトシルオキシ基を有するフェニルアセトニトリル類が挙げられる。 Examples of the AB type 2 monomer having an active methylene group and a leaving group in the nucleophilic substitution reaction of the active methylene group in one molecule include alkoxy halides such as bromoethoxy-phenylacetonitrile and chloromethylbenzyloxy-phenylacetonitrile. Examples include phenylacetonitriles having a tosyloxy group, such as phenylacetonitriles, tosyloxy- (ethyleneoxy) -phenylacetonitrile, tosyloxy-di (ethyleneoxy) -phenylacetonitrile.
1分子中に芳香環に直接結合した重合性二重結合と、活性メチレン基の求核置換反応における脱離基とを有する代表的な化合物としては、たとえば、クロロメチルスチレン、ブロモメチルスチレンなどが挙げられる。 Typical compounds having a polymerizable double bond directly bonded to an aromatic ring in one molecule and a leaving group in a nucleophilic substitution reaction of an active methylene group include, for example, chloromethylstyrene and bromomethylstyrene. Can be mentioned.
上記(1)は前駆体としての重縮合体を合成する反応であり、(2)は前駆体に芳香環に直接結合した重合性二重結合を導入して多分岐状マクロモノマーを合成する反応である。(1)の反応と(2)の反応は、それぞれの反応を逐次的に行うことができるが、同一の反応系で同時に行うこともできる。多分岐状マクロモノマーの分子量は、単量体と塩基性化合物との配合比を変えることによって制御することができる。 The above (1) is a reaction for synthesizing a polycondensate as a precursor, and (2) is a reaction for synthesizing a multi-branched macromonomer by introducing a polymerizable double bond directly bonded to an aromatic ring to the precursor. It is. The reactions (1) and (2) can be performed sequentially, but can also be performed simultaneously in the same reaction system. The molecular weight of the hyperbranched macromonomer can be controlled by changing the compounding ratio of the monomer and the basic compound.
本発明において使用する多分岐状マクロモノマーの好ましいものの他のものとして、好ましくはエステル結合、エーテル結合及びアミド結合から選ばれる繰り返し構造単位からなる分岐構造と、分岐末端のエチレン性重合性二重結合とを含有する多分岐状マクロモノマーを挙げることができる。 As other preferable ones of the multi-branched macromonomer used in the present invention, a branched structure composed of repeating structural units preferably selected from an ester bond, an ether bond and an amide bond, and an ethylenically polymerizable double bond at the branch end And a multi-branched macromonomer containing
エステル結合を繰り返し構造単位として有する多分岐状マクロモノマーは、分子鎖を形成するエステル結合のカルボニル基に隣接する炭素原子が飽和炭素原子であり、かつ該炭素原子上の水素原子がすべて置換されている分子鎖からなる多分岐ポリエステルポリオールに、ビニル基またはイソプロペニル基などのエチレン性重合性二重結合を導入したものである。多分岐ポリエステルポリオールにエチレン性重合性二重結合を導入する場合、エステル化反応や付加反応によって行なうことができる。
尚、上記多分岐ポリエステルポリオールとして、Perstorp社製「Boltorn H20、H30、H40」が市販されている。
In the multi-branched macromonomer having an ester bond as a repeating structural unit, the carbon atom adjacent to the carbonyl group of the ester bond forming the molecular chain is a saturated carbon atom, and all the hydrogen atoms on the carbon atom are substituted. An ethylenically polymerizable double bond such as a vinyl group or an isopropenyl group is introduced into a multi-branched polyester polyol having a molecular chain. When an ethylenically polymerizable double bond is introduced into a multi-branched polyester polyol, it can be carried out by an esterification reaction or an addition reaction.
As the above-mentioned multi-branched polyester polyol, “Boltorn H20, H30, H40” manufactured by Perstorp is commercially available.
上記多分岐ポリエステルポリオールは、そのヒドロキシル基の一部にあらかじめエーテル結合やその他の結合によって置換基が導入されていてもよいし、また、そのヒドロキシル基の一部が酸化反応やその他の反応で変性されていてもよい。
また、多分岐ポリエステルポリオールは、そのヒドロキシル基の一部が、あらかじめエステル化されていてもよい。
In the above-mentioned multi-branched polyester polyol, a substituent may be introduced into a part of the hydroxyl group by an ether bond or other bond in advance, and a part of the hydroxyl group is modified by an oxidation reaction or other reaction. May be.
Further, in the multi-branched polyester polyol, part of the hydroxyl group may be esterified in advance.
かかる多分岐状マクロモノマーの代表的なものとしては、例えば水酸基を1個以上有する化合物に、カルボキシル基に隣接する炭素原子が飽和炭素原子であり、かつ該炭素原子上の水素原子がすべて置換され、且つ水酸基を2個以上有するモノカルボン酸を反応することにより多分岐状ポリマーとし、次いで該ポリマーの末端基である水酸基にアクリル酸やメタクリル酸などの不飽和酸、イソシアネート基含有アクリル系化合物などを反応させて得られるものが挙げられる。尚、エステル結合を繰り返し構造単位として有する多分岐状ポリマーについては、タマリア(Tamalia)氏等による「Angew.Chem.Int.Ed.Engl.29」p138〜177(1990)にも記載されている。 A typical example of such a multi-branched macromonomer is a compound having one or more hydroxyl groups, in which the carbon atom adjacent to the carboxyl group is a saturated carbon atom, and all the hydrogen atoms on the carbon atom are substituted. In addition, a monobranched polymer having two or more hydroxyl groups is reacted to form a multi-branched polymer, and then the hydroxyl group which is a terminal group of the polymer is unsaturated acid such as acrylic acid or methacrylic acid, isocyanate group-containing acrylic compound, etc. Can be obtained by reacting. The multi-branched polymer having an ester bond as a repeating structural unit is also described in “Angew. Chem. Int. Ed. Engl. 29” p138-177 (1990) by Tamalia et al.
上記水酸基を1個以上有する化合物としては、a)脂肪族ジオール、脂環式ジオール、又は芳香族ジオール、b)トリオール、c)テトラオール、d)ソルビトール及びマンニトール等の糖アルコール、e)アンヒドロエンネア−ヘプチトール又はジペンタエリトリトール、f)α−メチルグリコシド等のα−アルキルグルコシド、g)エタノール、ヘキサノールなどの一官能性アルコール、h)分子量が多くとも8000であり、かつ、アルキレンオキシド或いはその誘導体と、上記a)〜g)のいずれかから選択されたアルコールの1種以上のヒドロキシル基とを反応させることにより生成された水酸基含有ポリマーなどを挙げることができる。 Examples of the compound having one or more hydroxyl groups include: a) aliphatic diol, alicyclic diol, or aromatic diol, b) triol, c) tetraol, d) sugar alcohols such as sorbitol and mannitol, e) anhydro Ennea-heptitol or dipentaerythritol, f) α-alkyl glucosides such as α-methyl glycoside, g) monofunctional alcohols such as ethanol and hexanol, h) a molecular weight of at most 8000, and alkylene oxides or derivatives thereof And a hydroxyl group-containing polymer produced by reacting with one or more hydroxyl groups of an alcohol selected from any of the above-mentioned a) to g).
脂肪族ジオール、脂環式ジオール及び芳香族ジオールとしては、1,2−エタンジオール、1,3−プロパンジオール、1,4−ブタンジオール、1,5−ペンタンジオール、1,6−ヘキサンジオール、ポリテトラヒドロフラン、ジメチロールプロパン、ネオペンチルプロパン、2−プロピル−2−エチル−1,3−プロパンジオール、1,2−プロパンジオール、1,3−ブタンジオール、ジエチレングリコール、トリエチレングリコール、ポリエチレングリコール、ジプロピレングリコール、トリプロピレングリコール、ポリプロピレングリコール;シクロヘキサンジメタノール、1,3−ジオキサン−5,5−ジメタノール;1,4−キシリレンジメタノール、1−フェニル−1,2−エタンジオールなどが挙げられる。
トリオールとしては、トリメチロールプロパン、トリメチロールエタン、トリメチロールブタン、グリセロール、1,2,5−ヘキサントリオールなどが挙げられる。
テトラオールとしては、ペンタエリスリトール、ジトリメチロールプロパン、ジグリセロール、ジトリメチロールエタンなどを挙げることができる。
芳香環に結合した水酸基を2個以上有する芳香族化合物としては、1,3,5−トリヒドロキシベンゼン、1,4−キシリレンジメタノール、1−フェニル−1,2−エタンジオールなどを挙げることができる。
カルボキシル基に隣接する炭素原子が飽和炭素原子であり、かつ該炭素原子上の水素原子がすべて置換され、且つ水酸基を2個以上有するモノカルボン酸としては、ジメチロールプロピオン酸、α,α−ビス(ヒドロキシメチル)酪酸、α,α,α−トリス(ヒドロキシメチル)酢酸、α,α−ビス(ヒドロキシメチル)吉草酸、α,α−ビス(ヒドロキシメチル)プロピオン酸などがある。かかるモノカルボン酸を使用することにより、エステル分解反応が抑制され、多分岐ポリエステルポリオールを形成することができる。
また、かかる多分岐状ポリマーを製造する際に、触媒を使用するのが好ましく、かかる触媒としては、例えばジアルキルスズオキシド、ハロゲン化ジアルキルスズ、ジアルキルスズビスカルボキシレート、あるいはスタノキサンなどの有機錫化合物、テトラブチルチタネートなどのチタネート、ルイス酸、パラトルエンスルホン酸などの有機スルホン酸などが挙げられる。
Examples of the aliphatic diol, alicyclic diol and aromatic diol include 1,2-ethanediol, 1,3-propanediol, 1,4-butanediol, 1,5-pentanediol, 1,6-hexanediol, Polytetrahydrofuran, dimethylolpropane, neopentylpropane, 2-propyl-2-ethyl-1,3-propanediol, 1,2-propanediol, 1,3-butanediol, diethylene glycol, triethylene glycol, polyethylene glycol, di- Examples include propylene glycol, tripropylene glycol, polypropylene glycol; cyclohexanedimethanol, 1,3-dioxane-5,5-dimethanol; 1,4-xylylenediethanol, 1-phenyl-1,2-ethanediol and the like.
Examples of the triol include trimethylolpropane, trimethylolethane, trimethylolbutane, glycerol, 1,2,5-hexanetriol and the like.
Examples of tetraols include pentaerythritol, ditrimethylolpropane, diglycerol, and ditrimethylolethane.
Examples of the aromatic compound having two or more hydroxyl groups bonded to the aromatic ring include 1,3,5-trihydroxybenzene, 1,4-xylylenediethanol, 1-phenyl-1,2-ethanediol and the like. it can.
Examples of the monocarboxylic acid in which the carbon atom adjacent to the carboxyl group is a saturated carbon atom and all the hydrogen atoms on the carbon atom are substituted and which has two or more hydroxyl groups include dimethylolpropionic acid, α, α-bis Examples include (hydroxymethyl) butyric acid, α, α, α-tris (hydroxymethyl) acetic acid, α, α-bis (hydroxymethyl) valeric acid, α, α-bis (hydroxymethyl) propionic acid. By using such a monocarboxylic acid, the ester decomposition reaction is suppressed and a multi-branched polyester polyol can be formed.
Further, when producing such a multi-branched polymer, it is preferable to use a catalyst, such as a dialkyl tin oxide, a dialkyl tin halide, a dialkyl tin biscarboxylate, or an organic tin compound such as stannoxane, Examples thereof include titanates such as tetrabutyl titanate, organic sulfonic acids such as Lewis acid, and paratoluenesulfonic acid.
エーテル結合を繰り返し構造単位として有する多分岐状マクロモノマーは、例えば水酸基を1個以上有する化合物に水酸基を1個以上有する環状エーテル化合物を反応することにより多分岐状ポリマーとし、次いで該ポリマーの末端基である水酸基にアクリル酸やメタクリル酸などの不飽和酸、イソシアネート基含有アクリル系化合物、4−クロロメチルスチレンなどのハロゲン化メチルスチレンを反応させて得られるものが挙げられる。また、多分岐状ポリマーの製法としては、Williamsonのエーテル合成法に基づいて、水酸基を1個以上有する化合物と、2個以上の水酸基とハロゲン原子、−OSO2−OCH3又は−OSO2CH3を含有する化合物とを反応する方法も有用である。 The multi-branched macromonomer having an ether bond as a repeating structural unit is, for example, made into a multi-branched polymer by reacting a compound having one or more hydroxyl groups with a cyclic ether compound having one or more hydroxyl groups, and then terminal groups of the polymer And those obtained by reacting an unsaturated acid such as acrylic acid or methacrylic acid, an isocyanate group-containing acrylic compound, or halogenated methylstyrene such as 4-chloromethylstyrene with the hydroxyl group. As a method for producing a multi-branched polymer, a compound having one or more hydroxyl groups, two or more hydroxyl groups and a halogen atom, —OSO 2 —OCH 3 or —OSO 2 CH 3 , based on Williamson's ether synthesis method. A method of reacting with a compound containing is also useful.
水酸基を1個以上有する化合物としては、前記するものが使用することができる。
水酸基を1個以上有する環状エーテル化合物としては、3−エチル−3−(ヒドロキシメチル)オキセタン、2,3−エポキシ−1−プロパノール、2,3−エポキシ−1−ブタノール、3,4−エポキシ−1−ブタノールなどが挙げられる。
Williamsonのエーテル合成法に於いて使用される水酸基を1個以上有する化合物としては、前記したものでよいが、芳香環に結合した水酸基を2個以上有する芳香族化合物が好ましい。かかる化合物の代表的なものとしては、1,3,5−トリヒドロキシベンゼン、1,4−キシリレンジメタノール、1−フェニル−1,2−エタンジオールなどが挙げられる。
また、2個以上の水酸基とハロゲン原子、−OSO2−OCH3又は−OSO2CH3を含有する化合物としては、5−(ブロモメチル)−1,3−ジヒドロキシベンゼン、2−エチル−2−(ブロモメチル)−1,3−プロパンジオール、2−メチル−2−(ブロモメチル)−1,3−プロパンジオール、2−(ブロモメチル)−2−(ヒドロキシメチル)−1,3−プロパンジオールなどが挙げられる。
なお、上記多分岐状ポリマーを製造する際には、通常触媒を使用するのが好ましく、かかる触媒としては例えばBF3ジエチルエーテル、FSO3H、ClSO3H、HClO4などを挙げることができる。
As the compound having one or more hydroxyl groups, those described above can be used.
As cyclic ether compounds having one or more hydroxyl groups, 3-ethyl-3- (hydroxymethyl) oxetane, 2,3-epoxy-1-propanol, 2,3-epoxy-1-butanol, 3,4-epoxy- Examples include 1-butanol.
As the compound having one or more hydroxyl groups used in Williamson's ether synthesis method, those described above may be used, but aromatic compounds having two or more hydroxyl groups bonded to an aromatic ring are preferred. Typical examples of such compounds include 1,3,5-trihydroxybenzene, 1,4-xylylenediethanol, 1-phenyl-1,2-ethanediol and the like.
Examples of the compound containing two or more hydroxyl groups and a halogen atom, -OSO 2 -OCH 3 or -OSO 2 CH 3 include 5- (bromomethyl) -1,3-dihydroxybenzene, 2-ethyl-2- ( Bromomethyl) -1,3-propanediol, 2-methyl-2- (bromomethyl) -1,3-propanediol, 2- (bromomethyl) -2- (hydroxymethyl) -1,3-propanediol, and the like. .
In producing the multi-branched polymer, it is preferable to use a conventional catalyst, as such catalyst can be, for example, BF 3 diethyl ether, FSO 3 H, ClSO 3 H , and HClO 4.
また、アミド結合を繰り返し構造単位として有する多分岐状マクロモノマーとしては、例えば分子中にアミド結合を窒素原子を介して繰り返し構造となったものがあり、Dentoritech社製のゼネレーション2.0(PAMAMデントリマー)が代表的なものである。 In addition, as the multi-branched macromonomer having an amide bond as a repeating structural unit, for example, there are those in which a amide bond has a repeating structure through a nitrogen atom in the molecule, and a generation 2.0 (PAMAM) manufactured by Dentortech. Dentrimer) is a typical one.
多分岐状マクロモノマーに導入される、末端反応性重合性二重結合の数が多いほど、スチレン、メタクリル酸エステル、アクリル酸エステルとの共重合体である多分岐状スチレン-(メタ)アクリル系共重合体の分岐度が高くなる。本発明に用いる多分岐状マクロモノマーの分岐度(DB)は、下記の式3により定義され、分岐度(DB)の範囲は0.3〜1.0が好ましい。 As the number of terminal reactive polymerizable double bonds introduced into the multi-branched macromonomer increases, the multi-branched styrene- (meth) acrylic system, which is a copolymer with styrene, methacrylic ester, and acrylate ester The degree of branching of the copolymer is increased. The degree of branching (DB) of the multibranched macromonomer used in the present invention is defined by the following formula 3, and the range of the degree of branching (DB) is preferably 0.3 to 1.0.
DB=(D+T)/(D+T+L) (式3)
(式中、Dはデンドリックユニットの数、Lは線状ユニットの数、Tは末端ユニットの数を表す)
DB = (D + T) / (D + T + L) (Formula 3)
(In the formula, D represents the number of dendritic units, L represents the number of linear units, and T represents the number of terminal units)
本発明において使用する多分岐状マクロモノマーの重量平均分子量は、多分岐状スチレン-(メタ)アクリル系共重合体の重量平均分子量を1000万以下に制御するために、1000〜15000であることが好ましく、2000〜5000であることがより好ましい。 The weight average molecular weight of the multibranched macromonomer used in the present invention is 1000 to 15000 in order to control the weight average molecular weight of the multibranched styrene- (meth) acrylic copolymer to 10 million or less. Preferably, it is 2000-5000.
多分岐状マクロモノマーに導入される重合性二重結合の含有量は、多分岐状マクロモノマー1g当たり0.1ミリモル〜5.5ミリモルであることが好ましく、0.5ミリモル〜3.5ミリモルがなお好ましい。0.1ミリモルより少ない場合は、高分子量の多分岐状スチレン-(メタ)アクリル系共重合体が得られにくく、5.5ミリモルを超える場合は、多分岐状スチレン-(メタ)アクリル系共重合体の分子量が過度に増大する。 The content of the polymerizable double bond introduced into the multibranched macromonomer is preferably 0.1 mmol to 5.5 mmol, and 0.5 mmol to 3.5 mmol per 1 g of the multibranched macromonomer. Is still preferred. When the amount is less than 0.1 mmol, it is difficult to obtain a high-molecular-weight multibranched styrene- (meth) acrylic copolymer. The molecular weight of the polymer increases excessively.
前記多分岐状マクロモノマーとスチレン系単量体、(メタ)アクリル系単量体とを重合させることにより、多分岐状マクロモノマーとスチレン、(メタ)アクリル系単量体との共重合体である多分岐状スチレン-(メタ)アクリル系共重合体が得られる。 By polymerizing the hyperbranched macromonomer and styrene monomer, a (meth) acrylic monomer, a copolymer of the hyperbranched macromonomer and styrene, (meth) acrylic monomer A certain multibranched styrene- (meth) acrylic copolymer is obtained.
スチレン系単量体/(メタ)アクリル系単量体の質量比は85/15〜70/30である。また、85/15〜78/22であることがより好ましい。 The mass ratio of styrene monomer / (meth) acrylic monomer is 85/15 to 70/30. Moreover, it is more preferable that it is 85 / 15-78 / 22.
また、さらに好ましいのは、スチレン系単量体、メタクリル系単量体、アクリル系単量体の比率としては、スチレン系単量体78〜85質量%、メタクリル系単量体3〜21質量%、アクリル系単量体1〜19質量%である。 More preferably, the ratio of the styrene monomer, the methacrylic monomer, and the acrylic monomer is 78 to 85% by mass of the styrene monomer and 3 to 21% by mass of the methacrylic monomer. The acrylic monomer content is 1 to 19% by mass.
モノマー(スチレン系単量体及び(メタ)アクリル単量体)に対する多分岐状マクロモノマーの配合率は、0.01〜1質量%が好ましく、0.01〜0.2質量%がより好ましい。多分岐状マクロモノマーの配合率が0.01質量%より少ない場合は、本発明の十分な効果が得られにくい。 The blending ratio of the hyperbranched macromonomer with respect to the monomers (styrene monomer and (meth) acrylic monomer) is preferably 0.01 to 1% by mass, and more preferably 0.01 to 0.2% by mass. When the blending ratio of the hyperbranched macromonomer is less than 0.01% by mass, it is difficult to obtain the sufficient effect of the present invention.
本発明に用いるスチレン-(メタ)アクリル系樹脂組成物をMALLS(多角度光散乱検出器)-GPCで分子量測定を行うと、直接的に分子量を測定することが可能である。以下に記す重量平均分子量はMALLS-GPCで測定した値である。また、MALLS-GPCでは、重量平均分子量と慣性半径の関係も求めることも可能である。かかる慣性半径の算出については、例えば高分子、微粒子のキャラクタリゼーション(昭光通商(株))などに記載されている。 When the molecular weight of the styrene- (meth) acrylic resin composition used in the present invention is measured by MALLS (multi-angle light scattering detector) -GPC, the molecular weight can be directly measured. The weight average molecular weight described below is a value measured by MALLS-GPC. In MALLS-GPC, the relationship between the weight average molecular weight and the radius of inertia can also be obtained. Such calculation of the radius of inertia is described in, for example, characterization of polymers and fine particles (Shoko Tsusho Co., Ltd.).
本発明のスチレン-(メタ)アクリル系樹脂のMALLS-GPCから求められる重量平均分子量は60万〜100万であり、好ましくは70万〜100万である。更に好ましくは、重量平均分子量が75万を超えて、100万以下である。かかる重量平均分子量が45万よりも小さいと成形品の曲げエネルギーが小さくなり多分岐状マクロモノマーの効果が得られない。また100万を越えると流動性が低下して成形ができなくなったり、生産性が落ちてしまうので好ましくない。 The weight average molecular weight calculated | required from MALLS-GPC of the styrene- (meth) acrylic-type resin of this invention is 600,000-1 million, Preferably it is 700,000-1 million. More preferably, the weight average molecular weight is more than 750,000 and 1 million or less. If the weight average molecular weight is less than 450,000, the bending energy of the molded product becomes small, and the effect of the multibranched macromonomer cannot be obtained. On the other hand, if it exceeds 1,000,000, the fluidity is lowered, making molding impossible, and the productivity is lowered.
また、該重量平均分子量を横軸とし、MALLS-GPCから求められる該樹脂組成物の慣性半径を縦軸とした両対数グラフにおける傾きが0.15〜0.40である。かかる傾きが0.40よりも大きくなると、多分岐状マクロモノマーを含まないスチレン-(メタ)アクリル系共重合体により近い物性となり、逆に0.15よりも小さくなると、流動性が低下するため、押出成形などする上では好ましくない。 The slope in a log-log graph with the weight average molecular weight as the horizontal axis and the radius of inertia of the resin composition determined from MALLS-GPC as the vertical axis is 0.15 to 0.40. When the slope is larger than 0.40, the physical properties are closer to those of a styrene- (meth) acrylic copolymer not containing a hyperbranched macromonomer. Conversely, when the slope is smaller than 0.15, the fluidity is lowered. It is not preferable for extrusion molding.
重合反応には公知慣用のスチレン-(メタ)アクリル系共重合体の重合方法を使用することができる。重合方式には特に限定はないが、塊状重合、懸濁重合、あるいは溶液重合が好ましい。重合開始剤を使用せずに熱重合させることもできるが、慣用のラジカル重合開始剤を使用するのが好ましい。また、重合に必要な懸濁剤や乳化剤などのような重合助剤は、通常のスチレン-(メタ)アクリル系共重合体の製造に使用される慣用のものを使用できる。 For the polymerization reaction, a known and commonly used polymerization method of styrene- (meth) acrylic copolymers can be used. The polymerization method is not particularly limited, but bulk polymerization, suspension polymerization, or solution polymerization is preferable. Although thermal polymerization can be carried out without using a polymerization initiator, it is preferable to use a conventional radical polymerization initiator. In addition, as a polymerization aid such as a suspending agent or an emulsifier necessary for polymerization, a conventional one used for production of a normal styrene- (meth) acrylic copolymer can be used.
さらに連続塊状重合を用いることも可能であり、多分岐状スチレン-(メタ)アクリル系樹脂を製造する方法については、特に限定されるものではないが、一個以上の攪拌式反応器(反応槽)と可動部分の無い複数のミキシングエレメントが内部に固定されている反応槽、即ち管状反応器(静的ミキシングエレメントを有する管状反応器)を組み込んだ連続塊状重合ライン中で、該管状反応器による静的な混合を行いながら連続的に塊状重合を行うことにより、ポリマー分子量の均一性を保つことが可能なことから好ましい。 Further, continuous bulk polymerization can be used, and the method for producing the multi-branched styrene- (meth) acrylic resin is not particularly limited, but one or more stirred reactors (reaction tanks) And a reaction vessel in which a plurality of mixing elements having no moving parts are fixed, that is, in a continuous bulk polymerization line incorporating a tubular reactor (tubular reactor having a static mixing element), It is preferable to carry out bulk polymerization continuously while performing regular mixing because the uniformity of the molecular weight of the polymer can be maintained.
上記管状反応器の内部に固定されている複数のミキシングエレメントとしては、例えば管内に流入した重合液の流れの分割と流れの方向を変え、分割と合流を繰り返すことにより、重合液を混合するものが挙げられ、このような管状反応器としては、例としてSMX型、SMR型のスルザー式の管状ミキサー、ケニックス式のスタティクミキサー、東レ式の管状ミキサーなどが挙げられるが、特にSMX型、SMR型のスルザー式の管状ミキサーが好ましい。 As the plurality of mixing elements fixed inside the tubular reactor, for example, the polymerization liquid is mixed by changing the flow of the polymerization liquid flowing into the pipe and changing the flow direction and repeating the division and merging. Examples of such tubular reactors include SMX type, SMR type sulzer type tubular mixers, Kenix type static mixers, Toray type tubular mixers, etc. Sulzer-type tubular mixers of the type are preferred.
この様な連続塊状重合ラインを用いて多分岐状部位を含有するスチレン-(メタ)アクリル系樹脂を製造する際、一個以上の攪拌式反応器からなる非循環重合ライン(II)に流出せずに、管状反応器からなる循環重合ライン(I)内を還流する混合溶液の流量をF1(リットル/時間)とし、循環重合ライン(I)から非循環重合ライン(II)に流出する混合溶液の流量F2(リットル/時間)とした場合の、還流比(R = F1/F2)は3〜15の範囲が好ましい。 When producing a styrene- (meth) acrylic resin containing a multi-branched site using such a continuous bulk polymerization line, it does not flow out to the non-circulation polymerization line (II) consisting of one or more stirred reactors. The flow rate of the mixed solution refluxed in the circulating polymerization line (I) comprising the tubular reactor is F1 (liter / hour), and the mixed solution flowing out from the circulating polymerization line (I) to the non-circulating polymerization line (II) When the flow rate is F2 (liter / hour), the reflux ratio (R = F1 / F2) is preferably in the range of 3-15.
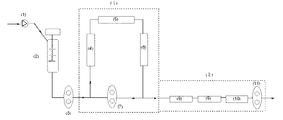
次ぎに、上記連続塊状重合ラインを用いたスチレン-(メタ)アクリル系樹脂の重合方法を、図1の工程図により説明する。
プランジャーポンプ(1)によってスチレンモノマーと(メタ)アクリルモノマーと多分岐状マクロモノマーとを含んでなる混合物などは、まず攪拌式反応器(2)へ送られ、攪拌下で初期重合させた後、ギアポンプ(3)により、静的ミキシングエレメントを有する管状反応器(4),(5)および(6)とギアポンプ(7)とを有する循環重合ライン(I)に送られる。
攪拌式反応器(2)での初期重合は、全モノマーの合計の重合転化率が、該反応器(2)の出口において10〜40重量%、好ましくは14〜30重量%となる迄実施することが好ましい。また、攪拌式反応器(2)としては、例えば攪拌式槽型反応器、攪拌式塔型反応器等が挙げられ、攪拌翼としては、例えばアンカー型、タービン型、スクリュー型、ダブルヘリカル型、ログボーン型等の攪拌翼が挙げられる。
次に、循環重合ライン(I)内で、重合液は循環しながら重合が進み、その一部の重合液は、次の非循環重合ライン(II)へ送られる。ここで、循環重合ライン(I)内を循環する重合液の流量と、非循環重合ライン(II)へ流出する重合液の流量との比、還流比Rは、非循環重合ライン(II)に流出せずに循環重合ライン(I)内を還流する混合溶液の流量をF1 (リットル /時間)とし、循環重合ライン(I)から非循環重合ライン(II)に流出する混合溶液の流量F2 (リットル/時間)とした場合、通常R=F1 /F2 が3〜15の範囲であることが好ましい。
Next, a method for polymerizing a styrene- (meth) acrylic resin using the continuous bulk polymerization line will be described with reference to the process diagram of FIG.
A mixture comprising a styrene monomer, a (meth) acrylic monomer, and a multi-branched macromonomer is first sent to the stirring reactor (2) by the plunger pump (1), and after initial polymerization is performed under stirring. , By a gear pump (3) and sent to a circulating polymerization line (I) having tubular reactors (4), (5) and (6) with static mixing elements and a gear pump (7).
The initial polymerization in the stirred reactor (2) is carried out until the total polymerization conversion rate of all monomers reaches 10 to 40% by weight, preferably 14 to 30% by weight, at the outlet of the reactor (2). It is preferable. Examples of the stirring reactor (2) include a stirring tank reactor, a stirring tower reactor, and the like, and examples of the stirring blade include an anchor type, a turbine type, a screw type, a double helical type, Examples include a stirring blade of a log bone type.
Next, in the circulation polymerization line (I), the polymerization proceeds while the polymerization solution is circulated, and a part of the polymerization solution is sent to the next non-circulation polymerization line (II). Here, the ratio of the flow rate of the polymerization liquid circulating in the circulation polymerization line (I) and the flow rate of the polymerization liquid flowing out to the non-circulation polymerization line (II), and the reflux ratio R are set in the non-circulation polymerization line (II). The flow rate of the mixed solution refluxed in the circulation polymerization line (I) without flowing out is defined as F1 (liter / hour), and the flow rate F2 of the mixed solution flowing out from the circulation polymerization line (I) into the non-circulation polymerization line (II) ( In general, R = F1 / F2 is preferably in the range of 3-15.
また、該循環重合ライン(I)での重合は、該循環重合ライン(I)出口での全モノマーの合計の重合転化率が、通常30〜70質量%、好ましくは35〜65質量%になる様に重合させる。重合温度としては120〜140℃が適している。
非循環重合ライン(II)での重合温度は、通常140〜160℃の重合温度であり、重合転化率60〜90質量%となるまで連続的に重合される。
次に、この混合溶液はギアポンプ(11)により予熱器、次いで脱揮発槽に送られ、減圧下にて未反応単量体および溶剤を除去した後、ペレット化することにより目的とする組成物が得られる。
In addition, in the polymerization in the circulation polymerization line (I), the total polymerization conversion rate of all monomers at the outlet of the circulation polymerization line (I) is usually 30 to 70% by mass, preferably 35 to 65% by mass. Polymerize in the same manner. A polymerization temperature of 120 to 140 ° C. is suitable.
The polymerization temperature in the non-circulation polymerization line (II) is usually a polymerization temperature of 140 to 160 ° C., and the polymerization is continuously performed until the polymerization conversion rate is 60 to 90% by mass.
Next, this mixed solution is sent to a preheater and then to a devolatilization tank by a gear pump (11), and after removing unreacted monomers and solvent under reduced pressure, the target composition is formed by pelletization. can get.
塊状重合や溶液重合などの重合反応では、反応物の粘性を低下させるために、反応系に有機溶剤を添加することが可能であり、その有機溶剤は、トルエン、エチルベンゼン、キシレン、アセトニトリル、ベンゼン、クロロベンゼン、ジクロロベンゼン、アニソール、シアノベンゼン、ジメチルフォルムアミド、N,N−ジメチルアセトアミド、メチルエチルケトン等が挙げられる。 In polymerization reactions such as bulk polymerization and solution polymerization, an organic solvent can be added to the reaction system in order to reduce the viscosity of the reaction product, and the organic solvent includes toluene, ethylbenzene, xylene, acetonitrile, benzene, Examples include chlorobenzene, dichlorobenzene, anisole, cyanobenzene, dimethylformamide, N, N-dimethylacetamide, and methyl ethyl ketone.
特に多分岐状マクロモノマーの添加量を多くしたい場合には、ゲル化を抑制する観点からも有機溶剤を使用することが好ましい。これにより、先に示した多分岐状マクロモノマーの添加量を飛躍的に増量させることができ、ゲル化が生じにくくする効果がある。 In particular, when it is desired to increase the amount of the hyperbranched macromonomer, it is preferable to use an organic solvent from the viewpoint of suppressing gelation. Thereby, the addition amount of the multibranched macromonomer shown previously can be increased dramatically, and there is an effect of making gelation difficult to occur.
用いるラジカル重合開始剤としては、特に制限はなく、公知慣用の例えば、1,1−ビス(t−ブチルパーオキシ)シクロヘキサン、2,2−ビス(t−ブチルパーオキシ)ブタン、2,2−ビス(4,4−ジ−ブチルパーオキシシクロヘキシル)プロパン等のパーオキシケタール類、クメンハイドロパーオキサイド、t−ブチルハイドロパーオキサイド等のハイドロパーオキサイド類、ジ−t−ブチルパーオキサイド、ジクミルパーオキサイド、ジ−t−ヘキシルパーオキサイド等のジアルキルパーオキサイド類、ベンゾイルパーオキサイド、ジシナモイルパーオキサイド等のジアシルパーオキサイド類、t−ブチルパーオキシベンゾエート、ジ−t−ブチルパーオキシイソフタレート、t−ブチルパーオキシイシプロピルモノカーボネート等のパーオキシエステル類、N,N’−アゾビスイソブチルニトリル、N,N’−アゾビス(シクロヘキサン−1−カルボニトリル)、N,N’−アゾビス(2−メチルブチロニトリル)、N,N’−アゾビス(2,4−ジメチルバレロニトリル)、N,N’−アゾビス[2−(ヒドロキシメチル)プロピオニトリル]等が挙げられ、これらの1種あるいは2種以上を組み合わせて使用することができる。 The radical polymerization initiator to be used is not particularly limited, and for example, 1,1-bis (t-butylperoxy) cyclohexane, 2,2-bis (t-butylperoxy) butane, 2,2- Peroxyketals such as bis (4,4-di-butylperoxycyclohexyl) propane, hydroperoxides such as cumene hydroperoxide, t-butyl hydroperoxide, di-t-butyl peroxide, dicumylper Dialkyl peroxides such as oxide, di-t-hexyl peroxide, diacyl peroxides such as benzoyl peroxide, disinamoyl peroxide, t-butyl peroxybenzoate, di-t-butyl peroxyisophthalate, t -Butylperoxy isopropyl mono carbonate Peroxyesters such as N, N′-azobisisobutylnitrile, N, N′-azobis (cyclohexane-1-carbonitrile), N, N′-azobis (2-methylbutyronitrile), N, N '-Azobis (2,4-dimethylvaleronitrile), N, N'-azobis [2- (hydroxymethyl) propionitrile] and the like may be mentioned, and these may be used alone or in combination. it can.
更にスチレン‐(メタ)アクリル系樹脂の分子量が過度に大きくなりすぎないように連鎖移動剤を添加してもよい。連鎖移動剤としては、連鎖移動基を1つ有する単官能連鎖移動剤でも連鎖移動剤を複数有する多官能連鎖移動剤を使用できる。単官能連鎖移動剤としては、アルキルメルカプタン類、チオグリコール酸エステル類等が挙げられる。 Furthermore, a chain transfer agent may be added so that the molecular weight of the styrene- (meth) acrylic resin does not become excessively large. As the chain transfer agent, a monofunctional chain transfer agent having one chain transfer group or a polyfunctional chain transfer agent having a plurality of chain transfer agents can be used. Examples of the monofunctional chain transfer agent include alkyl mercaptans and thioglycolic acid esters.
多官能連鎖移動剤としては、エチレングリコール、ネオペンチルグリコール、トリメチロールプロパン、ペンタエリスリトール、ジペンタエリスリトール、トリペンタエリスリトール、ソルビトール等の多価アルコール水酸基をチオグリコール酸または3−メルカプトプロピオン酸でエステル化したものが挙げられる。 Polyfunctional chain transfer agents such as ethylene glycol, neopentyl glycol, trimethylolpropane, pentaerythritol, dipentaerythritol, tripentaerythritol, sorbitol, etc. are esterified with thioglycolic acid or 3-mercaptopropionic acid. The thing which was done is mentioned.
本発明のスチレン-(メタ)アクリル系樹脂を製造するには、上述のように多分岐状マクロモノマーとスチレン系単量体、(メタ)アクリル系単量体とを上記の1段で重合させる方法の他に、予め別々に多分岐状スチレン-(メタ)アクリル系共重合体と多分岐状マクロモノマーを含んでいないスチレン‐(メタ)アクリル系共重合体とを混合し任意の混合比を有する分岐状スチレン-(メタ)アクリル系樹脂を製造してもよい。 In order to produce the styrene- (meth) acrylic resin of the present invention, as described above, the multi-branched macromonomer, the styrene monomer, and the (meth) acrylic monomer are polymerized in the above-mentioned one stage. In addition to the method, a multi-branched styrene- (meth) acrylic copolymer and a styrene- (meth) acrylic copolymer that does not contain a multi-branched macromonomer are separately mixed in advance to obtain an arbitrary mixing ratio. A branched styrene- (meth) acrylic resin may be produced.
本発明のスチレン-(メタ)アクリル系樹脂には、超高分子量の多分岐状スチレン-(メタ)アクリル系共重合体を含むが、本発明の樹脂は、このような超高分子量成分を含んでいても、ゲル化が実質的に生じないために、有機溶媒に容易に溶解する。 The styrene- (meth) acrylic resin of the present invention contains an ultrahigh molecular weight multi-branched styrene- (meth) acrylic copolymer, but the resin of the present invention contains such an ultrahigh molecular weight component. However, since gelation does not substantially occur, it dissolves easily in an organic solvent.
本発明の多分岐状スチレン-(メタ)アクリル系共重合体は、高分子量でありながら、メルトマスフローレイトが高く、スチレン-(メタ)アクリル系樹脂の製造時ならびに成形加工時の流動性に優れ、優れた生産性ならびに加工性が有する。このため、射出成形、押出成形、真空成形、圧空成形、押出発泡成形、カレンダー成形、ブロー成形などの成形方法による各種成形品として従来よりも広い用途に使用することができる。 The multi-branched styrene- (meth) acrylic copolymer of the present invention has a high melt mass flow rate while having a high molecular weight, and has excellent fluidity during the production of styrene- (meth) acrylic resins and during molding. Excellent productivity and processability. For this reason, it can be used for a wider use than the past as various molded products by molding methods such as injection molding, extrusion molding, vacuum molding, pressure forming, extrusion foam molding, calendar molding and blow molding.
以下に実施例を用いて本発明を更に具体的に説明する。本発明はもとより、これらの実施例の範囲に限定されるべきものではない。次に用いた測定方法について説明する。 Hereinafter, the present invention will be described more specifically with reference to examples. The present invention should not be limited to the scope of these examples. Next, the measurement method used will be described.
(多分岐状マクロモノマーのGPCによる測定条件)
高速液体クロマトグラフィー(東ソー株式会社製HLC−8220GPC)、RI検出器、TSKgel G6000H×1+G5000H×1+G4000H×l+G3000H×l+TSKguard column、溶媒THF、流速1.0ml/分、温度40℃にて測定した。
(Measurement conditions of GPC for hyperbranched macromonomer)
High performance liquid chromatography (HLC-8220 GPC manufactured by Tosoh Corporation), RI detector, TSKgel G6000H × 1 + G5000H × 1 + G4000H × l + G3000H × l + TSKguard column, solvent THF, flow rate 1.0 ml / min, temperature 40 ° C.
(スチレン系樹脂のMALLS-GPC測定条件)
Shodex HPLC(昭和電工(株)製GPC測定装置)、検出器Wyatt Technology DAWN EOS(Wyatt Technology社製)、Shodex RI-101(昭和電工(株)製)、カラム(東ソー株式会社製)TSKgel G6000H×1+G5000H×1+G4000H×l+G3000H×l+TSKguard column、溶媒THF、流量1.0ml/minにて測定した。また、MALLS-GPCの測定の解析は、Wyatt社の解析ソフトASTRAにより求めた。
(MALLS-GPC measurement conditions for styrene resin)
Shodex HPLC (manufactured by Showa Denko Co., Ltd. GPC measuring device), detector Wyatt Technology DAWN EOS (manufactured by Wyatt Technology), Shodex RI-101 (manufactured by Showa Denko KK), column (manufactured by Tosoh Corporation) TSKgel G6000H × 1 + G5000H × 1 + G4000H × l + G3000H × l + TSKguard column, solvent THF, flow rate 1.0 ml / min. Moreover, the analysis of the measurement of MALLS-GPC was calculated | required with the analysis software ASTRA of Wyatt.
実施例8及び9、比較例1のMALLS-GPCから求められる重量平均分子量(Molar Mass)―慣性半径(RMS Radius)の両対数グラフを図2に示した。 A log-log graph of weight average molecular weight (Molar Mass) -radius of inertia (RMS Radius) determined from MALLS-GPC in Examples 8 and 9 and Comparative Example 1 is shown in FIG.
(NMR測定法)
核磁気共鳴分光法(1H−NMR)により多分岐状マクロモノマーのエチレン性重合性二重結合の量を求め、試料質量当たりのモル数で示した。
(NMR measurement method)
The amount of the ethylenically polymerizable double bond of the multi-branched macromonomer was determined by nuclear magnetic resonance spectroscopy ( 1 H-NMR), and indicated by the number of moles per sample mass.
(試験片(ダンベル成形))
住友重機械工業(株)製 射出成形機MINIMAT 14/7B を使用し、180〜220℃で樹脂を溶解し、横65mm×縦13mm×厚さ3mmのダンベル片を作製した。
(Specimen (Dumbell molding))
Using an injection molding machine MINIMAT 14 / 7B manufactured by Sumitomo Heavy Industries, Ltd., the resin was melted at 180 to 220 ° C. to produce a dumbbell piece having a width of 65 mm × length of 13 mm × thickness of 3 mm.
(曲げエネルギー測定)
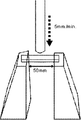
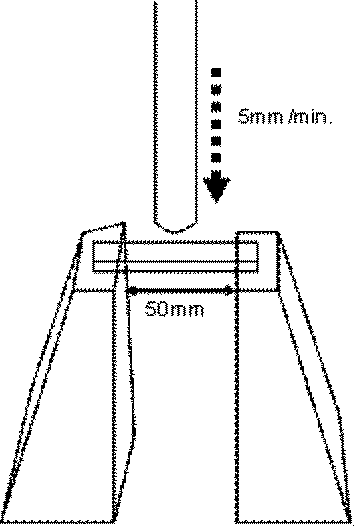
TOYO BALDWIN社のTENSION装置(SS−207−AP)を使用し、50mmの幅にダンベルを均等に置き、ロードセル500kg、押しこみスピード5mm/min.で曲げエネルギーを測定した。測定で得られたデータは、X軸を時間(チャートスピード50mm/min.)、Y軸を応力(チャート6cmで10kg)となり、グラフから得られる面積を普通コピー紙で重量換算し、曲げエネルギーの値(g)とした。(図3と図4参照)
(Bending energy measurement)
Using a TOYO BALDWIN TENSION device (SS-207-AP), dumbbells were evenly placed in a width of 50 mm, and bending energy was measured with a load cell of 500 kg and an indentation speed of 5 mm / min. The data obtained from the measurement is time (chart speed 50mm / min.) On the X-axis and stress (10kg on the chart 6cm) on the Y-axis. Value (g) was used. (See Fig. 3 and Fig. 4)
(参考例1)多分岐状マクロモノマー(M−m1)の合成
撹拌装置、滴下ロート、温度計、窒素導入装置およびバブラーを備えた1000mlの茄子型フラスコに、4−ブロモジ(エチレンオキシ)フェニルアセトニトリル35gを窒素雰囲気下にて800mlジメチルスルフォキシド(DMSO)に溶解した。水浴にて内温を30℃とした後、44mlの50%水酸化ナトリウム水溶液を3分間かけて滴下した。30℃に保持したまま2時間撹拌し多分岐状マクロモノマーの前駆体を得た。更に該反応物に50.0gの4−クロロメチルスチレンを滴下し2時間撹拌することにより、多分岐状マクロモノマー溶液を得た。
(Reference Example 1) Synthesis of multi-branched macromonomer (M-m1) 4-bromodi (ethyleneoxy) phenylacetonitrile was added to a 1000 ml cocoon flask equipped with a stirrer, a dropping funnel, a thermometer, a nitrogen introducing device and a bubbler. 35 g was dissolved in 800 ml dimethyl sulfoxide (DMSO) under a nitrogen atmosphere. After the internal temperature was adjusted to 30 ° C. in a water bath, 44 ml of 50% aqueous sodium hydroxide solution was added dropwise over 3 minutes. While maintaining at 30 ° C., the mixture was stirred for 2 hours to obtain a precursor of a hyperbranched macromonomer. Furthermore, 50.0 g of 4-chloromethylstyrene was added dropwise to the reaction product and stirred for 2 hours to obtain a multi-branched macromonomer solution.
得られた溶液を濾過して固形分を除き、この濾液を225mlの5モル/L塩酸水溶液を含むメタノール5L中に投入し多分岐状マクロモノマーを沈殿させた。沈殿した多分岐状マクロモノマーを吸引ろ過し、蒸留水、メタノールの順で3回繰り返し洗浄した。得られた多分岐状マクロモノマーを24時間減圧下で乾燥し、多分岐状マクロモノマー(M−m1)20gを得た。 The resulting solution was filtered to remove solids, and the filtrate was put into 5 L of methanol containing 225 ml of 5 mol / L hydrochloric acid aqueous solution to precipitate a multibranched macromonomer. The precipitated hyperbranched macromonomer was suction filtered and washed three times in the order of distilled water and methanol. The obtained multibranched macromonomer was dried under reduced pressure for 24 hours to obtain 20 g of a multibranched macromonomer (M-m1).
得られた多分岐状マクロモノマー(M−m1)をGPCにより測定した結果、重量平均分子量(Mw)は6,000であった。また1H−NMRの測定結果から、芳香環に直接結合した重合性二重結合導入量は2.70ミリモル/gであることが確認された。 As a result of measuring the obtained hyperbranched macromonomer (M-m1) by GPC, the weight average molecular weight (Mw) was 6,000. Moreover, from the measurement result of 1 H-NMR, it was confirmed that the amount of polymerizable double bonds introduced directly bonded to the aromatic ring was 2.70 mmol / g.
(参考例2)多分岐状マクロモノマー(M−m2)の合成
参考例1における4−ブロモジ(エチレンオキシ)フェニルアセトニトリルの代わりに4−トシルオキシジ(エチレンオキシ)フェニルアセトニトリルを用いた以外は、参考例1と同様にして、21gの多分岐状マクロモノマー(M−m2)を得た。得られた多分岐状マクロモノマー(M−m2)の重量平均分子量(Mw)は3,100であった。また1H−NMRの測定結果から芳香環に直接結合した重合性二重結合導入量は2.50ミリモル/gであった。
Reference Example 2 Synthesis of Multibranched Macromonomer (M-m2) Reference Example except that 4-tosyloxydi (ethyleneoxy) phenylacetonitrile was used instead of 4-bromodi (ethyleneoxy) phenylacetonitrile in Reference Example 1. In the same manner as in Example 1, 21 g of a hyperbranched macromonomer (M-m2) was obtained. The obtained multibranched macromonomer (M-m2) had a weight average molecular weight (Mw) of 3,100. From the result of 1 H-NMR measurement, the amount of polymerizable double bonds introduced directly bonded to the aromatic ring was 2.50 mmol / g.
(参考例3)多分岐状マクロモノマー(M−m3)の合成
撹拌装置、滴下ロート、温度計、窒素導入装置およびバブラーを備えた1000mlの茄子型フラスコに、窒素雰囲気下にてフェニルアセト二トリル0.8gを800mlジメチルスルフォキシド(DMSO)に溶解した。水浴にて内温を30℃とした後、44mlの50%水酸化ナトリウム水溶液をかけて加えた。その後に、4−トシルオキシモノ(エチレンオキシ)フェニルアセトニトリル40gを3分間かけて加え、30℃に保持したまま20分間撹拌し多分岐状マクロモノマーの前駆体を得た。更に該反応物に50.0gの4−クロロメチルスチレンを滴下し3時間撹拌することにより、多分岐状マクロモノマー溶液を得た。
(Reference Example 3) Synthesis of a multi-branched macromonomer (M-m3) Phenylacetonitrile was added to a 1000 ml insulator flask equipped with a stirrer, a dropping funnel, a thermometer, a nitrogen introducing device and a bubbler under a nitrogen atmosphere. 0.8 g was dissolved in 800 ml dimethyl sulfoxide (DMSO). The internal temperature was adjusted to 30 ° C. in a water bath, and 44 ml of 50% aqueous sodium hydroxide solution was added. Thereafter, 40 g of 4-tosyloxymono (ethyleneoxy) phenylacetonitrile was added over 3 minutes and stirred for 20 minutes while maintaining at 30 ° C. to obtain a precursor of a multi-branched macromonomer. Further, 50.0 g of 4-chloromethylstyrene was added dropwise to the reaction product and stirred for 3 hours to obtain a multi-branched macromonomer solution.
得られた溶液を濾過して固形分を除き、この濾液を225mlの5モル/L塩酸水溶液を含むメタノール5L中に投入し多分岐状マクロモノマーを沈殿させた。沈殿した多分岐状マクロモノマーを吸引ろ過し、蒸留水、メタノールの順で3回繰り返し洗浄した。得られた多分岐状マクロモノマーを24時間減圧下で乾燥し、多分岐状マクロモノマー(M−m3)20.5gを得た。 The resulting solution was filtered to remove solids, and the filtrate was put into 5 L of methanol containing 225 ml of 5 mol / L hydrochloric acid aqueous solution to precipitate a multibranched macromonomer. The precipitated hyperbranched macromonomer was suction filtered and washed three times in the order of distilled water and methanol. The obtained multibranched macromonomer was dried under reduced pressure for 24 hours to obtain 20.5 g of a multibranched macromonomer (M-m3).
得られた多分岐状マクロモノマー(M−m3)をGPCにより測定した結果、重量平均分子量(Mw)は2,400であった。また1H−NMRの測定結果から、芳香環に直接結合した重合性二重結合導入量は4.30ミリモル/gであることが確認された。 As a result of measuring the obtained multibranched macromonomer (M-m3) by GPC, the weight average molecular weight (Mw) was 2,400. Moreover, from the measurement result of 1 H-NMR, it was confirmed that the introduction amount of the polymerizable double bond directly bonded to the aromatic ring was 4.30 mmol / g.
(参考例4)多分岐状マクロモノマー(M−m4)の合成
<多分岐ポリエーテルポリオール1の合成>
攪拌機、温度計、滴下ロート及びコンデンサーを備えた2リットルフラスコに、室温下、エトキシ化ペンタエリスリトール(5モル−エチレンオキシド付加ペンタエリスリトール)50.5g、BF3ジエチルエーテル溶液(50パーセント)1gを加え、110℃に加熱した。これに3―エチルー3―(ヒドロキシメチル)オキセタン 450gを、反応による発熱を制御しつつ、25分間でゆっくり加えた。発熱が収まったところで、反応混合物をさらに120℃で3時間撹拌し、その後、室温に冷却した。
得られた多分岐ポリエーテルポリオールの重量平均分子量は3,000、水酸基価は530であった。
Reference Example 4 Synthesis of Multibranched Macromonomer (M-m4) <Synthesis of
To a 2 liter flask equipped with a stirrer, thermometer, dropping funnel and condenser, 50.5 g of ethoxylated pentaerythritol (5 mol-ethylene oxide-added pentaerythritol) and 1 g of BF3 diethyl ether solution (50 percent) were added at room temperature. Heated to ° C. To this, 450 g of 3-ethyl-3- (hydroxymethyl) oxetane was slowly added over 25 minutes while controlling the exotherm due to the reaction. When the exotherm had subsided, the reaction mixture was further stirred at 120 ° C. for 3 hours and then cooled to room temperature.
The resulting multi-branched polyether polyol had a weight average molecular weight of 3,000 and a hydroxyl value of 530.
<メタアクリロイル基及びアセチル基を有する多分岐ポリエーテル1の合成>
攪拌機、温度計、コンデンサーを備えたディーンスタークデカンター及び気体導入管を備えた反応器に、上述の<多分岐ポリエーテルポリオール1の合成>で得られた多分岐ポリエーテルポリオール50g、メタアクリル酸13.8g、トルエン 150g、ヒドロキノン 0.06g、パラトルエンスルホン酸 1gを加え、混合溶液中に3ミリリットル/分の速度で7%酸素含有窒素を吹き込みながら、常圧下で撹拌し、加熱した。デカンターへの留出液量が1時間あたり30gになるように加熱量を調節し、脱水量が2.9gに到達するまで加熱を続けた。
反応終了後、一度冷却し、無水酢酸 36g、スルファミン酸 5.7gを加え、60℃で10時間撹拌した。その後、残っている酢酸及びヒドロキノンを除去する為に5%水酸化ナトリウム水溶液50gで4回洗浄し、さらに1%硫酸水溶液50gで1回、水50gで2回洗浄した。得られた有機層にメトキノン0.02gを加え、減圧下、7%酸素を導入しながら溶媒を留去し、イソプロペニル基およびアセチル基を有する多分岐ポリエーテル60gを得た。得られた多分岐ポリエーテルの重量平均分子量は3900であり、多分岐ポリエーテルポリオールへのイソプロペニル基およびアセチル基導入率は、それぞれ30%および62%であった。
<Synthesis of
In a reactor equipped with a Dean-Stark decanter equipped with a stirrer, a thermometer, a condenser, and a gas introduction tube, 50 g of the multi-branched polyether polyol obtained in the above-mentioned <Synthesis of
After completion of the reaction, the reaction mixture was cooled once, 36 g of acetic anhydride and 5.7 g of sulfamic acid were added, and the mixture was stirred at 60 ° C. for 10 hours. Thereafter, in order to remove the remaining acetic acid and hydroquinone, it was washed with 50 g of 5% aqueous sodium hydroxide solution four times, and further washed once with 50 g of 1% aqueous sulfuric acid solution and twice with 50 g of water. To the obtained organic layer, 0.02 g of methoquinone was added and the solvent was distilled off while introducing 7% oxygen under reduced pressure to obtain 60 g of a multi-branched polyether having an isopropenyl group and an acetyl group. The weight average molecular weight of the obtained multibranched polyether was 3900, and the introduction ratios of isopropenyl group and acetyl group into the multibranched polyether polyol were 30% and 62%, respectively.
(参考例5)多分岐状マクロモノマー(M−m5)の合成
<スチリル基及びアセチル基を有する多分岐ポリエーテル1の合成>
攪拌機、乾燥管を備えたコンデンサー、滴下ロート及び温度計を備えた反応器に、上述の<多分岐ポリエーテルポリオール1の合成>で得られた多分岐ポリエーテルポリオール50g、テトラヒドロフラン 100g及び水素化ナトリウム 4.3gを加え、室温下、撹拌した。これに4−クロロメチルスチレン 26.7gを1時間かけて滴下し、得られた反応混合物を50℃でさらに4時間撹拌した。
反応終了後、一度冷却し、無水酢酸 34g、スルファミン酸 5.4gを加え、60℃で10時間撹拌した。その後、減圧下でテトラヒドロフランを留去し、得られた混合物をトルエン150gで溶解させ、残っている酢酸を除去する為に5%水酸化ナトリウム水溶液50gで4回洗浄し、さらに1%硫酸水溶液50gで1回、水50gで2回洗浄した。得られた有機層から減圧下で溶媒を留去し、スチリル基およびアセチル基を有する多分岐ポリエーテル70gを得た。得られた多分岐ポリエーテルの重量平均分子量は4800であり、多分岐ポリエーテルポリオールへのスチリル基およびアセチル基導入率は、それぞれ38%および57%であった。
Reference Example 5 Synthesis of Multibranched Macromonomer (M-m5) <Synthesis of
In a reactor equipped with a stirrer, a condenser equipped with a drying tube, a dropping funnel and a thermometer, 50 g of the multibranched polyether polyol obtained in the above-mentioned <Synthesis of
After completion of the reaction, the mixture was cooled once, 34 g of acetic anhydride and 5.4 g of sulfamic acid were added, and the mixture was stirred at 60 ° C. for 10 hours. Thereafter, the tetrahydrofuran was distilled off under reduced pressure, the resulting mixture was dissolved in 150 g of toluene, washed with 50 g of 5% aqueous sodium hydroxide solution to remove the remaining acetic acid, and further 50 g of 1% aqueous sulfuric acid solution. And once with 50 g of water. The solvent was distilled off from the obtained organic layer under reduced pressure to obtain 70 g of a multi-branched polyether having a styryl group and an acetyl group. The resulting multi-branched polyether had a weight average molecular weight of 4800, and the styryl group and acetyl group introduction rates into the multi-branched polyether polyol were 38% and 57%, respectively.
(参考例6)多分岐状マクロモノマー(M−m6)の合成
<スチリル基を有するPAMAMデンドリマーの合成>
攪拌機、乾燥管を備えたコンデンサー、滴下ロート及び温度計を備えた反応器にPAMAMデンドリマー(ゼネレーション2.0:Dentritech社製)のメタノール溶液(20重量パーセント) 50gを加え、減圧下、撹拌しながらメタノールを留去した。続いて、テトラヒドロフラン 50g及び微粉化した水酸化カリウム 3.0gを加え、室温下、撹拌した。これに4−クロロメチルスチレン 7.0gを10分間かけて滴下し、得られた反応混合物を50℃でさらに3時間撹拌した。
反応終了後、冷却し、固体を濾過した後に、テトラヒドロフランを減圧下、留去し、スチリル基を有するPAMAMデンドリマー 13gを得た。得られたデンドリマーのスチリル基含有量は2.7ミリモル/グラムであった。
(Reference Example 6) Synthesis of hyperbranched macromonomer (M-m6) <Synthesis of PAMAM dendrimer having a styryl group>
To a reactor equipped with a stirrer, a condenser equipped with a drying tube, a dropping funnel, and a thermometer, 50 g of a methanol solution (20 weight percent) of PAMAM dendrimer (Generation 2.0: manufactured by Dentritech) was added and stirred under reduced pressure. While methanol was distilled off. Subsequently, 50 g of tetrahydrofuran and 3.0 g of finely divided potassium hydroxide were added and stirred at room temperature. To this, 7.0 g of 4-chloromethylstyrene was added dropwise over 10 minutes, and the resulting reaction mixture was further stirred at 50 ° C. for 3 hours.
After completion of the reaction, the mixture was cooled and the solid was filtered, and then tetrahydrofuran was distilled off under reduced pressure to obtain 13 g of a PAMAM dendrimer having a styryl group. The obtained dendrimer had a styryl group content of 2.7 mmol / gram.
(参考例7)多分岐状マクロモノマー(M−m7)の合成
<スチリル基及びアセチル基を有する多分岐ポリエーテルポリオール2>
攪拌機、コンデンサー、遮光性滴下ロート及び温度計を備え、窒素シールが可能な遮光性反応容器に、窒素気流下、無水1,3,5−トリヒドロキシベンゼン 0.5g、炭酸カリウム 29g、18−クラウン−6 2.7g及びアセトン 180gを加え、撹拌しながら、5−(ブロモメチル)−1,3−ジヒドロキシベンゼン 21.7gとアセトン 180gからなる溶液を2時間かけて滴下、加えた。その後、5−(ブロモメチル)−1,3−ジヒドロキシベンゼンが消失するまで、撹拌下、加熱、還流させた。
その後、4−クロロメチルスチレン 9.0gを加え、これが消失するまで、さらに撹拌下、加熱、還流させた。その後、反応混合物に無水酢酸 4g、スルファミン酸 0.6gを加え、室温下、一晩撹拌した。冷却後、反応混合物中の固体を濾過で除き、溶媒を減圧下で留去した。得られた混合物をジクロロメタンに溶解し、水で3回洗浄した後、ジクロロメタン溶液をヘキサンに滴下し、多分岐ポリエーテルを沈殿させた。これを濾過し、乾燥させて、スチリル基及びアセチル基を有する多分岐ポリエーテルポリオール
12gを得た。重量平均分子量は3200で、スチリル基の含有量は3.5ミリモル/グラムであった。
Reference Example 7 Synthesis of Multibranched Macromonomer (M-m7) <Multibranched Polyether Polyol 2 Having Styryl Group and Acetyl Group>
A light-shielding reaction vessel equipped with a stirrer, a condenser, a light-shielding dropping funnel and a thermometer and capable of nitrogen sealing, under a nitrogen stream,
Thereafter, 9.0 g of 4-chloromethylstyrene was added, and the mixture was further heated and refluxed with stirring until the disappearance. Thereafter, 4 g of acetic anhydride and 0.6 g of sulfamic acid were added to the reaction mixture, and the mixture was stirred overnight at room temperature. After cooling, the solid in the reaction mixture was removed by filtration, and the solvent was distilled off under reduced pressure. The obtained mixture was dissolved in dichloromethane and washed three times with water, and then the dichloromethane solution was added dropwise to hexane to precipitate a multibranched polyether. This was filtered and dried to obtain 12 g of a multi-branched polyether polyol having a styryl group and an acetyl group. The weight average molecular weight was 3200, and the styryl group content was 3.5 mmol / gram.
(参考例8)多分岐状マクロモノマー(M−m8)の合成
<メタクリロイル基及びアセチル基を有する多分岐ポリエステルポリオールの合成>
7%酸素導入管、温度計、コンデンサーを備えたディーンスタークデカンター、および攪拌機を備えた反応容器に、「Boltorn H20」10g、ジブチル錫オキシド1.25g、官能基(B)としてイソプロペニル基を有するメチルメタクリレート100g、およびヒドロキノン0.05gを加え、混合溶液中に3ml/分の速度で7%酸素を吹き込みながら、撹拌下に加熱した。デカンターへの留出液量が1時間あたり15〜20gになるように加熱量を調節し、1時間ごとにデカンター内の留出液を取り出し、これに相当する量のメチルメタクリレートを加えながら4時間反応させた。
反応終了後、メチルメタクリレートを減圧下で留去し、残っているヒドロキシル基をキャッピングするために無水酢酸10g、スルファミン酸2gを加えて室温下、10時間撹拌した。濾過でスルファミン酸を除去し、減圧下で無水酢酸および酢酸を留去した後に、残留物を酢酸エチル70gに溶解し、ヒドロキノンを除去する為に5%水酸化ナトリウム水溶液20gで4回洗浄した。さらに7%硫酸水溶液20gで2回、水20gで2回洗浄した。得られた有機層にメトキノン0.0045gを加え、減圧下、7%酸素を導入しながら溶媒を留去し、イソプロペニル基およびアセチル基を有する多分岐ポリエステル11gを得た。得られた多分岐ポリエステルの重量平均分子量は3000、数平均分子量は2100であり、多分岐ポリエステルポリオール(A)へのイソプロペニル基およびアセチル基導入率は、それぞれ55%および36%であった。
Reference Example 8 Synthesis of Multibranched Macromonomer (M-m8) <Synthesis of Multibranched Polyester Polyol Having Methacryloyl Group and Acetyl Group>
In a reaction vessel equipped with a 7% oxygen introduction tube, a thermometer, a Dean-Stark decanter equipped with a condenser, and a stirrer, 10 g of “Boltorn H20”, 1.25 g of dibutyltin oxide, and isopropenyl group as a functional group (B) 100 g of methyl methacrylate and 0.05 g of hydroquinone were added, and the mixture was heated with stirring while blowing 7% oxygen at a rate of 3 ml / min. The amount of heating is adjusted so that the amount of distillate in the decanter is 15 to 20 g per hour, the distillate in the decanter is taken out every hour, and the corresponding amount of methyl methacrylate is added for 4 hours. Reacted.
After completion of the reaction, methyl methacrylate was distilled off under reduced pressure, and 10 g of acetic anhydride and 2 g of sulfamic acid were added to cap the remaining hydroxyl groups, followed by stirring at room temperature for 10 hours. After removing sulfamic acid by filtration and distilling off acetic anhydride and acetic acid under reduced pressure, the residue was dissolved in 70 g of ethyl acetate and washed 4 times with 20 g of 5% aqueous sodium hydroxide to remove hydroquinone. Further, it was washed twice with 20 g of a 7% aqueous sulfuric acid solution and twice with 20 g of water. To the obtained organic layer, 0.0045 g of methoquinone was added and the solvent was distilled off under introduction of 7% oxygen under reduced pressure to obtain 11 g of a hyperbranched polyester having an isopropenyl group and an acetyl group. The obtained multibranched polyester had a weight average molecular weight of 3000 and a number average molecular weight of 2100, and the introduction rates of isopropenyl group and acetyl group into the multibranched polyester polyol (A) were 55% and 36%, respectively.
(実施例1)
スチレン82部、メタクリル酸メチル16.8部、アクリル酸ブチル1.2部、参考例1の多分岐状マクロモノマーをスチレンに対し700ppm、及びトルエン5部からなる混合溶液を調整し、更に、有機過酸化物としてモノマーに対し100ppmのt-ブチルパーオキシベンゾエートを加え、図1に示す装置を用いて下記条件で、連続的に塊状重合させた。
Example 1
A mixed solution consisting of 82 parts of styrene, 16.8 parts of methyl methacrylate, 1.2 parts of butyl acrylate, 700 ppm of the hyperbranched macromonomer of Reference Example 1 with respect to styrene, and 5 parts of toluene was further prepared. As a peroxide, 100 ppm of t-butyl peroxybenzoate was added to the monomer, and continuous polymerization was carried out using the apparatus shown in FIG. 1 under the following conditions.
混合溶液の供給量:9リットル/時間
攪拌式反応器(2)での反応温度:115℃
循環重合ライン(I)での反応温度:120℃
非循環重合ライン(II)での反応温度:125〜160℃
還流比:R= F1/F2 = 6
Feed rate of mixed solution: 9 liters / hour Reaction temperature in stirred reactor (2): 115 ° C.
Reaction temperature in circulation polymerization line (I): 120 ° C
Reaction temperature in non-circulation polymerization line (II): 125 to 160 ° C
Reflux ratio: R = F1 / F2 = 6
重合させて得られた混合溶液を熱交換器で240℃まで加熱し、50mmHgの減圧下で揮発性成分を除去した後、ペレット化して本発明のスチレン-(メタ)アクリル系樹脂を得た。 The mixed solution obtained by polymerization was heated to 240 ° C. with a heat exchanger, volatile components were removed under reduced pressure of 50 mmHg, and pelletized to obtain the styrene- (meth) acrylic resin of the present invention.
(実施例2)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m2)を用いた以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Example 2)
A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that the hyperbranched macromonomer (Mm2) was used instead of the hyperbranched macromonomer (Mm1) in Example 1. It was.
(実施例3)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m3)を用いた以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Example 3)
A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that the hyperbranched macromonomer (M-m3) was used instead of the hyperbranched macromonomer (M-m1) in Example 1. It was.
(実施例4)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m4)を用いた以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
Example 4
A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that the hyperbranched macromonomer (M-m4) was used instead of the hyperbranched macromonomer (M-m1) in Example 1. It was.
(実施例5)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m5)を用いた以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Example 5)
A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that the hyperbranched macromonomer (Mm5) was used instead of the hyperbranched macromonomer (Mm1) in Example 1. It was.
(実施例6)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m6)を用いた以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Example 6)
A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that the hyperbranched macromonomer (M-m6) was used instead of the hyperbranched macromonomer (Mm1) in Example 1. It was.
(実施例7)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m7)を用いた以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Example 7)
A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that the hyperbranched macromonomer (Mm7) was used instead of the hyperbranched macromonomer (Mm1) in Example 1. It was.
(実施例8)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m8)を用いた以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Example 8)
A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that the hyperbranched macromonomer (M-m8) was used instead of the hyperbranched macromonomer (M-m1) in Example 1. It was.
(比較例1)
実施例1における多分岐状マクロモノマー(M−m1)の代わりに多分岐状マクロモノマー(M−m4)を用い、マクロモノマーの添加量を350ppmにした以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Comparative Example 1)
Styrene was used in the same manner as in Example 1 except that the hyperbranched macromonomer (M-m4) was used instead of the hyperbranched macromonomer (Mm1) in Example 1 and the amount of macromonomer added was 350 ppm. -(Meth) acrylic resin was obtained.
(比較例2)
実施例1における多分岐状マクロモノマーを0ppm(無添加)、100ppmのt-ブチルパーオキシベンゾエートの代わりに、150ppmの2,2ビス(4,4ジ,ターシャリブチルぺルオキシシクロヘキシル)プロパンにした以外は、実施例1と同様にしてスチレン-(メタ)アクリル系樹脂を得た。
(Comparative Example 2)
The hyperbranched macromonomer in Example 1 was changed to 0 ppm (no addition) and 100 ppm of 2,2 bis (4,4 di, tertiarybutylperoxycyclohexyl) propane instead of 100 ppm of t-butylperoxybenzoate. A styrene- (meth) acrylic resin was obtained in the same manner as in Example 1 except that.
(比較例3)(高(メタ)アクリル酸エステル含有重合物)
スチレン45部、メタクリル酸メチル44部、アクリル酸ブチル2.5部、トルエン9部からなる混合溶液を調整し、更に、有機過酸化物としてモノマーに対し300ppmの2,2ビス(4,4ジ,ターシャリブチルぺルオキシシクロヘキシル)プロパンを加え、図1に示す装置を用いてスチレン-(メタ)アクリル系樹脂を得た。
(Comparative Example 3) (High (meth) acrylic ester-containing polymer)
A mixed solution consisting of 45 parts of styrene, 44 parts of methyl methacrylate, 2.5 parts of butyl acrylate and 9 parts of toluene was prepared, and 300 ppm of 2,2bis (4,4 , Tertiarybutylperoxycyclohexyl) propane was added, and a styrene- (meth) acrylic resin was obtained using the apparatus shown in FIG.
混合溶液の供給量:9リットル/時間
攪拌式反応器(2)での反応温度:132℃
循環重合ライン(I)での反応温度:138℃
非循環重合ライン(II)での反応温度:140〜160℃
還流比:R= F1/F2 = 6
Feed rate of the mixed solution: 9 liter / hour Reaction temperature in the stirring reactor (2): 132 ° C.
Reaction temperature in circulation polymerization line (I): 138 ° C
Reaction temperature in non-circulation polymerization line (II): 140-160 ° C
Reflux ratio: R = F1 / F2 = 6
(比較例4)
スチレン90部、参考例8の多分岐状マクロモノマーをスチレンに対し700ppm、及びトルエン8部からなる混合溶液を調整し、更に、有機過酸化物としてスチレンに対し150ppmのt-ブチルパーオキシベンゾエートを加え、図4に示す装置を用いて下記条件で、連続的に塊状重合させた。
(Comparative Example 4)
A mixed solution consisting of 90 parts of styrene, 700 ppm of the hyperbranched macromonomer of Reference Example 8 with respect to styrene, and 8 parts of toluene was further prepared, and 150 ppm of t-butyl peroxybenzoate with respect to styrene as an organic peroxide. In addition, bulk polymerization was continuously performed using the apparatus shown in FIG. 4 under the following conditions.
混合溶液の供給量:9リットル/時間
攪拌式反応器(2)での反応温度:115℃
循環重合ライン(I)での反応温度:134℃
非循環重合ライン(II)での反応温度:140〜160℃
還流比:R= F1/F2 = 6
Feed rate of mixed solution: 9 liters / hour Reaction temperature in stirred reactor (2): 115 ° C.
Reaction temperature in circulating polymerization line (I): 134 ° C
Reaction temperature in non-circulation polymerization line (II): 140-160 ° C
Reflux ratio: R = F1 / F2 = 6
重合させて得られた混合溶液を熱交換器で220℃まで加熱し、50mmHgの減圧下で揮発性成分を除去した後、ペレット化してスチレン系樹脂組成物を得た。得られたスチレン系樹脂組成物を得た。 The mixed solution obtained by polymerization was heated to 220 ° C. with a heat exchanger, volatile components were removed under a reduced pressure of 50 mmHg, and pelletized to obtain a styrene resin composition. The obtained styrene resin composition was obtained.
(比較例5)
比較例3における多分岐状マクロモノマーを無添加(0ppm)した以外は、比較例3と同様にしてスチレン系樹脂を得た。
(Comparative Example 5)
A styrene resin was obtained in the same manner as in Comparative Example 3, except that the hyperbranched macromonomer in Comparative Example 3 was not added (0 ppm).
得られた重合物において、住友重機械工業(株)製 射出成形機MINIMAT 14/7B を使用し、180〜220℃で樹脂を溶解し、横65mm×縦13mm×厚さ3mmのダンベル片を作製した。 In the obtained polymer, an injection molding machine MINIMAT 14 / 7B manufactured by Sumitomo Heavy Industries, Ltd. was used, and the resin was dissolved at 180 to 220 ° C. to produce a dumbbell piece having a width of 65 mm × length 13 mm × thickness 3 mm. did.
さらにダンベル片をTOYO BALDWIN社のTENSION装置(SS−207−AP)を使用し、ロードセル500kg、押しこみスピード5mm/min.、ダンベル 測定で得られたデータについて、X軸を時間(チャートスピード50mm/min.)、Y軸を応力(チャート6cmで10kg)としたグラフから得られる面積を普通コピー紙で重量換算し、曲げエネルギーの値(g)とした。(図3と図4参照) Furthermore, using a TOYO BALDWIN TENSION device (SS-207-AP) for the dumbbell piece, load cell 500kg, indentation speed 5mm / min. For the data obtained by dumbbell measurement, the X axis is time (chart speed 50mm / min.), an area obtained from a graph in which the Y-axis is stress (10 kg at a chart of 6 cm) is converted into a weight of ordinary copy paper to obtain a bending energy value (g). (See Fig. 3 and Fig. 4)
得られた結果を表1から表2に示す。 The obtained results are shown in Tables 1 and 2.
表1、及び表2から明らかなように、多分岐状スチレン-(メタ)アクリル系共重合体を含む本発明のスチレン-(メタ)アクリル系樹脂は、超高重量平均分子量(Mw)でありながら、重量平均分子量(Mw)が30万程度の比較例の樹脂と同様に成形が可能である。また、比較例3の樹脂のように、(メタ)アクリル酸エステル成分の量が多い(高分子量化するとゲル化もしくは成形不良を生じるため成形材料としては使用できないモノマー組成)スチレン-(メタ)アクリル系共重合体よりも高曲げエネルギーが得られる。
なお、比較例3の樹脂の単量体組成において、更に高分子量化(重量平均分子量(Mw)が60万以上)を試みたが、そのような超高分子量タイプの直鎖状の樹脂は製造できなかった。また、ジビニルベンゼンのような従来の架橋剤を用いて高分子量化を試みたが、ゲル化が発生して製造できず、或いは成形不良が生じてしまい成形材料としては不適であった。
As is clear from Table 1 and Table 2, the styrene- (meth) acrylic resin of the present invention containing a hyperbranched styrene- (meth) acrylic copolymer has an ultrahigh weight average molecular weight (Mw). However, it can be molded in the same manner as the comparative resin having a weight average molecular weight (Mw) of about 300,000. In addition, like the resin of Comparative Example 3, the amount of the (meth) acrylic acid ester component is large (a monomer composition that cannot be used as a molding material because gelation or molding failure occurs when the molecular weight is increased). Styrene- (meth) acrylic Bending energy is higher than that of the copolymer.
In addition, in the monomer composition of the resin of Comparative Example 3, an attempt was made to further increase the molecular weight (weight average molecular weight (Mw) is 600,000 or more), but such an ultrahigh molecular weight type linear resin was produced. could not. Further, attempts have been made to increase the molecular weight by using a conventional crosslinking agent such as divinylbenzene, but it cannot be produced due to gelation, or a molding defect occurs, which is not suitable as a molding material.
(1):プラジャーポンプ
(2):攪拌式反応器
(3):ギヤポンプ
(4):静的ミキシングエレメントを有する管状反応器
(5):静的ミキシングエレメントを有する管状反応器
(6):静的ミキシングエレメントを有する管状反応器
(7):ギヤポンプ
(8):静的ミキシングエレメントを有する管状反応器
(9):静的ミキシングエレメントを有する管状反応器
(10):静的ミキシングエレメントを有する管状反応器
(I):循環重合ライン
(II):非循環重合ライン
(1): The plunger pump
(2): Stirred reactor
(3): Gear pump
(4): Tubular reactor with static mixing elements
(5): Tubular reactor with static mixing elements
(6): Tubular reactor with static mixing elements
(7): Gear pump
(8): Tubular reactor with static mixing elements
(9): Tubular reactor with static mixing elements
(10): Tubular reactor with static mixing elements
(I): Circulation polymerization line
(II): Acyclic polymerization line
Claims (10)
前記スチレン系単量体と前記(メタ)アクリル系単量体の重合比率(質量基準)が、スチレン系単量体/(メタ)アクリル系単量体=85/15〜70/30であり、
GPC-MALLS(多角度光散乱検出器)により求められる重量平均分子量が60万〜100万であり、
GPC-MALLS(多角度光散乱検出器)による慣性半径(R.M.S Radius)とMolar massの両対数の傾きが、0.15〜0.40の範囲(Molar massが50万から500万の範囲)であるスチレン系樹脂。 A resin obtained by copolymerizing a multi-branched macromonomer having a polymerizable double bond at a branch end, a styrene monomer, and a (meth) acrylic monomer,
The polymerization ratio (mass basis) of the styrene monomer and the (meth) acrylic monomer is styrene monomer / (meth) acrylic monomer = 85/15 to 70/30,
The weight average molecular weight required by GPC-MALLS (multi-angle light scattering detector) is 600,000 to 1,000,000,
Styrenic resin in which the slope of the logarithm of both the radius of inertia (RMS Radius) and Molar mass by GPC-MALLS (multi-angle light scattering detector) is in the range of 0.15 to 0.40 (Molar mass is in the range of 500,000 to 5,000,000). .
(1)電子吸引基と、該電子吸引基に結合する結合手以外の3つの結合手すべてが炭素原子に結合している飽和炭素原子とからなる分岐構造と、
(2)芳香環に直接結合した重合性二重結合を、
有する化合物である請求項1乃至5のいずれかに記載のスチレン系樹脂。 A multi-branched macromonomer having a polymerizable double bond at the branched end,
(1) a branched structure comprising an electron-withdrawing group and a saturated carbon atom in which all three bonds other than the bond that is bonded to the electron-withdrawing group are bonded to a carbon atom;
(2) A polymerizable double bond directly bonded to an aromatic ring,
The styrenic resin according to claim 1, which is a compound having
A film using the styrenic resin according to claim 1.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006114396A JP2007284591A (en) | 2006-04-18 | 2006-04-18 | Styrene- (meth) acrylic resin and molded product thereof |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006114396A JP2007284591A (en) | 2006-04-18 | 2006-04-18 | Styrene- (meth) acrylic resin and molded product thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007284591A true JP2007284591A (en) | 2007-11-01 |
Family
ID=38756677
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006114396A Pending JP2007284591A (en) | 2006-04-18 | 2006-04-18 | Styrene- (meth) acrylic resin and molded product thereof |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2007284591A (en) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009263512A (en) * | 2008-04-25 | 2009-11-12 | Dic Corp | Styrenic resin composition for foamed sheet, foamed sheet, and foamed container |
| JP2010126578A (en) * | 2008-11-26 | 2010-06-10 | Dic Corp | Polyphenylene ether based resin composition and molded product thereof |
| WO2017022498A1 (en) * | 2015-08-03 | 2017-02-09 | Dic株式会社 | Styrene resin composition, foam sheet and molded body using same |
| CN107210376A (en) * | 2015-02-20 | 2017-09-26 | Dic株式会社 | Ink composition for organic light emitting device and organic light emitting device |
| WO2017170591A1 (en) * | 2016-03-28 | 2017-10-05 | Psジャパン株式会社 | Styrenic copolymer and production method therefor, and extruded foam sheet and molded article thereof |
| JP2019052251A (en) * | 2017-09-15 | 2019-04-04 | Psジャパン株式会社 | Rubber-modified styrene resin composition and method for producing the same, sheet and molded article of the same |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06299039A (en) * | 1993-01-21 | 1994-10-25 | Akzo Nobel Nv | Water dispersible hybrid polymer |
| JP2002037823A (en) * | 2000-07-25 | 2002-02-06 | Kawamura Inst Of Chem Res | Copolymer of styrene dendorimer and olefin and method for producing the same |
| JP2003292707A (en) * | 2002-01-31 | 2003-10-15 | Dainippon Ink & Chem Inc | Styrene resin composition and method for producing the same |
| JP2006124498A (en) * | 2004-10-28 | 2006-05-18 | Dainippon Ink & Chem Inc | Styrene- (meth) acrylic resin composition and method for producing the same |
-
2006
- 2006-04-18 JP JP2006114396A patent/JP2007284591A/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06299039A (en) * | 1993-01-21 | 1994-10-25 | Akzo Nobel Nv | Water dispersible hybrid polymer |
| JP2002037823A (en) * | 2000-07-25 | 2002-02-06 | Kawamura Inst Of Chem Res | Copolymer of styrene dendorimer and olefin and method for producing the same |
| JP2003292707A (en) * | 2002-01-31 | 2003-10-15 | Dainippon Ink & Chem Inc | Styrene resin composition and method for producing the same |
| JP2006124498A (en) * | 2004-10-28 | 2006-05-18 | Dainippon Ink & Chem Inc | Styrene- (meth) acrylic resin composition and method for producing the same |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009263512A (en) * | 2008-04-25 | 2009-11-12 | Dic Corp | Styrenic resin composition for foamed sheet, foamed sheet, and foamed container |
| JP2010126578A (en) * | 2008-11-26 | 2010-06-10 | Dic Corp | Polyphenylene ether based resin composition and molded product thereof |
| CN107210376A (en) * | 2015-02-20 | 2017-09-26 | Dic株式会社 | Ink composition for organic light emitting device and organic light emitting device |
| CN107210376B (en) * | 2015-02-20 | 2019-06-28 | Dic株式会社 | Ink composition for organic light-emitting element and organic light-emitting element |
| WO2017022498A1 (en) * | 2015-08-03 | 2017-02-09 | Dic株式会社 | Styrene resin composition, foam sheet and molded body using same |
| WO2017170591A1 (en) * | 2016-03-28 | 2017-10-05 | Psジャパン株式会社 | Styrenic copolymer and production method therefor, and extruded foam sheet and molded article thereof |
| JP2019052251A (en) * | 2017-09-15 | 2019-04-04 | Psジャパン株式会社 | Rubber-modified styrene resin composition and method for producing the same, sheet and molded article of the same |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4423386B2 (en) | Styrene resin composition and method for producing the same | |
| JP4990995B2 (en) | Biaxially stretched styrene resin sheet and molded product using the same | |
| JP2005281405A (en) | Styrenic resin composition, foam sheet thereof and foam container | |
| JP2005179389A (en) | Styrene resin composition for biaxial stretching, biaxially stretched sheet and method for producing the same | |
| JP2009263512A (en) | Styrenic resin composition for foamed sheet, foamed sheet, and foamed container | |
| JP4815784B2 (en) | Styrene- (meth) acrylic resin composition and method for producing the same | |
| JP6083494B1 (en) | Styrene foam sheet and molded body using the same | |
| JP6481848B2 (en) | Styrene resin composition, biaxially stretched styrene resin sheet and molded article | |
| EP1471111B1 (en) | Styrene resin composition and process for producing the same | |
| JP5333808B2 (en) | Resin composition for biaxially oriented styrene resin sheet, and sheet and molded product using the same | |
| JP2007284591A (en) | Styrene- (meth) acrylic resin and molded product thereof | |
| JP4457291B2 (en) | Method for producing styrene resin composition | |
| JP5029722B2 (en) | Styrenic resin composition and molded product thereof | |
| JP6930422B2 (en) | Styrene-based resin composition, biaxially stretched styrene-based resin sheet and molded product | |
| JP4992271B2 (en) | Rubber-modified styrene resin composition, styrene resin sheet and molded body using the same | |
| JP6481847B2 (en) | Styrene resin sheet and molded body using the same | |
| JP4962758B2 (en) | Resin composition for heat-shrinkable film, heat-shrinkable film, and bottle wrapped around the same | |
| JP2012116875A (en) | Resin composition for heat-shrinkable film and heat-shrinkable film | |
| JP6507622B2 (en) | Styrene foam sheet and molded article using the same | |
| JP2007031660A (en) | Styrene resin composition, styrene resin sheet and molded body using the same | |
| JP6891877B2 (en) | Styrene-based resin composition and molded article using it | |
| JP6634812B2 (en) | Styrene-based resin composition, sheet, molded article and method for producing the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090406 |
|
| A977 | Report on retrieval |
Effective date: 20110629 Free format text: JAPANESE INTERMEDIATE CODE: A971007 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110705 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20111110 |