JP2006508124A - 低酸素誘導性因子に関連した病状を治療するためのメルファレンのn−オキシドと誘導体 - Google Patents
低酸素誘導性因子に関連した病状を治療するためのメルファレンのn−オキシドと誘導体 Download PDFInfo
- Publication number
- JP2006508124A JP2006508124A JP2004551738A JP2004551738A JP2006508124A JP 2006508124 A JP2006508124 A JP 2006508124A JP 2004551738 A JP2004551738 A JP 2004551738A JP 2004551738 A JP2004551738 A JP 2004551738A JP 2006508124 A JP2006508124 A JP 2006508124A
- Authority
- JP
- Japan
- Prior art keywords
- hif
- cells
- protein
- hypoxia
- vegf
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 206010021143 Hypoxia Diseases 0.000 title claims description 56
- 150000001204 N-oxides Chemical class 0.000 title abstract description 8
- 238000011282 treatment Methods 0.000 title description 21
- 150000001875 compounds Chemical class 0.000 claims abstract description 38
- 239000000126 substance Substances 0.000 claims abstract description 4
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 3
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims abstract 2
- 101001046870 Homo sapiens Hypoxia-inducible factor 1-alpha Proteins 0.000 claims description 93
- 102100022875 Hypoxia-inducible factor 1-alpha Human genes 0.000 claims description 90
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 claims description 37
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 claims description 36
- 230000001146 hypoxic effect Effects 0.000 claims description 17
- 239000003814 drug Substances 0.000 claims description 13
- 230000002401 inhibitory effect Effects 0.000 claims description 12
- 239000008194 pharmaceutical composition Substances 0.000 claims description 10
- -1 phenylpropionic acid N-oxide Chemical class 0.000 claims description 7
- 238000004519 manufacturing process Methods 0.000 claims description 6
- 229910052757 nitrogen Inorganic materials 0.000 claims description 5
- 239000003085 diluting agent Substances 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 4
- 230000012010 growth Effects 0.000 claims description 4
- 125000001340 2-chloroethyl group Chemical group [H]C([H])(Cl)C([H])([H])* 0.000 claims description 2
- 230000015572 biosynthetic process Effects 0.000 claims description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 2
- 208000005623 Carcinogenesis Diseases 0.000 claims 1
- 230000002491 angiogenic effect Effects 0.000 claims 1
- 230000036952 cancer formation Effects 0.000 claims 1
- 231100000504 carcinogenesis Toxicity 0.000 claims 1
- 201000010099 disease Diseases 0.000 abstract description 9
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 abstract description 9
- 125000003710 aryl alkyl group Chemical group 0.000 abstract description 2
- 210000004027 cell Anatomy 0.000 description 94
- GIGCDIVNDFQKRA-LTCKWSDVSA-N 4-[(2s)-2-amino-2-carboxyethyl]-n,n-bis(2-chloroethyl)benzeneamine oxide;dihydrochloride Chemical compound Cl.Cl.OC(=O)[C@@H](N)CC1=CC=C([N+]([O-])(CCCl)CCCl)C=C1 GIGCDIVNDFQKRA-LTCKWSDVSA-N 0.000 description 81
- 230000000694 effects Effects 0.000 description 48
- 102000016878 Hypoxia-Inducible Factor 1 Human genes 0.000 description 43
- 108010028501 Hypoxia-Inducible Factor 1 Proteins 0.000 description 43
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 36
- 230000007954 hypoxia Effects 0.000 description 34
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 28
- 239000001301 oxygen Substances 0.000 description 28
- 229910052760 oxygen Inorganic materials 0.000 description 28
- 230000023603 positive regulation of transcription initiation, DNA-dependent Effects 0.000 description 25
- 230000037361 pathway Effects 0.000 description 22
- 206010028980 Neoplasm Diseases 0.000 description 21
- 230000005764 inhibitory process Effects 0.000 description 19
- 230000007959 normoxia Effects 0.000 description 18
- 102000013090 Thioredoxin-Disulfide Reductase Human genes 0.000 description 16
- 108010079911 Thioredoxin-disulfide reductase Proteins 0.000 description 16
- 206010006187 Breast cancer Diseases 0.000 description 15
- 208000026310 Breast neoplasm Diseases 0.000 description 15
- 101710168651 Thioredoxin 1 Proteins 0.000 description 13
- 239000000203 mixture Substances 0.000 description 13
- 108090000623 proteins and genes Proteins 0.000 description 13
- 206010009944 Colon cancer Diseases 0.000 description 12
- 208000029742 colonic neoplasm Diseases 0.000 description 12
- 230000002829 reductive effect Effects 0.000 description 12
- 238000001727 in vivo Methods 0.000 description 11
- 230000001965 increasing effect Effects 0.000 description 11
- 239000003112 inhibitor Substances 0.000 description 10
- 238000000034 method Methods 0.000 description 10
- 102100030907 Aryl hydrocarbon receptor nuclear translocator Human genes 0.000 description 9
- 101000793115 Homo sapiens Aryl hydrocarbon receptor nuclear translocator Proteins 0.000 description 9
- 241000699666 Mus <mouse, genus> Species 0.000 description 9
- 102000002933 Thioredoxin Human genes 0.000 description 9
- 108060008226 thioredoxin Proteins 0.000 description 9
- 241000699670 Mus sp. Species 0.000 description 8
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical class OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 8
- 230000003247 decreasing effect Effects 0.000 description 8
- WSFSSNUMVMOOMR-UHFFFAOYSA-N formaldehyde Substances O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 8
- 108091007960 PI3Ks Proteins 0.000 description 7
- 102000003993 Phosphatidylinositol 3-kinases Human genes 0.000 description 7
- 108090000430 Phosphatidylinositol 3-kinases Proteins 0.000 description 7
- 102000011755 Phosphoglycerate Kinase Human genes 0.000 description 7
- 101001099217 Thermotoga maritima (strain ATCC 43589 / DSM 3109 / JCM 10099 / NBRC 100826 / MSB8) Triosephosphate isomerase Proteins 0.000 description 7
- 230000004913 activation Effects 0.000 description 7
- 230000033115 angiogenesis Effects 0.000 description 7
- 238000003556 assay Methods 0.000 description 7
- 239000013592 cell lysate Substances 0.000 description 7
- 229960004630 chlorambucil Drugs 0.000 description 7
- 229940079593 drug Drugs 0.000 description 7
- 238000002474 experimental method Methods 0.000 description 7
- 239000013612 plasmid Substances 0.000 description 7
- 235000018102 proteins Nutrition 0.000 description 7
- 102000004169 proteins and genes Human genes 0.000 description 7
- 101150046474 Vhl gene Proteins 0.000 description 6
- 239000000284 extract Substances 0.000 description 6
- 102100035070 von Hippel-Lindau disease tumor suppressor Human genes 0.000 description 6
- 108010040163 CREB-Binding Protein Proteins 0.000 description 5
- 102100021975 CREB-binding protein Human genes 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 5
- 101710113864 Heat shock protein 90 Proteins 0.000 description 5
- 230000015556 catabolic process Effects 0.000 description 5
- 238000006731 degradation reaction Methods 0.000 description 5
- 230000001419 dependent effect Effects 0.000 description 5
- 238000009472 formulation Methods 0.000 description 5
- 230000014509 gene expression Effects 0.000 description 5
- 229940094937 thioredoxin Drugs 0.000 description 5
- 238000001262 western blot Methods 0.000 description 5
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- RPTUSVTUFVMDQK-UHFFFAOYSA-N Hidralazin Chemical compound C1=CC=C2C(NN)=NN=CC2=C1 RPTUSVTUFVMDQK-UHFFFAOYSA-N 0.000 description 4
- 208000008839 Kidney Neoplasms Diseases 0.000 description 4
- 108060001084 Luciferase Proteins 0.000 description 4
- 239000005089 Luciferase Substances 0.000 description 4
- 102000011779 Nitric Oxide Synthase Type II Human genes 0.000 description 4
- 108010076864 Nitric Oxide Synthase Type II Proteins 0.000 description 4
- 206010060862 Prostate cancer Diseases 0.000 description 4
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 4
- 208000006265 Renal cell carcinoma Diseases 0.000 description 4
- 108010052090 Renilla Luciferases Proteins 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 230000006907 apoptotic process Effects 0.000 description 4
- 238000002512 chemotherapy Methods 0.000 description 4
- 229940088598 enzyme Drugs 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 230000009469 supplementation Effects 0.000 description 4
- 230000004083 survival effect Effects 0.000 description 4
- 230000001988 toxicity Effects 0.000 description 4
- 231100000419 toxicity Toxicity 0.000 description 4
- 238000013518 transcription Methods 0.000 description 4
- 230000035897 transcription Effects 0.000 description 4
- 238000001890 transfection Methods 0.000 description 4
- 210000004881 tumor cell Anatomy 0.000 description 4
- 101100297347 Caenorhabditis elegans pgl-3 gene Proteins 0.000 description 3
- 108090000331 Firefly luciferases Proteins 0.000 description 3
- JRZJKWGQFNTSRN-UHFFFAOYSA-N Geldanamycin Natural products C1C(C)CC(OC)C(O)C(C)C=C(C)C(OC(N)=O)C(OC)CCC=C(C)C(=O)NC2=CC(=O)C(OC)=C1C2=O JRZJKWGQFNTSRN-UHFFFAOYSA-N 0.000 description 3
- 108091054455 MAP kinase family Proteins 0.000 description 3
- 102000043136 MAP kinase family Human genes 0.000 description 3
- 102000004316 Oxidoreductases Human genes 0.000 description 3
- 108090000854 Oxidoreductases Proteins 0.000 description 3
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 3
- 102000004079 Prolyl Hydroxylases Human genes 0.000 description 3
- 108010043005 Prolyl Hydroxylases Proteins 0.000 description 3
- 102100033810 RAC-alpha serine/threonine-protein kinase Human genes 0.000 description 3
- 206010038389 Renal cancer Diseases 0.000 description 3
- 102000040945 Transcription factor Human genes 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- XJLXINKUBYWONI-DQQFMEOOSA-N [[(2r,3r,4r,5r)-5-(6-aminopurin-9-yl)-3-hydroxy-4-phosphonooxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [(2s,3r,4s,5s)-5-(3-carbamoylpyridin-1-ium-1-yl)-3,4-dihydroxyoxolan-2-yl]methyl phosphate Chemical compound NC(=O)C1=CC=C[N+]([C@@H]2[C@H]([C@@H](O)[C@H](COP([O-])(=O)OP(O)(=O)OC[C@@H]3[C@H]([C@@H](OP(O)(O)=O)[C@@H](O3)N3C4=NC=NC(N)=C4N=C3)O)O2)O)=C1 XJLXINKUBYWONI-DQQFMEOOSA-N 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 230000000259 anti-tumor effect Effects 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- QTQAWLPCGQOSGP-GBTDJJJQSA-N geldanamycin Chemical compound N1C(=O)\C(C)=C/C=C\[C@@H](OC)[C@H](OC(N)=O)\C(C)=C/[C@@H](C)[C@@H](O)[C@H](OC)C[C@@H](C)CC2=C(OC)C(=O)C=C1C2=O QTQAWLPCGQOSGP-GBTDJJJQSA-N 0.000 description 3
- 230000034659 glycolysis Effects 0.000 description 3
- 102000049131 human HIF1A Human genes 0.000 description 3
- 201000010982 kidney cancer Diseases 0.000 description 3
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 230000035772 mutation Effects 0.000 description 3
- 229930027945 nicotinamide-adenine dinucleotide Natural products 0.000 description 3
- 230000002018 overexpression Effects 0.000 description 3
- 201000002528 pancreatic cancer Diseases 0.000 description 3
- 208000008443 pancreatic carcinoma Diseases 0.000 description 3
- 239000012188 paraffin wax Substances 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 238000001959 radiotherapy Methods 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 150000003839 salts Chemical class 0.000 description 3
- 230000006641 stabilisation Effects 0.000 description 3
- 238000011105 stabilization Methods 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- 230000004614 tumor growth Effects 0.000 description 3
- QCPDBEXGCHOIDE-UHFFFAOYSA-N (-)-6xi-Methyl-(2ar,4axi,8at,12bt,12ct)-2a,3,4,4a,5,6,7,8a,12b,12c-decahydro-5xi,12dxi-aethano-furo[4',3',2';4,10]anthra[9,1-bc]oxepin-2,9,12-trion Natural products CC1COC2C(C(C=CC3=O)=O)=C3C3C4C22CCC1C2CCC4C(=O)O3 QCPDBEXGCHOIDE-UHFFFAOYSA-N 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- AZKSAVLVSZKNRD-UHFFFAOYSA-M 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide Chemical compound [Br-].S1C(C)=C(C)N=C1[N+]1=NC(C=2C=CC=CC=2)=NN1C1=CC=CC=C1 AZKSAVLVSZKNRD-UHFFFAOYSA-M 0.000 description 2
- KXMJTDMWYPDAPL-UHFFFAOYSA-N 4-(3-carboxypropyl)-n,n-bis(2-chloroethyl)benzeneamine oxide Chemical compound OC(=O)CCCC1=CC=C([N+]([O-])(CCCl)CCCl)C=C1 KXMJTDMWYPDAPL-UHFFFAOYSA-N 0.000 description 2
- 229920000936 Agarose Polymers 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 102100025064 Cellular tumor antigen p53 Human genes 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- 238000008157 ELISA kit Methods 0.000 description 2
- 101001076292 Homo sapiens Insulin-like growth factor II Proteins 0.000 description 2
- 101000602930 Homo sapiens Nuclear receptor coactivator 2 Proteins 0.000 description 2
- 101000808011 Homo sapiens Vascular endothelial growth factor A Proteins 0.000 description 2
- 102000004877 Insulin Human genes 0.000 description 2
- 108090001061 Insulin Proteins 0.000 description 2
- 102100025947 Insulin-like growth factor II Human genes 0.000 description 2
- 102000008201 Lamin Type A Human genes 0.000 description 2
- 108010021099 Lamin Type A Proteins 0.000 description 2
- 108010075639 MAP Kinase Kinase Kinase 5 Proteins 0.000 description 2
- 102100033127 Mitogen-activated protein kinase kinase kinase 5 Human genes 0.000 description 2
- 108010006519 Molecular Chaperones Proteins 0.000 description 2
- 102000005431 Molecular Chaperones Human genes 0.000 description 2
- 101000808007 Mus musculus Vascular endothelial growth factor A Proteins 0.000 description 2
- 108090001146 Nuclear Receptor Coactivator 1 Proteins 0.000 description 2
- 102100037223 Nuclear receptor coactivator 1 Human genes 0.000 description 2
- 102100037226 Nuclear receptor coactivator 2 Human genes 0.000 description 2
- 102000014160 PTEN Phosphohydrolase Human genes 0.000 description 2
- 108010011536 PTEN Phosphohydrolase Proteins 0.000 description 2
- 108010029485 Protein Isoforms Proteins 0.000 description 2
- 102000001708 Protein Isoforms Human genes 0.000 description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 2
- 102000006275 Ubiquitin-Protein Ligases Human genes 0.000 description 2
- 108010083111 Ubiquitin-Protein Ligases Proteins 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 230000001093 anti-cancer Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 230000001086 cytosolic effect Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 230000010437 erythropoiesis Effects 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 239000000833 heterodimer Substances 0.000 description 2
- 102000058223 human VEGFA Human genes 0.000 description 2
- 229960002474 hydralazine Drugs 0.000 description 2
- 238000003364 immunohistochemistry Methods 0.000 description 2
- 229940125396 insulin Drugs 0.000 description 2
- 229940068935 insulin-like growth factor 2 Drugs 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 108010082117 matrigel Proteins 0.000 description 2
- 238000000968 medical method and process Methods 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 230000006654 negative regulation of apoptotic process Effects 0.000 description 2
- YBYRMVIVWMBXKQ-UHFFFAOYSA-N phenylmethanesulfonyl fluoride Chemical compound FS(=O)(=O)CC1=CC=CC=C1 YBYRMVIVWMBXKQ-UHFFFAOYSA-N 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 230000009822 protein phosphorylation Effects 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 230000010282 redox signaling Effects 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 230000011664 signaling Effects 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 239000012096 transfection reagent Substances 0.000 description 2
- 230000005747 tumor angiogenesis Effects 0.000 description 2
- 230000006711 vascular endothelial growth factor production Effects 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- FDKWRPBBCBCIGA-REOHCLBHSA-N (2r)-2-azaniumyl-3-$l^{1}-selanylpropanoate Chemical compound [Se]C[C@H](N)C(O)=O FDKWRPBBCBCIGA-REOHCLBHSA-N 0.000 description 1
- GSKQMLGAUOTSKT-LBPRGKRZSA-N (2s)-2-azaniumyl-3-[4-[bis(2-chloroethyl)-oxidoazaniumyl]phenyl]propanoate Chemical compound OC(=O)[C@@H](N)CC1=CC=C([N+]([O-])(CCCl)CCCl)C=C1 GSKQMLGAUOTSKT-LBPRGKRZSA-N 0.000 description 1
- LOGFVTREOLYCPF-KXNHARMFSA-N (2s,3r)-2-[[(2r)-1-[(2s)-2,6-diaminohexanoyl]pyrrolidine-2-carbonyl]amino]-3-hydroxybutanoic acid Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)[C@H]1CCCN1C(=O)[C@@H](N)CCCCN LOGFVTREOLYCPF-KXNHARMFSA-N 0.000 description 1
- 108020004463 18S ribosomal RNA Proteins 0.000 description 1
- KPGXRSRHYNQIFN-UHFFFAOYSA-N 2-oxoglutaric acid Chemical compound OC(=O)CCC(=O)C(O)=O KPGXRSRHYNQIFN-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 102000003677 Aldehyde-Lyases Human genes 0.000 description 1
- 108090000072 Aldehyde-Lyases Proteins 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- ZHGNHOOVYPHPNJ-UHFFFAOYSA-N Amigdalin Chemical compound FC(F)(F)C(=O)OCC1OC(OCC2OC(OC(C#N)C3=CC=CC=C3)C(OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C2OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C1OC(=O)C(F)(F)F ZHGNHOOVYPHPNJ-UHFFFAOYSA-N 0.000 description 1
- 108010039627 Aprotinin Proteins 0.000 description 1
- 102100026189 Beta-galactosidase Human genes 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 229930188120 Carbomycin Natural products 0.000 description 1
- 101710150820 Cellular tumor antigen p53 Proteins 0.000 description 1
- 208000005590 Choroidal Neovascularization Diseases 0.000 description 1
- 206010060823 Choroidal neovascularisation Diseases 0.000 description 1
- 239000004971 Cross linker Substances 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- FDKWRPBBCBCIGA-UWTATZPHSA-N D-Selenocysteine Natural products [Se]C[C@@H](N)C(O)=O FDKWRPBBCBCIGA-UWTATZPHSA-N 0.000 description 1
- 102000003915 DNA Topoisomerases Human genes 0.000 description 1
- 108090000323 DNA Topoisomerases Proteins 0.000 description 1
- 230000033616 DNA repair Effects 0.000 description 1
- 102100037373 DNA-(apurinic or apyrimidinic site) endonuclease Human genes 0.000 description 1
- 101710109420 DNA-(apurinic or apyrimidinic site) endonuclease Proteins 0.000 description 1
- 230000004568 DNA-binding Effects 0.000 description 1
- 101710088194 Dehydrogenase Proteins 0.000 description 1
- 238000003718 Dual-Luciferase Reporter Assay System Methods 0.000 description 1
- 102000012199 E3 ubiquitin-protein ligase Mdm2 Human genes 0.000 description 1
- 108050002772 E3 ubiquitin-protein ligase Mdm2 Proteins 0.000 description 1
- 102100031780 Endonuclease Human genes 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 101800003838 Epidermal growth factor Proteins 0.000 description 1
- 102400001368 Epidermal growth factor Human genes 0.000 description 1
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 1
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 1
- 102000003983 Flavoproteins Human genes 0.000 description 1
- 108010057573 Flavoproteins Proteins 0.000 description 1
- 108700039691 Genetic Promoter Regions Proteins 0.000 description 1
- 108090000079 Glucocorticoid Receptors Proteins 0.000 description 1
- 102100033417 Glucocorticoid receptor Human genes 0.000 description 1
- 102000042092 Glucose transporter family Human genes 0.000 description 1
- 108091052347 Glucose transporter family Proteins 0.000 description 1
- 102000005548 Hexokinase Human genes 0.000 description 1
- 108700040460 Hexokinases Proteins 0.000 description 1
- 101000721661 Homo sapiens Cellular tumor antigen p53 Proteins 0.000 description 1
- 101001051777 Homo sapiens Protein kinase C alpha type Proteins 0.000 description 1
- 101000971468 Homo sapiens Protein kinase C zeta type Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 102000003777 Interleukin-1 beta Human genes 0.000 description 1
- 108090000193 Interleukin-1 beta Proteins 0.000 description 1
- 208000012659 Joint disease Diseases 0.000 description 1
- 108010059881 Lactase Proteins 0.000 description 1
- 241000254158 Lampyridae Species 0.000 description 1
- GDBQQVLCIARPGH-UHFFFAOYSA-N Leupeptin Natural products CC(C)CC(NC(C)=O)C(=O)NC(CC(C)C)C(=O)NC(C=O)CCCN=C(N)N GDBQQVLCIARPGH-UHFFFAOYSA-N 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 238000000134 MTT assay Methods 0.000 description 1
- 231100000002 MTT assay Toxicity 0.000 description 1
- 102100025169 Max-binding protein MNT Human genes 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 102000008109 Mixed Function Oxygenases Human genes 0.000 description 1
- 108010074633 Mixed Function Oxygenases Proteins 0.000 description 1
- 108010057466 NF-kappa B Proteins 0.000 description 1
- 102000003945 NF-kappa B Human genes 0.000 description 1
- 206010029113 Neovascularisation Diseases 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 102000043276 Oncogene Human genes 0.000 description 1
- 239000012828 PI3K inhibitor Substances 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 1
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 1
- 102100024924 Protein kinase C alpha type Human genes 0.000 description 1
- 102100021538 Protein kinase C zeta type Human genes 0.000 description 1
- 102000017332 Protein kinase C, delta Human genes 0.000 description 1
- 108050005326 Protein kinase C, delta Proteins 0.000 description 1
- 102000015840 Protein kinase C, epsilon Human genes 0.000 description 1
- 108050004067 Protein kinase C, epsilon Proteins 0.000 description 1
- 206010063837 Reperfusion injury Diseases 0.000 description 1
- 208000007135 Retinal Neovascularization Diseases 0.000 description 1
- 102000013275 Somatomedins Human genes 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 238000012233 TRIzol extraction Methods 0.000 description 1
- 102000046299 Transforming Growth Factor beta1 Human genes 0.000 description 1
- 101800002279 Transforming growth factor beta-1 Proteins 0.000 description 1
- 206010066901 Treatment failure Diseases 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 102000044209 Tumor Suppressor Genes Human genes 0.000 description 1
- 108700025716 Tumor Suppressor Genes Proteins 0.000 description 1
- 102000015098 Tumor Suppressor Protein p53 Human genes 0.000 description 1
- 108010078814 Tumor Suppressor Protein p53 Proteins 0.000 description 1
- 102000006108 VHL Human genes 0.000 description 1
- AEOBEOJCBAYXBA-KQYNXXCUSA-N [(2r,3r,4r,5r)-2-(6-aminopurin-9-yl)-4-hydroxy-5-(phosphonooxymethyl)oxolan-3-yl] dihydrogen phosphate Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@H]1OP(O)(O)=O AEOBEOJCBAYXBA-KQYNXXCUSA-N 0.000 description 1
- FQVHOULQCKDUCY-OGHXVOSASA-N [(2s,3s,4r,6s)-6-[(2r,3s,4r,5r,6s)-6-[[(1s,3r,7r,8s,9s,10r,12r,14e,16s)-7-acetyloxy-8-methoxy-3,12-dimethyl-5,13-dioxo-10-(2-oxoethyl)-4,17-dioxabicyclo[14.1.0]heptadec-14-en-9-yl]oxy]-4-(dimethylamino)-5-hydroxy-2-methyloxan-3-yl]oxy-4-hydroxy-2,4-dimeth Chemical class O([C@@H]1[C@@H](C)O[C@H]([C@@H]([C@H]1N(C)C)O)O[C@H]1[C@@H](CC=O)C[C@@H](C)C(=O)/C=C/[C@@H]2O[C@H]2C[C@@H](C)OC(=O)C[C@H]([C@@H]1OC)OC(C)=O)[C@H]1C[C@@](C)(O)[C@@H](OC(=O)CC(C)C)[C@H](C)O1 FQVHOULQCKDUCY-OGHXVOSASA-N 0.000 description 1
- 210000000683 abdominal cavity Anatomy 0.000 description 1
- 206010064930 age-related macular degeneration Diseases 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 229940041181 antineoplastic drug Drugs 0.000 description 1
- 229960004405 aprotinin Drugs 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 125000000613 asparagine group Chemical group N[C@@H](CC(N)=O)C(=O)* 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- 230000027455 binding Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- VSJKWCGYPAHWDS-FQEVSTJZSA-N camptothecin Chemical class C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-FQEVSTJZSA-N 0.000 description 1
- 230000005880 cancer cell killing Effects 0.000 description 1
- 229950005779 carbomycin Drugs 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000001516 cell proliferation assay Methods 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 230000018747 cellular response to hypoxia Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 230000003081 coactivator Effects 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 239000012531 culture fluid Substances 0.000 description 1
- RGWHQCVHVJXOKC-SHYZEUOFSA-J dCTP(4-) Chemical compound O=C1N=C(N)C=CN1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O)[C@@H](O)C1 RGWHQCVHVJXOKC-SHYZEUOFSA-J 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 230000037149 energy metabolism Effects 0.000 description 1
- 229940116977 epidermal growth factor Drugs 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 102000034356 gene-regulatory proteins Human genes 0.000 description 1
- 108091006104 gene-regulatory proteins Proteins 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 238000009650 gentamicin protection assay Methods 0.000 description 1
- 230000002414 glycolytic effect Effects 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 230000009422 growth inhibiting effect Effects 0.000 description 1
- 230000009036 growth inhibition Effects 0.000 description 1
- 239000003481 heat shock protein 90 inhibitor Substances 0.000 description 1
- 238000013537 high throughput screening Methods 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 230000033444 hydroxylation Effects 0.000 description 1
- 238000005805 hydroxylation reaction Methods 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 238000012744 immunostaining Methods 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- ZPNFWUPYTFPOJU-LPYSRVMUSA-N iniprol Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC=4C=CC=CC=4)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC=4C=CC=CC=4)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC2=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]2N(CCC2)C(=O)[C@@H](N)CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2[C@@H](CCC2)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N2[C@@H](CCC2)C(=O)N3)C(=O)NCC(=O)NCC(=O)N[C@@H](C)C(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H](C(=O)N1)C(C)C)[C@@H](C)O)[C@@H](C)CC)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZPNFWUPYTFPOJU-LPYSRVMUSA-N 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 230000002601 intratumoral effect Effects 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 229940116108 lactase Drugs 0.000 description 1
- GDBQQVLCIARPGH-ULQDDVLXSA-N leupeptin Chemical compound CC(C)C[C@H](NC(C)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C=O)CCCN=C(N)N GDBQQVLCIARPGH-ULQDDVLXSA-N 0.000 description 1
- 108010052968 leupeptin Proteins 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 208000002780 macular degeneration Diseases 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- HAWPXGHAZFHHAD-UHFFFAOYSA-N mechlorethamine Chemical class ClCCN(C)CCCl HAWPXGHAZFHHAD-UHFFFAOYSA-N 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 230000025308 nuclear transport Effects 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 208000028591 pheochromocytoma Diseases 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 229940043441 phosphoinositide 3-kinase inhibitor Drugs 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 229940075930 picrate Drugs 0.000 description 1
- OXNIZHLAWKMVMX-UHFFFAOYSA-M picrate anion Chemical compound [O-]C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O OXNIZHLAWKMVMX-UHFFFAOYSA-M 0.000 description 1
- 239000002574 poison Substances 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 230000001124 posttranscriptional effect Effects 0.000 description 1
- 230000001323 posttranslational effect Effects 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 238000002203 pretreatment Methods 0.000 description 1
- 125000001500 prolyl group Chemical group [H]N1C([H])(C(=O)[*])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000029983 protein stabilization Effects 0.000 description 1
- 230000004063 proteosomal degradation Effects 0.000 description 1
- 230000020874 response to hypoxia Effects 0.000 description 1
- 230000006335 response to radiation Effects 0.000 description 1
- 229940055619 selenocysteine Drugs 0.000 description 1
- ZKZBPNGNEQAJSX-UHFFFAOYSA-N selenocysteine Natural products [SeH]CC(N)C(O)=O ZKZBPNGNEQAJSX-UHFFFAOYSA-N 0.000 description 1
- 235000016491 selenocysteine Nutrition 0.000 description 1
- CMZUMMUJMWNLFH-UHFFFAOYSA-N sodium metavanadate Chemical compound [Na+].[O-][V](=O)=O CMZUMMUJMWNLFH-UHFFFAOYSA-N 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 108091006107 transcriptional repressors Proteins 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 229940099456 transforming growth factor beta 1 Drugs 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 230000005748 tumor development Effects 0.000 description 1
- 230000005909 tumor killing Effects 0.000 description 1
- 230000005751 tumor progression Effects 0.000 description 1
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 1
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000013585 weight reducing agent Substances 0.000 description 1
- 229940124024 weight reducing agent Drugs 0.000 description 1
- 229910000166 zirconium phosphate Inorganic materials 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6581—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus and nitrogen atoms with or without oxygen or sulfur atoms, as ring hetero atoms
- C07F9/6584—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus and nitrogen atoms with or without oxygen or sulfur atoms, as ring hetero atoms having one phosphorus atom as ring hetero atom
- C07F9/65842—Cyclic amide derivatives of acids of phosphorus, in which one nitrogen atom belongs to the ring
- C07F9/65846—Cyclic amide derivatives of acids of phosphorus, in which one nitrogen atom belongs to the ring the phosphorus atom being part of a six-membered ring which may be condensed with another ring system
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
細胞培養、及び低酸素処理
MCF−7ヒト乳癌細胞、及びHT−29大腸癌細胞は、the American Tissue Type Collectionから入手した。ヒト腎臓細胞癌RCC4細胞、及び野生型フォン・ヒッペル・リンドウ(VHL)遺伝子を形質移入したRCC4/VHLは、Dr.Peter Ratcliffeから入手した。細胞は、37℃で、湿度95%、空気5%のCO2インキュベーターにおいて、ダルベッコ変法イーグル培地(DMEM)に10%ウシ胎児血清、1mg/ml G418(RCC4及びRCC4/VHL細胞には適している)を添加した培地で培養した。低酸素にさらすために、培養フラスコを様々な時間、37℃で、5%CO2/74%N2/21%アルゴンを含有する混合ガスと共に湿度チェンバー内でインキュベートした。酸素レベルは、酸素センサー(製品番号:Ox110、Biospherix、レッドフィールド、ニューヨーク州)を用いてガス層において1%に保った。実験の最後で、細胞は氷冷リン酸緩衝液pH7.5(PBS)で2回洗浄した。VEGFレベルを測定するために、各フラスコからの1ml培養液を処理後取り除き、−80℃で貯蔵した。
増殖阻害アッセイは、3−[4,5−ジメチルチアゾール−2−イル]−2,5−ジフェニルテトラゾリウムブロマイド(MTT)アッセイを用いて以前記載されたように実行した。低酸素条件下での分析のため、プレートを薬剤存在下で1%酸素で16時間インキュベートし、次に20%酸素で72時間の残りの時間、インキュベートした。
約107細胞は、200μlの溶解バッファー(150mM NaCl、50mM Trisバッファー(pH7.5)、1mM フェニルメチルスルホニルフルオライド、2μg/ml アプロチニン、2μg/ml ロイペプチン、0.1mM バナジン酸ナトリウム、1% NP40、及び0.2% ドデシル硫酸ナトリウム(SDS))で1時間4℃で溶解した。溶解液は遠心分離(15分、4℃、10,000xg)し、上清を回収した。20μlの一定分量をタンパク質濃度の分析のために除去し、前記溶解液は必要になるまで−80℃で貯蔵した。細胞溶解液中のVEGFは、pg(VEGFタンパク質)/mg(総タンパク質)として表し、回収された培養液中のVEGFは、pg(VEGFタンパク質)/mg(同じフラスコからの細胞中で測定された総細胞タンパク質)で表した。細胞溶解液におけるヒトVEGFと、培養液に分泌されたVEGFの量は、製造元取り扱い説明書に従って、VEGF165及びVEGF121アイソフォームを測定するELISAキット(ヒトVEGF−ELISA;R&D Systems,ミネアポリス、ミネソタ州)を用いて決定した。血しょう中のマウスVEGFの量は、製造元取り扱い説明書に従って、マウスVEGF165及びVEGF121アイソフォームを測定するELISAキット(マウスVEGF−ELISA;R&D Systems)を用いて決定した。
核及び細胞質抽出物は、製造元取り扱い説明書に従って、NE−PER(登録商標)Nuclear and Cytoplasmic Extraction Reagentsを用いて調整した。ウェスタンブロッティング法は、マウス抗ヒトHIF−1α(1μg/ml);マウス抗ヒトHIF−1β(1μg/ml);マウス抗ヒトiNOS(5μg/ml);及びヤギ抗ヒトlamin A(0.5μg/ml)を用いて、以前記載したように実行した。抗マウス、若しくは抗ヤギ西洋ワサビペルオキシダーゼ−共役二次抗体は1:5000の希釈率で用い、化学発光によって検出され、ブロットはImageQuantソフトウェアを用いて定量した。
Trizol抽出法を用いて調製された15μg総RNAは、1.5%アガロース−ホルムアルデヒドゲルを用いた電気泳動によって分離され、ナイロンメンブレンに転写した。RNAは、Stratalinker UV クロスリンカーを用いてメンブレンにクロスリンク(架橋結合)した。ヒトHIF−1αに対する完全長プローブ(ランダムプライマー標識システム(Random Primers DNA Labeling System)を用いて[α−32P]dCTPでラベルされている)は、ULTRAhyb ハイブリダイゼーションバッファーを用いてメンブレンにハイブリダイズし、製造元プロトコールに従って洗浄工程を行った。ブロットはMD Storm 860ホスフォイメージャーを用いて画像化し、ImageQuantソフトウェアを用いて定量化した。18S rRNAに対する完全長cDNAプローブは、添加対照として用いた。
ホスホグリセリン酸キナーゼ(PGK)からの低酸素反応性因子(HRE)を含むpGL3ホタルルシフェラーゼ レポータープラスミドは、Dr.Ian Stratfordより寄贈された。プラスミドDNAは商業用キットを用いて調整した。空pGL3対照プラスミド、及び形質移入(トランスフェクション)効率に対する対象で用いられたプラスミドを含むpRL−CMV ウミシイタケルシフェラーゼは、Promegaから入手した。細胞は、製造元取扱説明書に従って、LipoTAXI mammalian transfection reagent(ほ乳類形質移入試薬:Stratagene、テキサス州)を用いて、5μgのHIF−1レポータープラスミド、若しくはpGL3対照プラスミド、及び0.025μgのpRL−CMV ウミシイタケルシフェラーゼプラスミド(形質移入効率のための対照として)で形質移入した。24時間後、細胞を以前に記載したように低酸素にさらした。ホタル及びウミシイタケルシフェラーゼ活性は、製造元取扱説明書に従って、Dual−Luciferase Reporter Assay System(デュアルルシフェラーゼレポートアッセイ系)を用いて測定した。
MFC−7及びMiaPaCa細胞(0.2mlマトリゲル中に107)をscidマウスの横腹に注入した。腫瘍が0.5gに到達した時、マウス(1グループに4匹)を100mg/kg PX−478若しくは溶媒対照を(腹腔内注入によって)処理した。4時間後、1mlの血液を各マウスから採取し、マウスは屠殺し、腫瘍を除去し、4%ホルムアルデヒド/PBSで固定し、パラフィンで包埋した。切片を、自動化免疫染色装置システムを用いてHIF−1α(10μg/ml)若しくはVEGF(7μg/ml)に対する抗体で染色した。HIF−1α染色の強度は、SimplePCIプログラムを用いて測定した。
総細胞溶解液は、VEGF ELISAで記載したように調整した。チオレドキシン還元酵素活性は、Berggenら(1999年)が記載したように測定した。簡潔には、0.2mlの一定分量の新鮮アデノシン2’,5’−二リン酸共役アガロースビーズ(ADPアガロース)(Sigma)を、0.2mlの一定分量の上清と1時間、4℃で混合し、内因性チオレドキシンと他の小分子量還元剤を除去した。前記ビーズは次に、2x1mlの、0.1M NaClで1000xgの再遠心分離によって洗浄し、チオレドキシン還元酵素は、0.5mlの1.0M KCLで溶出した。チオレドキシン還元酵素活性は次に、基質として5μM ヒトリコンビナントチオレドキシン、及び最終電子受容体として酸化型インシュリンを用いて、339nmでNADPHの酸化として測定した。活性は、上清タンパク質のミリグラム当たり、1分間に酸化されるナノモルNADPHとして表した。
ヒト乳癌MCF−7細胞(1マウス当たりマトリゲル中に107細胞)を、エストロゲンペレットを移植されたscidマウスの横腹に皮下的に注入した。腫瘍は0.5gまで成長した。次にマウスの腹腔内に、溶媒単独、若しくは120mg/kg PX−478を入れた。4時間後、腫瘍を切除し、ホルマリンで固定し、パラフィンで包埋した。切片は、自動化免疫染色装置システムを用いて、HIF−1α(10μg/mg;Transduction Labs)、若しくはVEGF(7μg/ml)に対する抗体で染色した。染色は、SimplePCI分析ソフトウェアを用いて定量化した。
PX−478は低酸素及び正常酸素圧で阻害作用を示す
ヒト乳癌MCF−7細胞及びヒト大腸癌HT−29細胞は、正常酸素圧(20%酸素)若しくは低酸素(1%酸素)条件下、様々な濃度のPX−278で、16時間処理した。次に細胞を薬剤を含まない温かい培地で3回洗浄し、72時間の残りの時間インキュベートした。次にMTTアッセイを行って、増殖阻害作用を決定した。データは、二組ずつ3回の実験から平均±SEで表した。PX−478は、低酸素(1%酸素)及び正常酸素圧(20%酸素)条件下で増殖阻害作用を示し(p=<0.01)、正常酸素圧条件下での増殖阻害作用に対して低酸素条件下の増殖阻害作用の比は、MCF−7で1.25、HT−20細胞で1.2であった。以下の表1は、これらの結果を示している;
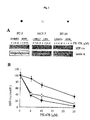
HIF−1αは、低酸素に対する細胞性反応の重要な調節要素である。従って我々は、PX−478のHIF−1αタンパク質レベルに対する影響を検討した。図2Aに示したように、PC−3前立腺癌細胞、MCF−7乳癌細胞、及びHT−29大腸癌細胞をPX−478存在下、低酸素(1%酸素)に16時間さらした。細胞核抽出物を調製し、HIF−1αタンパク質のレベルをウェスタンブロッティング法を用いて測定した。図2に示したように結果は、添加対照としてのlamin Aを含む典型的なウェスタンブロットを示した。図2において、MCF−7ヒト乳癌細胞及びHT−29ヒト大腸癌細胞は、PX−478存在下で正常酸素圧(20%酸素)若しくは低酸素(1%酸素)で16時間処理した。細胞核抽出物を調製し、HIF−1αとHIF−1βタンパク質のレベルをウェスタンブロッティング法を用いて測定した。ブロットは3回の実験の代表である。Lamin Aは、添加対照として用いた。データは、3回の実験の平均±S.E.で表し、(●)はPC−3前立腺癌細胞、(○)はMFC−7乳癌細胞、及び(▼)はHT−29ヒト大腸癌細胞を示している。図2Aに示されたように、PX−478は、ヒト乳癌細胞MCF−7(図2Aに示した)及びヒト大腸癌細胞HT−29(図2Bに示した)における低酸素(1%酸素)誘導性HIF−1αタンパク質を阻害し、各細胞のIC50値はそれぞれ3.5±2.0、及び17.8±5μMである。HIF−1αタンパク質レベルは、以前に報告されたように、正常酸素圧(20%酸素)下においては非常に低かったので、影響は見られなかった。しかしながら、正常酸素圧において検出可能なレベルのHIF−1αタンパク質を示したヒト膵臓癌PC−3細胞において、IC50値は2.5±1.2μMであった(図示せず)。この細胞株では、低酸素条件下でも同程度のIC50値が得られた(2.1±2.0μM)。
HIF−1トランス活性化は、PGKからのHREの複数コピーの制御下で、ルシフェラーゼをコンストラクト発現している一過性形質移入細胞によって測定した。図4Aは、MCF−7ヒト乳癌細胞、及び図4Bは、HT−29ヒト大腸癌(B)細胞を図示しており、各細胞は、様々な濃度のPX−478の存在下、正常酸素圧(20%酸素)若しくは低酸素(1%酸素)で16時間処理した。次にHIF−1トランス活性化は、PGKからのHREのいくつかのコピーの制御下で、コンストラクト発現しているホタルルシフェラーゼを用いて測定した。ウミシイタケルシフェラーゼは、形質移入効率の対照として同時形質移入した。データは、3回の実験の平均±SEで表した。*は、同条件下において、未処理対照から有意な変化があったことを示している(p=<0.001)。図4Bで示したように、HT−29細胞は、図4Aに示されたようなMCF−7細胞と比較して、HIF−1のトランス活性化の有意な増加が見られた(MCF−7細胞が10.1±1.9倍に対して、HT−29細胞13.9±1.5倍である)(p=<0.001)。しかしながら、PX−478は、10μM及び25μMのPX−478で16時間処理した後、両方の細胞株における低酸素誘導性のHIF−1トランス活性化を有意に減少した(p=<0.001)。低酸素誘導性トランス活性化の阻害に対するIC50値は、MCF−7細胞では20.5±1.4μM、HT−29細胞では23.1±1.8μMであった。HIF−1トランス活性化は、正常酸素圧下では非常に低く、両細胞株をPX−478で処理しても影響がなかった。
図5A及び5Bにそれぞれ示したように、MCF−7ヒト乳癌細胞及びHT−29ヒト大腸癌細胞を、PX−478存在下で、正常酸素圧(20%酸素:黒符号)若しくは低酸素(1%酸素:白符号)で16時間処理した。次に、丸で表示された細胞溶解液中のVEGFレベル、若しくは三角で表示された培養液中のVEGFレベルをELISAを用いて測定した。データは、3回の実験の平均±SEで表した。*は、同条件下(正常酸素圧、若しくは低酸素)で未処理対照から有意な差があることを示している(p=<0.001)。PX−478は、10μM PX−478で16時間処理した後、MCF−7細胞(図5A)及びHT−29細胞(図5B)の両方における低酸素誘導性VEGFタンパク質レベルを有意に減少した(p=<0.01)。IC50値は、MCF−7細胞及びHT−29細胞において、細胞溶解液中のVEGFに対してはそれぞれ17.1±4.0μM及び13.5±4.0μM、培養液中に分泌されたVEGFに対してはそれぞれ3.8±2.0μM及び11.5±2.5μMであった。培養液中に分泌されたVEGFのレベルは、MCF−7細胞において、10μM PX−478で処理した後、正常酸素圧レベルまで減少した。しかしながら、MCF−7細胞の細胞溶解液中のVEGFレベルだけでなく、HT−29の細胞溶解液と培養液中に分泌されたVEGFレベルは、25μM PX−478で処理した後も正常酸素圧レベルにまで戻らなかった。興味深いことに、PX−478は、両細胞株の正常酸素圧におけるVEGFレベルには影響を及ぼさなかった。
PX−478で細胞を処理した後、どのくらいの時間でHIF−1αタンパク質が阻害され続けるかを検討するために、図6に示したように、MCF−7細胞をPX−478で16時間処理し、次に薬剤を洗い流し、HIF−1αの回復を測定した。MCF−7ヒト乳癌細胞を16時間低酸素(1%酸素、H)にさらし、次に25μM PX−478に最大4時間まで処理した。細胞核抽出物は表示された時間で調製し、HIF−1αタンパク質のレベルを測定するためにウェスタンブロッティング法を行った。正常酸素圧(20%酸素、N)下で16時間処理した後のHIF−1αタンパク質のレベルも対照として示した。HIF−1αタンパク質レベルは薬剤の除去から4時間以内に処理前レベルにまで回復した。
MCF−7細胞をscidマウスの横腹で異種移植片として増殖した。異種移植片が0.3gに到達した時、マウスを溶媒対照若しくは100mg/kg PX−478(図7A及び7Bにそれぞれ図示した)で処理した。4時間後、腫瘍を除去し、ホルマリン固定し、パラフィン包埋し、HIF−1αタンパク質のレベルを免疫組織化学法を用いて測定した(A及びB)。(C)HIF−1α染色強度は、Simple PCIソフトウェアを用いて定量化した。*は、対照から有意な差があることを示している(p=<0.01)。データは、平均±SEで表した。図7A及び7Bに示したように、scidマウスの横腹で異種移植片として増殖したMCF−7細胞の処理によって、PX−478処理の4時間後、HIF−1αタンパク質のレベルが有意に減少した(p=<0.005)ことが示された。PX−478処理細胞中の局在化における染色残存核、及びHIF−1αのレベルは、図7Cに示された未処理対照と比較してPX−478処理マウスにおいて50%減少していた。
図8において、ヒト腎臓癌RCC4細胞及びRCC4/VHL細胞を、正常酸素圧(20%酸素)若しくは低酸素(1%酸素)条件下で、様々な濃度のPX−478で16時間処理した。図8Aは、HIF−1αタンパク質レベルを核抽出物中で測定した結果を示している。Lamin Aは添加対照として用いた。図8Bは、PGKからのHREの複数コピーの制御下で、コントラクト発現しているルシフェラーゼを用いてHIF−1トランス活性化を測定した結果を示している。ウミシイタケルシフェラーゼを形質移入効率を正確にするために同時形質移入した。データは、平均±SEで表した。*は、同条件下の未処理サンプルから有意な差があることを示している(p=<0.01)。VHL遺伝子を欠いたヒト腎臓癌細胞(RCC4)、及びVHL遺伝子が置換されているRCC4/VHL細胞は、PX−478によるHIF−1αの阻害メカニズムを検討するために用いた。RCC4細胞は、正常酸素圧下でも高レベルのHIF−1αタンパク質を発現しており、一方、RCC4/VHL細胞は、図8Aに示したように、正常酸素圧下で低レベルのHIF−1αタンパク質を発現していた。PX−478は、正常酸素圧(IC50=5.1±2.0μM)及び低酸素(IC50=16.9±1.9μM)の両方の条件下で、RCC4細胞中のHIF−1αタンパク質を阻害し、これはPX−478がVHL経路に非依存的にHIF−1αを減少することを示唆している。PX−478は、RCC4/VHL細胞中の低酸素誘導性HIF−1αも阻害し、IC50値は18.1±4.0μMであった。
我々の以前の研究によって、チオレドキシンを介したレドックスシグナル伝達の阻害は、HIF−1αタンパク質レベルを減少し、HIF−1下流標的であるVEGF及びiNOSのレベルの減少を導くHIF−1トランス活性化を減少することが可能であると示された。従って我々は、0若しくは10μM PX−478の存在下で、正常酸素圧(20%酸素、N)若しくは低酸素(1%酸素、H)で16時間さらしたHT−29細胞における、チオレドキシン還元酵素活性に対するPX−478の影響を検討した。細胞を溶解し、チオレドキシン還元酵素活性を測定した。*は、正常酸素条件下の未処理対照から有意な差があることを示している。BLDは以下のアッセイの検出限界を表示している。データは、二組ずつ少なくとも2回の実験から平均±SEで表した。10μM PX−478でのMFC−7細胞の処理は、正常酸素圧においてチオレドキシン還元酵素活性を40%も有意に減少した(p=<0.001)。低酸素でも同程度までチオレドキシン還元酵素活性を有意に減少したが、チオレドキシン還元酵素活性は、低酸素条件下での10μM PX−478での処理の後、アッセイの検出限界以下まで減少した。
本発明は、このような化合物を含む薬学的組成物にも関するものである。前記組成物は、薬学的に許容可能な担体、希釈剤、水溶液、アジュバンド、若しくは治療を必要とする患者を治療するために有用である別の化合物の1若しくはそれ以上と共に、このような化合物の1若しくはそれ以上を有するものである。適切な組成物は、静脈内注入として投与された前記化合物の1若しくはそれ以上を含む緩衝溶液も含む。本発明は、このような化合物の使用を有する医学的な治療方法を含む。前記方法は、放射線療法若しくは化学療法などの、特定な疾患を治療するために有用な他の治療方法と共にこのような化合物を用いる工程も有している。
Claims (9)
- 別の医薬品に加えた請求項1若しくは2の薬学的組成物。
- 請求項1若しくは2の薬学的組成物において、
前記化合物は、名称(S−2−アミノ−3−[4’−N,N,−ビス(2−クロロエチル)アミノ]フェニルプロピオン酸N−オキシドジヒドロクロライド)である。 - HIF−1αを阻害するための薬物を製造するための請求項1若しくは2の化合物の使用。
- 血管新生増殖を阻害するための薬物を製造するための請求項1若しくは2の化合物の使用。
- VEGF形成を阻害するための薬物を製造するための請求項1若しくは2の化合物の使用。
- 腫瘍形成を阻害するための薬物を製造するための請求項1若しくは2の化合物の使用。
- 正常酸素圧若しくは低酸素条件下で細胞を治療するための薬物の製造用の請求項1若しくは2の化合物の使用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/288,888 US20040087556A1 (en) | 2002-11-06 | 2002-11-06 | N-oxides and derivatives of melphalan for treating diseased states associated with hypoxia inducible factor |
| PCT/US2003/035226 WO2004043359A2 (en) | 2002-11-06 | 2003-11-03 | N-oxides and derivatives of melphalan for treating diseased states associated with hypoxia inducible factor |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006508124A true JP2006508124A (ja) | 2006-03-09 |
| JP2006508124A5 JP2006508124A5 (ja) | 2006-12-14 |
Family
ID=32175991
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004551738A Pending JP2006508124A (ja) | 2002-11-06 | 2003-11-03 | 低酸素誘導性因子に関連した病状を治療するためのメルファレンのn−オキシドと誘導体 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US20040087556A1 (ja) |
| EP (1) | EP1567476A4 (ja) |
| JP (1) | JP2006508124A (ja) |
| AU (1) | AU2003291282B2 (ja) |
| CA (1) | CA2504496C (ja) |
| MX (1) | MXPA05004845A (ja) |
| WO (1) | WO2004043359A2 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005007828A2 (en) * | 2003-07-14 | 2005-01-27 | Prolx Pharmaceuticals, Inc. | Regulation of hif protein levels via deubiquitination pathways |
| CA2720271A1 (en) * | 2008-02-15 | 2009-08-20 | Board Of Regents Of The University Of Texas System | Compositions and methods for treating lung cancer |
| WO2012058325A1 (en) * | 2010-10-29 | 2012-05-03 | Oncothyreon Inc. | Compounds and methods useful for treatment of diseases mediated by hif-1 |
| WO2012082765A2 (en) | 2010-12-16 | 2012-06-21 | The United State Of America. As Represented By The Secretary Department Of Health And Human Services | Methods for decreasing body weight and treating diabetes |
| SG11201606351VA (en) | 2014-02-03 | 2016-09-29 | Quadriga Biosciences Inc | Beta-substituted beta-amino acids and analogs as chemotherapeutic agents |
| BR112016017993A2 (pt) | 2014-02-03 | 2017-08-08 | Quadriga Biosciences Inc | Gama-aminoácidos beta-substituídos e análogos como agentes quimioterapêuticos |
| US10349839B2 (en) * | 2015-02-27 | 2019-07-16 | Biotronik Se & Co. | Implantable pressure sensor device |
| WO2017024009A1 (en) | 2015-08-03 | 2017-02-09 | Quadriga Biosciences, Inc. | Beta-substituted beta-amino acids and analogs as chemotherapeutic agents and uses thereof |
| WO2018160772A1 (en) | 2017-02-28 | 2018-09-07 | The United State Of America, As Represented By The Secretary, Department Of Health & Human Services | Method of treating obesity, insulin resistance, non-alcoholic fatty liver disease including non-alcoholic steatohepatitis |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5602278A (en) * | 1994-10-20 | 1997-02-11 | Kirkpatrick; Lynn | N-oxides and derivatives of chlorambucil for treating hypoxic tumor cells |
-
2002
- 2002-11-06 US US10/288,888 patent/US20040087556A1/en not_active Abandoned
-
2003
- 2003-11-03 AU AU2003291282A patent/AU2003291282B2/en not_active Ceased
- 2003-11-03 WO PCT/US2003/035226 patent/WO2004043359A2/en active Application Filing
- 2003-11-03 MX MXPA05004845A patent/MXPA05004845A/es active IP Right Grant
- 2003-11-03 CA CA2504496A patent/CA2504496C/en not_active Expired - Fee Related
- 2003-11-03 JP JP2004551738A patent/JP2006508124A/ja active Pending
- 2003-11-03 EP EP03768672A patent/EP1567476A4/en not_active Withdrawn
-
2004
- 2004-08-30 US US10/929,156 patent/US7399785B2/en not_active Expired - Fee Related
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5602278A (en) * | 1994-10-20 | 1997-02-11 | Kirkpatrick; Lynn | N-oxides and derivatives of chlorambucil for treating hypoxic tumor cells |
Also Published As
| Publication number | Publication date |
|---|---|
| MXPA05004845A (es) | 2005-10-05 |
| US20040087556A1 (en) | 2004-05-06 |
| US20050026872A1 (en) | 2005-02-03 |
| WO2004043359A3 (en) | 2004-09-10 |
| EP1567476A4 (en) | 2008-09-24 |
| WO2004043359B1 (en) | 2004-10-28 |
| EP1567476A2 (en) | 2005-08-31 |
| AU2003291282A1 (en) | 2004-06-03 |
| CA2504496A1 (en) | 2004-05-27 |
| AU2003291282B2 (en) | 2010-11-11 |
| WO2004043359A2 (en) | 2004-05-27 |
| US7399785B2 (en) | 2008-07-15 |
| CA2504496C (en) | 2010-05-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Wei et al. | Regulation of p53 tumor suppressor by Helicobacter pylori in gastric epithelial cells | |
| AU2021107577A4 (en) | Flavagline derivatives for inhibition of kras oncogene activation | |
| Yeo et al. | Amphotericin B blunts erythropoietin response to hypoxia by reinforcing FIH-mediated repression of HIF-1 | |
| HU229263B1 (en) | The use of pharmaceutical compositions containing 4-h-1-benzopyran-4-one derivatives as inhibitors of smooth muscle cell proliferation | |
| EP2178531A2 (en) | Methods, composition, targets for combinational cancer treatments | |
| US20200179284A1 (en) | Nanoliposomal c-MYC-siRNA Inhibits In Vivo Tumor Growth of Cisplatin-Resistant Ovarian Cancer | |
| Chen et al. | IL-6 signaling contributes to radioresistance of prostate cancer through key DNA repair-associated molecules ATM, ATR, and BRCA 1/2 | |
| CA2504496C (en) | N-oxides and derivatives of melphalan for treating diseased states associated with hypoxia inducible factor | |
| Ling et al. | E2F7 promotes mammalian target of rapamycin inhibitor resistance in hepatocellular carcinoma after liver transplantation | |
| WO2020146384A1 (en) | Organic compounds | |
| Paradziej-Łukowicz et al. | Anticancer imidazoacridinone C-1311 inhibits hypoxia-inducible factor-1α (HIF-1α), vascular endothelial growth factor (VEGF) and angiogenesis | |
| Wu et al. | Nuclear translocation of thioredoxin-1 promotes colorectal cancer development via modulation of the IL-6/STAT3 signaling axis through interaction with STAT3 | |
| Peng et al. | Mutation of TP53 confers ferroptosis resistance in lung cancer through the FOXM1/MEF2C axis | |
| JP2009544679A (ja) | 異常な細胞増殖に関連する疾患の治療におけるレチノイド及び小分子のNrf2アンタゴニストとしての使用 | |
| Matsuo et al. | Preventing the unfolded protein response via aberrant activation of 4E‐binding protein 1 by versipelostatin | |
| CN111671904A (zh) | 一种含有抑制核酸内切酶功能的药物及其抗肿瘤的用途 | |
| US20050049309A1 (en) | Regulation of HIF protein levels via deubiquitination pathway | |
| US20140235578A1 (en) | Methods for treating neoplasia and for identifying compositions useful in such therapy | |
| CN110665007A (zh) | 一种治疗癌症用组合药物及其用途 | |
| AU2019275453B2 (en) | Organic compounds | |
| WO2016090159A1 (en) | Compositions and methods relating to proliferative disorders | |
| Oak et al. | Curcumin mediates selective aggregation of mutant p53 in cancer cells: A promising therapeutic strategy | |
| Kalkur | The Role of TEADs1-4 in YAP/TAZ-Mediated Metastatic Melanoma | |
| WO2015073813A2 (en) | Compositions and methods for the treatment of diseases involving hippo pathway | |
| Lung | Thioredoxin-1 Modulates Transcription of Cyclooxygenase-2 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20061021 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061021 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100518 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100806 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100813 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101118 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110921 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20111210 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20111219 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120717 |