JP2005200302A - Metal-modified apatite and its manufacturing method - Google Patents
Metal-modified apatite and its manufacturing method Download PDFInfo
- Publication number
- JP2005200302A JP2005200302A JP2005070805A JP2005070805A JP2005200302A JP 2005200302 A JP2005200302 A JP 2005200302A JP 2005070805 A JP2005070805 A JP 2005070805A JP 2005070805 A JP2005070805 A JP 2005070805A JP 2005200302 A JP2005200302 A JP 2005200302A
- Authority
- JP
- Japan
- Prior art keywords
- metal
- apatite
- modified
- cahap
- present
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- VSIIXMUUUJUKCM-UHFFFAOYSA-D pentacalcium;fluoride;triphosphate Chemical class [F-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O VSIIXMUUUJUKCM-UHFFFAOYSA-D 0.000 title claims abstract description 70
- 238000004519 manufacturing process Methods 0.000 title claims description 11
- 229910052586 apatite Inorganic materials 0.000 claims abstract description 36
- 229910044991 metal oxide Inorganic materials 0.000 claims abstract description 22
- 150000004706 metal oxides Chemical class 0.000 claims abstract description 22
- 239000013078 crystal Substances 0.000 claims abstract description 17
- 238000005342 ion exchange Methods 0.000 claims abstract description 12
- 238000000975 co-precipitation Methods 0.000 claims abstract description 8
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical group [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 claims description 34
- 229910052751 metal Inorganic materials 0.000 claims description 25
- 239000002184 metal Substances 0.000 claims description 25
- 239000010936 titanium Substances 0.000 claims description 25
- 230000001699 photocatalysis Effects 0.000 claims description 20
- 229910021645 metal ion Inorganic materials 0.000 claims description 16
- 150000002500 ions Chemical class 0.000 claims description 9
- 239000000758 substrate Substances 0.000 claims description 7
- 229910052719 titanium Inorganic materials 0.000 claims description 4
- 239000000470 constituent Substances 0.000 claims description 3
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical group [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 claims description 2
- 238000000034 method Methods 0.000 abstract description 10
- 238000001179 sorption measurement Methods 0.000 abstract description 9
- 239000011941 photocatalyst Substances 0.000 abstract description 3
- 239000003054 catalyst Substances 0.000 abstract description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 25
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 25
- 239000000463 material Substances 0.000 description 23
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 14
- 239000010408 film Substances 0.000 description 12
- 239000002245 particle Substances 0.000 description 12
- 239000000126 substance Substances 0.000 description 12
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical class [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 10
- 239000001506 calcium phosphate Substances 0.000 description 9
- 239000011575 calcium Substances 0.000 description 8
- 239000007789 gas Substances 0.000 description 8
- 239000004065 semiconductor Substances 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 229910000389 calcium phosphate Inorganic materials 0.000 description 7
- 235000011010 calcium phosphates Nutrition 0.000 description 7
- 239000001569 carbon dioxide Substances 0.000 description 7
- 229910002092 carbon dioxide Inorganic materials 0.000 description 7
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical compound CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 description 6
- 238000000576 coating method Methods 0.000 description 6
- 239000005416 organic matter Substances 0.000 description 6
- 239000010409 thin film Substances 0.000 description 6
- 239000011248 coating agent Substances 0.000 description 5
- 239000002131 composite material Substances 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- -1 silver ions Chemical class 0.000 description 5
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 4
- 238000002441 X-ray diffraction Methods 0.000 description 4
- 125000004429 atom Chemical group 0.000 description 4
- ZCCIPPOKBCJFDN-UHFFFAOYSA-N calcium nitrate Chemical compound [Ca+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O ZCCIPPOKBCJFDN-UHFFFAOYSA-N 0.000 description 4
- 230000007613 environmental effect Effects 0.000 description 4
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 4
- 230000003287 optical effect Effects 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 239000007858 starting material Substances 0.000 description 4
- 238000005033 Fourier transform infrared spectroscopy Methods 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 230000003197 catalytic effect Effects 0.000 description 3
- 238000000354 decomposition reaction Methods 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 238000004817 gas chromatography Methods 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 3
- 238000006864 oxidative decomposition reaction Methods 0.000 description 3
- DCKVFVYPWDKYDN-UHFFFAOYSA-L oxygen(2-);titanium(4+);sulfate Chemical compound [O-2].[Ti+4].[O-]S([O-])(=O)=O DCKVFVYPWDKYDN-UHFFFAOYSA-L 0.000 description 3
- 239000000123 paper Substances 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 238000005211 surface analysis Methods 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 229910000348 titanium sulfate Inorganic materials 0.000 description 3
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- 229910014497 Ca10(PO4)6(OH)2 Inorganic materials 0.000 description 2
- 238000001157 Fourier transform infrared spectrum Methods 0.000 description 2
- 229910010413 TiO 2 Inorganic materials 0.000 description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 2
- 235000011114 ammonium hydroxide Nutrition 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 239000000919 ceramic Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 239000004745 nonwoven fabric Substances 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 235000019731 tricalcium phosphate Nutrition 0.000 description 2
- 229910000391 tricalcium phosphate Inorganic materials 0.000 description 2
- 229940078499 tricalcium phosphate Drugs 0.000 description 2
- 239000002759 woven fabric Substances 0.000 description 2
- 229910052726 zirconium Inorganic materials 0.000 description 2
- WUPHOULIZUERAE-UHFFFAOYSA-N 3-(oxolan-2-yl)propanoic acid Chemical compound OC(=O)CCC1CCCO1 WUPHOULIZUERAE-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical class [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- LCKIEQZJEYYRIY-UHFFFAOYSA-N Titanium ion Chemical compound [Ti+4] LCKIEQZJEYYRIY-UHFFFAOYSA-N 0.000 description 1
- 229910003089 Ti–OH Inorganic materials 0.000 description 1
- 238000004833 X-ray photoelectron spectroscopy Methods 0.000 description 1
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 230000000274 adsorptive effect Effects 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 239000003899 bactericide agent Substances 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 229910052796 boron Inorganic materials 0.000 description 1
- 229910052980 cadmium sulfide Inorganic materials 0.000 description 1
- FUFJGUQYACFECW-UHFFFAOYSA-L calcium hydrogenphosphate Chemical compound [Ca+2].OP([O-])([O-])=O FUFJGUQYACFECW-UHFFFAOYSA-L 0.000 description 1
- 229910001424 calcium ion Inorganic materials 0.000 description 1
- BRPQOXSCLDDYGP-UHFFFAOYSA-N calcium oxide Chemical compound [O-2].[Ca+2] BRPQOXSCLDDYGP-UHFFFAOYSA-N 0.000 description 1
- 239000000292 calcium oxide Substances 0.000 description 1
- ODINCKMPIJJUCX-UHFFFAOYSA-N calcium oxide Inorganic materials [Ca]=O ODINCKMPIJJUCX-UHFFFAOYSA-N 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 230000001877 deodorizing effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 235000019700 dicalcium phosphate Nutrition 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 229910052587 fluorapatite Inorganic materials 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 229910052746 lanthanum Inorganic materials 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000012567 medical material Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 150000002736 metal compounds Chemical class 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 235000019645 odor Nutrition 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 238000010525 oxidative degradation reaction Methods 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000002984 plastic foam Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 239000012890 simulated body fluid Substances 0.000 description 1
- 238000003980 solgel method Methods 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- MCQUVSSBBBZAKI-UHFFFAOYSA-B titanium(4+) tetraphosphate hydrate Chemical compound O.[Ti+4].[Ti+4].[Ti+4].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O MCQUVSSBBBZAKI-UHFFFAOYSA-B 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 239000002351 wastewater Substances 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
Images
Abstract
Description
本発明はアパタイトに関し、さらに詳しく述べると、アパタイトの奏する生体親和性及び吸着特性に加えて光触媒機能を発現することのできる、特にエレクトロニクスの分野において有用な金属修飾されたアパタイトに関する。本発明は、また、このような金属修飾アパタイトの製造方法に関する。 The present invention relates to apatite. More specifically, the present invention relates to a metal-modified apatite that can express a photocatalytic function in addition to the biocompatibility and adsorption characteristics exhibited by apatite, and is particularly useful in the field of electronics. The present invention also relates to a method for producing such metal-modified apatite.
酸化チタン等の半導体物質は、光触媒機能を奏することが知られている。すなわち、このような半導体物質では、価電子帯と伝導帯のバンドギャップに相当する波長の光エネルギーをそれが吸収すると、励起により価電子帯の電子が伝導帯に移り、価電子帯に正孔が発生する。伝導帯では、半導体物質の表面になんらかの物質(例えば有機物)が吸着せしめられているとして、それに移ってきた電子が半導体物質表面の有機物に移動してそれを還元し、また、価電子帯では、そこに発生した正孔が電子を奪い取り、有機物の酸化を行う。特に酸化チタンにおいては、価電子帯の正孔が非常に強い酸化力を有しているので、有機物を最終的には水と二酸化炭素に分解してしまう能力がある。このような酸化チタンの光触媒機能(酸化分解機能)を利用して、酸化チタン膜を抗菌剤、殺菌剤、脱臭剤、環境浄化剤などとして使用することが行われている。しかし、酸化チタンそのものは、なんらかの物質をその表面に吸着する特性を有していないので、得られる酸化分解機能には限界がある。 Semiconductor materials such as titanium oxide are known to exhibit a photocatalytic function. That is, in such a semiconductor material, when it absorbs light energy having a wavelength corresponding to the band gap between the valence band and the conduction band, excitation causes the electrons in the valence band to move to the conduction band, and holes in the valence band. Will occur. In the conduction band, it is assumed that some material (for example, organic matter) is adsorbed on the surface of the semiconductor material, and the electrons transferred to it move to the organic matter on the surface of the semiconductor material to reduce it. In the valence band, The holes generated there take the electrons and oxidize the organic matter. In particular, in titanium oxide, since holes in the valence band have a very strong oxidizing power, there is an ability to finally decompose organic matter into water and carbon dioxide. Utilizing such a photocatalytic function (oxidative decomposition function) of titanium oxide, a titanium oxide film has been used as an antibacterial agent, bactericidal agent, deodorizing agent, environmental purification agent, and the like. However, since titanium oxide itself does not have the property of adsorbing any substance on its surface, there is a limit to the oxidative decomposition function that can be obtained.
一方、カルシウムヒドロキシアパタイトCa10(PO4)6(OH)2(以下、CaHAPとも記す)は、歯や骨のような生体硬組織の主成分であり、さまざまなカチオンやアニオンとイオン交換しやく、したがって、高い生体親和性及び吸着特性を有している。カルシウムヒドロキシアパタイトは、したがって、人工歯根、人工骨、人工臓器などの医用材料を始めとして、クロマトグラフィ用吸着剤、化学センサ、イオン交換体、触媒など、幅広い分野への応用について研究が盛んに行われてきている。カルシウムヒドロキシアパタイトは、特に、蛋白質などの有機物を特異的に吸着する能力を有している。 On the other hand, calcium hydroxyapatite Ca 10 (PO 4 ) 6 (OH) 2 (hereinafter also referred to as CaHAP) is a main component of living hard tissues such as teeth and bones, and easily exchanges ions with various cations and anions. Therefore, it has high biocompatibility and adsorption properties. Therefore, calcium hydroxyapatite has been actively researched in a wide range of applications, including medical materials such as artificial tooth roots, artificial bones, and artificial organs, as well as chromatography adsorbents, chemical sensors, ion exchangers, and catalysts. It is coming. Calcium hydroxyapatite has an ability to specifically adsorb organic substances such as proteins.
最近では、酸化チタン等の半導体物質の電気的特性に着目して特にエレクトロニクスの分野での応用を意図したものではないが、上記したような2種類の物質、すなわち、酸化チタン等の半導体物質とCaHAP等の燐酸カルシウム系化合物を組み合わせて、両者の特性を効果的に引き出すことのできる製品の開発及び研究が行われている。 Recently, the electrical characteristics of semiconductor materials such as titanium oxide are not particularly intended for application in the field of electronics, but two types of materials as described above, namely, semiconductor materials such as titanium oxide and Development and research of products that can effectively bring out the characteristics of both by combining calcium phosphate compounds such as CaHAP have been carried out.
例えば、特許文献1には、抗菌性イオンとして少なくとも銀イオンを担持した難溶性燐酸塩(好ましくは、ヒドロキシアパタイト)の表面に、Ti、Zr又はZnの1種以上の金属化合物を被覆介在させたことを特徴とする抗菌剤が開示されている。また、特許文献2には、シート状に成形された基材(好ましくは、紙、織布、不織布又はプラスチックフォーム)中に、非晶質燐酸カルシウム(好ましくは、結晶水を含む燐酸三カルシウム)と光半導体組成物(好ましくは、酸化チタン、硫化カドミウム等)とを分散して含むか、さもなければそのような基材に非晶質燐酸カルシウムと光半導体組成物が接着剤を介して接着されていることを特徴とするフィルタが開示されている。
For example, in
より最近では、特許文献3において、活性炭、活性アルミナ、シリカゲル、ガラス、フォームセラミックス、フォームプラスチック等の基材を用意し、その基材の表面に酸化チタンからなる膜を形成するかもしくは酸化チタン粒子からなる基材を用意し、その酸化チタン膜又は酸化チタン粒子の表面に多孔質燐酸カルシウム(好ましくは、ヒドロキシアパタイト、弗化アパタイト等)をコートしたことを特徴とする環境浄化材料、具体的には悪臭の除去や空気中の有害物質又は汚れの分解除去、廃水処理、水の殺菌などを行うための材料が開示されている。このような環境浄化材料は、多孔質燐酸カルシウムの膜が生成しやすいように組成、pH等を調整した疑似体液中に、酸化チタン膜付きの基材又は酸化チタン粒子を浸漬することによって形成することができる。しかしながら、この環境浄化材料の場合には、酸化チタンの膜又は粒子の表面を燐酸カルシウムでコートした構造を有するので、そのコーティングがいかに多孔質であるとはいえ、下地となる酸化チタンにおいて満足し得るほどに十分に高い光触媒機能を発現させることができない。すなわち、十分な量の光が酸化チタンにとどかないので、酸化チタンは不活性なままであり、かえって酸化分解効率の低下を招くおそれがある。また、酸化チタンの上の燐酸カルシウムコーティングに吸着した有機物等も、そのコーティングのもつ吸着力の強さから、酸化チタンのところまで移動することなくそのコーティングの表面に留まっている可能性が高いので、光触媒による酸化分解を被ることがない。そうなると、いずれは吸着平衡に達するので、燐酸カルシウムコーティングの有機物等に対する吸着力が著しく低下することとなる。
More recently, in
本発明の目的は、上記したような従来の技術の現状に鑑みて、カルシウムヒドロキシアパタイトを始めとした各種のアパタイトの奏する触媒機能をさらに発展させて新規な触媒機能を発現させることができ、かつ、同時に、アパタイトに由来する、有機物等の特定の被吸着物質に対する優れた吸着特性を長期間にわたって維持することができる、特にエレクトロニクスの分野において有用な金属修飾されたアパタイトを提供することにある。 In view of the current state of the prior art as described above, the object of the present invention is to further develop the catalytic function exhibited by various apatites including calcium hydroxyapatite and to express a novel catalytic function, and At the same time, an object of the present invention is to provide a metal-modified apatite that is particularly useful in the field of electronics, which can maintain an excellent adsorption property for a specific adsorbed substance such as an organic substance derived from apatite over a long period of time.
本発明のもう1つの目的は、本発明による優れた金属修飾されたアパタイトを簡便にかつ高い信頼性をもって製造することのできる方法を提供することにある。 Another object of the present invention is to provide a method by which the excellent metal-modified apatite according to the present invention can be produced easily and with high reliability.
本発明者らは、このたび、カルシウムヒドロキシアパタイトを始めとしたアパタイトと光触媒作用を有する金属酸化物とを従来の技術とは異なる手法で複合化することによって、すなわち、アパタイト結晶中の金属イオン(例えば、カルシウムヒドロキシアパタイトの場合にはカルシウムイオン)の一部を光触媒作用を有する金属酸化物の金属イオン(例えば、酸化チタンの場合にはチタンイオン)とイオン交換することからなる原子レベルでの複合化技術によって、上記したような課題を解決し得るということを発見した。 The present inventors have recently synthesized apatite such as calcium hydroxyapatite and a metal oxide having a photocatalytic action by a method different from the conventional technique, that is, metal ions in the apatite crystal ( For example, a compound at the atomic level consisting of ion exchange of a part of a calcium oxide (in the case of calcium hydroxyapatite) with a metal ion of a metal oxide having a photocatalytic action (for example, titanium ion in the case of titanium oxide). It was discovered that the above-mentioned problems can be solved by using technology.
本発明は、その1つの面において、共沈法によって形成されたものであり、かつ光触媒作用を有する金属酸化物がアパタイト結晶構造中にイオン交換によって形成されていることを特徴とする金属修飾アパタイトにある。 One aspect of the present invention is a metal-modified apatite formed by a coprecipitation method, wherein a metal oxide having a photocatalytic action is formed by ion exchange in an apatite crystal structure. It is in.
本発明は、そのもう1つの面において、本発明の金属修飾アパタイトを製造するためのものであって、金属酸化物の所定量の金属イオンをあらかじめアパタイトの構成イオンに添加しておいて、両者の共存下において共沈法によって調製することを特徴とする金属修飾アパタイトの製造方法にある。 In another aspect of the present invention, the metal-modified apatite of the present invention is produced by adding a predetermined amount of metal ions of a metal oxide to constituent ions of the apatite. In the method for producing metal-modified apatite, it is prepared by coprecipitation in the presence of
以下の説明から理解されるように、本発明によれば、カルシウムヒドロキシアパタイトを始めとした各種のアパタイトの奏する触媒機能をさらに発展させて新規な光触媒機能を発現させることができ、かつ、同時に、アパタイトに由来する、有機物等の特定の被吸着物質に対する優れた特異的吸着特性を長期間にわたって維持することができる金属修飾されたアパタイトを提供することができる。また、本発明によれば、本発明による優れた金属修飾されたアパタイトを簡便にかつ高い信頼性をもって製造することのできる方法も提供することができる。 As will be understood from the following description, according to the present invention, it is possible to further develop the catalytic function exhibited by various apatites including calcium hydroxyapatite to express a novel photocatalytic function, and at the same time, It is possible to provide a metal-modified apatite that can maintain an excellent specific adsorption property for a specific adsorbed substance such as an organic substance derived from apatite over a long period of time. Further, according to the present invention, it is also possible to provide a method by which the excellent metal-modified apatite according to the present invention can be produced simply and with high reliability.
本発明による金属修飾アパタイト及びその製造方法は、その好ましい実施の形態に関して説明すると、次の通りである。なお、本発明は下記の実施の形態に限定されるものではないことを理解されたい。 The metal-modified apatite and the method for producing the metal-modified apatite according to the present invention will be described as follows with respect to preferred embodiments thereof. It should be understood that the present invention is not limited to the following embodiments.
本発明による金属修飾されたアパタイトにおいて、その主体を構成するアパタイトは、基本的に、次のような一般式によって表すことができる。
Ax(BOy)zX
In the metal-modified apatite according to the present invention, the apatite constituting the main body can basically be represented by the following general formula.
A x (BO y ) z X
上式において、Aは、Ca、Co、Ni、Cu、Al、La、Cr、Fe、Mgなどの各種の金属原子を表し、Bは、P、Sなどの原子を表し、そしてXは、水酸基(−OH)、ハロゲン原子(例えば、F、Cl)などである。このようなアパタイトの例としては、以下に列挙するものに限定されるわけではないけれども、アパタイト、ヒドロキシアパタイト、フルオロアパタイト、クロロアパタイト、燐酸三カルシウム、燐酸水素カルシウムなどである。本発明の実施において好適に用いることのできるアパタイトは、上式中のXが水酸基であるヒドロキシアパタイトであり、さらに好ましくは、上式中のXが水酸基でありかつAがカルシウム(Ca)であるカルシウムヒドロキシアパタイト(CaHAP)、すなわち、Ca10(PO4)6(OH)2である。したがって、以下における本発明のアパタイトの説明は、特にCaHAPを参照して説明することにする。 In the above formula, A represents various metal atoms such as Ca, Co, Ni, Cu, Al, La, Cr, Fe, and Mg, B represents an atom such as P and S, and X represents a hydroxyl group. (—OH), a halogen atom (for example, F, Cl) and the like. Examples of such apatite include, but are not limited to, apatite, hydroxyapatite, fluoroapatite, chloroapatite, tricalcium phosphate, and calcium hydrogen phosphate. The apatite that can be suitably used in the practice of the present invention is hydroxyapatite in which X in the above formula is a hydroxyl group, and more preferably, X in the above formula is a hydroxyl group and A is calcium (Ca). Calcium hydroxyapatite (CaHAP), that is, Ca 10 (PO 4 ) 6 (OH) 2 . Therefore, the following description of the apatite of the present invention will be described with reference to CaHAP.
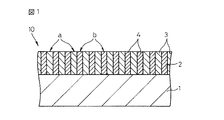
本発明の金属修飾アパタイトでは、アパタイトと光触媒作用を有する金属酸化物とを共沈法により原子レベルで複合化することによって、アパタイト結晶中の金属イオンの一部を光触媒作用を有する金属酸化物の金属イオンとイオン交換したことが特徴とする。これにより、図1に模式的に示すように、有機物等の特定の被吸着物質(図示せず)の吸着サイトaであるアパタイト領域3と光触媒作用に依存した被吸着物質分解サイトbである金属酸化物領域4とが、同一結晶面上において原子レベルのスケールで混在することができ、したがって、被吸着物質の吸着と分解が同時にかつ均一に効率的に行われる。また、本発明で採用されている共沈法に基づくイオン交換法は、先に参照した従来技術で採用されているゾル−ゲル法による酸化チタン膜の作製では、光触媒活性を示す酸化チタンの結晶構造となすために、500℃近傍の高温度における熱処理が必要であるのとは対照的に、熱処理が不要であり、光触媒活性を示す金属酸化物の結晶構造が形成されていないにもかかわらず、優れた光触媒活性を具現することができる。
In the metal-modified apatite of the present invention, apatite and a metal oxide having a photocatalytic action are combined at the atomic level by a coprecipitation method, whereby a part of the metal ions in the apatite crystal is converted into a metal oxide having a photocatalytic action. It is characterized by ion exchange with metal ions. Thereby, as schematically shown in FIG. 1, the
図1では、金属修飾アパタイト2を基材1の上に薄膜で形成した高機能複合材料10の例が示されているが、本発明の実施の形態はこれのみに限定されるものではない。すなわち、以下においても説明するけれども、本発明の金属修飾アパタイトは基材を有していなくてもよく、あるいは、金属修飾アパタイトの薄膜やフィルム、シート等を作製する時にのみ一時的に使用して、それらの作製が完了した後に取り除いてもよい。
Although FIG. 1 shows an example of the high-functional
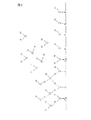
また、本発明の金属修飾アパタイトにおいて、アパタイト領域と金属酸化物領域とが同一結晶面上において原子レベルのスケールで混在することは、特にTiイオン交換CaHAPの表面構造モデルを示す図2から容易に理解することができるであろう。 Further, in the metal-modified apatite of the present invention, it is easy to mix the apatite region and the metal oxide region at the atomic level on the same crystal plane, particularly from FIG. 2 showing the surface structure model of Ti ion-exchanged CaHAP. Will be able to understand.
本発明に従いアパタイト結晶中の金属イオンの一部を光触媒作用を有する金属酸化物の金属イオンとイオン交換する場合に、光触媒作用を有する金属酸化物としては、この技術分野において有用性が知られている各種の金属酸化物を使用することができるが、好ましくは、チタン、ジルコニウム、鉄、タングステンなどの金属の酸化物を使用することができ、さらに好ましくは、チタンの酸化物、すなわち、TiO2を使用することができる。したがって、以下の説明においては、特にTiO2の使用を参照して本発明を説明する。 According to the present invention, when a part of metal ions in an apatite crystal is ion-exchanged with a metal ion of a metal oxide having a photocatalytic action, the metal oxide having a photocatalytic action is known to be useful in this technical field. Various metal oxides can be used, but preferably, metal oxides such as titanium, zirconium, iron, and tungsten can be used, and more preferably titanium oxide, that is, TiO 2. Can be used. Therefore, in the following description, the present invention will be described with particular reference to the use of TiO 2 .
本発明者らの知見によると、金属酸化物を使用してイオン交換を行う場合、その金属酸化物の金属イオンの含有量は、所望とする結果に応じて広く変更することができるというものの、通常、アパタイト結晶中の金属イオンとの比で、最高で15モル%であり、15モル%を上回ってもより顕著な効果を期待することができない。金属イオンの含有量は、Caイオン等の金属イオン比で一般的には3〜11モル%の範囲であることが好ましく、10モル%前後あるいはそれ以下であることが最も好ましい。 According to the knowledge of the present inventors, when ion exchange is performed using a metal oxide, the metal ion content of the metal oxide can be widely changed depending on the desired result, Usually, the ratio to the metal ion in the apatite crystal is 15 mol% at the maximum, and even if it exceeds 15 mol%, a more remarkable effect cannot be expected. The content of metal ions is generally preferably in the range of 3 to 11 mol% in terms of the ratio of metal ions such as Ca ions, and most preferably around 10 mol% or less.
本発明の金属修飾アパタイトは、その使途や、製造条件、その他のファクタに応じていろいろな形状及び寸法で提供することができる。適当な形状としては、例えば、粒子、タブレット、ロッド、プレート、ブロック、シート、フィルム、薄膜などを挙げることができる。また、このアパタイトが、シート、フィルム、薄膜などの場合、それらの材料は、単独で使用されてもよく、さもなければ、高機能複合構造体を構成するために、基材と組み合わせて、特に基材の片面又は両面に被覆した形で、使用されてもよい。ここで使用する基材としては、以下に列挙するものに限定されるわけではないけれども、例えば、紙(合成紙等も含む)、織布又は不織布、木材、ガラス、金属、セラミックス、プラスチック等の各種の材料の箔、フィルム、シート、板など、その他を挙げることができる。これらの基材は、必要に応じて、多孔質であってもよい。本発明の金属修飾アパタイトは、特に、基材の表面に薄膜として成膜された形で有利に使用することができる。 The metal-modified apatite of the present invention can be provided in various shapes and dimensions depending on its use, production conditions, and other factors. Suitable shapes include, for example, particles, tablets, rods, plates, blocks, sheets, films, thin films and the like. In addition, when this apatite is a sheet, a film, a thin film, etc., those materials may be used alone, or in combination with a base material in order to constitute a highly functional composite structure, You may use it in the form coat | covered on the single side | surface or both surfaces of the base material. The substrate used here is not limited to those listed below, but for example, paper (including synthetic paper), woven or non-woven fabric, wood, glass, metal, ceramics, plastic, etc. Other examples include foils, films, sheets, and plates of various materials. These substrates may be porous as necessary. The metal-modified apatite of the present invention can be advantageously used particularly in the form of a thin film formed on the surface of the substrate.
以上に説明したような、金属酸化物がアパタイト結晶構造中に形成されていることを特徴とする本発明の金属修飾アパタイトは、有利には、金属酸化物の所定量の金属イオン、すなわち、その出発原料をあらかじめアパタイトの構成イオン、すなわち、その出発原料に添加しておいて、両者の共存下において共沈法によって合成することができる。 As described above, the metal-modified apatite of the present invention characterized in that the metal oxide is formed in the apatite crystal structure is preferably a predetermined amount of metal ions of the metal oxide, that is, its The starting material can be added in advance to the constituent ions of apatite, that is, the starting material, and synthesized by coprecipitation in the presence of both.
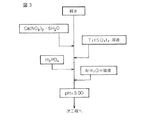
この本発明による金属修飾アパタイトの製造方法は、特にTiイオン交換CaHAPの製造工程の前半部分を示す図3から容易に理解することができるであろう。すなわち:
脱炭酸ガス処理をした純水に、CaHAPの出発原料、すなわち、硝酸カルシウムと、酸化チタンの出発原料、すなわち、硫酸チタンの溶液を所定量で混合する。この場合の所定量とは、好ましくは、それをXmetalとした場合、Xmetal=Ti/(Ti+Ca)=0.03〜0.11(モル比)となるような量である。なお、この規定は交換される金属原子がTiで、アパタイトの金属原子(先に一般式で示したアパタイトのAに相当)がCaである場合について示してあるが、本発明の実施において可能なその他の金属の組み合わせにもこの規定が有効である。また、Ti等の金属とCa等の金属の合計濃度は、0.1モルになるように調整するのが好ましい。次いで、得られた混合物に燐酸を添加し、さらにアンモニア水を添加してpHを調整する。このときのpHは、約9であることが好ましい。引き続いて、得られた懸濁液を、好ましくは100℃で6時間にわたってエージングし、さらにろ過する。ろ別した沈殿を純水で洗浄し、さらに乾燥すると、目的とするTiイオン交換CaHAPを得ることができる。これは、そのままで使用してもよく、あるいは適当な基材にスピンコートなどの塗布法、スパッタリングなどの蒸着法、その他の手法に従って適用して薄膜の形態となした後に使用してもよい。
The method for producing the metal-modified apatite according to the present invention can be easily understood from FIG. Ie:
A predetermined amount of a starting material of CaHAP, that is, calcium nitrate, and a starting material of titanium oxide, that is, titanium sulfate, is mixed with the decarbonized pure water. The the predetermined amount when, preferably, an amount such case, the X metal = Ti / (Ti + Ca) = 0.03~0.11 ( molar ratio) that it was the X metal. Although this rule is shown for the case where the metal atom to be exchanged is Ti and the metal atom of the apatite (corresponding to A of the apatite previously shown in the general formula) is Ca, this is possible in the practice of the present invention. This rule is effective for other metal combinations. Further, the total concentration of the metal such as Ti and the metal such as Ca is preferably adjusted to be 0.1 mol. Next, phosphoric acid is added to the resulting mixture, and ammonia water is further added to adjust the pH. The pH at this time is preferably about 9. Subsequently, the resulting suspension is preferably aged at 100 ° C. for 6 hours and further filtered. When the precipitate separated by filtration is washed with pure water and further dried, the target Ti ion-exchanged CaHAP can be obtained. This may be used as it is, or may be used after it is applied to an appropriate substrate according to a coating method such as spin coating, a vapor deposition method such as sputtering, or other methods to form a thin film.
本発明による金属修飾アパタイトは、特にエレクトロニクスの分野において有用であり、具体的には、レストランや公共の施設などに設置される表示デバイス、例えばPDPなどにおいて使用し、セルフクリーニング効果によりメンテナンスフリーとすることができる。また、コンピュータの周辺機器、例えばキーボード、マウス、筐体などに使用して、手垢などの汚れの付着を防止することができる。さらに、タッチパネル、プリンタなどの内部で使用されている光学部品(ミラー、レンズ等)に使用して、光学部品に付着した汚れに原因する光量減衰を抑制することができる。 The metal-modified apatite according to the present invention is particularly useful in the field of electronics. Specifically, the metal-modified apatite is used in a display device such as a PDP installed in a restaurant or public facility, and is maintenance-free due to a self-cleaning effect. be able to. Further, it can be used for peripheral devices of a computer, such as a keyboard, a mouse, a housing, and the like, to prevent adhesion of dirt such as hand dust. Furthermore, it can be used for optical components (mirrors, lenses, etc.) used inside touch panels, printers, etc., and light intensity attenuation caused by dirt attached to the optical components can be suppressed.
以下、本発明のその実施例を参照して説明する。なお、本発明は下記の実施例に限定されるものではないことを理解されたい。 The present invention will be described below with reference to the embodiments thereof. It should be understood that the present invention is not limited to the following examples.
例1
Tiイオン交換CaHAPの調製
1リットル(L)の脱炭酸ガス処理をした純水を用意し、窒素雰囲気下、その純水に対して0.1モルの硝酸カルシウムと、異なる量の硫酸チタン溶液を混合し、攪拌した。この場合の硫酸チタンの添加量は、得られる複合材料におけるTi量の影響を調べるため、Xmetal=Ti/(Ti+Ca)が0、0.01、0.03、0.1、0.5及び0.8(モル比)となるように変更した。また、TiとCa合計濃度は0.1モルであった。次いで、得られた混合物に0.06モルの燐酸を添加し、さらに15モル/Lのアンモニア水を添加してpHを9.00となるように調整した。引き続いて、得られた懸濁液をテフロンTM瓶に移し、100℃で6時間にわたってエージングを行った。沈殿が生成した懸濁液をろ過し、分別した沈殿を5Lの純水で洗浄し、さらに70℃のドライオーブン中で12時間にわたって乾燥した。Tiイオン交換なしのCaHAP(以下、CaHAPとも記す)とTiイオン交換されたCaHAP(以下、Ti−CaHAPとも記す)が得られた。
Example 1
Preparation of Ti ion-exchanged
例2
CaHAP及びTi−CaHAPのキャラクタリゼーション
前記例1で調製したCaHAP及びTi−CaHAPを試料として使用して、TEM、XRD、XPS及びFT−IRの各項目についてキャラクタリゼーションを行った。以下に、その結果を説明する。
Example 2
Characterization of CaHAP and Ti-CaHAP Using the CaHAP and Ti-CaHAP prepared in Example 1 as samples, TEM, XRD, XPS, and FT-IR were characterized. The results will be described below.
(1)結晶形態の観察
それぞれの試料の形態をJEOL社製の透過型電子顕微鏡(TEM)を使用して観察した。Ti添加量、すなわち、Xmetalが0.1までの試料は均一な粒子からなることが確認され、また、Ti添加量の増加にともない、HAPの結晶構造が保持されつつ、その形態が楕円形から針状へと変化していることが確認された。さらに、Xmetalが0.1を越えると、HAPの棒状巨大粒子と燐酸チタン水和物と思われる不定形粒子がそれぞれ生成することが明らかとなった。
(1) Observation of crystal form The form of each sample was observed using a transmission electron microscope (TEM) manufactured by JEOL. It was confirmed that samples with Ti addition amount, that is, X metal up to 0.1 consist of uniform particles, and as the Ti addition amount increased, the crystal structure of HAP was maintained and its shape was elliptical. It was confirmed that the shape changed from needle to needle. Furthermore, when X metal exceeds 0.1, it has been clarified that HAP rod-like giant particles and amorphous particles considered to be titanium phosphate hydrate are produced.
(2)結晶性の評価
それぞれの試料の結晶性をXRD(X線回折)によりより評価した。その結果、図4のグラフに示したように、Ti添加量の増加にともない結晶性が低下していることが確認された。
(2) Evaluation of crystallinity The crystallinity of each sample was further evaluated by XRD (X-ray diffraction). As a result, as shown in the graph of FIG. 4, it was confirmed that the crystallinity was lowered as the Ti addition amount increased.
(3)表面分析
それぞれの試料のXPSによる表面分析(パーキンエルマー社製の光電子分光装置を使用)及びFT−IRによる表面分析(パーキンエルマー社製のFT−IR装置を使用)から、Tiイオンは粒子内部に多く存在するが、Xmetal=0.1では一部の粒子の表面においてTi−OHとして存在することが明らかとなった。図5は、それぞれの試料のFT−IRスペクトルを示したグラフである。
(3) Surface analysis From the surface analysis of each sample by XPS (using a PerkinElmer photoelectron spectrometer) and the surface analysis by FT-IR (using a PerkinElmer FT-IR apparatus), Ti ions are Although it exists a lot in the inside of the particle, it became clear that X metal = 0.1 exists as Ti—OH on the surface of some particles. FIG. 5 is a graph showing the FT-IR spectrum of each sample.
以上のような評価結果から、Xmetal=0.1近傍までの試料においてHAP中へのTiのイオン交換が有効に可能であることが明らかになった。また、この結論は、本例で特に確認したTi−CaHAPはもちろんのこと、本発明の範囲に含まれる他の金属修飾アパタイトに対しても同様に適用し得ることが明らかである。 From the evaluation results as described above, it has been clarified that Ti ion exchange into HAP can be effectively performed in samples up to about X metal = 0.1. Moreover, it is clear that this conclusion can be similarly applied not only to Ti—CaHAP particularly confirmed in this example, but also to other metal-modified apatites included in the scope of the present invention.
例3
光触媒活性の評価
前記例1で調製したCaHAP(Xmetal=0)及びTi−CaHAP(Xmetal=0.1)をそれぞれ同じ比表面積を有するタブレットに加圧成形して試料として使用した。合成空気で置換した密封デシケータを用意し、試料とアセトアルデヒド(CH3CHO)蒸気を気相濃度が200ppm になるまで導入した。次いで、デシケータの上方から光量2.12mWの紫外線光を24時間にわたって照射し、その後、24時間の間隔をあけて同一光量の紫外線光を24時間にわたって照射した。デシケータ中におけるアセトアルデヒドガス及びその分解により発生した炭酸ガス(CO2)の濃度をガスクロマトグラフィにより測定したところ、CaHAP(Xmetal=0)からなる試料については図6にプロットするような結果が、また、Ti−CaHAP(Xmetal=0.1)からなる試料については図7にプロットするような結果がそれぞれ得られた。なお、それぞれの図において、曲線I及び曲線IIは、それぞれ、アセトアルデヒドガス及び炭酸ガスの濃度を示し、また、ON及びOFFは、それぞれ、紫外線光の照射及び照射停止のタイミングを示す。
Example 3
Evaluation of photocatalytic activity CaHAP (X metal = 0) and Ti-CaHAP (X metal = 0.1) prepared in Example 1 were respectively molded into tablets having the same specific surface area and used as samples. A sealed desiccator substituted with synthetic air was prepared, and a sample and acetaldehyde (CH 3 CHO) vapor were introduced until the gas phase concentration reached 200 ppm. Next, ultraviolet light having a light quantity of 2.12 mW was irradiated for 24 hours from above the desiccator, and thereafter, ultraviolet light having the same light quantity was irradiated for 24 hours at intervals of 24 hours. The concentration of acetaldehyde gas in the desiccator and the concentration of carbon dioxide gas (CO 2 ) generated by the decomposition thereof were measured by gas chromatography. As a result, the result plotted in FIG. 6 was obtained for a sample composed of CaHAP (X metal = 0). For the sample made of Ti-CaHAP (X metal = 0.1), the results plotted in FIG. 7 were obtained. In each figure, curve I and curve II indicate the concentrations of acetaldehyde gas and carbon dioxide gas, respectively, and ON and OFF indicate the timing of irradiation with ultraviolet light and irradiation stop, respectively.
図6及び図7にプロットした結果から理解されるように、比較例であるCaHAP(Xmetal=0)からなる試料の場合には紫外線光の照射による炭酸ガスの濃度の増加はほとんど認めることができなかった。なお、1回目の紫外線光の照射により炭酸ガスの濃度の若干の増加があったが、これは、2回目の紫外線光の照射によっても変化がないことから、試料中に最初から吸着されていた炭酸ガスに由来するものと理解される。これに対して、本発明例であるTi−CaHAP(Xmetal=0.1)からなる試料の場合、紫外線光の照射の都度に炭酸ガスの濃度の顕著な増加があり、優れた光触媒活性を有することが明らかとなった。 As understood from the results plotted in FIG. 6 and FIG. 7, in the case of a sample made of CaHAP (X metal = 0) as a comparative example, an increase in the concentration of carbon dioxide gas due to irradiation with ultraviolet light is almost recognized. could not. Although the carbon dioxide concentration was slightly increased by the first irradiation with ultraviolet light, it was adsorbed in the sample from the beginning because there was no change even with the second irradiation with ultraviolet light. It is understood that it is derived from carbon dioxide. On the other hand, in the case of a sample made of Ti-CaHAP (X metal = 0.1) which is an example of the present invention, there is a significant increase in the concentration of carbon dioxide gas with each irradiation of ultraviolet light, and excellent photocatalytic activity is achieved. It became clear to have.
1 基材
2 金属修飾アパタイト膜
3 アパタイト領域
4 金属酸化物領域
10 高機能複合材料
DESCRIPTION OF
Claims (6)
前記金属酸化物の所定量の金属イオンをあらかじめ前記アパタイトの構成イオンに添加しておいて、両者の共存下において共沈法によって調製することを特徴とする金属修飾アパタイトの製造方法。 A method for producing a metal-modified apatite in which a metal oxide having a photocatalytic action is formed in an apatite crystal structure,
A method for producing metal-modified apatite, wherein a predetermined amount of metal ions of the metal oxide is previously added to constituent ions of the apatite, and is prepared by coprecipitation in the presence of both.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005070805A JP4224598B2 (en) | 2005-03-14 | 2005-03-14 | Metal-modified apatite and method for producing the same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005070805A JP4224598B2 (en) | 2005-03-14 | 2005-03-14 | Metal-modified apatite and method for producing the same |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP14193199A Division JP3678606B2 (en) | 1999-05-21 | 1999-05-21 | Metal-modified apatite and method for producing the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005200302A true JP2005200302A (en) | 2005-07-28 |
| JP4224598B2 JP4224598B2 (en) | 2009-02-18 |
Family
ID=34824849
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005070805A Expired - Lifetime JP4224598B2 (en) | 2005-03-14 | 2005-03-14 | Metal-modified apatite and method for producing the same |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4224598B2 (en) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007262621A (en) * | 2006-03-29 | 2007-10-11 | Fujitsu Ltd | Fiber having photocatalytic ability, cloth using the fiber, and cloth product using the cloth |
| JP2012198874A (en) * | 2011-03-09 | 2012-10-18 | Fujitsu Ltd | Paper sheet storage device, stacker, adhered substance removal method, and program |
| WO2020003464A1 (en) | 2018-06-28 | 2020-01-02 | 富士通株式会社 | Photocatalyst, gas sensor device, gas sensor, and measuring method |
-
2005
- 2005-03-14 JP JP2005070805A patent/JP4224598B2/en not_active Expired - Lifetime
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007262621A (en) * | 2006-03-29 | 2007-10-11 | Fujitsu Ltd | Fiber having photocatalytic ability, cloth using the fiber, and cloth product using the cloth |
| JP2012198874A (en) * | 2011-03-09 | 2012-10-18 | Fujitsu Ltd | Paper sheet storage device, stacker, adhered substance removal method, and program |
| WO2020003464A1 (en) | 2018-06-28 | 2020-01-02 | 富士通株式会社 | Photocatalyst, gas sensor device, gas sensor, and measuring method |
Also Published As
| Publication number | Publication date |
|---|---|
| JP4224598B2 (en) | 2009-02-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3678606B2 (en) | Metal-modified apatite and method for producing the same | |
| JP4800813B2 (en) | Photocatalytic apatite composition, method for producing the same, and article | |
| JP3697608B2 (en) | Metal-modified apatite material and method for producing the same | |
| JP4320393B2 (en) | Photocatalyst material and method for producing the same | |
| KR101000821B1 (en) | Apatite and method for production thereof, and apatite base material | |
| JP4293801B2 (en) | Active tubular titanium oxide particles, catalyst containing the titanium oxide particles, and deodorant | |
| KR100912343B1 (en) | Forming Method for Film Containing Metal Modified Apatite, Coating Liquid Used Therefor, and Electronic Device Having Parts Coated with Film Containing Metal Modified Apatite | |
| WO2003102096A1 (en) | Antibacterial and anti-staining paint for building materia l and building material coated therewith | |
| KR100956843B1 (en) | Antimicrobial photocatalyst, antimicrobial articles coated with photocatalyst and manufacturing method thereof | |
| JP4224598B2 (en) | Metal-modified apatite and method for producing the same | |
| JP4324660B2 (en) | Metal-modified apatite and method for producing the same | |
| JP2000218161A (en) | Photo-catalyst body | |
| JP2001232206A (en) | Porous photocatalyst and method of manufacturing the same | |
| JP5888340B2 (en) | Photocatalyst and method for producing photocatalyst | |
| KR100562476B1 (en) | Photocatalytic coating solution containing the encapsulated natural fragnance and preparation method thereof | |
| JP3906355B2 (en) | Environmental protection composition | |
| KR200318828Y1 (en) | Gloss-catalyst Air Filter | |
| KR100980516B1 (en) | Photocatalyst sol and manufacturing method thereof | |
| JP3908717B2 (en) | How to remove air pollutants | |
| JP2011183352A (en) | Method for producing composite particle of natural zeolite and titanium dioxide | |
| JP5966754B2 (en) | Photocatalyst, method for producing photocatalyst, and photocatalytic electrode | |
| JP2008291261A (en) | Antibacterial coating material | |
| KR20090035748A (en) | Apatite and method for production thereof, and apatite base material | |
| JP2012166174A (en) | Photocatalyst, and method of manufacturing the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050614 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050902 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080513 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20081007 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20081104 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111205 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111205 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121205 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121205 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131205 Year of fee payment: 5 |
|
| EXPY | Cancellation because of completion of term |