FR2583060A1 - Production de butanol et d'acetone par fermentation avec recyclage de la biomasse par ultrafiltration - Google Patents
Production de butanol et d'acetone par fermentation avec recyclage de la biomasse par ultrafiltration Download PDFInfo
- Publication number
- FR2583060A1 FR2583060A1 FR8508535A FR8508535A FR2583060A1 FR 2583060 A1 FR2583060 A1 FR 2583060A1 FR 8508535 A FR8508535 A FR 8508535A FR 8508535 A FR8508535 A FR 8508535A FR 2583060 A1 FR2583060 A1 FR 2583060A1
- Authority
- FR
- France
- Prior art keywords
- sep
- fermentation
- ultrafiltration
- production
- biomass
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M21/00—Bioreactors or fermenters specially adapted for specific uses
- C12M21/12—Bioreactors or fermenters specially adapted for specific uses for producing fuels or solvents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M29/00—Means for introduction, extraction or recirculation of materials, e.g. pumps
- C12M29/18—External loop; Means for reintroduction of fermented biomass or liquid percolate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M41/00—Means for regulation, monitoring, measurement or control, e.g. flow regulation
- C12M41/26—Means for regulation, monitoring, measurement or control, e.g. flow regulation of pH
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M43/00—Combinations of bioreactors or fermenters with other apparatus
- C12M43/02—Bioreactors or fermenters combined with devices for liquid fuel extraction; Biorefineries
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/24—Preparation of oxygen-containing organic compounds containing a carbonyl group
- C12P7/26—Ketones
- C12P7/28—Acetone-containing products
Abstract
L'INVENTION CONCERNE UN PROCEDE DE FERMENTATION EN VUE DE PRODUIRE DU BUTANOL ET DE L'ACETONE, EN PRESENCE D'UNE SOUCHE DE CLOSTRIDIUM ACETOBUTYLICUM, LA FERMENTATION ETANT EFFECTUEE EN CONTINU OU EN DISCONTINU. L'INVENTION EST CARACTERISEE EN CE QUE LE MILIEU DE CULTURE EST ENSUITE ENVOYE DANS UNE ZONE D'ULTRAFILTRATION, LE RETENTAT CONTENANT LA BIOMASSE ETANT AU MOINS EN PARTIE RECYCLE VERS LA ZONE DE FERMENTATION.
Description
La présente invention a pour objet un nouveau procédé permettant d'obtenir par fermentation un mélange de butanol, d'acetone et d'méthanol avec une productivite elevée.
La fermentation concernée dite acétonobutylique a été pratiquee industriellement depuis longtemps. Une limitation importante a été de tous temps sa productivité qui ne dépasse pas dans les cas les plus favorables 0,6 gramme de produit (mélange de butanol, d'acétone et d'ethanol communément appelé mélange ABE) par litre de milieu de fermentation et par heure. Cette limitation est liee à la conduite discontinue de la fermentation, à la concentration finale en ABE dans le vin obtenu qui reste habituellement inferieure à 20 g/l et à la faible concentration de la biomasse bactérienne active dans les fermenteurs (habituellement 2 à 4 g/l). Ces deux dernières contraintes résultent en fait de la toxicité des produits formés en particulier le butanol qui inhibent la croissance des bactéries et la production d'ABE.
Diverses améliorations récentes ont permis d'obtenir des gains sur certains de ces points. Par exemple le brevet français N" 2523153 decrit l'obtention de mutants de Clostridium acetobutylicum, la bactérie utilisée dans cette fermentation, qui sont résistants à des concentrations plus élevées en butanol que les souches de départ et qui produisent des concentrations en ABE dépassant 20 g/l. Par ailleurs, la conduite en continu de la fermentation a été décrite récemment par divers auteurs comme H. BAHL, W. ANDERSCH et G.
GOTTSCHALK (Eur. J. Appl. Microbiol. Biotechnol. 15, 201, 1982) ou F.
MONOT et J.M. ENGASSER (Eur. J. Appl. Microbiol. Biotechnol. 18, 246 (1983) qui ont pu, par cette technique, obtenir des productivités en
ABE depassant celles accessibles par la fermentation discontinue. Des efforts ont été egalement fait pour augmenter la concentration en biomasse active dans le réacteur operé en continu pour éliminer les produits inhibiteurs.
ABE depassant celles accessibles par la fermentation discontinue. Des efforts ont été egalement fait pour augmenter la concentration en biomasse active dans le réacteur operé en continu pour éliminer les produits inhibiteurs.
Dans le cas d'autres fermentations notamment la fermentation alcoolique, il est maintenant entré dans la pratique industrielle de récupérer les levures productrices d'éthanol par exemple par centrifugation et de les recycler afin de travailler avec une biomasse active élevée. Dans le cas de la fermentation ABE la difficulté de récupérer des bactéries par centrifugation et les exigences de sterilite rigoureuses qu'elle présente ne permettent pas l'application des mêmes moyens. Cependant, des essais d'augmentation de la biomasse active ont été réalisés en utilisant les techniques d'immobilisation des cellules bactériennes et dans certains cas, un effet favorable sur la productivité a pu être obtenu.
Les procédés de séparation par membranes qui se sont développés en particulier dans la dernière décennie ont ouvert pour la fermentation des possibilités nouvelles pour le confinement ou la concentration de la biomasse microbienne. Les membranes utilisables en l'occurrence sont celles qui couvrent le domaine de l'ultrafiltration (retention de particules d'un diamètre compris entre 2 et 100 nanomètres, soit 2 x 100 x 10 9 m) et la partie du domaine de la microfiltration situe dans les diamètres de particules inférieurs à 1 micron (10 6 m).
La mise en oeuvre de l'ultrafiltration découle directement des principes qui la régissent. Le transport de matière à travers la membrane s'effectue en utilisant a pression hydraulique comme force motrice. La selection se fait au niveau de la taille des molecules ; celles de taille inférieure à celle correspondant au "seuil de coupure" sont transportées avec le solvant à travers la membrane et constituent le permeat. Du fait que les sels, les acides et autres molécules de petite taille sont transportés, seule une faible différence de pression osmotique existe entre les deux côtes de la membrane. La tendance des grosses molécules à s'accumuler au niveau de la membrane et à former une couche dite de polarisation est minimisée par l'utilisation d'un dispositif permettant de travailler à flux tangentiel avec la plus grande turbulence possible.
La technique d'ultrafiltration a déjà été appliquee à diverses fermentations bacteriennes. Ainsi dans le cas de la fabrication de bacteries lactiques, elle a permis d'améliorer la production de la biomasse bacterienne (Brevet Européen NO 0065895). Elle a été également utilisée dans le cas de la fermentation alcoolique par la bactérie Zymomnas mobilis en vue de l'amélioration de la productivité en éthanol en augmentant la concentration de la biomasse active.
Or, jusqu'à présent, l'ultrafiltration n'a pas été utilisée pour la fermentation acetonobutylique du fait des difficultés qui résultent des caractéristiques physiologiques particulières à Clostridium acetobutyl icum.
I1 est en effet bien connu que la production d'ABE est fort sensible à l'état physiologique des bactéries qui est influencé par différents paramètres incompletement connus et maîtrisées. Sommairement, on peut distinguer chez cette bactérie deux phénomènes physiologiques importants pour la production de solvants - l'existence, à côté du métabolisme solvantogene producteur d'ABE,
d'un metabolisme acidogène produisant les acides acetique et
butyrique. Dans une fermentation menee de façon classique en
discontinu, on observe une première phase de croissance rapide avec
production d'acides suivie d'une phase de production de solvants en
fin de croissance. Le mécanisme de passage d'une phase à l'autre est
mal connu.
d'un metabolisme acidogène produisant les acides acetique et
butyrique. Dans une fermentation menee de façon classique en
discontinu, on observe une première phase de croissance rapide avec
production d'acides suivie d'une phase de production de solvants en
fin de croissance. Le mécanisme de passage d'une phase à l'autre est
mal connu.
- l'existence du phénomène de sporulation. Lorsque les bonnes
conditions de croissance ne sont plus réunies, les bactéries se
lisent et une partie de la population passe d'une forme végétative
caractéristique de la croissance à la forme de spores qui correspond
à une phase de dormance. Les spores ne produisent pas de solvants.
conditions de croissance ne sont plus réunies, les bactéries se
lisent et une partie de la population passe d'une forme végétative
caractéristique de la croissance à la forme de spores qui correspond
à une phase de dormance. Les spores ne produisent pas de solvants.
Dans une fermentation discontinue, elles apparaissent en fin de
production de solvants.
production de solvants.
Dans la présente invention, on a defini les conditions dans lesquelles les bactéries, cultivées notamment en continu mais également en semi-continu comme detaille plus loin et constamment recyclées après separation par ultrafiltration, sont maintenues en croissance et en phase de production de solvants. Ces conditions sont de trois sortes - la composition du milieu doit contenir les éléments minéraux
habituels indispensables à la croissance, mais doit également être
enrichi en aminoacides et vitamines, présents dans certains milieux
naturels comme les farines de céréales mais qui doivent être
apportes aux milieux synthétiques habituellement sous forme
d'extrait de levure ou de liqueur de macération de mais à raison de
0,5 à 5 g par litre. Parmi les éléments minéraux nécessaires, il est
important d'apporter de l'azote sous forme ammoniacale. I1 peut être
avantageux d'effectuer cet apport sous forme d'ammoniaque, ce qui
permet d'utiliser cet apport pour la régulation du pH, comme
illustré dans les exemples.
habituels indispensables à la croissance, mais doit également être
enrichi en aminoacides et vitamines, présents dans certains milieux
naturels comme les farines de céréales mais qui doivent être
apportes aux milieux synthétiques habituellement sous forme
d'extrait de levure ou de liqueur de macération de mais à raison de
0,5 à 5 g par litre. Parmi les éléments minéraux nécessaires, il est
important d'apporter de l'azote sous forme ammoniacale. I1 peut être
avantageux d'effectuer cet apport sous forme d'ammoniaque, ce qui
permet d'utiliser cet apport pour la régulation du pH, comme
illustré dans les exemples.
- le pH qui est réglé par addition d'une base à une valeur constante
située entre 4 et 6. D'une façon générale, on a constaté que des pH
plus bas favorisaient la sélectivité de la production de solvants
(production d'acides plus faible) mais ralentissaient la croissance.
située entre 4 et 6. D'une façon générale, on a constaté que des pH
plus bas favorisaient la sélectivité de la production de solvants
(production d'acides plus faible) mais ralentissaient la croissance.
un compromis satisfaisant est obtenu dans une zone située entre pH 4
et 5,4.
et 5,4.
- la concentration en source carbonée (un sucre, et de préférence le
glucose) du milieu de fermentation qui doit être maintenue à tout
moment à une valeur égale ou supérieure à 0,5 g/l. Cette condition
est obtenue en réglant l'alimentation en sucre du fermenteur. Dans
une partie du procédé (cas de la conduite en continu), on peut soit
faire varier la concentration en sucre situé entre 10 et 70 g/1 dans
le milieu d'alimentation soit le taux de dilution (rapport du débit
horaire de sortie du permet eliminé hors du systeme de fermentation
au volume de fermentation), ce taux de dilution peut varier de 0,05
à 0,35 h 1.Ces deux variables sont ajustées pour obtenir pendant la
phase de production de solvants une consommation de la source
carbonée superieure ou égale à 85 %. La concentration en sucres, et
notamment en glucose résiduel ne doit pas être nulle pour eviter
l'influence défavorable sur l'état physiologique des cellules d'une
forte limitation en glucose. Pour obtenir et maintenir la
consommation de la source carbonée dans le domaine requis, on peut donc soit opérer avec une concentration en glucose constante et
ajuster le taux de dilution soit opérer à taux de dilution constant
et ajuster la concentration en glucose dans le milieu
d'alimentation. Le choix de taux de dilution élevés favorise la
croissance et la détoxification en assurant une élimination plus
rapide des produits formés (solvants, acides) qui sont toxiques pour
le microorganisme.Des taux de dilution plus faibles sont favorables
à la sélectivité de la production de solvants (plus faible
proportion d'acides) on a cependant obtenu, et c'est là un résultat
inattendu et remarquable, les productions de solvants les plus
importantes à des taux de dilution élevés supérieurs à 0,25 et
(de l'ordre notamment de D = 0,3 h 1) qui permettent des vitesses de
croissance élevées. En culture discontinue classique,ainsi qu'en
culture continue, sans recyclage, ces croissances rapides sont au
contraire caractéristiques de cellules en phase de production
d'acides, les divers éléments sont illustres dans les exemples
développés plus loin.
glucose) du milieu de fermentation qui doit être maintenue à tout
moment à une valeur égale ou supérieure à 0,5 g/l. Cette condition
est obtenue en réglant l'alimentation en sucre du fermenteur. Dans
une partie du procédé (cas de la conduite en continu), on peut soit
faire varier la concentration en sucre situé entre 10 et 70 g/1 dans
le milieu d'alimentation soit le taux de dilution (rapport du débit
horaire de sortie du permet eliminé hors du systeme de fermentation
au volume de fermentation), ce taux de dilution peut varier de 0,05
à 0,35 h 1.Ces deux variables sont ajustées pour obtenir pendant la
phase de production de solvants une consommation de la source
carbonée superieure ou égale à 85 %. La concentration en sucres, et
notamment en glucose résiduel ne doit pas être nulle pour eviter
l'influence défavorable sur l'état physiologique des cellules d'une
forte limitation en glucose. Pour obtenir et maintenir la
consommation de la source carbonée dans le domaine requis, on peut donc soit opérer avec une concentration en glucose constante et
ajuster le taux de dilution soit opérer à taux de dilution constant
et ajuster la concentration en glucose dans le milieu
d'alimentation. Le choix de taux de dilution élevés favorise la
croissance et la détoxification en assurant une élimination plus
rapide des produits formés (solvants, acides) qui sont toxiques pour
le microorganisme.Des taux de dilution plus faibles sont favorables
à la sélectivité de la production de solvants (plus faible
proportion d'acides) on a cependant obtenu, et c'est là un résultat
inattendu et remarquable, les productions de solvants les plus
importantes à des taux de dilution élevés supérieurs à 0,25 et
(de l'ordre notamment de D = 0,3 h 1) qui permettent des vitesses de
croissance élevées. En culture discontinue classique,ainsi qu'en
culture continue, sans recyclage, ces croissances rapides sont au
contraire caractéristiques de cellules en phase de production
d'acides, les divers éléments sont illustres dans les exemples
développés plus loin.
L'un des appareillages pouvant être utilisé pour la mise en oeuvre de l'invention est presenté dans la figure 1. La production d'ABE est effectuée dans un fermenteur (1) dont le volume est contrôle par exemple au moyen d'une électrode conductimétrique (2) qui commande la pompe d'alimentation du milieu (3) en provenance de la réserve d'alimentation (7). Une partie au moins du milieu de culture fait l'objet d'une recirculation permanente à travers un appareillage d'ultrafiltration (4 et 4a) avec retour au fermenteur du retentat contenant la biomasse par les vannes 6a, 6 et la conduite 13. Cette recirculation est assurée par une pompe (5) qui assure une vitesse de circulation qui peut varier habituellement entre 0,5 et 10 m/s, la pression de travail lue au moyen des manomètres (16) etant habituellement comprise entre 0,2 et 3 bars.Cette recirculation minimise l'effet de polarisation mentionné plus haut et diminue la fréquence des nettoyages. Un montage avantageux utilise comme représenté sur la figure 1, deux batteries d'ultrafiltres (4 et 4a) montées en parallele et mises en service de façon alternative pour permettre le nettoyage sans arrêt de l'utilisation. Le perméat obtenu est partiellement évacué (9) au moyen d'une pompe doseuse (10) tandis que l'excès ou reste du perméat (Il) est renvoye au fermenteur.Une vanne (15) en sortie de fermenteur permet l'échantillonnage et la purge éventuelle de biomasse ; on trouve ci dessous la légende complete de la figure 1:
1 Fermenteur
2 Electrode régulation de niveau
3 Pompe d'alimentation
4-4a Ultrafiltres
5 Pompage de circulation
6-6a Vannes
7 Réservoir d'alimentation
8 Barbotage d'azote
9 Sortie du perméat éliminé 10 Pompe doseuse 11 Perméat recyclé 12 Pompe pour régulation du pH 13 Recyclage de la biomasse (rétentat) 14 Sortie des gaz 15 Sortie pour prélèvements 16 Manometres
Le-rapport de la surface de membrane des ultrafiltres en service (4-4a) par rapport au volume de travail peut varier selon les conditions de travail et le type de membranes utilisées mais se situe fréquemment entre 50 et 200 cm2 par 1 de milieu de fermentation. Les membranes utilisables sont celles dont la porosité se situe dans le domaine qui a été défi n plus haut Dans ce domaine, les membranes commercialement disponibles sont diverses, fréquemment de nature organique, sous forme de fibres creuses (polymères du type polysulfones, polypropylène ou polyamide par exemple) ou de feuilles (notamment en polysulfone ou acétate de cellulose). Certaines sont aussi de nature minérale (tubes de céramique microporeux par exemple).
1 Fermenteur
2 Electrode régulation de niveau
3 Pompe d'alimentation
4-4a Ultrafiltres
5 Pompage de circulation
6-6a Vannes
7 Réservoir d'alimentation
8 Barbotage d'azote
9 Sortie du perméat éliminé 10 Pompe doseuse 11 Perméat recyclé 12 Pompe pour régulation du pH 13 Recyclage de la biomasse (rétentat) 14 Sortie des gaz 15 Sortie pour prélèvements 16 Manometres
Le-rapport de la surface de membrane des ultrafiltres en service (4-4a) par rapport au volume de travail peut varier selon les conditions de travail et le type de membranes utilisées mais se situe fréquemment entre 50 et 200 cm2 par 1 de milieu de fermentation. Les membranes utilisables sont celles dont la porosité se situe dans le domaine qui a été défi n plus haut Dans ce domaine, les membranes commercialement disponibles sont diverses, fréquemment de nature organique, sous forme de fibres creuses (polymères du type polysulfones, polypropylène ou polyamide par exemple) ou de feuilles (notamment en polysulfone ou acétate de cellulose). Certaines sont aussi de nature minérale (tubes de céramique microporeux par exemple).
Un critere de choix important pour la presente invention est le mode de stérilisation de ces membranes. La préférence -étant accordée à celles qui permettent une stérilisation efficace et commode. De ce point de vue, les membranes serilisables par voie thermique (vapeur) telles que les membranes minérales sont particulièrement avantageuses.
Ce point résulte comme exposé plus haut de la nécessité de conduire la fermentation dans des conditions de stérilité rigoureuse. De plus, elles autorisent des opérations de nettoyage efficaces, facilitant leur régénération.
L'utilisation de la technique d'ultrafiltration pour le recyclage de la biomasse active permet egalement d'autres modes de conduite de la fermentation qui peuvent être utilisés avantageusement industriellement. En particulier, on peut amener le perméat d'ultrafiltration à un bouilleur qui separera par distillation au moins une partie du flegme contenant un mélange de butanol d'acétone d'éthanol et d'eau, la phase aqueuse du perméat ainsi fortement appauvrie en solvants (tels que butanol, acétone, éthanol) étant recyclée dans le fermenteur ; on peut ainsi conduire la fermentation soit avec une alimentation continue en substrat soit en semi-continu en effectuant des alimentations succesives en substrat renouvelées quand le glucose residuel a baissé en dessous d'une valeur minimale;
C'est ce dernier mode de fonctionnement que l'on a présenté dans l'exemple 2 qui illustre bien l'intérêt de l'étape de distillation puisqu'elle permet de libérer la fermentation de l'inhibition par les solvants produits et de convertir en ABE avec- un même milieu une quantité de glucose plusieurs fois supérieure à celle voisine de 6Q g/l habituellement possible dans une conduite discontinue classique.
C'est ce dernier mode de fonctionnement que l'on a présenté dans l'exemple 2 qui illustre bien l'intérêt de l'étape de distillation puisqu'elle permet de libérer la fermentation de l'inhibition par les solvants produits et de convertir en ABE avec- un même milieu une quantité de glucose plusieurs fois supérieure à celle voisine de 6Q g/l habituellement possible dans une conduite discontinue classique.
Les exemples presentés ci-dessous illustrent les conditions operatoires de l'invention et les résultats obtenus.
Exemple 1
La fermentation est effectuee avec la souche type connue Clostridium acetobutylicum ATCC 824. Le milieu contient les élements minéraux suivant (en g/l) : 0,5 g K2HPO4,0,5 g KH2P04, 0,2 g MgS04.7H20, 0,01 g MnS04.H20, 0,01 g FeSO4.7H20, 0,01 g NaCl. Ce milieu est supplémenté en extrait de levure (4 g/l). La source de carbone est le glucose. Une source d'azote sous forme d'ammoniaque est également fournie comme décrit plus loin. On ajoute également dans le milieu de l'antimousse (Struktol) à raison de 1 g.l
L'appareillage utilisé est celui décrit plus haut (figure 1). Le fermenteur est d'une capacite de 3 1, le volume total de fermentation (fermenteur plus circuit de recirculation) étant de 3,45 1.La batterie d'ultrafiltres est composée de membranes minérales Carbosep M1 commercialisées par la Société SFEC, Bollene, France. Ces membranes sont constituées de tubes de carbone recouverts d'une couche de ceramique d'ultrafiltration. Chaque tube a une surface interne de 0,0226 m2. On a utilisé deux séries de deux tubes montées en parallèle. La circulation du moût à une vitesse d'environ 3 m.s-1 est assurée par une pompe Nemo Netzsch NL 20A.
La fermentation est effectuee avec la souche type connue Clostridium acetobutylicum ATCC 824. Le milieu contient les élements minéraux suivant (en g/l) : 0,5 g K2HPO4,0,5 g KH2P04, 0,2 g MgS04.7H20, 0,01 g MnS04.H20, 0,01 g FeSO4.7H20, 0,01 g NaCl. Ce milieu est supplémenté en extrait de levure (4 g/l). La source de carbone est le glucose. Une source d'azote sous forme d'ammoniaque est également fournie comme décrit plus loin. On ajoute également dans le milieu de l'antimousse (Struktol) à raison de 1 g.l
L'appareillage utilisé est celui décrit plus haut (figure 1). Le fermenteur est d'une capacite de 3 1, le volume total de fermentation (fermenteur plus circuit de recirculation) étant de 3,45 1.La batterie d'ultrafiltres est composée de membranes minérales Carbosep M1 commercialisées par la Société SFEC, Bollene, France. Ces membranes sont constituées de tubes de carbone recouverts d'une couche de ceramique d'ultrafiltration. Chaque tube a une surface interne de 0,0226 m2. On a utilisé deux séries de deux tubes montées en parallèle. La circulation du moût à une vitesse d'environ 3 m.s-1 est assurée par une pompe Nemo Netzsch NL 20A.
Apres stérilisation à la vapeur de l'appareillage, du milieu stérile contenant 40 g/l de glucose a été introduit dans le fermenteur et désaéré par barbotage d'azote. Le réacteur a été ensemencé par 300 ml d'une preculture sur le même milieu. La fermentation a été alors conduite en un premier temps sans alimentation en milieu (conduite discontinue) avec pendant cette période, recyclage total du perméat.
La conduite continue a été mise en route lorsque la concentration de glucose résiduel a atteint 5 g/1. Le taux de dilution D était imposé par reglage du debit du perméat en sortie du systeme, l'excès de permeat étant recyclé dans le fermenteur. Du milieu frais remplaçait le permet écoule de façon automatique par suite du contrôle de niveau dans le fermenteur.
La fermentation a été effectuée à 35 C. Le pH était régulé à 5,4 par addition automatique d'ammoniaque.
Dans ces conditions, la fermentation est poursuivie en continu après 20 h (concentration de glucose résiduelle inférieure à 5 g/l) et le taux de dilution s'est équilibré à une valeur de 0,06 h-l jusqu 'à 160 h. L'augmentation de biomasse a été assez limitée pendant cette période, les bactéries montrant une évolution nette vers une phase de sporulation (présence d'endospores qui présente un maximum à 60 h).
Cette tendance s'est ensuite inversée pour faire place à une croissance vigoureuse qui s'est traduite par une augmentation de D jusqu'à 0,33 h 1 à 200 h. Une tendance lente à la diminution a été ensuite observée jusqu'à 500 h où D atteignait 0,02 h 1. Une augmentation considérable de raz la biomasse consécutive à cette croissance a été obtenue puisque des concentrations cellulaires de plus de 100 g.l | ont été atteintes après 300 h. Cette biomasse active considérable a entrainé une augmentation de productivité pour la synthèse de solvants.Cette productivite a atteint jusqu'à 6 g d'ABE par 1 par h pendant de courtes periodes, et 4,3 g.l-1 h-l pendant 3 jours de fonctionnement ce qui constitue un progrès particulièrement sensible par rapport aux résultats cités plus haut des fermentations continues ou discontinues, sans ultrafiltration. Comme indiqué également dans le tableau 1, au-delà de 300 h, on observe une baisse graduelle de la productivité et de la concentration en solvants produite, du fait de l'augmentation de la production des acides acétique et butyrique.
Au cours de cet essai, deux nettoyages de la membrane utilisée ont été effectués apres 281 et 405 heures.
Exemple 2 a mise en oeuvre de la fermentation diffère de celle de l'exemple 1 en ce que l'on maintient, après la periode de fermentation discontinue initiale, un taux de dilution constant égal à 0,32 h-1 et que l'on ajuste la concentration de l'alimentation en glucose pour maintenir dans le fermenteur une concentration en glucose residuel faible. Cette concentration en glucose dans le milieu d'alimentation est ainsi passee de 11,7 g/l a 35 h à 47,5 g/l à 86 h. Dans ces conditions, une croissance plus rapide que dans le cas précédent a été obtenue puisqu'une concentration cellulaire de 50 g/l a été obtenue en 110 h (ou de 14 g/l dans le cas précédent) ce qui a permis d'atteindre plus rapidement des productivités élevées en solvants.La concentration en solvants pendant cette période de croissance était cependant plus faible que dans le cas précédent. La suite de l'évolution de la fermentation était analogue à celle de l'exemple 1.
Période <SEP> Concentration <SEP> Productivité <SEP> Concentration <SEP> Concentration <SEP> Taux <SEP> de
<tb> de <SEP> temps <SEP> en <SEP> solvants <SEP> en <SEP> solvants <SEP> en <SEP> biomasse <SEP> moyenne <SEP> dilution
<tb> (heures) <SEP> g.1-1 <SEP> moyenne <SEP> dans <SEP> le <SEP> en <SEP> acides <SEP> D
<tb> g.1-1.h-1 <SEP> fermenteur <SEP> (acétique <SEP> plus) <SEP> (h-1)
<tb> (g.1-1) <SEP> butyrique
<tb> (g.1-1)
<tb> entre
<tb> 20 <SEP> et <SEP> 50 <SEP> h <SEP> de <SEP> 2 <SEP> à <SEP> 18 <SEP> 1,0 <SEP> 5 <SEP> - <SEP> 17 <SEP> 10 <SEP> à <SEP> 6 <SEP> 0,06
<tb> entre
<tb> 150 <SEP> et <SEP> 200 <SEP> h <SEP> de <SEP> 18 <SEP> à <SEP> 15 <SEP> 4,3 <SEP> 17 <SEP> - <SEP> 30 <SEP> 6 <SEP> à <SEP> 7 <SEP> de <SEP> 0,06 <SEP> à <SEP> 0,33
<tb> entre
<tb> 200 <SEP> et <SEP> 300 <SEP> h <SEP> de <SEP> 15 <SEP> à <SEP> 10 <SEP> 2,4 <SEP> 30 <SEP> - <SEP> 90 <SEP> 7 <SEP> à <SEP> 9 <SEP> de <SEP> 0,3 <SEP> à <SEP> 0,22
<tb> entre
<tb> 300 <SEP> et <SEP> 500 <SEP> h <SEP> de <SEP> 10 <SEP> à <SEP> 8 <SEP> 1,4 <SEP> 90 <SEP> - <SEP> 100 <SEP> 9 <SEP> à <SEP> 14 <SEP> de <SEP> 0,22 <SEP> à <SEP> 0,15
<tb> TABLEAU 1
Evolution d'une fermentation continue de production d'ABE avec recyclage des cellules par ultrafiltration
Exemple 3
Le montage réalisé est présenté dans la figure 2. L'ensemble de l'appareillage situé avant le module de distillation (bouilleur (16) et annexes) est semblable à celui de la figure 1 et ne sera donc pas redécrit. Le volume total du milieu réactionnel est de 10,2 1.Le volume du liquide dans le bouilleur (16) est réglé à 0,5 1 au moyen d'une electrode conductimétrique (18) agissànt sur la pompe de permet traité (17). Le débit d'alimentation dans le bouilleur est réglé par une pompe doseuse (15) de façon à conduire à des temps de séjour limités (10 à 15 minutes) afin d'éviter la dégradation des sucres. Le perméat appauvri en ABE est réfrigéré (24) avant d'être recyclé dans le fermenteur. Une sortie de perméat (9, 10) est ménagée afin de compenser les volumes liquides ajoutes lors des alimentations successives en substrat. La colonne à distiller est munie d'un garnissage d'une hauteur de 60 cm. Le distillat contenant 1'ABE est recueilli (20). On trouve ci dessous la legende complète de la figure 2
1 Fermenteur 13 Cellules recyclées
2 Electrode régulation de niveau 14 Sortie gaz
3 Pompe d'alimentation 15 Pompe doseuse perméat
à traiter
4-4a Ultrafiltres 16 Bouilleur
5 Pompe circulation 17 Pompe recyclage perméat
traité
6-6a Vannes 18 Régulation niveau
bouilleur
7 Réservoir d'alimentation 19 Perméat traité recyclage
8 Barbotage d'azote 20 Distillat
9 Sortie perméat traité 21 Manomètres 10 Pompe doseuse 22 Prélèvements 11 Perméat recyclé 12 Pompe régulation pH 24 Réfrigérants
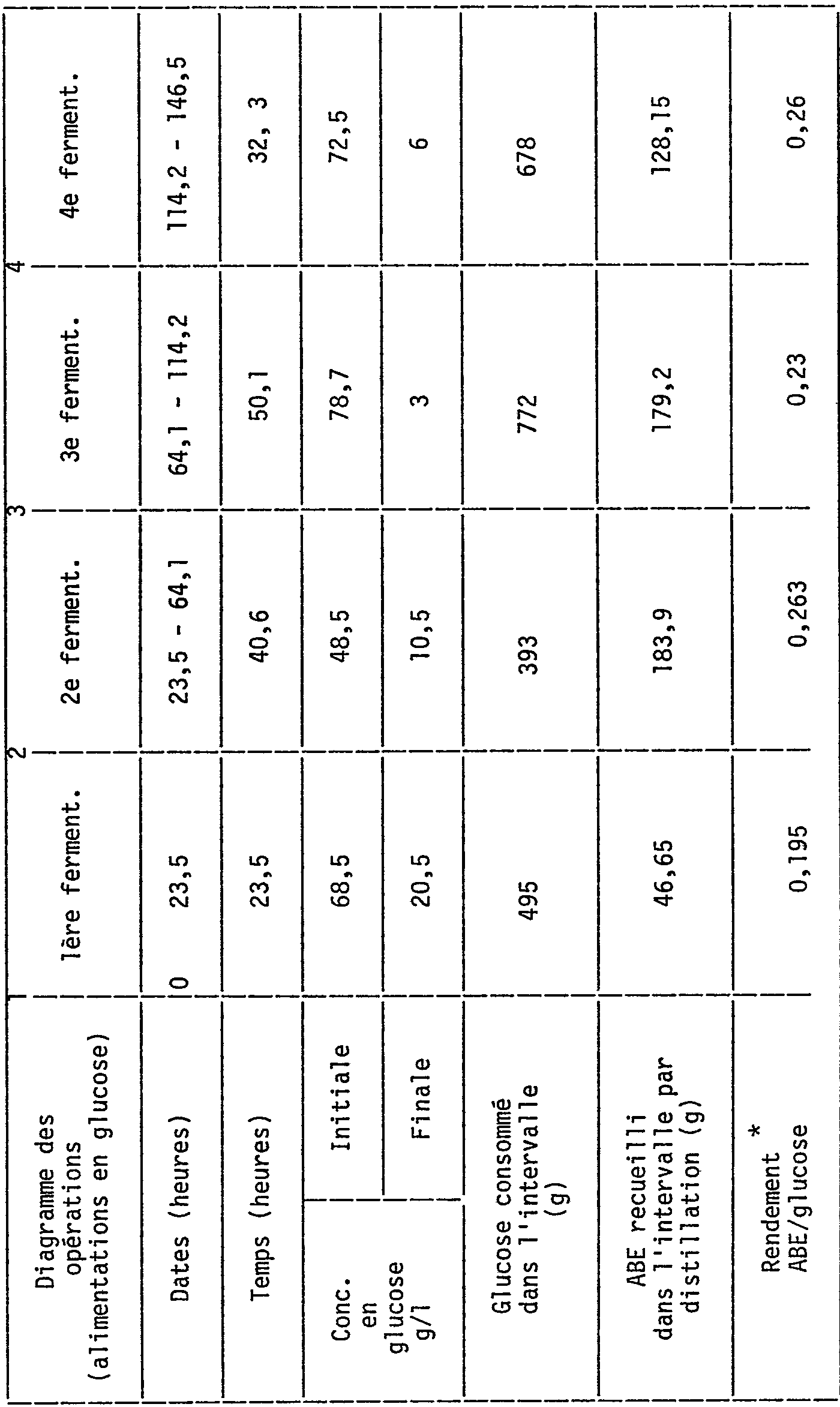
Le tableau 2 illustre les résultats obtenus avec cet appareillage lors d'une série de quatre fermentations successives utilisant la même biomasse active (conduite en semi continu) et un milieu recyclé à l'exception des additions successives de glucose et des soutirages liquides correspondants (800 ml pour chaque addition de substrat). Une partie de 1'ABE produit est recueilli dans le distillat comme illustre dans le tableau 2.
<tb> de <SEP> temps <SEP> en <SEP> solvants <SEP> en <SEP> solvants <SEP> en <SEP> biomasse <SEP> moyenne <SEP> dilution
<tb> (heures) <SEP> g.1-1 <SEP> moyenne <SEP> dans <SEP> le <SEP> en <SEP> acides <SEP> D
<tb> g.1-1.h-1 <SEP> fermenteur <SEP> (acétique <SEP> plus) <SEP> (h-1)
<tb> (g.1-1) <SEP> butyrique
<tb> (g.1-1)
<tb> entre
<tb> 20 <SEP> et <SEP> 50 <SEP> h <SEP> de <SEP> 2 <SEP> à <SEP> 18 <SEP> 1,0 <SEP> 5 <SEP> - <SEP> 17 <SEP> 10 <SEP> à <SEP> 6 <SEP> 0,06
<tb> entre
<tb> 150 <SEP> et <SEP> 200 <SEP> h <SEP> de <SEP> 18 <SEP> à <SEP> 15 <SEP> 4,3 <SEP> 17 <SEP> - <SEP> 30 <SEP> 6 <SEP> à <SEP> 7 <SEP> de <SEP> 0,06 <SEP> à <SEP> 0,33
<tb> entre
<tb> 200 <SEP> et <SEP> 300 <SEP> h <SEP> de <SEP> 15 <SEP> à <SEP> 10 <SEP> 2,4 <SEP> 30 <SEP> - <SEP> 90 <SEP> 7 <SEP> à <SEP> 9 <SEP> de <SEP> 0,3 <SEP> à <SEP> 0,22
<tb> entre
<tb> 300 <SEP> et <SEP> 500 <SEP> h <SEP> de <SEP> 10 <SEP> à <SEP> 8 <SEP> 1,4 <SEP> 90 <SEP> - <SEP> 100 <SEP> 9 <SEP> à <SEP> 14 <SEP> de <SEP> 0,22 <SEP> à <SEP> 0,15
<tb> TABLEAU 1
Evolution d'une fermentation continue de production d'ABE avec recyclage des cellules par ultrafiltration
Exemple 3
Le montage réalisé est présenté dans la figure 2. L'ensemble de l'appareillage situé avant le module de distillation (bouilleur (16) et annexes) est semblable à celui de la figure 1 et ne sera donc pas redécrit. Le volume total du milieu réactionnel est de 10,2 1.Le volume du liquide dans le bouilleur (16) est réglé à 0,5 1 au moyen d'une electrode conductimétrique (18) agissànt sur la pompe de permet traité (17). Le débit d'alimentation dans le bouilleur est réglé par une pompe doseuse (15) de façon à conduire à des temps de séjour limités (10 à 15 minutes) afin d'éviter la dégradation des sucres. Le perméat appauvri en ABE est réfrigéré (24) avant d'être recyclé dans le fermenteur. Une sortie de perméat (9, 10) est ménagée afin de compenser les volumes liquides ajoutes lors des alimentations successives en substrat. La colonne à distiller est munie d'un garnissage d'une hauteur de 60 cm. Le distillat contenant 1'ABE est recueilli (20). On trouve ci dessous la legende complète de la figure 2
1 Fermenteur 13 Cellules recyclées
2 Electrode régulation de niveau 14 Sortie gaz
3 Pompe d'alimentation 15 Pompe doseuse perméat
à traiter
4-4a Ultrafiltres 16 Bouilleur
5 Pompe circulation 17 Pompe recyclage perméat
traité
6-6a Vannes 18 Régulation niveau
bouilleur
7 Réservoir d'alimentation 19 Perméat traité recyclage
8 Barbotage d'azote 20 Distillat
9 Sortie perméat traité 21 Manomètres 10 Pompe doseuse 22 Prélèvements 11 Perméat recyclé 12 Pompe régulation pH 24 Réfrigérants
Le tableau 2 illustre les résultats obtenus avec cet appareillage lors d'une série de quatre fermentations successives utilisant la même biomasse active (conduite en semi continu) et un milieu recyclé à l'exception des additions successives de glucose et des soutirages liquides correspondants (800 ml pour chaque addition de substrat). Une partie de 1'ABE produit est recueilli dans le distillat comme illustre dans le tableau 2.
1 <SEP> 2 <SEP> 3 <SEP> 4
<tb> Diagramme <SEP> des
<tb> opérations <SEP> lère <SEP> ferment. <SEP> 2e <SEP> ferment. <SEP> 3e <SEP> ferment. <SEP> 4e <SEP> ferment.
<tb> (alimentations <SEP> en <SEP> glucose)
<tb> Dates <SEP> (heures) <SEP> 0 <SEP> 23,5 <SEP> 23,5 <SEP> - <SEP> 64,1 <SEP> 64,1 <SEP> - <SEP> 114,2 <SEP> 114,2 <SEP> - <SEP> 146,5
<tb> Temps <SEP> (heures) <SEP> 23,5 <SEP> 40,6 <SEP> 50,1 <SEP> 32,3
<tb> Conc. <SEP> Initiale <SEP> 68,5 <SEP> 48,5 <SEP> 78,7 <SEP> 72,5
<tb> en
<tb> glucose
<tb> g/l <SEP> Finale <SEP> 20,5 <SEP> 10,5 <SEP> 3 <SEP> 6
<tb> Glucose <SEP> consommé
<tb> dans <SEP> l'intervalle <SEP> 495 <SEP> 393 <SEP> 772 <SEP> 678
<tb> (g)
<tb> ABE <SEP> recueilli
<tb> dans <SEP> l'intervalle <SEP> par <SEP> 46,65 <SEP> 183,9 <SEP> 179,2 <SEP> 128,15
<tb> distillation <SEP> (g)
<tb> Rendement <SEP> *
<tb> ABE/glucose <SEP> 0,195 <SEP> 0,263 <SEP> 0,23 <SEP> 0,26
<tb>
<tb> Diagramme <SEP> des
<tb> opérations <SEP> lère <SEP> ferment. <SEP> 2e <SEP> ferment. <SEP> 3e <SEP> ferment. <SEP> 4e <SEP> ferment.
<tb> (alimentations <SEP> en <SEP> glucose)
<tb> Dates <SEP> (heures) <SEP> 0 <SEP> 23,5 <SEP> 23,5 <SEP> - <SEP> 64,1 <SEP> 64,1 <SEP> - <SEP> 114,2 <SEP> 114,2 <SEP> - <SEP> 146,5
<tb> Temps <SEP> (heures) <SEP> 23,5 <SEP> 40,6 <SEP> 50,1 <SEP> 32,3
<tb> Conc. <SEP> Initiale <SEP> 68,5 <SEP> 48,5 <SEP> 78,7 <SEP> 72,5
<tb> en
<tb> glucose
<tb> g/l <SEP> Finale <SEP> 20,5 <SEP> 10,5 <SEP> 3 <SEP> 6
<tb> Glucose <SEP> consommé
<tb> dans <SEP> l'intervalle <SEP> 495 <SEP> 393 <SEP> 772 <SEP> 678
<tb> (g)
<tb> ABE <SEP> recueilli
<tb> dans <SEP> l'intervalle <SEP> par <SEP> 46,65 <SEP> 183,9 <SEP> 179,2 <SEP> 128,15
<tb> distillation <SEP> (g)
<tb> Rendement <SEP> *
<tb> ABE/glucose <SEP> 0,195 <SEP> 0,263 <SEP> 0,23 <SEP> 0,26
<tb>
* Compte tenu de l'ABE non distillé restant dans le perméat
TABLEAU 2
Production d'ABE en fermentation semi-continue avec recyclage de la biomasse et distillation du perméat
TABLEAU 2
Production d'ABE en fermentation semi-continue avec recyclage de la biomasse et distillation du perméat
Claims (7)
- zone de fermentation.en ce que le perméat obtenu est renvoyé au moins en partie dans lade 0,5 à 10 m/s à travers au moins une zone d'ultrafiltration, etune partie au moins du milieu de culture circule avec une vitessemicroorganisme Clostridium acetobutylicum, caractérisé en ce quefermentation en presence d'au moins une souche qui est unREVENDICATIONS 1. Procéde de production de butanol et d'acétone ou d'ABE par
- 2. Procéde selon la revendication 1 caractérise en ce que le milieu deculture est enrichi en amino-acides et vitamines, en ce que le pHdans la zone de fermentation est réglé entre 4 et 6 en partie aumoyen d'une source azote sous forme ammoniacale, en ce que laconcentration en source carbonée dans le milieu de fermentation estréglée de façon à rester supérieure à 0,5 g/l et à ce que laconsommation de la source carbonée est su-périeure ou égale à 85 %.
- 3. Procédé selon la revendication 2 dans lequel le pH est comprisentre 4 et 5,4.
- 4. Procédé selon la revendication 3 dans lequel la source carbonée esten majeure partie composée de glucose.
- 5. Procédé selon l'une des revendications 1 à 4 dans lequel au moinsdeux zones d'ultrafiltration sont utilisées, disposées enparallèle.
- 6. Procédé selon l'une des revendications 1 à 5 appliqué à unefermentation effectuée en continu.
- 7. Procédé selon l'une des revendications 1 à 5 appliquée à unefermentation effectuee en semi-continu ou continu dans lequel unepartie du perméat est recyclée dans la zone de fermentation et danslequel une autre partie du permet est soumise à une distillation àl'issue de laquelle une phase aqueuse appauvrie en solvants estrenvoyée au moins en partie dans la zone de fermentation.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR8508535A FR2583060B1 (fr) | 1985-06-06 | 1985-06-06 | Production de butanol et d'acetone par fermentation avec recyclage de la biomasse par ultrafiltration |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR8508535A FR2583060B1 (fr) | 1985-06-06 | 1985-06-06 | Production de butanol et d'acetone par fermentation avec recyclage de la biomasse par ultrafiltration |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2583060A1 true FR2583060A1 (fr) | 1986-12-12 |
| FR2583060B1 FR2583060B1 (fr) | 1987-09-18 |
Family
ID=9319926
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR8508535A Expired FR2583060B1 (fr) | 1985-06-06 | 1985-06-06 | Production de butanol et d'acetone par fermentation avec recyclage de la biomasse par ultrafiltration |
Country Status (1)
| Country | Link |
|---|---|
| FR (1) | FR2583060B1 (fr) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0585180A1 (fr) * | 1992-07-24 | 1994-03-02 | Eastman Kodak Company | Procédé d'ultrafiltration à temps de cycle fixe |
| WO2005014840A1 (fr) * | 2003-08-01 | 2005-02-17 | Degussa Ag | Procede de preparation de l-threonine |
| US8236994B2 (en) | 2006-10-31 | 2012-08-07 | Metabolic Explorer | Process for the biological production of 1,3-propanediol from glycerol with high yield |
| US8399717B2 (en) | 2008-10-03 | 2013-03-19 | Metabolic Explorer | Method for purifying an alcohol from a fermentation broth using a falling film, a wiped film, a thin film or a short path evaporator |
| GB2520101A (en) * | 2013-06-28 | 2015-05-13 | Green Biologics Ltd | Solvent production |
| US9249431B2 (en) | 2008-02-28 | 2016-02-02 | Green Biologics Limited | Production process |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR915718A (fr) * | 1941-03-11 | 1946-11-15 | Perfectionnements relatifs aux procédés de fabrication d'acétone et d'alcool butylique par fermentation | |
| FR2477571A1 (fr) * | 1980-03-05 | 1981-09-11 | Unisearch Ltd | Procede de production d'ethanol a partir de milieux contenant un carbohydrate fermentable par culture de zymomonas mobilis et ethanol produit par ledit procede |
| DE3005605A1 (de) * | 1980-02-15 | 1981-10-01 | Sartorius GmbH, 3400 Göttingen | Verfahren und vorrichtung zur abtrennung von wirkstoffen aus einer zellsuspension |
| EP0082486A2 (fr) * | 1981-12-18 | 1983-06-29 | Gesellschaft für Biotechnologische Forschung mbH (GBF) | Méthode et appareillage pour le contrôle cinétique des réactions enzymatiques |
| FR2555200A1 (fr) * | 1983-11-23 | 1985-05-24 | Centre Nat Rech Scient | Procede de preparation d'acide lactique par fermentation de lactoserum et installation pour la mise en oeuvre en continu de ce procede |
-
1985
- 1985-06-06 FR FR8508535A patent/FR2583060B1/fr not_active Expired
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR915718A (fr) * | 1941-03-11 | 1946-11-15 | Perfectionnements relatifs aux procédés de fabrication d'acétone et d'alcool butylique par fermentation | |
| DE3005605A1 (de) * | 1980-02-15 | 1981-10-01 | Sartorius GmbH, 3400 Göttingen | Verfahren und vorrichtung zur abtrennung von wirkstoffen aus einer zellsuspension |
| FR2477571A1 (fr) * | 1980-03-05 | 1981-09-11 | Unisearch Ltd | Procede de production d'ethanol a partir de milieux contenant un carbohydrate fermentable par culture de zymomonas mobilis et ethanol produit par ledit procede |
| EP0082486A2 (fr) * | 1981-12-18 | 1983-06-29 | Gesellschaft für Biotechnologische Forschung mbH (GBF) | Méthode et appareillage pour le contrôle cinétique des réactions enzymatiques |
| FR2555200A1 (fr) * | 1983-11-23 | 1985-05-24 | Centre Nat Rech Scient | Procede de preparation d'acide lactique par fermentation de lactoserum et installation pour la mise en oeuvre en continu de ce procede |
Non-Patent Citations (1)
| Title |
|---|
| BIOTECHNOLOGY AND BIOENGINEERING SYMPOSIUM, 6th SYMPOSIUM ON BIOTECHNOLOGY FOR FUALS AND CHEMICALS, Nr. 14, pages 543-552, John Wiley & Sons, Inc., New York, US; A. GARCIA et al.: "Reverse osmosis application for butanol-acetone fermentation" * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0585180A1 (fr) * | 1992-07-24 | 1994-03-02 | Eastman Kodak Company | Procédé d'ultrafiltration à temps de cycle fixe |
| WO2005014840A1 (fr) * | 2003-08-01 | 2005-02-17 | Degussa Ag | Procede de preparation de l-threonine |
| US8236994B2 (en) | 2006-10-31 | 2012-08-07 | Metabolic Explorer | Process for the biological production of 1,3-propanediol from glycerol with high yield |
| US9249431B2 (en) | 2008-02-28 | 2016-02-02 | Green Biologics Limited | Production process |
| US8399717B2 (en) | 2008-10-03 | 2013-03-19 | Metabolic Explorer | Method for purifying an alcohol from a fermentation broth using a falling film, a wiped film, a thin film or a short path evaporator |
| GB2520101A (en) * | 2013-06-28 | 2015-05-13 | Green Biologics Ltd | Solvent production |
| GB2520101B (en) * | 2013-06-28 | 2017-07-26 | Green Biologics Ltd | Solvent production using monophasic clostridia |
| US10150974B2 (en) | 2013-06-28 | 2018-12-11 | Green Biologics Limited | Solvent production |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2583060B1 (fr) | 1987-09-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20120118827A1 (en) | Method of concentrating low titer fermentation broths using forward osmosis | |
| FR2572094A1 (fr) | Procede pour la preparation continue de l'ethanol | |
| JP2012115783A (ja) | 連続発酵用分離膜モジュールの洗浄方法および連続発酵用膜分離装置 | |
| US20080057553A1 (en) | Fermentation processes and systems | |
| Taleghani et al. | Thin film composite nanofiltration membrane for lactic acid production in membrane bioreactor | |
| EP0791657A1 (fr) | Procédé de production naturelle d'acide formique ou de formiate | |
| FR2583060A1 (fr) | Production de butanol et d'acetone par fermentation avec recyclage de la biomasse par ultrafiltration | |
| JP5262011B2 (ja) | 乳酸の製造方法および製造装置 | |
| FR2555200A1 (fr) | Procede de preparation d'acide lactique par fermentation de lactoserum et installation pour la mise en oeuvre en continu de ce procede | |
| FR2583431A1 (fr) | Procede d'hydrolyse de graisse ou d'huile | |
| JP2011188791A (ja) | 連続発酵装置の運転方法 | |
| FR2974311A1 (fr) | Recyclage de l'eau par osmose inverse dans un procede de production d'un produit d'interet par fermentation | |
| EP0139592A2 (fr) | Procédé et installation de production d'amino-acides par fermentation | |
| JP5458565B2 (ja) | コハク酸塩の製造方法 | |
| EP0967290B1 (fr) | Procédé de production d'Erythritol par fermentation discontinue alimentée répétée | |
| EP0265409A1 (fr) | Procédé de préparation d'acide lactique par fermentation de lactoserum | |
| JP2010161987A (ja) | 発酵によるブタノールの製造方法 | |
| CH665653A5 (fr) | Procede de production d'alcool par fermentation. | |
| WO2012036003A1 (fr) | Procédé de production de produits chimiques par fermentation continue | |
| WO2017051136A1 (fr) | Dispositif de production d'hydrogène | |
| EP0452240A1 (fr) | Procédé et dispositif de fermentation semi-continue, notamment pour la fabrication industrielle d'un mélange biologique à base d'acide propionique | |
| FR2616354A1 (fr) | Procede et appareil d'extraction continue d'ethanol contenu dans une phase aqueuse | |
| FR2816308A1 (fr) | Procede de production en continu d'un sel concentre d'acide succinique | |
| EP0312453B1 (fr) | Procédé de production d'acide pyruvique par fermentation | |
| WO2022002625A1 (fr) | Valorisation de l'acetone par procede de fermentation ibe impliquant des microorganismes genetiquement modifies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ST | Notification of lapse |