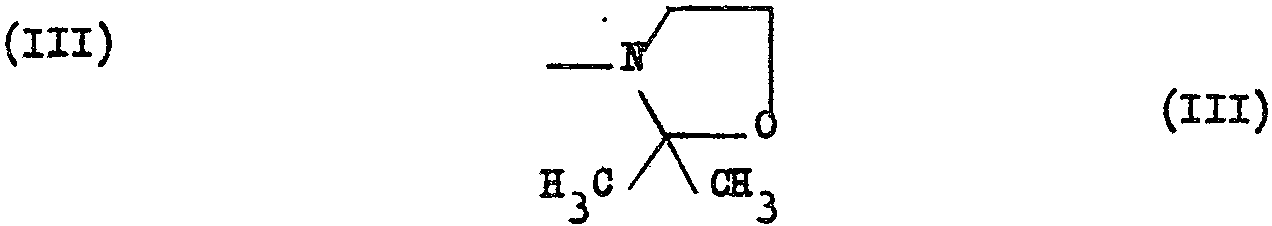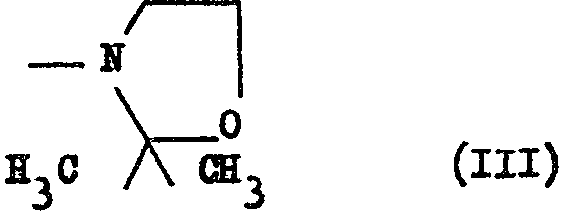FR2544311A2 - Forme medicamenteuse de theophylline a action prolongee - Google Patents
Forme medicamenteuse de theophylline a action prolongee Download PDFInfo
- Publication number
- FR2544311A2 FR2544311A2 FR8306075A FR8306075A FR2544311A2 FR 2544311 A2 FR2544311 A2 FR 2544311A2 FR 8306075 A FR8306075 A FR 8306075A FR 8306075 A FR8306075 A FR 8306075A FR 2544311 A2 FR2544311 A2 FR 2544311A2
- Authority
- FR
- France
- Prior art keywords
- sep
- theophylline
- hydrogen
- cinnamamide
- dimethyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/02—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings
- C07D263/04—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
- A61K31/52—Purines, e.g. adenine
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
Abstract
LE PRESENT PERFECTIONNEMENT CONCERNE DE NOUVELLES FORMES DE THEOPHYLLINE A ACTION PROLONGEE. LA THEOPHYLLINE, SOUS FORME LIBRE OU DE SEL, EST ASSOCIEE A UN COMPOSE REPONDANT A LA FORMULE GENERALE (CF DESSIN DANS BOPI) DANS LAQUELLE R EST L'HYDROGENE, UN HALOGENE OU LE RADICAL ACETYLE; R EST L'HYDROGENE OU LE RADICAL METHYLE; R REPRESENTE UN GROUPE DE
Description
"FORME MEDICAMENTEUSE DE THEOPHYLLINE A ACTION PROLONCEE
Le présent perfectionnement concerne de nouvelles formes de théophylline à action prolongée.
Le présent perfectionnement concerne de nouvelles formes de théophylline à action prolongée.
Selon le brevet principal, la théophylline, sous. forme libre ou de sel, est associée au N-(hydrozy-2 ethyl) oinnamamide, communément désigné "idrocilamide".
Dans le perfectionnement, on décrit un modèle animal mettant en évidence la prolongation de taux sanguins élevés de théophylline obtenue par l'association à l'"idrocilamid".
Ce modèle a permis de découvrir de nouvelles formes de théophylline à action prolongée, dans lesquelles la théophylline sous forme libre ou de sel, est associée à un analogue structural de l'"idrocilamide" répondant à la formule générale (I)
dans laquelle R est l'hydrogène, un halogène ou le radical méthyle 3 R1 est l'hydrogène ou le radical méthyle ; R2 représente un groupe de formule (II)
dans laquelle R3 est l'hydrogène-sauf quand R et R1 sont l'hydrogèneou le radical méthyle ;; R1 et R2 peuvent également former avec l'atome d'azote adjacent le groupe diméthyl-2,2 oxazolidinyl-3 de formule
dans laquelle R est l'hydrogène, un halogène ou le radical méthyle 3 R1 est l'hydrogène ou le radical méthyle ; R2 représente un groupe de formule (II)
dans laquelle R3 est l'hydrogène-sauf quand R et R1 sont l'hydrogèneou le radical méthyle ;; R1 et R2 peuvent également former avec l'atome d'azote adjacent le groupe diméthyl-2,2 oxazolidinyl-3 de formule
Parmi les composés associables à la théophylline on peut citer les dérivés N-(hydroxy-2 éthyl) chloro-4 cinnamamide, N-méthyl,
N-(hydroxy-2 éthyl) cinnamamide, N-[(hydroxy-1 propyl)-2] (chloro-4 cinnsmoyl)-3 diméthyl-2,2 oxazolidine, N-(hydroxy-1 propyl)-2] cinnamamide, fluoro-4 cinnamamide, N-(hydroxy-2 éthyl) acéthyl-4 cinnamamide, diméthyl-2,2 (fluoro-4 cinnamoyl)-3 oxazolidine et cinnamoyl-3 diméthyl2,2 oxazolidine.
N-(hydroxy-2 éthyl) cinnamamide, N-[(hydroxy-1 propyl)-2] (chloro-4 cinnsmoyl)-3 diméthyl-2,2 oxazolidine, N-(hydroxy-1 propyl)-2] cinnamamide, fluoro-4 cinnamamide, N-(hydroxy-2 éthyl) acéthyl-4 cinnamamide, diméthyl-2,2 (fluoro-4 cinnamoyl)-3 oxazolidine et cinnamoyl-3 diméthyl2,2 oxazolidine.
Les dérivés dans la formule desquels R2 est le groupe re- présenté par la formule II sont obtenus selon les techniques décrites dans le brevet frangais 2.040.181 au nom de la demanderesse. On peut par exemple avantageusement condenser un chlorure de cinnamoyle de
avec une amine de formule générale
ayant les memes significations que précédemment.
avec une amine de formule générale
ayant les memes significations que précédemment.
La réaction est mise en oeuvre dans un solvant inerte tel le dioxanne, le tétrahydrofuranne ou le chloroforme, en présence d'un agent alcalin qui peut être un carbonate ou un carbonate alcalin, une base organique comme la pyridine ou la triéthylamine ou encore un excès de l'amine de formule V. La réaction s'effectue à des températures comprises entre 0 C et la température d'ébullition du solvant utilisé.
Le composé I : N-(hydroxy-2 éthyl) chloro-4 cinamamide,
C11H12ClNO2, M = 225,68, cristallise sous forme d'aiguilles blanches de point de fusion 137-138,5 C, à une toxicité exprimée en DL 50 souris P.O de 1.600 mg/kg.
C11H12ClNO2, M = 225,68, cristallise sous forme d'aiguilles blanches de point de fusion 137-138,5 C, à une toxicité exprimée en DL 50 souris P.O de 1.600 mg/kg.
Le composé II : N-méthyl,N-(hydroxy-2 éthyl) cinnamamide,
C12H15NO2, M = 205,25, cristallise sous forme de poudre blanche, FF = 79-81 C, montre une toxicité DL 50 souris P.O de 3.000 mg/kg.
C12H15NO2, M = 205,25, cristallise sous forme de poudre blanche, FF = 79-81 C, montre une toxicité DL 50 souris P.O de 3.000 mg/kg.
Le composé III : N-[(hydroxy-1 propyl)-2] cinnamamide,
C12H15NO2, M = 205,25, cristallise sous forme de petites paillettes blanches, PF = 144-146 C, et montre une toxicité IL 50 souris P.O de 3200 mg/kg.
C12H15NO2, M = 205,25, cristallise sous forme de petites paillettes blanches, PF = 144-146 C, et montre une toxicité IL 50 souris P.O de 3200 mg/kg.
Le composé V : N-(hydroxy-2 éthyl) fluoro-4 cinnamamide,
C11H12FNO2, M = 209,22, F = 100-102 C, a également une DL 50 sourie
P.O supérieure à 3200 mg/kg.
C11H12FNO2, M = 209,22, F = 100-102 C, a également une DL 50 sourie
P.O supérieure à 3200 mg/kg.
Le composé Vi s N-(hydroxy-2 éthyl) acétyl-4 cinnamamide,
C13H1 5NO3, M = 233,26, F = 124-125 C, a une IL 50 souris P.0 de 3.200.
C13H1 5NO3, M = 233,26, F = 124-125 C, a une IL 50 souris P.0 de 3.200.
Les dérivés pour lesquels - NR1H2 représente le groupe diméthyl-2,2-oxazolidinyl-3, peuvent se préparer en condensant dans un premier temps, l'éthanolamine sur l'acétone puis en faisant réagir un chlorure de cinnamoyle (IV) sur l'oxazolidine intermédiaire, qu'il n'est pas nécessaire d'isoler. La réaction s'effectue avantageusement avec un excès d'éthanolamine.
Le composé IV : (chloro-4 cinnamoyl)-3 diméthyl-2,2 oxazolidine, C14H16ClNO2, M = 265,73, sous forme de cristaux blancs, F = 107,5-109,5 C, a une DL 50 souris P.O supérieure à 3.200 mg/kg.
Le composé VII : diméthyl-2,2 fluoro-4 cinnamoyl)-3 osazo- lidine, C14H16FNO2, M = 249,27,F = 106-108 C, a une DL 50 souris P.O de 2000 mg/kg.
Le composé VIII : cinnamoyl-3 diméthyl-2,2 oxazolidine, O H17NO2, M = 231,29, F = 107-109 C a une IL 50 souris P.0 supérieure à 3.200 mg/kg.
Les composés ci-dessus V et VI sont des produits nouveaux et en particulier ceux dans la formule desquels R1 et R2 forment avec ltatome d'azote adjacent le groupe diméthyl-2,2 oxazolidinyl-3.
Le modèle animal mettant en évidenca l'action prolongée de la théophylline associée à l"'idrocilamide" est décrit ci-après.
Des rats mâles, de souche Wistar, pesant 220-240 g, à jeun de nourriture aepuis 16 heures, reçoivent une administration orale de théophylline en solution dans l'eau.
La moitié des animaux reçoit, en même temps que la théophylline, l'idrocilamide en suspension dans la gomme arabique à 5 %, l'autre moitié recevant la gomme arabique seule. 15', 30', 1H, 2H, 3H, 4H, 6H, 8H, après administration de la théophylline, les animaux sont tués par section carotidienne. Le sang est recueilli dans des tubes héparinés et centrifugés, le plasma est décanté. La théophylline est dosée dans les échantillons plasmatiques après extraction par une méthode de chromatographie liquide.
Les moyennes des théophyllinémies obtenues, ainsi que les paramètres pharmacocinétiques calculés, sont donnés dans le tableau 1 ci-dessous :
TABLEAU 1
TABLEAU 1
<tb> <SEP> Concentration <SEP> Animaux <SEP> ayant <SEP> reçu <SEP> s <SEP> Animaux <SEP> ayant <SEP> reçu <SEP> la
<tb> <SEP> en <SEP> mg/l <SEP> de <SEP> la <SEP> théophylline <SEP> seule <SEP> théophylline+idrocilamide <SEP>
<tb> théophylline <SEP> à <SEP> : <SEP> Moyenne <SEP> (écart-type) <SEP> : <SEP> Moyenne <SEP> (écart-type) <SEP> :
<tb> <SEP> 15' <SEP> : <SEP> 17,54 <SEP> (5,77) <SEP> : <SEP> 14,94 <SEP> (3,19) <SEP> : <SEP> NS
<tb> <SEP> 30 <SEP> ' <SEP> : <SEP> <SEP> 20,26 <SEP> (4,88) <SEP> i <SEP> 16,68 <SEP> (2,29) <SEP> <SEP> NS <SEP>
<tb> <SEP> 1 <SEP> H <SEP> :<SEP> 18,86 <SEP> (3,09) <SEP> : <SEP> 15,79 <SEP> (1,39) <SEP> : <SEP> NS
<tb> <SEP> 2 <SEP> H <SEP> s <SEP> 16,69 <SEP> (1,95) <SEP> : <SEP> 17,26 <SEP> (3,46) <SEP> :NS <SEP>
<tb> <SEP> 3 <SEP> H <SEP> : <SEP> 13,93 <SEP> (2,05) <SEP> : <SEP> 17,57 <SEP> (2,21) <SEP> : <SEP> S
<tb> <SEP> 4 <SEP> H <SEP> : <SEP> 11,96 <SEP> (2,43) <SEP> = <SEP> 17,74 <SEP> (1,53) <SEP> : <SEP> S
<tb> <SEP> 6H <SEP> : <SEP> 8,04 <SEP> (2,17) <SEP> 14,10 <SEP> (2,81) <SEP> : <SEP> S
<tb> <SEP> 8H <SEP> : <SEP> 4,32 <SEP> (1,91) <SEP> : <SEP> 11,51 <SEP> (3,26): <SEP> S
<tb> <SEP> Surface# <SEP> 8 <SEP> H <SEP> : <SEP> : <SEP> :
<tb> <SEP> mg/1-1 <SEP> H <SEP> 95,10 <SEP> 123 <SEP> :
<tb> <SEP> : <SEP> :
<tb> <SEP> Demi-vie <SEP> plas- <SEP> . <SEP>
<tb>
<tb> <SEP> en <SEP> mg/l <SEP> de <SEP> la <SEP> théophylline <SEP> seule <SEP> théophylline+idrocilamide <SEP>
<tb> théophylline <SEP> à <SEP> : <SEP> Moyenne <SEP> (écart-type) <SEP> : <SEP> Moyenne <SEP> (écart-type) <SEP> :
<tb> <SEP> 15' <SEP> : <SEP> 17,54 <SEP> (5,77) <SEP> : <SEP> 14,94 <SEP> (3,19) <SEP> : <SEP> NS
<tb> <SEP> 30 <SEP> ' <SEP> : <SEP> <SEP> 20,26 <SEP> (4,88) <SEP> i <SEP> 16,68 <SEP> (2,29) <SEP> <SEP> NS <SEP>
<tb> <SEP> 1 <SEP> H <SEP> :<SEP> 18,86 <SEP> (3,09) <SEP> : <SEP> 15,79 <SEP> (1,39) <SEP> : <SEP> NS
<tb> <SEP> 2 <SEP> H <SEP> s <SEP> 16,69 <SEP> (1,95) <SEP> : <SEP> 17,26 <SEP> (3,46) <SEP> :NS <SEP>
<tb> <SEP> 3 <SEP> H <SEP> : <SEP> 13,93 <SEP> (2,05) <SEP> : <SEP> 17,57 <SEP> (2,21) <SEP> : <SEP> S
<tb> <SEP> 4 <SEP> H <SEP> : <SEP> 11,96 <SEP> (2,43) <SEP> = <SEP> 17,74 <SEP> (1,53) <SEP> : <SEP> S
<tb> <SEP> 6H <SEP> : <SEP> 8,04 <SEP> (2,17) <SEP> 14,10 <SEP> (2,81) <SEP> : <SEP> S
<tb> <SEP> 8H <SEP> : <SEP> 4,32 <SEP> (1,91) <SEP> : <SEP> 11,51 <SEP> (3,26): <SEP> S
<tb> <SEP> Surface# <SEP> 8 <SEP> H <SEP> : <SEP> : <SEP> :
<tb> <SEP> mg/1-1 <SEP> H <SEP> 95,10 <SEP> 123 <SEP> :
<tb> <SEP> : <SEP> :
<tb> <SEP> Demi-vie <SEP> plas- <SEP> . <SEP>
<tb>
<SEP> matique <SEP> en <SEP> H <SEP> 3,47 <SEP> 6,42
<tb> <SEP> Surface# <SEP> @
<tb> <SEP> mg/1-1 <SEP> H <SEP> : <SEP> 116,70 <SEP> 229,60
<tb>
NS = non significatif - S = significatif.
<tb> <SEP> Surface# <SEP> @
<tb> <SEP> mg/1-1 <SEP> H <SEP> : <SEP> 116,70 <SEP> 229,60
<tb>
NS = non significatif - S = significatif.
Ce tableau appelle les constatations suivantes : 1)- La concentration maximale de théophylline n'est pas augmentée 20,26 pour la théophylline seule, 17,74 pour l'association avec l'"idrocilamide" ; 2)-Les concentrations de théophylline obtenues avec l'association sont significativement supérieures à celles obtenues avec la théophyS line seule dès 3 heures après l'administration et la restent jusqu'à la fin de l'essai.A 8 heures la concentration est 2,7 fois plus élevée 3 3)- La demi-vie calculée à partir du maximum est augmentée de 85 % par l'administration simultanée d'"idrocilamide" ; 4)- La surface sous la courbe des concentrations en fonction du temps est augmentée de 29,4 % jusqu'à huit heures et de 166 Vo si extrapolée à l'infini.
Par ce test, on retrouve les résultats décrits chez l'homme, dans le brevet principal, à savoir, la prolongation dans le temps de théophyllinémies élevés grâce à l'administration concomitante d' "idrocilamide".
Sur la figure du dessin annexe sont représentées les courbes des concentrations de théophylline en fonction du temps après une administration de théophylline seule ou avec lt"idrocilamide" et l'on peut découvrir la stabilité de la théophyllinémie après association avec l'idrocilamide et l'augmentation considérable de la biodisponi- bilité. Le temps en heures est porté sur l'axe des absc-sse t (H) et la concentration en mg/l de théophylline Th.mg/l figure sur l'axe des ordonnées. La courbe I correspond à la théophylline seule et la courbe II à l'association théophylline + "idrocilamide".
Ce mode le a permis de découvrir qu'un certain nombre d'analogues structuraux de l'"idrocilamide"possède, chez l'animal, les mêmes propriétés que l'idrocilamide, à savoir, d'augmenter considéra bissent les surfaces sous la courbe de la théophyllinémie en fonction su temps lorsqau'ils sont administrés en même temps que la théophylline. Divers composés concernés par l'invention ont donné, dans le test décrit précédemment, les résultats présentés dans le tableau 2 cidessous.
<SEP> :Conoentration <SEP> : <SEP> Concentration <SEP> : <SEP> Demi-vie <SEP> : <SEP> Surface-@@
<tb> <SEP> maximum <SEP> mg/1 <SEP> à <SEP> 8 <SEP> H <SEP> mg/1 <SEP> plasmatique <SEP> H <SEP> mg/1-1 <SEP> H
<tb> <SEP> : <SEP> : <SEP> : <SEP> :
<tb> <SEP> Composé <SEP> I <SEP> : <SEP> 16,80 <SEP> : <SEP> 12,75 <SEP> : <SEP> 10 <SEP> : <SEP> 306,70
<tb> <SEP> Composé <SEP> II <SEP> : <SEP> 20,50 <SEP> : <SEP> 7,58 <SEP> : <SEP> 4,50 <SEP> : <SEP> 160
<tb> <SEP> Composé <SEP> III <SEP> : <SEP> 19,70 <SEP> : <SEP> 11,86 <SEP> : <SEP> 9,20 <SEP> : <SEP> 286
<tb> <SEP> Composé <SEP> IV <SEP> :: <SEP> 21,30 <SEP> : <SEP> 14,81 <SEP> : <SEP> 11,40 <SEP> : <SEP> 385,60
<tb> <SEP> Composé <SEP> V <SEP> : <SEP> 22,30 <SEP> : <SEP> 15,46 <SEP> : <SEP> 16,10 <SEP> : <SEP> 501,70
<tb> <SEP> Composé <SEP> VI <SEP> : <SEP> 18 <SEP> : <SEP> 10,27 <SEP> :<SEP> 10 <SEP> : <SEP> 269,40
<tb> <SEP> Composé <SEP> VII <SEP> : <SEP> 21,17 <SEP> : <SEP> 11,93 <SEP> : <SEP> 8,5 <SEP> : <SEP> 294
<tb> <SEP> Composé <SEP> VIII <SEP> : <SEP> 22,5 <SEP> : <SEP> 13,36 <SEP> : <SEP> 7,3 <SEP> : <SEP> 288,7
<tb> <SEP> Théophylline <SEP> : <SEP> : <SEP> : <SEP> :
<tb> <SEP> seule <SEP> : <SEP> 20,26 <SEP> : <SEP> 4,32 <SEP> : <SEP> 3,47 <SEP> : <SEP> 116,70
<tb> <SEP> : <SEP> : <SEP> : <SEP> :
<tb>
L'association de la théophylline et d'un analogue structural du N-(hydroxy-2 éthyl) cinnamamide constitue un médicament utilisable dans les applications de la théophylline et dérivés, notamment dans le traitement de l'asthme.
<tb> <SEP> maximum <SEP> mg/1 <SEP> à <SEP> 8 <SEP> H <SEP> mg/1 <SEP> plasmatique <SEP> H <SEP> mg/1-1 <SEP> H
<tb> <SEP> : <SEP> : <SEP> : <SEP> :
<tb> <SEP> Composé <SEP> I <SEP> : <SEP> 16,80 <SEP> : <SEP> 12,75 <SEP> : <SEP> 10 <SEP> : <SEP> 306,70
<tb> <SEP> Composé <SEP> II <SEP> : <SEP> 20,50 <SEP> : <SEP> 7,58 <SEP> : <SEP> 4,50 <SEP> : <SEP> 160
<tb> <SEP> Composé <SEP> III <SEP> : <SEP> 19,70 <SEP> : <SEP> 11,86 <SEP> : <SEP> 9,20 <SEP> : <SEP> 286
<tb> <SEP> Composé <SEP> IV <SEP> :: <SEP> 21,30 <SEP> : <SEP> 14,81 <SEP> : <SEP> 11,40 <SEP> : <SEP> 385,60
<tb> <SEP> Composé <SEP> V <SEP> : <SEP> 22,30 <SEP> : <SEP> 15,46 <SEP> : <SEP> 16,10 <SEP> : <SEP> 501,70
<tb> <SEP> Composé <SEP> VI <SEP> : <SEP> 18 <SEP> : <SEP> 10,27 <SEP> :<SEP> 10 <SEP> : <SEP> 269,40
<tb> <SEP> Composé <SEP> VII <SEP> : <SEP> 21,17 <SEP> : <SEP> 11,93 <SEP> : <SEP> 8,5 <SEP> : <SEP> 294
<tb> <SEP> Composé <SEP> VIII <SEP> : <SEP> 22,5 <SEP> : <SEP> 13,36 <SEP> : <SEP> 7,3 <SEP> : <SEP> 288,7
<tb> <SEP> Théophylline <SEP> : <SEP> : <SEP> : <SEP> :
<tb> <SEP> seule <SEP> : <SEP> 20,26 <SEP> : <SEP> 4,32 <SEP> : <SEP> 3,47 <SEP> : <SEP> 116,70
<tb> <SEP> : <SEP> : <SEP> : <SEP> :
<tb>
L'association de la théophylline et d'un analogue structural du N-(hydroxy-2 éthyl) cinnamamide constitue un médicament utilisable dans les applications de la théophylline et dérivés, notamment dans le traitement de l'asthme.
Les proportions du dérivé cinnamamide substitué dans l'as sociation sont adaptées, en particulier à l'age et au poids des malades. Ce dérivé exerce une action au niveau de la métabolisation de la théophylline, meme à faible dose. Il peut être associé à la théophyl line dans un rapport pouvant varier de 0,1 à 4 suivant le sujet et la forme galénique.
La théophylline peut être introduite dans l'association sous,forme libre ou combinée par exemple avec l'éthylène diamine (euphylline, aminophyllane). On peut envisage l'emploi en addition de théophylline et aminophylline
La dose unitaire en association principe actif théophylline ou dérivé + cinnamamide substitué peut varier entre 50 et 1.200mg.
La dose unitaire en association principe actif théophylline ou dérivé + cinnamamide substitué peut varier entre 50 et 1.200mg.
On peut proposer un traitement en deux prises par jour espacées de douze heures.
Il est donné ci-après, à titre illustratif quelques formulations associant la théophylline ou l'aminophylline à un composé cin namamide substitué selon l'invention, utilisables en thérapeutique.
Les proportions du drivé cinnamamide dans l'association sont variables afin de tenir compte, en particulier, de l'age et du poids des malades.
n 1-Comprimés
Théophylline 200 mg
Cinnamamide substitué 200 mg
Lactose 34 mg
Amidon 33 mg
Gélatine 10 mg
Acide alginique 20 mg
Stéarate de magnésium - 3 mg
500 mg n 2-Comprimés sécables en bâtonnets"
Théophylline 200 mg
Cinnamamide substitué 400 mg
Lactose 50 mg
Amidon 50 mg
Gélatine 15 mg
Acide alginique 30 mg
Stéarate de magnésium 5 mg
750 mg n0 3-Comprimés dragéifiés
Théophylline 200 mg 100 mg
Cinnamamide substitué 100 mg 100 mg
Lactose 37 mg 40 mg
Amidon 36 mg 40 mg
Gélatine 8 mg 6 mg
Acide alginique 16 mg 12 mg
Stéarate de magnésium 3 mg 2 mg
400 mg 300 mg
Enrobage de dragéifica
tion qe 600 mg 500 mg
Enrobage de dragéification : sucreS gomme arabique, gélatine, tale, cire blanche.
Théophylline 200 mg
Cinnamamide substitué 200 mg
Lactose 34 mg
Amidon 33 mg
Gélatine 10 mg
Acide alginique 20 mg
Stéarate de magnésium - 3 mg
500 mg n 2-Comprimés sécables en bâtonnets"
Théophylline 200 mg
Cinnamamide substitué 400 mg
Lactose 50 mg
Amidon 50 mg
Gélatine 15 mg
Acide alginique 30 mg
Stéarate de magnésium 5 mg
750 mg n0 3-Comprimés dragéifiés
Théophylline 200 mg 100 mg
Cinnamamide substitué 100 mg 100 mg
Lactose 37 mg 40 mg
Amidon 36 mg 40 mg
Gélatine 8 mg 6 mg
Acide alginique 16 mg 12 mg
Stéarate de magnésium 3 mg 2 mg
400 mg 300 mg
Enrobage de dragéifica
tion qe 600 mg 500 mg
Enrobage de dragéification : sucreS gomme arabique, gélatine, tale, cire blanche.
N 4-Comprimés gastrorésistants
Préparation des comprimes selon la formule n03. Avant dragéification les comprimés sont rendus gastrorésistants par application de phtalate d'hydroxyproylméthylcellulose en solution dans 1 'acétone-isopropanol.
Préparation des comprimes selon la formule n03. Avant dragéification les comprimés sont rendus gastrorésistants par application de phtalate d'hydroxyproylméthylcellulose en solution dans 1 'acétone-isopropanol.
n 5-Suppositoires
Aminophylline 300 mg
Cinnamamide substitué 100 mg
Glycérides semi-synthétiques qsq 1 suppositoire
d'environ 3 g n06 - Solution injectable
Théophylline 100 mg 50 mg
Cinnamamide substitue 15 mg 15 mg
Anisate de sodium 300 mg 150 mg
Ethanol à 96 0,25 ml 0,25 ml
eau ppi qsp 5 ml 5 ml
Il est donné ci-après des exemples préparatifs de quelques produits chimiques nouveaux utilisés en association avec la théophylline.
Aminophylline 300 mg
Cinnamamide substitué 100 mg
Glycérides semi-synthétiques qsq 1 suppositoire
d'environ 3 g n06 - Solution injectable
Théophylline 100 mg 50 mg
Cinnamamide substitue 15 mg 15 mg
Anisate de sodium 300 mg 150 mg
Ethanol à 96 0,25 ml 0,25 ml
eau ppi qsp 5 ml 5 ml
Il est donné ci-après des exemples préparatifs de quelques produits chimiques nouveaux utilisés en association avec la théophylline.
Exemple 1. Composé IV. (chloro-4 cinnamoyl)-3 diméthyl-2,2 oxazolidine
On ajoute goutte à goutte 13,4 g (0,22 mole) d'éthanolamine à 30 cm3 d'acétone. Le mélange s'échauffe. Lorsqu'il est revenu à température ambiante, on ajoute, en maintenant la température entre 15 et 200C, une solution de 18,3 g (0,09 mole) de chlorure de chloro4 cinnamoyle dans 30 cm3 d'acétone puis agite 2 heures à température ambiante. Le milieu réactionnel est dilué à l'eau. La (chloro-4 cinnamoyle-3 diméthyl-2,2 oxazolidine se sépare sous forme de cristaux blancs. Elle est filtrée, lavée à l'eau, séchée et recristallisée dans l'heptane. F = 107,5 - 109,5 C.
On ajoute goutte à goutte 13,4 g (0,22 mole) d'éthanolamine à 30 cm3 d'acétone. Le mélange s'échauffe. Lorsqu'il est revenu à température ambiante, on ajoute, en maintenant la température entre 15 et 200C, une solution de 18,3 g (0,09 mole) de chlorure de chloro4 cinnamoyle dans 30 cm3 d'acétone puis agite 2 heures à température ambiante. Le milieu réactionnel est dilué à l'eau. La (chloro-4 cinnamoyle-3 diméthyl-2,2 oxazolidine se sépare sous forme de cristaux blancs. Elle est filtrée, lavée à l'eau, séchée et recristallisée dans l'heptane. F = 107,5 - 109,5 C.
Analyse oentésimale C14H16ClNO2. M = 265,73
C % H % Cl % N%
Calculé : 63,29 6,07 13s35 5,27
Trouvé s 63,16 6,20 13,40 5,28
I.R. (KBr) #(C=O)= 1660 cm-
R.M.N(CDCl3) # = 1,7 (singulet, 4H)
3,6 - 4,4 (multiplet, 4H)
6,6 (doublet, J = 14 Hz, 1H)
7,2 - 7,6 (massif complexe, 4H)
7,6 (doublet, J = 14 Hz, 1H).
C % H % Cl % N%
Calculé : 63,29 6,07 13s35 5,27
Trouvé s 63,16 6,20 13,40 5,28
I.R. (KBr) #(C=O)= 1660 cm-
R.M.N(CDCl3) # = 1,7 (singulet, 4H)
3,6 - 4,4 (multiplet, 4H)
6,6 (doublet, J = 14 Hz, 1H)
7,2 - 7,6 (massif complexe, 4H)
7,6 (doublet, J = 14 Hz, 1H).
Exemple 2. Composé V. N-(hydroxy-2 éthyl) fluoro-4 cinnamamide.
Une solution de 374 g (2,03 moles) de chlorure de fluoro4 cinnamoyle dans 2 1 de dioxanne est ajoutéè goutte à goutte à 20 C, à une solution de 297 g (4,87 moles) d'éthanolamine dans 2 1 de diovanne. Le milieu réactionnel est agité 3 heures à température ambiante abandonné une nuit et concentré sous pression réduite. Le résidu est repris par une solution de bicarbonate de sodium. Le précipité de
N-(hydroxy-2 éthyl) fluoro-4 cinnamamide est filtré, lavé à l'eau et séché. Rdt 351 g (soit 83 % de la théorie). Le produit est purifié par recristallisation dans l'acétate d'éthyle. F = 100-102 C.
N-(hydroxy-2 éthyl) fluoro-4 cinnamamide est filtré, lavé à l'eau et séché. Rdt 351 g (soit 83 % de la théorie). Le produit est purifié par recristallisation dans l'acétate d'éthyle. F = 100-102 C.
Analyse centésimale C11H12FNO2 M = 209,22
C % H % F % N %
Calculé : 63,14 5,78 9,08 6,70
Trouvé : 63,09 5,68 9,32 6,72
I.R. (KBr) : # (C=O) = 1660 cm-
Exemple 3. Composé VI. N-(hydroxy-2 éthyl) acétyl-4 cinnamamide
Un mélange de 9,5 g (0,05 mole) d'acide acétyl-4 cinnamique [obtenu selon G.H. cleland J. Org. Chem. 34, 744 (1969)] de 30 g de chlorure de thionyle et de 40 cm3 de benzène est porté 20 minutes à reflux. La solution est concentrée à sec sous pression réduite. Le solide résiduel est dissous dans 100 cm3 de dioxanne et la solution obtenue est ajoutée goutte à goutte, à une température de 200C à une solution de 9,3 g (0,15 5 mole) d'éthanolamine dans 50 cm3 de dioxanne.
C % H % F % N %
Calculé : 63,14 5,78 9,08 6,70
Trouvé : 63,09 5,68 9,32 6,72
I.R. (KBr) : # (C=O) = 1660 cm-
Exemple 3. Composé VI. N-(hydroxy-2 éthyl) acétyl-4 cinnamamide
Un mélange de 9,5 g (0,05 mole) d'acide acétyl-4 cinnamique [obtenu selon G.H. cleland J. Org. Chem. 34, 744 (1969)] de 30 g de chlorure de thionyle et de 40 cm3 de benzène est porté 20 minutes à reflux. La solution est concentrée à sec sous pression réduite. Le solide résiduel est dissous dans 100 cm3 de dioxanne et la solution obtenue est ajoutée goutte à goutte, à une température de 200C à une solution de 9,3 g (0,15 5 mole) d'éthanolamine dans 50 cm3 de dioxanne.
Le mélange est agité 1 heure à température ambiante, versé dans un mélange de 500 g de glace et de 20 cm3 d'acide chlorhydrique iON puis extrait au chloroforme. La phase organique est lavée à l'eau et séchée sur sulfate de sodium. Par évaporation du solvant sous pression réduite on obtient le N-(hydroxy-2 éthyl) acétyl-4 cinnamamide qui est purifié par recristallisation dans l'acétate d'ethyle. F = 124-125 C.
Rdt 5 4,2 g (36 % de la théorie).
Analyse centésimale C13H15NO3 M = 233,26
C % H % N %
Calculé : 66,93 6,48 6,01
Trouvé t 66,80 6,35 6,12
I.R. (KBr): # (C=O) = 1680 et 1660 cm-
Exemple 4. Composé VII. Diméthyl-2,2 (fluoro-4 cinnamoyl)-3 oxazolidine
En opérant comme dans l'exemple 1 à partir de chlorure de fluoro-4 cinnamoyle, on obtient la (fluoro-4 cinnamoyl)-3 diméthyl-2,2 oxazolidine. Rdt : 77 %. F = 106-108 C (hexane-acétate d'éthyle).
C % H % N %
Calculé : 66,93 6,48 6,01
Trouvé t 66,80 6,35 6,12
I.R. (KBr): # (C=O) = 1680 et 1660 cm-
Exemple 4. Composé VII. Diméthyl-2,2 (fluoro-4 cinnamoyl)-3 oxazolidine
En opérant comme dans l'exemple 1 à partir de chlorure de fluoro-4 cinnamoyle, on obtient la (fluoro-4 cinnamoyl)-3 diméthyl-2,2 oxazolidine. Rdt : 77 %. F = 106-108 C (hexane-acétate d'éthyle).
Analyse centésimale C14H16FNO2 M = 249,27.
C % H % F % N %
Calculé : 67,45 6,47 7,62 5,62
Trouvé : 67,43 6,65 7,71 5,73
Exemple 5. Compos6 VIII. Cinnamoyl-3 diméthyl-2,2 oxazolidine.
Calculé : 67,45 6,47 7,62 5,62
Trouvé : 67,43 6,65 7,71 5,73
Exemple 5. Compos6 VIII. Cinnamoyl-3 diméthyl-2,2 oxazolidine.
En opérant comme dans l'exemple 1 à partir du chlorure de cinnamoyle, on obtient la cinnamoyl-3 diméthyl-2,2 oxazolidine. Rdt : 74%. F = 107-109 C (hexane-acétate d'éthyle).
Analyse centésimale C14H17NO2 M = 231,29. C % H % N %
Calculé : 72,69 C %. 7,41 H % . 6,06 N %. Trouvé : 72,62 7,42 6,05
Calculé : 72,69 C %. 7,41 H % . 6,06 N %. Trouvé : 72,62 7,42 6,05
Claims (9)
1. Médicament à base de théophylline à action prolongée selon le brevet principal, revendication 1, caractérisé en l'association de la théophylline (diméthyl-1,3 xanthine) ou dérivé à un composé du type cinnamamide substitué répondant à la formule générale
dans laquelle R est l'hydrogène, un halogène ou le radical acétyle ;
R1 est l'hydrogène ou le radical méthyle ;; R2 représente un groupe de formule (II)
dans laquelle R3 est l'hydrogène - sauf quand R et R1 sont l'hydrogène - ou le radical méthyle 3 R1 et R2 peuvent également former avec l'atome d'azote adjacent le groupe diméthyl- 2,2 oxazolidinyl-3 de formule III s
2. Médicament à base de théophylline selon la revendication 1 caractérisé par l'association de la théophylline ou dérivé au (oBloro-4 cinnamoyl-3 diméthyl-2, 2 orazolidine).
3. Médicament à base de théophylline selon la revendication 1, caractérisé par l'association de la théophylline ou dérivé au cin- namoyl-3 diméthyl-2,2 orazolidine.
4. Médicament selon la revendication 1, caractérisé en ce que la dose unitaire en association principe actif théophylline ou dérivé + cinnamamide substitué est comprise entre 50 et 1.200 mg.
5. Médicament selon la revendication 1, caractérisé en ce que la xanthine introduite dans l'association est la théophylline sous forme libre ou combinée avec l'éthylène diamine dite aminophylline, seule ou en mélange.
6. Médicament selon la revendication 1, caractérisé en ce qu'il est présenté sous forme de comprimés, ampoules injectables ou suppositoires.
7. Médicament selon la revendication 1 utilisable dans le traitement de l'asthme.
9. N-(hydroxy-2 éthyl) acétyl-4 cinnamamide.
Priority Applications (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR8306075A FR2544311A2 (fr) | 1983-04-14 | 1983-04-14 | Forme medicamenteuse de theophylline a action prolongee |
| CA000426747A CA1197512A (fr) | 1983-04-14 | 1983-04-26 | Preparation de derives cinnamamides substitues et produits obtenus |
| EP83400829A EP0094283B1 (fr) | 1982-05-04 | 1983-04-27 | Forme médicamenteuse de théophylline à action prolongée |
| DE8383400829T DE3361275D1 (en) | 1982-05-04 | 1983-04-27 | Sustained-release theophyllin drug formulation |
| AT83400829T ATE16566T1 (de) | 1982-05-04 | 1983-04-27 | Arzneimittelform von theophyllin mit verlaengerter wirkung. |
| IL68535A IL68535A (en) | 1982-05-04 | 1983-04-29 | Long-acting pharmaceutical compositions containing theo-phylline and cinnamic acid derivatives and certain such novel cinnamic acid derivatives |
| NZ204072A NZ204072A (en) | 1982-05-04 | 1983-05-02 | Pharmaceutical compositions which contain theophylline as active ingredient |
| IE1004/83A IE54903B1 (en) | 1982-05-04 | 1983-05-02 | Long-acting theophylline in medicinal form |
| US06/491,025 US4512994A (en) | 1982-05-04 | 1983-05-03 | Long-acting theophylline in medicinal form |
| CA000427333A CA1199582A (fr) | 1982-05-04 | 1983-05-03 | Forme medicamenteuse de theophylline a action prolongee |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR8306075A FR2544311A2 (fr) | 1983-04-14 | 1983-04-14 | Forme medicamenteuse de theophylline a action prolongee |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2544311A2 true FR2544311A2 (fr) | 1984-10-19 |
| FR2544311B2 FR2544311B2 (fr) | 1985-04-19 |
Family
ID=9287831
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR8306075A Granted FR2544311A2 (fr) | 1982-05-04 | 1983-04-14 | Forme medicamenteuse de theophylline a action prolongee |
Country Status (2)
| Country | Link |
|---|---|
| CA (1) | CA1197512A (fr) |
| FR (1) | FR2544311A2 (fr) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2040181A1 (fr) * | 1969-04-02 | 1971-01-22 | Lipha | |
| EP0094283A1 (fr) * | 1982-05-04 | 1983-11-16 | Lipha, Lyonnaise Industrielle Pharmaceutique | Forme médicamenteuse de théophylline à action prolongée |
-
1983
- 1983-04-14 FR FR8306075A patent/FR2544311A2/fr active Granted
- 1983-04-26 CA CA000426747A patent/CA1197512A/fr not_active Expired
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2040181A1 (fr) * | 1969-04-02 | 1971-01-22 | Lipha | |
| EP0094283A1 (fr) * | 1982-05-04 | 1983-11-16 | Lipha, Lyonnaise Industrielle Pharmaceutique | Forme médicamenteuse de théophylline à action prolongée |
Non-Patent Citations (3)
| Title |
|---|
| CHEMICAL ABSTRACTS, vol. 92, no. 25, 23 juin 1980, page 13, résumé no. 208747f, COLUMBUS, Ohio (US) * |
| CHIMIE THERAPEUTIQUE, vol. VIII, no. 2, mars-avril 1973, PARIS (FR) * |
| EUROPEAN JOURNAL OF MEDICINAL CHEMISTRY, CHIMICA THERAPEUTICA, vol. IX, septembre-octobre 1974, CHATENAY-MALABRY * |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2544311B2 (fr) | 1985-04-19 |
| CA1197512A (fr) | 1985-12-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0370901B1 (fr) | Nouveaux dérivés du chromanne actifs sur le système nerveux central, leur procédé de préparation et les compositions pharmaceutiques en contenant | |
| EP0040591A1 (fr) | Dérivés de pyridoxine, leur procédé de préparation ainsi que leur utilisation en thérapeutique | |
| EP0003383A2 (fr) | Dérivés de 4-amino-3-sulfonamido-pyridine | |
| EP0073161B1 (fr) | Nouveaux dérivés de la pyrazine actifs sur le système nerveux central | |
| FR2561647A1 (fr) | Derives de 1-(hydroxymethyl)-1,6,7,11b-tetrahydro-2h,4h-(1,3)-oxazino- ou -thiazino(4,3,a)isoquinoleine, procede pour leur preparation et compositions pharmaceutiques les contenant | |
| EP0109866B1 (fr) | Nouveaux dérivés de la sulfonylurée, leurs procédés de préparation et les compositions pharmaceutiques les renfermant | |
| FR2514761A1 (fr) | Nouvelles 1,4-dihydropyridines, utiles notamment comme hypotenseurs | |
| EP0138721A2 (fr) | Nouveaux benzenesulfonyl-lactames, leur procédé de préparation et leur application comme substance active de compositions pharmaceutiques | |
| FR2612517A1 (fr) | Derives de benzoxazine, procedes de preparation de ces derives et compositions pharmaceutiques les contenant | |
| EP0348257A2 (fr) | Nouveaux dérivés d'(hétéro)aryl diazole, leur procédé de préparation et leur application en thérapeutique | |
| EP0259206B1 (fr) | Dérivés de la dihydro-1,4 pyridine leurs procédés de préparation et les compositions pharmaceutiques qui les contiennent | |
| EP0000452B1 (fr) | Dérivés d'oxadiazole-1,2,4, leur préparation et leur application en thérapeutique. | |
| EP0094283B1 (fr) | Forme médicamenteuse de théophylline à action prolongée | |
| EP0196943B1 (fr) | Nouveaux dérivés 8-thiotétrahydroquinoléines et leurs sels | |
| FR2615188A1 (fr) | Derives d'hydrazine, procede d'obtention et compositions pharmaceutiques les contenant | |
| EP0008259A1 (fr) | Nouveaux dérivés de la pipéridylbenzimidazolinone, leurs procédés de préparation et les compositions pharmaceutiques les renfermant | |
| EP0079810A1 (fr) | Nouveaux dérivés de la phényl-4 quinazoline actifs sur le système nerveux central | |
| EP0138684B1 (fr) | 2-(N-pyrrolidino)-3-isobutoxy-N-phenyl substitué N-benzyl propylamines, leur préparation et leur application pharmaceutique | |
| EP0005091B1 (fr) | Nouvelles pipérazines monosubstituées, leurs procédés de préparation et les compositions pharmaceutiques les renfermant | |
| FR2506769A2 (fr) | Para-((cyano-5 n pentyl-1) phenyl)-3 methoxymethyl-5 oxazolidinone-2, son procede de preparation et ses applications en therapeutique | |
| FR2544311A2 (fr) | Forme medicamenteuse de theophylline a action prolongee | |
| EP0105881B1 (fr) | Nouvelles cyanoguanidines, leur procede d'obtention et les compositions pharmaceutiques en renfermant | |
| EP0100257B1 (fr) | Nouveaux dérivés aminoalkyl naphtaléniques, leurs sels d'addition d'acide et le procédé de préparation ainsi que l'application en thérapeutique de ces dérivés et sels | |
| CH620678A5 (en) | Process for the preparation of a derivative of piperidine | |
| FR2508032A1 (fr) | Nouveaux derives amino-3 aryloxymethyl-2 propanol-1, leur procede de preparation et leurs applications en therapeutique |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ER | Errata listed in the french official journal (bopi) |
Free format text: 42/84 |