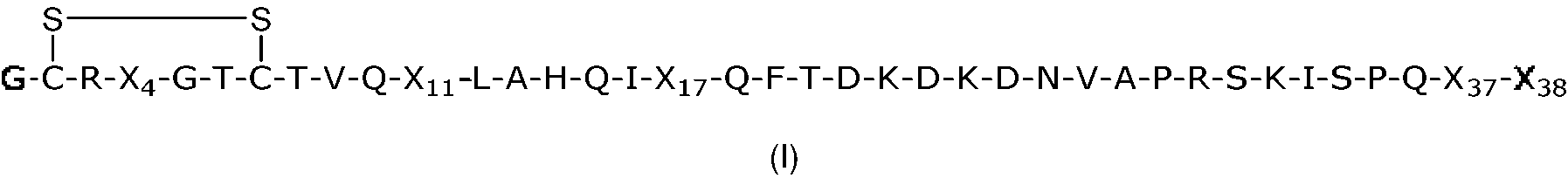ES2950137T3 - Análogos de hAM15-52 con potencia mejorada frente al receptor de amilina (hAMY3R) - Google Patents
Análogos de hAM15-52 con potencia mejorada frente al receptor de amilina (hAMY3R) Download PDFInfo
- Publication number
- ES2950137T3 ES2950137T3 ES21782735T ES21782735T ES2950137T3 ES 2950137 T3 ES2950137 T3 ES 2950137T3 ES 21782735 T ES21782735 T ES 21782735T ES 21782735 T ES21782735 T ES 21782735T ES 2950137 T3 ES2950137 T3 ES 2950137T3
- Authority
- ES
- Spain
- Prior art keywords
- ham
- identity
- hamy3r
- seq
- amino acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 108091005466 amylin receptors Proteins 0.000 title abstract description 27
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 8
- 229910052721 tungsten Inorganic materials 0.000 claims description 207
- 229910052727 yttrium Inorganic materials 0.000 claims description 184
- 229910052731 fluorine Inorganic materials 0.000 claims description 168
- 229910052739 hydrogen Inorganic materials 0.000 claims description 138
- 150000001413 amino acids Chemical class 0.000 claims description 124
- 229910052740 iodine Inorganic materials 0.000 claims description 124
- 229910052799 carbon Inorganic materials 0.000 claims description 54
- 101100394230 Caenorhabditis elegans ham-1 gene Proteins 0.000 claims description 38
- 101100045395 Mus musculus Tap1 gene Proteins 0.000 claims description 38
- 150000003839 salts Chemical class 0.000 claims description 36
- 229910052717 sulfur Inorganic materials 0.000 claims description 32
- 229910052698 phosphorus Inorganic materials 0.000 claims description 22
- 239000003814 drug Substances 0.000 claims description 3
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 3
- 239000003937 drug carrier Substances 0.000 claims description 2
- 125000003275 alpha amino acid group Chemical group 0.000 claims 2
- 108090000765 processed proteins & peptides Proteins 0.000 abstract description 27
- 102000004196 processed proteins & peptides Human genes 0.000 abstract description 20
- ULCUCJFASIJEOE-NPECTJMMSA-N adrenomedullin Chemical group C([C@@H](C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)NCC(=O)N[C@@H]1C(N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)NCC(=O)N[C@H](C(=O)N[C@@H](CSSC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(N)=O)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)[C@@H](C)O)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=CC=C1 ULCUCJFASIJEOE-NPECTJMMSA-N 0.000 abstract description 18
- 208000008589 Obesity Diseases 0.000 abstract description 17
- 235000020824 obesity Nutrition 0.000 abstract description 17
- 238000011282 treatment Methods 0.000 abstract description 13
- 206010012601 diabetes mellitus Diseases 0.000 abstract description 12
- 239000000556 agonist Substances 0.000 abstract description 10
- 229920001184 polypeptide Polymers 0.000 abstract description 10
- 206010053219 non-alcoholic steatohepatitis Diseases 0.000 abstract description 5
- 235000001014 amino acid Nutrition 0.000 description 95
- 229940024606 amino acid Drugs 0.000 description 91
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 56
- 230000036515 potency Effects 0.000 description 39
- 108010041872 Islet Amyloid Polypeptide Proteins 0.000 description 28
- 102000036770 Islet Amyloid Polypeptide Human genes 0.000 description 28
- 102000005962 receptors Human genes 0.000 description 20
- 108020003175 receptors Proteins 0.000 description 20
- 206010061592 cardiac fibrillation Diseases 0.000 description 14
- 210000004027 cell Anatomy 0.000 description 14
- 230000002600 fibrillogenic effect Effects 0.000 description 14
- 108091005468 AM1R Proteins 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- 238000003556 assay Methods 0.000 description 11
- JADVWWSKYZXRGX-UHFFFAOYSA-M thioflavine T Chemical group [Cl-].C1=CC(N(C)C)=CC=C1C1=[N+](C)C2=CC=C(C)C=C2S1 JADVWWSKYZXRGX-UHFFFAOYSA-M 0.000 description 11
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 10
- 230000037406 food intake Effects 0.000 description 10
- 235000012631 food intake Nutrition 0.000 description 10
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 10
- 101001081479 Homo sapiens Islet amyloid polypeptide Proteins 0.000 description 8
- 230000003389 potentiating effect Effects 0.000 description 8
- 108060001064 Calcitonin Proteins 0.000 description 7
- 108090000932 Calcitonin Gene-Related Peptide Proteins 0.000 description 7
- 230000037396 body weight Effects 0.000 description 7
- 230000003247 decreasing effect Effects 0.000 description 7
- 239000011347 resin Substances 0.000 description 7
- 229920005989 resin Polymers 0.000 description 7
- 238000007920 subcutaneous administration Methods 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 101800004616 Adrenomedullin Proteins 0.000 description 6
- 102000004379 Adrenomedullin Human genes 0.000 description 6
- 102000055006 Calcitonin Human genes 0.000 description 6
- 102000004414 Calcitonin Gene-Related Peptide Human genes 0.000 description 6
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 241000700159 Rattus Species 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 235000005911 diet Nutrition 0.000 description 6
- 230000037213 diet Effects 0.000 description 6
- 201000010099 disease Diseases 0.000 description 6
- 239000012634 fragment Substances 0.000 description 6
- FSYKKLYZXJSNPZ-UHFFFAOYSA-N sarcosine Chemical compound C[NH2+]CC([O-])=O FSYKKLYZXJSNPZ-UHFFFAOYSA-N 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 238000006467 substitution reaction Methods 0.000 description 6
- 108010001789 Calcitonin Receptors Proteins 0.000 description 5
- 102100024654 Calcitonin gene-related peptide type 1 receptor Human genes 0.000 description 5
- 101710118454 Calcitonin gene-related peptide type 1 receptor Proteins 0.000 description 5
- 102100038520 Calcitonin receptor Human genes 0.000 description 5
- 102000004877 Insulin Human genes 0.000 description 5
- 108090001061 Insulin Proteins 0.000 description 5
- BBBFJLBPOGFECG-VJVYQDLKSA-N calcitonin Chemical compound N([C@H](C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(N)=O)C(C)C)C(=O)[C@@H]1CSSC[C@H](N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1 BBBFJLBPOGFECG-VJVYQDLKSA-N 0.000 description 5
- 229960004015 calcitonin Drugs 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 230000008878 coupling Effects 0.000 description 5
- 238000010168 coupling process Methods 0.000 description 5
- 238000005859 coupling reaction Methods 0.000 description 5
- 229940125396 insulin Drugs 0.000 description 5
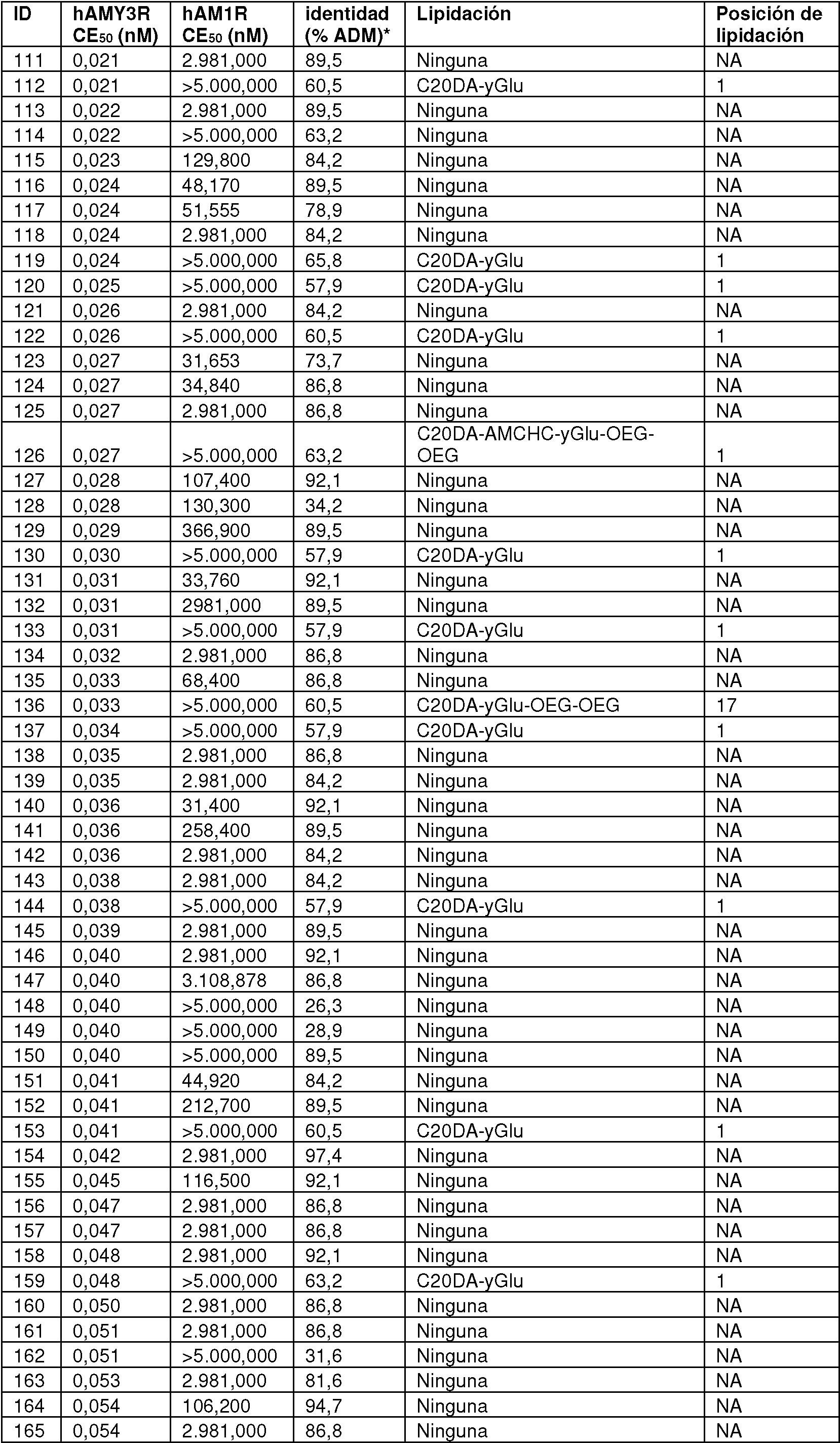
- 230000029226 lipidation Effects 0.000 description 5
- 208000030159 metabolic disease Diseases 0.000 description 5
- 235000018102 proteins Nutrition 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 5
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 4
- 238000011835 investigation Methods 0.000 description 4
- 230000002503 metabolic effect Effects 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 238000007637 random forest analysis Methods 0.000 description 4
- 235000000346 sugar Nutrition 0.000 description 4
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- BYEAHWXPCBROCE-UHFFFAOYSA-N 1,1,1,3,3,3-hexafluoropropan-2-ol Chemical compound FC(F)(F)C(O)C(F)(F)F BYEAHWXPCBROCE-UHFFFAOYSA-N 0.000 description 3
- FUOOLUPWFVMBKG-UHFFFAOYSA-N 2-Aminoisobutyric acid Chemical compound CC(C)(N)C(O)=O FUOOLUPWFVMBKG-UHFFFAOYSA-N 0.000 description 3
- 208000024172 Cardiovascular disease Diseases 0.000 description 3
- 108010077895 Sarcosine Proteins 0.000 description 3
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 3
- 230000008484 agonism Effects 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 238000010511 deprotection reaction Methods 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 239000000813 peptide hormone Substances 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- 230000009897 systematic effect Effects 0.000 description 3
- OZFAFGSSMRRTDW-UHFFFAOYSA-N (2,4-dichlorophenyl) benzenesulfonate Chemical compound ClC1=CC(Cl)=CC=C1OS(=O)(=O)C1=CC=CC=C1 OZFAFGSSMRRTDW-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- -1 Cit Chemical compound 0.000 description 2
- 239000012591 Dulbecco’s Phosphate Buffered Saline Substances 0.000 description 2
- 238000001061 Dunnett's test Methods 0.000 description 2
- 208000032928 Dyslipidaemia Diseases 0.000 description 2
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 2
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 2
- 102400000321 Glucagon Human genes 0.000 description 2
- 108060003199 Glucagon Proteins 0.000 description 2
- 208000002705 Glucose Intolerance Diseases 0.000 description 2
- 101000584583 Homo sapiens Receptor activity-modifying protein 1 Proteins 0.000 description 2
- 101000584590 Homo sapiens Receptor activity-modifying protein 2 Proteins 0.000 description 2
- 101000584593 Homo sapiens Receptor activity-modifying protein 3 Proteins 0.000 description 2
- 206010020772 Hypertension Diseases 0.000 description 2
- 208000031773 Insulin resistance syndrome Diseases 0.000 description 2
- RHGKLRLOHDJJDR-BYPYZUCNSA-N L-citrulline Chemical compound NC(=O)NCCC[C@H]([NH3+])C([O-])=O RHGKLRLOHDJJDR-BYPYZUCNSA-N 0.000 description 2
- 208000017170 Lipid metabolism disease Diseases 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 201000010769 Prader-Willi syndrome Diseases 0.000 description 2
- 102100030697 Receptor activity-modifying protein 1 Human genes 0.000 description 2
- 102100030696 Receptor activity-modifying protein 2 Human genes 0.000 description 2
- 102100030711 Receptor activity-modifying protein 3 Human genes 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 230000001154 acute effect Effects 0.000 description 2
- PLOPBXQQPZYQFA-AXPWDRQUSA-N amlintide Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H]1NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CCCCN)CSSC1)[C@@H](C)O)C(C)C)C1=CC=CC=C1 PLOPBXQQPZYQFA-AXPWDRQUSA-N 0.000 description 2
- 208000014679 binge eating disease Diseases 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 230000001593 cAMP accumulation Effects 0.000 description 2
- 238000013262 cAMP assay Methods 0.000 description 2
- 239000005018 casein Substances 0.000 description 2
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 2
- 235000021240 caseins Nutrition 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000003925 fat Substances 0.000 description 2
- 235000019197 fats Nutrition 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 230000030136 gastric emptying Effects 0.000 description 2
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 2
- 229960004666 glucagon Drugs 0.000 description 2
- 230000014101 glucose homeostasis Effects 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 125000005647 linker group Chemical group 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 208000010125 myocardial infarction Diseases 0.000 description 2
- CMWYAOXYQATXSI-UHFFFAOYSA-N n,n-dimethylformamide;piperidine Chemical compound CN(C)C=O.C1CCNCC1 CMWYAOXYQATXSI-UHFFFAOYSA-N 0.000 description 2
- 150000002923 oximes Chemical class 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 229960003611 pramlintide Drugs 0.000 description 2
- 108010029667 pramlintide Proteins 0.000 description 2
- NRKVKVQDUCJPIZ-MKAGXXMWSA-N pramlintide acetate Chemical compound C([C@@H](C(=O)NCC(=O)N1CCC[C@H]1C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CS)NC(=O)[C@@H](N)CCCCN)[C@@H](C)O)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 NRKVKVQDUCJPIZ-MKAGXXMWSA-N 0.000 description 2
- 201000009104 prediabetes syndrome Diseases 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- 229940043230 sarcosine Drugs 0.000 description 2
- 230000036186 satiety Effects 0.000 description 2
- 235000019627 satiety Nutrition 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- FGMPLJWBKKVCDB-UHFFFAOYSA-N trans-L-hydroxy-proline Natural products ON1CCCC1C(O)=O FGMPLJWBKKVCDB-UHFFFAOYSA-N 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- BDNKZNFMNDZQMI-UHFFFAOYSA-N 1,3-diisopropylcarbodiimide Chemical compound CC(C)N=C=NC(C)C BDNKZNFMNDZQMI-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- RUVRGYVESPRHSZ-UHFFFAOYSA-N 2-[2-(2-azaniumylethoxy)ethoxy]acetate Chemical compound NCCOCCOCC(O)=O RUVRGYVESPRHSZ-UHFFFAOYSA-N 0.000 description 1
- 229940124035 Amylin receptor agonist Drugs 0.000 description 1
- 201000001320 Atherosclerosis Diseases 0.000 description 1
- 206010052804 Drug tolerance Diseases 0.000 description 1
- 102100021243 G-protein coupled receptor 182 Human genes 0.000 description 1
- 101000690940 Homo sapiens Pro-adrenomedullin Proteins 0.000 description 1
- 206010022489 Insulin Resistance Diseases 0.000 description 1
- OYIFNHCXNCRBQI-BYPYZUCNSA-N L-2-aminoadipic acid Chemical compound OC(=O)[C@@H](N)CCCC(O)=O OYIFNHCXNCRBQI-BYPYZUCNSA-N 0.000 description 1
- 150000008575 L-amino acids Chemical class 0.000 description 1
- 239000004201 L-cysteine Substances 0.000 description 1
- 235000013878 L-cysteine Nutrition 0.000 description 1
- ZKZBPNGNEQAJSX-REOHCLBHSA-N L-selenocysteine Chemical compound [SeH]C[C@H](N)C(O)=O ZKZBPNGNEQAJSX-REOHCLBHSA-N 0.000 description 1
- 229930182853 L-selenocysteine Natural products 0.000 description 1
- 208000023178 Musculoskeletal disease Diseases 0.000 description 1
- KSPIYJQBLVDRRI-WDSKDSINSA-N N-methyl-L-isoleucine Chemical compound CC[C@H](C)[C@H](NC)C(O)=O KSPIYJQBLVDRRI-WDSKDSINSA-N 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 208000006011 Stroke Diseases 0.000 description 1
- GYDJEQRTZSCIOI-UHFFFAOYSA-N Tranexamic acid Chemical compound NCC1CCC(C(O)=O)CC1 GYDJEQRTZSCIOI-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 108010063640 adrenomedullin receptors Proteins 0.000 description 1
- 150000001447 alkali salts Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 230000002891 anorexigenic effect Effects 0.000 description 1
- 230000003466 anti-cipated effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 230000006472 autoimmune response Effects 0.000 description 1
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 229960002173 citrulline Drugs 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000007515 enzymatic degradation Effects 0.000 description 1
- LCFXLZAXGXOXAP-DAXSKMNVSA-N ethyl (2z)-2-cyano-2-hydroxyiminoacetate Chemical compound CCOC(=O)C(=N/O)\C#N LCFXLZAXGXOXAP-DAXSKMNVSA-N 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000026781 habituation Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 102000046663 human ADM Human genes 0.000 description 1
- 229960002591 hydroxyproline Drugs 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 201000002818 limb ischemia Diseases 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 238000010801 machine learning Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 238000000034 method Methods 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 235000021400 peanut butter Nutrition 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 229940044601 receptor agonist Drugs 0.000 description 1
- 239000000018 receptor agonist Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 239000012453 solvate Substances 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 238000013222 sprague-dawley male rat Methods 0.000 description 1
- 238000012453 sprague-dawley rat model Methods 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 239000007939 sustained release tablet Substances 0.000 description 1
- 230000001360 synchronised effect Effects 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Endocrinology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Gastroenterology & Hepatology (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Toxicology (AREA)
- Diabetes (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Emergency Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
La presente invención se refiere a análogos de hAM15-52 con potencia mejorada del receptor de amilina (hAMY3R) (hAMY3R-EC50 <= 250 pM) y que se basan en gran medida en la secuencia del fragmento de adrenomedulina humana hAM15-52. La invención se refiere además a análogos de hAM15-52 que son agonistas selectivos del receptor de amilina (hAMY3R) (hAMY3R-EC50 <= 250 pM y un hAM1R-EC50 >= 25 nM) y que se basan en gran medida en la secuencia del fragmento de adrenomedulina humana hAM15-52. . Los análogos de hAM15-52 según la invención mantienen la buena estabilidad física de hAM15-52. La invención se refiere además a composiciones farmacéuticas que comprenden dichos polipéptidos y su uso en el tratamiento de una afección médica tal como obesidad, EHNA y/o diabetes. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Análogos de hAM15-52 con potencia mejorada frente al receptor de amilina (hAMY3R)
Campo de la invención
La presente invención se refiere a análogos de hAM15-52 con potencia mejorada frente al receptor de amilina (hAMY3R) (hAMY3R-CE50 ≤ 250 pM) y que se basan en gran medida en la secuencia del fragmento de adrenomedulina humana hAM15-52. La invención se refiere además a análogos de hAM15-52 que son agonistas selectivos del receptor de amilina (hAMY3R) (hAMY3R-CE50 ≤ 250 pM y hAM1R-CE50 ≥ 25 nM). En particular, la presente invención se basa en la observación de que el fragmento de adrenomedulina humana hAM15-52 puede convertirse en agonistas de receptores de amilina altamente selectivos (hAMY3R-CE50 ≤ 250 pM y hAM1 R-CE50 s 25 nM) reemplazando el aminoácido en la posición X11 en hAM15-52 junto con uno o más de los aminoácidos en las posiciones X4, X37 y/o X38 en hAM15-52. Por lo tanto, el reemplazo de al menos dos aminoácidos en hAM15-52 da como resultado análogos de hAM15-52 con potencias frente a AMY3R y AM1R comparables a hAMY1-37 (amilina). La invención se refiere además a composiciones farmacéuticas que comprenden dichos análogos de hAM15-52 y a su uso médico en el tratamiento de una afección médica, tal como obesidad y/o diabetes.
Antecedentes de la invención
La obesidad es una afección médica en la que el exceso de grasa corporal se acumula hasta el punto de tener un impacto negativo en la salud. Está afectando a un gran número de personas en todo el mundo y está aumentando rápidamente en ciertas partes del mundo. La Organización Mundial de la Salud (OMS) estimó que, en 2016, aproximadamente 650 millones de personas eran obesas en todo el mundo. La obesidad se define como un índice de masa corporal (IMC) superior a 30. La obesidad se considera un factor de riesgo importante para desarrollar una variedad de afecciones médicas, tales como enfermedades cardiovasculares (p. ej., hipertensión, aterosclerosis, ataques cardíacos o accidentes cerebrovasculares), NASH, trastornos musculoesqueléticos, ciertos tipos de cáncer, depresión y diabetes tipo II, y por lo tanto es perjudicial para la salud humana. Las enfermedades cardiovasculares y la diabetes son dos enfermedades principales asociadas con la obesidad. Se ha realizado una gran cantidad de investigación en el campo de la obesidad en la búsqueda de nuevos tratamientos para la obesidad o enfermedades y trastornos relacionados con la obesidad.
La diabetes es un grupo de trastornos metabólicos caracterizados por un alto nivel de azúcar en la sangre. A partir de 2019, la Federación Internacional de Diabetes estimó que 463 millones de personas padecen de diabetes en todo el mundo, estando diagnosticados aproximadamente la mitad de los individuos . La diabetes se divide en dos tipos, a saber, diabetes tipo I y diabetes tipo II. La diabetes tipo I es el resultado de la incapacidad del páncreas para producir suficiente insulina debido a la pérdida de células beta provocada por una respuesta autoinmune. Por otro lado, la diabetes tipo II es una afección que comienza con la resistencia a la insulina en la que las células no responden a la insulina adecuadamente y, a medida que avanza la enfermedad, también puede dar lugar a una falta de insulina.
La amilina humana (hAMY1-37 o amilina) es una hormona peptídica de 37 residuos que se secreta conjuntamente con la insulina de las células p pancreáticas con la secuencia de aminoácidos Lys-Cys-Asn-Thr-Ala-Thr-Cys-Ala-Thr-Gln-Arg-Leu-Ala-Asn-Phe-Leu-Val-His-Ser-Ser-Asn-Asn-Phe-Gly-Ala-Ile-Leu-Ser-Ser-Thr-Asn-Val-Gly-Ser-Asn-Thr-Tyr con un puente disulfuro entre los residuos 2 y 7. La amilina suprime la liberación de glucagón e inhibe el vaciado gástrico y, por lo tanto, desempeña un papel importante en el mantenimiento de la homeostasis de la glucosa al disminuir la concentración de azúcar en la sangre. Por lo tanto, la amilina es un candidato potencial para el tratamiento de la diabetes. Además, se ha mostrado que la amilina reduce la ingesta de alimentos y juega un papel importante en la saciedad, lo que también la convierte en una candidata potencial para tratar la obesidad. Sin embargo, la amilina posee algunos inconvenientes tales como una alta tendencia a la fibrilación, una semivida in vivo corta e inestabilidad química a pH 7. Por tanto, la amilina nativa es subóptima para su uso como ingrediente farmacéuticamente activo.
En la técnica anterior, se conoce un gran número de derivados de amilina, tales como aquellos divulgados en WO2016/146739. Estos análogos de amilina intentan resolver algunos de los inconvenientes conocidos que posee la amilina humana. Un ejemplo exitoso es el análogo de amilina Pramlintida, que ha sido aprobado por la FDA para su uso en diabetes tipo I y tipo II. Sin embargo, la Pramlintida se formula a pH 4 ya que fibrila a pH 7. Por lo tanto, todavía existe la necesidad de nuevos análogos de amilina con mayor estabilidad química, mayor estabilidad metabólica y/o menor tendencia a la fibrilación. En particular, son deseables los análogos de amilina que sean estables en un intervalo de pH más amplio. Además, existe la necesidad de nuevos análogos de amilina con mayor eficacia mediante, p. ej., mayor potencia, mayor eficacia y/o semividas más largas para permitir una dosificación menos frecuente y un mayor cumplimiento del paciente. La presente invención pretende resolver uno o más de los problemas conocidos de la técnica anterior mediante la aplicación de una nueva estrategia química.
Resumen de la invención
En un primer aspecto, la presente divulgación se refiere a análogos de hAM15-52 con potencia mejorada frente al receptor de amilina (hAMY3R) (hAMY3R-CE50 á 250 pM). Por lo tanto, en un primer aspecto, la divulgación se refiere a análogos de hAM15-52 o una sal farmacéuticamente aceptable de los mismos que comprenden 38 aminoácidos (X1-X38), en donde el aminoácido en la posición X11 se selecciona de R, W o Cit y en donde el análogo de hAM15-52 tiene
al menos un 50% de identidad con hAM i 5-52 (SEQ ID NO: 1), tal como al menos un 60 % de identidad con hAMi 5-52 (SEQ ID NO: 1). Los inventores encontraron sorprendentemente que la posición del aminoácido X11 era muy importante para aumentar la potencia frente al receptor de amilina de hAM15-52. Por lo tanto, una única sustitución en X11 de K a R, W o Cit fue suficiente para mejorar significativamente la potencia frente al receptor de amilina (hAMY3R-CE50 ≤ 250 pM) de hAM 15-52 mientras se conservaba la potencia frente a adrenomedulina (hAM1 R).
En un segundo aspecto, la presente invención proporciona análogos selectivos de hAM15-52 (hAMY3R-CE50 ≤ 250 pM y un hAM1 R-CE50 > 25 nM), que actúan como agonistas sobre el receptor de amilina hAMY3R pero que, a diferencia de la técnica anterior (p. ej., WO2016/146739), se derivan del esqueleto del fragmento de adrenomedulina hAM15-52. Los inventores encontraron sorprendentemente que cada una de las posiciones X4 , X37 y X38 eran muy importantes para la potencia sobre hAM1 R de hAM15-52 y que la potencia sobre hAM1 R de hAM15-52 podía abolirse o reducirse (hAM1 R-CE50 > 25 nM) por ciertas sustituciones de aminoácidos en cualquiera de las posiciones X4, X37 y/o X38. Así, en un segundo aspecto, la invención se refiere a análogos de hAM15-52 que comprenden 38 aminoácidos (X1-X38) o una sal farmacéuticamente aceptable de los mismos, en donde el aminoácido en la posición X11 se selecciona de R, W o Cit y en donde el análogo de hAM15-52 tiene al menos un 50 % de identidad con hAM15-52 (SEQ ID NO: 1), tal como al menos un 60 % de identidad con hAM15-52 (SEQ ID NO: 1) y además en donde X4 se selecciona como F, Y, W, T, M, I, A o C; X37 se selecciona como G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona como Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K, con la condición de que en al menos una de las posiciones X4, X37 o X38 no esté el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición. Los inventores encontraron sorprendentemente que el fragmento de adrenomedulina humana hAM15-52 se puede convertir en agonistas altamente selectivos del receptor de amilina (valor de hAMY3R-CE50 ≤ 250 pM y un hAM1 R-CE50 > 25 nM) reemplazando el aminoácido en la posición X11 en hAM15-52 junto con uno o más de los aminoácidos en las posiciones X4, X37 y/o X38 en hAM15-52. Por lo tanto, el reemplazo de al menos dos aminoácidos en hAM15-52 dio como resultado análogos de hAM15-52 con potencias sobre hAMY3R y hAM1R comparables a la amilina en lugar de hAM15-52. Un beneficio de este enfoque es que, a diferencia de la amilina humana, hAM15-52 no es propenso a la fibrilación y, mediante el uso de esta nueva estrategia química, los inventores previeron además que las buenas propiedades de fibrilación de hAM15-52 podrían mantenerse en los nuevos análogos de hAM15-52. Por lo tanto, los análogos de hAM15-52 según con la invención comprenden una parte significativa del esqueleto presente en hAM15-52 como una parte importante de la secuencia (es decir, al menos un 50 % de identidad con hAM15-52 (SEQ ID NO: 1)). Así, en el segundo aspecto de la invención, el primer problema resuelto es la provisión de nuevos agonistas potentes de hAMY3R con alta selectividad sobre hAM1 R, que se obtienen modificando la polifarmacología del fragmento hAM15-52 en agonismo de hAMY3R. El segundo problema resuelto por el segundo aspecto es la provisión de nuevos agonistas de hAMY3R que son menos propensos a la fibrilación, superando así un problema inherente a la amilina humana. A diferencia de los derivados de amilina conocidos de la técnica anterior, los análogos de hAM15-52 de la presente invención poseen una secuencia estructuralmente distinta que pertenece al fragmento hAM15-52. Por lo tanto, los análogos de hAM15-52 de la invención poseen diferentes propiedades físico-químicas en comparación con los derivados de amilina en la técnica anterior, tales como diferente solubilidad, estabilidad química, física y/o metabólica.
En un tercer aspecto, la invención se refiere a análogos de hAM15-52 según el segundo aspecto para su uso como un medicamento. Más particularmente, el tercer aspecto de la invención se refiere a los análogos de hAM15-52 según el segundo aspecto para su uso en el tratamiento, prevención o mejora de una variedad de enfermedades, trastornos o afecciones, tales como, pero no limitados a, la ingesta excesiva de alimentos, exceso de peso corporal, obesidad, trastorno por atracones, síndrome de Prader-Willi, dislipidemia, enfermedades/trastornos metabólicos, diabetes tipo I o II, tolerancia alterada a la glucosa, síndrome de resistencia a la insulina y/o NASH.
En un cuarto aspecto, la invención se refiere a composiciones farmacéuticas que comprenden uno o más de los análogos de hAM15-52 según el segundo aspecto y su(s) uso(s) médico(s) para tratar, prevenir o mejorar una variedad de enfermedades, trastornos o afecciones según el tercer aspecto. Las composiciones farmacéuticas pueden comprender un portador (vehículo) y/o uno o más excipientes farmacéuticamente aceptables.
La invención se explicará ahora con más detalle a partir del alineamiento de la amilina (hAMY1-37) y el fragmento de adrenomedulina (hAM15-52) como se muestra en la Tabla 1 a continuación.
Definiciones
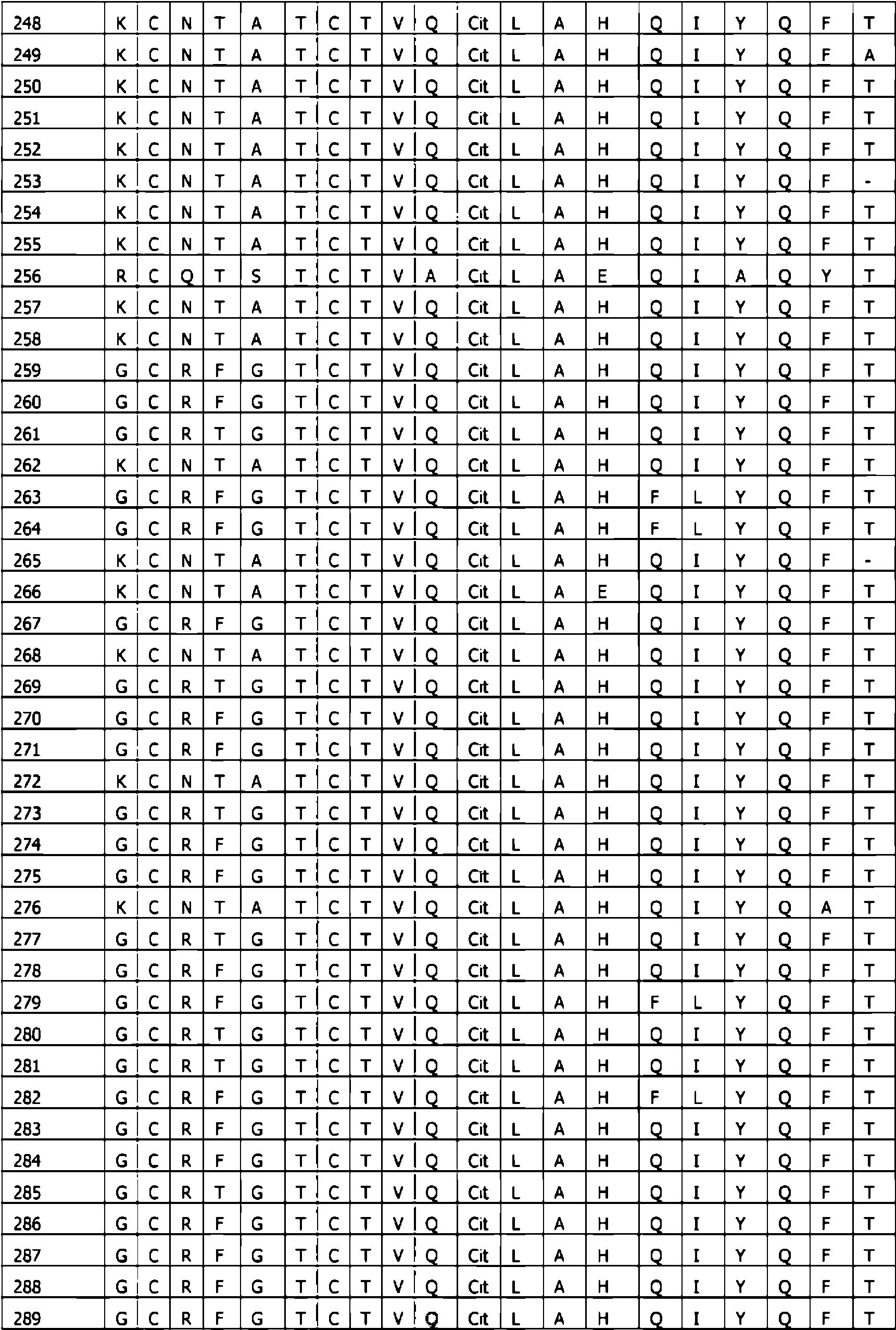
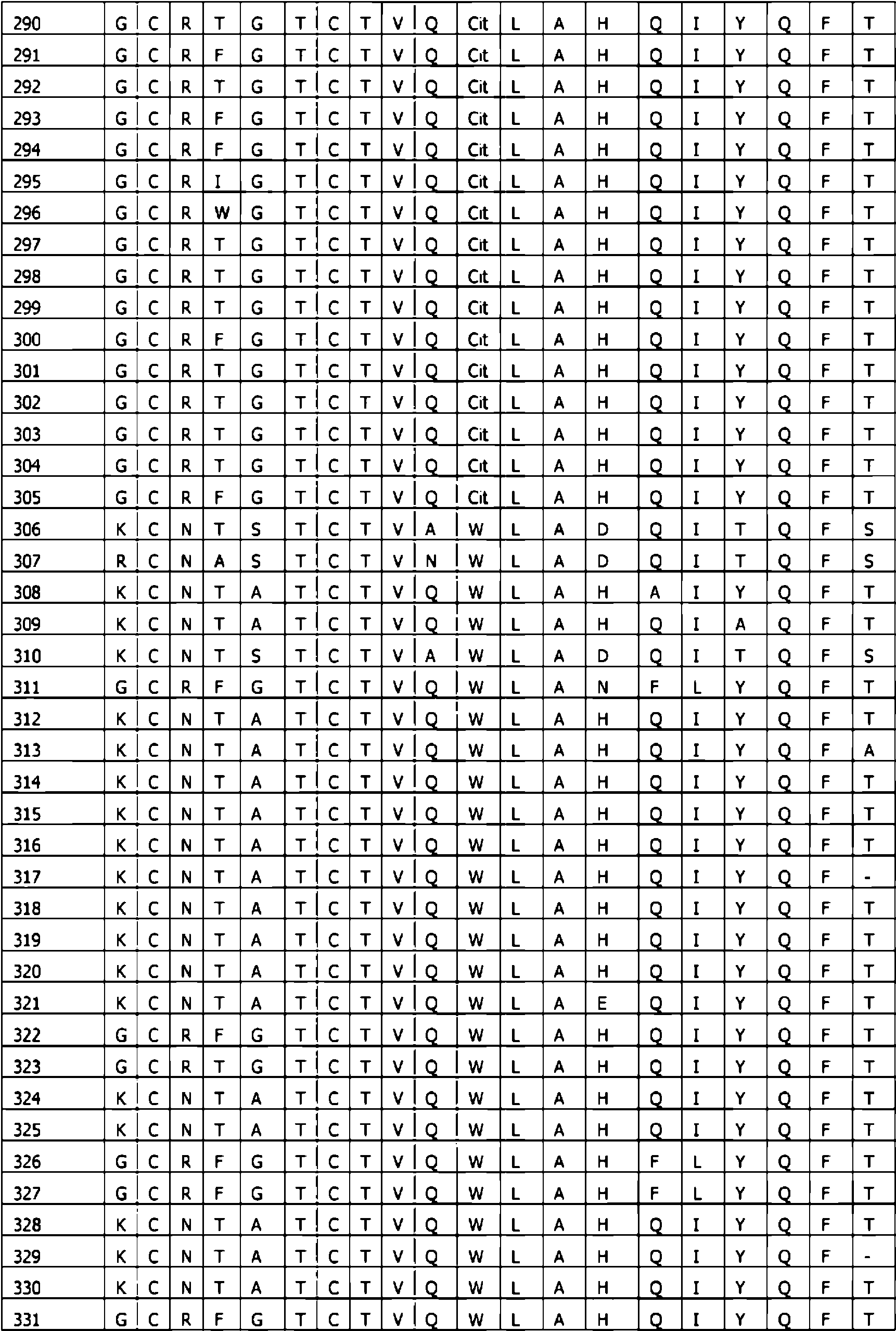
En el presente contexto, cuando la divulgación se refiere a posiciones de aminoácidos en los análogos de hAM15-52 (es decir, X1-X38) que se derivan/seleccionan de hAMY1-37 o se retienen/seleccionan del fragmento hAM15-52, se aplica el siguiente alineamiento mostrado en la Tabla 1. Así, la posición X1 en los análogos de hAM15-52 según la invención corresponde al primer aminoácido en la amilina humana (hAMY1-37) y al aminoácido número 15 (hAM15) en el fragmento hAM15-52.
hAMYi-37 K C N T A T C A T Q R L A N F L V H S S N N F - G A I L S S T N V G S N T Y
Tabla 1
Según la presente invención, los análogos de hAMi 5-52 generalmente están amidados en el extremo C (-CONH2), como los péptidos nativos; la amilina y la adrenomedulina. Sin embargo, los análogos de hAM15-52 de la presente invención también pueden tener un ácido carboxílico libre (-COOH) u otra modificación postraduccional tal como un éster metílico (-COOMe). En una realización altamente preferida de la invención, los análogos de hAM15-52 están amidados en el extremo C. Los análogos de hAM15-52 según la presente invención pueden tener una amina libre (-NH2), estar N-acilados (-NHCOR), N-metilados (-NHCH3 o -N(CH3)2) o desaminados en el extremo N. Los análogos de hAM15-52 también pueden estar lipidados, p. ej., en el extremo N como se ejemplifica en la presente memoria, dependiendo de la semivida deseada de los polipéptidos.
Según la presente invención, la lipidación tiene el significado habitual en la técnica. Por lo tanto, la lipidación en el presente contexto se refiere a la unión covalente de un lípido opcionalmente a través de un enlazador a los análogos de hAM 15-52 de la invención. La lipidación se realiza típicamente para mejorar el perfil farmacocinético de un polipéptido, p. ej., mejorando la estabilidad metabólica, reduciendo la degradación enzimática, disminuyendo la excreción y el metabolismo, todo lo cual da lugar a una semivida in vivo prolongada (t1/2) de los análogos de hAM15-52. Los análogos de hAM 15-52 según la invención, pueden estar lipidados o no lipidados. Los análogos de hAM15-52 lipidados ejemplificados en la presente memoria están lipidados con un diácido C20 saturado a través de varios enlazadores como se muestra en la tabla 2. Según la presente invención, las abreviaturas Hyp, Cit, Aib, Aad, (NMe)G/Sar, (NMe)I tienen el significado habitual en la técnica. Así, Hyp se refiere a L-hidroxiprolina, Cit se refiere a L-citrulina, Aib se refiere a ácido 2-aminoisobutírico, Aad se refiere a ácido L-homoglutámico, (NMe)G se refiere a N-metilglicina también conocida como Sar o sarcosina y (NMe)I se refiere a N-metil-L-isoleucina.
Según la presente invención, los valores de CE50 se usan como una medida de la potencia agonista en un receptor dado. Un valor de CE50 es una medida de la concentración de un compuesto requerida para lograr la mitad de la actividad máxima de ese compuesto en un ensayo particular. Por lo tanto, se considera que un análogo de hAM15-52 según la invención que tiene un hAMY3R-CE50 menor que el hAMY3R-CE50 de hAM15-52 en el ensayo dado tiene mayor potencia o actividad en el receptor hAMY3R que el fragmento de adrenomedulina hAM15-52. Asimismo, un análogo de hAM15-52 según la invención que tiene un hAM1R-CE50 mayor que el hAM1R-CE50 de hAM15-52, en el ensayo dado puede considerarse que tiene menor potencia o actividad en el receptor hAM1R que el fragmento de adrenomedulina hAM15-52.
Según la presente invención, un análogo de hAM15-52 o un derivado del mismo puede estar en forma de una sal farmacéuticamente aceptable. Por lo tanto, se pretende que las sales farmacéuticamente aceptables incluyan cualquier sal que se use comúnmente en formulaciones de péptidos. Dichas sales incluyen tanto sales de adición de ácidos como sales básicas, y se pueden encontrar ejemplos, p. ej., en Remington’s Pharmaceutical Sciences, 17a edición. Asimismo, varios solvatos de los análogos de hAM15-52 o sales farmacéuticamente aceptables d los mismos también están dentro del alcance de la invención.
Según la presente invención, los análogos de hAM15-52 son cadenas cortas de aminoácidos que se han unido mediante enlaces amida. En la realización más preferida de la invención, los análogos de hAM15-52 tienen una longitud de 38 aminoácidos, sin incluir ningunos de los aminoácidos que funciona como espaciador entre un lípido opcional y los polipéptidos híbridos.
En el presente contexto, a no ser que se indique lo contrario, los aminoácidos son todos L-aminoácidos (L-estereoisómero, aminoácidos naturales). Así, la configuración absoluta de los aminoácidos es la configuración (S) con la excepción de L-cisteína y L-selenocisteína que tienen la configuración (R).
En el presente contexto, debe entenderse que los aminoácidos Cys (X2) y Cys (X7) en los análogos de hAM15-52 están unidos covalentemente por un puente, preferiblemente un puente disulfuro (-S-S-) tal como el presente en hAMY1-37 y hAM 15-52. La ciclación del puente disulfuro se puede realizar después de la purificación de los polipéptidos híbridos o antes de la escisión de la resina en la síntesis peptídica en fase sólida, opcionalmente en presencia de grupos protectores adecuados. El puente disulfuro puede formarse espontáneamente agitando el polipéptido híbrido en presencia de oxígeno o puede formarse tratando los polipéptidos híbridos con otro oxidante adecuado tal como yodo (I2), opcionalmente en presencia de una base.
En el presente contexto, los análogos de hAM15-52 o derivados de los mismos según el primer o segundo aspecto tienen una potencia frente a hAMY3R (CE50) ≤ 250 pM, tal como ≤ 200 pM, preferiblemente hAMY3R-CE50 ≤ 150 pM, tal como ≤ 125 pM, más preferiblemente un hAMY3R-CE50 ≤ 100 pM, tal como ≤ 75 pM, aún más preferiblemente un hAMY3R-CE50 ≤ 50 pM, tal como ≤ 25 pM, más preferiblemente un hAMY3R-CE50 ≤ 15 pM, tal como ≤ 10 pM. Por tanto, los análogos de hAM15-52 más potentes sobre hAMY3R pueden ser más o menos equipotentes con la amilina humana nativa hAMY1-37. Por ejemplo, las SEQ ID NO: 3-44 tienen un hAMY3R-CE50 entre 6,0-10 pM y por lo tanto son más o equipotentes en comparación con hAMY1-37 (hAMY3R-CE50 = 10 pM) cuando se mide bajo las mismas condiciones de ensayo.
En el presente contexto, los análogos de hAM15-52 o derivados de los mismos según el segundo aspecto tienen una CE50 suprimida o reducida cuando el valor de CE50 en hAM1R > 25 nM, tal como el valor de CE50 en hAM1 R > 50 nM, tal como un hAM1R-CE50 > 100 nM, preferiblemente un hAM1R-CE50 > 150 nM, tal como > 200 nM, más preferiblemente hAM1 R-CE50 > 250 nM, tal como > 300 nM, aún más preferiblemente un hAM1 R-CE50 > 350 nM, tal
como > 400 nM, aún más preferiblemente un hAM1 R-CE50 > 450 nM, tal como > 500 nM, aún más preferiblemente un hAM1R-CE50 > 600 nM, tal como > 700 nM, aún más preferiblemente un hAM1 R-CE50 > 800 nM, tal como > 900 nM, aún más preferiblemente un hAM1R-CE50 > 1.000 nM, lo más preferiblemente un hAM1R-CE50 > 5.000 nM. Por lo tanto, en el presente contexto, selectivamente en términos de potencia hacia el receptor de amilina hAMY3R sobre el receptor de adrenomedulina hAM1R (es decir, un agonista selectivo del receptor de amilina) debe entenderse como un análogo de hAM15-52 o un derivado del mismo según el segundo aspecto que tiene un valor de hAMY3R-CE50 á 250 pM y un hAM1 R-CE50 > 25 nM. Por lo tanto, un análogo de hAM15-52 selectivo o un derivado del mismo tiene una relación de selectividad (hAM1R CE5ü/hAMY3R CE50) de al menos 100. Preferiblemente, los análogos de hAM15-52 o derivados de los mismos tienen un valor de hAMY3R-CE50 á 250 pM y un hAM1 R -CE50 > 50 nM y, por lo tanto, una relación de selectividad (hAM1 R CE50/hAMY3R CE50) > 200. Más preferiblemente, los análogos de hAM15-52 o derivados de los mismos tienen un hAMY3R-CE50 á 200 pM, un hAM1 R-CE50 > 100 nM y, por lo tanto, una relación de selectividad (hAM1R CE50/hAMY3R CE50) > 500. Más preferiblemente, un análogo de hAM15-52 o un derivado del mismo tiene un hAMY3R-CE50 á 125 pM, un hAM1 R-CE50 > 200 nM y por lo tanto una relación de selectividad (hAM1 R CE50/hAMY3R CE50) > 1.600. Aún más preferiblemente, el análogo de hAM15-52 o un derivado del mismo tiene un hAMY3R-CE50 á 100 pM, un hAM1 R-CE50 > 500 nM y, por lo tanto, una relación de selectividad (hAM1 R CE50/hAMY3R CE50) > 5.000. Lo más preferiblemente, el análogo hAM15-52 o un derivado del mismo tiene un hAMY3R-CE50 á 50 pM, un hAM1 R-CE50 > 1.000 nM y, por lo tanto, una relación de selectividad (hAM1 R CE50/hAMY3R CE50) > 20.000. Por ejemplo, cualquiera de las SEQ ID NO: 3-42 tiene una relación de selectividad de al menos 6.000 y la mayoría de ellas mucho mayor.
Un experto en la técnica sabe muy bien que los valores de CE50 dependen del tipo de ensayo y de las condiciones del ensayo. Así, en el presente contexto, cuando la divulgación se refiere a un valor de CE50, debe entenderse como un valor de CE50 obtenido cuando se mide según el procedimiento descrito en los ejemplos bajo protocolos generales para ensayos de AMPc para medir la activación del receptor in vitro. Sin embargo, la variación también puede estar presente dentro del mismo ensayo bajo condiciones de ensayo aparentemente idénticas debido a la variación en, p. ej., la expresión del receptor en las células (es decir, densidad del receptor). Por lo tanto, con el fin de comparar los valores de CE50, se han ensayado hAMY1-37 (SEQ ID NO: 2) y hAM15-52 (SEQ ID NO: 1) como estándares internos para comparar entre diferentes operaciones de ensayos o incluso diferentes ensayos. Se determinó hAMY3R-CE50 y hAM1R-CE50 de hAMY1-37 (SEQ ID NO: 2) a 10 pM y 5.000 nM, respectivamente, usando las mismas condiciones de ensayo y línea celular que los análogos de hAM15-52 (SEQ ID NO: 3-392). Asimismo, se determinó hAMY3R-CE50 y hAM1R-CE50 de hAM 15-52 (SEQ ID NO: 1) a 1,3 nM y 1,1 nM, respectivamente, usando las mismas condiciones de ensayo y línea celular que los análogos de hAM15-52 (SEQ ID NO: 3-392). Por lo tanto, se deduce que los análogos de hAM 15-52 o derivados del mismo según el primer o segundo aspecto tienen una relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAMY1-37-hAMY3R-CE50) á (250 pM)/(10 pM) á 25. Preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAMY1-37-hAMY3R-CE50) á 20. Más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAM1-37-hAMY3R-CE50) á 12,5. Aún más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAMY1-37-hAMY3R-CE50) á 10. Aún más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAMY1-37-hAMY3R-CE50) á 5. Aún más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAMY1-37-hAMY3R-CE50) á 2. Lo más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/( hAMY1 -37-AMY3 R-CE50) á 1 de manera que los análogos de hAM15-52 o derivados de los mismos son equipotentes o más potentes que hAMY1-37. Asimismo, los análogos selectivos de hAM15-52 o derivados de los mismos según el segundo aspecto tienen una relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAM15-52 -AMY3R-CE50) á (250 pM)/(1.300 pM) á 0,19 y una relación relativa de hAM1R-CE50 (hAM1 R-CE50)/(hAM15-52 -hAM1 R-CE50) > (25 nM)/(1,1 nM) > 22,7. Preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAM15-52 -hAMY3R-CE50) á (250 pM)/(1.300 pM) á 0,19 y una relación relativa hAM1R-CE50 (hAM1R-CE50)/(hAM15 -52-hAM1R-CE50) > (50 nM)/(1,1 nM) > 45,5. Más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAM15-52 -hAMY3R-CE50) á 0,15 y una relación relativa hAM1R-CE50 (hAM1R-CE50)/(hAM15-52 -hAM1R-CE50) > 76,9. Aún más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAM15-52 -hAMY3R-CE50) á 0,096 y una relación relativa hAM1R-CE50 (hAM1 R-CE50)/(hAM15-52 -hAM1 R-CE50) > 154. Aún más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAM15-52 -hAMY3R-CE50) á 0,077 y una relación relativa hAM1R-CE50 (hAM1R-CE50)/(hAM15-52 -hAM1 R-CE50 ) > 384. Aún más preferiblemente, la relación relativa hAMY3R-CE50 (hAMY3R-CE50)/(hAM15-52 -AMY3R-CE50) á 0,038 y una relación relativa hAM1R-CE50 (hAM1R-CE50)/(hAM15-52 -hAM1R-CE50) > 769. Más preferiblemente, la relación relativa hAM1 R-CE50 (hAM1 R-CE50)/(hAM15-52 -hAM1 R-CE50) > 2.000.
Según la presente invención, el término "tratamiento" debe entenderse en el sentido más amplio como prevención, mejora o tratamiento. Por lo tanto, también se pretende que el tratamiento incluya tratamiento profiláctico.
Según la presente invención, del aspecto o aspectos/realización o realizaciones que se refieren a “en donde el análogo de hAMi5-52 tiene (p. ej.) al menos un 50 % de identidad con hAMi5-52 (SEQ ID NO: 1)" o “un derivado del mismo con (p. ej.) al menos un 50 % de identidad con hAMis-52 ’, debe entenderse que el análogo de hAM15-52 o derivado del mismo tiene al menos un 50 % de identidad de secuencia con hAM15-52 (SEQ ID NO: 1) cuando se alinea. Como ejemplo, la SEQ ID NO: 169 que se ilustra a continuación difiere en dos aminoácidos (X11 y X38) de hAM15-52 (SEQ ID NO: 1) y, por lo tanto, tiene (38-2)/38 = 94,7 % de identidad de secuencia con hAM15-52 (s Ce ID No: 1).
SEQ ID NO:1 G C R F G T C T V Q K L A H Q I Y Q F T D K D K D N V A P R S K I S P Q G Y
Derivado X: G C R F G T C T V Q R L A H Q I Y Q F T D K D K D N V A P R S K I S P Q G Hyp
Descripción detallada de la invención
La familia de péptidos de calcitonina
La familia de péptidos de la calcitonina consiste en los péptidos hormonales calcitonina (CT), el péptido relacionado con el gen de la calcitonina (CGRP), el polipéptido amiloide de los islotes (IAPP, amilina o hAMY1-37) y la adrenomedulina (hAM), así como sus precursores. hAMY1-37 es una hormona peptídica de 37 residuos que se coexcreta con insulina de las células p pancreáticas con la secuencia de aminoácidos Lys-Cys-Asn-Thr-Ala-Thr-Cys-Ala-Thr-Gln-Arg-Leu-Ala-Asn-Phe-Leu-Val-His-Ser-Ser-Asn-Asn-Phe-Gly-Ala-Ile-Leu-Ser-Ser-Thr-Asn-Val-Gly-Ser-Asn-Thr-Tyr. La amilina suprime la liberación de glucagón e inhibe el vaciamiento gástrico y, por lo tanto, juega un papel importante en el mantenimiento de la homeostasis de la glucosa al disminuir la concentración de azúcar en la sangre. Además, se ha mostrado que la amilina reduce la ingesta de alimentos y desempeña un papel importante en la saciedad, lo que la convierte en una candidata potencial para tratar, p. ej., la obesidad y/o la diabetes. hAM es una hormona peptídica de 52 residuos expresada en todos los tejidos con la secuencia de aminoácidos Tyr-Arg-Gln-Ser-Met-Asn-Asn-Phe-Gln-Gly-Leu-Arg-Ser-Phe-Gly-Cys-Arg-Phe-Gly-Thr-Cys-Thr-Val-Gln-Lys-Leu-Ala-His-Gln-Ile-Tyr-Gln-Phe-Thr-Asp-Lys-Asp-Lys-Asp-Asn-Val-Ala-Pro-Arg-Ser-Lys-Ile-Ser-Pro-Gln-Gly-Tyr. Es un potente vasodilatador y ha mostrado influencia positiva en enfermedades cardiovasculares, tales como infarto de miocardio, isquemia de extremidades e hipertensión.
La actividad biológica de la familia de proteínas de la calcitonina generalmente está mediada por la unión al receptor de calcitonina (CTR) y al receptor similar al receptor de calcitonina (CRLR), ambos pertenecientes a la familia 2 de los receptores acoplados a la proteína G (GPCR). Estos receptores pueden coexpresarse en combinación con diferentes proteínas modificadoras de receptores (RAMP1-3) generando receptores funcionales para los péptidos individuales en la familia de proteínas de la calcitonina. La coexpresión de CTR con RAMP1 conduce a la formación de un receptor para amilina y CGRP (AMY1R), la coexpresión de CTR con RAMP2 conduce al receptor de amilina 2 (AMY2R) y la coexpresión de CTR con RAMP3 conduce al receptor de amilina (AMY3R). La coexpresión de CRLR con RAMP1 conduce a la formación de un receptor para CGRP (CGRP1R), la coexpresión de CRLR con RAMP2 conduce a la formación de un receptor para adrenomedulina (AM1R) y la coexpresión de CRLR con RAMP3 conduce a una formación de un receptor para adrenomedulina y CGRP (AM2R).
Varios de los péptidos nativos de la familia de proteínas de la calcitonina muestran un solapamiento considerable en la farmacología entre los receptores. Por ejemplo, la adrenomedulina es aproximadamente 100 veces menos potente en AMY3R en comparación con hAMY1-37. El fragmento de adrenomedulina (hAM15-52) es casi equipotente en AMY3R y AM1R con una CE50 de 1,3 nM en AMY3R y un valor de CE50 de 1,1 nM en AM1R (dicho valor de CE50 se mide según los ejemplos de la presente memoria). hAMY1-37, por otro lado, tiene un valor CE50 de 10 pM. en AMY3R mientras es inactivo en AM1R.
Determinación de posiciones de aminoácidos importantes en hAMis-52
Los inventores plantearon inicialmente la hipótesis de que, dado que hAM15-52 y hAMY1-37 pertenecen a la misma familia de hormonas, la familia Calcitonina/CGRP/IAPP, la potencia en AMY3R de hAM15-52 podría mejorarse o incluso convertirse en agonismo selectivo de AMY3R sobre agonismo de hAM1 R sustituyendo ciertos aminoácidos en hAM15-52 con aminoácidos derivados de la hAMY1-37, superando así algunos de los inconvenientes que son inherentes a hAMY1 -37. Todos los 37 aminoácidos de hAMY1-37 se sustituyeron sistemáticamente en la hAM15-52. Además, se seleccionó X38 como Hyp (Hidroxiprolina), que no está presente en hAMY1-37 ni en hAM15-52. Los inventores construyeron modelos de bosque aleatorio (Breiman, L. (2001), Random Forests, Machine Learning 45(1), 5-32.) que describen la relación entre la secuencia de péptidos y hAMY3R y la potencia sobre hAM1R, respectivamente, y sintetizaron y cribaron sistemáticamente secuencias peptídicas. Para cada análogo de hAM15-52, el aminoácido en cada posición de la secuencia se usó como característica, y los valores de CE50 del receptor se usaron como respuesta para construir los modelos. Se utilizó el paquete “randomForest” implementado en el lenguaje de programación estadística R para calcular la importancia de cada posición y se identificaron las posiciones más importantes como críticas para la actividad de hAMY3R y/o hAM1R (A. Liaw y M. Wiener (2002). Clasification and Reggression por randomForest. R News 2(3), 18-22.). Basándose en este análisis sistemático, los inventores identificaron que X4 , X37 y X38 eran importantes para la actividad de hAM1R, mientras que tenían menos importancia para la actividad de hAMY3R. Los inventores identificaron que X11 es crítico para la actividad de hAMY3R, mientras que tiene menos importancia para la actividad de hAM1 R. Finalmente, los inventores identificaron que X17 tiene cierta importancia para la actividad de hAMY3R, mientras que tiene menos importancia para la actividad de hAM1R. Por lo tanto, los inventores identificaron X11 como una posición clave para mejorar la potencia sobre hAMY3R en hAM15-52 y X4 , X37 y X38 como posiciones clave para eliminar la potencia sobre hAM1 R en hAM15-52. Dado que X17 solo tenía cierta importancia para la actividad de hAMY3R, esta posición no se consideró una posición clave sino solo una posición preferida para mejorar aún más la potencia sobre AMY3R de los análogos de hAM15-52.
La investigación sistemática mostró que la potencia sobre hAMY3R de hAM15-52 podría mejorarse sustituyendo el aminoácido K presente en hAM15-52 en la posición X11 con el aminoácido R presente en hAMY1-37. Además, la investigación sistemática mostró que la potencia sobre hAM1R de hAM15-52 podría disminuir sustituyendo los aminoácidos presentes en la posición X4 , X37 y X38 en hAM15-52 con los aminoácidos correspondientes que se encuentran presentes en hAMY1-37.
Investigación más profunda de los aminoácidos en la posición X4, X 11, X 17, X37 y X38.
Los inventores sustituyeron sistemáticamente los aminoácidos representativos que cubrían los aminoácidos representativos para todos los aminoácidos conocidos en las 5 posiciones identificadas, una posición cada vez (Tabla 6). Como se muestra en el ejemplo 1, todas (las SEQ ID: 1-360 habían perdido su actividad en el hAM1R, con un grado variable de potencia en AMY3R. Con el fin de calificar los aminoácidos individuales en las 5 posiciones, el valor de CE50 promedio para los péptidos que contenían un aminoácido dado en una posición dada se comparó con el valor promedio de CE50 de los análogos de hAM15-52 que contenían el aminoácido de referencia en esa posición. Dado un punto de corte de cambios de potencia de 4 veces, cada aminoácido en cada posición se calificó como dando una potencia aumentada (I), disminuida (D) o sin cambios (U), en relación con el aminoácido de referencia, en hAMY3R. Los resultados se resumen en la Tabla 6. A partir de estos datos, se mostró que cualquiera de los aminoácidos R, W o Cit eran capaces de mantener la potencia sobre AMY3R cuando estaban presentes en la posición X11 en comparación con la referencia, mientras que otros aminoácidos representativos disminuyeron la potencia. Se mostró además que cualquiera de los aminoácidos Y, W, T, M, I, F, A o C en X4 , cualquiera de los aminoácidos Y, W, T, Q, P, M, I, H, F, E, A, R, C o K en X37 y cualquiera de los aminoácidos Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K en X38 eran capaces de mantener o mejorar la potencia sobre AMY3R. mientras que permanecen inactivos en hAM1 R.
Aspecto 1: análogos de hAMw-52 con potencia de amilina mejorada
Así, en un primer aspecto, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende 38 aminoácidos (X1-X38) con un hAMY3R-CE50 ≤ 250 pM, en donde el aminoácido en la posición X11 se selecciona de R, W o Cit y en donde el análogo de hAM15-52 tiene al menos un 50 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos un 85 % de identidad con hAM15-52 (SEQ ID NO: 1). Del ejemplo 1 (Tabla 2), se puede ver que casi todos los análogos de hAM15-52 sintetizados tienen al menos un 50 % de identidad con hAM15-52, que la gran mayoría de los análogos de hAM15-52 sintetizados tienen al menos un 60 % de identidad con hAM15-52, y que una mayor parte de los análogos de hAM15-52 sintetizados tienen al menos un 80 % de identidad con hAM15-52 (SEq ID NO: 1). Todos estos análogos de hAM15-52 mantienen las buenas propiedades de fibrilación de hAM15-52 (SeQ ID NO: 1) en comparación con hAMY1-37 (SEQ ID NO: 2) (véase el ejemplo 2, Tabla 3). P. ej., la SEQ ID NO: 32 muestra que la buena estabilidad física (es decir, baja fibrilación) de hAM15-52 se puede mantener siempre que los análogos de hAM15-52 tengan al menos un 50 % de identidad con hAM15-52.
Por lo tanto, en un primer aspecto, la divulgación se refiere a una forma de mejorar en gran medida la potencia sobre hAMY3R del fragmento hAM15-52 mediante una sola sustitución a R, W o Cit en la posición X11, mientras se mantiene la buena estabilidad física (es decir, buenas propiedades de fibrilación de hAM15-52). Estos análogos de hAM15-52 serán, por lo tanto, agonistas muy potentes tanto en hAMY3R como en hAM1 R (véanse las SEQ ID NO: 361-392).
En la realización más preferida de la divulgación, X11 se selecciona como R. En otra realización, X11 se selecciona como W. En otra realización más, X11 se selecciona como Cit. Los inventores encontraron que esta sustitución de un único aminoácido en X11 proporcionaba una mayor potencia sobre hAMY3R a los análogos de hAM15-52 mientras conservaba la potencia sobre hAM1R. Los inventores encontraron además que la potencia sobre hAMY3R podía mantenerse cuando X17 era Y, T, Q, M, I, F, A, R o K, o incluso mejorarse más seleccionando X17 como W o H. Por lo tanto, en una realización X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K. En una realización preferida, X 17 se selecciona como Y, W o H, más preferiblemente W o H.
En una realización, la divulgación se refiere a un análogo de hAM15-52 que comprende 38 aminoácidos (X1-X38) o una sal farmacéuticamente aceptable del mismo, en donde el aminoácido en la posición X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K, preferiblemente X17 se selecciona como W o H y en donde el análogo de hAM15-52 tiene al menos un 50 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM 15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM 15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos 80 % de identidad con hAM15-52, tal como al menos un 85 % de identidad con hAM15-52 (SEQ ID NO: 1).
En una realización más, la divulgación se refiere a un análogo de hAM15-52 que comprende 38 aminoácidos (X1-X38) o una sal farmacéuticamente aceptable del mismo, en donde el aminoácido en la posición X11 es R; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K, preferiblemente X17 se selecciona como W o H y en donde el análogo de hAM15-52 tiene al menos un 50 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos 85 % de identidad con hAM15-52, (SEq ID NO: 1).
En una realización más, la invención se refiere a un análogo de hAM15-52 que comprende 38 aminoácidos (X1-X38) o una sal farmacéuticamente aceptable del mismo, en donde el aminoácido en la posición X11 es W; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K, preferiblemente X17 se selecciona como W o H y en donde el análogo de hAM15-52 tiene al menos un 50 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como
al menos un 75 % de identidad con hAMi5 -52, más preferiblemente al menos un 80 % de identidad con hAMi5 -52, tal como al menos un 85 % de identidad con hAM15-52, (SEQ ID NO: 1).
En una realización más, la divulgación se refiere a un análogo de hAM15-52 que comprende 38 aminoácidos (X1-X38) o una sal farmacéuticamente aceptable del mismo, en donde el aminoácido en la posición X11 es Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K, preferiblemente X17 se selecciona como W o H y en donde el análogo de hAM15-52 tiene al menos un 50 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos 85 % de identidad con hAM15-52, (SEQ ID NO: 1).
En una realización preferida, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K.
En otra realización preferida, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K.
En una realización más preferida, la divulgación se refiere a un análogo de hAMi5-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W o H;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K. En una realización más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W o H;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K.
En una realización más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W o H;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, W, P, H o F;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, Y, W, T, M, I, A, o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R, o K.
En una realización más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W o H;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, M o F;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, M o F.
En una realización más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;|
X17 se selecciona como Y, W o H;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, W, P, H o F;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K.
En una realización más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 o una sal
farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W o H;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, M o F;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C, o K; X38 se selecciona de Hyp, Y, W, M o F.
En una realización más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W o H;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, W, P, H o F;
X38 se selecciona de Hyp, Y, W, M o F;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, M o F.
En una realización aún más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R;
X17 se selecciona como Y, W o H;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, W, P, H o F;
X38 se selecciona de Hyp, Y, W, M o F;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, preferiblemente al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, aún más preferiblemente al menos un 85 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R; X17 se selecciona como Y, W o H; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, M o F.
En una realización más preferida adicional, la divulgación se refiere a un análogo de hAM15-52 que comprende la secuencia de aminoácidos de fórmula (I):
en donde, X11 se selecciona de R, W o Cit
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un
75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos un 85 % de identidad con hAM15-52, más preferiblemente al menos un 90 % de identidad con hAM15-52 con hAM15-52, tal como al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R, W o Cit.
En una realización lo más preferida, la divulgación se refiere a un análogo de hAM15-52 de las SEQ ID NO: 3-392 o un derivado del mismo con al menos un 90 % de identidad con una cualquiera de las SEQ ID NO: 3-392, preferiblemente al menos un 95 % de identidad con una cualquiera de las SEQ ID NO: 3-392, más preferiblemente al menos un 96 % de identidad con una cualquiera de las SEQ ID NO: 3-392, lo más preferiblemente al menos un 97 % de identidad con una cualquiera de SEQ ID NO: 3-392 con la condición de que un derivado del mismo tenga R, W o Cit en la posición X11, preferiblemente R en la posición X11.
En una realización lo más preferida, la divulgación se refiere a un análogo de hAM15-52 de las SEQ ID NO: 3-392 o un derivado del mismo con al menos un 90 % de identidad con una cualquiera de las SEQ ID NO: 3-392, preferiblemente al menos un 95 % de identidad con una cualquiera de las SEQ ID NO: 3-392, más preferiblemente al menos un 96 % de identidad con una cualquiera de las SEQ ID NO: 3-392, lo más preferiblemente al menos un 97 % de identidad con una cualquiera de las SEQ ID NO: 3-278, con la condición de que un derivado del mismo tenga el mismo aminoácido en la posición X11 que el respectivo de las SEQ ID NO: 3-392 del que se deriva.
Aspecto 2: Análogos selectivos de hAMi5-52 con potencia de amilina mejorada
Número de posiciones necesarias para suprimir o reducir la potencia sobre AM1R en I1AM 15-52.
Los inventores encontraron que la potencia sobre hAM1R podía suprimirse o reducirse en hAM15-52 cambiando al menos un aminoácido en cualquiera de las posiciones X4 , X37 o X38, ya que todos ellas eran críticas para la potencia sobre hAM1 R.
Disminución de la potencia sobre hAM1R con aminoácidos en la posición X4, X37 o X38.
X4 : Los inventores encontraron que los aminoácidos Y, W, T, M, I, A o C en la posición X4 eran capaces de disminuir la potencia sobre hAM1R. Por lo tanto, en una realización, X4 se selecciona de Y, W, T, M, I, A o C. Además, los aminoácidos W, M, I o C en la posición X4 fueron más efectivos para mejorar la potencia sobre hAMY3R (véanse el ejemplo 5, tabla 6). Por lo tanto, en una realización muy preferida de la invención, X4 se selecciona como W, M, I o C. Dado que los inventores encontraron que una sola posición elegida entre X4, X37 o X38 era suficiente para suprimir o reducir la potencia de AM1R, se deduce que, en algunas realizaciones, X4 es F (es decir, el aminoácido nativo presente en hAM15-52 (SEQ ID NO: 1) en dicha posición) y la potencia de AM1R se suprime o reduce usando la posición X37 y/o X38. Por lo tanto, en cualquiera de las realizaciones anteriores para X4 , se puede incluir F y suprimir o reducir la potencia sobre AM1R usando la posición X7 y/o X38.
X37: Asimismo, los inventores encontraron que los aminoácidos Y, S, W, T, Q, P, M, I, H, F, E, A, R, C en la posición X37 eran capaces de disminuir la potencia sobre hAM1 R. Así, en una realización, X37 se selecciona de Y, S, W, T, Q, P, M, I, H, F, E, A, R, C. Además, los aminoácidos Y, W, P, H o F en la posición X37 fueron más efectivos para mejorar
la potencia de hAMY3R (véanse el ejemplo 5, tabla 6). Por lo tanto, en una realización altamente preferida de la invención, X37 se selecciona como Y, W, P, H o F. Dado que los inventores encontraron que una sola posición elegida entre X4, X37 o X38 era suficiente para suprimir o reducir la potencia de AM1R, se deduce que en algunas realizaciones X37 es G (es decir, el amino nativo presente en hAM15-52 (SEQ ID NO: 1) en dicha posición), y la potencia de AM1R se suprime o reduce usando la posición X4 y/o X38. Por tanto, en cualquiera de las realizaciones anteriores para X37, se puede incluir G y suprimir o reducir la potencia sobre AM1R usando la posición X4 y/o X38.
X38: Asimismo, los inventores encontraron que los aminoácidos Hyp, W, T, Q, P, M, I, H, F, E, A, R o K en la posición X38 eran capaces de disminuir la potencia sobre hAM1 R. Por lo tanto, en una realización, X38 se selecciona de Hyp, W, T, Q, P, M, I, H, F, E, A, R o K. Además, los aminoácidos Hyp, W, M o F fueron los más efectivos para mejorar la potencia sobre hAMY3R (véanse el ejemplo 5, tabla 6). Por tanto, en una realización muy preferida de la invención, X38 se selecciona como Hyp, W, M o F. En la realización más preferida de la invención, X38 se selecciona como Hyp. Dado que los inventores encontraron que una sola posición elegida entre X4, X37 o X36 era suficiente para suprimir o reducir la potencia sobre AM1R, se deduce que en algunas realizaciones X38 es Y (es decir, el amino nativo presente en hAM15-52 (SEQ ID NO: 1) en dicha posición), y se suprime o reduce la potencia AM1R usando la posición X4 y/o X37. Por lo tanto, en cualquiera de las realizaciones anteriores para X38, se puede incluir Y y suprimir o reducir la potencia sobre AM1R usando la posición X4 y/o X37.
Puede verse una ilustración simple del aspecto 2 de la invención comparando el alineamiento de hAM15-52 (SEQ ID NO: 1) y la SEQ ID NO: 169 que se muestra a continuación.
SEQ ID NO:1 G C R F G T C T V Q K L A H Q I Y Q F T D K D K D N V A P R S K I S P Q G Y
SEQ ID NO:169 G C R F G T C T V Q R L A H Q I Y Q F T D K D K D N V A P R S K I S P Q G Hyp
SEQ ID NO:1 hAMY3R CE501,274 nM y hAM1 R CE501,113 nM
SEQ ID NO:169 hAMY3R CE500,063 nM y hAM1 R CE502.981,0 nM
Como puede verse, la R en la posición X11 ha mejorado la potencia en AMY3R aproximadamente 20 veces y la Hyp en la posición X38 ha disminuido la potencia en AM1R aproximadamente 2.500 veces. Por lo tanto, solo dos sustituciones han convertido hAM15-52 en un agonista de amilina con el mismo perfil farmacológico que hAMY1-37. Al mismo tiempo, la SEQ ID NO: 169 ha mantenido la estabilidad física (señal ThT: 2,700 %) de hAM15-52 (señal ThT: 2,600 %) en comparación con hAMY1-37 (señal ThT: 100,0 %) (véanse el ejemplo 2, Tabla 3). Así, en un segundo aspecto, la invención se refiere a una forma de suprimir más o menos completamente la potencia sobre hAM1 R del fragmento hAM15-52 mediante una o más sustituciones en la posición X4 , X37 y/o X38 y al mismo tiempo mejorar o mantener la potencia suficiente sobre AMY3R. Estos análogos de hAM15-52 serán, por lo tanto, análogos de hAMY3R muy potentes y selectivos. Al mismo tiempo, estos análogos de hAM15-52 mantienen la estabilidad física de hAM15-52 debido a la identidad de secuencia con hAM15-52. Como se muestra en el ejemplo 2, Tabla 3, la buena estabilidad física de hAM15-52 se puede mantener o incluso mejorar en los péptidos (debido a una identidad de al menos el 50 % con hAM15-52), mientras se proporcionan nuevos agonistas de hAMY3R que son tan potentes y selectivos como la amilina humana natural. En otras palabras, el segundo aspecto de la presente invención ha creado un análogo de amilina humana funcional oculto en un esqueleto de adrenomedulina.
Aumento de la potencia sobre hAMY3R con aminoácidos en la posición X 17.
Los inventores encontraron además que la potencia sobre hAMY3R podía mantenerse cuando X17 era Y, T, Q, M, I, F, A, R o K, o incluso mejorarse aún más cuando X17 era W o H. Así, en una realización, X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K. En una realización preferida, X17 se selecciona como W o H.
Así, en un segundo aspecto, la invención se refiere a análogos de hAM15-52 que comprenden 38 aminoácidos (X1-X38) o un sal farmacéuticamente aceptable de los mismos, en donde el aminoácido en la posición X 11 se selecciona de R, W o Cit y en donde el análogo de hAM15-52 tiene al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos un 85 % de identidad con hAM15-52, lo más preferiblemente al menos un 90 % de identidad con hAM15-52, tal como al menos un 95 % de identidad con hAM15-52 (SEQ ID NO: 1) y además en donde X4 se selecciona como F, Y, W, T, M, I, A o C; X37 se selecciona como G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona como Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K, con la condición de que al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición, más preferiblemente, al menos dos de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición. En el segundo aspecto, los análogos de hAM15-52 tienen un hAMY3R-CE50 ≤ 250 pM y un hAM1R-CE50 s 25 nM.
En una realización, X4 se selecciona como F, W, M, I o C; X37 se selecciona como G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona como Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K, con la condición de que al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición, más preferiblemente, al menos dos de las posiciones X4 , X37 o X38 no son el aminoácido presente en hAM15-52 (SEQ ID NO:
1) en dicha posición.
En una realización, X4 se selecciona como F, Y, W, T, M, I, A o C; X37 se selecciona como G, Y, W, P, H o F; X38 se selecciona como Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K, con la condición de que al menos una de las posiciones X4 ,
X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición, más preferiblemente, al menos dos de las posiciones X4 , X37 o X38 no son el aminoácido presente en hAM15-52 (SEQ ID NO: 1 ) en dicha posición.
En una realización, X4 se selecciona como F, Y, W, T, M, I, A o C; X37 se selecciona como G, Y, S, W, T, Q, P, M, I, H, F,
E, A, R, C o K; X38 se selecciona como Hyp, Y, W, M o F, con la condición de que al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición, más preferiblemente, al menos dos de las posiciones X4 , X37 o X38 no son el aminoácido presente en hAM15-52 (SEQ ID NO: 1 ) en dicha posición.
En una realización, X4 se selecciona como F, W, M, I o C; X37 se selecciona como G, Y, W, P, H o F; X38 se selecciona como Hyp, Y, W, M o F, con la condición de que al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición, más preferiblemente, al menos dos de las posiciones X4 , X37 o X38 no son el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización preferida, la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R, K;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID
NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad, incluso más preferiblemente al menos un 85 % de identidad, tal como al menos un 90 % de identidad, lo más preferiblemente al menos un 95 % de identidad, en donde
X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R, K; X4 se selecciona de F, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización más preferida adicional, la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad, tal como al menos un 85 % de identidad, más preferiblemente al menos un 90 % de identidad, lo más preferiblemente al menos un 95 % de identidad, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En otra realización más preferida, la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W, o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R, o K;
X4 se selecciona de F, Y, W, T, M, I, A, o C;
X37 se selecciona de G, Y, W, P, H, o F;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R, o K;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad, tal como al menos un 85 % de identidad, más preferiblemente al menos un 90 % de identidad, lo más preferiblemente al menos un 95 % de identidad, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización más preferida adicional, la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, M o F;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAMi5-52 (SEQ ID NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52) preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad, tal como al menos un 85 % de identidad, más preferiblemente al menos un 90 % de identidad, lo más preferiblemente al menos un 95 % de identidad, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, M o F; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización más preferida adicional, la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, W, P, H o F;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM^ - 52 , tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM^ -52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM^ -52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM^ -52, tal como al menos un 85 % de identidad con hAM15-52, más preferiblemente al menos un 90 % de identidad con hAM^ -52, lo más preferiblemente al menos un 95 % de identidad con hAM^ -52, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización preferida de la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, M o F;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID
NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52) preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos un 85 % de identidad con hAM15-52, más preferiblemente al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, M o F; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización preferida, la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, W, P, H o F;
X38 se selecciona de Hyp, Y, W, M o F;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad, tal como al menos un 85 % de identidad con hAM15-52, más preferiblemente al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, M o F; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización más preferida, la invención se refiere a un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, W, M, I o C;
X37 se selecciona de G, Y, W, P, H o F;
X38 se selecciona de Hyp, Y, W, M o F;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAMi 5-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM 15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos un 85 % de identidad con hAM15-52, más preferiblemente al menos un 90 % de identidad con hAM15-52, lo más preferiblemente al menos un 95 % de identidad con hAM15-52, en donde X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, W, M, I o C; X37 se selecciona de G, Y, W, P, H o F; X38 se selecciona de Hyp, Y, W, M o F; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (s Eq ID NO: 1) en dicha posición.
En cualquiera de las realizaciones mencionadas anteriormente, X11 es lo más preferiblemente R, y/o X17 es lo más preferiblemente Y, W o H. Además, en cualquiera de las realizaciones mencionadas anteriormente, lo más preferiblemente al menos dos de las posiciones X4 , X37 o X38 no son los aminoácidos presentes en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización más altamente preferida, la invención se refiere a un análogo de hAM15-52 con la secuencia SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360 o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM15-52, preferiblemente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM 15-52 (SEQ ID NO: 1), en donde, en el derivado, X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, Mv, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En una realización más altamente preferida adicional, la invención se refiere a un análogo de hAM15-52 con la secuencia SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360 o un derivado del mismo con al menos un 90 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360, preferiblemente al menos un 95 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360, lo más preferiblemente al menos un 97 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308 360, con la condición de que en el derivado, X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En cualquiera de las realizaciones mencionadas anteriormente, X4 se selecciona preferiblemente como F, W, M, I o C; X11 se selecciona preferiblemente como R; X37 se selecciona preferiblemente como G, Y, W, P, H o F; X38 se selecciona preferiblemente como Hyp, Y, W, M o F; X17 se selecciona preferentemente como W o H. Además, en cualquiera de las realizaciones mencionadas anteriormente, lo más preferiblemente al menos dos de las posiciones X4 , X37 o X38 no son el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
En la realización más preferida, la invención se refiere a un análogo de hAM15-52 con la secuencia de las SEQ ID NO: 3-57, 60-75, 77-79, 81 -92, 94-127, 129-147, 150-161, 163-179, 181 -206, 208-243, 246-305, o 308-360 o un derivado del mismo con al menos un 90 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94 127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360, preferiblemente al menos un 95 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181 206, 208-243, 246-305, o 308-360, lo más preferiblemente al menos un
97 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163 179, 181-206, 208-243, 246-305, o 308-360, con la condición de que un derivado del mismo tiene los mismos aminoácidos en las posiciones X4 , X11, X37 y X38, preferiblemente los mismos aminoácidos en la posición X4 , X11, X17, X37 y X38, como el respectivo análogo de hAM15-52 de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181 -206, 208-243, 246-305, o 308-360 del que se deriva.
Uso médico
En un tercer aspecto, la invención se refiere a análogos de hAM15-52 según el segundo aspecto para su uso como un medicamento. Más particularmente, el tercer aspecto de la invención se refiere a nálogos de hAM15-52 según el segundo aspecto para su uso en el tratamiento, prevención o mejora de una variedad de enfermedades, trastornos o afecciones, tales como, pero no limitados a, la ingesta excesiva de alimentos, exceso de peso corporal, obesidad, trastorno por atracones, síndrome de Prader-Willi, dislipidemia, enfermedades/trastornos metabólicos, diabetes I o II, tolerancia alterada a la glucosa, síndrome de resistencia a la insulina y/o NASH. Una realización preferida se refiere a uno o más análogos de hAM15-52 para su uso en el tratamiento de la obesidad, diabetes, NASH o combinaciones de las mismas.
Composiciones farmacéuticas
En un cuarto aspecto, la invención se refiere a composiciones farmacéuticas que comprenden uno o más de los análogos de hAM15-52 según el segundo aspecto y a su(s) uso(s) médico(s) para tratar, prevenir o mejorar una variedad de enfermedades, trastornos o afeccones según el tercer aspecto. Las composiciones farmacéuticas pueden comprender un portador (vehículo) farmacéuticamente aceptable y/o uno o más excipientes de acuerdo con técnicas convencionales en la técnica, tales como las descritas en 'Remington: Essentials of Pharmaceutics', Ed. por Linda A. Felton, Pharmaceutical press 2012.
Las formulaciones adecuadas incluyen, pero no se limitan a comprimidos, píldoras, cápsulas, emulsiones, suspensiones, de liberación sostenida o soluciones. Debe apreciarse que pueden usarse diferentes rutas de administración dependiendo de la elección de la formulación y la estabilidad química y/o metabólica de los polipéptidos. Dichas rutas de administración pueden incluir, pero no se limitan a, administración oral, administración parenteral (intravenosa (IV), subcutánea (SC), intradérmica (ID) e intramuscular (IM)), o inhalación. En una realización preferida de la invención, la ruta de administración es la administración parenteral. En una realización aún más preferida, la ruta de administración es subcutánea.
Ejemplos
Protocolos generales para la síntesis de los polipéptidos híbridos
Los péptidos se sintetizaron usando un sintetizador de péptidos en paralelo completamente automatizado SyroII (MultiSynTech GmbH, Alemania), equipado con un bloque calefactor, en Tentagel 5 RAM con una carga de 0,23-0,25 mmoles/g (Rapp Polymer GmbH, Alemania). La desprotección de Na-Fmoc se realizó en dos etapas mediante el tratamiento de la resina con piperidina al
40 %/DMF (HOBt 0,2 M (1-hidroxibenzotriazol)) durante 3 min a 45 °C, seguido de piperidina al 20 %/DMF (HOBt 0,1 M) durante 7-12 min a 75 °C. Excepto los residuos de Asp, Cys e His que fueron desprotecciones de Na-Fmoc a temperatura ambiente; es decir, piperidina al 40 %/DMF (HOBt 0,2 M) durante 3 min seguido de piperidina al 20 %/DMF (HOBt 0,1 M) durante 15 min. La química de acoplamiento fue DIC (N,N'-diisopropil-carbodiimida)/Oxima (acetato de ciano(hidroxiimino) de etilo) en d Mf usando soluciones de aminoácidos de 0,5 M en DMF y un exceso molar de 6 veces. Se usaron aminoácidos protegidos con Fmoc estándar. Las condiciones de acoplamiento fueron acoplamientos simples o dobles durante 15 min a 75 °C. Excepto los residuos de His y Cys, que se sometieron a acoplamiento doble durante 15 min a 50 °C. Los aminoácidos Fmoc se disolvieron a 0,5 M en DMF que contenía Oxima 0,5 M, excepto His que se disolvió en NMP. La resina se lavó 4 veces con NMP después de la desprotección con Na-Fmoc y 3 veces después de los acoplamientos.
El puente disulfuro se formó en la resina usando Tritilo (Trt) como grupo protector para la cisteína y tratándolo con yodo al 1 % en HFIP al 75 % (Hexafluoroisopropanol) en DCM durante 1 min. La resina se lavó 3 veces con HFIP al 75 % en DCM seguido de 4 veces con DCM.
Después de la síntesis, la resina se lavó con DCM y se secó, y el polipéptido se escindió de la resina mediante un tratamiento de
35 min con TFA (ácido trifluoroacético)/TES (trietilsilano)/agua (95/2,5/2,5) a 42 °C, seguido de precipitación con 4 volúmenes de éter dietílico frío, lavado adicional con éter dietílico y se dejó secar.
Los péptidos se caracterizaron por LC-MS (Waters, Dinamarca) y se cuantificaron por LC-CAD (ThermoFisher scientific, Dinamarca). Finalmente, los péptidos se liofilizaron para dar un polvo blanco usando un liofilizador de sobremesa Telstar.
Protocolos generales para ensayos de AMPc para medir la activación del receptor in vitro
hAMY3-R:
Se obtuvieron células que sobreexpresaban de forma estable el receptor hAMY3 de Ogeda (ahora Astellas Pharma), se subclonaron y una línea celular monoclonal con una ventana de ensayo apropiada se expandió, alicuotó y congeló. Se descongeló una alícuota y se sembró en placa en DPBS con caseína al 0,05 % e IBMX 0,5 mM como 2.000 células/pocillo en un formato de 384 pocillos. A continuación, las células se estimularon inmediatamente durante 30 min a temperatura ambiente con dosis graduadas del compuesto de ensayo usando amilina humana (Bachem, no. de cat. H-7905) como control positivo. La acumulación de AMPc se midió usando un ensayo Cisbio para receptores acoplados a Gs (no. de cat. 62AM4PEC), donde los reactivos del ensayo se añadieron según las instrucciones del fabricante y la transferencia de energía de fluorescencia en tiempo resuelto se registró después de una hora.
hAM1-R:
Se obtuvieron células que sobreexpresaban de forma estable el receptor hAM1 de Ogeda (ahora Astellas Pharma), se subclonaron y una línea celular monoclonal con una ventana de ensayo apropiada se expandió, alicuotó y congeló. Se descongeló una alícuota y se sembró en placa en DPBS con caseína al 0,05 % e IBMX 0,5 mM como 8.000
células/pocillo en un formato de 384 pocilios. A continuación, las células se estimularon inmediatamente durante 30 min a temperatura ambiente con dosis graduadas del compuesto de ensayo usando adrenomedulina humana 1-52 (Bachem, no. de cat. H-2932) como control positivo. La acumulación de AMPc se midió usando un ensayo Cisbio para receptores acoplados a Gs (no. de cat. 62AM4PEC), donde los reactivos del ensayo se añadieron según las instrucciones del fabricante y la transferencia de energía de fluorescencia en tiempo resuelto se registró después de una hora.
Protocolos generales para la determinación de la estabilidad física de los análogos peptídicos
Los péptidos se disolvieron en tampones (acetato de sodio 50 mM a pH 4 o fosfato de sodio 50 mM a pH 7) y se incubaron durante una hora. A continuación, las muestras se dividieron en dos réplicas de 80 μl en una placa negra de 384 pocillos (p-clear, Greiner Bio-One) y se mezclaron con Tioflavina T (ThT) hasta una concentración final de 4 pM. La placa se selló y se colocó en un lector de placas (CLARIOstar, BMG) donde la temperatura se ajustó a 40 °C durante el transcurso del experimento. Las muestras se tensaron aún más agitando la placa a 700 rpm (lineal) durante cinco minutos antes de cada medición. La fluorescencia se midió cada 10 min durante cuatro días excitando la ThT a 450 nm y midiendo la emisión a 480 nm. Para cada péptido, la señal de ThT a lo largo del tiempo se suavizó usando el ajuste de Regresión Polinomial Local (LOESS) implementado en el entorno de programación estadística R. Para los datos suavizados, la señal de ThT máxima se normalizó en porcentaje entre la señal de ThT máxima para hAMY y el fondo de tampón. Por lo tanto, los valores altos indican propiedades de fibrilación similares a hAMY, mientras que los valores bajos indican que no hay fibrilación.
Protocolos generales para el estudio de ingesta aguda de alimentos
El efecto sobre la ingesta acumulada de alimentos se midió en ratas macho Sprague Dawley (6 semanas de edad, Taconic, Dinamarca) después de una dosis única usando un sistema de monitorización de ingesta de alimentos totalmente automatizado (HM-2; MBROse ApS, Faaborg, Dinamarca), lo que permitió la monitorización avanzada sincrónica en tiempo real del comportamiento de ingesta de alimentos de animales individuales. Los animales se alojaron en grupos de 4 en una habitación con luz, temperatura y humedad controladas (ciclo 12/12 LD, luces encendidas a las 02:00 AM; 22 ± 2 °C; 50 % de humedad relativa). Los ratones tenían acceso ad libitum a una dieta de pienso regular (Altromin 1324, Brogaarden NS, Lynge, Dinamarca) y agua del grifo de calidad doméstica. Los ratones llegaron el día 7 y se permitió un mínimo de 5 días de habituación al sistema antes del comienzo del estudio. Durante estos días, los animales fueron manipulados diariamente para acostumbrarlos al paradigma experimental. El día de la dosificación, los animales se aleatorizaron en grupos según el peso corporal. Los animales se mantuvieron en ayunas durante cuatro horas antes de la dosificación. Los animales recibieron dosis SC 30 o 180 min antes de apagar las luces, y los datos de ingesta de alimentos se recopilaron automáticamente durante un total de 48 h posteriores a la dosificación con registros automáticos de alimentos cada 5 min.
Protocolos generales para el estudio de la obesidad crónica inducida por la dieta (DIO)
Las ratas Sprague-Dawley (Taconic, Dinamarca) llegaron a la edad de 5 semanas. Después de una semana de aclimatación, se agruparon de manera uniforme en función de su peso corporal en la línea base y se les ofreció acceso ad libitum a una dieta de dos opciones que consistía en gránulos de pienso (Altromin #1324, Brogaarden, Lynge, Dinamarca) y una dieta alta en azúcares/grasas de alta palatabilidad (mezcla 1:1:1 de Nutella (Ferrero, Alba, Italia), mantequilla de cacahuete (PCD, Rotterdam, Países Bajos) y pienso estándar en polvo (Altromin #1324, Brogaarden, Lynge, Dinamarca); 29,3 % de grasa, 33,2 % de carbohidratos, y 18 % de proteína) durante hasta 36 semanas. Las ratas se alojaron en parejas durante todo el estudio en condiciones ambientales controladas (ciclo de luz/oscuridad de 12 horas, luces apagadas a las 15:00; 22 ± 1 °C; 50 ± 10 % de humedad relativa). El peso corporal y la ingesta de alimentos y agua se monitorizaron diariamente durante todo el período del estudio. Un día antes del experimento, las ratas se aleatorizaron según el peso corporal en grupos experimentales (n = 9-10), que recibieron compuesto o vehículo SC. QD (una vez al día) durante 28 días.
Ejemplo 1
Los valores de CE50 en hAMY3R y hAM1 R se midieron según el protocolo general anterior. Se calculó el porcentaje de identidad para los análogos de hAM15 52 en comparación con hAM15-52. Los resultados se resumen en la Tabla 2 a continuación.
Tabla 2. La Tabla 2 muestra que los análogos de hAM15-52 (SEQ ID NO: 3-392) con potencia sobre hAMY3R mejorada en comparación con hAM15-52 pueden obtenerse cambiando el aminoácido K presente en hAM15-52 en la posición X11 en R, W o Cit. La Tabla 2 muestra además que los análogos de hAM15-52 altamente selectivos para hAMY3R (hAMY3R-CE50 ≤ 250 pM y un hAM1R-CE50 s 25 nM) (SEQ ID NO: 3-360) pueden obtenerse suprimiendo o reduciendo la potencia sobre hAM1R usando las posiciones X4 ,X37 y/o X38. Todas las lipidaciones en la posición 1 se realizaron en el extremo N y la lipidación en las otras posiciones se realizaron en un N épsilon en Lys. AMCHC se refiere al ácido trans-4-(aminometil)ciclohexanocarboxílico. OEG se refiere al ácido 8-amino-3,6-dioxaoctanoico u 8Ado.
Ejemplo 2
La fibrilación se determinó según el protocolo general para la determinación de la estabilidad física de los análogos peptídicos de péptidos. Los datos para los análogos de hAM15-52 seleccionados se resumen en la Tabla 3 a continuación.
Tabla 3. La Tabla 3 muestra que los análogos de hAM15-52 según la invención mantienen las buenas propiedades de fibrilación de hAM15-52 . La mayoría de los datos de fibrilación son comparables y algunos incluso mejores que hAM15-52 (SEQ ID NO: 1) a pH 7 (señal de ThT del 2,6%). Todos los datos de fibrilación son muy superiores en comparación con la referencia hAMY1-37 (SEQ ID NO: 2) (señal de ThT en 100 %).
Ejemplo 3
Se determinó el efecto de análogos de hAMi 5-52 seleccionados sobre la ingesta aguda de alimentos en ratas magras. Los resultados se resumen en la Tabla 4 a continuación.
Tabla 4. La Tabla 4 muestra que los análogos de hAM15-52 tienen potentes efectos anorexígenos hasta 48 horas después de una única inyección SC en ratas sanas magras (n=7-8), proporcionando así una prueba de principio. Modelo lineal de un factor de la prueba de Dunnett***: P < 0,001 en comparación con el vehículo (se realizaron tres operaciones independientes).
Ejemplo 4
Se determinó el efecto del tratamiento crónico de análogos de hAMi 5-52 seleccionados según la invención en ratas con obesidad inducida por la dieta (DIO). Los resultados se resumen en la Tabla 5 a continuación.
Tabla 5. La Tabla 5 muestra que las inyecciones SC diarias de SEQ ID NO: 46 o 78 causan una reducción significativa en el peso corporal en ratas con obesidad inducida por la dieta (n = 10) después de un período de tratamiento de 28 días, proporcionando así una prueba de concepto. Modelo lineal de un factor de la prueba de Dunnett***: P < 0,001 en comparación con el vehículo (se realizaron dos operaciones independientes).
Ejemplo 5
Investigación más profunda de los aminoácidos representativos en la posición X4, X11, X17, X37 y X38 y el correspondiente cambio de potencia. Los resultados se resumen en la Tabla 6 a continuación.
Tabla 6. La Tabla 6 muestra si el cambio de aminoácido provoca un incremento (I) en la potencia sobre hAMY3R, una potencia sin cambios (U) o una potencia disminuida (D) en comparación con el aminoácido de referencia (R). N/A No disponible.
Tabla 7. LISTADO DE SECUENCIAS
_ _
Tabla 7 continuación.
_ _
Claims (13)
1. Un análogo de hAMi5-52 o una sal farmacéuticamente aceptable del mismo que comprende 38 aminoácidos (X1-X38) con un hAMY3R-CE50 ^ 250 pM y un hAM1 R-CE50 ^ 25 nM, en donde el aminoácido en la posición X4 se selecciona como F, Y, W, T, M, I, A o C; X37 se selecciona como G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona como Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; X11 es R, W o Cit y en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición y además en donde el análogo de hAM15-52 tiene al menos al menos un 50 % de identidad con hAM15-52 (SeQ ID NO: 1).
2. Un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo según la reivindicación 1, en donde el análogo de hAM15-52 tiene al menos un 60 % de identidad con hAM15-52, tal como al menos un 70 % de identidad con hAM15-52, preferiblemente al menos un 80 % de identidad con hAM15-52 (SEQ ID No: 1).
3. Un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo según la reivindicación 1, que comprende la secuencia de aminoácidos de fórmula (I):
en donde
X11 se selecciona de R, W o Cit;
X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K;
X4 se selecciona de F, Y, W, T, M, I, A o C;
X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K;
y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición;
o un derivado del mismo con al menos un 50 % de identidad con hAM15-52, tal como al menos un 55 % de identidad con hAM15-52, tal como al menos un 60 % de identidad con hAM15-52, tal como al menos un 65 % de identidad con hAM1 emente al menos un 70 % de identidad con hAM15-52, tal como al menos un 75 % de identidad con hAM15-52, más preferiblemente al menos un 80 % de identidad con hAM15-52, tal como al menos un 90 % de identidad con hAM15-52, preferiblemente al menos un 95 % de identidad con hAM15-52, en donde, en el derivado, X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
4. Un análogo de hAM15-52 o una sal farmacéuticamente aceptable del mismo según la reivindicación 1 con la secuencia de las SEQ ID NO: 3-57, 60-75, 77-79, 81 -92, 94-127, 129-147, 150-161, 163-179, 181 -206, 208-243, 246-305 o 308 360 o un derivado de cualquiera de las mismas con al menos un 90 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360, preferiblemente al menos un 95 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94 127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360, lo más preferiblemente al menos un 97 % de identidad con una cualquiera de las SEQ ID NO: 3-57, 60-75, 77-79, 81-92, 94-127, 129-147, 150-161, 163-179, 181-206, 208-243, 246-305, o 308-360, con la condición de que en el derivado, X11 se selecciona de R, W o Cit; X17 se selecciona como Y, W, T, Q, M, I, H, F, A, R o K; X4 se selecciona de F, Y, W, T, M, I, A o C; X37 se selecciona de G, Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K; X38 se selecciona de Hyp, Y, W, T, Q, P, M, I, H, F, E, A, R o K; y además en donde al menos una de las posiciones X4 , X37 o X38 no es el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
5. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones anteriores, en donde al menos dos de las posiciones X4 , X37 y X38 no son el aminoácido presente en hAM15-52 (SEQ ID NO: 1) en dicha posición.
6. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones anteriores, en donde todas las posiciones X4 , X37 y X38 se seleccionan de la siguiente manera:
X4 se selecciona de Y, W, T, M, I, A o C;
X37 se selecciona de Y, S, W, T, Q, P, M, I, H, F, E, A, R, C o K;
X38 se selecciona de Hyp, W, T, Q, P, M, I, H, F, E, A, R o K;
7. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones anteriores, en donde X4 se selecciona como F, W, M, I o C.
8. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones anteriores, en donde X37 se selecciona como G, Y, W, P, H o F.
9. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones anteriores, en donde X38 se selecciona como Hyp, Y, W, M o F.
10. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones anteriores, en donde X17 se selecciona como W o H.
11. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones anteriores, en donde X11 es R.
12. Un análogo de hAM15-52 o un derivado del mismo según cualquiera de las reivindicaciones 1 -11 para su uso como un medicamento.
13. Una composición farmacéutica que comprende un análogo de hAM15-52 o un derivado del mismo según las reivindicaciones 1-11, un vehículo farmacéuticamente aceptable y, opcionalmente, uno o más excipientes.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20198117 | 2020-09-24 | ||
| PCT/EP2021/076250 WO2022063925A1 (en) | 2020-09-24 | 2021-09-23 | Ham15-52 analogues with improved amylin receptor (hamy3r) potency |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2950137T3 true ES2950137T3 (es) | 2023-10-05 |
Family
ID=72659001
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES21782735T Active ES2950137T3 (es) | 2020-09-24 | 2021-09-23 | Análogos de hAM15-52 con potencia mejorada frente al receptor de amilina (hAMY3R) |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US20240101634A1 (es) |
| EP (1) | EP4021929B1 (es) |
| JP (1) | JP2023544959A (es) |
| KR (1) | KR20230073176A (es) |
| CN (1) | CN116322741A (es) |
| AU (1) | AU2021350396A1 (es) |
| BR (1) | BR112023002525A2 (es) |
| CA (1) | CA3189267A1 (es) |
| DK (1) | DK4021929T5 (es) |
| ES (1) | ES2950137T3 (es) |
| FI (1) | FI4021929T3 (es) |
| HR (1) | HRP20230534T1 (es) |
| HU (1) | HUE062560T2 (es) |
| IL (1) | IL300620A (es) |
| MX (1) | MX2023002182A (es) |
| PL (1) | PL4021929T3 (es) |
| PT (1) | PT4021929T (es) |
| RS (1) | RS64256B1 (es) |
| SI (1) | SI4021929T1 (es) |
| WO (1) | WO2022063925A1 (es) |
| ZA (1) | ZA202301635B (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024003359A1 (en) | 2022-07-01 | 2024-01-04 | Gubra A/S | AMYLIN RECEPTOR (hAMY3R) AGONISTS WITH IMPROVED CHEMICAL STABILITY |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090286723A1 (en) | 2005-02-11 | 2009-11-19 | Amylin Pharmaceuticals, Inc. | Hybrid Polypeptides with Selectable Properties |
| US8722849B2 (en) | 2011-06-10 | 2014-05-13 | Novo Nordisk A/S | Polypeptides |
| AR097701A1 (es) * | 2013-09-19 | 2016-04-13 | Zealand Pharma As | Análogos de amilina |
| EP3271381B1 (en) | 2015-03-18 | 2021-09-08 | Zealand Pharma A/S | Amylin analogues |
| WO2019005623A1 (en) | 2017-06-30 | 2019-01-03 | Adepthera Llc | PEPTIDE ANALOGS |
| AR116632A1 (es) * | 2018-10-11 | 2021-05-26 | Intarcia Therapeutics Inc | Polipéptidos análogos de la amilina humana y sus métodos de uso |
-
2021
- 2021-09-23 KR KR1020237005061A patent/KR20230073176A/ko unknown
- 2021-09-23 MX MX2023002182A patent/MX2023002182A/es unknown
- 2021-09-23 US US18/024,879 patent/US20240101634A1/en active Pending
- 2021-09-23 FI FIEP21782735.1T patent/FI4021929T3/fi active
- 2021-09-23 IL IL300620A patent/IL300620A/en unknown
- 2021-09-23 HR HRP20230534TT patent/HRP20230534T1/hr unknown
- 2021-09-23 CA CA3189267A patent/CA3189267A1/en active Pending
- 2021-09-23 RS RS20230442A patent/RS64256B1/sr unknown
- 2021-09-23 SI SI202130047T patent/SI4021929T1/sl unknown
- 2021-09-23 EP EP21782735.1A patent/EP4021929B1/en active Active
- 2021-09-23 AU AU2021350396A patent/AU2021350396A1/en active Pending
- 2021-09-23 HU HUE21782735A patent/HUE062560T2/hu unknown
- 2021-09-23 JP JP2023510390A patent/JP2023544959A/ja active Pending
- 2021-09-23 CN CN202180056599.9A patent/CN116322741A/zh active Pending
- 2021-09-23 ES ES21782735T patent/ES2950137T3/es active Active
- 2021-09-23 PT PT217827351T patent/PT4021929T/pt unknown
- 2021-09-23 DK DK21782735.1T patent/DK4021929T5/da active
- 2021-09-23 WO PCT/EP2021/076250 patent/WO2022063925A1/en active Application Filing
- 2021-09-23 BR BR112023002525A patent/BR112023002525A2/pt unknown
- 2021-09-23 PL PL21782735.1T patent/PL4021929T3/pl unknown
-
2023
- 2023-02-09 ZA ZA2023/01635A patent/ZA202301635B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| SI4021929T1 (sl) | 2023-09-29 |
| WO2022063925A1 (en) | 2022-03-31 |
| AU2021350396A1 (en) | 2023-03-16 |
| RS64256B1 (sr) | 2023-07-31 |
| US20240101634A1 (en) | 2024-03-28 |
| PT4021929T (pt) | 2023-06-21 |
| JP2023544959A (ja) | 2023-10-26 |
| MX2023002182A (es) | 2023-11-16 |
| CA3189267A1 (en) | 2022-03-31 |
| HRP20230534T1 (hr) | 2023-08-04 |
| KR20230073176A (ko) | 2023-05-25 |
| CN116322741A (zh) | 2023-06-23 |
| FI4021929T3 (fi) | 2023-06-14 |
| DK4021929T3 (da) | 2023-07-10 |
| IL300620A (en) | 2023-04-01 |
| PL4021929T3 (pl) | 2023-07-31 |
| HUE062560T2 (hu) | 2023-11-28 |
| BR112023002525A2 (pt) | 2023-04-04 |
| ZA202301635B (en) | 2024-03-27 |
| DK4021929T5 (da) | 2024-07-29 |
| EP4021929A1 (en) | 2022-07-06 |
| EP4021929B1 (en) | 2023-04-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11834486B2 (en) | Incretin analogs and uses thereof | |
| KR102351313B1 (ko) | Gip/glp1 공효능제 화합물 | |
| AU2018388962B2 (en) | Incretin analogs and uses thereof | |
| AU2020408139B2 (en) | Incretin analogs and uses thereof | |
| ES2950137T3 (es) | Análogos de hAM15-52 con potencia mejorada frente al receptor de amilina (hAMY3R) | |
| US20240270821A1 (en) | Gip/glp1/gcg tri-receptor agonists and uses thereof | |
| WO2024003359A1 (en) | AMYLIN RECEPTOR (hAMY3R) AGONISTS WITH IMPROVED CHEMICAL STABILITY | |
| EA047788B1 (ru) | Аналоги инкретина и их применение | |
| EA043728B1 (ru) | Аналоги инкретина и их применение | |
| EA043950B1 (ru) | Аналоги инкретина и их применение |