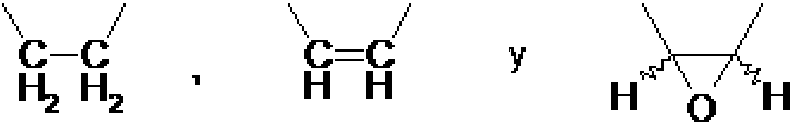ES2759247T3 - Antagonistas muscarínicos y combinaciones de estos para el tratamiento de enfermedades de las vías respiratorias en caballos - Google Patents
Antagonistas muscarínicos y combinaciones de estos para el tratamiento de enfermedades de las vías respiratorias en caballos Download PDFInfo
- Publication number
- ES2759247T3 ES2759247T3 ES15728025T ES15728025T ES2759247T3 ES 2759247 T3 ES2759247 T3 ES 2759247T3 ES 15728025 T ES15728025 T ES 15728025T ES 15728025 T ES15728025 T ES 15728025T ES 2759247 T3 ES2759247 T3 ES 2759247T3
- Authority
- ES
- Spain
- Prior art keywords
- lama
- halogen
- alkyl
- pharmaceutically acceptable
- inhaler
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 C*1(*)C(C2)[C@]3OC3C1C[C@@]2(OC(C(*)(c1ccccc1)c1ccccc1)=O)I Chemical compound C*1(*)C(C2)[C@]3OC3C1C[C@@]2(OC(C(*)(c1ccccc1)c1ccccc1)=O)I 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/46—8-Azabicyclo [3.2.1] octane; Derivatives thereof, e.g. atropine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/02—Medicinal preparations containing materials or reaction products thereof with undetermined constitution from inanimate materials
- A61K35/04—Tars; Bitumens; Mineral oils; Ammonium bituminosulfonate
- A61K35/06—Mineral oils, e.g. paraffinic oils or aromatic oils based on aromatic hydrocarbons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/008—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy comprising drug dissolved or suspended in liquid propellant for inhalation via a pressurized metered dose inhaler [MDI]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/009—Inhalators using medicine packages with incorporated spraying means, e.g. aerosol cans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2250/00—Specially adapted for animals
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pulmonology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Otolaryngology (AREA)
- Emergency Medicine (AREA)
- Hematology (AREA)
- Anesthesiology (AREA)
- Biomedical Technology (AREA)
- Heart & Thoracic Surgery (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
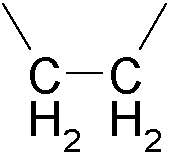
Un antagonista muscarínico de acción prolongada (LAMA) o una sal farmacéuticamente aceptable del catión del mismo para uso en un método de tratamiento de una enfermedad de las vías respiratorias en un équido, preferiblemente un caballo, en donde el LAMA es un compuesto de la fórmula general:**Fórmula** en donde A designa un grupo de doble enlace seleccionado entre**Fórmula** X- designa un anión con una sola carga negativa, R1 y R2 designan alquilo C1-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno; R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4, alquiloxi C1-C4, hidroxi, CF3, CN, NO2 o halógeno; R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1- C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-COCF3 o halógeno, opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos, siempre que si A designa**Fórmula** R1 y R2 designan metilo y R3, R4, R5 y R6 designan hidrógeno, entonces R7 no puede ser también hidrógeno, preferiblemente, el LAMA es un compuesto de la fórmula (LAMA 1):**Fórmula**
Description
DESCRIPCIÓN
Antagonistas muscarínicos y combinaciones de estos para el tratamiento de enfermedades de las vías respiratorias en caballos
Campo de la invención
La invención se refiere al campo de la medicina, en particular al campo de la medicina veterinaria. La invención se refiere, específicamente, a antagonistas muscarínicos de acción prolongada (LAMAs) para el tratamiento de enfermedades de las vías respiratorias tales como la enfermedad pulmonar, preferiblemente la obstrucción recurrente de las vías respiratorias (RAO), enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD) y la enfermedad inflamatoria de las vías respiratorias (IAD) en équidos tales como caballos.
Información de antecedentes
La enfermedad de las vías respiratorias en équidos es una enfermedad importante en muchos caballos. Se puede dividir en las enfermedades de las vías respiratorias superiores e inferiores. Existe un cierto número de enfermedades de las vías respiratorias inferiores en équidos con origen no infeccioso como tales como la RAO (o arcadas o enfermedad pulmonar obstructiva crónica equina), IAD, SPAOPD y hemorragia pulmonar inducida por el ejercicio (EIPH). Esta última se diagnostica típicamente en caballos de carreras. RAO, IAD y SPAOPD son enfermedades con un fondo alérgico. Trastornos adicionales de las vías respiratorias inferiores raramente diagnosticados son las neumonías granulomatosas, neoplásicas e intersticiales. Las enfermedades infecciosas de las vías respiratorias inferiores incluyen bronquitis, neumonía, pleuritis o una combinación de éstas provocadas por agentes víricos, bacterianos, fúngicos y parasitarios (Kutasi et al., 2011).
Manifestaciones fenotípicas comunes de enfermedades de las vías respiratorias en los caballos incluyen tos, descarga nasal, aumento del esfuerzo respiratorio y bajo rendimiento o intolerancia al ejercicio. Adicionalmente, fiebre, depresión, disminución del apetito y pérdida de peso pueden se pueden observar en enfermedades de las vías respiratorias infecciosas (Couetil et al., 2007 y Kutasi et al., 2011). Enfermedades de las vías respiratorias equinas con antecedentes de alergia no se pueden curar, sino sólo mantener asintomáticas. Las terapias conocidas para estos caballos incluyen cambios en el entorno y la administración de diferentes fármacos. El objetivo del cambio en el entorno estable es mejorar la calidad de las vías respiratorias y reducir la exposición a los alérgenos de los caballos, que podrían desencadenar exacerbaciones de la RAO, SPAOPD e IAD. Los siguientes fármacos se utilizan para el tratamiento de enfermedades de las vías respiratorias con origen no infeccioso: glucocorticoides, broncodilatadores (agonistas de los receptores beta 2 adrenérgicos y antagonistas muscarínicos), y mucosolventes (dembrexina y acetilcisteína). Además, se administran antibióticos para las enfermedades de las vías respiratorias infecciosas. Efectos secundarios prominentes de estas terapias convencionales son taquicardia, midriasis, cambio en el estado de hidratación de las membranas mucosas y cólico para broncodilatadores y supresión adrenocortical (reducción en los niveles de suero sanguíneo de cortisol), laminitis, hepatopatía, pérdida de masa muscular, metabolismo óseo alterado, aumento de la susceptibilidad a la infección (neutrofilia, linfopenia) y respuesta de anticuerpos disminuida a la vacunación para glucocorticoides (Couetil et al., 2007, Dauvillir et al., 2011). Otra publicación, Robinson et al. 1993, describe la respuesta de las vías respiratorias de los caballos con obstrucción recurrente de las vías respiratorias (jadeos) a la administración en aerosol de la sustancia bromuro de ipratropio. El problema subyacente de la presente invención es proporcionar un medicamento para caballos que permita el tratamiento de enfermedades de las vías respiratorias en caballos con un inicio rápido de la acción, al tiempo que se reduce el riesgo de efectos secundarios de los animales tratados.
Breve sumario de la invención
Se ha encontrado, sorprendentemente, que antagonistas muscarínicos de acción prolongada (LAMAs) son particularmente ventajosos para el uso en un método de tratar una enfermedad de las vías respiratorias en équidos, preferiblemente caballos, en donde los LAMAs de la presente invención tienen la siguiente estructura general:
en donde
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo C1-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4, alquiloxi C1-C4, hidroxi, CF3, Cn , NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-COCF3 o halógeno,
opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos, siempre que, si A designa
R1 y R2 designan metilo y
R3, R4, R5 y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno.
Además, se ha encontrado, sorprendentemente, que especialmente LAMA 1 u otra sal farmacéuticamente aceptable del catión del mismo o una composición que comprende LAMA 1 o una sal farmacéuticamente aceptable del mismo es particularmente ventajoso para el uso en un método de tratamiento de una enfermedad de las vías respiratorias en équidos, preferiblemente caballos.
Una ventaja de la presente invención es el rápido inicio del efecto después de la administración que dura hasta varias horas (véase, por ejemplo, el ejemplo 7). Además, el tratamiento una vez al día con LAMA 1 durante una semana es equiparable a la mejora significativa en la función pulmonar después de la administración dos veces al día de clenbuterol durante una semana. Esto va acompañado de un aumento significativo del pH en la sangre arterial y de una disminución significativa en la presión parcial de dióxido de carbono (paCO2) en la sangre arterial que se observan sólo después de la administración de LAMA 1 durante una semana.
Además, se ha encontrado, sorprendentemente, que una combinación de un antagonista muscarínico de acción prolongada (LAMA) de la fórmula I, preferiblemente LAMA 1 u otra sal farmacéuticamente aceptable del catión del mismo, y un glucocorticoide tal como ciclesonida, o una sal farmacéuticamente aceptable del mismo, es particularmente ventajoso para uso en un método de tratar una enfermedad de las vías respiratorias en équidos, preferiblemente caballos. Una ventaja de la presente invención es el rápido inicio del efecto después de la administración de la combinación.
Adicionalmente, se ha encontrado, sorprendentemente, que una combinación (triple) de un antagonista muscarínico de acción prolongada (LAMA) de la fórmula I, lo más preferiblemente LAMA 1 u otra sal farmacéuticamente aceptable del catión del mismo, y un glucocorticoide tal como ciclesonida o una sal farmacéuticamente aceptable del mismo y opcionalmente un agonista beta-2 adrenérgico de acción prolongada (LABA) o una sal farmacéuticamente aceptable del mismo es particularmente ventajoso para uso en un método de tratar una enfermedad de las vías respiratorias en équidos, preferiblemente caballos. Una ventaja de la presente invención es el gran alcance del efecto después de la administración de la combinación (triple).
LAMA 1 mejora la función pulmonar, aumenta el pH de la sangre y reduce la paCO2, en tanto que LABAs y/o LAMAs mejoran, en general, la función pulmonar y la puntuación clínica, mientras ciclesonida mejora asimismo la función pulmonar y la puntuación clínica.
LAMA 1 no está actualmente aprobado en équidos u otras especies. Clenbuterol está aprobado en équidos para ser utilizado para el tratamiento de enfermedades de las vías respiratorias acompañadas de broncoespasmos.
Aunque tanto LAMAs como LABAs, en general, así como glucocorticoides tales como ciclesonida se utilizan por
separado como medicación contra enfermedades pulmonares en determinadas especies, es sorprendente que la o las combinaciones arriba descritas (tales como combinaciones dobles o triples de LAMAs, glucocorticoides y, opcionalmente, LABAs preferiblemente la combinación de un LAMA, lo más preferiblemente LAMA 1, y un glucocorticoide, lo más preferiblemente ciclesonida) conduzcan realmente a un alivio rápido y extensivo durante las enfermedades pulmonares equinas tales como RAO, IAD y SPAOPD. Algunas combinaciones son conocidas en la medicina humana para el tratamiento del asma y/o la enfermedad pulmonar obstructiva crónica (p. ej. Symbicort® Turbohaler® que contienen budesonida y formoterol). Sin embargo, estas combinaciones no han demostrado ser eficaces hasta ahora en équidos tales como caballos.
La ventaja de la o las combinaciones arriba descritas (LAMA, preferiblemente LAMA 1, y un glucocorticoide, preferiblemente ciclesonida, así como combinaciones triples con un LABA) en comparación con el uso de un glucocorticoide tal como ciclesonida o budesonida o fluticasona en solitario es que el inicio del efecto es rápido (en el espacio de minutos después de la administración de la combinación).
Una ventaja adicional de la terapia de combinación (tal como las combinaciones arriba descritas, especialmente la combinación de un LAMA, preferiblemente LAMA 1, y un glucocorticoide, preferiblemente ciclesonida) comparada, por ejemplo, con el uso de un LAMA a solas, es que el efecto (técnico/terapéutico) observado es mayor para la combinación.
Breve descripción de los dibujos
FIGURA 1: FASE I
Variaciones temporales de la presión transpulmonar (APL) en dos caballos individuales (caballo ID 312 y 91) después de una administración única de 800 |jg de LAMA 1.
FIGURA 2: FASE I
Variaciones temporales de la resistencia pulmonar (RL) en dos caballos individuales (caballo ID 312 y 91) después de una administración única de 800 jg de LAMA 1.
FIGURA 3: FASE I
Variaciones temporales de la elastancia pulmonar (EL) en dos caballos individuales (caballo ID 312 y 91) después de una administración única de 800 jg de LAMA 1.
FIGURA 4: FASE IV - PERIODO 1
Variaciones temporales de la presión transpulmonar (APL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (20 inhalaciones, 100 jg/inhalación en formulación acuosa) FIGURA 5: FASE IV - PERIODO 1
Variaciones temporales de la resistencia pulmonar (RL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (20 inhalaciones, 100 jg/inhalación en formulación acuosa) FIGURA 6: FASE IV - PERIODO 1
Variaciones temporales de la elastancia pulmonar (EL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (20 inhalaciones, 100 jg/inhalación en formulación acuosa) FIGURA 7: FASE IV - PERIODO 2
Variaciones temporales de la presión transpulmonar (APL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (4 inhalaciones, 500 jg/inhalación en formulación etanólica) FIGURA 8: FASE IV - PERIODO 2
Variaciones temporales de la resistencia pulmonar (RL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (4 inhalaciones, 500 jg/inhalación en formulación etanólica) FIGURA 9: FASE IV - PERIODO 2
Variaciones temporales de la elastancia pulmonar (EL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (4 inhalaciones, 500 jg/inhalación en formulación etanólica) FIGURA 10: FASE IV - PERIODO 3
Variaciones temporales de la presión transpulmonar (APL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (20 inhalaciones, 100 jg/inhalación en formulación etanólica) FIGURA 11: FASE IV - PERIODO 3
Variaciones temporales de la resistencia pulmonar (RL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (20 inhalaciones, 100 jg/inhalación en formulación etanólica) FIGURA 12: FASE IV - PERIODO 3
Variaciones temporales de la elastancia pulmonar (EL) en dos caballos individuales (caballo ID 40 y 91) después de una administración única de 2000 jg de LAMA 1 (20 inhalaciones, 100 jg/inhalación en formulación etanólica)
FIGURA 13: FASE II
Variaciones temporales en la puntuación del esfuerzo respiratorio asociadas con la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 |jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) entre los días 1 y 7 (media ± SEM) (n =8), en donde SEM es “error típico de la media”. * significativamente diferente.
FIGURA 14: FASE II
Variaciones temporales en la presión transpulmonar (APL) asociadas con la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) entre los días 1 y 7 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
FIGURA 15: FASE II
Variaciones temporales en la elastancia pulmonar (EL) asociadas con la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) entre los días 1 y 7 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
FIGURA 16: FASE II
Variaciones temporales en la resistencia pulmonar (RL) asociadas con la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) entre los días 1 y 7 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
FIGURA 17: FASE II
Variaciones temporales en la presión transpulmonar (APL) antes y 30 minutos después de la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) el Día 4 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
FIGURA 18: FASE II
Variaciones temporales en la resistencia pulmonar (RL) antes y 30 minutos después de la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) el Día 4 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
FIGURA 19: FASE II
Variaciones temporales en la elastancia pulmonar (EL) antes y 30 minutos después de la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) el Día 4 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
FIGURA 20: FASE II
Variaciones temporales en el pH de muestras de sangre arterial asociadas con la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) entre los días 1 y 7 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
FIGURA 21: FASE II
Variaciones temporales en la paCO2 de muestras de sangre arterial asociadas con la administración de clenbuterol (barras en negro) y tres dosis diferentes de LAMA 1 (2 inhalaciones: 200 jg (barras en blanco), cuatro inhalaciones: 400 jg (barras en gris claro) y 8 inhalaciones: 800 jg (barras en gris oscuro) entre los días 1 y 7 (media ± SEM) (n =8), en donde SEM es “error típico de la media”.
Descripción detallada de la invención
Antes de describir los diversos aspectos de la presente invención se debe observar que tal como se utiliza en esta memoria y en las reivindicaciones adjuntas, las formas singulares "un", "una", y "el", “la” incluyen una referencia al plural, a menos que el contexto dicte claramente lo contrario. Así, por ejemplo, la referencia a "una preparación" incluye una pluralidad de referencias a preparaciones de este tipo, la referencia al "soporte" es una referencia a uno o más soportes y equivalentes de los mismos conocidos por los expertos en la técnica, y así sucesivamente. A menos que se defina lo contrario, todos los términos técnicos y científicos utilizados en esta memoria tienen los mismos significados que se entienden comúnmente por un experto ordinario en la técnica a la que pertenece esta invención. Todos los intervalos y valores dados pueden variar de 1 a 5%, a menos que se indique lo contrario o se conozca de otro modo por la persona experta en la técnica, por lo tanto, el término "aproximadamente" se omitió de la descripción. Aunque cualesquiera métodos y materiales similares o equivalentes a los descritos en esta memoria se pueden utilizar en la práctica o el ensayo de la presente invención, ahora se describen métodos, dispositivos y materiales preferidos. Todas las publicaciones se mencionan en esta memoria con el propósito de describir y
divulgar las sustancias, los excipientes, vehículos y las metodologías tal como se reseñan en las publicaciones que podrían ser utilizadas en conexión con la invención. Nada en esta memoria debe interpretarse como una admisión de que la invención no tiene derecho a antedatar dicha divulgación en virtud de la invención anterior. Términos y expresiones no definidos específicamente en esta memoria deben tener los significados que se les pueda dar por un experto en la técnica a la vista de la descripción y el contexto. Tal como se utiliza en la memoria descriptiva, sin embargo, a menos que se especifique lo contrario, los siguientes términos y expresiones tienen el significado indicado y las siguientes convenciones se cumplen.
Antagonistas muscarínicos:
La expresión “antagonistas muscarínicos” se refiere a un grupo de sustancias que bloquean los efectos de acetilcolina en los receptores muscarínicos para invertir la obstrucción de las vías respiratorias [Barnes, 2004]. Por lo tanto, “antagonistas muscarínicos” se designan también a menudo como “anticolinérgicos” o “agentes anticolinérgicos”.
Ejemplos de antagonistas muscarínicos incluyen bromuro de ipratropio (que a menudo se administra en la medicina equina), atropina, bromuro de aclidinio, umeclidinio y glicopirrolato. Se pueden definir los siguientes subgrupos de antagonistas muscarínicos:
1. “antagonistas muscarínicos de acción prolongada" o “LAMAs”;
2. “antagonistas muscarínicos de corta acción“ o “SAMAs”.
Un ejemplo de un LAMA es glicopirrolato. Un ejemplo de un SAMA es atropina.
La expresión “antagonistas muscarínicos de acción prolongada” o “LAMAs” se refiere a un grupo de sustancias que bloquean los efectos de acetilcolina en receptores muscarínicos durante un periodo de tiempo prolongado. Ejemplos de LAMAs incluyen bromuro de tiotropio o anticolinérgicos de la siguiente fórmula general I:
en donde
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo C1-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4, alquiloxi C1-C4, hidroxi, CF3 , CN, NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-C0 CF3 o halógeno,
opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos,
siempre que, si A designa
R1 y R2 designan metilo y
R3, R4, R5 y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno.
Anticolinérgicos de la fórmula general I y procedimientos para prepararlos se describen, por ejemplo, en el documento WO02/32899.
LAMA 1:
El término “LAMA 1” describe un nuevo agente anticolinérgico con el nombre químico (1a,2p,4p,5a,7p)-3-oxa-9-azoniatricicl[3.3.1.024]nonano, 7-(1-oxo-2,2-difenilpropoxi)-bromuro de 9,9-dimetilo o, alternativamente, (nombre corto) metobromuro de 2,2-difenilpropionato de escopina.
LAMA 1 (= metobromuro de 2,2-difenilpropionato de escopina) tiene la siguiente estructura química:
Fórmula II
LAMA 1 tiene la fórmula empírica C24H28NO3- Br y tiene un peso molecular de 458,39 g/mol.
LAMA 1 se caracteriza, además, como sigue:
Agonistas de adrenorreceptores beta-2:
La expresión “agonistas de adrenorreceptores beta-2” o “agonistas beta-2 adrenérgicos” se refiere a un grupo de sustancias que estimulan a los receptores p2-adrenérgicos para relajar la musculatura lisa de las vías respiratorias [Tashkin y Fabbri, 2010].
Se pueden definir los siguientes subgrupos de “agonistas de adrenorreceptores beta-2” o “agonistas beta-2 adrenérgicos”:
1. “agonistas beta-2 adrenérgicos de acción prolongada” o “LABAs”;
2. “agonistas beta-2 adrenérgicos de corta acción” o “SABAs”.
La expresión “agonistas beta-2 adrenérgicos de acción prolongada” o “LABAs” se refiere a un subgrupo de sustancias que estimulan a los receptores p2 -adrenérgicos para relajar la musculatura lisa de las vías respiratorias durante un período de tiempo prolongado.
Ejemplos de LABAs incluyen salmeterol, formoterol, bambuterol, indacaterol, vilanterol, abediterol e hidrocloruro de olodaterol.
Ejemplos de agonistas adrenorreceptores beta-2 del tipo SABA incluyen salbutamol o albuterol, clenbuterol, pirbuterol y fenoterol.
Glucocorticoides:
El término “glucocorticoide” se refiere a una clase de hormonas esteroideas que se unen al receptor de glucocorticoides (GR) que está presente en casi cualquier célula animal de los vertebrados. El nombre glucocorticoide (glucosa corteza esteroide) se deriva de su papel en la regulación del metabolismo de la glucosa, su síntesis en la corteza adrenal y su estructura esteroide.
Los glucocorticoides son parte del mecanismo de retroalimentación en el sistema inmunológico que reduce la actividad inmunológica (inflamación). Por lo tanto, se utilizan en medicina para tratar enfermedades provocadas por un sistema inmunológico superactivo tal como alergias, asma, enfermedades autoinmunes y sepsis.
Glucocorticoides preferidos de acuerdo con la siguiente invención con ciclesonida y/o budesonida y/o fluticasona. El término "ciclesonida" ((11p, 16a)-16,17-[[(R) ciclohexilmetileno]bis(oxi)]-11-hidroxi-21-(2-metiM-oxopropoxi)pregna-1,4-dieno-3,20-diona, C32H44O2, Mr = 540,7 g/mol) es bien conocido en la técnica y significa/describe un glucocorticoide utilizado para tratar el asma y la rinitis alérgica en los seres humanos. Se comercializa para su aplicación en seres humanos bajo el nombre de marca para Alvesco™ para el asma y Omnaris™/Omniair™ para la fiebre del heno en los Ee .UU. y Canadá. La ciclesonida es un profármaco. Se transforma en el metabolito activo C21-C21-desisobutirilciclesonida (= desciclesonida) a través de hidrólisis por parte de esterasas intracelulares en los pulmones. La ciclesonida es un glucocorticoide no halogenado, que existe predominantemente en su forma como enantiómero R.
Tal como se utiliza en esta memoria, el término "profármaco" se refiere a (i) una forma inactiva de un fármaco que ejerce sus efectos después de los procesos metabólicos en el cuerpo convirtiéndolo en una forma utilizable o activa, o (ii) una sustancia que da lugar a un metabolito farmacológicamente activo, aunque no por sí mismo activo (es decir, un precursor inactivo).
Los términos "profármaco" o "derivado de profármaco" significan un derivado, soporte o precursor unido covalentemente del compuesto parental o sustancia farmacológicamente activa que se somete a al menos alguna biotransformación antes de exhibir su o sus efectos farmacológicos. Tales profármacos tienen grupos metabólicamente escindibles o convertibles de otro modo y se transforman rápidamente in vivo para proporcionar el compuesto parental, (también llamado el metabolito activo), por ejemplo por hidrólisis en la sangre o por la activación a través de la oxidación como en el caso de grupos tioéter. Profármacos más comunes incluyen ésteres y análogos de amidas de los compuestos parentales. El profármaco se formula con los objetivos de una estabilidad química mejorada, aceptación y cumplimiento mejorados del paciente, biodisponibilidad mejorada, duración prolongada de la acción, selectividad de órganos mejorada, formulación mejorada (p. ej., hidrosolubilidad mejorada) y/o efectos secundarios disminuidos (p. ej., toxicidad). En general, los profármacos propiamente dichos tienen una débil o nula actividad biológica y son estables bajo condiciones ordinarias. Habitualmente, los profármacos se pueden preparar fácilmente a partir de los compuestos parentales utilizando métodos conocidos en la técnica.
El término "équido" significa de o que pertenece a la familia Equidae, que incluye a los caballos, asnos y cebras,
preferentemente caballos. Además, el término "équido" abarca también híbridos de miembros de la familia Equidae (por ejemplo, mulas, burdéganos, etc.).
El término "paciente" o "sujeto" incluye mamíferos tales como primates incluyendo seres humanos. El término "paciente" o "sujeto", tal como se utiliza en esta memoria, se refiere específicamente a caballos, especialmente caballos que padecen enfermedades de las vías respiratorias (particularmente enfermedad pulmonar), preferiblemente obstrucción recurrente de las vías respiratorias (RAO) también llamada arcadas o COPD equina y/o enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD) también llamada obstrucción recurrente de las vías respiratorias asociada al pasto del verano (SPARAO) y/o enfermedad inflamatoria de las vías respiratorias (IAD), lo más preferiblemente RAO.
La expresión "enfermedad de las vías respiratorias" en caballos significa lo siguiente: obstrucción recurrente de las vías respiratorias (RAO) también llamada arcadas o COPD equina, enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD), enfermedad inflamatoria de las vías respiratorias (IAD), hemorragia pulmonar inducida por el ejercicio (EIPH), enfermedades infecciosas, enfermedad pulmonar intersticial crónica y trastornos funcionales del tracto respiratorio superior.
La expresión "enfermedad pulmonar" significa: obstrucción recurrente de las vías respiratorias (RAO) también llamada arcadas o COPD equina, enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD), enfermedad inflamatoria de las vías respiratorias (IAD), hemorragia pulmonar inducida por el ejercicio (EIPH), enfermedades infecciosas, enfermedad pulmonar intersticial crónica.
La expresión "obstrucción recurrente de las vías respiratorias (RAO)" en caballos significa lo siguiente: un síndrome crónico de caballos maduros con obstrucción reversible de las vías respiratorias en los que muestra períodos estables de respiración dificultosa en reposo durante la exacerbación.
La expresión "enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD)" en caballos significa lo siguiente: un síndrome crónico, que comparte muchas similitudes clínicas y patológicas con RAO en reposo en el pasto, lo que sugiere una patogénesis similar, sin embargo, es provocada por diferentes antígenos.
La expresión "enfermedad inflamatoria de las vías respiratorias (IAD)" en caballos significa lo siguiente: un síndrome crónico de los caballos que muestran un rendimiento deficiente o tos o un exceso de moco traqueal sin mostrar períodos de respiración dificultosa en reposo.
La expresión "cantidad eficaz", tal como se utiliza en esta memoria, significa una cantidad suficiente para lograr una reducción de la enfermedad de las vías respiratorias en un caballo cuando se administra ciclesonida, preferiblemente a una dosis tal como se describe en esta memoria. El progreso de la terapia (mejora de la enfermedad de las vías respiratorias, particularmente la enfermedad pulmonar, preferiblemente la obstrucción recurrente de las vías respiratorias (RAO) y/o la enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD) y/o la enfermedad inflamatoria de las vías respiratorias (IAD), lo más preferiblemente RAO tal como se describe en esta memoria) se puede controlar mediante el diagnóstico estándar de las vías respiratorias/pulmonar, por ejemplo, mediante el examen clínico, citología del fluido de las vías respiratorias, endoscopia, medición de la función pulmonar, o el análisis de gases en sangre.
La expresión "derivado farmacéuticamente aceptable del mismo" significa, pero no se limita a sales, derivados, metabolitos o profármacos de un fármaco farmacéuticamente aceptables. Derivados, tal como se utiliza en esta memoria, incluye, pero no se limita a cualesquiera formas de hidratos, solvatos, isómeros, enantiómeros, racematos, conglomerado racémico y similares del compuesto de elección. Sales farmacéuticamente aceptables adecuadas son bien conocidas en la técnica y pueden estar formadas con un ácido inorgánico u orgánico tal como ácido clorhídrico, ácido bromhídrico, ácido sulfúrico, ácido fosfórico, ácido nítrico, ácido acético, ácido glicólico, ácido láctico, ácido pirúvico, ácido malónico, ácido succínico, ácido glutárico, ácido fumárico, ácido málico, ácido mandélico, ácido tartárico, ácido cítrico, ácido ascórbico, ácido palmítico, ácido maleico, ácido hidroximaleico, ácido benzoico, ácido hidroxibenzoico, ácido fenilacético, ácido cinámico, ácido salicílico, ácido metanosulfónico, ácido bencenosulfónico y ácido toluenosulfónico.
La expresión “excipiente (o soporte o adyuvante) farmacéuticamente aceptable” para uso con la o las composiciones farmacéuticas de acuerdo con la presente invención incluyen, por ejemplo, intercambiadores de iones, alúmina, estearato de aluminio, lecitina, proteínas del suero, sustancias tampón, agua, sales o electrolitos y sustancias basadas en celulosa. Esta no es una lista completa de posibles soportes, es decir excipientes y/o adyuvantes farmacéuticamente aceptables, y un experto ordinario en la técnica conocería otras posibilidades de las que está repleta la técnica.
Una composición/ preparación/ medicamento farmacéutico de acuerdo con la invención puede contener disolventes tales como agua y/o etanol, acidificantes tales como ácido clorhídrico, ácido cítrico y/o ácido fosfórico y otros excipientes tales como conservantes tales como cloruro de benzalconio o etanol, o estabilizadores tales como EDTA, butilhidroxianisol o butilhidroxitolueno, modificadores de la viscosidad tales como hidroxipropil-metil-celulosa o solubilizantes tales como hidroxipropil-beta-ciclodextrina, o sustancias para hacer más agradable la aplicación de la composición a los animales tales como aromas o sabores.
Las concentraciones de cada uno de los disolventes pueden oscilar entre 1% m/V y 100% m/V, la concentración de los otros excipientes puede oscilar entre 0,01% m/V y 10% m/V.
Administración
Formas adecuadas para la "administración" de LAMA 1 o combinaciones de glucocorticoides tales como ciclesonida con LAMA 1 u otros LAMAs y/o agonista del adrenorreceptor beta-2 tal como agonista beta-2 adrenérgico de acción prolongada (LABAs) son, por ejemplo, la administración por inhalación, parenteral u oral, preferiblemente por inhalación.
En la administración específica a través del inhalador Respimat® el contenido del LAMA 1 farmacéuticamente eficaz debería estar en el intervalo de 0,2 a 7% m/V, preferiblemente de 0,3 a 6,0% m/V o de 0,4 a 5% m/V de la composición total , es decir, en cantidades que son suficientes para alcanzar el intervalo de dosis especificado más adelante en esta memoria.
Cuando se administra por inhalación, la ciclesonida puede ser dado como una disolución etanólica o una disolución que contiene una mezcla de agua y etanol. Preferiblemente, por lo tanto, formulaciones farmacéuticas se caracterizan porque comprenden ciclesonida de acuerdo con los aspectos arriba preferidos.
Se prefiere particularmente que la combinación se administre por inhalación / ex inhalador, preferiblemente se administra una vez o dos veces al día. La administración de la combinación se puede realizar mediante un inhalador que contiene los dos componentes de la combinación. Además, la administración de la combinación se puede realizar subsiguientemente mediante dos inhaladores, cada uno de los cuales contiene uno de los componentes de la combinación. Las administraciones subsiguientes se pueden realizar con o sin una pausa entre las administraciones de los componentes individuales. Formulaciones adecuadas pueden obtenerse, por ejemplo, mezclando LAMA 1 con excipientes conocidos, por ejemplo, agua, disolventes orgánicos farmacéuticamente aceptables tales como alcoholes mono- o polifuncionales (p. ej., etanol o glicerol), o refrigerantes/ propulsores tales como hidrofluoroalcanos (HFA), específicamente HFA 227 y HFA 134a. Para una formulación líquida se pueden añadir excipientes adicionales, por ejemplo ácido clorhídrico o ácido cítri
Se prefiere especialmente que LAMA 1 sea administrado por / a través de un inhalador de gotas acuosas/ etanólicas, por ejemplo el inhalador Respimat® u otro dispositivo de inhalación utilizando la tecnología de generación de aerosol Respimat®. Preferiblemente, LAMA 1 se administra una vez o dos veces al día. Para este fin, LAMA 1 tiene que estar disponible en una disolución líquida que sea adecuada para el inhalador.
Lo más preferiblemente, el disolvente en la formulación líquida (disolución de inhalación) comprende agua sola o una mezcla de < 95% V/V de etanol y > 5% V/V de agua, tal como 90% V/V de etanol y 10% V/V de agua.
Un aspecto adicional de la presente invención es la aplicación de la formulación líquida (disolución de inhalación) utilizando el inhalador Respimat® u otro dispositivo de inhalación utilizando la tecnología de generación de aerosol Respimat®. El inhalador Respimat® se describe, por ejemplo, en el documento WO 97/12687. Este inhalador se puede utilizar ventajosamente para producir los aerosoles inhalables de acuerdo con la invención. La dosis de sustancia activa suministrada por el inhalador ex Respimat® se puede calcular a partir de:
• la concentración de sustancia activa en la formulación líquida [pg/pL],
• el "volumen suministrado", definido como el volumen de líquido expulsado del inhalador Respimat® por accionamiento [pL]. Se ha encontrado que el volumen suministrado por el inhalador ex Respimat® es de aproximadamente 11 pL por accionamiento,
de acuerdo con la siguiente fórmula:
Dosis [pg] = Concentración [pg/pL] ■ Volumen suministrado [pL]
En el contexto de la presente invención, el término “dosis” significa la dosis suministrada “ex inhalador”.
En un aspecto adicional de la presente invención la composición se administra a través de un dispositivo inhalador (équido). El dispositivo inhalador (équido) comprende, por ejemplo, un inhalador de dosis medida presurizada (pMDI) o un inhalador de gotas acuosas/etanólicas. Una forma específica de un inhalador de gotas acuosas / etanólicas es, por ejemplo, el inhalador Respimat®, u otro dispositivo inhalador utilizando la tecnología Respimat®. Preferiblemente, el dispositivo inhalador (équido) comprende/consiste en un aerosol que genera un núcleo basado en la tecnología de generación de aerosol Respimat®, y otras piezas para adaptar el inhalador al uso en équidos. Un dispositivo inhalador (équido) se describe, por ejemplo, en el documento WO2010149280.
En un aspecto preferido, la composición es una formulación acuosa y se administra a través de un dispositivo inhalador (équido).
En un aspecto adicional de la presente invención, la formulación líquida comprende uno o más de los disolventes/propulsores: agua, etanol, hidrofluoroalcano(s) tales como HFA 227 y h Fa 134a, hidrofluoroolefina(s)
tales como HFO-1234ze y, opcionalmente, excipientes adicionales. HFA es una abreviatura para hidrofluoroalcano y HFO es una abreviatura para hidrofluoroolefina.
Además de formulaciones que contienen LAMA 1 sólo, son posibles composiciones adicionales que contienen, además, un glucocorticoide y/o LABA. Para conseguir una formulación de combinación de este tipo se puede utilizar un disolvente que consista en etanol además de agua para aumentar la solubilidad de las sustancias farmacológicas individuales. Un disolvente de este tipo puede contener hasta 95% V/V de etanol y tan poco como 5% V/V de agua. Disolventes que contienen etanol tienen la ventaja adicional de requerir una concentración menor o ningún conservante, dado que combinaciones de etanol y agua pueden inhibir el crecimiento o exterminar microorganismos. La invención se refiere a antagonistas muscarínicos de acción prolongada (LAMAs) de la fórmula general I, más preferiblemente de la fórmula II (= LAMA 1) para uso en un método de tratamiento de enfermedades de las vías respiratorias tales como enfermedad pulmonar, preferiblemente obstrucción recurrente de las vías respiratorias (RAO), enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD) y enfermedad inflamatoria de las vías respiratorias (IAD) en équidos, preferiblemente caballos.
La invención se refiere, además, a una combinación de antagonistas muscarínicos de acción prolongada (LAMAs) de la fórmula general I, más preferiblemente de la fórmula II (= LAMA 1), con un glucocorticoide tal como ciclesonida o budesonida , preferiblemente ciclesonida, para uso en un método de tratamiento de una enfermedad de las vías respiratorias, tal como enfermedad pulmonar, preferiblemente obstrucción recurrente de las vías respiratorias (RAO), enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD) y enfermedad inflamatoria de las vías respiratorias (IAD) en équidos, preferiblemente caballos.
La invención se refiere, además, a una combinación de antagonistas muscarínicos de acción prolongada (LAMAs) de la fórmula general I, más preferiblemente de la fórmula II (= LAMA 1), con un glucocorticoide tal como ciclesonida o budesonida, y opcionalmente con agonistas de adrenorreceptores beta-2 (agonistas beta-2 adrenérgicos de acción prolongada (lAbAs)) para uso en un método de tratamiento de enfermedades de las vías respiratorias tales como enfermedad pulmonar, preferiblemente obstrucción recurrente de las vías respiratorias (RAO), enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD) y enfermedad inflamatoria de las vías respiratorias (IAD) en équidos, preferiblemente caballos.
La invención se refiere además a una combinación de antagonistas muscarínicos de acción prolongada (LAMA) de la fórmula general I, más preferiblemente de la fórmula II (= LAMA 1), con un glucocorticoide tal como ciclesonida o budesonida, y opcionalmente con agonistas del adrenorreceptor beta-2 (incluidos los agonistas del adrenorreceptor beta-2 de acción prolongada (LABA)) para uso en un método de tratamiento de una enfermedad de las vías respiratorias, como la enfermedad pulmonar, preferiblemente la obstrucción recurrente de las vías respiratorias (RAO), la enfermedad pulmonar obstructiva asociada al pasto de verano (SPAOPD) y la enfermedad inflamatoria de las vías respiratorias (DAI) en équidos, preferiblemente caballos. Preferiblemente, dicho agonista del adrenorreceptor beta-2 es salbutamol (albuterol), pirbuterol, clenbuterol, fenoterol, salmeterol, formoterol, indacaterol, vilanterol, abediterol y olodaterol (hidrocloruro).
En un aspecto adicional de la presente invención, el LAMA de la presente invención es glicopirrolato, bromuro de ipratropio, bromuro de aclidinio, bromuro de umeclidinio o tiotropio.
Adémas, se describe aquí un antagonista muscarínico de acción prolongada (LAMA) o a una sal farmacéuticamente aceptable del catión del mismo para uso como un medicamento en un équido tal como un caballo.
La invención se refiere a un antagonista muscarínico de acción prolongada (LAMA) o a otra sal farmacéuticamente aceptable del catión del mismo para uso en un método para tratar una enfermedad de las vías respiratorias en un équido, preferiblemente un caballo,. en donde el LAMA es un compuesto de la fórmula general:
en donde
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo C1-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4, alquiloxi C1-C4, hidroxi, CF3 , CN, NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-COCF3 o halógeno,
opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos, siempre que si A designa
R1 y R2 designan metilo y
R3, R4, R5 y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno.
Preferiblemente, el LAMA es un compuesto de la fórmula (LAMA 1):
En un aspecto específico de la presente invención, la concentración de LAMA 1 oscila entre 0,2 y 7% m/V, preferiblemente entre 0,3 y 6,0% m/V o entre 0,4 y 5% m/V de la composición total.
La invención se refiere, a un antagonista muscarínico de acción prolongada (LAMA) u otra sal farmacéuticamente aceptable del catión del mismo o a una composición farmacéutica que comprende un LAMA u otra sal farmacéuticamente aceptable del catión del mismo, en combinación con un glucocorticoide tal como ciclesonida o budesonida o fluticasona (preferiblemente ciclesonida) o una composición farmacéutica que comprende ciclesonida o budesonida o fluticasona o una sal farmacéuticamente aceptable del mismo para uso como un medicamento en un équido tal como un caballo.
La invención se refiere, además, a un antagonista muscarínico de acción prolongada (LAMA) u otra sal farmacéuticamente aceptable del catión del mismo o a una composición farmacéutica que comprende un LAMA u otra sal farmacéuticamente aceptable del catión del mismo, en combinación con un glucocorticoide tal como ciclesonida o una composición farmacéutica que comprende ciclesonida o una sal farmacéuticamente aceptable del mismo para uso en un método para tratar una enfermedad de las vías respiratorias en un équido tal como un caballo.
En un aspecto específico de la presente invención, la composición farmacéutica que comprende el LAMA es una combinación de dosis fija/ una composición farmacéutica que comprende un LAMA o sales farmacéuticamente aceptables del mismo, y un glucocorticoide tal como ciclesonida o budesonida o sales farmacéuticamente aceptables del mismo. Una combinación preferida es un LAMA de fórmula general I, lo más preferido LAMA 1 en combinación con ciclesonida o budesonida, preferiblemente ciclesonida. Opcionalmente, dicha composición farmacéutica que comprende el LAMA y el glucocorticoide contiene, adicionalmente, agonistas de adrenorreceptores beta-2 tales como un LABA.
En otro aspecto de la presente invención, el LAMA y el glucocorticoide se combinan adicionalmente con agonistas adrenorreceptores beta-2 tales como un LABA o sales farmacéuticamente aceptables del mismo. Estos compuestos o parte de ellos pueden formularse como composiciones farmacéuticas separadas o como combinaciones de dosis fijas.
En la presente invención, el LAMA es un compuesto de la fórmula general:
en donde
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo C1-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4, alquiloxi C1-C4, hidroxi, CF3 , CN, NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-COCF3 o halógeno,
opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos, siempre que, si A designa
R1 y R2 designan metilo y
R3, R4, R5 y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno.
Preferiblemente, el LAMA es un compuesto de la fórmula (LAMA 1):
En un aspecto específico de la presente invención, la concentración de LAMA 1 oscila entre 0,2 y 7% m/V, preferiblemente entre 0,3 y 6,0% m/V o entre 0,4 y 5% m/V de la composición total.
Un aspecto específico de la presente invención es la combinación de LAMA 1 o una sal farmacéuticamente aceptable del mismo con ciclesonida o una sal farmacéuticamente aceptable del mismo. Otro aspecto específico de la presente invención es la combinación de LAMA 1 o una sal farmacéuticamente aceptable del mismo con budesonida o una sal farmacéuticamente aceptable del mismo.
Un aspecto adicional de la presente invención es la combinación de LAMA 1 o una sal farmacéuticamente aceptable del mismo con clenbuterol o una sal farmacéuticamente aceptable del mismo. Otro aspecto específico de la presente invención es la combinación de LAMA 1 o una sal farmacéuticamente aceptable del mismo con ciclesonida o una sal farmacéuticamente aceptable del mismo y albuterol/sulfato de albuterol u otra sal farmacéuticamente aceptable del mismo.
Un aspecto específico adicional de la presente invención es la combinación de LAMA 1 o una sal farmacéuticamente aceptable del mismo con ciclesonida o una sal farmacéuticamente aceptable del mismo e hidrocloruro de olodaterol u otra sal farmacéuticamente aceptable del mismo.
En otro aspecto específico de la presente invención, el LAMA es bromuro de tiotropio o una sal farmacéuticamente aceptable del mismo. Un aspecto específico de la presente invención es la combinación de bromuro de tiotropio con ciclesonida y, opcionalmente, hidrocloruro de olodaterol.
En un aspecto específico de la presente invención, la enfermedad de las vías respiratorias es una enfermedad pulmonar. Preferiblemente, la enfermedad de las vías respiratorias se selecciona del grupo que consiste en: obstrucción recurrente de las vías respiratorias (RAO), enfermedad pulmonar estructura asociada con el pasto de verano (SPAOPD) y enfermedad inflamatoria de las vías respiratoria (IAD),
En un aspecto adicional específico de la presente invención, dicho LAMA o una composición farmacéutica que comprende el LAMA es (está en) una formulación líquida, preferiblemente una formulación parcialmente etanólica, lo más preferiblemente dicha formulación líquida es para inhalación.
En otro aspecto específico de la presente invención, dicho LAMA o la composición farmacéutica que comprende el LAMA se administra a través de un dispositivo inhalador (équido), preferiblemente dicho dispositivo inhalador comprende:
a. un inhalador de dosis medida presurizado o un inhalador de gotas acuosas/etanólicas, tales como el inhalador Respimat1®, u otro dispositivo de inhalación que utiliza la tecnología de generación de aerosol de Respimat®y b. un adaptador para uso en équidos.
En un aspecto preferido de la presente invención, LAMA 1 o una sal farmacéuticamente aceptable del catión del mismo se administra a una dosis de 100 |jg a 3000 |jg ex inhalador, 200 |jg a 2000 |jg ex inhalador, 200 |jg a 800 |jg es inhalador, preferiblemente a una dosis de 200 jig a 800 jig ex inhalador.
En otro aspecto preferido de la presente invención, ciclesonida o una composición farmacéutica que comprende ciclesonida o una sal farmacéuticamente aceptable de la misma, se administra a una dosis de 100 jig a 5000 jig ex inhalador, 450 jg a 3712,5 jg ex inhalador, 900 jg a 3712,5 jg ex inhalador, preferiblemente a una dosis de 900 jg a 3712,5 jg ex inhalador.
En un aspecto preferido adicional de la presente invención, el LAMA o una composición farmacéutica que comprende el LAMA se administra una vez o dos veces al día (una vez o dos veces diarias), preferiblemente una vez al día.
Además, se describe aquí una composición farmacéutica que comprende un antagonista muscarínico de acción prolongada (LAMA) o sales farmacéuticamente aceptables del mismo y un LABA o sales farmacéuticamente aceptables del mismo y, opcionalmente un glucocorticoide tal como ciclesonida o budesonida (preferiblemente ciclesonida) o sales farmacéuticamente aceptables del mismo y, opcionalmente, un excipiente farmacéuticamente aceptable.
Además, se describe aquí una composición farmacéutica que comprende un antagonista muscarínico de acción prolongada (LAMA) o sales farmacéuticamente aceptables del mismo y un glucocorticoide tal como ciclesonida o budesonida (preferiblemente ciclesonida) o sales farmacéuticamente aceptables del mismo y, opcionalmente, un LABA o sales farmacéuticamente aceptables del mismo y, opcionalmente, un excipiente farmacéuticamente aceptable.
Preferiblemente, dicha composición es una formulación líquida, lo más preferiblemente una disolución para inhalación.
En un aspecto aquí descrito, el LAMA es un compuesto de la fórmula general:
en donde
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo C1-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4, alquiloxi C1-C4, hidroxi, CF3 , CN, NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-COCF3 o halógeno,
opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos, siempre que si A designa ,
R1 y R2 designan metilo y
R3, R4, R5 y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno.
Lo más preferiblemente, el LAMA es un compuesto de la fórmula (LAMA 1):
En un aspecto específico de la presente invención, la concentración de LAMA 1 oscila entre 0,2 y 7% m/V, preferiblemente entre 0,3 y 6,0% m/V o entre 0,4 y 5% m/V de la composición total.
Ejemplos
Los siguientes ejemplos sirven para ilustrar adicionalmente la presente invención; pero los mismos no deben considerarse como una limitación del alcance de la invención descrita en esta memoria.
Los siguientes ejemplos 1 a 6 dan ejemplos de composiciones que se pueden administrar utilizando un inhalador basado en la tecnología de generación de pulverización Respimat®.
Ejemplo 1
LAMA 1 se puede formular en forma de una disolución acuosa o en forma de una disolución etanólica.
Esta primera tabla muestra ejemplos de una disolución acuosa:
Tabla 1:
en donde la concentración de iones hidrógeno [H+] se puede medir, por ejemplo, mediante valoración potenciométrica.
Ejemplo 2:
LAMA 1 se puede formular en forma de una disolución acuosa o en forma de una disolución etanólica. La segunda tabla muestra un ejemplo de formulación para una disolución etanólica con 50% V/V de etanol.
Tabla 2:
Ejemplo 3:
La siguiente tabla muestra un ejemplo de formulaciones de LAMA 1 para una disolución etanólica con 90% V/V de
etanol.
Tabla 3:
Ejemplo 4:
LAMA 1 se puede formular como una formulación de combinación etanólica con budesonida tal como se muestra en la siguiente tabla 4:
Tabla 4:
Ejemplo 5:
LAMA 1 se puede formular como una formulación de combinación etanólica con ciclesonida tal como se muestra en la siguiente tabla 5:
Tabla 5:
Ejemplo 6:
LAMA 1 se puede formular como una formulación de combinación etanólica con ciclesonida tal como se muestra en la siguiente tabla 6:
Tabla 6:
Ejemplo 7: Monoterapia con LAMA 1
LAMA 1 se investiga en un estudio con 4 fases.
LAMA 1 se utiliza en las formulaciones según se describe en los Ejemplos 1 y 2.
Fase I y IV:
LAMA 1 se investiga en dos caballos con RAO a diferentes fases o períodos como parte de un estudio de provocación con heno enmohecido. Los caballos son provocados cada día mediante exposición a heno enmohecido. LAMA 1 se administra a través del dispositivo inhalador équido a diferentes dosis o formulaciones. Los parámetros de la función pulmonar (cambio en la presión transpulmonar (APL), resistencia pulmonar (RL) y elastancia pulmonar (EL)) se miden durante 24 h. Una administración única de 800 |jg de LAMA 1 (8 accionamientos en formulación acuosa) se realiza por cada inhalación a dos caballos con RAO (números ID: 312 y 91) en la fase I. Dos caballos con RAO se tratan con LAMA 1 en la fase IV (números ID: 40 y 91) que se puede dividir en tres períodos. 2000 jg de LAMA 1 (20 accionamientos en formulación acuosa) se administran por inhalación en el periodo 1.2000 jg de LAMA 1 (4 accionamientos en formulación etanólica) se administran por inhalación en el periodo 2. 2000 jg de LAMA 1 (20 accionamientos en formulación etanólica) se administran por inhalación en el periodo 3.
Se observa una disminución en las variables de la función pulmonar que comienzan 5 minutos después de la administración de LAMA 1. Los valores continúan cayendo hasta 2-8 h, dependiendo del parámetro de la función pulmonar y de la dosis o formulación de LAMA 1. Las variables de la función pulmonar están por debajo o alcanzan los valores de pre-tratamiento a las 24 h después de la administración única de LAMA 1 (Fase I: Figuras 1-3; Fase IV, periodo 1: Figuras 4-6; Fase IV, periodo 2: Figuras 7-9; Fase IV, periodo 3: Figuras 10-12).
Fase II:
LAMA 1 se investiga en un estudio de provocación con heno enmohecido ciego de entrecruzamiento. 8 caballos con RAO son examinados en el estudio, que se divide en una fase de aclimatación y una fase de tratamiento. Placebo para LAMA 1 se administra una vez al día por inhalación a través del dispositivo inhalador équido a todos los caballos durante 1 semana en el periodo de aclimatación. LAMA 1 y clenbuterol se administran a los caballos en un diseño cruzado en la fase de tratamiento. Los caballos son provocados mediante exposición a heno enmohecido a lo largo de las fases de aclimatación y tratamiento.
LAMA 1 se administra con las dosis de 200 jg (2 accionamientos) / 400 jg (4 accionamientos) / 800 jg (8 accionamientos) /caballo (ex-Respimat®) una vez al día durante 7 días por inhalación a través del dispositivo inhalador équido. En el estudio se utiliza la boquilla A y un Respimat® comercialmente disponible. Clenbuterol se administra con una dosis de 0,8 jg/kg per os, dos veces al día durante 7 días.
Las variables de la función pulmonar (cambio en la presión transpulmonar (APL), resistencia pulmonar (RL) y elastancia pulmonar (EL)), la puntuación del esfuerzo respiratorio, la puntuación Borborygmi, el análisis de gas en sangre se examinan durante el estudio.
El tratamiento con placebo no induce cambios significativos en la puntuación del esfuerzo respiratorio, las variables de la función pulmonar (cambio en la presión transpulmonar (APL), resistencia pulmonar (RL) y elastancia pulmonar
(EL)), pH, paCO2 y paO2. Caballos tratados con clenbuterol tienen puntuaciones de esfuerzo respiratorio significativamente menores el día 6 del estudio que los caballos tratados con 2 ó 4 accionamientos de LAMA 1 (Figura 13). Ninguno de los tratamientos (LAMA 1 o clenbuterol) altera significativamente los valores de APL y EL a lo largo del tiempo (Días 4 y 8 en comparación con el Día 1) (Figuras 14 y 15). Los valores RL se reducen significativamente a lo largo del tiempo en los grupos de clenbuterol y de 800 |jg de LAMA 1 (Figura 16). Las variables de la función pulmonar se miden antes y 30 min después de la administración de LAMA 1 el día 4. Cuando se comparan con valores de pre-tratamiento, se observa una disminución en APL, RL y EL en todos los grupos de LAMA 1 a los 30 min después de la administración (Figuras 17-19). El cambio en APL y EL es estadísticamente significativo después de la administración de 200 y 400 jg de LAMA 1. El pH aumenta y la paCO2 se reduce significativamente en la sangre arterial en el grupo de 800 jg de LAMA 1 el Día 7 en comparación con el Día 0 (Figuras 20 y 21).
Fase III:
Se realiza una administración única de 800 jg de LAMA 1 (8 accionamientos en formulación acuosa) por inhalación a dos caballos sanos en la fase III. Subsiguientemente, se realizan mediciones de ECG durante 48 h. Se observan arritmias fisiológicas en ambos caballos antes y después de la administración de LAMA 1. Solamente una observación se clasifica como un bloqueo del corazón de primer grado con repolarización intraventricular aberrante o un artefacto debido al movimiento de los electrodos.
Ejemplo 8
La combinación de LAMA 1 y ciclesonida se investiga en un modelo de provocación con heno enmohecido. 8 caballos con RAO son tratados a través de inhalación utilizando el dispositivo inhalador équido. El tratamiento con monoterapia de LAMA 1 (máximo de 2000 jg por administración), con monoterapia con ciclesonida (máximo 3212,5 jg por administración) y con la combinación de LAMA 1 y ciclesonida (la dosis máxima de LAMA 1 es 2000 jg por administración y la dosis máxima de ciclesonida es 3712,5 jg por administración) se examinan en el estudio. Las variables de la función pulmonar (cambio en la presión transpulmonar (APL), resistencia pulmonar (RL) y elastancia pulmonar (EL)) y la puntuación clínica ponderada se miden en el estudio.
En todos los grupos de tratamiento se observa una mejora en las variables de la función pulmonar y la puntuación clínica ponderada con un grado variable. De manera similar, el inicio de la acción muestra diferencia entre los grupos de tratamiento que comienzan ya unos pocos minutos después de la administración del fármaco.
Referencias
1. Kutasi O., Balogh N., Lajos Z., Nagy K., Szenci O.: Diagnostic approaches for the assessment of equine chronic pulmonary disorders. J. Eq. Vet. Sci. (2011) 31: 400-410
2. Coutil L.L:, Hoffman A.M., Hodgson J., Buechner-Maxwell V., Viel L., Wood J.L.N. and Lavoie J.-P.:
Inflammatory airway disease of horses. J. Vet. Intern. Med. (2007) 21: 356-361
3. Dauvillier J., Felippe M.J.B., Lunn D.P., Lavoie-Lamoureux A., Leclere M., Beauchamp G., Lavoie J.-P.:
Effect of long-term fluticasone treatment on immune function in horses with heaves. J. Vet. Intern. Med. (2011) 25: 549-557
4. Tashkin D.P. and Fabbri L.M.: Long-acting beta-agonists in the management of chronic obstructive pulmonary disease: current and future agents. Resp. Research (2010) 11:149
5. Barnes P.J.: The role of anticholinergics in chronic obstructive pulmonary disease. Am J Med (2004) 117 (Suppl 12A):24S-32S.6
6. Robinson N.E., Derksen F.J., Berney C. and Goossens L.: The airway response of horses with recurrent airway obstruction (heaves) to aerosol administration of ipratropium bromide. Equine Veterinary Journal (1993), vol. 25, no. 4, pages 299 - 303.pdf
Claims (12)
1. Un antagonista muscarínico de acción prolongada (LAMA) o una sal farmacéuticamente aceptable del catión del mismo para uso en un método de tratamiento de una enfermedad de las vías respiratorias en un équido, preferiblemente un caballo, en donde el LAMA es un compuesto de la fórmula general:
en donde
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo C1-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4, alquiloxi C1-C4, hidroxi, CF3 , CN, NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-COCF3 o halógeno,
opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos,
siempre que si A designa
R1 y R2 designan metilo y
R3, R4, R5 y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno,
preferiblemente, el LAMA es un compuesto de la fórmula (LAMA 1):
2. Un antagonista muscarínico de acción prolongada (LAMA) o una sal farmacéuticamente aceptable del catión del mismo o una composición farmacéutica que comprende un LAMA o una sal farmacéuticamente aceptable del catión del mismo, en combinación con un glucocorticoide tal como ciclesonida o budesonida o una composición farmacéutica que comprende ciclesonida o una sal farmacéuticamente aceptable del mismo, para uso como un medicamento en un équido tal como un caballo, en donde el LAMA es un compuesto de fórmula general:
en donde
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo C1-C4 , que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4 , alquiloxi C1-C4, hidroxi, CF3 , CN, NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4, alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4, alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-Co CF3 o halógeno, opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos,
siempre que si A designa
R1 y R2 designan metilo y
R3, R4, R5y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno,
preferiblemente, el LAMA es un compuesto de la fórmula (LAMA 1):
3. Un antagonista muscarínico de acción prolongada (LAMA) o una sal del catión del mismo farmacéuticamente aceptable o una composición farmacéutica que comprende un LAMA o una sal del catión del mismo farmacéuticamente aceptable, en combinación con un glucocorticoide tal como ciclesonida o una composición farmacéutica que comprende ciclesonida o una sal del mismo farmacéuticamente aceptable, para uso en un método para tratar una enfermedad de las vías respiratorias en un équido, preferiblemente un caballo,
en donde:
A designa un grupo de doble enlace seleccionado entre
X- designa un anión con una sola carga negativa,
R1 y R2 designan alquilo Ci-C4, que puede estar opcionalmente sustituido con hidroxi o halógeno;
R3, R4, R5 y R6, que pueden ser idénticos o diferentes, designan hidrógeno, alquilo C1-C4 , alquiloxi C1-C4, hidroxi, CF3 , CN, NO2 o halógeno;
R7 designa hidrógeno, alquilo C1-C4, alquiloxi C1-C4 , alquilen C1-C4-halógeno, halógeno-alquiloxi C1-C4 , alquilen C1-C4-OH, CF3, -alquilen C1-C4-alquiloxi C1-C4, -O-COalquilo C1-C4, -O-COalquil C1-C4-halógeno, -O-COCF3 o halógeno,
opcionalmente en forma de los isómeros ópticos individuales, mezclas de los enantiómeros individuales o racematos de los mismos,
siempre que, si A designa
R1 y R2 designan metilo y
R3, R4, R5 y R6 designan hidrógeno,
entonces R7 no puede ser también hidrógeno,
preferiblemente, el LAMA es un compuesto de la fórmula (LAMA 1):
4. El LAMA para uso de acuerdo con la reivindicación 2 ó 3, en donde la composición farmacéutica es una composición farmacéutica que comprende un LAMA o una sal farmacéuticamente aceptable del mismo, y un glucocorticoide tal como ciclesonida o budesonida, o sales farmacéuticamente aceptables de los mismos y, opcionalmente, un agonista adrenorreceptor beta-2 tal como un agonista beta-2 adrenérgico de acción prolongada (LABA) o una sal farmacéuticamente aceptable del mismo y, opcionalmente, un excipiente farmacéuticamente aceptable.
5. El LAMA para uso de acuerdo con cualquiera de las reivindicaciones 2 a 4, en donde el LAMA y el glucocorticoide se combinan adicionalmente con un agonista adrenorreceptor beta-2 tal como un agonista beta-2 adrenérgico de acción prolongada (LABA) o sales farmacéuticamente aceptables del mismo.
6. El LAMA para uso de acuerdo con las reivindicaciones 1 y 3 a 5, en donde la enfermedad de las vías respiratorias, preferiblemente la enfermedad de las vías respiratorias se selecciona del grupo que consiste en: obstrucción recurrente de las vías respiratorias (RAO), enfermedad pulmonar obstructiva asociada al pasto del verano (SPAOPD) y la enfermedad inflamatoria de las vías respiratorias (IAD),
7. El LAMA para uso de acuerdo con las reivindicaciones 1 a 6, en donde dicho LAMA o la composición farmacéutica que comprende el LAMA es (está en) una formulación líquida, preferiblemente una formulación parcialmente etanólica, lo más preferiblemente dicha formulación líquida es para inhalación.
8. El LAMA para uso de acuerdo con las reivindicaciones 1 a 7, en donde dicho LAMA o la composición farmacéutica que comprende el LAMA se administra a través de un dispositivo inhalador (para équidos), preferiblemente dicho dispositivo inhalador comprende:
a. un inhalador de dosis medida presurizado o un inhalador de gotas acuosas/etanólicas, tal como el inhalador Respimat1®, u otro dispositivo de inhalación que utiliza la tecnología de generación de aerosol de Respimat®y b. un adaptador para uso en équidos.
9. El LAMA para uso de acuerdo con las reivindicaciones 1 a 8, en donde LAMA 1 o una sal farmacéuticamente aceptable del catión del mismo se administra a una dosis de 100 |jg a 3000 |jg ex inhalador, 200 |jg a 2000 |jg ex inhalador, 200 jig a 800 jig es inhalador, preferiblemente a una dosis de 200 jig a 800 jig ex inhalador.
10. El LAMA para uso de acuerdo con las reivindicaciones 2 a 8, en donde ciclesonida o una composición farmacéutica que comprende ciclesonida o una sal farmacéuticamente aceptable de la misma, se administra a una dosis de 100 jig a 5000 jig ex inhalador, 450 jig a 3712,5 jig ex inhalador, 900 jig a 3712,5 jig ex inhalador, preferiblemente a una dosis de 900 jig a 3712,5 jig ex inhalador.
11. El LAMA para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 10, en donde el LAMA o la composición farmacéutica que comprende el LAMA se administra una vez o dos veces al día, preferiblemente una vez al día.
12. El LAMA para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 11, en donde la concentración de LAMA 1 varía de 0,2 a 7% m/V, más preferiblemente de 0,3 a 6,0% m/V o de 0,4 a 5% m/V de la composición total.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14172925 | 2014-06-18 | ||
| PCT/EP2015/063265 WO2015193213A1 (en) | 2014-06-18 | 2015-06-15 | Muscarinic antagonists and combinations thereof for the treatment of airway disease in horses |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2759247T3 true ES2759247T3 (es) | 2020-05-08 |
Family
ID=50972546
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15728025T Active ES2759247T3 (es) | 2014-06-18 | 2015-06-15 | Antagonistas muscarínicos y combinaciones de estos para el tratamiento de enfermedades de las vías respiratorias en caballos |
Country Status (17)
| Country | Link |
|---|---|
| US (3) | US9474747B2 (es) |
| EP (2) | EP3157522B1 (es) |
| KR (1) | KR102618119B1 (es) |
| AU (2) | AU2015276310B2 (es) |
| CA (1) | CA2952701C (es) |
| CY (1) | CY1122335T1 (es) |
| DK (1) | DK3157522T3 (es) |
| ES (1) | ES2759247T3 (es) |
| HR (1) | HRP20192010T1 (es) |
| HU (1) | HUE051527T2 (es) |
| LT (1) | LT3157522T (es) |
| MX (2) | MX370430B (es) |
| PL (1) | PL3157522T3 (es) |
| PT (1) | PT3157522T (es) |
| RS (1) | RS59613B1 (es) |
| SI (1) | SI3157522T1 (es) |
| WO (1) | WO2015193213A1 (es) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2888428C (en) | 2012-12-21 | 2021-07-13 | Boehringer Ingelheim Vetmedica Gmbh | Ciclesonide for the treatment of airway disease in horses |
| DK2934544T3 (en) | 2012-12-21 | 2019-03-04 | Boehringer Ingelheim Vetmedica Gmbh | PHARMACEUTICAL FORMULA INCLUDING CICLESONID |
| ES2759247T3 (es) | 2014-06-18 | 2020-05-08 | Boehringer Ingelheim Vetmedica Gmbh | Antagonistas muscarínicos y combinaciones de estos para el tratamiento de enfermedades de las vías respiratorias en caballos |
| CN111840256A (zh) * | 2019-04-29 | 2020-10-30 | 上海谷森医药有限公司 | 一种雾化吸入剂及其制备方法 |
| CN112752572B (zh) * | 2019-05-23 | 2022-02-22 | 广州谷森制药有限公司 | 含有三苯乙酸维兰特罗和芜地溴铵的可吸入溶液组合物 |
| WO2021262648A1 (en) * | 2020-06-23 | 2021-12-30 | Anovent Pharmaceutical (U.S.), Llc | Preparation of a pharmaceutical composition of olodaterol and budesonide |
| CA3186956A1 (en) | 2020-07-31 | 2022-02-03 | Chemo Research , S.L. | Combination therapy for inhalation administration |
| EP4221707A1 (en) | 2020-09-29 | 2023-08-09 | Aerorx Therapeutics LLC | Liquid formulations of indacaterol |
Family Cites Families (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5954049A (en) | 1991-10-15 | 1999-09-21 | Trudell Medical Limited | Equine mask with MDI adapter |
| DE19536902A1 (de) | 1995-10-04 | 1997-04-10 | Boehringer Ingelheim Int | Vorrichtung zur Hochdruckerzeugung in einem Fluid in Miniaturausführung |
| US5823179A (en) * | 1996-02-13 | 1998-10-20 | 1263152 Ontario Inc. | Nebulizer apparatus and method |
| US6264923B1 (en) | 1998-05-13 | 2001-07-24 | 3M Innovative Properties Company | Medicinal aerosol formulation of ciclesonide and related compounds |
| US6706726B2 (en) | 2000-10-14 | 2004-03-16 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Anticholinergics which may be used as medicaments as well as processes for preparing them |
| DE10050994A1 (de) | 2000-10-14 | 2002-04-18 | Boehringer Ingelheim Pharma | Neue als Arneimittel einsetzbare Anticholinergika sowie Verfahren zu deren Herstellung |
| DE10062712A1 (de) | 2000-12-15 | 2002-06-20 | Boehringer Ingelheim Pharma | Neue Arzneimittelkompositionen auf der Basis von Anticholinergika und Corticosteroiden |
| US6904908B2 (en) * | 2002-05-21 | 2005-06-14 | Trudell Medical International | Visual indicator for an aerosol medication delivery apparatus and system |
| DE10237739A1 (de) * | 2002-08-17 | 2004-02-26 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Inhalative Arzneimittel enthaltend ein neues Anticholinergikum in Kombination mit Corticosteroiden und Betamimetika |
| US7244742B2 (en) | 2002-08-17 | 2007-07-17 | Boehringer Ingelheim Pharma Gmbh & Co Kg | Pharmaceutical compositions for inhalation containing an anticholinergic, corticosteroid and betamimetic |
| US20040053902A1 (en) * | 2002-09-13 | 2004-03-18 | Smith C. Steven | Novel composition and method for treatment of upper respiratory conditions |
| US20060293293A1 (en) | 2003-05-22 | 2006-12-28 | Altana Pharma Ag | Salmeterol and ciclesonide combination |
| US20050020692A1 (en) * | 2003-07-24 | 2005-01-27 | Ciofalo Vincent B. | Treatment of heaves |
| ES2452691T5 (es) | 2003-09-16 | 2022-09-14 | Covis Pharma Gmbh | Uso de ciclesonida para el tratamiento de enfermedades respiratorias |
| PE20050941A1 (es) | 2003-12-16 | 2005-11-08 | Nycomed Gmbh | Suspensiones acuosas de ciclesonida para nebulizacion |
| JP2007533706A (ja) | 2004-04-20 | 2007-11-22 | ニコメッド ゲゼルシャフト ミット ベシュレンクテル ハフツング | 喫煙患者における呼吸器疾患の治療のためのシクレソニドの使用 |
| JP2008504341A (ja) | 2004-06-29 | 2008-02-14 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | ステロイドと抗コリン作用剤とを含む吸入用薬剤 |
| DE102004056579A1 (de) * | 2004-11-23 | 2006-05-24 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Inhalative Arzneimittel enthaltend ein neues Anticholinergikum, Salmeterol und ein Steroid |
| US20070028923A1 (en) | 2005-08-08 | 2007-02-08 | Patrick Souris | Tip-laryngeal airway |
| UY30543A1 (es) | 2006-08-18 | 2008-03-31 | Boehringer Ingelheim Int | Formulacion de aerosol para la inhalacion de beta- agonistas |
| UY30542A1 (es) | 2006-08-18 | 2008-03-31 | Boehringer Ingelheim Int | Formulacion de aerosol para la inhalacion de agonistas beta |
| PL2346625T5 (pl) | 2008-10-30 | 2024-04-29 | Primetals Technologies Germany Gmbh | Sposób nastawiania grubości wylotowej materiału walcowanego przebiegającego przez wieloklatkowy zespół walcowniczy, urządzenie sterujące i/lub regulujące oraz instalacja walcownicza |
| US8815258B2 (en) * | 2009-05-29 | 2014-08-26 | Pearl Therapeutics, Inc. | Compositions, methods and systems for respiratory delivery of two or more active agents |
| WO2010149280A1 (en) * | 2009-06-25 | 2010-12-29 | Boehringer Ingelheim Vetmedica Gmbh | Inhaler |
| US20150202297A1 (en) * | 2012-07-05 | 2015-07-23 | Arven Ilac Sanayi Ve Ticaret Anonim Sirketi | Dry powder inhalers comprising a carrier other than lactose and a ternary component |
| US20150202148A1 (en) * | 2012-07-05 | 2015-07-23 | Arven llac Sanayi Ve Ticaret Anonim Sirketi | Dry powder inhalers comprising a carrier other than lactose |
| WO2014016548A2 (en) * | 2012-07-27 | 2014-01-30 | Cipla Limited | Pharmaceutical composition |
| US9539408B2 (en) * | 2012-10-31 | 2017-01-10 | Trudell Medical International | Nebulizer apparatus |
| DK2934544T3 (en) * | 2012-12-21 | 2019-03-04 | Boehringer Ingelheim Vetmedica Gmbh | PHARMACEUTICAL FORMULA INCLUDING CICLESONID |
| CA2888428C (en) | 2012-12-21 | 2021-07-13 | Boehringer Ingelheim Vetmedica Gmbh | Ciclesonide for the treatment of airway disease in horses |
| RS60034B1 (sr) * | 2013-08-20 | 2020-04-30 | Boehringer Ingelheim Vetmedica Gmbh | Inhalator |
| PT3035886T (pt) * | 2013-08-20 | 2021-01-04 | Boehringer Ingelheim Vetmedica Gmbh | Nalador |
| ES2759247T3 (es) | 2014-06-18 | 2020-05-08 | Boehringer Ingelheim Vetmedica Gmbh | Antagonistas muscarínicos y combinaciones de estos para el tratamiento de enfermedades de las vías respiratorias en caballos |
-
2015
- 2015-06-15 ES ES15728025T patent/ES2759247T3/es active Active
- 2015-06-15 CA CA2952701A patent/CA2952701C/en active Active
- 2015-06-15 AU AU2015276310A patent/AU2015276310B2/en active Active
- 2015-06-15 WO PCT/EP2015/063265 patent/WO2015193213A1/en active Application Filing
- 2015-06-15 KR KR1020177001472A patent/KR102618119B1/ko active IP Right Grant
- 2015-06-15 EP EP15728025.6A patent/EP3157522B1/en active Active
- 2015-06-15 SI SI201531016T patent/SI3157522T1/sl unknown
- 2015-06-15 PT PT157280256T patent/PT3157522T/pt unknown
- 2015-06-15 EP EP19192103.0A patent/EP3603640A1/en active Pending
- 2015-06-15 MX MX2016016720A patent/MX370430B/es active IP Right Grant
- 2015-06-15 HU HUE15728025A patent/HUE051527T2/hu unknown
- 2015-06-15 PL PL15728025T patent/PL3157522T3/pl unknown
- 2015-06-15 RS RS20191483A patent/RS59613B1/sr unknown
- 2015-06-15 DK DK15728025T patent/DK3157522T3/da active
- 2015-06-15 LT LT15728025T patent/LT3157522T/lt unknown
- 2015-06-16 US US14/740,582 patent/US9474747B2/en active Active
-
2016
- 2016-09-23 US US15/274,259 patent/US10342789B2/en active Active
- 2016-12-15 MX MX2019014935A patent/MX2019014935A/es unknown
-
2019
- 2019-05-08 US US16/406,918 patent/US10682345B2/en active Active
- 2019-11-06 HR HRP20192010TT patent/HRP20192010T1/hr unknown
- 2019-12-02 CY CY20191101258T patent/CY1122335T1/el unknown
-
2020
- 2020-04-06 AU AU2020202402A patent/AU2020202402B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3157522B1 (en) | 2019-09-04 |
| PT3157522T (pt) | 2019-12-13 |
| DK3157522T3 (da) | 2019-12-09 |
| AU2020202402B2 (en) | 2021-05-27 |
| LT3157522T (lt) | 2019-11-25 |
| HUE051527T2 (hu) | 2021-03-01 |
| KR102618119B1 (ko) | 2023-12-27 |
| CA2952701C (en) | 2023-09-19 |
| AU2015276310A1 (en) | 2016-12-08 |
| US9474747B2 (en) | 2016-10-25 |
| AU2015276310B2 (en) | 2020-01-16 |
| EP3157522A1 (en) | 2017-04-26 |
| PL3157522T3 (pl) | 2020-03-31 |
| US10682345B2 (en) | 2020-06-16 |
| WO2015193213A1 (en) | 2015-12-23 |
| HRP20192010T1 (hr) | 2020-02-07 |
| SI3157522T1 (sl) | 2020-01-31 |
| US20190262329A1 (en) | 2019-08-29 |
| US20150366855A1 (en) | 2015-12-24 |
| RS59613B1 (sr) | 2020-01-31 |
| EP3603640A1 (en) | 2020-02-05 |
| US10342789B2 (en) | 2019-07-09 |
| CA2952701A1 (en) | 2015-12-23 |
| MX2016016720A (es) | 2017-04-13 |
| MX370430B (es) | 2019-12-13 |
| MX2019014935A (es) | 2020-02-13 |
| US20170007593A1 (en) | 2017-01-12 |
| AU2020202402A1 (en) | 2020-04-30 |
| CY1122335T1 (el) | 2021-01-27 |
| KR20170016986A (ko) | 2017-02-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2759247T3 (es) | Antagonistas muscarínicos y combinaciones de estos para el tratamiento de enfermedades de las vías respiratorias en caballos | |
| US10258634B2 (en) | Ciclesonide for the treatment of airway disease in horses | |
| US11819549B2 (en) | Pharmaceutical formulation comprising ciclesonide | |
| CA2653744C (en) | Nebulizable compositions of quaternary ammonium muscarinic receptor antagonists | |
| US20230033224A1 (en) | Ciclesonide for ameliorating quality of life (qol) in equines |