EP2819951B1 - Leitsalz für lithium-basierte energiespeicher - Google Patents
Leitsalz für lithium-basierte energiespeicher Download PDFInfo
- Publication number
- EP2819951B1 EP2819951B1 EP13706047.1A EP13706047A EP2819951B1 EP 2819951 B1 EP2819951 B1 EP 2819951B1 EP 13706047 A EP13706047 A EP 13706047A EP 2819951 B1 EP2819951 B1 EP 2819951B1
- Authority
- EP
- European Patent Office
- Prior art keywords
- lithium
- trifluoromethoxy
- carbonate
- tetrafluoroethanesulfonate
- electrolyte
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 title claims description 33
- 229910052744 lithium Inorganic materials 0.000 title claims description 33
- 150000003839 salts Chemical class 0.000 title claims description 20
- 238000004146 energy storage Methods 0.000 title claims description 18
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 claims description 87
- JZKLVQHCLLQLSX-UHFFFAOYSA-M lithium;1,2,2,2-tetrafluoro-1-(trifluoromethoxy)ethanesulfonate Chemical compound [Li+].[O-]S(=O)(=O)C(F)(C(F)(F)F)OC(F)(F)F JZKLVQHCLLQLSX-UHFFFAOYSA-M 0.000 claims description 78
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 claims description 72
- 239000003792 electrolyte Substances 0.000 claims description 46
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 claims description 44
- 239000000203 mixture Substances 0.000 claims description 31
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 26
- 229910001416 lithium ion Inorganic materials 0.000 claims description 26
- 239000003960 organic solvent Substances 0.000 claims description 20
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 claims description 17
- UZOJHUKHDYYISK-UHFFFAOYSA-N 1,2,2,2-tetrafluoro-1-(trifluoromethoxy)ethanesulfonyl fluoride Chemical compound FC(F)(F)OC(F)(C(F)(F)F)S(F)(=O)=O UZOJHUKHDYYISK-UHFFFAOYSA-N 0.000 claims description 14
- 239000002608 ionic liquid Substances 0.000 claims description 14
- GAEKPEKOJKCEMS-UHFFFAOYSA-N gamma-valerolactone Chemical compound CC1CCC(=O)O1 GAEKPEKOJKCEMS-UHFFFAOYSA-N 0.000 claims description 12
- 229920000642 polymer Polymers 0.000 claims description 8
- BLTXWCKMNMYXEA-UHFFFAOYSA-N 1,1,2-trifluoro-2-(trifluoromethoxy)ethene Chemical compound FC(F)=C(F)OC(F)(F)F BLTXWCKMNMYXEA-UHFFFAOYSA-N 0.000 claims description 7
- OBTWBSRJZRCYQV-UHFFFAOYSA-N sulfuryl difluoride Chemical compound FS(F)(=O)=O OBTWBSRJZRCYQV-UHFFFAOYSA-N 0.000 claims description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims description 6
- 150000001768 cations Chemical class 0.000 claims description 6
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 claims description 6
- 239000003990 capacitor Substances 0.000 claims description 5
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 claims description 5
- PXELHGDYRQLRQO-UHFFFAOYSA-N 1-butyl-1-methylpyrrolidin-1-ium Chemical compound CCCC[N+]1(C)CCCC1 PXELHGDYRQLRQO-UHFFFAOYSA-N 0.000 claims description 4
- NJMWOUFKYKNWDW-UHFFFAOYSA-N 1-ethyl-3-methylimidazolium Chemical compound CCN1C=C[N+](C)=C1 NJMWOUFKYKNWDW-UHFFFAOYSA-N 0.000 claims description 4
- WTKZEGDFNFYCGP-UHFFFAOYSA-O Pyrazolium Chemical compound C1=CN[NH+]=C1 WTKZEGDFNFYCGP-UHFFFAOYSA-O 0.000 claims description 4
- RWRDLPDLKQPQOW-UHFFFAOYSA-O Pyrrolidinium ion Chemical compound C1CC[NH2+]C1 RWRDLPDLKQPQOW-UHFFFAOYSA-O 0.000 claims description 4
- 150000002892 organic cations Chemical class 0.000 claims description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-O pyridinium Chemical compound C1=CC=[NH+]C=C1 JUJWROOIHBZHMG-UHFFFAOYSA-O 0.000 claims description 4
- IQQRAVYLUAZUGX-UHFFFAOYSA-N 1-butyl-3-methylimidazolium Chemical compound CCCCN1C=C[N+](C)=C1 IQQRAVYLUAZUGX-UHFFFAOYSA-N 0.000 claims description 3
- IRGDPGYNHSIIJJ-UHFFFAOYSA-N 1-ethyl-2,3-dimethylimidazol-3-ium Chemical compound CCN1C=C[N+](C)=C1C IRGDPGYNHSIIJJ-UHFFFAOYSA-N 0.000 claims description 3
- YQFWGCSKGJMGHE-UHFFFAOYSA-N 1-methyl-1-propylpyrrolidin-1-ium Chemical compound CCC[N+]1(C)CCCC1 YQFWGCSKGJMGHE-UHFFFAOYSA-N 0.000 claims description 3
- RSEBUVRVKCANEP-UHFFFAOYSA-N 2-pyrroline Chemical compound C1CC=CN1 RSEBUVRVKCANEP-UHFFFAOYSA-N 0.000 claims description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-O Imidazolium Chemical compound C1=C[NH+]=CN1 RAXXELZNTBOGNW-UHFFFAOYSA-O 0.000 claims description 3
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 claims description 3
- 125000005210 alkyl ammonium group Chemical group 0.000 claims description 3
- 239000011159 matrix material Substances 0.000 claims description 3
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 claims description 3
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 claims description 2
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 claims description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 claims description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-O Piperidinium(1+) Chemical compound C1CC[NH2+]CC1 NQRYJNQNLNOLGT-UHFFFAOYSA-O 0.000 claims description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 claims description 2
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 claims description 2
- BTGRAWJCKBQKAO-UHFFFAOYSA-N adiponitrile Chemical compound N#CCCCCC#N BTGRAWJCKBQKAO-UHFFFAOYSA-N 0.000 claims description 2
- ZTOMUSMDRMJOTH-UHFFFAOYSA-N glutaronitrile Chemical compound N#CCCCC#N ZTOMUSMDRMJOTH-UHFFFAOYSA-N 0.000 claims description 2
- LLEVMYXEJUDBTA-UHFFFAOYSA-N heptanedinitrile Chemical compound N#CCCCCCC#N LLEVMYXEJUDBTA-UHFFFAOYSA-N 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 claims 1
- 229910013870 LiPF 6 Inorganic materials 0.000 description 23
- 239000000243 solution Substances 0.000 description 22
- 210000004027 cell Anatomy 0.000 description 17
- SBLRHMKNNHXPHG-UHFFFAOYSA-N 4-fluoro-1,3-dioxolan-2-one Chemical compound FC1COC(=O)O1 SBLRHMKNNHXPHG-UHFFFAOYSA-N 0.000 description 16
- 239000002904 solvent Substances 0.000 description 14
- 239000011877 solvent mixture Substances 0.000 description 14
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 12
- -1 lithium hexafluorophosphate Chemical compound 0.000 description 11
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 9
- 229910002804 graphite Inorganic materials 0.000 description 9
- 239000010439 graphite Substances 0.000 description 9
- 101000801643 Homo sapiens Retinal-specific phospholipid-transporting ATPase ABCA4 Proteins 0.000 description 8
- 102100033617 Retinal-specific phospholipid-transporting ATPase ABCA4 Human genes 0.000 description 8
- 238000000354 decomposition reaction Methods 0.000 description 8
- 239000012071 phase Substances 0.000 description 8
- 239000005518 polymer electrolyte Substances 0.000 description 7
- 210000005056 cell body Anatomy 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 6
- 150000001450 anions Chemical class 0.000 description 5
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 229910052731 fluorine Inorganic materials 0.000 description 5
- 238000007363 ring formation reaction Methods 0.000 description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 238000002484 cyclic voltammetry Methods 0.000 description 4
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 4
- 239000011888 foil Substances 0.000 description 4
- 229910003002 lithium salt Inorganic materials 0.000 description 4
- 159000000002 lithium salts Chemical class 0.000 description 4
- 239000007784 solid electrolyte Substances 0.000 description 4
- 229920002799 BoPET Polymers 0.000 description 3
- 241001295925 Gegenes Species 0.000 description 3
- 229910001290 LiPF6 Inorganic materials 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 239000010406 cathode material Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 239000011737 fluorine Substances 0.000 description 3
- 238000000034 method Methods 0.000 description 3
- 229910052697 platinum Inorganic materials 0.000 description 3
- 229920006267 polyester film Polymers 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 229910001220 stainless steel Inorganic materials 0.000 description 3
- 239000010935 stainless steel Substances 0.000 description 3
- 238000003878 thermal aging Methods 0.000 description 3
- ZXMGHDIOOHOAAE-UHFFFAOYSA-N 1,1,1-trifluoro-n-(trifluoromethylsulfonyl)methanesulfonamide Chemical compound FC(F)(F)S(=O)(=O)NS(=O)(=O)C(F)(F)F ZXMGHDIOOHOAAE-UHFFFAOYSA-N 0.000 description 2
- IHPWVGWUNMKDHG-UHFFFAOYSA-N 1,2,2,2-tetrafluoro-1-(trifluoromethoxy)ethanesulfonic acid Chemical compound OS(=O)(=O)C(F)(C(F)(F)F)OC(F)(F)F IHPWVGWUNMKDHG-UHFFFAOYSA-N 0.000 description 2
- ZPFAVCIQZKRBGF-UHFFFAOYSA-N 1,3,2-dioxathiolane 2,2-dioxide Chemical compound O=S1(=O)OCCO1 ZPFAVCIQZKRBGF-UHFFFAOYSA-N 0.000 description 2
- WDXYVJKNSMILOQ-UHFFFAOYSA-N 1,3,2-dioxathiolane 2-oxide Chemical compound O=S1OCCO1 WDXYVJKNSMILOQ-UHFFFAOYSA-N 0.000 description 2
- OYOKPDLAMOMTEE-UHFFFAOYSA-N 4-chloro-1,3-dioxolan-2-one Chemical compound ClC1COC(=O)O1 OYOKPDLAMOMTEE-UHFFFAOYSA-N 0.000 description 2
- BJWMSGRKJIOCNR-UHFFFAOYSA-N 4-ethenyl-1,3-dioxolan-2-one Chemical compound C=CC1COC(=O)O1 BJWMSGRKJIOCNR-UHFFFAOYSA-N 0.000 description 2
- SJHAYVFVKRXMKG-UHFFFAOYSA-N 4-methyl-1,3,2-dioxathiolane 2-oxide Chemical compound CC1COS(=O)O1 SJHAYVFVKRXMKG-UHFFFAOYSA-N 0.000 description 2
- ZKOGUIGAVNCCKH-UHFFFAOYSA-N 4-phenyl-1,3-dioxolan-2-one Chemical class O1C(=O)OCC1C1=CC=CC=C1 ZKOGUIGAVNCCKH-UHFFFAOYSA-N 0.000 description 2
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 2
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 2
- 239000002033 PVDF binder Substances 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 239000004372 Polyvinyl alcohol Substances 0.000 description 2
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical class CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 2
- YQOXCVSNNFQMLM-UHFFFAOYSA-N [Mn].[Ni]=O.[Co] Chemical compound [Mn].[Ni]=O.[Co] YQOXCVSNNFQMLM-UHFFFAOYSA-N 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 229930188620 butyrolactone Natural products 0.000 description 2
- 238000002485 combustion reaction Methods 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- BDUPRNVPXOHWIL-UHFFFAOYSA-N dimethyl sulfite Chemical compound COS(=O)OC BDUPRNVPXOHWIL-UHFFFAOYSA-N 0.000 description 2
- 239000000446 fuel Substances 0.000 description 2
- 238000002290 gas chromatography-mass spectrometry Methods 0.000 description 2
- 239000007770 graphite material Substances 0.000 description 2
- 150000004693 imidazolium salts Chemical class 0.000 description 2
- 230000016507 interphase Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 239000011244 liquid electrolyte Substances 0.000 description 2
- MOVBJUGHBJJKOW-UHFFFAOYSA-N methyl 2-amino-5-methoxybenzoate Chemical compound COC(=O)C1=CC(OC)=CC=C1N MOVBJUGHBJJKOW-UHFFFAOYSA-N 0.000 description 2
- 229920001483 poly(ethyl methacrylate) polymer Polymers 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 229920002239 polyacrylonitrile Polymers 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 229920002689 polyvinyl acetate Polymers 0.000 description 2
- 239000011118 polyvinyl acetate Substances 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 2
- KCXFHTAICRTXLI-UHFFFAOYSA-N propane-1-sulfonic acid Chemical class CCCS(O)(=O)=O KCXFHTAICRTXLI-UHFFFAOYSA-N 0.000 description 2
- 230000035882 stress Effects 0.000 description 2
- LSNNMFCWUKXFEE-UHFFFAOYSA-L sulfite Chemical class [O-]S([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-L 0.000 description 2
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- NTWSIWWJPQHFTO-AATRIKPKSA-N (2E)-3-methylhex-2-enoic acid Chemical compound CCC\C(C)=C\C(O)=O NTWSIWWJPQHFTO-AATRIKPKSA-N 0.000 description 1
- GEEKTXDSIAGUSI-UHFFFAOYSA-N 1,1,1,2,2-pentafluoroethane;trifluoroborane Chemical class FB(F)F.FC(F)C(F)(F)F GEEKTXDSIAGUSI-UHFFFAOYSA-N 0.000 description 1
- QARLOMBMXGVKNV-UHFFFAOYSA-N 1,2,2-trifluoroethenesulfonyl fluoride Chemical compound FC(F)=C(F)S(F)(=O)=O QARLOMBMXGVKNV-UHFFFAOYSA-N 0.000 description 1
- MXLZUALXSYVAIV-UHFFFAOYSA-N 1,2-dimethyl-3-propylimidazol-1-ium Chemical compound CCCN1C=C[N+](C)=C1C MXLZUALXSYVAIV-UHFFFAOYSA-N 0.000 description 1
- KLAYAUDKBPHROK-UHFFFAOYSA-N 2,3-diethyl-1,4-dimethylimidazol-1-ium Chemical compound CCC=1N(CC)C(C)=C[N+]=1C KLAYAUDKBPHROK-UHFFFAOYSA-N 0.000 description 1
- GKZFQPGIDVGTLZ-UHFFFAOYSA-N 4-(trifluoromethyl)-1,3-dioxolan-2-one Chemical compound FC(F)(F)C1COC(=O)O1 GKZFQPGIDVGTLZ-UHFFFAOYSA-N 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- 239000002000 Electrolyte additive Substances 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- LWTXYNTVYZGNCF-UHFFFAOYSA-N P(=O)(F)(F)F.FC(C(F)(F)F)F.FC(C(F)(F)F)F.FC(C(F)(F)F)F Chemical compound P(=O)(F)(F)F.FC(C(F)(F)F)F.FC(C(F)(F)F)F.FC(C(F)(F)F)F LWTXYNTVYZGNCF-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 1
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 1
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 1
- XQGUTBUWGIAGAA-UHFFFAOYSA-M [Li+].OC(O)=O.[O-]S(=O)(=O)C(F)(OC(F)(F)F)C(F)(F)F Chemical compound [Li+].OC(O)=O.[O-]S(=O)(=O)C(F)(OC(F)(F)F)C(F)(F)F XQGUTBUWGIAGAA-UHFFFAOYSA-M 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 239000000010 aprotic solvent Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- DKNRELLLVOYIIB-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;1-methyl-1-propylpyrrolidin-1-ium Chemical compound CCC[N+]1(C)CCCC1.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F DKNRELLLVOYIIB-UHFFFAOYSA-N 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 229940060799 clarus Drugs 0.000 description 1
- CXULZQWIHKYPTP-UHFFFAOYSA-N cobalt(2+) manganese(2+) nickel(2+) oxygen(2-) Chemical compound [O--].[O--].[O--].[Mn++].[Co++].[Ni++] CXULZQWIHKYPTP-UHFFFAOYSA-N 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 150000005676 cyclic carbonates Chemical class 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 101150047356 dec-1 gene Proteins 0.000 description 1
- 238000009831 deintercalation Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000012983 electrochemical energy storage Methods 0.000 description 1
- 239000007772 electrode material Substances 0.000 description 1
- 239000002001 electrolyte material Substances 0.000 description 1
- 238000009713 electroplating Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- XTPRURKTXNFVQT-UHFFFAOYSA-N hexyl(trimethyl)azanium Chemical compound CCCCCC[N+](C)(C)C XTPRURKTXNFVQT-UHFFFAOYSA-N 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-O hydron;1,3-oxazole Chemical compound C1=COC=[NH+]1 ZCQWOFVYLHDMMC-UHFFFAOYSA-O 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-O hydron;pyrimidine Chemical compound C1=CN=C[NH+]=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-O 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 230000002687 intercalation Effects 0.000 description 1
- 238000004502 linear sweep voltammetry Methods 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- ZYQNCHBTYCRDAH-UHFFFAOYSA-K lithium bis[[1,2,2,2-tetrafluoro-1-(trifluoromethoxy)ethyl]sulfonyloxy]lead 1,2,2,2-tetrafluoro-1-(trifluoromethoxy)ethanesulfonate Chemical compound [Pb+2].FC(OC(C(F)(F)F)(S(=O)(=O)[O-])F)(F)F.[Li+].FC(OC(C(F)(F)F)(S(=O)(=O)[O-])F)(F)F.FC(OC(C(F)(F)F)(S(=O)(=O)[O-])F)(F)F ZYQNCHBTYCRDAH-UHFFFAOYSA-K 0.000 description 1
- 150000002642 lithium compounds Chemical class 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- KTQDYGVEEFGIIL-UHFFFAOYSA-N n-fluorosulfonylsulfamoyl fluoride Chemical compound FS(=O)(=O)NS(F)(=O)=O KTQDYGVEEFGIIL-UHFFFAOYSA-N 0.000 description 1
- 229910001317 nickel manganese cobalt oxide (NMC) Inorganic materials 0.000 description 1
- 239000011255 nonaqueous electrolyte Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- XYFCBTPGUUZFHI-UHFFFAOYSA-O phosphonium Chemical compound [PH4+] XYFCBTPGUUZFHI-UHFFFAOYSA-O 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 229920005569 poly(vinylidene fluoride-co-hexafluoropropylene) Polymers 0.000 description 1
- 229920000867 polyelectrolyte Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920006254 polymer film Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- GTDKXDWWMOMSFL-UHFFFAOYSA-M tetramethylazanium;fluoride Chemical compound [F-].C[N+](C)(C)C GTDKXDWWMOMSFL-UHFFFAOYSA-M 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- SMBZJSVIKJMSFP-UHFFFAOYSA-N trifluoromethyl hypofluorite Chemical compound FOC(F)(F)F SMBZJSVIKJMSFP-UHFFFAOYSA-N 0.000 description 1
- 238000004832 voltammetry Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01D—COMPOUNDS OF ALKALI METALS, i.e. LITHIUM, SODIUM, POTASSIUM, RUBIDIUM, CAESIUM, OR FRANCIUM
- C01D15/00—Lithium compounds
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0567—Liquid materials characterised by the additives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/01—Sulfonic acids
- C07C309/02—Sulfonic acids having sulfo groups bound to acyclic carbon atoms
- C07C309/03—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton
- C07C309/07—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing oxygen atoms bound to the carbon skeleton
- C07C309/09—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing oxygen atoms bound to the carbon skeleton containing etherified hydroxy groups bound to the carbon skeleton
- C07C309/10—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing oxygen atoms bound to the carbon skeleton containing etherified hydroxy groups bound to the carbon skeleton with the oxygen atom of at least one of the etherified hydroxy groups further bound to an acyclic carbon atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/63—Esters of sulfonic acids
- C07C309/64—Esters of sulfonic acids having sulfur atoms of esterified sulfo groups bound to acyclic carbon atoms
- C07C309/65—Esters of sulfonic acids having sulfur atoms of esterified sulfo groups bound to acyclic carbon atoms of a saturated carbon skeleton
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/54—Electrolytes
- H01G11/58—Liquid electrolytes
- H01G11/62—Liquid electrolytes characterised by the solute, e.g. salts, anions or cations therein
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0565—Polymeric materials, e.g. gel-type or solid-type
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/04—Hybrid capacitors
- H01G11/06—Hybrid capacitors with one of the electrodes allowing ions to be reversibly doped thereinto, e.g. lithium ion capacitors [LIC]
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/54—Electrolytes
- H01G11/58—Liquid electrolytes
- H01G11/60—Liquid electrolytes characterised by the solvent
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
- H01M2300/0034—Fluorinated solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
- H01M2300/0037—Mixture of solvents
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/13—Energy storage using capacitors
Definitions
- the invention relates to a conductive salt and an electrolyte for lithium-based energy storage.
- Lithium-ion technology is the leading technology in the field of rechargeable battery storage systems for portable electronics. Due to their high cell voltage, their superior energy and power density as well as their extremely low self-discharge, lithium-ion batteries have a high potential for these applications.
- lithium hexafluorophosphate LiPF 6
- Lithium hexafluorophosphate has relatively high conductivity, but has significant disadvantages due to low thermal stability and toxicity of its combustion products.
- lithium bis (oxalato) borate LiBOB
- a disadvantage is that bis (oxalato) borate has only a low solubility in the usual carbonates used as a solvent in electrolytes. Show further LiBOB-based electrolytes have lower conductivity compared to LiPF 6 , especially at low temperatures, and higher viscosity.
- US 2006/276670 A1 discloses hydrofluoroalkanesulfonates of the general formula RO-CXH-CX 2 -SO 3 M, wherein R is selected from the group consisting of alkyl groups, functionalized alkyl groups, and alkenyl groups; X is selected from the group consisting of hydrogen and fluorine, provided that at least one X is fluorine; and M is a cation.
- Z + is a cation selected from the group consisting of pyridinium, pyridazinium, pyrimidinium, pyrazinium, imidazolium, pyrazolium,
- the present invention was therefore based on the object to provide a compound which at least one of the aforementioned disadvantages of the prior Technology overcomes.
- the object of the present invention was to provide a lithium compound suitable as a conductive salt.
- Lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate is also referred to as lithium 1,2,2,2-tetrafluoro-1- (trifluoromethoxy) ethanesulfonate.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate has good lithium-ion conductivity and high electrochemical stability.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate can be used in a wide temperature range as a conductive salt.
- cells in which electrolytes containing lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate as the conducting salt exhibit good cycle stability and capacity retention.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate is good thermal stability.
- it is advantageous that lithium-1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate shows no or almost no signs of decomposition even at high temperatures.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate exhibits lower toxicity of the combustion products than LiPF 6 .
- Lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate is therefore advantageously suitable as a conductive salt for commercial lithium-ion batteries.
- Another object of the present invention relates to the use of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoro-ethanesulfonate in lithium-based energy storage, especially as conducting salt.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate is useful as a conductive salt in electrolytes for lithium-based energy storage.
- Primary and secondary lithium-based energy stores are preferably selected from the group comprising lithium batteries, lithium-ion batteries, lithium-ion secondary batteries, lithium-polymer batteries and / or lithium-ion capacitors.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate is suitable as a conductive salt for a lithium-ion battery or a lithium-ion battery.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate in lithium-based energy storage, a thermally stable conductive salt can be provided.
- This is a lithium-based energy storage in one wide temperature range usable.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate in a concentration of 1 M is usable.
- the charge transport in lithium-based electrochemical energy storage takes place via an electrolyte.
- the conductive salt of a liquid electrolyte is therefore preferably dissolved in a solvent.
- the electrolyte comprises lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate preferably dissolved in an organic solvent.
- the electrolyte can be prepared, for example, by introducing and dissolving lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate in a solvent or a solvent mixture.
- Another object of the invention relates to an electrolyte for a lithium-based energy storage comprising lithium-1-trifluoromethoxy-1,2,2,2-tetrafluoro-ethanesulfonate.
- Electrolytes for lithium-based energy storage devices comprising lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate as conductive salt have in particular the advantage of good thermal and electrochemical stability.
- the electrolyte comprises an organic solvent, an ionic liquid and / or a polymer matrix.
- an electrolyte comprises an organic solvent and lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate. It has been found that lithium-1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate has good solubility in organic solvents, especially mixtures with cyclic or linear carbonates. This allows advantageously the Use of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate in the liquid electrolyte used in commercial lithium-ion batteries.
- the organic solvent is selected from the group comprising ethylene carbonate, propylene carbonate, diethyl carbonate, dimethyl carbonate, ethylmethyl carbonate, acetonitrile, glutaronitrile, adiponitrile, pimelonitrile, gamma-butyrolactone, gamma-valerolactone, dimethoxyethane, 1,3-dioxolane, methyl acetate and / or Mix of it.
- Suitable organic solvents are selected from the group comprising cyclic carbonates such as ethylene carbonate and propylene carbonate and / or linear carbonates such as diethyl carbonate, dimethyl carbonate and ethyl methyl carbonate.
- organic solvents are selected from the group comprising gamma-butyrolactone and / or gamma-valerolactone.
- the organic solvent is selected from the group comprising ethylene carbonate, diethyl carbonate, dimethyl carbonate, ethyl methyl carbonate, gamma-butyrolactone, gamma-valerolactone and / or mixtures thereof.
- a preferred solvent is ethylene carbonate.
- Ethylene carbonate is also referred to as 1,3-dioxolan-2-one according to the IUPAC nomenclature.
- Ethylene carbonate is commercially available and has a high boiling point and a high flash point. It is also advantageous that ethylene carbonate allows a high conductivity by a good Salzdissoziation.
- the organic solvent comprises a mixture of ethylene carbonate and at least one further organic solvent, preferably selected from the group comprising gamma-butyrolactone and / or diethyl carbonate.
- the organic solvent comprises a mixture of ethylene carbonate and gamma-butyrolactone.
- solvent mixtures comprising ethylene carbonate and gamma-butyrolactone could advantageously a high Conductivity in a temperature range of -20 ° C to + 60 ° C can be achieved.
- high conductivities in a temperature range from -30 ° C to + 60 ° C can be achieved in solvent mixtures comprising gamma-butyrolactone.
- binary mixtures of carbonates, in particular of ethylene carbonate with a further carbonate for example diethyl carbonate, dimethyl carbonate and / or ethylmethyl carbonate, in particular diethyl carbonate, are suitable.
- the ratio of ethylene carbonate and the at least one further organic solvent, preferably gamma-butyrolactone or diethyl carbonate, is preferably in the range from ⁇ 1:99 to ⁇ 99: 1, preferably in the range from ⁇ 1: 9 to ⁇ 9: 1, preferably. Range from ⁇ 3: 7 to ⁇ 1: 1. Unless indicated otherwise, the ratio given refers to the parts by weight of the solvents.
- ternary mixtures comprising at least one carbonate as solvent.
- Particular preference is given to mixtures of ethylene carbonate with a further solvent, for example gamma-butyrolactone or diethyl carbonate, and a compound which is suitable for forming a so-called solid electrolyte interphase (SEI), a solid-electrolyte interface.
- SEI solid electrolyte interphase
- the electrolyte may therefore further comprise additives, in particular film-forming electrolyte additives.
- the electrolyte comprises a compound selected from the group comprising chloroethylene carbonate, fluoroethylene carbonate, vinyl ethylene carbonate, ethylene sulfite, ethylene sulfate, propanesulfonates, sulfites, preferably dimethyl sulfite and propylene sulfite, sulfates, optionally F, Cl or Br substituted butyrolactones, phenylethylene carbonate, vinyl acetate and / or Trifluorpropylencarbonat.
- chloro or fluoro-substituted carbonates are preferred, especially fluoroethylene carbonate (FEC).
- FEC fluoroethylene carbonate
- the connections can be the Improve battery performance, such as the capacity or the cycle life.
- fluoroethylene carbonate can lead to improved long-term stability of a cell.
- the electrolyte contains an additive, in particular a compound selected from the group consisting of chloroethylene carbonate, fluoroethylene carbonate, vinyl ethylene carbonate, ethylene sulfite, ethylene sulfate, propanesulfonates, sulfites, preferably dimethyl sulfite and propylene sulfite, sulfates, optionally substituted by F, Cl or Br butyrolactones, phenylethylene carbonate, vinyl acetate and or trifluoropropylene carbonate, preferably fluoroethylene carbonate, in the range of ⁇ 0.1 wt .-% to ⁇ 10 wt .-%, preferably in the range of ⁇ 1 wt .-% to ⁇ 5 wt .-%, preferably in the range of ⁇ 2 Wt .-% to ⁇ 3 wt .-%, based on the total weight of the electrolyte.
- an additive in particular a compound selected from the group consisting
- the organic solvent preferably comprises a mixture of ethylene carbonate and at least one further organic solvent, preferably selected from the group comprising gamma-butyrolactone, gamma-valerolactone or diethyl carbonate and fluoroethylene carbonate.
- the ratio of ethylene carbonate and the at least one further organic solvent preferably selected from the group comprising gamma-butyrolactone, gamma-valerolactone or diethyl carbonate, and an additive, preferably fluoroethylene carbonate, in the range of ⁇ 98: 1: 1 to ⁇ 1: 1:98, preferably in the range of ⁇ 80: 15: 5 to ⁇ 15: 80: 5, preferably in the range of ⁇ 4.5: 4.5: 1 to ⁇ 1: 1: 0.01. Unless otherwise indicated, the indicated ratio refers to the parts by weight.
- the organic solvent particularly preferably comprises a mixture of ethylene carbonate, gamma-butyrolactone and fluoroethylene carbonate, in particular in a ratio of 4.5: 4.5: 1.
- a solvent mixture comprising ethylene carbonate, gamma-butyrolactone and fluoroethylene carbonate in a ratio of 4.5: 4.5: 1, a good conductivity in a temperature range of -20 ° C to + 60 ° C could be achieved in an advantageous manner.
- Preferred ionic liquids include a cation selected from the group consisting of 1-ethyl-3-methylimidazolium (EMI + ), 1,2-dimethyl-3-propylimidazolium (DMPI + ), 1,2-diethyl-3,5-dimethylimidazolium (DEDMI + ), Trimethyl- n- hexylammonium (TMHA + ), N- alkyl- N- methylpyrrolidinium (PYR 1R + ), N- alkyl- N- methylpiperidinium (PIP 1R + ) and / or N- alkyl- N- methylmorpholinium (MORP 1R + ) and an anion selected from the group comprising bis (trifluoromethanesulfonyl) imide (TFSI - ), bis (pentafluoroethanesulfonyl) imide (BETI - ), bis (fluorosulfonyl) imide (FSI
- Preferred N- alkyl- N- methylpyrrolidinium (PYR 1R + ) cations are selected from the group comprising N-butyl-N-methylpyrrolidinium (PYR 14 + ) and / or N-methyl-N-propylpyrrolidinium (PYR 13 + ).
- Preferred ionic liquids are selected from the group comprising N-butyl-N-methylpyrrolidinium bis (trifluoromethanesulfonyl) imide (PYR 14 TFSI) and / or N-methyl-N-propylpyrrolidinium bis (trifluoromethanesulfonyl) imide (PYR 13 TFSI).
- Suitable electrolyte materials are polymer electrolytes wherein the polymer electrolyte may be present as a gel polymer electrolyte or a solid polymer electrolyte.
- Solid polyelectrolytes show good properties with respect to the requirements of future accumulator generations. They enable a solvent-free structure that is easy to produce and versatile in shape. In addition, the energy density can be increased be, because it eliminates the three-layer structure of electrolyte-separator-electrolyte, so that only a thin polymer film between the electrodes is needed.
- solid electrolytes are chemically and electrochemically stable to electrode materials and furthermore do not leave the cell.
- Gel polymer electrolytes usually comprise an aprotic solvent and a polymer matrix.
- Preferred polymers for solid polymer electrolytes and gel polymer electrolytes are selected from the group comprising homo- or copolymers of polyethylene oxide (PEO), polypropylene oxide (PPO), polyvinylidene fluoride (PVdF), polyvinylidene fluoridehexafluoropropylene (PVdF-HFP), polyacrylonitrile (PAN), polymethylmethacrylate (PMMA), Polyethyl methacrylate (PEMA), polyvinyl acetate (PVAc), polyvinyl chloride (PVC), Polyphophazene, polysiloxanes, polyvinyl alcohol (PVA) and / or homo and (block) copolymers comprising functional side chains selected from the group consisting of ethylene oxide, propylene oxide, acrylonitrile and / or siloxanes.
- PEO polyethylene oxide
- PPO polypropylene oxide
- PVdF polyvinylidene fluoride
- PVdF-HFP poly
- the concentration of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate in the electrolyte is in the range of ⁇ 0.1 M to ⁇ 2 M, preferably in the range of ⁇ 0.5 M to ⁇ 1.5 M, more preferably in the range of ⁇ 0.7 M to ⁇ 1.2 M.
- the concentration of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate in the electrolyte at 1 M.
- concentrations of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate lead to good conductivity.
- Another object of the invention relates to a lithium-based energy storage, preferably a lithium battery, lithium-ion battery, lithium-ion battery, lithium-polymer battery or lithium-ion capacitor comprising lithium 2-trifluoromethoxy-1, 2,2,2-tetrafluoro-ethane sulfonate.
- a lithium-based energy storage preferably a lithium battery, Lithium-ion battery, lithium-ion battery, lithium-polymer battery or lithium-ion capacitor, comprising an electrolyte according to the invention comprising lithium-1-trifluoromethoxy-1,2,2,2-tetrafluoro-ethanesulfonate.
- the lithium-based energy storage devices are suitable for all areas of application, in particular for larger systems such as automobiles or as stationary energy storage for renewable energies.
- reaction of 1,1,2-trifluoro-2- (trifluoromethoxy) ethene, CF 3 OCF CF 2 , with sulfuryl difluoride, SO 2 F 2 , in the presence of catalytic amounts of tetramethylammonium fluoride.
- the reaction is preferably carried out with heating, in particular at a temperature in the range of 50 ° C to 60 ° C.
- the subsequent hydrolysis of 1,2,2,2-tetrafluoro-1- (trifluoromethoxy) ethanesulfonyl fluoride with lithium hydroxide is preferably carried out with ethanolic lithium hydroxide solution.
- the precursor obtained in step a) 1,2,2,2-tetrafluoro-1- (trifluoromethoxy) ethanesulfonyl fluoride.
- a larger yield can be achieved by the inventive method.
- Lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate is useful as a conductive salt in an electrolyte comprising, for example, an ionic liquid in lithium-based energy storage devices.
- Ionic liquids are useful as non-aqueous electrolytes, in particular for electrochemical uses, for example in batteries or electrochemical capacitors, but also for electroplating, catalysis or chemical reactions. Accordingly, ionic liquids with preferably broad electrochemical windows and low hygroscopicity are advantageously usable not only for electrochemical applications.
- Another object of the invention relates to an ionic liquid comprising 1-trifluoromethoxy-1,2,2,2-tetrafluoro-ethanesulfonate and an organic cation selected from the group comprising alkylammonium, pyridinium, pyrazolium, pyrrolium, pyrrolinium, piperidinium -, pyrrolidinium, imidazolium and / or sulfonium compounds.
- the organic cation is preferably selected from the group comprising alkylammonium, pyridinium, pyrazolium, pyrrolium, pyrrolinium, piperidinium, pyrrolidinium and / or imidazolium compounds, in particular pyrrolidinium and / or imidazolium compounds.
- the cation is selected from the group comprising N-butyl-N-methylpyrrolidinium (PYR14), N-methyl-N-propylpyrrolidinium (PYR13), 1-ethyl-3-methylimidazolium (EMIM), 1-ethyl-2,3- dimethylimidazolium (EDiMIM) and / or 1-butyl-3-methylimidazolium (BMIM).
- PYR14 N-butyl-N-methylpyrrolidinium
- PYR13 N-methyl-N-propylpyrrolidinium
- EMIM 1-ethyl-3-methylimidazolium
- EiMIM 1-ethyl-2,3- dimethylimidazolium
- BMIM 1-butyl-3-methylimidazolium
- Ionic liquids comprising 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate as anion and an organic cation can be used advantageously for electrochemical Applications find use, for example, in combination with a lithium salt in lithium-based energy storage. Furthermore, uses in solar cells or fuel cells are advantageous.
- ionic liquids comprising fluorinated anions are also useful as hydraulic fluid or inert liquid diluents for highly reactive chemicals.
- Lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate was dried at 60 ° C for 24 hours prior to use.
- the conductivity of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate was determined in different solvents in a temperature range from -40 ° C to + 60 ° C.
- ethylene carbonate (Ferro Corporation, battery grade) and 50% by weight of diethyl carbonate (DEC) (Ferro Corporation, battery grade) (EC: DEC, 1: 1), of 50% by weight of ethylene carbonate and 50% by weight of gamma-butyrolactone ( ⁇ BL) (Ferro Corporation, Battery Grade) (EC: ⁇ BL, 1: 1), and 45% by weight of ethylene carbonate, 45% by weight of gamma-butyrolactone and 10% by weight.
- % Fluoroethylene carbonate (Solvay GmbH) (EC: ⁇ BL: FEC, 4.5: 4.5: 1) were submitted.
- the conductivity of the electrolytes was determined using platinum conductivity cells (Amel Glassware, cell constant 1 cm -1 ) with a potentiostat (Solartron 1287A) in conjunction with an impedance measuring unit (Solartron 1260) in a temperature range of -40 ° C to + 60 ° C (Climatic cabinet, binder MK53) examined.
- platinum conductivity cells Al Glassware, cell constant 1 cm -1
- a potentiostat Solartron 1287A
- an impedance measuring unit Solartron 1260
- the conductivity cells were first heated to 60 ° C and then cooled at temperature intervals of 5 ° C to -40 ° C.
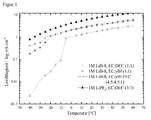
- FIG. 1 shows the course of the conductivity of the 1 M solutions of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate (LiB-8) in the various solvent mixtures in the temperature range from -40 ° C to + 60 ° C and the from LiPF 6 . How to get the FIG.
- ethylene carbonate and gamma-butyrolactone (EC: ⁇ BL, 1: 1) and ethylene carbonate, gamma-butyrolactone and fluoroethylene carbonate (EC: ⁇ BL: FEC) in the temperature range from - 40 ° C to + 0 ° C was significantly higher than the conductivity in ethylene carbonate and diethyl carbonate (EC: DEC, 1: 1) and nearly reached the conductivity of LiPF 6 in ethylene carbonate and diethyl carbonate (EC: DEC, 3: 7) over the entire temperature range.
- the cathodic stability limit the potential at which reduction begins, the potential at which the current density was - 0.1 mA cm -2 was defined .
- the potential at which oxidation begins the potential at which the current density exceeded + 0.1 mA cm -2 was defined .
- the anodic stability depends crucially on the stability of the electrolyte used.
- the experiments were carried out in a 3-electrode arrangement in modified Swagelok® T-pieces (tube connectors, stainless steel body) with a platinum electrode (eDAQ, model ET075, 1 mm diameter) as a working electrode and lithium foil (12 mm or 7 mm diameter, Chemetall) as Counter and reference electrode performed.
- a platinum electrode eDAQ, model ET075, 1 mm diameter
- lithium foil (12 mm or 7 mm diameter, Chemetall
- the cell body was lined with a one-side siliconized polyester film (Mylar®, PPI-SP 914, 100 ⁇ m) and the electrodes were introduced into the cell body.
- the electrodes were separated with a nonwoven (Freudenberg®, FS2226E, 6 layers), which was impregnated with the appropriate electrolyte.
- the feed rate was 1 mV s -1 .
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate (LiB-8) in a 1: 1 mixture of ethylene carbonate and diethyl carbonate reached the cathodic stability limit at 0.03V .
- the anodic stability of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate was 5.7 V and is complete sufficient for use of the electrolyte in combination with high-voltage cathode materials.
- the cyclization behavior of a 1 M solution of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate prepared according to Example 1 was measured in a mixture of 50% by weight of ethylene carbonate and 50% by weight of diethyl carbonate (EC: DEC, 1: 1) against the cyclization of a 1 M solution of LiPF 6 in a mixture of 30% by weight of ethylene carbonate and 70% by weight of diethyl carbonate (EC: DEC, 3: 7).
- the Zyklisier test included several phases.
- the formation of the graphite SEI formation
- C / 5 a constant current C rate of C / 5.
- Cyclic behavior checked at a charge and discharge rate of 1C.
- the cell system was kept at a voltage of 0.025 V for one hour after charging.
- the graphite was always charged at C / 2 and then held at 0.025V for one hour before the graphite was discharged at different rates.
- the applied D rates (Discharge rates) were D / 5, D / 3; D / 2, 1D, 2D, 3D, 5D and 10D.
- the D-rate test was followed by five cycles of C / 5 charge and discharge rates to verify that the graphite had been damaged by the stress test.
- the last phase included the same cycling parameters as phase 2 and was performed for 30 cycles.
- the discharge capacity of the 1 M solutions of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate and LiPF 6 are plotted against the number of cycles of the lithium ion battery half cell charged at a C rate of 1C.
- the half-cell with 1 M lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate after forming the cell has an initial capacity of about 373 mAh g -1 , the number of cycles to approx 374 mAh g -1 in the 15th cycle increased. This demonstrates the excellent cycle stability of the cell, which corresponds to that of LiPF 6 .
- Example 4 The Zyklisier on NCM cathodes in a half-cell was performed as shown in Example 4 in a 3-electrode arrangement, wherein a nickel-cobalt-manganese oxide electrode (NCM electrode, Toda Kogyo Europe GmbH) as a working electrode and lithium foil (12 mm or 5 mm diameter, Chemetall) was used as a counter and reference electrode.
- NCM electrode nickel-cobalt-manganese oxide electrode
- Chemetall a 1 M solution of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoro-ethanesulfonate prepared according to Example 1 in a Mixture of 50 wt .-% of ethylene carbonate and 50 wt .-% diethyl carbonate (EC: DEC, 1: 1) used.
- the FIG. 4 shows the discharge capacity or lithium storage capacity and the efficiency of the lithium-ion half-cell.
- the load capacity and the efficiency against the number of cycles are plotted.
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate showed an initial capacity of about 138 mAh g -1 after successfully passing the cell flow rate stress test (C-rate test) ( I).
- C-rate test C-rate test
- II cell flow rate stress test
- the capacity in the 80th cycle was still around 137 mAh g -1 .
- the efficiency of the cell after 2 standard cycles increased to over 99.6% of a maximum efficiency of 100%.
- the cell also showed excellent cycle stability with NCM cathode.
- FIG. 5 shows the results of cyclic voltammetry for three cycles (1), (2) and (3).
- the intercalation and deintercalation phases identifiable by the increased current density can be seen in the respective cycles in the range between 0 and 0.3V. This proves the reversibility of the system.
- the enlarged section of the range 0.5V to 1V shows the formation of the solid electrolyte interphase (SEI) of the lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate carbonate electrolyte.
- SEI solid electrolyte interphase
- LiPF 6 Sigma-Aldrich, battery grade
- the electrolytes were stored in a climate chamber for two weeks at 95 ° C and then examined by means of gas chromatography mass spectrometry (Clarus 600 GC Perkin Elmer).
- FIG. 6 shows the decomposition products of the thermal aging at 95 ° C of a 1 M solution of lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate (LiB-8) in ethylene carbonate and diethyl carbonate (EC: DEC) in the ratio 1: 1 compared to 1 M LiPF 6 in EC: DEC im Ratio 3: 7.
- LiB-8 lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate
- EC ethylene carbonate and diethyl carbonate
- lithium 1-trifluoromethoxy-1,2,2,2-tetrafluoroethanesulfonate offers a possibility to replace LiPF 6 as the conducting salt in lithium-ion batteries.
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Inorganic Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Physics & Mathematics (AREA)
- Materials Engineering (AREA)
- Power Engineering (AREA)
- Microelectronics & Electronic Packaging (AREA)
- Dispersion Chemistry (AREA)
- Secondary Cells (AREA)
Description
- Die Erfindung betrifft ein Leitsalz sowie einen Elektrolyten für Lithium-basierte Energiespeicher.
- Die Lithium-Ionen-Technologie ist die führende Technologie auf dem Gebiet der wiederaufladbaren Batteriespeichersysteme für die portable Elektronik. Aufgrund ihrer hohen Zellspannung, ihrer überlegenen Energie- und Leistungsdichte sowie ihrer ausgesprochen niedrigen Selbstentladung haben Lithium-Ionen Batterien ein hohes Potential für diese Anwendungen. Derzeit wird in kommerziell erhältlichen Lithium-Ionen Batterien Lithiumhexafluorophosphat (LiPF6) als Leitsalz verwendet. Lithiumhexafluorophosphat weist eine relativ hohe Leitfähigkeit auf, hat jedoch erhebliche Nachteile aufgrund einer geringen thermischen Stabilität und der Toxizität seiner Verbrennungsprodukte.
- Daher gibt es intensive Bemühungen, alternative Lithiumsalze zu entwickeln, die LiPF6 als Leitsalz ersetzen können. Die in den letzten Jahren entwickelten Lithiumsalze sind häufig komplexe Bor- oder Phosphorhaltige Anionen mit nicht-aromatischen Chelatbildnern wie Oxalat, beispielsweise das in der
DE 198 29 030 C1 offenbarte Lithium-Bis(oxalato)borat (LiBOB). Nachteilig ist jedoch, dass Bis(oxalato)borat eine nur geringe Löslichkeit in den üblichen als Lösungsmittel in Elektrolyten verwendeten Carbonaten aufweist. Weiter weisen LiBOB-basierte Elektrolyte im Vergleich zu LiPF6 eine geringere Leitfähigkeit, insbesondere bei niedrigen Temperaturen, und eine höhere Viskosität auf. - In Journal of Fluorine Chemistry, Bd. 129, Nr. 10, 2008, S. 1029-1035, werden neue Arylenthaltende fluorierte Sulfonsäuren und deren Ammoniumsalze offenbart, die als Elektrolyte für Brennstoffzellen oder ionische Flüssigkeiten verwendbar sind.
-
US 2006/276670 A1 offenbart Hydrofluoralkansulfonate der allgemeinen Formel R-O-CXH-CX2-SO3M, wobei R aus der Gruppe ausgewählt ist bestehend aus Alkylgruppen, funktionalisierten Alkylgruppen, und Alkenylgruppen; X ausgewählt ist aus der Gruppe bestehend aus Wasserstoff und Fluor, mit der Maßgabe, dass mindestens ein X Fluor ist; und M ein Kation ist. -
US 2007/0066822 A1 offenbart Zusammensetzungen der Formel Z+A-, wobei Z+ ein Kation ist ausgewählt aus der Gruppe bestehend aus Pyridinium, Pyridazinium, Pyrimidinium, Pyrazinium, Imidazolium, Pyrazolium, Thiazolium, Oxazolium, Triazolium, und Phosphonium, sowie Ammoniumkationen mit spezifizierten Substituenten, und A- ausgewählt ist aus der Gruppe bestehend aus den drei Anionen R11-CHF-CF2-SO3 -, R12-CF2-CF2-SO3 - und (R13-CHF-CF2-SO2)2N- mit spezifizierten Resten R11, R12 und R13, die als ionische Flüssigkeit verwendbar sind. - Trotz einer Vielzahl an Salzen und Lösungsmitteln wurde noch kein geeigneter Ersatz für LiPF6 als Leitsalz in Carbonatgemischen gefunden. Daher besteht ein Bedarf an alternativen Lithiumsalzen für die Verwendung in Lithium-Ionen Batterien.
- Der vorliegenden Erfindung lag daher die Aufgabe zu Grunde, eine Verbindung zur Verfügung zu stellen, die mindestens einen der vorgenannten Nachteile des Standes der Technik überwindet. Insbesondere lag der vorliegenden Erfindung die Aufgabe zu Grunde, eine als Leitsalz geeignete Lithiumverbindung zur Verfügung zu stellen.
- Diese Aufgabe wird gelöst durch die Verbindung Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat. Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat wird auch als Lithium-1,2,2,2-tetrafluor-1-(trifluormethoxy)ethansulfonat bezeichnet.
- Überraschend wurde gefunden, dass Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat eine gute Lithium-Ionen Leitfähigkeit und eine hohe elektrochemische Stabilität aufweist. In vorteilhafter Weise ist Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in einem weiten Temperaturbereich als Leitsalz verwendbar. Weiter zeigen Zellen, in denen Elektrolyte, die Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat als Leitsalz enthalten, verwendet wurden, eine gute Zyklenstabilität und Kapazitätsretention.
- Darüber hinaus ist ein großer Vorteil von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat eine gute thermische Stabilität. Insbesondere ist von Vorteil, dass Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat auch bei hohen Temperaturen keine oder fast keine Anzeichen einer Zersetzung zeigt. So wurde in thermischen Alterungsversuchen festgestellt, dass bei längerer Lagerung eines Elektrolyten umfassend Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in Karbonat-Lösungsmitteln bei 95 °C keine Karbonatzersetzungsprodukte im Elektrolyten feststellbar sind, welche beim thermischen Lagern von LiPF6 in Karbonat-Mischungen auftreten.
- Hierdurch kann im Vergleich zur Verwendung von LiPF6 als Leitsalz eine erhebliche Verbesserung der Betriebssicherheit zur Verfügung gestellt werden. In insbesondere vorteilhafter Weise ermöglicht dies eine Verwendung im Hochtemperaturbereich. Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat zeigt insbesondere eine geringere Toxizität der Verbrennungsprodukte als LiPF6. Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat ist daher in vorteilhafter Weise als Leitsalz für kommerzielle Lithium-Ionen Batterien geeignet. Weiterhin erwies sich in vorteilhafter Weise auch die anodische Stabilität eines Elektrolyten umfassend Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in Karbonatgemischen auf poliertem Platin mit über 5 V als ausreichend um mit den gängigen Kathodenmaterialien zyklisiert werden zu können.
- Ein weiterer Gegenstand der vorliegenden Erfindung betrifft die Verwendung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in Lithium-basierten Energiespeichern, insbesondere als Leitsalz. Insbesondere ist Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat als Leitsalz in Elektrolyten für Lithium-basierte Energiespeicher verwendbar. Primäre und sekundäre Lithium-basierte Energiespeicher sind vorzugsweise ausgewählt aus der Gruppe umfassend Lithium-Batterien, Lithium-Ionen-Batterien, Lithium-Ionen-Akkumulatoren, Lithium-Polymer-Batterien und/oder Lithium-Ionen-Kondensatoren. Insbesondere eignet sich Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat als Leitsalz für eine Lithium-Ionen Batterie oder einen Lithium-Ionen Akkumulator.
- In vorteilhafter Weise kann durch Verwendung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in Lithium-basierten Energiespeichern ein thermisch stabiles Leitsalz zur Verfügung gestellt werden. Hierdurch ist ein Lithium-basierter Energiespeicher in einem weiten Temperaturbereich verwendbar. Vorzugsweise ist Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in Elektrolyten für Lithium-basierte Energiespeicher in Konzentration im Bereich von ≥ 0,1 M bis ≤ 2 M, vorzugsweise im Bereich von ≥ 0,5 M bis ≤ 1,5 M, besonders bevorzugt im Bereich von ≥ 0,7 M bis ≤ 1,2 M, verwendbar. Insbesondere ist Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in einer Konzentration von 1 M verwendbar.
- Der Ladungstransport in Lithium-basierten elektrochemischen Energiespeichern erfolgt über einen Elektrolyten. Das Leitsalz eines flüssigen Elektrolyten liegt daher vorzugsweise in einem Lösungsmittel gelöst vor. Der Elektrolyt umfasst Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat vorzugsweise gelöst in einem organischen Lösungsmittel. Der Elektrolyt ist beispielsweise herstellbar durch Einbringen und Lösen von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in ein Lösungsmittel oder ein Lösungsmittelgemisch.
- Ein weiterer Gegenstand der Erfindung betrifft einen Elektrolyt für einen Lithium-basierten Energiespeicher umfassend Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat. Elektrolyte für Lithium-basierte Energiespeicher umfassend Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat als Leitsalz weisen insbesondere den Vorteil einer guten thermischen und elektrochemischen Stabilität auf.
- Vorzugsweise umfasst der Elektrolyt ein organisches Lösungsmittel, eine ionische Flüssigkeit und/oder eine Polymermatrix. Vorzugsweise umfasst ein Elektrolyt ein organisches Lösungsmittel und Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat. Es konnte festgestellt werden, dass Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in organischen Lösungsmitteln insbesondere Gemischen mit cyclischen oder linearen Carbonaten eine gute Löslichkeit aufweist. Dies ermöglicht in vorteilhafter Weise die Verwendung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in den in kommerziellen Lithium-Ionen Batterien eingesetzten Flüssigelektrolyten.
- In bevorzugten Ausführungsformen ist das organische Lösungsmittel ausgewählt aus der Gruppe umfassend Ethylencarbonat, Propylencarbonat, Diethylcarbonat, Dimethylcarbonat, Ethylmethylcarbonat, Acetonitril, Glutaronitril, Adiponitril, Pimelonitril, gamma-Butyrolacton, gamma-Valerolacton, Dimethoxyethan, 1,3-Dioxolan, Methylacetat und/oder Mischung davon. Geeignete organische Lösungsmittel sind ausgewählt aus der Gruppe umfassend cyclische Carbonate wie Ethylencarbonat und Propylencarbonat und/oder lineare Carbonate wie Diethylcarbonat, Dimethylcarbonat und Ethylmethylcarbonat. Weitere geeignete organische Lösungsmittel sind ausgewählt aus der Gruppe umfassend gamma-Butyrolacton und/oder gamma-Valerolacton. Vorzugsweise ist das organische Lösungsmittel ausgewählt aus der Gruppe umfassend Ethylencarbonat, Diethylcarbonat, Dimethylcarbonat, Ethylmethylcarbonat, gamma-Butyrolacton, gamma-Valerolacton und/oder deren Mischungen.
- Ein bevorzugtes Lösungsmittel ist Ethylencarbonat. Ethylencarbonat wird gemäß der IUPAC-Nomenklatur auch als 1,3-Dioxolan-2-on bezeichnet . Ethylencarbonat ist kommerziell erhältlich und weist einen hohen Siedepunkt und einen hohen Flammpunkt auf. Weiter vorteilhaft ist, dass Ethylencarbonat eine hohe Leitfähigkeit durch eine gute Salzdissoziation ermöglicht.
- In einer bevorzugten Ausführungsform umfasst das organische Lösungsmittel eine Mischung aus Ethylencarbonat und wenigstens einem weiteren organischen Lösungsmittel, vorzugsweise ausgewählt aus der Gruppe umfassend gamma-Butyrolacton und/oder Diethylcarbonat. Bevorzugt umfasst das organische Lösungsmittel eine Mischung aus Ethylencarbonat und gamma-Butyrolacton. In Lösungsmittelgemischen umfassend Ethylencarbonat und gamma-Butyrolacton konnte in vorteilhafter Weise eine hohe Leitfähigkeit in einem Temperaturbereich von -20°C bis +60°C erreicht werden. Insbesondere können in Lösungsmittelgemischen umfassend gamma-Butyrolacton hohe Leitfähigkeiten in einem Temperaturbereich von -30°C bis +60°C erreicht werden. Geeignet sind beispielsweise binäre Mischungen von Carbonaten, insbesondere von Ethylencarbonat mit einem weiteren Carbonat, beispielsweise Diethylcarbonat, Dimethylcarbonat und/oder Ethylmethylcarbonat, insbesondere Diethylcarbonat.
- Bevorzugt liegt das Verhältnis von Ethylencarbonat und dem wenigstens einen weiteren organischen Lösungsmittel, vorzugsweise gamma-Butyrolacton oder Diethylcarbonat, im Bereich von ≥ 1:99 bis ≤ 99:1, bevorzugt im Bereich von ≥ 1:9 bis ≤ 9:1, vorzugsweise im Bereich von ≥ 3:7 bis ≤ 1:1. Wenn nicht abweichend angegeben bezieht sich das angegebene Verhältnis auf die Gewichtsanteile der Lösungsmittel.
- Bevorzugt sind auch ternäre Mischungen, umfassend wenigstens ein Carbonat als Lösungsmittel. Insbesondere bevorzugt sind Mischungen von Ethylencarbonat mit einem weiteren Lösungsmittel beispielsweise gamma-Butyrolacton oder Diethylcarbonat und einer Verbindung, die geeignet ist, eine sogenannte Solid Electrolyte Interphase (SEI), eine Feststoff-Elektrolyt-Grenzfläche, auszubilden. Der Elektrolyt kann daher ferner Additive, insbesondere filmbildende Elektrolytadditive, umfassen.
- In bevorzugten Ausführungsformen umfasst der Elektrolyt eine Verbindung ausgewählt aus der Gruppe umfassend Chlorethylencarbonat, Fluorethylencarbonat, Vinylethylencarbonat, Ethylensulfit, Ethylensulfat, Propansulfonate, Sulfite, vorzugsweise Dimethylsulfit und Propylensulfit, Sulfate, optional mit F, Cl oder Br substituierte Butyrolactone, Phenylethylencarbonat, Vinylacetat und/oder Trifluorpropylencarbonat.
- Von den Verbindungen auf Carbonat-Basis sind mit Chlor oder Fluor substituierte Carbonate bevorzugt, insbesondere Fluorethylencarbonat (FEC). Die Verbindungen können die Batterieleistung verbessern, beispielsweise die Kapazität oder die Zyklenlebensdauer. Insbesondere Fluorethylencarbonat kann zu einer verbesserten Langzeitstabilität einer Zelle führen.
- Vorzugsweise enthält der Elektrolyt ein Additiv, insbesondere eine Verbindung ausgewählt aus der Gruppe umfassend Chlorethylencarbonat, Fluorethylencarbonat, Vinylethylencarbonat, Ethylensulfit, Ethylensulfat, Propansulfonate, Sulfite, vorzugsweise Dimethylsulfit und Propylensulfit, Sulfate, optional mit F, Cl oder Br substituierte Butyrolactone, Phenylethylencarbonat, Vinylacetat und/oder Trifluorpropylencarbonat, vorzugsweise Fluorethylencarbonat, im Bereich von ≥ 0,1 Gew.-% bis ≤ 10 Gew.-%, bevorzugt im Bereich von ≥ 1 Gew.-% bis ≤ 5 Gew.-%, vorzugsweise im Bereich von ≥ 2 Gew.-% bis ≤ 3 Gew.-%, bezogen auf das Gesamtgewicht des Elektrolyts.
- Bevorzugt umfasst das organische Lösungsmittel eine Mischung aus Ethylencarbonat und wenigstens einem weiteren organischen Lösungsmittel, vorzugsweise ausgewählt aus der Gruppe umfassend gamma-Butyrolacton, gamma-Valerolacton oder Diethylcarbonat und Fluorethylencarbonat.
- Bevorzugt liegt das Verhältnis von Ethylencarbonat und dem wenigstens einen weiteren organischen Lösungsmittel, vorzugsweise ausgewählt aus der Gruppe umfassend gamma-Butyrolacton, gamma-Valerolacton oder Diethylcarbonat, und einem Additiv, vorzugsweise Fluorethylencarbonat, im Bereich von ≥ 98:1:1 bis ≤ 1:1:98, bevorzugt im Bereich von ≥ 80:15:5 bis ≤ 15:80:5, vorzugsweise im Bereich von ≥ 4,5:4,5:1 bis ≤ 1:1:0,01. Wenn nicht abweichend angegeben bezieht sich das angegebene Verhältnis auf die Gewichtsanteile.
- Besonders bevorzugt umfasst das organische Lösungsmittel eine Mischung aus Ethylencarbonat, gamma-Butyrolacton und Fluorethylencarbonat, insbesondere in einem Verhältnis von 4,5:4,5:1. In einem Lösungsmittelgemisch umfassend Ethylencarbonat, gamma-Butyrolacton und Fluorethylencarbonat in einem Verhältnis von 4,5:4,5:1 konnte in vorteilhafter Weise eine gute Leitfähigkeit in einem Temperaturbereich von -20°C bis +60°C erreicht werden.
- Als vielversprechende Lösungsmittel haben sich weiterhin ionische Flüssigkeiten erwiesen, da diese eine hohe thermische wie elektrochemische Stabilität mit einer hohen ionischen Leitfähigkeit vereinen. Insbesondere ist dies vorteilhaft zur Verwendung mit Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat. Bevorzugte ionische Flüssigkeiten umfassen ein Kation ausgewählt aus der Gruppe umfassend 1-Ethyl-3-methylimidazolium (EMI+), 1,2-Dimethyl-3-propylimidazolium (DMPI+), 1,2-Diethyl-3,5-dimethylimidazolium (DEDMI+), Trimethyl-n-hexylammonium (TMHA+), N-alkyl-N-methylpyrrolidinium (PYR1R +), N-alkyl-N-methylpiperidinium (PIP1R +) und/oder N-alkyl-N-methylmorpholinium (MORP1R +) und ein Anion ausgewählt aus der Gruppe umfassend Bis(trifluormethansulfonyl)imid (TFSI-), Bis(pentafluorethansulfonyl)imid (BETI-), Bis(fluorsulfonyl)imid (FSI-), 2,2,2-Trifluor-N-(trifluormethansulfonyl)acetamid (TSAC-), Tetrafluorborat (BF4 -), Pentafluorethanetrifluoroborate (C2F5BF3 -), Hexafluorphosphat (PF6 -) und/oder Tri(pentafluorethan)trifluorphosphat ((C2F5)3PF3 -). Bevorzugte N-alkyl-N-methylpyrrolidinium (PYR1R +) Kationen sind ausgewählt aus der Gruppe umfassend N-butyl-N-methylpyrrolidinium (PYR14 +) und/oder N-methyl-N-propylpyrrolidinium (PYR13 +). Bevorzugte ionische Flüssigkeiten sind ausgewählt aus der Gruppe umfassend N-butyl-N-methylpyrrolidiniumbis(trifluoromethansulfonyl)imid (PYR14TFSI) und/oder N-methyl-N-propylpyrrolidiniumbis(trifluoromethansulfonyl)imid (PYR13TFSI).
- Weitere geeignete Elektrolytmaterialien sind Polymerelektrolyte, wobei der Polymerelektrolyt als Gelpolymerelektrolyt oder fester Polymerelektrolyt vorliegen kann. Feste Polyelektrolyte zeigen gute Eigenschaften bezüglich der Anforderungen an zukünftige Akkumulatorgenerationen. Sie ermöglichen einen solvensfreien Aufbau, der einfach herzustellen und vielfältig in der Form ist. Darüber hinaus kann die Energiedichte gesteigert werden, denn es entfällt der Dreischichtaufbau aus Elektrolyt-Separator-Elektrolyt, sodass lediglich eine dünne Polymerfolie zwischen den Elektroden benötigt wird. Festelektrolyte sind in der Regel chemisch und elektrochemisch stabil gegenüber Elektrodenmaterialien und treten weiterhin nicht aus der Zelle aus. Gelpolymerelektrolyte umfassen meist ein aprotisches Lösungsmittel und eine Polymermatrix.
- Bevorzugte Polymere für feste Polymerelektrolyte und Gelpolymerelektrolyte sind ausgewählt aus der Gruppe umfassend Homo- oder Copolymere von Polyethylenoxid (PEO), Polypropylenoxid (PPO), Polyvinylidenfluorid (PVdF), Polyvinylidenfluoridhexafluorpropylen (PVdF-HFP), Polyacrylnitril (PAN), Polymethylmethacrylat (PMMA), Polyethylmethacrylat (PEMA), Polyvinylacetat (PVAc), Polyvinylchlorid (PVC), Polyphophazene, Polysiloxane, Polyvinylalkohol (PVA) und/oder Homo- und (Block-) Copolymere umfassend funktionelle Seitenketten ausgewählt aus der Gruppe umfassend Ethylenoxid, Propylenoxid, Acrylnitril und/oder Siloxane.
- In bevorzugten Ausführungsformen liegt die Konzentration an Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat im Elektrolyten im Bereich von ≥ 0,1 M bis ≤ 2 M, vorzugsweise im Bereich von ≥ 0,5 M bis ≤ 1,5 M, besonders bevorzugt im Bereich von ≥ 0,7 M bis ≤ 1,2 M. In einer besonders bevorzugten Ausführungsform liegt die Konzentration an Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat im Elektrolyten bei 1 M. In vorteilhafter Weise führen solche Konzentrationen an Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat zu einer guten Leitfähigkeit.
- Ein weiterer Gegenstand der Erfindung betrifft einen Lithium-basierten Energiespeicher, vorzugsweise eine Lithium-Batterie, Lithium-Ionen-Batterie, Lithium-Ionen-Akkumulator, Lithium-Polymer-Batterie oder Lithium-Ionen-Kondensator umfassend Lithium-2-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat. Ein weiterer Gegenstand der Erfindung betrifft einen Lithium-basierten Energiespeicher, vorzugsweise eine Lithium-Batterie, Lithium-Ionen-Batterie, Lithium-Ionen-Akkumulator, Lithium-Polymer-Batterie oder Lithium-Ionen-Kondensator, umfassend einen erfindungsgemäßen Elektrolyten umfassend Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat.
- Die Lithium-basierten Energiespeicher eignen sich für alle Anwendungsgebiete, insbesondere auch für größere Systeme wie Automobile oder als stationäre Energiespeicher für erneuerbare Energien.
- Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat ist nach üblichen Synthesemethoden herstellbar. Bevorzugt ist ein Verfahren zur Herstellung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat, umfassend die folgenden Schritte:
- a) Umsetzung von 1,1,2-Trifluor-2-(trifluormethoxy)ethen mit Sulfuryldifluorid zu 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid, und
- b) Umsetzung von 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid mit Lithiumhydroxid zu Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat.
- Bevorzugt erfolgt die Umsetzung von 1,1,2-Trifluor-2-(trifluormethoxy)ethen, CF3OCF=CF2, mit Sulfuryldifluorid, SO2F2, in Gegenwart von katalytischen Mengen an Tetramethylammoniumfluorid. Die Umsetzung erfolgt vorzugsweise unter Erwärmen, insbesondere bei einer Temperatur im Bereich von 50°C bis 60°C. Die anschließende Hydrolyse von 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid mit Lithiumhydroxid erfolgt vorzugsweise mit ethanolischer Lithiumhydroxidlösung.
- Als Vorstufe erhält man in Schritt a) 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid. In vorteilhafter Weise ist die Umsetzung von 1,1,2-Trifluor-2-(trifluormethoxy)ethen mit Sulfuryldifluorid zu 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid weniger aufwendig und leichter handhabbar als eine aufwendige Umsetzung des schwer handhabbaren und schwer zugänglichen Trifluomethylhypofluorit, CF3OF, mit Trifluorvinylsulfonylfluorid, CF2=CFSO2F. Darüber hinaus kann durch das erfindungsgemäße Verfahren eine größere Ausbeute erzielt werden.
- Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat ist als Leitsalz in einem Elektrolyten umfassend beispielsweise eine ionische Flüssigkeit in Lithium-basierten Energiespeichern verwendbar.
- Ionische Flüssigkeiten sind als nicht-wässrige Elektrolyten insbesondere für elektrochemische Verwendungen beispielsweise in Batterien oder elektrochemischen Kondensatoren verwendbar, jedoch auch für die Elektroplattierung, Katalyse oder chemische Reaktionen. Ionische Flüssigkeiten mit vorzugsweise breitem elektrochemischem Fenster und geringer Hygroskopie sind entsprechend nicht nur für elektrochemische Anwendungen vorteilhaft verwendbar.
- Ein weiterer Gegenstand der Erfindung betrifft eine ionische Flüssigkeit umfassend 1-Trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat und ein organisches Kation ausgewählt aus der Gruppe umfassend Alkylammonium-, Pyridinium-, Pyrazolium-, Pyrrolium-, Pyrrolinium-, Piperidinium-, Pyrrolidinium-, Imidazolium- und/oder Sulfoniumverbindungen. Vorzugsweise ist das organische Kation ausgewählt aus der Gruppe umfassend Alkylammonium-, Pyridinium-, Pyrazolium-, Pyrrolium-, Pyrrolinium-, Piperidinium-, Pyrrolidinium- und/oder Imidazoliumverbindungen, insbesondere Pyrrolidinium- und/oder Imidazoliumverbindungen. Vorzugsweise ist das Kation ausgewählt aus der Gruppe umfassend N-butyl-N-methylpyrrolidinium (PYR14), N-methyl-N-propylpyrrolidinium (PYR13), 1-Ethyl-3-methylimidazolium (EMIM), 1-Ethyl-2,3-dimethylimidazolium (EDiMIM) und/oder 1-Butyl-3-methylimidazolium (BMIM).
- Ionische Flüssigkeiten umfassend 1-Trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat als Anion und ein organisches Kation können in vorteilhafter Weise für elektrochemische Anwendungen Verwendung finden, beispielsweise in Kombination mit einem Lithiumsalz in Lithium-basierten Energiespeichern. Weiterhin sind Verwendungen in Solarzellen oder Brennstoffzellen vorteilhaft. In vorteilhafter Weise sind ionische Flüssigkeiten umfassend fluorierte Anionen auch als Hydraulikflüssigkeit oder inerte flüssige Verdünnungsmittel für hochreaktive Chemikalien verwendbar.
- Beispiele und Figuren, die der Veranschaulichung der vorliegenden Erfindung dienen, sind nachstehend angegeben.
- Hierbei zeigen die Figuren:
- Figur 1
- zeigt die Leitfähigkeit einer 1 M Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in verschiedenen Lösungsmittelgemischen in Abhängigkeit von der Temperatur.
- Figur 2
- zeigt das elektrochemische Stabilitätsfenster einer 1 M Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in einem Lösungsmittelgemisch aus Ethylencarbonat und Diethylcarbonat (EC:DEC) im Verhältnis 1:1 und von LiPF6 in EC:DEC im Verhältnis 3:7. Aufgetragen ist die Stromdichte gegen das Potential.
- Figur 3
- zeigt die Entladekapazität einer Lithium-Ionen Halbzelle mit 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in einem Lösungsmittelgemisch aus Ethylencarbonat und Diethylcarbonat (EC:DEC) im Verhältnis 1:1 und Graphit als Arbeitselektrode im Vergleich zu LiPF6. Aufgetragen ist die Entladekapazität gegen die Zyklenzahl.
- Figur 4
- zeigt die Entladekapazität und die Effizienz einer Lithium-Ionen Halbzelle mit 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in einem Lösungsmittelgemisch aus Ethylencarbonat und Diethylcarbonat (EC:DEC) im Verhältnis 1:1. Als Arbeitselektrode diente das Kathodenmaterial Nickel-Mangan-Kobaltoxid. Aufgetragen ist die Entladekapazität gegen die Zyklenzahl.
- Figur 5
- zeigt die zyklische Voltammetrie einer 1 M Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in einem Lösungsmittelgemisch aus Ethylencarbonat und Diethylcarbonat (EC:DEC) im Verhältnis 1:1 auf einer Graphitanode für drei Zyklen (1), (2) und (3).
- Figur 6
- zeigt die Zerfallsprodukte der thermischen Alterung bei 95°C einer 1 M Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in Ethylencarbonat und Diethylcarbonat (EC:DEC) im Verhältnis 1:1 im Vergleich zu LiPF6 in EC:DEC im Verhältnis 3:7.
- Herstellung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat
- a) Herstellung von 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid 10 mg Tetramethylammoniumfluorid (ABCR) wurden in 10 ml trockenem Bis(2-methoxyethyl)ether (Diglyme, ABCR) suspendiert. Bei -197°C wurden 36 mmol Sulfuryldifluorid (ABCR) und 36 mmol 1,1,2-Trifluor-2-(trifluormethoxy)ethen (ABCR) aufkondensiert. Das Reaktionsgemisch wurde für 12 h auf 60°C erwärmt und anschließend das Produkt destilliert. 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid wurde als farblose Flüssigkeit in einer Ausbeute von 92 % erhalten.
- b) Herstellung von Lithium-1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonat 20 mmol des in Schritt a) hergestellten 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorids wurden in 10 ml Ethanol (ROTH) gelöst. Bei 0°C wurden 40 mmol Lithiumhydroxid (ROTH) zugegeben. Die Suspension wurde 2 h bei Raumtemperatur (20±3°C) gerührt, dann 15 min zentrifugiert und die flüssige Phase abdekantiert. Das Lösungsmittel wurde abgezogen und das Produkt im Vakuum (0,001mm) bei 60°C 6 h getrocknet. Die Ausbeute betrug 65 %.
- Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat wurde vor Gebrauch für 24 Stunden bei 60 °C getrocknet.
- Die Leitfähigkeit von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat wurde in unterschiedlichen Lösungsmitteln in einem Temperaturbereich von - 40°C bis + 60°C bestimmt.
- Mischungen von 50 Gew.-% Ethylencarbonat (EC) (Ferro Corporation, Batteriegrad) und 50 Gew.-% Diethylcarbonat (DEC) (Ferro Corporation, Batteriegrad) (EC:DEC, 1:1), von 50 Gew.-% Ethylencarbonat und 50 Gew.-% gamma-Butyrolacton (γBL) (Ferro Corporation, Batterygrade) (EC: γBL, 1:1), und von 45 Gew.-% Ethylencarbonat, 45 Gew.-% gamma-Butyrolacton und 10 Gew.-% Fluoroethylencarbonat (Solvay GmbH) (EC: γBL:FEC, 4,5:4,5:1) wurden vorgelegt. In diesen Lösungsmittelgemischen wurden pro Milliliter 217 mg des gemäß Beispiel 1 hergestellten Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonats gelöst, so dass sich eine Konzentration von 1 M ergab. Zum Vergleich wurde eine 1 M-Lösung von LiPF6 (Sigma-Aldrich, Batteriegrad) in einem Gemisch von 30 Gew.-% Ethylencarbonat und 70 Gew.-% Diethylcarbonat (EC:DEC, 3:7) hergestellt.
- Die Leitfähigkeit der Elektrolyten wurde unter Verwendung von Platin-Leitfähigkeitsmesszellen (Amel Glassware, Zellkonstante 1 cm-1) mit einem Potentiostaten (Solartron 1287A) in Verbindung mit einer Impedanzmesseinheit (Solartron 1260) in einem Temperaturbereich von - 40°C bis + 60°C (Klimaschrank, Binder MK53) untersucht. Hierzu wurden die Leitfähigkeitsmesszellen zunächst auf 60°C erwärmt und dann in Temperaturintervallen von 5°C auf -40°C gekühlt.
- Die
Figur 1 zeigt den Verlauf der Leitfähigkeit der 1 M Lösungen von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in den verschiedenen Lösungsmittelgemischen im Temperaturbereich von -40°C bis +60°C sowie die von LiPF6. Wie man derFigur 1 entnehmen kann, war die Leitfähigkeit in den Lösungsmittelgemischen Ethylencarbonat und gamma-Butyrolacton (EC: γBL, 1:1) und Ethylencarbonat, gamma-Butyrolacton und Fluoroethylencarbonat (EC:γBL:FEC) im Temperaturbereich von - 40°C bis + 0°C deutlich höher gegenüber der Leitfähigkeit in Ethylencarbonat und Diethylcarbonat (EC:DEC, 1:1) und erreichte über den gesamten Temperaturbereich nahezu die Leitfähigkeit von LiPF6 in einem Ethylencarbonat und Diethylcarbonat (EC:DEC, 3:7). - Die Leitfähigkeit von 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat bei 25°C betrug in den verschiedenen Lösungsmittelgemischen für ein 1:1-Gemisch Ethylencarbonat und Diethylcarbonat (EC:DEC 1:1) 1,8 mS cm-1, für ein 1:1-Gemisch Ethylencarbonat und gamma-Butyrolacton (EC: γBL, 1:1) 3,7 mS cm-1 und für ein Gemisch Ethylencarbonat, gamma-Butyrolacton und Fluoroethylencarbonat (EC:γBL:FEC) im Verhältnis 4,5:4,5:1 3,5 mS cm-1.
- Dies zeigt, dass Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in den üblichen Carbonat-Lösungsmitteln eine ausreichende Leitfähigkeit bei 25°C aufweist.
- Die elektrochemische Stabilität einer 1 M-Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat hergestellt gemäß Beispiel 1 in einem Lösungsmittelgemisch aus 50 Gew.-% Ethylencarbonat und 50 Gew.-% Diethylcarbonat (EC:DEC, 1:1) gegenüber der Stabilität einer 1 M-Lösung von LiPF6 (Sigma-Aldrich, Batteriegrad) in einem Gemisch von 30 Gew.-% Ethylencarbonat und 70 Gew.-% Diethylcarbonat (EC:DEC, 3:7) wurde mittels der sogenannten Linear Sweep-Voltammetrie (LSV) bestimmt. Bei diesem Verfahren erfolgt eine kontinuierliche Änderung der Elektrodenspannung (linear sweep).
- Als kathodisches Stabilitätslimit, das Potential, bei welchem eine Reduktion einsetzt, wurde jenes Potential definiert, bei welchem die Stromdichte - 0,1 mA cm-2 unterschritt. Als anodisches Stabilitätslimit, das Potential, bei welchem eine Oxidation einsetzt, wurde jenes Potential definiert, bei welchem die Stromdichte + 0,1 mA cm-2 überschritt. Insbesondere die anodische Stabilität hängt entscheidend von der Stabilität des verwendeten Elektrolyten ab.
- Die Versuche wurden in einer 3-Elektrodenanordnung in modifizierte Swagelok®-T-Stücke (Rohrverbinder, Edelstahlkörper) mit einer Platinelektrode (eDAQ, Modell ET075, 1 mm Durchmesser) als Arbeitselektrode und Lithiumfolie (12 mm bzw. 7 mm Durchmesser, Chemetall) als Gegen- und Referenzelektrode durchgeführt. Dazu wurde der Zellkörper mit einer einseitig silikonierten Polyester-Folie (Mylar®, PPI-SP 914, 100 µm) ausgekleidet und die Elektroden in den Zellkörper eingeführt. Die Elektroden wurden mit einem Vlies (Freudenberg®, FS2226E, 6 Lagen) separiert, welches mit dem entsprechenden Elektrolyten getränkt war. Die Vorschubgeschwindigkeit betrug 1 mV s-1.
- Wie in
Figur 2 gezeigt ist, wurde bei dem Elektrolyten 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in einer 1:1 Mischung von Ethylencarbonat und Diethylcarbonat das kathodische Stabilitätslimit bei 0,03 V erreicht. Die anodische Stabilität von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat betrug 5,7 V und ist völlig ausreichend für eine Verwendung des Elektrolyten in Kombination mit Hochvoltkathodenmaterialien. - Dieses Ergebnis zeigt, dass Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in den üblichen Carbonat-Lösungsmitteln eine für sämtliche elektrochemischen Anwendungen ausreichend gute elektrochemischen Stabilität aufweist.
- Das Zyklisierverhalten einer 1 M-Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat hergestellt gemäß Beispiel 1 wurde in einem Gemisch von 50 Gew.-% Ethylencarbonat und 50 Gew.-% Diethylcarbonat (EC:DEC, 1:1) gegenüber der Zyklisierung einer 1 M-Lösung von LiPF6 in einem Gemisch von 30 Gew.-% Ethylencarbonat und 70 Gew.-% Diethylcarbonat (EC:DEC, 3:7) bestimmt.
- Die Versuche wurden in einer 3-Elektrodenanordnung in modifizierte Swagelok®-T-Stücke (Rohrverbinder, Edelstahlkörper) mit einer Graphitelektrode (Timcal T44 Graphitmaterial) als Arbeitselektrode und Lithiumfolie (12 mm bzw. 5 mm Durchmesser, Chemetall) als Gegen- und Referenzelektrode durchgeführt. Dazu wurde der Zellkörper mit einer einseitig silikonierten Polyester-Folie (Mylar®, PPI-SP 914, 100 µm) ausgekleidet und die Elektroden in den Zellkörper eingeführt. Die Elektroden wurden mit einem Vlies (Freudenberg®, FS2226E, 6 Lagen) separiert, welches mit dem entsprechenden Elektrolyten getränkt war.
- Der Test zum Zyklisierverhalten umfasste mehrere Phasen. In der ersten Phase wurde die Formierung des Graphits (SEI Formation) durch drei Zyklen mit einer Konstantstrom C-Rate von C/5 sichergestellt. Im Anschluss wurde in der zweiten Phase über 20 Zyklen das Zyklisierverhalten bei einer Lade- und Entladerate von 1C überprüft. Dabei wurde das Zellsystem nach dem Laden für eine Stunde bei einer Spannung von 0,025 V gehalten. In der dritten Phase wurde der Graphit immer mit C/2 geladen und im Anschluss für eine Stunde bei 0,025 V gehalten bevor der Graphit mit unterschiedlichen Geschwindigkeiten entladen wurde. Die angewendeten D-Raten (Entladeraten) waren dabei D/5, D/3; D/2, 1D, 2D, 3D, 5D und 10D. Dem D-Ratentest folgten fünf Zyklen mit Lade- und Entladeraten von C/5, um zu überprüfen ob der Graphit durch den Belastungstest Schaden genommen hatte. Die letzte Phase beinhaltete die gleichen Zyklisierparameter wie Phase 2 und wurde für 30 Zyklen durchgeführt.
- In der
Figur 3 sind die Entladekapazität bzw. Lithiumauslagerungskapazität der 1 M-Lösungen von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat und LiPF6 gegen die Zyklenzahl der mit einer C-Rate von 1C geladenen Lithiumionen-Batteriehalbzelle dargestellt. Wie dieFigur 3 zeigt, wies die Halbzelle mit 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat nach dem Formieren der Zelle eine Anfangskapazität von ca. 373 mAh g-1 auf, die mit der Anzahl der Zyklen auf ca. 374 mAh g-1 im 15. Zyklus stieg. Dies zeigt die hervorragende Zyklenstabilität der Zelle, die der von LiPF6 entspricht. - Das Zyklisierverhalten auf NCM-Kathoden in einer Halbzelle wurde wie in Beispiel 4 dargestellt in einer 3-Elektrodenanordnung durchgeführt, wobei eine Nickel-Cobalt-Manganoxid-Elektrode (NCM-Elektrode, Toda Kogyo Europe GmbH) als Arbeitselektrode und Lithiumfolie (12 mm bzw. 5 mm Durchmesser, Chemetall) als Gegen- und Referenzelektrode verwendet wurde. Hierbei wurde eine 1 M-Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat hergestellt gemäß Beispiel 1 in einem Gemisch von 50 Gew.-% Ethylencarbonat und 50 Gew.-% Diethylcarbonat (EC:DEC, 1:1) verwendet.
- Die
Figur 4 zeigt die Entladekapazität bzw. Lithiumeinlagerungskapazität und die Effizienz der Lithium-Ionen Halbzelle. Aufgetragen ist die Ladekapazität und die Effizienz gegen die Zyklenzahl. Wie dieFigur 4 zeigt, wies die Halbzelle mit 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat eine Anfangskapazität von ca. 138 mAh g-1 nach dem erfolgreich bestandenen Stromraten-Belastungstest (C-Ratentest) der Zelle (I) auf. Nach der nachfolgenden Zyklisierung (II) lag die Kapazität im 80. Zyklus noch bei ca. 137 mAh g-1. Weiterhin stieg die Effizienz der Zelle nach 2 Standardzyklen auf über 99,6 % einer maximalen Effizienz von 100 %. Somit konnte festgestellt werden, dass die Zelle auch mit NCM-Kathode eine hervorragende Zyklenstabilität zeigte. - Die zyklische Voltammetrie einer 1 M-Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat hergestellt gemäß Beispiel 1 wurde in einem Gemisch von 50 Gew.-% Ethylencarbonat und 50 Gew.-% Diethylcarbonat (EC:DEC, 1:1) durchgeführt.
- Die Versuche wurden in einer 3-Elektrodenanordnung in modifizierte Swagelok®-T-Stücke (Rohrverbinder, Edelstahlkörper) mit einer Graphitelektrode (Timcal T44 Graphitmaterial) als Arbeitselektrode und Lithiumfolie (12 mm bzw. 4 mm Durchmesser, Chemetall) als Gegen- und Referenzelektrode durchgeführt. Dazu wurde der Zellkörper mit einer einseitig silikonierten Polyester-Folie (Mylar®, PPI-SP 914, 100 µm) ausgekleidet und die Elektroden in den Zellkörper eingeführt. Die Elektroden wurden mit einem Vlies (Freudenberg®, FS2226E, 6 Lagen) separiert, welches mit dem entsprechenden Elektrolyten getränkt war.
- Die
Figur 5 zeigt die Ergebnisse der zyklischen Voltammetrie für drei Zyklen (1), (2) und (3). In derFigur 5 sind die durch die erhöhte Stromdichte identifizierbaren Interkalations- und Deinterkalationsphasen in den jeweiligen Zyklen im Bereich zwischen 0 und 0,3 V erkennbar. Dies belegt die Reversibilität des Systems. - Der vergrößerte Ausschnitt des Bereichs von 0,5 V bis 1 V zeigt die Bildung der Solid Electrolyte Interphase (SEI) des Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat-Carbonat Elektrolyten. Im Vergleich dazu ist das Entstehungspotential der SEI für eine 1 M-Lösung von LiPF6 in einem Gemisch von 30 Gew.-% Ethylencarbonat und 70 Gew.-% Diethylcarbonat (EC:DEC, 3:7) gezeigt.
- Die Zerfallsprodukte einer 1 M-Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat hergestellt gemäß Beispiel 1 in einem Gemisch von 50 Gew.-% Ethylencarbonat und 50 Gew.-% Diethylcarbonat (EC:DEC, 1:1) wurden gegenüber den Zerfallsprodukten einer 1 M-Lösung von LiPF6 (Sigma-Aldrich, Batteriegrad) in einem Gemisch von 30 Gew.-% Ethylencarbonat und 70 Gew.-% Diethylcarbonat (EC:DEC, 3:7) bestimmt.
- Die Elektrolyte wurden in einer Klimakammer für zwei Wochen bei 95 °C gelagert und im Anschluss mittels einer Gaschromatographie-Massenspektrometrie (Clarus 600 GC von Perkin Elmer) untersucht.
-
Figur 6 zeigt die Zerfallsprodukte der thermischen Alterung bei 95°C einer 1 M Lösung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat (LiB-8) in Ethylencarbonat und Diethylcarbonat (EC:DEC) im Verhältnis 1:1 im Vergleich zu 1 M LiPF6 in EC:DEC im Verhältnis 3:7. Wie dieFigur 6 zeigt, wurden für den Elektrolyten 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat in EC:DEC mittels der GC-MS keine Carbonatzersetzungsprodukte in dem thermisch gealtertem Elektrolyten gefunden. Demgegenüber wurden für den Elektrolyten 1 M LiPF6 in EC:DEC anhand der Signale zwischen 2,5 min und 3,5 min Carbonat-Zersetzungsprodukte detektiert. Das Signal nach 12 min ist Diethylcarbonat zuzuordnen. Dies zeigt, dass die thermische Stabilität von 1 M Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat die Stabilität des LiPF6 Elektrolyten überstieg. - Diese Ergebnisse zeigen insgesamt, dass Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat eine Möglichkeit bietet, LiPF6 als Leitsalz in Lithium-Ionen Batterien zu ersetzen.
Claims (10)
- Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat.
- Verwendung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat als Leitsalz in Lithium-basierten Energiespeichern.
- Elektrolyt für einen Lithium-basierten Energiespeicher umfassend Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat.
- Elektrolyt nach Anspruch 3, dadurch gekennzeichnet, dass der Elektrolyt ein organisches Lösungsmittel, eine ionische Flüssigkeit und/oder eine Polymermatrix umfasst.
- Elektrolyt nach Anspruch 3 oder 4, dadurch gekennzeichnet, dass das organische Lösungsmittel ausgewählt ist aus der Gruppe umfassend Ethylencarbonat, Propylencarbonat, Diethylcarbonat, Dimethylcarbonat, Ethylmethylcarbonat, Acetonitril, Glutaronitril, Adiponitril, Pimelonitril, gamma-Butyrolacton, gamma-Valerolacton, Dimethoxyethan, 1,3-Dioxolan, Methylacetat und/oder Mischung davon, vorzugsweise aus der Gruppe umfassend Ethylencarbonat, Diethylcarbonat, Dimethylcarbonat und/oder deren Mischungen.
- Elektrolyt nach einem der Ansprüche 3 bis 5, dadurch gekennzeichnet, dass das organische Lösungsmittel eine Mischung aus Ethylencarbonat und wenigstens einem weiteren organischen Lösungsmittel vorzugsweise ausgewählt aus der Gruppe umfassend gamma-Butyrolacton und/oder Diethylcarbonat umfasst, bevorzugt im Verhältnis im Bereich von ≥ 1:99 bis ≤ 99:1, bevorzugt im Bereich von ≥ 1:9 bis ≤ 9:1, vorzugsweise im Bereich von ≥ 3:7 bis ≤ 1:1.
- Elektrolyt nach einem der Ansprüche 3 bis 6 , dadurch gekennzeichnet, dass die Konzentration von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat im Elektrolyten im Bereich von ≥ 0,1 M bis ≤ 2 M, vorzugsweise im Bereich von ≥ 0,5 M bis ≤ 1,5 M, besonders bevorzugt im Bereich von ≥ 0,7 M bis ≤ 1,2 M, liegt.
- Lithium-basierter Energiespeicher, vorzugsweise Lithium-Batterie, Lithium-Ionen-Batterie, Lithium-Ionen-Akkumulator, Lithium-Polymer-Batterie oder Lithium-Ionen-Kondensator, umfassend Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat.
- Verfahren zur Herstellung von Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat, umfassend die folgenden Schritte:a) Umsetzung von 1,1,2-Trifluor-2-(trifluormethoxy)ethen mit Sulfuryldifluorid zu 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid, undb) Umsetzung von 1,2,2,2-Tetrafluor-1-(trifluormethoxy)-ethansulfonylfluorid mit Lithiumhydroxid zu Lithium-1-trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat.
- Ionische Flüssigkeit umfassend 1-Trifluormethoxy-1,2,2,2-tetrafluor-ethansulfonat und ein organisches Kation ausgewählt aus der Gruppe umfassend Alkylammonium-, Pyridinium-, Pyrazolium-, Pyrrolium-, Pyrrolinium-, Piperidinium-, Pyrrolidinium-, Imidazolium- und/oder Sulfoniumverbindungen, wobei das Kation vorzugsweise ausgewählt ist aus der Gruppe umfassend N-butyl-N-methylpyrrolidinium, N-methyl-N-propylpyrrolidinium, 1-Ethyl-3-methylimidazolium, 1-Ethyl-2,3-dimethylimidazolium und/oder 1-Butyl-3-methylimidazolium.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102012101670A DE102012101670A1 (de) | 2012-02-29 | 2012-02-29 | Leitsalz für Lithium-basierte Energiespeicher |
| PCT/EP2013/053949 WO2013127866A1 (de) | 2012-02-29 | 2013-02-27 | Leitsalz für lithium-basierte energiespeicher |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP2819951A1 EP2819951A1 (de) | 2015-01-07 |
| EP2819951B1 true EP2819951B1 (de) | 2016-08-03 |
Family
ID=47749878
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP13706047.1A Active EP2819951B1 (de) | 2012-02-29 | 2013-02-27 | Leitsalz für lithium-basierte energiespeicher |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9843074B2 (de) |
| EP (1) | EP2819951B1 (de) |
| DE (1) | DE102012101670A1 (de) |
| WO (1) | WO2013127866A1 (de) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20170046698A (ko) * | 2014-08-29 | 2017-05-02 | 고쿠리츠켄큐카이하츠호진 상교기쥬츠 소고켄큐쇼 | 이온 액체 및 유점성 결정 |
| JP6018146B2 (ja) * | 2014-09-19 | 2016-11-02 | トヨタ自動車株式会社 | フッ化物イオン電池用電解液およびフッ化物イオン電池 |
| DE102014222372A1 (de) * | 2014-11-03 | 2016-05-04 | Bayerische Motoren Werke Aktiengesellschaft | Elektrolyt für Lithium-basierte Energiespeicher |
| EP3353844B1 (de) | 2015-03-27 | 2022-05-11 | Mason K. Harrup | Vollständig anorganische lösungsmittel für elektrolyte |
| CA3019132A1 (en) | 2016-04-01 | 2017-10-05 | NOHMs Technologies, Inc. | Modified ionic liquids containing phosphorus |
| US10707531B1 (en) | 2016-09-27 | 2020-07-07 | New Dominion Enterprises Inc. | All-inorganic solvents for electrolytes |
| CN118472388A (zh) * | 2017-06-01 | 2024-08-09 | 株式会社Lg新能源 | 电解质组合物和二次电池 |
| JP7296893B2 (ja) | 2017-07-17 | 2023-06-23 | ノームズ テクノロジーズ インコーポレイテッド | リン含有電解質 |
| FR3073982B1 (fr) * | 2017-11-20 | 2019-12-13 | Blue Solutions | Utilisation d'un melange de sels a titre d'additif dans une batterie au lithium gelifiee |
| DE102018116475B4 (de) * | 2018-07-06 | 2020-11-05 | Forschungszentrum Jülich GmbH | Elektrolyt umfassend wenigstens ein Lithiumsalz sowie Lithium-Sekundärbatterie |
| CN110935286B (zh) * | 2020-01-16 | 2022-03-01 | 浙江工业大学 | 一种利用离子液体复合生物基溶剂吸收残留熏蒸剂硫酰氟的方法 |
| US20220255133A1 (en) * | 2021-02-03 | 2022-08-11 | Kabushiki Kaisha Toshiba | Nonaqueous electrolyte, secondary battery, battery pack, vehicle, and stationary power supply |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1246357B (it) * | 1990-07-12 | 1994-11-17 | Ausimont Spa | Processo per la preparazione di composti perfluoroalcossisolfonici |
| DE19619233A1 (de) * | 1996-05-13 | 1997-11-20 | Hoechst Ag | Fluorhaltige Lösungsmittel für Lithiumbatterien mit erhöhter Sicherheit |
| DE19829030C1 (de) | 1998-06-30 | 1999-10-07 | Metallgesellschaft Ag | Lithium-bisoxalatoborat, Verfahren zu dessen Herstellung und dessen Verwendung |
| JP4085481B2 (ja) * | 1998-08-31 | 2008-05-14 | ソニー株式会社 | 電池 |
| US6855476B2 (en) * | 2001-04-05 | 2005-02-15 | Arch Specialty Chemicals, Inc. | Photoacid generators for use in photoresist compositions |
| US7834209B2 (en) * | 2005-06-07 | 2010-11-16 | E.I. Du Pont De Nemours And Company | Hydrofluoroalkanesulfonic acids from fluorovinyl ethers |
| US7544813B2 (en) * | 2005-09-22 | 2009-06-09 | E.I. Du Pont De Nemours And Company | Ionic liquids |
-
2012
- 2012-02-29 DE DE102012101670A patent/DE102012101670A1/de not_active Withdrawn
-
2013
- 2013-02-27 WO PCT/EP2013/053949 patent/WO2013127866A1/de active Application Filing
- 2013-02-27 EP EP13706047.1A patent/EP2819951B1/de active Active
- 2013-02-27 US US14/379,524 patent/US9843074B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2013127866A1 (de) | 2013-09-06 |
| DE102012101670A1 (de) | 2013-08-29 |
| US9843074B2 (en) | 2017-12-12 |
| EP2819951A1 (de) | 2015-01-07 |
| US20150044573A1 (en) | 2015-02-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2819951B1 (de) | Leitsalz für lithium-basierte energiespeicher | |
| EP2737568B1 (de) | Lithium-2-methoxy-1,1,2,2-tetrafluor-ethansulfonat und dessen verwendung als leitsalz in lithium-basierten energiespeichern | |
| EP2274291B1 (de) | Reaktive ionische flüssigkeiten | |
| EP3583653B1 (de) | Elektrolyt-zusatz für lithium-ionen-batterien | |
| DE102005029124A1 (de) | Filmbildner freies Elektrolyt-Separator-System sowie dessen Verwendung in elektrochemischen Energiespeichern | |
| EP2740178B1 (de) | Elektrolyt für lithium-basierte energiespeicher | |
| EP2820711B1 (de) | Leitsalz für lithium-basierte energiespeicher | |
| DE102016221172A1 (de) | Optimierter Hybridsuperkondensator | |
| EP1236732B1 (de) | Fluoralkylphosphat-Salze und Verfahren zur Herstellung dieser Substanzen | |
| WO2013135824A2 (de) | Ionenleitende polymere verbindung für elektrochemische zellen | |
| WO2018229109A1 (de) | Elektrolyt für lithium-ionen-batterien | |
| DE102014108012B4 (de) | Substituierte Pyrazole und deren Verwendung als Leitsalz für Lithium-basierte Energiespeicher | |
| DE102011055028A1 (de) | Elektrolyt-Zusatz für Lithium-basierte Energiespeicher | |
| DE102018105613A1 (de) | Elektrolyt-Zusatz für Lithium-Ionen-Batterien | |
| DE102017107257A1 (de) | Elektrolyt-Zusatz für Lithium-Ionen-Batterien | |
| DE102017103334A1 (de) | Elektrolyt-Zusatz für Lithium-Ionen-Batterien | |
| EP3427317A1 (de) | Verwendung von trialkylsiloxy-basierten metallkomplexen als additiv in lithium-ionen-batterien | |
| EP3560023B1 (de) | Elektrolyt für lithium-ionen-batterien | |
| DE102012104567A1 (de) | Lösungsmittel für Elektrolyte für Lithium-basierte Energiespeicher | |
| EP2975684B1 (de) | Elektrolytsystem für den einsatz in elektrochemischen bauteilen | |
| DE102018114146A1 (de) | Hybrider Elektrolyt für wässrige Lithium-Ionen-Batterien | |
| DE102017012022A1 (de) | AI(TFSI)3 als Additiv und Leitsalz für elektrochemische Doppelschichtkondensatoren und Hybridspeichersysteme | |
| DE102016125323A1 (de) | Elektrolyt für Lithium-Ionen-Batterien | |
| DE102017107253A1 (de) | Elektrolyt für Lithium-Ionen-Batterien | |
| DE102015201077A1 (de) | Elektrolyt für Lithium-basierte Energiespeicher |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 20140827 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): AL AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HR HU IE IS IT LI LT LU LV MC MK MT NL NO PL PT RO RS SE SI SK SM TR |
|
| AX | Request for extension of the european patent |
Extension state: BA ME |
|
| RIN1 | Information on inventor provided before grant (corrected) |
Inventor name: KALINOVICH, NATALIYA Inventor name: SCHREINER, CHRISTIAN Inventor name: MUELLER, ROMEK ANSGAR Inventor name: SCHMITZ, RENE Inventor name: LEX-BALDUCCI, ALEXANDRA Inventor name: PASSERINI, STEFANO Inventor name: WINTER, MARTIN Inventor name: SCHMITZ, RAPHAEL WILHELM Inventor name: VLASOV, KATJA Inventor name: KUNZE, MIRIAM Inventor name: ROESCHENTHALER, GERD-VOLKER Inventor name: SCHEDLBAUER, TANJA |
|
| DAX | Request for extension of the european patent (deleted) | ||
| GRAP | Despatch of communication of intention to grant a patent |
Free format text: ORIGINAL CODE: EPIDOSNIGR1 |
|
| RIC1 | Information provided on ipc code assigned before grant |
Ipc: C01D 15/00 20060101AFI20150930BHEP Ipc: H01M 10/0568 20100101ALI20150930BHEP Ipc: H01M 10/052 20100101ALI20150930BHEP Ipc: C07C 309/10 20060101ALI20150930BHEP Ipc: H01G 11/60 20130101ALN20150930BHEP Ipc: H01G 11/06 20130101ALN20150930BHEP Ipc: H01G 11/62 20130101ALI20150930BHEP |
|
| INTG | Intention to grant announced |
Effective date: 20151028 |
|
| GRAS | Grant fee paid |
Free format text: ORIGINAL CODE: EPIDOSNIGR3 |
|
| GRAP | Despatch of communication of intention to grant a patent |
Free format text: ORIGINAL CODE: EPIDOSNIGR1 |
|
| RIC1 | Information provided on ipc code assigned before grant |
Ipc: H01M 10/052 20100101ALI20160225BHEP Ipc: H01M 10/0568 20100101ALI20160225BHEP Ipc: C01D 15/00 20060101AFI20160225BHEP Ipc: H01G 11/06 20130101ALN20160225BHEP Ipc: H01G 11/62 20130101ALI20160225BHEP Ipc: C07C 309/10 20060101ALI20160225BHEP Ipc: H01G 11/60 20130101ALN20160225BHEP |
|
| INTG | Intention to grant announced |
Effective date: 20160329 |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): AL AT BE BG CH CY CZ DE DK EE ES FI FR GB GR HR HU IE IS IT LI LT LU LV MC MK MT NL NO PL PT RO RS SE SI SK SM TR |
|
| REG | Reference to a national code |
Ref country code: GB Ref legal event code: FG4D Free format text: NOT ENGLISH |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: EP Ref country code: AT Ref legal event code: REF Ref document number: 817208 Country of ref document: AT Kind code of ref document: T Effective date: 20160815 |
|
| REG | Reference to a national code |
Ref country code: IE Ref legal event code: FG4D Free format text: LANGUAGE OF EP DOCUMENT: GERMAN |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R096 Ref document number: 502013003929 Country of ref document: DE |
|
| REG | Reference to a national code |
Ref country code: NL Ref legal event code: MP Effective date: 20160803 |
|
| REG | Reference to a national code |
Ref country code: LT Ref legal event code: MG4D |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NO Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20161103 Ref country code: LT Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: NL Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: RS Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: FI Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: IS Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20161203 Ref country code: IT Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: HR Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: PL Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: LV Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: ES Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: GR Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20161104 Ref country code: PT Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20161205 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: RO Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: EE Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R097 Ref document number: 502013003929 Country of ref document: DE |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CZ Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: BE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170228 Ref country code: BG Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20161103 Ref country code: DK Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: SK Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 Ref country code: SM Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed |
Effective date: 20170504 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SI Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: MC Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 20170227 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CH Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170228 Ref country code: LI Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170228 |
|
| REG | Reference to a national code |
Ref country code: IE Ref legal event code: MM4A |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST Effective date: 20171031 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: LU Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170227 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170228 |
|
| REG | Reference to a national code |
Ref country code: BE Ref legal event code: MM Effective date: 20170228 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170227 Ref country code: IE Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20170227 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: MT Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: AL Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| REG | Reference to a national code |
Ref country code: AT Ref legal event code: MM01 Ref document number: 817208 Country of ref document: AT Kind code of ref document: T Effective date: 20180227 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: AT Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 20180227 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: HU Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT; INVALID AB INITIO Effective date: 20130227 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CY Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: MK Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: TR Free format text: LAPSE BECAUSE OF FAILURE TO SUBMIT A TRANSLATION OF THE DESCRIPTION OR TO PAY THE FEE WITHIN THE PRESCRIBED TIME-LIMIT Effective date: 20160803 |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R082 Ref document number: 502013003929 Country of ref document: DE Representative=s name: WEIDNER STERN JESCHKE PATENTANWAELTE PARTNERSC, DE |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R081 Ref document number: 502013003929 Country of ref document: DE Owner name: CONSTRUCTOR UNIVERSITY BREMEN GGMBH, DE Free format text: FORMER OWNERS: JACOBS UNIVERSITY BREMEN GGMBH, 28759 BREMEN, DE; WESTFAELISCHE WILHELMS-UNIVERSITAET MUENSTER, 48149 MUENSTER, DE Ref country code: DE Ref legal event code: R081 Ref document number: 502013003929 Country of ref document: DE Owner name: JACOBS UNIVERSITY BREMEN GGMBH, DE Free format text: FORMER OWNERS: JACOBS UNIVERSITY BREMEN GGMBH, 28759 BREMEN, DE; WESTFAELISCHE WILHELMS-UNIVERSITAET MUENSTER, 48149 MUENSTER, DE |
|
| REG | Reference to a national code |
Ref country code: DE Ref legal event code: R081 Ref document number: 502013003929 Country of ref document: DE Owner name: CONSTRUCTOR UNIVERSITY BREMEN GGMBH, DE Free format text: FORMER OWNER: JACOBS UNIVERSITY BREMEN GGMBH, 28759 BREMEN, DE |
|
| P01 | Opt-out of the competence of the unified patent court (upc) registered |
Effective date: 20230601 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 20231206 Year of fee payment: 12 |