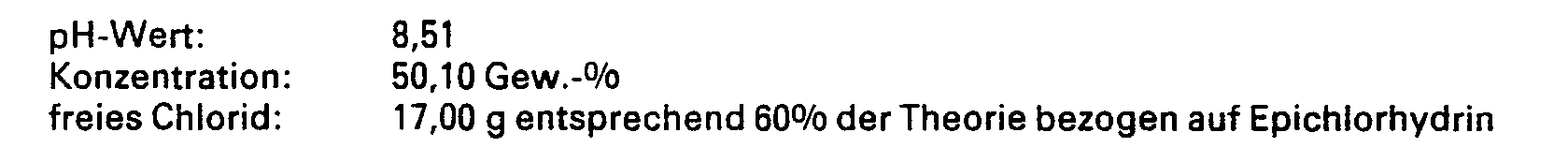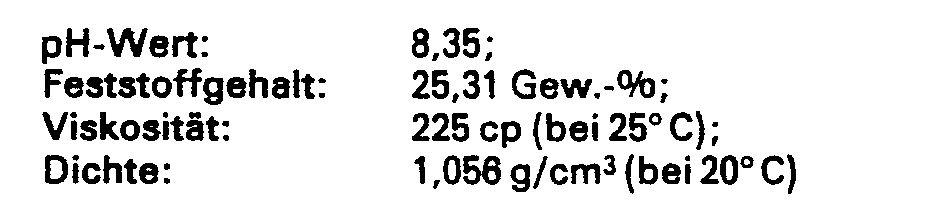EP0000714B1 - Auxiliary agent for the improvement of retention, dehydration and preparation, especially for the manufacture of paper - Google Patents
Auxiliary agent for the improvement of retention, dehydration and preparation, especially for the manufacture of paper Download PDFInfo
- Publication number
- EP0000714B1 EP0000714B1 EP78100444A EP78100444A EP0000714B1 EP 0000714 B1 EP0000714 B1 EP 0000714B1 EP 78100444 A EP78100444 A EP 78100444A EP 78100444 A EP78100444 A EP 78100444A EP 0000714 B1 EP0000714 B1 EP 0000714B1
- Authority
- EP
- European Patent Office
- Prior art keywords
- product
- integer
- polyethylene glycol
- component product
- retention
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/52—Treatment of water, waste water, or sewage by flocculation or precipitation of suspended impurities
- C02F1/54—Treatment of water, waste water, or sewage by flocculation or precipitation of suspended impurities using organic material
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G69/00—Macromolecular compounds obtained by reactions forming a carboxylic amide link in the main chain of the macromolecule
- C08G69/48—Polymers modified by chemical after-treatment
-
- D—TEXTILES; PAPER
- D21—PAPER-MAKING; PRODUCTION OF CELLULOSE
- D21H—PULP COMPOSITIONS; PREPARATION THEREOF NOT COVERED BY SUBCLASSES D21C OR D21D; IMPREGNATING OR COATING OF PAPER; TREATMENT OF FINISHED PAPER NOT COVERED BY CLASS B31 OR SUBCLASS D21G; PAPER NOT OTHERWISE PROVIDED FOR
- D21H17/00—Non-fibrous material added to the pulp, characterised by its constitution; Paper-impregnating material characterised by its constitution
- D21H17/20—Macromolecular organic compounds
- D21H17/33—Synthetic macromolecular compounds
- D21H17/46—Synthetic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
- D21H17/54—Synthetic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds obtained by reactions forming in the main chain of the macromolecule a linkage containing nitrogen
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S210/00—Liquid purification or separation
- Y10S210/928—Paper mill waste, e.g. white water, black liquor treated
Definitions
- the invention relates to polyethylene glycol-polyaminoamide condensation products for retention purposes. Improvement of washable solids, to accelerate the dewatering of suspensions and to process industrial water, waste water and sludge more quickly, especially in the paper industry.
- a polyamino amide production of the polyamino amide, for example, by condensation of adipic acid and diethylene triamine
- a polyether with a filiform molecular structure and terminal tertiary amino groups production of the polyether, for example from glycol, epichlorohydrin and dimethylamine
- this adduct is then reacted with epichlorohydrin.
- the aforementioned adduct is already highly branched, so that when it is subsequently crosslinked with epichlorohydrin, it leads to a considerably entangled molecular structure, which has a disadvantageous effect when this auxiliary is used as a retention and drainage agent. because because of this tangled molecular structure, only a fraction of the auxiliary molecule can be fully effective in the above sense.
- polyethylene polyamines having 15 to 500 alkyleneimine units with a crosslinking agent obtained from the reaction of polyalkylene glycol ether with epichlorohydrin, in amounts of 0.08 to 0.001 mol of crosslinking agent per 1 equivalent of nitrogen in the polyalkylene polyamine to react and thus to crosslink.
- a crosslinking agent obtained from the reaction of polyalkylene glycol ether with epichlorohydrin, in amounts of 0.08 to 0.001 mol of crosslinking agent per 1 equivalent of nitrogen in the polyalkylene polyamine to react and thus to crosslink.
- the basic polyamides used here are high molecular weight water-soluble products which are obtained by the action of compounds which are polyfunctional with respect to amino groups on basic polyamides dissolved or dispersed in water from polyvalent amines, dicarboxylic acids and aminocarboxylic acids or lactams containing at least three carbon atoms, and for their preparation from 1 val of the basic amino groups contained in the basic polyamides, less than 1 val of reactive groups were used in the polyfunctional compounds.
- the polyalkylene polyamines are crosslinked with, for example, epichlorohydrin.
- the resulting acid which has been subsequently acidified, has a structure due to the procedural interconnected starting blocks, in which, for example, cationic side chains are missing, which is why optimal reaction and dewatering performance cannot yet be achieved.
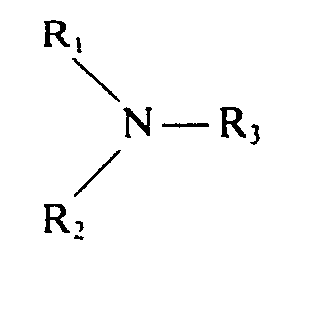
- composition as a building block has polyalkylene glycol compounds and is characterized in that it is a reaction product C which results from the reaction of an aliphatic polyethylene glycol ether amine as partial product A which, by the action of a), 0.25 to 1 mol, preferably 0.7 to 1 mole, of a polyalkylene polyamine of the general formula where y and z are an integer between 2 and 4, preferably 2 and 3; n represents an integer between 2 and 5 and m represents an integer between 0 and 5, preferably between 0 and 3, and / or 0.25 to 2 mol, preferably 0.8 to 2 mol, of an amine of the general formula where R and R 2 are
- products can be used equally well as polyfunctional compounds here, e.g. B. can be selected from a group which includes epibromohydrin, epifluorohydrin, the dihaloalkanes, glyoxal-bis-acrylamide, bis-acrylamidoacetic acid, acrylaminoglycolic acid, tetraallyloxyethane and other compounds, epichlorohydrin is preferred here.
- reaction product c) consists of 1 mol of the polyethylene glycol of the general formula where r is an integer between 1 and 27, preferably 1 and 24, when 2 mol of epichlorohydrin has been formed and when 0.5 to 7, preferably 2.5 to 6.8 mol, of partial product B, based on polyalkylene polyamine of the basic polyaminoamide, has been implemented.
- the aid can be varied in a relatively wide range without reducing its special performance.
- tools can be obtained in the aforementioned manner, the z. B. in 20% by weight aqueous solution at 25 ° C have a viscosity of 50 on the one hand to 1000 mPa on the other.
- This so-called partial product A in the form of its chloropolyethylene glycol ether amine is then combined with the part product B known per se, namely a basic polyamino amide to form a polyethylene glycol ether amine polyamino amide, which is called intermediate AB as mentioned above.
- This intermediate product AB is then reacted again with a polyfunctional compound selected from the special group of polyfunctional compounds mentioned above, here preferably with epichlorohydrin, in such a way that the end product C is finally in the form of a polyethylene glycol ether-amine-polyaminoamide-epichlorohydrin resin.
- Chloride determination (measurement method, at the same time explanation of the following Table 2)
- the above-mentioned newsprint suspension is obtained by mechanical defibration of commercially available newsprint and subsequent speck-free beating of the defibrated product in a conventional kitchen mixer.
- the measurements are carried out at a pH of 6.5 and 4.8, which is adjusted with a 1% by weight aqueous alum solution.
- the fiber concentration is 2 g / l water.
- the 0 sample listed in Table 5 is of course dependent on the choice of waste paper used.
- the same determination method is used both for the examples according to the invention and for the further comparative examples in order to achieve comparable values.
- the filler retention is characterized by the ash content of paper sheets that are produced on the »Rapid-Köthen réelle « in accordance with leaflet V / 8/57 of the Association of Pulp and Paper Chemists and Engineers (old version was leaflet 108).
- Diethylenetriamine is a 100% pure substance.
- Polyethylene glycol ether is present as the pure substance, the number added in the table indicates the average molecular weight of this compound, for example 400; 600; 1000; 6000 etc.
- Polyaminoamide resin solution which contains the secondary amines as a reactive group. 1 mole of this compound corresponds to 1 NH.
- Adipic acid is present as a 100 weight percent solid.
- Caprolactam is a 100% by weight solid.
- Salt from adipic acid and hexamethylenediamine is present as a 100 percent solid
- Diethanolamine is always available as a 100 percent by weight substance.
- Trimethylamine is always available as a 45 weight percent aqueous solution.
- Dimethylamine is always available as a 40 weight percent aqueous solution.
- intermediate B in the relevant examples 1b to 3b always contains the same amounts of adipic acids (AS) and diethylenetriamine (DTRA).
- AS adipic acids
- DTRA diethylenetriamine
- caprolactam (CL) was also used, and in example 3b the salt of adipic acid and hexamethylenediamine (hexamethylenediammonium adipate; AH-S) was also used.
- the reaction takes place at a reaction temperature of at most 65 ° C in a time of 2.5 hours in the form of an addition reaction.
- the resulting product namely polyethylene glycol bis-ß-hydroxy-y-chloropropyl ether, is now after adding 271.7 ml of deionized water, which is stirred in at 65 ° C in two minutes, with 35.4 g of DTRA, corresponding to 0.336 moles offset via an inlet funnel.
- the temperature is kept at 65 ° C if necessary by means of water cooling. After one hour, the reaction solution temperature drops due to the completion of the reaction between the aforementioned substances.
- the partial product A ( ⁇ -hydroxy-y-chloropropylpolyethylene glycol ether- ⁇ -hydroxy-y-propylamine) formed in this way gave the following values in its analysis:
- adipic acid (100% by weight corresponding to 10 mol, solid) were placed in a pressure vessel designed as a steel autoclave with a stirrer, a temperature sensor in the form of a thermal sensor and a distillation condenser; 1124.5 g of diethylenetriamine (100% by weight corresponding to 10.9 mol; liquid) and 226.34 g of caprolactam (100% by weight corresponding to 2 mol; solid) were introduced in the form of their pure substances. After the above-mentioned filling material has been overlaid with oxygen-free nitrogen, which thus replaces the supernatant residual gas mixture, the contents of the vessel are heated to 160 ° C. after the end of the reaction vessel and left at this temperature for 30 minutes with stirring.
- the water of reaction released is then distilled off (a total of 360 ml, corresponding to 100% of theory).
- the reaction mixture, which is now free of condensation, is then further heated to 180 ° C. and stirred at this temperature for a further two hours.
- the mixture reacts further, nitrogen being continuously passed through the condensing reaction mass.
- Example 10 of DE-OS 2 434 816 was reworked by adding the polyaminoamide V 12 (produced from adipic acid, diethylenetriamine and hexamethylenediamine adipate) with the crosslinker V 4 (reaction product from polyethylene glycol and epichlorohydrin) according to the description of Examples 1 to 14 on page 12 of the DE-OS was implemented.
- the viscosity of the 18 percent solution the condensation products were 609 mPa. s (shear rate 24.5 sec -1 at 20 ° C).
- the polyethylene glycol-polyaminoamide condensation product according to the invention for improving the retention of washable solids, for accelerating the dewatering of suspensions and for the faster treatment of industrial waters, wastewater and sludges by adding basic water-soluble polymers as an aqueous polymer solution can be used primarily advantageously in the paper industry, but is at the same time advantageous also very well suited for the treatment of industrial water, waste water purification and sludge conditioning in other branches of industry.
- sludge treatment includes the treatment of fresh sludge and activated sludge as well as the sludge thickening and sludge flotation processes known per se, in which the aid according to the invention can be used very well.
- auxiliaries for example in the clarification process, are insensitive to the addition of a number of different substances, which is why it is readily possible, for example inorganic flocculants, such as those based on aluminum and iron salts or on the base of lime compounds are commercially available, without the auxiliary properties of the invention being adversely affected in terms of their use properties.
- the aid according to the invention is used in sedimentation and clarification tanks, it is recommended to use it in an amount of approximately 0.1 to 4 mg per liter of the substance to be clarified.
- the water can be removed from the sludge better and more quickly if the auxiliary according to the invention is used in amounts of about 2 to 12 kg per ton of dry sludge is added to the substance to be treated.
- the sludge to be treated is to be stabilized, it is appropriate to add about 50 to 150 mg of the Aids according to the invention are added to the sludge for each corresponding unit of quantity.
- the stabilization advantageously occurs by promoting the formation of tear-resistant flakes by the aid.
- the said auxiliary can of course not only be added separately, but also in admixture with the other substances required in papermaking, such as dyes, antioxidants, optical brighteners and fluorescent agents, since the aid is not sensitive to these substances.
- the aforementioned additional method of prior mixing of the additives is often used because, for example, optical brighteners and fluorescent agents are generally only required in small amounts in the paper in order to achieve the desired change in the appearance of the paper.
- the auxiliary according to the invention can of course also be used in completely different areas than those mentioned above.
- the agent can be used as well as an improver for the wet strength of fabrics (especially paper). use, in the latter case, however, advantageously after acidification of the agent.
- the auxiliary according to the invention is very stable in storage even in the basic medium if, as the person skilled in the art knows, only as much crosslinking agent as required is added in the preparation of the crosslinking agent, for example using epichlorohydrin.
- the agent can still be used, but must then be acidified in order to achieve a suitable storage stability, which also reliably prevents any gelling that might otherwise occur in this case.
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Hydrology & Water Resources (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Environmental & Geological Engineering (AREA)
- Water Supply & Treatment (AREA)
- Paper (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Separation Of Suspended Particles By Flocculating Agents (AREA)
- Polyamides (AREA)
Description
Die Erfindung betrifft Polyethylenglykol-Polyaminoamid-Kondensationsprodukte zur Retentionsver. besserung von ausschwemmbaren Feststoffen, zur Entwässerungsbeschleunigung von Suspensionen und zur rascheren Aufbereitung von industriellen Wässern, Abwässern und Schlämmen, insbesondere in der Papierindustrie.The invention relates to polyethylene glycol-polyaminoamide condensation products for retention purposes. Improvement of washable solids, to accelerate the dewatering of suspensions and to process industrial water, waste water and sludge more quickly, especially in the paper industry.
Derartige Polymere und ihre Verwendung im oben aufgeführten Sinn bei der Papierherstellung sind bereits in der Fachwelt aus zahlreichen Veröffentlichungen bekannt. So sind in der DE-AS 1 546 290 Umsetzungsprodukte aus Polyalkylenpolyaminen und bifunktionellen Polyalkylenoxidderivaten beschrieben, die sich zwar für die Flotation von Fasern und Füllstoffen aus Papiermaschinenabwässern, jedoch nicht gleichzeitig auch, wie es an sich wünschenswert wäre, für den Einsatz als Retentions- und Entwässerungshilfsmittel in der Papierstoffindustrie gleich gut eignen. Auch in der US-PS 3 575 797 sind viskose Flotationsmittel für Papiermaschinenabwässer beschrieben. Diese Flotationsmittel sind Reaktionsprodukte von Polyalkylenpolyaminen mit Polyethylenglykolderivaten. die wenigstens 2 Chlorameisensäureester-Gruppen enthalten. Leider sind diese Produkte nur als eine 10%ige Lösung herstellbar und weisen überdies nur relativ geringe Retentions- und Entwässerungsleistungen auf.Such polymers and their use in the above-mentioned sense in papermaking are already known in the art from numerous publications. DE-AS 1 546 290 describes reaction products made from polyalkylene polyamines and bifunctional polyalkylene oxide derivatives which are suitable for the flotation of fibers and fillers from paper machine waste water, but not at the same time, as would be desirable, for use as retention and Drainage aids are equally suitable in the paper industry. US Pat. No. 3,575,797 also describes viscous flotation agents for paper machine waste water. These flotation agents are reaction products of polyalkylene polyamines with polyethylene glycol derivatives. which contain at least 2 chloroformate groups. Unfortunately, these products can only be produced as a 10% solution and, moreover, only have relatively low retention and drainage capacities.
Andere, für den oben angeführten Zweck empfohlene Hilfsmittel sind aus der DE-OS 2 162 567 zu ersehen. Hier wird an einen Polyäther mit fadenförmiger Molekülstruktur und endständigen tertiären Aminogruppen (Herstellung des Polyäthers zum Beispiel aus Glykol, Epichlorhydrin und Dimethylamin) ein Polyaminoamid (Herstellung des Polyaminoamids zum Beispiel durch Kondensation von Adipinsäure und Diäthylentriamin) über die CH2-CI-Gruppen angelagert und dieses Anlagerungsprodukt anschließend mit Epichlorhydrin umgesetzt. Bereits das vorgenannte Anlagerungsprodukt ist stark verzweigt, so daß es bei seiner anschließenden Vernetzung mit Epichlorhydrin zu einer erheblich verknäuelten Molekularstruktur führt, die sich nachteilig bei Verwendung dieses Hilfsmittels bei dessen Einsatz als Retentions- und Entwässerungsmittel auswirkt. weil wegen dieser verknäuelten Molekularstruktur nur ein Bruchteil des Hilfsmittel-Moleküls im o. a Sinn voll wirksam werden kann.Other aids recommended for the above-mentioned purpose can be seen from DE-OS 2 162 567. Here, a polyamino amide (production of the polyamino amide, for example, by condensation of adipic acid and diethylene triamine) via the CH 2 -CI groups is attached to a polyether with a filiform molecular structure and terminal tertiary amino groups (production of the polyether, for example from glycol, epichlorohydrin and dimethylamine) this adduct is then reacted with epichlorohydrin. The aforementioned adduct is already highly branched, so that when it is subsequently crosslinked with epichlorohydrin, it leads to a considerably entangled molecular structure, which has a disadvantageous effect when this auxiliary is used as a retention and drainage agent. because because of this tangled molecular structure, only a fraction of the auxiliary molecule can be fully effective in the above sense.
In der in diesem Zusammenhang weiterhin zu nennenden DE-AS 2 127 082 wird ein kompliziertes Verfahren zur Herstellung von Entwässerungs- und Retentionsmitteln beschrieben, wobei durch Vernetzung der Umsetzungsprodukte aus Polyepichlorhydrin und Polyamiden mit Bis-chlorhydrin relativ ungünstige Molekülstrukturen erhalten werden, die die an sich vorhandene hohe kationische Ladung des Moleküls bei einer wie eingangs genannten Verwendung nicht voll zur Entfaltung kommen lassen und somit keine optimale Leistung bei der Papierherstellung zeigen.In DE-AS 2 127 082, which is also to be mentioned in this context, a complicated process for the production of drainage and retention agents is described, whereby relatively unfavorable molecular structures are obtained by cross-linking the reaction products of polyepichlorohydrin and polyamides with bis-chlorohydrin, which in themselves the existing high cationic charge of the molecule does not fully develop when used as mentioned at the beginning and therefore does not show optimal performance in paper production.
Ähnliches trifft für das aus der DE-OS 2 255 586 ersichtliche Produkt, das lediglich als zusätzlichen Baustein Polyäthylenglykol bei sonst prinzipiell äquivalentem Aufbau zeigt, zu.The same applies to the product shown in DE-OS 2 255 586, which only shows polyethylene glycol as an additional building block with an otherwise equivalent structure.
In der in diesem Zusammenhang weiterhin anzuführenden DE-OS 2 244 513 sind ähnliche Produkte bekanntgeworden, die aus Polyepichlorhydrin, Diamin und Polyalkylenpolyaminen mit anschließender Vernetzung zum Beispiel mit Epichlorhydrin aufgebaut sind, beschrieben. Auch diese Produkte sind jedoch ebenfalls aufgrund der vorgegebenen Struktur nur unzureichend als Flockungs-, Retentions-und gleichzeitig als Entwässerungshilfsmittel bei der Papierherstellung zu verwenden.Similar products are known in DE-OS 2 244 513 to be cited in this connection, which are made up of polyepichlorohydrin, diamine and polyalkylene polyamines with subsequent crosslinking, for example with epichlorohydrin. However, due to the given structure, these products too are to be used only insufficiently as flocculation, retention and, at the same time, as drainage aids in papermaking.
Noch andere Produkte sind aus den DE-OS 2434816 und der hierzu gehörigen Zusatz-DE-OS 2515760 bekanntgeworden. Hier werden aus Polyglykoläthern und Epichlorhydrin hergestellte Polyaminoamide mit Vernetzern bis zur Erzielung einer gewünschten Viskosität umgesetzt. Es entstehen jedoch auch hier für den angestrebten Verwendungszweck in aer Papierindustrie ungünstige molekulare Strukturen, wobei insbesondere das Fehlen von Aminogruppen in den großen Äthylenoxidmolekülen eine stärkere pH-Abhängigkeit und so eine eingeschränkte Wirksamkeit zur Folge hat.Still other products have become known from DE-OS 2434816 and the associated additional DE-OS 2515760. Here, polyaminoamides made from polyglycol ethers and epichlorohydrin are reacted with crosslinking agents until a desired viscosity is achieved. However, molecular structures which are unfavorable for the intended use in the paper industry also arise here, the lack of amino groups in the large ethylene oxide molecules in particular resulting in a stronger pH dependence and thus a limited effectiveness.
In der schließlich noch in diesem Zusammenhang anzuführenden DE-OS 2 436 386 werden Polyäthylenpolyamine mit 15 bis 500 Alkylenimin-Einheiten mit einem Vernetzer, erhalten aus der Reaktion von Polyalkylenglykoläther mit Epichlorhydrin, in Mengen von 0,08 bis 0.001 Mol Vernetzer pro 1 Äquivalent Stickstoff im Polyalkylenpolyamin zur Reaktion und damit zur Vernetzung gebracht. Abgesehen von den Bedenken, die man bei der Verwendung von Alky'eniminen als reine Ausgangsstoffe wegen ihrer cancerogenen Eigenschaften hat, ist an den hohen technischen Aufwand zur sicheren Durchführung der vorgenannten Reaktion zu denken. Hierdurch werden die Herstellkosten negativ beeinflußt. Ferner können die hier erwähnten Polyalkylenglykole wegen ihrer aus vorstehendem Aufbau bedingten Verknüpfung mit der bestimmten Art anderer Bausteine des Makromoleküls keine besonders günstige Retentions- und Entwässerungsleistung erbringen.In DE-OS 2 436 386, which is finally to be mentioned in this connection, polyethylene polyamines having 15 to 500 alkyleneimine units with a crosslinking agent, obtained from the reaction of polyalkylene glycol ether with epichlorohydrin, in amounts of 0.08 to 0.001 mol of crosslinking agent per 1 equivalent of nitrogen in the polyalkylene polyamine to react and thus to crosslink. Apart from the concerns that one has when using alkyenimines as pure starting materials because of their carcinogenic properties, one has to think about the high technical expenditure for safely carrying out the above-mentioned reaction. This has a negative impact on manufacturing costs. Furthermore, the polyalkylene glycols mentioned here cannot provide particularly favorable retention and drainage performance owing to their linkage with the specific type of other building blocks of the macromolecule due to the above structure.
Der vorstehend gewürdigte Stand der Technik beschreibt Produkte, die als Produktbaustein Polyalkylenglykolverbindungen enthalten. Werden diese Produkte als Retentionsmittel verwendet, ist daran zu erinnern, daß Polyalkylenglykole keine von der Fachwelt zur Erzielung einer günstigen Retentionsleistung als notwendig erkannte kationische Ladungen aufweisen.The prior art recognized above describes products which contain polyalkylene glycol compounds as the product component. If these products are used as retention agents, it should be remembered that polyalkylene glycols do not have any cationic charges recognized as necessary by experts in order to achieve a favorable retention performance.
Daher hat die ständig weiterbestehende Aufgabe der fortgesetzten Verbesserung der Retentionsleistung derartiger Produkte schon seit längerem dazu geführt, auf diesen aus anderen Gründen bisher für notwendig erachteten Einbau eines PolyalkylenglykolbaustHins zu verzichten. Die in diesem Zusammenhang bisher bekanntgewordenen Polyalkylenglykol-bausreinfreien Retentionsmittel werden nun in der folgenden Stand-der-Technik-Würdigung aufgeführt. Zunächst ist hier auf die DE-PS 1 771 814 hinzuweisen, in welcher die Verwendung von basischen Polyaminoamiden zur Erhöhung der Retention von Füllstoffen und Pigmenten bei der Papierherstellung, zur Beschleunigung der Entwässerung von Papierrohstoffsuspensionen und zur Aufarbeitung von Papiermaschinenabwässern durch Filtration, Sedimentation und Flotation durch Zusatz basischer Polyamide zu den Papierrohstoffsuspensionen und/oder Papiermaschinenabwässern beschrieben wird. Hierbei verwendet man als basische Polyamide hochmolekulare wasserlösliche Produkte, die durch Einwirkung von gegenüber Aminogruppen polyfunktionellen Verbindungen auf in Wasser gelöste oder dispergierte basische Polyamide aus mehrwertigen Aminen, Dicarbonsäuren und mindestens drei Kohlenstoffatome enthaltenden Aminocarbonsäuren oder deren Lactame erhalten werden, und zu deren Herstellung aus 1 Val der in den basischen Polyamiden enthaltenen basischen Aminogruppen weniger als 1 Val reaktive Gruppen in den polyfunktionellen Verbindungen verwandt wurden. Hier werden also die Polyalkylenpolyamine mit zum Beispiel Epichlorhydrin vernetzt. Das entstandene, nachträglich sauer eingestellte Produkt besitzt aufgrund der verfahrensmäßig miteinander verbundenen Ausgangsbausteine eine Struktur, in der zum Beispiel kationische Seitenketten fehlen, weswegen eine optimale Reaktions- und Entwässerungsleistung noch nicht erbracht werden kann.Therefore, the ongoing task of continually improving the retention performance of such products has long led to those from others Reasons to forego the installation of a polyalkylene glycol building block previously considered necessary. The retention agents that have been disclosed in this connection so far in this connection are now listed in the following prior art assessment. First of all, reference should be made to DE-PS 1 771 814, in which the use of basic polyaminoamides to increase the retention of fillers and pigments in papermaking, to accelerate the dewatering of paper stock suspensions and to process paper machine waste water by filtration, sedimentation and flotation Addition of basic polyamides to the paper stock suspensions and / or paper machine waste water is described. The basic polyamides used here are high molecular weight water-soluble products which are obtained by the action of compounds which are polyfunctional with respect to amino groups on basic polyamides dissolved or dispersed in water from polyvalent amines, dicarboxylic acids and aminocarboxylic acids or lactams containing at least three carbon atoms, and for their preparation from 1 val of the basic amino groups contained in the basic polyamides, less than 1 val of reactive groups were used in the polyfunctional compounds. Here, the polyalkylene polyamines are crosslinked with, for example, epichlorohydrin. The resulting acid, which has been subsequently acidified, has a structure due to the procedural interconnected starting blocks, in which, for example, cationic side chains are missing, which is why optimal reaction and dewatering performance cannot yet be achieved.
Als Weiterentwicklung in dieser Richtung ist der auf der Basis der französischen Patentschrift 2 094 645 entstandene ältere Vorschlag der Anmelderin in Form der DE-OS 2 353 430 anzusehen. Dieser Vorschlag ist auf die Herstellung und Verwendung von wasserlösliclien Papiererzeugungshilfsmitteln auf Polyaminoamidbasis gerichtet, wobei die in der vorgenannten französischen Patentschrift als älterem Stand der Technik angegebenen dimeren Fettsäuren als Bestandteil des Ausgangsmonomerengemischs zur Herstellung eines retentionswirksamen Makromoleküls bei der Papierherstellung in der vorgenannten DE-OS 2353430 durch kurze aber kationaktivere und damit retentionswirksamere Seitenketten ersetzt worden sind. Prinzipiell werden in dieser DE-OS basische Polyaminoamide vor der Vernetzung mit polyfunktionellen Vernetzungsmitteln, wie zum Beispiel Epichlorhydrin, mit Ammoniumverbindungen, hergestellt durch Einwirkung einer polyfunktionellen Verbindung auf ein tertiäres Amin, umgesetzt. Diese bekannte makromolekulare Verbindung zeigt zwar eine wesentlich bessere Retentionsieirtung als praktisch alle aus dem davor angeführten Stand der Technik bekanntgewordenen Produkte, jedoch sind auch die hiermit erzielbaren Retentions-, Entwässerungs-und Wasseraufbereitungs-Leistungen bei der Papierherstellung nicht voll zufriedenstellend gewesen.A further development in this direction is the applicant's older proposal in the form of DE-OS 2 353 430, which was created on the basis of French patent specification 2,094,645. This proposal is directed to the production and use of water-soluble polyaminoamide-based paper production auxiliaries, the dimeric fatty acids specified in the aforementioned French patent as the prior art being used as a constituent of the starting monomer mixture for the production of a retention-effective macromolecule in paper production in the aforementioned DE-OS 2353430 short but more cation-active and thus more effective side chains have been replaced. In principle, in this DE-OS, basic polyaminoamides are reacted with ammonium compounds, prepared by the action of a polyfunctional compound on a tertiary amine, before crosslinking with polyfunctional crosslinking agents, such as, for example, epichlorohydrin. Although this known macromolecular compound shows a considerably better retention than practically all of the products known from the prior art cited above, the retention, drainage and water treatment achievable thereby have not been completely satisfactory in papermaking either.
Die daher fortlaufend weiter bestehende Aufgabe der Schaffung entsprechender Hilfsmittel mit immer weiter gesteigerter Retentionsleistung führte zu der Entwicklung eines anderen als in der vorbeschriebenen DE-OS 2353430 angeführten Makromoleküls, nämlicfi wie es aus den DE-PS 2 502 874 und 2 538 745 (Zusatz zu 2 502 874) ersichtlich ist. Hier werden Produkte mit besonderer Sedimentationsleistung geschaffen, wobei diese durch Verknüpfung von Polyaminoamiden und Polyaminen, die durch Einwirkung von ein- bzw. mehrwertigen Aminen auf das Umsetzungsprodukt aus Dimethylaminen und Epichlorhydrin erhalten werden, mittels Epichlorhydrin hergestellt werden. Auf diese Weise entstehen molekulare Raumstrukturen, die eine recht gute Wirkung bei der Papierfabrikation im sauren und neutralen pH-Bereich gewährleisten, jedoch optimal denkbare und nach wie vor von der Fachwelt gewünschte entsprechende Leistungen noch nicht erreichen.The task, which therefore continues to exist, of creating appropriate auxiliaries with an ever increasing retention rate led to the development of a macromolecule other than that described in the previously described DE-OS 2353430, namely as described in DE-PS 2 502 874 and 2 538 745 (addition to 2 502 874) can be seen. Products with special sedimentation performance are created here, these being produced by linking polyaminoamides and polyamines, which are obtained by the action of mono- or polyvalent amines on the reaction product of dimethylamines and epichlorohydrin, by means of epichlorohydrin. In this way, molecular spatial structures are created which guarantee a very good effect in paper production in the acidic and neutral pH range, but which do not yet achieve optimally conceivable and still desired corresponding performance by experts.
Zusammengefaßt ist bezüglich des vorstehend aufgeführten Standes der Technik festzuhalten, daß weder die dort beschriebenen Produkte, die Polyäthylinglykole als Baustein noch die Produkte, die Polyaminoamide als Baustein noch sogar die Produkte, die wie die DE-OS 2 434 816 und 2 515 760 sowohl Polyalkylenglykole als auch Polyaminoamide als Bausteine enthalten, eine optimale Retentionsleistung zeigen.In summary, with regard to the prior art listed above, it should be noted that neither the products described there, the polyethylene glycols as a building block, nor the products, the polyaminoamides as building blocks, nor even the products, such as DE-OS 2 434 816 and 2 515 760, both polyalkylene glycols and also contain polyaminoamides as building blocks, show an optimal retention performance.
Da die nicht zufriedenstellende Verwendungsfunktion dieser Produkte vermutlich auf »bausteinstandort-abhängige« Gründe des Makromoleküls zurückgehen dürfte, dies jedoch keinesfalls sicher ist, wäre zu erwarten, daß die Fachwelt nunmehr andere als die vorgenannten Wege einschlägt, wobei es nahegelegen hätte, makromolekulare Verbindungen mit Polyalkylenglykol als Baustein schon deswegen zu verlassen, weil bekanntlich Polyalkylenglykole keine positiven oder negativen Ladungen, die ja die Voraussetzung für eine gute Retentionsmittelleistung sind, tragen. Tatsächlich enthalten daher die neuesten bekannten und die relativ besten Retentionsleistungen aufweisenden Produkte, wie sie insbesondere in den DE-PS 2 502 874 und 2 538 745 beschrieben sind, keine Bausteine in Form von Polyalkylenglykol-Verbindungen bzw. deren Derivate mehr.Since the unsatisfactory use function of these products is probably due to the "site-dependent" reasons of the macromolecule, but this is by no means certain, it would be expected that the professional community would now take a path other than the aforementioned, whereby it would have been obvious to use macromolecular compounds with polyalkylene glycol to leave as a building block simply because, as is well known, polyalkylene glycols do not carry any positive or negative charges, which are the prerequisite for good retention agent performance. In fact, therefore, the latest known and relatively best retention products, as described in particular in DE-PS 2 502 874 and 2 538 745, no longer contain building blocks in the form of polyalkylene glycol compounds or their derivatives.
Im Rahmen der somit weiter bestehenden Aufgabe der Schaffung noch besserer Retentionsmittel ist daher die hier folgende erfindungsgemäße Lösung dieser Aufgabe insofern völlig unerwartet und überraschend, als trotz der dem Fachmann bisher bekannten nachteiligen vorstehend beschriebenen Eigenschaften der Polyalkylenglykolbausteine nunmehr ein noch leistungsfähigeres Kondensationsprodukt geschaffen ist, dessen erfindungsgemäße Zusammensetzung als Baustein unter anderem wiederum Polyalkylenglykolverbindungen aufweist und das dadurch gekennzeichnet ist, daß es ein Reaktionsprodukt C ist, welches aus der Umsetzung von einem aliphatischen Polyethylenglykoletheramin als Teilprodukt A, das durch Einwirkung von a) 0,25 bis 1 Mol, vorzugsweise 0,7 bis 1 Mol, eines Polyalkylenpolyamins der allgemeinen Formel
Obwohl hier als polyfunktionelle Verbindungen Produkte gleichgut verwendbar sind, die z. B. ausgewählt sein können aus einer Gruppe, die unter anderem Epibromhydrin, Epifluorhydrin, die Dihalogenalkane, Glyoxal-bis-acrylamid, bis-Acrylamidoessigsäure, Acrylaminoglykolsäure, Tetraallyloxyethan und andere Verbindungen enthält, ist Epichlorhydrin hier bevorzugt.Although products can be used equally well as polyfunctional compounds here, e.g. B. can be selected from a group which includes epibromohydrin, epifluorohydrin, the dihaloalkanes, glyoxal-bis-acrylamide, bis-acrylamidoacetic acid, acrylaminoglycolic acid, tetraallyloxyethane and other compounds, epichlorohydrin is preferred here.
Besonders gute Ergebnisse erhält man bei Einhaltung der oben angegebenen Vorzugsbereiche und wenn das Umsetzungsprodukt c) aus 1 Mol des Polyethylenglykols der allgemeinen Formel
Selbstverständlich ist es im Rahmen der Erfindung je nach Wunsch möglich, zwecks Erhaltung einer ganz bestimmten gewünschten Viskosität des Endprodukts C die zum Schluß der Reaktionsverbindung AB zugesetzte polyfunktionelle Verbindung mengenmäßig entsprechend zu variieren. Auf diese Weise läßt sich das Hilfsmittel in relativ breit gefächerter Form variieren, ohne daß seine besonderen Leistungen verringert werden. Beispielsweise kann man in der vorgenannten Weise Hilfsmittel erhalten, die z. B. in 20gewichtsprozentiger wäßriger Lösung bei 25° C eine Viskosität von einerseits 50 bis andererseits 1000 mPa - saufweisen.Of course, it is possible within the scope of the invention, as desired, to vary the quantity of the polyfunctional compound added at the end of the reaction compound AB in order to maintain a very specific desired viscosity of the end product C. In this way, the aid can be varied in a relatively wide range without reducing its special performance. For example, tools can be obtained in the aforementioned manner, the z. B. in 20% by weight aqueous solution at 25 ° C have a viscosity of 50 on the one hand to 1000 mPa on the other.
Durch die wie oben angeführten qualitativen und quantitativen Variationsmöglichkeiten des Aufbaus der erfindungsgemäßen Hilfsmittel ist eine Anpassung dieses Mittels an die verschiedensten Verwendungen insbesondere im Rahmen der papierherstellenden Industrie gewährleistet. Da der Aufbau des erfindungsgemäßen Teilprodukts B bereits aus den älteren Druckschriften DE-PS 2 502 874 und 2538745 bekannt ist, wird an dieser Stelle mehr auf den Aufbau des erfindungsgemäßen Teilprodukts A eingegangen. Ganz allgemein ist hierbei, soweit nicht bereits oben erwähnt, zu beachten, daß der weder positive noch negative Ladung aufweisende Polyäthylenglykoläther unter Zusatz eines speziellen Katalysators wie zum Beispiel eines Bortrifluorid-Ätherat-Katalysators auf beiden Seiten seines Kettenmoleküls mit je einem Mol Epichlorhydrin umgesetzt wird und danach nur auf einer Seite dieser Kette das dort befindliche Epichlorhydrin wiederum mit dem speziellen Amin der vorgenannten allgemeinen Formeln verbunden wird. Dieses sogenannte Teilprodukt A in Form seines Chloropolyäthylenglykolätheramins wird dann mit dem an sich bekannten Teilprodukt B, nämlich einem basischen Polyaminoamid zu einem Polyäthylenglykoläther-Amin-Polyaminoamid, welches wie vorgenannt Zwischenprodukt AB genannt wird, verbunden. Dieses Zwischenprodukt AB wird dann noch einmal mit einer polyfunktionellen Verbindung, ausgewählt aus der weiter oben angeführten speziellen Gruppe polyfunktioneller Verbindungen, hier bevorzugt mit Epichlorhydrin, so umgesetzt, daß das Endprodukt C schließlich in Form eines Polyäthylenglykoläther-Amin-Polyaminoamid-Epichlorhydrinharzes vorliegt. Obwohl der Gegenstand der Erfindung als Produkt nicht auf ein ganz bestimmtes Herstellungsverfahren beschränkt ist, soll nach diesen vorstehenden, mehr allgemeinen verfahrenstechnischen Hinweisen der Gegenstand der Erfindung an Hand der beispielsweisen Herstellungsverfahren näher erläutert und damit offenbart werden.The above-mentioned qualitative and quantitative variation possibilities of the construction of the aids according to the invention ensure that this agent is adapted to a wide variety of uses, in particular in the paper-making industry. Since the structure of partial product B according to the invention is already known from the older publications DE-PS 2 502 87 4 and 2538745, more details will be given here on the structure of partial product A according to the invention. In general, unless already mentioned above, it should be noted that the polyethylene glycol ether, which has neither a positive nor a negative charge, is reacted with one mole of epichlorohydrin on each side of its chain molecule with the addition of a special catalyst, such as a boron trifluoride etherate catalyst then the epichlorohydrin located there is in turn only connected to the special amine of the abovementioned general formulas on one side of this chain. This so-called partial product A in the form of its chloropolyethylene glycol ether amine is then combined with the part product B known per se, namely a basic polyamino amide to form a polyethylene glycol ether amine polyamino amide, which is called intermediate AB as mentioned above. This intermediate product AB is then reacted again with a polyfunctional compound selected from the special group of polyfunctional compounds mentioned above, here preferably with epichlorohydrin, in such a way that the end product C is finally in the form of a polyethylene glycol ether-amine-polyaminoamide-epichlorohydrin resin. Although the subject matter of the invention as a product is not restricted to a very specific manufacturing process, the subject matter of the invention is to be explained in more detail and thus disclosed according to these above, more general procedural instructions.
Die in allen folgende:i Beispielen angeführten Daten und Zahlen für freies Chlorid, für die Aminzahlen, für die Viskosität und für die Dichte werden stets nach der gleichen entsprechenden und hier folgenden Bestimmungsmethode ermittelt:The data and numbers given in all of the following: i Examples for free chloride, for the Amine numbers, for the viscosity and for the density are always determined using the same corresponding and following determination method:
Diese erfolgt nach der bekannten titrimetrischen Fällungsmethode nach F. Mohr. Um möglichen Komplexbildungen des Silberions mit Anionen, die den Endpunkt der Titration stören können, vorzubeugen, wird die zu untersuchende Lösung mit Essigsäure leicht angesäuert.This takes place according to the well-known titrimetric precipitation method according to F. Mohr. In order to prevent possible complex formation of the silver ion with anions, which can disturb the end point of the titration, the solution to be examined is slightly acidified with acetic acid.
Diese wird durch Titration der wäßrigen Harzlösung des o. a. Zwischenprodukts B, wobei 1 g Harz in 100 ml Wasser gelöst ist, mit 0,1 n-Salzsäure gegen Methylrot ermittelt. Die verbrauchte Salzsäure wird in mg KOH, die 1 g reinem Harz äquivalent sind, umgerechnet und so in der betreffenden Beispielstabelle angegeben.This is by titration of the aqueous resin solution of the above. Intermediate B, wherein 1 g of resin is dissolved in 100 ml of water, determined with 0.1 N hydrochloric acid against methyl red. The hydrochloric acid consumed is converted into mg KOH, which is equivalent to 1 g of pure resin, and is thus given in the relevant example table.
Diese wird im wesentlichen für die oben angeführten Produkte A, B und C in den entsprechenden Tabellen angegeben und in einem handelsüblichen Höppler-Viskosimeter bei 25° C an 20gewichtsprozentigen wäßrigen Lösungen der entsprechenden Produkte bestimmt (Kugel-Nr. 4).This is essentially given for the above-mentioned products A, B and C in the corresponding tables and determined in a commercially available Höppler viscometer at 25 ° C. in 20% by weight aqueous solutions of the corresponding products (ball number 4).
Diese erfolgt mittels eines handelsüblichen Dichtemeßgerätes bei 20°C in der Weise, daß sich ein genormtes Aräometer mit Schrotbelastung in der zu prüfenden 20° C warmen Flüssigkeit hinsichtlich seiner Eintauchtiefe freischwimmend einpendelt. Dann liest man den am unterten Meniskus der Flüssigkeit auf der Zahlenskala des Aräometers befindlichen Wert, der direkt die Dichte angibt, ab.This is done by means of a commercially available density meter at 20 ° C in such a way that a standardized hydrometer with shot load settles freely in the 20 ° C warm liquid to be immersed in terms of its immersion depth. Then you read the value on the bottom meniscus of the liquid on the number scale of the hydrometer, which directly indicates the density.
Es folgen nun die Meßmethoden, die bei der Prüfung der anwendungstechnischen Eigenschaften des Produktes zwecks optimaler Durchführung des Verfahrens für alle in den Beispielen aufgeführten Produkte unter gleichen Bedingungen durchgeführt werden und in den tabellarischen Übersichten 5 bis 6 zusammengestellt sind. Hierbei werden neben den in den Tabellen 1 bis 3 berücksichtigten erfindungsgemäßen Produkten auch andere, wie die nach dem Stand der Technik ausgeführten Vergleichsprodukte (Beispiele 12 bis 14) berücksichtigt.The measurement methods that follow when testing the application properties of the product for the purpose of optimally carrying out the process for all the products listed in the examples are carried out under the same conditions and are summarized in tabular overviews 5 to 6. In addition to the products according to the invention taken into account in Tables 1 to 3, other products such as the comparative products designed according to the prior art (Examples 12 to 14) are also taken into account.
Die charakteristische Mahlgradsenkung in ° SR wird nach der Vorschrift des Merkblattes 107 des Vereins der Zellstoff- und Papierchemiker und Ingenieure bestimmt. Sowohl die erfindungsgemäßen wie die Vergleichsprodukte werden in diesen Beispielen als Retentionsmittel in Form ihrer wäßrigen Lösungen der Zeitungspapierstoff-Suspension zugesetzt, wobei die Konzentration dieser wäßrigen Lösungen so gewählt wurde, daß 0,1 bzw. 0,2 g des Retentionsmittels zusammen mit 99,8 g bzw. 99,9 g der atro Gesamtfestbestandteile der Papierstoffsuspension 100=Gew.-% Gesamtfeststoffanteile ergeben. Da also die Zahlen für Gramm den Zahlen für Gew.-% entsprechen, sind in der Tabelle 5 die zugegebenen Retentionsmittelmengen in Gew.-% im o. a. Sinn angegeben. Die vorgenannte Zeitungspapierstoff-Suspension wird durch mechanische Zerfaserung handelsüblichen Zeitungspapiers und anschließendes stippenfreies Aufschlagen des zerfaserten Produktes in einem üblichen Küchenmixer erhalten. Die Messungen werden bei einem pH-Wert von 6,5 und 4,8, welcher mit einer 1 gewichtsprozentigen wäßrigen Alaunlösung eingestellt wird, durchgeführt. Die Faserstoffkonzentration beträgt 2 g/I Wasser. Die im übrigen in dieser Tabelle 5 aufgeführte 0-Probe ist natürlich abhängig von der Wahl des verwendeten Altpapiers.The characteristic reduction in grinding degree in ° SR is determined according to the specification of leaflet 107 of the Association of Pulp and Paper Chemists and Engineers. Both the inventive and the comparative products are added in these examples as retention agents in the form of their aqueous solutions to the newsprint suspension, the concentration of these aqueous solutions being chosen such that 0.1 or 0.2 g of the retention agent together with 99.8 g or 99.9 g of the atro total solid constituents of the paper stock suspension give 100 =% by weight total solids. Since the numbers for grams correspond to the numbers for% by weight, the amounts of retention agent added in% by weight are given in Table 5 above. Given meaning. The above-mentioned newsprint suspension is obtained by mechanical defibration of commercially available newsprint and subsequent speck-free beating of the defibrated product in a conventional kitchen mixer. The measurements are carried out at a pH of 6.5 and 4.8, which is adjusted with a 1% by weight aqueous alum solution. The fiber concentration is 2 g / l water. The 0 sample listed in Table 5 is of course dependent on the choice of waste paper used.
Auch hier wird wie in der Tabelle 5 zur Erzielung vergleichbarer Werte dieselbe Bestimmungsmethode sowohl für die erfindungsgemäßen Beispiele wie auch für die weiteren Vergleichsbeispiele angewendet. Allgemein erfolgt dabei die Charakterisierung der Füllstoffretention durch den Aschegehalt von Papierblättern, die am »Rapid-Köthengerät« entsprechend dem Merkblatt V/8/57 des Vereins der Zellstoff- und Papierchemiker und Ingenieure (alte Fassung war Merkblatt 108) hergestellt werden.Here too, as in Table 5, the same determination method is used both for the examples according to the invention and for the further comparative examples in order to achieve comparable values. In general, the filler retention is characterized by the ash content of paper sheets that are produced on the »Rapid-Köthengerät« in accordance with leaflet V / 8/57 of the Association of Pulp and Paper Chemists and Engineers (old version was leaflet 108).
Das vorgenannte Papierblatt, das der Ermittlung der Retentionsleistung der jeweiligen Vergleichsprodukte dient, besitzt einheitlich die folgende Stoffzusammensetzung:
- 80% gebleichter Sulfitzellstoff, (27° SR); 15% China-Clay; 5% Titandioxid und 0,5% Alaun (bezogen auf atro Papierfaser). Die Stoffdichte der Papierblätter zeigte = 0,24 g/I Wasser; der pH-Wert der aus dem Papierblatt durch Einbringen in Wasser herstellbaren Fasersuspension beträgt 6,2. Der Retentionsmittelzusatz bei der Stoffaufbereitung beträgt 0,02 Gew.-%, bezogen auf Atro-Retentionsmittel bzw. auf Atro-Papierfaserstoff.
- 80% bleached sulfite pulp, (27 ° SR); 15% china clay; 5% titanium dioxide and 0.5% alum (based on dry paper fiber). The consistency of the paper sheets showed = 0.24 g / l water; the pH of the fiber suspension that can be produced from the paper sheet by introducing it into water is 6.2. The retention agent additive in stock preparation is 0.02% by weight, based on the atro retention agent or on the atro paper pulp.
Die in dieser Tabelle 6 angegebenen Aschegehalte sind Gewichtsprozent-Angaben.The ash contents given in Table 6 are percentages by weight.
Es folgen nun die einzelnen Beispiele, wobei die Beispiele 1a, 1 b und 1 c ausführtich dargestellt sind, wogegen die folgenden weiteren Beispiele, da sie unter den gleichen Verfahrensbedingungen wie die Beispiele 1a, 1b und 1c durchgeführt werden, in verkürzter tabellarischer Form aufgeführt sind. Zur vollständigen Übersicht über das gesamte hier angeführte Beispielsmaterial wird auch das nachfolgende Textbeispiel 1a,1b und 1c in die Übersichtstabelle mit aufgenommen.The individual examples now follow, examples 1a, 1b and 1c being shown in detail, whereas the following further examples, since they are carried out under the same process conditions as examples 1a, 1b and 1c, are listed in abbreviated form in tabular form . For a complete overview of all the example material listed here, the following text examples 1a, 1b and 1c are also included in the overview table.
Aus Platzgründen werden die in den Textbeispielen 1a, 1 und 1 voll ausgeschriebenen Substanznamen in der nachfolgenden Tabellenreihe nur noch in Form ihrer Abkürzungen aufgeführt. Es folgt daher bereits an dieser Stelle eine Erklärung der in der nachstehenden Tabellenreihe verwendeten Kurzbezeichnungen für die chemischen Ausgangsprodukte unter Beifügung einiger Angaben zu ihrer Konzentration oder zu dem Medium, in dem sie gelöst sind.For reasons of space, the substance names fully written out in text examples 1a, 1 and 1 are only listed in the form of their abbreviations in the following table series. An explanation of the abbreviations for the chemical starting products used in the series of tables below is given at this point, with some information about their concentration or the medium in which they are dissolved.
Epichlorhydrin, Dichte 1,18 g - cm-1; liegt stets als 98gewichtsprozentige Lösung vor.Epichlorohydrin, density 1.18 g - cm -1 ; is always available as a 98 weight percent solution.
Diäthylentriamin, liegt vor als 100gewichtsprozentige reine Substanz.Diethylenetriamine is a 100% pure substance.
Polyäthylenglykoläther, liegt vor als Reinsubstanz, die in der Tabelle jeweils angefügte Zahl gibt das mittlere Molekulargewicht dieser Verbindung an, zum Beispiel 400; 600; 1000; 6000 usw.Polyethylene glycol ether is present as the pure substance, the number added in the table indicates the average molecular weight of this compound, for example 400; 600; 1000; 6000 etc.
Bortrifluorid-Ätherat der Summenformel C4H10BF3O; liegt stets als 65gewichtspro7entige Lösung vor.Boron trifluoride etherate of the empirical formula C 4 H 10 BF 3 O; always exists as 65gewichtspro 7 entige solution.
Polyaminoamidharzlösung, welche als reaktive Gruppe die sekundären Amine enthält. 1 Mol dieser Verbindung entspricht 1 NH.Polyaminoamide resin solution which contains the secondary amines as a reactive group. 1 mole of this compound corresponds to 1 NH.
Adipinsäure, liegt vor als 100gewichtsprozentiger Feststoff.Adipic acid is present as a 100 weight percent solid.
Caprolactam, liegt vor als 100gewichtsprozentiger Feststoff.Caprolactam, is a 100% by weight solid.
Salz aus Adipinsäure und Hexamethylendiamin, liegt vor als 100prozentiger FeststoffSalt from adipic acid and hexamethylenediamine is present as a 100 percent solid
Diäthanolamin, liegt stets als 100gewichtsprozentige Substanz vor.Diethanolamine, is always available as a 100 percent by weight substance.
Trimethylamin, liegt stets vor als 45gewichtsprozentige wäßrige Lösung.Trimethylamine, is always available as a 45 weight percent aqueous solution.
Dimethylamin, liegt stets vor als 40gewichtsprozentige wäßrige Lösung.Dimethylamine, is always available as a 40 weight percent aqueous solution.
Zur weiteren Erläuterung der nun folgenden Beispielsreihe ist zu den dort aufgeführten tabellarischen Zusammenstellungen erläuternd zu sagen, daß in der Tabelle 1 die erfindungsgemäßen Teilprodukte A, die stets die gleiche Mol-Menge, an Polydiolen jedoch mit unterschiedlichem Molekulargewicht enthalten, mit der doppelten Mol-Menge an Epichlorhydrin umgesetzt werden. Als aminische Komponente wurde Diäthylentriamin (DTRA), Dimethylamin (DMA), Trimethylamin (TMA) und Diäthanulamin (DÄAM) eingesetzt. Die Zwischenanalysenwerte der Teilprodukte Asind dann im Anschluß an die Tabelle 1 aufgeführte Tabelle 2 zusammengefaßt.To further explain the series of examples which now follows, it should be said in explanatory form regarding the tabular compilations listed there that, in Table 1, the partial products A according to the invention, which always contain the same molar amount, but of polydiols but with different molecular weights, with twice the molar amount be implemented on epichlorohydrin. Diethylenetriamine (DTRA), dimethylamine (DMA), trimethylamine (TMA) and diethanulamine (DÄAM) were used as the amine component. The intermediate analysis values of the partial products A are then summarized following Table 2 listed in Table 1.
Aus Tabelle 3 ist zu entnehmen, daß das Zwischenprodukt B in den betreffenden Beispielen 1 b bis 3b stets die gleichen Mengen an Adipinsäuren (AS) und Diäthylentriamin (DTRA) enthält. In Beispiel 1b wurde überdies zusätzlich Caprolactam (CL) und in Beispiel 3b entsprechend zusätzlich das Salz aus Adipinsäure und Hexamethylendiamin (Hexamethylendiammoniumadipat; AH - S) mit verwendet.It can be seen from Table 3 that intermediate B in the relevant examples 1b to 3b always contains the same amounts of adipic acids (AS) and diethylenetriamine (DTRA). In example 1b, caprolactam (CL) was also used, and in example 3b the salt of adipic acid and hexamethylenediamine (hexamethylenediammonium adipate; AH-S) was also used.
Wie aus der dann folgenden Tabelle 4 ersichtlich ist, wurde bei der Herstellung der Endprodukte C das Verhältnis von Teilprodukt A zu Teilprodukt B wie 1 zu 3,33 eingestellt. Nur in dem in dieser Tabelle ebenfalls befindlichen Beispiel 11c wurde das vorstehende Verhältnis geändert und auf 1 zu 6,65 eingestellt.As can be seen from the following Table 4, the ratio of partial product A to partial product B was set to 1 to 3.33 in the preparation of the end products C. Only in Example 11c, which is also in this table, was the above ratio changed and set to 1 in 6.65.
In Tabelle 5 wurde die Entwässerungsbeschleunigung, gemessen in ° SR, zusammengestellt, wobei in Beispiel 10c sich bereits der Einfluß des hier eingesetzten sehr hochmolekularen Polydiols mit einem durchschnittlichen Molekulargewicht von 6000 insofern negativ zeigt, als dadurch eine weniger starke Mahlgradsenkung im Vergleich zu den erfindungsgemäßen Beispielen resultiert. Obwohl also qualitativ gemäß der Erfindung vorgegangen wurde, wurde quantitativ, nämlich statt der Verwendung von für die Erfindung allein geeigneten Polydiolen mit durchschnittlichen Molekulargewichten 400 und 1000, ein Polydiol mit dem Molekulargewicht 6000 verwendet. Dies führt zu so schlechten Ergebnissen, daß diese gegenüber dem Stand der Technik keine Verbesserung mehr zeigen. Die Tabelle 5 lehrt demnach somit unter anderem, daß Polydiole mit einem durchschnittlichen Molekulargewicht, das möglichst nicht höher als etwa 1200 betragen sollte, verwendet werden sollen, wenn die Produkte erfindungsgemäß aufgebaut und demnach auch eine hervorragende Retentions- bzw. Entwässerungsleistung zeigen sollen. Das Beispiel, dessen Polydiolbaustein ein Durchschnittsmolekulargewicht von 6000 zeigt, ist demnach schon zu den nunmehr im folgenden kurz diskutierten Vergleichsbeispielen zu rechnen. Als weiteres Vergleichsbeispiel ist das in der Tabelle 4 aufgeführte Beispiel 1 bl zu werten. Es soll zeigen, daß ohne den Einbau des erfindungsgemäße,i Teilproduktes A, also nur bei Vernetzung des bekannten Zwischenproduktes B mit Epichlorhydrin das daraus resultierende Hilfsmittel zur Verbesserung der Retention, Entwässerung und Aufbereitung nur wesentlich schlechtere Retentions-, Entwässerungs- und Flockungswerte liefert als Produkte, die gemäß den erfindungsgemäßen Beispielen hergestellt worden sind. In der Tabelle 5 finden sich darüber hinaus noch weitere erfindungsgemäße Beispiele, die den hier wichtigsten Stand der Technik-Veröffentlichungen entnommen sind:
- Beispiel 12 entspricht dem Beispiel 1 aus der DE-PS 1 771 814;
- Beispiel 13 entspricht dem Beispiel 1 aus der DE-OS 2 353 430;
- Beispiel 14 entspricht dem Beispiel 1 aus der DE-PS 2 502 874.
- Example 12 corresponds to Example 1 from DE-PS 1 771 814;
- Example 13 corresponds to Example 1 from DE-OS 2 353 430;
- Example 14 corresponds to Example 1 from DE-PS 2 502 874.
Wie bereits weiter oben ausgeführt, beweist die Gegenüberstellung der erfindungsgemäßen Beispiele zu den Stand-der-Technik-Beispielen bei der Produktanwendung gemäß Tabelle 5, daß die erfindungsgemäßen Produkte hinsichtlich der Entwässerungsbeschleunigung den bisher bekanntgewordenen Produkten deutlich überlegen sind. Im gleichen Sinn ist hierzu auch die aus Tabelle 6 ersichtliche Gegenüberstellung der Füllstoffretentionsleistungen der entsprechenden Produkte zu interpretieren.As already explained above, the comparison of the examples according to the invention with the prior art examples in the use of products according to Table 5 proves that the products according to the invention are clearly superior to the previously known products with regard to the drainage acceleration. In the same sense, the comparison of filler retention performance of the corresponding products shown in Table 6 should also be interpreted.
Es folgen nun die einzelnen Beispiele:The individual examples now follow:
In einem 4 Liter fassenden Glasrundkolben, der mit einem handelsüblichen Ankerrührer, einem Thermometer, einem Rückflußkühler und einem Zulauftrichter ausgestattet ist, werden 160 g Polyäthylenglykoläther mit einem mittleren Molekulargewicht von 400 entsprechend 0,4 Mole vorgelegt und mit 2 ml der Bortrifluorid-Ätherat-Katalysatorlösung (Katalysator-Summenformel: C4H,oBF30) vermischt. Diese Mischung wird mit Hilfe eines Wasserbades auf 60° C erwärmt und das in der Mischung befindliche Polydiol mit langsam zugefügten 75,5 g Epichlorhydrin, entsprechend 0,8 Mole, umgesetzt. Die Umsetzung erfolgt bei einer Reaktionstemperatur von höchstens 65° C in einer Zeit von 2,5 Stunden in Form einer Anlagerungsreaktion. Das entstandene Produkt, nämlich Polyäthylenglykoläther-bis-ß-hydroxy-y-chlorpropyläther, wird nun nach Hinzufügung von 271,7 ml entionisiertem Wasser, welches bei 65°C in zwei Minuten eingerührt wird, mit 35,4 g DTRA, entsprechend 0,336 Mole über einen Zulauftrichter versetzt. Während der hierdurch ausgelösten Reaktion zwischen dem DTRA und dem vorgenannten Zwischenprodukt wird die Temperatur notfalls mittels Wasserkühlung bei 65°C gehalten. Nach einer Stunde sinkt infolge der Beendigung der Umsetzungsreaktion zwischen den vorgenannten Substanzen die Reaktionslösungs-Temperatur. Das auf diese Weise entstandene Teilprodukt A (ß-hydroxy-y-chlorpropylpolyäthylenglykoläther-ß-hydroxy-y-propylamin) ergab bei seiner Analyse folgende Werte:
In einem als Stahtautoklaven ausgebildeten Druckgefäß mit Rührer, Temperaturmesser in Form eines Thermofühlers und Abdestillationskondensator wurden 1460,2 g Adipinsäure (100gewichtsprozentig entsprechend 10 Mol, fest); 1124,5 g Diäthylentriamin (100gewichtsprozentig entsprechend 10,9 Mol; flüssig) und 226,34 g Caprolactam (100gewichtsprozentig entsprechend 2 Mol; fest) in Form ihrer Reinsubstanzen eingefüllt. Nach Überschichtung des vorgenannten Füllgutes mit sauerstofffreiem Stickstoff, der somit das überstehende Restgasgemisch ersetzt, wird nach Abschluß des Reaktionsgefäßes der Gefäßinhalt auf 160°C aufgeheizt und bei dieser Temperatur 30 Minuten lang unter Rühren belassen. Danach wird das freiwerdende Reaktionswasser abdestilliert (insgesamt 360 ml entsprechend 100% der Theorie). Das nunmehr kondensationswasserfreie Reaktionsgemisch wird darauf weiter bis auf 180° C erhitzt und bei dieser Temperatur zwei weitere Stunden gerührt. Hierbei reagiert das Gemisch weiter, wobei über die kondensierende Reaktionsmasse ständig Stickstoff geleitet wird.1460.2 g of adipic acid (100% by weight corresponding to 10 mol, solid) were placed in a pressure vessel designed as a steel autoclave with a stirrer, a temperature sensor in the form of a thermal sensor and a distillation condenser; 1124.5 g of diethylenetriamine (100% by weight corresponding to 10.9 mol; liquid) and 226.34 g of caprolactam (100% by weight corresponding to 2 mol; solid) were introduced in the form of their pure substances. After the above-mentioned filling material has been overlaid with oxygen-free nitrogen, which thus replaces the supernatant residual gas mixture, the contents of the vessel are heated to 160 ° C. after the end of the reaction vessel and left at this temperature for 30 minutes with stirring. The water of reaction released is then distilled off (a total of 360 ml, corresponding to 100% of theory). The reaction mixture, which is now free of condensation, is then further heated to 180 ° C. and stirred at this temperature for a further two hours. The mixture reacts further, nitrogen being continuously passed through the condensing reaction mass.
Nach Abkühlung der entstandenen Polykondensatschmelze auf 135° C werden dieser unter weiterer Abkühlung der Substanz insgesamt 2553 ml Wasser zugesetzt. Die entstandene wäßrige Polyaminoamidharzlösung wird nunmehr untersucht und zeigt folgende Untersuchungsergebnis-Werte:
In den bereits im vorstehenden Beispiel 1a beschriebenen 4 Liter Inhalt fassenden Glasrundkolben werden 543,4 g des 50gewichtsprozentigen Teilproduktes A entsprechend 0,4 Mole, bezogen auf Polydiol 400 in Form des β-hydroxy-γ-chlorpropyl-polyäthylenglykoläther-β-hydroxy-γ-propylamin zunächst mit der gleichen Gewichtsmenge an Wasser versetzt, so daß eine 25gewichtsprozentige Lösung entsteht.543.4 g of the 50% by weight partial product A corresponding to 0.4 mole, based on polydiol 400 in the form of β-hydroxy-γ-chloropropyl-polyethyleneglycol ether-β-hydroxy-γ, are added to the 4 liter glass round bottom flask already described in Example 1a above -propylamine first mixed with the same amount by weight of water, so that a 25 weight percent solution is formed.
Hierzu werden dann 624,4 g einer 48gewichtsprozentigen Lösung des Teilproduktes B, wie es in vorstehendem Beispiel 1b in bekannter Weise hergestellt worden ist, in Form der basischen Polyaminoamidharzlösung zugegeben und das Ganze dann mit 574,4 g Wasser unter Rühren versetzt. Dann wird unter weiter fortgesetztem Rühren der vorgenannte Gefäßinhalt innerhalb von zwei Stunden auf 80° C erwärmt, wobei die Halogengruppe des Teilprodukts A mit den - NH-Gruppierungen des Teilprodukts B unter Abspaltung von Halogenwasserstoffsäure unter Bildung des Zwischenprodukts AB reagierten. Sobald das Produkt AB entstanden ist, werden 11,35 ml Epichlorhydrin als 98gewichtsprozentiges Produkt mit einer Dichte von 1,18 g cm-3 unter Einhaltung der oben angeführten Temperatur dem Gefäßinhalt zudosiert. Nach 7,5 Stunden Reaktionsdauer zwischen dem o. a. Zwischenprodukt AB und dem diesen zugeführten Epichlorhydrin hört das reaktionsbedingte Ansteigen der Viskosität praktisch auf, womit das Endprodukt C in Form einer hochviskosen klaren Lösung von Polyäthylenglykoläther-Amin-Polyaminoamid-Epichlorhydrinharz entstanden ist. Die Untersuchung des vorstehenden erfindungsgemäßen Endproduktes C ergab folgende Werte:
Wie bereits oben ausgeführt, werden die folgenden weiteren, in den folgenden Tabellen zusammengefaßten Beispiele in der gleichen Weise wie für das vorstehende Beispiel 1a, 1b und 1c angegeben, unter den gleichen Verfahrensbedingungen durchgeführt. Wie ebenfalls bereits genannt, sind in den folgenden Tabellen die vorstehenden Textbeispiele 1a, 1b und 1c der besseren Übersicht halber noch einmal zusammengefaßt mit aufgeführt.As already stated above, the following further examples, summarized in the tables below, are carried out in the same manner as given for the above examples 1a, 1b and 1c, under the same process conditions. As already mentioned, the text examples 1a, 1b and 1c above are summarized in the following tables for the sake of clarity.
Beispiel 10 der DE-OS 2 434 816 wurde nachgearbeitet, indem das Polyaminoamid V 12 (hergestellt aus Adipinsäure, Diethylentriamin und Hexamethylendiaminadipat) mit dem Vernetzer V 4 (Umsetzungsprodukt aus Polyethylenglykol und Epichlorhydrin) gemäß der Beschreibung der Beispiele 1 bis 14 auf Seite 12 der DE-OS umgesetzt wurde. Die Viskosität der 18prozentigen Lösung der Kondensationsprodukte betrug 609 mPa . s (Schergefälle 24,5 sec-1 bei 20° C).Example 10 of DE-OS 2 434 816 was reworked by adding the polyaminoamide V 12 (produced from adipic acid, diethylenetriamine and hexamethylenediamine adipate) with the crosslinker V 4 (reaction product from polyethylene glycol and epichlorohydrin) according to the description of Examples 1 to 14 on page 12 of the DE-OS was implemented. The viscosity of the 18 percent solution the condensation products were 609 mPa. s (shear rate 24.5 sec -1 at 20 ° C).
Die Entwässerungsbeschleunigung durch Mahlgradsenkung und die Füllstoffretentionsleistung bestimmt durch den Aschegehalt wurde - wie in der vorliegenden Anmeldung angegeben - bestimmt und in die beiliegenden Tabellen 5 und 6 als Vergleichsbeispiel 15 eingetragen.
Das erfindungsgemäße Polyethylenglykol-Polyaminoamid-Kondensationsprodukt zur Retentionsverbesserung von ausschwemmbaren Feststoffen, zur Entwässerungsbeschleunigung von Suspensionen und zur rascheren Aufbereitung von industriellen Wässeren, Abwässern und Schlämmen durch Zusatz von basischen wasserlöslichen Polymeren als wäßrige Polymerlösung läßt sich zwar hauptsächlich in der Papierindustrie vorteilhaft verwenden, ist jedoch gleichzeitig auch sehr gut geeignet zur Aufbereitung von Industriewässern, zur Abwasserreinigung sowie zur Schlammkonditionierung in anderen Industriezweigen. Unter den Begriff »Schlammaufbereitung« fällt hierbei die Aufbereitung von Frischschlamm und Belebtschlamm wie auch die an sich bekannten Schlammeindickungs- und Schlammflotationsverfahren, bei denen das erfindungsgemäße Hilfsmittel sehr gut eingesetzt werden kann. Es ist hierbei sehr vorteilhaft, daß diese Hilfsmittel zum Beispiel im Klärprozeß unempfindlich gegen die Hinzufügung einer Reihe verschiedener anderer Stoffe sind, weswegen es ohne weiteres möglich ist, zum Beispiel anorganische Flockungsmittel, wie sie zum Beispiel auf der Basis von Aluminium- und Eisensalzen oder auf der Basis von Kalkverbindungen im Handel sind, zuzusetzen, ohne daß das erfindungsgemäße Hilfsmittel hinsichtlich seiner Verwendungseigenschaften hiervon nachteilig betroffen wird.The polyethylene glycol-polyaminoamide condensation product according to the invention for improving the retention of washable solids, for accelerating the dewatering of suspensions and for the faster treatment of industrial waters, wastewater and sludges by adding basic water-soluble polymers as an aqueous polymer solution can be used primarily advantageously in the paper industry, but is at the same time advantageous also very well suited for the treatment of industrial water, waste water purification and sludge conditioning in other branches of industry. The term "sludge treatment" includes the treatment of fresh sludge and activated sludge as well as the sludge thickening and sludge flotation processes known per se, in which the aid according to the invention can be used very well. It is very advantageous here that these auxiliaries, for example in the clarification process, are insensitive to the addition of a number of different substances, which is why it is readily possible, for example inorganic flocculants, such as those based on aluminum and iron salts or on the base of lime compounds are commercially available, without the auxiliary properties of the invention being adversely affected in terms of their use properties.
Wird das erfindungsgemäße Hilfsmittel in Absetz- und Klärbecken verwendet, empfiehlt sich seine Anwendung in einer Menge von etwa 0,1 bis 4 mg pro Liter der zu klärenden Substanz.If the aid according to the invention is used in sedimentation and clarification tanks, it is recommended to use it in an amount of approximately 0.1 to 4 mg per liter of the substance to be clarified.
In anderen Fällen, etwa bei der Konditionierung von Abwasserschlämmen, bei der Entwässerung in Trockengelen oder bei der Anwendung mechanischer Verfahren wie zum Beispiel Zentrifugieren kann dem Schlamm das Wasser besser und rascher entzogen werden, wenn man das erfindungsgemäße Hilfsmittel in Mengen von etwa 2 bis 12 kg pro Tonne Trockenschlamm der zu behandelnden Substanz zusetzt.In other cases, for example in the conditioning of waste water sludges, in dewatering in dry gels or in the use of mechanical processes such as centrifugation, the water can be removed from the sludge better and more quickly if the auxiliary according to the invention is used in amounts of about 2 to 12 kg per ton of dry sludge is added to the substance to be treated.
Soll der zu behandelnde Schlamm stabilisiert werden, ist es zweckmäßig, etwa 50 bis 150 mg des erfindungsgemäßen Hilfsmittels hierzu pro entsprechender Mengeneinheit des Schlamms diesem zuzusetzen. Die Stabilisierung tritt hierbei mittels Förderung der Bildung reißfester Flocken durch das Hilfsmittel in vorteilhafter Weise ein.If the sludge to be treated is to be stabilized, it is appropriate to add about 50 to 150 mg of the Aids according to the invention are added to the sludge for each corresponding unit of quantity. The stabilization advantageously occurs by promoting the formation of tear-resistant flakes by the aid.
Im Rahmen der als wesentlichstes Verwendungsgebiet für das erfindungsgemäße Hilfsmittel anzuführenden Papierherstellung kann das genannte Hilfsmittel selbstverständlich nicht nur gesondert, sondern auch unter Abmischung mit den bei der Papierherstellung benötigten anderen Stoffen, wie zum Beispiel Farbstoffen, Antioxydantien, optischen Aufhellern und fluoreszierenden Mitteln zugesetzt werden, da das Hilfsmittel gegen diese Stoffe nicht empfindlich ist. In der Praxis wird nämlich oft das vorgenannte Zusatzverfahren vorheriger Abmischung der Zusatzstoffe deswegen gerne angewendet, weil im allgemeinen zum Beispiel optische Aufheller und fluoreszierende Mittel in nur geringen Mengen im Papier benötigt werden, um die gewünschte Veränderung des Erscheinungsbildes des Papiers zu erreichen.In the context of the papermaking to be mentioned as the most important field of use for the auxiliary according to the invention, the said auxiliary can of course not only be added separately, but also in admixture with the other substances required in papermaking, such as dyes, antioxidants, optical brighteners and fluorescent agents, since the aid is not sensitive to these substances. In practice, the aforementioned additional method of prior mixing of the additives is often used because, for example, optical brighteners and fluorescent agents are generally only required in small amounts in the paper in order to achieve the desired change in the appearance of the paper.
Weitere Anwendungsgebiete des erfindungsgemäßen Hilfsmittels im Rahmen der Papierherstellung beziehen sich auf die vorteilhafte Leistung des Mittels bei der Erzielung einer guten Scherstabilität, die wichtig ist, wenn zum Beispiel Pumpen, Schwingsiebe und andere Vorrichtungen bei der Papierherstellung verwendet werden.Further areas of application of the aid according to the invention in the context of paper manufacture relate to the advantageous performance of the agent in achieving good shear stability, which is important if, for example, pumps, vibrating sieves and other devices are used in paper manufacture.
Außer bei der Papierherstellung kann natürlich das erfindungsgemäße Hilfsmittel auch auf ganz anderen als den vorgenannten Gebietsgruppen eingesetzt werden. Als Haarfixiermittel oder bei der Verankerung von an sich hydrophoben Beschichtungsmitteln, die in Form von wäßrigen Dispersionen oder sonstigen Lösungen etwa auf Trägersubstanzen wie zum Beispiel Flächengebilden aller Art aufgebracht werden, läßt sich das Mittel genausogut wie als Verbesserungsmittel für die Naßfestigkeit von Flächengebilden (insbesondere Papier) einsetzen, in letztgenanntem Fall jedoch vorteilhaft nach Sauerstellung des Mittels.In addition to papermaking, the auxiliary according to the invention can of course also be used in completely different areas than those mentioned above. As a hair fixative or for anchoring inherently hydrophobic coating compositions, which are applied in the form of aqueous dispersions or other solutions, for example to carrier substances such as fabrics of all kinds, the agent can be used as well as an improver for the wet strength of fabrics (especially paper). use, in the latter case, however, advantageously after acidification of the agent.
Im allgemeinen ist das erfindungsgemäße Hilfsmittel selbst im basischen Medium recht gut lagerstabil, wenn, wie der Fachmann an sich weiß, bei der Herstellung des Mittels zur Vernetzung zum Beispiel mit Hilfe von Epichlorhydrin nur soviel Vernetzungsmittel wie benötigt zugegeben wird.In general, the auxiliary according to the invention is very stable in storage even in the basic medium if, as the person skilled in the art knows, only as much crosslinking agent as required is added in the preparation of the crosslinking agent, for example using epichlorohydrin.
Bei unüblichem oder versehentlichem Zugeben des Vernetzungsmittels im Uberschuß kann das Mittel trotzdem verwendet werden, muß allerdings dann zwecks Erzielung einer geeigneten Lagerstabilität sauer gestellt werden, womit auch in diesem Fall ein eventuell sonst auftretendes Ausgelieren zuverlässig verhindert wird.If the crosslinking agent is added in excess or in an inadvertent manner, the agent can still be used, but must then be acidified in order to achieve a suitable storage stability, which also reliably prevents any gelling that might otherwise occur in this case.
Claims (6)
and/or
on the reaction product
the component product B has been formed from at least one polyalkylene polyamine and/or at least one aminocarboxylic acid or its lactam and/or hexamethylene diammonium adipate, the quantitative prooortions in the preparation of the intermediate product AB have been selected such that to each 1 mole, based on polyethylene glycol, of component product A, 0.5 to 7 moles, based on polyalkylene polyamine, of component product B, are added and the intermediate product AB has been obtained by reacting the halogen groups of component product A with the -NH-groupings of component product B with elimination of hydrohalic acids.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE2736651 | 1977-08-13 | ||
| DE19772736651 DE2736651A1 (en) | 1977-08-13 | 1977-08-13 | TOOLS FOR IMPROVING RETENTION, DRAINAGE AND PROCESSING, IN PARTICULAR IN PAPER MANUFACTURING |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| EP0000714A2 EP0000714A2 (en) | 1979-02-21 |
| EP0000714A3 EP0000714A3 (en) | 1979-03-21 |
| EP0000714B1 true EP0000714B1 (en) | 1982-03-31 |
Family
ID=6016378
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP78100444A Expired EP0000714B1 (en) | 1977-08-13 | 1978-07-19 | Auxiliary agent for the improvement of retention, dehydration and preparation, especially for the manufacture of paper |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US4267059A (en) |
| EP (1) | EP0000714B1 (en) |
| JP (1) | JPS5432186A (en) |
| AT (1) | AT365681B (en) |
| CA (1) | CA1124963A (en) |
| DE (2) | DE2736651A1 (en) |
| FI (1) | FI64177C (en) |
| IT (1) | IT1112697B (en) |
| NO (1) | NO151625C (en) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2141130A (en) * | 1983-06-09 | 1984-12-12 | Grace W R & Co | Polyamidoaminepolyamines |
| EP0158247A1 (en) * | 1984-04-11 | 1985-10-16 | Bayer Ag | Paper-making auxiliary agent |
| US5395412A (en) * | 1991-01-15 | 1995-03-07 | Poly Id Ag | Method and apparatus for the treatment of fiber pieces |
| WO1999006469A1 (en) * | 1997-07-29 | 1999-02-11 | Hercules Incorporated | Polyamidoamine/epichlorohydrin resins bearing polyol sidechains as dry strength agents |
| US5886095A (en) * | 1996-05-30 | 1999-03-23 | Wolff Walsrode Ag | Process for the preparation of retention and dewatering agents based on polyamino-ethers |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4347339A (en) * | 1981-05-08 | 1982-08-31 | Nalco Chemical Company | Cationic block copolymers |
| US6896769B2 (en) | 1999-01-25 | 2005-05-24 | Kimberly-Clark Worldwide, Inc. | Modified condensation polymers containing azetidinium groups in conjunction with amphiphilic hydrocarbon moieties |
| US6398911B1 (en) | 2000-01-21 | 2002-06-04 | Kimberly-Clark Worldwide, Inc. | Modified polysaccharides containing polysiloxane moieties |
| US6517678B1 (en) | 2000-01-20 | 2003-02-11 | Kimberly-Clark Worldwide, Inc. | Modified polysaccharides containing amphiphillic hydrocarbon moieties |
| US6596126B1 (en) | 1999-01-25 | 2003-07-22 | Kimberly-Clark Worldwide, Inc. | Modified polysaccharides containing aliphatic hydrocarbon moieties |
| US6465602B2 (en) | 2000-01-20 | 2002-10-15 | Kimberly-Clark Worldwide, Inc. | Modified condensation polymers having azetidinium groups and containing polysiloxane moieties |
| US10662586B2 (en) | 2017-06-28 | 2020-05-26 | Gpcp Ip Holdings Llc | Cationic polyetheramine dispersants for preparing papermaking stock |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1771043C3 (en) * | 1968-03-27 | 1979-05-23 | Bayer Ag, 5090 Leverkusen | Self-crosslinking water-soluble products and their use as wet strength agents for paper |
| DE1771814C2 (en) * | 1968-07-16 | 1974-05-09 | Bayer Ag, 5090 Leverkusen | Use of auxiliary materials for paper production |
| CH541595A (en) * | 1970-06-05 | 1973-09-15 | Sandoz Ag | Process for the production of new polyether amines |
| DE2353430C2 (en) * | 1973-10-25 | 1982-04-15 | Wolff Walsrode Ag, 3030 Walsrode | Process for the production of cationic polyamino polyamides and their use as paper-making auxiliaries |
| DE2434816C3 (en) * | 1974-07-19 | 1981-01-22 | Basf Ag, 6700 Ludwigshafen | Process for the production of nitrogen-containing condensation products and their use as retention aids, flocculants and dewatering accelerators in paper manufacture |
-
1977
- 1977-08-13 DE DE19772736651 patent/DE2736651A1/en not_active Withdrawn
-
1978
- 1978-07-19 EP EP78100444A patent/EP0000714B1/en not_active Expired
- 1978-07-19 DE DE7878100444T patent/DE2861707D1/en not_active Expired
- 1978-08-02 CA CA308,579A patent/CA1124963A/en not_active Expired
- 1978-08-10 NO NO782730A patent/NO151625C/en unknown
- 1978-08-11 AT AT0587278A patent/AT365681B/en active
- 1978-08-11 FI FI782461A patent/FI64177C/en not_active IP Right Cessation
- 1978-08-11 IT IT26760/78A patent/IT1112697B/en active
- 1978-08-11 JP JP9744478A patent/JPS5432186A/en active Pending
-
1979
- 1979-10-15 US US06/084,647 patent/US4267059A/en not_active Expired - Lifetime
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2141130A (en) * | 1983-06-09 | 1984-12-12 | Grace W R & Co | Polyamidoaminepolyamines |
| FR2547303A1 (en) * | 1983-06-09 | 1984-12-14 | Grace W R Ltd | WATER-SOLUBLE POLYAMIDOAMINEPOLYAMINE AND PROCESS FOR PRODUCING SHEET PRODUCT BASED ON CELLULOSIC FIBER |
| EP0158247A1 (en) * | 1984-04-11 | 1985-10-16 | Bayer Ag | Paper-making auxiliary agent |
| US5395412A (en) * | 1991-01-15 | 1995-03-07 | Poly Id Ag | Method and apparatus for the treatment of fiber pieces |
| US5886095A (en) * | 1996-05-30 | 1999-03-23 | Wolff Walsrode Ag | Process for the preparation of retention and dewatering agents based on polyamino-ethers |
| WO1999006469A1 (en) * | 1997-07-29 | 1999-02-11 | Hercules Incorporated | Polyamidoamine/epichlorohydrin resins bearing polyol sidechains as dry strength agents |
| US6165322A (en) * | 1997-07-29 | 2000-12-26 | Hercules Incorporated | Polyamidoamine/epichlorohydrin resins bearing polyol sidechains as dry strength agents |
| AU732514B2 (en) * | 1997-07-29 | 2001-04-26 | Hercules Incorporated | Polyamidoamine/epichlorohydrin resins bearing polyol sidechains as dry strength agents |
Also Published As
| Publication number | Publication date |
|---|---|
| DE2861707D1 (en) | 1982-05-06 |
| IT7826760A0 (en) | 1978-08-11 |
| NO151625B (en) | 1985-01-28 |
| US4267059A (en) | 1981-05-12 |
| EP0000714A2 (en) | 1979-02-21 |
| NO782730L (en) | 1979-02-14 |
| DE2736651A1 (en) | 1979-02-15 |
| ATA587278A (en) | 1981-06-15 |
| IT1112697B (en) | 1986-01-20 |
| CA1124963A (en) | 1982-06-08 |
| FI64177C (en) | 1983-10-10 |
| JPS5432186A (en) | 1979-03-09 |
| FI782461A7 (en) | 1979-02-14 |
| FI64177B (en) | 1983-06-30 |
| EP0000714A3 (en) | 1979-03-21 |
| AT365681B (en) | 1982-02-10 |
| NO151625C (en) | 1985-05-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE2835876C2 (en) | Cationic polymeric flocculant | |
| DE2616220C2 (en) | Cationic water-soluble amine-epichlorohydrin polycondensates, processes for their preparation and their use | |
| DE1771814C2 (en) | Use of auxiliary materials for paper production | |
| DE3027126C2 (en) | ||
| DE60311467T2 (en) | DISPERSION OF WATER-SOLUBLE POLYMER, METHOD OF MANUFACTURING THEREOF AND USE METHOD THEREFOR | |
| EP0675914B1 (en) | Water-soluble condensation products of compounds containing amino groups with cross-linking agents, method of preparing them and their use | |
| DE2434816C3 (en) | Process for the production of nitrogen-containing condensation products and their use as retention aids, flocculants and dewatering accelerators in paper manufacture | |
| DE1802435C3 (en) | Process for the production of crosslinked resins based on basic polyamidoamines and their use as drainage aids, retention aids and flocculants in paper manufacture | |
| DE2934854A1 (en) | METHOD FOR PRODUCING NITROGEN-CONDENSING PRODUCTS AND THE USE THEREOF | |
| DE1795392A1 (en) | Cation-active, water-soluble polyamides | |
| EP0000714B1 (en) | Auxiliary agent for the improvement of retention, dehydration and preparation, especially for the manufacture of paper | |
| DE2502914A1 (en) | FUNCTIONAL IONIC COMPOSITIONS AND THEIR USE | |
| DE3721426A1 (en) | N-VINYLFORMAMIDE COPOLYMERS AND METHOD FOR THE PRODUCTION THEREOF | |
| DE3135830A1 (en) | METHOD FOR THE PRODUCTION OF WATER-SOLUBLE, NITROGEN-CONDENSING PRODUCTS AND THE USE THEREOF IN PAPER PRODUCTION | |
| DE69400997T2 (en) | Composition for the production of wet-strength paper | |
| DE2127082B2 (en) | Process for the production of water-soluble, high molecular weight polyether amines and their salts and their use | |
| DE1176362B (en) | Process for the production of polyadducts | |
| DE2156215C3 (en) | Methods to increase retention and retention aids | |
| EP0005241A1 (en) | Polyalkylene polyamines containing quaternary ammonium groups, method for their preparation and their use as auxiliary agents in paper making | |
| CH663792A5 (en) | METHOD FOR PRODUCING A WATER-SOLUBLE POLYAMIDOAMINE POLYAMINE, ITS PRODUCT AND USE THEREOF FOR PRODUCING A CELLULOSE FIBER PRODUCT. | |
| DE2353430C2 (en) | Process for the production of cationic polyamino polyamides and their use as paper-making auxiliaries | |
| EP0158247B1 (en) | Paper-making auxiliary agent | |
| DE3783772T2 (en) | METHOD FOR PRODUCING CATIONIC WATER-EXTINGUISHABLE RESINS AND MEANS FOR TREATING WATER. | |
| DE1770150A1 (en) | Polyacrylamide-based wet strength resin and paper made with it | |
| EP0278336B1 (en) | Agents for paper production |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Designated state(s): CH DE FR GB NL SE |
|
| AK | Designated contracting states |
Designated state(s): CH DE FR GB NL SE |
|
| 17P | Request for examination filed | ||
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Designated state(s): CH DE FR GB NL SE |
|
| REF | Corresponds to: |
Ref document number: 2861707 Country of ref document: DE Date of ref document: 19820506 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: SE Payment date: 19840630 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19840709 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: NL Payment date: 19860731 Year of fee payment: 9 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Effective date: 19870720 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19880201 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee | ||
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19880331 |
|
| GBPC | Gb: european patent ceased through non-payment of renewal fee | ||
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES Effective date: 19881117 |
|
| EUG | Se: european patent has lapsed |
Ref document number: 78100444.5 Effective date: 19880713 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19950619 Year of fee payment: 18 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: CH Payment date: 19950726 Year of fee payment: 18 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: CH Effective date: 19960731 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19970402 |
|
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |