CN115873123A - 抗lag3双特异性抗体、药物组合物及用途 - Google Patents
抗lag3双特异性抗体、药物组合物及用途 Download PDFInfo
- Publication number
- CN115873123A CN115873123A CN202211199026.4A CN202211199026A CN115873123A CN 115873123 A CN115873123 A CN 115873123A CN 202211199026 A CN202211199026 A CN 202211199026A CN 115873123 A CN115873123 A CN 115873123A
- Authority
- CN
- China
- Prior art keywords
- antibody
- seq
- amino acid
- variable region
- chain variable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 6
- 230000027455 binding Effects 0.000 claims abstract description 116
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 98
- 238000009739 binding Methods 0.000 claims abstract description 95
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 92
- 239000012634 fragment Substances 0.000 claims abstract description 81
- 102000017578 LAG3 Human genes 0.000 claims abstract description 72
- 101001137987 Homo sapiens Lymphocyte activation gene 3 protein Proteins 0.000 claims abstract description 70
- 239000000427 antigen Substances 0.000 claims abstract description 63
- 108091007433 antigens Proteins 0.000 claims abstract description 62
- 102000036639 antigens Human genes 0.000 claims abstract description 62
- 125000003275 alpha amino acid group Chemical group 0.000 claims abstract 42
- 206010028980 Neoplasm Diseases 0.000 claims description 35
- 239000013598 vector Substances 0.000 claims description 33
- 150000007523 nucleic acids Chemical class 0.000 claims description 29
- 238000002965 ELISA Methods 0.000 claims description 28
- 108060003951 Immunoglobulin Proteins 0.000 claims description 27
- 102000018358 immunoglobulin Human genes 0.000 claims description 27
- 230000035772 mutation Effects 0.000 claims description 24
- 238000000034 method Methods 0.000 claims description 23
- 238000002360 preparation method Methods 0.000 claims description 21
- 238000011282 treatment Methods 0.000 claims description 12
- 108010047041 Complementarity Determining Regions Proteins 0.000 claims description 11
- 201000001441 melanoma Diseases 0.000 claims description 9
- 108020004707 nucleic acids Proteins 0.000 claims description 9
- 102000039446 nucleic acids Human genes 0.000 claims description 9
- 208000000461 Esophageal Neoplasms Diseases 0.000 claims description 8
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 8
- 206010030155 Oesophageal carcinoma Diseases 0.000 claims description 8
- 201000004101 esophageal cancer Diseases 0.000 claims description 8
- 208000019691 hematopoietic and lymphoid cell neoplasm Diseases 0.000 claims description 8
- 201000005202 lung cancer Diseases 0.000 claims description 8
- 208000020816 lung neoplasm Diseases 0.000 claims description 8
- 239000000126 substance Substances 0.000 claims description 8
- 230000008685 targeting Effects 0.000 claims description 8
- 101000961149 Homo sapiens Immunoglobulin heavy constant gamma 4 Proteins 0.000 claims description 7
- 102100039347 Immunoglobulin heavy constant gamma 4 Human genes 0.000 claims description 7
- 238000004113 cell culture Methods 0.000 claims description 7
- 206010009944 Colon cancer Diseases 0.000 claims description 6
- 206010033128 Ovarian cancer Diseases 0.000 claims description 6
- 206010061535 Ovarian neoplasm Diseases 0.000 claims description 6
- 208000006265 Renal cell carcinoma Diseases 0.000 claims description 6
- 239000003814 drug Substances 0.000 claims description 6
- 208000002154 non-small cell lung carcinoma Diseases 0.000 claims description 6
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 claims description 6
- 101000840257 Homo sapiens Immunoglobulin kappa constant Proteins 0.000 claims description 5
- 101710138871 Ig gamma-1 chain C region Proteins 0.000 claims description 5
- 102100039345 Immunoglobulin heavy constant gamma 1 Human genes 0.000 claims description 5
- 102100029572 Immunoglobulin kappa constant Human genes 0.000 claims description 5
- 208000007502 anemia Diseases 0.000 claims description 5
- 208000029742 colonic neoplasm Diseases 0.000 claims description 5
- 208000005017 glioblastoma Diseases 0.000 claims description 5
- 206010005003 Bladder cancer Diseases 0.000 claims description 4
- 208000003174 Brain Neoplasms Diseases 0.000 claims description 4
- 206010006187 Breast cancer Diseases 0.000 claims description 4
- 208000026310 Breast neoplasm Diseases 0.000 claims description 4
- 206010017993 Gastrointestinal neoplasms Diseases 0.000 claims description 4
- 208000002250 Hematologic Neoplasms Diseases 0.000 claims description 4
- 208000008839 Kidney Neoplasms Diseases 0.000 claims description 4
- 206010061902 Pancreatic neoplasm Diseases 0.000 claims description 4
- 206010060862 Prostate cancer Diseases 0.000 claims description 4
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims description 4
- 208000015634 Rectal Neoplasms Diseases 0.000 claims description 4
- 206010038389 Renal cancer Diseases 0.000 claims description 4
- 208000024770 Thyroid neoplasm Diseases 0.000 claims description 4
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 claims description 4
- 238000012258 culturing Methods 0.000 claims description 4
- 201000010536 head and neck cancer Diseases 0.000 claims description 4
- 208000014829 head and neck neoplasm Diseases 0.000 claims description 4
- 201000010982 kidney cancer Diseases 0.000 claims description 4
- 208000032839 leukemia Diseases 0.000 claims description 4
- 201000007270 liver cancer Diseases 0.000 claims description 4
- 208000014018 liver neoplasm Diseases 0.000 claims description 4
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 claims description 4
- 201000002528 pancreatic cancer Diseases 0.000 claims description 4
- 208000008443 pancreatic carcinoma Diseases 0.000 claims description 4
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 4
- 206010038038 rectal cancer Diseases 0.000 claims description 4
- 201000001275 rectum cancer Diseases 0.000 claims description 4
- 206010041823 squamous cell carcinoma Diseases 0.000 claims description 4
- 201000002510 thyroid cancer Diseases 0.000 claims description 4
- 201000005112 urinary bladder cancer Diseases 0.000 claims description 4
- 230000002265 prevention Effects 0.000 claims description 3
- 241001529936 Murinae Species 0.000 claims description 2
- 241000894007 species Species 0.000 claims description 2
- 210000004027 cell Anatomy 0.000 description 134
- 150000001413 amino acids Chemical class 0.000 description 117
- 102100040678 Programmed cell death protein 1 Human genes 0.000 description 61
- 101710089372 Programmed cell death protein 1 Proteins 0.000 description 57
- 235000018102 proteins Nutrition 0.000 description 51
- 230000000694 effects Effects 0.000 description 40
- 238000001514 detection method Methods 0.000 description 39
- 102100029193 Low affinity immunoglobulin gamma Fc region receptor III-A Human genes 0.000 description 28
- 101710099301 Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 26
- 102100024216 Programmed cell death 1 ligand 1 Human genes 0.000 description 25
- UVCJGUGAGLDPAA-UHFFFAOYSA-N ensulizole Chemical compound N1C2=CC(S(=O)(=O)O)=CC=C2N=C1C1=CC=CC=C1 UVCJGUGAGLDPAA-UHFFFAOYSA-N 0.000 description 25
- 229920009537 polybutylene succinate adipate Polymers 0.000 description 25
- 239000000872 buffer Substances 0.000 description 22
- 239000006228 supernatant Substances 0.000 description 22
- 108010074708 B7-H1 Antigen Proteins 0.000 description 18
- 108091028043 Nucleic acid sequence Proteins 0.000 description 16
- 108010021468 Fc gamma receptor IIA Proteins 0.000 description 15
- 108010073807 IgG Receptors Proteins 0.000 description 15
- 239000012895 dilution Substances 0.000 description 15
- 238000010790 dilution Methods 0.000 description 15
- 238000002474 experimental method Methods 0.000 description 15
- 238000005406 washing Methods 0.000 description 15
- 102100029204 Low affinity immunoglobulin gamma Fc region receptor II-a Human genes 0.000 description 14
- 210000001744 T-lymphocyte Anatomy 0.000 description 14
- 108010021472 Fc gamma receptor IIB Proteins 0.000 description 13
- 230000004001 molecular interaction Effects 0.000 description 13
- 229960003301 nivolumab Drugs 0.000 description 13
- 229960002621 pembrolizumab Drugs 0.000 description 13
- 102100026122 High affinity immunoglobulin gamma Fc receptor I Human genes 0.000 description 12
- 102100029205 Low affinity immunoglobulin gamma Fc region receptor II-b Human genes 0.000 description 12
- 239000013604 expression vector Substances 0.000 description 12
- 238000011534 incubation Methods 0.000 description 12
- 235000004279 alanine Nutrition 0.000 description 11
- 210000000170 cell membrane Anatomy 0.000 description 11
- UQLDLKMNUJERMK-UHFFFAOYSA-L di(octadecanoyloxy)lead Chemical compound [Pb+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O UQLDLKMNUJERMK-UHFFFAOYSA-L 0.000 description 11
- 235000001014 amino acid Nutrition 0.000 description 10
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 10
- 239000002299 complementary DNA Substances 0.000 description 10
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 10
- 229940121484 relatlimab Drugs 0.000 description 10
- 230000028327 secretion Effects 0.000 description 10
- 230000000903 blocking effect Effects 0.000 description 9
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 9
- 244000144725 Amygdalus communis Species 0.000 description 8
- 241000699666 Mus <mouse, genus> Species 0.000 description 8
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 description 8
- 239000000611 antibody drug conjugate Substances 0.000 description 8
- 229940049595 antibody-drug conjugate Drugs 0.000 description 8
- 229960002685 biotin Drugs 0.000 description 8
- 239000011616 biotin Substances 0.000 description 8
- 238000013461 design Methods 0.000 description 8
- 201000010099 disease Diseases 0.000 description 8
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 8
- 108020001507 fusion proteins Proteins 0.000 description 8
- 102000037865 fusion proteins Human genes 0.000 description 8
- 230000014509 gene expression Effects 0.000 description 8
- 238000004806 packaging method and process Methods 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- 108091026890 Coding region Proteins 0.000 description 7
- 102000009109 Fc receptors Human genes 0.000 description 7
- 108010087819 Fc receptors Proteins 0.000 description 7
- 101001117317 Homo sapiens Programmed cell death 1 ligand 1 Proteins 0.000 description 7
- 102000000588 Interleukin-2 Human genes 0.000 description 7
- 108010002350 Interleukin-2 Proteins 0.000 description 7
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 7
- 241000700605 Viruses Species 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 7
- 230000009137 competitive binding Effects 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 239000013612 plasmid Substances 0.000 description 7
- 239000013641 positive control Substances 0.000 description 7
- 238000011160 research Methods 0.000 description 7
- 108090000790 Enzymes Proteins 0.000 description 6
- 102000004190 Enzymes Human genes 0.000 description 6
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 6
- 101150030213 Lag3 gene Proteins 0.000 description 6
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 231100000673 dose–response relationship Toxicity 0.000 description 6
- 238000013401 experimental design Methods 0.000 description 6
- 239000003446 ligand Substances 0.000 description 6
- 238000007799 mixed lymphocyte reaction assay Methods 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 239000012898 sample dilution Substances 0.000 description 6
- 241000283707 Capra Species 0.000 description 5
- 102100037850 Interferon gamma Human genes 0.000 description 5
- 108010074328 Interferon-gamma Proteins 0.000 description 5
- 241000699670 Mus sp. Species 0.000 description 5
- 125000003295 alanine group Chemical group N[C@@H](C)C(=O)* 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 201000011510 cancer Diseases 0.000 description 5
- 230000002860 competitive effect Effects 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 229920001184 polypeptide Polymers 0.000 description 5
- 108090000765 processed proteins & peptides Proteins 0.000 description 5
- 102000004196 processed proteins & peptides Human genes 0.000 description 5
- 230000001737 promoting effect Effects 0.000 description 5
- 210000003289 regulatory T cell Anatomy 0.000 description 5
- 229940126586 small molecule drug Drugs 0.000 description 5
- 230000009385 viral infection Effects 0.000 description 5
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 4
- 101100510617 Caenorhabditis elegans sel-8 gene Proteins 0.000 description 4
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- 102100020862 Lymphocyte activation gene 3 protein Human genes 0.000 description 4
- 102000043131 MHC class II family Human genes 0.000 description 4
- 108091054438 MHC class II family Proteins 0.000 description 4
- 229940125644 antibody drug Drugs 0.000 description 4
- 239000002246 antineoplastic agent Substances 0.000 description 4
- 230000001588 bifunctional effect Effects 0.000 description 4
- 238000010494 dissociation reaction Methods 0.000 description 4
- 230000005593 dissociations Effects 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 238000000684 flow cytometry Methods 0.000 description 4
- 238000003670 luciferase enzyme activity assay Methods 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 108091033319 polynucleotide Proteins 0.000 description 4
- 102000040430 polynucleotide Human genes 0.000 description 4
- 239000002157 polynucleotide Substances 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 238000004445 quantitative analysis Methods 0.000 description 4
- 230000019491 signal transduction Effects 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 238000012546 transfer Methods 0.000 description 4
- 238000002054 transplantation Methods 0.000 description 4
- 102000000802 Galectin 3 Human genes 0.000 description 3
- 108010001517 Galectin 3 Proteins 0.000 description 3
- 241000713666 Lentivirus Species 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 125000000539 amino acid group Chemical group 0.000 description 3
- 210000003719 b-lymphocyte Anatomy 0.000 description 3
- 229940127089 cytotoxic agent Drugs 0.000 description 3
- 239000012636 effector Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 230000001506 immunosuppresive effect Effects 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 238000011068 loading method Methods 0.000 description 3
- 210000003712 lysosome Anatomy 0.000 description 3
- 230000001868 lysosomic effect Effects 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 238000010369 molecular cloning Methods 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 239000012089 stop solution Substances 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 241001515965 unidentified phage Species 0.000 description 3
- 239000012224 working solution Substances 0.000 description 3
- 102100028666 C-type lectin domain family 4 member G Human genes 0.000 description 2
- 102000014447 Complement C1q Human genes 0.000 description 2
- 108010078043 Complement C1q Proteins 0.000 description 2
- 101000867232 Escherichia coli Heat-stable enterotoxin II Proteins 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- 101000766915 Homo sapiens C-type lectin domain family 4 member G Proteins 0.000 description 2
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 2
- 101001117312 Homo sapiens Programmed cell death 1 ligand 2 Proteins 0.000 description 2
- 206010062016 Immunosuppression Diseases 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 2
- 239000012515 MabSelect SuRe Substances 0.000 description 2
- 206010057249 Phagocytosis Diseases 0.000 description 2
- 102100024213 Programmed cell death 1 ligand 2 Human genes 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 208000036142 Viral infection Diseases 0.000 description 2
- VORIUEAZEKLUSJ-UHFFFAOYSA-M [(6-chlorobenzotriazol-1-yl)oxy-(dimethylamino)methylidene]-dimethylazanium;trifluoroborane;fluoride Chemical compound [F-].FB(F)F.C1=C(Cl)C=C2N(OC(N(C)C)=[N+](C)C)N=NC2=C1 VORIUEAZEKLUSJ-UHFFFAOYSA-M 0.000 description 2
- 238000001994 activation Methods 0.000 description 2
- 238000007792 addition Methods 0.000 description 2
- 230000000259 anti-tumor effect Effects 0.000 description 2
- 210000004436 artificial bacterial chromosome Anatomy 0.000 description 2
- 210000004507 artificial chromosome Anatomy 0.000 description 2
- 210000001106 artificial yeast chromosome Anatomy 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 230000008827 biological function Effects 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 210000004899 c-terminal region Anatomy 0.000 description 2
- 229910002092 carbon dioxide Inorganic materials 0.000 description 2
- 239000001569 carbon dioxide Substances 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000012228 culture supernatant Substances 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 230000029087 digestion Effects 0.000 description 2
- 239000012149 elution buffer Substances 0.000 description 2
- 230000003511 endothelial effect Effects 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 239000000147 enterotoxin Substances 0.000 description 2
- 238000001976 enzyme digestion Methods 0.000 description 2
- 239000013613 expression plasmid Substances 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 238000000703 high-speed centrifugation Methods 0.000 description 2
- 210000002865 immune cell Anatomy 0.000 description 2
- 230000001900 immune effect Effects 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 210000002751 lymph Anatomy 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 238000005457 optimization Methods 0.000 description 2
- 239000008188 pellet Substances 0.000 description 2
- 230000008782 phagocytosis Effects 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 238000012772 sequence design Methods 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- 238000004088 simulation Methods 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 230000009870 specific binding Effects 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 230000035899 viability Effects 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical group COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 1
- GOZMBJCYMQQACI-UHFFFAOYSA-N 6,7-dimethyl-3-[[methyl-[2-[methyl-[[1-[3-(trifluoromethyl)phenyl]indol-3-yl]methyl]amino]ethyl]amino]methyl]chromen-4-one;dihydrochloride Chemical compound Cl.Cl.C=1OC2=CC(C)=C(C)C=C2C(=O)C=1CN(C)CCN(C)CC(C1=CC=CC=C11)=CN1C1=CC=CC(C(F)(F)F)=C1 GOZMBJCYMQQACI-UHFFFAOYSA-N 0.000 description 1
- 108010032595 Antibody Binding Sites Proteins 0.000 description 1
- 241000228212 Aspergillus Species 0.000 description 1
- 238000011725 BALB/c mouse Methods 0.000 description 1
- 244000063299 Bacillus subtilis Species 0.000 description 1
- 235000014469 Bacillus subtilis Nutrition 0.000 description 1
- 108010041397 CD4 Antigens Proteins 0.000 description 1
- 102000008203 CTLA-4 Antigen Human genes 0.000 description 1
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- 241000255581 Drosophila <fruit fly, genus> Species 0.000 description 1
- 241001061257 Emmelichthyidae Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 108700028146 Genetic Enhancer Elements Proteins 0.000 description 1
- 102100034458 Hepatitis A virus cellular receptor 2 Human genes 0.000 description 1
- 101710083479 Hepatitis A virus cellular receptor 2 homolog Proteins 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 102000018713 Histocompatibility Antigens Class II Human genes 0.000 description 1
- 108010027412 Histocompatibility Antigens Class II Proteins 0.000 description 1
- 101000917826 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-a Proteins 0.000 description 1
- 101000917824 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-b Proteins 0.000 description 1
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 206010061534 Oesophageal squamous cell carcinoma Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 101710160107 Outer membrane protein A Proteins 0.000 description 1
- 241001631646 Papillomaviridae Species 0.000 description 1
- 241001645095 Parisis Species 0.000 description 1
- 241000276498 Pollachius virens Species 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 108020005091 Replication Origin Proteins 0.000 description 1
- 108700008625 Reporter Genes Proteins 0.000 description 1
- 241000700584 Simplexvirus Species 0.000 description 1
- 208000036765 Squamous cell carcinoma of the esophagus Diseases 0.000 description 1
- 206010042602 Supraventricular extrasystoles Diseases 0.000 description 1
- 230000006044 T cell activation Effects 0.000 description 1
- 108091008874 T cell receptors Proteins 0.000 description 1
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 1
- 229940126547 T-cell immunoglobulin mucin-3 Drugs 0.000 description 1
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 1
- 108091005906 Type I transmembrane proteins Proteins 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 230000003698 anagen phase Effects 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 230000009830 antibody antigen interaction Effects 0.000 description 1
- 210000000612 antigen-presenting cell Anatomy 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 239000003972 antineoplastic antibiotic Substances 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 239000003560 cancer drug Substances 0.000 description 1
- 238000002619 cancer immunotherapy Methods 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- 239000012930 cell culture fluid Substances 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000032823 cell division Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 229940044683 chemotherapy drug Drugs 0.000 description 1
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000004154 complement system Effects 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 239000012531 culture fluid Substances 0.000 description 1
- 239000002254 cytotoxic agent Substances 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 231100000517 death Toxicity 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 210000004443 dendritic cell Anatomy 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 230000000857 drug effect Effects 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 239000002158 endotoxin Substances 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 208000007276 esophageal squamous cell carcinoma Diseases 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000017188 evasion or tolerance of host immune response Effects 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 230000002538 fungal effect Effects 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 201000011066 hemangioma Diseases 0.000 description 1
- 201000005787 hematologic cancer Diseases 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 210000003917 human chromosome Anatomy 0.000 description 1
- 210000004408 hybridoma Anatomy 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 239000000677 immunologic agent Substances 0.000 description 1
- 229940124541 immunological agent Drugs 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 230000031700 light absorption Effects 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 239000003002 pH adjusting agent Substances 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 210000005134 plasmacytoid dendritic cell Anatomy 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 238000010837 poor prognosis Methods 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 238000003259 recombinant expression Methods 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 238000003998 size exclusion chromatography high performance liquid chromatography Methods 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 230000001502 supplementing effect Effects 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 231100000027 toxicology Toxicity 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 230000005026 transcription initiation Effects 0.000 description 1
- 108091006106 transcriptional activators Proteins 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 108091008578 transmembrane receptors Proteins 0.000 description 1
- 102000027257 transmembrane receptors Human genes 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 230000005909 tumor killing Effects 0.000 description 1
- 238000007492 two-way ANOVA Methods 0.000 description 1
- 241000701161 unidentified adenovirus Species 0.000 description 1
- 241000701447 unidentified baculovirus Species 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 210000000689 upper leg Anatomy 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- 210000005253 yeast cell Anatomy 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Public Health (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Biomedical Technology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Microbiology (AREA)
- Epidemiology (AREA)
- Physics & Mathematics (AREA)
- Hematology (AREA)
- Plant Pathology (AREA)
- Oncology (AREA)
- Diabetes (AREA)
- Mycology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
本发明属于生物医药领域,涉及一种抗LAG3抗体的双特异性抗体、其药物组合物及用途。具体地,所述双特异性抗体,其包括第一蛋白功能区和第二蛋白功能区,其中:所述第一蛋白功能区靶向LAG3,所述第二蛋白功能区靶向不同于LAG3的靶点,其中,所述第一蛋白功能区为抗LAG3抗体或其抗原结合片段,包含重链可变区和轻链可变区,其中,所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:5‑7所示的HCDR1‑HCDR3;并且所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:8‑10所示的LCDR1‑LCDR3。本发明的双特异性抗体具有优越的亲和力和特异性,具有良好的应用前景。
Description
技术领域
本发明属于生物医药领域,涉及一种抗LAG3抗体的双特异性抗体、其药物组合物及用途。具体地,所述双特异性抗体为一种抗LAG3-抗PD-1双特异性抗体。
背景技术
肿瘤尤其是恶性肿瘤是当今世界严重危害人类健康的疾病,在各种疾病所致死亡中高居第二位。而且近年来,其发病率呈明显上升趋势。恶性肿瘤治疗效果差,晚期转移率高,预后多不佳。目前临床上所采用的常规治疗方法如放、化疗和手术治疗虽然在很大程度上缓解了病痛,延长了生存时间,但这些方法均存在很大的局限性,其疗效难以进一步提高。
淋巴细胞活化基因3(lymphocyte-activation gene 3,LAG3),即CD223,是一种由498个氨基酸组成的Ⅰ型跨膜蛋白,属于免疫球蛋白超家族(immunoglobulin superfamily,IgSF)成员。LAG3主要表达于活化的CD4+T细胞和CD8+T细胞,另外自然杀伤(naturalkiller,NK)细胞、B细胞、调节性T细胞(regulatory T cell,Treg)和浆细胞样树突状细胞(plasmacytoid dendritic cells,pDC)等细胞也表达LAG3。(Ruffo Elisa,Wu Richard C,Bruno Tullia C et al.Lymphocyte-activation gene 3(LAG3):The next immunecheckpoint receptor.[J].Semin Immunol,2019,42:101305.)。
LAG3分子基因定位于人12号染色体(20p13.3)上,与CD4分子基因相邻,二者具有相同的外显子和内含子。虽然二者的氨基酸序列同源性只有约20%,但LAG3分子与CD4分子在结构上具有较高的相似性。主要组织相容性复合体Ⅱ类分子(MHCⅡ)、肝窦内皮细胞凝集素(LSECtin)分子和半乳糖凝集素3(galectin-3)分子是LAG3分子的相关配体。MHCⅡ类分子是LAG3的主要配体,其与MHCⅡ类分子的亲和力(Kd:60nmol·L-1)是CD4分子的100倍,表明LAG3分子能够有效竞争CD4与MHCⅡ类分子的结合,抑制T细胞活化。
肿瘤微环境中,T细胞活化24小时后便能检测到免疫抑制分子LAG3分子的表达,进而导致T细胞失能或者凋亡。LAG3分子通过其D1结构域(含有1个富含脯氨酸的环状结构)形成二聚体分子与CD4+T细胞活化第一信号轴“CD3-TCR-MHCⅡ”中MHCⅡ分子特异性结合,一方面阻断T细胞活化的信号转导通路,另一方面LAG3分子胞内段(KIEELE基序)产生免疫抑制信号下调CD4+T细胞活性。LAG3分子能促进Treg细胞分化,参与信号转导及转录激活因子5下游信号,从而增强Treg细胞的抑制作用,这是肿瘤逃逸免疫系统杀伤的机制之一(Andrews Lawrence P,Marciscano Ariel E,Drake Charles G et al.LAG3(CD223)as acancer immunotherapy target.[J].Immunol Rev,2017,276:80-96.)。
多项研究表明,LAG3在各种恶性肿瘤的肿瘤浸润性CD8+T细胞中过表达。例如卵巢癌中,肿瘤浸润的纽约食管鳞状细胞癌1抗原(NY-ESO-1)特异性CD8+T细胞表达高水平的PD-1和LAG3,产生IFN-γ和TNF-α的能力降低,进而导致淋巴细胞失活。Galectin-3和LSECtin主要与LAG3相互作用来调节CD8+T细胞的活化与功能。另外从黑色素瘤转移患者中分离的黑色素瘤抗原特异性T细胞在LAG3及其他免疫检查点分子CTLA-4和TIM-3表达上调显著。(刘昊,李新颖,罗龙龙,等.淋巴细胞活化基因3分子生物学功能及其抗体药物临床应用研究进展[J].中国药理学与毒理学杂志,2019,33(01):70-78.)。
目前已有多种LAG3抗体药物进入临床研究阶段,其中,百时美施贵宝的Relatlimab进展最快,目前已开展了10个临床研究,绝大多数是以Relatlimab与纳武单抗进行联合用药,用于治疗血液瘤、黑色素瘤、神经胶质母细胞瘤、肾细胞癌和非小细胞肺癌等肿瘤。
跨膜受体PD-1(程序性细胞死亡-1)是CD28家族成员之一,在活化的T细胞,B细胞以及骨髓系细胞都有表达。PD-1的受体PDL1和PDL2均属于B7超家族,其中PDL1多种细胞都有表达,包括T细胞,B细胞以及内皮细胞和上皮细胞,PDL2则仅表达于抗原呈递细胞如树突状细胞和巨噬细胞。
PD-1在负调节T细胞的活化过程中起着非常重要的作用,PD-1介导的对T细胞负调节作用是肿瘤免疫逃避的重要机制之一,肿瘤表面表达的PD-L1可与免疫细胞表面的PD-1结合,进而通过PD-1/PD-L1信号通路抑制免疫细胞对肿瘤组织的杀伤,高表达PD-L1的肿瘤伴随着很难被检测到的癌症(Hamanishi et al.,Proc.Natl.Acad.Sci.USA 2007;104:3360-5)。拮抗PD-1,从而抑制PD-1/PD-L1信号通路的一种有效方法是体内注射抗PD-1抗体。
PD-1抗体具有广谱抗肿瘤前景和惊人的药效,针对PD-1通路的抗体将带来治疗多种肿瘤治疗的突破性的进展:用于治疗非小细胞性肺癌,肾细胞癌,卵巢癌,黑色素瘤(Homet M.B.,Parisi G.,et al.,Anti-PD-1Therapy in Melanoma.SeminOncol.2015Jun;42(3):466-473),血液肿瘤以及贫血(Held SA,Heine A,et al.,Advancesin immunotherapy of chronic myeloid leukemia CML.Curr Cancer DrugTargets.2013Sep;13(7):768-74)。
双功能抗体亦称为双特异性抗体(Bispecific Antibody),是同时靶向结合两种不同抗原的特异性抗体药物,其可通过免疫分选纯化生产,也可通过基因工程获得。基因工程在结合位点优化,合成形式的考量以及产量等方面都具有相应的灵活性,所以具有一定的优势。目前,双特异性抗体存在形式已被证明有超过45种(Müller D,KontermannRE.Bispecific antibodies for cancer immunotherapy:Currentperspectives.BioDrugs 2010;24:89-98)。IgG-ScFv形式即Morrison模式(Coloma MJ,Morrison SL.Design and production of novel tetravalent bispecificantibodies.Nat Biotechnol.Nature Biotechnology,1997;15:159-163)由于类似于天然存在的IgG的形式,在抗体工程、表达和纯化上具有优势,已被证明是双功能抗体的一种理想存在形式(Miller BR,Demarest SJ,et al.,Stability engineering of scFvs forthe development of bispecific and multivalent antibodies.Protein Eng Des Sel2010;23:549-57;Fitzgerald J,Lugovskoy A.Rational engineering of antibodytherapeutics targeting multiple oncogene pathways.MAbs 2011;3:299-309)。
目前,尚需要开发新的抗LAG3抗体以及同时靶向PD-1和LAG3的双功能抗体药物。
发明内容
本发明人经过深入的研究和创造性的劳动,得到了一种抗LAG3抗体,并在此基础上制得了抗LAG3-抗PD-1双特异性抗体。本发明人惊奇地发现,本发明的抗LAG3抗体(也简称为抗体或本发明的抗体)和抗LAG3-抗PD-1双特异性抗体(也简称为双特异性抗体或本发明的双特异性抗体)具有优越的亲和力和/或特异性,甚至在一个或多个方面优于阳性对照抗体(例如Nivolumab、Pembrolizumab、Relatlimab等)。由此提供了下述发明:
本发明的一个方面涉及一种抗LAG3抗体或其抗原结合片段,包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:5-7所示的HCDR1-HCDR3;并且所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:8-10所示的LCDR1-LCDR3;
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:5-7所示的HCDR1-HCDR3;并且所述轻链可变区包含:氨基酸序列分别如SEQ ID NO:8、SEQ ID NO:46和SEQ ID NO:47所示的LCDR1-LCDR3;
或者
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:5-7所示的HCDR1-HCDR3;并且所述轻链可变区包含:氨基酸序列分别如SEQ ID NO:48、SEQ ID NO:46和SEQ ID NO:10所示的LCDR1-LCDR3。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,
所述抗体的重链可变区的氨基酸序列如SEQ ID NO:2所示,并且所述抗体的轻链可变区的氨基酸序列如SEQ ID NO:4所示;
所述抗体的重链可变区的氨基酸序列如SEQ ID NO:2所示,并且所述抗体的轻链可变区的氨基酸序列如SEQ ID NO:42所示;
或者
所述抗体的重链可变区的氨基酸序列如SEQ ID NO:2所示,并且所述抗体的轻链可变区的氨基酸序列如SEQ ID NO:44所示。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,所述抗体或其抗原结合片段选自Fab、Fab'、F(ab')2、Fd、Fv、dAb、互补决定区片段、单链抗体、人源化抗体、嵌合抗体或双抗体。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,所述的抗体以小于0.2nM,例如小于0.15nM、小于0.1nM、小于0.08nM、0.06nM或小于0.05nM或更小的EC50结合人LAG3-mFc;优选地,所述EC50通过间接ELISA方法测得。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,
所述的抗体包括非-CDR区,且所述非-CDR区来自不是鼠类的物种,例如来自人抗体。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,
所述的抗体,其恒定区来自人抗体;
优选地,所述抗体的恒定区选自人IgG1、IgG2、IgG3或IgG4的恒定区。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,
所述抗LAG3抗体的重链恒定区为Ig gamma-1chain C region(例如,如SEQ IDNO:39所示)或Ig gamma-4chain C region(例如,如SEQ ID NO:45所示);轻链恒定区为Igkappa chain C region(例如,如SEQ ID NO:40所示)。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,
所述抗体为人IgG1亚型,
其中,按照EU编号系统,所述抗体的重链恒定区具有如下突变:
L234A和L235A,
L234A和G237A,
L235A和G237A,
或者
L234A、L235A和G237A;
优选地,所述抗体的重链的氨基酸序列如SEQ ID NO:11所示,并且轻链的氨基酸序列如SEQ ID NO:12所示。
在本发明的一些实施方式中,所述的抗体或其抗原结合片段,其中,
所述抗体为人IgG4亚型,
其中,按照EU编号系统,所述抗体的重链恒定区具有如下突变:
F234A和L235A,
F234A和G237A,
L235A和G237A,
或者
F234A、L235A和G237A;
优选地,所述抗体的重链的氨基酸序列如SEQ ID NO:13所示,并且轻链的氨基酸序列如SEQ ID NO:12所示。
在本发明的一些实施方式中,所述的抗LAG3抗体为单克隆抗体。
在本发明的一些实施方式中,所述的抗LAG3抗体为免疫球蛋白形式。
在本发明的一些实施方式中,所述的抗LAG3抗体为单链抗体。
本发明的另一方面涉及抗体药物偶联物(antibody-drug conjugate,ADC),其包括抗体或其抗原结合片段以及小分子药物,其中,所述抗体或其抗原结合片段为本发明中任一项所述的抗LAG3抗体或其抗原结合片段;优选地,所述小分子药物为小分子细胞毒药物;更优选地,所述小分子药物为肿瘤化疗药物。
所述化疗药物可以是常规的肿瘤化疗药物,例如烷化剂、抗代谢药、抗肿瘤抗生素、植物类抗癌药、激素、免疫制剂等。
在本发明的一个或多个实施方案中,所述的抗体药物偶联物,其中,所述抗体或其抗原结合片段通过连接子与小分子药物连接;所述连接子可以是本领域技术人员知悉的连接子,例如,所述连接子为腙键、二硫键或肽键。
在本发明的一个或多个实施方案中,所述的抗体药物偶联物,其中,所述抗体或其抗原结合片段与小分子药物的摩尔比为1:(2-4),例如1:2,1:3或1:4。
本发明的再一方面涉及一种双特异性抗体,其包括第一蛋白功能区和第二蛋白功能区,其中:
所述第一蛋白功能区靶向LAG3,
所述第二蛋白功能区靶向不同于LAG3的靶点(例如,PD-1),
其中,所述第一蛋白功能区为本发明中任一项所述的抗体或抗原结合片段;
优选地,所述双特异性抗体为IgG-scFv模式;
优选地,所述第一蛋白功能区为本发明中任一项所述的抗体,并且所述第二蛋白功能区为单链抗体;或者
优选地,所述第一蛋白功能区为单链抗体,并且所述第二蛋白功能区为本发明中任一项所述的抗体。
本发明的双特异性抗体为抗LAG3-抗PD-1双特异性抗体。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述第一蛋白功能区和第二蛋白功能区直接连接或者通过连接片段连接;
优选地,所述连接片段为(GGGGS)m,m为正整数,例如1、2、3、4、5或6;
优选地,所述连接片段为(GGGGS)nG,n为正整数,例如1、2、3、4、5或6。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述第一蛋白功能区和第二蛋白功能区独立地为1个、2个或者2个以上。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述单链抗体连接在抗体的重链的C末端。
在本发明的一些实施方式中,所述的双特异性抗体,其包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
其中,
所述第一蛋白功能区为本发明中任一项所述的抗LAG3抗体,并且所述抗LAG3抗体为免疫球蛋白形式,
所述第二蛋白功能区为抗PD-1的单链抗体。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗PD-1的单链抗体包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:26-28所示的HCDR1-HCDR3;和
所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:29-31所示的LCDR1-LCDR3。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗PD-1的单链抗体,
其重链可变区的氨基酸序列如SEQ ID NO:15所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:17所示;或者
其重链可变区的氨基酸序列如SEQ ID NO:19所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:21或SEQ ID NO:38所示。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗PD-1的单链抗体中的重链可变区和轻链可变区直接连接或者通过连接片段连接;
优选地,所述连接片段为(GGGGS)m,m为正整数,例如1、2、3、4、5或6;
优选地,所述连接片段为(GGGGS)nG,n为正整数,例如1、2、3、4、5或6。
在本发明的一些实施方式中,所述的双特异性抗体,其中,
所述双特异性抗体包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
所述第一蛋白功能区为1个,所述第二蛋白功能区为2个;
其中,所述第一蛋白功能区为免疫球蛋白,所述第二蛋白功能区为单链抗体;
所述免疫球蛋白的重链的氨基酸序列如SEQ ID NO:11或SEQ ID NO:13所示,并且其轻链的氨基酸序列如SEQ ID NO:12所示;
所述单链抗体的重链可变区的氨基酸序列如SEQ ID NO:19所示,并且所述单链抗体的轻链可变区的氨基酸序列如SEQ ID NO:21或SEQ ID NO:38所示;
所述单链抗体连接在免疫球蛋白的两条重链的C末端;
所述第一蛋白功能区与所述第二蛋白功能区通过第一连接片段连接;并且所述单链抗体的重链可变区与所述单链抗体的轻链可变区通过第二连接片段连接;所述第一连接片段和所述第二连接片段相同或不同;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列独立地选自SEQ IDNOs:35-37;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列均如SEQ ID NO:36所示。
在本发明的一些实施方式中,所述的双特异性抗体,其包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
其中,所述第一蛋白功能区为抗LAG3的单链抗体,所述第二蛋白功能区为抗PD-1的抗体,并且所述抗PD-1的抗体为免疫球蛋白形式;
其中,所述抗LAG3的单链抗体包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:5-7所示的HCDR1-HCDR3;和
所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:8-10所示的LCDR1-LCDR3。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗LAG3的单链抗体,
其重链可变区的氨基酸序列如SEQ ID NO:2所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:4所示;
其重链可变区的氨基酸序列如SEQ ID NO:2所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:42所示;或者
其重链可变区的氨基酸序列如SEQ ID NO:2所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:44所示。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗LAG3的单链抗体中的重链可变区和轻链可变区直接连接或者通过连接片段连接;
优选地,所述连接片段为(GGGGS)m,m为正整数,例如1、2、3、4、5或6;
优选地,所述连接片段为(GGGGS)nG,n为正整数,例如1、2、3、4、5或6。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗PD-1的抗体包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:26-28所示的HCDR1-HCDR3;和
所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:29-31所示的LCDR1-LCDR3。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗PD-1的抗体,
其重链可变区的氨基酸序列如SEQ ID NO:15所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:17所示;或者
其重链可变区的氨基酸序列如SEQ ID NO:19所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:21或SEQ ID NO:38所示。
在本发明的一些实施方式中,所述的双特异性抗体,其中,所述抗PD-1的抗体,其重链恒定区为Ig gamma-1chain C region(例如,如SEQ ID NO:39所示)或Ig gamma-4chain C region(例如,如SEQ ID NO:45所示);轻链恒定区为Ig kappa chain C region(例如,如SEQ ID NO:40所示)。
在本发明的一些实施方式中,所述的双特异性抗体,其中,
所述抗PD-1的抗体为人IgG1亚型,
其中,按照EU编号系统,所述抗PD-1的抗体具有如下突变:
L234A和L235A,
L234A和G237A,
L235A和G237A,
或者
L234A、L235A和G237A;
优选地,所述抗PD-1的抗体的重链的氨基酸序列如SEQ ID NO:34所示,并且轻链的氨基酸序列如SEQ ID NO:25所示。
在本发明的一些实施方式中,所述的双特异性抗体,其中,
所述抗PD-1的抗体为人IgG4亚型,
其中,按照EU编号系统,所述抗PD-1的抗体具有如下突变:
F234A和L235A,
F234A和G237A,
L235A和G237A,
或者
F234A、L235A和G237A;
优选地,所述抗PD-1的抗体的重链的氨基酸序列如SEQ ID NO:32所示,并且轻链的氨基酸序列如SEQ ID NO:25所示。
在本发明的一些实施方式中,所述的双特异性抗体,其中,
所述双特异性抗体包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
所述第一蛋白功能区为1个,所述第二蛋白功能区为2个;
其中,所述第一蛋白功能区为单链抗体,所述第二蛋白功能区为免疫球蛋白;
所述单链抗体的重链可变区的氨基酸序列如SEQ ID NO:2所示,并且所述单链抗体的轻链可变区的氨基酸序列如SEQ ID NO:4所示;
所述免疫球蛋白的重链的氨基酸序列如SEQ ID NO:34或SEQ ID NO:32所示,并且其轻链的氨基酸序列如SEQ ID NO:25所示;
所述单链抗体连接在免疫球蛋白的两条重链的C末端;
所述第一蛋白功能区与所述第二蛋白功能区通过第一连接片段连接;并且所述单链抗体的重链可变区与所述单链抗体的轻链可变区通过第二连接片段连接;所述第一连接片段和所述第二连接片段相同或不同;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列独立地选自SEQ IDNOs:35-37;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列均如SEQ ID NO:36所示。
在本发明的一些实施方式中,所述的双特异性抗体,其中,一个免疫球蛋白分子连接有两个单链抗体分子;优选地,两个单链抗体分子相同。
本发明的再一方面涉及一种分离的核酸分子,其编码本发明中任一项所述的抗LAG3抗体,或者编码本发明中任一项所述的双特异性抗体。
本发明的再一方面涉及一种重组载体,其包含本发明的分离的核酸分子。
本发明的再一方面涉及一种宿主细胞,其包含本发明的分离的核酸分子,或者包含本发明的重组载体。
本发明的再一方面涉及一种制备本发明中任一项所述的抗体或其抗原结合片段或者本发明中任一项所述的双特异性抗体的方法,其包括在合适的条件下培养本发明的宿主细胞,以及从细胞培养物中回收所述抗体或其抗原结合片段或者双特异性抗体的步骤。
本发明的再一方面涉及一种药物组合物,其包含本发明中任一项所述的抗体或其抗原结合片段、本发明中任一项所述的抗体药物偶联物或者本发明中任一项所述的双特异性抗体;可选地,其还包括药学上可接受的辅料。
本发明的再一方面涉及本发明中任一项所述的抗体或其抗原结合片段、本发明中任一项所述的抗体药物偶联物或者本发明中任一项所述的双特异性抗体在制备治疗和/或预防肿瘤或贫血病的药物中的用途;
优选地,所述肿瘤为选自卵巢癌、食管癌、黑色素瘤、血液瘤、神经胶质母细胞瘤、肾细胞癌、肺癌、前列腺癌、膀胱癌、结肠癌、直肠癌、肝癌、胃肠道癌、乳腺癌、脑癌、胰腺癌、甲状腺癌、头颈癌和肾癌中的一种或多种;
优选地,所述肺癌为非小细胞肺癌;
优选地,所述血液瘤为白血病;
优选地,所述食管癌为食管鳞癌。
根据本发明中任一项所述的抗体或其抗原结合片段、本发明中任一项所述的抗体药物偶联物或者本发明中任一项所述的双特异性抗体,其用于治疗和/或预防肿瘤或贫血病;
优选地,所述肿瘤为选自卵巢癌、食管癌、黑色素瘤、血液瘤、神经胶质母细胞瘤、肾细胞癌、肺癌、前列腺癌、膀胱癌、结肠癌、直肠癌、肝癌、胃肠道癌、乳腺癌、脑癌、胰腺癌、甲状腺癌、头颈癌和肾癌中的一种或多种;
优选地,所述肺癌为非小细胞肺癌;
优选地,所述血液瘤为白血病;
优选地,所述食管癌为食管鳞癌。
本发明的再一方面涉及一种治疗和/或预防肿瘤或贫血病的方法,包括给予有需求的受试者以有效量的本发明中任一项所述的抗体或其抗原结合片段、本发明中任一项所述的抗体药物偶联物或者本发明中任一项所述的双特异性抗体的步骤;
优选地,所述肿瘤为选自卵巢癌、食管癌、黑色素瘤、血液瘤、神经胶质母细胞瘤、肾细胞癌、肺癌、前列腺癌、膀胱癌、结肠癌、直肠癌、肝癌、胃肠道癌、乳腺癌、脑癌、胰腺癌、甲状腺癌、头颈癌和肾癌中的一种或多种;
优选地,所述肺癌为非小细胞肺癌;
优选地,所述血液瘤为白血病;
优选地,所述食管癌为食管鳞癌。
在本发明中,除非另有说明,否则本文中使用的科学和技术名词具有本领域技术人员所通常理解的含义。并且,本文中所用的细胞培养、分子遗传学、核酸化学、免疫学实验室操作步骤均为相应领域内广泛使用的常规步骤。同时,为了更好地理解本发明,下面提供相关术语的定义和解释。
如本文中所使用的,术语EC50是指半最大效应浓度(concentration for 50%ofmaximal effect),是指能引起50%最大效应的浓度。
如本文中所使用的,术语“抗体”是指通常由两对多肽链(每对具有一条“轻”(L)链和一条“重”(H)链)组成的免疫球蛋白分子。抗体轻链可分类为κ和λ轻链。重链可分类为μ、δ、γ、α或ε,并且分别将抗体的同种型定义为IgM、IgD、IgG、IgA和IgE。在轻链和重链内,可变区和恒定区通过大约12或更多个氨基酸的“J”区连接,重链还包含大约3个或更多个氨基酸的“D”区。各重链由重链可变区(VH)和重链恒定区(CH)组成。重链恒定区由3个结构域(CH1、CH2和CH3)组成。各轻链由轻链可变区(VL)和轻链恒定区(CL)组成。轻链恒定区由一个结构域CL组成。抗体的恒定区可介导免疫球蛋白与宿主组织或因子,包括免疫系统的各种细胞(例如,效应细胞)和经典补体系统的第一组分(C1q)的结合。VH和VL区还可被细分为具有高变性的区域(称为互补决定区(CDR)),其间散布有较保守的称为构架区(FR)的区域。各VH和VL由按下列顺序:FR1、CDR1、FR2、CDR2、FR3、CDR3和FR4从氨基末端至羧基末端排列的3个CDR和4个FR组成。各重链/轻链对的可变区(VH和VL)分别形成抗体结合部位。氨基酸至各区域或结构域的分配遵循Bethesda M.d.,Kabat Sequences of Proteins ofImmunological Interest(National Institutes of Health,(1987and 1991)),或Chothia&Lesk J.Mol.Biol.1987;196:901-917;Chothia等人Nature 1989;342:878-883,或者IMGT编号系统定义,见Ehrenmann F,Kaas Q,Lefranc M P.IMGT/3Dstructure-DB andIMGT/DomainGapAlign:a database and a tool for immunoglobulins or antibodies,Tcell receptors,MHC,IgSF and MhcSF[J].Nucleic acids research,2009;38(suppl_1):D301-D307的定义。
特别地,重链还可以包含3个以上CDR,例如6、9、或12个。例如在本发明的双特异性抗体中,重链可以是IgG抗体的重链的C端连接一个ScFv,这种情况下重链含有9个CDR。
术语“抗体”不受任何特定的产生抗体的方法限制。例如,其包括,重组抗体、单克隆抗体和多克隆抗体。抗体可以是不同同种型的抗体,例如,IgG(例如,IgG1,IgG2,IgG3或IgG4亚型),IgA1,IgA2,IgD,IgE或IgM抗体。
如本文中所使用的,术语“单抗”和“单克隆抗体”是指,来自一群高度同源的抗体分子中的一个抗体或抗体的一个片段,也即除可能自发出现的自然突变外,一群完全相同的抗体分子。单抗对抗原上的单一表位具有高特异性。多克隆抗体是相对于单克隆抗体而言的,其通常包含至少2种或更多种的不同抗体,这些不同的抗体通常识别抗原上的不同表位。单克隆抗体通常可采用Kohler等首次报道的杂交瘤技术获得(G,MilsteinC.Continuous cultures of fused cells secreting antibody of predefinedspecificity[J].nature,1975;256(5517):495),但也可采用重组DNA技术获得(如参见U.S.Patent4,816,567)。
如本文中所使用的,术语“人源化抗体”是指,人源免疫球蛋白(受体抗体)的全部或部分CDR区被一非人源抗体(供体抗体)的CDR区替换后得到的抗体或抗体片段,其中的供体抗体可以是具有预期特异性、亲和性或反应性的非人源(例如,小鼠、大鼠或兔)抗体。此外,受体抗体的构架区(FR)的一些氨基酸残基也可被相应的非人源抗体的氨基酸残基替换,或被其他抗体的氨基酸残基替换,以进一步完善或优化抗体的性能。关于人源化抗体的更多详细内容,可参见例如,Jones et al.,Nature 1986;321:522 525;Reichmann etal.,Nature,1988;332:323 329;Presta,Curr.Op.Struct.Biol.1992;2:593-596;和Clark,Immunol.Today 2000;21:397 402。在一些情况下,抗体的抗原结合片段是双抗体(Diabodies),其中VH和VL结构域在单个多肽链上表达,但使用太短的连接体以致不允许在相同链的两个结构域之间配对,从而迫使结构域与另一条链的互补结构域配对并且产生两个抗原结合部位(参见,例如,Holliger P.et al.,Proc.Natl.Acad.Sci.USA 1993;90:6444-6448和Poljak R.J.et al.,Structure 1994;2:1121-1123)。
如本文中所使用的,术语“单链抗体(single chain fragment variable,ScFv)”是指,包含通过连接体连接的抗体重链可变区(VH)和抗体轻链可变区(VL)的分子。其中VL和VH结构域通过使其能够产生为单个多肽链的连接体配对形成单价分子(参见,例如,Birdet al,Science 1988;242:423-426和Huston et al,Proc.Natl.Acad.Sci.USA1988;85:5879-5883)。此类scFv分子可具有一般结构:NH2-VL-连接片段-VH-COOH或NH2-VH-连接片段-VL-COOH。合适的现有技术接头由重复的GGGGS氨基酸序列或其变体组成。例如,可使用具有氨基酸序列(GGGGS)4的接头,但也可使用其变体(Holliger et al,Proc.Natl.Acad.Sci.USA 1993;90:6444-6448)。可用于本发明的其他接头由Alfthan etal,Protein Eng.1995;8:725-731,Choi et al,Eur.J.Immunol.2001;31:94-106,Hu etal,Cancer Res.1996;56:3055-3061,Kipriyanov et al,J.Mol.Biol.1999;293:41-56和Roovers et al,Cancer Immunology,Immunotherapy,2001,50(1):51-59.描述。
如本文中所使用的,术语“分离的”或“被分离的”指的是,从天然状态下经人工手段获得的。如果自然界中出现某一种“分离”的物质或成分,那么可能是其所处的天然环境发生了改变,或从天然环境下分离出该物质,或二者情况均有发生。例如,某一活体动物体内天然存在某种未被分离的多聚核苷酸或多肽,而从这种天然状态下分离出来的高纯度的相同的多聚核苷酸或多肽即称之为分离的。术语“分离的”或“被分离的”不排除混有人工或合成的物质,也不排除存在不影响物质活性的其它不纯物质。
如本文中所使用的,术语“载体(vector)”是指,可将多聚核苷酸插入其中的一种核酸运载工具。当载体能使插入的多核苷酸编码的蛋白获得表达时,载体称为表达载体。载体可以通过转化,转导或者转染导入宿主细胞,使其携带的遗传物质元件在宿主细胞中获得表达。载体是本领域技术人员公知的,包括但不限于:质粒;噬菌粒;柯斯质粒;人工染色体,例如酵母人工染色体(YAC)、细菌人工染色体(BAC)或P1来源的人工染色体(PAC);噬菌体如λ噬菌体或M13噬菌体及动物病毒等。可用作载体的动物病毒包括但不限于,逆转录酶病毒(包括慢病毒)、腺病毒、腺相关病毒、疱疹病毒(如单纯疱疹病毒)、痘病毒、杆状病毒、乳头瘤病毒、乳头多瘤空泡病毒(如SV40)。一种载体可以含有多种控制表达的元件,包括但不限于,启动子序列、转录起始序列、增强子序列、选择元件及报告基因。另外,载体还可含有复制起始位点。
如本文中所使用的,术语“宿主细胞”是指,可用于导入载体的细胞,其包括但不限于,如大肠杆菌或枯草杆菌等的原核细胞,如酵母细胞或曲霉菌等的真菌细胞,如S2果蝇细胞或Sf9等的昆虫细胞,或者如纤维原细胞,CHO细胞,GS细胞,COS细胞,NSO细胞,HeLa细胞,BHK细胞,HEK 293细胞或人细胞等的动物细胞。
如本文中使用的,术语“特异性结合”是指,两分子间的非随机的结合反应,如抗体和其所针对的抗原之间的反应。在某些实施方式中,特异性结合某抗原的抗体(或对某抗原具有特异性的抗体)是指,抗体以小于大约10-5M,例如小于大约10-6M、10-7M、10-8M、10-9M或10-10M或更小的亲和力(KD)结合该抗原。
如本文中所使用的,术语“KD”是指特定抗体-抗原相互作用的解离平衡常数,其用于描述抗体与抗原之间的结合亲和力。平衡解离常数越小,抗体-抗原结合越紧密,抗体与抗原之间的亲和力越高。通常,抗体以小于大约10-5M,例如小于大约10-6M、10-7M、10-8M、10- 9M或10-10M或更小的解离平衡常数(KD)结合抗原(例如,PD-1蛋白)。可以使用本领域技术人员知悉的方法测定KD,例如使用Fortebio分子相互作用仪测定。
如本文中所使用的,术语“单克隆抗体”和“单抗”具有相同的含义且可互换使用;术语“多克隆抗体”和“多抗”具有相同的含义且可互换使用。并且在本发明中,氨基酸通常用本领域公知的单字母和三字母缩写来表示。例如,丙氨酸可用A或Ala表示。
如本文中所使用的,术语“药学上可接受的载体和/或赋形剂”是指在药理学和/或生理学上与受试者和活性成分相容的载体和/或赋形剂,其是本领域公知的(参见例如Remington's Pharmaceutical Sciences.Edited by Gennaro AR,19thed.Pennsylvania:Mack Publishing Company,1995),并且包括但不限于:pH调节剂,表面活性剂,佐剂,离子强度增强剂。例如,pH调节剂包括但不限于磷酸盐缓冲液;表面活性剂包括但不限于阳离子,阴离子或者非离子型表面活性剂,例如Tween-80;离子强度增强剂包括但不限于氯化钠。
如本文中所使用的,术语“有效量”是指足以获得或至少部分获得期望的效果的量。例如,预防疾病(例如肿瘤)有效量是指,足以预防,阻止,或延迟疾病(例如肿瘤)的发生的量;治疗疾病有效量是指,足以治愈或至少部分阻止已患有疾病的患者的疾病和其并发症的量。测定这样的有效量完全在本领域技术人员的能力范围之内。例如,对于治疗用途有效的量将取决于待治疗的疾病的严重度、患者自己的免疫系统的总体状态、患者的一般情况例如年龄,体重和性别,药物的施用方式,以及同时施用的其他治疗等等。
如本文中所使用的,当提及PD-1蛋白(NCBI GenBank:NM_005018)的氨基酸序列时,其包括PD-1蛋白的全长,或者PD-1的胞外片段PD-1ECD或者包含PD-1ECD的片段;还包括PD-1蛋白的全长的融合蛋白或PD-1ECD的融合蛋白,例如与小鼠或人IgG的Fc蛋白片段(mFc或hFc)进行融合的片段。然而,本领域技术人员理解,在PD-1蛋白的氨基酸序列中,可天然产生或人工引入突变或变异(包括但不限于置换,缺失和/或添加),而不影响其生物学功能。因此,在本发明中,术语“添加),蛋白”应包括所有此类序列,包括其天然或人工的变体。并且,当描述PD-1蛋白的序列片段时,其还包括其天然或人工变体中的相应序列片段。
如本文中所使用的,当提及淋巴细胞活化基因3(lymphocyte-activation gene3,LAG3)的氨基酸序列时,其包括LAG3蛋白的全长,或者LAG3的胞外片段LAG3 ECD或者包含LAG3 ECD的片段;还包括LAG3蛋白的全长的融合蛋白或LAG3ECD的融合蛋白,例如与小鼠或人IgG的Fc蛋白片段(mFc或hFc)进行融合的片段。然而,本领域技术人员理解,在LAG3蛋白的氨基酸序列中,可天然产生或人工引入突变或变异(包括但不限于置换,缺失和/或添加),而不影响其生物学功能。因此,在本发明中,术语“添加),蛋白”应包括所有此类序列,包括其天然或人工的变体。并且,当描述LAG3蛋白的序列片段时,其还包括其天然或人工变体中的相应序列片段。
在本发明中,如果没有特别说明,所述“第一”(例如第一蛋白功能区)和“第二”(例如第二蛋白功能区)是为了指代上的区分或表述上的清楚,并不具有典型的次序上的含义。
发明的有益效果
本发明取得了如下效果中的一项或多项:
(1)本发明的抗LAG3抗体具有优越的亲和力和特异性;
(2)本发明的双特异性抗体例如BS-PL021A、BS-PL022B、BS-PL023C能够很好地特异性与LAG3结合,并且能够十分有效地阻断LAG3与MHCⅡ的结合,特异地解除LAG3对机体免疫抑制;
(3)本发明的双特异性抗体例如BS-PL021A、BS-PL022B、BS-PL023C能够很好地特异性与PD-1结合,并且能够十分有效地阻断PD-1与PDL1的结合,特异地解除PD-1对机体免疫抑制,激活免疫反应。
(4)本发明的双特异性抗体中的第一蛋白功能区和第二蛋白功能区之间具有协同作用。
(5)本发明的双特异性抗体特别是BS-PL022B,完全消除了其与Fc受体FcγRI、FcγRIIb、FcγRIIa_H131、FcγRIIIa_V158和/或FcγRIIIa_F158的结合活性,进而消除了其ADCC活性或ADCP活性。
(6)本发明的双特异性抗体特别是BS-PL022B,完全消除了其与补体C1q的结合活性,进而消除了其CDC活性。
附图说明
图1:间接ELISA方法测定BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)与抗原PD-1-mFc结合活性检测结果。
图2:间接ELISA方法测定BS-PL021A、BS-PL022B、BS-PL023C、BS-PLV02、Relatlimab、H7L8(hG1WT)与抗原LAG3-mFc结合活性检测结果。
图3:竞争ELISA方法测定抗体抗LAG3-抗PD-1双特异性抗体与人PDL1-mFc竞争结合人PD-1-mFc-Biotin活性检测结果。
图4:FACS检测抗LAG3-抗PD-1双特异性抗体与293T-PD1膜表面PD-1结合活性检测结果。
图5:FACS检测抗LAG3-抗PD-1双特异性抗体与293T-LAG3膜表面LAG3结合活性检测结果。
图6:竞争流式细胞法测定抗LAG3-抗PD-1双特异性抗体与PDL1竞争结合细胞膜表面抗原PD-1检测结果。
图7:竞争流式细胞法测定抗LAG3-抗PD-1双特异性抗体与LAG3竞争结合细胞膜表面抗原MHC II检测结果。
图8A:抗LAG3-抗PD-1双特异性抗体阻断LAG3与MHCII结合检测结果。
图8B:抗LAG3-抗PD-1双特异性抗体阻断LAG3与MHCII结合检测结果。
图9A:抗LAG3-抗PD-1双特异性抗体阻断PD-1与PD-L1结合检测结果。
图9B:抗LAG3-抗PD-1双特异性抗体阻断PD-1与PD-L1结合检测结果。
图10A:抗LAG3-抗PD-1双特异性抗体同时阻断LAG3与MHCII以及PD-1与PD-L1结合检测结果。
图10B:抗LAG3-抗PD-1双特异性抗体同时阻断LAG3与MHCII以及PD-1与PD-L1结合检测结果。
图11:抗LAG3-抗PD-1双特异性抗体桥连实验检测结果。
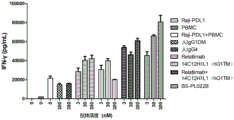
图12A:混合淋巴细胞反应MLR检测抗LAG3-抗PD-1双特异性抗体促IFN-γ分泌的生物活性检测结果。
图12B:混合淋巴细胞反应MLR检测抗LAG3-抗PD-1双特异性抗体促IL-2分泌的生物活性检测结果。
图13:BS-PL022B与FcγRI的亲和力常数检测结果。
图14:H7L8(hG1WT)与FcγRI的亲和力常数检测结果。
图15:BS-PL022B与FcγRIIIa_V158的亲和力常数检测结果。
图16:H7L8(hG1WT)与FcγRIIIa_V158的亲和力常数检测结果图。
图17:BS-PL022B与FcγRIIIa_F158的亲和力常数检测结果。
图18:H7L8(hG1WT)与FcγRIIIa_F158的亲和力常数检测结果。
图19:BS-PL022B与FcγRIIa_H131的亲和力常数检测结果。
图20:H7L8(hG1WT)与FcγRIIa_H131的亲和力常数检测结果。
图21:BS-PL022B与FcγRIIb的亲和力常数检测结果。
图22:H7L8(hG1WT)与FcγRIIb的亲和力常数检测结果。
图23:BS-PL022B与C1q的亲和力常数检测结果。
图24:H7L8(hG1WT)与C1q的亲和力常数检测结果。
图25:BS-PL022B的ADCP效应结果。
图26:抗LAG3-抗PD-1双特异性抗体对BALB/c-hPD1/hLAG3小鼠CT26移植瘤模型药效。*P<0.05,**P<0.01,***P<0.001,VS同型对照组(two-way ANOVA)
图27:抗LAG3-抗PD-1双特异性抗体对BALB/c-hPD1/hLAG3小鼠CT26移植瘤模型体重影响。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述。本领域技术人员将会理解,下面的实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件(例如参考J.萨姆布鲁克等著,黄培堂等译的《分子克隆实验指南》,第三版,科学出版社)或按照产品说明书进行。所用试剂或仪器未注明生产厂商者,为可以通过市场购买获得的常规产品。例如MDA-MB-231细胞和U87-MG细胞可以购自ATCC。
BALB/c小鼠购自广东省医学实验动物中心。
Nivolumab购自BMS公司,批号:ABA0330。Nivolumab是抗PD-1抗体。
Pembrolizumab购自MSD Ireland(Carlow)公司,货号:S023942。Pembrolizumab是抗PD-1抗体。
阳性对照抗体Relatlimab,其序列参考美国专利公开:US20160326248A1。其中重链氨基酸序列参照该专利公开中的SEQ ID NO:1,轻链氨基酸序列参照该专利公开中的SEQID NO:2。Relatlimab是抗LAG-3抗体。
293T-PD1细胞系由中山康方生物医药有限公司构建。293T-PD1细胞系由HEK293T细胞经病毒感染制得,病毒制备使用的是3rd Generation Lentiviral Systems,参见,例如A Third Generation Lentivirus Vector with a Conditional PackagingSystem.Dull T,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,and Naldini L.JVirol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为plenti6.3/V5-PD1FL-BSD(其中PD1,Genebank ID:NM_005018;载体plenti6.3/V5-BSD,购自Invitrogen,产品编号:K5315-20)。
293T-LAG3细胞系由中山康方生物医药有限公司构建。293T-LAG3细胞系由HEK293T细胞经病毒感染制得,病毒制备使用的是3rd Generation Lentiviral Systems,参见,例如A Third Generation Lentivirus Vector with a Conditional PackagingSystem.Dull T,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,and Naldini L.JVirol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为plenti6.3/V5-huLAG3FL-BSD(其中LAG3,Genebank ID:NM_002277.4;载体plenti6.3/V5-BSD,购自Invitrogen,产品编号:K5315-20)。
Raji-PDL1细胞系由中山康方生物医药有限公司构建。Raji-PDL1细胞系由Raji细胞经病毒感染制得,病毒制备使用的是3rd Generation Lentiviral Systems,参见,例如AThird Generation Lentivirus Vector with a Conditional Packaging System.DullT,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,and Naldini L.J Virol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为plenti6.3/V5-PDL1(其中PDL1,Genebank ID:NP_054862.1;载体plenti6.3/V5,购自Invitrogen,货号:K5315-20)。
Jurkat-NFAT-PD1-LAG3细胞系由中山康方生物医药有限公司构建。Jurkat-NFAT-PD1-LAG3细胞系由PD-1效应细胞(PD-1 Effector cells(CPM),厂家:Promega,货号:J112A)细胞经病毒感染制得,病毒制备使用的是3rd Generation Lentiviral Systems,参见,例如A Third Generation Lentivirus Vector with a Conditional PackagingSystem.Dull T,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,and Naldini L.JVirol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为pCDH-huLAG3FL-RFP-NEO(其中LAG3,Genebank ID:NM_002277.4;载体pCDH-CMV-MCS-EF1-RFP+Neo,购自优宝生物,产品编号:VT9005)。
CHO-K1-PD1细胞系由中山康方生物医药有限公司构建。CHO-K1-PD1细胞系由CHO-K1细胞经病毒感染制得,病毒制备使用的是3rd Generation Lentiviral Systems,参见,例如A Third Generation Lentivirus Vector with a Conditional PackagingSystem.Dull T,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,and Naldini L.JVirol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为pCDH-CMV-PD-1FL-Puro(其中PD1,Genebank ID:NM_005018;载体pCDH-CMV-Puro,购自优宝生物,产品编号:VT1480)。
CHO-K1-LAG3细胞系由中山康方生物医药有限公司构建。CHO-K1-LAG3细胞系由CHO-K1细胞经病毒感染制得,病毒制备使用的是3rd Generation Lentiviral Systems,参见,例如A Third Generation Lentivirus Vector with a Conditional PackagingSystem.Dull T,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,and Naldini L.JVirol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为plenti6.3/V5-huLAG3FL-BSD(其中LAG3,Genebank ID:NM_002277.4;载体plenti6.3/V5-BSD,购自Invitrogen,产品编号:K5315-20)。
Jurkat-NFAT-CD64-CD32R细胞系由中山康方生物医药有限公司构建。Jurkat-NFAT-CD64-CD32R细胞系由Jurkat细胞经病毒感染制得,病毒制备使用的是3rdGeneration Lentiviral Systems,参见,例如A Third Generation Lentivirus Vectorwith a Conditional Packaging System.Dull T,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,and Naldini L.J Virol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为pCDH-NFAT-Hygro(其中载体pCDH-Hygro基于pCDH-CMV-MCS-EF1-Puro(购自优宝生物,货号:VT1480)基础上,本实验室改造获得)、pcDH-hFCGR1AFL-Neo(载体pCDH-Neo基于pCDH-CMV-MCS-EF1-Puro(购自优宝生物,货号:VT1480)基础上,本实验室改造获得)和pCDH-hFCGR2A(H167)-puro(其中hFCGR2A(H167),Genebank ID:P12318;载体pCDH-CMV-MCS-EF1-Puro购自优宝生物,货号:VT1480)。
CHO-K1-PD1-LAG3细胞系由中山康方生物医药有限公司构建。CHO-K1-PD1-LAG3细胞系由CHO-K1细胞经病毒感染制得,病毒制备使用的是3rd Generation LentiviralSystems,参见,例如A Third Generation Lentivirus Vector with a ConditionalPackaging System.Dull T,Zufferey R,Kelly M,Mandel RJ,Nguyen M,Trono D,andNaldini L.J Virol.1998.72(11):8463-8471.其中所使用的慢病毒表达载体为pCDH-hPD1-FL-puro(其中PD-1,Genebank ID:NM_005018;其载体pCDH-CMV-MCS-EF1-Puro购自优宝生物,货号:VT1480)和plenti6.3/V5-huLAG3FL-BSD(其中LAG3,Genebank ID:NM_002277.4;载体plenti6.3/V5-BSD,购自Invitrogen,货号:K5315-20)
制备例1:抗LAG3抗体的设计和制备
1.抗体的设计
本发明人根据已有的LAG3蛋白序列(NCBI Reference Sequence:NP_002277.4)及其蛋白三维晶体结构等,创造性地人工设计了一系列的抗体序列。通过大量的筛选和检测,最终得到了与LAG3特异性结合的人源化单克隆抗体,分别命名为H7L8、H7L9、H7L10。该单克隆抗体重链和轻链可变区的氨基酸序列及其编码序列如下。
H7L8的重链可变区H7v的核酸序列(360bp):
CAGGTGCAGCTGCAGCAGTGGGGAGCTGGACTGCTGAAACCTAGCGAGACACTGAGCCTGACCTGTGCTGTGTACGGCGGATCTATCAGCGATTACTACTGGAACTGGATCAGGCAGCCCCCTGGAAAGGGACTGGAATGGATCGGAGAGATCAACCACAGGGGCACCACCAACTCCAATCCCTCTCTGAAGAGCAGGGTGACACTGAGCCTCGACACAAGCAAGAATCAGTTCAGCCTGAAGCTGAGGTCCGTGACCGCTGCTGATACAGCTGTGTACTACTGTGCCTTCGGCTACAGCGATTACGAGTACGATTGGTTCGACCCTTGGGGCCAGGGAACACTGGTTACAGTGAGCTCC(SEQ ID NO:1)
H7L8的重链可变区H7v的氨基酸序列(120aa):
QVQLQQWGAGLLKPSETLSLTCAVYGGSISDYYWNWIRQPPGKGLEWIGEINHRGTTNSNPSLKSRVTLSLDTSKNQFSLKLRSVTAADTAVYYCAFGYSDYEYDWFDPWGQGTLVTVSS(SEQ ID NO:2)
H7L8的轻链可变区L8v的核酸序列(321bp):
GAGATCGTTCTGACCCAGAGCCCAGCTACACTGAGCCTGTCTCCTGGAGAGAGGGCTACACTGTCCTGCAGAGCTAGCCAGACCATCAGCAGCTACCTGGCTTGGTACCAGCAGAAGCCTGGCCAAGCTCCAAGGCTGCTGATCTACGACGCCTCTAATAGGGCCACCGGCATCCCTGCTAGATTCTCTGGAAGCGGCAGCGGAACCGACTTTACACTGACAATCAGCTCCCTGGAGCCCGAGGATTTCGCTGTTTACTACTGTCAGCAGCGCAGCAACTGGCCCATCACATTCGGACAGGGCACAAATCTGGAGATCAAG(SEQ ID NO:3)
H7L8的轻链可变区L8v的氨基酸序列(107aa):
EIVLTQSPATLSLSPGERATLSCRASQTISSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPITFGQGTNLEIK(SEQID NO:4)
H7L9的重链可变区H7v的核酸序列与H7L8的重链可变区H7v的核酸序列相同,即SEQ ID NO:1。
H7L9的重链可变区H7v的氨基酸序列与H7L8的重链可变区H7v的氨基酸序列相同,即SEQ ID NO:2。
H7L9的轻链可变区L9v的核酸序列(321bp):
GAGATCGTTCTGACCCAGAGCCCAGCTACACTGAGCCTGTCTCCTGGAGAGAGGGCTACACTGTCCTGCAGAGCTAGCCAGACCATCAGCAGCTACCTGGCTTGGTACCAGCAGAAGCCTGGCCAAGCTCCAAGGCTGCTGATCTACGACGGCTCTAATAGGGCCACCGGCATCCCTGCTAGATTCTCTGGAAGCGGCAGCGGAACCGACTTTACACTGACAATCAGCTCCCTGGAGCCCGAGGATTTCGCTGTTTACTACTGTCAGCAGCGCAGCAACTGGCCCCTCACATTCGGACAGGGCACAAATCTGGAGATCAAG(SEQ ID NO:41)
H7L9的轻链可变区L9v的氨基酸序列(107bp):
EIVLTQSPATLSLSPGERATLSCRASQTISSYLAWYQQKPGQAPRLLIYDGSNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPLTFGQGTNLEIK(SEQ ID NO:42)
H7L10的重链可变区H7v的核酸序列与H7L8的重链可变区H7v的核酸序列相同,即SEQ ID NO:1。
H7L10的重链可变区H7v的氨基酸序列与H7L8的重链可变区H7v的氨基酸序列相同,即SEQ ID NO:2。
H7L10的轻链可变区L10v的核酸序列(321bp):
GAGATCGTTCTGACCCAGAGCCCAGCTACACTGAGCCTGTCTCCTGGAGAGAGGGCTACACTGTCCTGCAGAGCTAGCCAGTCCATCAGCAGCTACCTGGCTTGGTACCAGCAGAAGCCTGGCCAAGCTCCAAGGCTGCTGATCTACGACGGCTCTAATAGGGCCACCGGCATCCCTGCTAGATTCTCTGGAAGCGGCAGCGGAACCGACTTTACACTGACAATCAGCTCCCTGGAGCCCGAGGATTTCGCTGTTTACTACTGTCAGCAGCGCAGCAACTGGCCCATCACATTCGGACAGGGCACAAATCTGGAGATCAAG(SEQ ID NO:43)
H7L10的轻链可变区L10v的氨基酸序列(107bp):
EIVLTQSPATLSLSPGERATLSCRASQSISSYLAWYQQKPGQAPRLLIYDGSNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPITFGQGTNLEIK(SEQ ID NO:44)
抗体H7L8的CDR的氨基酸序列如下(按照IMGT编号系统):
HCDR1:GGSISDYY(SEQ ID NO:5);
HCDR2:INHRGTT(SEQ ID NO:6);
HCDR3:AFGYSDYEYDWFDP(SEQ ID NO:7);
LCDR1:QTISSY(SEQ ID NO:8);
LCDR2:DAS(SEQ ID NO:9);
LCDR3:QQRSNWPIT(SEQ ID NO:10)。
抗体H7L9的CDR的氨基酸序列如下(按照IMGT编号系统):
HCDR1:GGSISDYY(SEQ ID NO:5);
HCDR2:INHRGTT(SEQ ID NO:6);
HCDR3:AFGYSDYEYDWFDP(SEQ ID NO:7);
LCDR1:QTISSY(SEQ ID NO:8);
LCDR2:DGS(SEQ ID NO:46);
LCDR3:QQRSNWPLT(SEQ ID NO:47)。
抗体H7L10的CDR的氨基酸序列如下(按照IMGT编号系统):
HCDR1:GGSISDYY(SEQ ID NO:5);
HCDR2:INHRGTT(SEQ ID NO:6);
HCDR3:AFGYSDYEYDWFDP(SEQ ID NO:7);
LCDR1:QSISSY(SEQ ID NO:48);
LCDR2:DGS(SEQ ID NO:46);
LCDR3:QQRSNWPIT(SEQ ID NO:10)。
2.人源化抗体抗体H7L8(hG1WT)的表达和纯化
将H7L8(hG1WT)的重链cDNA序列(可变区编码序列如SEQ ID NO:1所示;恒定区是Ig gamma-1chain C region,SEQ ID NO:39)和轻链的cDNA序列(可变区编码序列如SEQ IDNO:3所示;恒定区为P01834.1(human Ig kappa chain C region,SEQ ID NO:40)分别克隆到pUC57simple(金斯瑞公司提供)载体中,分别获得pUC57simple-H7和pUC57simple-L8质粒。分别将质粒pUC57simple-H7和pUC57simple-L8进行酶切(HindIII&EcoRI),电泳回收得到的重链轻链分别亚克隆到pcDNA3.1载体中,提取重组质粒共转染293F细胞。细胞培养7天后,将培养液通过高速离心、上清浓缩后上样至HiTrap MabSelect SuRe柱,用ElutionBuffer一步洗脱蛋白并回收目标样品并换液至PBS。
H7L8(hG1WT)重链恒定区氨基酸序列
ASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(SEQ ID NO:39)
H7L8(hG1WT)轻链恒定区氨基酸序列
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ ID NO:40)
3、人源化抗体H7L8(hG1TM)的设计
本发明人在H7L8(hG1WT)的基础上,通过在其重链的第234号位点(按照EU编号系统,下同)引进了亮氨酸到丙氨酸的点突变(L234A),第235号位点引进了亮氨酸到丙氨酸的点突变(L235A),第237号位点引进了甘氨酸到丙氨酸的点突变(G237A)获得了恒定区突变的人源化抗体H7L8(hG1TM)。H7L8(hG1TM)的重链H7(hG1TM)的氨基酸序列如SEQ ID NO:11所示;轻链L8的氨基酸序列如SEQ ID NO:12所示。
人源化抗体H7L8(hG1TM)的制备可以参照上面步骤2中的方法。
H7L8(hG1TM)的重链H7(hG1TM)的氨基酸序列
QVQLQQWGAGLLKPSETLSLTCAVYGGSISDYYWNWIRQPPGKGLEWIGEINHRGTTNSNPSLKSRVTLSLDTSKNQFSLKLRSVTAADTAVYYCAFGYSDYEYDWFDPWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGAPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(SEQ ID NO:11)
H7L8(hG1TM)的轻链L8的氨基酸序列
EIVLTQSPATLSLSPGERATLSCRASQTISSYLAWYQQKPGQAPRLLIYDASNRATGIPARFSGSGSGTDFTLTISSLEPEDFAVYYCQQRSNWPITFGQGTNLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ IDNO:12)
4、人源化抗体H7L8(hG4DM)的设计
本发明人在H7L8(hG1WT)的基础上,抗体可变区不变,采用Ig gamma-4chain Cregion作为重链恒定区,并通过在其重链恒定区的第234号位点引进了苯丙氨酸到丙氨酸的点突变(F234A),和第235号位点引进了亮氨酸到丙氨酸的点突变(L235A)获得了恒定区突变的人源化抗体H7L8(hG4DM)。H7L8(hG4DM)的重链氨基酸序列如SEQ ID NO:13所示;轻链氨基酸序列如SEQ ID NO:12所示。
H7L8(hG4DM)的重链H7(hG4DM)的氨基酸序列:
QVQLQQWGAGLLKPSETLSLTCAVYGGSISDYYWNWIRQPPGKGLEWIGEINHRGTTNSNPSLKSRVTLSLDTSKNQFSLKLRSVTAADTAVYYCAFGYSDYEYDWFDPWGQGTLVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK(SEQ ID NO:13)
H7L8(hG4DM)的轻链L8的氨基酸序列与H7L8(hG1TM)轻链氨基酸序列相同,即为SEQ ID NO:12。
5.人源化抗体H7L8(hG4WT)、H7L9(hG4WT)以及H7L10(hG4WT)的表达和纯化
将H7L8(hG4WT)、H7L9(hG4WT)以及H7L10(hG4WT)的重链cDNA序列(可变区编码序列如SEQ ID NO:1所示;恒定区是Ig gamma-4chain C region,如SEQ ID NO:45所示)和H7L8(hG4WT)轻链的cDNA序列(可变区编码序列如SEQ ID NO:3所示;恒定区为human Igkappa chain C region,如SEQ ID NO:40所示)、H7L9(hG4WT)轻链的cDNA序列(可变区编码序列如SEQ ID NO:42所示;恒定区为human Ig kappa chain C region,如SEQ ID NO:40所示)、H7L10(hG4WT)轻链的cDNA序列(可变区编码序列如SEQ ID NO:44所示;恒定区为humanIg kappa chain C region,如SEQ ID NO:40所示)分别克隆到pUC57simple(金斯瑞公司提供)载体中,分别获得pUC57simple-H7和pUC57simple-L8、pUC57simple-L9、pUC57simple-L10质粒。分别将质粒pUC57simple-H7和pUC57simple-L8、pUC57simple-L9、pUC57simple-L10进行酶切(HindIII&EcoRI),电泳回收得到的重链轻链分别亚克隆到pcDNA3.1载体中,提取重组质粒共转染293F细胞。细胞培养7天后,将培养液通过高速离心、上清浓缩后上样至HiTrap MabSelect SuRe柱,用Elution Buffer一步洗脱蛋白并回收目标样品并换液至PBS。
H7L8(hG4WT)、H7L9(hG4WT)或H7L10(hG4WT)重链恒定区氨基酸序列:
ASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEFLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK(SEQ ID NO:45)
H7L8(hG4WT)、H7L9(hG4WT)或H7L10(hG4WT)轻链恒定区氨基酸序列:
RTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ ID NO:40)
制备例2:抗PD-1的抗体14C12及其人源化抗体14C12H1L1的设计和制备
抗PD-1的抗体14C12及其人源化抗体14C12H1L1的重链和轻链的氨基酸序列、以及编码核酸序列分别与中国专利公开CN106967172A(或者CN 106977602A)中的14C12、14C12H1L1完全相同。
(1)14C12的重链可变区序列和轻链可变区序列
14C12的重链可变区的核酸序列:(354bp)
GAGGTCAAACTGGTGGAGAGCGGCGGCGGGCTGGTGAAGCCCGGCGGGTCACTGAAACTGAGCTGCGCCGCTTCCGGCTTCGCCTTTAGCTCCTACGACATGTCATGGGTGAGGCAGACCCCTGAGAAGCGCCTGGAATGGGTCGCTACTATCAGCGGAGGCGGGCGATACACCTACTATCCTGACTCTGTCAAAGGGAGATTCACAATTAGTCGGGATAACGCCAGAAATACTCTGTATCTGCAGATGTCTAGTCTGCGGTCCGAGGATACAGCTCTGTACTATTGTGCAAACCGGTACGGCGAAGCATGGTTTGCCTATTGGGGACAGGGCACCCTGGTGACAGTCTCTGCC(SEQ ID NO:14)
14C12的重链可变区的氨基酸序列:(118aa)
EVKLVESGGGLVKPGGSLKLSCAASGFAFSSYDMSWVRQTPEKRLEWVATISGGGRYTYYPDSVKGRFTISRDNARNTLYLQMSSLRSEDTALYYCANRYGEAWFAYWGQGTLVTVSA(SEQ ID NO:15)
14C12的轻链可变区的核酸序列:(321bp)
GACATTAAGATGACACAGTCCCCTTCCTCAATGTACGCTAGCCTGGGCGAGCGAGTGACCTTCACATGCAAAGCATCCCAGGACATCAACACATACCTGTCTTGGTTTCAGCAGAAGCCAGGCAAAAGCCCCAAGACCCTGATCTACCGGGCCAATAGACTGGTGGACGGGGTCCCCAGCAGATTCTCCGGATCTGGCAGTGGGCAGGATTACTCCCTGACCATCAGCTCCCTGGAGTATGAAGACATGGGCATCTACTATTGCCTGCAGTATGATGAGTTCCCTCTGACCTTTGGAGCAGGCACAAAACTGGAACTGAAG(SEQ ID NO:16)
14C12的轻链可变区的氨基酸序列:(107aa)
DIKMTQSPSSMYASLGERVTFTCKASQDINTYLSWFQQKPGKSPKTLIYRANRLVDGVPSRFSGSGSGQDYSLTISSLEYEDMGIYYCLQYDEFPLTFGAGTKLELK(SEQ ID NO:17)
(2)人源化单克隆抗体14C12H1L1的重链可变区序列和轻链可变区序列、重链序列和轻链序列
14C12H1L1的重链可变区14C12H1v的核酸序列:(354bp)
GAAGTGCAGCTGGTCGAGTCTGGGGGAGGGCTGGTGCAGCCCGGCGGGTCACTGCGACTGAGCTGCGCAGCTTCCGGATTCGCCTTTAGCTCCTACGACATGTCCTGGGTGCGACAGGCACCAGGAAAGGGACTGGATTGGGTCGCTACTATCTCAGGAGGCGGGAGATACACCTACTATCCTGACAGCGTCAAGGGCCGGTTCACAATCTCTAGAGATAACAGTAAGAACAATCTGTATCTGCAGATGAACAGCCTGAGGGCTGAGGACACCGCACTGTACTATTGTGCCAACCGCTACGGGGAAGCATGGTTTGCCTATTGGGGGCAGGGAACCCTGGTGACAGTCTCTAGT(SEQ ID NO:18)
14C12H1L1的重链可变区14C12H1v的氨基酸序列:(118aa)
EVQLVESGGGLVQPGGSLRLSCAASGFAFSSYDMSWVRQAPGKGLDWVATISGGGRYTYYPDSVKGRFTISRDNSKNNLYLQMNSLRAEDTALYYCANRYGEAWFAYWGQGTLVTVSS(SEQ ID NO:19)
14C12H1L1的轻链可变区14C12L1v的核酸序列:(321bp)
GACATTCAGATGACTCAGAGCCCCTCCTCCATGTCCGCCTCTGTGGGCGACAGGGTCACCTTCACATGCCGCGCTAGTCAGGATATCAACACCTACCTGAGCTGGTTTCAGCAGAAGCCAGGGAAAAGCCCCAAGACACTGATCTACCGGGCTAATAGACTGGTGTCTGGAGTCCCAAGTCGGTTCAGTGGCTCAGGGAGCGGACAGGACTACACTCTGACCATCAGCTCCCTGCAGCCTGAGGACATGGCAACCTACTATTGCCTGCAGTATGATGAGTTCCCACTGACCTTTGGCGCCGGGACAAAACTGGAGCTGAAG(SEQ ID NO:20)
14C12H1L1的轻链可变区14C12L1v的氨基酸序列:(107aa)
DIQMTQSPSSMSASVGDRVTFTCRASQDINTYLSWFQQKPGKSPKTLIYRANRLVSGVPSRFSGSGSGQDYTLTISSLQPEDMATYYCLQYDEFPLTFGAGTKLELK(SEQ ID NO:21)
14C12H1L1的重链14C12H1的核酸序列:(1344bp)
GAAGTGCAGCTGGTCGAGTCTGGGGGAGGGCTGGTGCAGCCCGGCGGGTCACTGCGACTGAGCTGCGCAGCTTCCGGATTCGCCTTTAGCTCCTACGACATGTCCTGGGTGCGACAGGCACCAGGAAAGGGACTGGATTGGGTCGCTACTATCTCAGGAGGCGGGAGATACACCTACTATCCTGACAGCGTCAAGGGCCGGTTCACAATCTCTAGAGATAACAGTAAGAACAATCTGTATCTGCAGATGAACAGCCTGAGGGCTGAGGACACCGCACTGTACTATTGTGCCAACCGCTACGGGGAAGCATGGTTTGCCTATTGGGGGCAGGGAACCCTGGTGACAGTCTCTAGTGCCAGCACCAAAGGACCTAGCGTGTTTCCTCTCGCCCCCTCCTCCAAAAGCACCAGCGGAGGAACCGCTGCTCTCGGATGTCTGGTGAAGGACTACTTCCCTGAACCCGTCACCGTGAGCTGGAATAGCGGCGCTCTGACAAGCGGAGTCCATACATTCCCTGCTGTGCTGCAAAGCAGCGGACTCTATTCCCTGTCCAGCGTCGTCACAGTGCCCAGCAGCAGCCTGGGCACCCAGACCTACATCTGTAACGTCAACCACAAGCCCTCCAACACCAAGGTGGACAAGAAAGTGGAGCCCAAATCCTGCGACAAGACACACACCTGTCCCCCCTGTCCTGCTCCCGAACTCCTCGGAGGCCCTAGCGTCTTCCTCTTTCCTCCCAAACCCAAGGACACCCTCATGATCAGCAGAACCCCTGAAGTCACCTGTGTCGTCGTGGATGTCAGCCATGAGGACCCCGAGGTGAAATTCAACTGGTATGTCGATGGCGTCGAGGTGCACAACGCCAAAACCAAGCCCAGGGAGGAACAGTACAACTCCACCTACAGGGTGGTGTCCGTGCTGACAGTCCTCCACCAGGACTGGCTGAACGGCAAGGAGTACAAGTGCAAGGTGTCCAACAAGGCTCTCCCTGCCCCCATTGAGAAGACCATCAGCAAGGCCAAAGGCCAACCCAGGGAGCCCCAGGTCTATACACTGCCTCCCTCCAGGGACGAACTCACCAAGAACCAGGTGTCCCTGACCTGCCTGGTCAAGGGCTTTTATCCCAGCGACATCGCCGTCGAGTGGGAGTCCAACGGACAGCCCGAGAATAACTACAAGACCACCCCTCCTGTCCTCGACTCCGACGGCTCCTTCTTCCTGTACAGCAAGCTGACCGTGGACAAAAGCAGGTGGCAGCAGGGAAACGTGTTCTCCTGCAGCGTGATGCACGAAGCCCTCCACAACCACTACACCCAGAAAAGCCTGTCCCTGAGCCCCGGCAAA(SEQ ID NO:22)
14C12H1L1的重链14C12H1的氨基酸序列:(448aa)
EVQLVESGGGLVQPGGSLRLSCAASGFAFSSYDMSWVRQAPGKGLDWVATISGGGRYTYYPDSVKGRFTISRDNSKNNLYLQMNSLRAEDTALYYCANRYGEAWFAYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(SEQ ID NO:23)
14C12H1L1的轻链14C12L1的核酸序列:(642bp)
GACATTCAGATGACTCAGAGCCCCTCCTCCATGTCCGCCTCTGTGGGCGACAGGGTCACCTTCACATGCCGCGCTAGTCAGGATATCAACACCTACCTGAGCTGGTTTCAGCAGAAGCCAGGGAAAAGCCCCAAGACACTGATCTACCGGGCTAATAGACTGGTGTCTGGAGTCCCAAGTCGGTTCAGTGGCTCAGGGAGCGGACAGGACTACACTCTGACCATCAGCTCCCTGCAGCCTGAGGACATGGCAACCTACTATTGCCTGCAGTATGATGAGTTCCCACTGACCTTTGGCGCCGGGACAAAACTGGAGCTGAAGCGAACTGTGGCCGCTCCCTCCGTCTTCATTTTTCCCCCTTCTGACGAACAGCTGAAATCAGGCACAGCCAGCGTGGTCTGTCTGCTGAACAATTTCTACCCTAGAGAGGCAAAAGTGCAGTGGAAGGTCGATAACGCCCTGCAGTCCGGCAACAGCCAGGAGAGTGTGACTGAACAGGACTCAAAAGATAGCACCTATTCCCTGTCTAGTACACTGACTCTGTCCAAGGCTGATTACGAGAAGCACAAAGTGTATGCATGCGAAGTGACACATCAGGGACTGTCAAGCCCCGTGACTAAGTCTTTTAACCGGGGCGAATGT(SEQ ID NO:24)
14C12H1L1的轻链14C12L1的氨基酸序列:(214aa)
DIQMTQSPSSMSASVGDRVTFTCRASQDINTYLSWFQQKPGKSPKTLIYRANRLVSGVPSRFSGSGSGQDYTLTISSLQPEDMATYYCLQYDEFPLTFGAGTKLELKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC(SEQ IDNO:25)
抗体14C12和14C12H1L1的CDR相同,如下(按照IMGT编号系统):
HCDR1:GFAFSSYD(SEQ ID NO:26)
HCDR2:ISGGGRYT(SEQ ID NO:27)
HCDR3:ANRYGEAWFAY(SEQ ID NO:28)
LCDR1:QDINTY(SEQ ID NO:29)
LCDR2:RAN(SEQ ID NO:30)
LCDR3:LQYDEFPLT(SEQ ID NO:31)
14C12H1L1(M)的重链可变区序列和轻链可变区序列
以14C12H1L1为基础对其骨架区(轻链)中个别氨基酸进行了突变得到14C12H1L1(M)。
14C12H1L1(M)的重链可变区14C12H1(M):
与14C12H1L1的重链可变区14C12H1相同,即氨基酸序列如SEQ ID NO:19所示。
14C12H1L1(M)的轻链可变区14C12L1(M):
DIQMTQSPSSMSASVGDRVTFTCRASQDINTYLSWFQQKPGKSPKTLIYRANRLVSGVPSRFSGSGSGQDYTLTISSLQPEDMATYYCLQYDEFPLTFGAGTKLELKR(SEQ ID NO:38)
制备例3:人源化抗体14C12H1L1(hG4DM)的设计
本发明人在14C12H1L1的基础上,抗体可变区不变,采用Ig gamma-4chain Cregion作为重链恒定区,并通过在其重链恒定区的第234号位点引进了苯丙氨酸到丙氨酸的点突变(F234A),和第235号位点引进了亮氨酸到丙氨酸的点突变(L235A)获得了恒定区突变的人源化抗体14C12H1L1(hG4DM)。14C12H1L1(hG4DM)的重链14C12H1(hG4DM)的氨基酸序列如SEQ ID NO:32所示;轻链氨基酸序列如SEQ ID NO:25所示。
14C12H1L1(hG4DM)重链氨基酸序列
EVQLVESGGGLVQPGGSLRLSCAASGFAFSSYDMSWVRQAPGKGLDWVATISGGGRYTYYPDSVKGRFTISRDNSKNNLYLQMNSLRAEDTALYYCANRYGEAWFAYWGQGTLVTVSSASTKGPSVFPLAPCSRSTSESTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTKTYTCNVDHKPSNTKVDKRVESKYGPPCPPCPAPEAAGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSQEDPEVQFNWYVDGVEVHNAKTKPREEQFNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKGLPSSIEKTISKAKGQPREPQVYTLPPSQEEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSRLTVDKSRWQEGNVFSCSVMHEALHNHYTQKSLSLSLGK(SEQID NO:32)
14C12H1L1(hG4DM)轻链氨基酸序列与14C12H1L1的轻链14C12L1的氨基酸序列相同,即为SEQ ID NO:25。
制备例4:人源化抗体14C12H1L1(hG1TM)的序列设计
本发明人在人源化抗体14C12H1L1的基础上,按照EU编号系统(EU numberingsystem),通过在其重链铰链区域第234号位点引进了亮氨酸到丙氨酸的点突变(L234A),第235号位点引进了亮氨酸到丙氨酸的点突变(L235A),第237号位点引进了甘氨酸到丙氨酸的点突变(G237A),获得了突变的人源化14C12H1L1(hG1TM)。
14C12H1L1(hG1TM)的重链14C12H1(hG1TM)的核酸序列:(1344bp)
GAAGTGCAGCTGGTCGAGTCTGGGGGAGGGCTGGTGCAGCCCGGCGGGTCACTGCGACTGAGCTGCGCAGCTTCCGGATTCGCCTTTAGCTCCTACGACATGTCCTGGGTGCGACAGGCACCAGGAAAGGGACTGGATTGGGTCGCTACTATCTCAGGAGGCGGGAGATACACCTACTATCCTGACAGCGTCAAGGGCCGGTTCACAATCTCTAGAGATAACAGTAAGAACAATCTGTATCTGCAGATGAACAGCCTGAGGGCTGAGGACACCGCACTGTACTATTGTGCCAACCGCTACGGGGAAGCATGGTTTGCCTATTGGGGGCAGGGAACCCTGGTGACAGTCTCTAGTGCCAGCACCAAAGGGCCCAGCGTGTTTCCTCTCGCCCCCTCCTCCAAAAGCACCAGCGGAGGAACCGCTGCTCTCGGATGTCTGGTGAAGGACTACTTCCCTGAACCCGTCACCGTGAGCTGGAATAGCGGCGCTCTGACAAGCGGAGTCCATACATTCCCTGCTGTGCTGCAAAGCAGCGGACTCTATTCCCTGTCCAGCGTCGTCACAGTGCCCAGCAGCAGCCTGGGCACCCAGACCTACATCTGTAACGTCAACCACAAGCCCTCCAACACCAAGGTGGACAAGAAAGTGGAGCCCAAATCCTGCGACAAGACACACACCTGTCCCCCCTGTCCTGCTCCCGAAGCTGCTGGAGCCCCTAGCGTCTTCCTCTTTCCTCCCAAACCCAAGGACACCCTCATGATCAGCAGAACCCCTGAAGTCACCTGTGTCGTCGTGGATGTCAGCCATGAGGACCCCGAGGTGAAATTCAACTGGTATGTCGATGGCGTCGAGGTGCACAACGCCAAAACCAAGCCCAGGGAGGAACAGTACAACTCCACCTACAGGGTGGTGTCCGTGCTGACAGTCCTCCACCAGGACTGGCTGAACGGCAAGGAGTACAAGTGCAAGGTGTCCAACAAGGCTCTCCCTGCCCCCATTGAGAAGACCATCAGCAAGGCCAAAGGCCAACCCAGGGAGCCCCAGGTCTATACACTGCCTCCCTCCAGGGACGAACTCACCAAGAACCAGGTGTCCCTGACCTGCCTGGTCAAGGGCTTTTATCCCAGCGACATCGCCGTCGAGTGGGAGTCCAACGGACAGCCCGAGAATAACTACAAGACCACCCCTCCTGTCCTCGACTCCGACGGCTCCTTCTTCCTGTACAGCAAGCTGACCGTGGACAAAAGCAGGTGGCAGCAGGGAAACGTGTTCTCCTGCAGCGTGATGCACGAAGCCCTCCACAACCACTACACCCAGAAAAGCCTGTCCCTGAGCCCCGGCAAA(SEQ ID NO:33)
14C12H1L1(hG1TM)的重链14C12H1(hG1TM)的氨基酸序列:(448aa)
EVQLVESGGGLVQPGGSLRLSCAASGFAFSSYDMSWVRQAPGKGLDWVATISGGGRYTYYPDSVKGRFTISRDNSKNNLYLQMNSLRAEDTALYYCANRYGEAWFAYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPEAAGAPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK(SEQ ID NO:34)
14C12H1L1(hG1TM)的轻链的核酸序列同SEQ ID NO:24。
14C12H1L1(hG1TM)的轻链的氨基酸序列同14C12H1L1的轻链14C12L1的氨基酸序列,即SEQ ID NO:25。
制备例5:抗LAG3/PD-1双功能抗体的设计和制备
1.序列设计
本发明中的双功能抗体BS-PL021A、Bs-PL022B、BS-PL023C、Bs-PLV02的结构模式属于Morrison模式(IgG-scFv),即在一个IgG抗体的两条重链的C端均连接另一个抗体的scFv片段,其重链和轻链的主要组成设计如下面的表1。
上面的表1中:
(1)连接片段(GGGGS)3氨基酸序列:
GGGGSGGGGSGGGGS(SEQ ID NO:35)
连接片段(GGGGS)4氨基酸序列:
GGGGSGGGGSGGGGSGGGGS(SEQ ID NO:36)
连接片段(GGGGS)4G氨基酸序列:
GGGGSGGGGSGGGGSGGGGSG(SEQ ID NO:37)
(2)右下角标注“v”的,是指相应重链的可变区或者相应轻链的可变区。没有标注“v”的,相应重链或者轻链为包含恒定区的全长。这些可变区或者全长的氨基酸序列及其编码核酸序列均参照上面的制备例中记载的相应序列。
2.抗体的表达和纯化
分别将Bs-PL021A、Bs-PL022B、Bs-PL023C、Bs-PLV02的重链cDNA序列和轻链的cDNA序列克隆到pUC57simple(金斯瑞公司提供)载体中,分别获得pUC57simple-Bs-PL021AH/pUC57simple-Bs-PL021AL、pUC57simple-Bs-PL022BH/pUC57simple-Bs-PL022BL、pUC57simple-Bs-PL023CH/pUC57simple-Bs-PL023CL、pUC57simple-Bs-PLV02H/pUC57simple-Bs-PLV02L、pUC57simple-Bi-PGV02/pUC57simple-Bi-PGV02质粒。
分别将质粒pUC57simple-Bs-PL021AH/pUC57simple-Bs-PL021AL、pUC57simple-Bs-PL022BH/pUC57simple-Bs-PL022BL、pUC57simple-Bs-PL023CH/pUC57simple-Bs-PL023CL、pUC57simple-Bs-PLV02H/pUC57simple-Bs-PLV02L pUC57simple-Bi-PGV02/pUC57simple-Bi-PGV02进行酶切(HindIII&EcoRI),电泳回收得到的重链轻链分别亚克隆到pcDNA3.1载体中,提取重组质粒共转染293F细胞。细胞培养7天后,将培养液通过高速离心、上清浓缩后上样至HiTrap MabSelect SuRe柱,用Elution Buffer一步洗脱蛋白并回收目标样品并换液至PBS。
制备例6:融合蛋白PD-1-mFc、PD-1-hFc和PDL1-hFc的制备
融合蛋白PD-1-mFc、PD-1-hFc和PDL1-hFc的制备以及SDS-PAGE电泳检测完全参照中国专利公开CN106632674A的制备例1进行。
其中,本制备例中的融合蛋白PD-1-mFc、PD-1-hFc和PDL1-hFc的氨基酸序列及其编码核酸序列分别与中国专利公开CN106632674A的制备例1中的PD-1-mFc、PD-1-hFc和PDL1-hFc相同。
制得了融合蛋白PD-1-mFc、PD-1-hFc和PDL1-hFc。
制备例7:人抗鸡蛋溶酶体抗体的制备
人抗鸡蛋溶酶体抗体(human anti-Hen Egg Lysozyme IgG,anti-HEL,即humanIgG,简称hIgG),其序列来自于Acierno等人发表的Affinity maturation increases thestability and plasticity of the Fv domain of anti-protein antibodies研究中FabF10.6.6序列的可变区序列(Acierno等人.J Mol Biol.2007;374(1):130-46.)。制备方法如下:
human IgG委托南京金斯瑞生物对抗体的重轻链(全序列或可变区)基因进行氨基酸的密码子优化和基因合成,参照《分子克隆实验指南(第三版)》介绍的标准技术,采用PCR、酶切、DNA胶回收、连接转化、菌落PCR或酶切鉴定等标准的分子克隆技术将重轻链基因分别亚克隆到哺乳动物表达系统的抗体重链表达载体和抗体轻链表达载体,并进一步对重组表达载体的重轻链基因进行测序分析。测序验证正确后,中大量制备去内毒素级别的表达质粒并将重轻链表达质粒瞬时共转染HEK293细胞进行重组抗体的表达。培养7天后收集细胞培养液,进行rProtein A柱(GE)亲和纯化,收获的抗体样品用SDS-PAGE和SEC-HPLC标准分析技术对其进行质量鉴定。
实验例1:ELISA方法测定抗LAG3-抗PD-1双特异性抗体与抗原的结合活性
1.间接ELISA方法分别测定BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)与抗原PD-1-mFc的结合活性。具体方法如下:
将人PD-1-mFc,0.5μg/mL包被酶标板置于4℃孵育过夜,然后使用PBST洗板包被了抗原的酶标板1次,再使用1%BSA的PBS溶液作为封闭液在37℃下对酶标板进行封闭2小时。酶标板封闭结束后用PBST洗板3次,加入PBST溶液梯度稀释的抗体(抗体稀释梯度详见表2),加入待测抗体的酶标板置于37℃条件下孵育30分钟,孵育完成后用PBST洗板3次。洗板后加入1:5000比例稀释的HRP标记羊抗人IgG FC(H+L)(Jackson,货号:109-035-098)二抗工作液,然后置于37℃条件下孵育30分钟。孵育完成后使用PBST洗板4次,后加入TMB(Neogen,308177)避光显色5min,加入终止液终止显色反应。立即把酶标板放入酶标仪中,选择450nm光波长读取酶标板各孔的OD数值。用SoftMax Pro 6.2.1软件对数据进行分析处理。
检测结果如表2和图1所示。
表2:ELISA检测BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)与人PD-1-mFc的结合
由图1可知,BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)与抗原人PD-1-mFc能够有效地结合,并且其结合效率呈剂量依赖关系。通过对结合的抗体进行吸光度定量分析,曲线模拟计算获得抗体BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)(作为对照)的结合效率EC50分别为0.066nM、0.074nM、0.046nM、0.103nM、0.02nM。
结果表明,在相同实验条件下,BS-PL021A、BS-PL022B、BS-PL023C结合PD-1-mFc的活性与同靶点阳性对照14C12H1L1(hG1TM)基本相当,提示BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02具有有效结合PD-1-mFc的活性。
2.间接ELISA方法分别测定BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、Relatlimab、H7L8(hG1WT)与抗原LAG3-mFc的结合活性。
具体方法如下:
将人LAG3-mFc(康方生物,批号:20200417),2μg/mL包被酶标板置于4℃孵育过夜,然后使用PBST洗板包被了抗原的酶标板1次,再使用1%BSA的PBS溶液作为封闭液在37℃下对酶标板进行封闭2小时。酶标板封闭结束后用PBST洗板3次,加入PBST溶液梯度稀释的抗体(抗体稀释梯度详见表3),加入待测抗体的酶标板置于37℃条件下孵育30分钟,孵育完成后用PBST洗板3次。洗板后加入1:5000比例稀释的HRP标记羊抗人IgG FC(H+L)(Jackson,货号:109-035-098)二抗工作液,然后置于37℃条件下孵育30分钟。孵育完成后使用PBST洗板4次,后加入TMB(Neogen,308177)避光显色5min,加入终止液终止显色反应。立即把酶标板放入酶标仪中,选择450nm光波长读取酶标板各孔的OD数值。用SoftMax Pro 6.2.1软件对数据进行分析处理。
检测结果如表3和图2所示。
表3:ELISA检测BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、Relatlimab、H7L8(hG1WT)与LAG3-mFc的结合
由图2可知,BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、Relatlimab、H7L8(hG1WT)与抗原人LAG3-mFc能够有效的结合,并且其结合效率呈剂量依赖关系,各剂量的吸光度强度见表3,通过对结合的抗体进行吸光度定量分析,曲线模拟计算获得抗体BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、Relatlimab(作为阳性对照)、H7L8(hG1WT)(作为对照)的结合效率EC50分别为0.073nM、0.081nM、0.377nM、0.685nM、0.106nM、0.045nM。
以上实验结果表明,在相同实验条件下,BS-PL021A、BS-PL022B、H7L8(hG1WT)具有有效结合LAG3-mFc的活性,且BS-PL021A、BS-PL022B、H7L8(hG1WT)结合人LAG3-mFc的活性强于靶点阳性药Relatlimab。特别是H7L8(hG1WT),其结合人LAG3-mFc的活性显著强于靶点阳性药Relatlimab。
实验例2:竞争ELISA方法分别测定抗体抗LAG3-抗PD-1双特异性抗体与人PDL1-
mFc竞争结合人PD-1-mFc-Biotin的活性
将人PDL1-mFc(PD-L1 Genbank ID:NP_054862.1,mFc SEQ ID NO:)以2μg/mL包被酶标板后,4℃孵育过夜。孵育结束后用1%BSA的PBS溶液在37℃条件下对酶标板进行封闭2小时,封闭结束后洗板三次并拍干。在稀释板上以80nM(终浓度40nM)作为起始浓度进行一系列3倍稀释比例将抗体进行梯度稀释至7个浓度,并设空白对照,然后加入等体积的1.2μg/mL(终浓度0.6μg/mL)的人PD-1-mFc-Biotin溶液,和抗体混匀后在室温孵育10分钟。然后将反应后的混合液加入到包被好的酶标板,在37℃条件下孵育30分钟。孵育结束用PBST洗板三次并拍干,加入SA-HRP(KPL,14-30-00)工作液,在37℃条件下孵育30分钟。孵育完成后洗板四次拍干,后加入TMB(Neogen,308177)避光显色5min,加入终止液终止显色反应。立即把酶标板放入酶标仪中,选择450nm光波长读取酶标板各孔的OD数值,用SoftMax Pro6.2.1软件对数据进行分析处理。
检测结果如图3所示。各剂量的OD值见表4。通过对结合的抗体进行吸光强度定量分析,曲线模拟抗体阻断人PD-1-mFc-Biotin与其配体人PDL1-mFc的结合效率获得竞争结合EC50(表4)。
表4:BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)与人PDL1-mFc竞争结合人PD-1-mFc-Biotin的活性检测结果
结果表明,BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)(作为对照)能有效地阻断抗原人PD-1-mFc-Biotin与其配体人PDL1-mFc的结合,且阻断效率呈现剂量依赖关系,BS-PL021A、BS-PL022B、BS-PL023C、Bs-PLV02、14C12H1L1(hG1TM)阻断人PD-1-mFc-Biotin与其配体人PDL1-mFc结合的EC50分别为3.031nM、3.462nM、2.982nM、5.045nM、2.606nM。BS-PL021A、BS-PL022B、BS-PL023C阻断人PD-1-mFc-Biotin与其配体人PDL1-mFc结合的效率与14C12H1L1(hG1TM)基本相当。
实验例3:FACS检测抗LAG3-抗PD-1双特异性抗体的结合活性
1.FACS检测抗LAG3-抗PD-1双特异性抗体与293T-PD1膜表面PD-1的结合活性
收集对数生长期293T-PD1细胞,按3×105个细胞/孔将细胞转移至尖底96孔板中,加入100μL 1%PBSA,350×g离心5min,去上清。加入PBSA稀释的抗体100μL(终浓度分别为300、100、33.3、11.1、3.7、1.23、0.123和0.0123nM),轻柔混匀后于冰上孵育1h。加入100μL1%PBSA,350×g离心5min,去上清,并用200μL 1%PBSA洗涤两次。加入400倍稀释的FITC标记羊抗人IgG二抗(Jackson,货号:109-095-098)重悬混匀,冰上避光孵育0.5h。加入100μL1%PBSA,350xg离心5min,去上清,并用200μL 1%PBSA洗涤两次。加入400μL 1%PBSA重悬细胞沉淀,并转移至流式管,FACSCalibur检测。
实验结果如表5和图4所示,14C12H1L1(hG1TM)、BS-PL021A、BS-PL022B、Bs-PLV02、Bi-PGV02、Nivolumab、Pembrolizumab均可特异性与293T-PD1细胞膜表面PD-1受体结合。
表5:FACS检测14C12H1L1(hG1TM)、BS-PL021A、BS-PL022B、Bs-PLV02、Bi-PGV02、Nivolumab、Pembrolizumab 293T-PD1细胞表面PD-1的结合活性
在相同实验条件下,14C12H1L1(hG1TM)、BS-PL021A、BS-PL022B、Bs-PLV02、Bi-PGV02、Nivolumab、Pembrolizumab与293T-PD1细胞结合的EC50分别为5.351nM、6.851nM、6.066nM、6.866nM、7.206nM、3.073nM、3.970nM。以上实验结果表明,在相同实验条件下14C12H1L1(hG1TM)、BS-PL021A、BS-PL022B、Bs-PLV02、Bi-PGV02与293T-PD1细胞结合活性与对照抗体Nivolumab、Pembrolizumab相当,提示14C12H1L1(hG1TM)、BS-PL021A、BS-PL022B、Bs-PLV02、Bi-PGV02具有有效结合293T-PD1细胞膜表面PD-1的活性。
2.FACS检测抗LAG3-抗PD-1双特异性抗体与293T-LAG3细胞膜表面LAG3的结合活性
常规胰酶消化对数期293T-LAG3细胞,按3×105个细胞/孔将细胞转移至尖底96孔板中,加入100μL 1%PBSA,350×g离心5min,去上清。加入1%PBSA稀释的抗体100μL(终浓度分别为300、100、33.3、11.1、3.7、1.23、0.123、0.0123和0.00123nM),混匀后于冰上孵育1h。加入100μL 1%PBSA,350×g离心5min,去上清,并用200μL 1%PBSA洗涤两次。加入300倍稀释的FITC标记羊抗人IgG二抗(Jackson,货号:109-095-098)重悬混匀,冰上避光孵育0.5h。加入500μLPBSA,350×g离心5min,去上清,并用200μL 1%PBSA洗涤两次。加入300μL1%PBSA重悬细胞沉淀,并转移至流式管,FACSCalibur检测。
实验结果如表6和图5所示。
表6:FACS检测BS-PL022B、Relatlimab与293T-LAG3细胞表面LAG33的结合活性。
结果显示,在相同实验条件下,BS-PL022B、Relatlimab与293T-LAG3细胞膜表面LAG3结合的EC50分别为3.213nM、4.113nM,可见BS-PL022B与293T-LAG3细胞膜表面LAG3的结合活性高于Relatlimab。
以上实验结果表明,BS-PL022B和同靶点阳性药Relatlimab均可呈剂量依赖性与293T-LAG3细胞膜表面LAG-3特异性结合。提示BS-PL022B具有有效结合293T-LAG3膜表面LAG3的活性,且其结合能力强于Relatlimab。
实验例4:抗LAG3-抗PD-1双特异性抗体对细胞膜表面抗原的竞争性结合
1、竞争流式细胞法测定抗LAG3-抗PD-1双特异性抗体与PDL1竞争结合细胞膜表面抗原PD-1。
取293T-PD1细胞常规消化,按3×105个细胞/孔将细胞转移至尖底96孔板中,加入100μL 1%PBSA离心洗涤。加入相应梯度稀释的抗体(终浓度分别为300、100、33.3、11.1、3.7、1.23、0.123和0.0123nM),每样本100μL,冰上孵育30min。每管加入100μL PDL-1-mFc,混匀,使得最终浓度为20nM,冰上孵育1h。350×g离心5min,去上清;用200μL 1%PBSA洗涤两次。加入100μL 400倍稀释的FITC羊抗鼠IgG/IgM抗体(BD,货号:555988),空白样本则加入100μL 1%PBSA,混匀后冰上避光孵育30min。洗涤离心后重悬,转移至流式上样管,上机测试。
结果如图6所示,各样品的EC50值见表7。通过荧光定量分析和曲线拟合,计算出抗体Nivolumab、Pembrolizumab、14C12H1L1(hG1TM)、BS-PL022B的竞争结合EC50分别为3.608nM、2.769nM、2.511nM、5.123nM。
表7:FACS检测Nivolumab、Pembrolizumab、14C12H1L1(hG1TM)、BS-PL022B竞争结合293T-PD-1表面抗原的荧光强度分析
结果显示,BS-PL022B抗体能有效地阻断PD-L1对293T-PD1宿主细胞表面的PD-1的结合,且呈剂量依赖关系。
2、竞争流式细胞法测定抗LAG3-抗PD-1双特异性抗体与LAG3-mG1Fc竞争结合细胞膜表面抗原MHC II。
按实验设计稀释抗体和LAG3-mG1Fc,1:1混合均匀,使得LAG3-mG1Fc(康方生产,批号20190508)终浓度为3nM,抗体终浓度为300、100、33.3、11.1、3.7、1.23、0.123、0.0123、0.00123nM,冰上孵育30min;收集Raji细胞(中国科学院上海生命科学研究院细胞资源中心,货号:TCHu 44),每样本300000细胞接种至96孔尖底板,补加1%PBSA,500xg离心5min弃上清;100μL抗体与蛋白预孵液重悬细胞,设计空白对照(细胞+PBSA+PBSA)、阴性对照(细胞+PBSA+二抗)及同型对照,冰上避光孵育1h;加入100μL 1%PBSA,500xg离心5min,去上清;200μL 1%PBSA重悬细胞,500xg离心5min,去上清,重复洗涤一次;100μL APC goat antimouse IgG二抗(BioLegend,货号:405308)(1:300稀释)重悬细胞,空白对照则用100μL 1%PBSA重悬,冰上避光孵育30min;加入100μL 1%PBSA,500xg离心5min,去上清;200μL 1%PBSA重悬细胞,500xg离心5min,去上清,重复洗涤一次;200μL 1%PBSA重悬细胞,转移至流式上样管,上机测试。
结果如图7、表8所示,各样品的EC50值见表。通过荧光定量分析和曲线拟合,计算出抗体Relatlimab、BS-PL022B的竞争结合EC50分别为0.9689nM、1.306nM。
表8:FACS检测Relalimab、BS-PL022B竞争结合Raji细胞表面抗原的荧光强度分析
| Relatlimab | BS-PL022B | |
| EC<sub>50</sub>(nM) | 0.9689 | 1.306 |
| R2 | 0.9964 | 0.9948 |
结果显示,BS-PL022B抗体能有效地阻断LAG-3对Raji宿主细胞表面的MHC II的结合,且呈剂量依赖关系。
实验例5:抗LAG3-抗PD-1双特异性抗体阻断实验
1、抗LAG3-抗PD-1双特异性抗体阻断LAG3与MHCII结合
收集Jurkat-NFAT-PD1-LAG3(康方生物构建,P9,活率:97.75%)细胞和Raji细胞(中国科学院上海生命科学研究院细胞资源中心,货号:TCHu 44),110×g离心5min,去上清,用1640培养基(含10%FBS)重悬细胞,计数。将Jurkat-NFAT-PD1-LAG3细胞按10×104个细胞/孔接种至黑底96孔板(Corning,型号:3916),25μL/孔;按实验设计加入抗体,30μL/孔(终浓度分别为900nM、300nM、100nM、33.3nM、3.3nM、0.3nM、0.03nM和0.003nM),置于37℃,5%CO2培养箱中预先孵育30min。将SEE(Staphylococcal enterotoxin E)(终浓度0.05ng/mL,Toxin Technology,货号:ET404)和Raji细胞置于37℃,5%CO2培养箱中孵育30min;孵育30min后,将Raji细胞按2×104/孔、25μL/孔加入到96孔板中,体系终体积为80μL;混匀后置于37℃,5%CO2培养箱中孵育16h。取出培养板,平衡至室温,加入Bright-GloTMLuciferase Assay System(Promega,货号:E2650)80μL/孔,避光孵育2min后读取RLU值。
结果如图8A、图8B和表9所示。
表9:抗LAG3-抗PD-1双特异性抗体阻断LAG3与MHCII结合
| Relatlimab | Bs-PLV02 | Bi-PGV02 | BS-PL022B | |
| EC<sub>50</sub>(nM) | 8.563 | 1.210 | 1.483 | 0.9762 |
结果显示,Bs-PLV02、Bi-PGV02、BS-PL022B和Relatlimab阻断LAG3与MHCII结合的EC50(nM)分别为1.21nM、1.483nM、0.9762nM、8.563nM。Bs-PLV02、Bi-PGV02、BS-PL022B阻断LAG3与MHCII结合的能力强于阳性对照抗体Relatlimab。
2、抗LAG3-抗PD-1双特异性抗体阻断PD-1与PD-L1结合
PDL1 aAPC/CHO-K1细胞(Promega,货号:J1081A)4×104个细胞/孔接种于96孔平底黑板(Corning,型号:3916)培养过夜,每孔100μL(培养基为该细胞的生长培养基:Ham F-12+10%FBS)。次日,去板内培养基,加入PD1效应细胞(Promega,货号:J1121A)5×104个细胞/孔,40μL/孔(培养基为:1640+10%FBS);加入抗体,40μL/孔(终浓度分别为1000nM、300nM、100nM、33.3nM、11.1nM、3.7nM、1.23nM、0.123nM和0.0123nM),与此同时设置同型对照组和阴性对照组,终体积为80μL/孔;置于培养箱孵育6h。取出培养板,平衡至室温,加入Bright-GloTM Luciferase Assay System(Promega,货号:E2650)80μL/孔,避光孵育2min后读取RLU值。
结果如图9A、图9B和表10所示。
表10:抗LAG3-抗PD-1双特异性抗体阻断PD-1与PD-L1结合
结果显示,Nivolumab、Pembrolizumab、14C12H1L1(hG1TM)、BS-PL022B阻断PD-1和PD-L1结合的EC50(nM)分别为4.089nM、1.281nM、5.219nM、20.01nM。结果说明Nivolumab、Pembrolizumab、14C12H1L1(hG1TM)、BS-PL022B均能阻断PD-1和PD-L1结合。
3、抗LAG3-抗PD-1双特异性抗体同时阻断LAG-3与MHCII以及PD-1与PD-L1结合
收集Jurkat-NFAT-PD1-LAG3细胞和Raji-PDL1细胞,110×g离心5min去上清,用1640培养基(含10%FBS)重悬细胞,计数。
Jurkat-NFAT-PD1-LAG3细胞10×104个细胞/孔接种至黑底96孔板(Corning,型号:3916),25μL/孔,按实验设计加入抗体,30μL/孔(终浓度分别为3000、1000、300、30、3、0.3、0.03和0.003nM),置于37℃,5%CO2培养箱中预先孵育30min;向Raji-PDL1细胞加入SEE(Staphylococcal enterotoxin E)(终浓度0.1ng/mL)后置于37℃,5%CO2培养箱中孵育30min。孵育30min后,将Raji-PDL1细胞按3×104/孔、25μL/孔加入到96孔板中,体系终体积为80μL;混匀后置于37℃,5%CO2培养箱中孵育15h。取出培养板,平衡至室温,加入Bright-GloTMLuciferase Assay System(Promega,货号:E2650)80μL/孔,避光孵育5min后读取RLU值。
结果如图10A、图10B和表11所示。
表11:抗LAG3-抗PD-1双特异性抗体同时阻断LAG-3与MHCII以及PD-1与PD-L1结合
结果显示,Pembrolizumab、Relatlimab、14C12H1L1(hG1TM)、14C12H1L1(hG1TM)+Relatlimab、BS-PL022B同时阻断PD1和PD-L1结合以及LAG3与MHCII结合的EC50(nM)分别为24.01nM、5.525nM、44.86nM、29.75nM、16.21nM。Pembrolizumab、Relatlimab、14C12H1L1(hG1TM)、14C12H1L1(hG1TM)+Relatlimab、Bs-PL022B均能同时阻断PD-1和PD-L1结合以及LAG3与MHCII结合,且Bs-PL022B的阻断能力要强于其他抗体。
实验例6:抗LAG3-抗PD-1双特异性抗体桥连实验
常规消化CHO-K1(中国医学科学院基础医学研究所细胞资源中心,货号:3111C0001CCC000004),CHO-K1-PD1(康方生物构建),CHO-K1-LAG3(康方生物构建)细胞,170×g离心5min,弃上清;用完全培养基重悬细胞后,计数及活率。对CHO-K1-PD1细胞染CFSE(CFSE Cell Division Tracker Kit,Biolegend,货号:423801)(处理浓度1μM,1mL/10×106个细胞),CHO-K1-LAG3细胞染Far red(Thermofisher,货号:C34564)(处理浓度0.3μM,1mL/10×106个细胞),CHO-K1细胞染Far red或CFSE,培养箱中染色20min;完全培养基终止染色,170×g离心5min弃上清,再加入完全培养基培养箱孵育10min,170×g离心5min弃上清,重复洗涤1次,完全培养基重悬计数。染色后的CHO-K1-PD1、CHO-K1-LAG3及CHO-K1细胞按1.5×105个细胞/孔分别转移至尖底96孔板中,补加buffer(PBS+1%人血清)(人血清,中科晨宇,货号:168014-100mL),离心弃上清;按实验设计向CHO-K1-PD1加入抗体(终浓度为30、3、1、0.3、0.1nM),向CHO-K1-LAG3补加buffer或加入抗体(终浓度为30nM、3nM、1nM、0.3nM、0.1nM),向CHO-K1补加buffer,100μL/孔,冰上孵育60min。
加100μL buffer,350×g离心5min,弃上清,200μL buffer重复洗涤2次。用100μLbuffer分别重悬CHO-K1-LAG3及CHO-K1细胞,并转移至相应的CHO-K1-PD1样品孔,混匀,1.5×105个细胞/孔冰上避光孵育40min。加200μL buffer重悬细胞,转至流式上样管,上机测试。
结果如图11所示。与同型对照相比,抗LAG3-抗PD-1双特异性抗体可同时结合CHO-K1-PD1和CHO-K1-LAG3细胞,将两个细胞桥连起来,而14C12H1L1(hG1TM)、Relatlimab即便是联用也无此作用。
实验例7:混合淋巴细胞反应MLR检测抗LAG3-抗PD-1双特异性抗体促IFN-γ和IL-
2分泌的生物活性
1.抗LAG3-抗PD-1双特异性抗体促Raji-PDL1混合淋巴反应体系分泌IFN-γ的生物活性检测
Raji-PDL1细胞常规传代培养;复苏PBMC,用10mL 1640完全培养基培养,0.5μg/mL的SEB(Staphylococcal enterotoxin B)(德诺泰克,货号:S010201)刺激两天。Raji-PDL1细胞用终浓度为2μg/mL的MMC(Stressmarq,货号:SIH-246-10MG)处理,置于37℃、5%CO2二氧化碳培养箱中1小时;收集经SEB刺激2天后PBMC和经MMC处理1小时的Raji-PDL1细胞,用PBS洗涤两次;完全培养基重悬计数后,各10×104个细胞/孔加入到U型96孔板(Corning,型号:3799)中共培养。按实验设计加入抗体(终浓度为300nM、30nM、3nM),于培养箱共培养3天;3天后,1200rpm离心5min,收集细胞培养上清,ELISA法进行IFN-γ检测。
如图12A所示,人PBMC和Raji-PDL1细胞混合培养后对PBMC的IFN-γ的分泌具有显著促进作用,在混合培养体系中同时加入抗体能显著诱导PBMC进一步分泌IFN-γ,促IFN-γ分泌活性水平方面,BS-PL022B抗体的活性优于PD-1单靶点抗体14C12H1L1(hG1TM)以及LAG-3单靶点对照抗体Relatlimab。甚至与14C12H1L1(hG1TM)和体Relatlimab联用相比,BS-PL022B在两个不同抗体浓度水平(30nM和300nM)都具更佳的促IFN-γ分泌潜能。
2.抗LAG-3-抗PD-1双特异性抗体促Raji-PDL1混合淋巴反应体系分泌IL-2的生物活性检测
Raji-PDL1细胞常规传代培养;复苏PBMC,用10mL 1640完全培养基培养,添加0.5μg/mL的SEB(Staphylococcal enterotoxin B)(德诺泰克,货号:S010201)刺激两天。Raji-PDL1细胞用终浓度为2μg/mL的MMC(Stressmarq,货号:SIH-246-10MG)处理,置于37℃、5%CO2二氧化碳培养箱中1小时。收集经SEB刺激2天后的PBMC和经MMC处理1小时的Raji-PDL1细胞,用PBS洗两次;完全培养基重悬计数后,各10×104个细胞/孔加入U型96孔板(Corning,型号:3799)中共培养。按实验设计加入抗体(终浓度为300nM、30nM、3nM),共培养3天;3天后,1200rpm离心5min,收集细胞培养上清,ELISA法进行IL-2检测。
如图12B所示,人PBMC和Raji-PDL1细胞混合培养后对PBMC的IL-2的分泌有一定的促进作用,在混合培养体系中同时加入抗体能显著诱导PBMC进一步分泌IL-2,具有显著剂量依赖关系,促IL-2分泌活性水平方面,与PD-1单靶点抗体14C12H1L1(hG1TM)以及LAG-3单靶点对照抗体Relatlimab相比,BS-PL022B在三个不同抗体浓度水平都具更佳的促IL-2分泌潜能。甚至与14C12H1L1(hG1TM)和体Relatlimab联用相比,BS-PL022B在三个不同抗体浓度水平都具更佳的促IL-2分泌潜能。
实验例8:BS-PL022B与Fc受体FcγRI亲和力检测
Fc受体FcγRI(又名CD64)可与IgG抗体的Fc端结合,参与抗体依赖细胞介导的细胞毒作用(ADCC)。治疗性抗体与Fc受体结合的能力影响到该抗体的安全性和有效性。本实验使用Fortebio Octet分子相互作用仪检测BS-PL022B与FcγRI的亲和力常数,以评价抗体的ADCC活性。
Fortebio Octet分子相互作用仪检测相应抗体与FcγRI的亲和力常数实验方法简述如下:样品稀释缓冲液为PBS,0.02%Tween-20,0.1%BSA,pH7.4的溶液。HIS1K传感器上加入浓度为1μg/mL的FcγRI(购自Sinobio)溶液,固定时间50s,以使得FcγRI固定于传感器表面。抗体与FcγRI的结合和解离参数的测定均在缓冲液中进行,抗体浓度为3.12-50nM(两倍梯度稀释)。样品板震动速率为1000rpm,检测温度为30℃,频率为5.0Hz。数据以1:1模型拟合分析,得到亲和力常数。
FcγRI与BS-PL022B的亲和力常数测定结果如表12和图13-图14所示。
表12:BS-PL022B与FcγRI结合的动力学参数
N/A表示抗体与抗原没有结合或结合信号极低,没有对结果进行分析,故未能获得相应数据。
结果显示,H7L8(hG1WT)能够与FcγRI结合,亲和力常数为6.59E-09M,BS-PL022B由于与FcγRI没有结合或结合信号极低,没有对结果进行分析,故而未能获得相应数据。
结果表明,BS-PL022B与FcγRI的结合活性被有效地消除。
实验例9:BS-PL022B与Fc受体FcγRIIIa及其亚型的亲和力测定
(1)FcγRIIIa_V158与BS-PL022B的亲和力常数测定
Fc受体FcγRIIIa_V158(又名CD16a_V158),可与IgG抗体的Fc端结合,介导ADCC效应。实验中使用Fortebio Octet分子相互作用仪检测BS-PL022B与FcγRIIIa_V158的亲和力常数,以评价抗体的ADCC活性。
Fortebio Octet分子相互作用仪检测相应抗体亲和力常数实验方法简述如下:样品稀释缓冲液为PBS,0.02%Tween-20,0.1%BSA,pH7.4。5μg/mL的FcγRIIIa_V158固定在HIS1K传感器上,时间60s,传感器在缓冲液中平衡60s,固定在传感器上的FcγRIIIa_V158与各抗体结合,抗体浓度为31.25-500nM(两倍稀释),时间60s,抗体在缓冲液中解离,时间60s。样品板震动速率为1000rpm,检测温度为30℃,频率为5.0Hz。数据以1:1模型拟合分析,得到亲和力常数。
FcγRIIIa_V158与BS-PL022B的亲和力常数测定结果如表13和图15-图16所示。
表13:BS-PL022B与FcγRIIIa_V158结合的动力学参数
N/A表示抗体与抗原没有结合或结合信号极低,没有对结果进行分析,故未能获得相应数据。
结果显示,H7L8(hG1WT)能够与FcγRIIIa_V158结合,亲和力常数为8.77E-08M,BS-PL022B由于与FcγRIIIa_V158没有结合或结合信号极低,没有对结果进行分析。
结果表明,BS-PL022B与FcγR IIIa_V158的结合活性被有效地消除。
(2)FcγRIIIa_F158与BS-PL022B的亲和力常数测定
Fc受体FcγRIIIa_F158(又名CD16a_F158)可与IgG抗体的Fc端结合,介导ADCC。本实验使用Fortebio Octet分子相互作用仪检测BS-PL022B与FcγRIIIa_F158的亲和力常数,以评价各抗体的ADCC活性。
Fortebio Octet分子相互作用仪检测TF01与FcγRIIIa_F158的亲和力常数实验方法简述如下:样品稀释缓冲液为PBS,0.02%Tween-20,0.1%BSA,pH7.4。5μg/mL的FcγRIIIa_F158固定在HIS1K传感器上,时间120s,传感器在缓冲液中平衡60s,固定在传感器上的FcγRIIIa_F158与各抗体结合,抗体浓度为31.25-500nM(两倍稀释),时间60s,抗体在缓冲液中解离,时间60s。样品板震动速率为1000rpm,检测温度为30℃,频率为5.0Hz。数据以1:1模型拟合分析,得到亲和力常数。
FcγRIIIa_F158与BS-PL022B的亲和力常数测定结果如表14和图17-图18所示。
表14:TF01FcγRIIIa_F158结合的动力学参数
N/A表示抗体与抗原没有结合或结合信号极低,没有对结果进行分析,故未能获得相应数据。
结果显示,H7L8(hG1WT)能够与FcγRIIIa_F158结合,亲和力常数为3.64E-07M,BS-PL022B与FcγRIIIa_F158没有结合或结合信号极低,没有对结果进行分析,故而未能获得相应数据。
结果表明,BS-PL022B与FcγRIIIa_F158的结合活性被有效地消除。
实验例10:BS-PL022B与Fc受体FcγRIIa及其亚型的亲和力测定
(1)FcγRIIa_H131与BS-PL022B的亲和力常数测定
Fc受体FcγRIIa_H131(又名CD32a_H131)可与IgG抗体的Fc端结合,参与抗体依赖性细胞介导的细胞吞噬作用(ADCP)或者抗体依赖细胞介导的细胞毒作用(ADCC)。治疗性抗体与Fc受体结合的能力影响到该抗体的安全性和有效性。本实验使用Fortebio Octet分子相互作用仪检测BS-PL022B与FcγRIIa_H131的亲和力常数,以评价各待测抗体与Fc受体的结合能力。
Fortebio Octet分子相互作用仪检测BS-PL022B与FcγRIIa_H131的亲和力常数实验方法简述如下:样品稀释缓冲液为PBS,0.02%Tween-20,0.1%BSA,pH7.4。5μg/mL的FcγRIIa_H131固定在NTA传感器上,固定高度约为1.0nm,传感器在缓冲液中平衡60s,固定在传感器上的FcγRIIa_H131与各抗体结合,抗体浓度为12.5-200nM(两倍梯度稀释),时间60s,抗体在缓冲液中解离,时间60s。样品板震动速率为1000rpm,检测温度为30℃,频率为5.0Hz。数据以1:1模型拟合分析,得到亲和力常数。
FcγRIIa_H131与BS-PL022B的亲和力常数测定结果如表15和图19-图20所示。
表15:BS-PL022B与FcγRIIa_H131结合的动力学参数
| Sample ID | K<sub>D</sub>(M) | kon(1/Ms) | SE(kon) | kdis(1/s) | SE(kdis) | Rmax(nm) |
| BS-PL022B | N/A | N/A | N/A | N/A | N/A | N/A |
| H7L8(hG1WT) | 1.78E-07 | 4.19E+05 | 3.55E+04 | 7.44E-02 | 1.66E-03 | 1.14-1.46 |
N/A表示抗体与抗原没有结合或结合信号极低,没有对结果进行分析,故未能获得相应数据。
结果显示,H7L8(hG1WT)能够与FcγRIIa_H131结合,亲和力常数为1.78E-07M,BS-PL022B与FcγRIIa_H131没有结合或结合信号极低,没有对结果进行分析,故而未能获得相应数据。
结果表明,BS-PL022B与FcγRIIa_H131的结合活性被有效地消除。
实验例11:FcγRIIb与BS-PL022B的亲和力常数测定
Fc受体FcγRIIb(又名CD32b)可与IgG抗体的Fc端结合。本实验使用FortebioOctet分子相互作用仪检测各待测抗体与FcγRIIb的亲和力常数,以评价BS-PL022B与Fc受体的结合能力。
Fortebio Octet分子相互作用仪检测BS-PL022B与FcγRIIb的亲和力常数实验方法简述如下:样品稀释缓冲液为PBS,0.02%Tween-20,0.1%BSA,pH7.4。5μg/mL的FcγRIIb固定在NTA传感器上,固定高度约为1.0nm,传感器在缓冲液中平衡60s,固定在传感器上的hFCGR2B-his与各抗体结合,抗体浓度为12.5-200nM(两倍梯度稀释),时间60s,抗体在缓冲液中解离,时间60s。样品板震动速率为1000rpm,检测温度为30℃,频率为5.0Hz。数据以1:1模型拟合分析,得到亲和力常数。
FcγRIIb与BS-PL022B的亲和力常数测定结果如表17和图21-图22所示。
表16:BS-PL022B与FcγRIIb结合的动力学参数
N/A表示抗体与抗原没有结合或结合信号极低,没有对结果进行分析,故未能获得相应数据。
结果显示,H7L8(hG1WT)能够与FcγRIIb结合,亲和力常数为1.21E-07M,BS-PL022B由于与FcγRIIb没有结合或结合信号极低,没有对结果进行分析,故而未能获得相应数据。
结果表明,BS-PL022B与FcγRIIb的结合活性被有效地消除。
实验例12:BS-PL022B与C1q的亲和力测定
血清补体C1q可与IgG抗体的Fc端结合,介导CDC效应,治疗性抗体与C1q结合的能力影响到该抗体的安全性和有效性。本实验使用Fortebio Octet分子相互作用仪检测BS-PL022B与C1q的亲和力常数,以评价抗体的CDC活性。
Fortebio Octet分子相互作用仪检测相应抗体与C1q的亲和力常数实验方法简述如下:样品稀释缓冲液为PBS,0.02%Tween-20,0.1%BSA,pH7.4。50μg/mL的抗体固定在FAB2G传感器上,固定高度约为2.0nm,传感器在缓冲液中平衡60s,固定在传感器上的抗体与抗原C1q结合,抗原浓度为0.625-10nM(两倍梯度稀释),时间60s,抗原抗体在缓冲液中解离,时间60s。样品板震动速率为1000rpm,检测温度为30度,检测频率为5.0Hz。数据以1:1模型拟合分析,得到亲和力常数。数据采集软件为Fortebio Data Acquisition 7.0,数据分析软件为Fortebio Data Analysis 7.0。
BS-PL022B与C1q的亲和力常数测定结果如表18和图23-图24所示。
表17:BS-PL022B与C1q结合的动力学参数
N/A表示抗体与抗原没有结合或结合信号极低,没有对结果进行分析,故未能获得相应数据。
结果显示,H7L8(hG1WT)能够与C1q结合,亲和力常数为1.75E-09M,BS-PL022B由于与C1q没有结合或结合信号极低,没有对结果进行分析,故而未能获得相应数据。
结果表明,BS-PL022B与C1q的结合活性被有效地消除。
实验例13:BS-PL022B对CHO-K1-PD1-LAG3的抗体介导的细胞吞噬的活性
常规收集Jurkat-NFAT-CD64-CD32R(康方生物构建),CHO-K1-PD1-LAG3(康方生物构建)细胞,110xg离心5min,弃上清;用1640+4%FBS重悬后计数并测定细胞活率,调整细胞浓度;按实验设计用1640+4%FBS将抗体稀释至50nM、5nM、0.5nM(工作浓度为10nM、1nM、0.1nM或5nM、0.5nM、0.05nM),对照抗体稀释至50nM(工作浓度为10nM);按40μL/样本将Jurkat-NFAT-CD64-CD32R细胞悬液加至96孔黑板中(4万细胞/孔);按40μL/样本将靶细胞CHO-K1-PD1-LAG3细胞(4万细胞/孔)加至已含Jurkat-NFAT-CD64-CD32R的样本中;按20μL/孔将抗体加至相应样本,混匀;同时设置空白对照和同型性对照,置于培养箱孵育5h;按50μL/孔将Bright-GloTM Luciferase Assay System(Promega,货号:E2650)加至样本,混匀,读板。
结果如图25所示。
结果显示,同浓度时14C12H1L1(G1WT)+H7L8(hG1WT)、Nivolumab+Relatlimab具有ADCP效应;而BS-PL022B不具有ADCP效应。
实验例14:抗LAG3-抗PD-1双特异性抗体在小鼠肿瘤细胞皮下移植模型中的药效
学评价
为检测抗LAG3-抗PD-1双特异性抗体体内抑瘤活性,首先用CT26结肠癌细胞(购自江苏集萃药康生物科技股份有限公司),接种于7.1-7.3周龄的雌性BALB/c-hPD1/hLAG3小鼠(购自江苏集萃药康生物科技股份有限公司)小鼠右侧背部大腿上方皮下。分组当天定义为D0天。给药方式为腹腔注射(ip),每周给药2次(BIW),共给药6次。造模与具体给药方式见表18。给药后测量各组肿瘤的长宽,计算肿瘤体积。
表18:抗LAG3-抗PD-1双特异性抗体治疗BALB/c-hPD1/hLAG3小鼠CT26结肠癌细胞移植瘤模型的给药方案
注:同型对照15mg/kg、Relatlimab 15mg/kg与BS-PL022B 20mg/kg的剂量为等摩尔浓度;Relatlimab 3mg/kg与BS-PL022B 4mg/kg的剂量为等摩尔浓度。
结果如图26所示。结果显示,相比同型对照抗体,抗LAG3-抗PD-1双特异性抗体BS-PL022B以及阳性对照抗体Relatlimab均能有效地抑制小鼠肿瘤的生长。结果表明,抗LAG3-抗PD-1双特异性抗体BS-PL022B抑瘤效果显著优于阳性对照抗体Relatimab。
此外,如图27所示,荷瘤鼠对受试药BS-PL022B的耐受性均良好,各组对荷瘤小鼠体重无影响。
尽管本发明的具体实施方式已经得到详细的描述,本领域技术人员将会理解。根据已经公开的所有教导,可以对那些细节进行各种修改和替换,这些改变均在本发明的保护范围之内。本发明的全部范围由所附权利要求及其任何等同物给出。
Claims (34)
1.一种双特异性抗体,其包括第一蛋白功能区和第二蛋白功能区,其中:
所述第一蛋白功能区靶向LAG3,
所述第二蛋白功能区靶向不同于LAG3的靶点(例如,PD-1),
其中,所述第一蛋白功能区为抗LAG3抗体或其抗原结合片段,包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:5-7所示的HCDR1-HCDR3;并且所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:8-10所示的LCDR1-LCDR3。
2.根据权利要求1所述的双特异性抗体,其中,
所述抗LAG3抗体的重链可变区的氨基酸序列如SEQ ID NO:2所示,并且所述抗LAG3抗体的轻链可变区的氨基酸序列如SEQ ID NO:4所示。
3.根据权利要求1至2中任一权利要求所述的双特异性抗体,其中,所述抗LAG3抗体或其抗原结合片段选自Fab、Fab'、F(ab')2、Fd、Fv、dAb、互补决定区片段、单链抗体、人源化抗体、嵌合抗体或双抗体。
4.根据权利要求1至3中任一权利要求所述的双特异性抗体,其中,所述抗LAG3抗体以小于0.2nM,例如小于0.15nM、小于0.1nM、小于0.08nM、0.06nM或小于0.05nM或更小的EC50结合人LAG3-mFc;优选地,所述EC50通过间接ELISA方法测得。
5.根据权利要求1至4中任一权利要求所述的双特异性抗体,其中,
所述抗LAG3抗体包括非-CDR区,且所述非-CDR区来自不是鼠类的物种,例如来自人抗体。
6.根据权利要求1至5中任一权利要求所述的双特异性抗体,其中,
所述抗LAG3抗体,其恒定区来自人抗体;
优选地,所述抗体的恒定区选自人IgG1、IgG2、IgG3或IgG4的恒定区。
7.根据权利要求1至6中任一权利要求所述的双特异性抗体,其中,
所述抗LAG3抗体的重链恒定区为Ig gamma-1chain C region(例如,如SEQ ID NO:39所示)或Ig gamma-4chain C region(例如,如SEQ ID NO:45所示);轻链恒定区为Ig kappachain C region(例如,如SEQ ID NO:40所示)。
8.根据权利要求1至7中任一权利要求所述的双特异性抗体,其中,
所述抗LAG3抗体为人IgG1亚型,
其中,按照EU编号系统,所述抗体的重链恒定区具有如下突变:
L234A和L235A,
L234A和G237A,
L235A和G237A,
或者
L234A、L235A和G237A;
优选地,所述抗LAG3抗体的重链的氨基酸序列如SEQ ID NO:11所示,并且轻链的氨基酸序列如SEQ ID NO:12所示。
9.根据权利要求1至8中任一权利要求所述的双特异性抗体,其中,
所述抗LAG3抗体为人IgG4亚型,
其中,按照EU编号系统,所述抗体的重链恒定区具有如下突变:
F234A和L235A,
F234A和G237A,
L235A和G237A,
或者
F234A、L235A和G237A;
优选地,所述抗LAG3抗体的重链的氨基酸序列如SEQ ID NO:13所示,并且轻链的氨基酸序列如SEQ ID NO:12所示。
10.根据权利要求1至9中任一权利要求所述的双特异性抗体,其中,所述双特异性抗体为IgG-scFv模式。
11.根据权利要求1至10中任一权利要求所述的双特异性抗体,其中,
所述第一蛋白功能区为抗LAG3抗体的抗体,并且所述第二蛋白功能区为单链抗体;或者
所述第一蛋白功能区为单链抗体,并且所述第二蛋白功能区为靶向不同于LAG3的靶点的抗体。
12.根据权利要求1至11中任一权利要求所述的双特异性抗体,其中,所述第一蛋白功能区和第二蛋白功能区直接连接或者通过连接片段连接;
优选地,所述连接片段为(GGGGS)m,m为正整数,例如1、2、3、4、5或6;
优选地,所述连接片段为(GGGGS)nG,n为正整数,例如1、2、3、4、5或6。
13.根据权利要求1至12中任一权利要求所述的双特异性抗体,其中,所述第一蛋白功能区和第二蛋白功能区独立地为1个、2个或者2个以上。
14.根据权利要求1至13中任一权利要求所述的双特异性抗体,其中,所述单链抗体连接在抗体的重链的C末端。
15.根据权利要求1至14中任一权利要求所述的双特异性抗体,其包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
其中,
所述第一蛋白功能区为抗LAG3抗体,并且所述抗LAG3抗体为免疫球蛋白形式,
所述第二蛋白功能区为抗PD-1的单链抗体。
16.根据权利要求15所述的双特异性抗体,其中,所述抗PD-1的单链抗体包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:26-28所示的HCDR1-HCDR3;和
所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:29-31所示的LCDR1-LCDR3。
17.根据权利要求15至16中任一权利要求所述的双特异性抗体,其中,所述抗PD-1的单链抗体,
其重链可变区的氨基酸序列如SEQ ID NO:15所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:17所示;或者
其重链可变区的氨基酸序列如SEQ ID NO:19所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:21或SEQ ID NO:38所示。
18.根据权利要求15至17任一权利要求所述的双特异性抗体,其中,所述抗PD-1的单链抗体中的重链可变区和轻链可变区直接连接或者通过连接片段连接;
优选地,所述连接片段为(GGGGS)m,m为正整数,例如1、2、3、4、5或6;
优选地,所述连接片段为(GGGGS)nG,n为正整数,例如1、2、3、4、5或6。
19.根据权利要求15至18中任一权利要求所述的双特异性抗体,其中,
所述双特异性抗体包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
所述第一蛋白功能区为1个,所述第二蛋白功能区为2个;
其中,所述第一蛋白功能区为免疫球蛋白,所述第二蛋白功能区为单链抗体;
所述免疫球蛋白的重链的氨基酸序列如SEQ ID NO:11或SEQ ID NO:13所示,并且其轻链的氨基酸序列如SEQ ID NO:12所示;
所述单链抗体的重链可变区的氨基酸序列如SEQ ID NO:19所示,并且所述单链抗体的轻链可变区的氨基酸序列如SEQ ID NO:21或SEQ ID NO:38所示;
所述单链抗体连接在免疫球蛋白的两条重链的C末端;
所述第一蛋白功能区与所述第二蛋白功能区通过第一连接片段连接;并且所述单链抗体的重链可变区与所述单链抗体的轻链可变区通过第二连接片段连接;所述第一连接片段和所述第二连接片段相同或不同;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列独立地选自SEQ IDNOs:35-37;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列均如SEQ ID NO:36所示。
20.根据权利要求1至14中任一权利要求所述的双特异性抗体,其包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
其中,所述第一蛋白功能区为抗LAG3的单链抗体,所述第二蛋白功能区为抗PD-1的抗体,并且所述抗PD-1的抗体为免疫球蛋白形式;
其中,所述抗LAG3的单链抗体包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:5-7所示的HCDR1-HCDR3;和
所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:8-10所示的LCDR1-LCDR3。
21.根据权利要求20所述的双特异性抗体,其中,所述抗LAG3的单链抗体,
其重链可变区的氨基酸序列如SEQ ID NO:2所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:4所示。
22.根据权利要求20至21中任一权利要求所述的双特异性抗体,其中,所述抗LAG3的单链抗体中的重链可变区和轻链可变区直接连接或者通过连接片段连接;
优选地,所述连接片段为(GGGGS)m,m为正整数,例如1、2、3、4、5或6;
优选地,所述连接片段为(GGGGS)nG,n为正整数,例如1、2、3、4、5或6。
23.根据权利要求20至22中任一权利要求所述的双特异性抗体,其中,所述抗PD-1的抗体包含重链可变区和轻链可变区,其中,
所述重链可变区包含:氨基酸序列分别如SEQ ID NOs:26-28所示的HCDR1-HCDR3;和
所述轻链可变区包含:氨基酸序列分别如SEQ ID NOs:29-31所示的LCDR1-LCDR3。
24.根据权利要求20至23中任一权利要求所述的双特异性抗体,其中,所述抗PD-1的抗体,
其重链可变区的氨基酸序列如SEQ ID NO:15所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:17所示;或者
其重链可变区的氨基酸序列如SEQ ID NO:19所示,并且其轻链可变区的氨基酸序列如SEQ ID NO:21或SEQ ID NO:38所示。
25.根据权利要求22至26中任一权利要求所述的双特异性抗体,其中,所述抗PD-1的抗体,其重链恒定区为Ig gamma-1chain C region(例如,如SEQ ID:39所示)或Ig gamma-4chain C region(例如,如SEQ ID NO:45所示);轻链恒定区为Ig kappa chain C region(例如,如SEQ ID:40所示)。
26.根据权利要求20至25中任一权利要求所述的双特异性抗体,其中,
所述抗PD-1的抗体为人IgG1亚型,
其中,按照EU编号系统,所述抗PD-1的抗体具有如下突变:
L234A和L235A,
L234A和G237A,
L235A和G237A,
或者
L234A、L235A和G237A;
优选地,所述抗PD-1的抗体的重链的氨基酸序列如SEQ ID NO:34所示,并且轻链的氨基酸序列如SEQ ID NO:25所示。
27.根据权利要求20至25中任一权利要求所述的双特异性抗体,其中,
所述抗PD-1的抗体为人IgG4亚型,
其中,按照EU编号系统,所述抗PD-1的抗体具有如下突变:
F234A和L235A,
F234A和G237A,
L235A和G237A,
或者
F234A、L235A和G237A;
优选地,所述抗PD-1的抗体的重链的氨基酸序列如SEQ ID NO:32所示,并且轻链的氨基酸序列如SEQ ID NO:25所示。
28.根据权利要求20至27中任一权利要求所述的双特异性抗体,其中,
所述双特异性抗体包括:
靶向LAG3的第一蛋白功能区,和
靶向PD-1的第二蛋白功能区;
所述第一蛋白功能区为1个,所述第二蛋白功能区为2个;
其中,所述第一蛋白功能区为单链抗体,所述第二蛋白功能区为免疫球蛋白;
所述单链抗体的重链可变区的氨基酸序列如SEQ ID NO:2所示,并且所述单链抗体的轻链可变区的氨基酸序列如SEQ ID NO:4所示;
所述免疫球蛋白的重链的氨基酸序列如SEQ ID NO:34或SEQ ID NO:32所示,并且其轻链的氨基酸序列如SEQ ID NO:25所示;
所述单链抗体连接在免疫球蛋白的两条重链的C末端;
所述第一蛋白功能区与所述第二蛋白功能区通过第一连接片段连接;并且所述单链抗体的重链可变区与所述单链抗体的轻链可变区通过第二连接片段连接;所述第一连接片段和所述第二连接片段相同或不同;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列独立地选自SEQ IDNOs:35-37;
优选地,所述第一连接片段和所述第二连接片段的氨基酸序列均如SEQ ID NOs:36所示。
29.分离的核酸分子,其编码权利要求1至28中任一权利要求所述的双特异性抗体。
30.一种重组载体,其包含权利要求29所述的分离的核酸分子。
31.一种宿主细胞,其包含权利要求29所述的分离的核酸分子,或者包含权利要求30所述的重组载体。
32.制备权利要求13至30中任一权利要求所述的双特异性抗体的方法,其包括在合适的条件下培养权利要求31的宿主细胞,以及从细胞培养物中回收双特异性抗体的步骤。
33.一种药物组合物,其包含权利要求1至28中任一权利要求所述的双特异性抗体;可选地,其还包括药学上可接受的辅料。
34.权利要求1至28中任一权利要求所述的双特异性抗体在制备治疗和/或预防肿瘤或贫血病的药物中的用途;
优选地,所述肿瘤为选自卵巢癌、食管癌、黑色素瘤、血液瘤、神经胶质母细胞瘤、肾细胞癌、肺癌、前列腺癌、膀胱癌、结肠癌、直肠癌、肝癌、胃肠道癌、乳腺癌、脑癌、胰腺癌、甲状腺癌、头颈癌和肾癌中的一种或多种;
优选地,所述肺癌为非小细胞肺癌;
优选地,所述血液瘤为白血病;
优选地,所述食管癌为食管鳞癌。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202111149114 | 2021-09-29 | ||
| CN2021111491149 | 2021-09-29 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN115873123A true CN115873123A (zh) | 2023-03-31 |
Family
ID=85770153
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202211192782.4A Pending CN115873116A (zh) | 2021-09-29 | 2022-09-28 | 抗lag3抗体、药物组合物及用途 |
| CN202211199026.4A Pending CN115873123A (zh) | 2021-09-29 | 2022-09-29 | 抗lag3双特异性抗体、药物组合物及用途 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202211192782.4A Pending CN115873116A (zh) | 2021-09-29 | 2022-09-28 | 抗lag3抗体、药物组合物及用途 |
Country Status (5)
| Country | Link |
|---|---|
| CN (2) | CN115873116A (zh) |
| AU (2) | AU2022355381A1 (zh) |
| CA (2) | CA3233205A1 (zh) |
| IL (2) | IL311738A (zh) |
| WO (2) | WO2023051621A1 (zh) |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| AR091649A1 (es) * | 2012-07-02 | 2015-02-18 | Bristol Myers Squibb Co | Optimizacion de anticuerpos que se fijan al gen de activacion de linfocitos 3 (lag-3) y sus usos |
| HUE062317T2 (hu) * | 2013-09-20 | 2023-10-28 | Bristol Myers Squibb Co | Anti-LAG-3 antitestek és anti-PD-1 antitestek kombinációja tumorok kezeléséhez |
| EP3988572A1 (en) | 2014-01-28 | 2022-04-27 | Bristol-Myers Squibb Company | Anti-lag-3 antibodies to treat hematological malignancies |
| JO3663B1 (ar) * | 2014-08-19 | 2020-08-27 | Merck Sharp & Dohme | الأجسام المضادة لمضاد lag3 وأجزاء ربط الأنتيجين |
| CN106632674B (zh) | 2015-10-30 | 2018-11-16 | 泽达生物医药有限公司 | 一种抗pd-1单克隆抗体、其药物组合物及其用途 |
| JP7000322B2 (ja) * | 2015-12-16 | 2022-02-04 | メルク・シャープ・アンド・ドーム・コーポレーション | 抗lag3抗体および抗原結合性フラグメント |
| CN106977602B (zh) | 2016-08-23 | 2018-09-25 | 中山康方生物医药有限公司 | 一种抗pd1单克隆抗体、其药物组合物及其用途 |
| CN106967172B (zh) | 2016-08-23 | 2019-01-08 | 康方药业有限公司 | 抗ctla4-抗pd-1 双功能抗体、其药物组合物及其用途 |
| CN110615840A (zh) * | 2018-06-19 | 2019-12-27 | 信达生物制药(苏州)有限公司 | 全人源的抗lag-3抗体及其应用 |
| CN113248618B (zh) * | 2018-08-21 | 2022-03-18 | 天境生物科技(杭州)有限公司 | 抗pd-l1/抗lag3双特异性抗体及其用途 |
| CN115340606B (zh) * | 2019-05-31 | 2023-12-19 | 瑞阳(苏州)生物科技有限公司 | 与人lag-3蛋白结合的抗体及其编码基因和应用 |
| JP2022550243A (ja) * | 2019-09-30 | 2022-12-01 | シチュアン ケルン-バイオテック バイオファーマシューティカル カンパニー リミテッド | 抗pd-1抗体及びその使用 |
| CN113348182B (zh) * | 2019-12-30 | 2022-07-12 | 上海海路生物技术有限公司 | Lag-3抗体及其医药用途 |
| WO2022188867A1 (zh) * | 2021-03-12 | 2022-09-15 | 中山康方生物医药有限公司 | 提高含有免疫球蛋白Fc片段的药物的安全性的方法 |
-
2022
- 2022-09-28 CN CN202211192782.4A patent/CN115873116A/zh active Pending
- 2022-09-28 IL IL311738A patent/IL311738A/en unknown
- 2022-09-28 CA CA3233205A patent/CA3233205A1/en active Pending
- 2022-09-28 WO PCT/CN2022/122185 patent/WO2023051621A1/zh active Application Filing
- 2022-09-28 AU AU2022355381A patent/AU2022355381A1/en active Pending
- 2022-09-29 CN CN202211199026.4A patent/CN115873123A/zh active Pending
- 2022-09-29 CA CA3233192A patent/CA3233192A1/en active Pending
- 2022-09-29 WO PCT/CN2022/122556 patent/WO2023051683A1/zh active Application Filing
- 2022-09-29 AU AU2022355986A patent/AU2022355986A1/en active Pending
- 2022-09-29 IL IL311692A patent/IL311692A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| AU2022355381A1 (en) | 2024-05-02 |
| IL311738A (en) | 2024-05-01 |
| WO2023051621A1 (zh) | 2023-04-06 |
| AU2022355986A1 (en) | 2024-04-18 |
| CN115873116A (zh) | 2023-03-31 |
| CA3233205A1 (en) | 2023-04-06 |
| CA3233192A1 (en) | 2023-04-06 |
| IL311692A (en) | 2024-05-01 |
| WO2023051683A1 (zh) | 2023-04-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102469286B1 (ko) | 항-pd1 단일클론 항체, 이의 약제학적 조성물 및 이의 용도 | |
| US20230340097A1 (en) | Anti-pd-1/vegfa bifunctional antibody, pharmaceutical composition thereof and use thereof | |
| JP6432121B2 (ja) | Pdl−1抗体、その医薬組成物及びその使用 | |
| EP3992209A1 (en) | Cldn18.2 antibody and use thereof | |
| TWI805121B (zh) | 抗SIRPα抗體及其用途 | |
| JP2023527583A (ja) | Lag3に結合する抗体およびその使用 | |
| EP4273170A1 (en) | Pharmaceutical composition comprising anti-tigit antibody and anti-pd-1-anti-vegfa bispecific antibody, and use | |
| CN114478769B (zh) | 抗tigit抗体、其药物组合物及用途 | |
| CN115873123A (zh) | 抗lag3双特异性抗体、药物组合物及用途 | |
| WO2023241629A1 (zh) | 抗cldn18.2抗体、其药物组合物及用途 | |
| EA042365B1 (ru) | Бифункциональное антитело против ctla4 и против pd-1, его фармацевтическая композиция и их применение |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| TA01 | Transfer of patent application right | ||
| TA01 | Transfer of patent application right |
Effective date of registration: 20231010 Address after: 200137 Floor 3, No. 665, Zhangjiang Road, China (Shanghai) Pilot Free Trade Zone, Pudong New Area, Shanghai Applicant after: Kangfang Huike (Shanghai) Biology Co.,Ltd. Address before: 528437 No. 6 Shennong Road, Torch Development Zone, Zhongshan, Guangdong Applicant before: AKESO BIOPHARMA, Inc. |