CN113728477A - 氧化还原液流电池用负极电解液及氧化还原液流电池 - Google Patents
氧化还原液流电池用负极电解液及氧化还原液流电池 Download PDFInfo
- Publication number
- CN113728477A CN113728477A CN202080027269.2A CN202080027269A CN113728477A CN 113728477 A CN113728477 A CN 113728477A CN 202080027269 A CN202080027269 A CN 202080027269A CN 113728477 A CN113728477 A CN 113728477A
- Authority
- CN
- China
- Prior art keywords
- negative electrode
- electrolyte
- redox flow
- flow battery
- solvent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000003792 electrolyte Substances 0.000 title claims abstract description 182
- 239000002904 solvent Substances 0.000 claims abstract description 93
- 239000003115 supporting electrolyte Substances 0.000 claims abstract description 50
- 239000007773 negative electrode material Substances 0.000 claims abstract description 36
- 238000005192 partition Methods 0.000 claims abstract description 9
- HGASFNYMVGEKTF-UHFFFAOYSA-N octan-1-ol;hydrate Chemical group O.CCCCCCCCO HGASFNYMVGEKTF-UHFFFAOYSA-N 0.000 claims abstract description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 29
- 239000007774 positive electrode material Substances 0.000 claims description 25
- -1 fluoromethanesulfonyl Chemical group 0.000 claims description 24
- 150000001450 anions Chemical class 0.000 claims description 13
- 150000003949 imides Chemical class 0.000 claims description 12
- CRWNQZTZTZWPOF-UHFFFAOYSA-N 2-methyl-4-phenylpyridine Chemical compound C1=NC(C)=CC(C=2C=CC=CC=2)=C1 CRWNQZTZTZWPOF-UHFFFAOYSA-N 0.000 claims description 8
- SKTCDJAMAYNROS-UHFFFAOYSA-N methoxycyclopentane Chemical compound COC1CCCC1 SKTCDJAMAYNROS-UHFFFAOYSA-N 0.000 claims description 8
- KZEXVNKGDKTRPC-UHFFFAOYSA-N triethyl(2-methoxyethyl)phosphanium Chemical compound CC[P+](CC)(CC)CCOC KZEXVNKGDKTRPC-UHFFFAOYSA-N 0.000 claims description 8
- 125000001033 ether group Chemical group 0.000 claims description 7
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 claims description 7
- REVVFBIOIFGJRH-JTQLQIEISA-N 4-[[(2s)-1-hydroxybutan-2-yl]amino]benzaldehyde Chemical compound CC[C@@H](CO)NC1=CC=C(C=O)C=C1 REVVFBIOIFGJRH-JTQLQIEISA-N 0.000 claims description 6
- DKNRELLLVOYIIB-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;1-methyl-1-propylpyrrolidin-1-ium Chemical compound CCC[N+]1(C)CCCC1.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F DKNRELLLVOYIIB-UHFFFAOYSA-N 0.000 claims description 6
- ZXMGHDIOOHOAAE-UHFFFAOYSA-N 1,1,1-trifluoro-n-(trifluoromethylsulfonyl)methanesulfonamide Chemical compound FC(F)(F)S(=O)(=O)NS(=O)(=O)C(F)(F)F ZXMGHDIOOHOAAE-UHFFFAOYSA-N 0.000 claims description 4
- 229910014351 N(SO2F)2 Inorganic materials 0.000 claims description 4
- YQFWGCSKGJMGHE-UHFFFAOYSA-N 1-methyl-1-propylpyrrolidin-1-ium Chemical compound CCC[N+]1(C)CCCC1 YQFWGCSKGJMGHE-UHFFFAOYSA-N 0.000 claims description 3
- 239000008151 electrolyte solution Substances 0.000 description 33
- 239000000126 substance Substances 0.000 description 21
- 238000000034 method Methods 0.000 description 15
- 230000002209 hydrophobic effect Effects 0.000 description 14
- 150000002500 ions Chemical class 0.000 description 14
- 238000002360 preparation method Methods 0.000 description 14
- 238000005868 electrolysis reaction Methods 0.000 description 13
- 238000003756 stirring Methods 0.000 description 12
- 230000000052 comparative effect Effects 0.000 description 11
- 238000010248 power generation Methods 0.000 description 11
- 239000011149 active material Substances 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- 238000007600 charging Methods 0.000 description 9
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 8
- 150000001768 cations Chemical class 0.000 description 8
- 229910003473 lithium bis(trifluoromethanesulfonyl)imide Inorganic materials 0.000 description 8
- QSZMZKBZAYQGRS-UHFFFAOYSA-N lithium;bis(trifluoromethylsulfonyl)azanide Chemical compound [Li+].FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F QSZMZKBZAYQGRS-UHFFFAOYSA-N 0.000 description 8
- IAEGWXHKWJGQAZ-UHFFFAOYSA-N trimethylpyrazine Chemical compound CC1=CN=C(C)C(C)=N1 IAEGWXHKWJGQAZ-UHFFFAOYSA-N 0.000 description 8
- 239000002608 ionic liquid Substances 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 239000011259 mixed solution Substances 0.000 description 7
- KBPLFHHGFOOTCA-UHFFFAOYSA-N 1-Octanol Chemical compound CCCCCCCCO KBPLFHHGFOOTCA-UHFFFAOYSA-N 0.000 description 6
- ALHUXMDEZNLFTA-UHFFFAOYSA-N 2-methylquinoxaline Chemical compound C1=CC=CC2=NC(C)=CN=C21 ALHUXMDEZNLFTA-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 229910052782 aluminium Inorganic materials 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 239000012454 non-polar solvent Substances 0.000 description 5
- 238000012546 transfer Methods 0.000 description 5
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 238000007599 discharging Methods 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- ACFSQHQYDZIPRL-UHFFFAOYSA-N lithium;bis(1,1,2,2,2-pentafluoroethylsulfonyl)azanide Chemical compound [Li+].FC(F)(F)C(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)C(F)(F)F ACFSQHQYDZIPRL-UHFFFAOYSA-N 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 3
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 3
- 239000004698 Polyethylene Substances 0.000 description 3
- 238000000354 decomposition reaction Methods 0.000 description 3
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 238000004146 energy storage Methods 0.000 description 3
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 3
- 239000010439 graphite Substances 0.000 description 3
- 229910002804 graphite Inorganic materials 0.000 description 3
- 229910052744 lithium Inorganic materials 0.000 description 3
- 229910001416 lithium ion Inorganic materials 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 229920000573 polyethylene Polymers 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- AZQWKYJCGOJGHM-UHFFFAOYSA-N 1,4-benzoquinone Chemical compound O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 2
- XUAXVBUVQVRIIQ-UHFFFAOYSA-N 1-butyl-2,3-dimethylimidazol-3-ium Chemical compound CCCCN1C=C[N+](C)=C1C XUAXVBUVQVRIIQ-UHFFFAOYSA-N 0.000 description 2
- MBCYYLURSZYHFZ-UHFFFAOYSA-N 1-methyl-1-propylimidazol-1-ium Chemical compound CCC[N+]1(C)C=CN=C1 MBCYYLURSZYHFZ-UHFFFAOYSA-N 0.000 description 2
- QPUYECUOLPXSFR-UHFFFAOYSA-N 1-methylnaphthalene Chemical compound C1=CC=C2C(C)=CC=CC2=C1 QPUYECUOLPXSFR-UHFFFAOYSA-N 0.000 description 2
- RKMGAJGJIURJSJ-UHFFFAOYSA-N 2,2,6,6-tetramethylpiperidine Chemical compound CC1(C)CCCC(C)(C)N1 RKMGAJGJIURJSJ-UHFFFAOYSA-N 0.000 description 2
- OXQOBQJCDNLAPO-UHFFFAOYSA-N 2,3-Dimethylpyrazine Chemical compound CC1=NC=CN=C1C OXQOBQJCDNLAPO-UHFFFAOYSA-N 0.000 description 2
- LCZUOKDVTBMCMX-UHFFFAOYSA-N 2,5-Dimethylpyrazine Chemical compound CC1=CN=C(C)C=N1 LCZUOKDVTBMCMX-UHFFFAOYSA-N 0.000 description 2
- QIMMUPPBPVKWKM-UHFFFAOYSA-N 2-methylnaphthalene Chemical compound C1=CC=CC2=CC(C)=CC=C21 QIMMUPPBPVKWKM-UHFFFAOYSA-N 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- 229920002943 EPDM rubber Polymers 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 229920000557 Nafion® Polymers 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- DJLLTFRHLPVCEL-UHFFFAOYSA-N Propylpyrazine Chemical compound CCCC1=CN=CC=N1 DJLLTFRHLPVCEL-UHFFFAOYSA-N 0.000 description 2
- FINHMKGKINIASC-UHFFFAOYSA-N Tetramethylpyrazine Chemical compound CC1=NC(C)=C(C)N=C1C FINHMKGKINIASC-UHFFFAOYSA-N 0.000 description 2
- 239000006183 anode active material Substances 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000006258 conductive agent Substances 0.000 description 2
- 238000004090 dissolution Methods 0.000 description 2
- KVFIJIWMDBAGDP-UHFFFAOYSA-N ethylpyrazine Chemical compound CCC1=CN=CC=N1 KVFIJIWMDBAGDP-UHFFFAOYSA-N 0.000 description 2
- VDVLPSWVDYJFRW-UHFFFAOYSA-N lithium;bis(fluorosulfonyl)azanide Chemical compound [Li+].FS(=O)(=O)[N-]S(F)(=O)=O VDVLPSWVDYJFRW-UHFFFAOYSA-N 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- CAWHJQAVHZEVTJ-UHFFFAOYSA-N methylpyrazine Chemical compound CC1=CN=CC=N1 CAWHJQAVHZEVTJ-UHFFFAOYSA-N 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 229920001296 polysiloxane Polymers 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000007784 solid electrolyte Substances 0.000 description 2
- HUXKTWJQSHBZIV-UHFFFAOYSA-N 1-ethyl-3-phenylbenzene Chemical group CCC1=CC=CC(C=2C=CC=CC=2)=C1 HUXKTWJQSHBZIV-UHFFFAOYSA-N 0.000 description 1
- LKDZKBGYSBBZEQ-UHFFFAOYSA-N 1-tert-butyl-2h-pyrazine Chemical compound CC(C)(C)N1CC=NC=C1 LKDZKBGYSBBZEQ-UHFFFAOYSA-N 0.000 description 1
- FXQMGPWUMNMGHH-UHFFFAOYSA-N 2,5-difluoropyrazine Chemical compound FC1=CN=C(F)C=N1 FXQMGPWUMNMGHH-UHFFFAOYSA-N 0.000 description 1
- 239000001934 2,5-dimethylpyrazine Substances 0.000 description 1
- UWKQJZCTQGMHKD-UHFFFAOYSA-N 2,6-di-tert-butylpyridine Chemical compound CC(C)(C)C1=CC=CC(C(C)(C)C)=N1 UWKQJZCTQGMHKD-UHFFFAOYSA-N 0.000 description 1
- 239000001154 2-(methoxymethyl)pyrazine Substances 0.000 description 1
- VKJIAEQRKBQLLA-UHFFFAOYSA-N 2-Methoxy-3-methylpyrazine Chemical compound COC1=NC=CN=C1C VKJIAEQRKBQLLA-UHFFFAOYSA-N 0.000 description 1
- GELVZYOEQVJIRR-UHFFFAOYSA-N 2-chloropyrazine Chemical compound ClC1=CN=CC=N1 GELVZYOEQVJIRR-UHFFFAOYSA-N 0.000 description 1
- ATIUKJHILQVQLE-UHFFFAOYSA-N 2-ethoxypyrazine Chemical compound CCOC1=CN=CC=N1 ATIUKJHILQVQLE-UHFFFAOYSA-N 0.000 description 1
- LJSMYNRELBSLKT-UHFFFAOYSA-N 2-methyl-3-propylquinoxaline Chemical compound C1=CC=C2N=C(C)C(CCC)=NC2=C1 LJSMYNRELBSLKT-UHFFFAOYSA-N 0.000 description 1
- SFXHWRCRQNGVLJ-UHFFFAOYSA-N 4-methoxy-TEMPO Chemical group COC1CC(C)(C)N([O])C(C)(C)C1 SFXHWRCRQNGVLJ-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 229910001290 LiPF6 Inorganic materials 0.000 description 1
- JLVVSXFLKOJNIY-UHFFFAOYSA-N Magnesium ion Chemical compound [Mg+2] JLVVSXFLKOJNIY-UHFFFAOYSA-N 0.000 description 1
- WKSXRWSOSLGSTN-UHFFFAOYSA-N Methoxypyrazine Chemical compound COC1=CN=CC=N1 WKSXRWSOSLGSTN-UHFFFAOYSA-N 0.000 description 1
- 229910014347 N(SO2F) Inorganic materials 0.000 description 1
- NPYPAHLBTDXSSS-UHFFFAOYSA-N Potassium ion Chemical compound [K+] NPYPAHLBTDXSSS-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- FKNQFGJONOIPTF-UHFFFAOYSA-N Sodium cation Chemical compound [Na+] FKNQFGJONOIPTF-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 239000003011 anion exchange membrane Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- RXKLBLXXQQRGJH-UHFFFAOYSA-N bis(fluorosulfonyl)azanide 1-methyl-1-propylpyrrolidin-1-ium Chemical compound CCC[N+]1(C)CCCC1.FS(=O)(=O)[N-]S(F)(=O)=O RXKLBLXXQQRGJH-UHFFFAOYSA-N 0.000 description 1
- LRESCJAINPKJTO-UHFFFAOYSA-N bis(trifluoromethylsulfonyl)azanide;1-ethyl-3-methylimidazol-3-ium Chemical compound CCN1C=C[N+](C)=C1.FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F LRESCJAINPKJTO-UHFFFAOYSA-N 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229910001424 calcium ion Inorganic materials 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 238000005341 cation exchange Methods 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 238000010277 constant-current charging Methods 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 239000011889 copper foil Substances 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 229910001882 dioxygen Inorganic materials 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 230000005611 electricity Effects 0.000 description 1
- 238000003487 electrochemical reaction Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 239000002360 explosive Substances 0.000 description 1
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 229910021385 hard carbon Inorganic materials 0.000 description 1
- 238000009434 installation Methods 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- DEUISMFZZMAAOJ-UHFFFAOYSA-N lithium dihydrogen borate oxalic acid Chemical compound B([O-])(O)O.C(C(=O)O)(=O)O.C(C(=O)O)(=O)O.[Li+] DEUISMFZZMAAOJ-UHFFFAOYSA-N 0.000 description 1
- GELKBWJHTRAYNV-UHFFFAOYSA-K lithium iron phosphate Chemical compound [Li+].[Fe+2].[O-]P([O-])([O-])=O GELKBWJHTRAYNV-UHFFFAOYSA-K 0.000 description 1
- 229910001425 magnesium ion Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000012982 microporous membrane Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 229910000476 molybdenum oxide Inorganic materials 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 230000033116 oxidation-reduction process Effects 0.000 description 1
- PQQKPALAQIIWST-UHFFFAOYSA-N oxomolybdenum Chemical compound [Mo]=O PQQKPALAQIIWST-UHFFFAOYSA-N 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 229910001414 potassium ion Inorganic materials 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 229910052814 silicon oxide Inorganic materials 0.000 description 1
- VCCATSJUUVERFU-UHFFFAOYSA-N sodium bis(fluorosulfonyl)azanide Chemical compound FS(=O)(=O)N([Na])S(F)(=O)=O VCCATSJUUVERFU-UHFFFAOYSA-N 0.000 description 1
- FJPWIJZUVYYHQE-UHFFFAOYSA-N sodium dihydrogen borate oxalic acid Chemical compound B([O-])(O)O.C(C(=O)O)(=O)O.C(C(=O)O)(=O)O.[Na+] FJPWIJZUVYYHQE-UHFFFAOYSA-N 0.000 description 1
- 229910001415 sodium ion Inorganic materials 0.000 description 1
- YLKTWKVVQDCJFL-UHFFFAOYSA-N sodium;bis(trifluoromethylsulfonyl)azanide Chemical compound [Na+].FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F YLKTWKVVQDCJFL-UHFFFAOYSA-N 0.000 description 1
- 229910021384 soft carbon Inorganic materials 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 229910000314 transition metal oxide Inorganic materials 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- LEONUFNNVUYDNQ-UHFFFAOYSA-N vanadium atom Chemical compound [V] LEONUFNNVUYDNQ-UHFFFAOYSA-N 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/08—Fuel cells with aqueous electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/18—Regenerative fuel cells, e.g. redox flow batteries or secondary fuel cells
- H01M8/184—Regeneration by electrochemical means
- H01M8/188—Regeneration by electrochemical means by recharging of redox couples containing fluids; Redox flow type batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0002—Aqueous electrolytes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Sustainable Development (AREA)
- Sustainable Energy (AREA)
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Fuel Cell (AREA)
Abstract
[技术问题]本发明提供一种氧化还原液流电池用负极电解液,在用于氧化还原液流电池时在高电压下能够具有高能量密度。[技术手段]本发明所述的氧化还原液流电池用负极电解液具有负极活性物质、负极支持电解质和负极溶剂;所述负极溶剂为以LogP表示的水‑辛醇分配系数LogPOW在1.5以上的溶剂。
Description
技术领域
本发明涉及氧化还原液流电池用负极电解液以及氧化还原液流电池。
背景技术
近年来,随着环境问题越来越严重,风力发电和太阳能发电等以自然能量进行发电的设备以全球规模急速普及。由自然能量而来的发电具有发电量不稳定、难以应电力需求进行供给、容易发生输出变动而且对系统线路影响大等问题。作为其对策技术之一,设置大容量的蓄电池,谋求输出变动的平滑化、剩余电力的储存、负载均衡化等受到瞩目。
作为这种大容量的能量储存用蓄电池,已知有氧化还原液流电池。氧化还原液流电池由于不使用燃烧性或爆炸性的物质,因此稳定性优异,即使重复充放电也能确保长寿命,具有耐久性高、成本低、维修频率也低这样的优点。此外,由于活性物质可储存于外部槽,因此具有容易大型化和大容量化这样的优点。
氧化还原液流电池由于将能量储存于液体中,例如通过补充、填充、更换预先完成充电的液体即可完成补充电动车能量的过程,相较于目前的锂离子电池电动车的充电时间,可大幅缩短充电所需的时间。
作为氧化还原液流电池,例如公开了一种氧化还原液流电池,所述氧化还原液流电池具有正的半电池、负的半电池、将2个半电池分离的隔膜(セパレーター)、2个电极以及位于电池外侧的2个电解质容器,其中正的半电池和负的半电池具有至少包含一种离子性液体的电解质(例如,参照专利文献1)。
现有技术文献
专利文献
专利文献1:日本特许第5468090号公报
发明内容
发明要解决的技术问题
然而,专利文献1中公开的氧化还原液流电池的电解液中,若水侵入电解质内,则会发生水的电解而产生氢气和氧气等,有可能导致氧化还原液流电池劣化。由于氧化还原液流电池劣化,因此具有氧化还原液流电池的能量密度降低这样的问题。
本发明的第一方面是鉴于上述情况而完成的,其目的在于提供一种氧化还原液流电池用负极电解液,在用于氧化还原液流电池时,可在高电压下具有高能量密度。
解决技术问题的技术手段
本发明所述的第一方面的氧化还原液流电池用负极电解液具有负极活性物质、负极支持电解质(支持塩)和负极溶剂;上述负极溶剂为以LogP表示的水-辛醇分配系数LogPOW在1.5以上的溶剂。
本发明的第二方面是,根据上述第一方面所述的氧化还原液流电池用负极电解液,其中,上述负极溶剂含有醚基。
本发明的第三方面是,根据上述第二方面所述的氧化还原液流电池用负极电解液,其中,上述负极支持电解质的阴离子为选自于由N(SO2CF3)2、N(SO2CH3)2、N(SO2C4H9)2、N(SO2C2F5)2、N(SO2C4F9)2、N(SO2F3)(SO2C4F9)、N(SO2C2F5)(SO2C4F9)、N(SO2C2F4SO2)、N(SO2F)2和N(SO2F)(SO2CF3)所组成的组中的一种以上的成分。
本发明的第四方面是,根据上述第二或第三方面所述的氧化还原液流电池用负极电解液,其中,上述负极溶剂为选自于由甲氧基环戊烷、二乙二醇二丁醚和乙二醇二苄醚所组成的组中的一种以上的成分。
本发明的第五方面是,根据上述第一方面所述的氧化还原液流电池用负极电解液,其中,上述负极溶剂为选自于由1-甲基-1-丙基吡咯烷鎓·双(三氟甲磺酰基)酰亚胺、1-甲基-1-丙基吡咯烷鎓·双(氟甲磺酰基)酰亚胺、三乙基-(2-甲氧基乙基)磷双(三氟甲磺酰基)酰亚胺和三乙基-(2-甲氧基乙基)磷双(氟甲磺酰基)酰亚胺所组成的组中的一种以上的成分。
本发明的第六方面是,根据第一至第五方面中任一项所述的氧化还原液流电池用负极电解液,其中,上述负极溶剂在室温下于100g水中的溶解度为5g以下。
本发明的氧化还原液流电池,具有:
正极电解液;
正极集电体,所述正极集电体使上述正极电解液所包含的正极活性物质氧化还原;
负极电解液;
负极集电体,所述负极集电体使上述负极电解液所包含的负极活性物质氧化还原;以及
离子导电性的隔离部,所述隔离部将上述正极电解液与上述负极电解液隔离;
上述负极电解液为第一至第六方面中任一项所述的氧化还原液流电池用负极电解液。
有益效果
本发明所述的第一方面的氧化还原液流电池用负极电解液在用于氧化还原液流电池时,可在高电压下具有高能量密度。
附图说明
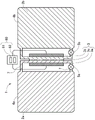
图1是示意性示出使用本发明的实施方式所述的氧化还原液流电池用负极电解液的氧化还原液流电池的剖面图。
图2是示出氧化还原液流电池系统中在放电时电子流动的一个实例的说明图。
图3是示出氧化还原液流电池系统中在充电时电子流动的一个实例的说明图。
具体实施方式
以下详细说明本发明的实施方式。另外,附图中的各构件的比例可能与实际不同。除非另外说明,本说明书中所示的数值范围的「~」是指包含其前后所记载的数值作为下限值和上限值。
<氧化还原液流电池用负极电解液>
本发明的实施方式所述的氧化还原液流电池用负极电解液(以下简称为“负极电解液”)是用于氧化还原液流电池的负极电解液,具有负极活性物质、负极溶剂(也称为负极溶媒)和负极支持电解质。
(负极活性物质)
负极活性物质可使用负极固态活性物质、在室温为液体的有机活性物质。
作为负极固态活性物质,可使用锂、钠、钾、钙、镁、铝、石墨(黒鉛)、硬碳、软碳、硅、氧化硅、锡、钛酸锂、氧化钛、氧化钼、硫、锌等。这些可单独使用一种,也可以组合使用2种以上。这些之中,可特别优选使用石墨。
在使用负极固态活性物质作为负极活性物质的情况下,负极电解液也可包含将电子从负极集电体传递至负极活性物质的媒介物质(即介质(mediator))和铜、碳等导电剂。
通过使用在室温下为液体的有机活性物质来作为负极活性物质,可相对于负极溶剂以高浓度进行混合。作为这种在室温为液体的有机活性物质,可使用2-甲基喹喔啉、2-甲基-3-丙基喹喔啉、2-甲氧基-3-甲基吡嗪、2,3,5-三甲基吡嗪、2,3-二甲基吡嗪、2,5-二甲基吡嗪、2-乙基吡嗪、2-丙基吡嗪、2-乙氧基吡嗪、2-甲氧基吡嗪、氯吡嗪、4-叔丁基吡嗪、2,6-二-叔丁基吡啶、2,5-二氟吡嗪、2,3,5,6-四甲基吡嗪、3-乙基联苯、2-甲基萘、1-甲基萘、2-甲基吡嗪等。这些可单独使用一种,也可以组合使用2种以上。这些之中,可以优选使用2,3,5-三甲基吡嗪和2-甲基喹喔啉。
(负极溶剂)
负极溶剂为以LogP表示的水-辛醇分配系数LogPOW在1.5以上的溶剂。LogPOW优选为1.8以上,进一步优选为3.4以上。另外,分配系数LogPOW为辛醇/水分配系数,即表示在辛醇相与水相之间分配有机溶剂情况下的分配程度的系数。例如,LogPOW由下式(1)表示。另外,下式(1)中的Co为辛醇相中有机溶剂的摩尔浓度,Cw为水相中有机溶剂的摩尔浓度。
LogPOW=Log(Co/Cw)…(1)
负极溶剂优选为疏水性溶剂。本实施方式中,疏水性是指将在室温(23℃±2℃)下于100g水中的溶解量在5g以下的溶剂定义为疏水性溶剂。优选地使用在室温下于100g水中的溶解量在5g以下的溶剂,更优选地使用在室温下于100g水中的溶解量在1g以下的溶剂。
负极溶剂优选含有醚基,优选包含具有醚基的结构。负极电解液为负极侧的电解液,因此主要是在还原气氛下使用。作为氧化还原液流电池,为了达成更高的电压,优选负极活性物质的氧化还原电位较低。即,负极溶剂优选地至少在与所使用的负极活性物质的氧化还原电位同等或同等以下的电位中不发生还原分解。醚基不易发生还原分解而可提高负极溶剂的还原耐性,因此负极溶剂优选具有可提高还原耐性的醚基的结构。
作为这样的负极溶剂,例如,可使用甲氧基环戊烷、二乙二醇二丁醚和乙二醇二苄醚等。这些可单独使用一种,也可以组合使用2种以上。
此外,作为负极溶剂,也可使用离子液体。作为在还原气氛下不易发生还原分解的离子液体,可使用1-甲基-1-丙基吡咯烷鎓·双(三氟甲磺酰基)酰亚胺、1-甲基-1-丙基吡咯烷鎓·双(氟磺酰基)酰亚胺、三乙基-(2-甲氧基乙基)磷双(三氟甲磺酰基)酰亚胺和三乙基-(2-甲氧基乙基)磷双(氟甲磺酰基)酰亚胺等。这些可单独使用一种,也可以组合使用2种以上。这些之中,优选使用疏水性高的1-甲基-1-丙基吡咯烷鎓·双(三氟甲磺酰基)酰亚胺。
(负极支持电解质)
负极支持电解质优选包含大体积阴离子。由此,负极支持电解质可使电子态离域化(非局在化)。
可作为负极溶剂使用的疏水性溶剂是疏水性高、极性低的非极性溶剂。在本文中,极性是因为分子内存在电性偏移而由电偶极矩所产生。疏水性物质一般为电中性的非极性物质,支持电解质是由正离子与负离子构成的物质,其为极性分子。一般而言,非极性分子易溶解于非极性溶剂,极性分子易溶解于极性溶剂。
即,作为极性物质的负极支持电解质不易溶解于作为非极性溶剂的疏水性溶剂。因此,负极支持电解质必须溶解于非极性溶剂中。为了提升对非极性溶剂的溶解性,必须使负极支持电解质的电子态离域化。作为使电子态离域化的方法,可使用大体积阴离子。
作为负极支持电解质的阴离子,可使用N(SO2CF3)2、N(SO2CH3)2、N(SO2C4H9)2、N(SO2C2F5)2、N(SO2C4F9)2、N(SO2F3)(SO2C4F9)、N(SO2C2F5)(SO2C4F9)、N(SO2C2F4SO2)、N(SO2F)2、N(SO2F)(SO2CF3)等。这些可单独使用一种,也可以组合使用2种以上。这些之中,优选N(SO2CF3)2和N(SO2F)2。
负极支持电解质的阳离子只要是在正极活性物质氧化时通过离子导电性隔离膜的阴离子或阳离子即可。作为负极支持电解质的阳离子,具体而言,可使用锂离子、钠离子、钾离子、镁离子、铝离子、钙离子、铵离子等。
本实施方式所述的负极电解液具有负极活性物质、负极支持电解质和负极溶剂,负极溶剂是使用以LogP表示的水-辛醇分配系数LogPOW在1.5以上的溶剂,由此,负极溶剂为具有疏水性的溶剂,因此可抑制水的电解。因此,本实施方式所述的负极电解液,在用于氧化还原液流电池时,可在高电压下具有高能量密度。
此外,本实施方式所述的负极电解液包含疏水性的负极溶剂,因此可取得(取り出す)水的电解以上的电压。进一步地,即使为开放系统,也可抑制水分的侵入。
由此,本实施方式所述的负极电解液可有效地用作氧化还原液流电池用的负极电解液,可以合适地用于使用负极电解液的氧化还原液流电池以及使用氧化还原液流电池的应用等。
本实施方式所述的负极电解液中,负极溶剂可含有醚基。由此,负极溶剂可改善负极溶剂本身对还原分解的耐性,因而可使用能够发挥更高电压的负极活性物质。因此,负极电解液不易发生还原分解,可作为稳定的负极电解液。因此,负极电解液可取得水的电解以上的电压。进一步地,即使为开放系统,负极电解液也可抑制水分的侵入。
本实施方式所述的负极电解液中,作为负极支持电解质的阴离子,可使用选自于由N(SO2CF3)2、N(SO2CH3)2、N(SO2C4H9)2、N(SO2C2F5)2、N(SO2C4F9)2、N(SO2F3)(SO2C4F9)、N(SO2C2F5)(SO2C4F9)、N(SO2C2F4SO2)、N(SO2F)2和N(SO2F)(SO2CF3)所组成的组中的一种以上的成分。由此,可使负极支持电解质的电子离域化,因此可溶解于极性低的疏水性溶剂。因此,负极电解液可得到即使在极性低的疏水性溶剂中也可溶解的负极支持电解质。
此外,对于侵入的水,负极支持电解质的阴离子可在与水的固液界面中形成溶剂化结构(溶媒和構造)。因此,即使少量的水侵入,对于侵入的水分子,负极支持电解质的阴离子形成溶剂化结构,因而可以抑制水的电解。
由此,本实施方式所述的负极电解液通过包含疏水性且耐还原性高的负极溶剂和支持电解质(该支持电解质含有电子经离域化的阴离子),从而即使在大气下,无需严密的密闭结构即可抑制水侵入电解液内,并且即使水侵入也可抑制水发生电解。因此,负极电解液可更有效地用作氧化还原液流电池用负极电解液。
本实施方式所述的负极电解液中,作为负极溶剂,可使用选自于由甲氧基环戊烷、二乙二醇二丁醚和乙二醇二苄醚所组成的组中的一种以上的成分。由此,负极电解液可具有高疏水性。
本实施方式所述的负极电解液中,作为负极溶剂,可使用选自于由1-甲基-1-丙基吡咯烷鎓·双(三氟甲磺酰基)酰亚胺、1-甲基-1-丙基吡咯烷鎓·双(氟甲磺酰基)酰亚胺、三乙基-(2-甲氧基乙基)磷双(三氟甲磺酰基)酰亚胺和三乙基-(2-甲氧基乙基)磷双(氟甲磺酰基)酰亚胺所组成的组中的一种以上的成分。由此,负极电解液可得到能够发挥疏水性效果并且能够发挥作为负极支持电解质的效果的负极溶剂。
本实施方式所述的负极电解液中,作为负极溶剂,在室温下于100g水中的溶解度可在5g以下。由此,负极溶剂可具有充分的疏水性,因此负极电解液可具有高疏水性。
<氧化还原液流电池>
对具有本发明所述的实施方式的负极电解液的氧化还原液流电池(氧化还原液流电池系统)进行说明。图1是示意性示出使用了本发明的实施方式所述的负极电解液的氧化还原液流电池的剖面图。另外,图1虽仅图示出了用来说明氧化还原液流电池所需的要件,但实际上具有用于驱动等的图中未示出的其它构件。
如图1所示,氧化还原液流电池1具有正极电解液2a、氧化还原液流电池用负极电解液(负极电解液)2b、氧化还原液流电池主体(电池主体)3、正极电解液槽4a、负极电解液槽4b、正极泵5a、负极泵5b、电源/负载部6和连接管7。电池主体3、正极电解液槽4a、负极电解液槽4b、正极泵5a及负极泵5b通过连接管7连接。填充于正极电解液槽4a中的正极电解液2a与填充于负极电解液槽4b中的负极电解液2b分别通过正极泵5a和负极泵5b在电池主体3内循环供给。
作为正极电解液2a,可使用公知的正极电解液。
另外,正极电解液2a还可包含将电子从正极集电体传递至正极活性物质的媒介物质(即介质)和铝、碳等导电剂。
负极电解液2b由于使用上述的本实施方式所述的负极电解液而省略说明。
电池主体3具有正极集电体3a、负极集电体3b、离子导电性隔离膜(隔离部)3c。供给至电池主体3的正极电解液2a从离子导电性隔离膜3c与正极集电体3a之间穿过,回到正极电解液槽4a内。供给至电池主体3的负极电解液2b从离子导电性隔离膜3c与负极集电体3b之间穿过,回到负极电解液槽4b内。
正极集电体3a包含正极活性物质、正极溶剂和正极支持电解质,负极集电体3b包含负极活性物质、负极溶剂和负极支持电解质。
正极活性物质可使用至少包含锂、钠、钾、镁、铝的任一种的过渡金属氧化物、以二茂铁为代表的有机金属络合物、以2,2,6,6-四甲基哌啶1-氧(2,6,6-テトラメチルピペリジン1-オキシル)和醌为代表的可生成自由基的有机化合物等。
正极溶剂为可使正极活性物质溶解或分散的液体,不受特别限定,使用水、碳酸亚乙酯、碳酸亚丙酯、碳酸甲乙酯、碳酸二乙酯、碳酸二甲酯、碳酸二乙酯、二甲基甲酰胺、离子液体、甲氧基环戊烷、1-乙基-3-甲基咪唑鎓双(三氟甲磺酰基)酰亚胺、1-丁基-2,3-二甲基咪唑鎓双(三氟甲磺酰基酰亚胺)、1-丁基-2,3-二甲基咪唑鎓双(氟磺酰基酰亚胺)、1-丁基-3-甲基咪唑鎓六氟化磷酸、1-甲基-1-丙基咪唑鎓双(三氟甲磺酰基酰亚胺)、1-甲基-1-丙基咪唑鎓双(氟磺酰基酰亚胺)、三乙基-(2-甲氧基乙基)磷双(三氟甲磺酰基)酰亚胺、三乙基-(2-甲氧基乙基)磷双(氟磺酰基)酰亚胺、三乙基甲氧基甲基磷双(三氟甲磺酰基)酰亚胺、三乙基甲氧基甲基磷双(氟磺酰基)酰亚胺等。
正极支持电解质只要是溶解于正极溶剂的电解质(塩)即可,优选为六氟磷酸锂、六氟磷酸钠、双(三氟甲磺酰基)酰亚胺锂、双(氟磺酰基)酰亚胺锂、双(三氟甲磺酰基)酰亚胺钠、双(氟磺酰基)酰亚胺钠、二草酸硼酸锂、二草酸硼酸钠等。
另外,正极溶剂为离子液体的情况下,由于离子液体成为正极支持电解质,因此不需要添加正极支持电解质。
正极集电体3a,从其表面进行电子相对于正极活性物质和介质的接收与传递。即,表面积越大的材料,电化学反应量越多,因此优选。此外,由于暴露于正极充放电电位,因此必须使用至少在正极活性物质和介质的氧化还原电位中也不会氧化溶解、氧化分解的材料。作为这样的材料,可使用碳纸、碳毡等。
此外,正极集电体3a其表面也可以进行表面处理,也可用粘合剂将成为正极活性物质的材料固定于正极集电体3a的表面。由此,正极集电体3a其表面上可储存电荷,因此即使在需要瞬间产生大电流放电的情况下也可应对。
负极集电体3b所包含的负极活性物质、负极溶剂和负极支持电解质可使用公知的负极活性物质、负极溶剂和负极支持电解质,也可使用上述本实施方式所述的负极电解液所包含的负极活性物质、负极溶剂和负极支持电解质。
离子导电性隔离膜3c可为下述任一类型:阳离子移动型,充电时阳离子从正极向负极移动、放电时阳离子从负极向正极移动的类型;以及阴离子移动型,充电时阴离子从负极向正极移动、放电时阴离子从正极向负极移动的类型。在离子导电性隔离膜3c为阳离子移动型的情况下,可使用氧化物的固体电解质和高分子固体电解质等的阳离子交换膜等。另一方面,在阴离子移动型的情况下,可使用碱型的阴离子交换膜等。
此外,离子导电性隔离膜3c也可使用具有尺寸小于活性物质的连续气孔的多孔质膜。
正极电解液槽4a为储存正极电解液2a的槽。
负极电解液槽4b为储存负极电解液2b的槽。
正极泵5a设置于连接管7,将正极电解液槽4a内的正极电解液2a供给至电池主体3。
负极泵5b设置于连接管7,将负极电解液槽4b内的负极电解液2b供给至电池主体3。
电源/负载部6具有电池等直流电源和马达等负载,充电时作为负载发挥功能,放电时作为电源发挥功能。
连接管7将电池主体3与正极电解液槽4a连接,同时将电池主体3与负极电解液槽4b连接,使正极电解液槽4a内的正极电解液2a在电池主体3与正极电解液槽4a之间循环,同时使负极电解液槽4b内的负极电解液2b在电池主体3与负极电解液槽4b之间循环。
氧化还原液流电池1中,在使充电完成的电解液放电时,将电源/负载部6内的负载61连接至正极集电体3a和负极集电体3b。图2是示出氧化还原液流电池1中在放电时电子流动的一个实例的说明图。另外,图2中的箭头表示电子流动。如图2所示,电子从负极电解液2b所包含的负极活性物质向负极集电体3b移动,通过配线移动至负载61。之后,电子通过负载61从正极集电体3a向正极电解液2a所包含的正极活性物质移动。同时,为了补偿电荷,阳离子(cation)通过离子导电性隔离膜3c而从负极电解液2b移动至正极电解液2a。此外,阴离子(anion)通过离子导电性隔离膜3c从正极移动至负极。
在使放电完成的电解液充电时,将电源/负载部6内的直流电源62连接至正极集电体3a和负极集电体3b。图3是示出氧化还原液流电池1中在充电时电子流动的一个实例的说明图。另外,图3中的箭头表示电子流动。如图3所示,电子从正极电解液2a所包含的正极活性物质向正极集电体3a移动,电子通过直流电源62从负极集电体3b向负极电解液2b所包含的负极活性物质移动。同时,为了补偿电荷,阴离子通过离子导电性隔离膜3c从负极电解液2b移动至正极电解液2a。此外,阳离子通过离子导电性隔离膜3c从正极移动至负极。
这样,如上所述,氧化还原液流电池1由于使用了本实施方式所述的负极电解液作为负极电解液2b,从而可抑制水的电解。因此,氧化还原液流电池1可在高电压下具有高能量密度。
此外,氧化还原液流电池1因为具有本实施方式所述的负极电解液,从而不需要使用近年价格明显高涨的钒即可构成氧化还原液流电池。进一步地,如上所述,因为也可以使用多孔质膜作为离子导电性隔离膜,通过使离子导电性隔离膜为多孔质膜,可大幅降低设置费用。
实施例
以下,示出实施例和比较例来更具体地对实施方式进行说明,但实施方式并不限于这些的实施例。
<实施例1>
[氧化还原液流电池的制作]
(负极电解液的制作)
将负极活性物质(2,3,5-三甲基吡嗪,东京化成工业社制造)1.988g(16.3mmol)与负极支持电解质(双(三氟甲磺酰基)酰亚胺锂(LiTFSI),东京化成工业社制造)1.168g(4.07mmol)混合生成混合物后,在混合物中添加疏水性溶剂(甲氧基环戊烷(MCP),LogPOW:1.575,东京化成工业社制造)1.291g作为负极溶剂,得到负极电解液。得到的负极电解液的总体积为4.07mmL,负极活性物质的浓度为4.00mol/L。
(正极电解液的制作)
将正极活性物质(4-甲氧基-2,2,6,6-四甲基哌啶1-氧自由基,东京化成工业社制造)3.031g(16.3mmol)与正极支持电解质(双(氟磺酰基)酰亚胺锂,东京化成工业社制造)3.043g(16.3mmol)混合生成混合物后,在混合物中添加离子交换水0.774g,得到正极电解液。得到的正极电解液的总体积为5.00mmL,正极活性物质的浓度为3.25mol/L。
(离子导电性隔离膜)
离子导电性隔离膜使用Nafion(ナフィオン,注册商标)117(Sigma-Aldrich Japan(シグマアルドリッチジャパン)合同会社制造)。Nafion(注册商标)117为质子型,因此在室温浸渍于1mol/L的氢氧化锂水溶液约12小时,由此进行从质子到锂离子的离子交换。
(集电体)
正极集电体和负极集电体使用流通式全电解池的工作电极(フロー全電解セルの作用電極)用碳毡(直径12mm,厚度5mm,表面积约850cm2,株式会社イーシーフロンティア制造)。
(氧化还原液流电池)
使正极集电体与离子导电性隔离膜的单面接触,并使负极集电体与另一面接触,以制作发电部。正极电解液槽与发电部以及负极电解液槽与发电部以内径2mm的硅胶管连接,并将硅胶管与软管泵连接,制作氧化还原液流电池。
<氧化还原液流电池的特性评价>
作为氧化还原液流电池的特性评价,进行充放电试验、测量充电容量、放电容量、充放电效率(库伦效率)和理论放电容量。
[充放电试验]
在大气中,使用氧化还原液流电池,向正极电解液用槽和负极电解液用槽分别注入正极电解液、负极电解液,通过软管泵以10mL/min的速度流动。在使正极电解液和负极电解液流动的状态下,以43.6mA的电流进行定电流充电至2.3V,测量充电容量。暂停10分钟后,以43.6mA的电流进行定电流放电至1.0V,测量放电容量。从得到的充电容量和放电容量求出以放电容量/充电容量表示的库伦效率。另外,也计算出理论放电容量。
<实施例2>
在实施例1中,改变负极电解液的构成,除此之外,与实施例1相同地进行。
(负极电解液的制作)
将负极活性物质(2-甲基喹喔啉,东京化成工业社制造)2.346g(16.3mmol)与负极溶剂(1-甲基-1-丙基吡咯烷鎓·双(三氟甲磺酰基)酰亚胺;PP13 TFSI,LogPOW:4.8165,东京化成工业社制造)2.827g混合,得到负极电解液。另外,1-甲基-1-丙基吡咯烷鎓·双(三氟甲磺酰基)酰亚胺为疏水性的离子液体,也作为支持电解质发挥功能,因此并未额外添加负极支持电解质。此负极电解液的总体积为4.07mmL,活性物质的浓度为4.00mol/L。
<比较例1>
在实施例1中,改变负极电解液的构成,除此之外,与实施例1相同地进行。
(负极电解液的制作)
将负极活性物质(双(三氟甲磺酰基)酰亚胺锂,东京化成工业社制造)1.988g(16.3mmol)与负极支持电解质(N-N’二甲基甲酰胺,东京化成工业社制造)1.168g(4.07mmol)混合生成混合物后,向混合物添加负极溶剂(2,3,5-三甲基吡嗪,LogPOW:1.40180,东京化成工业社制造)1.411g,得到负极电解液。得到的负极电解液的总体积为4.07mmL,活性物质的浓度为4.00mol/L。
<实施例3>
[氧化还原液流电池的制作]
(负极电解液的制作)
将负极活性物质(石墨)1.55g与负极溶剂(甲氧基环戊烷(MCP),LogPOW:1.575,Sigma-Aldrich Japan合同会社制造)1.40g与负极支持电解质(双(三氟甲磺酰基)酰亚胺锂(LiTFSI),KISHIDA(キシダ)化学社制造)0.59g放入容器混合,制备混合液。使用混合机以旋转数2000rpm搅拌所制备的混合液60秒。重复此搅拌5次。搅拌后,混合溶液中的负极活性物质仍未溶解而呈现分散状态。该负极电解液的总体积为2.76mL,负极活性物质的浓度为25vol%,负极电解液的电解质浓度为1mol/L。
(正极电解液的制作)
将正极活性物质(磷酸铁锂)3.08g、正极导电材料(碳黑)0.03g、正极溶剂(甲氧基环戊烷MCP,Sigma-Aldrich Japan合同会社制造)2.30g与正极支持电解质(双(三氟甲磺酰基)酰亚胺锂LiTFSI,KISHIDA化学社制造)0.98g放入容器混合,制备混合液。使用混合机以旋转数2000rpm将所制备的混合液搅拌60秒。重复该搅拌5次。搅拌后正极活性物质也未溶解而呈现分散状态。得到的正极电解液的总体积为4.28mL,正极活性物质的浓度为25vol%,正极电解液的电解质浓度为1mol/L。
(离子导电性隔离膜)
离子导电性隔离膜使用聚乙烯微多孔膜(W-SCOPE(ダブル·スコープ)株式会社制造)。
(集电体)
正极集电体使用铝箔,负极集电体使用铜箔。
(氧化还原液流电池)
以在离子导电性隔离膜与正极集电体之间形成100μm空间的方式配置聚乙烯制的肋部(リブ),以在离子导电性隔离膜与负极集电体之间形成100μm空间的方式配置聚乙烯制的肋部,以制作发电部。正极电解液槽与发电部以及负极电解液槽与发电部以内径2mm的乙烯丙烯二烯橡胶管连接,并将乙烯丙烯二烯橡胶管与软管泵连接,制作氧化还原液流电池。
<氧化还原液流电池的特性评价>
作为氧化还原液流电池的特性评价,进行充放电试验,测量充电容量、放电容量、库伦效率和理论放电容量。
<充放电试验>
在大气中,使用氧化还原液流电池,分别向正极电解液用槽和负极电解液用槽注入正极电解液、负极电解液,通过软管泵,以10mL/min速度流动。正极电解液在由设置在离子导电性隔离膜与正极集电体之间的肋部所形成的空间中流动。负极电解液在由设置在离子导电性隔离膜与负极集电体之间的肋部所形成的空间中流动。
在使正极电解液和负极电解液流动的状态下,以43.6mA的电流进行定电流充电至4V,测量充电容量。暂停10分钟后,以43.6mA的电流进行定电流放电至1.0V,测量放电容量。从得到的充电容量和放电容量求得库伦效率。另外,也计算出理论放电容量。
<实施例4>
在实施例3中,改变构成负极电解液的负极溶剂的种类与构成正极电解液的正极溶剂的种类及其添加量,除此之外,与实施例3相同地进行。
(负极电解液的制作)
在实施例3中,将负极溶剂改变为二乙二醇二丁醚(DEGDBE,LogPOW:1.92,东京化成工业社制造),除此之外,与实施例3相同地进行。搅拌后,混合溶液中的负极活性物质也未溶解而呈现分散状态。该负极电解液的总体积为2.76mL,负极活性物质的浓度为25vol%,负极电解液的电解质浓度为1mol/L。
(正极电解液的制作)
在实施例3中,将正极溶剂改变为二乙二醇二丁醚DEGDBE(东京化成工业社制造),将正极溶剂的添加量改变为2.36g,除此之外,与实施例3相同地进行。搅拌后正极活性物质也未溶解而呈现分散状态。得到的正极电解液的总体积为4.28mL,正极活性物质的浓度为20vol%,正极电解液的电解质浓度为1mol/L。
<实施例5>
在实施例3中,改变构成负极电解液的负极溶剂的种类及其添加量、构成正极电解液的正极溶剂的种类及其添加量,除此之外,与实施例3相同地进行。
(负极电解液的制作)
在实施例3中,将负极溶剂改变为乙二醇二苄醚(EGDBE,LogPOW:3.42,东京化成工业社制造),将负极溶剂的添加量改变为1.72g,除此之外,与实施例3相同地进行。搅拌后混合溶液中的负极活性物质也未溶解而呈现分散状态。该负极电解液的总体积为2.76mL,负极活性物质的浓度为25Vol%,负极电解液的电解质浓度为1mol/L。
(正极电解液的制作)
在实施例3中,将正极溶剂改变为乙二醇二苄醚EGDBE(东京化成工业社制造),将正极溶剂的添加量变更为2.83g,除此之外,与实施例3相同地进行。搅拌后正极活性物质也未溶解而呈现分散状态。得到的正极电解液的总体积为4.28mL,正极活性物质的浓度为20vol%,正极电解液的电解质浓度为1mol/L。
<实施例6>
在实施例3中,改变构成负极电解液的负极溶剂和负极支持电解质的种类及这些的添加量、构成正极电解液的正极溶剂的种类及其添加量,除此之外,与实施例3相同地进行。
(负极电解液的制作)
在实施例3中,将负极溶剂改变为二乙二醇二丁醚(DEGDBE,LogPOW:1.92,东京化成工业社制造),使负极溶剂的添加量为1.46g,将负极支持电解质改变为双(五氟乙磺酰基)酰亚胺锂LiBETI,将负极支持电解质的添加量改变为0.80g,除此之外,与实施例3相同地进行。搅拌后,混合溶液中的负极活性物质也未溶解而呈现分散状态。此负极电解液的总体积为2.76mL,负极活性物质的浓度为25vol%,负极电解液的电解质浓度为1mol/L。
(正极电解液的制作)
在实施例3中,将正极溶剂改变为二乙二醇二丁醚DEGDBE(东京化成工业社制造),将正极溶剂的添加量改变为2.40g,将正极支持电解质改变为双(五氟乙磺酰基)酰亚胺锂LiBETI,将负极支持电解质的添加量改变为1.32g,除此之外,与实施例3相同地进行。搅拌后,正极活性物质也未溶解而呈现分散状态。得到的正极电解液的总体积为4.28mL,正极活性物质的浓度为20vol%,正极电解液的电解质浓度为1mol/L。
<比较例2>
在实施例3中,改变构成负极电解液的负极溶剂和负极支持电解质的种类与这些的添加量、构成正极电解液的正极溶剂的种类及其添加量,除此之外,与实施例3相同地进行。
(负极电解液的制作)
在实施例3中,将负极溶剂改变为以等容积比包含碳酸亚乙酯EC、碳酸甲乙酯EMC与碳酸二乙酯DMC的混合物(LogPOW:0.707,东京化成工业社制造),使负极溶剂的添加量为2.10g,将负极支持电解质改变为六氟磷酸锂LiPF6(KISHIDA化学社制造),将负极支持电解质的添加量改变为0.31g,除此之外,与实施例3相同地进行。搅拌后,混合溶液中的负极活性物质也未溶解而呈现分散状态。该负极电解液的总体积为2.76mL,负极活性物质的浓度为25vol%,负极电解液的电解质浓度为1mol/L。
(正极电解液的制作)
在实施例3中,将正极溶剂改变为以等容积比包含碳酸亚乙酯EC、碳酸甲乙酯EMC与碳酸二乙酯DMC的混合物(KISHIDA化学社制造),将正极溶剂的添加量改变为3.46g,将正极支持电解质改变为六氟化磷酸锂LIPF6(KISHIDA化学社制),将正极支持电解质的添加量改变为0.31g,除此之外,与实施例3相同地进行。搅拌后,正极活性物质也未溶解而呈现分散状态。得到的正极电解液的总体积为4.28mL,正极活性物质的浓度为20vol%,正极电解液的电解质浓度为1mol/L。
测量各实施例和比较例的充电容量、放电容量、库伦效率、理论放电容量,结果显示于表1。
由表1可知,实施例1~实施例6中,库伦效率在83%以上。特别地,实施例1和实施例2中,库伦效率为94%。另一方面,比较例1和比较例2中,库伦效率为43%以下。此外,实施例1~实施例6中,放电容量在389mAh以上。另一方面,比较例1和比较例2中,放电容量在198mAh以下。LogP值的大小表示疏水性的高低。实施例1~实施例6的负极电解液与比较例1和比较例2的负极电解液不同,通过使用水-辛醇分配系数LogPOW在1.58以上的高疏水性负极溶剂,在大气中,即使在高电压下仍不易发生水的电解,因此使用负极电解液所构成的氧化还原液流电池可提高库伦效率并且可具有高容量。
另外,实施例2中,将绿色LED连接于正极集电体与负极集电体时,确认绿色LED发光。为了使绿色LED发光,需要2.0V以上,实施例2中所输出的电压高于在包含水分的大气中水电解的理论电压(1.3V),确认具有高质量能量密度。因此,一方面抑制水的电解,一方面达成水的电解以上的2.0V电压,因此确认使用本实施方式所述的负极电解液是有效的。
此外,比较例1中,关于充电容量与从所使用的负极活性物质的质量所计算出的理论放电容量的差值,充电容量超过理论放电容量。这表示电流在负极活性物质的充电以外被消耗,推测是因为比较例1中使用非疏水性的溶剂而在充电中发生水的电解。
因此,在将本实施方式所述的负极电解液用于氧化还原液流电池时,可在高电压下具有高能量密度,因此可具有优异的充放电特性。因此,使用了本实施方式所述的负极电解液的氧化还原液流电池容易操作且具有高能量密度,因此若应用于例如能量储存设施,在相同规模下能储存更多电能。此外,电动车中,更换一次电解液即可行进更长的距离。
另外,本发明的氧化还原液流电池并不限于上述附图所示的实施方式,在不脱离其主旨的范围内可实施各种变化。即,也可不应用于使电解液相对于氧化还原液流电池主体循环而进行充放电,而是应用于仅通入氧化还原液流电池主体一次即完成充放电的系统。此外,本发明的氧化还原液流电池不仅可应用于发电设施附属的能量储存设施和电动车等,也可应用于使用来自所搭载的氧化还原液流电池电力的至少一部分来进行驱动的船舶和飞机等,此外,也可配合电力消耗设施所在的住宅和工场而各自应用。
虽根据上述对实施方式进行了说明,但上述实施方式仅作为示例提出,本发明并不限于上述实施方式。上述实施方式也可以以其它各种方式实施,在不脱离发明主旨的范围内,可进行各种组合、省略、取代、变更等。这些实施方式及其变化包含在发明的范围及主旨中,并且也包含在本申请权利要求所记载的发明及其等同的范围中。
本申请要求2019年4月8日申请的日本专利申请2019-073282号的优先权,其内容作为整体参考并引用至本说明书中。
[符号说明]
1 氧化还原液流电池
2a 正极电解液
2b 负极电解液(氧化还原液流电池用负极电解液)
3 氧化还原液流电池主体(电池主体)
3a 正极集电体
3b 负极集电体
3c 离子导电性隔离膜
4a 正极电解液槽
4b 负极电解液槽
5a 正极泵
5b 负极泵
6 电源/负载部
61 负载
62 直流电源
Claims (7)
1.一种氧化还原液流电池用负极电解液,所述氧化还原液流电池用负极电解液具有负极活性物质、负极支持电解质和负极溶剂;
所述负极溶剂为以LogP表示的水-辛醇分配系数LogPOW在1.5以上的溶剂。
2.如权利要求1所述的氧化还原液流电池用负极电解液,其中,所述负极溶剂含有醚基。
3.如权利要求2所述的氧化还原液流电池用负极电解液,其中,所述负极支持电解质的阴离子为选自于由N(SO2CF3)2、N(SO2CH3)2、N(SO2C4H9)2、N(SO2C2F5)2、N(SO2C4F9)2、N(SO2F3)(SO2C4F9)、N(SO2C2F5)(SO2C4F9)、N(SO2C2F4SO2)、N(SO2F)2和N(SO2F)(SO2CF3)所组成的组中的一种以上的成分。
4.如权利要求2或3所述的氧化还原液流电池用负极电解液,其中,所述负极溶剂为选自于由甲氧基环戊烷、二乙二醇二丁醚和乙二醇二苄醚所组成的组中的一种以上的成分。
5.如权利要求1所述的氧化还原液流电池用负极电解液,其中,所述负极溶剂为选自于由1-甲基-1-丙基吡咯烷鎓·双(三氟甲磺酰基)酰亚胺、1-甲基-1-丙基吡咯烷鎓·双(氟甲磺酰基)酰亚胺、三乙基-(2-甲氧基乙基)磷双(三氟甲磺酰基)酰亚胺和三乙基-(2-甲氧基乙基)磷双(氟甲磺酰基)酰亚胺所组成的组中的一种以上的成分。
6.如权利要求1-5中任一项所述的氧化还原液流电池用负极电解液,其中,所述负极溶剂在室温下于100g水中的溶解度为5g以下。
7.一种氧化还原液流电池,所述氧化还原液流电池具有:
正极电解液;
正极集电体,所述正极集电体使所述正极电解液所包含的正极活性物质氧化还原;
负极电解液;
负极集电体,所述负极集电体使所述负极电解液所包含的负极活性物质氧化还原;以及
离子导电性的隔离部,所述隔离部将所述正极电解液与所述负极电解液隔离,
其中,所述负极电解液为如权利要求1-6中任一项所述的氧化还原液流电池用负极电解液。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019-073282 | 2019-04-08 | ||
| JP2019073282 | 2019-04-08 | ||
| PCT/JP2020/015759 WO2020209274A1 (ja) | 2019-04-08 | 2020-04-08 | レドックスフロー電池用負極電解液及びレドックスフロー電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN113728477A true CN113728477A (zh) | 2021-11-30 |
Family
ID=72750728
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202080027269.2A Pending CN113728477A (zh) | 2019-04-08 | 2020-04-08 | 氧化还原液流电池用负极电解液及氧化还原液流电池 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20220166043A1 (zh) |
| EP (1) | EP3955351A1 (zh) |
| JP (1) | JPWO2020209274A1 (zh) |
| CN (1) | CN113728477A (zh) |
| TW (1) | TW202105816A (zh) |
| WO (1) | WO2020209274A1 (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11894590B2 (en) * | 2020-07-10 | 2024-02-06 | Washington University | Electrode-decoupled redox flow battery |
| CN113707927B (zh) * | 2021-10-28 | 2022-02-15 | 长沙理工大学 | 高体积容量液流电池系统 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010018840A (ja) * | 2008-07-10 | 2010-01-28 | Teijin Pharma Ltd | 電解質中の水除去方法、その装置、及び水分量測定装置 |
| JP2010244972A (ja) * | 2009-04-09 | 2010-10-28 | Sharp Corp | レドックスフロー電池 |
| US20140170460A1 (en) * | 2012-12-14 | 2014-06-19 | Samsung Electronics Co., Ltd. | Redox flow battery |
| KR20150008353A (ko) * | 2014-12-01 | 2015-01-22 | 주식회사 씨트리 | 비스플로로술포닐이미드 음이온을 갖는 전해질용 이온성 액체 |
| US20180026293A1 (en) * | 2016-07-19 | 2018-01-25 | Panasonic Intellectual Property Management Co., Ltd. | Flow battery |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102009009357B4 (de) | 2009-02-18 | 2011-03-03 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Redox-Flow-Batterie zur Speicherung von elektrischer Energie in ionischen Flüssigkeiten |
| CN102771000A (zh) * | 2010-02-22 | 2012-11-07 | 丰田自动车株式会社 | 非水电解液型二次电池以及非水电解液型二次电池用非水电解液 |
| JP2013251211A (ja) * | 2012-06-04 | 2013-12-12 | Hitachi Ltd | マグネシウムイオン二次電池用電解液、マグネシウムイオン二次電池 |
| JP6922881B2 (ja) | 2014-11-07 | 2021-08-18 | 大日本印刷株式会社 | 表示装置及び移動体 |
-
2020
- 2020-04-08 EP EP20787773.9A patent/EP3955351A1/en not_active Withdrawn
- 2020-04-08 CN CN202080027269.2A patent/CN113728477A/zh active Pending
- 2020-04-08 WO PCT/JP2020/015759 patent/WO2020209274A1/ja unknown
- 2020-04-08 JP JP2021513659A patent/JPWO2020209274A1/ja active Pending
- 2020-04-08 TW TW109111832A patent/TW202105816A/zh unknown
- 2020-04-08 US US17/602,389 patent/US20220166043A1/en not_active Abandoned
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010018840A (ja) * | 2008-07-10 | 2010-01-28 | Teijin Pharma Ltd | 電解質中の水除去方法、その装置、及び水分量測定装置 |
| JP2010244972A (ja) * | 2009-04-09 | 2010-10-28 | Sharp Corp | レドックスフロー電池 |
| US20140170460A1 (en) * | 2012-12-14 | 2014-06-19 | Samsung Electronics Co., Ltd. | Redox flow battery |
| KR20150008353A (ko) * | 2014-12-01 | 2015-01-22 | 주식회사 씨트리 | 비스플로로술포닐이미드 음이온을 갖는 전해질용 이온성 액체 |
| US20180026293A1 (en) * | 2016-07-19 | 2018-01-25 | Panasonic Intellectual Property Management Co., Ltd. | Flow battery |
Also Published As
| Publication number | Publication date |
|---|---|
| US20220166043A1 (en) | 2022-05-26 |
| TW202105816A (zh) | 2021-02-01 |
| EP3955351A1 (en) | 2022-02-16 |
| JPWO2020209274A1 (zh) | 2020-10-15 |
| WO2020209274A1 (ja) | 2020-10-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Zhu et al. | Ionic liquid-based electrolytes for aluminum/magnesium/sodium-ion batteries | |
| US9941559B2 (en) | Water enhanced ionic liquid electrolytes for metal-air batteries | |
| EP2999044B1 (en) | Liquid electrolyte for fluoride ion battery and fluoride ion battery | |
| US9548509B2 (en) | Polyoxometalate active charge-transfer material for mediated redox flow battery | |
| JP5050847B2 (ja) | 二次電池とこれを用いた電源システム、電源システムの使用方法 | |
| JP5397533B2 (ja) | 非水電解液型二次電池及び非水電解液型二次電池用非水電解液 | |
| US9627727B2 (en) | Lithium-air battery with cathode separated from free lithium ion | |
| Ortiz-Martínez et al. | The roles of ionic liquids as new electrolytes in redox flow batteries | |
| US20100266907A1 (en) | Metal air battery system | |
| US9666916B2 (en) | Biphase electrolyte for a metal-air battery | |
| JP2010086935A (ja) | レドックスフロー電池 | |
| EP3168916B1 (en) | Electrolytic solution and electrochemical device | |
| JP6682852B2 (ja) | レドックスフロー電池 | |
| Thomas et al. | Suppression of water absorption by molecular design of ionic liquid electrolyte for Li–air battery | |
| KR101918788B1 (ko) | 전해질 및 이차 전지 | |
| WO2010124172A2 (en) | A metal air battery system | |
| CN106732766A (zh) | 用于锂‑空气电池的可溶性催化剂 | |
| CN112086683A (zh) | 一种锂离子电池电解液及其制备方法、高压锂离子电池和电池模组 | |
| CN113728477A (zh) | 氧化还原液流电池用负极电解液及氧化还原液流电池 | |
| Pozo-Gonzalo et al. | Recent progress, advances, and future prospects in Na–O2 batteries | |
| CN102396095A (zh) | 电解质和二次电池 | |
| JP6643183B2 (ja) | 再充電可能な電池のための有機活物質 | |
| KR20190006375A (ko) | 소듐-바이페닐을 이용한 레독스 플로우 배터리 | |
| JP5277922B2 (ja) | 空気電池 | |
| WO2015195571A1 (en) | Hybrid electrolytes for group 2 cation-based electrochemical energy storage devices |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20211130 |