CN110730826A - 分析物检测 - Google Patents
分析物检测 Download PDFInfo
- Publication number
- CN110730826A CN110730826A CN201880030752.9A CN201880030752A CN110730826A CN 110730826 A CN110730826 A CN 110730826A CN 201880030752 A CN201880030752 A CN 201880030752A CN 110730826 A CN110730826 A CN 110730826A
- Authority
- CN
- China
- Prior art keywords
- analyte
- probe
- binding
- query probe
- query
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6809—Methods for determination or identification of nucleic acids involving differential detection
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/16—Hydrolases (3) acting on ester bonds (3.1)
- C12N9/22—Ribonucleases RNAses, DNAses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/26—Preparation of nitrogen-containing carbohydrates
- C12P19/28—N-glycosides
- C12P19/30—Nucleotides
- C12P19/34—Polynucleotides, e.g. nucleic acids, oligoribonucleotides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6834—Enzymatic or biochemical coupling of nucleic acids to a solid phase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/06—Libraries containing nucleotides or polynucleotides, or derivatives thereof
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/5308—Immunoassay; Biospecific binding assay; Materials therefor for analytes not provided for elsewhere, e.g. nucleic acids, uric acid, worms, mites
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/536—Immunoassay; Biospecific binding assay; Materials therefor with immune complex formed in liquid phase
- G01N33/542—Immunoassay; Biospecific binding assay; Materials therefor with immune complex formed in liquid phase with steric inhibition or signal modification, e.g. fluorescent quenching
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54306—Solid-phase reaction mechanisms
Abstract
本文提供了涉及检测分析物的技术,和特别但非排他地涉及使用基于检测探针的瞬时结合的技术检测分析物例如核酸、蛋白、小分子和其它分子的方法、系统、组合物和试剂盒的技术。
Description
本申请要求2017年3月8日提交的美国临时专利申请系列号62/468,578的优先权,所述临时专利申请通过引用以其整体结合到本文中。
关于联邦资助研究或开发的声明
本发明在美国国立卫生研究院授予的资助GM062357下和在美国海军海军研究办公室授予的资助W911NF-12-1-0420下在政府支持下完成。政府具有本发明的某些权利。
领域
本文提供了涉及检测分析物的技术,和特别但非排他地涉及使用基于检测探针的瞬时结合的技术检测分析物例如核酸、蛋白、小分子和其它分子的方法、系统、组合物和试剂盒。
背景
检测和定量复杂的混合物中的低浓度分析物在生物学研究和临床诊断中具有许多应用。许多重要的生物学分析物是疾病和其它生物学状态的生物标志物。例如,在血液、尿、唾液和其它体液中少部分的携带致癌突变的循环核酸的检测与某些类型的癌症的发生率相关。此外,蛋白分析物例如前列腺特异性抗原(PSA)和白介素也具有当前或潜在的临床和研究意义。小分子代谢物的水平提供了在生物学系统中关于健康和药物处理的信息。在分子诊断和研究中抗体、适体、核酸和其它亲和试剂广泛用于这些测定。
低丰度分子分析物的检测中的挑战是灵敏度和特异性之间的权衡。即,随着测定的灵敏度增加,假阳性的可能性增加,这降低了特异性。例如,普通ELISA (酶联免疫吸附测定)方法中的假阳性起因于第一或第二抗体与测定表面的非特异性结合,因此当预期的靶分析物不存在时产生信号。在这样的情况下,改进检测器灵敏度或信号放大效率增加真阳性和假阳性检测事件二者,导致更低的特异性。尽管已开发策略来降低假阳性事件,包括用封闭溶液孵育表面、严格性洗涤方案和使用必须共同结合靶分析物以产生信号的分裂探针,然而当前方法遭受到假阳性,因为在实践中假阳性信号不能完全被消除。结果是,对于许多类型的生物标志物,在单分子水平上以高特异性检测靶分析物仍然是困难的。
简述
之前已经描述了使用查询探针的瞬时结合的强度对比时间数据的动力学建模和分析检测核酸的策略(参见Johnson-Buck等(2015) Nat. Biotechnol. 33: 730-32; 美国专利申请公开号20160046988; 国际专利申请号PCT/US2017/016977,其各自通过引用以其整体结合到本文中)。相比之下,本发明的技术在一些实施方案中提供一种通过确定低亲和力查询探针的每个结合和解离事件的空间和时间坐标,然后按位置簇集结合事件,和使每个簇事件经历动力学分析(例如,确定每单位时间每个靶分子的事件数量或事件之间停留时间的平均数、中值、最大值、最小值、标准偏差或其它度量),检测与表面稳定结合的靶分析物的新方法。该方法允许区别非特异性探针结合和探针与靶分析物的结合,这是因为在查询探针与单个靶分析物的多个结合事件上的位置对比时间统计学累积得到在分析物的身份方面比任何以下各项更大的置信度:单一结合事件、跨越观察区域的结合事件的累积计数或跨越观察区域的探针信号的累积计数。此外,该方法使用基于强度波动(而不是总体信号强度)的空间位置信息和簇集来超越检测装置的分辨率极限,以提供“超分辨率”测量。因此,在一些实施方案中该技术提供比之前公开的方法更高的动态范围(图2),和检测探针与靶分析物的特异性结合和检测探针与成像表面或其它表面结合分析物的非特异性结合的区别力的改进(图3)。特别地,来自靶标结合的信号的紧密簇集的空间定位和探针与靶标结合的独特动力学行为用于提供靶标信号与非特异性(例如,假阳性)信号的区别力的改进。在一些实施方案中,当应用于大的检测器区域上的查询探针结合事件时,该方法可用于在单分子水平上数字计数一种或多种靶分析物。
该技术提供超过现有技术的优点,包括但不限于,改进分析物相对于背景结合的区别力;改进密切相关的分析物之间的区别力;和极度稀释或低体积样本的分析(例如,相对于分析相同分析物的现有技术,灵敏度和/或特异性改进)。
因此,在一些实施方案中,该技术提供一种表征样品中的分析物的方法。
在检测的分析物方面,该技术不受限制。例如,实施方案提供分析物的检测,所述分析物是核酸、多肽、碳水化合物、多糖、脂肪酸、磷脂、糖脂、鞘脂、小分子、代谢物、辅因子等。
在一些实施方案中,查询和/或捕获探针是核酸、多肽(例如,抗体、抗体片段、线性抗体、单链抗体或其它抗原-结合抗体衍生物;酶;特异性识别分析物的结合蛋白);在其中分析物包含碳水化合物或多糖的一些实施方案中,查询探针包含碳水化合物-结合蛋白,例如凝集素或碳水化合物-结合抗体。在一些实施方案中,在碳水化合物单体之间特定的糖苷键或糖苷键组的存在产生查询探针结合的可区别模式。在一些实施方案中,捕获探针是兔单克隆抗体;和在一些实施方案中,查询探针是小鼠单克隆抗体。
例如,在一些实施方案中该方法包括作为表面上(x, y)位置的函数,记录固定至表面的分析物的查询探针事件的时间依赖性信号;按(x, y)位置将事件簇集至局部簇;和计算每个事件簇的动力学参数以表征所述分析物。在一些实施方案中,表面是固体支持物。在一些实施方案中,表面是可扩散的。在一些实施方案中,记录查询探针事件的时间依赖性信号包括以单分子灵敏度测量分析物的信号。在一些实施方案中,方法进一步包括计算差示强度图,其包含表面处作为(x, y)位置的函数的时间依赖性信号强度变化。在一些实施方案中,(x, y)位置以亚像素准确度确定。
在一些实施方案中,簇集的事件代表单分析物分子的结合事件。在一些实施方案中,表征分析物包含指示样品中分析物的存在、不存在、浓度或数量。在一些实施方案中,分析物包含多肽。在一些实施方案中,该方法指示多肽上翻译后修饰的存在或不存在。在一些实施方案中,翻译后修饰介导查询探针与多肽的瞬时缔合。在一些实施方案中,化学亲和标签介导翻译后修饰和查询探针之间的瞬时缔合。在一些实施方案中,化学亲和标签是核酸。在一些实施方案中,分析物是核酸。在一些实施方案中,查询探针与分析物的瞬时缔合通过分析物的共价修饰而可区别地受到影响。在一些实施方案中,查询探针是核酸或适体。在一些实施方案中,查询探针是低亲和力抗体、抗体片段或纳米抗体。在一些实施方案中,查询探针是DNA-结合蛋白、RNA-结合蛋白或DNA-结合核糖核蛋白复合物。
在一些实施方案中,每个查询探针事件的(x, y)位置通过使用形心确定、最小二乘拟合至高斯函数、最小二乘拟合至艾里斑函数、最小二乘拟合至多项式函数(例如,抛物线)或最大似然估计处理差示强度分布图来确定。在一些实施方案中,在表面固定之前分析物在载体的存在下经历热变性。在一些实施方案中,在表面固定之前分析物在载体的存在下经历化学变性,例如,分析物用变性剂例如尿素、甲酰胺、盐酸胍、高离子强度、低离子强度、高pH、低pH或十二烷基硫酸钠(SDS)变性。
进一步的实施方案提供一种用于定量样品中的分析物的系统。例如,在一些实施方案中,系统包含将分析物稳定固定至表面的功能性;以低亲和力结合靶分析物的自由扩散性查询探针;和记录分析物的查询探针事件和查询探针事件的空间位置的检测系统。在一些实施方案中,系统进一步包含根据所述靶分析物的重复结合和解离事件的空间位置和时机鉴定靶分析物的单个分子拷贝的分析程序。在一些实施方案中,查询探针是核酸或适体。在一些实施方案中,查询探针是低亲和力抗体、抗体片段或纳米抗体。在系统的一些实施方案中,查询探针和/或捕获探针是DNA-结合蛋白、RNA-结合蛋白或DNA-结合核糖核蛋白复合物。在一些实施方案中,查询和/或捕获探针是核酸、多肽(例如,抗体、抗体片段、线性抗体、单链抗体或其它抗原-结合抗体衍生物;酶;特异性识别分析物的结合蛋白);在其中分析物包含碳水化合物或多糖的一些实施方案中,查询探针包含碳水化合物-结合蛋白,例如凝集素或碳水化合物-结合抗体。在一些实施方案中,在碳水化合物单体之间特定的糖苷键或糖苷键组的存在产生查询探针结合的可区别模式。在一些实施方案中,捕获探针是兔单克隆抗体;和在一些实施方案中,查询探针是小鼠单克隆抗体。
在一些系统实施方案中,分析物通过稳定结合靶分析物的表面-结合捕获探针,稳定固定至表面。在一些实施方案中,捕获探针是高亲和力抗体、抗体片段或纳米抗体。在一些实施方案中,分析物通过交联靶分析物与表面的共价键,稳定固定至表面。在一些实施方案中,在表面固定之前分析物在载体的存在下经历热变性。在一些实施方案中,在表面固定之前分析物在载体的存在下经历化学变性,例如,分析物用变性剂例如尿素、甲酰胺、盐酸胍、高离子强度、低离子强度、高pH、低pH或十二烷基硫酸钠(SDS)变性。根据本文包含的教导,其它实施方案对相关领域的技术人员而言将是显而易见的。
附图简述
参考以下附图将更好地理解本技术的这些和其它特征、方面和优点:
图1是显示本文描述的技术的方法实施方案的步骤和在开发本文描述的技术的实施方案期间收集的实验数据的示意图。
图2是在本文描述的实验期间收集的数据的信号(“接受的计数”)对比浓度(皮摩尔单位)的曲线图。曲线图指示本文描述的技术的动态范围(实心方块)相对于现有方法(空心圆)改进。
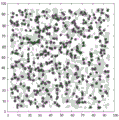
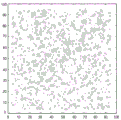
图3A-B显示在仅靶分析物的存在下(图3A)和在干扰性背景分析物的存在下,但在靶分析物的不存在下(图3B),在本文描述的实验期间鉴定的结合事件簇的示意图。图3A显示来自靶分析物的显著阳性信号。由于方法的特异性,在图3B中未检测到靶分析物信号。该实验指示本文描述的技术的实施方案的高特异性。
应当理解,附图不一定按比例绘制,附图中的对象也不一定彼此关联地按比例绘制。附图是意图将清楚和理解带给本文中公开的设备、系统和方法的不同实施方案的描述。在可能时,贯穿附图使用相同的参考数字来指示相同或类似的部分。此外,应当理解,附图无意以任何方式限制本教导的范围。
详细描述
在一些实施方案中,本文提供的技术涉及通过与一种或多种查询探针瞬时(例如,动力学),而非稳定(平衡、热力学)相互作用来检测生物分子分析物。分析物用捕获探针固定在表面上,然后用瞬时结合查询探针检测。该技术在分析物、捕获探针或查询探针方面不受限制。例如,在一些实施方案中,查询探针是抗体、纳米抗体、多肽、寡肽或适体;例如,在一些实施方案中,分析物是核酸、蛋白、肽、脂质、小分子、代谢物或任何分子或化合物。
与现有技术相反,本文描述的技术通过分析探针-靶标相互作用的动力学行为,以任意的精确度区别密切相关的分析物(例如,磷酸化和非磷酸化蛋白靶标)。
在各种的实施方案中,测定条件受到控制,使得使查询探针与靶分析物的相互作用瞬时。例如,在一些实施方案中该技术包含以下一项或多项,以提供其中发生探针和分析物的瞬时相互作用的条件:(1) 工程改造查询探针,使得它与靶标弱相互作用(例如,在纳摩尔亲和力范围);(2) 控制温度,使得查询探针与靶分析物弱相互作用;(3) 控制溶液条件,例如,离子强度、离子组成、添加离液剂、添加竞争探针等,使得查询探针与靶分析物弱相互作用。
在一些实施方案中,该技术包括使用例如光子力和/或超声能量。例如,在一些实施方案中,光子力促进在特定位置中材料(特别是较大颗粒)的浓集。在一些实施方案中,超声促进混合,例如以调节动力学缔合,例如通过增加混合速率超过简单扩散进行。
在一些实施方案中,查询探针与靶分析物的结合通过全内反射荧光显微术或能够单分子灵敏度的另一技术测量。
在各种实施方案的该详细描述中,为了解释的目的,阐述了众多具体细节来提供公开的实施方案的彻底理解。但是,本领域技术人员会明白,可以在有或没有这些具体细节的情况下实践这些各种的实施方案。在其它情况下,以框图形式显示了结构和装置。此外,本领域技术人员可以容易地认识到,呈现和执行所述方法的具体顺序是示例性的,且预见到,所述顺序可以被改变且仍然保留在本文中公开的各种实施方案的精神和范围内。
在本申请中引用的所有文献和类似的材料(包括但不限于,专利、专利申请、文章、书籍、论文和因特网网页)明确地通过引用整体并入用于任意目的。除非另外定义,在本文中使用的所有技术和科学术语具有与本文描述的各个实施方案所属领域的普通技术人员通常理解相同的含义。当在并入的参考文献中的术语的定义看起来不同于在本教导中提供的定义时,以在本教导中提供的定义为准。在本文中使用的章节标题仅仅用于组织目的,不应解释为以任何方式限制所述的主题。
定义
为了便利本技术的理解,在下面定义了许多术语和短语。在整个详细描述中阐述了另外定义。
在整个说明书和权利要求书中,下述术语采用在本文中明确相关的含义,除非上下文另外清楚地指明。本文中使用的短语“在一个实施方案中”不一定是指相同的实施方案,尽管可能如此。此外,本文中使用的短语“在另一个实施方案中”不一定是指不同的实施方案,尽管可能如此。因而,如下所述,可以容易地组合本发明的各种实施方案,而不背离本发明的范围或精神。
另外,如本文中使用的,术语“或”是包含性的“或者” 算符,且等同于术语“和/或”,除非上下文另外清楚地指明。术语“基于”不是排除性的,且允许基于未描述的另外因素,除非上下文另外清楚地指明。另外,在整个说明书中,“一个”、“一种”和“所述”的含义包括复数所指。“在……中”的含义包括“在……中”和“在……上”。
本文中使用的术语“受试者”和“患者”是指任何生物,包括植物、微生物和动物(例如,哺乳动物诸如狗、猫、家畜和人)。
术语“样品”在本说明书和权利要求书中以它的最宽含义使用。在一些实施方案中,样品是或包含动物细胞或组织。在一些实施方案中,样品包括从任何来源获得的样本或培养物(例如,微生物培养物),以及生物和环境样品。生物样品可获自植物或动物(包括人)和包括流体、固体、组织和气体。环境样品包括环境材料,例如表面物质、土壤、水和工业样品。这些实例不应被解释为限制可适用于本发明的技术的样品类型。
本文中使用的“生物样品”是指生物组织或流体的样品。例如,生物样品可以是得自动物(包括人)的样品;流体、固体或组织样品;以及液体和固体食品和饲料产品和成分,诸如乳制品、蔬菜、肉和肉副产品和废物。生物样品可以得自家养动物的所有不同家族,以及未驯服的或野生的动物,包括但不限于,动物诸如有蹄动物、熊、鱼、兔类动物、啮齿类动物等。生物样品的实例包括组织的切片、血液、血液级分、血浆、血清、尿或来自其它周围来源的样品,或细胞培养物、细胞菌落、单个细胞或单个细胞的集合。此外,生物样品包括上述样品的集合或混合物。生物样品可以通过从受试者取出细胞样品来提供,但是也可以通过使用以前分离的样品来提供。例如,通过常规活组织检查技术,可以从疑似具有疾病的受试者取出组织样品。在某些实施方案中,血液样品取自受试者。来自患者的生物样品是指来自疑似受疾病影响的受试者的样品。
环境样品包括环境材料诸如表面物质、土壤、水和工业样品,以及得自食品和乳制品加工仪器、装置、设备、器具、一次用弃的和非一次用弃的物品的样品。这些实例不应解释为限制可适用于本发明的样品类型。
本文使用的术语“标记”是指任何原子、分子、分子复合物(例如,金属螯合物)或胶体颗粒(例如,量子点、纳米颗粒、微粒等),其可用于提供可检测(优选可量化)的效果,和可连接至核酸或蛋白。标记包括但不限于染料(例如,光学可检测的标记、荧光染料或部分等);放射性标记例如32P;结合部分例如生物素;半抗原例如地高辛;发光、磷光、光学可检测或荧光部分;质量标签;和单独或与可通过荧光共振能量转移(FRET)抑制或改变发射光谱的部分组合的荧光染料。标记可以提供可通过荧光、发光、放射性、比色法、重量分析法、X-射线衍射或吸收、磁性、酶活性、质量特征或受质量影响的行为(例如,MALDI飞行时间质谱法;荧光偏振)等检测的信号。标记可以是带电荷的部分(正或负电荷),或者可替换地,可以是电荷中性的。标记可以包括核酸或蛋白序列或由其组成,只要包含所述标记的序列是可检测的。
本文中使用的“支持物”或“固体支持物”是指这样的基质:在其上或内可以固定核酸分子、微粒等,例如,它们可以与其共价地或非共价地连接,或它们可以部分地或完全地包埋在其内或上,使得它们在很大程度上或完全被阻止免于自由扩散或相对于彼此移动。
本文中使用的“部分”是指某物可以分成的两个或更多个部分之一,例如,寡核苷酸、分子、化学基团、结构域、探针等的各个部分。
如本文中使用的,“核酸”或“核酸序列”是指嘧啶和/或嘌呤碱基(优选地分别为胞嘧啶、胸腺嘧啶和尿嘧啶,和腺嘌呤和鸟嘌呤)的聚合物或寡聚体(参见Albert L.Lehninger, Principles of Biochemistry, 在793-800 (Worth Pub. 1982))。本技术预见到任何脱氧核糖核苷酸、核糖核苷酸或肽核酸组分、和它们的任何化学变体,诸如这些碱基的甲基化、羟基甲基化或糖基化形式等。所述聚合物或寡聚体可以在组成上是异源的或同源的,且可以分离自天然存在的来源,或可以人工地或合成地产生。另外,所述核酸可以是DNA或RNA或其混合物,且可以永久地或暂时地以单链或双链形式(包括同源双链体、异源双链体和杂合状态)存在。在某些实施方案中,核酸或核酸序列包含其它种类的核酸结构,例如,DNA/RNA螺旋、肽核酸(PNA)、吗啉代、锁核酸(LNA)和/或核酶。因此,术语“核酸”或“核酸序列”也可以包括这样的链:其包含可以表现出与天然核苷酸相同功能的非天然的核苷酸、修饰的核苷酸和/或非-核苷酸结构单元(例如,“核苷酸类似物”);此外,本文中使用的术语“核酸序列”是指寡核苷酸、核苷酸或多核苷酸、及其片段或部分,且是指基因组或合成起源的DNA或RNA,其可以是单链的或双链的,且表示有义或反义链。
本文中使用的术语“核苷酸类似物”是指修饰的或非天然存在的核苷酸,包括、但不限于:具有改变的堆叠相互作用的类似物诸如7-脱氮杂嘌呤(即,7-脱氮杂-dATP和7-脱氮杂-dGTP);具有替代氢键合构型的碱基类似物(例如,诸如Iso-C和Iso-G和在S. Benner的美国专利号6,001,983(通过引用并入本文)中描述的其它非标准碱基对);非氢键合类似物(例如,非极性的芳族核苷类似物诸如2,4-二氟甲苯,由B. A. Schweitzer和E. T.Kool, J. Org. Chem., 1994, 59, 7238-7242,B. A. Schweitzer和E. T. Kool, J. Am.Chem. Soc., 1995, 117, 1863-1872描述;它们中的每一篇通过引用并入本文);“通用”碱基诸如5-硝基吲哚和3-硝基吡咯;和通用嘌呤和嘧啶(分别诸如“K”和“P”核苷酸;P. Kong,等人, Nucleic Acids Res., 1989, 17, 10373-10383, P. Kong等人, Nucleic AcidsRes., 1992, 20, 5149-5152)。核苷酸类似物包括在糖部分上具有修饰的核苷酸,诸如二脱氧核苷酸和2'-O-甲基核苷酸。核苷酸类似物包括脱氧核糖核苷酸以及核糖核苷酸的修饰形式。
“肽核酸”是指包含肽-样聚酰胺主链的DNA模仿物。
如本文中使用的,术语“互补的”或“互补性”关于通过碱基配对规则关联的多核苷酸(例如,核苷酸诸如寡核苷酸捕获探针、查询探针或作为核酸的靶分析物的序列)使用。例如,序列“5'-A-G-T-3'”是与序列“3'-T-C-A-5'”互补的。互补性可以是“部分的”,其中核酸的碱基的仅一些根据碱基配对规则匹配。或者,在核酸之间可能存在“完全的”或“总的”互补性。核酸链之间的互补性程度对核酸链之间的杂交的效率和强度具有显著影响。这在扩增反应以及依赖于核酸之间的结合的检测方法中是特别重要的。任一个术语也可以参照各个核苷酸使用,特别是在多核苷酸的背景下。例如,可以为在寡核苷酸内的特定核苷酸指出它与另一个核酸链内的核苷酸的互补性或其缺乏,这不同于所述寡核苷酸的其余部分和所述核酸链之间的互补性或与其形成对比。
在某些背景下,术语“互补性”和有关的术语(例如,“互补的”、“互补物”)是指可以通过氢键结合另一个核酸序列的核酸序列的核苷酸,例如,能够碱基配对(例如,通过沃森-克里克碱基配对或其它碱基配对)的核苷酸。可以形成碱基对(例如彼此互补)的核苷酸是这样的配对:胞嘧啶和鸟嘌呤,胸腺嘧啶和腺嘌呤,腺嘌呤和尿嘧啶,和鸟嘌呤和尿嘧啶。不需要在核酸序列的整个长度上计算百分比互补性。互补性的百分比可以限于碱基配对的核酸序列的特定区域,例如,从第一个碱基配对的核苷酸开始并在最后一个碱基配对的核苷酸处结束。本文中使用的核酸序列的互补物是指这样的寡核苷酸:其当与核酸序列比对使得一个序列的5'末端与另一个序列的3'末端配对时处于“反平行的缔合”中。在天然核酸中通常不存在的某些碱基可以被包括在本发明的核酸中,且包括,例如,肌苷和7-脱氮杂鸟嘌呤。互补性不需要是完美的;稳定的双链体可以含有错配的碱基对或未匹配的碱基。核酸技术领域的技术人员经验地考虑许多变量可以确定双链体稳定性,所述变量包括例如寡核苷酸的长度、寡核苷酸的碱基组成和序列、离子强度和错配碱基对的发生率。
因而,在某些实施方案中,“互补的”是指在8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100个或更多个核碱基的区域上与第二个核碱基序列的互补物具有至少60%、65%、70%、75%、80%、85%、90%、95%、97%、98%或99%同一性的第一个核碱基序列,或两个序列在严格杂交条件下杂交。“完全互补的”是指第一个核酸的每个核碱基能够在第二个核酸中的对应位置处与每个核碱基配对。例如,在某些实施方案中,寡核苷酸(其中每个核碱基具有与核酸的互补性)具有这样的核碱基序列:其在8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100个或更多个核碱基的区域上与所述核酸的互补物相同。
“错配”是指不能与在第二个核酸的对应位置处的核碱基配对的第一个核酸的核碱基。
术语“结构域”当关于多肽使用时是指多肽的子部分,其具有独特的结构和/或功能特征;通常,该特征在各种多肽之间类似。子部分通常包含连续的氨基酸,但它也可包含一致起作用的或由于折叠或其它构型而紧密靠近的氨基酸。蛋白结构域的实例包括跨膜结构域、糖基化位点等。
术语“基因”是指包含对于产生RNA或多肽或其前体(例如,胰岛素原)所必需的编码序列的核酸(例如,DNA或RNA)序列。功能性多肽可由全长编码序列或由编码序列的任何部分编码,只要多肽的所需活性或功能性质(例如,酶促活性、配体结合、信号转导等)得到保持。术语“部分”当关于基因使用时是指该基因的片段。片段的大小范围可以是几个核苷酸至整个基因序列减去一个核苷酸。因此,“包含至少基因的一部分的核苷酸”可包含该基因的片段或整个基因。
术语“基因”还包括结构基因的编码区,和包括在5′和3′两端上邻近编码区(在任一端相距约1 kb)的序列,使得基因对应于全长mRNA的长度。位于编码区的5′和存在于mRNA上的序列称为5′非翻译序列。位于编码区的3′或下游和存在于mRNA上的序列称为3′非翻译序列。术语“基因”包括基因的cDNA和基因组两种形式。基因的基因组形式或克隆包含编码区,其被称为“内含子”或“间隔区”或“间隔序列”的非编码序列间断。内含子是被转录为核RNA (hnRNA)的基因段;内含子可包含调节元件,例如增强子。内含子从核或初级转录物除去或“剪接掉”;因此内含子不存在于信使RNA (mRNA)转录物中。mRNA在翻译期间发挥功能以规定在新生多肽中氨基酸的序列或次序。
除了含有内含子之外,基因的基因组形式还可包括位于在RNA转录物上存在的序列的5′和3′两端的序列。这些序列被称为“侧翼”序列或区域(这些侧翼序列位于在mRNA转录物上存在的非翻译序列的5′或3′)。5′侧翼区域可含有调节序列例如启动子和增强子,其控制或影响基因的转录。3′侧翼区域可含有指导转录终止、转录后切割和多腺苷酸化的序列。
术语“野生型”是指这样的基因或基因产物:其当从天然存在的来源分离时具有该基因或基因产物的特征。野生型基因是在群体中最频繁地观察到且因而任意地命名为该基因的“正常”或“野生型”形式的基因。相反,术语“修饰的”、“突变体”或“多态的”是指,当与野生型基因或基因产物相比时,表现出序列和/或功能性质的改变(即,改变的特征)的基因或基因产物。应当指出,可以分离天然存在的突变体;这些通过以下事实来鉴别:当与野生型基因或基因产物相比时,它们具有改变的特征。因此,术语“变体”和“突变体”当关于核苷酸序列使用时是指与另一个通常相关的核苷酸序列有一个或多个核苷酸不同的核酸序列。“变异”是两个不同核苷酸序列之间的差异;在一些实施方案中,一个序列是参考序列。
术语“等位基因”是指在基因中不同的变异;变异包括但不限于变体和突变体、多态性基因座和单核苷酸多态性基因座、移码和剪接突变。等位基因可天然存在于群体中,或它可在群体的任何特定个体的寿命期间产生。
本文中使用的术语“杂交”关于互补核酸的配对使用。杂交和杂交的强度(例如,核酸之间的缔合的强度)受诸如以下因素影响:核酸之间的互补程度,涉及的条件的严格性,和形成的杂合物的Tm。“杂交”方法涉及一个核酸与另一个互补核酸(例如,具有互补核苷酸序列的核酸)的退火。含有互补序列的两种核酸聚合物找到彼此并通过碱基配对相互作用退火的能力是充分公认的现象。Marmur和Lane, Proc. Natl. Acad. Sci. USA 46:453(1960)和Doty等人, Proc. Natl. Acad. Sci. USA 46:461 (1960)对“杂交”过程的最初观察结果以后,已经将该过程细化为现代生物学的基本工具。
本文中使用的术语“Tm”参照“解链温度”使用。解链温度是双链核酸分子的群体变得半解离成单链时的温度。几个用于计算核酸的Tm的方程式是本领域众所周知的。如标准参考文献指出的,可以通过以下方程式计算Tm值的简单估计:Tm = 81.5 + 0.41 * (%G+C)(当核酸是在1 M NaCl的水溶液中时)(参见例如,Anderson和Young, QuantitativeFilter Hybridization, in Nucleic Acid Hybridization (1985)。其它参考文献(例如,Allawi和SantaLucia, Biochemistry 36: 10581-94 (1997)包括更复杂的计算,其考虑结构、环境和序列特征来计算Tm。例如,在某些实施方案中,这些计算会提供关于短核酸探针和靶标(例如,如在实施例中使用的)的Tm的改进估计。
术语“蛋白”和“多肽”是指包含通过肽键连接的氨基酸的化合物,和可互换使用。由基因编码的“蛋白”或“多肽”不受限于由基因编码的氨基酸序列,而是包括蛋白的翻译后修饰。在术语“氨基酸序列”在本文叙述以指蛋白分子的氨基酸序列时,“氨基酸序列”和类似术语例如“多肽”或“蛋白”不意图限制氨基酸序列为与所述蛋白分子相关的完全天然氨基酸序列。此外,“氨基酸序列”可从编码蛋白的核酸序列推断。常规的单字母和三字母氨基酸密码在本文如下使用 – 丙氨酸:Ala,A;精氨酸:Arg,R;天冬酰胺:Asn,N;天冬氨酸:Asp,D;半胱氨酸:Cys,C;谷氨酸:Glu,E;谷氨酰胺:Gln,Q;甘氨酸:Gly,G;组氨酸:His,H;异亮氨酸:Ile,I;亮氨酸:Leu,L;赖氨酸:Lys,K;甲硫氨酸:Met,M;苯丙氨酸:Phe,F;脯氨酸:Pro,P;丝氨酸:Ser,S;苏氨酸:Thr,T;色氨酸:Trp,W;酪氨酸:Tyr,Y;缬氨酸:Val,V。如本文使用的,密码Xaa和X是指任何氨基酸。
术语“变体”和“突变体”在关于多肽使用时是指与另一个通常相关的多肽具有一个或多个氨基酸不同的氨基酸序列。
如本文中使用的,当关于核酸使用时,术语“解链”是指双链核酸或核酸区域解离成单链核酸或核酸区域。
本文中使用的“查询探针”或“读出探针”是识别分析物(例如,结合分析物,例如,特异性地结合分析物)的任何实体(例如,分子、生物分子等)。在示例性实施方案中,所述查询探针是识别分析物的蛋白。在某些其它示例性实施方案中,所述查询探针是识别分析物的核酸(例如,DNA、RNA、包含DNA和RNA的核酸、包含经修饰的碱基和/或经修饰的碱基间连接的核酸;例如,如上所述的核酸,核酸适体)。在某些实施方案中,所述查询探针被例如可检测标记(例如,如本文中所述的荧光部分)标记。在某些实施方案中,所述查询探针包含超过一种类型的分子(例如,蛋白、核酸、化学接头或化学部分中的多于一种)。
如本文使用的,“事件”是指查询探针与分析物结合的情况,或查询探针从分析物解离的情况,例如,通过监测指示查询探针与分析物结合和/或查询探针从分析物解离的可检测性质来测量。
本文中使用的“捕获探针”是识别分析物(例如,结合分析物,例如,特异性地结合分析物)并将分析物连接至固体支持物的任何实体(例如,分子、生物分子等)。在示例性实施方案中,所述捕获探针是识别分析物的蛋白。在某些其它示例性实施方案中,捕获探针是识别分析物的核酸(例如,DNA、RNA、包含DNA和RNA的核酸、包含经修饰的碱基和/或经修饰的碱基间连接的核酸;例如,如上文所述的核酸,核酸适体)。在某些实施方案中,捕获探针被例如可检测标记(例如,如本文中所述的荧光部分)标记。在某些实施方案中,所述捕获探针包含超过一种类型的分子(例如,蛋白、核酸、化学接头或化学部分中的多于一种)。
如本文使用的,术语“灵敏度”是指当样品包含分析物时测定提供分析物的阳性结果的可能性。灵敏度按照真阳性结果的数量除以真阳性和假阴性的总和来计算。灵敏度是测定如何良好地检测分析物的度量。
如本文使用的,术语“特异性”是指当样品不包含分析物时测定提供阴性结果的可能性。特异性按照真阴性结果的数量除以真阴性和假阳性的总和来计算。特异性是本发明的方法如何良好地从确实包含分析物的样品排除不包含分析物的样品的度量。
如本文使用的,“平衡常数” (Keq)、“平衡缔合常数” (Ka)和“缔合结合常数” (或“结合常数”(KB))对于在平衡时A和B的以下结合反应可互换使用:
其中A和B是彼此缔合的两个实体(例如,捕获探针和分析物、查询探针和分析物)和Keq= [AB] / ([A] × [B])。解离常数KD = 1/KB。KD是一种描述一个结合配偶体A对它所缔合的配偶体B的亲和力的有用方式,例如,数值KD代表得到显著量的AB所需的A或B的浓度。Keq= koff / kon;KD = koff / kon。
如本文使用的,彼此缔合的两个实体的产物(例如,根据上文方程式从A和B形成AB)的“显著量”,是指等于或大于A或B的游离浓度(以较小的为准)的AB的浓度。
如本文使用的,“纳摩尔亲和力范围”是指具有在纳摩尔范围的平衡解离常数KD(例如,koff / kon的比率),例如,1 × 10–10至1 × 10–5 M (例如,在一些实施方案中1 ×10–9至1 × 10–6 M)的解离常数(KD)的两个组分的缔合。解离常数具有摩尔单位(M)。解离常数越小,两个组分(例如,捕获探针和分析物;查询探针和分析物)之间的亲和力越高。
如本文使用的,“弱亲和力”或“弱结合”或“弱缔合”是指具有大约100纳摩尔(例如,大约10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、300、400或500纳摩尔)和/或在一些实施方案中1纳摩尔至10微摩尔的范围的KD的缔合。
术语“特异性结合”或“特异性地结合”当关于彼此缔合的两个组分A和B的相互作用使用时是指具有小于A或B与溶液中的其它类似组分(例如,溶液中不是A或B的至少一种其它分子物类)的相互作用的KD的KD的A和B的缔合。
如本文使用的,词语“存在”或“不存在” (或者,“存在的”或“不存在的”)以相对意义用于描述特定实体(例如,分析物)的量或水平。例如,当分析物被认为在样品中“存在”时,它意指该分析物的水平或量高于预定的阈值;相反地,当分析物被认为在样品中“不存在”时,它意指该分析物的水平或量低于预定的阈值。预定的阈值可以是与用于检测分析物的特定测试相关的检测能力的阈值或任何其它阈值。当分析物在样品中被“检出”时,它在样品中“存在”;当分析物“未被检出”时,它在样品中“不存在”。此外,其中分析物被“检出”或其中分析物“存在”的样品是对于分析物为“阳性”的样品。其中分析物“未被检出”或其中分析物“不存在”的样品是对于分析物为“阴性”的样品。
如本文使用的,“增加”或“降低”是指相对于之前测量的变量的值、相对于预建立的值和/或相对于标准对照的值,变量的值的可检测的(例如,测量的)阳性或阴性变化。增加是相对于之前测量的变量的值、预建立的值和/或标准对照的值,优选至少10%、更优选50%、还更优选2倍、甚至更优选至少5倍和最优选至少10倍的正变化。类似地,降低是之前测量的变量的值,预建立的值和/或标准对照的值的优选至少10%、更优选50%、还更优选至少80%和最优选至少90%的负变化。指示数量变化或差异的其它术语,例如“更多”或“更少”,在本文以与上述相同的方式使用。
术语“检测测定”是指用于检测分析物的存在或不存在或分析物的活性或效果或用于检测分析物的变体的存在或不存在的测定。
“系统”表示一组组分(真实或抽象的),其包含其中各组分与整体内的至少一种其它组分相互作用或与整体内的至少一种其它组分相关的整体。
在一些实施方案中,该技术包含抗体组分或部分,例如,抗体或其片段或衍生物。如本文使用的,“抗体”,亦称为“免疫球蛋白” (例如,IgG、IgM、IgA、IgD、IgE),包含彼此通过二硫键连接的两条重链和各自通过二硫键连接重链的两条轻链。抗体的特异性在于抗体的抗原结合位点(或互补位)和抗原决定簇(或表位)之间的结构互补性。抗原结合位点由主要来自高变区或互补决定区(CDR)的残基组成。有时,来自非高变区或框架区的残基影响总体结构域结构和因此结合位点。一些实施方案包含抗体的片段,例如,包含至少一部分免疫球蛋白分子的任何含有蛋白或多肽的分子,例如以允许所述分子和抗原之间的特异性相互作用。免疫球蛋白分子的该部分可包括但不限于重链或轻链的至少一个互补决定区(CDR)或其配体结合部分、重链或轻链可变区、重链或轻链恒定区、框架区或其任何部分。这样的片段可通过酶法裂解、合成或重组技术产生,如本领域已知的和/或如本文所述。抗体也可使用其中一个或多个终止密码子已被引入天然终止位点的上游的抗体基因,以各种截短形式产生。抗体的各个部分可通过常规技术经化学连接在一起,或可使用基因工程改造技术作为连续蛋白制备。
抗体的片段包括但不限于Fab (例如,通过木瓜蛋白酶消化)、F(ab')2 (例如,通过胃蛋白酶消化)、Fab' (例如,通过胃蛋白酶消化和部分还原)和Fv或scFv (例如,通过分子生物学技术)片段。
Fab片段可通过用蛋白酶木瓜蛋白酶处理抗体获得。此外,Fab可通过将编码抗体的Fab的DNA插入用于原核表达系统或用于真核表达系统的载体,和将载体引入原核细胞或真核细胞以表达Fab而产生。F(ab')2可通过用蛋白酶胃蛋白酶处理抗体获得。此外,F(ab')2可通过经硫醚键或二硫键结合Fab'而产生。Fab可通过用还原剂,例如二硫苏糖醇处理F(ab')2而获得。此外,Fab'可通过将编码抗体的Fab'片段的DNA插入原核细胞表达载体或真核细胞表达载体,和将载体引入原核细胞或真核细胞用于其表达而产生。Fv片段可例如,在4℃和pH 4.0下通过胃蛋白酶的限制性裂解产生(称为“冷胃蛋白酶消化”的方法)。Fv片段由通过强非共价相互作用保持在一起的重链可变结构域(VH)和轻链可变结构域(VL)组成。scFv片段可通过按之前所述获得编码VH和VL结构域的cDNA,构建编码scFv的DNA,将DNA插入原核细胞表达载体或真核细胞表达载体,和然后将表达载体引入原核细胞或真核细胞以表达scFv而产生。
一般而言,抗体通常可使用目前本领域众所周知的许多常规技术,对任何抗原产生。
如本文使用的,术语“缀合”是指一个分子或试剂经物理或化学偶联或粘附至另一个分子或试剂的情况。缀合的实例包括共价连接和静电复合。术语“复合”、“与……复合”和“缀合”在本文可互换使用。
如本文使用的,“稳定的相互作用”或提及“稳定结合”相互作用是指在相互作用的热力学平衡条件下相对持久的缔合。在一些实施方案中,“稳定的相互作用”是具有小于大约10–9 M的KD或在一些实施方案中小于10–8 M的KD的两个组分之间的相互作用。在一些实施方案中,“稳定的相互作用”具有小于1/小时的解离速率常数koff或在一些实施方案中小于1/分钟的解离速率常数koff。在一些实施方案中,“稳定的相互作用”被定义为不是“瞬时相互作用”。在一些实施方案中,“稳定的相互作用”包括通过共价键介导的相互作用和通常不是通过KD值来描述,而是涉及按每个相互作用大于大约1分钟(例如,30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、105、110、115、120、125、130、135、140、145、150、155、160、165、170、175或180秒)的两个实体之间的平均缔合寿命的其它相互作用。
在一些实施方案中,“稳定的相互作用”和“瞬时相互作用”之间的区别通过KD和/或koff和/或描述缔合的另一动力学或热力学值的截止值确定,其中截止值用于区别否则如果以KD和/或koff或描述缔合的另一动力学或热力学值的绝对术语描述可能不同表征的稳定和瞬时相互作用。例如,通过KD值表征的“稳定的相互作用”在甚至更稳定的另一相互作用的情况下也可能表征为“瞬时相互作用”。本领域技术人员将理解稳定和瞬时相互作用的其它相对比较,例如,通过KD值表征的“瞬时相互作用”在甚至更瞬时(更不稳定)的另一相互作用的情况下也可能表征为“稳定的相互作用”。
本文中使用的“部分”是指某物可以分成的两个或更多个部分之一,例如,寡核苷酸、分子、化学基团、结构域、探针、“R”基团、多肽等的各个部分。
如本文使用的,在一些实施方案中“信号”是与测定的样品的一种或多种性质(例如,查询探针与分析物的结合和/或查询探针从分析物的解离)有关的时间改变量。信号可以是时域连续的或时域离散的。作为数学抽象概念,连续时间信号的域是实数(或其区间)的集合和离散时间信号的域是整数(或其区间)的集合。离散信号通常通过连续信号的“数字采样”产生。例如,声音信号由在一条线上的连续波动电压组成,其可通过以规律间隔,例如,每50微秒读取该线上的电压水平被数字化。得到的数字串作为离散时间数字信号储存。在一些实施方案中,信号作为空间位置(例如,x, y坐标;例如,x, y, z坐标)的函数记录。在一些实施方案中,信号作为时间的函数记录。在一些实施方案中,信号作为时间和位置的函数记录。
如本文使用的术语“基本上”是一个宽泛术语,和以其普通意义使用,包括但不限于在很大程度上但不必然完全是所指定的事物。
如本文使用的术语“算法”是一个宽泛术语,和以其普通意义使用,包括但不限于涉及将信息从一个状态变换为另一个状态的计算过程(例如,程序),例如使用计算机处理。
描述
尽管本文公开内容提及某些举例说明的实施方案,应当理解,这些实施方案作为示例且不作为限制呈现。
泊松过程
所述技术的实施方案涉及通过记录查询探针与靶分析物结合的特征动力学而进行的单分子识别。在特定实施方案中,该过程是泊松过程。泊松过程是计数事件的数目和在给定的时间间隔中发生事件(例如,可检测地标记的(例如,荧光的)查询探针与固定化的靶分析物的短暂结合)的次数的连续时间随机过程。每对连续事件之间的时间间隔具有指数分布,且每个间隔假定独立于其它间隔。泊松分布是表达在给定时间间隔中发生给定数目的事件的概率的离散概率分布(如果这些事件以已知的平均速率且独立于自最后事件以来的时间发生)。泊松分布还可以用于在其它指定间隔(诸如距离、面积或体积)中的事件的数目。
泊松分布是一般二项式分布的特殊情况,其中试验的数目n是大的,成功的概率p是小的,且乘积np = λ是中等的。在泊松过程中,事件的数目N在任何任意时间t是j的概率遵循泊松概率分布P j (t):
也就是说,直到时间t发生的事件的数目N具有含参数λt的泊松分布。与泊松过程和泊松分布有关的统计和数学方法是本领域已知的。参见,例如,“Stochastic Processes(i): Poisson Processes and Markov Chains”,见Statistics for Biology and Health - Statistical Methods in Bioinformatics (Ewans和Grant, 编), Springer (NewYork, 2001), 第129页以及以后,通过引用整体并入本文。软件包诸如Matlab和R可以用于执行与泊松过程、概率和分布有关的数学和统计方法。
检测的动力学
所述技术的特定实施方案涉及通过分析查询探针与要检测的分析物的相互作用的动力学来检测分析物。关于查询探针Q (例如,在平衡浓度[Q])与靶分析物T (例如,在平衡浓度[T])的相互作用,动力学速率常数k on 描述了复合物QT的时间依赖性形成,所述复合物QT包含与分析物T杂交的探针Q。在特定实施方案中,尽管QT复合物的形成与依赖于查询探针浓度且具有M-1min-1 (等)的单位的二阶速率常数有关,但是QT复合物的形成足以通过k on 来描述,所述k on 是与QT复合物的形成有关的假-一阶速率常数。因而,本文中使用的k on 是表观(“假”)一阶速率常数。
同样地,动力学速率常数k off 描述了复合物QT向探针Q和分析物T的时间依赖性解离。动力学速率通常在本文中以min-1或s-1的单位提供。在结合状态的查询探针Q的“停留时间”(τon)是在查询探针Q结合分析物T以形成QT复合物的每个情况期间,探针Q与分析物T杂交的时间间隔(例如,时间长度)。在未结合状态的查询探针Q的“停留时间”(τoff)是,在查询探针Q结合分析物以形成QT复合物的每个情况之间,探针Q没有与分析物T杂交的时间间隔(例如,时间长度) (例如,在查询探针Q与靶分析物T的连续结合事件之间从靶分析物T解离查询探针Q的时间)。可以将停留时间提供为对众多结合和非结合事件积分的平均值或加权平均值。
此外,在某些实施方案中,将探针(例如,可检测地标记的查询探针(例如,荧光探针)与靶分析物的重复随机结合建模为每单位时间以恒定概率发生的泊松过程,且其中每单位时间的结合和解离事件的数目的标准偏差(Nb+d)增加为(Nb+d)1/2。因而,统计噪音随着观察时间增加变成Nb+d的较小分数。因此,在某些实施方案中根据需要延长观察以实现靶标和脱靶结合之间的区分。并且,随着获取时间增加,在Nb+d直方图中的信号和背景峰变得逐渐分离,且信号分布的宽度随着Nb+d的平方根增加,这与动力学Monte Carlo模拟一致。
此外,在一些实施方案中测定条件经控制以调整动力学行为,以改进查询探针与靶分析物的结合事件和背景结合的区别。例如,在一些实施方案中,该技术包括控制测定条件,例如使用经设计以与靶分析物弱相互作用(例如,在纳摩尔亲和力范围)的查询探针;控制温度,使得查询探针与靶分析物弱相互作用;控制溶液条件,例如,离子强度、离子组成、添加离液剂和添加竞争探针。
分析物
该技术在检测、定量、鉴定或以其它方式表征(例如,存在、不存在、量、浓度、状态)的分析物方面不受限制。如本文使用的术语“分析物”是一个宽泛术语和以其普通意义使用,包括但不限于是指可分析的样品例如生物流体(例如,血液、间质液、脑脊液、淋巴液或尿)中的物质或化学成分。分析物可包括天然存在的物质、人工物质、代谢物和/或反应产物。在一些实施方案中,分析物包含盐、糖、蛋白、脂肪、维生素或激素。在一些实施方案中,分析物天然存在于生物样品中(例如,是“内源的”);例如,在一些实施方案中,分析物是代谢产物、激素、抗原、抗体等。或者,在一些实施方案中,分析物被引入生物有机体中(例如,是“外源的),例如,药物、药物代谢物、药物前体(例如,前药)、用于成像的造影剂、放射性同位素、化学试剂等。药物和药用组合物的代谢产物也是预期分析物。
在一些实施方案中,分析物是多肽、核酸、小分子、脂质、碳水化合物、多糖、脂肪酸、磷脂、糖脂、鞘脂、有机分子、无机分子、辅因子、药物、生物活性剂、细胞、组织、生物体等。在一些实施方案中,分析物包含多肽、核酸、小分子、脂质、碳水化合物、多糖、脂肪酸、磷脂、糖脂、鞘脂、有机分子、无机分子、辅因子、药物、生物活性剂、细胞、组织、生物体等。在一些实施方案中,分析物包含多肽、核酸、小分子、脂质、碳水化合物、多糖、脂肪酸、磷脂、糖脂、鞘脂、有机分子、无机分子、辅因子、药物、生物活性剂、细胞、组织、生物体等的一种或多种的组合。
在一些实施方案中,分析物是多分子复合物的一部分,例如,多蛋白复合物、核酸/蛋白复合物、分子机器、细胞器(例如,无细胞线粒体,例如,在血浆中;质体;高尔基体、内质网、液泡、过氧物酶体、溶酶体和/或细胞核)、细胞、病毒颗粒、组织、生物体或任何大分子复合物或结构或可捕获和适合通过本文描述的技术分析的其它实体(例如,核糖体、剪接体、穹窿(vault)、蛋白酶体、DNA聚合酶III全酶、RNA聚合酶II全酶、对称病毒衣壳、GroEL/GroES;膜蛋白复合物:光系统I、ATP合酶、核小体、中心粒和微管组织中心(MTOC)、细胞骨架、鞭毛、核仁、应激颗粒、生殖细胞颗粒或神经元运输颗粒)。例如,在一些实施方案中,分离多分子复合物和该技术可用于表征、鉴定、定量和/或检测与多分子复合物相关(例如,作为其组分)的一种或多种分子(分析物)。在一些实施方案中,分离细胞外囊泡和该技术可用于表征、鉴定、定量和/或检测与囊泡相关的一种或多种分子(分析物)。在一些实施方案中,该技术可用于表征、鉴定、定量和/或检测囊泡内部存在的蛋白(例如,表面蛋白)和/或分析物,例如,蛋白、核酸或本文所述的其它分析物。在一些实施方案中,在分析前囊泡被固定和渗透。
在一些实施方案中,分析物经化学修饰以提供用于查询探针结合的位点。例如,在一些实施方案中,磷酸丝氨酸和磷酸苏氨酸在强碱性条件下的β-消除用于引入烯烃,接着将亲核试剂例如二硫醇经迈克尔加成至烯烃。然后将剩余的游离硫醇用于缀合至具有与寡核苷酸查询探针互补的序列的含有马来酰亚胺的寡核苷酸。磷酸丝氨酸和磷酸苏氨酸的翻译后修饰然后可使用查询探针探查和分析,如本文所述。
如本文使用的“检测分析物”或“检测物质”将被理解为包括直接检测分析物本身或通过检测其副产物间接检测分析物。
捕获
该技术的实施方案包括捕获分析物。在一些实施方案中,分析物被捕获和固定。在一些实施方案中,分析物被稳定连接至固体支持物。在一些实施方案中,相对于接触固体支持物的主体液相,固体支持物是固定的。在一些实施方案中,在接触固体支持物的主体液相内,固体支持物是可扩散的。
在一些实施方案中,靶分析物与表面或其它固体基质的稳定连接通过高亲和力或不可逆相互作用提供(例如,如本文使用的,“不可逆相互作用”是指具有长于观察时间的解离半衰期的相互作用,例如,在一些实施方案中,所述时间为1-5分钟(例如,60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290、300、310、320、330、340、350、360、370、380、390、400、410、420、430、440、450、460、470、480、490、500、510、520、530、540、550、560、570、580、590或600秒或更长)。该技术在用于捕获分析物的组分和/或方法方面不受限制。例如,稳定连接通过各种方法提供,包括但不限于以下一种或多种。
在一些实施方案中,分析物通过具有对分析物小于大约1纳摩尔(nM) (例如,小于1.5、1.4、1.3、1.2、1.1、1.0、0.9、0.8、0.7、0.6、0.5纳摩尔)的解离常数(KD)和对分析物小于大约1 min–1 (例如,小于大约1.5、1.4、1.3、1.2、1.1、1.0、0.9、0.8、0.7、0.6、0.5 min–1)的解离速率常数的表面结合捕获探针固定。示例性的表面结合捕获探针包括例如抗体、抗体片段、纳米抗体或其它蛋白;高亲和力DNA-结合蛋白或核糖核蛋白复合物例如Cas9、dCas9、Cpf1、转录因子或转录激活物样效应核酸酶(TALEN);寡核苷酸;小有机分子;或金属离子复合物。
在一些实施方案中,分析物通过直接非共价连接至表面(例如,通过分析物和表面例如玻璃表面或尼龙、硝酸纤维素或聚偏二氟乙烯膜之间的相互作用)固定。
在一些实施方案中,分析物通过分析物与固体支持物的化学连接(例如,通过共价键)固定。在一些实施方案中,分析物通过例如碳二亚胺、N-羟基琥珀酰亚胺(NHS)酯、马来酰亚胺、卤代乙酰基、酰肼或烷氧基胺,化学连接至固体支持物。在一些实施方案中,分析物通过靶分析物与表面和/或与连接至表面的捕获探针的辐射(例如,紫外光)-诱导的交联固定。在一些实施方案中,捕获探针是兔单克隆抗体。在其中分析物包含碳水化合物或多糖的一些实施方案中,捕获探针包含碳水化合物-结合蛋白,例如凝集素或碳水化合物-结合抗体。
或者,代替将靶分析物固定至相对于如上所述接触固体支持物的主体相相对静止的固体支持物,一些实施方案提供靶分析物与在接触自由扩散颗粒的主体液相内扩散的自由扩散颗粒缔合。因此,在一些实施方案中,靶分析物共价或非共价结合至自由扩散基质。在一些实施方案中,自由扩散基质是例如胶体颗粒(例如,直径大约10-1000 nm (例如,10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、200、250、300、350、400、450、500、550、600、650、700、750、800、850、900、950或1000 nm)的颗粒)。在一些实施方案中,自由扩散基质包含例如聚苯乙烯、二氧化硅、葡聚糖、金或DNA折纸(origami),和/或由其构成。在一些实施方案中,靶分析物与相对于查询探针的扩散缓慢扩散的自由扩散颗粒缔合,例如,靶分析物的扩散系数为小于查询探针的扩散系数的大约10% (例如,小于15、14、13、12、11、10.5、10.4、10.3、10.2、10.1、10.0、9.9、9.8、9.7、9.6、9.5或9.0%或更少)。
此外,在一些实施方案中靶分析物与自由扩散颗粒缔合,和靶分析物的位置是可观察的和/或可记录的,不依赖于观察和/或记录查询探针结合。例如,在一些实施方案中可检测标记(例如,荧光团、荧光蛋白、量子点)共价或非共价连接至靶分析物,例如,用于检测和定位靶分析物。因此,在一些实施方案中同时和独立地测量靶分析物的位置和查询探针结合事件的位置。
查询
该技术的实施方案包含瞬时和重复结合分析物的查询探针(例如,可检测标记的查询探针),例如,结合靶分析物和与靶分析物解离数次(例如,大于1、2、3、4、5、6、7、8、9、10次或更多次)/观察窗的查询探针。在一些实施方案中,在测定条件下查询探针具有大于大约1纳摩尔(例如,大于0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2.0、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3.0、3.1、3.2、3.3、3.4、3.5、3.6、3.7、3.8、3.9、4.0、4.1、4.2、4.3、4.4、4.5、4.6、4.7、4.8、4.9或5.0或更大纳摩尔)的对于分析物的解离常数(KD)。在一些实施方案中,查询探针具有大于大约1 min–1 (例如,大于0.5、0.6、0.7、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2.0、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3.0、3.1、3.2、3.3、3.4、3.5、3.6、3.7、3.8、3.9、4.0、4.1、4.2、4.3、4.4、4.5、4.6、4.7、4.8、4.9或5.0或更大min–1)的对于分析物的结合和/或解离常数。
该技术在查询探针方面不受限制。在一些实施方案中,查询探针是抗体或抗体片段。在一些实施方案中,查询探针是低亲和力抗体或抗体片段。在一些实施方案中,查询探针是纳米抗体、DNA-结合蛋白或蛋白结构域、甲基化结合结构域(MBD)、激酶、磷酸酶、乙酰化酶、脱乙酰化酶、酶或多肽。在一些实施方案中,查询探针是与靶分析物相互作用的寡核苷酸。例如,在一些实施方案中查询探针是与靶分析物杂交以形成双链体的寡核苷酸,所述双链体具有在进行观察的温度的大约10℃内的解链温度(例如,对于在室温下进行的观察,大约7-12个核苷酸)。在一些实施方案中,查询探针是单核苷酸。在一些实施方案中,查询探针是小有机分子(例如,分子量小于大约2000道尔顿,例如小于2100、2050、2000、1950、1900、1850、1800、1750、1700、1650、1600、1550、1500道尔顿或更小的分子)。在一些实施方案中,查询探针是药剂,例如药物或其它生物活性分子。在一些实施方案中,查询探针是金属离子复合物。在一些实施方案中,查询探针是甲基-结合结构域(例如,MBD1)。在一些实施方案中,查询探针用本文所述的可检测标记进行标记。在一些实施方案中,查询探针共价连接至可检测标记。在一些实施方案中,查询探针与可检测标记间接和/或非共价连接和/或缔合。在一些实施方案中,可检测标记是荧光的。
在一些实施方案中,查询探针是小鼠单克隆抗体。
在其中分析物包含碳水化合物或多糖的一些实施方案中,查询探针包含碳水化合物-结合蛋白,例如凝集素或碳水化合物-结合抗体。
检测
该技术例如在类似分析物的存在下,和在一些实施方案中在背景噪声的存在下,提供靶分析物的检测。在一些实施方案中,来源于查询探针与靶分析物的瞬时结合的信号可与由未结合查询探针产生的信号区分(例如,通过观察、监测和/或记录在结合事件期间信号强度的局部变化)。在一些实施方案中,观察查询探针(例如,荧光标记的查询探针)与靶分析物的瞬时结合通过技术例如全内反射荧光(TIRF)或近-TIRF显微术、零模式波导(ZMW)、光片显微术、受激发射损耗(STED)显微术或共焦显微术提供。在一些实施方案中,本文提供的技术使用具有当未结合靶分析物时被淬灭的荧光发射和/或当结合靶分析物时被去淬灭的荧光发射的查询探针。
该技术包括在观察的面积的离散区域和/或体积的离散区域内,例如在平面或体积的特定空间坐标处,定位和/或观察查询探针与分析物的瞬时结合。在一些实施方案中,相对于固定(例如,表面结合)的靶分析物之间的平均间距,在确定结合或解离事件的空间坐标方面的误差(例如,由于有限的信号、检测器噪声或检测器中的空间分箱导致)小(例如,最小化、消除)。在包含使用宽视野荧光显微术的一些实施方案中,通过在样本平面中使用不大于固定(例如,表面结合)的靶分析物之间的平均距离的有效检测器像素尺寸和每个检测时间点收集许多荧光光子(在一些实施方案中,超过100个,例如超过80、85、90、95、100、105、110、115、120、125或130或更多个),最小化和/或消除测量误差。
在某些实施方案中,当它接近固体支持物的表面(例如,在固体支持物的表面的约100 nm内)时,所述可检测的(例如,荧光的)查询探针会产生荧光发射信号。当未结合的查询探针快速地扩散且因而不可单独地检测时;因此,当处于未结合状态时,所述查询探针产生低水平的扩散背景荧光。结果,在某些实施方案中,结合的查询探针的检测包含使用全内反射荧光显微术(TIRF)、HiLo显微术(参见,例如,US20090084980、EP2300983 B1、WO2014018584 A1、WO2014018584 A1,通过引用并入本文)、共焦扫描显微术或包含照明方案的其它技术,所述照明方案仅照亮(例如,激发)在固体支持物表面附近或上面的那些查询探针分子。因而,在某些实施方案中,仅与表面附近或上面的固定化靶标结合的查询探针会产生点样发射信号(例如,“斑点”),其可以证实为源自单个分子。
在某些实施方案中,所述查询探针包含具有发射波长的荧光标记。在荧光标记的发射波长处的荧光发射的检测指示,所述查询探针结合至固定化的靶分析物。所述查询探针与靶分析物的结合是“结合事件”。在所述技术的某些实施方案中,结合事件具有这样的荧光发射:其具有大于限定的阈值的测量强度。例如,在某些实施方案中,结合事件具有高于背景荧光强度(例如,在没有靶分析物存在下观察到的荧光强度)的荧光强度。在某些实施方案中,结合事件具有比背景荧光强度(例如,在没有靶分析物存在下观察到的荧光强度)高至少1、2、3、4个或更多个标准偏差的荧光强度。在某些实施方案中,结合事件具有比背景荧光强度(例如,在没有靶分析物存在下观察到的荧光强度)高至少2个标准偏差的荧光强度。在某些实施方案中,结合事件具有是背景荧光强度(例如,在没有靶分析物存在下观察到的平均荧光强度)的至少1.5、2、3、4或5倍的荧光强度。
因此,在某些实施方案中,在具有高于限定的阈值(例如,比背景强度高至少2个标准偏差)的强度的查询探针的发射波长处检出荧光指示,结合事件已经发生(例如,在靶分析物所固定化的固体支持物上的离散位置)。此外,在某些实施方案中,在具有高于限定的阈值(例如,比背景强度高至少2个标准偏差)的强度的查询探针的发射波长处检出荧光指示,结合事件已经开始。因此,在某些实施方案中,在具有高于限定的阈值(例如,比背景强度高至少2个标准偏差)的强度的查询探针的发射波长处检出荧光的缺失指示,结合事件已经结束(例如,所述查询探针已经从靶分析物解离)。当结合事件开始时和当结合事件结束时之间的时间长度(例如,在具有高于限定的阈值(例如,比背景强度高至少2个标准偏差)的强度的荧光探针的发射波长处检出荧光的时间长度)是结合事件的停留时间。“转换”是指查询探针与靶分析物的结合和解离(例如,开/关事件),例如,查询探针从结合状态解离或查询探针从未结合状态与靶分析物缔合。
根据所述技术的方法包含在是“获取时间”的确定的时间间隔(例如,几十至几百至几千秒的时间间隔,例如,5、10、15、20、25、30、35、40、45、50、55或60秒;例如,5、10、15、20、25、30、35、40、45、50、55或0分钟;例如,1、1.5、2、2.5或3小时)期间,计数在固体支持物上的每个离散位置处(例如,在通过x, y坐标鉴定的位置处)发生的查询探针结合事件的数目。在某些实施方案中,所述获取时间是大约1-10秒至1-10分钟(例如,大约1-100秒,例如,1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、40、50、60、70、80、90或100秒,例如,1-100分钟,例如,1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、30、40、50、60、70、80、90或100分钟)。
此外,查询探针在结合事件期间保持结合至靶分析物的时间长度是结合事件的“停留时间”。在获取时间期间检测到的结合事件的数目和/或为结合事件记录的停留时间的长度是与靶分析物结合的查询探针的特征,且因而提供以下指示:所述靶分析物被固定化在所述离散位置,且因而所述靶分析物存在于样品中。
在确定的时间间隔期间(例如,在获取时间期间)监测(例如,使用光源来激发荧光探针并检测来自结合的查询探针的荧光发射,例如,使用荧光显微镜)和/或记录查询探针与固定化的靶分析物的结合和/或查询探针从固定化的靶分析物的解离。确定在获取时间期间查询探针结合核酸的次数和/或在每个结合事件中查询探针保持结合至核酸的时间长度和在每个结合事件之间查询探针保持未结合至核酸的时间长度(例如,分别在结合和未结合状态的“停留时间”),例如,通过使用计算机和软件(例如,使用隐马尔科夫模型和泊松统计学分析数据)。
在某些实施方案中,测量阳性和/或阴性对照样品(例如,已知包含或不包含靶标的对照样品)。在阴性对照样品中检测到的荧光是“背景荧光”或“背景(荧光)强度”或“基线”。
在某些实施方案中,将包含在查询探针的发射波长处的荧光强度的测量结果的数据记录为时间的函数。在某些实施方案中,从所述数据确定(例如,通过确定荧光强度高于阈值背景荧光强度的次数和时间长度)结合事件的数目和结合事件的停留时间(例如对于每种固定化的分析物)。在某些实施方案中,为靶分析物所固定化的固体支持物上的每个离散位置计数转换(例如,查询探针的结合和解离)。在某些实施方案中,使用转换的阈值数目将靶分析物在固体支持物上的离散位置的存在与背景信号、非靶分析物和/或查询探针的假结合区分开。
在某些实施方案中,确定每个固定化的靶标的转换次数的分布- 例如,为观察的每个固定化的分析物计数转换数目。在某些实施方案中,产生直方图。在某些实施方案中,确定分布的特征参数,例如,确定分布的平均值、中值、峰、形状等。在某些实施方案中,通过识别数据中的模式和规律的算法来分析数据和/或参数(例如,荧光数据(例如,在时域中的荧光数据)、动力学数据、分布的特征参数等),例如,使用人工智能、模式识别、机器学习、统计推论、神经网等。在某些实施方案中,所述分析包含频率分析的应用,且在某些实施方案中,所述分析包含贝叶斯分析的应用。在某些实施方案中,使用已知的“训练”数据(例如,使用监督学习)训练模式识别系统,且在某些实施方案中,使用算法来发现以前未知的模式(例如,无监督学习)。参见,例如,Duda等人(2001) Pattern classification (第2版),Wiley,New York; Bishop (2006) Pattern Recognition and Machine Learning,Springer。
模式识别(例如,使用训练集、监督学习、无监督学习和未知样品的分析)将鉴别的模式与分析物关联,使得特定模式会提供可用于检测、定量和鉴别分析物的特定分析物的“指纹”。
在某些实施方案中,从靶分析物产生的分布显著不同于从非靶分析物产生的分布或在没有靶分析物存在下产生的分布。在某些实施方案中,为多个固定化的靶分析物确定转换的平均数目。在某些实施方案中,将对包含靶分析物的样品观察到的转换的平均数目近似线性相关为时间的函数,且具有正斜率(例如,转换的平均数目作为时间的函数大约线性地增加)。
在某些实施方案中,使用统计学(例如,泊松统计学)处理数据以确定在固体支持物上的每个离散位置处作为时间的函数发生的转换的概率。在某些特定实施方案中,在固体支持物上的离散位置处作为时间的函数发生的转换事件的相对恒定的概率指示靶分析物在固体支持物上的所述离散位置处的存在。在某些实施方案中,从在固体支持物上的离散位置处作为时间的函数发生的转换事件的概率计算与事件数目和消逝时间有关的相关系数。在某些实施方案中,当从在固体支持物上的离散位置处作为时间的函数发生的转换事件的概率计算时大于0.95的与事件数目和消逝时间有关的相关系数指示靶分析物在固体支持物上的所述离散位置处的存在。
在某些实施方案中,使用结合的查询探针(τon)和未结合的查询探针(τoff)的停留时间来鉴别靶分析物在样品中的存在和/或将包含靶分析物的样品与包含非靶分析物和/或不包含靶分析物的样品区分开。例如,靶分析物的τon大于非靶分析物的τon;并且,靶分析物的τoff小于非靶分析物的τoff。在某些实施方案中,测量阴性对照和样品的τon和τoff指示靶分析物在样品中的存在或不存在。在某些实施方案中,为在固体支持物上成像的多个斑点中的每一个,例如,为对照(例如,阳性和/或阴性对照)和疑似包含靶分析物的样品,确定多个τon和τoff值。在某些实施方案中,为在固体支持物上成像的多个斑点中的每一个,例如,为对照(例如,阳性和/或阴性对照)和疑似包含靶分析物的样品,确定平均τon和/或τoff。在某些实施方案中,所有成像的斑点的τon相对于τoff (例如,平均τon和τoff,按时间平均的τon和τoff,等)的曲线图指示靶分析物在样品中的存在或不存在。
荧光部分
在某些实施方案中,查询探针和/或分析物包含荧光部分(例如,发荧光的染料,也被称作“荧光团”或“fluor”)。多种荧光部分是本领域已知的,且已知将荧光部分连接至分析物和/或查询探针的方法。
可以用作荧光部分的化合物的实例包括但不限于呫吨、蒽、花青、卟啉和香豆素染料。与本技术一起使用的呫吨染料的实例包括但不限于荧光素、6-羧基荧光素(6-FAM)、5-羧基荧光素(5-FAM)、5-或6-羧基-4,7,2',7'- 四氯荧光素(TET)、5-或6-羧基-4'5'2'4'5'7' 六氯荧光素(HEX)、5'或6'-羧基-4',5'-二氯-2,'7'-二甲氧基荧光素(JOE)、5-羧基-2',4',5',7'-四氯荧光素(ZOE)、rhodol、罗丹明、四甲基罗丹明(TAMRA)、4,7-二氯四甲基罗丹明(DTAMRA)、罗丹明X (ROX)和德克萨斯红。可以与本发明一起使用的花青染料的实例包括、但不限于Cy 3、Cy 3B、Cy 3.5、Cy 5、Cy 5.5、Cy 7和Cy 7.5。与本技术一起使用的其它荧光部分和/或染料包括、但不限于能量转移染料、复合染料和产生荧光信号的其它芳族化合物。在某些实施方案中,所述荧光部分包含量子点。
在某些实施方案中,所述荧光部分包含荧光蛋白(例如,绿色荧光蛋白(GFP)、经修饰的GFP的衍生物(例如,包含S65T的GFP、增强的GFP (例如,包含F64L))、或本领域已知的其它荧光蛋白,例如,蓝色荧光蛋白(例如,EBFP、EBFP2、蓝铜矿、mKalama1)、蓝绿色荧光蛋白(例如,ECFP、Cerulean、CyPet、mTurquoise2)和黄色荧光蛋白衍生物(例如,YFP、Citrine、Venus、YPet)。实施方案提供,所述荧光蛋白可以共价地或非共价地键合至一种或多种查询探针、分析物和/或捕获探针。
荧光染料包括但不限于:d-罗丹明受体染料,包括Cy 5、二氯[R110]、二氯[R6G]、二氯[TAMRA]、二氯[ROX]等,荧光素供体染料,包括荧光素、6-FAM、5-FAM等;吖啶,包括吖啶橙、吖啶黄、二氨基吖啶、pH 7等;芳烃,包括2-甲基苯并噁唑、对-二甲基氨基苯甲酸乙酯、苯酚、吡咯、苯、甲苯等;芳基次甲基染料,包括金胺O、结晶紫、结晶紫、甘油、孔雀石绿等;香豆素染料,包括7-甲氧基香豆素-4-乙酸、香豆素1、香豆素30、香豆素314、香豆素343、香豆素6等;花青染料,包括1,1'-二乙基-2,2'-花青碘化物、隐花青、吲哚羰花青(C3)染料、吲哚二羰花青(C5)染料、吲哚三羰花青(C7)染料、氧杂羰花青(C3)染料、氧杂二羰花青(C5)染料、氧杂三羰花青(C7)染料、碘化频那氰醇、Stains all、硫杂羰花青(C3)染料、乙醇、硫杂羰花青(C3)染料、正丙醇、硫杂二羰花青(C5)染料、硫杂三羰花青(C7)染料等;二吡咯甲烯染料,包括N,N'-二氟硼基-1,9-二甲基-5-(4-碘苯基)-二吡咯甲烯、N,N'-二氟硼基-1,9-二甲基-5-[(4-(2-三甲基甲硅烷基乙炔基)、N,N'-二氟硼基-1,9-二甲基-5-苯基二吡咯甲烯等;部花青,包括4-(二氰基亚甲基)-2-甲基-6-(对二甲基氨基苯乙烯基)-4H-吡喃(DCM)、乙腈、4-(二氰基亚甲基)-2-甲基-6-(对二甲基氨基苯乙烯基)-4H-吡喃(DCM)、甲醇、4-二甲基氨基-4'-硝基均二苯乙烯、部花青540等;各种染料,包括4',6-二脒基-2-苯基吲哚(DAPI)、二甲基亚砜、7-苄基氨基-4-硝基苯并-2-氧杂-1,3-二唑、丹磺酰基甘氨酸、丹磺酰基甘氨酸、二氧杂环己烷、Hoechst 33258、DMF、Hoechst 33258、萤光黄CH、吡罗昔康、硫酸奎宁、硫酸奎宁、方酸菁染料III等;亚苯基寡聚物(Oligophenylenes),包括2,5-二苯基噁唑(PPO)、联苯、POPOP、对四联苯、对三联苯等;噁嗪,包括高氯酸甲酚紫、尼罗蓝、甲醇、尼罗红、乙醇、噁嗪1、噁嗪170等;多环芳烃,包括9,10-双(苯基乙炔基)蒽、9,10-二苯基蒽、蒽、萘、苝、芘等;多烯/多炔,包括1,2-二苯基乙炔、1,4-二苯基丁二烯、1,4-二苯基丁二炔、1,6-二苯基己三烯、β-胡萝卜素、均二苯乙烯等;氧化还原活性生色团,包括蒽醌、偶氮苯、苯并醌、二茂铁、核黄素、三(2,2'-二吡啶基钌(II)、四吡咯、胆红素、叶绿素a、乙醚、叶绿素a、甲醇、叶绿素b、二质子化的四苯基卟啉、高铁血红素、八乙基卟啉镁、八乙基卟啉镁(MgOEP)、酞菁镁(MgPc)、PrOH、酞菁镁(MgPc)、吡啶、四间三甲基苯基卟啉镁(MgTMP)、四苯基卟啉镁(MgTPP)、八乙基卟啉、酞菁(Pc)、卟吩、ROX、TAMRA、四叔丁基氮杂卟吩、四叔丁基萘酞菁、四(2,6-二氯苯基)卟啉、四(邻-氨基苯基)卟啉、四间三甲基苯基卟啉(TMP)、四苯基卟啉(TPP)、维生素B12、八乙基卟啉锌(ZnOEP)、酞菁锌(ZnPc)、吡啶、四间三甲基苯基卟啉锌(ZnTMP)、四间三甲基苯基卟啉锌自由基阳离子、四苯基卟啉锌(ZnTPP)等;呫吨,包括曙红Y、荧光素、碱性乙醇、荧光素、乙醇、罗丹明123、罗丹明6G、罗丹明B、玫瑰红、磺酰罗丹明101等;或它们的混合物或组合或它们的合成衍生物。
已知对于本技术的特定实施方案而言适当的几类发荧光的染料和具体化合物:呫吨衍生物诸如荧光素、罗丹明、俄勒冈绿、曙红和德克萨斯红;花青衍生物诸如花青、吲哚羰花青、氧杂羰花青、硫杂羰花青和部花青;萘衍生物(丹磺酰基和氟硅酸钠(prodan)衍生物);香豆素衍生物;噁二唑衍生物诸如吡啶基噁唑、硝基苯并噁二唑和苯并噁二唑;芘衍生物诸如级联蓝(cascade blue);噁嗪衍生物诸如尼罗红、尼罗蓝、甲酚紫和噁嗪170;吖啶衍生物诸如二氨基吖啶、吖啶橙和吖啶黄;芳基次甲基衍生物诸如金胺、结晶紫和孔雀石绿;和四吡咯衍生物诸如卟吩、酞菁、胆红素。在某些实施方案中,染料的荧光部分是呫吨、荧光素、罗丹明、BODIPY、花青、香豆素、芘、酞菁、藻胆蛋白、ALEXA FLUOR®350、ALEXA FLUOR®405、ALEXA FLUOR®430、ALEXA FLUOR®488、ALEXA FLUOR®514、ALEXA FLUOR®532、ALEXAFLUOR®546、ALEXA FLUOR®555、ALEXA FLUOR®568、ALEXA FLUOR®568、ALEXA FLUOR®594、ALEXA FLUOR®610、ALEXA FLUOR®633、ALEXA FLUOR®647、ALEXA FLUOR®660、ALEXAFLUOR®680、ALEXA FLUOR®700、ALEXA FLUOR®750或方酸菁染料。在某些实施方案中,所述标记是在例如以下文献中描述的荧光可检测的部分:Haugland (2005年9月) MOLECULARPROBES HANDBOOK OF FLUORESCENT PROBES AND RESEARCH CHEMICALS (第10版),其通过引用整体并入本文。
在某些实施方案中,所述标记(例如,荧光可检测的标记)是可得自ATTO-TEC GmbH(Am Eichenhang 50,57076 Siegen,德国)的标记,例如,如在以下文献中所述:美国专利申请公开号20110223677、20110190486、20110172420、20060179585和20030003486;和美国专利号7,935,822,它们都通过引用并入本文(例如,ATTO 390、ATTO 425、ATTO 465、ATTO488、ATTO 495、ATTO 514、ATTO 520、ATTO 532、ATTO Rho6G、ATTO 542、ATTO 550、ATTO565、ATTO Rho3B、ATTO Rho11、ATTO Rho12、ATTO Thio12、ATTO Rho101、ATTO 590、ATTO594、ATTO Rho13、ATTO 610、ATTO 620、ATTO Rho14、ATTO 633、ATTO 647、ATTO 647N、ATTO655、ATTO Oxa12、ATTO 665、ATTO 680、ATTO 700、ATTO 725、ATTO740)。
本领域普通技术人员会认识到,同样可以使用具有在这些范围以外的发射极值的染料。在某些情况下,在500 nm至700 nm范围内的染料具有在可见光谱中的优点,且可以使用现有的光电倍增管检测。在某些实施方案中,可利用的染料的宽范围允许选择染料集合,其具有跨检测范围分布的发射波长。能够区分许多染料的检测系统是本领域已知的。
方法
一些实施方案提供通过重复的查询探针结合鉴定分析物的方法。在一些实施方案中,方法包括固定分析物至固体支持物。在一些实施方案中,固体支持物是表面(例如,基本上平坦的表面、圆形表面),例如,与主体溶液(例如,包含分析物的主体溶液)接触的表面。在一些实施方案中,固体支持物是自由可扩散的固体支持物(例如,珠、胶体颗粒,例如,直径大约10-1000 nm (例如,10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、200、250、300、350、400、450、500、550、600、650、700、750、800、850、900、950或1000 nm)的胶体颗粒),例如,在主体溶液(例如,包含分析物的主体溶液)内自由扩散的固体支持物。在一些实施方案中,固定分析物至固体支持物包括固体支持物和分析物之间的共价相互作用。在一些实施方案中,固定分析物至固体支持物包括固体支持物和分析物之间的非共价相互作用。在一些实施方案中,分析物(例如,分子,例如分子,例如,蛋白、肽、核酸、小分子、脂质、代谢物、药物等)被稳定固定至表面,和方法包括查询探针与靶分析物的重复(例如,瞬时、低亲和力)结合。在一些实施方案中,方法包括检测查询探针与靶分析物的重复(例如,瞬时、低亲和力)结合。在一些实施方案中,方法包括产生包含由查询探针与分析物结合产生的信号的数据集(例如,查询探针信号作为时间的函数的数据集)和描述表面上查询探针与分析物结合的空间位置的信息(例如,坐标,例如,x, y坐标)。在一些实施方案中,处理(例如,操纵、转换、可视化等)数据集,例如,以改进查询探针结合事件的空间分辨率。例如,在特定的实施方案中,数据集(例如,包含作为时间的函数的查询探针信号和描述表面上查询探针与分析物结合的空间位置的信息(例如,坐标,例如,x, y坐标))经过处理。在一些实施方案中,处理包含逐帧减法处理以产生差示强度分布图,其显示时间序列数据的每一帧内的查询探针结合或解离事件。在开发本文描述的技术期间收集的数据指示差示强度分布图具有比查询探针结合信号对比位置图更高的分辨率。在一些实施方案中,在确定每个查询探针结合和/或解离事件的空间位置(例如,x, y坐标)后,多个事件根据空间位置被簇集,和每个簇内事件的动力学经历统计学分析以确定事件簇是否源自给定的靶分析物。
例如,用于定量一种或多种表面-固定或扩散性靶分析物的方法的一些实施方案包含一个或多个步骤,其包括例如以单分子灵敏度测量一种或多种瞬时结合查询探针与固定靶分析物的信号。在一些实施方案中,方法包括不依赖于查询探针结合,跟踪靶分析物(例如,检测和/或记录其位置)。在一些实施方案中,方法进一步包括计算在表面处作为位置(例如,x, y位置)的函数的时间依赖性探针结合信号强度变化。在一些实施方案中,计算在表面处作为位置(例如,x, y位置)的函数的时间依赖性查询探针结合信号强度变化产生对于查询探针与分析物结合的“差示强度分布图”。在一些实施方案中,方法包括用亚像素准确度从差示强度分布图确定每个查询探针结合和解离事件(“事件”)的位置(例如,x, y位置)。在一些实施方案中,方法包括按表面上的位置(例如,x, y位置)将事件分组为局部簇,例如,以针对单个固定靶分析物关联事件。在一些实施方案中,方法包括从每个事件局部簇计算动力学参数以确定该簇是否源自特定的分析物,例如,源自与特定分析物的瞬时探针结合。
方法的实施方案在检测的分析物方面不受限制。例如,在一些实施方案中分析物是多肽,例如,蛋白或肽。在一些实施方案中,靶分析物是核酸。在一些实施方案中,靶分析物是小分子。
在一些实施方案中,靶分析物和查询探针之间的相互作用可区别地受到靶分析物的共价修饰的影响。例如,在一些实施方案中,分析物是包含翻译后修饰的多肽,例如,包含翻译后修饰的蛋白或肽。在一些实施方案中,多肽的翻译后修饰影响查询探针与分析物的瞬时结合,例如,查询探针信号是多肽上翻译后修饰的存在或不存在的函数。例如,在一些实施方案中,分析物是包含外遗传修饰的核酸,例如,包含甲基化碱基的核酸。在一些实施方案中,分析物是包含对靶分析物的核碱基、核糖或脱氧核糖部分的共价修饰的核酸。
在一些实施方案中,核酸的修饰影响查询探针与分析物的瞬时结合,例如,查询探针信号是核酸上修饰的存在或不存在的函数。
在一些实施方案中,翻译后修饰和查询探针之间的瞬时相互作用由化学亲和标签,例如,包含核酸的化学亲和标签介导。
在一些实施方案中,查询探针是核酸或适体。
在一些实施方案中,查询探针是低亲和力抗体、抗体片段或纳米抗体。
在一些实施方案中,查询探针是DNA-结合蛋白、RNA-结合蛋白或DNA-结合核糖核蛋白复合物。
在一些实施方案中,每个结合或解离事件的位置,例如,(x,y)位置,通过使差示强度分布图经历形心确定、最小二乘拟合至高斯函数、最小二乘拟合至艾里斑函数、最小二乘拟合至多项式函数(例如,抛物线)或最大似然估计来确定。
在一些实施方案中,捕获探针是高亲和力抗体、抗体片段或纳米抗体。在一些实施方案中,捕获探针是核酸。在一些实施方案中,捕获由交联靶分析物与表面的共价键介导。在一些实施方案中,在表面固定之前,靶分析物在载体的存在下经历热变性。在一些实施方案中,在表面固定之前,分析物在载体的存在下经历化学变性,例如,分析物用变性剂例如尿素、甲酰胺、盐酸胍、高离子强度、低离子强度、高pH、低pH或十二烷基硫酸钠(SDS)变性。
超分辨率成像
该技术提供基于通过查询探针与分析物的瞬时结合产生的信号向提供涉及分析物的鉴定、检测、定量和/或表征的信息的数据中的转化,超分辨率鉴定、检测、定量和/或表征分析物。一些实施方案包含如本文所述的一个或多个步骤,例如,如本文所述的一个或多个有序步骤。在一些实施方案中,一个或多个步骤取决于和跟随一个或多个其它步骤;然而,一些实施方案包含一个或多个所述步骤,不论任何特定次序。
如本文使用的,术语“数据集”或“影片”涉及包含时间序列的传感器阵列数据(例如,来自CCD、增强CCD、电子倍增CCD、CMOS传感器等)的数据,其中时间序列的传感器阵列数据的每个时间点(或“帧”)包含一组信号强度值,其作为传感器阵列内的位置(例如,x, y坐标)的函数。在一些实施方案中,(x, y)位置是指在二维传感器阵列内,例如,在影片数据集的帧中,在水平(x)和垂直(y)方向的传感器元件(例如,像素)的坐标。
在一些实施方案中,所述的数据集从包含查询探针的样品收集(例如,一些实施方案包含从包含查询探针的样品收集数据集)。在一些实施方案中,样品包含分析物。在一些实施方案中,认为样品包含分析物。在一些实施方案中,不知道样品是否包含分析物。
在一些实施方案中,数据集的一个或多个帧被校正,例如,对于成像表面相对于传感器的横向漂移,这导致成像表面的表观(x, y)移动(例如,一些实施方案任选地包含校正成像表面相对于传感器的漂移)。例如,大多数光学显微镜显示镜台漂移,这导致在获得影片期间投射的图像移动(例如,数纳米至数微米),导致物体的表观移动,所述物体实际上相对于成像表面是静止的(例如,影片的一个或多个帧与影片的一个或多个其它帧没有配准)。在一些实施方案中,当数据集未校正时,该技术的分辨率降低,这通过加宽与单一固定靶分析物的查询探针结合事件的表观(x, y)位置的分布,使随后的簇集操作更具挑战性。在一些实施方案中,用于漂移校正的方法包括但不限于,例如,使用独立测量其位置的基准标记(例如,使用用于检测查询探针结合的相同传感器和/或使用不用于检测查询探针结合的其它独立的传感器)。在一些实施方案中,随时间跟踪一个或多个基准标记的位置以确定在每个影片帧中(x, y)漂移的程度和方向。在一些实施方案中,分析影片的每个帧N以确定(x, y)偏移量,其提供帧N的像素强度值与帧1 (影片的第一个帧)的强度值的最大关联。
一些实施方案包含产生差示强度图影片。例如,一些实施方案包含从在影片的下一帧N+1中相同像素P的相应强度值减去在影片的每一帧N中每个像素P的强度值。这些减法的结果是时间序列的差示强度图,其与初始影片相比包含少一个帧。一些实施方案包含从在影片的帧N+2、N+3、N+4、N+n中相同像素P的相应强度值减去在影片的每一帧N中每个像素P的强度值,以产生时间序列的差示强度图,其与初始影片相比包含少2、3、4或n个帧。
一些实施方案包含记录在差示强度图的每个帧内每个强度最大值(例如,对应于查询探针结合事件)的位置、强度和/或帧数量的一个或多个。在一些实施方案中,通过转化数据确定位置,所述转化包括例如二维高斯拟合、形心拟合或用于确定粒子的位置的其它方法,例如,在一些实施方案中误差为1个像素或更小。
一些实施方案包含记录在差示强度图的每个帧内每个强度最小值(例如,对应于查询探针解离事件)的位置、强度(例如,强度绝对值)和/或帧数量的一个或多个。在一些实施方案中,通过转化数据确定位置,所述转化包括例如二维高斯拟合、形心拟合或用于确定粒子的位置的其它方法,例如,在一些实施方案中误差为1个像素或更小。
一些实施方案任选地包含将步骤中计算的漂移校正应用于从差示强度图确定的(x, y)位置系列(例如,一些实施方案包含对于横向漂移校正从差示强度图确定的(x, y)位置系列,例如,如上所述)。
一些实施方案包含组合强度最大值和/或强度最小值的(x, y)位置。一些实施方案进一步包含在强度最大值和/或强度最小值的(x, y)位置上进行簇集分析(例如,分层簇集)以鉴定查询探针结合和解离事件的高密度区域。在一些实施方案中,簇集分析产生簇,其中每个簇含有1个或多个结合和/或解离事件,其在传感器的有限区域内检出。
在一些实施方案中,任选地,如果在每个簇内在差示强度图的连续帧中多个强度最大值(或多个强度最小值)被鉴定,将所述多个强度最大值(或多个强度最小值)假定为对应于相同的结合事件(或解离事件),和通过平均所述多个强度最大值(或多个强度最小值)的它们的(x, y)位置和对所述多个强度最大值(或多个强度最小值)的强度值求和来组合。
一些实施方案包含对于每个簇内的事件计算一个或多个统计学度量,包括但不限于,查询探针结合和/或解离事件的数量;给定的结合事件和下一个解离事件之间的帧数量的平均值、中值、最大值、最小值、范围和标准偏差的一项或多项;给定的解离事件和下一个结合事件之间的帧数量的平均值、中值、最大值、最小值、范围和标准偏差的一项或多项;查询探针结合和解离事件的(x, y)位置的平均值、中值、最大值、最小值、范围和标准偏差的一项或多项;和/或与查询探针结合和解离事件有关的信号强度变化的平均值、中值、最大值、最小值、范围和标准偏差的一项或多项。
一些实施方案包含将对于查询探针结合事件的每个簇按上所述测量的统计学与使用标准参考材料(例如,阳性对照)测量的统计学进行比较。一些实施方案包含将对于查询探针结合事件的每个簇按上所述测量的统计学与使用阴性对照(例如,不包含分析物、与分析物密切相关的物质、包含修饰和/或不包含修饰的分析物等)测量的统计学进行比较。在一些实施方案中,将对于查询探针结合事件的每个簇按上所述测量的统计学与使用标准参考材料和/或阴性对照测量的统计学进行比较用于确定查询探针结合事件的簇是否可能源自查询探针与靶分析物的单分子的结合。
一些实施方案包含计算在数据集中代表查询探针与靶分析物结合的簇数量。在一些实施方案中,计算在数据集中代表查询探针与靶分析物结合的簇数量包含使用一种或多种上文所述的统计学检验。在一些实施方案中,计算在数据集中代表查询探针与靶分析物结合的簇数量提供通过该方法测定的成像表面的区域中存在的分析物数量(例如,分析物的表观数量)的度量。在一些实施方案中,计算在数据集中代表查询探针与靶分析物结合的簇数量提供分析物浓度的度量,提供分析物在样品中存在或不存在的指示,和/或提供样品中的分析物的状态(例如,修饰、未修饰)的指示。
一些实施方案任选地包含将如上所述的分析物的表观数量、浓度、状态、存在或不存在与对于已知分析物浓度的分析物的表观数量、浓度、状态、存在或不存在的之前测定的值进行比较。一些实施方案包含使用标准曲线(例如,用一种或多种包含具有已知浓度的靶分析物的标准参考材料的组合物产生)以确定样品中靶分析物的浓度。
在一些实施方案中,所述方法的步骤以软件代码实施,例如,命令计算机和/或微处理器如上所述产生和/或转化数据的一系列程序步骤。在一些实施方案中,软件指令用编程语言编码,例如,BASIC、C、C++、Java、MATLAB、Mathematica、Perl、Python或R。
在一些实施方案中,超分辨率鉴定、检测、定量和/或表征分析物的一个或多个步骤或组件以在模块系统中连接的单独软件对象提供。在一些实施方案中,软件对象是可扩展的和可移植的。在一些实施方案中,对象包含数据结构和转化对象数据的操作。在一些实施方案中,对象通过操作它们的数据和调用它们的方法来使用。因此,实施方案提供软件对象,其模拟、建模或提供真实的实体,例如对于可操作的数量、形状、数据结构。在一些实施方案中,软件对象在计算机或微处理器中操作。在一些实施方案中,软件对象在计算机可读介质上储存。
在一些实施方案中,本文所述的方法的步骤作为对象方法提供。在一些实施方案中,本文所述的数据和/或数据结构作为对象数据结构提供。
一些实施方案提供面向对象的管线(pipeline),用于处理时间序列的传感器阵列数据,例如,包含一个或多个软件对象,以产生漂移-校正的数据集和/或差示强度图影片;鉴定一个或多个强度最大值和/或强度最小值的位置、强度和/或帧数量的一项或多项;转化数据,例如使用二维高斯拟合、形心拟合或用于确定粒子位置的其它方法;对于横向漂移校正从差示强度图确定的(x, y)位置系列;组合强度最大值和/或强度最小值的(x, y)位置;对多个强度最大值(或多个强度最小值)的强度值求和;对于每个簇内的事件,计算一个或多个统计学度量;将对于查询探针结合事件的每个簇如上所述测量的统计学与使用标准参考材料测量的统计学和/或与阴性对照进行比较;计算数据集中代表查询探针与靶分析物结合的簇数量,例如,以产生通过所述方法测定的成像表面的区域中存在的分析物数量(例如,分析物的表观数量)的度量、分析物浓度的度量、分析物在样品中存在或不存在的指示和/或在样品中分析物状态的指示;和/或将如上所述的分析物的表观数量、浓度、状态、存在或不存在与对于已知分析物浓度的分析物的表观数量、浓度、状态、存在或不存在的之前测定的值进行比较。
实施方案包含使用产生和操作软件对象的代码,例如,使用语言例如但不限于Java、C++、C#、Python、PHP、Ruby、Perl、Object Pascal、Objective-C、Swift、Scala、CommonLisp和Smalltalk编码的代码。
系统
该技术的实施方案涉及用于检测分析物的系统。例如,在一些实施方案中该技术提供用于定量一种或多种靶分析物的系统,其中所述系统包含稳定结合靶分析物的表面-结合捕获探针或表面-结合部分。在一些实施方案中,表面-结合捕获探针或表面-结合部分通过结合位点、表位或识别位点(例如,第一结合位点、第一表位或第一识别位点)稳定结合分析物。在一些实施方案中,系统进一步包含在第二结合位点、第二表位或第二识别位点以低亲和力结合靶分析物的查询探针。在一些实施方案中查询探针在接触系统表面的主体溶液中是自由可扩散的。此外,一些系统实施方案包含检测组件,其记录来自查询探针与靶分析物的相互作用的信号。例如,在一些实施方案中检测组件记录从查询探针与靶分析物的相互作用产生的作为时间的函数的信号变化。在一些实施方案中检测组件记录查询探针与所述靶分析物的结合事件和从所述靶分析物的解离事件的空间位置(例如,作为x, y坐标对)和强度。在一些实施方案中,检测组件记录查询探针与所述靶分析物的结合事件和从所述靶分析物的解离事件的空间位置(例如,作为x, y坐标对)和开始和/或结束时间。在一些实施方案中检测组件记录查询探针与所述靶分析物的结合事件和从所述靶分析物的解离事件的空间位置(例如,作为x, y坐标对)和时间长度。
系统实施方案包含分析过程(例如,具体为一组指令,其例如在软件中编码的,命令微处理器进行分析过程)以鉴定靶分析物的单个分子。在一些实施方案中,分析过程使用对所述靶分析物的重复结合和解离事件的空间位置数据和时机(例如,开始、结束或时间长度)作为输入数据。
系统的实施方案在检测的分析物方面不受限制。例如,在一些实施方案中分析物是多肽,例如,蛋白或肽。在一些实施方案中,靶分析物是核酸。在一些实施方案中,靶分析物是小分子。
在一些实施方案中,靶分析物和查询探针之间的相互作用可区别地受到靶分析物的共价修饰的影响。例如,在一些实施方案中,分析物是包含翻译后修饰的多肽,例如,包含翻译后修饰的蛋白或肽。在一些实施方案中,多肽的翻译后修饰影响查询探针与分析物的瞬时结合,例如,查询探针信号是多肽上翻译后修饰的存在或不存在的函数。例如,在一些实施方案中分析物是包含外遗传修饰的核酸,例如,包含甲基化碱基的核酸。在一些实施方案中,核酸的修饰影响查询探针与分析物的瞬时结合,例如,查询探针信号是核酸上修饰的存在或不存在的函数。
在一些实施方案中,翻译后修饰和查询探针之间的瞬时相互作用由化学亲和标签、例如包含核酸的化学亲和标签介导。
在一些实施方案中,查询探针是核酸或适体。
在一些实施方案中,查询探针是低亲和力抗体、抗体片段或纳米抗体。
在一些实施方案中,查询探针是DNA-结合蛋白、RNA-结合蛋白或DNA-结合核糖核蛋白复合物。
在一些实施方案中,分析物是包含对靶分析物的核碱基、核糖或脱氧核糖部分的共价修饰的核酸。
在一些实施方案中,捕获探针是高亲和力抗体、抗体片段或纳米抗体。在一些实施方案中,捕获探针是核酸。在一些实施方案中,捕获由交联靶分析物与表面的共价键介导。在一些实施方案中,在表面固定之前靶分析物在载体的存在下经历热变性。在一些实施方案中,在表面固定之前分析物在载体的存在下经历化学变性,例如,分析物用变性剂例如尿素、甲酰胺、盐酸胍、高离子强度、低离子强度、高pH、低pH或十二烷基硫酸钠(SDS)变性。
该技术的一些系统实施方案包含用于检测和定量靶分析物的组件。根据该技术的系统包含例如固体支持物(例如,显微镜玻片、盖玻片、亲和素(例如,链霉亲和素)-缀合的显微镜玻片或盖玻片、包含零模式波导阵列的固体支持物等)和本文所述的查询探针。
一些系统实施方案包含检测组件,其为包含激发结合的查询探针的照明构造的荧光显微镜(例如,棱镜型全内反射荧光(TIRF)显微镜、物镜型TIRF显微镜、近-TIRF或HiLo显微镜、共焦激光扫描显微镜、零模式波导和/或能够平行监测大面积玻片或盖玻片(> 100 μm2)同时限制照明在表面附近的小区域空间的照明构造)。一些实施方案包含荧光检测器,例如,包含强化电荷耦合装置(ICCD)、电子倍增电荷耦合装置(EM-CCD)、互补金属氧化物半导体(CMOS)、光电增倍管(PMT)、雪崩光电二极管(APD)的检测器和/或能够检测来自单个发色团的荧光发射的另一检测器。一些特定的实施方案包含经配制用于无透镜成像的组件,例如,无透镜显微镜,例如,用于不使用透镜而直接在检测器(例如,CMOS)上成像的检测和/或成像组件。
一些实施方案包含计算机和编码用于计算机执行例如以控制数据采集和/或分析过程以处理数据的指令的软件。
一些实施方案包含光学器件,例如透镜、反射镜、双色镜、滤光片等,例如,以选择性检测在特定波长范围或多个波长范围内的荧光。
例如,在一些实施方案中,基于计算机的分析软件用于为临床医师将通过检测测定产生的原始数据(例如,一种或多种分析物的存在、不存在或量,例如,作为时间和/或表面上的位置(例如,x, y坐标)的函数)转变为预测值的数据。临床医师可使用任何合适的方式访问预测数据。
一些系统实施方案包含计算机系统,在其上面可以实现本技术的实施方案。在不同的实施方案中,计算机系统包括总线或其它用于传达信息的通信机构和用于处理信息的与所述总线耦合的处理器。在不同的实施方案中,所述计算机系统包括与所述总线耦合的存储器(其可以是随机存取存储器(RAM)或其它动态存储装置),和要由所述处理器执行的指令。存储器也可以用于在执行由所述处理器执行的指令的过程中存储临时变量或其它中间信息。在不同的实施方案中,所述计算机系统还可以包括与所述总线耦合的只读存储器(ROM)或其它静态存储装置,用于为所述处理器存储静态信息和指令。可以提供存储装置,诸如磁盘或光盘,并与所述总线耦合,用于存储信息和指令。
在不同的实施方案中,所述计算机系统经由所述总线耦合至显示器,诸如阴极射线管(CRT)或液晶显示器(LCD),用于将信息显示给计算机用户。输入装置(包括字母数字键和其它键)可以耦合至所述总线用于将信息和命令选择传达给处理器。另一类用户输入装置是光标控制,诸如鼠标、跟踪球或光标方向键,其用于将方向信息和命令选择传达给处理器和用于控制显示器上的光标移动。该输入装置通常具有在两个轴(第一轴(例如,x)和第二轴(例如,y))上的两个自由度,这允许所述装置在平面中指定位置。
计算机系统可以执行本技术的实施方案。与本技术的某些实现相一致,计算机系统响应于处理器可以提供结果,所述处理器执行在存储器中所含的一个或多个指令的一个或多个序列。这样的指令可以从另一种计算机可读介质(诸如存储装置)读入存储器中。在存储器中所含的指令的序列的执行,可以造成所述处理器执行本文所述的方法。可替换地,可以替代软件指令或与软件指令组合地使用硬线电路来实现本教导。因而,本技术的实现不限于硬件电路和软件的任何具体组合。
本文中使用的术语“计算机可读介质”是指参与将指令提供给处理器用于执行的任何介质。这样的介质可以呈许多形式,包括、但不限于,非易失性介质、易失性介质和传输介质。非易失性介质的实例可以包括、但不限于光盘或磁盘,诸如存储装置。易失性介质的实例可以包括、但不限于动态存储器。传输介质的实例可以包括但不限于同轴电缆、铜丝和纤维光学器件,包括包含总线的导线。
计算机可读介质的常见形式包括,例如,软盘、软磁盘、硬盘、磁带或任意其它磁性介质、CD-ROM、任意其它光学介质、穿孔卡片、纸带、具有孔模式的任意其它物理介质、RAM、PROM和EPROM、FLASH-EPROM、任意其它存储芯片或筒、或计算机可以从其读出的任意其它有形介质。
计算机可读介质的不同形式可以参与将一个或多个指令的一个或多个序列携带至处理器用于执行。例如,所述指令可以最初携带在远程计算机的磁盘上。所述远程计算机可以将所述指令负载进它的动态存储器中并通过网络连接(例如,LAN、WAN、因特网、电话线)发送所述指令。局部计算机系统可以接收所述数据并将它传递至总线。所述总线可以将所述数据携带至存储器,所述处理器从其取回和执行指令。由所述存储器接收的指令可以任选地在所述处理器执行之前或之后储存在存储装置上。
根据不同的实施方案,将被构造成由处理器执行以实现方法的指令储存在计算机可读介质上。所述计算机可读介质可以是储存数字信息的装置。例如,计算机可读介质包括光盘只读存储器(CD-ROM),如本领域已知用于存储软件的。所述计算机可读介质被处理器访问,所述处理器适合用于执行被构造成执行的指令。
根据这样的计算机系统,本文提供的技术的一些实施方案进一步包含用于收集、存储和/或分析数据(例如,分析物的存在、不存在、浓度)的功能性。例如,一些实施方案预见到这样的系统:其包含处理器、存储器和/或数据库,例如,用于存储和执行指令,分析荧光、图像数据,使用所述数据执行计算,转化所述数据,和存储所述数据。在某些实施方案中,算法将统计模型(例如,泊松模型或隐马尔可夫模型)应用于所述数据。
许多诊断涉及确定一种或多种核酸的存在或核苷酸序列。
在某些实施方案中,包含变量(其代表一种或多种分析物的存在、不存在、浓度、量或序列性质)的方程式产生这样的值:其用于做出诊断或评估分析物的存在或特性。因此,在某些实施方案中,该值由装置呈现,例如,由与结果有关的指示器(例如,LED、在显示器上的图标、声音等)呈现。在某些实施方案中,装置存储所述值,传递所述值,或使用所述值用于另外的计算。在某些实施方案中,方程式包含变量,其代表一种或多种分析物的存在、不存在、浓度、量或性质。
因而,在某些实施方案中,本技术提供了另外益处:临床医师(其可能没有经过分析测定培训)不需要理解原始数据。所述数据以它的最有用形式直接呈现给临床医师。所述临床医师然后能够利用所述信息来优化受试者的护理。本发明的技术预见到能够接收、处理来自进行测定的实验室、信息提供者、医学人员和/或受试者的信息和将信息传递给进行测定的实验室、信息提供者、医学人员和/或受试者的任何方法。例如,在本技术的某些实施方案中,从受试者得到样品并经受位于世界上的任何部分(例如,在这样的国家:其不同于受试者所居住的国家或最终使用所述信息的国家)的概况分析服务(profiling service)(例如,在医疗设施处的临床实验室,基因组概况分析商业,等)以产生原始数据。在所述样品包含组织或其它生物样品的情况下,所述受试者可以访问医学中心以获得样品和将其送至概况分析中心,或受试者可以自己收集样品并直接地将它送至概况分析中心。在样品包含以前确定的生物学信息的情况下,所述信息可以由受试者直接送至概况分析服务(例如,可以由计算机扫描含有信息的信息卡,并使用电子通信系统将数据传送至概况分析中心的计算机)。一旦被概况分析服务接收到,样品就被处理并产生对于受试者需要的诊断或预后信息而言特异性的概况(profile)。然后以适合主治临床医师解释的形式制备概况数据。例如,不是提供原始表达数据,制备的形式可能代表受试者的诊断或风险评估,以及关于具体治疗选择的推荐。所述数据可以通过任意合适的方法显示给临床医师。例如,在某些实施方案中,所述概况分析服务产生这样的报告:其可以打印给临床医师(例如,在护理点)或在计算机监视器上显示给临床医师。在某些实施方案中,首先在护理点处或在区域设施处分析信息。然后将原始数据发送至中心处理设施用于进一步分析和/或将原始数据转化成对于临床医师或患者有用的信息。所述中心处理设施提供数据分析的私密性(所有数据都以一致的安全协议存储在中心设施中)、速度和一致性的优点。所述中心处理设施然后可以在受试者的治疗以后控制数据的命运。例如,使用电子通信系统,中心设施可以将数据提供给临床医师、受试者或研究人员。在某些实施方案中,所述受试者能够使用电子通信系统访问数据。所述受试者可以基于结果选择进一步干预或咨询。在某些实施方案中,将所述数据用于研究用途。例如,可以将所述数据用于进一步优化标志物的包含或消除作为与疾病有关的特定情况的有用指标。
样品
在某些实施方案中,从生物样品分离分析物。分析物可以得自任何材料(例如,细胞材料(活的或死的)、细胞外材料、病毒材料、环境样品(例如,宏基因组样品)、合成材料(例如,扩增子,诸如通过PCR或其它扩增技术提供的)),得自动物、植物、细菌、古细菌、真菌或任意其它生物体。用于用在本技术中的生物样品包括病毒颗粒或其制品。分析物可以直接得自生物体或得自从生物体得到的生物样品,例如,得自血液、尿、脑脊液、精液、唾液、痰、粪便、毛发、汗液、泪水、皮肤和组织。示例性的样品包括、但不限于全血、淋巴流体、血清、血浆、口颊细胞、汗液、泪水、唾液、痰、毛发、皮肤、活组织检查、脑脊液(CSF)、羊水、精液、阴道排泄物、浆液、滑液、心包液、腹膜液、胸膜液、漏出液、渗出液、囊液、胆汁、尿、胃液、肠液、粪便样品和拭子、抽吸物(例如,骨髓、细针等)、洗液(例如,口腔、鼻咽、支气管、支气管肺泡、眼、直肠、肠、阴道、表皮等)、呼吸冷凝液和/或其它样本。
任何组织或体液样本可以用作在所述技术中使用的分析物的来源,包括法医样本、存档的样本、保留的样本和/或储存长时间段的样本,例如,新鲜-冷冻的、甲醇/乙酸固定的、或福尔马林固定的石蜡包埋的(FFPE)样本和样品。分析物还可以分离自培养的细胞,诸如原代细胞培养物或细胞系。可以用病毒或其它细胞内病原体感染从其得到分析物的细胞或组织。样品还可以是从生物样本、cDNA文库、病毒或基因组DNA提取的总RNA。样品也可以是来自非细胞起源的分离的DNA,例如已经在冰柜中储存的扩增的/分离的DNA。
例如,通过从生物样品提取,例如,通过多种技术诸如Maniatis,等人(1982)Molecular Cloning: A Laboratory Manual,Cold Spring Harbor,N.Y. (参见,例如,第280-281页)描述的那些,可以得到分析物(例如,核酸分子、多肽、脂质)。
在一些实施方案中,该技术提供分析物的大小选择,例如,以提供限定的大小范围的分子(包括靶分析物)。
用途
各种实施方案涉及各种分析物的检测。例如,在一些实施方案中该技术用于检测核酸(例如,DNA或RNA)。在一些实施方案中,该技术用于检测包含特定靶标序列的核酸。在一些实施方案中,该技术用于检测包含特定突变(例如,单核苷酸多态性、插入、缺失、错义突变、无义突变、基因重排、基因融合等)的核酸。在一些实施方案中,该技术用于检测多肽(例如,蛋白、肽)。在一些实施方案中,该技术用于检测由包含突变的核酸编码的多肽(例如,包含置换的多肽、截短的多肽、突变体或变体多肽)。
在一些实施方案中,该技术用于检测多肽的翻译后修饰,例如,磷酸化、甲基化、乙酰化、糖基化(例如,O-连接糖基化、N-连接糖基化、遍在蛋白化、官能团连接(例如,豆蔻酰化、棕榈酰化、异戊二烯化、异戊烯化、法尼基化、香叶基化、香叶基香叶基化、糖基磷脂酰肌醇化、糖基磷脂酰肌醇(GPI)锚形成)、羟基化、生物素化、聚乙二醇化、氧化、SUMO化、二硫桥形成、二硫桥裂解、蛋白水解裂解、酰胺化、硫酸化、吡咯烷酮羧酸形成。在一些实施方案中,该技术用于检测这些特征的丢失,例如,去磷酸化、去甲基化、去乙酰化、去糖基化、去酰胺化、去羟基化、去遍在蛋白化等。在一些实施方案中,该技术用于检测DNA或RNA的外遗传修饰(例如,甲基化(例如,CpG位点的甲基化)、羟基甲基化)。在一些实施方案中,该技术用于检测这些特征的丢失,例如,DNA或RNA的去甲基化等。在一些实施方案中,该技术用于检测染色质结构、核小体结构、组蛋白修饰等的改变,和检测对核酸的损伤。
在一些实施方案中,该技术用作分子诊断测定,例如,以测定具有小样本体积的样品(例如,一滴血液,例如,用于邮寄服务)。在一些实施方案中,该技术使用极低丰度分析物生物标志物的灵敏检测,提供癌症或感染性疾病的早期检测。在一些实施方案中,该技术用于分子诊断以测定蛋白生物标志物的外遗传修饰(例如,翻译后修饰)。
在一些实施方案中,该技术用于表征多分子复合物(例如,表征多分子复合物的一个或多个组分),例如,多蛋白复合物、核酸/蛋白复合物、分子机器、细胞器(例如,无细胞线粒体,例如,在血浆中)、细胞、病毒颗粒、生物体、组织或可捕获和适于通过本文描述的技术分析的任何大分子结构或实体。例如,在一些实施方案中分离多分子复合物和该技术用于表征、鉴定、定量和/或检测与多分子复合物相关的一种或多种分子(分析物)。在一些实施方案中分离细胞外囊泡和该技术用于表征、鉴定、定量和/或检测与囊泡相关的一种或多种分子(分析物)。在一些实施方案中,该技术用于表征、鉴定、定量和/或检测囊泡内部存在的蛋白(例如,表面蛋白)和/或分析物,例如,蛋白、核酸或本文所述的其它分析物。在一些实施方案中,在分析前囊泡被固定和渗透。
实施例
实施例1 – 通过重复查询探针结合鉴定表面-固定靶标
在开发本文描述的技术的实施方案期间,进行实验,其中靶分析物(例如,分子,例如蛋白、肽、核酸等)被稳定固定至表面。然后,加入低亲和力探针,和检测并记录低亲和力查询探针与靶分析物的重复结合以产生查询探针信号对比表面上的空间位置的数据集(见图1)。
在实验期间,采集数据,其包含时间序列的查询探针信号(缔合(查询探针与分析物的结合)和解离事件)对比表面上的位置。这些数据使用逐帧减法的方法分析以产生差示强度分布图,其显示每一帧内的查询探针结合或解离事件。通过这种数据处理产生的差示强度分布图提供强度最小值和最大值,其比初始信号对比位置图内的强度最大值更好分辨。确定每个事件的位置(例如使用x, y坐标)后,所有事件根据空间位置簇集,和每个簇内的事件的动力学经历统计学分析以确定事件簇是否源自给定的靶分析物(图1)。
实施例2 – 与其它成像方法比较
在开发本文描述的技术的实施方案期间,进行实验以比较使用本文描述的技术采集的数据与使用其它成像技术采集的数据。具体地,DNA分析物被固定至表面和使用如本文所述的超分辨率成像和事件簇集成像(见例如,实施例1)。如图2所示,相对于衍射限制成像方法(例如,描述于US20160046988) (空心圆),当使用本文所述的超分辨率成像和来自差示强度图的事件簇集(实心方块)时,本发明的技术提供以皮摩尔范围存在的DNA靶分析物的测量的动态范围的改进。每个单独的结合或解离事件的定位,接着结合或解离事件的簇集和动力学分析,允许表面上多个密集的靶分析物的分辨。
实施例3 – 测定的特异性
在开发本文描述的技术期间,进行实验以评价本文所述的超分辨率成像和事件簇集技术的特异性。具体地,包含突变体序列的核酸的检测特异性通过比较在存在(1) 仅已知浓度的突变体序列或(2) 仅10,000倍浓度的野生型序列时检测的分子数量进行测试。在存在突变体DNA序列时,成像视野内的数个(例如,大约399个)结合事件簇(图3A,深黑色点)显示查询探针与突变体序列结合特有的动力学,而非特异性结合事件(图3A,浅灰色圆圈)通过统计学分析去除。相比之下,当在不存在突变体和存在10,000倍浓度的野生型DNA序列下进行相同实验时,所有查询探针结合事件通过局部事件簇的统计学分析去除,导致没有假阳性检测事件(图3B)。
在以上说明书中提及的所有出版物和专利都通过引用整体并入本文用于所有目的。所述技术的所述组合物、方法和用途的各种修改和变化对本领域技术人员而言是显然的,而不脱离所述技术的范围和精神。尽管已经结合具体示例性实施方案描述了所述技术,但是应当理解,要求保护的发明不应当不适当地限于这样的具体实施方案。实际上,对本领域技术人员显而易见的所述的用于实现本发明的模式的各种修改意图是在以下权利要求的范围内。
Claims (30)
1.一种表征样品中的分析物的方法,所述方法包括:
(a) 作为表面上(x, y)位置的函数,记录固定至表面的分析物的查询探针事件的时间依赖性信号;
(b) 按(x, y)位置将事件簇集成局部簇;和
(c) 计算每个事件簇的动力学参数以表征所述分析物。
2.权利要求1的方法,其中所述表面为固体支持物。
3.权利要求1的方法,其中所述表面为可扩散的。
4.权利要求1的方法,其中记录查询探针事件的时间依赖性信号包括以单分子灵敏度测量分析物的信号。
5.权利要求1的方法,其进一步包括计算差示强度图,所述差示强度图包含表面处作为(x, y)位置的函数的时间依赖性信号强度变化。
6.权利要求1的方法,其中(x, y)位置以亚像素准确度确定。
7.权利要求1的方法,其中簇集的事件代表单分析物分子的结合事件。
8.权利要求1的方法,其中表征所述分析物包括指示样品中分析物的存在、不存在、浓度或数量。
9.权利要求1的方法,其中所述分析物包含多肽。
10.权利要求9的方法,其中所述方法指示多肽上翻译后修饰的存在或不存在。
11.权利要求10的方法,其中所述翻译后修饰介导查询探针与多肽的瞬时缔合。
12.权利要求10的方法,其中化学亲和标签介导翻译后修饰和查询探针之间的瞬时缔合。
13.权利要求12的方法,其中所述化学亲和标签是核酸。
14.权利要求1的方法,其中所述分析物是核酸。
15.权利要求1的方法,其中查询探针与分析物的瞬时缔合可区别地受分析物的共价修饰的影响。
16.权利要求1的方法,其中所述查询探针是核酸或适体。
17.权利要求1的方法,其中所述查询探针是低亲和力抗体、抗体片段或纳米抗体。
18.权利要求1的方法,其中所述查询探针是DNA-结合蛋白、RNA-结合蛋白或DNA-结合核糖核蛋白复合物。
19.权利要求5的方法,其中每个查询探针事件的(x, y)位置通过使用形心确定、最小二乘拟合至高斯函数、最小二乘拟合至艾里斑函数、最小二乘拟合至多项式函数或最大似然估计处理差示强度分布图确定。
20.权利要求1的方法,其中在表面固定之前所述分析物在载体的存在下经历热或化学变性。
21.一种用于定量样品中的分析物的系统,所述系统包含:
(a) 将分析物稳定固定至表面的功能性;
(b) 以低亲和力结合靶分析物的自由扩散性查询探针;和
(c) 记录分析物的查询探针事件和查询探针事件的空间位置的检测系统。
22.权利要求21的系统,其进一步包含分析程序以根据所述靶分析物的重复结合和解离事件的空间位置和时机鉴定靶分析物的单个分子拷贝。
23.权利要求21的系统,其中所述查询探针是核酸或适体。
24.权利要求21的系统,其中所述查询探针是低亲和力抗体、抗体片段或纳米抗体。
25.权利要求24的系统,其中所述查询探针是DNA-结合蛋白、RNA-结合蛋白或DNA-结合核糖核蛋白复合物。
26.权利要求24的系统,其中将分析物稳定固定至表面的功能性包含稳定结合靶分析物的表面结合捕获探针。
27.权利要求26的系统,其中所述捕获探针是高亲和力抗体、抗体片段或纳米抗体。
28.权利要求24的系统,其中将分析物稳定固定至表面的功能性是交联靶分析物与表面的共价键。
29.权利要求24的系统,其中在表面固定之前所述分析物在载体的存在下经历热或化学变性。
30.权利要求1的方法或权利要求21的系统,其中所述分析物是大分子复合物的组分。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762468578P | 2017-03-08 | 2017-03-08 | |
| US62/468578 | 2017-03-08 | ||
| PCT/US2018/021356 WO2018165309A1 (en) | 2017-03-08 | 2018-03-07 | Analyte detection |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN110730826A true CN110730826A (zh) | 2020-01-24 |
Family
ID=63446126
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201880030752.9A Pending CN110730826A (zh) | 2017-03-08 | 2018-03-07 | 分析物检测 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20180258469A1 (zh) |
| EP (1) | EP3592768A4 (zh) |
| JP (1) | JP7145517B2 (zh) |
| CN (1) | CN110730826A (zh) |
| AU (1) | AU2018231211A1 (zh) |
| CA (1) | CA3055565A1 (zh) |
| WO (1) | WO2018165309A1 (zh) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111562389A (zh) * | 2020-05-19 | 2020-08-21 | 重庆宏道拓土科技有限公司 | 构成血糖仪“扩展坞”的复合材料及其制备方法与应用 |
| CN112782138A (zh) * | 2020-12-24 | 2021-05-11 | 生物岛实验室 | 用于检测细胞外囊泡的试剂盒及其应用 |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK3472351T3 (da) | 2016-06-15 | 2020-11-09 | Univ Muenchen Ludwig Maximilians | Enkeltmolekylepåvisning eller -kvantificering ved hjælp af DNA-nanoteknologi |
| US11380438B2 (en) | 2017-09-27 | 2022-07-05 | Honeywell International Inc. | Respiration-vocalization data collection system for air quality determination |
| AU2019309923A1 (en) * | 2018-07-24 | 2021-02-04 | The Regents Of The University Of Michigan | Intramolecular kinetic probes |
| US10876949B2 (en) * | 2019-04-26 | 2020-12-29 | Honeywell International Inc. | Flow device and associated method and system |
| US10794810B1 (en) | 2019-08-02 | 2020-10-06 | Honeywell International Inc. | Fluid composition sensor device and method of using the same |
| CN115461458A (zh) * | 2019-12-10 | 2022-12-09 | 伊努梅里斯公司 | 核酸扩增的组合物和方法 |
| US11221288B2 (en) | 2020-01-21 | 2022-01-11 | Honeywell International Inc. | Fluid composition sensor device and method of using the same |
| CN115003827A (zh) * | 2020-01-29 | 2022-09-02 | 密歇根大学董事会 | 分析物检测 |
| US11181456B2 (en) | 2020-02-14 | 2021-11-23 | Honeywell International Inc. | Fluid composition sensor device and method of using the same |
| US11333593B2 (en) | 2020-02-14 | 2022-05-17 | Honeywell International Inc. | Fluid composition sensor device and method of using the same |
| US11391613B2 (en) | 2020-02-14 | 2022-07-19 | Honeywell International Inc. | Fluid composition sensor device and method of using the same |
| US20210292837A1 (en) * | 2020-03-19 | 2021-09-23 | The Regents Of The University Of Michigan | Analyte detection |
| WO2021247837A1 (en) * | 2020-06-05 | 2021-12-09 | Access Medical Systems, Ltd. | Method for determining antibody dissociation rate |
| US11835432B2 (en) | 2020-10-26 | 2023-12-05 | Honeywell International Inc. | Fluid composition sensor device and method of using the same |
| US20220364973A1 (en) * | 2021-05-13 | 2022-11-17 | Honeywell International Inc. | In situ fluid sampling device and method of using the same |
| WO2023250364A1 (en) * | 2022-06-21 | 2023-12-28 | Nautilus Subsidiary, Inc. | Method for detecting analytes at sites of optically non-resolvable distances |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050244863A1 (en) * | 2002-09-19 | 2005-11-03 | The Chancellor, Master And Scholars Of The University Of Oxford | Molecular arrays and single molecule detection |
| US20160046988A1 (en) * | 2014-08-12 | 2016-02-18 | The Regents Of The University Of Michigan | Detection of nucleic acids |
| US20160161472A1 (en) * | 2013-07-30 | 2016-06-09 | President And Fellows Of Harvard College | Quantitative dna-based imaging and super-resolution imaging |
| US20160169903A1 (en) * | 2014-12-15 | 2016-06-16 | President And Fellows Of Harvard College | Methods and compositions relating to super-resolution imaging and modification |
| US20160312272A1 (en) * | 2013-12-15 | 2016-10-27 | President And Fellows Of Harvard College | Methods and compositions relating to optical super-resolution patterning |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5432272A (en) | 1990-10-09 | 1995-07-11 | Benner; Steven A. | Method for incorporating into a DNA or RNA oligonucleotide using nucleotides bearing heterocyclic bases |
| ATE270344T1 (de) | 1999-11-16 | 2004-07-15 | Atto Tec Gmbh | Farbstoffmarkiertes oligonukleotid zum markieren eines nukleinsäuremoleküls |
| US20060014212A1 (en) * | 2002-05-10 | 2006-01-19 | Epitome Biosystems, Inc. | Proteome epitope tags and methods of use thereof in protein modification analysis |
| DE10259374A1 (de) | 2002-12-18 | 2004-07-08 | Atto-Tec Gmbh | Carboxamid-substituierte Farbstoffe für analytische Anwendungen |
| DE10329860A1 (de) | 2003-07-02 | 2005-01-20 | Atto-Tec Gmbh | Sulfonamidderivate polycyclischer Farbstoffe für analytische Anwendungen |
| US8198604B2 (en) | 2007-09-28 | 2012-06-12 | Trustees Of Boston University | System and method for providing enhanced background rejection in thick tissue with differential-aberration two-photon microscopy |
| JP4865930B2 (ja) | 2008-06-05 | 2012-02-01 | トラスティーズ オブ ボストン ユニバーシティ | 構造化された照射および均一な照射の両方を用いて光学的に切片化された画像を生成するためのシステムおよび方法 |
| WO2010085548A2 (en) | 2009-01-22 | 2010-07-29 | Li-Cor, Inc. | Single molecule proteomics with dynamic probes |
| WO2014018584A1 (en) | 2012-07-24 | 2014-01-30 | Trustees Of Boston University | Partitioned aperture wavefront imaging method and system |
| CN109072205A (zh) | 2016-02-10 | 2018-12-21 | 密歇根大学董事会 | 核酸的检测 |
-
2018
- 2018-03-07 JP JP2019549000A patent/JP7145517B2/ja active Active
- 2018-03-07 WO PCT/US2018/021356 patent/WO2018165309A1/en unknown
- 2018-03-07 CN CN201880030752.9A patent/CN110730826A/zh active Pending
- 2018-03-07 US US15/914,729 patent/US20180258469A1/en active Pending
- 2018-03-07 AU AU2018231211A patent/AU2018231211A1/en not_active Abandoned
- 2018-03-07 EP EP18763232.8A patent/EP3592768A4/en active Pending
- 2018-03-07 CA CA3055565A patent/CA3055565A1/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050244863A1 (en) * | 2002-09-19 | 2005-11-03 | The Chancellor, Master And Scholars Of The University Of Oxford | Molecular arrays and single molecule detection |
| US20160161472A1 (en) * | 2013-07-30 | 2016-06-09 | President And Fellows Of Harvard College | Quantitative dna-based imaging and super-resolution imaging |
| US20160312272A1 (en) * | 2013-12-15 | 2016-10-27 | President And Fellows Of Harvard College | Methods and compositions relating to optical super-resolution patterning |
| US20160046988A1 (en) * | 2014-08-12 | 2016-02-18 | The Regents Of The University Of Michigan | Detection of nucleic acids |
| US20160169903A1 (en) * | 2014-12-15 | 2016-06-16 | President And Fellows Of Harvard College | Methods and compositions relating to super-resolution imaging and modification |
Non-Patent Citations (3)
| Title |
|---|
| MARIO RAAB等: "《Fluorescence microscopy with 6 nm resolution on DNA origami》", 《CHEMPHYSCHEM》 * |
| MINGJIE DAI等: "《Optical imaging of individual biomolecules in densely packed clusters》", 《NATURE NANOTECHNOLOGY》 * |
| RALF JUNGMANN等: "《Multiplexed 3D cellular super-resolution imaging with DNA-PAINT and Exchange-PAINT》", 《NATURE METHODS》 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111562389A (zh) * | 2020-05-19 | 2020-08-21 | 重庆宏道拓土科技有限公司 | 构成血糖仪“扩展坞”的复合材料及其制备方法与应用 |
| CN112782138A (zh) * | 2020-12-24 | 2021-05-11 | 生物岛实验室 | 用于检测细胞外囊泡的试剂盒及其应用 |
| CN112782138B (zh) * | 2020-12-24 | 2021-10-29 | 生物岛实验室 | 用于检测细胞外囊泡的试剂盒及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA3055565A1 (en) | 2018-09-13 |
| EP3592768A1 (en) | 2020-01-15 |
| JP2020511648A (ja) | 2020-04-16 |
| AU2018231211A1 (en) | 2019-10-03 |
| US20180258469A1 (en) | 2018-09-13 |
| EP3592768A4 (en) | 2021-04-14 |
| JP7145517B2 (ja) | 2022-10-03 |
| WO2018165309A1 (en) | 2018-09-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7145517B2 (ja) | 分析物の検出 | |
| JP7327826B2 (ja) | 核酸の検知 | |
| Käll et al. | Assigning significance to peptides identified by tandem mass spectrometry using decoy databases | |
| US20210318296A1 (en) | Intramolecular kinetic probes | |
| US11773429B2 (en) | Reduction of bias in genomic coverage measurements | |
| JP2021501332A (ja) | タンパク質同定のための方法およびシステム | |
| US20210292837A1 (en) | Analyte detection | |
| US20220128556A1 (en) | Methods of diagnosing disease | |
| JP2009540326A (ja) | 結合及び非結合ラベルの測定による検体検出の増加した特異性 | |
| Smith et al. | Expanding the dynamic range of fluorescence assays through single-molecule counting and intensity calibration | |
| CN111971380A (zh) | 分析物的浓缩 | |
| Orsburn | Time-of-flight fragmentation spectra generated by the proteomic analysis of single human cells do not exhibit atypical fragmentation patterns | |
| Kaur et al. | MASH-FRET: a simplified approach for single-molecule multiplexing using FRET | |
| US20210230688A1 (en) | Analyte detection | |
| US10844424B2 (en) | Reduction of bias in genomic coverage measurements | |
| Hua et al. | The single-molecule centroid localization algorithm improves the accuracy of fluorescence binding assays | |
| US20240036035A1 (en) | Analyte detection using fluorogenic probes or multiplex technologies | |
| WO2024015927A2 (en) | Analyte detection using aptamers | |
| NL2032916B1 (en) | Single-molecule aptamer FRET for protein identification and structural analysis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |