CN103874526A - 预测补体介导的疾病的发展的方法 - Google Patents
预测补体介导的疾病的发展的方法 Download PDFInfo
- Publication number
- CN103874526A CN103874526A CN201280031235.6A CN201280031235A CN103874526A CN 103874526 A CN103874526 A CN 103874526A CN 201280031235 A CN201280031235 A CN 201280031235A CN 103874526 A CN103874526 A CN 103874526A
- Authority
- CN
- China
- Prior art keywords
- experimenter
- haplotype
- macular degeneration
- age
- snp
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/34—Allele or polymorphism specific uses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2565/00—Nucleic acid analysis characterised by mode or means of detection
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2565/00—Nucleic acid analysis characterised by mode or means of detection
- C12Q2565/50—Detection characterised by immobilisation to a surface
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2565/00—Nucleic acid analysis characterised by mode or means of detection
- C12Q2565/50—Detection characterised by immobilisation to a surface
- C12Q2565/501—Detection characterised by immobilisation to a surface being an array of oligonucleotides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/118—Prognosis of disease development
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/172—Haplotypes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/46—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans from vertebrates
- G01N2333/47—Assays involving proteins of known structure or function as defined in the subgroups
- G01N2333/4701—Details
- G01N2333/4716—Complement proteins, e.g. anaphylatoxin, C3a, C5a
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/16—Ophthalmology
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/16—Ophthalmology
- G01N2800/164—Retinal disorders, e.g. retinopathy
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/28—Neurological disorders
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/50—Determining the risk of developing a disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/54—Determining the risk of relapse
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/56—Staging of a disease; Further complications associated with the disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/60—Complex ways of combining multiple protein biomarkers for diagnosis
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Analytical Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Immunology (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Physics & Mathematics (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biophysics (AREA)
- General Engineering & Computer Science (AREA)
- Pathology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Ophthalmology & Optometry (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Cell Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本文中公开了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者对患有或发展补体介导的疾病的易感性。
Description
致谢
本发明是在由NIH授予的基金R24EY017404下通过政府资助进行的。政府具有本发明的某些权利。
相关申请的交叉参考
本申请要求保护2011年4月29日提交的美国临时专利申请No.61/480,929的利益。将美国临时专利申请No.61/480,929的完整内容通过引用并入本文。
发明领域
本发明总体上涉及人受试者的补体介导的疾病的诊断和治疗。具体地,本发明涉及通过检测一批由CFH-至-F13B基因座中的多个变异组成的多态性和单倍型进行的年龄相关性黄斑变性的预测或诊断。
背景
年龄相关性黄斑变性(AMD),一种补体介导的疾病,是老年人失明的首要原因,其是随人口老龄化而日益恶化的问题。发展补体介导的疾病例如AMD的风险的准确鉴定对于在疾病进展的早期开始治疗和鉴定因果遗传突变以获得更好的靶向策略和发展是必需的。先前表明Chr1、Chr10、Chr6(CFB)和Chr19(C3)上的基因座牵涉AMD的风险。
RCA基因簇,有时在下文中称为“CFH-至-F13B基因座”,位于染色体1q32上并且包括补体因子H(CFH)的因子、5个因子H相关基因(CFHR1、CFHR2、CFHR3、CFHR4和CFHR5)和编码凝血因子XIII的β亚基的基因。参见美国专利公布US2007/0020647,通过引用并入本文)。CFH是补体活性的重要调节剂,并且被认为是防止自身组织被不适当的C3活化损伤所必需的。此外,CFH活性的改变与改变的对膜结合糖蛋白、其它补体抑制剂和病原菌的表面的结合相关。
先前,单倍型研究聚焦在CFH上并且只有极少扩展至远至CFHR2。然而,完全CFH基因座是包含另外的与补体介导的疾病例如AMD关联的变体的基因组的区域。因此,所需的是更有效的描述在该基因座上患有或发展补体介导的疾病的风险的方法。此外,所需的是将已知的风险和保护性变体置于它们存在于其中的更广的遗传背景中,即整个CHF-至-F13B基因座。
概述
本文中公开了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个单倍型的存在表明所述受试者对患有或发展补体介导的疾病的易感性。
本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其组合,并且其中一个或多个或其互补序列,并且其中一个或多个单倍型的存在表明所述受试者对患有或发展补体介导的疾病的易感性。
本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个单倍型的存在表达受试者对患有或发展补体介导的疾病的易感性。
本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的方法,包括测定高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份,其中所述SNP是:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中至少6个所述SNP的存在表明受试者对患有或发展补体介导的疾病的易感性。
本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明受试者对患有或发展补体介导的疾病的易感性。
本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的方法,包括测定受试者的CFH-至-F13B基因座中的缺失标记SNP的身份,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中SNP的存在表明受试者对患有或发展补体介导的疾病的易感性。
本文中还公开了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否需要治疗补体介导的疾病。
本文中还公开了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否需要治疗补体介导的疾病。
本文中还公开了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否需要治疗补体介导的疾病。
本文中还公开了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份,其中所述SNP是:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中至少6个所述SNP的存在表明受试者是否需要治疗补体介导的疾病。
本文中还公开了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明受试者是否需要治疗补体介导的疾病。
本文中还公开了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的缺失标记SNP的身份,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明受试者是否需要治疗补体介导的疾病。
本文中还描述了鉴定需要预防性治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否需要治疗补体介导的疾病。
本文中还描述了鉴定需要预防性治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否需要治疗补体介导的疾病。
本文中还描述了鉴定需要预防性治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否需要治疗补体介导的疾病。
本文中还描述了鉴定需要预防性治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否需要治疗补体介导的疾病。
本文中还描述了鉴定需要预防性治疗补体介导的疾病的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明受试者是否需要预防性治疗补体介导的疾病。
本文中还描述了鉴定需要预防性治疗补体介导的疾病的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的缺失标记SNP的身份,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明受试者是否需要预防性治疗补体介导的疾病。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否适合进行临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否适合进行临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的一个或多个单倍型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个单倍型的存在表明受试者是否适合进行临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份,其中所述SNP是:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中至少6个所述SNP的存在表明受试者是否适合进行临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明受试者是否适合进行临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的缺失标记SNP的身份,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明受试者是否适合进行临床试验。
本文中还描述了包括用于检测受试者的核酸样品中的一个或多个单倍型的测定的试剂盒,其中一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。
本文中还描述了用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者对患有或发展年龄相关性黄斑变性的易感性。
本文中还描述了鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者是否需要治疗年龄相关性黄斑变性。
本文中还描述了鉴定需要预防性治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者是否需要预防性治疗年龄相关性黄斑变性。
本文中还描述了鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者是否适合进行临床试验。
附图简述
包含在本说明书中并且构成本说明书的部分的附图举例说明了几个方面并且在说明书中一起用于解释本发明的原理。
图1显示主单倍型H1_61_A至H15_62_A。
图2显示初步单倍型研究中使用的63个SNP。
图3显示次单倍型H16_62_A至H163_62_A。
图4显示来源于GSH-1073队列和GSH-927队列的单倍型的验证。
图5显示GSH队列中62SNP小组的单个SNP关联数据。
图6显示使用Haploview4.2针对完整扩展单倍型分析的疾病关联。
图7显示62个SNP单倍型的单倍型标记SNP。
图8显示51_A单倍型标记SNP(51_A htSNP)。
图9显示51_B单倍型标记SNP(51_A htSNP)。
图10显示使用越来越少的SNP产生单倍型对单倍型的关联值的影响。
图11显示R3-1缺失的qPCR测定、纯合的缺失或非缺失的常规PCR测定。
图12显示同胞对队列中的51个SNP单倍型的评估。
图13显示GSH病例-对照对列中62个单标记(SNP)和单倍型与性别的关联以及‘927队列中的男性和女性的性别的关联。
图14显示被63个SNP覆盖的单倍型边界之外的延伸。图中提供了所有Hapmap SNP的列表。
图15显示51_B队列中的CFH基因座和单倍型。
图16显示51_A与62_A单倍型的比较。
图17显示62_A单倍型的频率。
图18显示按照P值重新分组的62_A SNP单倍型方案。
图19显示1073队列与组合队列中的51SNP单倍型的比较。
图20显示‘927队列和62_A至51_A的转换。
图21显示62_A队列的单倍型树。图21(A)显示163个基于62_ASNP的单倍型之间的等级关系。
图22显示使用基于51SNP的单倍型的‘927队列中的单倍型的关联。
图23显示62_A单倍型的性别关联。
图24显示51_B单倍型的性别关联。
图25显示单倍型的疾病关联。
图26显示基于性别的单倍型的疾病关联。
图27显示用于单倍型重建的SNP。
图28显示Taqman qPCR拷贝数变异数据。
图29显示具有不同数目的经筛选的SNP的受试者的频率。
图30显示被制成预测来自3个SNP的缺失状态的缺失决策树。
图31显示用于测定CFHR3和CFHR1基因的拷贝数状态的实时定量PCR(qPCR)的结果。
图32显示针对63个SNP筛选的基于1073队列的H1-H19单倍型。
图33显示使用Haploview程序的定相单倍型输入模式Haps格式基于136个无关UGRP个体计算的单倍型频率,所述个体大部分为第一代祖父母。
图34显示基于63个SNP的CFH-至-F13B单倍型与AMD的关联。
图35显示整个51_B队列的二倍体型分析。
图36显示51_B队列中的男性的二倍体型分析。
图37显示51_B队列中的女性的二倍体型分析。
图38显示经突出显示以匹配主HapMap单倍型的具有所有单倍型的组合队列0vs1b-4。
图39显示对于CEU具有大于0.5%的频率的主CFH-至-F13BHapMap单倍型。
图40显示图39中显示的标记-rs编号ID。
图41显示基于51_B的单倍型与频率大于0.05%的HapMap单倍型的比较。
图42显示单标记关联;51_B队列中的对照(0)对所有AMD。
图43显示单标记关联;51_B队列中的对照(0)对早期AMD(1b-3)。
图44显示单标记关联;51B队列中的对照(0)对地图样萎缩(4A)。
图45显示单标记关联;51_B队列中的对照(0)对CNV(4B)。
图46显示单倍型关联:51_B队列中的对照对(0)对所有AMD、早期AMD(1B-3)、仅GA(4A)&仅CNV(4B)。
图47显示二倍体型关联;51_B队列中的对照(0)对早期AMD(1B-3)。
图48显示二倍体型关联;51_B队列中的对照(0)对CNV(4B)。
本发明的其它有利方面将部分示于随后的说明中,并且部分根据说明是显而易见的,或可通过本发明的实践得知。本发明的有利方面可通过所附权利要求中具体指出的组件和组合来实现和获得。应理解,上文中的一般描述和下列详细描述仅是示例性的和说明性的,并且不是对本发明的限定,如所要求保护的。
描述
本发明可通过参考下列本发明的详述和在其中包括的实施例来更容易地理解。
除非另外明确地声明,否则本文中所示的任何方法或方面绝对无意解释为要求其步骤以指定的顺序进行。因此,其中所述方法没有明确地在权利要求或说明书中声明步骤将被限定于特定的顺序,绝对无意在任何方面推导顺序。这对解释保持了任何可能的非表达偏向性,包括关于步骤或操作流程的排列的逻辑主题,来源于语法组织或标点的普通含义或本说明书中描述的方法的数目或类型。
定义
如本说明书和所附权利要求中所用,除非上下文明确另有所指,否则单数形式“一个/一种(a)”、“一个/一种(an)”和“所指物(the)”包括复数所指物。因此,例如,提及的“药用载体”包括两种或更多种载体等的混合物。
范围在本文中可表达从“约”一个具体值,和/或至“约”另一个具体值。当表达这样的范围时,另一个实施方案包括从一个具体值和/或至另一个具体值。类似地,当值表达为近似值,通过使用先行词“约”,应理解具体值形成另一个实施方案。还应理解,每个范围的终点相对于另一个终点都是显著的,并且不依赖于另一个终点。还应理解,在本文中描述了许多值,每一个值在本文中,除了该值本身以外,还公开为“约”该具体值。例如,例如值“10”被公开,则“约10”也被公开。还应理解,当“小于或等于”该值的值被公开时,“大于或等于该值”以及值之间的可能范围也被公开,如本领域技术人员适当地理解的。例如,如果值“10”被公开,则“小于或等于10”以及“大于或等于10”也被公开。还应理解,在整个申请中,数据以许多不同的形式提供,并且这些数据代表终点、起点以及数据点的任何组合的范围。例如,如果特定数据点“10”和特定数据点15被公开,则应理解,大于、大于或等于、小于、小于或等于以及等于10和15以及10与15之间的数也被认为是公开的。还应理解,两个具体单位之间的每一个单位也被公开。例如,如果10和15被公开,则11、12、13和14也被公开。
“任选的”或“任选地”意指随后描述的事件或情况可以存在或可以不存在以及描述包括其中所述事件或情况存在的情况和其中其不存在的情况。
如本文中所用的单词“或”,意指特定列表的任一个成员,并且还包括该列表的成员的任何组合。
如本文中所用的“补体介导的疾病”,是指由异常补体激活或其4个主要途径的功能引起或造成的疾病。补体途径由3个阶段组成:识别、酶促活化和导致细胞死亡的膜攻击。如本文中所用的“补体介导的疾病”,还指由经典的外源甘露聚糖结合凝集素(MBL)或旁路途径的改变引起的或造成的疾病。补体介导的疾病的实例包括但不限于非典型溶血性尿毒综合征(aHUS)、膜性增生性肾小球肾炎II型(MPGNII;也称为致密沉积物病)、全身性红斑狼疮(SLE)、化脓性感染、溶血和血栓形成、部分脂肪代谢障碍、遗传性血管水肿、阵发性睡眠性血红蛋白尿症(PNH)、年龄相关性黄斑变性(AMD)、类风湿关节炎、心肌炎、多发性硬化、IgA肾病、亨-希氏紫癜、青光眼、链球菌感染后病、抗磷脂抗体综合征、反复性妊娠失败、哮喘、抗体介导的皮肤病和抗核质抗原相关的寡免疫脉管炎。
如本文中所用的“单倍型”,是指被一起传递的存在于染色体上不同基因座上的DNA序列或DNA序列的组合;取决于已在给定的一组基因座之间发生的重组事件的数目,单倍型可以是一个基因座、几个基因座或整个染色体。
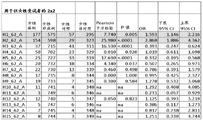
如本文中所用的“风险单位型”是指其中单倍型的存在表明当与不具有所述风险单倍型的受试者相比较时,受试者的增加的发展补体介导的疾病(例如AMD)的风险的受试者的单倍型。“风险单倍型”还指在给定的队列中在患有补体介导的疾病(例如AMD)的受试者(病例)中比在未患补体介导的疾病(例如AMD)的受试者(对照)中更常存在的单倍型。换句话说,病例对对照百分比在病例中与在对照中是不同,如在本文中的表中举例说明的(参见图15)。虽然不是必需的,但患有补体介导的疾病(例如AMD)的受试者(病例)的数目与未患补体介导的疾病(例如AMD)的受试者(对照)的数目之差在统计上可以是显著的。例如,H2_62_A、H2_51_A和H2_51_B当它们与AMD关联时,是“风险单倍型”的实例。
如本文中所用的“保护性单倍型”,是指其中单倍型的存在表明当与不具有所述保护性单倍型的受试者比较时,受试者的减小的发展补体介导的疾病(例如AMD)的风险的受试者的单倍型。“保护性单倍型”还指在患有补体介导的疾病(例如AMD)的受试者(病例)中比在未患补体介导的疾病(例如AMD)的受试者(对照)中更少存在的单倍型,换句话说,病例对对照百分比在病例中比在对照中低,如本文中的表中举例说明的(参见图15)。虽然不是必需的,但患有补体介导的疾病(例如AMD)的受试者(病例)的数目与未患补体介导的疾病(例如AMD)的受试者(对照)的数目之差在统计上可以是显著的。例如,H5_62_A、H5_51_A和H5_51_B当它们与AMD关联时,是“保护性单倍型”的实例。
如本文中所用的“中性单倍型”,是指其中单倍型的存在不表明受试者的增加的或减小的发展补体介导的疾病(例如AMD)的风险的受试者的单倍型。“中性单倍型”还指在患有补体介导的疾病(例如AMD)的受试者(病例)中和在未患补体介导的疾病(例如AMD)的受试者(对照)中大致等同地存在的单倍型,换句话说,病例对对照百分比在病例和对照中大致相等,如本文中的表中举例说明的(参见图15)。虽然不是必需的,但患有补体介导的疾病(例如AMD)的受试者(病例)的数目与未患补体介导的疾病(例如AMD)的受试者(对照)的数目之差在统计上可以是显著的。例如,H4_62_A、H4_51_A和H4_51_B当它们与AMD关联时,是“中性单倍型”的实例。
本文中描述的单倍型可按通用命名法命名为:“Hx_Y_Z”,其中“Hx”表示特定单倍型的编号,如通过特定单倍型在给定的群体或队列中的频率测定的。例如,H2表示以第二高的频率存在于给定的数据组、群体或队列中的特定单倍型。“Y”,在该命名法的背景中,特指从其测定全部单倍型的SNP的小组。例如,Hx_62_Z是指如本文中所述的62SNP小组,然而Hx_51_Z是指如本文中所述的51SNP小组。“Z”,在该命名法的背景中,是指用于确定特定单倍型的特定队列。例如,Hx_Y_A是指如本文中所述的‘927队列’,然而Hx_Y_B是指如本文中所述的组合队列。
“单倍型标记单倍型”是指可标记本文中描述的单倍型的一个或多个的单倍型。这样的单倍型可以称为“标记单倍型”。这样的标记单倍型可基于本文中描述的HapMap分析来鉴定。当在本文中引用这样的标记单倍型时,可使用通用命名法:“Hx_Y_Z_t”,其中“t”代表“标记单倍型”并且Hx、Y和Z代表与上文中针对通用命名法“Hx_Y_Z”所描述的相同的范畴。例如,H2_62_A_1表示标记H2_62_A单倍型的第一单倍型。
如本文中所用的“主单倍型”是指存在于超过1%的群体、数据集或待检查的队列中的单倍型。
如本文中所用的“次单倍型”是指存在于1%或低于1%的群体、数据集或待检查的队列中的单倍型。
如本文中所用的“CFH-至-F13B基因座”是指包含下列基因和假基因的染色体1q25-q31的区域(大致196,580,000至197,053,000;hg19):补体因子H(CFH)及其截短同种型(CFHT)、补体因子H相关基因3、1、4、2和5(CFHR3、CFHR1、CFHR4、CFHR2和CFHR5)、CFHR假基因()以及因子13B(F13B)。CFH-至-F13B基因座包括所有非基因DNA,包括近端延伸至CFH和远端延伸至F13B的非基因DNA。还包括始于CFH-至-F13B内并且近端延伸至CFH和/或远端延伸至F13b的连锁不平衡(LD)的区域。
如本文中所用的“62SNP小组”是指基于它们的关联的显著性以及被选择来提供横跨整个CFH-至-F13B基因座及其LD区域的覆盖的位置进行选择的62个SNP。62个SNP小组由图17中显示的SNP组成。
如本文中所用的“51SNP小组”是指本文中描述的62SNP小组中的51个SNP。51SNP小组由图15中显示的SNP组成。
如本文中所用的“HapMap”是指作为存在于人类中的常见遗传变体的目录的人基因组的单倍型图谱。HapMap描述了这些变体是什么,它们在DNA中存在的位置,它们在单倍型中如何分布,以及它们在人群内的人中和在世界不同部分的群体中的频率。(The InternationalHapMap Consortium.The International HapMap Project.Nature426,789-796(2003))。
如本文中所用的“HapMap分析”是指可使用Haploview软件(Barrett JC,Fry B,Maller J,Daly MJ.Haploview:analysis andvisualization of LD and haplotype maps.Bioinformatics.2005年1月15日[PubMed ID:15297300])进行的分析。
如本文中所用的“连锁不平衡”是指两个或更多个基因座(不一定在相同染色体上)上的两个或更多个等位基因之间的非随机关联,以便等位基因的某些组合比基于它们的频率从等位基因随机形成单倍型所预期的更可能一起存在于染色体上。
A.预测高加索人受试者的患有或发展补体介导的疾病的风险的方法
本文中描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。如本文中所用的“其互补序列”意指位于本文中描述的任何SNP、单倍型或二倍体型的互补DNA或RNA链上的SNP、单倍型或二倍体型。例如,但不限于,单倍型序列“ATGC”可被转换成其互补序列“TACG”。因此,例如,如果“ATGC”代表表明受试者对患有或发展补体介导的疾病的易感性的单倍型,则其互补单倍型序列“TACG”也代表表明受试者对患有或发展补体介导的疾病的易感性的单倍型。如本文中所述,一个或多个本文中公开的单倍型的存在可表明受试者对患有或发展补体介导的疾病的易感性。在一个方面,补体介导的疾病可以是年龄相关性黄斑变性(AMD)。在另一个方面,补体介导的疾病可包括但不限于非典型溶血性尿毒综合征(aHUS)、膜性增生性肾小球肾炎II型(MPGN II;也称为致密沉积物病)、全身性红斑狼疮(SLE)、化脓性感染、溶血和血栓形成、部分脂肪代谢障碍、遗传性血管水肿、阵发性睡眠性血红蛋白尿症(PNH)、类风湿关节炎、心肌炎、多发性硬化、IgA肾病、亨-希氏紫癜、青光眼、链球菌感染后病、抗磷脂抗体综合征、反复性妊娠失败、哮喘、抗体介导的皮肤病和抗核质抗原相关的寡免疫脉管炎。
在一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者具有增加的患有或发展补体介导的疾病的风险。这样的单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H2_51_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定所述高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明受试者的增加的患有或发展补体介导的疾病的风险。在一个方面,还公开了测定高加索人受试者的增加的对患有或发展补体介导的疾病的风险易感性的方法,其中方法还包括当增加的风险被确定时给受试者施用治疗性组合物。在一个方面,还公开了测定高加索人受试者的增加的对患有或发展补体介导的疾病的风险易感性的方法,其中受试者具有增加的患有或发展补体介导的疾病的风险,并且还包括当增加的风险被确定时给受试者施用治疗性组合物。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者具有减小的患有或发展补体介导的疾病的风险。这样的单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_A、H5_51_A、H10_51_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定所述高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型表明受试者的减少的患有或发展补体介导的疾病的风险。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者不具有增加的或减小的患有或发展补体介导的疾病的风险。这样的单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H4_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。因此,本文中描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定所述高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型不表明受试者具有增加的或减少的患有或发展补体介导的疾病的风险。
如本文中所用,术语“受试者”意指个体。在一个方面,受试者是哺乳动物例如人。在另一个方面,受试者可以高加索人受试者。在其它方面,受试者可以是非人灵长类动物。非人灵长类动物包括绒猴、猴、黑猩猩、大猩猩、猩猩和长臂猿,仅举少数几例。术语“受试者”还包括家养动物例如猫、狗等,家畜(例如,牛(母牛)、马、猪、绵羊、山羊等)、实验室动物(例如,白鼬、毛丝鼠、小鼠、免、大鼠、沙鼠、豚鼠等)和鸟类(例如,鸡、火鸡、鸭、雉鸡、鸽子(pigeon)、鸽子(dove)、鹦鹉、凤头鹦鹉、鹅等)。受试者还可包括但不限于鱼(例如,斑马鱼、金鱼、罗非鱼、鲑鱼和鳟鱼)、两栖动物和爬行动物。如本文中所用的“受试者”与“患者”相同,并且术语可互换使用。
单倍型可以指单个基因、基因间序列中的或更大序列(包括基因和基因间序列,例如基因的集合或基因和基因间序列的集合)中的一组多态性。例如,单倍型可以指CFH-至-F13B基因座中的一组多态性。CFH-至-F13B基因座包含染色体1q25-q31(约196,580,000至197,053,000;hg19)的包含下列基因和假基因的染色体区域:补体因子H(CFH)及其截断的同种型(CFHT)、补体因子H相关基因3、1、4、2和5(CFHR3、CFHR1、CFHR4、CFHR2和CFHR5)、CFHR假基因和因子13B(F13B)。基因座还可包括所有非基因DNA,包括近端延伸至CFH和远端延伸至F13B的非基因DNA。基因座中还包括始于CFH-至-F13B内并且近端延伸至CFH和/或远端延伸至F13b的连锁不平衡(LD)的区域。
如本文中所用的术语“单倍型”还可指一组经发现在单个染色体上在统计上彼此相关的单核苷酸多态性(SNP)。单倍型还可指经发现在单个染色体上在统计上彼此相关的多态性(例如,SNP)与其它遗传标记(例如,插入或缺失)的组合。
术语“多态性”是指一个或多个遗传上确定的备选序列或等位基因在群体中的存在。“多态性位点”是在其上存在序列趋异的基因座。多态性位点具有至少一个等位基因。二等位基因多态性具有两个等位基因。三等位基因具有3个等位基因。二倍体生物对于等位基因形式可以是纯合的或异源的。多态性位点可以小至一个碱基对。多态性位点的实例包括:限制性长度多态性(RFLP)、可变数目串联重复序列(VNTR)、高变区、小卫星序列、二核苷酸重复、三核苷酸重复、四核苷酸重复和单序列重复。如本文中所用的“多态性”可包括一组多态性(即,单倍型)。
“单核苷酸多态性(SNP)”可在被单个核苷酸占据的多态性位点上发生,所述位点是等位基因序列之间变异的位点。所述位点之前和之后是高度保守的等位基因的序列。SNP可因在多态性位点上一个核苷酸对于另一个核苷酸的置换而产生。另一个嘌呤对一个嘌呤的替换或另一个嘧啶对一个嘧啶的替换称为转换。嘧啶对嘌呤的替换或反之亦然称为颠换。同义SNP是指编码区中一个核苷酸对另一个核苷酸的置换,所述置换不改变编码的多肽的氨基酸序列。非同义SNP是指编码区中一个核苷酸对另一个核苷酸的置换,所述置换改变编码的多肽的氨基酸序列。SNP还可因相对于参照等位基因核苷酸的缺失或插入而产生。
一“组”多态型意指例如CFH-至-F13B基因座中的一个或多个多态型,例如至少1个、至少2个、至少3个、至少4个、至少5个、至少6个或至少6个已知的多态型。
如本文中所用的“核酸”、“多核苷酸”或“寡核苷酸”可以是具有任何长度的核苷酸的聚合物形式,可以是DNA或RNA,并且可以是单链或双链的。核酸可包括启动子或其它调控序列。寡核苷酸可通过合成方法来制备。核酸包括横跨或侧翼连接CFH-至-F13B基因座中已知的多态性位点之任一的DNA的区段,或其互补序列。区段可以是5至100个连续碱基并且可从5、10、15、20或25个核苷酸的下限变化至10、15、20、25、30、50或100个核苷酸的上限(其中上限大于下限)。5-10、5-20、10-20、12-30、15-30、10-50、20-50或20-100个碱基的核苷酸是常见的。多态性位点可存在于区段的任何位置内。提及的双链核酸的一条链的序列定义了互补序列,并且除非根据上下文另有所指外,否则核酸的一条链也指其互补链。
本文中描述的“核苷酸”是指当连接时产生核酸RNA和DNA的单个结构单位的分子。核苷酸由核碱基(含氮碱基)、五碳糖(核糖或2-脱氧核糖)和一个磷酸基团组成。“核酸”是由核苷酸单体组成的聚合物大分子。在DNA中,嘌呤碱基是腺嘌呤(A)和鸟嘌呤(G),而嘧啶是胸腺嘧啶(T)和胞嘧啶(C)。RNA使用尿嘧啶(U)替代胸腺嘧啶(T)。如图中所用,“S”表示短的;“L”表示“长的”,“D”在SNP分析的背景中表示缺失的。为了序列的缘故,“S”、“L”和“D”表示为“N”,其指确定的位置上的任何具体的核苷酸。
CFH-至-F13B基因座中的示例性多态性位点在本文中作为实例进行了描述并且无意是限定性的。这些多态性位点、SNP或单倍型还可用于进行本文中描述的方法。此外,应理解这些CFH-至-F13B基因座多态性用于连锁和关联研究,对临床群体进行基因分型,使基因型信息与表型信息相关联,杂合性丢失分析,细胞样品的来源的鉴定,并且还可用于将潜在治疗剂靶向细胞。
应理解,本文中未明确描述的CFH-至-F13B基因座中的其它多态性位点还可改善该分析。在CFH-至-F13B基因座中使用非同义多态性的SNP分析可用于鉴定变体多肽。与风险关联的其它SNP可编码蛋白质,所述蛋白质与由中性或保护性SNP编码的蛋白质具有相同的序列,但在启动子或内含子中包含等位基因,例如,改变基因表达的水平和位点。还应理解,可将CFH-至-F13B基因座中的多态性与相邻基因中的变异发生关联。相邻基因中的变异可导致编码的蛋白质的表达或形式的改变,并且在携带者中具有有害或保护性效应。
如本文中所用的术语“变体”还可指其中序列与群体中最普遍的序列相异例如一个核苷酸(在本文中描述的SNP的情况下)的核苷酸序列。例如,CFH-至-F13B基因座的核苷酸序列中的一些变异或置换改变密码子,以便不同的氨基酸被编码,从而导致变体多肽。术语“变体”还可指其中序列在不改变编码的多肽的氨基酸序列(即,保守变化)的位置上与群体中出现最多的序列不同的多肽。变体多肽可由风险单倍型编码,由保护性单倍型编码,或可由中性单倍型编码。变体多肽可与风险关联,与保护作用相关,或可以是中性的。
本文中描述的方法和材料可用于确定受试者(例如,人)的核酸是否包含多态性,例如单核苷酸多态性(SNP)。例如,本文中提供的方法和材料可用于确定受试者是否具有变体SNP。可使用任何方法检测CFH-至-F13B基因座中的多态性。例如,多态性可通过对外显子、内含子或非翻译序列进行测序、变性高效液相色谱(DHPLC)、等位基因特异性杂交、等位基因特异性限制酶切消化、突变特异性聚合酶链式反应、单链构象多态性检测和此类方法的组合来检测。
在一个方面,可在从受试者分离的靶核酸中检测到多态性。通常分析基因组DNA。为了进行基因组DNA的测定,实际上包含基因组DNA或RNA的任何生物样品例如有核细胞都是适当的。例如,在本文实施例部分描述的实验中,基因组DNA获自从病例和对照受试者收集的外周血白细胞(QIAamp DNA Blood Maxi试剂盒,Qiagen,Valencia,Calif.)。其它适当的样品包括但不限于唾液、刮脸碎屑、视网膜、肾或肝或其它器官或组织的活检组织;皮肤活检组织;羊水或CNS样品等。在一个方面,可测定RNA或cDNA。在一个方面,测定可检测由存在于CFH-至-F13B中的一个或多个基因编码的变体蛋白。用于从用于诊断或其它测定的患者样品纯化或部分纯化核酸或蛋白质的方法在本领域是已知的。
“分离的核酸”或“纯化的核酸”意指不含在本发明的DNA所源自的生物的天然存在的基因组中侧翼连接所述基因的基因的DNA。术语因而包括例如被整合进入载体例如自主复制的质粒或病毒的重组DNA;或被整合进入原核或真核生物的基因组DNA(例如,转基因)的重组DNA;或作为单独的分子存在的重组DNA(例如,通过PCR、限制性内切核酸酶消化或化学合成或体外合成产生的cDNA或基因组或cDNA片段)。其还包括作为编码额外多肽序列的融合基因的部分的重组DNA。术语“分离的核酸”还指RNA,例如由分离的DNA分子编码的,或化学合成的,或与至少一些细胞组分(例如其它类型的RNA分子或多肽分子)分离的或大体上不含所述组分的mRNA分子。
可使用本领域已知的几个方法的任何方法测定受试者例如待分析的患者的占据CFH-至-F13B基因座中的多态性位点的碱基的身份。例如,但不限于等位基因特异性探针的使用、等位基因特异性引物的使用、直接序列分析、变性梯度凝胶电泳(DGGE)分析、单链构象多态性(SSCP)分析和变性高效液相色谱(DHPLC)分析。检测DNA中的多态性的其它公知方法包括如下技术的使用:分子信标技术(参见,例如,Piatek等人,1998;Nat.Biotechnol.16:359-63;Tyagi和Kramer,1996,Nat.Biotechnology14:303-308;以及Tyagi等人,1998,Nat.Biotechnol.16:49-53)、侵入者技术(参见,例如,Neri等人,2000,Advances in Nucleic Acid and Protein Analysis3826:117-125和美国专利No.6,706,471)、基于核酸序列的扩增(Nasba)(Compton,1991)、Scorpion技术(Thelwell等人,2000,Nuc.Acids Res,28:3752-3761和Solinas等人,2001,″Duplex Scorpion primers in SNP analysis andFRETapplications″Nuc.Acids Res,29:20.)、限制性片段长度多态性(RFLP)分析等。其它方法对于本领域技术人员来说将是显然易见的。
术语“引物”是指能够在适当的条件下,在适当的缓冲液中和在适当的温度下用作模板指导的DNA合成的起始点的单链寡核苷酸。引物的适当长度取决于引物的期望用途,但通常为15至30个核苷酸。引物序列不必与模板完全互补,但必须充分互补以与模板杂交。术语“引物位点”是指引物所杂交至的靶DNA的区域。术语“引物对”意指包括与待扩增的DNA序列的5′末端杂交的5′上游引物和与待扩增的序列的3′末端的互补序列杂交的3′下游引物的一组引物。
用于短的探针和引物的示例性杂交条件为低于计算的Tm约5至12℃。用于计算Tm的公式是已知的,包括:Tm=4℃x(引物中的G和C的数目)+2℃x(引物中的A和T的数目)(对于少14个碱基的寡核苷酸并且假定在50mM单价阳离子存在的情况下进行反应)。对于更长的寡核苷酸,可使用下列公式:Tm=64.9℃+41℃x(引物中的G和C的数目-16.4)/N,其中N是引物的长度。另一个通常使用的公式考虑了反应的盐浓度(Rychlik,同上,Sambrook,同上,Mueller,同上):Tm=81.5℃+16.6℃x(log10[Na+]+[K+])+0.41℃x(%GC)-675/N,其中N是寡核苷酸中的核苷酸的数目。上述公式提供了用于某些应用的起始点;然而,特定探针和引物的设计可考虑另外或不同的因素。用于设计用于本发明的方法的探针和引物的方法在本领域是公知的。
用于分析多态性的等位基因特异性探针的设计和使用如由例如Saiki等人,1986;Dattagupta,EP235,726,Saiki,WO89/11548所描述的。简而言之,等位基因特异性探针被设计来与来自个体的靶DNA的区段杂交但不与来自另一个个体的对应区段杂交,如果两个区段代表不同多态性形式的话。选择杂交条件,所述条件足够严格,以便给定的探针基本上只与等位基因之一杂交。通常地,等位基因特异性探针可被设计来与靶DNA的区段杂交,以便多态性位点与探针的中心位置对齐。
如本文中所用,“探针”是能够以碱基特异性方式结合核酸的互补链的核酸。此类探针包括核酸和肽核酸(Nielsen等人,1991)。可在本领域已知的严格条件下进行杂交。例如,参见Berge和Kimmel(1987)Methods In Enzymology,第152:Guide To Molecular CloningTechniques,San Diego:Academic Press,Inc.;Sambrook等人(1989)Molecular Cloning:A Laboratory Manual,第2版,第1-3卷,ColdSpring Harbor Laboratory;Sambook(2001)第3版;Rychlik,W.和Rhoads,R.E.,1989,Nucl.Acids Res.17,8543;Mueller,P.R.等人(1993)In:Current Protocols in Molecular Biology15.5,Greene PublishingAssociates,Inc.以及John Wiley和Sons,New York;以及Anderson和Young,Quantitative Filter Hybridization in Nucleic AcidHybridization(1985))。如本文中所用的术语“探针”包括引物。探针和引物有时称为“寡核苷酸”。
等位基因特异性探针可成对使用,对的一个成员被设计来与靶序列的参照等位基因杂交,另一个成员被设计来与变体等位基因杂交。可将几对探针固定在相同支持载体上以同时分析相同靶基因序列内的多个多态性。
用于分析多态性的等位基因特异性引物的设计和使用由例如WO93/22456和Gibbs,1989进行了描述。简而言之,等位基因特异性引物被设计来仅当引物显示对特定等位基因形式的完全互补性时,才与靶DNA上与多态性重叠的位点杂交并且按照标准PCR方案引发DNA扩增。单碱基错配阻止DNA扩增并且无可检测的PCR产物形成。当多态性位点在引物的最3′末端时,该方法表现最好,因为该位置最容易脱离从引物延伸。
在一些实施方案中,基因组DNA可用于检测CFH-至-F13B基因座中的多态性。可从样品例如外周血样品或组织样品提取基因组DNA。标准方法可用于从样品提取(例如酚提取)基因组DNA。在一些情况下,可使用商购可得的试剂盒(例如,来自Qiagen,Chatsworth,Calif.;Promega,Madison,Wis.;或Gentra Systems,Minneapolis,Minn.)提取基因组DNA。
用于检测多态性的其它方法包括从获自受试者的样品扩增核酸(例如,使用CFH-至-F13B基因座特异性引物扩增来自CFH-至-F13B基因座的核酸的区段)和分析扩增的核酸。这可通过标准聚合酶链式反应(PCR、qPCT和RT-PCR)方案或本领域已知的其它方法来实现。扩增可导致CFH/F13B等位基因特异性寡核苷酸产生,所述寡核苷酸覆盖CFH-至-F13B基因座中的单核苷酸多态性位点。CFH/F13B特异性引物序列和CFH/F13B等位基因特异性寡核苷酸可来源于CFH-至-F13B基因座的编码(外显子)或非编码(启动子、5′非翻译、内含子或3′非翻译)区。在一个方面,可利用QIAamp DNA Blood Maxi试剂盒(Qiagen,Valencia,CA),从外周血白细胞分离所有受试者的基因组DNA。可筛选DNA样品的CFH-至-F13B基因座内包含的基因中的SNP。可在5uL的反应中,使用10ng模板DNA,通过TaqMan测定(Applied Biosystems,Foster City,California)来进行基因分型。384孔热循环仪(PTC-225,MJ Research)中的热循环条件可由如下方面组成:在95℃初始保持10分钟,随后进行40个循环(15秒95℃的变性步骤和1分钟60℃的退火和延伸步骤)。可在7900HT Fast Real-Time PCR系统(Applied Biosystems)读取板。
使用PCR产生的扩增产物可通过使用变性梯度凝胶电泳(DGGE)来分析。可基于序列依赖性解链性质和在溶液中的电泳迁移鉴定不同的等位基因。参见Erlich编,PCR Technology,Principles andApplications for DNA Amplification,第7章(W.H.Freeman和Co,NewYork,1992)。
靶序列的等位基因可使用单链构象多态性(SSCP)分析来区分。可基于单链PCR产物的序列和结构依赖性电泳迁移鉴定不同的等位基因(Orita等人,1989)。可按照标准方案产生扩增的PCR产物,加热PCR产物,或另外地使PCR产物变性以形成单链产物,所述单链产物可重新折叠或形成部分依赖于碱基序列的二级结构。
可使用变性高效液相色谱(DHPLC)分析区分靶序列的等位基因。可通过单链PCR产物的色谱迁移的改变,基于碱基差异来鉴定不同的等位基因(Frueh和Noyer-Weidner,2003)。可按照标准方案产生扩增的PCR产物,加热PCR产物或另外地使其变性以形成单链产物,所述单链产物可重新折叠或形成部分依赖于碱基序列的二级结构。
可使用本领域公知的DNA测序方法进行多态性的直接序列分析。参见Sambrook等人,Molecular Cloning,A Laboratory Manual(第2版,CSHP,New York1989)和Zyskind等人,Recombinant DNALaboratory Manual(Acad.Press,1988)。
用于检测生物样品中的多态性的多种其它方法在本领域是已知的。参见,例如,Ullman等人“Methods for single nucleotidepolymorphism detection”美国专利No.6,632,606;Shi,2002,“Technologies for individual genotyping:detection of geneticpolymorphisms in drug targets and disease genes”Am JPharmacogenomics2:197-205;Kwok等人,2003,“Detection of singlenucleotide polymorphisms”Curr Issues Biol.5:43-60)。
本文中还描述了用于测定女性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定女性高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。
在一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者具有增加的患有或发展补体介导的疾病的风险。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H1_62_A、H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于测定女性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明女性受试者的增加的患有或发展补体介导的疾病的风险。
在另一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者具有减少的患有或发展补体介导的疾病的风险。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于测定女性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型表明女性受试者的减少的患有或发展补体介导的疾病的风险。
在另一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者不具有增加的或减少的患有或发展补体介导的疾病的风险。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。因此,本文中描述了用于测定女性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型不表明男性受试者具有增加的或减少的患有或发展补体介导的疾病的风险。
本文中还描述了用于测定男性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定男性高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B或其互补序列。
在一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者具有增加的患有或发展补体介导的疾病的风险。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于测定男性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明男性受试者具有增加的患有或发展补体介导的疾病的风险。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者具有减少的患有或发展补体介导的疾病的风险。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H11_62_A、H3_51_B、H14_51_B或其互补序列。因此,本文中描述了用于测定男性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型表明男性受试者具有减少的患有或发展补体介导的疾病的风险。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者具有增加的或减少的患有或发展补体介导的疾病的风险。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其补体。因此,本文中描述了用于测定男性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型未指明男性受试者具有增加的或减少的患有或发展补体介导的疾病的风险。
在一个方面,可从获自受试者的样品测定本文中描述的SNP、单倍型或二倍体型。在另一个方面,受试者的SNP、单倍型或二倍体型可通过扩增获自受试者的核酸样品或对其进行测序来测定。在其它方面,本文中描述的方法还可包括给受试者施用治疗性组合物或用有效量的治疗性组合物治疗受试者。
如本文中所用,“治疗”是指意欲治愈、改善、稳定或预防疾病、病理状况或障碍的患者的医学管理。该术语包括主动治疗,即,特异性导向疾病、病理状况或障碍的改善的治疗,还包括病因治疗,即,导向除去相关疾病、病理状况或障碍的原因的治疗。此外,该术语包括姑息治疗,即,被设计用于缓解症状而非治愈疾病、病理状况或障碍的治疗;预防性治疗,即,导向使相关疾病、病理状况或障碍的发展减轻至最低程度,或部分或完全抑制所述疾病、病理状况或障碍的发展的治疗;和支持性治疗,即,用于补充导向相关疾病、病症状况或障碍的改善的另一种特异疗法的治疗。在不同方面,该术语涵盖受试者,包括哺乳动物(例如,人),的任何治疗,并且包括:(i)防止疾病在可对疾病易感但还未被诊断为患有所述疾病的受试者中发生;(ii)抑制疾病,即阻止其发展;或(iii)缓解疾病,即,引起疾病的消退。
术语“施用”和“给药”是指给受试者提供药物制剂的任何方法。此类方法对于本领域技术人员来说是公知的,包括但不限于口服施用、舌下施用、经颊粘膜施用、经皮肤施用、通过吸入施用、经鼻施用、局部施用、阴道内施用、经眼施用、鼻内施用、大脑内施用、鞘内施用、直肠施用、腹膜内施用和胃肠外施用,包括可注射途径例如静脉内施用、动脉内施用、肌内施用、真皮内施用和皮下施用。经眼施用可包括局部施用、结膜下施用、眼球筋膜囊下施用、眼球上施用、眼球后施用、眼眶内施用和眼内施用,所述眼内施用包括玻璃体内施用。施用可以是连续的或间歇性的。在不同的方面,可治疗性施用制剂;即,施用以治疗现有疾病或病况。在其它不同方面,可预防性施用制剂;即,施用以预防疾病或病况。
如本文中所用的术语“治疗有效量”是指足以实现期望的结果或对不期望的病况具有作用的量。
在另一个方面,用于测定高加索人受试者对患有或发展本文中描述的补体介导的疾病的易感性还可包括利用眼科方法检查受试者。
可进行本领域技术人员已知的各种眼科方法来检查受试者,包括但不限于自体荧光成像技术、红外成像技术、相干光断层扫描术(OCT)、Stratus相干光断层扫描术(Stratus OCT)、傅里叶频域相干光断层扫描术(Fd-OCT)、双光子激发荧光(TPEF)成像、自适应光学扫描激光眼底镜检查(AOSLO)、扫描激光眼底镜检查、与近红外线成像-频域相干光断层扫描术(SD-OCT)、眼底彩色照相、眼底自发荧光成像、无红共焦成像、荧光素血管造影术、吲哚青绿血管造影、多焦视网膜电图(ERG)记录、微视野仪、彩色多普勒光学相干层析术(CDOCT)和视野评估。此外,可通过使用Heidelberg Spectralis、Zeiss Cirrus、Topcon3D OCT2000、Optivue RTVue SD-OCT、Opko OCT SLO、NIDEK F-10或Optopol SOCT Copernicus HR来检查受试者。
1.预测疾病的进展
本文中还描述了用于预测高加索人受试者的补体介导的疾病的进展的方法。补体介导的疾病可以是,但不限于年龄相关性黄斑变性。在一个方面,该方法包括测定高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。如本文中所述,一个或多个本文中公开的单倍型的存在可表明受试者对患有或发展晚期年龄相关性黄斑变性的易感性。
在一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者有增加的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H2_51_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于测定高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_A、H5_51_A、H10_51_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于测定高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者不具有增加的或减少的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H4_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。因此,本文中描述了用于测定高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型表不明受试者具有增加的或减加的患有或发展晚期年龄相关性黄斑变性的风险。
本文中还描述了用于测定女性高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定女性高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。
在一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H1_62_A、H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于测定女高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明女性受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。
在另一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于测定女高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型表明女性受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。
在另一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者不具有增加的或减少的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。因此,本文中描述了用于测定女高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型不表明女性受试者具有增加的或减少的患有或发展晚期年龄相关性黄斑变性的风险。
本文中还描述了用于测定男性高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定男性高加索人受试者的一个或多个主或次单倍型的身份。H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B或其互补序列。
在一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于测定男性高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H11_62_A、H3_51_B、H14_51_B或其互补序列。因此,本文中描述了用于测定男性高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者不具有增加的或减少的患有或发展晚期年龄相关性黄斑变性的风险。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。因此,本文中描述了用于测定男性高加索人受试者对患有或发展晚期年龄相关性黄斑变性的易感性的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型不表明男性受试者具有增加的或减少的患有或发展晚期年龄相关性黄斑变性的风险。
2.二倍体型
本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的方法,包括测定高加索人受试者的一个或多个本文中描述的二倍体型的身份。人常染色体通常成对存在,并且在一个个体中这两个单倍型的组合在本文中称为“二倍体型”。这样,“基于”,当用于“基于”单倍型的二倍体型的上下文中时,可以指鉴定一个个体中的这两个单倍型的组合。
本文中描述的单倍型可用于产生二倍体型。例如,二倍体型可包含保护性单倍型和风险单倍型、两个保护性单倍型、两个风险单倍型、中性单倍型和风险单倍型、中性单倍型和保护性单倍型或两个中性单倍型。在一个方面,一个单倍型可以是显性的或一个单倍型可以是隐性的。
例如,但不限于,单个H1单倍型,当与另一个H1单倍型组合时,可以是H1_Y_Z:H1_Y_Z二倍体型;单个H1单倍型,当组合H2、H8或H13单倍型时,可以是H1_Y_Z:H2_Y_Z二倍体型、H1_Y_Z:H8_Y_Z二倍体型或H1_Y_Z:H13_Y_Z二倍体型。在一个方面,本文中描述的二倍体型可与增加的发展AMD的风险关联。在另一个方面,本文中描述的二倍体型可与减少的发展AMD的风险关联。
本文中描述了用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者对患有或发展年龄相关性黄斑变性的易感性。在一个方面,可从获自受试者的样品来测定受试者的单倍型。在一些方面,受试者单倍型可通过扩增获自受试者的核酸样品或对其进行测序来测定。
本文中描述了用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者对患有或发展年龄相关性黄斑变性的易感性。
本文中描述了用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。
在一些其中增加的风险被鉴定的方面,该方法还包括给受试者施用治疗性组合物。
本文中描述了用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。
在一些方面,受试者是女性。在一些其中受试者是女性的方面,图37中鉴定的二倍体型的一个或多个可用于表明受试者具有患有或发展年龄相关性黄斑变性的风险。
在一些方面,受试者是男性。在一些其中受试者是男性的方面,图36中鉴定的二倍体型的一个或多个可用于表明受试者具有患有或发展年龄相关性黄斑变性的风险。
本文中描述了鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者是否需要治疗年龄相关性黄斑变性。
在一些方面,可从获自受试者的样品受试者的单倍型。在一些方面,受试者的单倍型可通过扩增获自受试者的核酸样品或对其进行测序来测定。
本文中描述了鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表示受试者需要治疗年龄相关性黄斑变性。
本文中描述了鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
本文中描述了鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中图36中鉴定的二倍体型的一个或多个或其互补序列的存在可用于确定所述受试者是否可能需要治疗年龄相关性黄斑变性。在一些方面,受试者是女性。在一些其中受试者是女性的方面,图37中鉴定的二倍体型的一个或多个可用于些确定受试者是否需要治疗年龄相关性黄斑变性。在一些方面,受试者是男性。在一些其中受试者是男性的方面,图36中鉴定的二倍体型的一个或多个可用于确定受试者是否需要治疗年龄相关性黄斑变性。
本文中描述了鉴定需要预防性治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者是否需要预防性治疗年龄相关性黄斑变性。
本文中描述了鉴定需要预防性治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表明所述受试者需要预防性治疗年龄相关性黄斑变性。
本文中描述了鉴定需要预防性治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
本文中描述了鉴定需要预防性治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中图36中鉴定的二倍体型的一个或多个或其互补序列的存在可用于确定所述受试者是否可需要预防性治疗年龄相关性黄斑变性。
本文中描述了鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明受试者是否适合进行临床试验。
本文中描述了鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表明所述受试者适合进行临床试验。
本文中描述了鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明所述受试者不适合进行临床试验。
本文中描述了鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,其中图36中鉴定的二倍体型的一个或多个或其互补序列的存在表明所述受试者可以适合进行临床试验。
3.单倍型标记SNP
本文中描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以是,但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者对患有或发展年龄相关性黄斑变性的易感性。在另一个方面,SNP可以是单倍型标记SNP(htSNP)。如本文中所用,单倍型标记SNP意指可鉴定或代表本文中描述的单倍型或多个单倍型的SNP或多个SNP。标记SNP或多个标记SNP可用于鉴定或描述受试者的单倍型或多个单倍型,因此,可用于测定受试者对患有或发展补体介导的疾病的易感性。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。
本文中还描述了用于测定女性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定女性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以是,但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者对患有或发展补体介导的疾病的易感性。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的G可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在其它方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。
本文中还描述了用于测定男性高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定男性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可包括但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在表明受试者对患有或发展补体介导的疾病的易感性。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者具有增加的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。
本文中还描述了用于预测高加索人受试者的补体介导的疾病的进展的方法,包括测定高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以是,但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153、rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者具有患有或发展晚期年龄相关性黄斑变性的风险。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。
本文中还描述了用于预测女性高加索人受试者的补体介导的疾病的进展的方法,包括测定女性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以包括但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在表明受试者具有患有或发展晚期年龄相关性黄斑变性的风险。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的G可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。
本文中还描述了用于预测男性高加索人受试者的补体介导的疾病的进展的方法,包括测定男性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以包括但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者具有患有或发展晚期年龄相关性黄斑变性的风险。
在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。
4.单个SNP
本文中描述了由CFH-至-F13B基因座中的多个变异组成的大量多态性和单倍型。这些多态性或单倍型的一个或多个可与补体介导的疾病相关联。这些和其它多态性以及多态性的组(例如,单倍型)的检测可用于设计和进行补体介导的疾病的诊断测定。多态性和成组的多态性可通过分析核酸,通过分析由CFH-至-F13B基因座编码序列编码的多肽(包括由剪接变体编码的多肽),通过分析CFH-至-F13B基因座非编码序列或通过本领域已知的其它方法来检测。此类多态性和单倍型的分析还可用于设计用于补体介导的疾病的预防性和治疗性方案。
更具体地,本文中描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份。在一个方面,SNP可包括但不限于:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP。在另一个方面,本文中描述的SNP的一个或多个的存在可表明受试者对患有或发展年龄相关性黄斑变性的易感性。
在一个方面,rs1061170SNP上的A可表明受试者具有增加的患有或发展补体介导的疾病的风险。在另一个方面,rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G可表明受试者具有减少的患有或发展补体介导的疾病的风险。在另一个方面,rs3753396SNP上的G不表明受试者具有增加的或减少的患有或发展年龄相关性黄斑变性的风险。
本文中还描述了用于预测高加索人受试者的年龄相关性黄斑变性的进展的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份。在一个方面,SNP可包括但不限于:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP。在另一个方面,本文中描述的SNP的一个或多个的存在可表明受试者具有患有或发展晚期年龄相关性黄斑变性的风险。
在一个方面,rs1061170SNP上的A可表明受试者具有增加的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs3753396SNP上的G不表明受试者具有增加的或减少的患有或发展晚期年龄相关性黄斑变性的风险。
本文中还描述了筛选与本文中描述的风险、保护作用或另外地信息型SNP或遗传标记(包括但不限于CFH-至-F13B基因座中的多态性位点)处于连锁不平衡(LD)的其它基因中的多态性位点的方法。这些方法可包括鉴定与CFH-至-F13B基因座中的多态性位点处于连锁不平衡的基因中的多态性位点,其中CFH-至-F13B基因座中的多态性位点的多态性形式与补体介导的疾病相关联(例如,增加的或减少的风险),和测定个体的群体中的单倍型以表明连锁的多态性位点是否具有与CFH/F13B基因的多态性形式处于连锁不平衡的多态性形式,所述CFH/F13B基因的多态性形式与补体介导的疾病表型关联。与本文中描述的SNP处于LD的SNP包括但不限于rs10737680、rs7535263、rs10922106、rs395998、rs1329428和rs7540032。在另一个方面,与本文中描述的SNP处于LD的SNP可以是,但不限于rs10489456、rs70620、rs742855、rs11799380、rs1065489、rs11582939、rs385390、rs421820、rs426736、rs370953、rs371075。
如本文中所用,“连锁不平衡”是两个或更多个基因座(不必在相同染色体上)上的等位基因的非随机关联。其与连锁不同,所述连锁描述染色体上在它们之间具有有限重组的两个或更多个基因座的关联。连锁不平衡描述这样的情况,在所述情况中,等位基因或遗传标记的一些组合在群体中比从来自等位基因的单倍型的随机形成基于它们的频率所预期的更加频繁或更不频繁地存在。不同基因座上的多态性之间的非随机关联通过连锁不平衡(LD)的程度来测量。连锁不平衡的水平可受许多因素影响,包括遗传连锁、重组率、突变率、随机漂移、非随机交配和人口结构。“连锁不平衡”或“等位基因关联”从而意指特定等位基因或遗传标记与另一个特定等位基因或遗传标记的非随机关联,该非随机关联的频率比对于群体中任何特定等位基因的频率随机关联所预期的更高。与信息型标记例如CFH/F13B SNP或本文中描述的单倍型之一处于连锁不平衡的标记可用于检测对补体介导的疾病的易感性。与本文中描述的风险、保护作用或另外地信息型SNP、单倍型或遗传标记处于连锁不平衡的SNP可称为“取代”或“替代”SNP。取代SNP可以以至少50%、60%或70%与本文中描述的风险、保护作用或另外地信息型SNP、单倍型或遗传标记处于连锁不平衡,在一个方面以至少约80%、90%,在另一个方面以91%、92%、93%、94%、95%、96%、97%、98%、99%或约100%与本文中描述的风险、保护作用或另外地信息型SNP、单倍型或遗传标记处于LD。
公共可获得的数据库例如HapMap数据库(http://ftp.hapmap.org/ld_data/latest/)和Haploview(Barrett,J.C.等人,Bioinformatics21,263(2005))可用于计算两个SNP之间的连锁不平衡。疾病对对照群体中的鉴定的等位基因的频率可使用本文中描述的方法来测定。可将统计分析(例如,Hardy-Weinberg平衡、基因型似然比(基因型p值)、卡方分析、费希尔精确检验)用于测定两个SNP之间的非随机关联的显著性。两个SNP之间统计上显著的非随机关联表明它们处于连锁不平衡并且一个SNP可用作第二SNP的取代物。
在另一个方面,CFH-至-F13B基因座中的多态性例如本文中描述的那些多态性可用于建立与目的性状相关的遗传基因座与不与该性状相关(但与负责该性状的遗传基因座物理上接近并且与其共分离的)多态性标记之间的物理连锁。定位与目的性状相关的遗传基因座有利于按照本领域公知的方法克隆负责该性状的基因。
如本文中所用,“物理连锁”描述基因、等位基因、基因座或遗传标记因它们位于相同染色体上而被一起遗传的趋势。连锁可通过两个基因、等位基因、基因座或遗传标记之间的百分比重组来测量。通常地,在彼此相距50厘摩(cM)内存在的基因座是连锁的。连锁标记可存在于相同的基因或基因簇内。
5.缺失标记SNP
本文中公开了标记CFHR-3/CFHR-1基因的缺失状态的SNP。因此,本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的方法,包括测定受试者的CFH-至-F13B基因座中的缺失标记SNP的身份。SNP可以是,但不限于:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP。在一个方面,SNP的存在可表示受试者对患有或发展年龄相关性黄斑变性的易感性。在另一个方面,rs12144939SNP上的T可表明受试者具有减少的患有或发展年龄相关性黄斑变性的风险。在另一个方面,本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定受试者的至少一个标记本文中描述的缺失标记SNP的SNP的身份。标记SNP可以是,但不限于rs6689009、rs35253683、rs731557和rs60642321。在另一个方面,本文中还描述了用于测定高加索人受试者对患有或发展补体介导的疾病的易感性的方法,包括测定受试者的至少一个与本文中描述的缺失标记SNP处于LD的SNP的身份。SNP可以是,但不限于rs6677604、rs16840522和rs2019727。
本文中还描述了用于预测高加索人受试者的补体介导的疾病的进展的方法,包括测定受试者的CFH-至-F13B基因座中的缺失标记SNP的身份。SNP可包括但不限于:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP。在一个方面,缺失标记SNP的存在可表明受试者具有患有或发展晚期年龄相关性黄斑变性的风险。在另一个方面,rs12144939SNP上的T可表明受试者具有减少的患有或发展晚期年龄相关性黄斑变性的风险。
6.单倍型标记单倍型
在一个方面,可将本文中描述的单倍型与使用遗传变异数据库例如HapMap产生的单倍型相比较,以进一步改善单倍型与补体介导的疾病例如AMD的关联。可在http://hapmap.ncbi.nlm.nih.gov/上获得的国际HapMap Project在包括CFH-至-F13B基因座(Hg18chr1:194869137-195303491)的区域中包含超过500个SNP。因此,在一个方面,可下载这500多个SNP的每一个的高加索人个体(称为CEU群体)的基因型。随后可下载来自CEU组的定相基因型数据,包括该目的区域中提供最多信息的SNP(即在CEU群体中分离的那些SNP)。在一个方面,Haploview(www.broadinstitute.org)可用于构建CEU数据集组的单倍型以及可计算它们的频率。从该分析获得的重叠SNP可用作‘标记’SNP以将本文中描述的病例/对照单倍型与它们的等同HapMap CEU单倍型匹配,从而允许本文中描述的疾病关联扩展至等同HapMap单倍型。
在一个方面,该方法可鉴定不包括在本文中描述的基于51SNP的单倍型中的HapMap SNP。这些新鉴定的SNP还可改善本文中描述的基于51SNP的单倍型的区分值,以及这些单倍型与补体介导的疾病的关联。
本文中描述了用于鉴定标记CFH-至-F13B基因座中的一个或多个单倍型的单核苷酸多态性的方法。一个或多个单倍型可以是本文中描述为与患有或发展补体介导的疾病相关的任何单倍型。在一个方面,该方法可包括将一个或多个CFH/F13B单倍型的SNP序列输入遗传变异数据库,和测定一个或多个标记SNP或单倍型的身份。在一个方面,一个或多个CFH/F13B单倍型可以是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。
在另一个方面,遗传变异数据库可以是HapMap。在另一个方面,一个或多个CFH/F13B单倍型可以是风险单倍型,包括但不限于H2_62_A、H2_51_A、H1_51_B、H2_51_B或其互补序列。在另一个方面,一个或多个CFH/F13B单倍型可以是保护性单倍型,包括但不限于H3_62_A、H5_62_A、H11_62_A、H3_51_A、H5_51_A、H10_51_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。
B.鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法
本文中描述了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。如本文中所述,本文中公开的一个或多个单倍型的存在可表明受试者是否需要治疗补体介导的疾病。如本文中所用,“治疗”还可意指预防性或防治性治疗。在一个方面,补体介导的疾病可以是年龄相关性黄斑变性(AMD)。因此,本文中描述的方法可用于鉴定需要治疗年龄相关性黄斑变性的高加索人受试者。
在一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者需要治疗补体介导的疾病。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H2_51_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明受试者需要治疗。在一个方面,鉴定需要治疗的受试者的方法还可包括给鉴定为需要治疗的受试者施用治疗性组合物。在另一个方面,本文中描述的方法可用于鉴定需要更频繁地筛选补体介导的疾病(包括但不限于年龄相关性黄斑变性)的高加索人受试者。例如,鉴定具有风险单倍型的受试者可表明需要更密切和更频繁地监测受试者的补体介导的疾病例如AMD的发展。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者不需要治疗补体介导的疾病。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_A、H5_51_A、H10_51_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型表明受试者不需要治疗补体介导的疾病。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者需要连续筛选补体介导的疾病的发展。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H4_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。因此,本文中描述了鉴定需要筛选补体介导的疾病的发展的高加索人受试者的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型表明受试者需要筛选补体介导的疾病的发展。例如,但不限于,鉴定具有中性单倍型的受试者可表明应当在早些时候并且比通常在一般群体中进行的筛选更频繁地筛选受试者的补体介导的疾病例如AMD的发展。
本文中描述了鉴定需要治疗补体介导的疾病的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。
在一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者需要治疗补体介导的疾病。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H1_62_A、H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于鉴定需要治疗补体介导的疾病的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明女性受试者需要治疗。在一个方面,鉴定需要治疗的女性受试者的方法还可包括给鉴定为需要治疗的女性受试者施用治疗性组合物。在另一个方面,本文中描述的方法可用于鉴定需要更频繁地筛选补体介导的疾病(包括但不限于年龄相关性黄斑变性)的女性高加索人受试者。例如,鉴定具有风险单倍型的女性受试者可表明需要更密切和更频繁地监测女性受试者的补体介导的疾病例如AMD的发展。
在另一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者不需要治疗补体介导的疾病。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于鉴定需要治疗补体介导的疾病的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型可表明女性受试者不需要治疗补体介导的疾病。
在另一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者需要连续筛选补体介导的疾病的发展。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。因此,本文中描述了鉴定需要筛选补体介导的疾病的发展的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型可表明女性受试者需要筛选补体介导的疾病的发展。例如,但不限于,鉴定具有中性单倍型女性的受试者可表明应当在早些时候并且比通常在一般群体中进行的筛选更频繁地筛选女性受试者的补体介导的疾病例如AMD的发展。
本文中描述了鉴定需要治疗补体介导的疾病的男性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B或其互补序列。
在一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者需要治疗补体介导的疾病。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于鉴定需要治疗补体介导的疾病的男性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型表明男性受试者需要治疗。在一个方面,鉴定需要治疗的男性受试者的方法还可包括给鉴定为需要治疗的男性受试者施用治疗性组合物。在另一个方面,本文中描述的方法可用于鉴定需要更频繁地筛选补体介导的疾病(包括但不限于年龄相关性黄斑变性)的男性高加索人受试者。例如,鉴定具有风险单倍型的男性受试者可表明需要更密切和更频繁地监测男性受试者的补体介导的疾病例如AMD的发展。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者不需要治疗补体介导的疾病。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H11_62_A、H3_51_B、H14_51_B或其互补序列。因此,本文中描述了用于鉴定需要治疗补体介导的疾病的男性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型可表明男性受试者不需要治疗补体介导的疾病。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者需要连续筛选补体介导的疾病的发展。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_AH4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。因此,本文中描述了鉴定需要筛选补体介导的疾病的发展的男性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型表明男性受试者需要筛选补体介导的疾病的发展。例如,但不限于,鉴定具有中性单倍型男性的受试者可表明应当在早些时候并且比通常在一般群体中进行的筛选更频繁地筛选男性受试者的补体介导的疾病例如AMD的发展。
本文中还描述了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份。SNP可包括但不限于:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,一个或多个所述SNP的存在可表明受试者是否需要治疗补体介导的疾病。在一个方面,rs1061170SNP上的A可表明受试者需要治疗补体介导的疾病。在另一个方面,rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G可表明受试者不需要治疗补体介导的疾病。在另一个方面,rs3753396SNP上的G可表明受试者可能需要治疗补体介导的疾病。
本文中还描述了鉴定需要治疗补体介导的疾病的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个缺失标记SNP的身份。SNP可包括但不限于:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP。在一个方面,一个或多个所述SNP的存在可表明受试者是否需要治疗年龄相关性黄斑变性。在另一个方面,rs12144939SNP上的T可表明受试者不需要治疗年龄相关性黄斑变性。
本文中还描述了用于鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可包括但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者是否需要治疗年龄相关性黄斑变性。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不需要治疗年龄相关性黄斑变性。
本文中还描述了鉴定需要治疗补体介导的疾病的女性高加索人受试者的方法,包括测定女性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以是,但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者是否需要治疗年龄相关性黄斑变性。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的G可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不需要治疗年龄相关性黄斑变性。
本文中还描述了鉴定需要治疗补体介导的疾病的男性高加索人受试者的方法,包括测定男性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以是,但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者是否需要治疗年龄相关性黄斑变性。
在一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不需要治疗年龄相关性黄斑变性。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不需要治疗年龄相关性黄斑变性。
1.鉴定适合进行临床试验的患者的方法
此外,本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。如本文中所述,一个或多个本文中公开的单倍型的存在可表明受试者是否适合进行补体介导的疾病临床试验。在一个方面,补体介导的疾病可以是年龄相关性黄斑变性(AMD),临床试验可以是年龄相关性黄斑变性临床试验。因此,本文中描述的方法可用于鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者。如本文中所用,临床试验意指被进行以通过监测治疗或医学设备对受试者或一组受试者的作用来评价它们的效力和安全性的实验研究。在一个方面,可进行临床试验以评价用于补体介导的疾病例如AMD的药物的效力和安全性。
在一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者适合进行补体介导的疾病临床试验。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H2_51_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型可表明受试者适合进行临床试验。在一个方面,鉴定适合进行临床试验的受试者的方法还可包括给被鉴定为适合进行临床试验的受试者施用治疗性组合物。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者不适合进行补体介导的疾病临床试验。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_A、H5_51_A、H10_51_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型可表明受试者不适合进行临床试验。例如,经鉴定具有本文中描述的保护性单倍型的受试者可被排除参与被设计来评价补体介导的疾病的治疗的临床试验。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明受试者可能适合进行补体介导的疾病临床试验。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H4_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型可表明受试者可能适合进行临床试验。
此外,本文中还描述了鉴定适合进行补体介导的疾病临床试验的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。如本文中所述,一个或多个本文中公开的单倍型的存在可表明女性受试者适合进行补体介导的疾病临床试验。在一个方面,补体介导的疾病可以是年龄相关性黄斑变性(AMD),临床试验可以是年龄相关性黄斑变性临床试验。因此,本文中描述的方法可用于鉴定适合进行年龄相关性黄斑变性临床试验的女性高加索人受试者。
在一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者适合进行补体介导的疾病临床试验。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H1_62_A、H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型可表明女性受试者适合进行临床试验。在一个方面,鉴定适合进行临床试验的女性受试者的方法还可包括给被鉴定为适合进行临床试验的女性受试者施用治疗性组合物。
在另一个方面,测定女性受试者的某个单倍型或某些单倍型的身份可表明女性受试者不适合进行补体介导的疾病临床试验。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H3_62_A、H5_62_A、H11_62_A、H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型可表明女性受试者不适合进行临床试验。例如,经鉴定具有本文中描述的保护性单倍型的女性受试者可被排除参与被设计来评价补体介导的疾病的治疗的临床试验。
在另一个方面,测定受试者的某个单倍型或某些单倍型的身份可表明女性受试者可能适合进行补体介导的疾病临床试验。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H4_51_B、H6_51B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的女性高加索人受试者的方法,包括测定女性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型可表明女性受试者可能适合进行补体介导的疾病临床试验。
此外,本文中还描述了鉴定适合进行补体介导的疾病临床试验的男性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个主或次单倍型的身份。单倍型可包括但不限于H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B或其互补序列。如本文中所述,一个或多个本文中公开的单倍型的存在可表明男性受试者适合进行补体介导的疾病临床试验。在一个方面,补体介导的疾病可以是年龄相关性黄斑变性(AMD),临床试验可以是年龄相关性黄斑变性临床试验。因此,本文中描述的方法可用于鉴定适合进行年龄相关性黄斑变性临床试验的男性高加索人受试者受试者。
在一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者适合进行补体介导的疾病临床试验。此类单倍型可以是风险单倍型。例如,但不限于,风险单倍型可以是H2_62_A、H1_51_B、H2_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的女性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中风险单倍型可表明男性高加索人受试者适合进行临床试验。在一个方面,鉴定适合进行临床试验的男性受试者的方法还可包括给被鉴定为适合进行临床试验的男性受试者施用治疗性组合物。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明男性受试者不适合进行补体介导的疾病临床试验。此类单倍型可以是保护性单倍型。例如,但不限于,保护性单倍型可以是H11_62_A、H3_51_B、H14_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的男性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中保护性单倍型可表明男性受试者不适合进行临床试验。例如,经鉴定具有本文中描述的保护性单倍型的男性受试者可被排除参与被设计来评价补体介导的疾病的治疗的临床试验。
在另一个方面,测定男性受试者的某个单倍型或某些单倍型的身份可表明受试者可能适合进行补体介导的疾病临床试验。此类单倍型可以是中性单倍型。例如,但不限于,中性单倍型可以是H1_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_AH4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。因此,本文中描述了用于鉴定适合进行补体介导的疾病临床试验的男性高加索人受试者的方法,包括测定男性高加索人受试者的一个或多个本文中描述的单倍型的身份,其中中性单倍型可表明男性受试者可能适合进行补体介导的疾病临床试验。
本文中还公开了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个SNP的身份。SNP可以是,但不限于:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,本文中公开的一个或多个所述SNP的存在可表明受试者是否适合进行临床试验。在一个方面,rs1061170SNP上的A可表明受试者适合进行临床试验。在另一个方面,rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G可表明受试者不适合进行临床试验。因此,例如,当确定高加索人受试者具有rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP的G时,可将受试者从补体介导的疾病临床试验排除。在另一个方面,rs3753396SNP上的G可表明受试者可能适合者临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定受试者的CFH-至-F13B基因座中的一个或多个缺失标记SNP的身份。SNP可包括但不限于:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP。在一个方面,一个或多个所述SNP的存在可表明受试者是否适合进行临床试验。在另一个方面,rs12144939SNP上的T可表明受试者不适合进行临床试验。
本文中公开了鉴定适合进行补体介导的疾病临床试验的高加索人受试者的方法,包括测定高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以是,但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者是否适合进行临床试验。
在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不适合进行临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的女性高加索人受试者的方法,包括测定女性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可包括但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者是否适合进行临床试验。
在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的G可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不适合进行临床试验。
本文中还描述了鉴定适合进行补体介导的疾病临床试验的男性高加索人受试者的方法,包括测定男性高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份。SNP可以是,但不限于:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP。在一个方面,至少6个所述SNP的存在可表明受试者是否适合进行临床试验。
在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T可表明受试者适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C可表明受试者不适合进行临床试验。在另一个方面,rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T可表明受试者不适合进行临床试验。
本文中还公开了增强临床试验的方法,包括选择适当的患者群体来进行那些临床试验。在一个方面,该方法可用于基于它们是否对待研究的实验性治疗剂起反应来确保患者经鉴定参与临床试验。该方法可包括监测接受补体介导的疾病例如AMD的治疗的受试者的状况。成功的治疗结果可通过补体途径活性例如表达水平、生物化学活性(例如,补体成分的酶促活性)或抗补体途径相关分子的血清自身抗体从异常水平至或朝向正常水平的回归来表明。在一个方面,该方法可包括在受试者已接受治疗之前,测量异常活性的水平的初始值(例如,自身抗体的异常存在,或补体途径分子的异常水平)。随后可在一段时期进行重复测量。例如,但不限于,该时期可以为约1天、2天、5天、1周、2周、3周、1个月、2个月、3个月、4个月、6个月、9个月、1年或超过1年。如果初始水平相对于对照群体中的平均水平升高,则随后测量的水平的显著降低可表明阳性治疗结果。同样地,如果测量标记的初始水平相对于对照群体的平均值降低,则相对于初始水平测量的水平的显著升高可发出阳性治疗结果的信号。如果随后测量的水平与初始水平的重复测的平均值相异超过一个标准差的话,则随后测量的水平被认为相对于初始水平具有显著的改变。如果监测显示最性治疗结果,则这表明患者可被选择来参与该特定治疗剂的临床试验。如果监测显示阴性治疗结果,则这表明患者不应当被选择来参与该特定治疗剂的临床试验。
C.试剂盒
本文中还描述了用于利用本文中描述的方法的试剂盒。本文中描述的试剂盒可包括用于检测受试者的核酸样品中的一个或多个单倍型的测定,其中一个或多个单倍型是本文中描述的单倍型。例如,但不限于,一个或多个单倍型可以是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。在一个方面,一个或多个单倍型可以是本文中描述的单倍型标记单倍型以及图41中显示的单倍型标记单倍型。
本文中描述的试剂盒还可包括用于扩增CHF-至-F13B基因座或本文中描述的任何基因或核酸的扩增试剂。
D.实施例
提出下列实施例以便为本领域技术人员提供关于如何制备和评价本文中所要求保护的化合物、组合物、制品、装置和/或方法的完全公开内容和描述,所述实施例意欲仅为本发明的示例,并且无意限定本发明人所认为的他们的发明的范围。已作出努力来确保数字(例如,量、温度等)的准确性,但应当解释一些误差和偏差。除非另有所指,否则部分是按重量计的部分,温度以℃表示或是环境温度,压力是在大气压下或接近大气压。
1.实施例1:患者队列
将来源于良好表征的研究患者(患有AMD和未患AMD)的队列的DNA样品用于本文中描述的各种研究(参见Abrera-Abeleda等人2006;Allikmets等人2009;Baird等人2006;DeAngelis等人2008;Gold等人2006;Hageman等人,2005,2006,2011;Lim等人2012;Robman等人2010;Wickremasinghe等人2011;Zhang2008)。这些集合由超过5,000份来自患有AMD和未患AMD的高加索人患者的DNA样品组。除两个同胞对队列(一个同胞对队列显示高度不一致,一个同胞对队列同时显示不一致和一致(284个家族,657个受试者))外,所有对列都是病例-对照队列。同胞对队列的索引患者为50岁或更老,并且在至少一只眼中具有CNV,如通过在研究招募时或之前记录的视网膜下出血、纤维化或新生血管形成的荧光素血管造影的存在定义的。未受影响的同胞在高于索引患者首次被诊断出CNV时的年龄的年龄上具有正常的黄斑。病例-对照和同胞对队列中的所有个体都是超过60岁的欧裔美国人后代,并且年龄和种族性匹配。由受过训练的眼科医生检查患者并给患者照相。大部分这些患者的尿、血清、血浆、DNA和详尽的医学和眼科数据是可获得的。按照如参考资料中描述的和上文中注释的标准化分类系统将立体眼底摄影分级。对所有队列中的大部分样品的CFH至F13B基因座的变体和SNP以及其它基因(如本文中所描述的)进行基因分型。
来自几个另外的队列的DNA样品也是可获得的:1)早发型脉络膜小疣病例(EOD)(103);2)高加索人新生儿(1,870);3)MPGN II(65);非典型溶血尿毒综合征(aHUS)(211);4)青光眼(330);5)阿尔茨海默病(1,214);6)来自犹他大学遗传参照项目的45个家族(UGRP);和7)来自人多样性小组(Human Diversity Panels)的个体。此外,许多其它系统性和眼疾病示于样品的集组中。
实施例2:横跨染色体1q32CFH-至-F13B基因座的缺失状态和扩展单倍型的测定;发现期(Discovery Phase)
2.1背景
最近的遗传学研究已显示年龄相关性黄斑变性(AMD)与补体因子H基因(CFH)的特定单倍型之间的关联,所述基因位于染色体1q25-q31上的“补体活化调节剂”(RCA)基因簇内(Hageman等人2005)。尽管对与AMD关联的基因座中的核苷酸多态性的理解已增加,但疾病相关CFH风险和保护性单倍型的表征仍未进行过全面评估。最近的报导建议日本人和中国人群体中的CFH基因的风险变体与AMD无关,与高加索人群体显著不同,和/或风险单倍型以显著更低的频率存在(Lau等人2006;Gotoh等人2006)。
5个CFH相关基因(CFHR1、CFHR2、CFHR3、CFHR4和CFHR5)、一个CFHR假基因(LOC100289145)和一个额外的包含补体SCR结构域的基因(因子13B或F13B)位于染色体1q32上的补体活化调节剂(RCA)基因座内。在CFH保护性单倍型之一中已鉴定了包括CFHR1和CFHR3基因的共同缺失(Hageman等人2006)。
由于这7个基因之间的强同源性、关于该1q32基因座的显著拷贝数变异以及对该基因座内补体介导的疾病的因果关系的理解的缺乏,因此测定包括CFH的扩展单倍型、5个CFHR基因、CFHR假基因(LOC100289145)和因子13B(F13B)以及评估它们与AMD的关联。
2.2方法:研究患者样品
使用患有或未患AMD的研究患者(包括同胞对)的DNA样品。用于本研究的来自1,073个受试者的DNA样品(称为‘1,073队列’、‘GSH队列’或‘ParAllele对列’)是欧裔美国人后代并且选自更大的队列(参见上述实施例1)。受试者的平均年龄为76.2岁。59%是男性。56%的受试者具有年龄相关性黄斑病变(ARM)或年龄相关性黄斑变性(AMD),34.5%为对照。该队列中0.6%的患者可不进行分级。
2.3方法:用于发现队列的CFH-至-F13B单倍型测定和验证的策略的概述
在1,073个高加索人个体中对横跨CFH-至-F13B区域的63个SNP(图2)进行基因分级。推算丢失的基因型。最初使用单链构象多态性(SSCP)和qPCR测定(其被开发来检测单个染色体上的缺失)来评估CFHR3/CFHR1的缺失状态。使用PHASE v2.1.1对基因型进行5次独立定相,将结果组合,提取所有1,073个个体的最可能的定相单倍型。随后构建(定相)所有染色体的单倍型。在3代家族中确认单倍型有效性。使用适当的统计评估法评估单倍型和SNP疾病关联。
2.4方法:单核苷酸多态性(SNP)基因分型
使用基于SSCP的基因分型[5]、基于Taqman的基因分型(ABI)、桑格测序和分子倒置探针基因分型(ParAllele BioScience)[6]对1,073个人基因组DNA样品中的CFH-至-F13B基因座内的63个单核苷酸多态性(SNP)(包括至CFH和F13B基因的近端和远端的非基因区)(图2)进行基因分型。在ParAllele研究(其中使用Affymetrix3K‘IowaAMD小组’对1,162个DNA样品进行基因分型;终数据产生1,113个样品的成功基因型,在尝试的3,308个测定中最终成功的测定数目为3,266个)之前,基于关联的显著性以及在整个CFH-至-F13B基因座上提供相对致密的覆盖的位置选择SNP。使用PHASE v.2.1.1(Am.J.Hum.Gen.68:978-989,2001)在单倍型构建过程中对丢失的值进行乘法推算。
2.5方法:CFHR3/CFHR1缺失染色体的鉴定
使用SSCP和qPCR测定(被开发来检测单个染色体上的缺失的测定)评估CFHR-3/CFHR-1基因的缺失状态。SSCP测定用于鉴定对于CFHR3/CFHR1缺失是纯合的所有个体。通过使用一对扩增CFH外显子22和CFHR1中的同源区的PCR引物(关于引物,参见Hageman等人2006),所得的SSCP构象之一(称为‘shifT4’)是对于其两个拷贝的CFHR1都不存在的受试者的诊断。
实时定量PCR(qPCR)也用于测定CFHR3和CFHR1基因的拷贝数状态(图31)。一组5至6个独立TaqMan测定同时测量CFHR3上游的染色体DNA(‘缺失扩增子’)(通过使用6-FAM荧光信号测量)和RNA酶P的内源对照扩增子(通过使用VIC标记(Applied BiosystemsRNase P Control Reagent))的量。用于缺失测定的引物和探针的序列基于mrd_3855扩增子来进行设计。它们被命名为mrd_3855-ANYF(TCTGCT CCT GCT CTT CTT TTC C SEQ ID NO.285)、mrd_3855-ANYR(CTC TAT GCT TGC TAC AAG AGA CAC A SEQ IDNO.286)和mrd_3855-PROBE(6-FAM-AAC AGC ATG GAA TATC-MGB SEQ ID NO.287)。参照扩增子为RNA酶P,一个单拷贝基因,试剂购自Applied Biosystems(产品号4316844),其附着有VIC荧光标记。因此,可在相同rtPCR孔中同时检测缺失扩增子的FAM标记和对照扩增子的VIC标记。Applied Biosystems Fast Universal PCR预混合物提供了聚合酶和ROX外源非扩增本底荧光基团。将AppliedBiosystems7900HT Fast实时PCR系统用于所有实验。
在数据获取后,使用以R统计软件语言书写的程序进行分析。用于检测指数扩增期的最佳荧光阈值使用一组对照样品(每染色体含有一个拷贝的CFHR3/CFHR1)的系列稀释物来测定。在所有阶段扩大不确定性以获得所有样品和所有重复的Ct值的分配。如果大部分样品重复对于缺失扩增子和RNA酶P的Ct值都与正常对照相似,则样品被分类为不具有缺失染色体(纯合正常的)。对于CFHR3/CFHR1缺失是杂合的样品具有比基于它们的RNA酶P Ct值预期的晚大约1个循环的缺失扩增子的Ct值。最后,对于缺失是纯合的样品不具有缺失扩增子的扩增或几乎不具有扩增。在每一个qPCR板上进行正常对照的系列稀释物。
2.6方法:缺失预测
将缺失状态建模为二等位基因标记:对于每一条染色体缺失或无缺失(正常)。实时qPCR能够鉴定对于缺失是纯合(DD)或杂合(ND)的个体以及不包含缺失(NN)的个体。基于CFH基因座SNP的缺失状态和基因分型检出,使用R统计软件包中的rpart文库产生能够根据基因分型的SNP预测缺失状态的决策树。除了该预测树以外,还可使用对于4个在CFHR3/CFHR1基因区域中筛选的SNP(rs11807997、rs389897、rs4230或rs414628)之一是杂合的任何个体不能包含CFHR3和CFHR1的缺失的策略。所有这些SNP在缺失区域的中央部分中,并且当CFHR3和CFHR1都不存在时都不存在。
2.7方法:单倍型推断
将qPCR缺失测定用于将536个(和在第二测定中801个)个体分类为纯合缺失(DD)、杂合缺失(ND)或纯合无缺失(NN)。按照它们对于CFHR3和CFHR1中的SNP的基因型将所有剩余个体进行分类。所有在CFHR3或CFHR1中包含超过一个杂合SNP的个体被假定与任一染色体上的缺失不一致(基因型NN)。将所有其它个体被分配有一条正常染色体和一条未知染色体(N?)。对于CFH与CFHR4之间的那些SNP,所有杂合缺失个体被分配给一个未知的等位基因(缺失的区域);利用一个已知的和一个未知的等位基因(C?)替代该区域中的纯合SNP(例如CC),然而与杂合缺失不一致的杂合SNP用两个未知的等位基因(??)来替代。对于相同区域中的每一个SNP,所有纯合缺失个体被分配了2个未知的等位基因(??)。
PHASE2.1.1版用于推算每一个个体的丢失的基因型和相基因型,需小心地正确地将CFHR3/1SNP的存在或缺失归为一组。使用参照人基因组(构造18)从NCBI dbSNP构造129获得每一个SNP的染色体位置。使用横跨rs11807997至rs414628的缺失区域中的4个SNP,将在CFHR3/CFHR1区域中的SNP和7个不同的-SNP单倍型上分型的所有个体归入CFHR3/CFHR1缺失区。将PHASE的5个独立运行用于确认单倍型一致性,并且将2个单倍型分配至每一个个体。7个不同的4-SNP单倍型被归入该区域。虽然前两个单倍型足以定相99%的染色体,但随后使用全部7个推算的单倍型来避免定相基因型的过度拟合。
检测状态随后被处理为八等位基因SNP-该SNP对于七个推算的CFHR-3/CFHR-1单倍型中的每一个以及第8个等位基因表示为缺失。从而将整个CFH基因座建模为58个二等位基因和一个八等位基因SNP。PHASE的5个独立运行用于推算和定相基因型。PHASE的5个独立运行用于确认定相基因型一致性。在基因型定相后,将多等位基因缺失状态向后扩展进入4个独立的三等位基因SNP,D等位基因代表缺失单倍型。在一些评估中,将所有具有小于1%的频率的次单倍型反复重新分配至最相似的剩余单倍型。
PHASE为所有个体提供了概率加权的、推算的和定相的基因型。PHASE的每一个运行产生每一个个体的定相基因型的多个加权估计值(使用来自PHASE的对输出文件)。PHASE的5个独立运行产生达到5个不同的丢失基因型的推算,随后对所有所述基因型同等地加权。为了将最后一对单倍型分配至每一个个体,使用下列算法:1)输入是其中每一个个体具有一组潜在二倍体型和其估计概率(来自PHASE对输出文件)的个体的集合;2)初始化活性组以包括所有可能的单倍型;3)基于个体的二倍体概率分配个体二倍体型,限制是二倍体型仅可使用活性组中的单倍型。如果所有个体的潜在二倍体型需要不在活性组中的单倍型,则可能不将二倍体型分配给个体;4)如果任何个体未被分配给二倍体型,则略过步骤#7;5)分配的个体二倍体型用作当前的解决方案;6)从活性组除去最少使用的单倍型,并且返回步骤#3;7)当前解决方案输出为存在于群体中的个体二倍体型,从而单倍型的列表。
在一些分析中,也使用Beagle(3.0.1版)处理定相基因型以获得两个单倍型网络-一个是以5’→3’方向存在的合并相似单倍型,第二个以3’→5’的方向存在。将来自PHASE的5个独立运行的每一个个体的所有10个定相基因型用作输入以解释丢失基因型的定相或推算中的不确定性。将Beagle的单倍型合并法的尺度参数设置至4.0。通过Beagle产生的定向非循环图单倍型输出显示哪个SNP形成单倍体区段以及如何使这些区段相关联。基于其通过两个网络的途径将单倍型分配给每一条染色体,从而导致rs4230SNP。占据小于1%的染色体的单倍型未有报导。
2.8方法:单倍型验证
从犹他大学遗传参照项目的家族的成员获得参照对照定相单倍型(Ann.Rev.Genomics Hum.Genet.9:347-3582008)。UGRP家族成员由超过600个来自43个三代家庭的个体组成,所述家庭也是原始Utah CEPH(人类多态性研究中心)家族的部分。使用AffymetrixGenome-Wide Human SNP阵列6.0在来自整个UGRP成员的血液DNA样品上获得66个SNP基因型。使用来自Bioconductor2.3Oligo包的CRLMM的检出算法进行基因型的检出。其置信度小于0.95的基因型的检出用漏失值替代。其检出率小于95%的SNP标记也下降。还进行Taqman SNP基因型测定以获得23个额外SNP标记的基因型。将PedCheck程序用于检测孟德尔不一致,并且除去misinherited基因型检出。基于三代家族的每一个中的孟德尔不一致构建定型单倍型。不使用任一单倍型推断程序。使用Haploview程序的定相单倍型输入模式Haps格式基于136个无关UGRP个体计算单倍型频率,所述个体大部分是第一代祖父母(图33)。
2.9方法:AMD疾病关联
单倍型与AMD的关联通过536个个体(中位年龄=79岁)(216个未患AMD的个体和320个患有AREDS分类2、3、地图样萎缩或新生血管AMD的个体)中的个别SNP的Bayesian逻辑回归来进行评估。补体介导的疾病关联使用Bayesian逻辑回归模型(对系数利用柯西先验)(Ann.Appl.Stat.2:1360-1383,2008)来测定。也评估该病例-对照队列中的单个SNP关联。
2.10结果:新型CFH基因座SNP的基因分型和鉴定
对于所使用的63个SNP的41至63个SNP筛选每一个受试者的DNA(图2和图29)。在使用MIP基因分型,通过ParAllele分型的SNP中,5个在它们发现时在文献中未见报导(图27)。使用错配修复检测(MRD)鉴定这些SNP以扩增经扩增的基因组DNA的富含变体的库。随后对该扩增的DNA的库测序以鉴定稀有等位基因。稀有mrd_3876和mrd_3877SNP位于CFHR4的启动子区域内。mrd_3876的次等位基因存在于倾向发生AMD的风险的单倍型中,mrd_3877的次等位基因存在于显著倾向于AMD风险的单倍型中。mrd_3902的次等位基因(位于CFHR2的外显子2内)导致Cys72Tyr编码突变并且存在于似乎倾向于保护AMD的单倍型中。SNP mrd_3905和mrd_3906的次等位基因更常见(约20%的次等位基因频率)并且位于CFHR5的启动子区域内;它们似乎不倾向于AMD风险或保护作用(参见图1和5)。
在进行这些测定的同时在CFH-至-F13B基因座内鉴定了一个另外的新型SNP。该变体位于CFH外显子10A-截断形式的补体因子H的最后一个外显子内(图2)。该SNP通过SSCP鉴定,并且根据测序,其被认为是至外显子10A的3’非翻译区内的1或2个碱基对的插入。次等位基因(1-2bp的缺失)存在于仅1.2%的染色体中。
2.11结果:缺失染色体的鉴定-TaqMan qPCR拷贝数变异测定
缺失测定的结果示于图28中。通过SSCP分析确认纯合缺失样品。在给予确定的拷贝数值的这些样品中,28%具有一个或两个拷贝的CFHR3和CFHR1的缺失。15%的个别染色体不包含这些基因。在包括推算的缺失状态后,19%的个别染色体不包含缺失(CFHR3和CFHR1的不存在)。
还进行实验来测定该测定的可靠性。作为实例,对于两个DNA样品(一个是纯合无缺失样品及另一个是相关的杂合缺失样品)的每一个,一个实验产生192个重复。使用100ng至0.6ng的总基因组DNA进行每一个qPCR测定。基于这些数据,对于给定量的基因组DNA,使用杂合缺失DNA的测定经预测具有比使用纯合正常DNA的相同测定多0.645±0.002个循环的Ct值。预期的来自个体样品的直线Ct,缺失=Ct,RNA酶P的距离为0.16。因此,使用5至6个qPCR重复正确分类CFHR3/CFHR1基因的杂合缺失的预期的功效为83%。这与(图28)中显示的75%的检出率相似。因此,为了以5%的I型差错率获得95%的功效,对每一个DNA样品运行9个重复。
2.12结果:缺失预测
基于测量的(非推算的)基因型,产生决策树(图30)来预测来自3个SNP的缺失状态。所有纯合缺失个体在CFH的SNP rs12144939上具有TT基因型,尽管17个杂合缺失个体在该位置上具有基因型GG。因此,确定高加索人的缺失状态可通过位于内含子15内的rs12144939上的‘T’可靠地预测。基于该单个SNP的基因型,可以以97%的特异性和96%的灵敏性预测CFHR3/CFHR1基因的缺失状态。在发现队列中14%的染色体包含该缺失。rs12406509和rs7546940(mrd_3878)的包含略微增加了缺失预测的灵敏性和特异性。
2.13结果:基于63SNP的CFH-至-F13B单倍型的鉴定和验证
测定横跨扩展的CFH-至-F13B基因座和包含CFHR3/CFHR1缺失的基于63SNP的单倍型(图32)。使用PHASE v.2.1.1,基于单倍型构建在约260kb的CFH-至-F13B基因座内鉴定了19个主单倍型(频率大于1%)(图32)。在大型多代犹他大学遗传参照项目家族(Annu.Rev.Genomics Hum.Genet.9:347-3582008)中确认单倍型精确度(图33)。单倍型H1和H2(两个最普遍的单倍型(在该队列中约47%的染色体))包含绝大多数CFH Y402H变体。19个单倍型中的5个(H3、H8、H10、H14和H19)包含所有具有CFHR3/CFHR1缺失的染色体的绝大部分。CFH162V保护性变体主要包含在单倍型H4、H9和H12中。11个SNP(图32中箭头标示的)足以推断出19个单倍型。
2.15结果:基于63SNP的CFH-至-F13B单倍型与疾病的关联
在计算引导程序(bootstrap)置信区间和控制年龄、性别及吸烟状态后,AMD疾病关联的初步评价显示19个主单倍型中的3个与不同AMD风险表型(作为二分类和数量性状)的显著关联(p<0.01)。在控制年龄、性别及吸烟状态后,单倍型H3、H4和H8与显示减少的发展AMD(作为二分类性状(p<0.01)和作为数量性状(p<0.05))的风险关联联(图34)。
实施例3:横跨染色体1q32CFH-至-F13B基因座的扩展的单倍型的改善的评价
3.1方法:研究队列
将实施例2中描述的相同的1,073个受试者的队列(‘1,073队列’、‘GSH队列’或‘ParAllele队列’)用于研究以改善扩展的CFH-至-F13B单倍型以及它们与AMD和其它疾病的关联的理解。此外,使用高度不一致的同胞对队列(来自284个家族的657个受试者)、由在犹他州(837个受试者)、爱荷华州(1,555个受试者)、澳大利亚墨尔本(1,704个受试者)中确定的受试者组成的组合AMD病例-对照队列(该集合队列称为‘组合队列’)和UGRP队列(604个受试者)。
3.2方法:基因分型
将实施例2中使用的63个SNP中的62个SNP用于改善的评价。已测定用于产生63个SNP单倍型的SNP之一rs432366在其于NCBI或其它数据库中所列的位置中不是多态性的。因此,从所有将来的分析除去该SNP。基于rs432366的除去再评价单倍型测定和疾病关联。对于62个变体中的51个获得超过99%的基因型检出率,对于剩余的SNP获得小于99%的基因型检出率;使用PHASE2.1.1推算丢失基因型。使用预先设计的或客户定制的Taqman测定(ABI)对所有其它队列进行基因分型,这样基因分型限于51个SNP(参见图2和图16中的粗体标示的SNP)。
3.3方法:基于62SNP的和基于51SNP的单倍型的产生
PHASE2.1.1用于测定存在于1,073患者队列中的基于SNP的单倍型。所使用的染色体位置来自使用参照人基因组(构造18)的NCBIdbSNP构造129。在基因型定相后,使多等位基因缺失状态向后扩展进入4个分开的三等位基因SNP(主、次和缺失的)。
此外,关于高度不一致的同胞对队列、在犹他州、爱荷华州、澳大利亚确定的AMD病例-对照队列(‘组合对列’)和UGRP队列,产生基于51SNP的单倍型。在用于基于62SNP的单倍型测定的62个SNP中,不用存在于基于62SNP的组中的CFHR3/CFHR1缺失区域内的4个SNP(rs11807997、rs389897、rs4230和rs14628)(相反地,缺失标记SNP rs12144939用作取代物)来产生基于51SNP的单倍型。此外,Taqman测定不能被设计来对剩余58个SNP的7个进行基因分型,因此这些SNP也不用于产生基于51SNP的单倍型(关于用于产生基于51SNP的CFH-至-F13B单倍型的SNP,参见图15和16)。
3.4方法:基于51SNP的单倍型的验证
为了验证单倍型及其频率,从犹他大学遗传参照项目(UGRP)家族(Annu.Rev.Genomics Hum.Genet.9:347-358,2008)的成员获得参照对照定相单倍型。TaqMan SNP基因分型测定用于获得先前在GSH队列(参见上面)中基因分型的相同51个另外的SNP标记的基因型。将PedCheck程序用于检测孟德尔不一致并且除去错误继承的基因型检出。仅基于每一个三代家族中的孟德尔遗传模型构建定相单倍型。不使用任一单倍型推断程序。使用Haploview程序的定相单倍型输入模型Haps Format(Bioinformatics21:263-265,2005)基于136个无关UGRP个体计算单倍型频率,所述个体大多为第一代祖父母。
3.5方法:使用单标记以及基于62SNP的和基于51SNP的单倍型进行的疾病关联评价
为了使用基于62SNP的单倍型测定无关病例/对照疾病(AMD)关联,仅使用1,073队列中60岁或更大年龄的受试者。对照被定义为AMD等级为0的受试者,然而,病例由所有等级为1B-4C(如实施例1中描述的)的受试者组成。通过使用这些标准,将927个来自GSH队列的样品(‘927GSH队列’)用于分析疾病关联。用于疾病关联的GSH927队列中的扩展单倍型的频率几乎与针对整个1,073GSH队列推算的那些频率相同(图4)。使用基于等位基因频率的Chi-2的Vassar2x2列联表评价AMD与基于62SNP的单倍型的疾病关联。
也在示例性不一致同胞对队列(来自284个家族的657个受试者)中对51个SNP进行基因分型。使用正常受试者(对于家族队列,每家族仅1个正常同胞对)(即偏离Hardy Weinberg平衡(HWE))和群体中的次等位基因,将Haploview(v4.2)用于测定描述性统计。在假定为加性遗传模型的情况下,进行次等位基因与AMD的关联的测试,将所有AMD亚型与整个队列中的正常成员相比较,随后仅在男性中进行比较,以及单独地仅在女性中进行比较。对于家族队列,使用条件逻辑回归(CLR)在整个队列中进行关联的测试。在仅使用男性和女性的分析中,每家族选择每个性别的一个受试者(选择具有最严重疾病的受试者),使用逻辑回归测试其与所有AMD亚型的关联。逻辑回归也用于评价来源于‘927GSH队列’的基于51SNP的单倍型。在SAS(v9.1)和/或Haploview中进行所有分析。使综合元分析(Comprehensive Meta-Analysis)2.0进行元分析。
3.6结果:从1,073队列产生的基于62SNP的CFH-至-F13B单倍型
为了产生包括CFH-至-F13B基因座的单倍型,使用测定的组合,利用使用PHASE2.1.1推算的丢失基因型对1,073个西欧和北欧高加索人后裔的62个SNP进行基因分型,如上文中所描述的。随后使用PHASE2.1.1测定所有样品的单倍型。
该分析导致15个以大于1%的频率存在的主单倍型(H1_62_A至H15_62_A;图1和图17)和148个各自以小于1%的频率存在的次单倍型(H16_62_A至H163_62_A;图3和图17)的检测。总计地,主单倍型占据1,599条总染色体,然而次单倍型包含547条染色体,或该队列中的染色体的25.5%。163个基于62SNP的单倍型之间的等级关系示于图21(H1_62_A至H163_62_A)中。使用R统计包的hclust功能,使用层序聚类分析,基于相似基因座的数目将163个单倍型聚集至该树中。相似单倍型是最相关的(更靠近在一起),且相异单倍型在该‘树’中进一步分开,图21中显示的。重要地,观察到3个分别包含风险、保护性和中性单倍型的主要聚簇。中性单倍型聚集在树的左部或顶部。具体地,中性单倍型聚簇横跨从H126_62_A至H163_62_A的区域。风险单倍型聚集在树的中间部分。具体地,风险单倍型聚簇横跨从H46_62_A至H73_62_A的区域。保护性单倍型聚集在树的右部或底部。具体地,保护性单倍型聚簇横跨从H152_62_A至H98_62_A的区域。
15个主单倍型中的两个频率最高的单倍型H1_62_A(总单倍型的19.2%)和H2_62_A(总单倍型的15.4%)都包含rs1061170的风险等位基因“C”(402H)。基于在该区域内检查到的变体,H1_62_A与H2_62_A从CFH的近端至CFHR2的区域是相同的;仅在F13B基因(始于F13B的3’UTR中的rs698859)中,SNP才真正区分H1_62_A与H2_62_A单倍型(图1)。区分H1_62_A与H2_62_A的其它F13B SNP包括rs5998、rs2990510和rs1615413。3个其它主单倍型包含CFH402H风险等位基因(H8、H12、H14)。两个主单倍型(H3_62_A和H6_62_A)包含CFH rs800292的保护性次等位基因“A”。此外,4个主单倍型包含CFHR3/CFHR1缺失(H5_62_A、H11_62_A、H13_62_A和H15_62_A;图1)。几乎处于完全LD的4个SNP(rs11807997、rs389897、rs4230和rs414628)位于CFHR3/CFHR1缺失区域;它们在图1中显示为三等位基因SNP(主等位基因以白色显示,次等位基因以填充线框显示,且缺失的CFHR3/CFHR1以黑色阴影框显示)。
1,073队列(参见实施例2)以及来自UGRP队列的家族的全面评估导致在>98%的高加索人个体中将rs12144939鉴定为CFHR3/CFHR1缺失的可靠替代“标记”,次等位基因“T”精确地鉴定了相伴的缺失。处于完全LD的该SNP的替代物包括rs6677604、rs16840522和rs2019727。包含CFHR3/CFHR1的缺失的主单倍型(H5_62_A、H11_62_A、H13_62_A和H15_62_A;图1和图18),除H13_62_A外,在该队列中具有抗AMD的发展的高度保护作用(图18)。
重要地,所有包含rs800292上的保护性等位基因(H5_62_A、H11_62_A、H13_62_A和H15_62_A)或CFHR3/CFHR1缺失(H5_62_A、H11_62_A、H13_62_A和H15_62_A;包括rs11807997、rs389897、rs4230和rs414628并且利用上文中所列的rs12144939或替代SNP来标记)的主单倍型还包含次等位基因rs2274700、rs3753395、rs393955、rs403846和rs1410996变体(图1和图18)。变体rs1409153也与所有与保护作用相关的主单倍型几乎处于完全LD。这些SNP中的任何SNP和与这些SNP处于几乎LD的任何其它SNP可单独地或组合地用作主保护性单倍型H3_62_A、H6_62_A、H5_62_A、H11_62_A、H13_62_A和H15_62_A以及一些次保护性单倍型的替代物。处于几乎完全LD(并且可用作替代物)的DNA的该区域内的其它SNP通过使用在HapMap中位于CFH-至-CFHR4区域内的全部SNP产生LD曲线来测定。这使用CEU队列(CEU,犹他州居民与来自CEPH集合的西欧和北欧祖先,是HapMap Phase3中的11个群体之一)基因型来进行。在该群体中,7个SNP被鉴定为与rs1410996(在该“区段”最显著关联的变体)处于完全或几乎完全LD。它们是(按5’-至-3’方向的顺序)rs10737680、rs7535263(LD=0.96)、rs3753395、rs10922106、rs395998、rs1329428和rs7540032。在该22kb区域中存在多个与rs1410996处于不同水平的LD的其它SNP。
3.7结果:1,073(927亚组)队列中的基于51SNP的CFH-至-F13B单倍型
基于51SNP的单倍型还可使用1,073(927亚组)队列来产生(图22)。从62个SNP转变成51个SNP引起基于62SNP的单倍型中的一些单倍型崩解成基于51SNP的单倍型(图20)。17个主单倍型以大于1%的频率存在于该队列中。
3.8结果:使用UGRP队列验证基于62SNP和基于51SNP的单倍型
因为单倍型是被推算的,因此寻求测定的单倍型结构和频率是真实的并且代表高加索人群体的独立验证。如参见实施例2中所述,验证基于62SNP的单倍型。
通过使用136个来自CEPH/UGRP参照队列的无关个体,使用51个SNP产生非推算的单倍型。鉴于UGRP无关队列的较小的大小,预期在GSH队列与UGRP队列之间存在一定的单倍型频率差异。然而,当与图1中显示的单倍型相比较时,这些差异较小,并且单倍型频率几乎相似(图33),从而表明这些单倍型频率代表了一般成年高加索人群体(图10)。
3.9结果:使用62个SNP的1,073队列(927亚组)中的单SNPAMD疾病关联
在我们的原始队列中的1,073个样品中,927个在诊断时为60岁或更老,并且患有AMD(等级1B-4C)或未患有AMD,并且用作对照(等级0)。使用单个标记关联的逻辑回归进行风险的病例/对照分析(图5)。结果显示关联的模式。rs1061170与风险显著关联(p=2.5e-11,OR=1.953,95%CI1.604-2.377)。rs1410996、rs2274700和rs3753395的次等位基因[以及标记含有与大部分保护性单倍型关联的变体的DNA的区段的其它替代物(chr1:196679455-196701284;Hg19)]甚至比rs1061170更强地相关,但具有免于发展AMD的保护作用而非发展AMD的风险(p=1.12e-14,OR=0.436,95%CI0.353-0.538)。包含CFHR5和F13B的该基因座的远端区域中的变体也与AMD显著关联(虽然以低得多的水平)(图5)。
3.10结果:与AMD风险关联的基于62SNP的单倍型:1,073队列(927亚组)
使用Haploview4.2(图6)(Barrett JC,Bioinformatics,2005年1月15日)分析整个扩展的单倍型的疾病关联。
在15个以大于1%的频率存在的主单倍型当中,H2_62_A显示对于AMD的显著风险(图6和图18;p<0.0001;注意值因在进行这两个分析的时间之间少数患者的临床重新分类而在图6与18之间略微变化)。还包含402H风险等位基因的H1_62_A在该队列中稍微倾向于AMD的风险(p=0.098),但显著少于H1_62_A。然而4个来自62SNP小组的远端SNP可区分H1_62_A与H2_62_A,这些SNP中仅有一个在单标记评价中与AMD显著关联(rs698859,p=0.0111)(图5)。这表明通过这些SNP标记的单倍型中的其它特征/组件负责H2_62_A中的风险或H1_62_A中的风险的不存在。鉴于多个单倍型包含rs1061170上的风险等位基因(H1_62_A、H2_62_A、H8_62_A、H12_62_A和H14_62_A)并且这些单倍型中仅有一个在该队列中与风险显著关联,因此在H2_62_A单倍型中可能存在不存在于所有其它非H2_62_A402H单倍型中的风险因子。事实上,使用未包括F13BSNP的较少扩展的单倍型的先前研究已将发展AMD的显著风险归因于包含Y402H风险等位基因的所有患者(GSH队列中,42.3%的主单倍型或49%的所有单倍型),此时事实上风险仅与H2_62_A或16.5%的本文中描述的队列相关。因此,本文中描述的单倍型代表CFH基因座上界定风险的敏感性的显著增加。
此外,绝大多数AMD风险关联(尽管不是全部)存在于该队列的被CFH402H标记的主单倍型(H2_62_A、H8_62_A、H12_62_A、H14_62_A和H16_62_A;图6和图18)中。然而,CFH402H并非总与AMD的风险关联;H2_62_A是与AMD风险最强相关的单倍型,然而主单倍型H1_62_A、H8_62_A、H12_62_A和H14_62_A在该队列中不是显著关联的。次单倍型H16_62_A在该队列中倾向于风险。
3.11结果:与AMD保护作用关联的基于62SNP的单倍型:1,073队列(927亚组)
除了风险以外,数个主CFH-至-F13B单倍型显示相对于整个队列免于发展AMD的保护作用。H3_62_A(包括rs800292A等位基因)具有显著的保护作用(图6)。正如同H1_62_A与H2_62_A相异在于它们的风险关联,H3_62_A(保护作用)与另一个包含rs800292A等位基因的主单体型H6_62_A(中性)也相异在于它们的风险关联。在包含CFHR3/CFHR1缺失的单倍型当中,H5_62_A和H11_62_A显示显著的保护作用,然而H13_62_A显示边际保护性,H15_62_A是中性的。H3_62_A与H6_62_A直到mrd_3905/rs75816959(其存在于CFHR5中)为止是相同的。类似地包含CFHR3/CFHR1缺失的单倍型H5_62_A、H13_62_A和H15_62_A直到mrd_3905为止是相同的。因此,将这些单倍型置于包括CFHR5和F13B的扩展单倍型的背景中导致显著改善的与AMD的关联(图6和18)。
3.12结果:与中性关联的基于62SNP的单倍型:GSH队列
几个主CFH-至-F13B单倍型(包括H4_62_A、H7_62_A、H10_62_A、H12_62_A和H14_62_A)在AMD的发展方面相对于整个队列而言是中性的。rs3753396的次等位基因标记了许多这类中性单倍型(图1、图3、图6和图18)。以90或更大的r2值与rs3753396处于LD以及可用作rs3753396的替代物的其它SNP包括(从近端至远端罗列的):rs10489456、rs70620、rs742855、rs11799380、rs1065489、rs11582939、rs385390、rs421820、rs426736、rs370953和rs371075。
3.13结果:基于62SNP的单倍型的性别关联:1,073队列(927亚组)
在GSH病例-对照队列中检查62个单标记(SNP)和单倍型的与性别的潜在关联。使用整个队列、仅男性子队列和仅女性子队列来评价关联(图13和图23)。当与‘927GSH队列相比较时,女性队列显示水平非常相似的62个个体SNP与AMD的关联的显著性(图13)。男性关联与女性关联不同。例如,在男性子队列中观察到rs800292、rs1061170和rs1329421的关联,相对于女性约11个数量级的差异。男性确实显示更低水平的与rs1410996、rs3753395和rs393955的显著关联,尽管也在达到比在女性队列中看到的低11个数据级的水平(图13)。rs800292A等位基因(先前与对AMD的保护作用或减少的风险关联)也在男性子队列中显示了减少的关联。该数据表明通过控制性别,先前的研究可能由于掩蔽而已丢失该分层现象。
虽然与AMD的关联在男性中丢失在整个CFH基因中是显著的,但显著关联的一个区段得到保留,尽管以降低的水平。rs1410996显示5.94e-5的p-值(相较于全队列中的3.26e-16和女性中的6.31e-13)(图13)。该SNP经发现与几个取代SNP(rs2274700、rs3753395和rs10737680)接近100%的LD。当观看女性子队列时,rs1410996具有与对于rs1061170所进行的相似的与AMD关联的强度。正是男性rs1410996的关联(在rs1061170上缺乏的关联)解释了rs1410996(及其取代SNP rs2274700、rs3753395和rs10737680)的更高的显著性。通过独立地分析男性和女性,鉴定了rs1061170与rs1410996上的风险之间的差异的基础。
研究表明在CFH上看到的男性/女性分层现象不是一般AMD疾病的结果,而是与CFH相关的疾病的特定机制的结果。C3和C2/CFB中的SNP的分析显示与对于CFH的几乎一样的倾向:在完全927队列和仅女性的队列中发现更弱但显著的风险,然而在仅男性的队列中未发现风险。因此,男性的AMD风险与补体系统的关联在整体上相较于在女性中要弱得多。
还在男性和女性中独立地检查到单体型疾病相关。H2_62_A在男性中几乎不显著但在女性十分显著(图23)。H2_51_B在男性中比H2_62_A更显著,但在女性中仍然不太显著(图24)。H1_62_A在女性中显著,但在男性根本不显著。然而,H1_51_B在男性和女性中都显著;然而,再次地在女性中更显著(图24)。H11_62_A在男性和女性中都显著,但在男性中更显著。H2_62_A、H3_62_A、H5_62_A和H11_62_A都与所有受试者的AMD显著关联(图6)并且在女性中也是显著关联的(图23)。在H1_62_A和H6_62_A中,女性的关联比所有受试者略显著,在H13_62_A中相关不太显著,但这些差异是相当小的。
3.14结果:与AMD关联的基于51SNP的单倍型:1,073队列(927亚组)
也使用基于51SNP的单倍型分析来评价GSH927队列中的单倍型的关联(图22)。包括的51个SNP描述于图22中。风险与保护性单倍型的关联与在基于62SNP的单倍型分析中观察到的相似(图6和图18;也参见图20和图22).
3.15结果:基于51SNP的单倍型以及它们与AMD和AMD表型的关联:‘组合队列’和示例性不一致同胞对队列
将由来自爱荷华州、犹他州和墨尔本队列的患有和未患AMD的个体组成的大型病例-对照队列(‘组合队列’)用于评价具有AMD(对照对所有AMD)风险、保护作用和中性的基于51SNP的CFH-至-F13B单倍型。从组合队列产生56个单倍型,它们中的18个以高于1%的频率存在(图15)。基于51SNP的主单倍型与基于62SNP的主单倍型之间的关系示于图16中,1,073中的基于51SNP的单倍型与组合队列中的基于51SNP的单倍型之间的关系描述于图19中。观察到与GSH927队列中基于62SNP的单倍型(Hx_62_A)和基于51SNP的单倍型(Hx_51_A)的评价相似的关联(图15)。然而,H1_51_B在该更大的队列变得更显著。
几个次CFH-至-F13B单倍型相对于整个队列显示来自AMD的风险和免于AMD的保护作用。例如,H24_62_A和H28_62_A倾向于风险,但H30_62_A(p=0.007)和H40_62_A倾向于保护(图15)。
‘组合队列’也用于评价51SNP小组的单个SNP关联和基于51SNP的CFH-至-F13B单倍型与AMD的不同表型/分期的关联,包括对照(分期0)与所有AMD(分期1B-4C)、早期AMD(分期1B-3)和地图样萎缩的晚期(分期4A)以及CNV(分期4B)的比较。当将对照与所有AMD相比较时,该队列中的单标记关联(图42)与1,073和高度不一致同胞对队列的单标记关联不同。此外,单标记与风险、保护作用和中性的关联,当将对照与所有AMD分期(图42)、仅早期(图43)、仅地图样萎缩(图44)或仅CNV(图45)相比较时,未发生显著变化。
当将对照与仅早期、与仅地图样萎缩或与仅CNV相比较时,单倍型与风险、保护作用和中性的关联在组合队列(它们与1,073队列的分析也无显著不同;图20和图22)中的AMD表型之间变化不显著(图46)。注意,单倍型顺序(基于频率)在图46中显示的3个分析中是不相同的。
使用高度不一致的同胞对队列验证H1_51_B和H2_51_B与AMD风险的差异相关。产生该队列的基于51SNP的单倍型。通过使用逻辑回归,看到其中H1_51_A(如GSH队列中所描述的)不与风险显著关联的模式。H2_51_A的等同物即H2_51_B与风险高度相关,并且是与风险关联的唯一单倍型(图12)。在剩余的单倍型当中,仅H5_51_B(包含CFHR3/CFHR1缺失)与AMD关联:在该情况下作为保护性单倍型(图12)。因此,将H1_51_A与H2_51_A的风险关联的差异在第二独立队列中重复。
3.16结果:基于51SNP的二倍体型与AMD风险、保护作用和中性的关联:组合队列
使用BEAGLE3.3.2版(S R Browning和B L Browning,2007,Rapid and accurate haplotype phasing and mis sing data inference forwhole genome association studies using localized haplotype clustering.Am J Hum Genet81:1084-1097)在组合队列中定相和测定基于51SNP的二倍体型。在整个队列中(图35)、仅在男性中(图36)和仅在女性中(图37)评价与AMD风险、保护作用和中性的关联。对于其存在适当的统计功效的所有二倍体型组合中的组合示于图35中;统计功效足以通过单倍型7评价关联。
当与另一个H1单倍型或H2、H8或H13单倍型组合时单个H1与增加的发展AMD的风险关联,然而,H1单倍型与H3或H5单倍型的组合与保护作用相关。仅当单个H2单倍型与另一个H2单倍型一起存在时,H1单倍型或H10单倍型才与风险关联。未观察到显示与保护作用的关联的组合,这表明H2单倍型与风险的关联强于H1与风险的关联。对于与任何其它单倍型组合的单个H3、H4、H5、H6或H7单倍型的任意组合未观察到风险关联。然而,这些组合中的许多组合是保护性的,如图35中描述的。仅有男性的组和仅有女性的组的总体结果与整个队列的结果相似,在仅有男性的组中记录了一些小的差异,可能归因于统计功效的损失(图36和37)。
‘组合队列’还用于评价基于51SNP的CFH-至-F13B二倍体型与AMD的不同表型/分期的关联,包括对照(分期0)与所有AMD(分期1B-4C)、与早期AMD(分期1B-3)和与仅CNV(分期4B)的比较。二倍体型与风险、保护作用和中性的关联在下列组之间变化不显著:1)与所有AMD分期相比较的对照(图35);和2)与仅CNV相比较的对照(图48)。这些关联与其它队列中的关联也无差异。然而,早在将对照与仅早期AMD相比较时(图47),所有H3组合的保护作用大大减小,表明H3二倍体型组合对于与早期AMD发展关联的表型(脉络膜小疣)或与特定类型的与早期AMD发展关联的脉络膜小疣关联的表型可以不具有保护作用。
3.17结果:单倍型标记SNP
基于62SNP的主单倍型的每一个和基于51SNP的主单倍型的每一个可使用8个单倍型标记SNP的组合(htSNP;图7;指出rs800292和rs35928059对于标记基于62SNP的和基于51SNP的单倍型是任选的)来独特地鉴定。使用Haploview4.2,仅使用8个htSNP对GSH1,073队列重复进行病例/对照分析以确定单倍型。相较于基于62SNP的分析,与H1的风险关联相差几个数量级并且在统计上是显著的(图10;8htSNPs-H1p-值=0.0024;62SNPs-H1p-值=0.116;要指出,基于62SNP的显著性值在图10中相较于图6中略高,因为Haploview不能处理三等位基因缺失SNP)。为了更清楚地显示该作用,按下列编号使用逐渐减少的SNP在Haploview中重新分析927GSH队列:1)所有CFH基因座SNP(62);2)所有SNP减去4个缺失相关SNP(58);3)所有针对其开发了Taqman测定的SNP(51);4)所有对于其MAF>5%的频率的SNP(43);6)所有与AMD具有高度显著的关联的SNP+rs698859(31);和7)仅htSNP(8)(图10)。当将更少的SNP用于产生单倍型时,更多次单倍型变换为主单倍型并且H1变得与AMD的风险显著关联。所有其它显著的单倍型在它们与AMD的关联上仅显示不影响风险的解释的小变化。
3.18结果:基于51SNP的CFH-至-F13B单倍型至基因组水平单倍型的扩展;HapMap单倍型与AMD的关联
将基于51SNP的单倍型与使用HapMap数据产生的单倍型相比较以进一步精确测定与AMD的单倍型关联。国际HapMap Project数据库(http://hapmap.ncbi.nlm.nih.gov/)在包括包含CFH-至-F13B基因座(Hg18chr1:194869137-195303491)的区域中包含超过500个SNP。下载这500多个SNP的每一个的来自180个高加索人个体(称为CEU群体)的基因型。下载来自CEU组的定相基因型数据,在该目的区域中包含信息最丰富的SNP(即,在CEU群体中分离的那些SNP)。通过使用Haploview(www.broadinstitute.org),构建单倍型的CEU数据集组并且计算其频率(图39和40)。在AMD病例/对照(‘组合队列’)基于51SNP的单倍型与HapMap单倍型之间存在显著的重叠(图38、39和40)。将这些交叠的SNP用作‘标记’SNP来将病例/对照单倍型与它们的等同HapMap CEU单倍型匹配(图38和41)。先前已在基于51SNP的病例/对照(‘组合’)队列中建立了AMD与单倍型的关联(图22);因此关联可被扩展至等同的HapMap单倍型。在一些情况下,基于51SNP的单倍型因未包含在基于51SNP的单倍型中的HapMapSNP的存在而与多个HapMap单倍型交叠,反之亦然。因此,在其中HapMap单倍型与多个等同病例/对照单倍型交叠的情况下,鉴定了进一步改善我们的基于51SNP的主单倍型的区分值的至关重要的SNP。作为实例,‘组合队列’单倍型H1(图39和41)匹配两个频率最高的主HapMap产生的单倍型(图39和41)。区分这两个HapMap单倍型的唯一SNP是rs10494745。在本分析中发现的其它相似的信息型SNP(其将改善疾病关联的评价)用星号标示,它们与基于组合队列51SNP的单倍型的关系描述于图40中。它们是rs7524776、rs7513157、rs419137和rs10494745。
3.19结果:扩展单倍型区段
确定SNP在由基于62SNP的单倍型界定的边界的近端还是远端,所述SNP与确定的主单倍型区段处于LD。下载位于Chr1:194,814,311与195,431,890之间的高加索人的所有Hapmap SNP和受试者信息,在Haploview中进行分析(图14)。缺省(Gabriel等人)区段包括整个区域。由rs10801551(194,848,662)至rs800292(194,908,856)定义的第二区段包括rs35928059,62-SNP组中使用的最5’SNP。这表明rs35928059与远至近端的rs10801551的SNP处于LD。类似地,在我们的基因座的远端3’末端上,rs6428380(62_A SNP组中的最3’SNP)位于rs4915148(195,302,161)与rs1537319(195,319,427)之间,这表明位于该区段内的远端SNP可能与rs1537319处于LD。
3.20结果:CFHR3/CFHR1缺失边界的表征
对代表每一个缺失标记SNP基因型的多个CEPH个体进行对定量PCR(qPCR)。3个qPCR引物组被设计来等同地扩增两个重复区域,在区段性重复之间的序列中设计两个另外的探针。使用QuantiFastSYBR RT-PCR预混合物(Qiagen)和MyiQ Single Color实时PCR检测系统(BioRad)进行所有实验。非缺失纯合子显示两个区段性重复的存在,以及重复之间的探针的正常扩增。杂合子显示重复内的探针的中间值和重复之间的区域中的一个拷贝的缺失。对于缺失标记等位基因是纯化的个体显示仅一个区段性重复区域的存在并且无位于重复区域之间的探针扩增。因此该qPCR测定可用于可靠地将个体鉴定为纯合R3/R1缺失、杂合R3/R1缺失或纯化R3/R1非缺失。
3.21结果:替代性CFHR3/CFHR1缺失状态测定的开发和rs12144939作为CFHR3/CFHR1缺失标记SNP的确认
两个另外的PCR测定被开发来确认缺失的存在或确认在非缺失染色体上的存在(图11)。这些测定不是设计来区分杂合子的,而是测定纯合缺失或非缺失样品的状态。通过在缺失纯合子中发现的序列变体特征,将引物设计来仅当缺失以杂合或纯合形式存在时产生3.7kbPCR产物。使用AccuPrime高保真聚合酶、缓冲液和方案(Invitrogen)来进行反应。扩增来自12个无关CEPH个体和5个非洲个体的样品,随后在1%的琼脂糖凝胶上运行。所有纯合缺失和杂合个体在被设计来扩增整个缺失的测定中产生3.7kb条带,然而纯合子和非缺失个体都未被扩增。此外,设计引物且引物用于仅当缺失不存在时扩增小的(200bp)PCR产物。对88个CEPH个体进行反应。除缺失纯合子外所有样品都得到良好扩增,所述缺失纯合子毫无例外都未能扩增。因此这两个测定可用于明确地鉴定对于CFHR3-R1缺失或对于非缺状态是纯合的个体,并且两者组合可测定杂合子。
3.21缺失标记SNP的确认
对全部604个CEPH个体进行预先设计的Taqman CNV测定以确认缺失状态。该测定位于chr1:195011298-195011397上,正好紧邻CFHR3基因。在7900HT Fast Real-Time PCR系统(Applied Biosystems)上进行测定,使用CopyCaller软件(Applied Biosystems)进行分析。针对rs12144939(缺失标记SNP)基因型比较拷贝数检出。在所有其中通过CopyCaller软件产生清楚的检出的情况下,拷贝数检出与通过rs12144939预测的一致,除一个其中6个个体对于标记SNP是杂合的但在CNV分析中被检出纯合的非缺失的家族例外。这确认了在高加索人中,rs12144939以几乎100%的可靠性标记缺失。因此,CFHR1/R3缺失状态现可使用上述3个测定来获得。1000-基因组数据的分析表明下列SNP准确地标记rs12144939,从而准确地标记CFHR3/CFHR1缺失:rs6689009、rs35253683、rs731557和rs60642321。
对于本领域技术人员来说显而易见的是,可在不背离本发明的范围或精神的情况下在本发明中作出各种的修改和变化。根据本文中描述的本发明的说明书和实践,本发明的其它方面对于本领域技术人员来说将是显而易见的。说明书和实施例意欲仅为示例性的,本发明的真实范围和精神由下列权利要求指明。
在整个本申请中,参考各种出版物。这些公版物的公开内容据此通过引用整体并入本申请以更全面地描述本发明所属的领域的现有技术水平。公开的参考资料也个别地和明确地通过引用将其中包含的材料并入本文,所述材料在其中参考文献所依赖的句子进行了讨论。此处的任何信息,都不能被解释为承认本发明由于现有发明而无权先于此类出版物。此外,本文中提供的出版物的日期可与实际出版日期不同,其可要求独立的确认。
E.参考文献
1.Abrera-Abeleda MA,Nishimura C,Smith JL,Sethi S,McRae JL,Murphy BF,Silvestri G,Skerka C,Józsi M,Zipfel PF,Hageman GS,Smith RJ.Variations in the complement regulatory genes factor H(CFH)and factor H related5(CFHR5)are associated withmembranoproliferative glomerulonephritis type II(dense deposit disease).J Med Genet.2006Jul;43(7):582-9.
2.Allikmets R,Bergen AA,Dean M,Guymer RH,Hageman GS,Klaver CC,Stefansson K,Weber BH;International Age-related MacularDegeneration Genetic s Consortium.Geographic atrophy in age-relatedmacular degeneration and TLR3.N Engl J Med.2009May21;360(21):2252.
3.Baird PN,Islam FM,Richardson AJ,Cain M,Hunt N,Guymer R.Analysis of the Y402H variant of the complement factor H gene inage-related macular degeneration.Invest Ophthalmol Vis Sci.2006Oct;47(10):4194-4198.
4.Breiman,Friedman,Olshen,and Stone.Classification andRegression Trees.Wadsworth,1984.
5.S.R.Browning.Multilocus association mapping usingvariable-length Markov chains.Am J Hum Genet,78:903-913,2006.
6.DeAngelis MM,Ji F,Adams S,Morrison MA,Harring AJ,Sweeney MO,Capone A Jr,Miller JW,Dryja TP,Ott J,Kim IK.Allelesin the HtrA serine peptidase1gene alter the risk of neovascularage-related macular degeneration.Ophthalmolog y.2008Jul;115(7):1209-1215.e7.
7.W.S.De Jong,D.M.De Jong,and M.Bodis.A fluorogenic50nuclease(taqman)assay to assess dosage of a marker tightly linked to redskin color in autotetraploid potato.Theor Appl Genet,107:1384-1390,2003.
8.H.Fakhrai-Rad,J.Zheng,T.D.Willis,K.Wong,K.Suyenaga,M.Moorhead,J.Eberle,Y.R.Thorstenson,T.Jones,R.W.Davis,E.Namsaraev,and M.Faham.Snp discovery in pooled samples withmismatch repair detection.Genome Res,14:1404-1412,2004.
9.Gold B,Merriam JE,Zernant J,Hancox LS,Taiber AJ,Gehrs K,Cramer K,Neel J,Bergeron J,Barile GR,Smith RT;AMD GeneticsClinical Study Group,Hageman GS,Dean M,Allikmets R.Variation infactor B(BF)and complement component2(C2)genes is associated withage-related macular degeneration.Nat Genet.2006Apr;38(4):458-62.
10.Gotoh N,Yamada R,Hiratani H,Renault V,Kuroiwa S,MonetM,et al.No association between complement factor H genepolymorphism and exudative age-related macular degeneration inJapanese.Hum Genet.2006Aug;120(1):139-43.
11.Hageman GS,Gehrs K,Lejnine S,Bansal AT,Deangelis MM,Guymer RH,Baird PN,Allikmets R,Deciu C,OethP,Perlee LT.Clinical validation of a genetic model to estimate the risk of developingchoroidal neovascular age-related macular degeneration.Hum Genomic s.2011Jul;5(5):420-40.
12.Hageman GS,Anderson DH,Johnson LV,Hancox LS,Taiber AJ,Hardisty LI,Hageman JL,Stockman HA,Borchardt JD,Gehrs KM,Smith RJ,Silvestri G,Russell SR,Klaver CC,Barbazetto I,Chang S,Yannuzzi LA,Barile GR,Merriam JC,Smith RT,Olsh AK,Bergeron J,Zernant J,Merriam JE,Gold B,Dean M,Allikmets R.A commonhaplotype in the complement regulatory gene factor H(HF1/CFH)predisposes individuals to age-related macular degeneration.Proc NatlAcad Sci U S A.2005May17;102(20):7227-7232.
13.Hageman GS,Hancox LS,Taiber AJ,Gehrs KM,Anderson DH,Johnson LV,Radeke MJ,Kavanagh D,Richards A,Atkinson J,Meri S,Bergeron J,Zernant J,Merriam J,Gold B,Allikmets R,Dean M;AMDClinical Study Group.Extended haplotypes in the complement factorH(CFH)and CFH-related(CFHR)family of genes protect againstage-related macular degeneration:characterization,ethnic distributionand evolutionary implications.Ann Med.2006;38(8):592-604.
14.P.Hardenbol,J.Banr,M.Jain,M.Nilsson,E.A.Namsaraev,G.A.Karlin-Neumann,H.Fakhrai-Rad,M.Ronaghi,T.D.Willis,U.Landegren,and R.W.Davis.Multiplexed genotyping withsequence-tagged molecular inversion probes.Nat Biotechnol,21:673-678,2003.
15.Lau LI,Chen SJ,Cheng CY,Yen MY,Lee FL,Lin MW,et al.Association of the Y402H polymorphism in complement factor H geneand neovascular age-related macular degeneration in Chinese patients.Invest Ophthalmol Vis Sci.2006Aug;47(8):3242-6.
16.Lim JH,Wickremasinghe SS,Xie J,Chauhan DS,Baird PN,Robman LD,Hageman GS,Guymer RH.Delay to treatment and visualoutcomes in patients treated with anti-vascular endothelial growth factorfor age-related macular degeneration.Am J Ophthalmol.2012Apr;153(4):678-686.
17.R Development Core Team.R:A Language and Environment forStatistical Computing.R Foundation for Statistical Computing,Vienna,Austria,2006,ISBN3-900051-07-0.
18.Robman L,Baird PN,Dimitrov PN,Richardson AJ,Guymer RH.C-reactive protein levels and complement factor H polymorphisminteraction in age-related macular degeneration and its progression.Ophthalmol.2010Oct;117(10):1982-1988.
19.M.N.Stephens and P.Donnell y.A comparison of bayesianmethods for haplotype reconstruction.Am J Hum Genet,73:1162-1169,2003.
20.M.N.Stephens,N.J.Smith,and P.Donnelly.A new statisticalmethod for haplotype reconstruction from population data.Am J HumGenet,68:978-989,2001.
21.Wickremasinghe SS,Xie J,Lim J,Chauhan DS,Robman L,Richardson AJ,Hageman G,Baird PN,Guymer R.Variants in theAPOE gene are associated with improved outcome after anti-VEGFtreatment for neovascular AMD.Invest Ophthalmol Vis Sci.2011Jun8;52(7):4072-9.
22.Zhang H,Morrison MA,Dewan A,Adams S,AndreoliM,Huynh N,Regan M,Brown A,Miller JW,Kim IK,Hoh J,Deangelis MM.The NEI/NCBI dbGAP database:genotypes and haplotypes that mayspecifically predispose to risk of neovascular age-related maculardegeneration.BMC Med Genet.2008Jun9;9:51.
Claims (240)
1.一种用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者对患有或发展年龄相关性黄斑变性的易感性。
2.根据权利要求1所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
3.根据权利要求1所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
4.根据权利要求1所述的方法,其中H2_62_A或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
5.根据权利要求4所述的方法,其还包括给所述受试者施用治疗性组合物。
6.根据权利要求1所述的方法,其中H3_62_A、H5_62_A、H11_62_A或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
7.根据权利要求1所述的方法,其中所述受试者是女性。
8.根据权利要求7所述的方法,其中H1_62_A、H2_62_A或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
9.根据权利要求7所述的方法,其中H3_62_A、H5_62_A、H11_62_A或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
10.根据权利要求1所述的方法,其中所述受试者是男性。
11.根据权利要求10所述的方法,其中H2_62_A或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
12.根据权利要求10所述的方法,其中H11_62_A或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
13.一种用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者对患有或发展年龄相关性黄斑变性的易感性。
14.根据权利要求13所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
15.根据权利要求13所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
16.根据权利要求13所述的方法,其中H2_51_A或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
17.根据权利要求16所述的方法,其还包括给所述受试者施用治疗性组合物。
18.根据权利要求13所述的方法,其中H3_51_A、H5_51_A、H10_51_A或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
19.一种用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者对患有或发展年龄相关性黄斑变性的易感性。
20.根据权利要求19所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
21.根据权利要求19所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
22.根据权利要求19所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
23.根据权利要求22所述的方法,其还包括给所述受试者施用治疗性组合物。
24.根据权利要求16所述的方法,其中H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
25.根据权利要求19所述的方法,其中所述受试者是女性。
26.根据权利要求25所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
27.根据权利要求25所述的方法,其中H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
28.根据权利要求19所述的方法,其中所述受试者是男性。
29.根据权利要求28所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
30.根据权利要求28所述的方法,其中H3_51_B、H14_51_B或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
31.一种用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定所述高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份,其中所述SNP是:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中至少6个所述SNP的存在表明所述受试者对患有或发展年龄相关性黄斑变性的易感性。
32.根据权利要求31所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
33.根据权利要求31所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
34.根据权利要求31所述的方法,其中所述至少6个SNP由至少rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859组成。
35.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
36.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
37.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
38.根据权利要求35-37中任一项所述的方法,其还包括给所述受试者施用治疗性组合物。
39.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
40.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
41.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
42.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
43.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
44.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
45.根据权利要求31所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
46.根据权利要求31所述的方法,其中所述受试者是女性。
47.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的G表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
48.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
49.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
50.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
51.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
52.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
53.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
54.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
55.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
56.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
57.根据权利要求46所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
58.根据权利要求31所述的方法,其中所述受试者是男性。
59.根据权利要求58所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
60.根据权利要求58所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
61.根据权利要求58所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
62.根据权利要求58所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
63.根据权利要求58所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
64.根据权利要求58所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
65.一种用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定所述受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明所述受试者对患有或发展年龄相关性黄斑变性的易感性。
66.根据权利要求65所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
67.根据权利要求65所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
68.根据权利要求65所述的方法,其中rs1061170SNP上的A表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
69.根据权利要求65所述的方法,其中rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
70.一种用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定所述受试者的CFH-至-F13B基因座中的缺失标记SNP的身份,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中所述SNP的存在表明所述受试者对患有或发展年龄相关性黄斑变性的易感性。
71.根据权利要求70所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
72.根据权利要求70所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
73.根据权利要求70所述的方法,其中rs12144939SNP上的T表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
74.一种鉴定需要治疗年龄相关性黄斑变性高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否需要治疗年龄相关性黄斑变性。
75.根据权利要求74所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
76.根据权利要求74所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
77.根据权利要求74所述的方法,其中H2_62_A或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
78.根据权利要求74所述的方法,其中H3_62_A、H5_62_A、H11_62_A或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
79.根据权利要求所述的方法74,其中H1_62_A、H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
80.根据权利要求74所述的方法,其中所述受试者是女性。
81.根据权利要求80所述的方法,其中H1_62_A、H2_62_A或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
82.根据权利要求80所述的方法,其中H3_62_A、H5_62_A、H11_62_A或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
83.根据权利要求80所述的方法,其中H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
84.根据权利要求74所述的方法,其中所述受试者是男性。
85.根据权利要求84所述的方法,其中H2_62_A或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
86.根据权利要求84所述的方法,其中H11_62_A或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
87.根据权利要求84所述的方法,其中H1_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
88.一种鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否需要治疗年龄相关性黄斑变性。
89.根据权利要求88所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
90.根据权利要求88所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
91.根据权利要求88所述的方法,其中H2_51_A或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
92.根据权利要求88所述的方法,其中H3_51_A、H5_51_A、H10_51_A或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
93.根据权利要求88所述的方法,其中H1_51_A、H4_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
94.一种鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否需要治疗年龄相关性黄斑变性。
95.根据权利要求94所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
96.根据权利要求94所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
97.根据权利要求94所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
98.根据权利要求94所述的方法,其中H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
99.根据权利要求94所述的方法,其中H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
100.根据权利要求94所述的方法,其中所述受试者是女性。
101.根据权利要求100所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
102.根据权利要求100所述的方法,其中H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
103.根据权利要求100所述的方法,其中H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
104.根据权利要求94所述的方法,其中所述受试者是男性。
105.根据权利要求104所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
106.根据权利要求104所述的方法,其中H3_51_B、H14_51_B或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
107.根据权利要求104所述的方法,其中H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
108.一种鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份,其中所述SNP是:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中至少6个所述SNP的存在表明所述受试者是否需要治疗年龄相关性黄斑变性。
109.根据权利要求108所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
110.根据权利要求108所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
111.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A表明所述受试者需要治疗年龄相关性黄斑变性。
112.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T表明所述受试者需要治疗年龄相关性黄斑变性。
113.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C表明所述受试者需要治疗年龄相关性黄斑变性。
114.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者不需要治疗年龄相关性黄斑变性。
115.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者不需要治疗年龄相关性黄斑变性。
116.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A表明所述受试者不需要治疗年龄相关性黄斑变性。
117.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者不需要治疗年龄相关性黄斑变性。
118.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者不需要治疗年龄相关性黄斑变性。
119.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者不需要治疗年龄相关性黄斑变性。
120.根据权利要求108所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者不需要治疗年龄相关性黄斑变性。
121.一种鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定所述受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明所述受试者是否需要治疗年龄相关性黄斑变性。
122.根据权利要求121所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
123.根据权利要求121所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
124.根据权利要求121所述的方法,其中rs1061170SNP上的A表明所述受试者需要治疗年龄相关性黄斑变性。
125.根据权利要求121所述的方法,其中rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G表明所述受试者不需要治疗年龄相关性黄斑变性。
126.根据权利要求121所述的方法,其中rs3753396SNP上的G表明所述受试者可能需要治疗年龄相关性黄斑变性。
127.一种鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定所述受试者的CFH-至-F13B基因座中的缺失标记SNP的身分,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明所述受试者是否需要治疗年龄相关性黄斑变性。
128.根据权利要求127所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
129.根据权利要求127所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
130.根据权利要求127所述的方法,其中rs12144939SNP上的T表明所述受试者不需要治疗年龄相关性黄斑变性。
131.一种鉴定需要预防性治疗老年黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否需要预防性治疗年龄相关性黄斑变性。
132.根据权利要求131所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
133.根据权利要求131所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
134.根据权利要求131所述的方法,其中H2_62_A或其互补序列表明所述受试者需要预防性治疗年龄相关性黄斑变性。
135.根据权利要求131所述的方法,其中H3_62_A、H5_62_A、H11_62_A或其互补序列表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
136.根据权利要求131所述的方法,其中H1_62_A、H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列表明所述受试者可能需要预防性治疗年龄相关性黄斑变性。
137.一种鉴定需要预防性治疗老年黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否需要预防性治疗年龄相关性黄斑变性。
138.根据权利要求137所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
139.根据权利要求137所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
140.根据权利要求137所述的方法,其中H2_51_A或其互补序列表明所述受试者需要预防性治疗年龄相关性黄斑变性。
141.根据权利要求137所述的方法,其中H3_51_A、H5_51_A、H10_51_A或其互补序列表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
142.根据权利要求137所述的方法,其中H1_51_A、H4_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列表明所述受试者可能需要预防性治疗年龄相关性黄斑变性。
143.一种鉴定需要预防性治疗老年黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否需要预防性治疗年龄相关性黄斑变性。
144.根据权利要求143所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
145.根据权利要求143所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
146.根据权利要求143所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者需要预防性治疗年龄相关性黄斑变性。
147.根据权利要求143所述的方法,其中H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
148.根据权利要求143所述的方法,其中H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列表明所述受试者可能需要预防性治疗年龄相关性黄斑变性。
149.一种鉴定需要预防性治疗老年黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份,其中所述SNP是:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中至少6个所述SNP的存在表明所述受试者是否需要预防性治疗年龄相关性黄斑变性。
150.根据权利要求149所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
151.根据权利要求149所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
152.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A表明所述受试者需要预防性治疗年龄相关性黄斑变性。
153.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T表明所述受试者需要预防性治疗年龄相关性黄斑变性。
154.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C表明所述受试者需要预防性治疗年龄相关性黄斑变性。
155.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
156.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
157.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
158.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
159.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
160.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
161.根据权利要求149所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
162.一种鉴定需要预防性治疗老年黄斑变性的高加索人受试者的方法,包括测定所述受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明所述受试者是否需要预防性治疗年龄相关性黄斑变性。
163.根据权利要求162所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
164.根据权利要求162所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
165.根据权利要求162所述的方法,其中rs1061170SNP上的A表明所述受试者需要预防性治疗年龄相关性黄斑变性。
166.根据权利要求162所述的方法,其中rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
167.根据权利要求162所述的方法,其中rs3753396SNP上的G表明所述受试者可能需要预防性治疗年龄相关性黄斑变性。
168.一种鉴定需要预防性治疗老年黄斑变性的高加索人受试者的方法,包括测定所述受试者的CFH-至-F13B基因座中的缺失标记SNP的身份,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明所述受试者是否需要预防性治疗年龄相关性黄斑变性。
169.根据权利要求168所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
170.根据权利要求168所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
171.根据权利要求168所述的方法,其中rs12144939SNP上的T表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
172.一种鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否适合进行临床试验。
173.根据权利要求172所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
174.根据权利要求172所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
175.根据权利要求172所述的方法,其中H2_62_A或其互补序列表明所述受试者适合进行临床试验。
176.根据权利要求172所述的方法,其中H3_62_A、H5_62_A、H11_62_A或其互补序列表明所述受试者不适合进行临床试验。
177.根据权利要求172所述的方法,其中H1_62_A、H4_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A或其互补序列表明所述受试者可能适合进行临床试验。
178.一种鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者是否适合进行临床试验。
179.根据权利要求178所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
180.根据权利要求178所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
181.根据权利要求178所述的方法,其中H2_51_A或其互补序列表明所述受试者需要预防性治疗年龄相关性黄斑变性。
182.根据权利要求178所述的方法,其中H3_51_A、H5_51_A、H10_51_A或其互补序列表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
183.根据权利要求178所述的方法,其中H1_51_A、H4_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A或其互补序列表明所述受试者可能需要预防性治疗年龄相关性黄斑变性。
184.一种鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定所述高加索人受试者的一个或多个单倍型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述单倍型的存在表明所述受试者适合进行临床试验。
185.根据权利要求184所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
186.根据权利要求184所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
187.根据权利要求184所述的方法,其中H1_51_B、H2_51_B或其互补序列表明所述受试者适合进行临床试验。
188.根据权利要求184所述的方法,其中H3_51_B、H5_51_B、H12_51_B、H14_51_B或其互补序列表明所述受试者不适合进行临床试验。
189.根据权利要求184所述的方法,其中H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列表明所述受试者可能适合进行临床试验。
190.一种鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定所述高加索人受试者的CFH-至-F13B基因座中的至少6个SNP的身份,其中所述SNP是:(i)rs35928059、rs800292、rs1061170、rs12144939、rs7546940、rs1409153、rs10922153或rs698859或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中至少6个所述SNP的存在表明所述受试者是否适合进行临床试验。
191.根据权利要求190所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
192.根据权利要求190所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
193.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的G、rs10922153上的G或rs698859上的A表明所述受试者适合进行临床试验。
194.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的T表明所述受试者适合进行临床试验。
195.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的C、rs12144939上的G、rs7546940上的G、rs1409153上的C、rs10922153上的G或rs698859上的C表明所述受试者适合进行临床试验。
196.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者不适合进行临床试验。
197.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的A、rs10922153上的T或rs698859上的G表明所述受试者不适合进行临床试验。
198.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的A、rs10922153上的T或rs698859上的A表明所述受试者不适合进行临床试验。
199.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的A、rs1061170上的T、rs12144939上的G、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者不适合进行临床试验。
200.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的C表明所述受试者不适合进行临床试验。
201.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的A、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者不适合进行临床试验。
202.根据权利要求190所述的方法,其中rs35928059上的A、rs800292上的G、rs1061170上的T、rs12144939上的T、rs7546940上的G、rs1409153上的T、rs10922153上的T或rs698859上的T表明所述受试者不适合进行临床试验。
203.一种鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定所述受试者的CFH-至-F13B基因座中的一个或多个SNP的身份,其中所述SNP是:(i)rs1061170、rs1410996、rs2274700、rs3753395、rs403846或rs3753396或(ii)与(i)的SNP处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明所述受试者适合进行临床试验。
204.根据权利要求203所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
205.根据权利要求203所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
206.根据权利要求203所述的方法,其中rs1061170SNP上的A表明所述受试者适合进行临床试验。
207.根据权利要求203所述的方法,其中rs1410996SNP上的A、rs2274700SNP上的A、rs3753395SNP上的T或rs403846SNP上的G表明所述受试者不适合进行临床试验。
208.根据权利要求203所述的方法,其中rs3753396SNP上的G表明所述受试者可能适合进行临床试验。
209.一种鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法包括测定所述受试者的CFH-至-F13B基因座中的缺失标记SNP的身份,其中所述SNP是:(i)rs12144939或(ii)与rs12144939处于连锁不平衡的SNP,并且其中一个或多个所述SNP的存在表明所述受试者是否适合进行临床试验。
210.根据权利要求209所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
211.根据权利要求209所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
212.根据权利要求209所述的方法,其中rs12144939SNP上的T表明所述受试者不适合进行临床试验。
213.一种试剂盒,其包含用于检测受试者的核酸样品中的一个或多个单倍型的测定,其中所述一个或多个单倍型是H1_62_A、H2_62_A、H3_62_A、H4_62_A、H5_62_A、H6_62_A、H7_62_A、H8_62_A、H9_62_A、H10_62_A、H11_62_A、H12_62_A、H13_62_A、H14_62_A、H15_62_A、H1_51_A、H2_51_A、H3_51_A、H4_51_A、H5_51_A、H6_51_A、H7_51_A、H8_51_A、H9_51_A、H10_51_A、H11_51_A、H12_51_A、H13_51_A、H14_51_A、H15_51_A、H16_51_A、H17_51_A、H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列。
214.根据权利要求213所述的试剂盒,其还包含用于扩增CHF-至-F13B基因座的扩增试剂。
215.根据权利要求213所述的试剂盒,其还包含用于使测定结果与所述受试者的患有或发展年龄相关性黄斑变性的风险相关联的说明书。
216.一种试剂盒,其包括用于检测受试者的核酸样品中的一个或多个SNP的测定,其中所述SNP是(i)rs12144939、rs1061170、rs1410996、rs2274700、rs3753395或rs403846;(ii)(i)的SNP的组合;或(iii)与(i)的SNP处于连锁不平衡的SNP。
217.根据权利要求216所述的试剂盒,,其还包含用于扩增CHF-至-F13B基因座的扩增试剂。
218.根据权利要求216所述的试剂盒,其还包含用于使测定结果与所述受试者的患有或发展年龄相关性黄斑变性的风险相关联的说明书。
219.一种用于测定高加索人受试者对患有或发展年龄相关性黄斑变性的易感性的方法,包括测定所述高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明所述受试者对患有或发展年龄相关性黄斑变性的易感性。
220.根据权利要求219所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
221.根据权利要求219所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
222.根据权利要求219所述的方法,其中所述二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表明所述受试者的增加的患有或发展年龄相关性黄斑变性的风险。
223.根据权利要求222所述的方法,其还包括给所述受试者施用治疗性组合物。
224.根据权利要求219所述的方法,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明所述受试者的减少的患有或发展年龄相关性黄斑变性的风险。
225.一种鉴定需要治疗年龄相关性黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明所述受试者是否需要治疗年龄相关性黄斑变性。
226.根据权利要求225所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
227.根据权利要求225所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
228.根据权利要求225所述的方法,其中二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表明所述受试者需要治疗年龄相关性黄斑变性。
229.根据权利要求225所述的方法,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明所述受试者不需要治疗年龄相关性黄斑变性。
230.根据权利要求225所述的方法,其中二倍体型H4_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H13_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列表明所述受试者可能需要治疗年龄相关性黄斑变性。
231.一种鉴定需要预防性治疗老年黄斑变性的高加索人受试者的方法,包括测定所述高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明所述受试者是否需要预防性治疗年龄相关性黄斑变性。
232.根据权利要求231所述的方法,其中从获自所述受试者的样品测定所述受试者的单倍型。
233.根据权利要求231所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
234.根据权利要求231所述的方法,其中二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表明所述受试者需要预防性治疗年龄相关性黄斑变性。
235.根据权利要求231所述的方法,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明所述受试者不需要预防性治疗年龄相关性黄斑变性。
236.一种鉴定适合进行年龄相关性黄斑变性临床试验的高加索人受试者的方法,包括测定所述高加索人受试者的基于一个或多个单倍型的一个或多个二倍体型的身份,其中所述一个或多个单倍型是H1_51_B、H2_51_B、H3_51_B、H4_51_B、H5_51_B、H6_51_B、H7_51_B、H8_51_B、H9_51_B、H10_51_B、H11_51_B、H12_51_B、H13_51_B、H14_51_B、H15_51_B、H16_51_B、H17_51_B、H18_51_B、H19_51_B、H20_51_B、H21_51_B、H22_51_B或其互补序列,并且其中一个或多个所述二倍体型的存在表明所述受试者是否适合进行临床试验。
237.根据权利要求236所述的方法,其中从获自所述受试者的样品来测定所述受试者的单倍型。
238.根据权利要求236所述的方法,其中所述受试者的单倍型通过扩增获自所述受试者的核酸样品或对其进行测序来测定。
239.根据权利要求236所述的方法,其中二倍体型H1_51_B:H1_51_B、H1_51_B:H2_51_B、H1_51_B:H8_51_B、H1_51_B:H13_51_B、H2_51_B:H2_51_B、H2_51_B:H10_51_B、H1_51_B:任何次51_B单倍型、H2_51_B:任何次51_B单倍型或其互补序列表明所述受试者适合于临床试验。
240.根据权利要求236所述的方法,其中二倍体型H1_51_B:H3_51_B、H1_51_B:H5_51_B、H1_51_B:H14_51_B、H3_51_B:H3_51_B、H3_51_B:H4_51_B、H3_51_B:H5_51_B、H3_51_B:H6_51_B、H3_51_B:任何51_B次单倍型、H4_51_B:H5_51_B、H5_51_B:H5_51_B、H5_51_B:任何51_B次单倍型、H6_51_B:H6_51_B、H6_51_B:任何51_B次单倍型或其互补序列表明所述受试者不适合进行临床试验。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161480929P | 2011-04-29 | 2011-04-29 | |
| US61/480,929 | 2011-04-29 | ||
| PCT/US2012/035467 WO2012149329A2 (en) | 2011-04-29 | 2012-04-27 | Methods of predicting the development of complement-mediated disease |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103874526A true CN103874526A (zh) | 2014-06-18 |
Family
ID=47073084
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201280031235.6A Pending CN103874526A (zh) | 2011-04-29 | 2012-04-27 | 预测补体介导的疾病的发展的方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (3) | US20140357732A1 (zh) |
| EP (1) | EP2704800B1 (zh) |
| JP (1) | JP2014513958A (zh) |
| KR (1) | KR20140074258A (zh) |
| CN (1) | CN103874526A (zh) |
| AU (1) | AU2012249521A1 (zh) |
| BR (1) | BR112013027851A2 (zh) |
| CA (1) | CA2834676A1 (zh) |
| DK (1) | DK2704800T3 (zh) |
| SG (1) | SG194235A1 (zh) |
| WO (1) | WO2012149329A2 (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10155983B2 (en) | 2014-03-31 | 2018-12-18 | Machaon Diagnostics, Inc. | Method of diagnosis of complement-mediated thrombotic microangiopathies |
| KR102333953B1 (ko) * | 2020-07-10 | 2021-12-02 | 인제대학교 산학협력단 | 신규한 황반변성 진단용 유전자 마커 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006096561A2 (en) * | 2005-03-04 | 2006-09-14 | Duke University | Genetic variants increase the risk of age-related macular degeneration |
| WO2008008986A2 (en) * | 2006-07-13 | 2008-01-17 | University Of Iowa Research Foundation | Methods and reagents for treatment and diagnosis of vascular disorders and age-related macular degeneration |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8088579B2 (en) * | 2005-02-14 | 2012-01-03 | University Of Iowa Research Foundation | Complement factor H for diagnosis of age-related macular degeneration |
| EP2217720A4 (en) * | 2007-11-01 | 2010-12-08 | Univ Iowa Res Found | RNA LOCUS ANALYSIS TO ASSESS THE STUNNING FOR AMD AND MPGNII |
| US8114592B2 (en) * | 2008-03-18 | 2012-02-14 | Cambridge Enterprise Limited | Genetic markers associated with age-related macular degeneration, methods of detection and uses thereof |
| WO2010075519A2 (en) * | 2008-12-23 | 2010-07-01 | Massachusetts Eye & Ear Infirmary | Allelic variants associated with advanced age-related macular degeneration |
| US20120202708A1 (en) * | 2010-10-14 | 2012-08-09 | Sequenom, Inc. | Complement factor h copy number variants found in the rca locus |
| US20140087960A1 (en) * | 2010-12-14 | 2014-03-27 | Johanna M. Seddon | Markers Related to Age-Related Macular Degeneration and Uses Therefor |
| US20140303013A1 (en) * | 2011-03-15 | 2014-10-09 | University Of Utah Research Foundation | Methods of diagnosing and treating vascular associated maculopathy and symptoms thereof |
| US20150211065A1 (en) * | 2012-09-14 | 2015-07-30 | University Of Utah Research Foundation | Methods of predicting the development of amd based on chromosome 1 and chromosome 10 |
| US9896728B2 (en) * | 2013-01-29 | 2018-02-20 | Arcticrx Ltd. | Method for determining a therapeutic approach for the treatment of age-related macular degeneration (AMD) |
-
2012
- 2012-04-27 EP EP12776262.3A patent/EP2704800B1/en active Active
- 2012-04-27 DK DK12776262.3T patent/DK2704800T3/en active
- 2012-04-27 JP JP2014508602A patent/JP2014513958A/ja active Pending
- 2012-04-27 WO PCT/US2012/035467 patent/WO2012149329A2/en active Application Filing
- 2012-04-27 SG SG2013080502A patent/SG194235A1/en unknown
- 2012-04-27 US US14/114,751 patent/US20140357732A1/en not_active Abandoned
- 2012-04-27 CN CN201280031235.6A patent/CN103874526A/zh active Pending
- 2012-04-27 AU AU2012249521A patent/AU2012249521A1/en not_active Abandoned
- 2012-04-27 CA CA2834676A patent/CA2834676A1/en not_active Abandoned
- 2012-04-27 KR KR1020137031638A patent/KR20140074258A/ko not_active Application Discontinuation
- 2012-04-27 BR BR112013027851A patent/BR112013027851A2/pt not_active IP Right Cessation
-
2017
- 2017-06-27 US US15/634,892 patent/US20180155788A1/en not_active Abandoned
-
2020
- 2020-01-03 US US16/734,168 patent/US20200239958A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006096561A2 (en) * | 2005-03-04 | 2006-09-14 | Duke University | Genetic variants increase the risk of age-related macular degeneration |
| WO2008008986A2 (en) * | 2006-07-13 | 2008-01-17 | University Of Iowa Research Foundation | Methods and reagents for treatment and diagnosis of vascular disorders and age-related macular degeneration |
Non-Patent Citations (2)
| Title |
|---|
| HUGHES ANNE等: "A common CFH haplotype,with deletion of CFHR1 and CFGR3,is associated with lower risk of age-related macular degeneration", 《NATURE GENETICS》, vol. 38, no. 10, 31 October 2006 (2006-10-31), pages 1173 - 1177 * |
| SEPIDEH ZAREPARSI等: "Strong Association of the Y402H Variant in Complement Factor H at 1q32 with Susceptibility to Age-Related Macular Degeneration", 《AMERICAN JOURNAL OF HUMAN GENETICS》, vol. 77, no. 1, 31 July 2005 (2005-07-31), pages 152, XP002423452, DOI: doi:10.1086/431426 * |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2012249521A1 (en) | 2013-11-14 |
| KR20140074258A (ko) | 2014-06-17 |
| WO2012149329A3 (en) | 2012-12-20 |
| WO2012149329A2 (en) | 2012-11-01 |
| DK2704800T3 (en) | 2019-01-14 |
| US20200239958A1 (en) | 2020-07-30 |
| EP2704800B1 (en) | 2018-09-12 |
| CA2834676A1 (en) | 2012-11-01 |
| EP2704800A4 (en) | 2015-04-29 |
| BR112013027851A2 (pt) | 2017-11-07 |
| SG194235A1 (en) | 2013-12-30 |
| US20180155788A1 (en) | 2018-06-07 |
| JP2014513958A (ja) | 2014-06-19 |
| US20140357732A1 (en) | 2014-12-04 |
| EP2704800A2 (en) | 2014-03-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Shi et al. | Exome sequencing identifies ZNF644 mutations in high myopia | |
| Lam et al. | A genome-wide scan maps a novel high myopia locus to 5p15 | |
| Tremelling et al. | IL23R variation determines susceptibility but not disease phenotype in inflammatory bowel disease | |
| Sullivan et al. | Genome-wide association for major depressive disorder: a possible role for the presynaptic protein piccolo | |
| Chapman et al. | Whole exome sequencing in extended families with autism spectrum disorder implicates four candidate genes | |
| Mackay et al. | Exome sequencing identifies a missense variant in EFEMP1 co-segregating in a family with autosomal dominant primary open-angle glaucoma | |
| Wojciechowski et al. | Matrix metalloproteinases and educational attainment in refractive error: Evidence of gene–environment interactions in the Age-Related Eye Disease Study | |
| Alkelai et al. | Identification of new schizophrenia susceptibility loci in an ethnically homogeneous, family‐based, Arab‐Israeli sample | |
| Alvarez-Mora et al. | Comprehensive molecular testing in patients with high functioning autism spectrum disorder | |
| Xu et al. | Molecular genetics of Leber congenital amaurosis in Chinese: new data from 66 probands and mutation overview of 159 probands | |
| Engelman et al. | Interaction between two cholesterol metabolism genes influences memory: findings from the Wisconsin Registry for Alzheimer's Prevention | |
| Tatour et al. | A novel intronic mutation of PDE6B is a major cause of autosomal recessive retinitis pigmentosa among Caucasus Jews | |
| Miyadera et al. | Phenotypic variation and genotype-phenotype discordance in canine cone-rod dystrophy with an RPGRIP1 mutation | |
| Wojciechowski et al. | Genomewide linkage scans for ocular refraction and meta-analysis of four populations in the Myopia Family Study | |
| Kroes et al. | DNA analysis of AHI1, NPHP1 and CYCLIN D1 in Joubert syndrome patients from the Netherlands | |
| US20200239958A1 (en) | Methods of predicting the development of complement-mediated disease | |
| Chioza et al. | Genome wide high density SNP-based linkage analysis of childhood absence epilepsy identifies a susceptibility locus on chromosome 3p23-p14 | |
| Ting et al. | Cockayne Syndrome due to a maternally-inherited whole gene deletion of ERCC8 and a paternally-inherited ERCC8 exon 4 deletion | |
| Georgiou et al. | Molecular analysis of Cypriot patients with Glutaric aciduria type I: identification of two novel mutations | |
| CN103725687B (zh) | 多巴反应性肌张力障碍相关基因突变、其检测方法及其用途 | |
| Krohn et al. | Fine-mapping of SNCA in REM sleep behavior disorder and overt synucleinopathies | |
| JP6829878B2 (ja) | 加齢黄斑変性の発症リスクの評価方法 | |
| Chew | De novo mutations in canine evolution and disease | |
| Lázaro-Guevara et al. | Identification of RP1 as the genetic cause of retinitis pigmentosa in a multi-generational pedigree using Extremely Low-Coverage Whole Genome Sequencing (XLC-WGS) | |
| Ganapathi et al. | Clinical Exome Sequencing for Inherited Retinal Disorders at a Tertiary Care Center |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20140618 |